Тянущая или режущая боль внизу живота
Такие боли бывают, когда один или несколько органов увеличились в размерах и давят на окружающие их мышцы. Почему это происходит?
Причины могут совершенно разные.
Разберем примеры у мужчин и женщин. У обоих полов такие боли могут быть причиной сильного перенапряжения мышц и невозможности их сокращения.
Также стоит помнить, что такие боли сопровождают половые инфекции. Всегда обращайте внимание на цвет и запах выделений из половых органов. У здорового человека выделения прозрачные и практически не имеют запаха.
Женщины
Такие боли часто бывают при месячных. Если они случаются на 12-14 день обычного 28 дневного цикла, без привычных выделений, то нужно немедленно обратиться к гинекологу. Это может свидетельствовать о различных воспалениях в матке и яичниках. Если боли увеличиваются во время месячных или становятся невыносимыми – это свидетельствует о стремительно развивающемся эндометриозе или более страшных заболеваниях, вплоть до рака.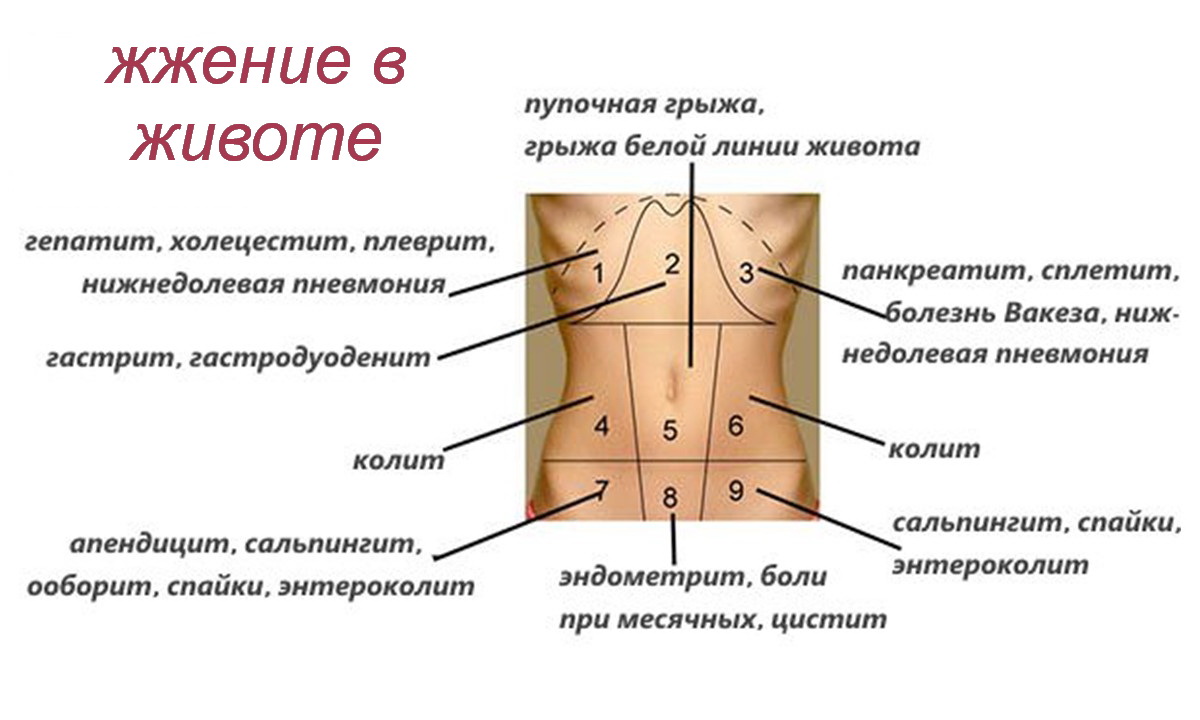
Боли внизу живота у женщин часто говорят о беременности, в том числе, внематочной.
Если вы испытываете подобные боли во время полового акта, то следует также обратиться к гинекологу. Он выяснит, почему в этот момент матка увеличивается в размерах, хотя так быть не должно. Если боли возникают во время мочеиспускания или после – это свидетельствует об инфекции в мочевом пузыре. Это могут быть распространенные у женщин пиелонефрит или цистит. Тогда вам срочно нужно показаться урологу и сдать анализ мочи. Не доводите болезнь до камней в почках.
Мужчины
Врачу важно понять, где именно и при каких условиях вы испытываете боль. Помимо половых инфекций – это могут быть воспаления простаты и мочевыводящих путей, поражения кишечника.
Такие боли свидетельствуют о хроническом простатите.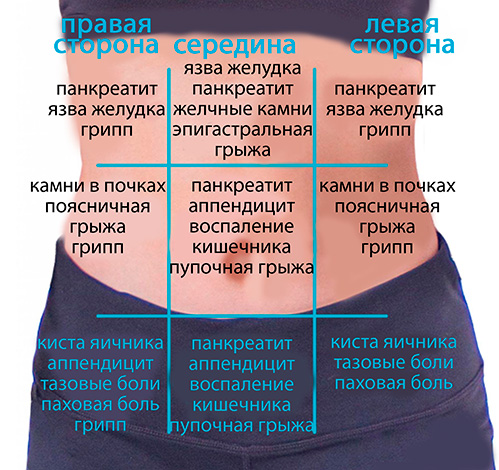 Они чреваты проблемами в половой жизни и недержанием мочи.
Они чреваты проблемами в половой жизни и недержанием мочи.
Помните, что если вы хотя бы раз ночью встаете в туалет – это говорит о проблемах с мочеполовой системой. При любых болях и дискомфорте при мочеиспускании обратитесь к урологу. Не доводите до операции.
Если болит справа, то это аппендицит. Срочно отправляйтесь в больницу. Он может «лопнуть» и тогда произойдет заражение крови.
Также боли справа могут говорить о злокачественной опухоли в кишечнике. Чтобы его установить необходимо рентгенологическое исследование кишечника. Если боль возникает слева при ходьбе или тряске в автомобиле, это также воспаление отделов кишечника.
Специалисты клиники «Элеос» ответят на все ваши вопросы. Мы знаем, как вам помочь.
«Боль в левом боку живота внизу: причины» – Яндекс.Кью
Содержание:
Тупая, острая, ноющая или колющая боль с левой стороны в нижней части живота обычно тревожит и настораживает человека.
Болит живот внизу слева: возможные причины
Брюшная полость вмещает в себя многие жизненно важные органы человека. В частности, с левой стороны находится селезенка, толстый и тонкий кишечник и органы мочеполовой системы. И в каждом из этих органов может произойти сбой — они воспаляются, травмируются, деформируются, на них развиваются опухоли и т. д. Большая часть болезней и состояний, дающих левостороннюю боль внизу живота, требует безотлагательного лечения.
Селезенка
В селезенке происходит образование и утилизация кровяных клеток. Любые патологии этого органа способны давать левосторонние боли внизу живота. В частности, речь идет о таких болезнях и состояниях селезенки, как:
Любые патологии этого органа способны давать левосторонние боли внизу живота. В частности, речь идет о таких болезнях и состояниях селезенки, как:
- Острое расширение селезенки — патология может возникнуть в результате воспаления или нарушения оттока крови, в любом случае пациента будет беспокоить боль внизу живота слева, не исключено появление симптомов в виде тошноты, рвоты, повышения температуры тела.
- Инфаркт селезенки — закупорка артерии и образование некрозного очага, окружающего тромб; резкая боль появляется в левом подреберье и опускается вниз, ее интенсивность увеличивается при движении, кашле и даже глубоком дыхании, у пациента так же отмечается высокая температура тела (около 39 градусов).
- Заворот селезенки — иногда (чаще всего из-за врожденных особенностей строения брыжеечных связок человека или вследствие травмы) селезеночная артерия перекручивается, вызывая тем самым постепенно опускающуюся вниз боль в левом боку; боль сопровождается и такими симптомами, как вздутие кишечника, запоры, рвота, ухудшение общего самочувствия.

- Абсцесс селезенки — потенциально опасны для жизни крупные абсцессы: вскрываясь в брюшную полость, они вызывают разлитую боль, которая вполне может ощущаться и внизу живота слева.
- Лимфолейкоз и миелолейкоз (хронические формы) — онкология органов кроветворения начинается безболезненно, но по мере роста опухоли боли нарастают: сначала они появляются после еды и при пальпации.
Кишечник
Со стороны кишечника левосторонние боли внизу живота могут возникать по различным причинам — от банального метеоризма до куда более серьезных состояний и болезней:
- Мальабсорбция — заключается в неспособности слизистой оболочки тонкого кишечника воспринимать определенный продукт (или группу продуктов), например, фрукты или молоко; протекает с распирающей болью внизу живота слева (объясняется скоплением газов) и схваткообразной болью в той же области (в результате спазмирвания сосудов и мышц стенок кишечника).
- Болезнь Крона — узелковое воспаление ЖКТ проявляется не только левосторонней болью в низу живота, но еще и рвотой, поносом, общей усталостью, снижением аппетита.

- Синдром раздраженной кишки — сопровождается болями, которые могут беспокоить и слева внизу живота, а так же метеоризмом, поносом или запором. Для заболевания характерно наличие периодов ремиссии и обострений.
- Неспецифический язвенный колит — протекает с морфологическими изменениями стенок кишечника, сопровождается приступообразными коликами разной интенсивности.
- Полипоз — появление на слизистых некоторых отделов кишечника доброкачественных образований (полипов) способно провоцировать левосторонние боли внизу живота.
- Непроходимость кишечника- сопровождается выраженной болью, а так же скоплением в кишечнике газов и запорами, тошнотой и рвотой, вздутием живота и явной асимметрией.
- Заворот кишок — сопровождается сильными приступообразными болями, которые на время совсем отступают, а затем возвращаются вновь, а так же рвотой.
- Онкология.
Репродуктивная система
Существует ряд причин, провоцирующих боли в нижней части живота слева именно у женщин.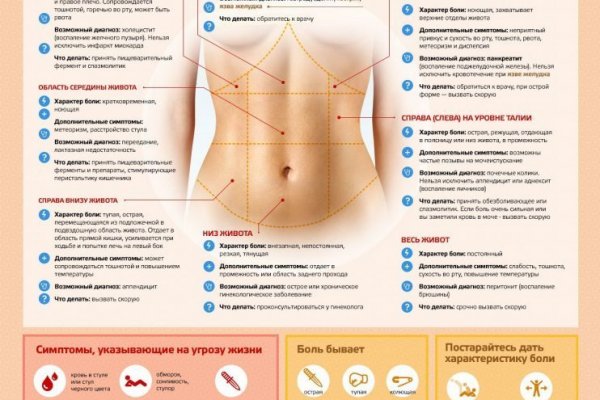 К их числу относятся следующие недуги:
К их числу относятся следующие недуги:
- Воспаление маточных труб — помимо резкой боли в паху (в том числе, локализация возможна и слева) пациентки страдают от влагалищных выделений, болезненных месячных и высокой температуры.
- Эндометриоз — при этой патологии клетки эпителия размножаются и за пределами матки, возможно их разрастание и в кишечнике.
- Разрыв и\или перекручивание ножки яичника — это опасное состояние проявляется болями очень высокой интенсивности и нарушениями общего состояния пациентки: бледность кожных покровов, падение давления, повышение температуры, рвота. В этом случае больная нуждается в экстренной помощи.
- Аднексит и сальпингоофорит — воспаление придатков сопровождается острыми болями внизу живота, которые усиливаются при прощупывании.
- Внематочная беременность — это опасное для жизни женщины состояние проявляется схваткообразными болями, интенсивность которых постепенно нарастает; в случае разрыва маточной трубы боль становится непереносимой, пациентке при этом необходима срочная медицинская помощь.

- Синдром Аллена-Мастерса — возникает вследствие разрыва связок матки из-за тяжелых либо стремительных родов, аборта и т.д.
Еще одной из множества причин, провоцирующих левостороннюю боль в нижней части живота как у мужчин, так и у женщин, со стороны мочеполовой системы является расширение почечной лоханки.
Классификация боли: какой она может быть
Левосторонние боли внизу живота могут иметь разный характер, по которому и можно заподозрить развитие того или иного заболевания.
Тупая боль обычно сопровождает односторонние «женские» заболевания. Если притупленные болевые ощущения сочетаются с повышением температуры, быстрой утомляемостью, общей слабостью то, скорее всего, речь идет о воспалительных патологиях.
Тянущая левосторонняя боль обычно характерна для гнойных патологий органов малого таза, она возникает при растяжении связок в паху и ущемленных грыжах, а так же сопровождает онкологические заболевания (в этом случае ее интенсивность нарастает со временем).
Резкие боли слева внизу живота бывают вызваны спазмами, прохождением уралитов по мочевым путям, разрывом паховых связок, воспалениями, разрывом яичника, расширением почечной лоханки или мочевого пузыря.
Колющая боль может быть предвестником разрыва яичника, последствием распирания кишечника газами, спутником болезней почек или изъязвления слизистых уретры или мочеточников.
В любом случае наличие таких болей должно стать основанием для обращения за помощью к врачу. При этом важно уделить внимание и сопутствующим симптомам — повышенной температуре тела, поносу, рвоте, бледности, вялости и т. д. О них обязательно нужно сообщить специалисту – эта информация пригодится для постановки точного диагноза.
Что делать болях внизу живота слева?
Левосторонние боли внизу живота игнорировать нельзя. Они могут свидетельствовать о развивающейся острой патологии, требующей экстренной медицинской помощи. Поэтому прием болеутоляющих с целью снятия болевого синдрома в этом случае не вариант. Причина никуда не денется, а притупленные ощущения могут осложнить постановку диагноза.
Причина никуда не денется, а притупленные ощущения могут осложнить постановку диагноза.
Ощутив боль любой интенсивности и любого характера слева внизу живота необходимо действовать следующим образом:
- Обеспечить себе покой и принять наиболее комфортную позу, при которой боль не ощущается или, по крайней мере, не усиливается.
- Оценить боль с позиции имеющихся хронических заболеваний, состояния организма в целом и наличествующих других симптомов (беременность, понос, рвота, высокая температура и т. д.).
- В случае первичного возникновения боли (если раньше человек никогда не испытывал подобных ощущений внизу живота слева) рекомендуется вызвать скорую помощь.
- Если боль уже заявляла о себе ранее, решение о целесообразности обращения за экстренной медицинской помощью пациент способен принять самостоятельно — вызвать «скорую» при явном ухудшении состояния, вызвать участкового врача на дом в случае стабильности состояния или обратиться в поликлинику за направлением на обследование при кратковременном приступе.

Важно помнить о том, что даже если интенсивность боли внизу живота слева не высока, это ощущение может свидетельствовать о развитии серьезного заболевания.
Лечение боли внизу живота слева
Разумеется, само лечение направлено не на снятие болевого синдрома, а на устранение его причины. Очень часто пациентам, страдающим левосторонними болями внизу живота, требуется экстренная медицинская помощь и госпитализация. Лечение может быть как консервативным (при помощи различных препаратов), так и хирургическим.
Чаще всего занимаются пациентами с левосторонними болями внизу живота врачи следующих специальностей:
- гинеколог;
- хирург;
- травматолог;
- гастроэнтеролог;
- инфекционист.
Как правило, для постановки точного диагноза требуется осмотр и опрос пациента, лабораторные анализы крови и мочи, анализы ферментов печени и поджелудочной железы, а так же рентгенографические, ультразвуковые и эндоскопические исследования. На основании полученных результатов обследования для каждого пациента разрабатывается индивидуальный план лечебных мероприятий.
На основании полученных результатов обследования для каждого пациента разрабатывается индивидуальный план лечебных мероприятий.
Здравствуйте. Возникают боли внизу живота, которые потом отдают в прямую кишку.Подскажите к какому …
Выберите клинику из списка
Все клиники
Гинекологическое отделение
Центр вспомогательных репродуктивных технологий (ЭКО)
Родовое отделение
Клиника педиатрии
Клиника терапии
Клиника стоматологии, имплантологии и челюстно-лицевой хирургии
Клиника кардиологии и сердечно-сосудистой хирургии
Клиника неврологии и нейрохирургии
Клиника хирургии
Клиника травматологии и ортопедии
Клиника урологии
Клиника онкологии
Клиника оториноларингологии
Клиника офтальмологии и микрохирургии глаза
Клиника пластической и реконструктивной хирургии
Лабораторная служба
Лаборатория медицинской генетики
Клинико-диагностическая лаборатория
Клиника лучевой диагностики
Клиника восстановительного лечения
Медицинская помощь на дому
Чем могут быть вызваны боли во влагалище? Популярные статьи
Боли во влагалище беспокоят многих женщин, возникают они по различным причинам и в некоторых случаях проходят самостоятельно. Однако боли могут свидетельствовать о серьезных заболеваниях, требующих лечения, поэтому не следует оставлять тревожные симптомы без внимания.
Однако боли могут свидетельствовать о серьезных заболеваниях, требующих лечения, поэтому не следует оставлять тревожные симптомы без внимания.
Как правило, диагностика причины болей во влагалище не составляет труда для опытного врача, однако существует такое понятие, как вульводиния: наличие боли в области половых губ и влагалища, причину которой установить не удается. Считается, что если после полного обследования не найдена причина подобной боли, происхождение ее связано с нейрогенным фактором, а также иммунными и генетическими факторами.
Боль представляет собой защитную реакцию организма в ответ на какие-либо раздражители.
Боли во влагалище могут быть следующими:
- связаны или не связаны с физическими нагрузками, половым актом.
- интенсивность: варьирует от слабой до сильной.
- характер: тянущая, колющая, режущая, тупая, острая.
- продолжительность: острая, хроническая.
- постоянство: постоянная, периодическая, рецидивирующая.

- сопровождающие симптомы: выделения из влагалища, зуд, жжение.
Каковы возможные причины болей во влагалище?
- воспалительные заболевания половых органов, в частности, вызываемые половыми инфекциями. Кольпит (воспаление слизистой оболочки влагалища) проявляется болями во влагалище, жжением и зудом во время и после полового акта, выделениями желтоватого цвета с неприятным запахом. Кольпит может быть вызван как специфической (гонококки, трихомонады, хламидии), так и неспецифической флорой (стрептококки, стафилококки, кишечная палочка). Кольпит может переходить в цервицит (воспаление слизистой шейки матки), метрит и эндометрит (воспаление матки), аднексит (воспаление придатков матки).
- кандидоз влагалища (молочница). Провоцируется такими состояниями, как снижение иммунитета, прием антибиотиков, ношение тесного и узкого белья, некачественная гигиена, эндокринные заболевания (сахарный диабет), неправильное питание (употребление жирной, пряной, копченой пищи).

- воспаление бартолиновой железы. Бартолиновы железы располагаются в преддверии влагалища, вырабатывают слизь для увлажнения вульвы и входа во влагалище. Воспаление желез чаще носит односторонний характер, характеризуется колющими болями при движении, во время полового акта.
- эндометриоз. Это состояние вызывает болезненность во влагалище, в особенности при половом контакте. После контакта возможно выделение крови из влагалища и тянущая боль внизу живота.
- крауроз вульвы: у женщин пожилого возраста нередко возникает такое состояние, характеризующееся истончением кожи наружных половых органов. Вследствие недостатка гормонов кожа становится легко ранимой, травмируется даже при соприкосновении с нижним бельем, зудит.
- травмы, инородные тела во влагалище.
- сухость слизистой оболочки во время климакса. Вследствие нарушения функционирования яичников и недостатка эстрогенов возникает сухость слизистой оболочки влагалища, которая становится причиной болезненности, усиливающейся при половом акте.

- медицинские манипуляции (лечебные и диагностические). Болевой синдром нередко возникает после гистероскопии, установке внутриматочной спирали.
- разнообразные аномалии развития влагалища.
- доброкачественные новообразования (фибромы, фибромиомы) влагалища чаще причиняют боль при осмотре и во время полового акта, злокачественные новообразования проявляются болью, но чаще на поздних стадиях.
- острая хирургическая патология: апоплексия яичника. Это кровоизлияние в яичник вследствие разрыва кисты или сосудов фолликула. Апоплексия сопровождается кровоизлиянием в брюшную полость. Это состояние провоцируют травмы, спринцевания влагалища, агрессивный секс. Общее состояние женщины ухудшается, беспокоит слабость, сильные боли в животе, возможны тошнота и рвота. Апоплексия требует неотложного хирургического лечения.
- выпадение тела матки (полное, неполное), опущение стенок влагалища. Чаще встречаются у женщин старше 45 лет. Одновременно с тянущими болями отмечается недержание мочи и кала.

- рубцовые изменения после медицинских вмешательств: разрывы и разрезы промежности в родах. Характеризуются периодически возникающими тупыми или тянущими болями во влагалище, возникающими периодически.
- проктит, парапроктит, воспаление внутренних геморроидальных узлов, цистит, уретрит.
При перечисленных состояниях боли могут иррадиировать во влагалище.
При появлении болей во влагалище следует незамедлительно обратиться к врачу-гинекологу с целью обследования.
Почему кесарево сечение или подтяжка живота вызывают нервную боль
Как правило, после операции вы можете ожидать определенной степени боли или дискомфорта. Хирургические процедуры травматичны для человеческого тела, и боль может быть вызвана тем, что ваше тело пытается заживить поврежденные ткани. Однако в некоторых случаях впоследствии развивается нервная боль, и это не та боль, которую вы, вероятно, должны ожидать.
Как мы уже отмечали на нашем веб-сайте, нервная боль часто сопровождается такими симптомами, как жжение, стреляющая, колющая и жгучая боль. У некоторых пациентов внешняя стимуляция — даже на слабых уровнях (например, ветер, дующий на кожу или вода, стекающая из душа) — вызывает сильные физические ощущения. Другие испытывают «булавки и иголки» или чувствуют, как будто определенная часть тела или область были подключены к электрической розетке.
У некоторых пациентов внешняя стимуляция — даже на слабых уровнях (например, ветер, дующий на кожу или вода, стекающая из душа) — вызывает сильные физические ощущения. Другие испытывают «булавки и иголки» или чувствуют, как будто определенная часть тела или область были подключены к электрической розетке.
Если у вас есть такие симптомы, скорее всего, боль вызвана каким-либо нервным расстройством.
В некоторых случаях эти симптомы начинаются после таких процедур, как кесарево сечение (родоразрешение) и подтяжка живота.Когда это происходит, пациентам понятно, почему это с ними происходит. Итак, давайте сегодня посмотрим, почему у вас возникают нервные боли после таких процедур.
Для начала стоит отметить, что нервная боль не означает, что во время операции что-то было сделано неправильно. Хирурги, по самому определению своей работы, должны разрезать ткани, чтобы исправить проблемы со здоровьем. В вашем теле есть целая сеть нервов, поэтому это означает, что бывают случаи, когда нервы также будут перерезаны во время операции. Это просто факт.
Это просто факт.
Нервная боль после кесарева сечения
Как и при других хирургических вмешательствах, практически невозможно выполнить кесарево сечение без разрезания некоторых нервов. Тем не менее, длительное повреждение нервов после кесарева сечения, как правило, встречается довольно редко.
Часто нервы заживают, не вызывая длительных проблем. Когда поврежденные нервы не заживают правильно, это считается повреждением нерва. В зависимости от того, какие нервы повреждены — и их соответствующих функций — могут развиваться различные краткосрочные и долгосрочные симптомы.Эти симптомы могут включать нарушение двигательной функции и нервную боль.
Если у вас было кесарево сечение и вы испытываете поверхностную боль по краям рубца, вероятно, были затронуты подвздошно-паховые, подвздошно-гипогастральные и / или генитофеморальные нервы. Обычно боль проявляется в виде жгучей боли и гиперчувствительности, что означает даже легкое прикосновение (как в предыдущих примерах ветра и воды). Также могут возникать ощущения «поражения электрическим током».
Также могут возникать ощущения «поражения электрическим током».
Если надавливание на пораженный участок не приводит к воспроизведению боли, менее вероятно, что именно эти нервы ответственны за это.
Причина, по которой мы обращаем внимание на подвздошно-паховый, подвздошно-гипогастральный и генитофеморальный нервы, сводится к их расположению. Хирурги и стараются максимально избегать важных нервов, но эти нервы проходят близко к краю разреза кесарева сечения. Это позволяет им легко получить травмы во время процедуры (ушибы, раздавливания и т. Д.) Или впоследствии попасть в рубцовую ткань.
Если вы испытываете болезненные ощущения, скорее всего, нервы были повреждены, а не порезаны.Мы можем сказать это, потому что перерезанные нервы, как правило, вызывают онемение вместо боли. Хотя бывают случаи, когда и онемение, и боль возникают в результате перерезания нервов (это состояние называется anesthesia dolorosa ).
При диагностике нервной боли после кесарева сечения мы используем блокаду нерва. Это связано с использованием анестетика, чтобы вызвать временное онемение пораженного нерва. Когда есть и онемение, и облегчение боли, это указывает на повреждение периферического нерва. Если онемение без обезболивания, скорее всего, дело в другом.
Это связано с использованием анестетика, чтобы вызвать временное онемение пораженного нерва. Когда есть и онемение, и облегчение боли, это указывает на повреждение периферического нерва. Если онемение без обезболивания, скорее всего, дело в другом.
Нервная боль после подтяжки живота
Подтяжки живота — абдоминопластика — являются одними из наиболее распространенных косметических процедур, выполняемых в Соединенных Штатах, при этом Американское общество пластических хирургов сообщило о 127 633 в 2016 году. Это на 104% больше по сравнению с 62 713, выполненными в 2000 году.
Эксперты полагают, что количество операций по абдоминопластике будет только увеличиваться за счет как количества эстетических хирургических процедур, так и увеличения числа пациентов с ожирением, которые достигают значительной потери веса после бариатрической операции.
Как и при других операциях, нервы пораженного участка травмируются в результате подтяжки живота. Это может вызвать онемение на несколько недель или месяцев, прежде чем нервы преодолеют временную нейропраксию (потеря нервной проводимости). Обычно для разрешения ситуации требуется около 6–12 недель, но в некоторых случаях это может занять больше времени.
Обычно для разрешения ситуации требуется около 6–12 недель, но в некоторых случаях это может занять больше времени.
Хотя это онемение и определенная степень дискомфорта можно ожидать, это может стать проблемой, если нервная боль появилась и не проходит по прошествии разумного времени.
В случае нервной боли после подтяжки живота, вероятно, поражается небольшой нерв, называемый латеральным кожным нервом бедра. Этот конкретный нерв проходит непосредственно через области, на которые манипулируют во время подтяжки живота, и может быть легко поврежден непосредственно швом или скальпелем, или косвенно, когда нерв оказывается зажатым в рубцовой ткани.
Тем не менее, важно отметить, что за боль и сенсорные нарушения могут быть ответственны не только нервные повреждения, но и другие факторы.Например, значительная потеря веса может вызвать чрезмерное расширение кожи, а у пациента, перенесшего бариатрическую операцию, также могли быть исправлены другие проблемы (вторичный фиброз, грыжа) во время подтяжки живота.
Диагностика и лечение
Если после операции у вас возникла нервная боль — особенно если боль присутствует в течение длительного периода — вы заслуживаете того, чтобы выяснить, в чем причина. В случае кесарева сечения и подтяжки живота это может быть случайное повреждение нерва. В таком случае мы сможем предоставить вам необходимое обслуживание.
Чтобы получить дополнительную информацию или запросить консультацию в нашем офисе Мэриленд в Балтиморе, позвоните нам по телефону (410) 337-5400.причин резкой боли в животе при тренировке
Если это растяжение мышц, могут развиться отеки и синяки.
Кредит изображения: JGI / Tom Grill / Tetra images / GettyImages
Упражнения должны быть полезны для вас, поэтому, когда они начинают вызывать у вас боли в животе, вы можете усомниться в их ценности. Боковые швы — наиболее частая причина боли в животе во время тренировки.Однако также могут быть виноваты мышечные судороги, расстройство желудка и растяжение мышц. Кроме того, всегда возможно, что резкие боли могут быть признаком более серьезного состояния, требующего медицинской помощи.
Кроме того, всегда возможно, что резкие боли могут быть признаком более серьезного состояния, требующего медицинской помощи.
Совет
Боль в животе во время тренировки может быть вызвана судорогами, проблемами с пищеварением, боковыми швами или растяжением мышц.
Старые добрые боковые швы
Практически каждый, кто занимается спортом, хотя бы раз испытал на себе боль от боковых швов. Также известна как преходящая абдоминальная боль, связанная с физической нагрузкой (ЭТАБ), она может ощущаться в боковой части живота или внизу живота.
Согласно Berkeley Wellness, боковые швы чаще всего возникают во время интенсивных упражнений, включающих повторяющиеся движения туловища. Также они, как правило, ощущаются на правой стороне живота.
Боль от бокового шва может быть тупой или ноющей, а также острой и колющей. Это часто начинается с тупого, судорожного или тянущего ощущения и усиливается до более сильной боли.
Причины боковых швов
Никто точно не знает, что вызывает боковые стежки, но есть несколько теорий:
- Трение между слоем ткани брюшной полости, покрывающей органы, и слизистой оболочкой брюшной стенки.
 Это происходит из-за увеличения количества или толщины жидкости, которая смазывает желудок, сообщает диетолог Натали Риццо из Нью-Йорка.
Это происходит из-за увеличения количества или толщины жидкости, которая смазывает желудок, сообщает диетолог Натали Риццо из Нью-Йорка. - Употребление еды или напитков перед тренировкой.
- Плохая осанка.
- Неправильная техника дыхания, включая поверхностное дыхание и не вдыхание нижними легкими.
Некоторые люди подвергаются более высокому риску возникновения боли в животе во время упражнений из-за боковых швов, в том числе:
- Юные спортсмены.Частота и интенсивность боковых швов уменьшается с возрастом.
- женщин, у которых вероятность возникновения боковых швов в четыре раза выше, чем у мужчин, согласно статье 2015 года в Sports Medicine.
- Лица, лишенные условности.
Лечение и профилактика боковых швов
Боковые стежки проходят сами по себе, но есть несколько шагов, которые можно предпринять, чтобы ускорить процесс:
- Остановите или замедлите свою активность.

- Глубоко вдохните и медленно выдохните.
- Растяните мышцы живота.
- Осторожно прижмите пальцы к животу в том месте, где вы чувствуете боль, и слегка наклонитесь вперед.
Вы можете предотвратить образование боковых швов в будущем:
- Повышение уровня физической подготовки. Чем лучше вы станете, тем меньше вы будете делать боковые швы.
- Улучшение осанки за счет укрепления мышц спины и кора.
- Избегайте большого количества еды и напитков в течение двух часов после занятия.Пейте воду маленькими глотками до и во время тренировки.
- Избегайте продуктов с высоким содержанием жиров и клетчатки, а также сладких напитков перед тренировкой.
- Уменьшение интенсивности, но увеличение продолжительности тренировок, особенно если вы новичок в тренировках.
Спазмы мышц живота
Мышечные судороги могут ощущаться как боковые швы, но это не то же самое. Эти непроизвольные мышечные спазмы кажутся беспричинными, но чаще встречаются у спортсменов. Во время мышечного спазма вы можете почувствовать очень острую боль, когда мышца схватится. Мышца также могут стать твердыми и напряженными.
Во время мышечного спазма вы можете почувствовать очень острую боль, когда мышца схватится. Мышца также могут стать твердыми и напряженными.
Распространенные причины мышечных судорог:
- Недостаточная разминка и растяжка перед упражнением
- Обезвоживание
- Разминка в жару
- Перенапряжение и мышечная усталость
При появлении мышечной судороги прекратите деятельность, аккуратно растяните и помассируйте брюшную мышцу кончиками пальцев.Боль должна быстро исчезнуть сама по себе. Вы можете приложить тепло, чтобы расслабить напряженные мышцы, и лед, чтобы уменьшить сохраняющуюся болезненность.
Предотвратите мышечные судороги в будущем, разогреваясь и растягиваясь перед каждой тренировкой. Не переусердствуйте и делайте частые перерывы, если вы тренируетесь в жаркую погоду. Также не забывайте пить много воды до, во время и после тренировки.
Подробнее: Причины боли и утомляемости в животе
Боль в желудочно-кишечном тракте во время упражнений
Желудочно-кишечные расстройства часто встречаются у спортсменов, по словам бостонского гастроэнтеролога доктора Э. Дж. Томас Ламонт. Это связано с физиологическими изменениями активности кишечной нервной системы, уровней циркулирующих гормонов кишечника, кишечного кровотока, всасывания питательных веществ и электролитов, кишечной секреции и моторики.
Дж. Томас Ламонт. Это связано с физиологическими изменениями активности кишечной нервной системы, уровней циркулирующих гормонов кишечника, кишечного кровотока, всасывания питательных веществ и электролитов, кишечной секреции и моторики.
Расстройство пищеварения во время тренировки часто вызвано приемом пищи в течение нескольких часов после тренировки. Ламонт говорит, что обезвоживание и использование анальгетиков также связаны с расстройством желудочно-кишечного тракта во время упражнений.
Длительные упражнения и интенсивные упражнения могут с большей вероятностью вызвать боль в животе.Как и в случае с боковыми швами, ограничение продолжительности и интенсивности тренировок может уменьшить желудочно-кишечные расстройства. Вам также следует избегать обильной еды в течение трех часов после тренировки. Вместо этого перекусите легким перекусом, содержащим углеводы и белок, но не слишком много жира, так как это может увеличить риск расстройства желудка. Кроме того, не забывайте правильно пить до и во время тренировки.
Боль от растяжения живота
Чрезмерное растяжение или травма мышц живота может привести к растяжению мышц, вызывая разрыв мышечных волокон.Результатом часто бывает внезапная острая боль. В зависимости от тяжести напряжения также может наблюдаться отек, синяк, мышечная слабость или потеря мышечной функции.
Мышцы живота могут быть напряжены от прямого удара, перенапряжения или переутомления. К частым причинам напряжения мышц живота относятся:
- Резкие скручивающие движения
- Очень интенсивные упражнения
- Неправильная техника тяжелой атлетики
Если боль сильная и / или происходит полная потеря мышечной функции, вам следует обратиться к врачу, поскольку это может указывать на полный разрыв.В противном случае большинство штаммов можно лечить дома с помощью:
- Максимально расслабляйте мышцы живота.
- Прикладывайте пакет со льдом на 10–15 минут в течение часа, чтобы уменьшить отек.

- Ношение бандажа для живота или обертывание эластичной повязки вокруг живота, чтобы уменьшить подвижность и отек.
Продолжайте лечение в течение 48–72 часов после травмы. Возвращайтесь к своей обычной деятельности постепенно, только когда боль и отек утихнут.
Что еще это может быть?
Есть много других потенциальных причин боли в животе во время упражнений. Если это разовое событие и других симптомов нет, скорее всего, беспокоиться не о чем.
Но если это случается часто или сопровождается другими тревожными симптомами, лучше записаться на прием к лечащему врачу. Грыжа, камни в желчном пузыре, камни в почках, болезнь Крона и синдром раздраженного кишечника — это лишь некоторые из причин боли в желудке, которая может усугубиться физическими упражнениями.
Подробнее: Каковы причины боли в животе и болезненности?
Редкая причина боли в животе: рубцовый эндометриоз
Введение . Эндометриоз рубца (ЭЭ) — редкая патология, которая развивается в рубцовой ткани, образующейся на передней брюшной стенке, обычно после кесарева сечения. Были случаи, когда женщины обращались в клиники неотложной или общей хирургии с болью в животе из-за SE. Материалы и методы .В этом исследовании ретроспективно рассматриваются 19 пациентов, прооперированных в нашей клинике в период с января 2010 года по январь 2017 года с предрасположенным диагнозом SE, у которых на основании результатов патологии сообщалось, что у них была SE. Результаты . Средний возраст пациентов составлял 30,8 года (от 20 до 49 лет). Индексы массы тела у 12 (63,2%) пациентов были ≥ 25. Все пациенты в анамнезе перенесли кесарево сечение, а 9 (47,4%) пациентов перенесли кесарево сечение один раз. За исключением одной пациентки, у которой SE была локализована в паховой области, все пациенты имели образование, локализованное на передней брюшной стенке рядом с разрезом, и жаловались на циклическую боль, начинающуюся в предменструальный период.
Эндометриоз рубца (ЭЭ) — редкая патология, которая развивается в рубцовой ткани, образующейся на передней брюшной стенке, обычно после кесарева сечения. Были случаи, когда женщины обращались в клиники неотложной или общей хирургии с болью в животе из-за SE. Материалы и методы .В этом исследовании ретроспективно рассматриваются 19 пациентов, прооперированных в нашей клинике в период с января 2010 года по январь 2017 года с предрасположенным диагнозом SE, у которых на основании результатов патологии сообщалось, что у них была SE. Результаты . Средний возраст пациентов составлял 30,8 года (от 20 до 49 лет). Индексы массы тела у 12 (63,2%) пациентов были ≥ 25. Все пациенты в анамнезе перенесли кесарево сечение, а 9 (47,4%) пациентов перенесли кесарево сечение один раз. За исключением одной пациентки, у которой SE была локализована в паховой области, все пациенты имели образование, локализованное на передней брюшной стенке рядом с разрезом, и жаловались на циклическую боль, начинающуюся в предменструальный период. Жалобы появились через 2 года после кесарева сечения у 10 (52,6%) пациентов. В основном с диагностической целью использовалось УЗИ брюшной полости. Поражения были полностью иссечены, и всем пациентам был поставлен диагноз SE путем гистопатологического исследования. Послеоперационных осложнений или рецидивов ни у одного из пациентов не было. Заключение . Подозрение на СЭ важно у женщин репродуктивного возраста, у которых в анамнезе было кесарево сечение и жалобы на образование передней брюшной стенки и боль в месте рубца, связанную с их менструальным циклом.Таким пациентам можно поставить точный и ранний диагноз на основе тщательного анамнеза и тщательного медицинского осмотра, а возможные заболевания можно предотвратить с помощью соответствующего хирургического вмешательства.
Жалобы появились через 2 года после кесарева сечения у 10 (52,6%) пациентов. В основном с диагностической целью использовалось УЗИ брюшной полости. Поражения были полностью иссечены, и всем пациентам был поставлен диагноз SE путем гистопатологического исследования. Послеоперационных осложнений или рецидивов ни у одного из пациентов не было. Заключение . Подозрение на СЭ важно у женщин репродуктивного возраста, у которых в анамнезе было кесарево сечение и жалобы на образование передней брюшной стенки и боль в месте рубца, связанную с их менструальным циклом.Таким пациентам можно поставить точный и ранний диагноз на основе тщательного анамнеза и тщательного медицинского осмотра, а возможные заболевания можно предотвратить с помощью соответствующего хирургического вмешательства.
1. Введение
Эндометриоз рубцов (SE) — это относительно редкое заболевание, которое обычно развивается на коже, подкожных тканях, мускулатуре брюшной полости и тазовой стенки в месте хирургического рубца, который возникает после различных акушерских или гинекологических операций, в частности после кесарева сечения [1, 2]. Среди теорий, выдвигаемых для объяснения этиологии СЭ, наиболее широко распространенной является теория ятрогенной прямой имплантации, которая утверждает, что клетки эндометрия, отделяющиеся от матки во время операции, инокулируются на краю операционного рубца или внутри него [ 3, 4]. Общие симптомы — образование в брюшной стенке и циклическая боль, связанная с менструацией. При пальпации это образование можно спутать с липомой, абсцессом, гематомой, грыжей, гранулемой, десмоидной опухолью или саркомой [5, 6].По этой причине следует тщательно расспросить анамнез пациентов, раскрыть их историю кесарева сечения и выяснить, имеет ли их боль циклический характер. Хотя УЗИ брюшной полости (УЗИ), компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) дают неспецифическую информацию, они полезны при постановке диагноза [7]. Лечебным лечением является иссечение новообразования, которое также позволяет поставить окончательный диагноз SE посредством гистопатологического исследования.
Среди теорий, выдвигаемых для объяснения этиологии СЭ, наиболее широко распространенной является теория ятрогенной прямой имплантации, которая утверждает, что клетки эндометрия, отделяющиеся от матки во время операции, инокулируются на краю операционного рубца или внутри него [ 3, 4]. Общие симптомы — образование в брюшной стенке и циклическая боль, связанная с менструацией. При пальпации это образование можно спутать с липомой, абсцессом, гематомой, грыжей, гранулемой, десмоидной опухолью или саркомой [5, 6].По этой причине следует тщательно расспросить анамнез пациентов, раскрыть их историю кесарева сечения и выяснить, имеет ли их боль циклический характер. Хотя УЗИ брюшной полости (УЗИ), компьютерная томография (КТ) и магнитно-резонансная томография (МРТ) дают неспецифическую информацию, они полезны при постановке диагноза [7]. Лечебным лечением является иссечение новообразования, которое также позволяет поставить окончательный диагноз SE посредством гистопатологического исследования. В этом исследовании был проведен ретроспективный обзор пациентов, которых наблюдали и лечили по поводу диагноза SE в нашей клинике, и полученные результаты были представлены со ссылками на литературу.
В этом исследовании был проведен ретроспективный обзор пациентов, которых наблюдали и лечили по поводу диагноза SE в нашей клинике, и полученные результаты были представлены со ссылками на литературу.
2. Материалы и методы
2.1. Пациенты и протокол исследования
В этом исследовании последовательно участвовали 19 пациентов из европеоидной расы, оперированных с предварительным диагнозом SE в клинике общей хирургии в Трабзонской учебно-исследовательской больнице Кануни, Турция, в период с января 2010 года по январь 2017 года, и результаты патологии которых подтвердились. SE.Демографические характеристики, анамнез, количество перенесенных кесарева сечения, жалобы пациентов, возникновение этих жалоб, локализация и размер новообразования, используемые методы диагностики, используемые хирургические процедуры лечения, продолжительность пребывания в больнице и пациент все результаты были записаны.
Протокол этого исследования был одобрен местным комитетом по этике, и все пациенты подписали письменное согласие. Исследование было проведено в соответствии с принципами Хельсинкской декларации, пересмотренной в 2000 году.
Исследование было проведено в соответствии с принципами Хельсинкской декларации, пересмотренной в 2000 году.
2.2. Статистический анализ
Все статистические анализы данных выполнялись с использованием статистического пакета для социальных наук (SPSS), версия 15.0, для Windows (SPSS Inc., Чикаго, Иллинойс, США). Для сравнения использовалась описательная статистика.
3. Результаты
Средний возраст 19 пациенток составлял 30,8 года (диапазон 20-49 лет). Индексы массы тела (ИМТ) 12 (63,2%) пациентов были ≥ 25, а у 7 (36,8%) <25 (медиана: 26 (IQR: 23–29)). Всем больным выполнено кесарево сечение, 9 (47.4%) пациентов один раз, 6 (31,6%) пациентов дважды и 4 (21,0%) пациентов трижды (медиана: 2 (IQR: 1-2)).
За исключением одной пациентки, у которой SE была локализована в паховой области, у всех пациенток было образование, локализованное на передней брюшной стенке рядом с разрезом, и все они жаловались на циклические боли, начинающиеся в предменструальный период. SE был внедрен в подкожные ткани у 17 (89,5%) пациентов и в мышечные слои брюшной стенки у 2 (10,5%) пациентов. Типичная опухоль на ощупь была умеренно твердой, твердой и частично подвижной при пальпации и была размером примерно 2 × 3 см, увеличиваясь во время менструации.Жалобы появились через 1, 2, 3 и 4 года после кесарева сечения у 4 (21,1%) пациентов, 10 (52,6%) пациентов, 4 (21,1%) пациентов и 1 (5,3%) пациента соответственно (медиана: 2 (IQR: 2-3)). SE был обнаружен на правой стороне рубца у 9 (47,4%) пациентов, на левой стороне рубца у 7 (36,8%) пациентов, на срединном рубце у 2 (10,5%) пациентов и в паховой области. у 1 (5,3%) пациента. СЭ, локализованная в паховой области, приближалась к медиальной половине правой паховой области и также вызывала циклическую боль.
SE был внедрен в подкожные ткани у 17 (89,5%) пациентов и в мышечные слои брюшной стенки у 2 (10,5%) пациентов. Типичная опухоль на ощупь была умеренно твердой, твердой и частично подвижной при пальпации и была размером примерно 2 × 3 см, увеличиваясь во время менструации.Жалобы появились через 1, 2, 3 и 4 года после кесарева сечения у 4 (21,1%) пациентов, 10 (52,6%) пациентов, 4 (21,1%) пациентов и 1 (5,3%) пациента соответственно (медиана: 2 (IQR: 2-3)). SE был обнаружен на правой стороне рубца у 9 (47,4%) пациентов, на левой стороне рубца у 7 (36,8%) пациентов, на срединном рубце у 2 (10,5%) пациентов и в паховой области. у 1 (5,3%) пациента. СЭ, локализованная в паховой области, приближалась к медиальной половине правой паховой области и также вызывала циклическую боль.
Всем пациентам в диагностических целях проводилось УЗИ брюшной полости (рис. 1). Кроме того, КТ использовалась у 5 (26,3%) пациентов, а МРТ — у 3 (15,8%) пациентов (рис. 2). Повреждения были полностью иссечены хирургическим путем вместе с окружающими их здоровыми тканями размером не менее 1 см (рисунки 3 (а), 3 (b) и 3 (с)). Диагноз SE был установлен путем гистопатологического исследования у всех пациентов (рисунки 4 (a) и 4 (b)). Измерения во время патологического исследования показали, что средний диаметр новообразований SE составил 3 см (IQR: 2.5-3,5). Средняя продолжительность госпитализации составила 2 дня (IQR: 1-3). Послеоперационных осложнений ни у одного из пациентов не было. Все пациенты наблюдались, и ни у одного из них не было рецидивов (медиана: 2 года (IQR: 2-4)). Все вышеперечисленные демографические и клинические характеристики пациентов сведены в Таблицу 1.
Диагноз SE был установлен путем гистопатологического исследования у всех пациентов (рисунки 4 (a) и 4 (b)). Измерения во время патологического исследования показали, что средний диаметр новообразований SE составил 3 см (IQR: 2.5-3,5). Средняя продолжительность госпитализации составила 2 дня (IQR: 1-3). Послеоперационных осложнений ни у одного из пациентов не было. Все пациенты наблюдались, и ни у одного из них не было рецидивов (медиана: 2 года (IQR: 2-4)). Все вышеперечисленные демографические и клинические характеристики пациентов сведены в Таблицу 1.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(ИМТ: индекс массы тела, SE: эндометриоз рубцов, УЗИ: УЗИ, КТ: компьютерная томография, МРТ: магнитно-резонансная томография). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
4. Обсуждение
В этом исследовании подчеркивается пять моментов: (a) SE возникала в основном у женщин в возрасте около 30 лет, перенесших кесарево сечение, (b) большинство пациентов были ожирение с ИМТ более 25, (c) жалобы, связанные с SE, возникли через 2 года после кесарева сечения у более чем половины пациентов, (d) наиболее часто используемыми диагностическими методами были УЗИ и КТ брюшной полости, и (e) излечение было достигнуто путем хирургического массового иссечения у всех пациентов, рецидивов не наблюдалось.
SE — это патологическое состояние, часто неправильно диагностируемое с частотой от 0,03 до 1,7% [6]. В качестве общей информации, SE часто встречается у женщин репродуктивного возраста, перенесших кесарево сечение. Средний возраст пациентов в этом исследовании составлял примерно 30 лет, и все пациенты в анамнезе перенесли кесарево сечение, в основном один раз, как это было обнаружено у 9 (47,4%) пациентов. Эти результаты согласуются с информацией в литературе [8].
Эти результаты согласуются с информацией в литературе [8].
Важным моментом в возникновении СЭ является старательность хирурга при проведении хирургического вмешательства.Во время кесарева сечения околоплодным водам становится легче переносить клетки эндометрия к коже и подкожным тканям. Многие хирурги-акушеры очищают полость матки сухими или влажными тампонами после кесарева сечения. Контакт этих тампонов с местом разреза увеличивает риск заражения, и их быстрое удаление из зоны операции необходимо для предотвращения возникновения SE. Есть два важных момента, о которых следует соблюдать осторожность во время операции. Первый — это формирование физического барьера путем наложения брюшных компрессов на подкожную ткань и кожу перед открытием полости матки для защиты хирургических полей и недопущения повторного использования уже использованных хирургических инструментов, таких как иглодержатели, щипцы и шовные материалы при наложении швов. матка для закрытия мышц, фасций, подкожных тканей и кожи. Вторым важным моментом является орошение кожи, подкожных тканей, мышц и фасций после наложения швов в полости матки путем промывания их физиологическим раствором под давлением перед продолжением закрытия брюшной полости, убедившись, что в подкожной области не осталось мертвого пространства. Хотя настоящее исследование не выявило из-за его ретроспективного характера, были ли приняты вышеупомянутые защитные меры, мы полагаем, что эти вышеупомянутые умозрительные практики могут предотвратить имплантацию эпителиальных и железистых клеток эндометрия в мышцы, подкожные ткани, кожу и следовательно, препятствуют образованию SE.
Вторым важным моментом является орошение кожи, подкожных тканей, мышц и фасций после наложения швов в полости матки путем промывания их физиологическим раствором под давлением перед продолжением закрытия брюшной полости, убедившись, что в подкожной области не осталось мертвого пространства. Хотя настоящее исследование не выявило из-за его ретроспективного характера, были ли приняты вышеупомянутые защитные меры, мы полагаем, что эти вышеупомянутые умозрительные практики могут предотвратить имплантацию эпителиальных и железистых клеток эндометрия в мышцы, подкожные ткани, кожу и следовательно, препятствуют образованию SE.
Тот факт, что большинство пациентов в нашем исследовании имели ИМТ 25 и выше, предполагает, что частота SE может быть выше у женщин с ожирением. Поскольку подкожная жировая клетчатка на передней брюшной стенке толще и покрывает большую площадь у пациентов с ожирением, это может быть фактором, способствующим имплантации тканей эндометрия.
В этом исследовании жалобы пациентов с SE в основном начинались через 2 года после кесарева сечения. Это может дать представление о том, сколько времени требуется эндометриальным клеткам, железам и строме, имплантированным во время кесарева сечения, чтобы локализоваться в коже и подкожных тканях, пролиферировать, образовывать массу и, достигнув определенного размера, реагировать на стимуляция гормона яичников во время менструального цикла, что приводит к отеку и циклической боли.
Это может дать представление о том, сколько времени требуется эндометриальным клеткам, железам и строме, имплантированным во время кесарева сечения, чтобы локализоваться в коже и подкожных тканях, пролиферировать, образовывать массу и, достигнув определенного размера, реагировать на стимуляция гормона яичников во время менструального цикла, что приводит к отеку и циклической боли.
В единственном случае, когда SE была локализована в паховой области, расстояние между разрезом и местом локализации предполагает, что образование SE у этого пациента произошло не в результате имплантации, а в результате гематогенного или лимфатического распространения [9].
У пациентов с сомнительным диагнозом СЭ другие патологии, в том числе липома, послеоперационная грыжа, шовная гранулема и опухоли брюшной стенки, должны рассматриваться для дифференциальной диагностики [6, 10, 11]. В таком случае для диагностики следует использовать дополнительные радиологические процедуры.Первый выбор — это УЗИ брюшной полости, довольно практичный и легкодоступный метод, который предоставляет информацию о размере, расположении, краях и внутренней структуре поражения [11–13]. При УЗИ-сканировании поражения SE обычно выглядят как гетерогенные, гипоэхогенные, твердые и круглые / овальные узелки с неправильными краями. Помимо помощи в диагностике, КТ и МРТ могут выявить ассоциацию новообразования с брюшной полостью и сыграть важную роль в исключении других поражений во время дифференциальной диагностики [13].Чаще всего УЗИ с последующей КТ или МРТ также использовались на этапе диагностики и в нашем исследовании. Использование только УЗИ без последующей КТ или МРТ не приведет к окончательному диагнозу и будет связано с риском пропуска других патологий. КТ и МРТ очень помогли выявить локализацию и размер пальпируемого образования на передней брюшной стенке, его взаимосвязь с окружающими тканями, а также наличие каких-либо других патологий в брюшной полости [6, 13]. Мы считаем, что КТ или МРТ следует более активно использовать у пациентов, которые прошли УЗИ, но чей диагноз СЭ остается подозрительным.Однако невозможно поставить окончательный диагноз, используя только эти радиологические исследования.
При УЗИ-сканировании поражения SE обычно выглядят как гетерогенные, гипоэхогенные, твердые и круглые / овальные узелки с неправильными краями. Помимо помощи в диагностике, КТ и МРТ могут выявить ассоциацию новообразования с брюшной полостью и сыграть важную роль в исключении других поражений во время дифференциальной диагностики [13].Чаще всего УЗИ с последующей КТ или МРТ также использовались на этапе диагностики и в нашем исследовании. Использование только УЗИ без последующей КТ или МРТ не приведет к окончательному диагнозу и будет связано с риском пропуска других патологий. КТ и МРТ очень помогли выявить локализацию и размер пальпируемого образования на передней брюшной стенке, его взаимосвязь с окружающими тканями, а также наличие каких-либо других патологий в брюшной полости [6, 13]. Мы считаем, что КТ или МРТ следует более активно использовать у пациентов, которые прошли УЗИ, но чей диагноз СЭ остается подозрительным.Однако невозможно поставить окончательный диагноз, используя только эти радиологические исследования. Окончательный диагноз SE ставится после того, как гистопатологическое исследование хирургически удаленной ткани ясно показало присутствие в ткани гладкомышечных клеток эндометрия, стромы, желез и макрофагов, нагруженных гемосидерином.
Окончательный диагноз SE ставится после того, как гистопатологическое исследование хирургически удаленной ткани ясно показало присутствие в ткани гладкомышечных клеток эндометрия, стромы, желез и макрофагов, нагруженных гемосидерином.
Окончательное лечение достигается за счет полного хирургического удаления новообразования SE вместе как минимум с 1 см окружающей здоровой ткани без нарушения целостности новообразования.Это удаление предотвращает возникновение потенциального злокачественного перерождения или рецидива. В литературе сообщается, что послеоперационный рецидив составляет 1,5-9,1%; За время наблюдения у наших пациентов рецидивов не наблюдалось [8]. Благодаря хирургическому удалению, выполненному у всех пациентов в нашем исследовании, было достигнуто излечение, и окончательный диагноз SE был поставлен гистопатологическим путем.
Ограничения этого исследования включают его ретроспективный характер, небольшой размер выборки только из одного центра и отсутствие информации о том, сколько времени потребовалось для возобновления регулярных менструальных циклов после кесарева сечения. Дальнейшие проспективные исследования будут полезны для внесения вклада в эти выводы.
Дальнейшие проспективные исследования будут полезны для внесения вклада в эти выводы.
5. Заключение
SE следует всегда рассматривать у женщин репродуктивного возраста, у которых в анамнезе имеется кесарево сечение, боль в месте рубца, связанная с менструальным циклом, и образование на передней брюшной стенке. Точная и ранняя диагностика может быть достигнута у таких пациентов при тщательном анамнезе и хорошем физикальном обследовании, а качество их жизни может быть улучшено с помощью быстрого хирургического вмешательства.Поскольку в последние годы частота кесарева сечения постоянно увеличивается, в ближайшем будущем можно чаще сталкиваться с SE. Следовательно, для профилактики СЭ важно увеличивать и расширять образование, которое повысило бы осведомленность акушеров и гинекологических хирургов.
Доступность данных
Данные, использованные для подтверждения выводов этого исследования, в настоящее время находятся под запретом, а результаты исследований коммерциализируются. Запросы данных через 6/12 месяцев после публикации статьи будут рассмотрены соответствующим автором.
Запросы данных через 6/12 месяцев после публикации статьи будут рассмотрены соответствующим автором.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Боль в животе после обходного желудочного анастомоза: подозрения и решения
Am J Surg. Авторская рукопись; доступно в PMC 2012 1 июня.
Опубликован в окончательной отредактированной форме как:
PMCID: PMC3123682
NIHMSID: NIHMS235524
Департамент хирургии, Орегонский университет здоровья и науки, Портленд, OR
Для корреспонденции: Роберт У.О’Рурк, доктор медицины, Орегонский университет здоровья и науки, отдел хирургии, L-223A, 3181 SW Sam Jackson Park Rd, Портленд, штат Орегон, 97239-3098, США, телефон: 503-494-2681; Факс: 503-494-8884; ude.usho@orkruoro Окончательная отредактированная версия этой статьи издателем доступна на сайте Am J Surg См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Введение
Шунтирование желудка остается основой хирургической терапии ожирения. Боль в животе после обходного желудочного анастомоза является обычным явлением и составляет до половины всех послеоперационных жалоб и обращений в отделение неотложной помощи.В этой рукописи рассматриваются наиболее важные причины боли в животе, характерные для обходного желудочного анастомоза, и обсуждаются рекомендации по лечению.
Боль в животе после обходного желудочного анастомоза является обычным явлением и составляет до половины всех послеоперационных жалоб и обращений в отделение неотложной помощи.В этой рукописи рассматриваются наиболее важные причины боли в животе, характерные для обходного желудочного анастомоза, и обсуждаются рекомендации по лечению.
Источники данных
Текущая хирургическая литература была проанализирована с помощью PubMed с акцентом на боль в животе после желудочного обходного анастомоза и известные патологии, лежащие в основе ее патогенеза.
Выводы
Дифференциальный диагноз боли в животе после желудочного обходного анастомоза обширен и включает доброкачественные и опасные для жизни состояния.Его разнообразные причины требуют широкой оценки, которая должна определяться анамнезом и клиническими проявлениями. При отсутствии четкого диагноза порог хирургического вмешательства у пациентов с абдоминальной болью после желудочного обходного анастомоза должен быть низким.
Ключевые слова: Ожирение, внутренняя грыжа, лапароскопия, боль в животе, желудочный обходной анастомоз
Введение, эпидемиология
Число операций обходного желудочного анастомоза, выполняемых ежегодно в США, резко увеличилось за последнее десятилетие и приближается к 200000 (1 ).Хотя преимущества обходного желудочного анастомоза очевидны, этот взрыв популярности связан с конечной заболеваемостью. Боль в животе — одна из самых частых и неприятных проблем после желудочного обходного анастомоза. От 15 до 30% пациентов обращаются в отделение неотложной помощи или нуждаются в госпитализации в течение трех лет после желудочного обходного анастомоза, и боль в животе является основной жалобой более чем в половине этих случаев (2-4). Клинические проявления сильно различаются, и оценка может быть затруднена тем фактом, что пациенты с ожирением ощущают абдоминальные симптомы сильнее, чем худые (5).Дифференциальный диагноз абдоминальной боли после желудочного обходного анастомоза разнообразен и представляет собой диагностические и терапевтические проблемы. Тем не менее, важность полного понимания этих разнообразных этиологий подчеркивается в едином отчете центра, в котором документируется снижение числа повторных госпитализаций после желудочного обходного анастомоза в течение многих лет с изменениями в оперативной технике, основанными на наблюдении за причинами повторной госпитализации (4). Таким образом, понимание патогенеза боли в животе после желудочного обходного анастомоза может положительно повлиять на исход.В этом обзоре основное внимание уделяется причинам абдоминальной боли, характерной для обходного желудочного анастомоза (), но, конечно же, необходимо помнить о других несвязанных патологических процессах, таких как аппендицит, мезентериальная ишемия и другие «небариатрические» состояния.
Тем не менее, важность полного понимания этих разнообразных этиологий подчеркивается в едином отчете центра, в котором документируется снижение числа повторных госпитализаций после желудочного обходного анастомоза в течение многих лет с изменениями в оперативной технике, основанными на наблюдении за причинами повторной госпитализации (4). Таким образом, понимание патогенеза боли в животе после желудочного обходного анастомоза может положительно повлиять на исход.В этом обзоре основное внимание уделяется причинам абдоминальной боли, характерной для обходного желудочного анастомоза (), но, конечно же, необходимо помнить о других несвязанных патологических процессах, таких как аппендицит, мезентериальная ишемия и другие «небариатрические» состояния.
Таблица 1
Причины боли в животе после обходного желудочного анастомоза
| Поведенческие расстройства, диетические расстройства | Функциональные расстройства | Расстройства желчевыводящих путей | Сумка, остаточные расстройства желудка | Другие расстройства тонкого кишечника | Переедание, быстрое питание | Запор, диарея, метеоризм | Холелитиаз: колики, холецистит | Язвенная болезнь | Грыжи брюшной стенки: вентральные, троакар | Инфаркт сальника | Инфаркт сальника : холангит, панкреатитЖелудочно-желудочный свищ | Спайки | Синдром СМА |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Дефицит микронутриентов | Нарушения моторики пищевода | Сфинктер внутренней дисфункции Одди 9025ER 9025ER 251 | Безоар | ||||||||||
| Микронутриентные добавки | Синдром демпинга | Грыжа пищеводного отверстия диафрагмы | Инвагинация | ||||||||||
| Гастроеюно-адреналиновый стеноз | Распространенное нарушение пищеварения | Мижеуноэтозное нарушение пищеварения | причина болей в животе в раннем послеоперационном периоде. Обходной желудочный анастомоз влияет на чувство насыщения, и пациенты могут не ощущать наполнения желудка до тех пор, пока мешок не растянется до боли. Такая боль обычно бывает эпигастральной и постпрандиальной, и тщательный диетический анамнез обычно выявляет корреляцию с быстрым приемом пищи. Изменение поведения, чтобы есть медленно и использовать определенные размеры порций, приносит облегчение. Такие проблемы редко сохраняются более шести месяцев после операции, после которой большинство пациентов усваивают правильное пищевое поведение. Обходной желудочный анастомоз влияет на чувство насыщения, и пациенты могут не ощущать наполнения желудка до тех пор, пока мешок не растянется до боли. Такая боль обычно бывает эпигастральной и постпрандиальной, и тщательный диетический анамнез обычно выявляет корреляцию с быстрым приемом пищи. Изменение поведения, чтобы есть медленно и использовать определенные размеры порций, приносит облегчение. Такие проблемы редко сохраняются более шести месяцев после операции, после которой большинство пациентов усваивают правильное пищевое поведение. Определенные продукты питания могут вызывать временную закупорку и вызывать боль.Чаще всего это происходит в течение шести месяцев после операции, и частота такой непереносимости может увеличиваться при использовании обходного желудочного анастомоза (6). Такая пищевая непереносимость очень индивидуальна, что затрудняет обобщение в отношении конкретных продуктов. Тем не менее, гигроскопичные продукты, такие как рис, макароны и хлеб, или волокнистые продукты, такие как мясо, некоторые овощи и фрукты, являются частыми виновниками, и их следует есть в небольших количествах или вовсе избегать. Избыточный бактериальный рост в неработающем желудке или тонком кишечнике может вызвать боль в животе и другие неспецифические желудочно-кишечные симптомы (8). Недавние исследования указывают на то, что чрезмерный бактериальный рост в кишечнике после желудочного обходного анастомоза приводит к усилению воспаления (9).Кроме того, в одном исследовании манипулирование кишечной флорой с помощью пробиотиков улучшило потерю веса после желудочного обходного анастомоза (10). Однако, помимо этих данных, механизмы, связывающие флору кишечника с клиническим заболеванием, плохо изучены, а причинно-следственная связь между избыточным бактериальным ростом и клинически значимой патологией желудочно-кишечного тракта после желудочного обходного анастомоза остается неопределенной (11). Функциональные расстройства Функциональные расстройства моторики желудочно-кишечного тракта могут вызывать боль в животе после желудочного обходного анастомоза.Ожирение является независимым фактором риска множественной моторики и других функциональных нарушений желудочно-кишечного тракта (14, 15), и хирургическое вмешательство может усугубить ранее существовавшее субклиническое заболевание. Запор часто встречается в раннем послеоперационном периоде и может быть связан с болью в животе, которая обычно локализуется в нижней части живота и носит диффузный и спастический характер.Запор может возникнуть в результате обезвоживания в раннем послеоперационном периоде, а слабительные и повышенное потребление воды обеспечивают простые решения. Шунтирование желудка реже вызывает диарею и / или увеличение количества газов, что может быть связано с болью в животе (16). Эти симптомы, вероятно, являются результатом легкой степени мальабсорбции и потери остатка желудка в качестве хранилища для проглоченного воздуха. Разумное использование пищевых добавок и противодиарейных препаратов может облегчить диарею, в то время как лекарства на основе симетикона могут облегчить чрезмерное выделение газов. Более сложные функциональные расстройства не так легко поддаются лечению. Ожирение является фактором риска синдрома раздраженного кишечника (17). Пациенты с хроническим запором или синдромом раздраженного кишечника в анамнезе должны быть предупреждены о том, что эти симптомы могут ухудшиться после желудочного обходного анастомоза, хотя практически нет данных, документирующих долгосрочное влияние обходного желудочного анастомоза на синдром раздраженного кишечника. Расстройства моторики пищевода также увеличиваются по распространенности при ожирении (15, 18) и могут вызывать боль после желудочного обходного анастомоза, которая обычно локализуется под грудной клеткой.Манометрия пищевода помогает в диагностике, хотя результаты часто неспецифичны. Интересно, что многие люди с ожирением демонстрируют перистальтические сокращения с высокой амплитудой, что указывает на синдром, похожий на пищевод щелкунчика (18), состояние, обычно связанное с болью. Демпинг-синдром характеризуется разнообразными симптомами, включая постпрандиальную тошноту, головокружение, приливы крови и тахикардию. Заболевание желчевыводящих путейЖелчная колика — хорошо известная причина боли в животе после желудочного обходного анастомоза. Сильная потеря веса после бариатрической операции может способствовать увеличению литогенности желчи и является широко признанным фактором риска холелитиаза.В то время как распространенность холелитиаза после бариатрических операций может превышать 40% в некоторых исследованиях (27–30), добавление профилактики урсодиолом в современную эпоху снижает эти показатели распространенности до менее 3% (27, 31). Роль сопутствующей профилактической холецистэктомии во время желудочного обходного анастомоза продолжает обсуждаться. Большинство хирургов не проводят профилактическую холецистэктомию, хотя ее делают до 30% (32). Хотя сторонники этой операции утверждают, что холецистэктомия безопасна (30, 33), большинство данных демонстрируют, что в ней нет необходимости с точки зрения соотношения риск-польза и затраты (29, 34, 35).Мы считаем, что холецистэктомия показана пациентам с бариатрической операцией только в контексте симптоматической желчнокаменной болезни, как и у небариатрических пациентов. В поддержку этого подхода большинство исследований демонстрируют низкую частоту прогрессирования холелитиаза в клиническое заболевание (28). Кроме того, как и у других пациентов, желчная колика является предвестником симптомов у большинства пациентов после желудочного обходного анастомоза. Кроме того, похудание, вызванное хирургическим вмешательством, вероятно, повысит безопасность отсроченной холецистэктомии, если в этом возникнет необходимость.Наконец, появление урсодиола еще больше поддерживает выжидательную тактику. Шесть месяцев послеоперационной терапии урсоидолом — это широко используемый режим, поддерживаемый консенсусным заявлением многих обществ (36). Холедохолитиаз и его последствия, включая холангит и желчнокаменный панкреатит, нечасто вызывают боль в животе после обходного желудочного анастомоза. Доступность специальных знаний определяет предпочтительное терапевтическое вмешательство, а анатомия конечностей по Ру привела к разработке различных подходов к доступу к желчевыводящему дереву.К ним относятся лапароскопическое исследование общего желчного протока, чрескожная чреспеченочная инструментация общего желчного протока, пероральная эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ) с использованием специализированных эндоскопов, чрескожная или лапароскопическая трансгастральная ЭРХПГ и трансентериальная ЭРХПГ (37-39). Как только доступ будет достигнут, выполняется удаление камня и другие процедуры. Такие методы, хотя и эффективны, требуют значительного опыта, поэтому лапароскопическое или открытое исследование общего желчного протока является наиболее разумной стратегией для пациентов, которым требуется экстренное вмешательство. Дисфункция сфинктера Одди — редкая причина боли в животе после желудочного обходного анастомоза. Для диагностики используется стимулированная секретином магнитно-резонансная холангиопанкреатография, а хирургическая трансдуоденальная панкреатическая сфинктеропластика является подходящей терапией (40). Заболевание, связанное с мешочкомРяд проблем может повлиять на желудочный мешок после обходного желудочного анастомоза и вызвать боль в животе, включая язвенную болезнь, фистулу, рефлюксную болезнь и стеноз. Язвенная болезньЯзвенная болезнь желудочного мешка или гастроеюнального анастомоза может возникнуть в любой момент после желудочного обходного анастомоза и встречается у 2-15% пациентов (41, 42).Желудочно-желудочный свищ, задержанные париетальные клетки мешочка и чрезмерное натяжение анастомоза были вовлечены в качестве причин. Желудочно-желудочный свищ был более распространен в эпоху неразделенного желудочного обходного анастомоза, с зарегистрированными показателями до 50% (43, 44). Появление степлеров с линейной резкой привело к повсеместному внедрению разделенного обходного желудочного анастомоза, что значительно снизило частоту возникновения свищей до нынешних показателей 0-6% (45, 46). Гастрогастральные свищи в современную эпоху часто являются результатом неполного отделения мешка от остаточного желудка при первоначальной операции.Желудочно-желудочный свищ вызывает язвенную болезнь из-за кислоты из остаточного желудка, проникающей через свищ в желудочный мешок. Верхний отдел желудочно-кишечного тракта является предпочтительным диагностическим исследованием. Визуализация мелких свищей с помощью эндоскопии может быть затруднена, и поэтому представляет собой вторичный диагностический тест. Свищи чаще бывают маленькими и являются причиной язвенной болезни, а не большими и причиной восстановления веса и могут долгое время оставаться нераспознанными у пациентов с рефрактерной язвенной болезнью. Недавние исследования эндоскопической инъекции фибринового клея демонстрируют многообещающие перспективы, но обычно требуется хирургическое вмешательство (43). Анатомия сумки изменилась за последние десятилетия. Ранние желудочные мешочки были горизонтальными и располагались на основе глазного дна, что позволяло использовать податливые ткани глазного дна для создания анастомоза. Повышенная податливость глазного дна привела к тому, что мешочки были большими и малоподвижными, что затрудняло опорожнение и способствовало плохой потере веса. Это привело к переходу к мешочкам с «меньшей кривой», введенным в начале 1980-х годов, в которых длинный и узкий мешочек создается вдоль меньшего изгиба живота (47).Это изменение морфологии мешка уменьшило его расширение, но привело к увеличению язвенной болезни анастомоза из-за увеличения париетальных клеток, расположенных на дистальной части малой кривизны, которые сохраняются в желудочном мешочке. (48). Создание еще меньших, «более коротких» (в направлении от головы к кауде) мешочков на основе меньшего изгиба, таким образом, может уменьшить язвенную болезнь за счет удаления сохраненных париетальных клеток мешочка вдоль меньшего изгиба (49, 50). Язвенная болезнь может развиться в любое время после желудочного обходного анастомоза и редко проявляется перфорацией (51).Боль — наиболее распространенный симптом, который обычно носит эпигастральный характер, имеет жгучий характер и часто возникает сразу после приема пищи, вторичный по отношению к прохождению пищи, раздражающей язву. Верхняя эндосокопия позволяет поставить окончательный диагноз. Язвенная болезнь обычно поддается медикаментозной терапии (41). Стойкая язвенная болезнь при отсутствии желудочно-желудочного свища, не поддающаяся лечению, может быть результатом чрезмерного хронического натяжения анастомоза или большого количества сохраненных париетальных клеток мешочка.В таких случаях может потребоваться ревизионная операция, которая состоит из резекции дистального язвенного мешка и ревизии гастроеюнального анастомоза. К конечности Ру могут применяться удлиняющие маневры для уменьшения напряжения по мере необходимости, например, удлинение брыжеечного расщепления или преобразование в ретроколическое положение. Такие ревизионные операции связаны со значительной заболеваемостью и должны выполняться хирургами, обладающими соответствующими знаниями (52). Менее распространенные причины язвенной болезни включают прием НПВП, H.pylori и инородный материал, такой как скобки или шовный материал. Хотя большинство клиницистов рекомендуют предоперационный скрининг и лечение инфекции H. pylori (53, 54), эффективность этой практики в снижении клинической картины язвенной болезни и ее осложнений сомнительна (53, 55). Следует избегать использования нерассасывающихся швов при создании желудочно-кишечного анастомоза, поскольку это связано с повышенным риском развития язвы анастомоза (56, 42). Наконец, язвенная болезнь также может поражать остаточный желудок или двенадцатиперстную кишку.Двойная баллонная энтероскопия или энтероскопия с замком формы использовалась для исследования двенадцатиперстной кишки и остаточного желудка (57, 58). Однако такие методы широко не применяются, и поэтому лечение подозреваемой язвенной болезни остаточного желудка часто носит эмпирический характер. Гастроэзофагеальная рефлюксная болезнь и грыжа пищеводного отверстия диафрагмыОжирение является независимым фактором риска гастроэзофагеальной рефлюксной болезни (ГЭРБ). К счастью, желудочный обходной анастомоз приводит к ремиссии уже существовавшей ГЭРБ у более чем 85% пациентов из-за отвода желудочного содержимого из желудочно-пищеводного перехода (59, 60).Стойкая ГЭРБ после желудочного обходного анастомоза обычно не так серьезна, как ранее существовавшее заболевание, и чаще всего связана либо с сохранением париетальных клеток мешочка, либо с фистулой, как обсуждалось выше. Рефлюкс желчи также считается причиной ГЭРБ после желудочного обходного анастомоза (61). Грыжа пищеводного отверстия диафрагмы способствует развитию ГЭРБ у пациентов с ожирением до и после желудочного обходного анастомоза. Распространенность грыжи пищеводного отверстия диафрагмы увеличивается при ожирении, и этот анатомический дефект может быть недооценен и недолечен во время первичного обходного желудочного анастомоза.Как и при первичной ГЭРБ, медикаментозная терапия приносит облегчение большинству пациентов. Было показано, что плановая пластика грыжи пищеводного отверстия диафрагмы в небольших сериях облегчает боль в животе и другие симптомы ГЭРБ после желудочного обходного анастомоза (62). СтенозСтеноз анастомоза чаще всего проявляется в течение трех месяцев после операции с частотой от 3 до 20%, чаще всего от 5 до 10% (63, 64). Стеноз характеризуется дисфагией и не является частой причиной боли как таковой, но может сопровождать язвенную болезнь, несостоятельность анастомоза или другие патологии сумки, которые связаны с болью.Изолированный стеноз редко является причиной значительной боли в животе, и если боль является доминирующим симптомом, следует искать другую патологию. Стеноз, по-видимому, чаще встречается после желудочно-кишечного анастомоза, наложенного циркулярными скобами (64). Серия UGI может быть двусмысленной, поэтому предпочтительным диагностическим тестом является эндоскопия. Эндоскопическая баллонная дилатация обеспечивает эффективное лечение большинства пациентов. Редким пациентам, невосприимчивым к дилатации, может потребоваться хирургическое вмешательство. Заболевания тонкой кишкиОсложнения тонкой кишки, вызывающие боль в животе после обходного желудочного анастомоза, включают вентральные грыжи и грыжи в области троакара, спаечную болезнь, внутренние грыжи и, в редких случаях, инвагинацию. Послеоперационная грыжа, спаечные процессыВ то время как большие вентральные (послеоперационные) грыжи были устранены лапароскопической бариатрической хирургией, у пациентов с болью в животе после обходного желудочного анастомоза всегда следует учитывать наличие троакарных грыж. Грыжи в месте расположения троакара возникают в 0–1% случаев после желудочного обходного анастомоза (65, 66), хотя это, вероятно, заниженная информация. Компьютерная томография может быть необходима для установления диагноза грыжи в области троакара у пациента с толстой подкожной жировой подушечкой на брюшной стенке.При антеколической реконструкции конечность Ру лежит непосредственно под брюшной стенкой и особенно подвержена ущемлению при троакарных грыжах, а конфигурация Рихтера может затруднить диагностику. Лечение обычно осуществляется лапароскопическим методом. Для профилактики мы используем троакары, расширяющиеся в радиальном направлении, и имеем низкий порог первичного фасциального закрытия участков троакаров. Спаечная непроходимость тонкой кишки — редкость в эпоху лапароскопии, с частотой 0,2–1%, но всегда должна рассматриваться как причина боли в животе после обходного желудочного анастомоза (67, 68).Еюноэуноанастомоз представляет собой обычный очаг образования спаек. Слипчивую непроходимость тонкой кишки после лапароскопического обходного желудочного анастомоза часто можно лечить с помощью лапароскопического доступа. Внутренняя грыжаВнутренняя грыжа — важная причина боли в животе после желудочного обходного анастомоза с частотой от 1 до 9% (69-76). Хотя факторы риска четко не определены, считается, что внутренняя грыжа чаще всего возникает в течение двух-трех лет после первичного желудочного обходного анастомоза, часто в контексте значительной потери веса.Другие сообщения предполагают, что беременность может предрасполагать к внутренней грыже, предположительно вторичной по отношению к изменениям внутрибрюшной анатомии из-за расширяющейся матки (77). Типы внутренней грыжиБольшинство конечностей Ру при обходном желудочном анастомозе располагаются антеколическим, в то время как меньшая часть являются ретроколическими, ретрогастральными и еще меньше — ретроколическими, антегастральными. Эти разные анатомии связаны с разными типами внутренних грыж (). Практически любой сегмент тонкой кишки может ущемляться при любом типе внутренней грыжи, хотя часто поражается желчная конечность, а большая длина желчной конечности может быть связана с повышенным риском грыжи (70).Брыжеечная грыжа создается путем рассечения брыжейки тощей кишки при тощеностомии и присутствует во всех типах реконструкций. Грыжа Петерсена в антеколической реконструкции ограничена конечностью Ру и ее брыжейкой спереди / снизу и поперечной ободочной кишкой и ее брыжейкой сзади / дорсально. При ретроколической конфигурации дефект Петерсена находится между конечностью Ру и брыжейкой толстой кишки, расположенной ниже (каудой) до входа конечности Ру через мезоколенный дефект.Мезоколенная грыжа пересекает дефект поперечной брыжейки ободочной кишки при ретроколической реконструкции. В серии ретроколических обходных анастомозов мезоколезные грыжи составляют большинство внутренних грыж (69, 74), поэтому считается, что антегастральная реконструкция приводит к меньшему количеству грыж в целом и является доминирующим доступом (78). Наконец, необычный участок внутренней грыжи находится между конечностями тощей кишки дистальнее конца линии скобки и проксимальнее дистального фиксирующего шва, используемого для создания тощей кишки из стороны в сторону (79).Профилактика заключается в том, чтобы убедиться, что линия скобок полностью проходит по фиксирующим швам. Анатомия внутренней грыжи обходного желудочного анастомозаПоказана антеколическая конфигурация конечности по Ру, стрелки указывают на брыжеечную грыжу и грыжу Петерсена. Плановое закрытие внутренних грыжевых дефектовВопрос о профилактическом закрытии внутренних грыжевых дефектов во время первичного обходного желудочного анастомоза вызывает много споров. Эффективность такого закрытия сомнительна: закрытие швов мезентериального жира является тонким и не заживает, а скорее оставляет шрамы или спайки; лапароскопия связана с меньшим количеством спаек, что может предрасполагать к несостоятельности этих закрытий.Кроме того, при похудании могут открыться ранее закрытые дефекты из-за потери жира в брыжейке. Хотя некоторые выступают за рутинное закрытие (78), литература в целом не демонстрирует однозначно снижение частоты внутренних грыж при такой практике. Серии без закрытия и другие с обычным закрытием сообщают об аналогичных случаях в диапазоне от 0,2 до 9% (72-76). Несмотря на эти дебаты, обычное закрытие не вызывает затруднений и связано с низкой заболеваемостью, и по этим причинам мы поддерживаем эту практику. Обращение, диагностика, лечение внутренней грыжиВнутренняя грыжа обычно связана с диффузной, эпизодической, сильной болью в животе, которая длится несколько часов и может быть или не быть постпрандиальной. Боль может продолжаться месяцами у тех, кто не обращается за лечением, но всегда присутствует риск тюремного заключения. В случае билиопанкреатической обструкции конечности запор может отсутствовать, что еще больше затрудняет диагностику. КТ-признаки внутренней грыжи имеют различные прогностические значения, а признаки непроходимости кишечника могут отсутствовать до тех пор, пока ущемление не станет неизбежным.«Признак мезентериального завихрения» имеет чувствительность от 78% до 100% и специфичность от 80 до 90% (80-82) (). Другие результаты КТ менее специфичны и демонстрируют плохое согласие между наблюдателями. Высокая частота отрицательных изображений может быть связана с тем, что сканирование не может быть получено во время эпизода лишения свободы или что ущемление короткого сегмента билиарной конечности может не вызвать заметного расширения тонкой кишки. По этим причинам сильная боль в животе у пациента с предшествующим желудочным обходным анастомозом требует хирургического вмешательства, если не установлен четкий альтернативный диагноз.Хотя конкретные технические аспекты хирургического лечения внутренних грыж выходят за рамки данного обзора, уменьшение грыж и устранение дефектов с помощью нерассасывающегося шва обычно можно выполнить с помощью лапароскопического доступа. Заключение, которое во многих случаях является временным, может не быть обнаружено при обследовании, но закрытие дефектов, тем не менее, дает хорошие результаты с облегчением боли у большинства пациентов. Например, Gandhi et al. изучили более 700 пациентов с обходным желудочным анастомозом за пятилетний период 27 (3.8%) из которых развилась послеоперационная непроходимость тонкой кишки. У всех этих пациентов в анамнезе были боли в животе, вздутие живота и тошнота. В течение последнего года исследования плановое лапароскопическое обследование с закрытием дефектов было предложено 9 пациентам с аналогичными симптомами, которые впоследствии были купированы у всех пациентов (83). Agaba et al. изучили 1500 пациентов, у 75 из которых подозревались внутренние грыжи. Исследовательская лапароскопия выявила внутреннюю грыжу у 98% пациентов с диагностической КТ и у 69% пациентов с недиагностической КТ.Следует отметить, что лапароскопия выявила излечимый альтернативный диагноз у всех последних пациентов (84). Наконец, из 13 пациентов, которым была выполнена диагностическая лапароскопия по поводу боли после желудочного обходного анастомоза, у 11 была излечимая причина боли, включая внутреннюю грыжу у четырех (85). Эти данные подтверждают низкий порог исследования необъяснимой боли в животе после желудочного обходного анастомоза. Признак мезентериального завихрениястрелка указывает на признак завихрения ИнвагинацияИнвагинация — редкая причина боли в животе после желудочного обходного анастомоза, встречающаяся с частотой около 0.1% (86). Инвагинация может возникнуть через месяцы или годы после обходного желудочного анастомоза и связана с тошнотой, рвотой, болями в животе и непроходимостью кишечника (87). Как и внутренняя грыжа, инвагинация может быть преходящей и хронической. Инвагинация часто бывает ретроградной, при этом тощееюноанастомоз выступает в качестве ведущей точки и прогрессирует в проксимальном направлении вдоль пищеварительной или билиопанкреатической конечности. Сообщалось также об антеградной инвагинации (88). Измененные мигрирующие двигательные комплексы из-за эктопических миоэлектрических кардиостимуляторов в конечности Ру были вовлечены как возможная причина (89).Обычные снимки брюшной полости, контрастные исследования желудочно-кишечного тракта и УЗИ брюшной полости — ненадежные диагностические инструменты. Компьютерная томография может выявить «целевой признак» или расширенный исключенный желудок, но эти результаты относительно нечувствительны (90). Высокий уровень клинического подозрения в контексте показаний к операции, включая непроходимость или сильную боль, требует проведения обследования. Удушение требует резекции. При отсутствии удушения приемлемыми подходами являются резекция или репозиция и складка, и большинство хирургов отдают предпочтение первому (87). Менее распространенные виновникиСтеноз еюноеюностомии может вызывать боль в животе и встречается примерно в 0,5% случаев (91). Использование более длинных (60 мм) линейных степлеров может свести к минимуму это осложнение. В то время как ранний стеноз еюноеюностомии может быть вызван отеком и часто поддается выжидательному лечению (92), хирургическая ревизия анастомоза может потребоваться в позднем послеоперационном периоде. Эндоскопическая дилатация с использованием двойной баллонной энтероскопии представляет собой альтернативу хирургическому вмешательству.Перекрут и / или инфаркт сальника — редко встречающаяся причина боли в животе после обходного желудочного анастомоза, обычно возникающая из-за деления сальника, выполненного при антеколической реконструкции (93, 94). Профилактика состоит из тщательного медиального разделения сальника и резекции деваскуляризованного сальника по мере необходимости. Синдром верхней брыжеечной артерии редко сообщается после желудочного обходного анастомоза и может поддаваться лапароскопической дуоденоеюностомии (95). Безоары в мешочке или где-либо еще — редкая причина боли в животе и непроходимости после обходного желудочного анастомоза (96, 97). Общий диагностический подход, выводыУчитывая широкий спектр дифференциального диагноза у пациента с абдоминальной болью после желудочного обходного анастомоза, диагностические алгоритмы должны быть гибкими и основываться на истории болезни и физикальном обследовании. Тщательный диетический и пищевой анамнез, а также химический состав сыворотки и уровни витаминов могут выявить поведенческие или пищевые причины боли, которые часто легко поддаются лечению. Однако большинству пациентов потребуется ЭГДС и компьютерная томография, которые во многих случаях являются хорошими начальными тестами, позволяющими поставить диагноз.Если EGD и CT не являются диагностическими, могут быть показаны серия UGI, ультразвуковое исследование и манометрия пищевода в зависимости от клинической картины. У пациентов с подозрением на заболевание этих систем органов следует рассмотреть возможность более сложных эндоскопических и лапароскопических вмешательств для изучения желчного дерева или остаточного желудка. При отрицательной диагностической оценке следует рассмотреть возможность проведения исследовательской лапароскопии. Боль в животе после желудочного обходного анастомоза — важная проблема общественного здравоохранения, которая представляет собой серьезные диагностические и терапевтические проблемы.Его разнообразные причины требуют широкой оценки, которая должна определяться анамнезом и клиническими проявлениями. При отсутствии четкого диагноза порог хирургического вмешательства должен быть низким. Наконец, понимание патогенеза абдоминальной боли в связи с оперативной техникой при первичном желудочном обходном анастомозе поможет изменить операционную технику и снизить общую послеоперационную заболеваемость. БлагодарностиД-р О’Рурк получил стипендию Фонда Американской хирургической ассоциации и грант Национального института здравоохранения K08 DK074397.Благодарим Линн Китагава за создание. СноскиЗаявление издателя: Это PDF-файл неотредактированной рукописи, принятой к публикации. В качестве услуги для наших клиентов мы предоставляем эту раннюю версию рукописи. Рукопись будет подвергнута копирайтингу, верстке и проверке полученного доказательства, прежде чем она будет опубликована в окончательной форме для цитирования. Обратите внимание, что во время производственного процесса могут быть обнаружены ошибки, которые могут повлиять на содержание, и все юридические оговорки, относящиеся к журналу, имеют отношение. Ссылки1. Сантри HP, Гиллен Д.Л., Лодердейл Д.С. Тенденции в бариатрических хирургических процедурах. ДЖАМА. 2005; 294: 1909–1917. [PubMed] [Google Scholar] 2. Чо М., Кайдар-Персона О, Шомштейн С., Розенталь Р.Дж. Посещение отделения неотложной помощи после лапароскопического обходного желудочного анастомоза по Ру при патологическом ожирении. Surg Obes Relat Dis. 2008. 4 (2): 104–9. [PubMed] [Google Scholar] 3. Сондерс Дж., Баллантайн Г. Х., Белсли С., Стивенс Д. Д., Триведи А., Юинг Д. Р., Яннас В. А., Капелла Р. Ф., Василевски А., Моран С., Шмидт Х. Дж.. Годовая повторная госпитализация в центр бариатрической хирургии большого объема: лапароскопическое регулируемое бандажирование желудка, лапароскопическое шунтирование желудка и гастропластика с вертикальной полосой желудочного анастомоза с обходным желудочным анастомозом по Ру и Y.Obes Surg. 2008. 18 (10): 1233–40. [PubMed] [Google Scholar] 4. Келлог Т.А., Свон Т., Лесли Д.А., Бухвальд Х., Икрамуддин С. Модели повторной госпитализации и повторной операции в течение 90 дней после желудочного обходного анастомоза по Ру. Surg Obes Relat Dis. 2009. 5 (4): 416–23. [PubMed] [Google Scholar] 5. Фостер А., Ричардс В.О., Макдауэлл Дж., Лоус Х.Л. Clements RH. Желудочно-кишечные симптомы более выражены у пациентов с болезненным ожирением. Surg Endosc. 2003. 17 (11): 1766–8. [PubMed] [Google Scholar] 6. Арасаки СН, Дель Гранде ЮК, Янагита ЭТ, Алвес АК, Оливейра ДР.Частота срыгивания после обходного желудочного анастомоза. Obes Surg. 2005. 15 (10): 1408–17. [PubMed] [Google Scholar] 7. Walker SP, Wein P, Ihle BU. Тяжелая недостаточность фолиевой кислоты, маскирующаяся под синдром гемолиза, повышения ферментов печени и низкого уровня тромбоцитов. Obstet Gynecol. 1997. 90 (4 Pt 2): 655–7. [PubMed] [Google Scholar] 8. Декер Г. А., ДиБайз Дж. К., Лейтон Дж. А., Суэйн Дж. М., Кроуэлл, доктор медицины. Тошнота, вздутие живота и боль в животе у пациента с обходным желудочным анастомозом по Ру: больше вопросов, чем ответов. Obes Surg.2007. 17 (11): 1529–33. [PubMed] [Google Scholar] 9. Файнтуч Дж., Исида Р.К., Джакаби М., Рибейро А.С., Куга Р., Сакаи П., Барбейро Х.В., Барбейро Д.Ф., Сориано Ф.Г., Чекконелло И. Повышенная продукция цитокинов желудка после обходного желудочного анастомоза по Ру при патологическом ожирении. Arch Surg. 2007. 142 (10): 962–8. [PubMed] [Google Scholar] 10. Вудард Г.А., Энкарнасьон Б., Дауни Дж. Р., Пераза Дж., Чонг К., Эрнандес-Буссар Т., Мортон Дж. М.. Пробиотики улучшают результаты после операции шунтирования желудка по Ру: проспективное рандомизированное исследование.J Gastrointest Surg. 2009. 13 (7): 1198–204. [PubMed] [Google Scholar] 11. Исида Р.К., Файнтуч Дж., Паула А.М., Ристтори К.А., Сильва С.Н., Гомес Е.С., Маттар Р., Куга Р., Рибейро А.С., Сакаи П., Барбейро Х.В., Барбейро Д.Ф., Сориано Ф.Г., Чекконелло И. Микробная флора желудка после обходного желудочного анастомоза при патологическом ожирении. Obes Surg. 2007. 17 (6): 752–8. [PubMed] [Google Scholar] 12. Мачадо Дж. Д., Кампос К. С., Лопес Дах Силва К., Маркес Суен В. М., Барбоса Нонино-Борхес С., Дос Сантос Дж. Э., Сеневива Р., Маркини Дж. С.. Избыточный бактериальный рост в кишечнике после желудочного обходного анастомоза по Ру.Obes Surg. 2008. 18 (1): 139–43. [PubMed] [Google Scholar] 13. Dallal RM, Cottam D. Candy cane »Синдром Ру — возможное осложнение после операции обходного желудочного анастомоза. Surg Obes Relat Dis. 2007. 3 (3): 408–10. [PubMed] [Google Scholar] 14. Тейтельбаум Дж. Э., Синха П., Микале М., Йунг С., Джегер Дж. Ожирение связано с множественными функциональными заболеваниями брюшной полости. J Pediatr. 2009. 154 (3): 444–6. [PubMed] [Google Scholar] 15. Suter M, Dorta G, Giusti V, Calmes JM. Гастроэзофагеальный рефлюкс и нарушения моторики пищевода у пациентов с патологическим ожирением.Obes Surg. 2004. 14 (7): 959–66. [PubMed] [Google Scholar] 16. Potoczna N, Harfmann S, Steffen R, Briggs R, Bieri N, Horber FF. Привычки кишечника после бариатрической операции. Obes Surg. 2008. 18 (10): 1287–96. [PubMed] [Google Scholar] 17. Сведберг П., Йоханссон С., Валландер М.А., Хамелин Б., Педерсен Н.Л. Внекишечные проявления, связанные с синдромом раздраженного кишечника: двойное исследование. Алимент Pharmacol Ther. 2002. 16 (5): 975–83. [PubMed] [Google Scholar] 18. Хонг Д., Хаджанчи Ю.С., Перейра Н., Локхарт Б., Паттерсон Э.Дж., Суонстрем Л.Л.Манометрические аномалии и гастроэзофагеальная рефлюксная болезнь у больных ожирением. Obes Surg. 2004. 14 (6): 744–9. [PubMed] [Google Scholar] 19. Merrouche M, Sabaté JM, Jouet P, Harnois F, Scaringi S, Coffin B, Msika S. Гастроэзофагеальный рефлюкс и нарушения моторики пищевода у пациентов с болезненным ожирением до и после бариатрической хирургии. Obes Surg. 2007. 17 (7): 894–900. [PubMed] [Google Scholar] 20. Ямамото Х, Мори Т., Цучихаши Х, Акабори Х, Наито Х, Тани Т. Возможная роль GLP-1 в патофизиологии синдрома раннего демпинга.Dig Dis Sci. 2005. 50 (12): 2263–7. [PubMed] [Google Scholar] 21. Service GJ, Thompson GB, Service FJ, Andrews JC, Collazo-Clavell ML, Lloyd RV. Гиперинсулинемическая гипогликемия с несидиобластозом после операции обходного желудочного анастомоза. N Engl J Med. 2005. 353 (3): 249–54. [PubMed] [Google Scholar] 22. Kellogg TA, Bantle JP, Leslie DB, Redmond JB, Slusarek B, Swan T., Buchwald H, Ikramuddin S. Синдром гиперинсулинемической гипогликемии после желудочного шунтирования: характеристика и реакция на модифицированную диету. Surg Obes Relat Dis.2008. 4 (4): 492–9. [PubMed] [Google Scholar] 23. Морейра Р.О., Морейра Р.Б., Мачадо Н.А., Гонсалвеш Т.Б., Коутиньо В.Ф. Постпрандиальная гипогликемия после бариатрической хирургии: фармакологическое лечение верапамилом и акарбозой. Obes Surg. 2008. 18 (12): 1618–21. [PubMed] [Google Scholar] 24. Гусева Н, Филипс Д, Мордес Дж. Успешное лечение стойкой гиперинсулинемической гипогликемии нифедипином у взрослого пациента. Endocr Pract. 2010. 16 (1): 107–11. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. З’грагген К., Гувейди А., Штеффен Р., Поточна Н., Бирал Р., Вальтер Ф., Комминот П., Хорбер Ф.Тяжелая рецидивирующая гипогликемия после операции обходного желудочного анастомоза. Obes Surg. 2008. 18 (8): 981–8. [PubMed] [Google Scholar] 26. Миками Д., Нидлман Б., Нарула В., Дюрант Дж., Мелвин В.С. Хирургия естественного отверстия: первоначальный опыт использования устройства StomaphyX в США для уменьшения желудочных мешков после желудочного обходного анастомоза по Ру. Surg Endosc. 2010. 24 (1): 223–8. [PubMed] [Google Scholar] 27. Wudel LJ, младший, Wright JK, Debelak JP, Allos TM, Shyr Y, Chapman WC. Профилактика образования камней в желчном пузыре у пациентов с болезненным ожирением, подвергающихся быстрой потере веса: результаты рандомизированного контролируемого пилотного исследования.J Surg Res. 2002. 102 (1): 50–6. [PubMed] [Google Scholar] 28. Swartz DE, Felix EL. Избирательная холецистэктомия после обходного желудочного анастомоза по Ру: почему бессимптомные камни в желчном пузыре следует лечить по-другому у пациентов с патологическим ожирением? Surg Obes Relat Dis. 2005; 1: 555–560. [PubMed] [Google Scholar] 29. Портенье Д.Д., Грант Дж. П., Блэквуд С. С., Прайор А., МакМахон Р. Л., ДеМария Е. Ожидаемое лечение бессимптомного желчного пузыря при обходном желудочном анастомозе по Ру. Surg Obes Relat Dis. 2007. 3 (4): 476–9. [PubMed] [Google Scholar] 30.Tucker ON, Fajnwaks P, Szomstein S, Rosenthal RJ. Необходима ли сопутствующая холецистэктомия пациентам с ожирением, перенесшим лапароскопическое шунтирование желудка? Surg Endosc. 2008. 22 (11): 2450–4. [PubMed] [Google Scholar] 31. Миллер К., Хелл Э., Ланг Б., Ленгауэр Э. Профилактика образования камней в желчном пузыре после желудочных рестриктивных процедур для похудания: рандомизированное двойное слепое плацебо-контролируемое исследование. Ann Surg. 2003. 238: 697–702. [Бесплатная статья PMC] [PubMed] [Google Scholar] 32. Мейсон Э., Ренквист К. Э. Управление желчным пузырем в хирургии ожирения.Obes Surg. 2002. 12 (2): 222–9. [PubMed] [Google Scholar] 33. Нугу А., Сутер М. Практически обычная профилактическая холецистэктомия во время лапароскопического обходного желудочного анастомоза безопасна. Obes Surg. 2008. 18 (5): 535–9. [PubMed] [Google Scholar] 34. Patel KR, White SC, Tejirian T, Han SH, Russell D, Vira D, Liao L, Patel KB, Gracia C, Haigh P, Dutson E, Mehran A. Управление желчным пузырем во время лапароскопической операции по шунтированию желудка по Ру: стандартная процедура предоперационный скрининг на камни в желчном пузыре и послеоперационное профилактическое лечение не требуются.Am Surg. 2006. 72 (10): 857–61. [PubMed] [Google Scholar] 35. Фуллер В., Расмуссен Дж. Дж., Гош Дж., Али МР. Показана ли плановая холецистэктомия при бессимптомном желчекаменной болезни у пациентов, перенесших желудочный обходной анастомоз? Obes Surg. 2007. 17 (6): 747–51. [PubMed] [Google Scholar] 36. Механик Дж. И., Кушнер Р. Ф., Сугерман Х. Дж. И др. Американская ассоциация клинических эндокринологов, Общество ожирения и Американское общество метаболической и бариатрической хирургии. Медицинские рекомендации по клинической практике для периоперационной пищевой, метаболической и нехирургической поддержки пациентов, перенесших бариатрическую хирургию.Ожирение. 2009; 17 (Приложение 1): С1–70. v. [PubMed] [Google Scholar] 37. Паганини AM, Guerrieri M, Sarnari J, et al. Тринадцатилетний опыт лапароскопического чрезкистозного исследования общего желчного протока на камни. Эффективность и долгосрочные результаты. Surg Endosc. 2007; 21: 34–40. [PubMed] [Google Scholar] 38. Ахмед А.Р., Хусейн С., Саад Н. и др. Доступ к общему желчному протоку после желудочного обходного анастомоза по Ру. Surg Obes Relat Dis. 2007. 3: 640–643. [PubMed] [Google Scholar] 39. Peeters G, Himpens J. Лапароскопическая трансжелудочная эндоскопия в обходном желудочном анастомозе Roux-en-Y: модификация методики.Эндоскопия. 2009; 41 (Дополнение 2): E190. [PubMed] [Google Scholar] 40. Морган К.А., Гленн Дж.Б., Бирн Т.К., Адамс Д.Б. Дисфункция сфинктера Одди после желудочного обходного анастомоза Rouxen-Y. Surg Obes Relat Dis. 2009. 5 (5): 571–5. [PubMed] [Google Scholar] 41. Расмуссен Дж. Дж., Фуллер В., Али МР. Краевые язвы после лапароскопического обходного желудочного анастомоза: анализ предрасполагающих факторов у 260 пациентов. Surg Endosc. 2007. 21 (7): 1090–4. [PubMed] [Google Scholar] 42. Васкес Дж. С., Уэйн Оверби Д., Фаррелл TM. Меньшее количество стриктур и краевых язв при гастроеюностомии рассасывающимся швом.Surg Endosc. 2009; 23 (9): 2011–5. [PubMed] [Google Scholar] 43. Станчик М., Девени К.В., Трэкслер С.А., МакКоннелл Д.Б., Джоб Б.А., О’Рурк Р.В. Желудочно-желудочный свищ в эпоху раздельного обходного желудочного анастомоза по Ру: стратегии профилактики, диагностики и лечения. Obes Surg. 2006. 16 (3): 359–364. [PubMed] [Google Scholar] 44. Поднос Ю.Д., Хименес Дж.С., Уилсон С.Е. и др. Осложнения после лапароскопического обходного желудочного анастомоза: обзор 3464 случаев. Arch Surg. 2003. 138: 957–61. [PubMed] [Google Scholar] 45. Капелла JF, Капелла РФ.Желудочно-желудочные свищи и краевые язвы в процедурах обходного желудочного анастомоза для снижения веса. Obes Surg. 1999; 9: 22–7. [PubMed] [Google Scholar] 46. Карродегуас Л., Сомштейн С., Сото Ф. и др. Ведение желудочно-желудочного свища после разделенного желудочного анастомоза по Ру при патологическом ожирении: анализ 1292 последовательных пациентов и обзор литературы. Surg Obes Relat Dis. 2005; 1: 467–74. [PubMed] [Google Scholar] 47. Торрес JC, Oca CF, Garrison RN. Обходной желудочный анастомоз: гастроеюностомия по Ру по малой кривизне.Саут Мед Дж. 1983; 76: 1217–1221. [PubMed] [Google Scholar] 48. Siilin H, Wanders A, Gustavsson S, Sundbom M. Проксимальный желудочный мешок неизменно содержит продуцирующие кислоту париетальные клетки в обходном желудочном анастомозе Roux-en-Y. Obes Surg. 2005; 15: 771–777. [PubMed] [Google Scholar] 49. Бернс К.Э., Смит С.Д., Келли К.А., Сарр М.Г. Реоперационная бариатрическая хирургия. Извлеченные уроки для улучшения отбора пациентов и результатов. Ann Surg. 1993; 218: 646–653. [Бесплатная статья PMC] [PubMed] [Google Scholar] 50. Сапала Дж. А., Вуд М. Х., Сапала М. А. и др.Обходной желудочный анастомоз с микропакетом: технические аспекты первичных и ревизионных операций. Obes Surg. 2001; 11: 3–17. [PubMed] [Google Scholar] 51. Чин EH, Hazzan D, Sarpel U, Herron DM. Мультимедийная статья. Лапароскопическая пластика перфорированной краевой язвы через 2 года после желудочного обходного анастомоза. Surg Endosc. 2007; 21 (11): 2110. [PubMed] [Google Scholar] 52. Коакли Б.А., Девени С.В., Спайт Д.Х., Джоб Б.А., Томпсон С.К., Ле Д., Вулф Б.М., МакКоннелл Д.Б., О’Рурк Р.В. Ревизионная хирургия при неудачных рестриктивных бариатрических операциях.Surg Obes Relat Dis. 2008. 4 (5): 581–6. [PubMed] [Google Scholar] 53. Хартин CW, младший, Ремайн Д.С., Лактонг TA. Предоперационный бариатрический скрининг и лечение Helicobacter pylori. Surg Endosc. 2009 15 мая; Epub впереди печати. [PubMed] [Google Scholar] 54. де Моура Алмейда A, Cotrim HP, Santos AS, Bitencourt AG, Barbosa DB, Lobo AP, Rios A, Alves E. Предоперационная эндоскопия верхних отделов желудочно-кишечного тракта у пациентов с ожирением, перенесших бариатрическую операцию: нужна ли она? Surg Obes Relat Dis. 2008. 4 (2): 144–9. [PubMed] [Google Scholar] 55.Papasavas PK, Gagné DJ, Donnelly PE, Salgado J, Urbandt JE, Burton KK, Caushaj PF. Распространенность инфекции Helicobacter pylori и значение предоперационного тестирования и лечения пациентов, перенесших лапароскопический желудочный обходной анастомоз по Ру. Surg Obes Relat Dis. 2008. 4 (3): 383–8. [PubMed] [Google Scholar] 56. Sacks BC, Mattar SG, Qureshi FG, Eid GM, Collins JL, Barinas-Mitchell EJ, Schauer PR, Ramanathan RC. Заболеваемость краевыми язвами и использование рассасывающихся анастомотических швов при лапароскопическом обходном желудочном анастомозе по Ру.Surg Obes Relat Dis. 2006; 2 (1): 11–6. [PubMed] [Google Scholar] 57. Пай Р.Д., Карр-Локк Д.Л., Томпсон С.К. Эндоскопическая оценка дефункционального желудка с использованием технологии ShapeLock (с видео) Gastrointest Endosc. 2007. 66 (3): 578–81. [PubMed] [Google Scholar] 58. Барон TH. Энтероскопия с двойным баллоном для облегчения ретроградного размещения ПЭГ в качестве доступа к терапевтической ЭРХПГ у пациентов с желудочным обходным анастомозом на длинных конечностях. Gastrointest Endosc. 2006; 64: 973–974. [PubMed] [Google Scholar] 59. Мадалоссо К.А., Гурски Р.Р., Каллегари-Жак С.М., Наварини Д., Тисен В., Форнари Ф.Влияние обходного желудочного анастомоза на гастроэзофагеальную рефлюксную болезнь у пациентов с патологическим ожирением: проспективное исследование, основанное на Монреальском консенсусе. Ann Surg. 2010 февраль; 251 (2): 244–8. [PubMed] [Google Scholar] 60. Де Гроот Н.Л., Бургерхарт Дж.С., Ван Де Миберг ПК, де Фрис Д.Р., Смаут А.Дж., Сирсема П.Д. Систематический обзор: влияние консервативного и хирургического лечения ожирения на гастроэзофагеальную рефлюксную болезнь. Алимент Pharmacol Ther. 2009. 30 (11-12): 1091–102. [PubMed] [Google Scholar] 61. Swartz DE, Mobley E, Felix EL.Рефлюкс желчи после обходного желудочного анастомоза по Ру: нераспознанная причина послеоперационной боли. Surg Obes Relat Dis. 2009; 5: 27–30. [PubMed] [Google Scholar] 62. Фланагин Б.А., Митчелл М.Т., Тистлтуэйт, Вашингтон, Алверди Дж. Диагностика и лечение атипичных проявлений грыжи пищеводного отверстия диафрагмы после бариатрической хирургии. Obes Surg. 2010. 20 (3): 386–92. [PubMed] [Google Scholar] 63. Мэтью А., Велиуона М.А., ДеПальма Ф.Дж., Куни Р.Н. Стриктура желудочно-кишечного тракта после обходного желудочного анастомоза и эффективность эндоскопического вмешательства. Dig Dis Sci.2009. 54 (9): 1971-8. [PubMed] [Google Scholar] 64. Суггсы В.Дж., Кули В., Луповичи М., Чау В.Й., Бролин Р.Э. Осложнения при гастроеюностомии после лапароскопического обходного желудочного анастомоза по Ру: сравнение циркулярных степлеров диаметром 21 и 25 мм. Surg Obes Relat Dis. 2007. 3 (5): 508–14. [PubMed] [Google Scholar] 65. Чиу С.К., Ли В.Дж., Ван В., Вэй П.Л., Хуанг М.Т. Профилактика троакарной грыжи при лапароскопических бариатрических операциях. Obes Surg. 2006. 16 (7): 913–8. [PubMed] [Google Scholar] 66. Джонсон У.Х., Фехер А.М., МакМахон Р.Л., Грант Дж. П., Прайор А. Д..Частота троакарных грыж VersaStep при незакрытых фасциальных дефектах у пациентов с ожирением. Surg Endosc. 2006. 20 (10): 1584–6. [PubMed] [Google Scholar] 67. Хусейн С., Ахмед А.Р., Джонсон Дж., Босс Т., О’Мэлли В. Обструкция тонкой кишки после лапароскопического обходного желудочного анастомоза по Ру: этиология, диагностика и лечение. Arch Surg. 2007. 142 (10): 988–93. [PubMed] [Google Scholar] 68. Гунабушанам Дж., Шанкар С., Черняк Д. Р., Келли Дж. Дж., Перуджини Р. А.. Обструкция тонкой кишки после лапароскопической операции по шунтированию желудка по Ру.J Comput Assist Tomogr. 2009. 33 (3): 369–75. [PubMed] [Google Scholar] 69. Хига К.Д., Хо Т, Бун КБ. Внутренние грыжи после лапароскопического обходного желудочного анастомоза по Ру: частота, лечение и профилактика. Obes Surg. 2003. 13: 350–354. [PubMed] [Google Scholar] 70. Бауман Р.В., Пиррелло-младший. Внутренняя грыжа в пространстве Петерсена после лапароскопического обходного желудочного анастомоза Rouxen-Y: 6,2% случаев без закрытия — одна хирургическая серия из 1047 случаев. Surg Obes Relat Dis. 2009; 5: 565–570. [PubMed] [Google Scholar] 71. Швейцер М.А., ДеМария Э.Дж., Бродерик Т.Дж., Сугерман Х.Дж.Лапароскопическое закрытие дефектов брыжейки после желудочного обходного анастомоза по Ру. J. Laparoendosc Adv Surg Tech A. 2000; 10: 173–175. [PubMed] [Google Scholar] 72. Paroz A, Calmes JM, Giusti V, Suter M. Внутренняя грыжа после лапароскопического обходного желудочного анастомоза Roux-en-Y при патологическом ожирении: постоянная проблема в бариатрической хирургии. Obes Surg. 2006. 16: 1482–1487. [PubMed] [Google Scholar] 73. Гарза Э. мл., Кун Дж., Арнольд Д. и др. Внутренние грыжи после лапароскопического обходного желудочного анастомоза по Ру. Am J Surg. 2004. 188: 796–800.[PubMed] [Google Scholar] 74. Чемпион JK, Уильямс М. Непроходимость тонкой кишки и внутренние грыжи после лапароскопического обходного желудочного анастомоза по Ру. Obes Surg. 2003. 13: 596–600. [PubMed] [Google Scholar] 75. Кармоди Б., ДеМария Э.Дж., Джамал М. и др. Внутренняя грыжа после лапароскопического обходного желудочного анастомоза по Ру. Surg Obes Relat Dis. 2005; 1: 543–548. [PubMed] [Google Scholar] 76. Чо М., Пинто Д., Карродегуас Л. и др. Частота и лечение внутренних грыж после лапароскопического антеколического антегастрального обходного желудочного анастомоза по Ру без разделения брыжейки тонкой кишки или закрытия дефектов брыжейки: обзор 1400 последовательных случаев.Surg Obes Relat Dis. 2006; 2: 87–91. [PubMed] [Google Scholar] 77. Торрес-Вильялобос Г.М., Келлог Т.А., Лесли Д.Б., Антанавичус Г., Андраде Р.С., Слюсарек Б., Просен Т.Л., Икрамуддин С. Обструкция тонкой кишки и внутренние грыжи во время беременности после операции обходного желудочного анастомоза. Obes Surg. 2009. 19 (7): 944–50. [PubMed] [Google Scholar] 78. Стил К.Е., Прокопович Г.П., Магнусон Т. и др. Лапароскопический антеколический обходной желудочный анастомоз по Ру с закрытием внутренних дефектов приводит к меньшему количеству внутренних грыж, чем ретроколический доступ.Surg Endosc. 2008; 22: 2056–2061. [PubMed] [Google Scholar] 79. Пароз А., Калмес Дж. М., Роми С. и др. Новый тип внутренней грыжи после лапароскопического желудочного обходного анастомоза по Ру. Obes Surg. 2009; 19: 527–530. [PubMed] [Google Scholar] 80. Patel RY, Baer JW, Texeira J, Frager D, Cooke K. Внутренние грыжевые осложнения операции обходного желудочного анастомоза в острых условиях: спектр результатов визуализации. Emerg Radiol. 2009. 16 (4): 283–9. [PubMed] [Google Scholar] 81. Ианнуччилли Дж. Д., Гранд Д., Мерфи Б. Л. и др. Чувствительность и специфичность восьми признаков компьютерной томографии в предоперационной диагностике внутренней брыжеечной грыжи после операции обходного желудочного анастомоза по Ру.Clin Radiol. 2009. 64: 373–380. [PubMed] [Google Scholar] 82. Локхарт М.Э., Тесслер Ф.Н., Canon CL и др. Внутренняя грыжа после желудочного обходного анастомоза: чувствительность и специфичность семи признаков КТ с хирургической корреляцией и контролем. AJR Am J Roentgenol. 2007. 188: 745–750. [PubMed] [Google Scholar] 83. Ганди А.Д., Патель Р.А., Бролин Р.Э. Плановая лапароскопия для выявления симптомов мезентериальной / внутренней грыжи после лапароскопического обходного желудочного анастомоза по Ру. Surg Obes Relat Dis. 2009. 5 (2): 144–9. [PubMed] [Google Scholar] 84.Agaba EA, Gentles CV, Shamseddeen H, Sasthakonar V, Kandel A, Gadelata D, Gellman L. Ретроспективный анализ боли в животе у пациентов с послеоперационным лапароскопическим шунтированием желудка по Ру: простой алгоритм — ответ? Surg Obes Relat Dis. 2008; 4 (5): 587–93. [PubMed] [Google Scholar] 85. Питт Т., Бретауэр С., Шерман В., Удомсаваенгсуп С., Мец М., Чикунгуво С., Чанд Б., Шауэр П. Диагностическая лапароскопия при хронической боли в животе после обходного желудочного анастомоза. Surg Obes Relat Dis. Май-июнь 2008 г .; 4 (3): 394–8.обсуждение 398. Epub 2008 14 апреля [PubMed] [Google Scholar] 86. Гунабушанам Дж., Шанкар С., Черняк Д. Р., Келли Дж. Дж., Перуджини Р. А.. Обструкция тонкой кишки после лапароскопической операции по шунтированию желудка по Ру. J Comput Assist Tomogr. 2009. 33 (3): 369–75. [PubMed] [Google Scholar] 87. Костер Д.Д., Сандберг С.М., Кермод Д.С. и др. Обструкция тонкой кишки из-за антеградной и ретроградной инвагинации после желудочного обходного анастомоза: три отчета о случаях у двух пациентов, обзор литературы и рекомендации по диагностике и лечению.Surg Obes Relat Dis. 2008; 4: 69–72. [PubMed] [Google Scholar] 88. Зайнабади К., Раманатан Р. Инвагинация после лапароскопического обходного желудочного анастомоза по Ру. Obes Surg. 2007; 17: 1619–1623. [PubMed] [Google Scholar] 89. Хокинг М.П., Маккой Д.М., Фогель С.Б. и др. Антиперистальтическая и изоперистальтическая инвагинация, связанная с аномальной моторикой после желудочного обходного анастомоза по Ру: отчет о болезни. Операция. 1991; 110: 109–112. [PubMed] [Google Scholar] 90. Срикант М.С., Кески Т., Фокс С.Р. и др. Картины компьютерной томографии при непроходимости тонкой кишки после открытого дистального обходного желудочного анастомоза.Obes Surg. 2004. 14: 811–822. [PubMed] [Google Scholar] 91. Чо М., Карродегуас Л., Пинто Д., Ласкано К., Сото Ф., Уиппл О., Гордон Р., Симпфендорфер С., Гонсалво Дж. П., Шомштейн С., Розенталь Р. Дж. Диагностика и лечение частичной непроходимости тонкой кишки после лапароскопического антеколического антегастрального обходного желудочного анастомоза по Ру при патологическом ожирении. J Am Coll Surg. 2006. 202 (2): 262–8. [PubMed] [Google Scholar] 92. Lewis CE, Jensen C, Tejirian T., Dutson E, Mehran A. Ранняя обструкция еюноеюностомии после лапароскопического обходного желудочного анастомоза: серия случаев и алгоритм лечения.Surg Obes Relat Dis. 2009. 5 (2): 203–7. [PubMed] [Google Scholar] 93. Bestman TJ, Valk JW, Gypen B, Declercq S, Hendrickx L. Необычное осложнение после обходного желудочного анастомоза по Ру: перекрут и инфаркт разделенного сальника. Obes Surg. 2009. 19 (12): 1731–3. [PubMed] [Google Scholar] 94. Даллал Р. М., Бейли Л. А.. Инфаркт сальника: причина острой боли в животе после антеколического обходного желудочного анастомоза. Surg Obes Relat Dis. 2006; 2 (4): 451–4. [PubMed] [Google Scholar] 95. Goitein D, Gagné DJ, Papasavas PK, Dallal R, Quebbemann B, Eichinger JK, Johnston D, Caushaj PF.Синдром верхней брыжеечной артерии после лапароскопического обходного желудочного анастомоза по Ру при патологическом ожирении. Obes Surg. 2004. 14 (7): 1008–11. [PubMed] [Google Scholar] 96. Pratt JS, Van Noord M, Christison-Lagay E. Привязанный безоар как отсроченное осложнение лапароскопического обходного желудочного анастомоза по Ру: отчет о болезни. J Gastrointest Surg. 2007. 11 (5): 690–2. [PubMed] [Google Scholar] 97. Стил К., Швейцер М., Лидор А., Магнусон Т. Необычный случай желудочного безоара, вызывающего обструкцию после желудочного обходного анастомоза по Ру.Surg Obes Relat Dis. 2006. 2 (5): 536–7. [PubMed] [Google Scholar]Отсроченное проявление шока из-за забрюшинного кровотечения после паденияAbstractВо время травмы живот — это та область, которую нельзя игнорировать. Из-за сложной анатомии очень важно, чтобы все области брюшной полости были исследованы как клинически, так и радиологически, чтобы исключить абдоминальное кровотечение как причину геморрагического шока после травмы. Наш случай оправдывает сказанное выше. Ключевые слова: Тупая травма живота, забрюшинное кровоизлияние и шок ВВЕДЕНИЕМы представляем случай с неясной историей, который, как выяснилось, имел абдоминальную причину шока СЛУЧАЙНЫЙ СЛУЧАЙA 53 года -старый хорошо сложенный мужчина поскользнулся на полу и приземлился на спину.В течение следующих нескольких дней он продолжал страдать от резких болей в животе, которые постепенно усиливались. Боль локализовалась в эпигастрии, левом подреберье и спине. Поскольку он не заметил своего падения, его местный врач объяснил эти боли гастритом. На четвертый день после травмы он обратился в отделение травм специализированной больницы Университета Айн-Шамс с шоком и болями в животе. Он не мог предоставить соответствующую историю, так как его уровень сознания продолжал ухудшаться.Никто из сопровождающих его членов семьи не знал о его травме. Его систолическое артериальное давление составляло 50–60 мм рт. Ст., А частота сердечных сокращений — 130 ударов в минуту. Осмотр показал новообразование в брюшной полости. При осмотре брюшная стенка была болезненной и жесткой. Масса была зафиксирована и не пульсировала. Немедленно начались интенсивные реанимационные мероприятия. Кровь брали для перекрестного сопоставления и исследований. Принято решение о исследовательской лапаротомии. Пациента временно реанимировали, а по пути в операционную ему сделали быстрое компьютерное исследование (без контраста), чтобы исключить разрыв аневризмы из-за отсутствия надлежащего анамнеза.Было трудно поддерживать его жизненные показатели, которые снова начали ухудшаться; поэтому его бросили в театр. Компьютерная томография показала огромную многокомпонентную кисту брюшной полости с плотной кровью жидкостью внутри. Происхождение кисты было неясным из-за ее размера. В полости кисты плавала крошечная кальцинированная структура. Конечно, возможность протекающей аневризмы аорты была исключена. Других отклонений от нормы [Рисунки и] не обнаружено. КТ показывает огромную многокомпонентную кисту крови, заполняющую большую часть брюшной полости КТ; несколько разрезов показывают степень кровяной кисты на разных уровнях. При лапаротомии огромная темно-синяя киста заполняла большую часть брюшной полости и выталкивала весь кишечник в небольшой отсек.При вскрытии кисты были обнаружены темные сгустки крови и дефибринированная кровь. Киста была множественной, как показано на компьютерной томографии. Сгустки крови были удалены, а локулы прослежены до забрюшинного пространства. Забрюшинное пространство было заполнено сгустками крови неустановленного происхождения. Активного кровотечения не было. Небольшая разветвленная атерома, имеющая форму кровеносного сосуда в месте его разветвления, извлечена из полости кисты крови. Его диаметр был около 4 мм. Он обозначал предыдущий разрыв забрюшинного кровеносного сосуда при его бифуркации (поясничной артерии).Это представляло собой кальцинированную структуру, идентифицированную при компьютерной томографии. Пациент к этому времени получил 15 единиц крови и 12 единиц свежезамороженной плазмы. Как следствие, а также из-за большого размера забрюшинной гематомы и того факта, что не было активного кровотечения или идентифицируемого кровотечения, и у пациента начали проявляться признаки коагулопатии, было принято решение не прерывать забрюшинную гематому. Псевдостенка кисты, которая фактически образовалась из забрюшинной стенки, была ушита непрерывным викриловым швом для тампонады оставшейся гематомы. Пациент переведен в отделение интенсивной терапии. Он пробыл там 3 дня и был переведен в палату. Он был выписан через 10 дней после лапаротомии. Через месяц контрольная компьютерная томография показала повторное накопление некоторых тромбов и умеренный левый гидроуретер и гидронефроз. Пациент протекал бессимптомно, но, чтобы избежать дальнейшего давления на левую почку, ему была сделана плановая лапаротомия. Была обнаружена, открыта и эвакуирована более мелкая многокомпонентная кровяная киста. Были удалены другие сгустки крови, а стенка кисты оставлена открытой для дренажа.Брюшная полость закрыта двумя дренажами внутри. Пациент уехал домой на пятый послеоперационный день. После второй лапаротомии у него развилась раневая инфекция. Некоторые кожные швы были сняты, чтобы помочь оттоку гноя. Через шесть месяцев УЗИ брюшной полости не выявило давления на левую почку и кист или новообразований в брюшной полости. ОБСУЖДЕНИЕНесмотря на улучшения в оказании помощи при травмах, неконтролируемое кровотечение является причиной 30–40% смертей, связанных с травмами, и является основной причиной потенциально предотвратимых ранних смертей в больницах.[1] Наличие летальной триады гипотермии, коагулопатии и ацидоза представляет собой серьезный риск ухудшения состояния и неблагоприятного исхода у пациентов с политравмой. [2] Реанимация пациента с травмой с неконтролируемым кровотечением требует раннего выявления потенциальных источников кровотечения с последующими незамедлительными действиями по минимизации кровопотери, восстановлению перфузии тканей и достижению гемодинамической стабильности. [1] Клинические симптомы шока — это три окна для микроциркуляции, которые можно оценить с точки зрения неадекватной перфузии органов: уровень сознания (церебральная перфузия), пульс (периферическая перфузия) и диурез (почечная перфузия).Они должны различать, является ли пациент гемодинамически нормальным или просто гемодинамически стабильным. Основываясь на реакции на первоначальную реанимацию, более поздняя группа пациентов определяется как преходящие респонденты или не отвечающие на лечение и, вероятно, потребует хирургического вмешательства для контроля кровотечения. [2] Проблема может заключаться в «компенсированном шоке», при котором перфузия клеток отстает от общих физиологических параметров. Не все пациенты с травмами с гипоперфузией тканей в результате массивного кровотечения поступают в отделение неотложной помощи с признаками шока.[3] Нет объективных данных, описывающих взаимосвязь между риском кровотечения и механизмом травмы. Уменьшение серийных измерений гематокрита может отражать продолжающееся кровотечение, но пациенты со значительным кровотечением могут поддерживать свой серийный гематокрит. [1] Клинические исследования показали, что уровни лактата и дефицит оснований представляют собой высокочувствительные параметры для распознавания «скрытого шока» при травматическом кровотечении. [2] Отсутствие конкретного диагноза не должно задерживать реанимацию, если кровоизлияние предполагается на основании анамнеза, физикального обследования или лабораторных данных.[3] Тем не менее, отсроченные проявления брюшного кровотечения у пострадавших от падения встречаются редко. Уитон и Цаламандрис представили 17-летнего мальчика с отсроченным абдоминальным кровотечением через 24 часа после падения [4]. В этом случае пациент обратился в больницу на четвертый день после падения. Гематома и кровотечение в забрюшинное пространство наблюдаются у 44% пациентов с тупой травмой живота. Травмы, пропущенные во время вторичного обследования в больнице, являются причиной смертности до 50% из-за несвоевременного лечения, в то время как ранняя диагностика, напротив, не означает высокой частоты тяжелых осложнений.[5] Оценка пациентов, перенесших тупую травму живота, остается одним из наиболее сложных аспектов оказания помощи при острых травмах. Результаты физикального обследования общеизвестно ненадежны, так как большое количество крови может накапливаться в брюшной и тазовой полостях без каких-либо значительных или ранних изменений в результатах физикального обследования. [6] Пациентам с тупой травмой живота может быть целесообразно визуализировать брюшную полость и таз, чтобы исключить сопутствующую скрытую травму живота.Согласно европейским рекомендациям Многопрофильной целевой группы по расширенной помощи при кровотечениях, пациенты с травмами, поступившие с геморрагическим шоком и неустановленным источником кровотечения, должны подвергаться немедленному дальнейшему обследованию. [7] Хотя FAST дает высокочувствительные результаты в хорошо обученных руках, в отличие от КТ, он не зависит от места происхождения и степени повреждения. [8] КТ часто дает подробный диагноз в случаях с вводящими в заблуждение симптомами и, таким образом, определяет необходимость оперативного вмешательства.Для получения лучших изображений КТ требуется как оральный, так и внутривенный контраст [9]. Стулфаут и его коллеги пришли к выводу, что получение первоначальных компьютерных томографов без перорального контрастного вещества помогает нам обеспечить как безопасность (определенный риск аспирации и потенциальная задержка в оказании помощи пациенту), так и эффективность без ущерба для диагностической точности [10]. Решение оперировать пациента в описанном клиническом случае было принято, потому что пациент находился в шоке. Проведенная нами компьютерная томография — спорный вопрос. Это было сделано без контраста и без надлежащего времени для подробного радиологического исследования.Но из-за отсутствия подробной истории его травмы мы решили исключить разрыв аневризмы или другую экстраабдоминальную причину кровотечения. Для пациентов с серьезными травмами брюшной полости, требующих экстренной лапаротомии, вероятность смерти показывает взаимосвязь как со степенью гипотонии, так и с продолжительностью пребывания в отделении неотложной помощи для тех, кто находился там не более 90 минут [11]. ] Хилл и его коллеги наблюдали значительное снижение смертности от шока, введя образовательную программу по травмам и установив 60-минутный лимит времени в отделении неотложной помощи для пациентов в состоянии геморрагического шока.[12] В нашем тематическом исследовании для перевода этого пациента в операционную потребовалось менее 60 минут, включая время, затраченное на компьютерную томографию. Забрюшинное кровотечение, вызванное тупыми травмами, по-прежнему остается проблемой для хирургов, поскольку всегда существует риск превратить его в непреодолимое кровотечение. Muftuoglu et al. подчеркивается, что стратегию лечения должен определять хирург с учетом возраста, типа травмы, сопутствующих заболеваний, дополнительных повреждений органов и особенно гемодинамической стабильности пациентов.Показаниями к операции являются перфорированные полые вязкостные и гемодинамические параметры, которые не могут быть стабилизированы [13]. В 1983 году Стоун и его коллеги описали методы сокращенной лапаротомии, тампонирования для остановки кровотечения и отложенного окончательного хирургического вмешательства до установления коагуляции [14]. С тех пор ряд авторов описали положительные результаты этой концепции, которая теперь называется «борьба с ущербом». В этом случае была проведена борьба с повреждениями, и брюшина была зашита, чтобы предотвратить распространение гематомы.Пациента перевели в реанимацию, а позже ему сделали еще одну плановую операцию по поводу давления на почку. Забрюшинное кровотечение, вызванное перерывом в поясничных и тазовых артериях, является наиболее частой причиной геморрагического шока в результате травм, вызванных вертикальным замедлением [15]. Сяблис и его коллеги сообщили о том, что пациент выжил после падения и имел относительно небольшую забрюшинную гематому, обнаруженную во время срочной спленэктомии. Это было недооценено; Через 2 недели основной разрыв поясничной артерии привел к формированию псевдоаневризмы, которая затем разорвалась, вызвав большую забрюшинную гематому и постепенный полный паралич бедренного нерва.Травматический разрыв поясничной артерии — редкое осложнение тупой травмы живота, которое может привести к потенциально массивному забрюшинному кровотечению и шоку или к последующему формированию псевдоаневризмы и отсроченной забрюшинной гематоме. [16] В этом случае точная причина кровотечения не была установлена, поскольку не было активного кровотечения. Было высказано предположение, что причиной кровотечения был разрыв поясничной артерии из-за плавающей кальцифицированной атеромы, извлеченной из кисты крови. Атоматическая хирургическая находка имела форму кровеносного сосуда диаметром 4-5 мм, что указывало на выстилку поясничной артерии. Смертность от 18% до 60% наблюдается у пациентов с забрюшинной гематомой. Основная причина смерти — геморрагический шок. В качестве хирургической стратегии исследование забрюшинной гематомы должно быть последним средством для хирурга, если только имеется сильное активное забрюшинное кровотечение, поскольку открытие этой закрытой системы создает «эффект дымохода» и когда давление на кровоточащие ткани снимается; кровотечение может стать еще более серьезным и смертельным. Muftuoglu et al., сообщили в своем исследовании, что более половины пациентов с забрюшинной гематомой умерли в послеоперационном периоде из-за решения об обследовании забрюшинного пространства [13]. Многие коллатеральные сосуды снабжают любую конкретную область забрюшинного пространства. Это может объяснить, почему, если кровоточащая артерия находится под контролем, побочное кровоснабжение той же области может привести к новому кровотечению. Это одна из основных причин, по которой хирурги избегают исследования забрюшинного пространства в условиях травмы.Кроме того, особенно трудно контролировать поясничные артерии [17]. Поскольку в нашем случае была применена операция по уменьшению повреждений, мы не рисковали дальнейшим исследованием гематомы. Спасти пациента важнее, чем контролировать гематому. Реанимация — это непрерывный процесс. На протяжении фазы реанимации и оценки медицинские работники должны следить за общей картиной — каковы травмы пациента и что является наивысшим приоритетом? Перевод в стационар, особенно в операционную, не следует откладывать из-за менее важных проблем.[18] Несмотря на отсутствие окончательных научных данных, многочисленные исследования и запросы на финансирование основаны на достижении «Золотого часа» для всех пациентов с травмами. [19] У пациентов с тупой политравмой эта ранняя фаза золотого часа не ограничивается лечением только в течение первых 60 минут после травмы, но может быть безопасно продлена до первых нескольких часов после травмы [20]. Первые 24 часа реанимации сильно связаны с повышением заболеваемости и смертности.Существует посттравматическое терапевтическое окно в 24 часа (серебряный день), которое при эффективном использовании может существенно повлиять на исход травмированных пациентов. [21] Установленные зависящие от времени фазы ведения пациентов с травмами в первые 24 часа включают следующее:
Третичный осмотр в первые 24 часа позволяет еще пропустить травмы.Требуются бдительность и тщательное повторное обследование, чтобы свести к минимуму последствия этих травм и начать лечение как можно раньше. [22] Конечные точки реанимации следующие:
Швы для порезов, проколов и укусовВы нарезаете еду на ужин и случайно режете себя.Или, может быть, ваш ребенок поранился, играя на гравии. Похоже, это может быть серьезно. Прежде всего, если это экстренный вызов, позвоните 911. Некоторые признаки возникают при травме:
Если травма не является экстренной, а хуже простой царапины или царапины, возможно, вы не знаете, что делать. Вы просто перевязываете более глубокие порезы и раны или накладываете швы? Что такое швы?Швы на коже похожи на швы на одежде — нити, скрепляющие вещи. Они сделаны из самых разных материалов, например, из нейлона или шелка. А некоторые, например те, которые используются при травмах рта, растворяются сами по себе. Когда они вам нужны, швы важны, потому что они:
Так что это помогает знать, когда делать уход за порезом самостоятельно и при необходимости обращения к врачу. Как узнать, нужны ли мне швы?От размера раны до ее расположения есть много признаков того, что вам нужно наложить швы или, по крайней мере, обратиться к врачу. Насколько он большой? Вы захотите обратиться к врачу, если рана:
Насколько сильно кровотечение? Скорее всего, вам понадобятся швы, если рана:
Что это вызвало? При некоторых ранах может потребоваться прививка от столбняка, а также наложение швов.Столбняк — одна из стандартных прививок для детей. Взрослым требуется ревакцинация каждые 10 лет. Немедленно обратитесь за медицинской помощью, если рана образовалась от:
Где рана? Обратитесь к врачу, если рана находится на любой из этих областей:
Заражается? Наконец, вам понадобится врач, если у вас или вашего ребенка есть какие-либо признаки инфекции:
Если у вас есть какие-либо сомнения, лучше позвонить своему врачу. Перед тем, как пойти к врачуЕсли вам все же нужно наложить швы, вот несколько советов, прежде чем идти к врачу. Оставьте его. Если у вас есть предмет, например, гвоздь, застрявший под кожей, оставьте его там. Это может предотвратить обострение кровотечения. Но если предмет, вызвавший прокол, небольшой и вы легко можете его удалить, сделайте это. Не ешьте и не пейте. Это в основном для детей. Им может потребоваться лекарство, чтобы успокоить их, чтобы врач наложил швы.Если они ели или что-нибудь выпили, им, возможно, придется дольше ждать лечения. Подайте давление. Используйте чистое полотенце или повязку, чтобы надавить на рану. Постарайтесь держать травмированную область выше сердца, чтобы остановить или замедлить кровотечение. Если кровь просочится, не снимайте старую повязку. Просто положите еще одну прямо поверх нее. Очистите рану. Если можете, очистите рану. Не используйте перекись водорода или йод — они могут вызвать раздражение раны.Кроме того, избегайте чистки. Вместо этого вы можете:
Снимите боль. От боли дайте ацетаминофен или ибупрофен. Однако сначала проконсультируйтесь с врачом, есть ли у вас какие-либо заболевания или принимаете ли вы какие-либо другие лекарства. Что вызывает у меня внезапную боль в животе?Ариана спрашивает: У меня сильные спазмы в животе, когда я бегаю, а также необычную одышку и неспособность двигать ногами. [Я бегаю] на дистанцию 5 км, и обычно первая миля или около того чувствую себя прекрасно, и мое промежуточное время идет именно там, где и должно быть, но затем мои ноги начинают гореть, моя грудь болит, и я не могу толкаться дальше .Остальная часть забега обычно приводит к аномально болезненным спазмам во всем животе, которые продолжаются даже после забега. Я также испытываю чувство, что меня рвет. Обычно помогает замедление, но когда я снова ускоряюсь, оно возвращается. Я бегаю уже много лет, и этого не случалось до последней недели или около того. И мой тренер, и спортивный тренер сбиты с толку. Спортивный тренер сначала предположил, что это неровный таз, но после лечения симптомы остались прежними. Это непростая проблема. Мы действительно не знаем, что вызывает спазмы в животе или почему бегунам накладывают боковые швы. Я предполагаю, что вы хорошо едите и пьете достаточно жидкости, чтобы поддерживать водный баланс (но не потребляете слишком много жидкости). Если вы постоянно потребляете жидкости, попробуйте сократить потребление вдвое и посмотреть, как вы себя чувствуете. Выравнивание таза — хорошая мысль, но если решение проблемы с тазом не помогло, попросите своего тренера проверить, нет ли подвывиха или смещения ребер.Это еще одна проблема опорно-двигательного аппарата, которая может повлиять на живот и вызвать спазмы. Это происходит, когда сустав головки ребер испытывает движение. Чаще всего спазмы в животе или боковые швы связаны с ритмом и подачей кислорода к мышцам, особенно диафрагме. Большинство спазмов в животе проходят, когда вы замедляете темп и дышите глубже. Практикуйте дыхание диафрагмой (брюшное дыхание), чтобы заполнить все легкое. Если вы не используете диафрагму, вы ограничите поступление кислорода, и это может быть причиной спазмов и тяжести в ногах. Вы и ваш тренер должны также обсудить, где вы находитесь на тренировке по сравнению со своим темпом гонки. Возможно, более медленный старт и более быстрый финиш помогут вам пройти гонку более комфортно. Я помню, как один молодой бегун из команды моей дочери совершил прорывной забег и сказал тренеру: «Больно ехать быстро». Часть обучения хорошему бегу — это балансирование темпа со своими способностями. Нервы и стресс также могут играть роль в некоторых случаях спазмов. Возможно, вам потребуется оценить уровень «стресса» во время гонок и поработать со своим тренером и спортивным тренером, чтобы уменьшить стресс, который может возникнуть у вас во время гонок. Этот контент создается и поддерживается третьей стороной и импортируется на эту страницу, чтобы помочь пользователям указать свои адреса электронной почты. Вы можете найти больше информации об этом и подобном контенте на сайте piano.io. . Leave a Reply |

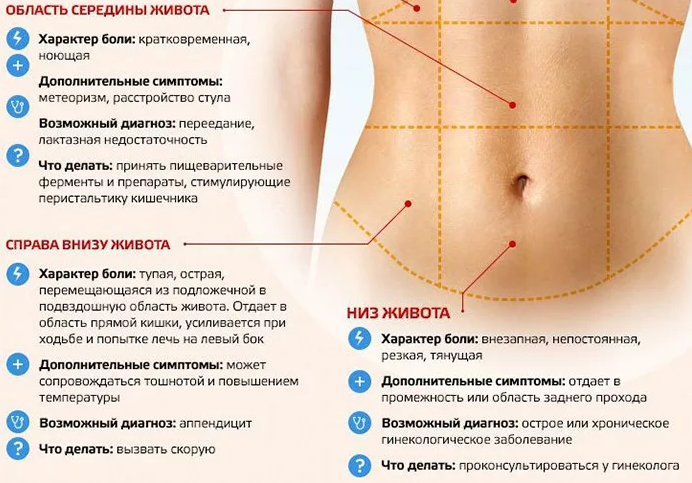






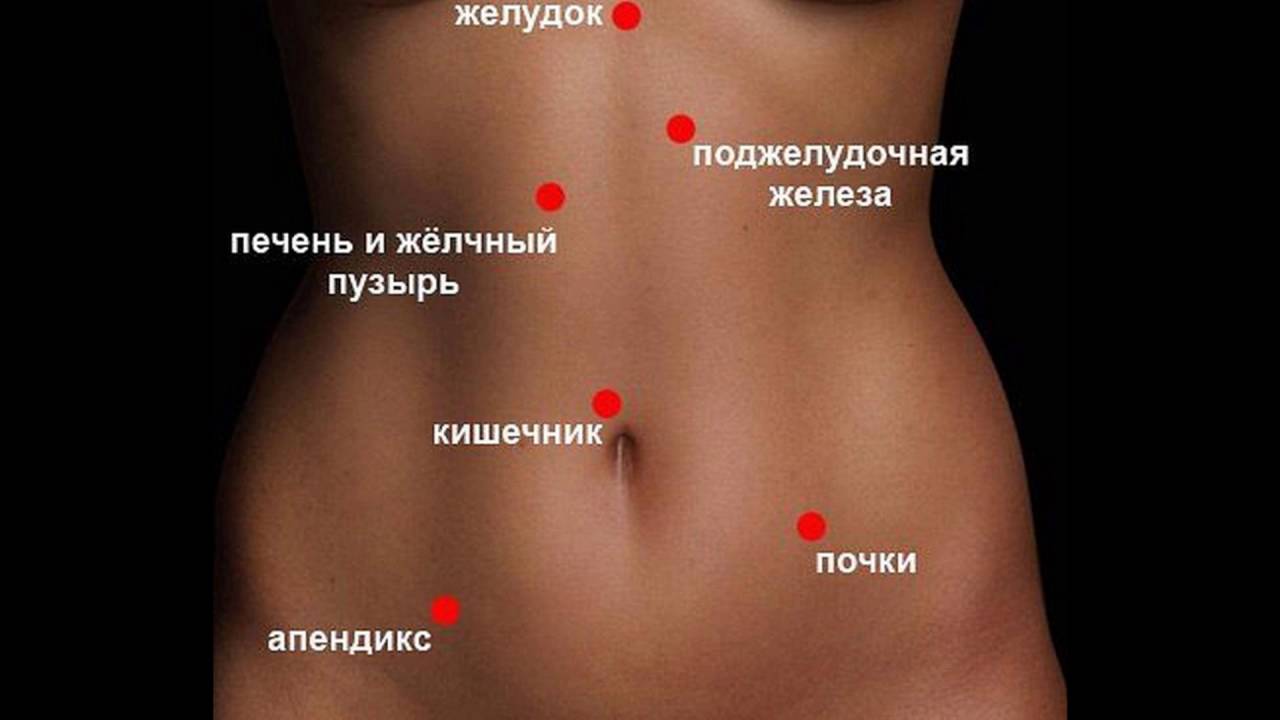
 Это происходит из-за увеличения количества или толщины жидкости, которая смазывает желудок, сообщает диетолог Натали Риццо из Нью-Йорка.
Это происходит из-за увеличения количества или толщины жидкости, которая смазывает желудок, сообщает диетолог Натали Риццо из Нью-Йорка./Peter-Dazeley-149627810-56a32a9d3df78cf7727c1d48.jpg)
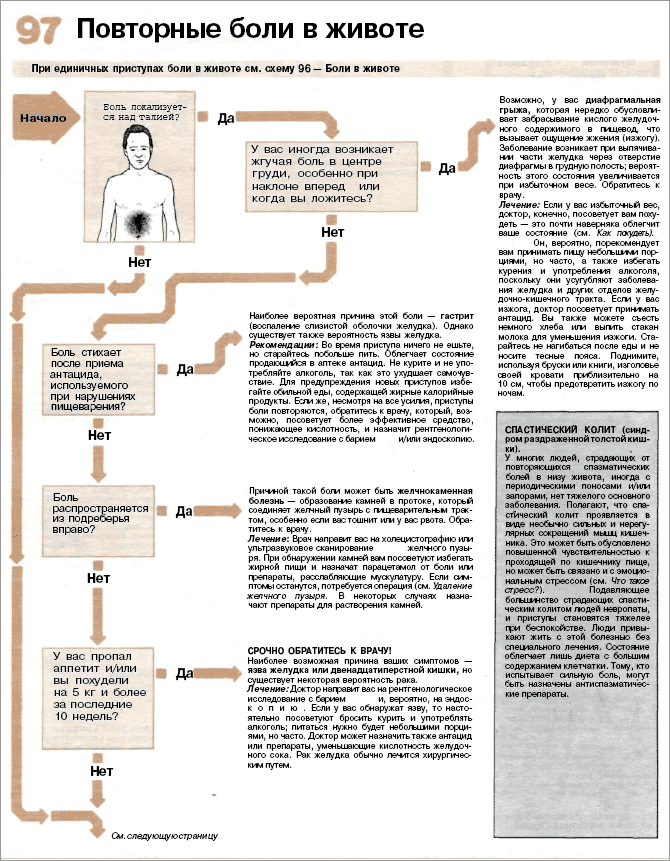 1%)
1%)
 Другие соображения должны включать аллергию на глютен, непереносимость лактозы и другие подобные «небариатрические» пищевые причины боли.Наконец, дефицит железа и B-12 считается причинами боли в животе, хотя механизмы действия неизвестны (7). Эти наблюдения подчеркивают важность подробного диетического анамнеза и диагностической лабораторной оценки для выявления пищевой аллергии и дефицита питательных микроэлементов.
Другие соображения должны включать аллергию на глютен, непереносимость лактозы и другие подобные «небариатрические» пищевые причины боли.Наконец, дефицит железа и B-12 считается причинами боли в животе, хотя механизмы действия неизвестны (7). Эти наблюдения подчеркивают важность подробного диетического анамнеза и диагностической лабораторной оценки для выявления пищевой аллергии и дефицита питательных микроэлементов. Поэтому избыточный бактериальный рост во многих случаях является диагнозом исключения, а лечение часто является эмпирическим. Тем не менее, водородные дыхательные тесты использовались для диагностики, а эмпирическая антибактериальная терапия улучшает симптомы в отдельных отчетах (12).Была предложена эмпирическая хирургическая резекция дефункционализированных компонентов желудочно-кишечного тракта с риском разрастания, чаще всего остаточного желудка или антиперистальтического («леденцового») сегмента конечности Ру, прилегающего к гастроеюностомии (13). Однако при отсутствии явной патологии в предполагаемом патогенном сегменте (например, дилатация, дистальная непроходимость, свищ, изъязвление, гастрит), преимущества таких вмешательств не доказаны.
Поэтому избыточный бактериальный рост во многих случаях является диагнозом исключения, а лечение часто является эмпирическим. Тем не менее, водородные дыхательные тесты использовались для диагностики, а эмпирическая антибактериальная терапия улучшает симптомы в отдельных отчетах (12).Была предложена эмпирическая хирургическая резекция дефункционализированных компонентов желудочно-кишечного тракта с риском разрастания, чаще всего остаточного желудка или антиперистальтического («леденцового») сегмента конечности Ру, прилегающего к гастроеюностомии (13). Однако при отсутствии явной патологии в предполагаемом патогенном сегменте (например, дилатация, дистальная непроходимость, свищ, изъязвление, гастрит), преимущества таких вмешательств не доказаны. Такие проблемы, вероятно, более распространены, чем предполагаются, часто представляют собой диагноз исключения и особенно трудны в управлении, поскольку патогенез заболевания, а также алгоритмы диагностики и лечения плохо определены.
Такие проблемы, вероятно, более распространены, чем предполагаются, часто представляют собой диагноз исключения и особенно трудны в управлении, поскольку патогенез заболевания, а также алгоритмы диагностики и лечения плохо определены. Эти проблемы, такие как запор, обычно проходят со временем.
Эти проблемы, такие как запор, обычно проходят со временем. Также может присутствовать дисфагия. Как правило, обострение нарушений моторики пищевода считается более частым после бандажирования желудка, которое представляет собой фиксированную обструкцию выходного отверстия пищевода, в отличие от обходного желудочного анастомоза, при котором ткани дистальнее пищевода относительно более растяжимы (19).Шунтирование желудка с применением бандажа может вызывать аналогичные проблемы, хотя о дисфагии чаще сообщают, чем о боли (6). Как и при синдроме раздраженного кишечника, пациентов с нарушениями моторики пищевода следует тщательно проконсультировать относительно возможного обострения после бариатрической операции. Учитывая плохо изученный патогенез заболевания и ограниченную эффективность хирургического лечения таких нарушений, мы предпочитаем консервативное лечение, включая изменение диеты и блокаторы кальциевых каналов, если это показано манометрией.
Также может присутствовать дисфагия. Как правило, обострение нарушений моторики пищевода считается более частым после бандажирования желудка, которое представляет собой фиксированную обструкцию выходного отверстия пищевода, в отличие от обходного желудочного анастомоза, при котором ткани дистальнее пищевода относительно более растяжимы (19).Шунтирование желудка с применением бандажа может вызывать аналогичные проблемы, хотя о дисфагии чаще сообщают, чем о боли (6). Как и при синдроме раздраженного кишечника, пациентов с нарушениями моторики пищевода следует тщательно проконсультировать относительно возможного обострения после бариатрической операции. Учитывая плохо изученный патогенез заболевания и ограниченную эффективность хирургического лечения таких нарушений, мы предпочитаем консервативное лечение, включая изменение диеты и блокаторы кальциевых каналов, если это показано манометрией.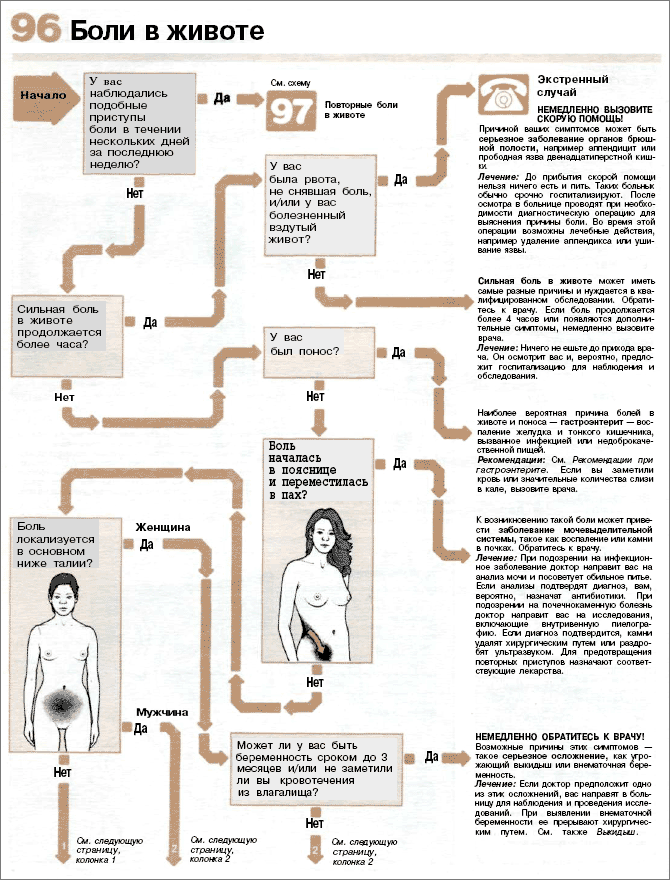 Боль, как правило, не является доминирующим симптомом, но может быть связана с вздутием живота, спазмами и диареей, которые сопровождают эпизоды демпинга. Симптомы часто возникают из-за продуктов с высоким содержанием рафинированного сахара, но могут быть вызваны и другими продуктами. Патогенез демпинг-синдрома до конца не изучен, и его полное обсуждение выходит за рамки настоящего обзора. Тем не менее, недавние данные предполагают, что демпинг может быть связан с повышенными уровнями циркулирующего GLP-1 и других гормонов кишечника (20).В других сообщениях указывается на повышенный постпрандиальный инсулиновый ответ и гиперинсулинемическую гипогликемию, возможно, из-за островковой гиперплазии (21), хотя последнее явление остается редким и малоизученным. Большинство случаев демпинг-синдрома легкие и поддаются изменению диеты (22). Антагонисты кальциевых каналов или акарбоза могут принести облегчение (23, 24). Изнуряющий демпинг-синдром, невосприимчивый к консервативному лечению, встречается редко. В таких случаях было предложено ревизионное хирургическое вмешательство, включая процедуры, направленные на отсрочку опорожнения мешка и восстановление ограничений в питании, такие как уменьшение мешка и ревизия анастомоза с или без установки перианастомического кольца или бандажа (25).Эндоскопическая складка гастроеунального анастомоза также изучалась, но ее эффективность еще не была четко продемонстрирована (26). Частичная панкреатэктомия по поводу гиперинсулинемической гипогликемии использовалась как последнее средство лечения с различной эффективностью (25).
Боль, как правило, не является доминирующим симптомом, но может быть связана с вздутием живота, спазмами и диареей, которые сопровождают эпизоды демпинга. Симптомы часто возникают из-за продуктов с высоким содержанием рафинированного сахара, но могут быть вызваны и другими продуктами. Патогенез демпинг-синдрома до конца не изучен, и его полное обсуждение выходит за рамки настоящего обзора. Тем не менее, недавние данные предполагают, что демпинг может быть связан с повышенными уровнями циркулирующего GLP-1 и других гормонов кишечника (20).В других сообщениях указывается на повышенный постпрандиальный инсулиновый ответ и гиперинсулинемическую гипогликемию, возможно, из-за островковой гиперплазии (21), хотя последнее явление остается редким и малоизученным. Большинство случаев демпинг-синдрома легкие и поддаются изменению диеты (22). Антагонисты кальциевых каналов или акарбоза могут принести облегчение (23, 24). Изнуряющий демпинг-синдром, невосприимчивый к консервативному лечению, встречается редко. В таких случаях было предложено ревизионное хирургическое вмешательство, включая процедуры, направленные на отсрочку опорожнения мешка и восстановление ограничений в питании, такие как уменьшение мешка и ревизия анастомоза с или без установки перианастомического кольца или бандажа (25).Эндоскопическая складка гастроеунального анастомоза также изучалась, но ее эффективность еще не была четко продемонстрирована (26). Частичная панкреатэктомия по поводу гиперинсулинемической гипогликемии использовалась как последнее средство лечения с различной эффективностью (25).