Базис и надстройка схем эрадикационной терапии Helicobacter pylori
Юрий Павлович Успенский, профессор, доктор медицинских наук:
– Уважаемые коллеги, следующая часть нашей гастроэнтерологической секции посвящена проблеме хеликобактериоза человека. И я с удовольствием хотел бы предоставить слово глубокоуважаемой Татьяне Львовне Лапиной с таким философичным докладом: «Базис и надстройка схем эрадикационной терапии Helicobacter pylori».
Татьяна Львовна Лапина, доцент, кандидат медицинских наук:
– Спасибо большое, Юрий Павлович. Итак, дорогие коллеги, действительно из старой философии взяты эти термины: «Базис и надстройка схем эрадикационной терапии пилорического хеликобактера». Если говорить о многообразии схем, которые применялись когда-либо и описаны в литературе для того, чтобы провести эрадикацию пилорического хеликобактера, то это многообразие схем невозможно описать. Это такое обилие различных лекарственных препаратов, самые разные комбинации, самая разная продолжительность, попытка давать двухступенчатые схемы и так далее.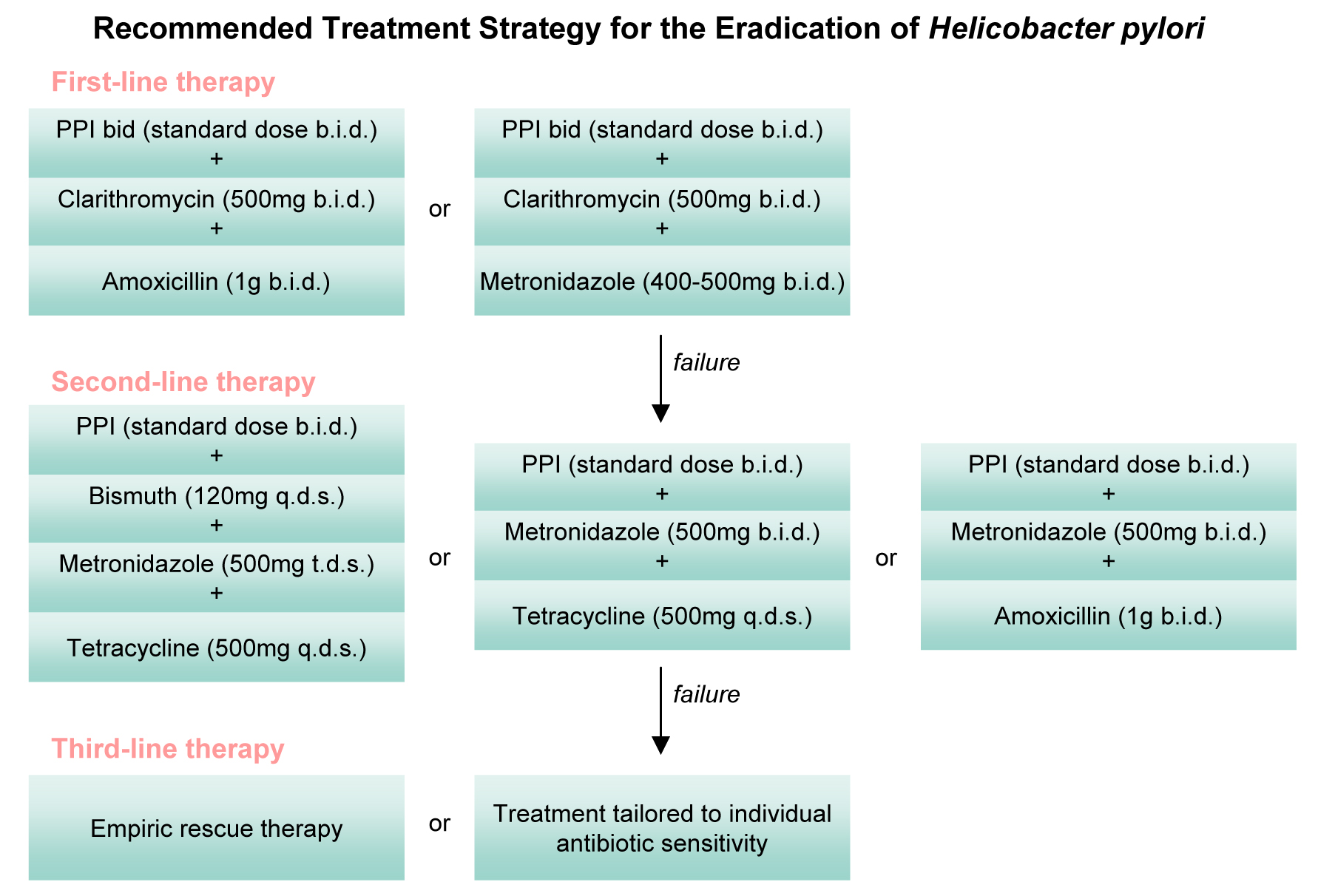
Российская Гастроэнтерологическая Ассоциация в своих рекомендациях по диагностике и лечению инфекции пилорического хеликобактера постаралась очень четко для практикующих врачей обозначить порядок обращения к этим схемам лечения. В качестве первой линии мы можем выбрать стандартную тройную терапию или квадротерапию. В случае неудачи терапии первой линии мы можем обратиться к квадротерапии с препаратом висмута. А в случае неудачи этой схемы лечения мы можем обратиться к резервному антибиотику в составе тройной терапии с «Левофлоксацином».
В качестве первой линии мы можем выбрать стандартную тройную терапию или квадротерапию. В случае неудачи терапии первой линии мы можем обратиться к квадротерапии с препаратом висмута. А в случае неудачи этой схемы лечения мы можем обратиться к резервному антибиотику в составе тройной терапии с «Левофлоксацином».
Так вот, вроде бы мы занимаемся лечением микробного агента. Может быть, главное в схеме эрадикационной терапии, базис – это антибактериальные препараты. Вы знаете, я бы все-таки говорила о том, что главное в схеме эрадикационной терапии, базис – это ингибиторы протонной помпы. Обратите внимание, при перечислении всех схем на первое место установлены препараты из группы ингибиторов протонной помпы. Почему ингибиторы протонной помпы имеют такое принципиальное значение для эрадикационной терапии? Все дело в том, что мы очень хорошо можем предсказать эффективность ингибиторов протонной помпы. Если обратиться к вот этой классической схеме необходимого поддержания уровня интрагастрального pH для лечения кислотозависимых заболеваний, то мы здесь видим полученный pH >3 для успешного заживления дуоденальной язвы.
Вернемся к классическим представлениям о пилорическом хеликобактере (Helicobacter pylori). Любая бактерия продуцирует АТФ (ATP) с помощью так называемой протон-движущей силы, то есть электрохимического градиента ионов водорода. Вот редукс-помпа (на схеме это окислительно-восстановительный насос) создает отрицательный заряд электрохимического градиента внутри клетки, что, собственно, и используется для образования АТФ (ATP).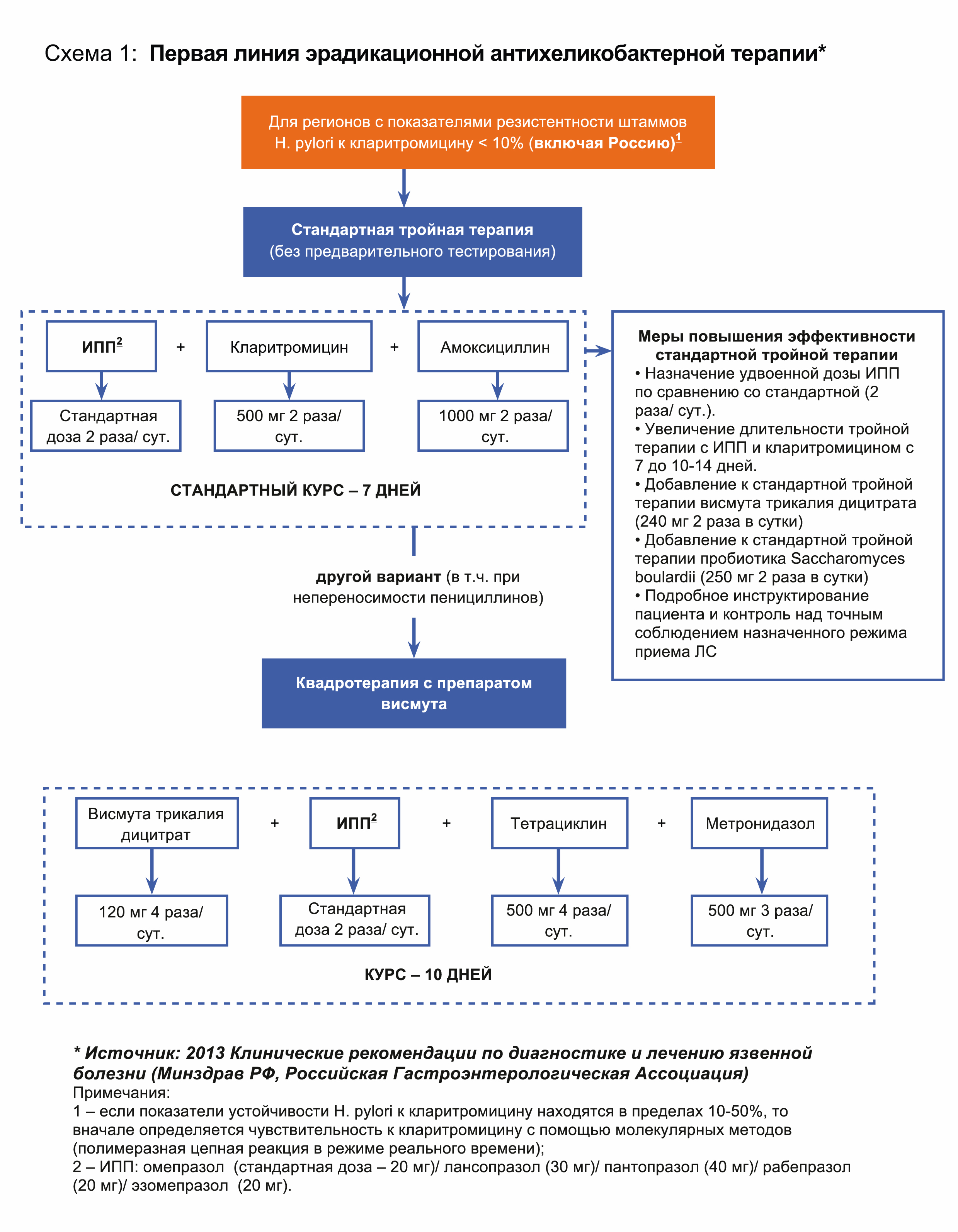
Что позволяет хеликобактеру активно выживать? Фермент уреаза, который разлагает мочевину с образованием ионов аммония. Ионы аммония по сути дела предохраняют вот этот самый электрохимический градиент ионов водорода. Совершенно другая ситуация складывается, когда мы назначаем пациенту ингибиторы протонной помпы, и мы искусственно приводим к желаемым значениям pH энтерогастральным для того, чтобы у нас успешно рубцевалась дуоденальная язва, заживали эрозии при гастроэзофагеальной рефлюксной болезни или проходила эрадикация пилорического хеликобактера.
Позвольте представить вам очень старое классическое исследование. Мы видим здесь две группы столбиков. Первые столбики показывают нам процент эрадикации при назначении любимых наших антибиотиков «Амоксициллина» и «Кларитромицина», но только желтый столбик без ингибиторов протонной помпы. Посмотрите, пожалуйста – никакой эрадикации, по сути дела, не наступает. А вот если мы даем три препарата на основе ингибиторов протонной помпы, то разница в проценте эрадикации просто колоссальная.
То же самое касается других вариантов стандартной тройной терапии: «Кларитромицин», «Метронидазол». Мы видим, что если мы даем пациенту только «Кларитромицин» с «Метронидазолом» без ингибитора протонной помпы, то существует очень большой прирост в эффективной эрадикации, который дает нам ингибитор протонной помпы.

Итак, ингибиторы протонной помпы – действительно основа схем эрадикационной терапии, и они тем лучше работают, тем лучше они могут поддерживать энтерогастральный pH>5. Почему? Потому что именно в таких условиях пилорический хеликобактер становится особо чувствительным для действия тех антибиотиков, которые составляют надстройку схемы эрадикационной терапии. В основном мы сегодня будем в качестве примера базиса схемы эрадикационной терапии оперировать препаратом «Рабепразол». С удовольствием обращаю ваше внимание на график биоэквивалентности «Рабепразола» производства компании КРКА оригинальному препарату.
Итак, что является базисом для назначения схемы эрадикационной терапии? Конечно, способность ингибиторов протонной помпы поддерживать энтерогастральный pH в заданных пределах в течение заданного периода времени. И если мы посмотрим недавний мета-анализ, то действительно ингибиторы протонной помпы последнего поколения, в том числе «Рабепразол», с точки зрения процента среднего времени pH>4 при курсовом приеме стандартной дозы, показывают, конечно, очень и очень хороший результат.
Вернемся к схемам эрадикационной терапии. В качестве схемы первой линии лечения принята стандартная тройная схема эрадикационной терапии: ингибитор протонной помпы (ИПП) в стандартной дозе два раза в день, «Кларитромицин» (КЛА) 500 миллиграмм два раза в суки, «Амоксициллин» (АМО) 1000 миллиграмм два раза в сутки.
Возможно выбрать квадротерапию с препаратом висмута в определенных клинических ситуациях. Например, нам очень важно дать схему с максимально высокой эффективностью, например, в случае MALT-лимфомы желудка, когда мы планируем эрадикацию пилорического хеликобактера для того, чтобы достичь гистологической ремиссии опухоли. Это, конечно, комбинация ингибитора протонной помпы в стандартной дозе два раза в сутки, «Висмута трикалия дицитрата» (ВТД) 120 миллиграмм четыре раза в сутки, «Тетрациклина» (ТЕТ) и «Метронидазола» (МЕТ).
В качестве схемы, которую могут назначать гастроэнтерологи в спорных, сложных случаях Российская Гастроэнтерологическая Ассоциация рекомендует использование схемы с «Левофлоксацином». Еще раз повторюсь, конечно, это не назначение врача первичного звена здравоохранения, это все-таки назначение, которое должен делать гастроэнтеролог. Есть ли в России данные по последовательной терапии? К сожалению, не очень много данных, хотя есть единичные работы, которые говорят о том, что можно применять эту схему. Опять же, вот эта последовательная терапия достаточно сложная, которая стоит из двух этапов назначения препаратов для эрадикации пилорического хеликобактера, скорее, входит в арсенал гастроэнтеролога, чем врача первичного звена здравоохранения. Давайте посмотрим, как работает стандартная тройная терапия на основе «Рабепразола». Посмотрите, пожалуйста, доза «Рабепразола» здесь достаточно маленькая, 10 миллиграмм два раза в сутки. И, несмотря на то, что это азиатская популяция, в которой всегда сложно добиться успешной эрадикации пилорического хеликобактера, все-таки в реальной клинической практике процент эрадикации превышает 80.
Еще раз повторюсь, конечно, это не назначение врача первичного звена здравоохранения, это все-таки назначение, которое должен делать гастроэнтеролог. Есть ли в России данные по последовательной терапии? К сожалению, не очень много данных, хотя есть единичные работы, которые говорят о том, что можно применять эту схему. Опять же, вот эта последовательная терапия достаточно сложная, которая стоит из двух этапов назначения препаратов для эрадикации пилорического хеликобактера, скорее, входит в арсенал гастроэнтеролога, чем врача первичного звена здравоохранения. Давайте посмотрим, как работает стандартная тройная терапия на основе «Рабепразола». Посмотрите, пожалуйста, доза «Рабепразола» здесь достаточно маленькая, 10 миллиграмм два раза в сутки. И, несмотря на то, что это азиатская популяция, в которой всегда сложно добиться успешной эрадикации пилорического хеликобактера, все-таки в реальной клинической практике процент эрадикации превышает 80.
Можно ли увеличить эффективность стандартной тройной терапии? Можно, причем работая как с базисом схемы, так и с надстройкой схемы. Например, мы можем добавить к стандартной тройной терапии препарат висмута. Я думаю, что это очень удачное дополнение к надстройке схемы. Мы можем увеличить дозу ингибитора протонной помпы, и этот дополнительный антикислотный эффект скажется на приросте эрадикации инфекции пилорического хеликобактера. Мы можем увеличить продолжительность стандартной тройной терпи. Сложно, конечно, сказать, что любой из нас получит вот такой замечательный прирост в проценте эрадикации, в зависимости от того, 7, 10 или 14 дней мы назначаем стандартную тройную терапию. Но все-таки современная тенденция, конечно, говорит о том, что чем дольше мы проводим эрадикационную терапию в рамках обозначенных сроков, тем выше процент эрадикации.
Например, мы можем добавить к стандартной тройной терапии препарат висмута. Я думаю, что это очень удачное дополнение к надстройке схемы. Мы можем увеличить дозу ингибитора протонной помпы, и этот дополнительный антикислотный эффект скажется на приросте эрадикации инфекции пилорического хеликобактера. Мы можем увеличить продолжительность стандартной тройной терпи. Сложно, конечно, сказать, что любой из нас получит вот такой замечательный прирост в проценте эрадикации, в зависимости от того, 7, 10 или 14 дней мы назначаем стандартную тройную терапию. Но все-таки современная тенденция, конечно, говорит о том, что чем дольше мы проводим эрадикационную терапию в рамках обозначенных сроков, тем выше процент эрадикации.
И, конечно, хочется обратить внимание еще раз на базисные препараты в схемах эрадикационной терапии. Посмотрите, пожалуйста, 35 исследований, практически 6 тысяч больных. Мета-анализ, который изучал: есть ли преимущества более современных ингибиторов протонной помпы, «Рабепразола» и «Эзомепразола», по сравнению с более старыми, более классическими ингибиторами протонной помпы. И, видите, здесь число больных, которых необходимо пролечить – 23. Действительно есть данные о том, что схемы на основе «Рабепразола» обладают большей эффективностью. Что мне хочется показать? Мне хочется показать этот мета-анализ с точки зрения разных дозировок ингибиторов протонной помпы. Посмотрите, пожалуйста: здесь 10 миллиграмм два раза в сутки «Рабепразол» использовался. А вот этот же мета-анализ – 20 миллиграмм два раза в сутки. И мы видим, что благодаря мощному, кислотоподавляющему эффекту «Рабепразола» здесь даже доза 10 миллиграмм два раза в сутки отлично действует для эрадикации пилорического хеликобактера.
И, видите, здесь число больных, которых необходимо пролечить – 23. Действительно есть данные о том, что схемы на основе «Рабепразола» обладают большей эффективностью. Что мне хочется показать? Мне хочется показать этот мета-анализ с точки зрения разных дозировок ингибиторов протонной помпы. Посмотрите, пожалуйста: здесь 10 миллиграмм два раза в сутки «Рабепразол» использовался. А вот этот же мета-анализ – 20 миллиграмм два раза в сутки. И мы видим, что благодаря мощному, кислотоподавляющему эффекту «Рабепразола» здесь даже доза 10 миллиграмм два раза в сутки отлично действует для эрадикации пилорического хеликобактера.
Я должна сказать, что когда я увидела вот этот терракотовый барельеф Римской эпохи – вы видите Геракла с дубиной, он расправляется с лернейской гидрой – мне сразу показалось, что лернейская гидра кого-то мне сильно напоминает. Мне кажется, что аналогия с пилорическим хеликобактером здесь налицо. И очень приятно сказать в заключение моей лекции, что действительно у нас есть оружие для того, чтобы победить гидру пилорического хеликобактера – это схемы эрадикационной терапии инфекции пилорического хеликобактера. Только должны мы четко соблюдать стандарты ведения пациентов с инфекцией пилорического хеликобактера.
Только должны мы четко соблюдать стандарты ведения пациентов с инфекцией пилорического хеликобактера.
Что предлагает медицина для борьбы с Helicobacter pylori
Хеликобактерная инфекция является одной из потенциальных причин развития гастрита и язвенной болезни желудка. Роль инфекционного фактора в развитии данных заболеваний была клинически доказана. Любая терапия воспалительного процесса в области желудка окажется неэффективной без использования средств, губительно воздействующих на данный микроорганизм. Консервативная медицина использует различные схемы эрадикации хеликобактер пилори, при этом каждая схема имеет свои особенности, преимущества и недостатки.
Что такое эрадикация
Эрадикация helicobacter pylori объединяет несколько стандартных лечебных режимов, направленных на подавление жизнедеятельности данного микроорганизма. После уничтожения хеликобактерной инфекции, в слизистой оболочке желудка создаются благоприятные условия для купирования воспалительного процесса и заживление эрозивно-язвенных очагов..gif) Любая из схем эрадикации helicobacter pylori может быть использована в том случае, если оно соответствует таким критериям:
Любая из схем эрадикации helicobacter pylori может быть использована в том случае, если оно соответствует таким критериям:
- Эффективность терапии составляет не менее 80% при повторном обследовании пациента. На эффективность указывает исчезновение воспалительного процесса и полное заживление эрозивно-язвенных очагов.
- Продолжительность схемы эрадикации составляет не более 14 дней.
- Используемые препараты обладают низкой токсичностью и вызывают побочные эффекты не более чем в 15% случаев.
- Простой режим приёма препаратов. Человек, проходящий схему эрадикации не должен обладать специализированными навыками.
Говоря о том, что это такое эрадикация, нельзя не упомянуть, что этот процесс даже с возможностями современной медицины является продолжительным и не всегда обеспечивает нужный результат.
Разновидности схем
Для лечения хеликобактерной инфекции используются препараты 1 и 2 линии, при этом каждая схема может иметь трехкомпонентный или четырехкомпонентный состав.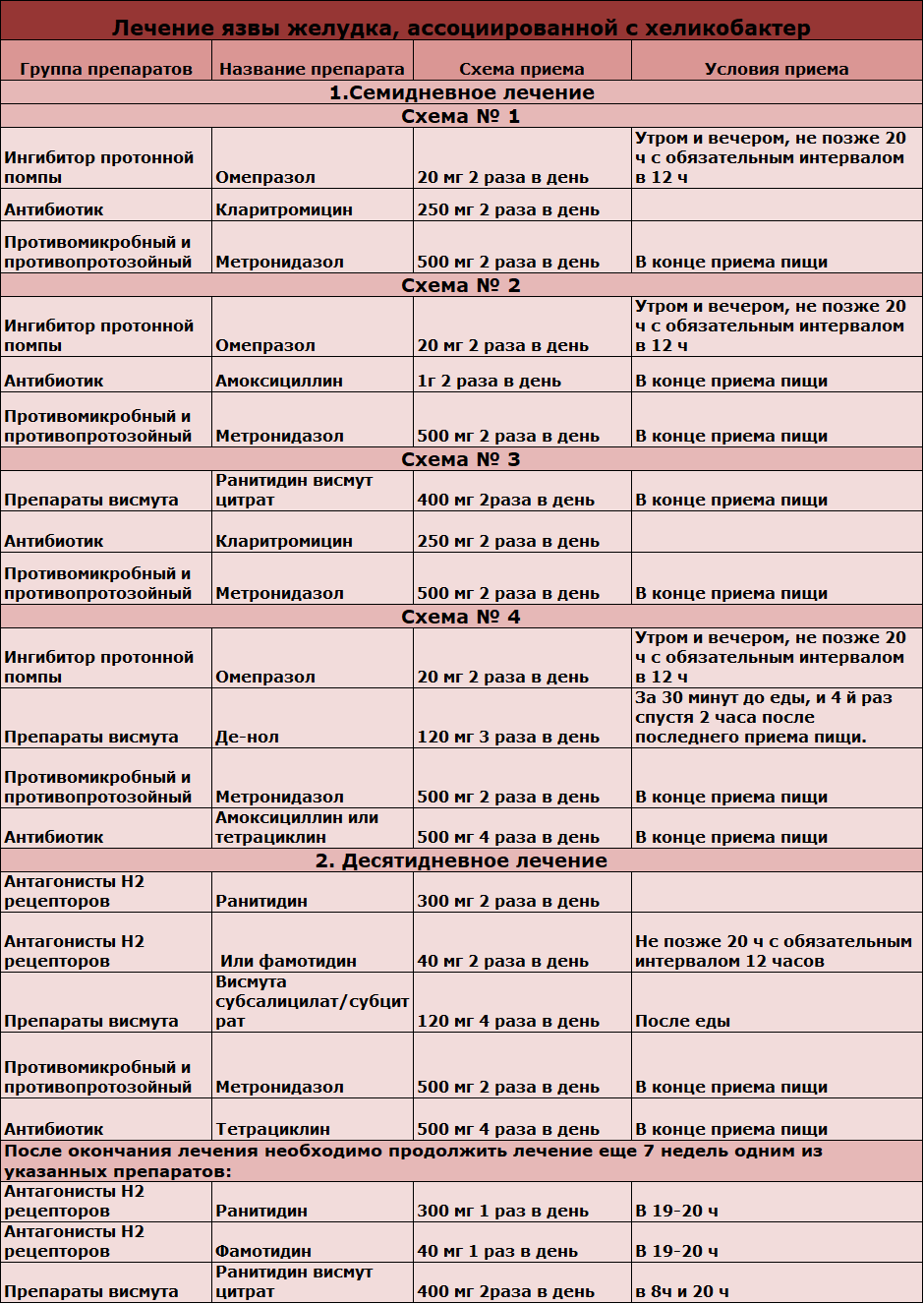
Первая линия
Трехкомпонентная схема лечения при эрадикации хеликобактер пилори, включает прием таких медикаментов:
- Один из ингибиторов протонного насоса в стандартной дозировке (Пантопразол, Лансопразол, Омепразол, Рабепразол, Эзомепразол).
- Метронидазол или Амоксициллин.
- Кларитромицин.
Эффективность трехкомпонентной схемы эрадикации может быть усилена за счёт увеличения её продолжительности до 10-14 дней.
Вторая линия
В данном случае используется четырехкомпонентная схема эрадикации хеликобактерной инфекции .Данная схема включает такие препараты:
- Тетрациклин.
- Субсалицилат висмута.
- Метронидазол.
- Одно из наименований ингибиторов протонной помпы в стандартной дозировке (продолжительность терапии более 10 дней).
Выбор схемы эрадикационной терапии при хеликобактер пилори проводится индивидуально, на основании результатов медицинского обследования.
Несмотря на то, что традиционная медицина продолжает использовать стандартные методики эрадикации хеликобактерной инфекции, этот вариант лечения продолжает находиться под сомнением, так как антибактериальные средства не только частично уничтожают бактерию, но и провоцируют ряд побочных реакций.
Полноценной альтернативой стандартным схемам лечения хеликобактерной инфекции, является метапребиотик Стимбифид Плюс, который помогает ускорить процесс эрадикации бактериальной инфекции, восстановить структуру слизистой оболочки желудка и побороть воспалительный процесс. Биодобавка одинаково эффективна при гастрите как с повышенной, так и со сниженной кислотностью.
Стандартная эрадикационная терапия хеликобактерной инфекции основана на внешнем воздействии на бактерию. Клинически доказано, что этот метод лечения является тупиковым и не гарантирует полное уничтожение микроорганизма. Принципиально новым способом является так называемое эндогенное воздействие на хеликобактер пилори посредством увеличения популяции собственной микробиоты желудка. Инновационный путь эрадикации был успешно испытан на людях-добровольцах. Метапребиотик Стимбифид Плюс помогает избавиться от хеликобактерной инфекции посредством таких механизмов:
Инновационный путь эрадикации был успешно испытан на людях-добровольцах. Метапребиотик Стимбифид Плюс помогает избавиться от хеликобактерной инфекции посредством таких механизмов:
- Прямой механизм. Компоненты метапребиотика создают неблагоприятные условия для поддержания жизнедеятельности хеликобактер пилори.
- Косвенный механизм. Угнетение популяции хеликобактерной инфекции достигается за счет увеличения количества собственной микрофлоры желудка.
Биодобавка одинаково эффективна как при остром, так и при хроническом течении воспалительного процесса в области желудка. Продолжительность терапии метапребиотиком Стимбифид Плюс составляет от 12 до 28 дней. В ходе клинических испытаний, спустя 30 дней после начала приёма метапребиотика, был проведён контрольный анализ на определение хеликобактерной инфекции. В 100% случаев отмечалась полная эрадикация бактерии.
Метапребиотик используется в качестве монотерапии, при этом отсутствует необходимость в дополнительном приёме препаратов из стандартных схем эрадикации. Важно помнить, что хеликобактерная инфекция является одним из потенциальных факторов развития не только гастрита и язвенной болезни желудка, но и онкологии данного органа.
Важно помнить, что хеликобактерная инфекция является одним из потенциальных факторов развития не только гастрита и язвенной болезни желудка, но и онкологии данного органа.
Своевременная эрадикация бактериальной инфекции помогает снизить риск до минимума. При использовании стандартных методик, эрадикация хеликобактер пилори + схема лечения должна регулярно согласовываться с лечащим врачом. Используя метапребиотик Стимбифид Плюс, человек может самостоятельно проводить терапию в домашних условиях, принимая только одно средство.
К основным преимуществам использования метапребиотика Стимбифид Плюс при гастрите, ассоциированном с хеликобактер пилори можно отнести:
- Биодобавка может быть одинаково использована для взрослых, так и детей, старшей 3-х лет.
- В отличие от антибиотиков, Стимбифид Плюс уничтожает хеликобактерную инфекцию, активизирует рост нормальной микрофлоры в желудке и не вызывает побочные реакции.
/ Доктор Стимбифид
Поделиться в соцсетях:
СХЕМЫ ЭРАДИКАЦИИ ШТАММОВ HELICOBACTER PYLORI, РЕЗИСТЕНТНЫХ К МЕТРОНИДАЗОЛУ У ДЕТЕЙ | Щербаков
1. Щербаков П.Л. Поражения верхних отделов пищеварительного тракта у детей (клинико-эндоскопические исследования). Автореф. дис…. докт. мед. наук. М. 1997. 34 с.
Щербаков П.Л. Поражения верхних отделов пищеварительного тракта у детей (клинико-эндоскопические исследования). Автореф. дис…. докт. мед. наук. М. 1997. 34 с.
2. Schwarz K. Ueber penetrierende Magen und Jejunalgeschwunde. Beitr. Klin. Chir. 1910; 67: 96-128.
3. Marshall B.J., Warren J.R. Unindencifield curved bacilli in the stomach of patient with gastritis and peptic ulceration. Lancet. 1984; 1: 1311.
4. Satoh K., Kimura K., Takimoto T., Kihira K. A follow up study of atrophic gastritis and intestinal metaplasia after eradication of Helicobacter pylori. Helicobacter. 1998; 3 (4): 236-240.
5. Eradication of Helicobacter pylori normalizes elevated mucosal levels of epidermal growth factor and its receptor. Am. J. Gastroenterol. 1999; 94 (10): 2885–2889.
Am. J. Gastroenterol. 1999; 94 (10): 2885–2889.
6. Ganga-Zandzou P.S., Michaud L., Vincent P. еt al. http://www3.infotrieve.com/medline/infotrieve/results.asp?search+simplesearch+view1+nmed98-99+25+0+wAAA+(‘Helicobacter’):TANatural outcome of Helicobacter pylori infection in asymptomatic children: a two-year follow up study. Pediatrics. 1999; 104 (2): 216–221.
7. Nawaz A., Mohammed I., Ahsan K. et al. Clostridium difficult colitis associated with treatment of Helicobacter pylori infection. Am. J. Gastroenterol. 1998; 93(7): 1175–1176.
8. Sёoderlin M.K., Alasaarela E.,; Hakala M. Reactive arthritis induced by Clostridium difficult enteritis as a complication of Helicobacter pylori eradication. Clin. Rheumatol. 1999; 18 (4): 337–338.
9. http://www3.infotrieve.com/medline/infotrieve/results.asp?search+simplesearch+view1+nmed98-99+25+0+wAAA+(‘Adamsson+I’):AUAdamsson I.., Nord C.E., Lundquist P. et al. Comparative effects of omeprazole, amoxycillin plus metronidazole versus omeprazole, clarithromycin plus metronidazole on the oral, gastric and intestinal microflora in Helicobacter pylori-infected patients. J. Antimicrob. Chemother. 1999; 44 (5): 629–640.
http://www3.infotrieve.com/medline/infotrieve/results.asp?search+simplesearch+view1+nmed98-99+25+0+wAAA+(‘Adamsson+I’):AUAdamsson I.., Nord C.E., Lundquist P. et al. Comparative effects of omeprazole, amoxycillin plus metronidazole versus omeprazole, clarithromycin plus metronidazole on the oral, gastric and intestinal microflora in Helicobacter pylori-infected patients. J. Antimicrob. Chemother. 1999; 44 (5): 629–640.
10. Mahony D.E., Lim-Morrison S., Bryden L. et al. Antimicrobial activities of synthetic bismuth compounds against Clostridium difficile. Antimicrob. Agents. Chemother. 1999; 43 (3): 582–588.
11. Лыкова Е.А., Сидоренко С.В., Бондаренко В.М. и др. Антибактериальная терапия и коррекция микроэкологических нарушений при хеликобактериозе у детей. Диагностика и лечение. 1996; 12: 75–77.
12. Мазурин А.В. Болезни органов пищеварения. М.: Медицина. 1984. С. 254–333.
Мазурин А.В. Болезни органов пищеварения. М.: Медицина. 1984. С. 254–333.
13. Аруин Л.И., Григорьев П.Я., Исаков В.А., Яковенко Э.П. Хронический гастрит. Амстердам. 1993. 362 с.
14. Zala G., Wirth H.P., Bauer S. et al. Eradication of metronidazole-resistant Helicobacter pylori: is omeprazole/amoxicillin a therapeutic alternative? Schweiz. Med. Wochenschr. 1994; 124 (31–32): 1385–1390.
15. Sieber C.C.; Frei R.; Beglinger C. et al. Helicobacter pylori resistance against metronidazole in Switzerland: implications for eradication therapy? Schweiz. Med. Wochenschr. 1994; 124 (31–32): 1381–1384.
16. Hudson N., Brydon W.G., Eastwood M.A. et al. Successful Helicobacter pylori eradication incorporating a one week antibiotic regimen. Aliment. Pharmacol. Ther. 1995; 9 (1): 47.
Aliment. Pharmacol. Ther. 1995; 9 (1): 47.
17. Holton J., Vaira D., Menegatti M. The susceptibility of Helicobacter pylori to the rifamycin, rifaximin. Antimicrob. Chemother. 1995; 35 (4): 545–549.
Хеликобактер пилори: мифы и реальность
Helicobacter pylori (хеликобактер пилори, в дальнейшем — НР) — бактерия, которая инфицирует различные области желудка и двенадцатиперстной кишки, вызывая в слизистой оболочке изменения, приводящие к развитию гастрита, язвы, рака.
Международное агентство по изучению рака (IARC) отнесло НР к канцерогенам первой группы (определенный канцероген). НР — не единственный этиологический фактор рака желудка, но он играет причинную роль в цепи событий, ведущих к его развитию.
Следует отметить, что заболеваемость раком желудка в Беларуси достаточно высока, в Европейском регионе в 2016 г. мы занимали первое место по этому показателю, в 2017 году второе. Именно поэтому стратегия поголовного лечения этой инфекции является абсолютно оправданной, это действительно сохраняет чьи-то реальные жизни в перспективе.
мы занимали первое место по этому показателю, в 2017 году второе. Именно поэтому стратегия поголовного лечения этой инфекции является абсолютно оправданной, это действительно сохраняет чьи-то реальные жизни в перспективе.
Бактерия была вновь открыта в 1979 году австралийским патологом Робином Уорреном, который затем провёл дальнейшие исследования её вместе с Барри Маршаллом, начиная с 1981 года.
Уоррен и Маршалл высказали предположение, что большинство язв желудка и гастритов у человека вызываются инфицированием микроорганизмом НР, а не стрессом или острой пищей, как предполагалось ранее.
В 2005 году Робин Уоррен и Барри Маршалл были удостоены Нобелевской премии по медицине за открытие НР.
Сколько же людей в Беларуси инфицировано?
Около 80% взрослого населения Беларуси заражены НР, а в странах Западной Европы и США — 30—40%. Такой же уровень заражения НР, как в нашей стране, наблюдается в Украине и России.
В Японии, где отмечается высокая заболеваемость раком желудка, существует национальная программа по эрадикации HР (пациенты получают препараты для эрадикации бесплатно), что позволило значительно снизить не только количество носителей НР в популяции, но и заболеваемость раком желудка.
Каким образом можно заразиться НР-инфекцией?
В первую очередь, следует отметить, что заражение в основном происходит в семьях, в случаях, если инфицированы родители, инфицируются и дети. Заражение может происходить через столовые приборы и посуду, а также пустышку или бутылочку, в случае с маленькими детьми, через слюну и прочие слизистые выделения, например, при поцелуе; через предметы индивидуальной гигиены и личную косметику (губную помаду).
Поскольку носителями различных видов НР являются домашние животные (собаки, кошки) – важно соблюдение мер личной гигиены при общении с ними.
Также возможны случаи заражения через медицинское оборудование, после обследования больного.
Всегда ли нужно лечить НР-инфекцию?
Существуют определенные ситуации, в которых обязательно нужно проводить эрадикацию НР:
— Язва 12-перстной кишки и/или желудка в настоящее время или в прошлом
— Лимфома желудка
— Атрофический (аутоиммунный) гастрит
— У пациентов – родственников 1-й степени родства (мать, отец, братья, сестры) больных раком желудка
— Диспепсия (наличие жалоб, связанных с желудком)
— Желание пациента
В любом случае врач всегда должен найти общий язык с пациентом, объяснить ему, зачем назначает эрадикационную терапию, и только после этого назначать лечение.
Какие схемы лечения лучше использовать?
В 2016-2017 годах было принято несколько глобальных соглашений по диагностике и лечению НР-инфекции: это Маастрихтское соглашение, Киотский консенсус. Врачи и эксперты всего мира договорились о стратегии, выработали тактику для более успешного выявления и лечения этой инфекции.
Схемы лечения легко найти в интернете, однако самостоятельно назначать себе лечение не стоит. Лучше предварительно проконсультироваться с участковым терапевтом, который и должен назначить вам схему лечения с учетом индивидуальных особенностей (аллергия на лекарственные препараты, наличие сопутствующих заболеваний, прием антибактериальных препаратов в анамнезе).
Если раньше схема эрадикации по длительности занимала 7-10 дней, то по последним рекомендациям – продолжительность ее увеличилась до 14 дней. Это повышает вероятность успеха в лечении.
Также для улучшения переносимости эрадикационных схем и уменьшения вероятности развития побочных эффектов, таких, как антибиотик-ассоциированная диарея, рекомендуется параллельно с антибиотиками принимать препарат из группы пробиотиков (энтерол, энтерожермина и др. ).
).
Нужно ли делать контроль после лечения и каким образом?
Последние вышедшие клинические протоколы диагностики и лечения заболеваний органов пищеварения рекомендуют проводить контроль эрадикации НР после лечения. Способы могут быть разными – это либо гастроскопия с взятием биопсии (морфологический контроль является «золотым стандартом»), либо проведение дыхательного теста, а также определение антигенов НР в кале.
В нашей стране сейчас доступны разные виды дыхательных тестов для определения наличия НР, однако наиболее надежным является С13-УДТ (С13-уреазный дыхательный тест), который проводится с помощью газоанализатора, в основном в РБ используются аппараты немецкой фирмы FAN. Определение антигенов НР в кале в Минске пока недоступно, однако в некоторых городах РБ этот анализ можно сделать.
Врач-гастроэнтеролог консультационного отделения
О.С. Полякова
RECOMMENDATIONS OF THE AMERICAN GASTROENTEROLOGIST BOARD, MASSTRIKHT v/FLORENTINE AND TORONTO CONSENSUSES
16 МЕДИЦИНСКИЙ СОВЕТ • №15, 2017
ЗАБОЛЕВАНИЯ ПИЩЕВОДА И ЖЕЛУДКА
ность штаммов с двойной резистентностью <15%. В реги-
В реги-
онах с высокой (>15%) двойной резистентностью H.pylori
к кларитромицину и метронидазолу висмут-содержащая
квадротерапия является лечением выбора [1].
Вторая линия эрадикационной терапии используется
при неэффективности первой попытки лечения H.pylori.
Если применялась тройная терапия с кларитромицином,
оптимальным вариантом второй линии будет квадротера-
пия с препаратами висмута. Также допустим любой про-
токол с левофлоксацином, но лучше его назначить, если
лечение квадротерапией с препаратами висмута оказа-
лось безуспешным.
Оптимальным вариантом третьей линии терапии после
неудачи с тройной терапией, включающей кларитромицин,
и последующего висмут-содержащего лечения является
схема с левофлоксацином. Если она уже использовалась, а
применение протокола с кларитромицином нецелесоо-
бразно по какой-либо из вышеописанных причин, жела-
тельно в качестве третьей линии использовать еще раз
какой-либо прочий, не идентичный вариант оптимизиро-
ванной терапии с висмутом. Возможны другие варианты
Возможны другие варианты
третьей и даже четвертой линии лечения без рифабутина
(табл.) при учете приведенного ранее факта, что к препара-
там висмута резистентность микроорганизма H. pylori не
формируется, а к тетрациклину, амоксициллину и фуразоли-
дону наблюдается реже чем в 2% случаев. Таким образом,
протоколы с этими антибактериальными препаратами
можно повторять в более длительном или измененном
вариантах, но в рамках стандартных протоколов.
Обязательным правилом эрадикационной терапии остается
строгое соблюдение стандартных, апробированных в РКИ
протоколов эрадикации (табл.). В практической работе не
допускается «рационализация» с составом компонентов
схемы лечения, дозировкой ЛС и продолжительностью тера-
пии. Разумеется, при проведении РКИ применяется новый
вариант лечения, который сравнивается со стандартным.
Последней линией лечения, которая используется
после безуспешности 3–4 схем эрадикации, является про-
токол с рифабутином. Резистентность H.pylori к рифабутину
Резистентность H.pylori к рифабутину
в настоящее время практически отсутствует. Рифабутин
применяется внутрь независимо от приема пищи. Для
лечения туберкулеза используется в комбинации с други-
ми средствами. Хотя резистентность к Mycobacterium
tuberculosis является актуальной проблемой, эпизодиче-
ское применение рифабутина не может существенно
повлиять на развитие этой устойчивости. Следует учиты-
вать возможный миелотоксический эффект рифабутина.
Оценивать результаты лечения следует не раньше чем
через месяц после окончания эрадикационной терапии. С
нашей точки зрения, лучше это сделать через два месяца.
Это позволит уменьшить количество ложноотрицатель-
ных случаев диагностики микроорганизма H.pylori.
КАК УЛУЧШИТЬ РЕЗУЛЬТАТЫ ЛЕЧЕНИЯ?
Первый и самый простой, а также фармакоэкономиче-
ски оправданный путь повышения эффективности лече-
ния– увеличение дозы ИПП. На сегодняшний день убе-
дительно доказано, в том числе метаанализами, что сни-
жение кислотопродукции желудка (подъем внутрижелу-
дочной рН) повышает эффективность эрадикационной
терапии, особенно при использовании амоксициллина и
кларитромицина [1, 8, 12].
Таким образом, в состав эрадикационной терапии дол-
жен входить ИПП в двойной дозе, например омепразол
40мг (2 капсулы по 20 мг) два раза в день. В соответствии
с проведенными исследованиями надежным ИПП являет-
ся препарат Омитокс (омепразол). Он показал высокую
эффективность в лечении кислотозависимых заболеваний
и эрадикации микроорганизма H.pylori [13, 14]. В эради-
кационных протоколах Омитокс можно использовать в
дозе 40мг (2 капсулы по 20 мг) два раза в день. По дан-
ным О.Н. Минушкина и соавт., эффективность эрадикации
при использовании последовательной терапии с
Омитоксом (Омитокс 20 мг 2 раза в день + Азитрал 500 мг
2 раза в день в течение 5 дней, затем Омитокс 20 мг 2
раза в день + амоксициллин 1000 мг 2 раза в день в тече-
ние последующих 5 дней) достигает 90% [15]. Отмечено
также уменьшение активности воспаления слизистой
оболочки желудка после проведения эрадикации с про-
токолом, включающей Омитокс.
Для улучшения результатов лечения хеликобактерной
инфекции предпочтение следует отдавать оптимизирован-
ным вариантам. Такой выбор, кроме использования высо-
кой дозы ИПП, предполагает максимальную длительность
лечения. Последовательная и гибридная терапия, судя по
ряду исследований, обладает более мощным эрадикацион-
ным потенциалом, чем простые тройные варианты лечения.
Что касается дополнительной терапии пробиотиками
для снижения побочных эффектов эрадикации H.pylori, то
эксперты Торонтского консенсуса высказались против ее
рутинного применения, поскольку его эффективность не
имеет убедительных доказательств. В американских реко-
мендациях указывается, что использование пробиотиков в
качестве адъювантной терапии при эрадикации вызывает
растущий интерес в США. Показано, что штаммы
Lactobacillus и Bifidobacterium оказывают угнетающий
эффект на H.pylori. Хотя появился метаанализ, показываю-
щий повышение частоты успешной эрадикации при
использовании пробиотиков, снижение числа случаев
побочных эффектов и повышение приверженности лече-
нию [16], авторы рекомендаций отмечают, что многие
вопросы в этой области (дозировка, время, длительность
приема) остаются неясными и рекомендации по их исполь-
зованию отсутствуют. Эксперты Маастрихт V/Флорен тий-
Эксперты Маастрихт V/Флорен тий-
ского консенсуса отметили положительный эффект отдель-
ных пробиотиков (Saccharomyces boulardii, Lacto bacillus) на
снижение побочных эффектов во время проведения эра-
дикационного лечения, однако в заключении этого разде-
ла указывается на необходимость дальнейших исследова-
ний для более определенного понимания проблемы. В то
же время снижение частоты антибиотико-ассоциирован-
ной диареи предрасполагает к повышению привержен-
ности лечению. Нередко при использовании макролидов
наблюдается неопасная диарея, связанная с прокинетиче-
ским эффектом этой группы антибиотиков.
Последовательная терапия первой линии в сравнении со стандартной тройной терапией для эрадикации Helicobacter pylori
Вопрос обзора
Для того, чтобы оценить разницу в частоте излечения между обоими методами лечения, и выявить факторы, которые могут улучшить или уменьшить частоту излечения для обоих методов лечения.
Актуальность
Основной причиной язва и рака желудка является инфекция, вызванная бактерией Helicobacter pylori, вредным микроорганизмом, способным колонизировать человеческий желудок. Опубликованные данные свидетельствуют о том, что эта бактерия присутствует почти у половины населения земного шара. Бактериальная колонизация приводит к хронической инфекции, которая с течением времени может изменить функцию желудка, структуру тканей, и даже клеточный цикл, вызывая множество симптомов и заболеваний.
Хотя на этот микроорганизм действуют традиционные антибиотики, он характеризуется сильной резистентностью к лечению, и в высоком проценте случаев может выживать при большинстве схем однокомпонентной и двухкомпонентной терапии. Поэтому применялись различные комбинации антибиотиков, и какое лечение является наилучшим, до сих пор неясно. Наиболее часто рекомендуемой схемой является стандартная тройная терапия (СТТ), содержащая два антибиотика (кларитромицин и нитроимидазол или амоксициллин) и препарат, защищающий желудок (омепразол). Однако, некоторые исследования показали, что СТТ терпит неудачу у более, чем одного из пяти человек, поэтому исследователи предложили заменить её на висмут не содержащую четырехкомпонентную последовательную (ПДТ) терапию, включающую первый этап двойной терапии (амоксициллин и омепразол), и последующий этап тройной терапии (нитроимидазол, кларитромицин и омепразол).
Характеристика исследований
Мы провели поиск в электронных базах данных и в сообщениях конференций, с целью найти любые релевантные исследования. Мы включили 44 исследования, в которых тестировали и сравнили частоту излечения последовательной терапии (ПДТ) по отношению к СТТ. Наш обзор охватывает научные исследования по апрель 2015 года.
Основные результаты
В обзоре указано, что до 2008 года частота излечения при последовательной терапии (ПДТ) была выше, чем при стандартной тройной терапии (СТТ). Однако, частота излечения при обоих методах ниже, чем мы хотели бы. Обзор показал, что эффективность зависит от нескольких факторов, включая географический регион исследования, резистентность бактерий, и дату проведения исследования. Например, мы нашли уменьшение частоты излечения с течением времени как при СТТ, так и при ПДТ, с более сильным снижением частоты излечения при ПДТ. Это означало, что в исследованиях, опубликованных после 2008 года, ПДТ была не более эффективной, чем тройная терапия, когда и ПДТ, и СТТ были применены в течение 10 дней.
Доказательства, собранные и объединенные в этом обзоре, не поддерживают использование последовательной терапии (ПДТ) потому, что ее эффективность соответствует СТТ, и даже может быть улучшена стандартной тройной терапией (СТТ), назначаемой в течение 10 или 14 дней, или с более сильным ингибированием кислотообразования. Результаты при ПДТ были лишь частично успешными. Нам нужно найти другую форму терапии, чтобы обеспечить лучшее лечение для пациентов.
Качество доказательств
Исследования, включенные в этот обзор, были смешанного качества, однако, наши анализы не предполагают, что качество исследований повлияло на частоту излечения.
Антихеликобактерная терапия | Клиника «Медлайн» в Кемерово
Helicobacter pylori — один из наиболее «популярных» микроорганизмов, широко изучаемый учеными из многих стран и известный как микроб. Попадание Helicobacter pylori в организм человека приводит к развитию язвенной болезни и гастрита, может способствовать формированию злокачественных новообразований желудка.
Установлено, что H. pylori выявляется приблизительно у 30-35% населения в детском возрасте и 50-85% — у взрослых. При наличии показаний врач-гастроэнтеролог назначает проведение эрадикационной антихеликобактерной терапии.
Источники и пути передачи возбудителя
Источником инфекции является человек. Жизнеспособные штаммы H.pylori выделены из содержимого желудка, двенадцатиперстной кишки, пищевода, фекалий людей с активным гастритом и язвенной болезнью. Наиболее изученным является контактный механизм передачи инфекции от больного человека или бактерионосителя орально-оральным или фекально-оральным путем. Возможен также механизм передачи инфекции через грязные руки.
Факторы передачи возбудителя
Наиболее вероятные факторы передачи — вода и пища. H.pylori способен выживать в охлажденной речной воде в течение нескольких дней. Имеются данные о возможности выживания H.pylori в зубном налете, слюне, рвотных массах и желудочном соке.
Группы риска
Факторами риска развития хеликобактерной инфекции являются: перенаселенность жилых помещений, общие кровати, отсутствие достаточного количества горячей воды. Здесь же – семьи, где есть заболевший, а также медицинский персонал гастроэнтерологических клиник (хирурги, эндоскописты, обслуживающий персонал), контингенты специнтернатов, психиатрических стационаров, детских домов.
Диагностика хеликобактерной инфекции в клинике «Медлайн»
Диагностика Helicobacter pylori выполняется при помощи инвазивных и неинвазивных методик (инвазивные тесты (биопсия) и неинвазивные тесты) до лечения – первичная диагностика, и после проведения противохеликобактерной терапии — контроль эффективности выбранной схемы лечения.
Лечение хеликобактерной инфекции
Лечение хеликобактерной инфекции называется эрадикационной терапией. Основным принципом терапии является принцип эрадикации Н.pylori.
Эрадикация – полное уничтожение вегетативных и кокковых форм Н.pylori в желудке и двенадцатиперстной кишке человека.
Показания к проведению эрадикационной терапии:
- Язвенная болезнь желудка или 12-перстной кишки в стадии обострения или ремиссии, включая осложненную язвенную болезнь
- MALT-лимфома
- Атрофический гастрит
- Состояние после резекции желудка по поводу рака
- Ближайшим родственникам больных раком желудка – по желанию пациента (после подробной консультации врача)
Кроме того, проведение эрадикационной терапии целесообразно по следующим показаниям:
- Функциональная диспепсия
- Гастроэзофагеальная рефлюксная болень (ГЭРБ)
Требования, предъявляемые к антихеликобактерной терапии:
- Способность уничтожить бактерию Н.pylori как минимум в 80% случаев
- Не вызывать вынужденной отмены терапии врачом, вследствие побочных эффектов (допустимо менее чем в 5% случаев) или прекращения пациентом приёма лекарств по схеме, рекомендованной врачом
- Эффективность при продолжительности курса не более 7-14 дней
Принципы антихеликобактерной терапии:
- Использование многокомпонентных схем лечения — тройная терапия или квадротерапия
- Строгое соблюдение выбранной схемы лечения
- Прием выбранных лекарственных препаратов в определенных дозах и при определённой продолжительности терапии
- Учёт совместимости (синергизма) лекарственных препаратов
Инфекция H. pylori: ACG обновляет Рекомендации по лечению — Практическое руководство
Ключевые моменты практики
• Тестирование на Helicobacter pylori показано при определенных состояниях, таких как язвенная болезнь, и его следует лечить у любого пациента с положительным результатом теста.
• Пациентов следует спросить о предыдущем воздействии антибиотиков, чтобы помочь составить схему лечения и избежать неудач из-за резистентности.
• Для определения успеха лечения следует использовать дыхательный тест на мочевину, анализ фекальных антигенов или биопсию.
От редакции AFP
Инфекция Helicobacter pylori — одна из наиболее распространенных хронических бактериальных инфекций. Американский колледж гастроэнтерологии (ACG) обновил свои клинические рекомендации в ответ на значительные научные достижения в лечении этого заболевания.
Поскольку в Северной Америке (определенных в данном руководстве как Соединенные Штаты и Канада) отсутствуют рандомизированные контролируемые испытания, оценивающие современные схемы лечения, рекомендации ACG в основном основываются на данных клинических испытаний, полученных в других частях мира.Эти лечебные рекомендации основаны на ряде вопросов.
Что известно об эпидемиологии инфекции H. pylori в Северной Америке? Какие группы риска?
Инфекция H. pylori обычно возникает в детстве, хотя способы заражения неясны. Факторы риска включают низкий социально-экономический статус; увеличение количества братьев и сестер; и наличие инфицированного родителя, особенно матери. Заболеваемость и распространенность заболевания обычно выше среди лиц, родившихся за пределами Северной Америки.В Северной Америке это чаще встречается у иммигрантов и в определенных расовых группах. (в целом распространенность среди неиспаноязычных белых ниже, чем среди других групп, таких как чернокожие, латиноамериканцы, коренные американцы и коренные жители Аляски).
Каковы показания для тестирования и лечения H. pylori?
Некоторым пациентам показано обследование на H. pylori. Любой пациент с положительным результатом на инфекцию H. pylori должен получить лечение.
Все пациенты с активной или ранее перенесенной язвенной болезнью должны быть проверены на H.pylori, если нет документации о том, что инфекция была ранее излечена. Пациенты с лимфомой лимфоидной ткани, ассоциированной со слизистой оболочкой желудка низкой степени злокачественности, или с анамнезом эндоскопической резекции раннего рака желудка также должны быть обследованы. Тестирование у пациентов с гастроэзофагеальной рефлюксной болезнью не рекомендуется, если у пациента в анамнезе нет язвенной болезни или диспепсии. Если при обследовании пациента с гастроэзофагеальной рефлюксной болезнью обнаруживается инфекция H. pylori, лечение следует предлагать с учетом того, что симптомы гастроэзофагеальной рефлюксной болезни вряд ли улучшатся.
Основываясь на доказательствах низкого качества, ACG также рекомендует тестирование тем, кто начинает длительную терапию нестероидными противовоспалительными препаратами, пациентам с необъяснимой железодефицитной анемией и взрослым с идиопатической тромбоцитопенической пурпурой.
В идеале для диагностики инфекции H. pylori следует использовать тесты для выявления активной инфекции, такие как дыхательный тест на мочевину, тест на фекальный антиген или эндоскопическая биопсия. Однако, поскольку предварительная вероятность заражения выше у пациентов с документально подтвержденной язвенной болезнью, для этих пациентов приемлемо тестирование на антитела к иммуноглобулину G.Неэндоскопическое тестирование — это вариант у пациентов моложе 60 лет с неисследованной диспепсией без красных флажков. Если у пациентов с диспепсией используется эндоскопия, следует выполнить биопсию желудка.
Недостаточно доказательств, чтобы дать рекомендации относительно тестирования и лечения бессимптомных пациентов с семейным анамнезом рака желудка или пациентов с лимфоцитарным гастритом, гиперпластическими полипами желудка или гиперемезисом беременных.
Каковы научно обоснованные стратегии лечения первой линии для врачей в Северной Америке?
H.pylori обычно лечат комбинацией антибиотиков и ингибитора протонной помпы (ИПП). Пациентов следует спросить о предыдущем приеме антибиотиков, чтобы помочь составить схему лечения. Не существует схемы со 100% излечением от инфекции H. pylori, и очень мало схем с коэффициентом излечения 90%, если таковые вообще имеются. Авторы использовали рекомендованные и предложенные термины, чтобы выразить свои предпочтения.
РЕКОМЕНДУЕТСЯ
Тройная терапия кларитромицином состоит из ИПП, кларитромицина (биаксина) и амоксициллина или метронидазола (флагил) в течение 14 дней.Эффект устойчивости H. pylori к кларитромицину хорошо задокументирован. Следует избегать применения кларитромицина в местах, где резистентность превышает 15%, а также у пациентов, ранее подвергавшихся воздействию макролидов.
Квартальная терапия висмутом состоит из ИПП, висмута, тетрациклина и нитроимидазола в течение 10–14 дней. Это может быть особенно хорошим вариантом для пациентов, подвергшихся воздействию макролидов или страдающих аллергией на пенициллин. Хотя резистентность к метронидазолу влияет на эффективность этого режима, она не так сильна, как тройная терапия кларитромицином.Четырехкратную терапию висмутом следует строго рассматривать как терапию первой линии при высокой резистентности к кларитромицину или у пациентов, ранее подвергавшихся воздействию макролидов.
Сопутствующая терапия включает ИПП, кларитромицин, амоксициллин и нитроимидазол (тинидазол [Тиндамакс] или метронидазол) в течение 10–14 дней. Эта схема является многообещающим вариантом, который, как показали международные исследования, не менее эффективен, чем тройная терапия кларитромицином с аналогичной переносимостью.Ограниченные данные показывают, что эффекты устойчивости к кларитромицину при этой схеме меньше, чем при тройной терапии кларитромицином. Продолжительность от 10 до 14 дней кажется подходящей, хотя исследования для оценки того, улучшает ли эрадикацию продление терапии до 14 дней, продолжаются.
ПРЕДЛАГАЕМЫЙ
Последовательная терапия состоит из ИПП и амоксициллина в течение пяти-семи дней, а затем ИПП, кларитромицина и нитроимидазола в течение пяти-семи дней. Хотя 10 дней последовательной терапии кажутся жизнеспособной альтернативой 14 дням тройной терапии кларитромицином, 10 дней последовательной терапии не превосходили 14 дней тройной терапии кларитромицином.Продление последовательной терапии до 14 дней может улучшить показатели эрадикации, но необходимы дополнительные исследования. Сложность последовательной терапии может ограничивать ее использование.
Гибридная терапия, гибрид последовательной и сопутствующей терапии, состоит из ИПП и амоксициллина в течение семи дней, за которыми следуют ИПП, амоксициллин, кларитромицин и нитроимидазол в течение семи дней. Эта схема является многообещающим вариантом, который, как показали международные исследования, не менее эффективен, чем тройная терапия кларитромицином с аналогичной переносимостью.Хотя рандомизированные контролируемые испытания показали, что гибридная терапия похожа на сопутствующую терапию, сложность гибридной терапии может ограничивать ее использование.
Тройная терапия левофлоксацином состоит из ИПП, левофлоксацина (левакина) и амоксициллина в течение 10–14 дней. Левофлоксацин — это фторхинолон, обладающий антимикробной активностью in vitro в отношении грамположительных и грамотрицательных бактерий, включая H. pylori. Немногочисленные имеющиеся данные позволяют предположить, что устойчивость к фторхинолонам может быть такой же, если не выше, чем устойчивость к кларитромицину в Северной Америке.Также отсутствуют данные о влиянии устойчивости к фторхинолонам на лечение. Тройная терапия левофлоксацином в течение 10–14 дней представляется сопоставимой альтернативой тройной терапии кларитромицином. Лучшими вариантами, по-видимому, являются последовательная терапия фторхинолоном (ИПП и амоксициллин в течение пяти-семи дней, затем ИПП, фторхинолон и нитроимидазол в течение пяти-семи дней) или терапия НАГРУЗКОЙ (левофлоксацин, омепразол [Прилосек], нитазоксанид [ Алиния] и доксициклин в течение 7-10 дней).
Какие факторы предсказывают успешную ликвидацию при лечении инфекции H. pylori?
Факторы успеха могут быть связаны с факторами пациента или с инфекцией. Основными детерминантами являются выбор режима, соблюдение пациентом режима приема нескольких лекарственных препаратов с частыми побочными эффектами, а также чувствительность штамма H. pylori к комбинации используемых антибиотиков. Количество доз в день и тяжесть побочных эффектов влияют на приверженность лечению. Перед тем, как начать лечение, врачи должны обсудить преимущества и проблемы терапии.Другие факторы пациента, такие как курение сигарет, сахарный диабет и генетика, также могут играть роль в неэффективности лечения.
Из факторов, связанных с инфекцией, чувствительность к антибиотикам оказалась наиболее важным фактором успеха лечения в клинических испытаниях и популяционных исследованиях. Устойчивость к кларитромицину, метронидазолу и левофлоксацину ограничивает их эффективность и увеличивает распространенность инфекции H. pylori. Устойчивость к амоксициллину, тетрациклину и рифабутину (микобутину) встречается редко.
Что мы знаем об устойчивости к противомикробным препаратам H. pylori в Северной Америке? Какие методы можно использовать для оценки устойчивости и когда их следует использовать?
Данных о сопротивлении немного. Необходимы дополнительные исследования для определения местных, региональных и национальных моделей устойчивости H. pylori к антибиотикам, которые помогут выбрать режим лечения.
Устойчивость можно оценить с помощью культурального или молекулярного тестирования; однако эти методы не широко доступны в Соединенных Штатах.Тестирование посредством посева сложно выполнить и занимает несколько дней. В случае успеха методы культивирования включают разбавление в агаре, дисковую диффузию и Е-тест. Молекулярные тесты, такие как полимеразная цепная реакция или гибридизация флуоресцентно меченых нуклеиновых кислот, являются более быстрой и простой альтернативой культивированию. Однако молекулярное тестирование на устойчивость к H. pylori в настоящее время не одобрено Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США.
Отсутствие знаний об устойчивости к H. pylori в Соединенных Штатах резко контрастирует с другими частями мира, создавая препятствия для рекомендаций по лечению, основанных на фактических данных.
Должны ли мы проверять эффективность лечения после эрадикационной терапии H. pylori?
Поскольку эффективность эрадикационной терапии H. pylori снижается, после лечения нередко возникает хроническая инфекция. Для определения успеха лечения следует использовать дыхательный тест на мочевину, анализ фекальных антигенов или биопсию. Тестирование следует проводить как минимум через четыре недели после завершения антибактериальной терапии и после того, как лечение ИПП было прекращено в течение одной-двух недель. Хотя рекомендация по посттестированию интуитивно понятна, научных доказательств рентабельности такого тестирования нет, за исключением сценария кровотечения из пептических язв.
В случае неудачи терапии первой линии, каковы варианты терапии спасения?
Если инфекция сохраняется после лечения, следует избегать применения тех же антибиотиков при повторном лечении пациента. Режимы четырехкратной терапии висмутом или левофлоксацина предпочтительны для пациентов, которые первоначально получали режим, содержащий кларитромицин. Схема, содержащая кларитромицин или левофлоксацин, предпочтительна для пациентов, которые первоначально получали четырехкратную терапию висмутом. При выборе терапии спасения следует учитывать данные о местной устойчивости к противомикробным препаратам и предыдущее воздействие антибиотиков на пациента.Как и терапия первой линии, рекомендации ACG по спасательной терапии основаны на эмпирическом отборе, а не на результатах культурального исследования и тестирования чувствительности к противомикробным препаратам.
Четырехкратная терапия висмутом (ИПП, висмут, тетрациклин, метронидазол) в течение 14 дней или тройная терапия левофлоксацином (ИПП, левофлоксацин, амоксициллин) в течение 14 дней являются рекомендуемыми режимами спасения. Другие предлагаемые схемы включают сопутствующую терапию (ИПП, кларитромицин, амоксициллин, нитроимидазол) в течение 10–14 дней, тройную терапию рифабутином (ИПП, амоксициллин и рифабутин) в течение 10 дней и двойную терапию высокими дозами (ИПП и амоксициллин) в течение 14 дней. .Тройная терапия кларитромицином не рекомендуется для терапии спасения.
Когда следует рассмотреть возможность проведения теста на аллергию на пенициллин у пациентов с инфекцией H. pylori?
Амоксициллин — важный компонент схем лечения H. pylori. Однако есть альтернативы, которые не включают амоксициллин, в первую очередь четырехкратная терапия висмутом. Тестирование на аллергию может быть рассмотрено после одного или двух неудачных попыток терапии первой линии. Чаще всего исключается истинная аллергия на пенициллин, и можно безопасно начинать терапию, содержащую амоксициллин.
Источник рекомендаций: Американский колледж гастроэнтерологии
Используется ли система оценки доказательств? Да
Описан систематический поиск литературы? Да
Руководство разработано участниками, не имеющими финансовых связей с промышленностью? №
Рекомендации, основанные на результатах, ориентированных на пациента? Да
Опубликованный источник: Am J Gastroenterol. Февраль 2017 г .; 112 (2): 212–239
Доступно по адресу: https://www.nature.com/ajg/journal/v112/n2/full/ajg2016563a.html [требуется вход в систему]
Лучшая стратегия ликвидации Helicobacter pylori в эпоху устойчивости к антибиотикам
Антибиотики (Базель). 2020 Aug; 9 (8): 436.
Су Ён Ким
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; moc.revan@2121ezeerb
Джун-Вон Чунг
2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдон-даэро 774beon-gil, Namdong-gu, Инчхон 21565, Корея
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу Университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; мок.revan @ 2121ezeerb2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдонг-даэро 774beon-gil, Namdong-gu, Инчхон 21565, Корея
Получено 30 июня 2020 г .; Принято 21 июля 2020 г.
Лицензиат MDPI, Базель, Швейцария. Эта статья — статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution (CC BY) (http://creativecommons.org/licenses/by/4.0/). Эта статья цитировалась другими статьями в PMC. .Abstract
Устойчивость к антибиотикам является основной причиной неэффективности лечения Helicobacter pylori , а учащение случаев устойчивости к антибиотикам является проблемой для клиницистов. Особую проблему представляет устойчивость к кларитромицину и метронидазолу. Стандартная тройная терапия (ингибитор протонной помпы, амоксициллин и кларитромицин) больше не подходит в качестве лечения первой линии в большинстве регионов. Недавние рекомендации по лечению инфекции H. pylori рекомендуют четырехкратную схему лечения (висмут или невисмут) в качестве терапии первой линии.Эта стратегия лечения эффективна для областей с высокой резистентностью к кларитромицину или метронидазолу, но частота резистентности неизбежно возрастает в результате длительной терапии несколькими антибиотиками. Новая терапия на основе калий-конкурентных блокаторов кислоты может быть эффективной, но данные ограничены. Индивидуальная терапия, основанная на результатах теста на чувствительность к противомикробным препаратам, является идеальным вариантом. В этом обзоре обсуждались текущие важные схемы лечения H. pylori и оптимальные H.pylori .
Ключевые слова: Helicobacter pylori , устойчивость к антибиотикам, эрадикация
1. Введение
Helicobacter pylori — грамотрицательная, жгутиковая, спиралевидная бактерия, проникающая в слизистую оболочку верхнего отдела желудочно-кишечного тракта [1] , 2]. Он вызывает пептические язвы, рак желудка и другие желудочные заболевания [3,4] и составляет 25% всех злокачественных новообразований, связанных с инфекциями; это также связано с повышенным риском рака желудочно-кишечного тракта [5].Искоренение H. pylori облегчает язвенную болезнь и снижает риск рака желудка [6,7]. В глобальном масштабе рекомендации по лечению H. pylori постепенно меняются, а показания расширяются [4,8,9,10]. Кроме того, с экономическим развитием многих развивающихся стран и увеличением стареющего населения число людей, получающих лечение H. pylori , увеличивается.
В 1990-х годах для эрадикации H.pylori и в настоящее время является стандартом во всем мире [11,12]. С тех пор уровень искоренения тройной терапии во многих регионах заметно снизился [13,14]. Причины этого снижения включают бактериальные факторы, повторное инфицирование, генетический полиморфизм CYP2C19 и соблюдение пациентом режима лечения [15]. Устойчивость к антибиотикам является наиболее важной причиной неудач лечения H. pylori [13,16]. Резистентность к кларитромицину H. pylori особенно серьезна; Схемы, содержащие кларитромицин, больше не подходят из-за степени эрадикации <80% [14,17].Уровень устойчивости к метронидазолу и хинолонам (которые в основном используются в качестве схем второго или третьего ряда) во всем мире составляет> 15% [14,16]. Поскольку количество антибиотиков, подходящих для эрадикации H. pylori , ограничено (кларитромицин, амоксициллин, метронидазол, левофлоксацин, тетрациклин и рифабутин), повышение устойчивости к антибиотикам является серьезной проблемой. Следовательно, исключения кларитромицина недостаточно для предотвращения устойчивости к антибиотикам H. pylori .
Текущие рекомендации подчеркивают важность местной распространенности устойчивости к антибиотикам при выборе подходящего H.pylori [4,9,10]. В регионах с высокой устойчивостью к определенным антибиотикам успех лечения можно улучшить, отказавшись от использования таких антибиотиков. Однако, хотя новая комбинация антибиотиков может повысить скорость эрадикации, она может вызвать резистентность. Правительство Тайваня ограничило использование противомикробных препаратов, что привело к низкому уровню первичной устойчивости к кларитромицину и метронидазолу у H. pylori [18]. Однако частота первичной резистентности к левофлоксацину увеличилась с 4.От 9% в 2000–2007 гг. До 13,4% в 2011–2012 гг. [18]. Кроме того, использование нескольких антибиотиков увеличивает частоту осложнений [4]. Поэтому важно определить оптимальную стратегию эрадикации H. pylori в соответствии с результатами теста на антибактериальную чувствительность (AST). Однако возможность ложноотрицательных результатов и возможность применения во всех медицинских учреждениях являются проблемой [19,20]. Мы рассмотрели наиболее важные схемы лечения против H. pylori , которые преодолевают устойчивость к антибиотикам, и стратегии, которые можно применять на практике.
2.
H. pylori Лечение на основе результатов ASTБактериальный посев обычно проводится перед выбором антибиотика, но посев H. pylori сложен и требует много времени. Исследование чувствительности к кларитромицину H. pylori улучшает скорость эрадикации [21,22]. Герритс и др. с помощью полимеразной цепной реакции (ПЦР) показали, что мутации A2142G и A2143G в 23S рРНК связаны с устойчивостью к антибиотикам [22]. ПЦР сравнительно прост и экономичен [21].Следовательно, для H. pylori лечение на основе AST, такое как диагностический тест на устойчивость к кларитромицину, является полезным. Однако в некоторых случаях уровень эрадикации составляет <100%. Это связано с тем, что точечные мутации, отличные от A2142G или A2143G, приводят к ненадежным результатам, например, A2142C, A2115G, G2142T, A2142T и T2182C [23,24]. Кроме того, распространение мутаций отличается географически. Мутация A2142C встречается <10% в США и Европе, но не зарегистрирована в Японии [25,26,27,28].В Гонконге частота мутации A2144G выше, чем в других регионах [29]. Различное распределение этих мутаций, вероятно, влияет на скорость эрадикации.
Терапия H. pylori , основанная на результатах AST, значительно улучшает скорость эрадикации. Однако, в отличие от других схем, мало исследований оценивали схемы первого ряда на основе АСТ. Уровень искоренения намерения лечить (ITT) для схемы первого ряда составляет> 90% [30,31,32]. В Южной Корее индивидуализированная терапия первой линии на основе ПЦР превосходит стандартную тройную терапию (STT; амоксициллин, кларитромицин и ИПП) [30,31].В греческом исследовании тройная терапия на основе генотипической резистентности (тестирование чувствительности к кларитромицину и левофлоксацину с помощью анализа GenoType HelicoDR) позволила достичь высокого уровня эрадикации H. pylori (90,2% по ITT и 97,8% по протоколам анализа (PP)). [32]. Кроме того, тройные схемы первой линии под контролем АСТ приводят к эрадикации> 90% у пациентов с H. pylori , устойчивым к двум антибиотикам [33]. Поскольку частота полирезистентности H. pylori увеличивается, это обнадеживающее открытие.Схемы первой линии эрадикации H. pylori на основе культивирования демонстрируют превосходный терапевтический эффект даже в регионах с высоким уровнем устойчивости к противомикробным препаратам [34]. Общие показатели устойчивости к амоксициллину, кларитромицину, метронидазолу и моксифлоксацину составляют 6,7%, 31,0%, 41,8% и 39,2% соответственно. Однако уровень эрадикации составляет 93,1% (ITT) и 100,0% (PP) [34]. Chen et al. сообщили, что управляемый по чувствительности модифицированный четырехкратный режим висмута первой линии для H. pylori в регионе с высокой степенью устойчивости к противомикробным препаратам имел высокий уровень эрадикации [35].
Показатель успеха схем второго ряда / спасения под контролем AST ниже, чем у схем первого ряда. Уровень эрадикации низкий (68%), несмотря на тестирование чувствительности для лечения спасения [36]. Аналогичным образом, в Соединенных Штатах терапия с культуральным контролем показала 60% -ный успех у пациентов, у которых не удалось по крайней мере три лечения [37]. Даже если посев определяет чувствительность к кларитромицину, повторный анализ кларитромицина после неудачи лечения не рекомендуется [38]. Следовательно, одна только терапия под контролем АСТ не может достичь требуемой скорости эрадикации.Liou et al. показали, что терапия с учетом генотипа не была значительно более эффективной, чем эмпирическая терапия для стратегии спасательной терапии (78,0% против 72,2%, p = 0,170) [39]. Следовательно, соответствующая эмпирическая терапия является альтернативой индивидуализированной генотипической терапии рефрактерной инфекции H. pylori .
3. Четырехкратная терапия висмутом
Четырехкратная терапия висмутом (BQT) состоит из висмута, PPI, метронидазола и тетрациклина. Он рекомендован как схема первой линии Торонтским консенсусом, Маастрихтским V / Флорентийским консенсусом и рекомендациями Американского колледжа гастроэнтерологии (ACG) [4,9,10].На режим BQT не влияет резистентность к кларитромицину. Согласно сетевому метаанализу, BQT в течение 10 или 14 дней превосходит STT в течение 7 дней [40]. Более того, BQT очень эффективен в качестве эмпирической схемы первого ряда (уровень эрадикации PP и ITT составляет 98,8% и 92,7% соответственно) [41]. Рандомизированное контролируемое исследование (РКИ) на Тайване показало, что уровень эрадикации у пациентов, получавших BQT, составил 96,0%, хотя частота нежелательных явлений составила 47,7% [42]. BQT оказался высокоэффективным в качестве схемы первого ряда для H.pylori в проспективном исследовании в Испании (94,4% (ITT) и 96,2% (PP)) [43]. BQT имеет отличную скорость эрадикации H. pylori , но комплаентность пациента может быть снижена из-за большого количества лекарств. Кроме того, BQT вводят четыре раза в день, что также может снизить комплаентность пациента. Чтобы преодолеть это, были введены схемы приема BQT два раза в день, и исследования в Южной Корее продемонстрировали их эффективность [44,45]. Kim et al. продемонстрировали, что два раза в день BQT в течение 1 недели был так же эффективен и безопасен, как традиционный четырехкратный ежедневный BQT (93.9% против 92,9%) [45]. Кроме того, большинство пациентов демонстрируют хорошую комплаентность, а уровень эрадикации BQT два раза в день высок (88,2% (ITT) и 98,4% (PP)) [44]. Разработана единая капсула, содержащая висмут, метронидазол и тетрациклин. Xie et al. показали, что терапия BQT одной капсулой была эффективной для эрадикации H. pylori и хорошо переносилась (86,5% (ITT) и 94,6% (PP)) [46]. В итальянском исследовании однокапсульная терапия BQT позволила достичь уровня эрадикации 91% (ITT) и 97% (PP) [47].Согласно метаанализу, при терапии BQT с одной капсулой первого и второго ряда уровень эрадикации приближался к 90%. Даже это применимо, независимо от типа и дозы ИПП, у пациентов со штаммом, резистентным к антибиотикам, и у тех, кто ранее лечился кларитромицином [48]. При 7-дневной схеме лечения BQT второго ряда уровень эрадикации составляет 93,6% (PP). Скорость эрадикации 7-дневного BQT значительно выше, чем у 14-дневного моксифлоксацина, содержащего тройной режим (93,6% против 73,8% (PP), p <0.001) [49].
Неясно, улучшится ли скорость эрадикации при увеличении периода лечения с 7 до 14 дней. Маастрихтский V / Флорентийский консенсус рекомендует прием препарата в течение не менее 10 дней [10]. Сообщается, что уровень устойчивости к тетрациклину во всем мире низкий [50,51]. Следовательно, устойчивость к метронидазолу является основным фактором успеха эрадикации H. pylori . Устойчивость к метронидазолу можно преодолеть путем увеличения частоты, количества и продолжительности приема, поэтому лечение в течение ≥10 дней рекомендуется в регионах с высокой степенью устойчивости к метронидазолу [52].
BQT показал отличные результаты в различных исследованиях, и сфера его применения постепенно расширяется. Кроме того, BQT можно относительно безопасно применять у пациентов с аллергией на пенициллин [4]. Сообщается, что BQT имеет более высокий уровень нежелательных явлений, чем STT, но схожий уровень соблюдения пациентом режима лечения [53,54]. Однако, поскольку показания BQT расширяются в качестве лечения первой линии, также возникают опасения. Количество схем второго ряда, которые можно применять, значительно сокращается, когда эрадикация с помощью BQT не дает результатов по первой линии.Кроме того, в будущем может повыситься уровень устойчивости к тетрациклину, который в настоящее время является относительно низким. Для решения этой проблемы в будущем необходимы различные исследования.
4. Сопутствующая терапия
Рекомендуется одновременное введение трех антибиотиков (кларитромицин, метронидазол или нитроимидазол и амоксициллин) и ИПП в течение 10–14 дней [4,9,10]. Несколько метаанализов показали, что сопутствующая терапия превосходит STT [55,56,57].Кроме того, недавний метаанализ показал, что сопутствующая терапия в течение 5 или 10 дней превосходила STT в течение 5, 7 или 10 дней [58]. Испанское исследование продемонстрировало, что сопутствующая терапия была значительно лучше, чем тройная терапия (92% против 70% (ITT), p = 0,02 и 92% против 74% (PP), p = 0,05) и эрадикация Скорость сопутствующей терапии была выше, чем у последовательной терапии устойчивых к антибиотикам штаммов [59]. Кроме того, сопутствующая терапия и BQT в качестве схем первого ряда показали сходные результаты H.pylori в анализах PP (97,7% против 96,2%, p = 0,605) и ITT (98,0% против 94,4%, p = 0,346) [43]. Более того, сетевой метаанализ показал, что сопутствующая терапия имеет более высокую эффективность, чем несколько других схем [40,60].
Сопутствующая терапия предпочтительнее последовательной терапии (ИПП и амоксициллин в течение 5 дней, затем ИПП, кларитромицин и тинидазол в течение еще 5 дней), потому что это проще. Существуют разногласия по поводу того, превосходит ли сопутствующая терапия над последовательной терапией [61,62,63,64,65].В испанском РКИ сопутствующая терапия была незначительно лучше (~ 5%) по сравнению с последовательной терапией (87% против 81% (ITT), p = 0,15; 91% против 86% (PP), p = 0,131) [65]. Кроме того, два метаанализа не выявили значительной разницы в скорости эрадикации между сопутствующей терапией и последовательной терапией [66,67].
Маастрихтский / Флорентийский консенсус не рекомендует последовательную терапию, в отличие от предыдущих руководств [10]. Это связано с тем, что последовательная терапия имеет более низкий уровень эрадикации, чем сопутствующая терапия в случаях резистентности к кларитромицину и чувствительности к метронидазолу H.pylori . И наоборот, когда H. pylori чувствителен к кларитромицину и устойчив к метронидазолу, последовательная терапия показывает более низкий уровень эрадикации, чем STT [10]. Увеличение дозы или продолжительности лечения метронидазолом может привести к эрадикации метронидазол-резистентного H. pylori . Скорость эрадикации при последовательной терапии невысока, поскольку период приема метронидазола составляет всего 5 дней.
Сопутствующая терапия имеет несколько ограничений, таких как более высокая частота нежелательных явлений, чем последовательная терапия [68].Повышенная частота осложнений может повлиять на соблюдение режима лечения H. pylori [69,70]. Хотя частота нежелательных явлений относительно высока, период лечения составляет менее 2 недель, поэтому большинство пациентов завершают курс лечения. Кроме того, есть опасения, что устойчивость к антибиотикам может повыситься из-за чрезмерного воздействия ненужных антибиотиков [71]. Наконец, эффекты сопутствующей терапии ниже у H . pylori, устойчивы как к кларитромицину, так и к метронидазолу [72].
5. Гибридная терапия
Гибридная терапия — это комбинация последовательной и сопутствующей терапии. Гибридная терапия включает ИПП и амоксициллин в течение 7 дней, затем ИПП, амоксициллин, кларитромицин и метронидазол в течение 7 дней [4]. Хотя Торонтский консенсус и Маастрихтский / Флорентийский консенсус не рекомендуют гибридную терапию, в клинических рекомендациях ACG рекомендуется использовать ее в качестве лечения первой линии у пациентов без предварительного воздействия макролидов в регионах с низким уровнем устойчивости к кларитромицину.Несколько метаанализов сообщили об эффективности и переносимости гибридной терапии [40,67,73]. Wang et al. продемонстрировали, что гибридная терапия была альтернативой сопутствующей или последовательной терапии (уровни эрадикации ITT гибридной, сопутствующей и последовательной терапии составили 88,6%, 86,3% и 84,7% соответственно; частота эрадикации PP составила 92,1%, 92,5% и 87,5%. ) [73]. Кроме того, нет значительных различий в переносимости или комплаентности между гибридной терапией и STT, последовательными или сопутствующими схемами [40,67,73].
В проспективном многоцентровом исследовании гибридная терапия вылечила> 90% пациентов с инфекцией H. pylori в регионах с высокими показателями устойчивости к кларитромицину и метронидазолу; это похоже на скорость эрадикации сопутствующей терапии [74]. Кроме того, комплаентность к гибридной терапии выше, чем к сопутствующей терапии (98,8% против 95,2%, p = 0,05). Однако скорость искоренения гибридной терапии значительно ниже для H.pylori . В проспективном исследовании частота эрадикации у пациентов с двойной устойчивостью к антибиотикам (кларитромицину и метронидазолу) была заметно снижена (50%) по сравнению с пациентами с резистентностью только к кларитромицину (91,4%) или метронидазолу (90,5%) [75].
6. Терапия на основе левофлоксацина
Левофлоксацин активен в отношении большого спектра различных бактерий, и в некоторых исследованиях левофлоксацин используется в качестве средства первой линии лечения инфекции H. pylori [15]. Проспективное исследование в Китае показало, что цефуроксим, левофлоксацин, ИПП и висмут в качестве терапии первой линии позволили достичь H.pylori составляет 97,2% случаев чувствительности к левофлоксацину и 84,0% случаев резистентности к левофлоксацину [76]. Однако в случаях устойчивости к цефуроксиму и левофлоксацину уровень эрадикации составил 0%. 14- и 7-дневные режимы дозирования левофлоксацина (левофлоксацин, кларитромицин, рабепразол и висмут) один раз в сутки показали уровень эрадикации 94% и 84% соответственно [77]. Gan et al. сравнили эффективность различных доз левофлоксацина для эрадикации H.pylori [78]. Показатели эрадикации в группах, получавших один и два раза в день, составили 77,5% и 79,5% (ITT) и 82,9% и 86,4% (PP), соответственно [78]. Нет значительных различий в степени искоренения или соблюдения режима лечения. Бычий лактоферрин усиливает эффективность схем первой линии на основе левофлоксацина при инфекции H. pylori [79]. Успешная эрадикация составляет 96,1% для эзомепразола / амоксициллина / левофлоксацина / бычьего лактоферрина и 75% для эзомепразола / амоксициллина / левофлоксацина [79].Режим LOAD (левофлоксацин, омепразол, нитазоксанид и доксициклин) был введен недавно [71]. Basu et al. сообщили, что уровень эрадикации LOAD составил 89,4% по сравнению с 73,3% для STT ( p <0,05) [80].
Левофлоксацин представляет собой хинолон и широко используется во всем мире, например, при пневмонии, инфекции мочевыводящих путей, туберкулезе и H. pylori . Таким образом, многие пациенты в анамнезе принимали левофлоксацин. В большинстве руководств рекомендуется применять схемы на основе левофлоксацина в качестве экстренной помощи, а не в качестве терапии первой линии [81].Клинические рекомендации ACG слабо рекомендуют тройной (амоксициллин, левофлоксацин и ИПП), последовательный (5-7 дней ИПП и амоксициллин, затем 5-7 дней ИПП, нитроимидазол и левофлоксацин) или четырехкратный (амоксициллин, левофлоксацин и ИПП). ИПП, левофлоксацин, доксициклин и нитазоксанид в течение 7 или 10 дней) по схемам первого ряда [4].
Ситафлоксацин представляет собой фторхинолон четвертого поколения и обладает высокой активностью против штаммов gyr A с положительной мутацией H. pylori [82].Ситафлоксацин в основном используется с амоксициллином или метронидазолом в качестве экстренной помощи, а не терапии первой линии. Сообщается, что схемы третьей линии, содержащие ситафлоксацин, эффективны для эрадикации H. pylori (75,8% (ITT) и 83,3% (PP)) [83]. Фторхинолоны четвертого поколения, такие как ситафлоксацин и гареноксацин, могут преодолеть устойчивость к хинолонам H. pylori [84,85]. Среди 100 штаммов с высокими показателями устойчивости к кларитромицину, метронидазолу и левофлоксацину> 95% чувствительны к ситафлоксацину [86].Следует оценить эффективность схем, содержащих ситафлоксацин или гареноксацин, против gyr A с положительной мутацией H. pylori .
7. Терапия на основе рифабутина
Рифабутин — это производное рифамицина, структурно сходное с рифампицином (противотуберкулезным препаратом). Он в основном используется при атипичном туберкулезе, таком как Mycobacterium avium -intracellulare и M. tuberculosis , устойчивых к рифампицину [87]. Рифабутин подавляет синтез белка путем ингибирования бета-субъединицы ДНК-зависимой РНК-полимеразы Helicobacter , которая кодируется rpoB .Следовательно, мутация rpoB придает устойчивость к рифабутину [88]. Все существующие руководящие принципы предполагают, что схемы на основе рифабутина следует рассматривать только как терапию «спасения» при эрадикации H. pylori [81]. Согласно метаанализу, эффективность лечения на основе рифабутина второй, третьей и четвертой / пятой линий составляет 79%, 66% и 70% соответственно [87]. В итальянском исследовании тройная терапия на основе рифабутина (рифабутин, амоксициллин и ИПП) в течение 14 дней позволила достичь скорости эрадикации 72.7% (PP) и 71,5% (ITT) у пациентов, у которых эрадикация H. pylori оказалась неэффективной после лечения традиционными антибиотиками [89]. Рифабутин не обладает такой же устойчивостью к антибиотикам, как кларитромицин и амоксициллин, а также является жирорастворимым и легко всасывается после перорального приема [88, 90]. Кроме того, рифабутин стабилен в широком диапазоне значений pH и не разлагается желудочной кислотой, а уровень устойчивости у H. pylori низкий, поскольку он редко используется в клинических условиях [87,91]. Следовательно, схемы на основе рифабутина важны для спасательной терапии.Однако другое исследование показало, что уровень искоренения терапии на основе рифабутина был невысоким: 50,0% в анализе ITT и 54,5% в анализе PP [92]. Поскольку есть некоторые части, которые не достигают стабильной скорости эрадикации в качестве спасательной терапии, можно считать, что необходимы соответствующие исследования.
На сегодняшний день большинство исследований схем на основе рифабутина сосредоточено на спасательной терапии. Недавно Graham et al. показали, что тройная схема на основе рифабутина (амоксициллин, рифабутин и ИПП) имела более высокий уровень эрадикации, чем амоксициллин плюс ИПП в качестве эмпирического лечения первой линии H.pylori (83,8% против 57,7%, p <0,001) [93]. Это говорит о том, что рифабутин является революционным препаратом первой линии в эпоху устойчивости к антибиотикам. Однако он дороже других антибиотиков. Кроме того, он может вызвать устойчивость к режиму лечения туберкулеза [94]. Более того, поскольку использование рифампицина способствует точечной мутации rpoB и увеличивает минимальную ингибирующую концентрацию (МИК) рифабутина, перед назначением рифабутина необходимо определить предшествующее лечение рифампицином [95].Наконец, рифабутин имеет небольшой риск миелотоксичности [87].
8. Терапия на основе калий-конкурентных кислотных блокаторов
Калий-конкурентные кислотные блокаторы (P-CAB) — это ингибитор секреции кислоты желудочного сока, с более быстрым началом и более длительным действием подавления кислоты, и более эффективен, чем ИПП. [96,97]. Кроме того, P-CAB не требует активации желудочной кислотой, поэтому его можно принимать независимо от времени приема пищи. В обращении H . pylori, pH желудка должен поддерживаться выше определенного уровня, чтобы активировать антибиотик [98].P-CAB ингибирует опосредованную H + и K + -АТФазу секрецию кислоты желудочного сока и является кислотоустойчивым и менее подвержен влиянию системы CYP2C19, чем ИПП [71,99]. Поскольку ИПП имеют короткую продолжительность действия и на их эффективность влияют различные подтипы цитохрома Р450 (ИПП в основном метаболизируются CYP2C19 и CYP3A4), внимание привлекла новая схема лечения против H. pylori , содержащая PCAB [99,100]. Вонопразан в настоящее время продается в Японии, продвигая исследования P-CAB для H.pylori лечение.
По данным многоцентрового РКИ в Японии, частота эрадикации первой линии тройной терапии на основе фонопразана (фонопразан, амоксициллин и кларитромицин) составила 92,6% по сравнению с 75,9% для STT ( p <0,0001) [101]. Метаанализ японских исследований с участием 1599 пациентов показал, что тройная терапия на основе фонопразана значительно превосходила STT у пациентов с устойчивыми к кларитромицину штаммами (82,0% против 40,0%, p <0,0001) [102].Напротив, уровень эрадикации чувствительных к кларитромицину штаммов существенно не отличается. Если организм устойчив к кларитромицину, STT переключается на двойную терапию (ИПП + амоксициллин), и двойная терапия важна для поддержания pH желудочного сока на уровне ≥6. В этом отношении считается, что у вонопразана есть сильные стороны. Кроме того, тройная схема на основе фонопразана так же эффективна, как и STT на основе ИПП на основе чувствительности, для эрадикации H. pylori (97,4% против 95,7%) [103]. В исследовании эффективности двойной терапии 7-дневного фонопразана и низких доз амоксициллина в качестве препарата первой линии H.pylori , уровни эрадикации двойной (фонопразан и низкие дозы амоксициллина) и тройной терапии (фонопразан, амоксициллин с низкой дозой и кларитромицин) составили 84,5% и 89,2% ( p = 0,203) по ITT-анализу соответственно. и 87,1% и 90,2% ( p = 0,372) по данным PP-анализа, соответственно [104]. В реальности увеличения устойчивости к противомикробным препаратам можно сказать, что снижение общего количества антибиотиков с использованием вонопразана показывает положительный аспект в будущем лечении H.pylori .
В Японии схемы на основе P-CAB лицензированы в качестве лечения первого и второго ряда для эрадикации H. pylori . Мураками и др. продемонстрировали эффективность тройной схемы второго ряда на основе P-CAB (частота успеха 98,0%) [101]. Другое РКИ показало, что тройная терапия на основе фонопразана (фонопразан, амоксициллин и ситафлоксацин) была более эффективной, когда ИПП использовался с этими антибиотиками в качестве схемы лечения третьей линии для H. pylori (83,3% против 57.1% (PP), p = 0,043) [83]. Следовательно, терапия на основе P-CAB может быть жизнеспособной альтернативой схемам первого и второго ряда для эрадикации H. pylori .
9. Лечение при неэффективности первичной терапии
Все руководства рекомендуют избегать ранее принимаемых пациентом антибиотиков [4,8,9,10]. В частности, следует избегать повторного использования кларитромицина и левофлоксацина из-за высоких показателей устойчивости. Они также рекомендуют схему лечения тройной второй линии на основе BQT или левофлоксацина для H.pylori [81]. Если терапия первой или второй линии оказалась неэффективной, следует рассмотреть возможность проведения теста на восприимчивость к соответствующей терапии экстренной помощи [10,81].
Согласно Маастрихтскому / Флорентийскому консенсусу, после неэффективности BQT в качестве терапии первой линии рекомендуется трех- или четырехкратная терапия, содержащая хинолон [10]. После неэффективности четырехкомпонентного режима без висмута первой линии рекомендуется трех- или четырехкратный режим, содержащий BQT или хинолон [10]. BQT, четырехкомпонентная терапия без висмута и трехкомпонентная терапия, содержащая хинолоны, могут использоваться без перекрытия со схемами лечения второй или третьей линии [10].
Торонтский консенсус и рекомендации ACG, такие как Маастрихтский V / Флорентийский консенсус, подчеркивают важность BQT и левофлоксацин-содержащих схем лечения в качестве препаратов второго ряда [4,9]. Важным отличием от Маастрихтского V / Флорентийского консенсуса является возражение против использования четырехкратной схемы второго ряда без висмута, поскольку это менее эффективно, чем другие методы лечения [9]. Кроме того, схемы на основе рифабутина следует использовать только для пациентов, у которых в прошлом было не менее трех неудач лечения [9].В рекомендациях ACG указывается, что режим второго ряда следует выбирать на основе предыдущего воздействия антибиотиков и данных о местной устойчивости к антибиотикам [4].
10. Выводы
обобщает важные схемы лечения H. pylori . Лечение H. pylori — важная глобальная проблема, потому что оно было напрямую связано как причина нескольких желудочно-кишечных заболеваний. Существует явная озабоченность по поводу увеличения показателей устойчивости с течением времени, что подчеркивает необходимость использования подходящих антибиотиков в будущем, чтобы минимизировать дальнейший рост устойчивости к антибиотикам.Специальная терапия на основе AST показала хорошую скорость эрадикации при применении первой линии. Поскольку уровень устойчивости к антибиотикам H. pylori увеличивается, следует расширить роль индивидуализированных методов лечения. Однако, если индивидуальная терапия не может быть применена ко всем пациентам из-за реальных проблем, разумной альтернативой является использование высокоэффективного эмпирического режима на местном уровне. Кроме того, при использовании такой эмпирической схемы необходима простая и эффективная стратегия лечения H. pylori .Поэтому мы предлагаем BQT в качестве терапии первой линии, когда данные по AST или региональной резистентности недоступны (). Если BQT недоступен, мы предлагаем эмпирическую сопутствующую терапию. P-CAB может быть альтернативой, но данные немногочисленны и ограничены Восточной Азией.
Упрощенная стратегия лечения H. pylori .
Таблица 1
Схемы лечения инфекции Helicobacter pylori .
| Лечение | Схема | Продолжительность | Недавняя частота эрадикации первой линии (ITT) | Рекомендации в соответствии с Руководством | Примечания | |
|---|---|---|---|---|---|---|
| Стандартная тройная терапия (STT) | Стандартная тройная терапия (STT) | Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день | 7–14 дней | 63.9% [105], 74,1% [106] | Первая линия: необязательно рекомендована KCHUGR и JSHR Спасательная операция: ограничена рекомендована MAA | За последние 20 лет эффективность STT заметно снизилась, и STT обычно не рекомендуется в качестве схемы первого ряда |
| Квартальная терапия висмутом (BQT) | Стандартная доза ИПП 2 раза в день Стандартная доза висмута 4 раза в день Метронидазол 500 мг 3 раза в день Тетрациклин 500 мг 4 раза в день | 7–14 дней | .8% [107], 88,2% [44], 91,5% [108] Первая линия: рекомендовано ACG, MAA, TOR и KCHUGR (необязательно) Rescue: рекомендовано ACG, MAA, TOR и KCHUGR | BQT был предложен в качестве варианта лечения первой линии во многих руководствах, особенно для регионов с высокой устойчивостью к кларитромицину. | ||
| Сопутствующая терапия (четырехкратная терапия без висмута) | Стандартная доза ИПП 2 раза в день Кларитромицин 500 мг 2 раза в день Амоксициллин 1 г 2 раза в день Метронидазол 500 мг 2 раза в день | 10–14 дней | 84.6% [106], 90,1% [109], 93,5% [110] | Первая линия: рекомендовано ACG, MAA и TOR Спасение: рекомендовано ACG и MAA | Скорость искоренения превосходит это CTT, а метод введения прост по сравнению с последовательной терапией. Но побочные эффекты могут быть более вероятными при сопутствующей терапии. | |
| Последовательная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день (только первая половина) Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 10–14 д | 69.5% [106], 82,0% [111], 87,0% [112] | Первая линия: необязательно рекомендуется (не идеально) ACG Спасение: не рекомендуется во всех руководствах | В качестве терапии первой линии роль постепенно исчезает. Это обременительный способ снизить комплаентность пациента. | |
| Гибридная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 14 дней | 85.8% [75], 92,8% [113] | Первая линия: необязательно рекомендуется (не идеально) ACG Rescue: не рекомендуется во всех руководствах | Это метод, сочетающий последовательную терапию и сопутствующую терапию. | |
| Терапия на основе левофлоксацина | Левофлоксацин можно назначать в виде тройной или четырехкратной терапии. | 10–14 дней | 85,5% [76], 94,0% [77] | Первая линия: рекомендована ACG Rescue: рекомендована ACG, MAA и TOR | В большинстве руководств рекомендуется проводить терапию на основе левофлоксацина. применяется как терапия спасения, а не как первая линия.Он менее эффективен для областей с высокой устойчивостью к хинолонам. | |
| Терапия на основе рифабутина | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Рифабутин 150 мг 2 раза в день | 10 дней | 83,8% [93] | Первая линия: не рекомендуется во всех рекомендациях Спасение: необязательно (третья или четвертая линия) по MAA и TOR | Все руководства рекомендуют терапию на основе рифабутина в качестве терапии спасения. Рифабутин имеет редкий риск миелотоксичности; поэтому требуется осторожное использование. | |
| Терапия на основе калий-конкурентных кислотных блокаторов | P-CAB можно назначать как тройную терапию или четырехкратную терапию, заменяя PPI на P-CAB. | 7–14 d | 89,2% [104], 90,2% [114] | Не указано в алгоритме руководящих принципов | Ожидается, что роль мощного подавления кислоты будет постепенно возрастать, и необходимы дополнительные исследования. | |
| Лечение H. pylori на основе теста на антибактериальную чувствительность | Индивидуальная терапия в соответствии с результатами AST | 7–14 дней | 92.7% [31], 92,9% [115] | MAA рекомендует проводить АСТ после неэффективности терапии второй линии. | Результаты индивидуализированной терапии на основе AST превосходны, и ожидается, что она сыграет роль в улучшении лечения H. pylori в будущем. Требуются усилия для облегчения применения AST в клинической практике. |
Индивидуальная терапия, согласно результатам AST, способствует лечению H. pylori без повышения устойчивости к антибиотикам, поэтому следует уделять особое внимание тестированию на чувствительность.Есть также дополнительные соображения; например, как установить продолжительность лечения при чувствительности к кларитромицину и как выбрать режим (BQT или амоксициллин-метронидазол-ИПП), если устойчивость к кларитромицину не изучалась. Дальнейшая работа должна быть сосредоточена на максимальном терапевтическом эффекте индивидуализированной терапии, основанной на результатах AST.
Вклад авторов
S.Y.K. написал рукопись, и J.-W.C. способствовал разработке концепции и дизайна исследования. Все авторы прочитали и согласились с опубликованной версией рукописи.
Финансирование
Это исследование было поддержано Программой фундаментальных научных исследований через Национальный исследовательский фонд Кореи (NRF), финансируемым Министерством образования (номер гранта: 2020R1I1A306686511) и Исследовательским фондом Кореи (NRF), финансируемым Министерством образования. Образование (номер гранта: 2020R1F1A1076839).
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
1. Кандульски А., Селград М., Малфертхайнер П. Инфекция Helicobacter pylori : клинический обзор. Копать землю. Печень. Дис. 2008. 40: 619–626. DOI: 10.1016 / j.dld.2008.02.026. [PubMed] [CrossRef] [Google Scholar] 2. Макколл К. Клиническая практика. Инфекция Helicobacter pylori . N. Engl. J. Med. 2010; 362: 1597–1604. DOI: 10.1056 / NEJMcp1001110. [PubMed] [CrossRef] [Google Scholar] 3. Пламмер М., Франчески С., Винья Дж., Форман Д., де Мартель С. Глобальное бремя рака желудка, связанное с Helicobacter pylori . Int.J. Рак. 2015; 136: 487–490. DOI: 10.1002 / ijc.28999. [PubMed] [CrossRef] [Google Scholar] 4. Чей В.Д., Леонтиадис Г.И., Хауден К.В., Мосс С.Ф. Клинические рекомендации ACG: Лечение инфекции Helicobacter pylori . Являюсь. J. Gastroenterol. 2017; 112: 212–239. DOI: 10.1038 / ajg.2016.563. [PubMed] [CrossRef] [Google Scholar] 5. Тестерман Т.Л., Моррис Дж. За пределами желудка: обновленный взгляд на патогенез, диагностику и лечение Helicobacter pylori . Мир J. Gastroenterol. 2014; 20: 12781–12808.DOI: 10.3748 / wjg.v20.i36.12781. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ли Ю.К., Чан Т.Х., Чжоу С.К., Ту Ю.К., Ляо В.С., Ву М.С., Грэм Д.Ю. Связь между Helicobacter pylori Эрадикация и заболеваемость раком желудка: систематический обзор и метаанализ. Гастроэнтерология. 2016; 150: 1113–1124. DOI: 10.1053 / j.gastro.2016.01.028. [PubMed] [CrossRef] [Google Scholar] 7. Судзуки Х., Нисидзава Т., Хиби Т. Эрадикационная терапия Helicobacter pylori . Будущее.Microbiol. 2010. 5: 639–648. DOI: 10.2217 / fmb.10.25. [PubMed] [CrossRef] [Google Scholar] 8. Ким С.Г., Юнг Х.К., Ли Х.Л., Чан Дж.Й., Ли Х., Ким С.Г., Шин В.Г., Шин Э.С., Ли Ю.С. Корейский колледж хеликобактер и исследований верхних отделов желудочно-кишечного тракта. Корейский J. Gastroenterol. 2013; 62: 3–26. DOI: 10.4166 / kjg.2013.62.1.3. [PubMed] [CrossRef] [Google Scholar] 9. Фаллон К.А., Чиба Н., ван Зантен С.В., Фишбах Л., Гисберт Дж. П., Хант Р. Х., Джонс Н. Л., Рендер К., Леонтиадис Г. И., Моайеди П. и др. Торонтский консенсус по лечению инфекции Helicobacter pylori у взрослых.Гастроэнтерология. 2016; 151: 51–69. DOI: 10.1053 / j.gastro.2016.04.006. [PubMed] [CrossRef] [Google Scholar] 10. Малфертхайнер П., Мегро Ф., О’Морайн С.А., Гисберт Дж. П., Койперс Э. Дж., Аксон А. Т., Баццоли Ф., Гасбаррини А., Атертон Дж., Грэм Д. Ю. и др. Управление инфекцией Helicobacter pylori — Маастрихт V / Флорентийский консенсусный доклад. Кишечник. 2017; 66: 6–30. DOI: 10.1136 / gutjnl-2016-312288. [PubMed] [CrossRef] [Google Scholar] 11. Гисберт Дж. П., Гонсалес Л., Кальвет X., Гарсия Н., Лопес Т., Roque M., Gabriel R., Pajares J.M. Ингибитор протонной помпы, кларитромицин и амоксициллин или нитроимидазол: метаанализ эрадикации Helicobacter pylori . Алимент. Pharmacol. Ther. 2000; 14: 1319–1328. DOI: 10.1046 / j.1365-2036.2000.00844.x. [PubMed] [CrossRef] [Google Scholar] 12. Современные европейские концепции лечения инфекции Helicobacter pylori Маастрихтский консенсусный доклад. Европейская группа по изучению Helicobacter pylori. Кишечник. 1997; 41: 8–13. DOI: 10.1136 / gut.41.1.8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 13. Грэм Д.Ю., Фишбах Л. Лечение Helicobacter pylori в эпоху повышения устойчивости к антибиотикам. Кишечник. 2010; 59: 1143–1153. DOI: 10.1136 / gut.2009.1. [PubMed] [CrossRef] [Google Scholar] 14. Савольди А., Каррара Э., Грэм Д. Ю., Конти М., Такконелли Э. Распространенность устойчивости к антибиотикам у Helicobacter pylori : систематический обзор и метаанализ в регионах Всемирной организации здравоохранения. Гастроэнтерология.2018; 155: 1372–1382. DOI: 10.1053 / j.gastro.2018.07.007. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 15. Ким С.Ю., Чхве Д.Дж., Чунг Дж.В. Лечение антибиотиками от Helicobacter pylori : приближается конец? Мир J. Gastrointest. Pharmacol. Ther. 2015; 6: 183–198. DOI: 10.4292 / wjgpt.v6.i4.183. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 16. Тунг И., Арамин Х., Вавинская В., Гупта С., Парк Дж. Ю., Кроу С.Э., Валасек М.А. Обзорная статья: Глобальное появление устойчивости к антибиотикам Helicobacter pylori .Алимент. Pharmacol. Ther. 2016; 43: 514–533. DOI: 10.1111 / apt.13497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Woo H.Y., Park D.I., Park H., Kim M.K., Kim D.H., Kim I.S., Kim Y.J. Мультиплексная ПЦР на основе олигонуклеотидов с двойным примированием для обнаружения Helicobacter pylori и определения устойчивости к кларитромицину с помощью биоптатов желудка. Helicobacter. 2009. 14: 22–28. DOI: 10.1111 / j.1523-5378.2009.00654.x. [PubMed] [CrossRef] [Google Scholar] 18. Лиу Дж. М., Чанг К.Y., Chen M.J., Chen C.C., Fang Y.J., Lee J.Y., Wu J., Luo J., Liou T., Chang W. и др. Первичная устойчивость Helicobacter pylori на Тайване после проведения национальной политики ограничения потребления антибиотиков и ее связи с факторами вирулентности — общенациональное исследование. PLoS ONE. 2015; 10: e0124199. DOI: 10.1371 / journal.pone.0124199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 19. Ли Дж.Й., Пак К.С. Оптимальное лечение первой линии для инфекции Helicobacter pylori : последние стратегии.Гастроэнтерол. Res. Практик. 2016; 2016: 81. DOI: 10.1155 / 2016/81. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 20. Альба К., Бланко А., Аларкон Т. Устойчивость к антибиотикам у Helicobacter pylori . Curr. Opin. Заразить. Дис. 2017; 30: 489–497. DOI: 10.1097 / QCO.0000000000000396. [PubMed] [CrossRef] [Google Scholar] 21. Hwang T.J., Kim N., Kim H.B., Lee B.H., Nam R.H., Park J.H., Lee M.K., Park Y.S., Lee D.H., Jung H.C. и др. Изменение устойчивости к антибиотикам штаммов Helicobacter pylori и влияние точечной мутации A2143G 23S рРНК на эрадикацию H.pylori в едином центре Кореи. J. Clin. Гастроэнтерол. 2010; 44: 536–543. DOI: 10.1097 / MCG.0b013e3181d04592. [PubMed] [CrossRef] [Google Scholar] 22. Герритс М.М., ван Влит А.Х., Кейперс Э.Дж., Кустерс Дж.Г. Helicobacter pylori и устойчивость к противомикробным препаратам: молекулярные механизмы и клинические последствия. Lancet Infect. Дис. 2006; 6: 699–709. DOI: 10.1016 / S1473-3099 (06) 70627-2. [PubMed] [CrossRef] [Google Scholar] 24. Халтен К., Гибриль А., Скольд О., Энгстранд Л. Устойчивость к макролидам у Helicobacter pylori : механизм и стабильность в штаммах от пациентов, получавших кларитромицин.Противомикробный. Агенты. Chemother. 1997; 41: 2550–2553. DOI: 10.1128 / AAC.41.11.2550. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25. Стоун Г.Г., Шортридж Д., Версалович Дж., Бейер Дж., Фламм Р.К., Грэм Д.Ю., Гонейм А.Т., Танака С.К. ПЦР-анализ лигирования олигонуклеотидов для определения распространенности мутаций гена 23S рРНК у устойчивых к кларитромицину Helicobacter pylori . Противомикробный. Агенты Chemother. 1997. 41: 712–714. DOI: 10.1128 / AAC.41.3.712. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26.Аларкон Т., Доминго Д., Прието Н., Лопес-Бреа М. Стабильность устойчивости к кларитромицину у Helicobacter pylori : влияние MIC и типа мутации в 23S рРНК. J. Antimicrob. Chemother. 2000. 46: 613–616. DOI: 10.1093 / jac / 46.4.613. [PubMed] [CrossRef] [Google Scholar] 27. Van Doorn LJ, Glupczynski Y., Kusters JG, Megraud F., Midolo P., Maggi-Solca N., Queiroz DM, Nouhan N., Stet E., Quint WG Точное прогнозирование устойчивости к макролидам у Helicobacter pylori с помощью Анализ зонда ПЦР для обнаружения мутаций в гене 23S рРНК: многоцентровое валидационное исследование.Противомикробный. Агенты Chemother. 2001; 45: 1500–1504. DOI: 10.1128 / AAC.45.5.1500-1504.2001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 28. Като С., Фудзимура С., Удагава Х., Симидзу Т., Майсава С., Одзава К., Иинума К. Устойчивость к антибиотикам штаммов Helicobacter pylori у японских детей. J. Clin. Microbiol. 2002; 40: 649–653. DOI: 10.1128 / JCM.40.2.649-653.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Ван В.Х., Вонг Б.С., Мукхопадхьяй А.К., Берг Д.Э., Чо К.Х., Лай К.С., Ху В.Х., Фунг Ф.М., Хуэй В.М., Лам С.К. Высокая распространенность инфекции Helicobacter pylori с двойной устойчивостью к метронидазолу и кларитромицину в Гонконге. Алимент. Pharmacol. Ther. 2000; 14: 901–910. DOI: 10.1046 / j.1365-2036.2000.00795.x. [PubMed] [CrossRef] [Google Scholar] 30. Ли Х. Дж., Ким Дж. И., Чунг Д. Ю., Ким Т. Х., Джун Э. Дж., О Дж. Х., Чунг В. К., Ким Б., Ким С. С., Пак С. и др. Искоренение Helicobacter pylori в соответствии с точечными мутациями 23S рибосомной РНК, связанными с устойчивостью к кларитромицину.J. Infect. Дис. 2013; 208: 1123–1130. DOI: 10.1093 / infdis / jit287. [PubMed] [CrossRef] [Google Scholar] 31. Чо Дж. Х., Чон С. Р., Ким Х. Г., Джин С. Ю., Пак С. Экономическая эффективность адаптированной стратегии ликвидации Helicobacter pylori , основанной на наличии точечной мутации 23S рибосомной РНК, которая вызывает устойчивость к кларитромицину у корейских пациентов. J. Gastroenterol. Гепатол. 2019; 34: 700–706. DOI: 10.1111 / jgh.14383. [PubMed] [CrossRef] [Google Scholar] 32. Папастержиу В., Мату Н., Ликуси С., Евгениди А., Параскева К.Д., Яннакопулос А., Ставру П., Платсука Э., Караджаннис Ю.А. Семидневная тройная эрадикационная терапия Helicobacter pylori на основе генотипической устойчивости может быть высокоэффективной. Анна. Гастроэнтерол. 2018; 31: 198–204. DOI: 10.20524 / aog.2017.0219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 33. Cosme A., Montes M., Ibarra B., Tamayo E., Alonso H., Mendarte U., Lizasoan J., Herreros-Villanueva M., Bujanda L. Тестирование на чувствительность к противомикробным препаратам перед лечением первой линии для Helicobacter pylori инфекция у пациентов с двойной или тройной устойчивостью к антибиотикам.Мир J. Gastroenterol. 2017; 23: 3367–3373. DOI: 10.3748 / wjg.v23.i18.3367. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Ли Дж. У., Ким Н., Нам Р. Х., Ли С. М., Квон Ю. Х., Сон С. Д., Ким Дж. М., Ли Д. Х., Юнг Х. С. Благоприятные исходы эрадикационной терапии Helicobacter pylori на основе посева в регионе с высокой устойчивостью к противомикробным препаратам. Helicobacter. 2019; 24: e12561. DOI: 10.1111 / hel.12561. [PubMed] [CrossRef] [Google Scholar] 35. Чен К., Лонг X., Цзи Ю., Лян X., Ли Д., Гао Х., Сюй Б., Лю М., Чен Ю., Сунь Ю. Рандомизированное контролируемое исследование: терапия на основе чувствительности в сравнении с эмпирической четырехкратной терапией висмутом для лечения первой линии Helicobacter pylori . Алимент. Pharmacol. Ther. 2019; 49: 1385–1394. DOI: 10.1111 / apt.15273. [PubMed] [CrossRef] [Google Scholar] 36. Блюмель Б., Гёльц Х., Кист М., Глокер Э.О. Ретроспективное исследование результатов эрадикационной терапии «спасение» Helicobacter pylori на основе молекулярно-генетического тестирования чувствительности. Helicobacter.2018; 23: e12494. DOI: 10.1111 / hel.12494. [PubMed] [CrossRef] [Google Scholar] 37. Бхакта Д., Грэм Д. Ю., Чан Дж., Эль-Сераг Х. Б. Уроки использования культурального лечения после направления к специалисту по поводу множественной неудачи лечения инфекции, вызванной Helicobacter pylori . Clin. Гастроэнтерол. Гепатол. 2018; 16: 1531–1532. DOI: 10.1016 / j.cgh.2017.12.040. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Байлина М., Муньос Н., Санчес-Дельгадо Дж., Лопес-Гонгора С., Кальвет X., Пуч И. Систематический обзор: Достигнет ли лечение на основе чувствительности приемлемых показателей излечения для терапии второй линии Helicobacter pylori , как в настоящее время практиковал? Helicobacter.2019; 24: e12584. DOI: 10.1111 / hel.12584. [PubMed] [CrossRef] [Google Scholar] 39. Лиу Дж. М., Чен П. Ю., Ло Дж. К., Ли Дж. Ю., Чен К. С., Фанг Ю. Дж., Ян Т. Х., Чанг С. Ю., Баир М. Дж., Ченет М. Дж. И др. Эффективность управляемой генотипической резистентности по сравнению с эмпирической терапией рефрактерной инфекции Helicobacter pylori . Гастроэнтерология. 2018; 155: 1109–1119. DOI: 10.1053 / j.gastro.2018.06.047. [PubMed] [CrossRef] [Google Scholar] 40. Ли Б.З., Треэплтон Д.Э., Ван Дж.Й., Сюй Дж.М., Юань Дж.К., Чжан К., Ли П., Е К. Л., Го Б., Мао С. и др. Сравнительная эффективность и переносимость лечения Helicobacter pylori : систематический обзор и сетевой метаанализ. BMJ. 2015; 351: ч5052. DOI: 10.1136 / bmj.h5052. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 41. Лю К.С., Хунг И.Ф., Сето В.К., Тонг Т., Сюй А.С., Лам Ф.Й., Но Д.Й.К., Вонг С.Й., Люн В.К. Десятидневная последовательная и 10-дневная модифицированная четырехкратная терапия висмутом в качестве эмпирической терапии первой и второй линии для Helicobacter pylori у китайских пациентов: открытое рандомизированное перекрестное исследование.Кишечник. 2014; 63: 1410–1415. DOI: 10.1136 / gutjnl-2013-306120. [PubMed] [CrossRef] [Google Scholar] 42. Hsu P.I., Tsay F.W., Graham D.Y., Tsai T.J., Tsai K.W., Kao J.Y., Peng N.J., Kuo C.H., Kao S.S., Wang H.M. и др. Эквивалентная эффективность обратной гибридной и четверной терапии висмутом в искоренении инфекции Helicobacter pylori в рандомизированном контролируемом исследовании. Clin. Гастроэнтерол. Гепатол. 2018; 16: 1427–1433. DOI: 10.1016 / j.cgh.2018.03.031. [PubMed] [CrossRef] [Google Scholar] 43.Масиас-Гарсия Ф., Бастон-Рей И., де ла Иглесиа-Гарсия Д., Кальвино-Суарес К., Ньето-Гарсия Л., Домингес-Муньос Дж. Э. Висмутсодержащая четырехкратная терапия по сравнению с сопутствующей четырехкратной терапией в качестве лечения первой линии для инфекции Helicobacter pylori в области высокой устойчивости к кларитромицину: проспективное, перекрестное, сравнительное, открытое исследование. Helicobacter. 2019; 24: e12546. DOI: 10.1111 / hel.12546. [PubMed] [CrossRef] [Google Scholar] 44. Ким С.Дж., Чунг Дж.В., Ву Х.С., Ким С.Й., Ким Дж.Х., Ким Й.Дж., Ким К.О., Квон К.А., Пак Д.К. Двухнедельная четырехкратная терапия висмутом и сопутствующая терапия являются эффективными препаратами первой линии для эрадикации Helicobacter pylori : проспективное открытое рандомизированное исследование. Мир. J. Gastroenterol. 2019; 25: 6790–6798. DOI: 10.3748 / wjg.v25.i46.6790. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 45. Ким Дж.Й., Ли С.Й., Ким Дж.Х., Сунг И.К., Пак Х.С. Эффективность и безопасность четырехкратной висмутсодержащей терапии два раза в день с использованием высоких доз тетрациклина и метронидазола для эрадикации второй линии Helicobacter pylori .Helicobacter. 2020; 25: e12683. DOI: 10.1111 / hel.12683. [PubMed] [CrossRef] [Google Scholar] 46. Xie Y., Pan X., Li Y., Wang H., Du Y., Xu J., Wang J., Zeng Z., Chen Y., Zhang G. и др. Новая однократная капсула висмута, метронидазола и тетрациклина, вводимая с омепразолом, по сравнению с четырехкратной терапией, состоящей из висмута, омепразола, амоксициллина и кларитромицина для эрадикации Helicobacter pylori у пациентов с язвой двенадцатиперстной кишки: проспективное, многоцелевое исследование в Китае. J. Antimicrob.Chemother. 2018; 73: 1681–1687. [PubMed] [Google Scholar] 47. Фиорини Г., Зулло А., Сарачино И.М., Гатта Л., Павони М., Вайра Д. Пилера и последовательная терапия для эрадикации первой линии Helicobacter pylori : исследование на основе культуры в реальной клинической практике. Евро. J. Gastroenterol. Гепатол. 2018; 30: 621–625. DOI: 10.1097 / MEG.0000000000001102. [PubMed] [CrossRef] [Google Scholar] 48. Ниссен О.П., МакНичолл А.Г., Гисберт Дж.П. Метаанализ четырехкратной терапии, содержащей висмут, три-в-одной одной капсуле для уничтожения Helicobacter pylori .Helicobacter. 2019; 24: e12570. DOI: 10.1111 / hel.12570. [PubMed] [CrossRef] [Google Scholar] 49. Ким С.Э., Ро Дж. Х., Парк М. И., Пак С. Дж., Мун В., Ким Дж. Х., Юнг К., Хео Дж. Дж. Эффект 7-дневной четырехкратной терапии висмутом по сравнению с 14-дневной тройной терапией моксифлоксацином для второй линии Helicobacter pylori эрадикационной терапии. Корейский язык. J. Gastroenterol. 2019; 73: 26–34. DOI: 10.4166 / kjg.2019.73.1.26. [PubMed] [CrossRef] [Google Scholar] 50. Боянова Л., Митов И. Географическая карта и эволюция первичной устойчивости Helicobacter pylori к антибактериальным препаратам.Эксперт. Преподобный Anti. Заразить. Ther. 2010; 8: 59–70. DOI: 10.1586 / eri.09.113. [PubMed] [CrossRef] [Google Scholar] 51. Megraud F., Coenen S., Versporten A., Kist M., Lopez-Brea M., Hirschl AM, Andersen LP, Goossens H., Glupczynski Y., участники исследовательской группы Устойчивость Helicobacter pylori к антибиотикам в Европе и ее отношение к употреблению антибиотиков. Кишечник. 2013; 62: 34–42. DOI: 10.1136 / gutjnl-2012-302254. [PubMed] [CrossRef] [Google Scholar] 52. Фишбах Л., Эванс Э. Мета-анализ: влияние статуса устойчивости к антибиотикам на эффективность тройной и четверной терапии первой линии для Helicobacter pylori .Алимент. Pharmacol. Ther. 2007. 26: 343–357. DOI: 10.1111 / j.1365-2036.2007.03386.x. [PubMed] [CrossRef] [Google Scholar] 53. Venerito M., Krieger T., Ecker T., Leandro G., Malfertheiner P. Метаанализ четырехкратной терапии висмутом по сравнению с тройной терапией кларитромицином для эмпирического первичного лечения инфекции Helicobacter pylori . Пищеварение. 2013; 88: 33–45. DOI: 10,1159 / 000350719. [PubMed] [CrossRef] [Google Scholar] 54. Манцарис Г.Дж., Петраки К., Арчавлис Э., Амбериадис П., Христофоридис П., Kourtessas D., Chiotakakou E., Triantafyllou G. Тройная терапия омепразолом по сравнению с четырехкратной терапией омепразолом для заживления язвы двенадцатиперстной кишки и эрадикации инфекции Helicobacter pylori : последующее исследование через 24 месяца. Евро. J. Gastroenterol. Гепатол. 2002; 14: 1237–1243. DOI: 10.1097 / 00042737-200211000-00012. [PubMed] [CrossRef] [Google Scholar] 55. Gisbert J.P., Calvet X. Обзорная статья: Четырехкратная (сопутствующая) терапия без висмута для искоренения Helicobater pylori. Алимент. Pharmacol.Ther. 2011; 34: 604–617. DOI: 10.1111 / j.1365-2036.2011.04770.x. [PubMed] [CrossRef] [Google Scholar] 56. Essa A.S., Kramer J.R., Graham D.Y., Treiber G. Мета-анализ: «Сопутствующая терапия» с четырьмя лекарствами, тремя антибиотиками, без висмута по сравнению с тройной терапией для эрадикации Helicobacter pylori . Helicobacter. 2009. 14: 109–118. DOI: 10.1111 / j.1523-5378.2009.00671.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 57. Gisbert J.P., Calvet X. Последние данные о четырехкратной (сопутствующей) терапии без висмута для эрадикации Helicobacter pylori .Clin. Exp. Гастроэнтерол. 2012; 5: 23–34. [Бесплатная статья PMC] [PubMed] [Google Scholar] 58. Chen MJ, Chen CC, Chen YN, Chen CC, Fang YJ, Lin JT, Wu MS, Liou JM, Taiwan Gastrointestinal Disease Helicobacter Consortium Систематический обзор с метаанализом: сопутствующая терапия против тройной терапии для лечения первой линии Helicobacter pylori Инфекция. Являюсь. J. Gastroenterol. 2018; 113: 1444–1457. DOI: 10.1038 / s41395-018-0217-2. [PubMed] [CrossRef] [Google Scholar] 59. Молина-Инфанте Дж., Пазос-Пачеко К., Винагре-Родригес Г., Перес-Галлардо Б., Дуэнас-Садорнил К., Эрнандес-Алонсо М., Гонсалес-Гарсия Г., Матеос-Родригес Дж. М., Фернандес-Бермехо М., Гисберт Дж. П. Невисмут четырехкратная (сопутствующая) терапия: эмпирическая и индивидуализированная эффективность по сравнению со стандартной тройной терапией для чувствительных к кларитромицину Helicobacter pylori и по сравнению с последовательной терапией для устойчивых к кларитромицину штаммов. Helicobacter. 2012; 17: 269–276. DOI: 10.1111 / j.1523-5378.2012.00947.x. [PubMed] [CrossRef] [Google Scholar] 60.Jung Y.S., Park C.H., Park J.H., Nam E., Lee H.L. Эффективность эрадикационной терапии Helicobacter pylori в Корее: систематический обзор и сетевой метаанализ. Helicobacter. 2017; 22 DOI: 10.1111 / hel.12389. [PubMed] [CrossRef] [Google Scholar] 61. Чунг Дж. У., Хан Дж. П., Ким К. О., Ким С. Ю., Хонг С. Дж., Ким Т. Х., Ким С. В., Ким Дж. С., Ким Б. В., Банг Б. Десятидневная эмпирическая последовательная или сопутствующая терапия более эффективна, чем тройная терапия для эрадикации Helicobacter pylori : многоцентровое проспективное исследование.Копать землю. Печень. Дис. 2016; 48: 888–892. DOI: 10.1016 / j.dld.2016.05.005. [PubMed] [CrossRef] [Google Scholar] 62. Park S.M., Kim J.S., Kim B.W., Ji J.S., Choi H. Рандомизированное клиническое испытание, сравнивающее 10- или 14-дневную последовательную терапию и 10- или 14-дневную сопутствующую терапию для эмпирического лечения первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2017; 32: 589–594. DOI: 10.1111 / jgh.13510. [PubMed] [CrossRef] [Google Scholar] 63. Ким С. Ю., Ли С. В., Чхве Дж. В., Чон С. В., Хён Дж.J., Jung Y.K., Koo J.S., Yim H.J. Helicobacter pylori Показатели эрадикации сопутствующей и последовательной терапии в Корее. Helicobacter. 2017; 22: e12441. DOI: 10.1111 / hel.12441. [PubMed] [CrossRef] [Google Scholar] 64. Анг Т.Л., Фок К.М., Сонг М., Анг Д., Квек А.Б., Онг Дж., Тан Дж., Тео Е.К., Дхамодаран С. Десятидневная тройная терапия по сравнению с последовательной терапией по сравнению с сопутствующей терапией в качестве лечения первой линии для Helicobacter pylori инфекция. J. Gastroenterol. Гепатол. 2015; 30: 1134–1139.DOI: 10.1111 / jgh.12892. [PubMed] [CrossRef] [Google Scholar] 65. Макниколл А.Г., Марин А.С., Молина-Инфанте Дж., Кастро М., Баррио Дж., Дуконс Дж., Кальвет X., Коба К., Монторо М., Бори Ф. и др. Рандомизированное клиническое испытание, сравнивающее последовательную и сопутствующую терапию для эрадикации Helicobacter pylori в рутинной клинической практике. Кишечник. 2014; 63: 244–249. DOI: 10.1136 / gutjnl-2013-304820. [PubMed] [CrossRef] [Google Scholar] 66. Гатта Л., Вакил Н., Вайра Д., Скарпигнато С. Глобальные показатели эрадикации инфекции Helicobacter pylori : систематический обзор и метаанализ последовательной терапии.BMJ. 2013; 347: f4587. DOI: 10.1136 / bmj.f4587. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 67. Хе Л., Дэн Т., Луо Х. Мета-анализ последовательной, сопутствующей и гибридной терапии для эрадикации Helicobacter pylori . Междунар. Med. 2015; 54: 703–710. DOI: 10.2169 / internalmedicine.54.3442. [PubMed] [CrossRef] [Google Scholar] 68. Zullo A., Scaccianoce G., De Francesco V., Ruggiero V., D’Ambrosio P., Castorani L., Bonfrate L., Vannella L., Hassan C., Portincasa P. Сопутствующая, последовательная и гибридная терапия для ЧАС.pylori: пилотное исследование. Clin. Res. Гепатол. Гастроэнтерол. 2013; 37: 647–650. DOI: 10.1016 / j.clinre.2013.04.003. [PubMed] [CrossRef] [Google Scholar] 69. Ким С.Й., Ли С.В., Хён Дж.Дж., Юнг С.В., Ку Дж.С., Йим Х.Дж., Пак Дж.Дж., Чун Х.Дж., Чой Дж.Х. Сравнительное исследование степени эрадикации Helicobacter pylori с 5-дневной четырехкратной «сопутствующей» терапией и 7-дневной стандартной тройной терапией. J. Clin. Гастроэнтерол. 2013; 47: 21–24. DOI: 10.1097 / MCG.0b013e3182548ad4. [PubMed] [CrossRef] [Google Scholar] 70.Лим Дж. Х., Ли Д. Х., Чой К., Ли С. Т., Ким Н., Чон С. Х., Ким Дж. У., Хван Дж. Х., Пак Ю. С., Ли С. Х. и др. Клинические результаты двухнедельной последовательной и сопутствующей терапии для эрадикации Helicobacter pylori : рандомизированное пилотное исследование. Helicobacter. 2013. 18: 180–186. DOI: 10.1111 / hel.12034. [PubMed] [CrossRef] [Google Scholar] 71. Гевара Б., Когдилл А.Г. Helicobacter pylori : Обзор текущих стратегий диагностики и управления. Копать землю. Дис. Sci. 2020; 65: 1917–1931.DOI: 10.1007 / s10620-020-06193-7. [PubMed] [CrossRef] [Google Scholar] 72. Грэм Д.Ю., Ли Ю.С., Ву М.С. Рациональная терапия Helicobacter pylori : доказательная медицина, а не доказательная медицина. Clin. Гастроэнтерол. Гепатол. 2014; 12: 177–186. DOI: 10.1016 / j.cgh.2013.05.028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 73. Wang B., Wang Y.H., Lv Z.F., Xiong H.F., Wang H., Yang Y., Xie Y. Обзор: Эффективность и безопасность гибридной терапии для инфекции Helicobacter pylori : систематический обзор и метаанализ.Helicobacter. 2015; 20: 79–88. DOI: 10.1111 / hel.12180. [PubMed] [CrossRef] [Google Scholar] 74. Молина-Инфанте Дж., Романо М., Фернандес-Бермехо М., Федерико А., Гравина А.Г., Поццати Л., Гарсия-Абадиа Э., Винагре-Родригес Г., Мартинес-Алькала К., Эрнандес-Алонсо М. , и другие. Оптимизированная четырехкомпонентная терапия без висмута излечивает большинство пациентов с инфекцией Helicobacter pylori в популяциях с высокими показателями устойчивости к антибиотикам. Гастроэнтерология. 2013; 145: 121–128. DOI: 10.1053 / j.gastro.2013.03.050. [PubMed] [CrossRef] [Google Scholar] 75. Georgopoulos SD, Papastergiou V., Martinez-Gonzalez B., Xirouchakis E., Familias I., Sgouras D., Mentis A., Karatapanis S. Гибридная терапия как схема первой линии для эрадикации Helicobacter pylori при высокой устойчивости к кларитромицину область: перспективное открытое испытание. Анна. Гастроэнтерол. 2018; 31: 205–210. DOI: 10.20524 / aog.2017.0221. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Сонг З., Фу В., Чжоу Л. Цефуроксим, левофлоксацин, эзомепразол и висмут в качестве терапии первой линии для ликвидации Helicobacter pylori у пациентов с аллергией на пенициллин.BMC Gastroenterol. 2019; 19: 132. DOI: 10.1186 / s12876-019-1056-3. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 77. Auttajaroon J., Vilaichone R.K., Chotivitayatarakorn P., Mahachai V. Рабепразол, левофлоксацин, кларитромицин-MR и висмут один раз в день для эрадикации Helicobacter pylori : рандомизированное исследование продолжительностью 7 или 14 дней (исследование ONCE) Helicobacter. 2019; 24: e12615. DOI: 10.1111 / hel.12615. [PubMed] [CrossRef] [Google Scholar] 78. Ган Х.Ю., Пэн Т.Л., Хуан Ю.М., Су К.Х., Чжао Л.Л., Яо Л.Ю., Ян Р.Дж. Эффективность двух различных доз левофлоксацина в лечении инфекции Helicobacter pylori : проспективное одноцентровое рандомизированное клиническое испытание. Sci. Отчет 2018; 8: 9045. DOI: 10.1038 / s41598-018-27482-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 79. Ciccaglione AF, Di Giulio M., Di Lodovico S., Di Campli E., Cellini L., Marzio L. Бычий лактоферрин повышает эффективность тройной терапии на основе левофлоксацина в качестве лечения первой линии инфекции Helicobacter pylori : An in vitro и in vivo исследования.J. Antimicrob. Chemother. 2019; 74: 1069–1077. DOI: 10,1093 / jac / dky510. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 80. Басу П.П., Раяпуди К., Пакана Т., Шах Н.Дж., Кришнасвами Н., Флинн М. Рандомизированное исследование, сравнивающее левофлоксацин, омепразол, нитазоксанид и доксициклин с тройной терапией для ликвидации Helicobacter pylori . Являюсь. J. Gastroenterol. 2011; 106: 1970–1975. DOI: 10.1038 / ajg.2011.306. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 81. Фэллон К.А., Мосс С.Ф., Малфертхайнер П. Согласование последних рекомендаций по лечению Helicobacter pylori во времена повышения устойчивости к антибиотикам. Гастроэнтерология. 2019; 157: 44–53. DOI: 10.1053 / j.gastro.2019.04.011. [PubMed] [CrossRef] [Google Scholar] 82. Мори Х., Судзуки Х. Обновленная информация о хинолон-содержащих терапии спасения от инфекции Helicobacter pylori . Мир J. Gastroenterol. 2020; 26: 1733–1744. DOI: 10.3748 / wjg.v26.i15.1733. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83.Sue S., Shibata W., Sasaki T., Kaneko H., Irie K., Kondo M., Maeda S. Рандомизированное испытание тройной терапии третьей линии на основе вонопразана и ингибитора протонной помпы с ситафлоксацином для Helicobacter pylori . J. Gastroenterol. Гепатол. 2019; 34: 686–692. DOI: 10.1111 / jgh.14456. [PubMed] [CrossRef] [Google Scholar] 84. Судзуки Х., Нишизава Т., Мураока Х., Хиби Т. Ситафлоксацин и гареноксацин могут преодолеть устойчивость к антибиотикам Helicobacter pylori с мутацией gyrA.Противомикробный. Агенты. Chemother. 2009; 53: 1720–1721. DOI: 10.1128 / AAC.00049-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 85. Miftahussurur M., Waskito LA, Syam AF, Nusi IA, Siregar G., Richardo M., Bakry AF, Rezkitha YAA, Wibawa IDN, Yamaoka Y. Альтернативные схемы эрадикации инфекции Helicobacter pylori в регионах Индонезии с высоким содержанием метронидазола и левофлоксина сопротивление. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 345–358. DOI: 10.2147 / IDR.S187063. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 86.Мифтахуссурур М., Афтаб Х., Шреста П.К., Шарма Р.П., Субсомвонг П., Васкито Л.А., Духан Д., Фаузия К.А., Ямаока Ю. Эффективные терапевтические схемы в двух странах Южной Азии с высокой устойчивостью к основным антибиотикам Helicobacter pylori . Противомикробный. Оказывать сопротивление. Заразить. Контроль. 2019; 8:40. DOI: 10.1186 / s13756-019-0482-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 87. Гисберт Дж. П., Кальвет X. Обзорная статья: Рифабутин в лечении рефрактерной инфекции Helicobacter pylori .Алимент. Pharmacol. Ther. 2012; 35: 209–221. DOI: 10.1111 / j.1365-2036.2011.04937.x. [PubMed] [CrossRef] [Google Scholar] 88. Хип М., Бек Д., Байердорфер Э., Лен Н. Механизм устойчивости к рифампину и рифабутину в Helicobacter pylori . Противомикробный. Агенты. Chemother. 1999; 43: 1497–1499. DOI: 10.1128 / AAC.43.6.1497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 89. Рибалдоне Д.Г., Фагуни С., Астеджано М., Дураццо М., Моргандо А., Спруджевник Т., Джорданино К., Баронио М., Анжелис К.D., Saracco G.M. и др. Спасательная терапия на основе рифабутина для эрадикации Helicobacter pylori : долгосрочное проспективное исследование в большой когорте трудно поддающихся лечению пациентов. J. Clin. Med. 2019; 8: 199. DOI: 10,3390 / jcm8020199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 90. Akada J.K., Shirai M., Fujii K., Okita K., Nakazawa T. Активность новых производных рифамицина, KRM-1648 и KRM-1657, in vitro против Helicobacter pylori in vitro. Противомикробный. Агенты. Chemother. 1999; 43: 1072–1076.DOI: 10.1128 / AAC.43.5.1072. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 91. Кунин С.М. Антимикробная активность рифабутина. Clin. Заразить. Дис. 1996; 22 (Дополнение 1: S3-13): 30. DOI: 10.1093 / Clinids / 22.Supplement_1.S3. [PubMed] [CrossRef] [Google Scholar] 92. Сунг Дж., Ким Н., Пак И. Х., Хван Ю. Дж., Квон С., На Г., Чой Дж. Ю., Кан Дж. Б., Ким Х. Р., Ким Дж. В. и др. Спасательная терапия четвертой и пятой линий на основе рифабутина у пациентов с неэффективностью эрадикации Helicobacter pylori . Корейский язык.J. Gastroenterol. 2017; 69: 109–118. DOI: 10.4166 / kjg.2017.69.2.109. [PubMed] [CrossRef] [Google Scholar] 93. Грэм Д.Ю., Ханаан Ю., Махер Дж., Винер Г., Халтен К.Г., Калфус И.Н. Тройная терапия на основе рифабутина (RHB-105) для ликвидации Helicobacter pylori : двойное слепое рандомизированное контролируемое исследование. Анна. Междунар. Med. 2020; 172: 795–802. DOI: 10.7326 / M19-3734. [PubMed] [CrossRef] [Google Scholar] 94. Бок Х., Куп Х., Лен Н., Хип М. Тройная терапия на основе рифабутина после неудачной эрадикационной терапии Helicobacter pylori : предварительный опыт.J. Clin. Гастроэнтерол. 2000. 31: 222–225. DOI: 10.1097 / 00004836-200010000-00007. [PubMed] [CrossRef] [Google Scholar] 95. Сузуки С., Сузуки Х., Нисидзава Т., Канеко Ф., Отани С., Мураока Х., Сайто Ю., Кобаяши И., Хиби Т. Прошлое дозирование рифампицина определяет устойчивость к рифабутину Helicobacter pylori . Пищеварение. 2009; 79: 1–4. DOI: 10,1159 / 0001. [PubMed] [CrossRef] [Google Scholar] 96. Скотт Дж. Я., Мансон К. Б., Маркус Э. А., Ламбрехт Н. В., Сакс Г. Селективность связывания фонопразана (TAK-438) с H +, K + -АТФазой желудка.Алимент. Pharmacol. Ther. 2015; 42: 1315–1326. DOI: 10.1111 / apt.13414. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 97. Park J.Y., Kim J.G. [New Helicobacter pylori Eradication Therapies] Корейский. J. Gastroenterol. 2018; 72: 237–244. DOI: 10.4166 / kjg.2018.72.5.237. [PubMed] [CrossRef] [Google Scholar] 99. Грэм Д.Ю., Дор М.П. Обновленная информация об использовании вонопразана: конкурентного блокатора кислоты. Гастроэнтерология. 2018; 154: 462–466. DOI: 10.1053 / j.gastro.2018.01.018. [PubMed] [CrossRef] [Google Scholar] 100.Лю Q.J., Пу Q.H., Чжун X.F., Чжан Дж. Эффективность и безопасность тройной терапии на основе вонопразана и ингибитора протонной помпы для искоренения Helicobacter pylori : метаанализ рандомизированных клинических испытаний. Биомед. Res. Int. 2019; 3: 1–8. DOI: 10.1155 / 2019/9781212. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 101. Murakami K., Sakurai Y., Shiino M., Funao N., Nishimura A., Asaka M. Vonoprazan, новый калий-конкурентный блокатор кислоты, в качестве компонента тройной терапии первой и второй линии против Helicobacter pylori Эрадикация : рандомизированное двойное слепое исследование фазы III.Кишечник. 2016; 65: 1439–1446. DOI: 10.1136 / gutjnl-2015-311304. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 102. Ли М., Осима Т., Хорикава Т., Тозава К., Томита Т., Фукуи Х., Ватари Дж., Мива Х. Систематический обзор с метаанализом: вонопразан, мощный блокатор кислоты, превосходит протонный ингибиторы помпы для уничтожения устойчивых к кларитромицину штаммов Helicobacter pylori . Helicobacter. 2018; 23: e12495. DOI: 10.1111 / hel.12495. [PubMed] [CrossRef] [Google Scholar] 103. Танабэ Х., Yoshino K., Ando K., Nomura Y., Ohta K., Satoh K., Ichiishi E., Ishizuka A., Otake T., Kohgo Y., et al. Тройная терапия на основе вонопразана не уступает тройной терапии на основе ингибиторов протонной помпы на основе чувствительности для эрадикации Helicobacter pylori . Анна. Clin. Microbiol Antimicrob. 2018; 17:29. DOI: 10.1186 / s12941-018-0281-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 104. Судзуки С., Готода Т., Кусано К., Икехара Х., Итидзима Р., Охьяучи М., Ито Х., Кавамура М., Огата Ю., Отака М. и др. Семидневная двойная терапия фонопразаном и низкими дозами амоксициллина в качестве терапии первой линии Helicobacter pylori : многоцентровое рандомизированное исследование в Японии. Кишечник. 2020; 69: 1019–1026. DOI: 10.1136 / gutjnl-2019-319954. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 105. Ким Б.Дж., Ли Х., Ли Ю.С., Чон С.В., Ким Г.Х., Ким Х.С., Сунг Дж.К., Ли Д.Х., Ким Х.У., Пак М.И. и др. Десятидневная сопутствующая, 10-дневная последовательная и 7-дневная тройная терапия в качестве лечения первой линии для инфекции Helicobacter pylori : общенациональное рандомизированное исследование в Корее.Кишечник. Печень. 2019; 13: 531–540. DOI: 10.5009 / gnl19136. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 106. Zhou Y., Ye Z., Wang Y., Zhang Y., Tang Z., Yan W., Jiang Y., Huang Y. Сравнение четырех различных схем лечения против Helicobacter pylori в качестве лечения первой линии: перспектива , перекрестное, сравнительное, открытое испытание на китайских детях. Helicobacter. 2020; 25: e12679. DOI: 10.1111 / hel.12679. [PubMed] [CrossRef] [Google Scholar] 107. Банг К.С., Лим Х., Чон Х.М., Шин В.Г., Чой Дж. Х., Со Дж. С., Кан Х. С., Ян Й. Дж., Хонг Дж. Т., Шин С. П. и др. Амоксициллин или тетрациклин в висмутсодержащей четверной терапии в качестве лечения первой линии для инфекции Helicobacter pylori . Кишечные микробы. 2020; 11: 1314–1323. DOI: 10.1080 / 194.2020.1754118. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 108. Романо М., Гравина А.Г., Нардоне Г., Федерико А., Даллио М., Марторано М., Мучерино К., Ромити А., Аваллоне Л., Граната Л. и др. Четырехкратная терапия без висмута и висмута, основанная на предыдущем воздействии кларитромицина, столь же эффективна и безопасна в области высокой устойчивости к кларитромицину: исследование в реальной жизни.Helicobacter. 2020; 25: e12694. DOI: 10.1111 / hel.12694. [PubMed] [CrossRef] [Google Scholar] 109. Tai W.C., Liang C.M., Bi K.W., Kuo C.M., Lu L..S., Wu C.K., Yang S.C., Kuo Y.H., Lee C.H., Huang C.F. и др. Сравнение четырехкомпонентной (сопутствующей) терапии на основе декслансопразола с модифицированным высвобождением и на основе лансопразола для эрадикации первой линии Helicobacter pylori : проспективное рандомизированное исследование. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 2923–2931. DOI: 10.2147 / IDR.S213998. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 110.Hsu P.I., Tsay F.W., Kao J.Y., Peng N.J., Tsai K.W., Tsai T.J., Kuo C.H., Kao S.S., Wang H.M., Chen Y.H. и др. Эквивалентная эффективность обратного гибрида и сопутствующей терапии в лечении первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2020 doi: 10.1111 / jgh.15034. [PubMed] [CrossRef] [Google Scholar] 111. Myint N., Zaw T.T., Sain K., Waiyan S., Danta M., Cooper D., Aung N.M., Kyi M.M., Hanson J. Sequential Helicobacter pylori эрадикационная терапия в Мьянме; рандомизированное клиническое испытание эффективности и переносимости.J. Gastroenterol. Гепатол. 2020; 35: 617–623. DOI: 10.1111 / jgh.14942. [PubMed] [CrossRef] [Google Scholar] 112. Зулло А., Фиорини Г., Скаччаноче Г., Портинкаса П., Де Франческо В., Вассалло Р., Урбан Ф., Моника Ф., Могаверо Г., Амато А. и др. Последовательная терапия для эрадикации первой линии Helicobacter pylori : 10- или 14-дневный режим? J. Gastrointestin. Печень. Дис. 2019; 28: 11–14. DOI: 10.15403 / jgld.2014.1121.281.hpy. [PubMed] [CrossRef] [Google Scholar] 113. Цай Ф.В., Ву Д.С., Ю Х.С., Kao S.S., Lin K.H., Cheng J.S., Wang H.M., Chen W.C., Sun W.C., Tsai K.W. и др. Рандомизированное контролируемое исследование показывает, что как 14-дневная гибридная, так и четырехкомпонентная терапия висмутом излечивают большинство пациентов с инфекцией Helicobacter pylori в группах населения со средней устойчивостью к антибиотикам. Противомикробный. Агенты. Chemother. 2017; 61: e00140-17. DOI: 10.1128 / AAC.00140-17. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 114. Нисида Т., Цудзи Ю., Окамото А., Томита Р., Хигаки Ю., Осуги Н., Сугимото А., Такахаши К., Мукаи К., Накамацу Д. и др. Лекарство с тройным лекарством в блистерной упаковке с вонопразаном улучшает эрадикацию первой линии Helicobacter pylori у пожилых пациентов: когортное исследование с ретроспективной оценкой склонности. Пищеварение. 2019: 1–7. DOI: 10,1159 / 000501608. [PubMed] [CrossRef] [Google Scholar] 115. Луо Л., Хуанг Ю., Лян Х., Цзи Ю., Ю. Л., Лу Х. Терапия на основе чувствительности для Helicobacter pylori -инфицированных пациентов с аллергией на пенициллин: проспективное клиническое испытание терапии первой линии и терапии спасения .Helicobacter. 2020; 25: e12699. DOI: 10.1111 / hel.12699. [PubMed] [CrossRef] [Google Scholar] 116. Kim SG, Jung HK, Lee HL, Jang JY, Lee H., Kim CG, Shin WG, Shin ES, Lee YC, Korean College of Helicobacter and Upper Gastrointestinal Research Guidelines для диагностики и лечения инфекции Helicobacter pylori в Корее , Редакция 2013 г. J. Gastroenterol. Гепатол. 2014; 29: 1371–1386. DOI: 10.1111 / jgh.12607. [PubMed] [CrossRef] [Google Scholar] 117. Като М., Ота Х., Окуда М., Кикучи С., Сато К., Шимояма Т., Судзуки Х., Ханда О., Фурута Т., Мабе К. и др. Руководство по лечению инфекции Helicobacter pylori в Японии: пересмотренное издание 2016 г. Helicobacter. 2019; 24: e12597. DOI: 10.1111 / hel.12597. [PubMed] [CrossRef] [Google Scholar]
Лучшая стратегия ликвидации Helicobacter pylori в эпоху устойчивости к антибиотикам
Антибиотики (Базель). 2020 Aug; 9 (8): 436.
Су Ён Ким
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; мок.revan @ 2121ezeerb
Джун-Вон Чунг
2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдон-даэро 774beon-gil, Намдонг-гу, Инчхон 21565, Корея
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу Университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; moc.revan@2121ezeerb2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдонг-даэро 774beon-gil, Namdong-gu, Инчхон 21565, Корея
Поступило 30 июня 2020 г .; Принята в печать 21 июля 2020 г.
Лицензиат MDPI, Базель, Швейцария. Эта статья — статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution (CC BY) (http://creativecommons.org/licenses/by/4.0/). Эта статья цитировалась другими статьями в PMC. .Abstract
Устойчивость к антибиотикам является основной причиной неэффективности лечения Helicobacter pylori , а учащение случаев устойчивости к антибиотикам является проблемой для клиницистов. Особую проблему представляет устойчивость к кларитромицину и метронидазолу.Стандартная тройная терапия (ингибитор протонной помпы, амоксициллин и кларитромицин) больше не подходит в качестве лечения первой линии в большинстве регионов. Недавние рекомендации по лечению инфекции H. pylori
рекомендуют четырехкратную схему лечения (висмут или невисмут) в качестве терапии первой линии. Эта стратегия лечения эффективна для областей с высокой резистентностью к кларитромицину или метронидазолу, но частота резистентности неизбежно возрастает в результате длительной терапии несколькими антибиотиками.Новая терапия на основе калий-конкурентных блокаторов кислоты может быть эффективной, но данные ограничены. Индивидуальная терапия, основанная на результатах теста на чувствительность к противомикробным препаратам, является идеальным вариантом. В этом обзоре обсуждались текущие важные схемы лечения H. pylori и оптимальная стратегия эрадикации H. pylori .Ключевые слова: Helicobacter pylori , устойчивость к антибиотикам, эрадикация
1. Введение
Helicobacter pylori — грамотрицательная, жгутиковая, спиралевидная бактерия, проникающая в слизистую оболочку верхнего отдела желудочно-кишечного тракта [1] , 2].Он вызывает пептические язвы, рак желудка и другие желудочные заболевания [3,4] и составляет 25% всех злокачественных новообразований, связанных с инфекциями; это также связано с повышенным риском рака желудочно-кишечного тракта [5]. Искоренение H. pylori облегчает язвенную болезнь и снижает риск рака желудка [6,7]. В глобальном масштабе рекомендации по лечению H. pylori постепенно меняются, а показания расширяются [4,8,9,10]. Кроме того, с экономическим развитием многих развивающихся стран и увеличением старения населения количество людей, получающих H.pylori увеличивается.
В 1990-х годах тройная терапия, состоящая из ингибитора протонной помпы (ИПП), кларитромицина и амоксициллина, была введена для искоренения инфекции H. pylori и в настоящее время является стандартом во всем мире [11,12]. С тех пор уровень искоренения тройной терапии во многих регионах заметно снизился [13,14]. Причины этого снижения включают бактериальные факторы, повторное инфицирование, генетический полиморфизм CYP2C19 и соблюдение пациентом режима лечения [15].Устойчивость к антибиотикам является наиболее важной причиной неудач лечения H. pylori [13,16]. Резистентность к кларитромицину H. pylori особенно серьезна; Схемы, содержащие кларитромицин, больше не подходят из-за степени эрадикации <80% [14,17]. Уровень устойчивости к метронидазолу и хинолонам (которые в основном используются в качестве схем второго или третьего ряда) во всем мире составляет> 15% [14,16]. Поскольку количество антибиотиков, подходящих для эрадикации H. pylori , ограничено (кларитромицин, амоксициллин, метронидазол, левофлоксацин, тетрациклин и рифабутин), повышение устойчивости к антибиотикам является серьезной проблемой.Следовательно, исключения кларитромицина недостаточно для предотвращения устойчивости к антибиотикам H. pylori .
Текущие руководства подчеркивают важность местной распространенности устойчивости к антибиотикам при выборе подходящей схемы лечения H. pylori [4,9,10]. В регионах с высокой устойчивостью к определенным антибиотикам успех лечения можно улучшить, отказавшись от использования таких антибиотиков. Однако, хотя новая комбинация антибиотиков может повысить скорость эрадикации, она может вызвать резистентность.Правительство Тайваня ограничило использование противомикробных препаратов, что привело к низкому уровню первичной устойчивости к кларитромицину и метронидазолу у H. pylori [18]. Однако частота первичной устойчивости к левофлоксацину увеличилась с 4,9% в 2000–2007 гг. До 13,4% в 2011–2012 гг. [18]. Кроме того, использование нескольких антибиотиков увеличивает частоту осложнений [4]. Поэтому важно определить оптимальную стратегию эрадикации H. pylori в соответствии с результатами теста на антибактериальную чувствительность (AST).Однако возможность ложноотрицательных результатов и возможность применения во всех медицинских учреждениях являются проблемой [19,20]. Мы рассмотрели наиболее важные схемы лечения против H. pylori , которые преодолевают устойчивость к антибиотикам, и стратегии, которые можно применять на практике.
2.
H. pylori Лечение на основе результатов ASTБактериальный посев обычно проводится перед выбором антибиотика, но посев H. pylori сложен и требует много времени. Исследование чувствительности к кларитромицину H.pylori улучшает скорость эрадикации [21,22]. Герритс и др. с помощью полимеразной цепной реакции (ПЦР) показали, что мутации A2142G и A2143G в 23S рРНК связаны с устойчивостью к антибиотикам [22]. ПЦР сравнительно прост и экономичен [21]. Следовательно, для H. pylori лечение на основе AST, такое как диагностический тест на устойчивость к кларитромицину, является полезным. Однако в некоторых случаях уровень эрадикации составляет <100%. Это связано с тем, что точечные мутации, отличные от A2142G или A2143G, приводят к ненадежным результатам, например.g., A2142C, A2115G, G2142T, A2142T и T2182C [23,24]. Кроме того, распространение мутаций отличается географически. Мутация A2142C встречается <10% в США и Европе, но не зарегистрирована в Японии [25,26,27,28]. В Гонконге частота мутации A2144G выше, чем в других регионах [29]. Различное распределение этих мутаций, вероятно, влияет на скорость эрадикации.
Терапия H. pylori , основанная на результатах AST, значительно улучшает скорость эрадикации.Однако, в отличие от других схем, мало исследований оценивали схемы первого ряда на основе АСТ. Уровень искоренения намерения лечить (ITT) для схемы первого ряда составляет> 90% [30,31,32]. В Южной Корее индивидуализированная терапия первой линии на основе ПЦР превосходит стандартную тройную терапию (STT; амоксициллин, кларитромицин и ИПП) [30,31]. В греческом исследовании тройная терапия на основе генотипической резистентности (определение чувствительности к кларитромицину и левофлоксацину с помощью анализа GenoType HelicoDR) позволила достичь высокого уровня H.pylori (90,2% по ITT и 97,8% по протоколу (PP) анализа) [32]. Кроме того, тройные схемы первой линии под контролем АСТ приводят к эрадикации> 90% у пациентов с H. pylori , устойчивым к двум антибиотикам [33]. Поскольку частота полирезистентности H. pylori увеличивается, это обнадеживающее открытие. Схемы первой линии эрадикации H. pylori на основе культивирования демонстрируют превосходный терапевтический эффект даже в регионах с высоким уровнем устойчивости к противомикробным препаратам [34].Общие показатели устойчивости к амоксициллину, кларитромицину, метронидазолу и моксифлоксацину составляют 6,7%, 31,0%, 41,8% и 39,2% соответственно. Однако уровень эрадикации составляет 93,1% (ITT) и 100,0% (PP) [34]. Chen et al. сообщили, что управляемый по чувствительности модифицированный четырехкратный режим висмута первой линии для H. pylori в регионе с высокой степенью устойчивости к противомикробным препаратам имел высокий уровень эрадикации [35].
Показатель успеха схем второго ряда / спасения под контролем AST ниже, чем у схем первого ряда.Уровень эрадикации низкий (68%), несмотря на тестирование чувствительности для лечения спасения [36]. Аналогичным образом, в Соединенных Штатах терапия с культуральным контролем показала 60% -ный успех у пациентов, у которых не удалось по крайней мере три лечения [37]. Даже если посев определяет чувствительность к кларитромицину, повторный анализ кларитромицина после неудачи лечения не рекомендуется [38]. Следовательно, одна только терапия под контролем АСТ не может достичь требуемой скорости эрадикации. Liou et al. показали, что терапия с учетом генотипа не была значительно более эффективной, чем эмпирическая терапия для стратегии спасательной терапии (78.0% против 72,2%, p = 0,170) [39]. Следовательно, соответствующая эмпирическая терапия является альтернативой индивидуализированной генотипической терапии рефрактерной инфекции H. pylori .
3. Четырехкратная терапия висмутом
Четырехкратная терапия висмутом (BQT) состоит из висмута, PPI, метронидазола и тетрациклина. Он рекомендован как схема первой линии Торонтским консенсусом, Маастрихтским V / Флорентийским консенсусом и рекомендациями Американского колледжа гастроэнтерологии (ACG) [4,9,10].На режим BQT не влияет резистентность к кларитромицину. Согласно сетевому метаанализу, BQT в течение 10 или 14 дней превосходит STT в течение 7 дней [40]. Более того, BQT очень эффективен в качестве эмпирической схемы первого ряда (уровень эрадикации PP и ITT составляет 98,8% и 92,7% соответственно) [41]. Рандомизированное контролируемое исследование (РКИ) на Тайване показало, что уровень эрадикации у пациентов, получавших BQT, составил 96,0%, хотя частота нежелательных явлений составила 47,7% [42]. BQT оказался высокоэффективным в качестве схемы первого ряда для H.pylori в проспективном исследовании в Испании (94,4% (ITT) и 96,2% (PP)) [43]. BQT имеет отличную скорость эрадикации H. pylori , но комплаентность пациента может быть снижена из-за большого количества лекарств. Кроме того, BQT вводят четыре раза в день, что также может снизить комплаентность пациента. Чтобы преодолеть это, были введены схемы приема BQT два раза в день, и исследования в Южной Корее продемонстрировали их эффективность [44,45]. Kim et al. продемонстрировали, что два раза в день BQT в течение 1 недели был так же эффективен и безопасен, как традиционный четырехкратный ежедневный BQT (93.9% против 92,9%) [45]. Кроме того, большинство пациентов демонстрируют хорошую комплаентность, а уровень эрадикации BQT два раза в день высок (88,2% (ITT) и 98,4% (PP)) [44]. Разработана единая капсула, содержащая висмут, метронидазол и тетрациклин. Xie et al. показали, что терапия BQT одной капсулой была эффективной для эрадикации H. pylori и хорошо переносилась (86,5% (ITT) и 94,6% (PP)) [46]. В итальянском исследовании однокапсульная терапия BQT позволила достичь уровня эрадикации 91% (ITT) и 97% (PP) [47].Согласно метаанализу, при терапии BQT с одной капсулой первого и второго ряда уровень эрадикации приближался к 90%. Даже это применимо, независимо от типа и дозы ИПП, у пациентов со штаммом, резистентным к антибиотикам, и у тех, кто ранее лечился кларитромицином [48]. При 7-дневной схеме лечения BQT второго ряда уровень эрадикации составляет 93,6% (PP). Скорость эрадикации 7-дневного BQT значительно выше, чем у 14-дневного моксифлоксацина, содержащего тройной режим (93,6% против 73,8% (PP), p <0.001) [49].
Неясно, улучшится ли скорость эрадикации при увеличении периода лечения с 7 до 14 дней. Маастрихтский V / Флорентийский консенсус рекомендует прием препарата в течение не менее 10 дней [10]. Сообщается, что уровень устойчивости к тетрациклину во всем мире низкий [50,51]. Следовательно, устойчивость к метронидазолу является основным фактором успеха эрадикации H. pylori . Устойчивость к метронидазолу можно преодолеть путем увеличения частоты, количества и продолжительности приема, поэтому лечение в течение ≥10 дней рекомендуется в регионах с высокой степенью устойчивости к метронидазолу [52].
BQT показал отличные результаты в различных исследованиях, и сфера его применения постепенно расширяется. Кроме того, BQT можно относительно безопасно применять у пациентов с аллергией на пенициллин [4]. Сообщается, что BQT имеет более высокий уровень нежелательных явлений, чем STT, но схожий уровень соблюдения пациентом режима лечения [53,54]. Однако, поскольку показания BQT расширяются в качестве лечения первой линии, также возникают опасения. Количество схем второго ряда, которые можно применять, значительно сокращается, когда эрадикация с помощью BQT не дает результатов по первой линии.Кроме того, в будущем может повыситься уровень устойчивости к тетрациклину, который в настоящее время является относительно низким. Для решения этой проблемы в будущем необходимы различные исследования.
4. Сопутствующая терапия
Рекомендуется одновременное введение трех антибиотиков (кларитромицин, метронидазол или нитроимидазол и амоксициллин) и ИПП в течение 10–14 дней [4,9,10]. Несколько метаанализов показали, что сопутствующая терапия превосходит STT [55,56,57].Кроме того, недавний метаанализ показал, что сопутствующая терапия в течение 5 или 10 дней превосходила STT в течение 5, 7 или 10 дней [58]. Испанское исследование продемонстрировало, что сопутствующая терапия была значительно лучше, чем тройная терапия (92% против 70% (ITT), p = 0,02 и 92% против 74% (PP), p = 0,05) и эрадикация Скорость сопутствующей терапии была выше, чем у последовательной терапии устойчивых к антибиотикам штаммов [59]. Кроме того, сопутствующая терапия и BQT в качестве схем первого ряда показали сходные результаты H.pylori в анализах PP (97,7% против 96,2%, p = 0,605) и ITT (98,0% против 94,4%, p = 0,346) [43]. Более того, сетевой метаанализ показал, что сопутствующая терапия имеет более высокую эффективность, чем несколько других схем [40,60].
Сопутствующая терапия предпочтительнее последовательной терапии (ИПП и амоксициллин в течение 5 дней, затем ИПП, кларитромицин и тинидазол в течение еще 5 дней), потому что это проще. Существуют разногласия по поводу того, превосходит ли сопутствующая терапия над последовательной терапией [61,62,63,64,65].В испанском РКИ сопутствующая терапия была незначительно лучше (~ 5%) по сравнению с последовательной терапией (87% против 81% (ITT), p = 0,15; 91% против 86% (PP), p = 0,131) [65]. Кроме того, два метаанализа не выявили значительной разницы в скорости эрадикации между сопутствующей терапией и последовательной терапией [66,67].
Маастрихтский / Флорентийский консенсус не рекомендует последовательную терапию, в отличие от предыдущих руководств [10]. Это связано с тем, что последовательная терапия имеет более низкий уровень эрадикации, чем сопутствующая терапия в случаях резистентности к кларитромицину и чувствительности к метронидазолу H.pylori . И наоборот, когда H. pylori чувствителен к кларитромицину и устойчив к метронидазолу, последовательная терапия показывает более низкий уровень эрадикации, чем STT [10]. Увеличение дозы или продолжительности лечения метронидазолом может привести к эрадикации метронидазол-резистентного H. pylori . Скорость эрадикации при последовательной терапии невысока, поскольку период приема метронидазола составляет всего 5 дней.
Сопутствующая терапия имеет несколько ограничений, таких как более высокая частота нежелательных явлений, чем последовательная терапия [68].Повышенная частота осложнений может повлиять на соблюдение режима лечения H. pylori [69,70]. Хотя частота нежелательных явлений относительно высока, период лечения составляет менее 2 недель, поэтому большинство пациентов завершают курс лечения. Кроме того, есть опасения, что устойчивость к антибиотикам может повыситься из-за чрезмерного воздействия ненужных антибиотиков [71]. Наконец, эффекты сопутствующей терапии ниже у H . pylori, устойчивы как к кларитромицину, так и к метронидазолу [72].
5. Гибридная терапия
Гибридная терапия — это комбинация последовательной и сопутствующей терапии. Гибридная терапия включает ИПП и амоксициллин в течение 7 дней, затем ИПП, амоксициллин, кларитромицин и метронидазол в течение 7 дней [4]. Хотя Торонтский консенсус и Маастрихтский / Флорентийский консенсус не рекомендуют гибридную терапию, в клинических рекомендациях ACG рекомендуется использовать ее в качестве лечения первой линии у пациентов без предварительного воздействия макролидов в регионах с низким уровнем устойчивости к кларитромицину.Несколько метаанализов сообщили об эффективности и переносимости гибридной терапии [40,67,73]. Wang et al. продемонстрировали, что гибридная терапия была альтернативой сопутствующей или последовательной терапии (уровни эрадикации ITT гибридной, сопутствующей и последовательной терапии составили 88,6%, 86,3% и 84,7% соответственно; частота эрадикации PP составила 92,1%, 92,5% и 87,5%. ) [73]. Кроме того, нет значительных различий в переносимости или комплаентности между гибридной терапией и STT, последовательными или сопутствующими схемами [40,67,73].
В проспективном многоцентровом исследовании гибридная терапия вылечила> 90% пациентов с инфекцией H. pylori в регионах с высокими показателями устойчивости к кларитромицину и метронидазолу; это похоже на скорость эрадикации сопутствующей терапии [74]. Кроме того, комплаентность к гибридной терапии выше, чем к сопутствующей терапии (98,8% против 95,2%, p = 0,05). Однако скорость искоренения гибридной терапии значительно ниже для H.pylori . В проспективном исследовании частота эрадикации у пациентов с двойной устойчивостью к антибиотикам (кларитромицину и метронидазолу) была заметно снижена (50%) по сравнению с пациентами с резистентностью только к кларитромицину (91,4%) или метронидазолу (90,5%) [75].
6. Терапия на основе левофлоксацина
Левофлоксацин активен в отношении большого спектра различных бактерий, и в некоторых исследованиях левофлоксацин используется в качестве средства первой линии лечения инфекции H. pylori [15]. Проспективное исследование в Китае показало, что цефуроксим, левофлоксацин, ИПП и висмут в качестве терапии первой линии позволили достичь H.pylori составляет 97,2% случаев чувствительности к левофлоксацину и 84,0% случаев резистентности к левофлоксацину [76]. Однако в случаях устойчивости к цефуроксиму и левофлоксацину уровень эрадикации составил 0%. 14- и 7-дневные режимы дозирования левофлоксацина (левофлоксацин, кларитромицин, рабепразол и висмут) один раз в сутки показали уровень эрадикации 94% и 84% соответственно [77]. Gan et al. сравнили эффективность различных доз левофлоксацина для эрадикации H.pylori [78]. Показатели эрадикации в группах, получавших один и два раза в день, составили 77,5% и 79,5% (ITT) и 82,9% и 86,4% (PP), соответственно [78]. Нет значительных различий в степени искоренения или соблюдения режима лечения. Бычий лактоферрин усиливает эффективность схем первой линии на основе левофлоксацина при инфекции H. pylori [79]. Успешная эрадикация составляет 96,1% для эзомепразола / амоксициллина / левофлоксацина / бычьего лактоферрина и 75% для эзомепразола / амоксициллина / левофлоксацина [79].Режим LOAD (левофлоксацин, омепразол, нитазоксанид и доксициклин) был введен недавно [71]. Basu et al. сообщили, что уровень эрадикации LOAD составил 89,4% по сравнению с 73,3% для STT ( p <0,05) [80].
Левофлоксацин представляет собой хинолон и широко используется во всем мире, например, при пневмонии, инфекции мочевыводящих путей, туберкулезе и H. pylori . Таким образом, многие пациенты в анамнезе принимали левофлоксацин. В большинстве руководств рекомендуется применять схемы на основе левофлоксацина в качестве экстренной помощи, а не в качестве терапии первой линии [81].Клинические рекомендации ACG слабо рекомендуют тройной (амоксициллин, левофлоксацин и ИПП), последовательный (5-7 дней ИПП и амоксициллин, затем 5-7 дней ИПП, нитроимидазол и левофлоксацин) или четырехкратный (амоксициллин, левофлоксацин и ИПП). ИПП, левофлоксацин, доксициклин и нитазоксанид в течение 7 или 10 дней) по схемам первого ряда [4].
Ситафлоксацин представляет собой фторхинолон четвертого поколения и обладает высокой активностью против штаммов gyr A с положительной мутацией H. pylori [82].Ситафлоксацин в основном используется с амоксициллином или метронидазолом в качестве экстренной помощи, а не терапии первой линии. Сообщается, что схемы третьей линии, содержащие ситафлоксацин, эффективны для эрадикации H. pylori (75,8% (ITT) и 83,3% (PP)) [83]. Фторхинолоны четвертого поколения, такие как ситафлоксацин и гареноксацин, могут преодолеть устойчивость к хинолонам H. pylori [84,85]. Среди 100 штаммов с высокими показателями устойчивости к кларитромицину, метронидазолу и левофлоксацину> 95% чувствительны к ситафлоксацину [86].Следует оценить эффективность схем, содержащих ситафлоксацин или гареноксацин, против gyr A с положительной мутацией H. pylori .
7. Терапия на основе рифабутина
Рифабутин — это производное рифамицина, структурно сходное с рифампицином (противотуберкулезным препаратом). Он в основном используется при атипичном туберкулезе, таком как Mycobacterium avium -intracellulare и M. tuberculosis , устойчивых к рифампицину [87]. Рифабутин подавляет синтез белка путем ингибирования бета-субъединицы ДНК-зависимой РНК-полимеразы Helicobacter , которая кодируется rpoB .Следовательно, мутация rpoB придает устойчивость к рифабутину [88]. Все существующие руководящие принципы предполагают, что схемы на основе рифабутина следует рассматривать только как терапию «спасения» при эрадикации H. pylori [81]. Согласно метаанализу, эффективность лечения на основе рифабутина второй, третьей и четвертой / пятой линий составляет 79%, 66% и 70% соответственно [87]. В итальянском исследовании тройная терапия на основе рифабутина (рифабутин, амоксициллин и ИПП) в течение 14 дней позволила достичь скорости эрадикации 72.7% (PP) и 71,5% (ITT) у пациентов, у которых эрадикация H. pylori оказалась неэффективной после лечения традиционными антибиотиками [89]. Рифабутин не обладает такой же устойчивостью к антибиотикам, как кларитромицин и амоксициллин, а также является жирорастворимым и легко всасывается после перорального приема [88, 90]. Кроме того, рифабутин стабилен в широком диапазоне значений pH и не разлагается желудочной кислотой, а уровень устойчивости у H. pylori низкий, поскольку он редко используется в клинических условиях [87,91]. Следовательно, схемы на основе рифабутина важны для спасательной терапии.Однако другое исследование показало, что уровень искоренения терапии на основе рифабутина был невысоким: 50,0% в анализе ITT и 54,5% в анализе PP [92]. Поскольку есть некоторые части, которые не достигают стабильной скорости эрадикации в качестве спасательной терапии, можно считать, что необходимы соответствующие исследования.
На сегодняшний день большинство исследований схем на основе рифабутина сосредоточено на спасательной терапии. Недавно Graham et al. показали, что тройная схема на основе рифабутина (амоксициллин, рифабутин и ИПП) имела более высокий уровень эрадикации, чем амоксициллин плюс ИПП в качестве эмпирического лечения первой линии H.pylori (83,8% против 57,7%, p <0,001) [93]. Это говорит о том, что рифабутин является революционным препаратом первой линии в эпоху устойчивости к антибиотикам. Однако он дороже других антибиотиков. Кроме того, он может вызвать устойчивость к режиму лечения туберкулеза [94]. Более того, поскольку использование рифампицина способствует точечной мутации rpoB и увеличивает минимальную ингибирующую концентрацию (МИК) рифабутина, перед назначением рифабутина необходимо определить предшествующее лечение рифампицином [95].Наконец, рифабутин имеет небольшой риск миелотоксичности [87].
8. Терапия на основе калий-конкурентных кислотных блокаторов
Калий-конкурентные кислотные блокаторы (P-CAB) — это ингибитор секреции кислоты желудочного сока, с более быстрым началом и более длительным действием подавления кислоты, и более эффективен, чем ИПП. [96,97]. Кроме того, P-CAB не требует активации желудочной кислотой, поэтому его можно принимать независимо от времени приема пищи. В обращении H . pylori, pH желудка должен поддерживаться выше определенного уровня, чтобы активировать антибиотик [98].P-CAB ингибирует опосредованную H + и K + -АТФазу секрецию кислоты желудочного сока и является кислотоустойчивым и менее подвержен влиянию системы CYP2C19, чем ИПП [71,99]. Поскольку ИПП имеют короткую продолжительность действия и на их эффективность влияют различные подтипы цитохрома Р450 (ИПП в основном метаболизируются CYP2C19 и CYP3A4), внимание привлекла новая схема лечения против H. pylori , содержащая PCAB [99,100]. Вонопразан в настоящее время продается в Японии, продвигая исследования P-CAB для H.pylori лечение.
По данным многоцентрового РКИ в Японии, частота эрадикации первой линии тройной терапии на основе фонопразана (фонопразан, амоксициллин и кларитромицин) составила 92,6% по сравнению с 75,9% для STT ( p <0,0001) [101]. Метаанализ японских исследований с участием 1599 пациентов показал, что тройная терапия на основе фонопразана значительно превосходила STT у пациентов с устойчивыми к кларитромицину штаммами (82,0% против 40,0%, p <0,0001) [102].Напротив, уровень эрадикации чувствительных к кларитромицину штаммов существенно не отличается. Если организм устойчив к кларитромицину, STT переключается на двойную терапию (ИПП + амоксициллин), и двойная терапия важна для поддержания pH желудочного сока на уровне ≥6. В этом отношении считается, что у вонопразана есть сильные стороны. Кроме того, тройная схема на основе фонопразана так же эффективна, как и STT на основе ИПП на основе чувствительности, для эрадикации H. pylori (97,4% против 95,7%) [103]. В исследовании эффективности двойной терапии 7-дневного фонопразана и низких доз амоксициллина в качестве препарата первой линии H.pylori , уровни эрадикации двойной (фонопразан и низкие дозы амоксициллина) и тройной терапии (фонопразан, амоксициллин с низкой дозой и кларитромицин) составили 84,5% и 89,2% ( p = 0,203) по ITT-анализу соответственно. и 87,1% и 90,2% ( p = 0,372) по данным PP-анализа, соответственно [104]. В реальности увеличения устойчивости к противомикробным препаратам можно сказать, что снижение общего количества антибиотиков с использованием вонопразана показывает положительный аспект в будущем лечении H.pylori .
В Японии схемы на основе P-CAB лицензированы в качестве лечения первого и второго ряда для эрадикации H. pylori . Мураками и др. продемонстрировали эффективность тройной схемы второго ряда на основе P-CAB (частота успеха 98,0%) [101]. Другое РКИ показало, что тройная терапия на основе фонопразана (фонопразан, амоксициллин и ситафлоксацин) была более эффективной, когда ИПП использовался с этими антибиотиками в качестве схемы лечения третьей линии для H. pylori (83,3% против 57.1% (PP), p = 0,043) [83]. Следовательно, терапия на основе P-CAB может быть жизнеспособной альтернативой схемам первого и второго ряда для эрадикации H. pylori .
9. Лечение при неэффективности первичной терапии
Все руководства рекомендуют избегать ранее принимаемых пациентом антибиотиков [4,8,9,10]. В частности, следует избегать повторного использования кларитромицина и левофлоксацина из-за высоких показателей устойчивости. Они также рекомендуют схему лечения тройной второй линии на основе BQT или левофлоксацина для H.pylori [81]. Если терапия первой или второй линии оказалась неэффективной, следует рассмотреть возможность проведения теста на восприимчивость к соответствующей терапии экстренной помощи [10,81].
Согласно Маастрихтскому / Флорентийскому консенсусу, после неэффективности BQT в качестве терапии первой линии рекомендуется трех- или четырехкратная терапия, содержащая хинолон [10]. После неэффективности четырехкомпонентного режима без висмута первой линии рекомендуется трех- или четырехкратный режим, содержащий BQT или хинолон [10]. BQT, четырехкомпонентная терапия без висмута и трехкомпонентная терапия, содержащая хинолоны, могут использоваться без перекрытия со схемами лечения второй или третьей линии [10].
Торонтский консенсус и рекомендации ACG, такие как Маастрихтский V / Флорентийский консенсус, подчеркивают важность BQT и левофлоксацин-содержащих схем лечения в качестве препаратов второго ряда [4,9]. Важным отличием от Маастрихтского V / Флорентийского консенсуса является возражение против использования четырехкратной схемы второго ряда без висмута, поскольку это менее эффективно, чем другие методы лечения [9]. Кроме того, схемы на основе рифабутина следует использовать только для пациентов, у которых в прошлом было не менее трех неудач лечения [9].В рекомендациях ACG указывается, что режим второго ряда следует выбирать на основе предыдущего воздействия антибиотиков и данных о местной устойчивости к антибиотикам [4].
10. Выводы
обобщает важные схемы лечения H. pylori . Лечение H. pylori — важная глобальная проблема, потому что оно было напрямую связано как причина нескольких желудочно-кишечных заболеваний. Существует явная озабоченность по поводу увеличения показателей устойчивости с течением времени, что подчеркивает необходимость использования подходящих антибиотиков в будущем, чтобы минимизировать дальнейший рост устойчивости к антибиотикам.Специальная терапия на основе AST показала хорошую скорость эрадикации при применении первой линии. Поскольку уровень устойчивости к антибиотикам H. pylori увеличивается, следует расширить роль индивидуализированных методов лечения. Однако, если индивидуальная терапия не может быть применена ко всем пациентам из-за реальных проблем, разумной альтернативой является использование высокоэффективного эмпирического режима на местном уровне. Кроме того, при использовании такой эмпирической схемы необходима простая и эффективная стратегия лечения H. pylori .Поэтому мы предлагаем BQT в качестве терапии первой линии, когда данные по AST или региональной резистентности недоступны (). Если BQT недоступен, мы предлагаем эмпирическую сопутствующую терапию. P-CAB может быть альтернативой, но данные немногочисленны и ограничены Восточной Азией.
Упрощенная стратегия лечения H. pylori .
Таблица 1
Схемы лечения инфекции Helicobacter pylori .
| Лечение | Схема | Продолжительность | Недавняя частота эрадикации первой линии (ITT) | Рекомендации в соответствии с Руководством | Примечания | |
|---|---|---|---|---|---|---|
| Стандартная тройная терапия (STT) | Стандартная тройная терапия (STT) | Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день | 7–14 дней | 63.9% [105], 74,1% [106] | Первая линия: необязательно рекомендована KCHUGR и JSHR Спасательная операция: ограничена рекомендована MAA | За последние 20 лет эффективность STT заметно снизилась, и STT обычно не рекомендуется в качестве схемы первого ряда |
| Квартальная терапия висмутом (BQT) | Стандартная доза ИПП 2 раза в день Стандартная доза висмута 4 раза в день Метронидазол 500 мг 3 раза в день Тетрациклин 500 мг 4 раза в день | 7–14 дней | .8% [107], 88,2% [44], 91,5% [108] Первая линия: рекомендовано ACG, MAA, TOR и KCHUGR (необязательно) Rescue: рекомендовано ACG, MAA, TOR и KCHUGR | BQT был предложен в качестве варианта лечения первой линии во многих руководствах, особенно для регионов с высокой устойчивостью к кларитромицину. | ||
| Сопутствующая терапия (четырехкратная терапия без висмута) | Стандартная доза ИПП 2 раза в день Кларитромицин 500 мг 2 раза в день Амоксициллин 1 г 2 раза в день Метронидазол 500 мг 2 раза в день | 10–14 дней | 84.6% [106], 90,1% [109], 93,5% [110] | Первая линия: рекомендовано ACG, MAA и TOR Спасение: рекомендовано ACG и MAA | Скорость искоренения превосходит это CTT, а метод введения прост по сравнению с последовательной терапией. Но побочные эффекты могут быть более вероятными при сопутствующей терапии. | |
| Последовательная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день (только первая половина) Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 10–14 д | 69.5% [106], 82,0% [111], 87,0% [112] | Первая линия: необязательно рекомендуется (не идеально) ACG Спасение: не рекомендуется во всех руководствах | В качестве терапии первой линии роль постепенно исчезает. Это обременительный способ снизить комплаентность пациента. | |
| Гибридная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 14 дней | 85.8% [75], 92,8% [113] | Первая линия: необязательно рекомендуется (не идеально) ACG Rescue: не рекомендуется во всех руководствах | Это метод, сочетающий последовательную терапию и сопутствующую терапию. | |
| Терапия на основе левофлоксацина | Левофлоксацин можно назначать в виде тройной или четырехкратной терапии. | 10–14 дней | 85,5% [76], 94,0% [77] | Первая линия: рекомендована ACG Rescue: рекомендована ACG, MAA и TOR | В большинстве руководств рекомендуется проводить терапию на основе левофлоксацина. применяется как терапия спасения, а не как первая линия.Он менее эффективен для областей с высокой устойчивостью к хинолонам. | |
| Терапия на основе рифабутина | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Рифабутин 150 мг 2 раза в день | 10 дней | 83,8% [93] | Первая линия: не рекомендуется во всех рекомендациях Спасение: необязательно (третья или четвертая линия) по MAA и TOR | Все руководства рекомендуют терапию на основе рифабутина в качестве терапии спасения. Рифабутин имеет редкий риск миелотоксичности; поэтому требуется осторожное использование. | |
| Терапия на основе калий-конкурентных кислотных блокаторов | P-CAB можно назначать как тройную терапию или четырехкратную терапию, заменяя PPI на P-CAB. | 7–14 d | 89,2% [104], 90,2% [114] | Не указано в алгоритме руководящих принципов | Ожидается, что роль мощного подавления кислоты будет постепенно возрастать, и необходимы дополнительные исследования. | |
| Лечение H. pylori на основе теста на антибактериальную чувствительность | Индивидуальная терапия в соответствии с результатами AST | 7–14 дней | 92.7% [31], 92,9% [115] | MAA рекомендует проводить АСТ после неэффективности терапии второй линии. | Результаты индивидуализированной терапии на основе AST превосходны, и ожидается, что она сыграет роль в улучшении лечения H. pylori в будущем. Требуются усилия для облегчения применения AST в клинической практике. |
Индивидуальная терапия, согласно результатам AST, способствует лечению H. pylori без повышения устойчивости к антибиотикам, поэтому следует уделять особое внимание тестированию на чувствительность.Есть также дополнительные соображения; например, как установить продолжительность лечения при чувствительности к кларитромицину и как выбрать режим (BQT или амоксициллин-метронидазол-ИПП), если устойчивость к кларитромицину не изучалась. Дальнейшая работа должна быть сосредоточена на максимальном терапевтическом эффекте индивидуализированной терапии, основанной на результатах AST.
Вклад авторов
S.Y.K. написал рукопись, и J.-W.C. способствовал разработке концепции и дизайна исследования. Все авторы прочитали и согласились с опубликованной версией рукописи.
Финансирование
Это исследование было поддержано Программой фундаментальных научных исследований через Национальный исследовательский фонд Кореи (NRF), финансируемым Министерством образования (номер гранта: 2020R1I1A306686511) и Исследовательским фондом Кореи (NRF), финансируемым Министерством образования. Образование (номер гранта: 2020R1F1A1076839).
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
1. Кандульски А., Селград М., Малфертхайнер П. Инфекция Helicobacter pylori : клинический обзор. Копать землю. Печень. Дис. 2008. 40: 619–626. DOI: 10.1016 / j.dld.2008.02.026. [PubMed] [CrossRef] [Google Scholar] 2. Макколл К. Клиническая практика. Инфекция Helicobacter pylori . N. Engl. J. Med. 2010; 362: 1597–1604. DOI: 10.1056 / NEJMcp1001110. [PubMed] [CrossRef] [Google Scholar] 3. Пламмер М., Франчески С., Винья Дж., Форман Д., де Мартель С. Глобальное бремя рака желудка, связанное с Helicobacter pylori . Int.J. Рак. 2015; 136: 487–490. DOI: 10.1002 / ijc.28999. [PubMed] [CrossRef] [Google Scholar] 4. Чей В.Д., Леонтиадис Г.И., Хауден К.В., Мосс С.Ф. Клинические рекомендации ACG: Лечение инфекции Helicobacter pylori . Являюсь. J. Gastroenterol. 2017; 112: 212–239. DOI: 10.1038 / ajg.2016.563. [PubMed] [CrossRef] [Google Scholar] 5. Тестерман Т.Л., Моррис Дж. За пределами желудка: обновленный взгляд на патогенез, диагностику и лечение Helicobacter pylori . Мир J. Gastroenterol. 2014; 20: 12781–12808.DOI: 10.3748 / wjg.v20.i36.12781. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ли Ю.К., Чан Т.Х., Чжоу С.К., Ту Ю.К., Ляо В.С., Ву М.С., Грэм Д.Ю. Связь между Helicobacter pylori Эрадикация и заболеваемость раком желудка: систематический обзор и метаанализ. Гастроэнтерология. 2016; 150: 1113–1124. DOI: 10.1053 / j.gastro.2016.01.028. [PubMed] [CrossRef] [Google Scholar] 7. Судзуки Х., Нисидзава Т., Хиби Т. Эрадикационная терапия Helicobacter pylori . Будущее.Microbiol. 2010. 5: 639–648. DOI: 10.2217 / fmb.10.25. [PubMed] [CrossRef] [Google Scholar] 8. Ким С.Г., Юнг Х.К., Ли Х.Л., Чан Дж.Й., Ли Х., Ким С.Г., Шин В.Г., Шин Э.С., Ли Ю.С. Корейский колледж хеликобактер и исследований верхних отделов желудочно-кишечного тракта. Корейский J. Gastroenterol. 2013; 62: 3–26. DOI: 10.4166 / kjg.2013.62.1.3. [PubMed] [CrossRef] [Google Scholar] 9. Фаллон К.А., Чиба Н., ван Зантен С.В., Фишбах Л., Гисберт Дж. П., Хант Р. Х., Джонс Н. Л., Рендер К., Леонтиадис Г. И., Моайеди П. и др. Торонтский консенсус по лечению инфекции Helicobacter pylori у взрослых.Гастроэнтерология. 2016; 151: 51–69. DOI: 10.1053 / j.gastro.2016.04.006. [PubMed] [CrossRef] [Google Scholar] 10. Малфертхайнер П., Мегро Ф., О’Морайн С.А., Гисберт Дж. П., Койперс Э. Дж., Аксон А. Т., Баццоли Ф., Гасбаррини А., Атертон Дж., Грэм Д. Ю. и др. Управление инфекцией Helicobacter pylori — Маастрихт V / Флорентийский консенсусный доклад. Кишечник. 2017; 66: 6–30. DOI: 10.1136 / gutjnl-2016-312288. [PubMed] [CrossRef] [Google Scholar] 11. Гисберт Дж. П., Гонсалес Л., Кальвет X., Гарсия Н., Лопес Т., Roque M., Gabriel R., Pajares J.M. Ингибитор протонной помпы, кларитромицин и амоксициллин или нитроимидазол: метаанализ эрадикации Helicobacter pylori . Алимент. Pharmacol. Ther. 2000; 14: 1319–1328. DOI: 10.1046 / j.1365-2036.2000.00844.x. [PubMed] [CrossRef] [Google Scholar] 12. Современные европейские концепции лечения инфекции Helicobacter pylori Маастрихтский консенсусный доклад. Европейская группа по изучению Helicobacter pylori. Кишечник. 1997; 41: 8–13. DOI: 10.1136 / gut.41.1.8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 13. Грэм Д.Ю., Фишбах Л. Лечение Helicobacter pylori в эпоху повышения устойчивости к антибиотикам. Кишечник. 2010; 59: 1143–1153. DOI: 10.1136 / gut.2009.1. [PubMed] [CrossRef] [Google Scholar] 14. Савольди А., Каррара Э., Грэм Д. Ю., Конти М., Такконелли Э. Распространенность устойчивости к антибиотикам у Helicobacter pylori : систематический обзор и метаанализ в регионах Всемирной организации здравоохранения. Гастроэнтерология.2018; 155: 1372–1382. DOI: 10.1053 / j.gastro.2018.07.007. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 15. Ким С.Ю., Чхве Д.Дж., Чунг Дж.В. Лечение антибиотиками от Helicobacter pylori : приближается конец? Мир J. Gastrointest. Pharmacol. Ther. 2015; 6: 183–198. DOI: 10.4292 / wjgpt.v6.i4.183. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 16. Тунг И., Арамин Х., Вавинская В., Гупта С., Парк Дж. Ю., Кроу С.Э., Валасек М.А. Обзорная статья: Глобальное появление устойчивости к антибиотикам Helicobacter pylori .Алимент. Pharmacol. Ther. 2016; 43: 514–533. DOI: 10.1111 / apt.13497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Woo H.Y., Park D.I., Park H., Kim M.K., Kim D.H., Kim I.S., Kim Y.J. Мультиплексная ПЦР на основе олигонуклеотидов с двойным примированием для обнаружения Helicobacter pylori и определения устойчивости к кларитромицину с помощью биоптатов желудка. Helicobacter. 2009. 14: 22–28. DOI: 10.1111 / j.1523-5378.2009.00654.x. [PubMed] [CrossRef] [Google Scholar] 18. Лиу Дж. М., Чанг К.Y., Chen M.J., Chen C.C., Fang Y.J., Lee J.Y., Wu J., Luo J., Liou T., Chang W. и др. Первичная устойчивость Helicobacter pylori на Тайване после проведения национальной политики ограничения потребления антибиотиков и ее связи с факторами вирулентности — общенациональное исследование. PLoS ONE. 2015; 10: e0124199. DOI: 10.1371 / journal.pone.0124199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 19. Ли Дж.Й., Пак К.С. Оптимальное лечение первой линии для инфекции Helicobacter pylori : последние стратегии.Гастроэнтерол. Res. Практик. 2016; 2016: 81. DOI: 10.1155 / 2016/81. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 20. Альба К., Бланко А., Аларкон Т. Устойчивость к антибиотикам у Helicobacter pylori . Curr. Opin. Заразить. Дис. 2017; 30: 489–497. DOI: 10.1097 / QCO.0000000000000396. [PubMed] [CrossRef] [Google Scholar] 21. Hwang T.J., Kim N., Kim H.B., Lee B.H., Nam R.H., Park J.H., Lee M.K., Park Y.S., Lee D.H., Jung H.C. и др. Изменение устойчивости к антибиотикам штаммов Helicobacter pylori и влияние точечной мутации A2143G 23S рРНК на эрадикацию H.pylori в едином центре Кореи. J. Clin. Гастроэнтерол. 2010; 44: 536–543. DOI: 10.1097 / MCG.0b013e3181d04592. [PubMed] [CrossRef] [Google Scholar] 22. Герритс М.М., ван Влит А.Х., Кейперс Э.Дж., Кустерс Дж.Г. Helicobacter pylori и устойчивость к противомикробным препаратам: молекулярные механизмы и клинические последствия. Lancet Infect. Дис. 2006; 6: 699–709. DOI: 10.1016 / S1473-3099 (06) 70627-2. [PubMed] [CrossRef] [Google Scholar] 24. Халтен К., Гибриль А., Скольд О., Энгстранд Л. Устойчивость к макролидам у Helicobacter pylori : механизм и стабильность в штаммах от пациентов, получавших кларитромицин.Противомикробный. Агенты. Chemother. 1997; 41: 2550–2553. DOI: 10.1128 / AAC.41.11.2550. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25. Стоун Г.Г., Шортридж Д., Версалович Дж., Бейер Дж., Фламм Р.К., Грэм Д.Ю., Гонейм А.Т., Танака С.К. ПЦР-анализ лигирования олигонуклеотидов для определения распространенности мутаций гена 23S рРНК у устойчивых к кларитромицину Helicobacter pylori . Противомикробный. Агенты Chemother. 1997. 41: 712–714. DOI: 10.1128 / AAC.41.3.712. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26.Аларкон Т., Доминго Д., Прието Н., Лопес-Бреа М. Стабильность устойчивости к кларитромицину у Helicobacter pylori : влияние MIC и типа мутации в 23S рРНК. J. Antimicrob. Chemother. 2000. 46: 613–616. DOI: 10.1093 / jac / 46.4.613. [PubMed] [CrossRef] [Google Scholar] 27. Van Doorn LJ, Glupczynski Y., Kusters JG, Megraud F., Midolo P., Maggi-Solca N., Queiroz DM, Nouhan N., Stet E., Quint WG Точное прогнозирование устойчивости к макролидам у Helicobacter pylori с помощью Анализ зонда ПЦР для обнаружения мутаций в гене 23S рРНК: многоцентровое валидационное исследование.Противомикробный. Агенты Chemother. 2001; 45: 1500–1504. DOI: 10.1128 / AAC.45.5.1500-1504.2001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 28. Като С., Фудзимура С., Удагава Х., Симидзу Т., Майсава С., Одзава К., Иинума К. Устойчивость к антибиотикам штаммов Helicobacter pylori у японских детей. J. Clin. Microbiol. 2002; 40: 649–653. DOI: 10.1128 / JCM.40.2.649-653.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Ван В.Х., Вонг Б.С., Мукхопадхьяй А.К., Берг Д.Э., Чо К.Х., Лай К.С., Ху В.Х., Фунг Ф.М., Хуэй В.М., Лам С.К. Высокая распространенность инфекции Helicobacter pylori с двойной устойчивостью к метронидазолу и кларитромицину в Гонконге. Алимент. Pharmacol. Ther. 2000; 14: 901–910. DOI: 10.1046 / j.1365-2036.2000.00795.x. [PubMed] [CrossRef] [Google Scholar] 30. Ли Х. Дж., Ким Дж. И., Чунг Д. Ю., Ким Т. Х., Джун Э. Дж., О Дж. Х., Чунг В. К., Ким Б., Ким С. С., Пак С. и др. Искоренение Helicobacter pylori в соответствии с точечными мутациями 23S рибосомной РНК, связанными с устойчивостью к кларитромицину.J. Infect. Дис. 2013; 208: 1123–1130. DOI: 10.1093 / infdis / jit287. [PubMed] [CrossRef] [Google Scholar] 31. Чо Дж. Х., Чон С. Р., Ким Х. Г., Джин С. Ю., Пак С. Экономическая эффективность адаптированной стратегии ликвидации Helicobacter pylori , основанной на наличии точечной мутации 23S рибосомной РНК, которая вызывает устойчивость к кларитромицину у корейских пациентов. J. Gastroenterol. Гепатол. 2019; 34: 700–706. DOI: 10.1111 / jgh.14383. [PubMed] [CrossRef] [Google Scholar] 32. Папастержиу В., Мату Н., Ликуси С., Евгениди А., Параскева К.Д., Яннакопулос А., Ставру П., Платсука Э., Караджаннис Ю.А. Семидневная тройная эрадикационная терапия Helicobacter pylori на основе генотипической устойчивости может быть высокоэффективной. Анна. Гастроэнтерол. 2018; 31: 198–204. DOI: 10.20524 / aog.2017.0219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 33. Cosme A., Montes M., Ibarra B., Tamayo E., Alonso H., Mendarte U., Lizasoan J., Herreros-Villanueva M., Bujanda L. Тестирование на чувствительность к противомикробным препаратам перед лечением первой линии для Helicobacter pylori инфекция у пациентов с двойной или тройной устойчивостью к антибиотикам.Мир J. Gastroenterol. 2017; 23: 3367–3373. DOI: 10.3748 / wjg.v23.i18.3367. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Ли Дж. У., Ким Н., Нам Р. Х., Ли С. М., Квон Ю. Х., Сон С. Д., Ким Дж. М., Ли Д. Х., Юнг Х. С. Благоприятные исходы эрадикационной терапии Helicobacter pylori на основе посева в регионе с высокой устойчивостью к противомикробным препаратам. Helicobacter. 2019; 24: e12561. DOI: 10.1111 / hel.12561. [PubMed] [CrossRef] [Google Scholar] 35. Чен К., Лонг X., Цзи Ю., Лян X., Ли Д., Гао Х., Сюй Б., Лю М., Чен Ю., Сунь Ю. Рандомизированное контролируемое исследование: терапия на основе чувствительности в сравнении с эмпирической четырехкратной терапией висмутом для лечения первой линии Helicobacter pylori . Алимент. Pharmacol. Ther. 2019; 49: 1385–1394. DOI: 10.1111 / apt.15273. [PubMed] [CrossRef] [Google Scholar] 36. Блюмель Б., Гёльц Х., Кист М., Глокер Э.О. Ретроспективное исследование результатов эрадикационной терапии «спасение» Helicobacter pylori на основе молекулярно-генетического тестирования чувствительности. Helicobacter.2018; 23: e12494. DOI: 10.1111 / hel.12494. [PubMed] [CrossRef] [Google Scholar] 37. Бхакта Д., Грэм Д. Ю., Чан Дж., Эль-Сераг Х. Б. Уроки использования культурального лечения после направления к специалисту по поводу множественной неудачи лечения инфекции, вызванной Helicobacter pylori . Clin. Гастроэнтерол. Гепатол. 2018; 16: 1531–1532. DOI: 10.1016 / j.cgh.2017.12.040. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Байлина М., Муньос Н., Санчес-Дельгадо Дж., Лопес-Гонгора С., Кальвет X., Пуч И. Систематический обзор: Достигнет ли лечение на основе чувствительности приемлемых показателей излечения для терапии второй линии Helicobacter pylori , как в настоящее время практиковал? Helicobacter.2019; 24: e12584. DOI: 10.1111 / hel.12584. [PubMed] [CrossRef] [Google Scholar] 39. Лиу Дж. М., Чен П. Ю., Ло Дж. К., Ли Дж. Ю., Чен К. С., Фанг Ю. Дж., Ян Т. Х., Чанг С. Ю., Баир М. Дж., Ченет М. Дж. И др. Эффективность управляемой генотипической резистентности по сравнению с эмпирической терапией рефрактерной инфекции Helicobacter pylori . Гастроэнтерология. 2018; 155: 1109–1119. DOI: 10.1053 / j.gastro.2018.06.047. [PubMed] [CrossRef] [Google Scholar] 40. Ли Б.З., Треэплтон Д.Э., Ван Дж.Й., Сюй Дж.М., Юань Дж.К., Чжан К., Ли П., Е К. Л., Го Б., Мао С. и др. Сравнительная эффективность и переносимость лечения Helicobacter pylori : систематический обзор и сетевой метаанализ. BMJ. 2015; 351: ч5052. DOI: 10.1136 / bmj.h5052. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 41. Лю К.С., Хунг И.Ф., Сето В.К., Тонг Т., Сюй А.С., Лам Ф.Й., Но Д.Й.К., Вонг С.Й., Люн В.К. Десятидневная последовательная и 10-дневная модифицированная четырехкратная терапия висмутом в качестве эмпирической терапии первой и второй линии для Helicobacter pylori у китайских пациентов: открытое рандомизированное перекрестное исследование.Кишечник. 2014; 63: 1410–1415. DOI: 10.1136 / gutjnl-2013-306120. [PubMed] [CrossRef] [Google Scholar] 42. Hsu P.I., Tsay F.W., Graham D.Y., Tsai T.J., Tsai K.W., Kao J.Y., Peng N.J., Kuo C.H., Kao S.S., Wang H.M. и др. Эквивалентная эффективность обратной гибридной и четверной терапии висмутом в искоренении инфекции Helicobacter pylori в рандомизированном контролируемом исследовании. Clin. Гастроэнтерол. Гепатол. 2018; 16: 1427–1433. DOI: 10.1016 / j.cgh.2018.03.031. [PubMed] [CrossRef] [Google Scholar] 43.Масиас-Гарсия Ф., Бастон-Рей И., де ла Иглесиа-Гарсия Д., Кальвино-Суарес К., Ньето-Гарсия Л., Домингес-Муньос Дж. Э. Висмутсодержащая четырехкратная терапия по сравнению с сопутствующей четырехкратной терапией в качестве лечения первой линии для инфекции Helicobacter pylori в области высокой устойчивости к кларитромицину: проспективное, перекрестное, сравнительное, открытое исследование. Helicobacter. 2019; 24: e12546. DOI: 10.1111 / hel.12546. [PubMed] [CrossRef] [Google Scholar] 44. Ким С.Дж., Чунг Дж.В., Ву Х.С., Ким С.Й., Ким Дж.Х., Ким Й.Дж., Ким К.О., Квон К.А., Пак Д.К. Двухнедельная четырехкратная терапия висмутом и сопутствующая терапия являются эффективными препаратами первой линии для эрадикации Helicobacter pylori : проспективное открытое рандомизированное исследование. Мир. J. Gastroenterol. 2019; 25: 6790–6798. DOI: 10.3748 / wjg.v25.i46.6790. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 45. Ким Дж.Й., Ли С.Й., Ким Дж.Х., Сунг И.К., Пак Х.С. Эффективность и безопасность четырехкратной висмутсодержащей терапии два раза в день с использованием высоких доз тетрациклина и метронидазола для эрадикации второй линии Helicobacter pylori .Helicobacter. 2020; 25: e12683. DOI: 10.1111 / hel.12683. [PubMed] [CrossRef] [Google Scholar] 46. Xie Y., Pan X., Li Y., Wang H., Du Y., Xu J., Wang J., Zeng Z., Chen Y., Zhang G. и др. Новая однократная капсула висмута, метронидазола и тетрациклина, вводимая с омепразолом, по сравнению с четырехкратной терапией, состоящей из висмута, омепразола, амоксициллина и кларитромицина для эрадикации Helicobacter pylori у пациентов с язвой двенадцатиперстной кишки: проспективное, многоцелевое исследование в Китае. J. Antimicrob.Chemother. 2018; 73: 1681–1687. [PubMed] [Google Scholar] 47. Фиорини Г., Зулло А., Сарачино И.М., Гатта Л., Павони М., Вайра Д. Пилера и последовательная терапия для эрадикации первой линии Helicobacter pylori : исследование на основе культуры в реальной клинической практике. Евро. J. Gastroenterol. Гепатол. 2018; 30: 621–625. DOI: 10.1097 / MEG.0000000000001102. [PubMed] [CrossRef] [Google Scholar] 48. Ниссен О.П., МакНичолл А.Г., Гисберт Дж.П. Метаанализ четырехкратной терапии, содержащей висмут, три-в-одной одной капсуле для уничтожения Helicobacter pylori .Helicobacter. 2019; 24: e12570. DOI: 10.1111 / hel.12570. [PubMed] [CrossRef] [Google Scholar] 49. Ким С.Э., Ро Дж. Х., Парк М. И., Пак С. Дж., Мун В., Ким Дж. Х., Юнг К., Хео Дж. Дж. Эффект 7-дневной четырехкратной терапии висмутом по сравнению с 14-дневной тройной терапией моксифлоксацином для второй линии Helicobacter pylori эрадикационной терапии. Корейский язык. J. Gastroenterol. 2019; 73: 26–34. DOI: 10.4166 / kjg.2019.73.1.26. [PubMed] [CrossRef] [Google Scholar] 50. Боянова Л., Митов И. Географическая карта и эволюция первичной устойчивости Helicobacter pylori к антибактериальным препаратам.Эксперт. Преподобный Anti. Заразить. Ther. 2010; 8: 59–70. DOI: 10.1586 / eri.09.113. [PubMed] [CrossRef] [Google Scholar] 51. Megraud F., Coenen S., Versporten A., Kist M., Lopez-Brea M., Hirschl AM, Andersen LP, Goossens H., Glupczynski Y., участники исследовательской группы Устойчивость Helicobacter pylori к антибиотикам в Европе и ее отношение к употреблению антибиотиков. Кишечник. 2013; 62: 34–42. DOI: 10.1136 / gutjnl-2012-302254. [PubMed] [CrossRef] [Google Scholar] 52. Фишбах Л., Эванс Э. Мета-анализ: влияние статуса устойчивости к антибиотикам на эффективность тройной и четверной терапии первой линии для Helicobacter pylori .Алимент. Pharmacol. Ther. 2007. 26: 343–357. DOI: 10.1111 / j.1365-2036.2007.03386.x. [PubMed] [CrossRef] [Google Scholar] 53. Venerito M., Krieger T., Ecker T., Leandro G., Malfertheiner P. Метаанализ четырехкратной терапии висмутом по сравнению с тройной терапией кларитромицином для эмпирического первичного лечения инфекции Helicobacter pylori . Пищеварение. 2013; 88: 33–45. DOI: 10,1159 / 000350719. [PubMed] [CrossRef] [Google Scholar] 54. Манцарис Г.Дж., Петраки К., Арчавлис Э., Амбериадис П., Христофоридис П., Kourtessas D., Chiotakakou E., Triantafyllou G. Тройная терапия омепразолом по сравнению с четырехкратной терапией омепразолом для заживления язвы двенадцатиперстной кишки и эрадикации инфекции Helicobacter pylori : последующее исследование через 24 месяца. Евро. J. Gastroenterol. Гепатол. 2002; 14: 1237–1243. DOI: 10.1097 / 00042737-200211000-00012. [PubMed] [CrossRef] [Google Scholar] 55. Gisbert J.P., Calvet X. Обзорная статья: Четырехкратная (сопутствующая) терапия без висмута для искоренения Helicobater pylori. Алимент. Pharmacol.Ther. 2011; 34: 604–617. DOI: 10.1111 / j.1365-2036.2011.04770.x. [PubMed] [CrossRef] [Google Scholar] 56. Essa A.S., Kramer J.R., Graham D.Y., Treiber G. Мета-анализ: «Сопутствующая терапия» с четырьмя лекарствами, тремя антибиотиками, без висмута по сравнению с тройной терапией для эрадикации Helicobacter pylori . Helicobacter. 2009. 14: 109–118. DOI: 10.1111 / j.1523-5378.2009.00671.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 57. Gisbert J.P., Calvet X. Последние данные о четырехкратной (сопутствующей) терапии без висмута для эрадикации Helicobacter pylori .Clin. Exp. Гастроэнтерол. 2012; 5: 23–34. [Бесплатная статья PMC] [PubMed] [Google Scholar] 58. Chen MJ, Chen CC, Chen YN, Chen CC, Fang YJ, Lin JT, Wu MS, Liou JM, Taiwan Gastrointestinal Disease Helicobacter Consortium Систематический обзор с метаанализом: сопутствующая терапия против тройной терапии для лечения первой линии Helicobacter pylori Инфекция. Являюсь. J. Gastroenterol. 2018; 113: 1444–1457. DOI: 10.1038 / s41395-018-0217-2. [PubMed] [CrossRef] [Google Scholar] 59. Молина-Инфанте Дж., Пазос-Пачеко К., Винагре-Родригес Г., Перес-Галлардо Б., Дуэнас-Садорнил К., Эрнандес-Алонсо М., Гонсалес-Гарсия Г., Матеос-Родригес Дж. М., Фернандес-Бермехо М., Гисберт Дж. П. Невисмут четырехкратная (сопутствующая) терапия: эмпирическая и индивидуализированная эффективность по сравнению со стандартной тройной терапией для чувствительных к кларитромицину Helicobacter pylori и по сравнению с последовательной терапией для устойчивых к кларитромицину штаммов. Helicobacter. 2012; 17: 269–276. DOI: 10.1111 / j.1523-5378.2012.00947.x. [PubMed] [CrossRef] [Google Scholar] 60.Jung Y.S., Park C.H., Park J.H., Nam E., Lee H.L. Эффективность эрадикационной терапии Helicobacter pylori в Корее: систематический обзор и сетевой метаанализ. Helicobacter. 2017; 22 DOI: 10.1111 / hel.12389. [PubMed] [CrossRef] [Google Scholar] 61. Чунг Дж. У., Хан Дж. П., Ким К. О., Ким С. Ю., Хонг С. Дж., Ким Т. Х., Ким С. В., Ким Дж. С., Ким Б. В., Банг Б. Десятидневная эмпирическая последовательная или сопутствующая терапия более эффективна, чем тройная терапия для эрадикации Helicobacter pylori : многоцентровое проспективное исследование.Копать землю. Печень. Дис. 2016; 48: 888–892. DOI: 10.1016 / j.dld.2016.05.005. [PubMed] [CrossRef] [Google Scholar] 62. Park S.M., Kim J.S., Kim B.W., Ji J.S., Choi H. Рандомизированное клиническое испытание, сравнивающее 10- или 14-дневную последовательную терапию и 10- или 14-дневную сопутствующую терапию для эмпирического лечения первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2017; 32: 589–594. DOI: 10.1111 / jgh.13510. [PubMed] [CrossRef] [Google Scholar] 63. Ким С. Ю., Ли С. В., Чхве Дж. В., Чон С. В., Хён Дж.J., Jung Y.K., Koo J.S., Yim H.J. Helicobacter pylori Показатели эрадикации сопутствующей и последовательной терапии в Корее. Helicobacter. 2017; 22: e12441. DOI: 10.1111 / hel.12441. [PubMed] [CrossRef] [Google Scholar] 64. Анг Т.Л., Фок К.М., Сонг М., Анг Д., Квек А.Б., Онг Дж., Тан Дж., Тео Е.К., Дхамодаран С. Десятидневная тройная терапия по сравнению с последовательной терапией по сравнению с сопутствующей терапией в качестве лечения первой линии для Helicobacter pylori инфекция. J. Gastroenterol. Гепатол. 2015; 30: 1134–1139.DOI: 10.1111 / jgh.12892. [PubMed] [CrossRef] [Google Scholar] 65. Макниколл А.Г., Марин А.С., Молина-Инфанте Дж., Кастро М., Баррио Дж., Дуконс Дж., Кальвет X., Коба К., Монторо М., Бори Ф. и др. Рандомизированное клиническое испытание, сравнивающее последовательную и сопутствующую терапию для эрадикации Helicobacter pylori в рутинной клинической практике. Кишечник. 2014; 63: 244–249. DOI: 10.1136 / gutjnl-2013-304820. [PubMed] [CrossRef] [Google Scholar] 66. Гатта Л., Вакил Н., Вайра Д., Скарпигнато С. Глобальные показатели эрадикации инфекции Helicobacter pylori : систематический обзор и метаанализ последовательной терапии.BMJ. 2013; 347: f4587. DOI: 10.1136 / bmj.f4587. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 67. Хе Л., Дэн Т., Луо Х. Мета-анализ последовательной, сопутствующей и гибридной терапии для эрадикации Helicobacter pylori . Междунар. Med. 2015; 54: 703–710. DOI: 10.2169 / internalmedicine.54.3442. [PubMed] [CrossRef] [Google Scholar] 68. Zullo A., Scaccianoce G., De Francesco V., Ruggiero V., D’Ambrosio P., Castorani L., Bonfrate L., Vannella L., Hassan C., Portincasa P. Сопутствующая, последовательная и гибридная терапия для ЧАС.pylori: пилотное исследование. Clin. Res. Гепатол. Гастроэнтерол. 2013; 37: 647–650. DOI: 10.1016 / j.clinre.2013.04.003. [PubMed] [CrossRef] [Google Scholar] 69. Ким С.Й., Ли С.В., Хён Дж.Дж., Юнг С.В., Ку Дж.С., Йим Х.Дж., Пак Дж.Дж., Чун Х.Дж., Чой Дж.Х. Сравнительное исследование степени эрадикации Helicobacter pylori с 5-дневной четырехкратной «сопутствующей» терапией и 7-дневной стандартной тройной терапией. J. Clin. Гастроэнтерол. 2013; 47: 21–24. DOI: 10.1097 / MCG.0b013e3182548ad4. [PubMed] [CrossRef] [Google Scholar] 70.Лим Дж. Х., Ли Д. Х., Чой К., Ли С. Т., Ким Н., Чон С. Х., Ким Дж. У., Хван Дж. Х., Пак Ю. С., Ли С. Х. и др. Клинические результаты двухнедельной последовательной и сопутствующей терапии для эрадикации Helicobacter pylori : рандомизированное пилотное исследование. Helicobacter. 2013. 18: 180–186. DOI: 10.1111 / hel.12034. [PubMed] [CrossRef] [Google Scholar] 71. Гевара Б., Когдилл А.Г. Helicobacter pylori : Обзор текущих стратегий диагностики и управления. Копать землю. Дис. Sci. 2020; 65: 1917–1931.DOI: 10.1007 / s10620-020-06193-7. [PubMed] [CrossRef] [Google Scholar] 72. Грэм Д.Ю., Ли Ю.С., Ву М.С. Рациональная терапия Helicobacter pylori : доказательная медицина, а не доказательная медицина. Clin. Гастроэнтерол. Гепатол. 2014; 12: 177–186. DOI: 10.1016 / j.cgh.2013.05.028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 73. Wang B., Wang Y.H., Lv Z.F., Xiong H.F., Wang H., Yang Y., Xie Y. Обзор: Эффективность и безопасность гибридной терапии для инфекции Helicobacter pylori : систематический обзор и метаанализ.Helicobacter. 2015; 20: 79–88. DOI: 10.1111 / hel.12180. [PubMed] [CrossRef] [Google Scholar] 74. Молина-Инфанте Дж., Романо М., Фернандес-Бермехо М., Федерико А., Гравина А.Г., Поццати Л., Гарсия-Абадиа Э., Винагре-Родригес Г., Мартинес-Алькала К., Эрнандес-Алонсо М. , и другие. Оптимизированная четырехкомпонентная терапия без висмута излечивает большинство пациентов с инфекцией Helicobacter pylori в популяциях с высокими показателями устойчивости к антибиотикам. Гастроэнтерология. 2013; 145: 121–128. DOI: 10.1053 / j.gastro.2013.03.050. [PubMed] [CrossRef] [Google Scholar] 75. Georgopoulos SD, Papastergiou V., Martinez-Gonzalez B., Xirouchakis E., Familias I., Sgouras D., Mentis A., Karatapanis S. Гибридная терапия как схема первой линии для эрадикации Helicobacter pylori при высокой устойчивости к кларитромицину область: перспективное открытое испытание. Анна. Гастроэнтерол. 2018; 31: 205–210. DOI: 10.20524 / aog.2017.0221. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Сонг З., Фу В., Чжоу Л. Цефуроксим, левофлоксацин, эзомепразол и висмут в качестве терапии первой линии для ликвидации Helicobacter pylori у пациентов с аллергией на пенициллин.BMC Gastroenterol. 2019; 19: 132. DOI: 10.1186 / s12876-019-1056-3. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 77. Auttajaroon J., Vilaichone R.K., Chotivitayatarakorn P., Mahachai V. Рабепразол, левофлоксацин, кларитромицин-MR и висмут один раз в день для эрадикации Helicobacter pylori : рандомизированное исследование продолжительностью 7 или 14 дней (исследование ONCE) Helicobacter. 2019; 24: e12615. DOI: 10.1111 / hel.12615. [PubMed] [CrossRef] [Google Scholar] 78. Ган Х.Ю., Пэн Т.Л., Хуан Ю.М., Су К.Х., Чжао Л.Л., Яо Л.Ю., Ян Р.Дж. Эффективность двух различных доз левофлоксацина в лечении инфекции Helicobacter pylori : проспективное одноцентровое рандомизированное клиническое испытание. Sci. Отчет 2018; 8: 9045. DOI: 10.1038 / s41598-018-27482-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 79. Ciccaglione AF, Di Giulio M., Di Lodovico S., Di Campli E., Cellini L., Marzio L. Бычий лактоферрин повышает эффективность тройной терапии на основе левофлоксацина в качестве лечения первой линии инфекции Helicobacter pylori : An in vitro и in vivo исследования.J. Antimicrob. Chemother. 2019; 74: 1069–1077. DOI: 10,1093 / jac / dky510. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 80. Басу П.П., Раяпуди К., Пакана Т., Шах Н.Дж., Кришнасвами Н., Флинн М. Рандомизированное исследование, сравнивающее левофлоксацин, омепразол, нитазоксанид и доксициклин с тройной терапией для ликвидации Helicobacter pylori . Являюсь. J. Gastroenterol. 2011; 106: 1970–1975. DOI: 10.1038 / ajg.2011.306. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 81. Фэллон К.А., Мосс С.Ф., Малфертхайнер П. Согласование последних рекомендаций по лечению Helicobacter pylori во времена повышения устойчивости к антибиотикам. Гастроэнтерология. 2019; 157: 44–53. DOI: 10.1053 / j.gastro.2019.04.011. [PubMed] [CrossRef] [Google Scholar] 82. Мори Х., Судзуки Х. Обновленная информация о хинолон-содержащих терапии спасения от инфекции Helicobacter pylori . Мир J. Gastroenterol. 2020; 26: 1733–1744. DOI: 10.3748 / wjg.v26.i15.1733. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83.Sue S., Shibata W., Sasaki T., Kaneko H., Irie K., Kondo M., Maeda S. Рандомизированное испытание тройной терапии третьей линии на основе вонопразана и ингибитора протонной помпы с ситафлоксацином для Helicobacter pylori . J. Gastroenterol. Гепатол. 2019; 34: 686–692. DOI: 10.1111 / jgh.14456. [PubMed] [CrossRef] [Google Scholar] 84. Судзуки Х., Нишизава Т., Мураока Х., Хиби Т. Ситафлоксацин и гареноксацин могут преодолеть устойчивость к антибиотикам Helicobacter pylori с мутацией gyrA.Противомикробный. Агенты. Chemother. 2009; 53: 1720–1721. DOI: 10.1128 / AAC.00049-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 85. Miftahussurur M., Waskito LA, Syam AF, Nusi IA, Siregar G., Richardo M., Bakry AF, Rezkitha YAA, Wibawa IDN, Yamaoka Y. Альтернативные схемы эрадикации инфекции Helicobacter pylori в регионах Индонезии с высоким содержанием метронидазола и левофлоксина сопротивление. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 345–358. DOI: 10.2147 / IDR.S187063. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 86.Мифтахуссурур М., Афтаб Х., Шреста П.К., Шарма Р.П., Субсомвонг П., Васкито Л.А., Духан Д., Фаузия К.А., Ямаока Ю. Эффективные терапевтические схемы в двух странах Южной Азии с высокой устойчивостью к основным антибиотикам Helicobacter pylori . Противомикробный. Оказывать сопротивление. Заразить. Контроль. 2019; 8:40. DOI: 10.1186 / s13756-019-0482-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 87. Гисберт Дж. П., Кальвет X. Обзорная статья: Рифабутин в лечении рефрактерной инфекции Helicobacter pylori .Алимент. Pharmacol. Ther. 2012; 35: 209–221. DOI: 10.1111 / j.1365-2036.2011.04937.x. [PubMed] [CrossRef] [Google Scholar] 88. Хип М., Бек Д., Байердорфер Э., Лен Н. Механизм устойчивости к рифампину и рифабутину в Helicobacter pylori . Противомикробный. Агенты. Chemother. 1999; 43: 1497–1499. DOI: 10.1128 / AAC.43.6.1497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 89. Рибалдоне Д.Г., Фагуни С., Астеджано М., Дураццо М., Моргандо А., Спруджевник Т., Джорданино К., Баронио М., Анжелис К.D., Saracco G.M. и др. Спасательная терапия на основе рифабутина для эрадикации Helicobacter pylori : долгосрочное проспективное исследование в большой когорте трудно поддающихся лечению пациентов. J. Clin. Med. 2019; 8: 199. DOI: 10,3390 / jcm8020199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 90. Akada J.K., Shirai M., Fujii K., Okita K., Nakazawa T. Активность новых производных рифамицина, KRM-1648 и KRM-1657, in vitro против Helicobacter pylori in vitro. Противомикробный. Агенты. Chemother. 1999; 43: 1072–1076.DOI: 10.1128 / AAC.43.5.1072. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 91. Кунин С.М. Антимикробная активность рифабутина. Clin. Заразить. Дис. 1996; 22 (Дополнение 1: S3-13): 30. DOI: 10.1093 / Clinids / 22.Supplement_1.S3. [PubMed] [CrossRef] [Google Scholar] 92. Сунг Дж., Ким Н., Пак И. Х., Хван Ю. Дж., Квон С., На Г., Чой Дж. Ю., Кан Дж. Б., Ким Х. Р., Ким Дж. В. и др. Спасательная терапия четвертой и пятой линий на основе рифабутина у пациентов с неэффективностью эрадикации Helicobacter pylori . Корейский язык.J. Gastroenterol. 2017; 69: 109–118. DOI: 10.4166 / kjg.2017.69.2.109. [PubMed] [CrossRef] [Google Scholar] 93. Грэм Д.Ю., Ханаан Ю., Махер Дж., Винер Г., Халтен К.Г., Калфус И.Н. Тройная терапия на основе рифабутина (RHB-105) для ликвидации Helicobacter pylori : двойное слепое рандомизированное контролируемое исследование. Анна. Междунар. Med. 2020; 172: 795–802. DOI: 10.7326 / M19-3734. [PubMed] [CrossRef] [Google Scholar] 94. Бок Х., Куп Х., Лен Н., Хип М. Тройная терапия на основе рифабутина после неудачной эрадикационной терапии Helicobacter pylori : предварительный опыт.J. Clin. Гастроэнтерол. 2000. 31: 222–225. DOI: 10.1097 / 00004836-200010000-00007. [PubMed] [CrossRef] [Google Scholar] 95. Сузуки С., Сузуки Х., Нисидзава Т., Канеко Ф., Отани С., Мураока Х., Сайто Ю., Кобаяши И., Хиби Т. Прошлое дозирование рифампицина определяет устойчивость к рифабутину Helicobacter pylori . Пищеварение. 2009; 79: 1–4. DOI: 10,1159 / 0001. [PubMed] [CrossRef] [Google Scholar] 96. Скотт Дж. Я., Мансон К. Б., Маркус Э. А., Ламбрехт Н. В., Сакс Г. Селективность связывания фонопразана (TAK-438) с H +, K + -АТФазой желудка.Алимент. Pharmacol. Ther. 2015; 42: 1315–1326. DOI: 10.1111 / apt.13414. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 97. Park J.Y., Kim J.G. [New Helicobacter pylori Eradication Therapies] Корейский. J. Gastroenterol. 2018; 72: 237–244. DOI: 10.4166 / kjg.2018.72.5.237. [PubMed] [CrossRef] [Google Scholar] 99. Грэм Д.Ю., Дор М.П. Обновленная информация об использовании вонопразана: конкурентного блокатора кислоты. Гастроэнтерология. 2018; 154: 462–466. DOI: 10.1053 / j.gastro.2018.01.018. [PubMed] [CrossRef] [Google Scholar] 100.Лю Q.J., Пу Q.H., Чжун X.F., Чжан Дж. Эффективность и безопасность тройной терапии на основе вонопразана и ингибитора протонной помпы для искоренения Helicobacter pylori : метаанализ рандомизированных клинических испытаний. Биомед. Res. Int. 2019; 3: 1–8. DOI: 10.1155 / 2019/9781212. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 101. Murakami K., Sakurai Y., Shiino M., Funao N., Nishimura A., Asaka M. Vonoprazan, новый калий-конкурентный блокатор кислоты, в качестве компонента тройной терапии первой и второй линии против Helicobacter pylori Эрадикация : рандомизированное двойное слепое исследование фазы III.Кишечник. 2016; 65: 1439–1446. DOI: 10.1136 / gutjnl-2015-311304. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 102. Ли М., Осима Т., Хорикава Т., Тозава К., Томита Т., Фукуи Х., Ватари Дж., Мива Х. Систематический обзор с метаанализом: вонопразан, мощный блокатор кислоты, превосходит протонный ингибиторы помпы для уничтожения устойчивых к кларитромицину штаммов Helicobacter pylori . Helicobacter. 2018; 23: e12495. DOI: 10.1111 / hel.12495. [PubMed] [CrossRef] [Google Scholar] 103. Танабэ Х., Yoshino K., Ando K., Nomura Y., Ohta K., Satoh K., Ichiishi E., Ishizuka A., Otake T., Kohgo Y., et al. Тройная терапия на основе вонопразана не уступает тройной терапии на основе ингибиторов протонной помпы на основе чувствительности для эрадикации Helicobacter pylori . Анна. Clin. Microbiol Antimicrob. 2018; 17:29. DOI: 10.1186 / s12941-018-0281-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 104. Судзуки С., Готода Т., Кусано К., Икехара Х., Итидзима Р., Охьяучи М., Ито Х., Кавамура М., Огата Ю., Отака М. и др. Семидневная двойная терапия фонопразаном и низкими дозами амоксициллина в качестве терапии первой линии Helicobacter pylori : многоцентровое рандомизированное исследование в Японии. Кишечник. 2020; 69: 1019–1026. DOI: 10.1136 / gutjnl-2019-319954. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 105. Ким Б.Дж., Ли Х., Ли Ю.С., Чон С.В., Ким Г.Х., Ким Х.С., Сунг Дж.К., Ли Д.Х., Ким Х.У., Пак М.И. и др. Десятидневная сопутствующая, 10-дневная последовательная и 7-дневная тройная терапия в качестве лечения первой линии для инфекции Helicobacter pylori : общенациональное рандомизированное исследование в Корее.Кишечник. Печень. 2019; 13: 531–540. DOI: 10.5009 / gnl19136. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 106. Zhou Y., Ye Z., Wang Y., Zhang Y., Tang Z., Yan W., Jiang Y., Huang Y. Сравнение четырех различных схем лечения против Helicobacter pylori в качестве лечения первой линии: перспектива , перекрестное, сравнительное, открытое испытание на китайских детях. Helicobacter. 2020; 25: e12679. DOI: 10.1111 / hel.12679. [PubMed] [CrossRef] [Google Scholar] 107. Банг К.С., Лим Х., Чон Х.М., Шин В.Г., Чой Дж. Х., Со Дж. С., Кан Х. С., Ян Й. Дж., Хонг Дж. Т., Шин С. П. и др. Амоксициллин или тетрациклин в висмутсодержащей четверной терапии в качестве лечения первой линии для инфекции Helicobacter pylori . Кишечные микробы. 2020; 11: 1314–1323. DOI: 10.1080 / 194.2020.1754118. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 108. Романо М., Гравина А.Г., Нардоне Г., Федерико А., Даллио М., Марторано М., Мучерино К., Ромити А., Аваллоне Л., Граната Л. и др. Четырехкратная терапия без висмута и висмута, основанная на предыдущем воздействии кларитромицина, столь же эффективна и безопасна в области высокой устойчивости к кларитромицину: исследование в реальной жизни.Helicobacter. 2020; 25: e12694. DOI: 10.1111 / hel.12694. [PubMed] [CrossRef] [Google Scholar] 109. Tai W.C., Liang C.M., Bi K.W., Kuo C.M., Lu L..S., Wu C.K., Yang S.C., Kuo Y.H., Lee C.H., Huang C.F. и др. Сравнение четырехкомпонентной (сопутствующей) терапии на основе декслансопразола с модифицированным высвобождением и на основе лансопразола для эрадикации первой линии Helicobacter pylori : проспективное рандомизированное исследование. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 2923–2931. DOI: 10.2147 / IDR.S213998. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 110.Hsu P.I., Tsay F.W., Kao J.Y., Peng N.J., Tsai K.W., Tsai T.J., Kuo C.H., Kao S.S., Wang H.M., Chen Y.H. и др. Эквивалентная эффективность обратного гибрида и сопутствующей терапии в лечении первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2020 doi: 10.1111 / jgh.15034. [PubMed] [CrossRef] [Google Scholar] 111. Myint N., Zaw T.T., Sain K., Waiyan S., Danta M., Cooper D., Aung N.M., Kyi M.M., Hanson J. Sequential Helicobacter pylori эрадикационная терапия в Мьянме; рандомизированное клиническое испытание эффективности и переносимости.J. Gastroenterol. Гепатол. 2020; 35: 617–623. DOI: 10.1111 / jgh.14942. [PubMed] [CrossRef] [Google Scholar] 112. Зулло А., Фиорини Г., Скаччаноче Г., Портинкаса П., Де Франческо В., Вассалло Р., Урбан Ф., Моника Ф., Могаверо Г., Амато А. и др. Последовательная терапия для эрадикации первой линии Helicobacter pylori : 10- или 14-дневный режим? J. Gastrointestin. Печень. Дис. 2019; 28: 11–14. DOI: 10.15403 / jgld.2014.1121.281.hpy. [PubMed] [CrossRef] [Google Scholar] 113. Цай Ф.В., Ву Д.С., Ю Х.С., Kao S.S., Lin K.H., Cheng J.S., Wang H.M., Chen W.C., Sun W.C., Tsai K.W. и др. Рандомизированное контролируемое исследование показывает, что как 14-дневная гибридная, так и четырехкомпонентная терапия висмутом излечивают большинство пациентов с инфекцией Helicobacter pylori в группах населения со средней устойчивостью к антибиотикам. Противомикробный. Агенты. Chemother. 2017; 61: e00140-17. DOI: 10.1128 / AAC.00140-17. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 114. Нисида Т., Цудзи Ю., Окамото А., Томита Р., Хигаки Ю., Осуги Н., Сугимото А., Такахаши К., Мукаи К., Накамацу Д. и др. Лекарство с тройным лекарством в блистерной упаковке с вонопразаном улучшает эрадикацию первой линии Helicobacter pylori у пожилых пациентов: когортное исследование с ретроспективной оценкой склонности. Пищеварение. 2019: 1–7. DOI: 10,1159 / 000501608. [PubMed] [CrossRef] [Google Scholar] 115. Луо Л., Хуанг Ю., Лян Х., Цзи Ю., Ю. Л., Лу Х. Терапия на основе чувствительности для Helicobacter pylori -инфицированных пациентов с аллергией на пенициллин: проспективное клиническое испытание терапии первой линии и терапии спасения .Helicobacter. 2020; 25: e12699. DOI: 10.1111 / hel.12699. [PubMed] [CrossRef] [Google Scholar] 116. Kim SG, Jung HK, Lee HL, Jang JY, Lee H., Kim CG, Shin WG, Shin ES, Lee YC, Korean College of Helicobacter and Upper Gastrointestinal Research Guidelines для диагностики и лечения инфекции Helicobacter pylori в Корее , Редакция 2013 г. J. Gastroenterol. Гепатол. 2014; 29: 1371–1386. DOI: 10.1111 / jgh.12607. [PubMed] [CrossRef] [Google Scholar] 117. Като М., Ота Х., Окуда М., Кикучи С., Сато К., Шимояма Т., Судзуки Х., Ханда О., Фурута Т., Мабе К. и др. Руководство по лечению инфекции Helicobacter pylori в Японии: пересмотренное издание 2016 г. Helicobacter. 2019; 24: e12597. DOI: 10.1111 / hel.12597. [PubMed] [CrossRef] [Google Scholar]
Лучшая стратегия ликвидации Helicobacter pylori в эпоху устойчивости к антибиотикам
Антибиотики (Базель). 2020 Aug; 9 (8): 436.
Су Ён Ким
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; мок.revan @ 2121ezeerb
Джун-Вон Чунг
2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдон-даэро 774beon-gil, Намдонг-гу, Инчхон 21565, Корея
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу Университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; moc.revan@2121ezeerb2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдонг-даэро 774beon-gil, Namdong-gu, Инчхон 21565, Корея
Поступило 30 июня 2020 г .; Принята в печать 21 июля 2020 г.
Лицензиат MDPI, Базель, Швейцария. Эта статья — статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution (CC BY) (http://creativecommons.org/licenses/by/4.0/). Эта статья цитировалась другими статьями в PMC. .Abstract
Устойчивость к антибиотикам является основной причиной неэффективности лечения Helicobacter pylori , а учащение случаев устойчивости к антибиотикам является проблемой для клиницистов. Особую проблему представляет устойчивость к кларитромицину и метронидазолу.Стандартная тройная терапия (ингибитор протонной помпы, амоксициллин и кларитромицин) больше не подходит в качестве лечения первой линии в большинстве регионов. Недавние рекомендации по лечению инфекции H. pylori
рекомендуют четырехкратную схему лечения (висмут или невисмут) в качестве терапии первой линии. Эта стратегия лечения эффективна для областей с высокой резистентностью к кларитромицину или метронидазолу, но частота резистентности неизбежно возрастает в результате длительной терапии несколькими антибиотиками.Новая терапия на основе калий-конкурентных блокаторов кислоты может быть эффективной, но данные ограничены. Индивидуальная терапия, основанная на результатах теста на чувствительность к противомикробным препаратам, является идеальным вариантом. В этом обзоре обсуждались текущие важные схемы лечения H. pylori и оптимальная стратегия эрадикации H. pylori .Ключевые слова: Helicobacter pylori , устойчивость к антибиотикам, эрадикация
1. Введение
Helicobacter pylori — грамотрицательная, жгутиковая, спиралевидная бактерия, проникающая в слизистую оболочку верхнего отдела желудочно-кишечного тракта [1] , 2].Он вызывает пептические язвы, рак желудка и другие желудочные заболевания [3,4] и составляет 25% всех злокачественных новообразований, связанных с инфекциями; это также связано с повышенным риском рака желудочно-кишечного тракта [5]. Искоренение H. pylori облегчает язвенную болезнь и снижает риск рака желудка [6,7]. В глобальном масштабе рекомендации по лечению H. pylori постепенно меняются, а показания расширяются [4,8,9,10]. Кроме того, с экономическим развитием многих развивающихся стран и увеличением старения населения количество людей, получающих H.pylori увеличивается.
В 1990-х годах тройная терапия, состоящая из ингибитора протонной помпы (ИПП), кларитромицина и амоксициллина, была введена для искоренения инфекции H. pylori и в настоящее время является стандартом во всем мире [11,12]. С тех пор уровень искоренения тройной терапии во многих регионах заметно снизился [13,14]. Причины этого снижения включают бактериальные факторы, повторное инфицирование, генетический полиморфизм CYP2C19 и соблюдение пациентом режима лечения [15].Устойчивость к антибиотикам является наиболее важной причиной неудач лечения H. pylori [13,16]. Резистентность к кларитромицину H. pylori особенно серьезна; Схемы, содержащие кларитромицин, больше не подходят из-за степени эрадикации <80% [14,17]. Уровень устойчивости к метронидазолу и хинолонам (которые в основном используются в качестве схем второго или третьего ряда) во всем мире составляет> 15% [14,16]. Поскольку количество антибиотиков, подходящих для эрадикации H. pylori , ограничено (кларитромицин, амоксициллин, метронидазол, левофлоксацин, тетрациклин и рифабутин), повышение устойчивости к антибиотикам является серьезной проблемой.Следовательно, исключения кларитромицина недостаточно для предотвращения устойчивости к антибиотикам H. pylori .
Текущие руководства подчеркивают важность местной распространенности устойчивости к антибиотикам при выборе подходящей схемы лечения H. pylori [4,9,10]. В регионах с высокой устойчивостью к определенным антибиотикам успех лечения можно улучшить, отказавшись от использования таких антибиотиков. Однако, хотя новая комбинация антибиотиков может повысить скорость эрадикации, она может вызвать резистентность.Правительство Тайваня ограничило использование противомикробных препаратов, что привело к низкому уровню первичной устойчивости к кларитромицину и метронидазолу у H. pylori [18]. Однако частота первичной устойчивости к левофлоксацину увеличилась с 4,9% в 2000–2007 гг. До 13,4% в 2011–2012 гг. [18]. Кроме того, использование нескольких антибиотиков увеличивает частоту осложнений [4]. Поэтому важно определить оптимальную стратегию эрадикации H. pylori в соответствии с результатами теста на антибактериальную чувствительность (AST).Однако возможность ложноотрицательных результатов и возможность применения во всех медицинских учреждениях являются проблемой [19,20]. Мы рассмотрели наиболее важные схемы лечения против H. pylori , которые преодолевают устойчивость к антибиотикам, и стратегии, которые можно применять на практике.
2.
H. pylori Лечение на основе результатов ASTБактериальный посев обычно проводится перед выбором антибиотика, но посев H. pylori сложен и требует много времени. Исследование чувствительности к кларитромицину H.pylori улучшает скорость эрадикации [21,22]. Герритс и др. с помощью полимеразной цепной реакции (ПЦР) показали, что мутации A2142G и A2143G в 23S рРНК связаны с устойчивостью к антибиотикам [22]. ПЦР сравнительно прост и экономичен [21]. Следовательно, для H. pylori лечение на основе AST, такое как диагностический тест на устойчивость к кларитромицину, является полезным. Однако в некоторых случаях уровень эрадикации составляет <100%. Это связано с тем, что точечные мутации, отличные от A2142G или A2143G, приводят к ненадежным результатам, например.g., A2142C, A2115G, G2142T, A2142T и T2182C [23,24]. Кроме того, распространение мутаций отличается географически. Мутация A2142C встречается <10% в США и Европе, но не зарегистрирована в Японии [25,26,27,28]. В Гонконге частота мутации A2144G выше, чем в других регионах [29]. Различное распределение этих мутаций, вероятно, влияет на скорость эрадикации.
Терапия H. pylori , основанная на результатах AST, значительно улучшает скорость эрадикации.Однако, в отличие от других схем, мало исследований оценивали схемы первого ряда на основе АСТ. Уровень искоренения намерения лечить (ITT) для схемы первого ряда составляет> 90% [30,31,32]. В Южной Корее индивидуализированная терапия первой линии на основе ПЦР превосходит стандартную тройную терапию (STT; амоксициллин, кларитромицин и ИПП) [30,31]. В греческом исследовании тройная терапия на основе генотипической резистентности (определение чувствительности к кларитромицину и левофлоксацину с помощью анализа GenoType HelicoDR) позволила достичь высокого уровня H.pylori (90,2% по ITT и 97,8% по протоколу (PP) анализа) [32]. Кроме того, тройные схемы первой линии под контролем АСТ приводят к эрадикации> 90% у пациентов с H. pylori , устойчивым к двум антибиотикам [33]. Поскольку частота полирезистентности H. pylori увеличивается, это обнадеживающее открытие. Схемы первой линии эрадикации H. pylori на основе культивирования демонстрируют превосходный терапевтический эффект даже в регионах с высоким уровнем устойчивости к противомикробным препаратам [34].Общие показатели устойчивости к амоксициллину, кларитромицину, метронидазолу и моксифлоксацину составляют 6,7%, 31,0%, 41,8% и 39,2% соответственно. Однако уровень эрадикации составляет 93,1% (ITT) и 100,0% (PP) [34]. Chen et al. сообщили, что управляемый по чувствительности модифицированный четырехкратный режим висмута первой линии для H. pylori в регионе с высокой степенью устойчивости к противомикробным препаратам имел высокий уровень эрадикации [35].
Показатель успеха схем второго ряда / спасения под контролем AST ниже, чем у схем первого ряда.Уровень эрадикации низкий (68%), несмотря на тестирование чувствительности для лечения спасения [36]. Аналогичным образом, в Соединенных Штатах терапия с культуральным контролем показала 60% -ный успех у пациентов, у которых не удалось по крайней мере три лечения [37]. Даже если посев определяет чувствительность к кларитромицину, повторный анализ кларитромицина после неудачи лечения не рекомендуется [38]. Следовательно, одна только терапия под контролем АСТ не может достичь требуемой скорости эрадикации. Liou et al. показали, что терапия с учетом генотипа не была значительно более эффективной, чем эмпирическая терапия для стратегии спасательной терапии (78.0% против 72,2%, p = 0,170) [39]. Следовательно, соответствующая эмпирическая терапия является альтернативой индивидуализированной генотипической терапии рефрактерной инфекции H. pylori .
3. Четырехкратная терапия висмутом
Четырехкратная терапия висмутом (BQT) состоит из висмута, PPI, метронидазола и тетрациклина. Он рекомендован как схема первой линии Торонтским консенсусом, Маастрихтским V / Флорентийским консенсусом и рекомендациями Американского колледжа гастроэнтерологии (ACG) [4,9,10].На режим BQT не влияет резистентность к кларитромицину. Согласно сетевому метаанализу, BQT в течение 10 или 14 дней превосходит STT в течение 7 дней [40]. Более того, BQT очень эффективен в качестве эмпирической схемы первого ряда (уровень эрадикации PP и ITT составляет 98,8% и 92,7% соответственно) [41]. Рандомизированное контролируемое исследование (РКИ) на Тайване показало, что уровень эрадикации у пациентов, получавших BQT, составил 96,0%, хотя частота нежелательных явлений составила 47,7% [42]. BQT оказался высокоэффективным в качестве схемы первого ряда для H.pylori в проспективном исследовании в Испании (94,4% (ITT) и 96,2% (PP)) [43]. BQT имеет отличную скорость эрадикации H. pylori , но комплаентность пациента может быть снижена из-за большого количества лекарств. Кроме того, BQT вводят четыре раза в день, что также может снизить комплаентность пациента. Чтобы преодолеть это, были введены схемы приема BQT два раза в день, и исследования в Южной Корее продемонстрировали их эффективность [44,45]. Kim et al. продемонстрировали, что два раза в день BQT в течение 1 недели был так же эффективен и безопасен, как традиционный четырехкратный ежедневный BQT (93.9% против 92,9%) [45]. Кроме того, большинство пациентов демонстрируют хорошую комплаентность, а уровень эрадикации BQT два раза в день высок (88,2% (ITT) и 98,4% (PP)) [44]. Разработана единая капсула, содержащая висмут, метронидазол и тетрациклин. Xie et al. показали, что терапия BQT одной капсулой была эффективной для эрадикации H. pylori и хорошо переносилась (86,5% (ITT) и 94,6% (PP)) [46]. В итальянском исследовании однокапсульная терапия BQT позволила достичь уровня эрадикации 91% (ITT) и 97% (PP) [47].Согласно метаанализу, при терапии BQT с одной капсулой первого и второго ряда уровень эрадикации приближался к 90%. Даже это применимо, независимо от типа и дозы ИПП, у пациентов со штаммом, резистентным к антибиотикам, и у тех, кто ранее лечился кларитромицином [48]. При 7-дневной схеме лечения BQT второго ряда уровень эрадикации составляет 93,6% (PP). Скорость эрадикации 7-дневного BQT значительно выше, чем у 14-дневного моксифлоксацина, содержащего тройной режим (93,6% против 73,8% (PP), p <0.001) [49].
Неясно, улучшится ли скорость эрадикации при увеличении периода лечения с 7 до 14 дней. Маастрихтский V / Флорентийский консенсус рекомендует прием препарата в течение не менее 10 дней [10]. Сообщается, что уровень устойчивости к тетрациклину во всем мире низкий [50,51]. Следовательно, устойчивость к метронидазолу является основным фактором успеха эрадикации H. pylori . Устойчивость к метронидазолу можно преодолеть путем увеличения частоты, количества и продолжительности приема, поэтому лечение в течение ≥10 дней рекомендуется в регионах с высокой степенью устойчивости к метронидазолу [52].
BQT показал отличные результаты в различных исследованиях, и сфера его применения постепенно расширяется. Кроме того, BQT можно относительно безопасно применять у пациентов с аллергией на пенициллин [4]. Сообщается, что BQT имеет более высокий уровень нежелательных явлений, чем STT, но схожий уровень соблюдения пациентом режима лечения [53,54]. Однако, поскольку показания BQT расширяются в качестве лечения первой линии, также возникают опасения. Количество схем второго ряда, которые можно применять, значительно сокращается, когда эрадикация с помощью BQT не дает результатов по первой линии.Кроме того, в будущем может повыситься уровень устойчивости к тетрациклину, который в настоящее время является относительно низким. Для решения этой проблемы в будущем необходимы различные исследования.
4. Сопутствующая терапия
Рекомендуется одновременное введение трех антибиотиков (кларитромицин, метронидазол или нитроимидазол и амоксициллин) и ИПП в течение 10–14 дней [4,9,10]. Несколько метаанализов показали, что сопутствующая терапия превосходит STT [55,56,57].Кроме того, недавний метаанализ показал, что сопутствующая терапия в течение 5 или 10 дней превосходила STT в течение 5, 7 или 10 дней [58]. Испанское исследование продемонстрировало, что сопутствующая терапия была значительно лучше, чем тройная терапия (92% против 70% (ITT), p = 0,02 и 92% против 74% (PP), p = 0,05) и эрадикация Скорость сопутствующей терапии была выше, чем у последовательной терапии устойчивых к антибиотикам штаммов [59]. Кроме того, сопутствующая терапия и BQT в качестве схем первого ряда показали сходные результаты H.pylori в анализах PP (97,7% против 96,2%, p = 0,605) и ITT (98,0% против 94,4%, p = 0,346) [43]. Более того, сетевой метаанализ показал, что сопутствующая терапия имеет более высокую эффективность, чем несколько других схем [40,60].
Сопутствующая терапия предпочтительнее последовательной терапии (ИПП и амоксициллин в течение 5 дней, затем ИПП, кларитромицин и тинидазол в течение еще 5 дней), потому что это проще. Существуют разногласия по поводу того, превосходит ли сопутствующая терапия над последовательной терапией [61,62,63,64,65].В испанском РКИ сопутствующая терапия была незначительно лучше (~ 5%) по сравнению с последовательной терапией (87% против 81% (ITT), p = 0,15; 91% против 86% (PP), p = 0,131) [65]. Кроме того, два метаанализа не выявили значительной разницы в скорости эрадикации между сопутствующей терапией и последовательной терапией [66,67].
Маастрихтский / Флорентийский консенсус не рекомендует последовательную терапию, в отличие от предыдущих руководств [10]. Это связано с тем, что последовательная терапия имеет более низкий уровень эрадикации, чем сопутствующая терапия в случаях резистентности к кларитромицину и чувствительности к метронидазолу H.pylori . И наоборот, когда H. pylori чувствителен к кларитромицину и устойчив к метронидазолу, последовательная терапия показывает более низкий уровень эрадикации, чем STT [10]. Увеличение дозы или продолжительности лечения метронидазолом может привести к эрадикации метронидазол-резистентного H. pylori . Скорость эрадикации при последовательной терапии невысока, поскольку период приема метронидазола составляет всего 5 дней.
Сопутствующая терапия имеет несколько ограничений, таких как более высокая частота нежелательных явлений, чем последовательная терапия [68].Повышенная частота осложнений может повлиять на соблюдение режима лечения H. pylori [69,70]. Хотя частота нежелательных явлений относительно высока, период лечения составляет менее 2 недель, поэтому большинство пациентов завершают курс лечения. Кроме того, есть опасения, что устойчивость к антибиотикам может повыситься из-за чрезмерного воздействия ненужных антибиотиков [71]. Наконец, эффекты сопутствующей терапии ниже у H . pylori, устойчивы как к кларитромицину, так и к метронидазолу [72].
5. Гибридная терапия
Гибридная терапия — это комбинация последовательной и сопутствующей терапии. Гибридная терапия включает ИПП и амоксициллин в течение 7 дней, затем ИПП, амоксициллин, кларитромицин и метронидазол в течение 7 дней [4]. Хотя Торонтский консенсус и Маастрихтский / Флорентийский консенсус не рекомендуют гибридную терапию, в клинических рекомендациях ACG рекомендуется использовать ее в качестве лечения первой линии у пациентов без предварительного воздействия макролидов в регионах с низким уровнем устойчивости к кларитромицину.Несколько метаанализов сообщили об эффективности и переносимости гибридной терапии [40,67,73]. Wang et al. продемонстрировали, что гибридная терапия была альтернативой сопутствующей или последовательной терапии (уровни эрадикации ITT гибридной, сопутствующей и последовательной терапии составили 88,6%, 86,3% и 84,7% соответственно; частота эрадикации PP составила 92,1%, 92,5% и 87,5%. ) [73]. Кроме того, нет значительных различий в переносимости или комплаентности между гибридной терапией и STT, последовательными или сопутствующими схемами [40,67,73].
В проспективном многоцентровом исследовании гибридная терапия вылечила> 90% пациентов с инфекцией H. pylori в регионах с высокими показателями устойчивости к кларитромицину и метронидазолу; это похоже на скорость эрадикации сопутствующей терапии [74]. Кроме того, комплаентность к гибридной терапии выше, чем к сопутствующей терапии (98,8% против 95,2%, p = 0,05). Однако скорость искоренения гибридной терапии значительно ниже для H.pylori . В проспективном исследовании частота эрадикации у пациентов с двойной устойчивостью к антибиотикам (кларитромицину и метронидазолу) была заметно снижена (50%) по сравнению с пациентами с резистентностью только к кларитромицину (91,4%) или метронидазолу (90,5%) [75].
6. Терапия на основе левофлоксацина
Левофлоксацин активен в отношении большого спектра различных бактерий, и в некоторых исследованиях левофлоксацин используется в качестве средства первой линии лечения инфекции H. pylori [15]. Проспективное исследование в Китае показало, что цефуроксим, левофлоксацин, ИПП и висмут в качестве терапии первой линии позволили достичь H.pylori составляет 97,2% случаев чувствительности к левофлоксацину и 84,0% случаев резистентности к левофлоксацину [76]. Однако в случаях устойчивости к цефуроксиму и левофлоксацину уровень эрадикации составил 0%. 14- и 7-дневные режимы дозирования левофлоксацина (левофлоксацин, кларитромицин, рабепразол и висмут) один раз в сутки показали уровень эрадикации 94% и 84% соответственно [77]. Gan et al. сравнили эффективность различных доз левофлоксацина для эрадикации H.pylori [78]. Показатели эрадикации в группах, получавших один и два раза в день, составили 77,5% и 79,5% (ITT) и 82,9% и 86,4% (PP), соответственно [78]. Нет значительных различий в степени искоренения или соблюдения режима лечения. Бычий лактоферрин усиливает эффективность схем первой линии на основе левофлоксацина при инфекции H. pylori [79]. Успешная эрадикация составляет 96,1% для эзомепразола / амоксициллина / левофлоксацина / бычьего лактоферрина и 75% для эзомепразола / амоксициллина / левофлоксацина [79].Режим LOAD (левофлоксацин, омепразол, нитазоксанид и доксициклин) был введен недавно [71]. Basu et al. сообщили, что уровень эрадикации LOAD составил 89,4% по сравнению с 73,3% для STT ( p <0,05) [80].
Левофлоксацин представляет собой хинолон и широко используется во всем мире, например, при пневмонии, инфекции мочевыводящих путей, туберкулезе и H. pylori . Таким образом, многие пациенты в анамнезе принимали левофлоксацин. В большинстве руководств рекомендуется применять схемы на основе левофлоксацина в качестве экстренной помощи, а не в качестве терапии первой линии [81].Клинические рекомендации ACG слабо рекомендуют тройной (амоксициллин, левофлоксацин и ИПП), последовательный (5-7 дней ИПП и амоксициллин, затем 5-7 дней ИПП, нитроимидазол и левофлоксацин) или четырехкратный (амоксициллин, левофлоксацин и ИПП). ИПП, левофлоксацин, доксициклин и нитазоксанид в течение 7 или 10 дней) по схемам первого ряда [4].
Ситафлоксацин представляет собой фторхинолон четвертого поколения и обладает высокой активностью против штаммов gyr A с положительной мутацией H. pylori [82].Ситафлоксацин в основном используется с амоксициллином или метронидазолом в качестве экстренной помощи, а не терапии первой линии. Сообщается, что схемы третьей линии, содержащие ситафлоксацин, эффективны для эрадикации H. pylori (75,8% (ITT) и 83,3% (PP)) [83]. Фторхинолоны четвертого поколения, такие как ситафлоксацин и гареноксацин, могут преодолеть устойчивость к хинолонам H. pylori [84,85]. Среди 100 штаммов с высокими показателями устойчивости к кларитромицину, метронидазолу и левофлоксацину> 95% чувствительны к ситафлоксацину [86].Следует оценить эффективность схем, содержащих ситафлоксацин или гареноксацин, против gyr A с положительной мутацией H. pylori .
7. Терапия на основе рифабутина
Рифабутин — это производное рифамицина, структурно сходное с рифампицином (противотуберкулезным препаратом). Он в основном используется при атипичном туберкулезе, таком как Mycobacterium avium -intracellulare и M. tuberculosis , устойчивых к рифампицину [87]. Рифабутин подавляет синтез белка путем ингибирования бета-субъединицы ДНК-зависимой РНК-полимеразы Helicobacter , которая кодируется rpoB .Следовательно, мутация rpoB придает устойчивость к рифабутину [88]. Все существующие руководящие принципы предполагают, что схемы на основе рифабутина следует рассматривать только как терапию «спасения» при эрадикации H. pylori [81]. Согласно метаанализу, эффективность лечения на основе рифабутина второй, третьей и четвертой / пятой линий составляет 79%, 66% и 70% соответственно [87]. В итальянском исследовании тройная терапия на основе рифабутина (рифабутин, амоксициллин и ИПП) в течение 14 дней позволила достичь скорости эрадикации 72.7% (PP) и 71,5% (ITT) у пациентов, у которых эрадикация H. pylori оказалась неэффективной после лечения традиционными антибиотиками [89]. Рифабутин не обладает такой же устойчивостью к антибиотикам, как кларитромицин и амоксициллин, а также является жирорастворимым и легко всасывается после перорального приема [88, 90]. Кроме того, рифабутин стабилен в широком диапазоне значений pH и не разлагается желудочной кислотой, а уровень устойчивости у H. pylori низкий, поскольку он редко используется в клинических условиях [87,91]. Следовательно, схемы на основе рифабутина важны для спасательной терапии.Однако другое исследование показало, что уровень искоренения терапии на основе рифабутина был невысоким: 50,0% в анализе ITT и 54,5% в анализе PP [92]. Поскольку есть некоторые части, которые не достигают стабильной скорости эрадикации в качестве спасательной терапии, можно считать, что необходимы соответствующие исследования.
На сегодняшний день большинство исследований схем на основе рифабутина сосредоточено на спасательной терапии. Недавно Graham et al. показали, что тройная схема на основе рифабутина (амоксициллин, рифабутин и ИПП) имела более высокий уровень эрадикации, чем амоксициллин плюс ИПП в качестве эмпирического лечения первой линии H.pylori (83,8% против 57,7%, p <0,001) [93]. Это говорит о том, что рифабутин является революционным препаратом первой линии в эпоху устойчивости к антибиотикам. Однако он дороже других антибиотиков. Кроме того, он может вызвать устойчивость к режиму лечения туберкулеза [94]. Более того, поскольку использование рифампицина способствует точечной мутации rpoB и увеличивает минимальную ингибирующую концентрацию (МИК) рифабутина, перед назначением рифабутина необходимо определить предшествующее лечение рифампицином [95].Наконец, рифабутин имеет небольшой риск миелотоксичности [87].
8. Терапия на основе калий-конкурентных кислотных блокаторов
Калий-конкурентные кислотные блокаторы (P-CAB) — это ингибитор секреции кислоты желудочного сока, с более быстрым началом и более длительным действием подавления кислоты, и более эффективен, чем ИПП. [96,97]. Кроме того, P-CAB не требует активации желудочной кислотой, поэтому его можно принимать независимо от времени приема пищи. В обращении H . pylori, pH желудка должен поддерживаться выше определенного уровня, чтобы активировать антибиотик [98].P-CAB ингибирует опосредованную H + и K + -АТФазу секрецию кислоты желудочного сока и является кислотоустойчивым и менее подвержен влиянию системы CYP2C19, чем ИПП [71,99]. Поскольку ИПП имеют короткую продолжительность действия и на их эффективность влияют различные подтипы цитохрома Р450 (ИПП в основном метаболизируются CYP2C19 и CYP3A4), внимание привлекла новая схема лечения против H. pylori , содержащая PCAB [99,100]. Вонопразан в настоящее время продается в Японии, продвигая исследования P-CAB для H.pylori лечение.
По данным многоцентрового РКИ в Японии, частота эрадикации первой линии тройной терапии на основе фонопразана (фонопразан, амоксициллин и кларитромицин) составила 92,6% по сравнению с 75,9% для STT ( p <0,0001) [101]. Метаанализ японских исследований с участием 1599 пациентов показал, что тройная терапия на основе фонопразана значительно превосходила STT у пациентов с устойчивыми к кларитромицину штаммами (82,0% против 40,0%, p <0,0001) [102].Напротив, уровень эрадикации чувствительных к кларитромицину штаммов существенно не отличается. Если организм устойчив к кларитромицину, STT переключается на двойную терапию (ИПП + амоксициллин), и двойная терапия важна для поддержания pH желудочного сока на уровне ≥6. В этом отношении считается, что у вонопразана есть сильные стороны. Кроме того, тройная схема на основе фонопразана так же эффективна, как и STT на основе ИПП на основе чувствительности, для эрадикации H. pylori (97,4% против 95,7%) [103]. В исследовании эффективности двойной терапии 7-дневного фонопразана и низких доз амоксициллина в качестве препарата первой линии H.pylori , уровни эрадикации двойной (фонопразан и низкие дозы амоксициллина) и тройной терапии (фонопразан, амоксициллин с низкой дозой и кларитромицин) составили 84,5% и 89,2% ( p = 0,203) по ITT-анализу соответственно. и 87,1% и 90,2% ( p = 0,372) по данным PP-анализа, соответственно [104]. В реальности увеличения устойчивости к противомикробным препаратам можно сказать, что снижение общего количества антибиотиков с использованием вонопразана показывает положительный аспект в будущем лечении H.pylori .
В Японии схемы на основе P-CAB лицензированы в качестве лечения первого и второго ряда для эрадикации H. pylori . Мураками и др. продемонстрировали эффективность тройной схемы второго ряда на основе P-CAB (частота успеха 98,0%) [101]. Другое РКИ показало, что тройная терапия на основе фонопразана (фонопразан, амоксициллин и ситафлоксацин) была более эффективной, когда ИПП использовался с этими антибиотиками в качестве схемы лечения третьей линии для H. pylori (83,3% против 57.1% (PP), p = 0,043) [83]. Следовательно, терапия на основе P-CAB может быть жизнеспособной альтернативой схемам первого и второго ряда для эрадикации H. pylori .
9. Лечение при неэффективности первичной терапии
Все руководства рекомендуют избегать ранее принимаемых пациентом антибиотиков [4,8,9,10]. В частности, следует избегать повторного использования кларитромицина и левофлоксацина из-за высоких показателей устойчивости. Они также рекомендуют схему лечения тройной второй линии на основе BQT или левофлоксацина для H.pylori [81]. Если терапия первой или второй линии оказалась неэффективной, следует рассмотреть возможность проведения теста на восприимчивость к соответствующей терапии экстренной помощи [10,81].
Согласно Маастрихтскому / Флорентийскому консенсусу, после неэффективности BQT в качестве терапии первой линии рекомендуется трех- или четырехкратная терапия, содержащая хинолон [10]. После неэффективности четырехкомпонентного режима без висмута первой линии рекомендуется трех- или четырехкратный режим, содержащий BQT или хинолон [10]. BQT, четырехкомпонентная терапия без висмута и трехкомпонентная терапия, содержащая хинолоны, могут использоваться без перекрытия со схемами лечения второй или третьей линии [10].
Торонтский консенсус и рекомендации ACG, такие как Маастрихтский V / Флорентийский консенсус, подчеркивают важность BQT и левофлоксацин-содержащих схем лечения в качестве препаратов второго ряда [4,9]. Важным отличием от Маастрихтского V / Флорентийского консенсуса является возражение против использования четырехкратной схемы второго ряда без висмута, поскольку это менее эффективно, чем другие методы лечения [9]. Кроме того, схемы на основе рифабутина следует использовать только для пациентов, у которых в прошлом было не менее трех неудач лечения [9].В рекомендациях ACG указывается, что режим второго ряда следует выбирать на основе предыдущего воздействия антибиотиков и данных о местной устойчивости к антибиотикам [4].
10. Выводы
обобщает важные схемы лечения H. pylori . Лечение H. pylori — важная глобальная проблема, потому что оно было напрямую связано как причина нескольких желудочно-кишечных заболеваний. Существует явная озабоченность по поводу увеличения показателей устойчивости с течением времени, что подчеркивает необходимость использования подходящих антибиотиков в будущем, чтобы минимизировать дальнейший рост устойчивости к антибиотикам.Специальная терапия на основе AST показала хорошую скорость эрадикации при применении первой линии. Поскольку уровень устойчивости к антибиотикам H. pylori увеличивается, следует расширить роль индивидуализированных методов лечения. Однако, если индивидуальная терапия не может быть применена ко всем пациентам из-за реальных проблем, разумной альтернативой является использование высокоэффективного эмпирического режима на местном уровне. Кроме того, при использовании такой эмпирической схемы необходима простая и эффективная стратегия лечения H. pylori .Поэтому мы предлагаем BQT в качестве терапии первой линии, когда данные по AST или региональной резистентности недоступны (). Если BQT недоступен, мы предлагаем эмпирическую сопутствующую терапию. P-CAB может быть альтернативой, но данные немногочисленны и ограничены Восточной Азией.
Упрощенная стратегия лечения H. pylori .
Таблица 1
Схемы лечения инфекции Helicobacter pylori .
| Лечение | Схема | Продолжительность | Недавняя частота эрадикации первой линии (ITT) | Рекомендации в соответствии с Руководством | Примечания | |
|---|---|---|---|---|---|---|
| Стандартная тройная терапия (STT) | Стандартная тройная терапия (STT) | Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день | 7–14 дней | 63.9% [105], 74,1% [106] | Первая линия: необязательно рекомендована KCHUGR и JSHR Спасательная операция: ограничена рекомендована MAA | За последние 20 лет эффективность STT заметно снизилась, и STT обычно не рекомендуется в качестве схемы первого ряда |
| Квартальная терапия висмутом (BQT) | Стандартная доза ИПП 2 раза в день Стандартная доза висмута 4 раза в день Метронидазол 500 мг 3 раза в день Тетрациклин 500 мг 4 раза в день | 7–14 дней | .8% [107], 88,2% [44], 91,5% [108] Первая линия: рекомендовано ACG, MAA, TOR и KCHUGR (необязательно) Rescue: рекомендовано ACG, MAA, TOR и KCHUGR | BQT был предложен в качестве варианта лечения первой линии во многих руководствах, особенно для регионов с высокой устойчивостью к кларитромицину. | ||
| Сопутствующая терапия (четырехкратная терапия без висмута) | Стандартная доза ИПП 2 раза в день Кларитромицин 500 мг 2 раза в день Амоксициллин 1 г 2 раза в день Метронидазол 500 мг 2 раза в день | 10–14 дней | 84.6% [106], 90,1% [109], 93,5% [110] | Первая линия: рекомендовано ACG, MAA и TOR Спасение: рекомендовано ACG и MAA | Скорость искоренения превосходит это CTT, а метод введения прост по сравнению с последовательной терапией. Но побочные эффекты могут быть более вероятными при сопутствующей терапии. | |
| Последовательная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день (только первая половина) Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 10–14 д | 69.5% [106], 82,0% [111], 87,0% [112] | Первая линия: необязательно рекомендуется (не идеально) ACG Спасение: не рекомендуется во всех руководствах | В качестве терапии первой линии роль постепенно исчезает. Это обременительный способ снизить комплаентность пациента. | |
| Гибридная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 14 дней | 85.8% [75], 92,8% [113] | Первая линия: необязательно рекомендуется (не идеально) ACG Rescue: не рекомендуется во всех руководствах | Это метод, сочетающий последовательную терапию и сопутствующую терапию. | |
| Терапия на основе левофлоксацина | Левофлоксацин можно назначать в виде тройной или четырехкратной терапии. | 10–14 дней | 85,5% [76], 94,0% [77] | Первая линия: рекомендована ACG Rescue: рекомендована ACG, MAA и TOR | В большинстве руководств рекомендуется проводить терапию на основе левофлоксацина. применяется как терапия спасения, а не как первая линия.Он менее эффективен для областей с высокой устойчивостью к хинолонам. | |
| Терапия на основе рифабутина | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Рифабутин 150 мг 2 раза в день | 10 дней | 83,8% [93] | Первая линия: не рекомендуется во всех рекомендациях Спасение: необязательно (третья или четвертая линия) по MAA и TOR | Все руководства рекомендуют терапию на основе рифабутина в качестве терапии спасения. Рифабутин имеет редкий риск миелотоксичности; поэтому требуется осторожное использование. | |
| Терапия на основе калий-конкурентных кислотных блокаторов | P-CAB можно назначать как тройную терапию или четырехкратную терапию, заменяя PPI на P-CAB. | 7–14 d | 89,2% [104], 90,2% [114] | Не указано в алгоритме руководящих принципов | Ожидается, что роль мощного подавления кислоты будет постепенно возрастать, и необходимы дополнительные исследования. | |
| Лечение H. pylori на основе теста на антибактериальную чувствительность | Индивидуальная терапия в соответствии с результатами AST | 7–14 дней | 92.7% [31], 92,9% [115] | MAA рекомендует проводить АСТ после неэффективности терапии второй линии. | Результаты индивидуализированной терапии на основе AST превосходны, и ожидается, что она сыграет роль в улучшении лечения H. pylori в будущем. Требуются усилия для облегчения применения AST в клинической практике. |
Индивидуальная терапия, согласно результатам AST, способствует лечению H. pylori без повышения устойчивости к антибиотикам, поэтому следует уделять особое внимание тестированию на чувствительность.Есть также дополнительные соображения; например, как установить продолжительность лечения при чувствительности к кларитромицину и как выбрать режим (BQT или амоксициллин-метронидазол-ИПП), если устойчивость к кларитромицину не изучалась. Дальнейшая работа должна быть сосредоточена на максимальном терапевтическом эффекте индивидуализированной терапии, основанной на результатах AST.
Вклад авторов
S.Y.K. написал рукопись, и J.-W.C. способствовал разработке концепции и дизайна исследования. Все авторы прочитали и согласились с опубликованной версией рукописи.
Финансирование
Это исследование было поддержано Программой фундаментальных научных исследований через Национальный исследовательский фонд Кореи (NRF), финансируемым Министерством образования (номер гранта: 2020R1I1A306686511) и Исследовательским фондом Кореи (NRF), финансируемым Министерством образования. Образование (номер гранта: 2020R1F1A1076839).
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
1. Кандульски А., Селград М., Малфертхайнер П. Инфекция Helicobacter pylori : клинический обзор. Копать землю. Печень. Дис. 2008. 40: 619–626. DOI: 10.1016 / j.dld.2008.02.026. [PubMed] [CrossRef] [Google Scholar] 2. Макколл К. Клиническая практика. Инфекция Helicobacter pylori . N. Engl. J. Med. 2010; 362: 1597–1604. DOI: 10.1056 / NEJMcp1001110. [PubMed] [CrossRef] [Google Scholar] 3. Пламмер М., Франчески С., Винья Дж., Форман Д., де Мартель С. Глобальное бремя рака желудка, связанное с Helicobacter pylori . Int.J. Рак. 2015; 136: 487–490. DOI: 10.1002 / ijc.28999. [PubMed] [CrossRef] [Google Scholar] 4. Чей В.Д., Леонтиадис Г.И., Хауден К.В., Мосс С.Ф. Клинические рекомендации ACG: Лечение инфекции Helicobacter pylori . Являюсь. J. Gastroenterol. 2017; 112: 212–239. DOI: 10.1038 / ajg.2016.563. [PubMed] [CrossRef] [Google Scholar] 5. Тестерман Т.Л., Моррис Дж. За пределами желудка: обновленный взгляд на патогенез, диагностику и лечение Helicobacter pylori . Мир J. Gastroenterol. 2014; 20: 12781–12808.DOI: 10.3748 / wjg.v20.i36.12781. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ли Ю.К., Чан Т.Х., Чжоу С.К., Ту Ю.К., Ляо В.С., Ву М.С., Грэм Д.Ю. Связь между Helicobacter pylori Эрадикация и заболеваемость раком желудка: систематический обзор и метаанализ. Гастроэнтерология. 2016; 150: 1113–1124. DOI: 10.1053 / j.gastro.2016.01.028. [PubMed] [CrossRef] [Google Scholar] 7. Судзуки Х., Нисидзава Т., Хиби Т. Эрадикационная терапия Helicobacter pylori . Будущее.Microbiol. 2010. 5: 639–648. DOI: 10.2217 / fmb.10.25. [PubMed] [CrossRef] [Google Scholar] 8. Ким С.Г., Юнг Х.К., Ли Х.Л., Чан Дж.Й., Ли Х., Ким С.Г., Шин В.Г., Шин Э.С., Ли Ю.С. Корейский колледж хеликобактер и исследований верхних отделов желудочно-кишечного тракта. Корейский J. Gastroenterol. 2013; 62: 3–26. DOI: 10.4166 / kjg.2013.62.1.3. [PubMed] [CrossRef] [Google Scholar] 9. Фаллон К.А., Чиба Н., ван Зантен С.В., Фишбах Л., Гисберт Дж. П., Хант Р. Х., Джонс Н. Л., Рендер К., Леонтиадис Г. И., Моайеди П. и др. Торонтский консенсус по лечению инфекции Helicobacter pylori у взрослых.Гастроэнтерология. 2016; 151: 51–69. DOI: 10.1053 / j.gastro.2016.04.006. [PubMed] [CrossRef] [Google Scholar] 10. Малфертхайнер П., Мегро Ф., О’Морайн С.А., Гисберт Дж. П., Койперс Э. Дж., Аксон А. Т., Баццоли Ф., Гасбаррини А., Атертон Дж., Грэм Д. Ю. и др. Управление инфекцией Helicobacter pylori — Маастрихт V / Флорентийский консенсусный доклад. Кишечник. 2017; 66: 6–30. DOI: 10.1136 / gutjnl-2016-312288. [PubMed] [CrossRef] [Google Scholar] 11. Гисберт Дж. П., Гонсалес Л., Кальвет X., Гарсия Н., Лопес Т., Roque M., Gabriel R., Pajares J.M. Ингибитор протонной помпы, кларитромицин и амоксициллин или нитроимидазол: метаанализ эрадикации Helicobacter pylori . Алимент. Pharmacol. Ther. 2000; 14: 1319–1328. DOI: 10.1046 / j.1365-2036.2000.00844.x. [PubMed] [CrossRef] [Google Scholar] 12. Современные европейские концепции лечения инфекции Helicobacter pylori Маастрихтский консенсусный доклад. Европейская группа по изучению Helicobacter pylori. Кишечник. 1997; 41: 8–13. DOI: 10.1136 / gut.41.1.8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 13. Грэм Д.Ю., Фишбах Л. Лечение Helicobacter pylori в эпоху повышения устойчивости к антибиотикам. Кишечник. 2010; 59: 1143–1153. DOI: 10.1136 / gut.2009.1. [PubMed] [CrossRef] [Google Scholar] 14. Савольди А., Каррара Э., Грэм Д. Ю., Конти М., Такконелли Э. Распространенность устойчивости к антибиотикам у Helicobacter pylori : систематический обзор и метаанализ в регионах Всемирной организации здравоохранения. Гастроэнтерология.2018; 155: 1372–1382. DOI: 10.1053 / j.gastro.2018.07.007. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 15. Ким С.Ю., Чхве Д.Дж., Чунг Дж.В. Лечение антибиотиками от Helicobacter pylori : приближается конец? Мир J. Gastrointest. Pharmacol. Ther. 2015; 6: 183–198. DOI: 10.4292 / wjgpt.v6.i4.183. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 16. Тунг И., Арамин Х., Вавинская В., Гупта С., Парк Дж. Ю., Кроу С.Э., Валасек М.А. Обзорная статья: Глобальное появление устойчивости к антибиотикам Helicobacter pylori .Алимент. Pharmacol. Ther. 2016; 43: 514–533. DOI: 10.1111 / apt.13497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Woo H.Y., Park D.I., Park H., Kim M.K., Kim D.H., Kim I.S., Kim Y.J. Мультиплексная ПЦР на основе олигонуклеотидов с двойным примированием для обнаружения Helicobacter pylori и определения устойчивости к кларитромицину с помощью биоптатов желудка. Helicobacter. 2009. 14: 22–28. DOI: 10.1111 / j.1523-5378.2009.00654.x. [PubMed] [CrossRef] [Google Scholar] 18. Лиу Дж. М., Чанг К.Y., Chen M.J., Chen C.C., Fang Y.J., Lee J.Y., Wu J., Luo J., Liou T., Chang W. и др. Первичная устойчивость Helicobacter pylori на Тайване после проведения национальной политики ограничения потребления антибиотиков и ее связи с факторами вирулентности — общенациональное исследование. PLoS ONE. 2015; 10: e0124199. DOI: 10.1371 / journal.pone.0124199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 19. Ли Дж.Й., Пак К.С. Оптимальное лечение первой линии для инфекции Helicobacter pylori : последние стратегии.Гастроэнтерол. Res. Практик. 2016; 2016: 81. DOI: 10.1155 / 2016/81. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 20. Альба К., Бланко А., Аларкон Т. Устойчивость к антибиотикам у Helicobacter pylori . Curr. Opin. Заразить. Дис. 2017; 30: 489–497. DOI: 10.1097 / QCO.0000000000000396. [PubMed] [CrossRef] [Google Scholar] 21. Hwang T.J., Kim N., Kim H.B., Lee B.H., Nam R.H., Park J.H., Lee M.K., Park Y.S., Lee D.H., Jung H.C. и др. Изменение устойчивости к антибиотикам штаммов Helicobacter pylori и влияние точечной мутации A2143G 23S рРНК на эрадикацию H.pylori в едином центре Кореи. J. Clin. Гастроэнтерол. 2010; 44: 536–543. DOI: 10.1097 / MCG.0b013e3181d04592. [PubMed] [CrossRef] [Google Scholar] 22. Герритс М.М., ван Влит А.Х., Кейперс Э.Дж., Кустерс Дж.Г. Helicobacter pylori и устойчивость к противомикробным препаратам: молекулярные механизмы и клинические последствия. Lancet Infect. Дис. 2006; 6: 699–709. DOI: 10.1016 / S1473-3099 (06) 70627-2. [PubMed] [CrossRef] [Google Scholar] 24. Халтен К., Гибриль А., Скольд О., Энгстранд Л. Устойчивость к макролидам у Helicobacter pylori : механизм и стабильность в штаммах от пациентов, получавших кларитромицин.Противомикробный. Агенты. Chemother. 1997; 41: 2550–2553. DOI: 10.1128 / AAC.41.11.2550. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25. Стоун Г.Г., Шортридж Д., Версалович Дж., Бейер Дж., Фламм Р.К., Грэм Д.Ю., Гонейм А.Т., Танака С.К. ПЦР-анализ лигирования олигонуклеотидов для определения распространенности мутаций гена 23S рРНК у устойчивых к кларитромицину Helicobacter pylori . Противомикробный. Агенты Chemother. 1997. 41: 712–714. DOI: 10.1128 / AAC.41.3.712. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26.Аларкон Т., Доминго Д., Прието Н., Лопес-Бреа М. Стабильность устойчивости к кларитромицину у Helicobacter pylori : влияние MIC и типа мутации в 23S рРНК. J. Antimicrob. Chemother. 2000. 46: 613–616. DOI: 10.1093 / jac / 46.4.613. [PubMed] [CrossRef] [Google Scholar] 27. Van Doorn LJ, Glupczynski Y., Kusters JG, Megraud F., Midolo P., Maggi-Solca N., Queiroz DM, Nouhan N., Stet E., Quint WG Точное прогнозирование устойчивости к макролидам у Helicobacter pylori с помощью Анализ зонда ПЦР для обнаружения мутаций в гене 23S рРНК: многоцентровое валидационное исследование.Противомикробный. Агенты Chemother. 2001; 45: 1500–1504. DOI: 10.1128 / AAC.45.5.1500-1504.2001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 28. Като С., Фудзимура С., Удагава Х., Симидзу Т., Майсава С., Одзава К., Иинума К. Устойчивость к антибиотикам штаммов Helicobacter pylori у японских детей. J. Clin. Microbiol. 2002; 40: 649–653. DOI: 10.1128 / JCM.40.2.649-653.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Ван В.Х., Вонг Б.С., Мукхопадхьяй А.К., Берг Д.Э., Чо К.Х., Лай К.С., Ху В.Х., Фунг Ф.М., Хуэй В.М., Лам С.К. Высокая распространенность инфекции Helicobacter pylori с двойной устойчивостью к метронидазолу и кларитромицину в Гонконге. Алимент. Pharmacol. Ther. 2000; 14: 901–910. DOI: 10.1046 / j.1365-2036.2000.00795.x. [PubMed] [CrossRef] [Google Scholar] 30. Ли Х. Дж., Ким Дж. И., Чунг Д. Ю., Ким Т. Х., Джун Э. Дж., О Дж. Х., Чунг В. К., Ким Б., Ким С. С., Пак С. и др. Искоренение Helicobacter pylori в соответствии с точечными мутациями 23S рибосомной РНК, связанными с устойчивостью к кларитромицину.J. Infect. Дис. 2013; 208: 1123–1130. DOI: 10.1093 / infdis / jit287. [PubMed] [CrossRef] [Google Scholar] 31. Чо Дж. Х., Чон С. Р., Ким Х. Г., Джин С. Ю., Пак С. Экономическая эффективность адаптированной стратегии ликвидации Helicobacter pylori , основанной на наличии точечной мутации 23S рибосомной РНК, которая вызывает устойчивость к кларитромицину у корейских пациентов. J. Gastroenterol. Гепатол. 2019; 34: 700–706. DOI: 10.1111 / jgh.14383. [PubMed] [CrossRef] [Google Scholar] 32. Папастержиу В., Мату Н., Ликуси С., Евгениди А., Параскева К.Д., Яннакопулос А., Ставру П., Платсука Э., Караджаннис Ю.А. Семидневная тройная эрадикационная терапия Helicobacter pylori на основе генотипической устойчивости может быть высокоэффективной. Анна. Гастроэнтерол. 2018; 31: 198–204. DOI: 10.20524 / aog.2017.0219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 33. Cosme A., Montes M., Ibarra B., Tamayo E., Alonso H., Mendarte U., Lizasoan J., Herreros-Villanueva M., Bujanda L. Тестирование на чувствительность к противомикробным препаратам перед лечением первой линии для Helicobacter pylori инфекция у пациентов с двойной или тройной устойчивостью к антибиотикам.Мир J. Gastroenterol. 2017; 23: 3367–3373. DOI: 10.3748 / wjg.v23.i18.3367. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Ли Дж. У., Ким Н., Нам Р. Х., Ли С. М., Квон Ю. Х., Сон С. Д., Ким Дж. М., Ли Д. Х., Юнг Х. С. Благоприятные исходы эрадикационной терапии Helicobacter pylori на основе посева в регионе с высокой устойчивостью к противомикробным препаратам. Helicobacter. 2019; 24: e12561. DOI: 10.1111 / hel.12561. [PubMed] [CrossRef] [Google Scholar] 35. Чен К., Лонг X., Цзи Ю., Лян X., Ли Д., Гао Х., Сюй Б., Лю М., Чен Ю., Сунь Ю. Рандомизированное контролируемое исследование: терапия на основе чувствительности в сравнении с эмпирической четырехкратной терапией висмутом для лечения первой линии Helicobacter pylori . Алимент. Pharmacol. Ther. 2019; 49: 1385–1394. DOI: 10.1111 / apt.15273. [PubMed] [CrossRef] [Google Scholar] 36. Блюмель Б., Гёльц Х., Кист М., Глокер Э.О. Ретроспективное исследование результатов эрадикационной терапии «спасение» Helicobacter pylori на основе молекулярно-генетического тестирования чувствительности. Helicobacter.2018; 23: e12494. DOI: 10.1111 / hel.12494. [PubMed] [CrossRef] [Google Scholar] 37. Бхакта Д., Грэм Д. Ю., Чан Дж., Эль-Сераг Х. Б. Уроки использования культурального лечения после направления к специалисту по поводу множественной неудачи лечения инфекции, вызванной Helicobacter pylori . Clin. Гастроэнтерол. Гепатол. 2018; 16: 1531–1532. DOI: 10.1016 / j.cgh.2017.12.040. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Байлина М., Муньос Н., Санчес-Дельгадо Дж., Лопес-Гонгора С., Кальвет X., Пуч И. Систематический обзор: Достигнет ли лечение на основе чувствительности приемлемых показателей излечения для терапии второй линии Helicobacter pylori , как в настоящее время практиковал? Helicobacter.2019; 24: e12584. DOI: 10.1111 / hel.12584. [PubMed] [CrossRef] [Google Scholar] 39. Лиу Дж. М., Чен П. Ю., Ло Дж. К., Ли Дж. Ю., Чен К. С., Фанг Ю. Дж., Ян Т. Х., Чанг С. Ю., Баир М. Дж., Ченет М. Дж. И др. Эффективность управляемой генотипической резистентности по сравнению с эмпирической терапией рефрактерной инфекции Helicobacter pylori . Гастроэнтерология. 2018; 155: 1109–1119. DOI: 10.1053 / j.gastro.2018.06.047. [PubMed] [CrossRef] [Google Scholar] 40. Ли Б.З., Треэплтон Д.Э., Ван Дж.Й., Сюй Дж.М., Юань Дж.К., Чжан К., Ли П., Е К. Л., Го Б., Мао С. и др. Сравнительная эффективность и переносимость лечения Helicobacter pylori : систематический обзор и сетевой метаанализ. BMJ. 2015; 351: ч5052. DOI: 10.1136 / bmj.h5052. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 41. Лю К.С., Хунг И.Ф., Сето В.К., Тонг Т., Сюй А.С., Лам Ф.Й., Но Д.Й.К., Вонг С.Й., Люн В.К. Десятидневная последовательная и 10-дневная модифицированная четырехкратная терапия висмутом в качестве эмпирической терапии первой и второй линии для Helicobacter pylori у китайских пациентов: открытое рандомизированное перекрестное исследование.Кишечник. 2014; 63: 1410–1415. DOI: 10.1136 / gutjnl-2013-306120. [PubMed] [CrossRef] [Google Scholar] 42. Hsu P.I., Tsay F.W., Graham D.Y., Tsai T.J., Tsai K.W., Kao J.Y., Peng N.J., Kuo C.H., Kao S.S., Wang H.M. и др. Эквивалентная эффективность обратной гибридной и четверной терапии висмутом в искоренении инфекции Helicobacter pylori в рандомизированном контролируемом исследовании. Clin. Гастроэнтерол. Гепатол. 2018; 16: 1427–1433. DOI: 10.1016 / j.cgh.2018.03.031. [PubMed] [CrossRef] [Google Scholar] 43.Масиас-Гарсия Ф., Бастон-Рей И., де ла Иглесиа-Гарсия Д., Кальвино-Суарес К., Ньето-Гарсия Л., Домингес-Муньос Дж. Э. Висмутсодержащая четырехкратная терапия по сравнению с сопутствующей четырехкратной терапией в качестве лечения первой линии для инфекции Helicobacter pylori в области высокой устойчивости к кларитромицину: проспективное, перекрестное, сравнительное, открытое исследование. Helicobacter. 2019; 24: e12546. DOI: 10.1111 / hel.12546. [PubMed] [CrossRef] [Google Scholar] 44. Ким С.Дж., Чунг Дж.В., Ву Х.С., Ким С.Й., Ким Дж.Х., Ким Й.Дж., Ким К.О., Квон К.А., Пак Д.К. Двухнедельная четырехкратная терапия висмутом и сопутствующая терапия являются эффективными препаратами первой линии для эрадикации Helicobacter pylori : проспективное открытое рандомизированное исследование. Мир. J. Gastroenterol. 2019; 25: 6790–6798. DOI: 10.3748 / wjg.v25.i46.6790. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 45. Ким Дж.Й., Ли С.Й., Ким Дж.Х., Сунг И.К., Пак Х.С. Эффективность и безопасность четырехкратной висмутсодержащей терапии два раза в день с использованием высоких доз тетрациклина и метронидазола для эрадикации второй линии Helicobacter pylori .Helicobacter. 2020; 25: e12683. DOI: 10.1111 / hel.12683. [PubMed] [CrossRef] [Google Scholar] 46. Xie Y., Pan X., Li Y., Wang H., Du Y., Xu J., Wang J., Zeng Z., Chen Y., Zhang G. и др. Новая однократная капсула висмута, метронидазола и тетрациклина, вводимая с омепразолом, по сравнению с четырехкратной терапией, состоящей из висмута, омепразола, амоксициллина и кларитромицина для эрадикации Helicobacter pylori у пациентов с язвой двенадцатиперстной кишки: проспективное, многоцелевое исследование в Китае. J. Antimicrob.Chemother. 2018; 73: 1681–1687. [PubMed] [Google Scholar] 47. Фиорини Г., Зулло А., Сарачино И.М., Гатта Л., Павони М., Вайра Д. Пилера и последовательная терапия для эрадикации первой линии Helicobacter pylori : исследование на основе культуры в реальной клинической практике. Евро. J. Gastroenterol. Гепатол. 2018; 30: 621–625. DOI: 10.1097 / MEG.0000000000001102. [PubMed] [CrossRef] [Google Scholar] 48. Ниссен О.П., МакНичолл А.Г., Гисберт Дж.П. Метаанализ четырехкратной терапии, содержащей висмут, три-в-одной одной капсуле для уничтожения Helicobacter pylori .Helicobacter. 2019; 24: e12570. DOI: 10.1111 / hel.12570. [PubMed] [CrossRef] [Google Scholar] 49. Ким С.Э., Ро Дж. Х., Парк М. И., Пак С. Дж., Мун В., Ким Дж. Х., Юнг К., Хео Дж. Дж. Эффект 7-дневной четырехкратной терапии висмутом по сравнению с 14-дневной тройной терапией моксифлоксацином для второй линии Helicobacter pylori эрадикационной терапии. Корейский язык. J. Gastroenterol. 2019; 73: 26–34. DOI: 10.4166 / kjg.2019.73.1.26. [PubMed] [CrossRef] [Google Scholar] 50. Боянова Л., Митов И. Географическая карта и эволюция первичной устойчивости Helicobacter pylori к антибактериальным препаратам.Эксперт. Преподобный Anti. Заразить. Ther. 2010; 8: 59–70. DOI: 10.1586 / eri.09.113. [PubMed] [CrossRef] [Google Scholar] 51. Megraud F., Coenen S., Versporten A., Kist M., Lopez-Brea M., Hirschl AM, Andersen LP, Goossens H., Glupczynski Y., участники исследовательской группы Устойчивость Helicobacter pylori к антибиотикам в Европе и ее отношение к употреблению антибиотиков. Кишечник. 2013; 62: 34–42. DOI: 10.1136 / gutjnl-2012-302254. [PubMed] [CrossRef] [Google Scholar] 52. Фишбах Л., Эванс Э. Мета-анализ: влияние статуса устойчивости к антибиотикам на эффективность тройной и четверной терапии первой линии для Helicobacter pylori .Алимент. Pharmacol. Ther. 2007. 26: 343–357. DOI: 10.1111 / j.1365-2036.2007.03386.x. [PubMed] [CrossRef] [Google Scholar] 53. Venerito M., Krieger T., Ecker T., Leandro G., Malfertheiner P. Метаанализ четырехкратной терапии висмутом по сравнению с тройной терапией кларитромицином для эмпирического первичного лечения инфекции Helicobacter pylori . Пищеварение. 2013; 88: 33–45. DOI: 10,1159 / 000350719. [PubMed] [CrossRef] [Google Scholar] 54. Манцарис Г.Дж., Петраки К., Арчавлис Э., Амбериадис П., Христофоридис П., Kourtessas D., Chiotakakou E., Triantafyllou G. Тройная терапия омепразолом по сравнению с четырехкратной терапией омепразолом для заживления язвы двенадцатиперстной кишки и эрадикации инфекции Helicobacter pylori : последующее исследование через 24 месяца. Евро. J. Gastroenterol. Гепатол. 2002; 14: 1237–1243. DOI: 10.1097 / 00042737-200211000-00012. [PubMed] [CrossRef] [Google Scholar] 55. Gisbert J.P., Calvet X. Обзорная статья: Четырехкратная (сопутствующая) терапия без висмута для искоренения Helicobater pylori. Алимент. Pharmacol.Ther. 2011; 34: 604–617. DOI: 10.1111 / j.1365-2036.2011.04770.x. [PubMed] [CrossRef] [Google Scholar] 56. Essa A.S., Kramer J.R., Graham D.Y., Treiber G. Мета-анализ: «Сопутствующая терапия» с четырьмя лекарствами, тремя антибиотиками, без висмута по сравнению с тройной терапией для эрадикации Helicobacter pylori . Helicobacter. 2009. 14: 109–118. DOI: 10.1111 / j.1523-5378.2009.00671.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 57. Gisbert J.P., Calvet X. Последние данные о четырехкратной (сопутствующей) терапии без висмута для эрадикации Helicobacter pylori .Clin. Exp. Гастроэнтерол. 2012; 5: 23–34. [Бесплатная статья PMC] [PubMed] [Google Scholar] 58. Chen MJ, Chen CC, Chen YN, Chen CC, Fang YJ, Lin JT, Wu MS, Liou JM, Taiwan Gastrointestinal Disease Helicobacter Consortium Систематический обзор с метаанализом: сопутствующая терапия против тройной терапии для лечения первой линии Helicobacter pylori Инфекция. Являюсь. J. Gastroenterol. 2018; 113: 1444–1457. DOI: 10.1038 / s41395-018-0217-2. [PubMed] [CrossRef] [Google Scholar] 59. Молина-Инфанте Дж., Пазос-Пачеко К., Винагре-Родригес Г., Перес-Галлардо Б., Дуэнас-Садорнил К., Эрнандес-Алонсо М., Гонсалес-Гарсия Г., Матеос-Родригес Дж. М., Фернандес-Бермехо М., Гисберт Дж. П. Невисмут четырехкратная (сопутствующая) терапия: эмпирическая и индивидуализированная эффективность по сравнению со стандартной тройной терапией для чувствительных к кларитромицину Helicobacter pylori и по сравнению с последовательной терапией для устойчивых к кларитромицину штаммов. Helicobacter. 2012; 17: 269–276. DOI: 10.1111 / j.1523-5378.2012.00947.x. [PubMed] [CrossRef] [Google Scholar] 60.Jung Y.S., Park C.H., Park J.H., Nam E., Lee H.L. Эффективность эрадикационной терапии Helicobacter pylori в Корее: систематический обзор и сетевой метаанализ. Helicobacter. 2017; 22 DOI: 10.1111 / hel.12389. [PubMed] [CrossRef] [Google Scholar] 61. Чунг Дж. У., Хан Дж. П., Ким К. О., Ким С. Ю., Хонг С. Дж., Ким Т. Х., Ким С. В., Ким Дж. С., Ким Б. В., Банг Б. Десятидневная эмпирическая последовательная или сопутствующая терапия более эффективна, чем тройная терапия для эрадикации Helicobacter pylori : многоцентровое проспективное исследование.Копать землю. Печень. Дис. 2016; 48: 888–892. DOI: 10.1016 / j.dld.2016.05.005. [PubMed] [CrossRef] [Google Scholar] 62. Park S.M., Kim J.S., Kim B.W., Ji J.S., Choi H. Рандомизированное клиническое испытание, сравнивающее 10- или 14-дневную последовательную терапию и 10- или 14-дневную сопутствующую терапию для эмпирического лечения первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2017; 32: 589–594. DOI: 10.1111 / jgh.13510. [PubMed] [CrossRef] [Google Scholar] 63. Ким С. Ю., Ли С. В., Чхве Дж. В., Чон С. В., Хён Дж.J., Jung Y.K., Koo J.S., Yim H.J. Helicobacter pylori Показатели эрадикации сопутствующей и последовательной терапии в Корее. Helicobacter. 2017; 22: e12441. DOI: 10.1111 / hel.12441. [PubMed] [CrossRef] [Google Scholar] 64. Анг Т.Л., Фок К.М., Сонг М., Анг Д., Квек А.Б., Онг Дж., Тан Дж., Тео Е.К., Дхамодаран С. Десятидневная тройная терапия по сравнению с последовательной терапией по сравнению с сопутствующей терапией в качестве лечения первой линии для Helicobacter pylori инфекция. J. Gastroenterol. Гепатол. 2015; 30: 1134–1139.DOI: 10.1111 / jgh.12892. [PubMed] [CrossRef] [Google Scholar] 65. Макниколл А.Г., Марин А.С., Молина-Инфанте Дж., Кастро М., Баррио Дж., Дуконс Дж., Кальвет X., Коба К., Монторо М., Бори Ф. и др. Рандомизированное клиническое испытание, сравнивающее последовательную и сопутствующую терапию для эрадикации Helicobacter pylori в рутинной клинической практике. Кишечник. 2014; 63: 244–249. DOI: 10.1136 / gutjnl-2013-304820. [PubMed] [CrossRef] [Google Scholar] 66. Гатта Л., Вакил Н., Вайра Д., Скарпигнато С. Глобальные показатели эрадикации инфекции Helicobacter pylori : систематический обзор и метаанализ последовательной терапии.BMJ. 2013; 347: f4587. DOI: 10.1136 / bmj.f4587. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 67. Хе Л., Дэн Т., Луо Х. Мета-анализ последовательной, сопутствующей и гибридной терапии для эрадикации Helicobacter pylori . Междунар. Med. 2015; 54: 703–710. DOI: 10.2169 / internalmedicine.54.3442. [PubMed] [CrossRef] [Google Scholar] 68. Zullo A., Scaccianoce G., De Francesco V., Ruggiero V., D’Ambrosio P., Castorani L., Bonfrate L., Vannella L., Hassan C., Portincasa P. Сопутствующая, последовательная и гибридная терапия для ЧАС.pylori: пилотное исследование. Clin. Res. Гепатол. Гастроэнтерол. 2013; 37: 647–650. DOI: 10.1016 / j.clinre.2013.04.003. [PubMed] [CrossRef] [Google Scholar] 69. Ким С.Й., Ли С.В., Хён Дж.Дж., Юнг С.В., Ку Дж.С., Йим Х.Дж., Пак Дж.Дж., Чун Х.Дж., Чой Дж.Х. Сравнительное исследование степени эрадикации Helicobacter pylori с 5-дневной четырехкратной «сопутствующей» терапией и 7-дневной стандартной тройной терапией. J. Clin. Гастроэнтерол. 2013; 47: 21–24. DOI: 10.1097 / MCG.0b013e3182548ad4. [PubMed] [CrossRef] [Google Scholar] 70.Лим Дж. Х., Ли Д. Х., Чой К., Ли С. Т., Ким Н., Чон С. Х., Ким Дж. У., Хван Дж. Х., Пак Ю. С., Ли С. Х. и др. Клинические результаты двухнедельной последовательной и сопутствующей терапии для эрадикации Helicobacter pylori : рандомизированное пилотное исследование. Helicobacter. 2013. 18: 180–186. DOI: 10.1111 / hel.12034. [PubMed] [CrossRef] [Google Scholar] 71. Гевара Б., Когдилл А.Г. Helicobacter pylori : Обзор текущих стратегий диагностики и управления. Копать землю. Дис. Sci. 2020; 65: 1917–1931.DOI: 10.1007 / s10620-020-06193-7. [PubMed] [CrossRef] [Google Scholar] 72. Грэм Д.Ю., Ли Ю.С., Ву М.С. Рациональная терапия Helicobacter pylori : доказательная медицина, а не доказательная медицина. Clin. Гастроэнтерол. Гепатол. 2014; 12: 177–186. DOI: 10.1016 / j.cgh.2013.05.028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 73. Wang B., Wang Y.H., Lv Z.F., Xiong H.F., Wang H., Yang Y., Xie Y. Обзор: Эффективность и безопасность гибридной терапии для инфекции Helicobacter pylori : систематический обзор и метаанализ.Helicobacter. 2015; 20: 79–88. DOI: 10.1111 / hel.12180. [PubMed] [CrossRef] [Google Scholar] 74. Молина-Инфанте Дж., Романо М., Фернандес-Бермехо М., Федерико А., Гравина А.Г., Поццати Л., Гарсия-Абадиа Э., Винагре-Родригес Г., Мартинес-Алькала К., Эрнандес-Алонсо М. , и другие. Оптимизированная четырехкомпонентная терапия без висмута излечивает большинство пациентов с инфекцией Helicobacter pylori в популяциях с высокими показателями устойчивости к антибиотикам. Гастроэнтерология. 2013; 145: 121–128. DOI: 10.1053 / j.gastro.2013.03.050. [PubMed] [CrossRef] [Google Scholar] 75. Georgopoulos SD, Papastergiou V., Martinez-Gonzalez B., Xirouchakis E., Familias I., Sgouras D., Mentis A., Karatapanis S. Гибридная терапия как схема первой линии для эрадикации Helicobacter pylori при высокой устойчивости к кларитромицину область: перспективное открытое испытание. Анна. Гастроэнтерол. 2018; 31: 205–210. DOI: 10.20524 / aog.2017.0221. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Сонг З., Фу В., Чжоу Л. Цефуроксим, левофлоксацин, эзомепразол и висмут в качестве терапии первой линии для ликвидации Helicobacter pylori у пациентов с аллергией на пенициллин.BMC Gastroenterol. 2019; 19: 132. DOI: 10.1186 / s12876-019-1056-3. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 77. Auttajaroon J., Vilaichone R.K., Chotivitayatarakorn P., Mahachai V. Рабепразол, левофлоксацин, кларитромицин-MR и висмут один раз в день для эрадикации Helicobacter pylori : рандомизированное исследование продолжительностью 7 или 14 дней (исследование ONCE) Helicobacter. 2019; 24: e12615. DOI: 10.1111 / hel.12615. [PubMed] [CrossRef] [Google Scholar] 78. Ган Х.Ю., Пэн Т.Л., Хуан Ю.М., Су К.Х., Чжао Л.Л., Яо Л.Ю., Ян Р.Дж. Эффективность двух различных доз левофлоксацина в лечении инфекции Helicobacter pylori : проспективное одноцентровое рандомизированное клиническое испытание. Sci. Отчет 2018; 8: 9045. DOI: 10.1038 / s41598-018-27482-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 79. Ciccaglione AF, Di Giulio M., Di Lodovico S., Di Campli E., Cellini L., Marzio L. Бычий лактоферрин повышает эффективность тройной терапии на основе левофлоксацина в качестве лечения первой линии инфекции Helicobacter pylori : An in vitro и in vivo исследования.J. Antimicrob. Chemother. 2019; 74: 1069–1077. DOI: 10,1093 / jac / dky510. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 80. Басу П.П., Раяпуди К., Пакана Т., Шах Н.Дж., Кришнасвами Н., Флинн М. Рандомизированное исследование, сравнивающее левофлоксацин, омепразол, нитазоксанид и доксициклин с тройной терапией для ликвидации Helicobacter pylori . Являюсь. J. Gastroenterol. 2011; 106: 1970–1975. DOI: 10.1038 / ajg.2011.306. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 81. Фэллон К.А., Мосс С.Ф., Малфертхайнер П. Согласование последних рекомендаций по лечению Helicobacter pylori во времена повышения устойчивости к антибиотикам. Гастроэнтерология. 2019; 157: 44–53. DOI: 10.1053 / j.gastro.2019.04.011. [PubMed] [CrossRef] [Google Scholar] 82. Мори Х., Судзуки Х. Обновленная информация о хинолон-содержащих терапии спасения от инфекции Helicobacter pylori . Мир J. Gastroenterol. 2020; 26: 1733–1744. DOI: 10.3748 / wjg.v26.i15.1733. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83.Sue S., Shibata W., Sasaki T., Kaneko H., Irie K., Kondo M., Maeda S. Рандомизированное испытание тройной терапии третьей линии на основе вонопразана и ингибитора протонной помпы с ситафлоксацином для Helicobacter pylori . J. Gastroenterol. Гепатол. 2019; 34: 686–692. DOI: 10.1111 / jgh.14456. [PubMed] [CrossRef] [Google Scholar] 84. Судзуки Х., Нишизава Т., Мураока Х., Хиби Т. Ситафлоксацин и гареноксацин могут преодолеть устойчивость к антибиотикам Helicobacter pylori с мутацией gyrA.Противомикробный. Агенты. Chemother. 2009; 53: 1720–1721. DOI: 10.1128 / AAC.00049-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 85. Miftahussurur M., Waskito LA, Syam AF, Nusi IA, Siregar G., Richardo M., Bakry AF, Rezkitha YAA, Wibawa IDN, Yamaoka Y. Альтернативные схемы эрадикации инфекции Helicobacter pylori в регионах Индонезии с высоким содержанием метронидазола и левофлоксина сопротивление. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 345–358. DOI: 10.2147 / IDR.S187063. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 86.Мифтахуссурур М., Афтаб Х., Шреста П.К., Шарма Р.П., Субсомвонг П., Васкито Л.А., Духан Д., Фаузия К.А., Ямаока Ю. Эффективные терапевтические схемы в двух странах Южной Азии с высокой устойчивостью к основным антибиотикам Helicobacter pylori . Противомикробный. Оказывать сопротивление. Заразить. Контроль. 2019; 8:40. DOI: 10.1186 / s13756-019-0482-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 87. Гисберт Дж. П., Кальвет X. Обзорная статья: Рифабутин в лечении рефрактерной инфекции Helicobacter pylori .Алимент. Pharmacol. Ther. 2012; 35: 209–221. DOI: 10.1111 / j.1365-2036.2011.04937.x. [PubMed] [CrossRef] [Google Scholar] 88. Хип М., Бек Д., Байердорфер Э., Лен Н. Механизм устойчивости к рифампину и рифабутину в Helicobacter pylori . Противомикробный. Агенты. Chemother. 1999; 43: 1497–1499. DOI: 10.1128 / AAC.43.6.1497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 89. Рибалдоне Д.Г., Фагуни С., Астеджано М., Дураццо М., Моргандо А., Спруджевник Т., Джорданино К., Баронио М., Анжелис К.D., Saracco G.M. и др. Спасательная терапия на основе рифабутина для эрадикации Helicobacter pylori : долгосрочное проспективное исследование в большой когорте трудно поддающихся лечению пациентов. J. Clin. Med. 2019; 8: 199. DOI: 10,3390 / jcm8020199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 90. Akada J.K., Shirai M., Fujii K., Okita K., Nakazawa T. Активность новых производных рифамицина, KRM-1648 и KRM-1657, in vitro против Helicobacter pylori in vitro. Противомикробный. Агенты. Chemother. 1999; 43: 1072–1076.DOI: 10.1128 / AAC.43.5.1072. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 91. Кунин С.М. Антимикробная активность рифабутина. Clin. Заразить. Дис. 1996; 22 (Дополнение 1: S3-13): 30. DOI: 10.1093 / Clinids / 22.Supplement_1.S3. [PubMed] [CrossRef] [Google Scholar] 92. Сунг Дж., Ким Н., Пак И. Х., Хван Ю. Дж., Квон С., На Г., Чой Дж. Ю., Кан Дж. Б., Ким Х. Р., Ким Дж. В. и др. Спасательная терапия четвертой и пятой линий на основе рифабутина у пациентов с неэффективностью эрадикации Helicobacter pylori . Корейский язык.J. Gastroenterol. 2017; 69: 109–118. DOI: 10.4166 / kjg.2017.69.2.109. [PubMed] [CrossRef] [Google Scholar] 93. Грэм Д.Ю., Ханаан Ю., Махер Дж., Винер Г., Халтен К.Г., Калфус И.Н. Тройная терапия на основе рифабутина (RHB-105) для ликвидации Helicobacter pylori : двойное слепое рандомизированное контролируемое исследование. Анна. Междунар. Med. 2020; 172: 795–802. DOI: 10.7326 / M19-3734. [PubMed] [CrossRef] [Google Scholar] 94. Бок Х., Куп Х., Лен Н., Хип М. Тройная терапия на основе рифабутина после неудачной эрадикационной терапии Helicobacter pylori : предварительный опыт.J. Clin. Гастроэнтерол. 2000. 31: 222–225. DOI: 10.1097 / 00004836-200010000-00007. [PubMed] [CrossRef] [Google Scholar] 95. Сузуки С., Сузуки Х., Нисидзава Т., Канеко Ф., Отани С., Мураока Х., Сайто Ю., Кобаяши И., Хиби Т. Прошлое дозирование рифампицина определяет устойчивость к рифабутину Helicobacter pylori . Пищеварение. 2009; 79: 1–4. DOI: 10,1159 / 0001. [PubMed] [CrossRef] [Google Scholar] 96. Скотт Дж. Я., Мансон К. Б., Маркус Э. А., Ламбрехт Н. В., Сакс Г. Селективность связывания фонопразана (TAK-438) с H +, K + -АТФазой желудка.Алимент. Pharmacol. Ther. 2015; 42: 1315–1326. DOI: 10.1111 / apt.13414. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 97. Park J.Y., Kim J.G. [New Helicobacter pylori Eradication Therapies] Корейский. J. Gastroenterol. 2018; 72: 237–244. DOI: 10.4166 / kjg.2018.72.5.237. [PubMed] [CrossRef] [Google Scholar] 99. Грэм Д.Ю., Дор М.П. Обновленная информация об использовании вонопразана: конкурентного блокатора кислоты. Гастроэнтерология. 2018; 154: 462–466. DOI: 10.1053 / j.gastro.2018.01.018. [PubMed] [CrossRef] [Google Scholar] 100.Лю Q.J., Пу Q.H., Чжун X.F., Чжан Дж. Эффективность и безопасность тройной терапии на основе вонопразана и ингибитора протонной помпы для искоренения Helicobacter pylori : метаанализ рандомизированных клинических испытаний. Биомед. Res. Int. 2019; 3: 1–8. DOI: 10.1155 / 2019/9781212. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 101. Murakami K., Sakurai Y., Shiino M., Funao N., Nishimura A., Asaka M. Vonoprazan, новый калий-конкурентный блокатор кислоты, в качестве компонента тройной терапии первой и второй линии против Helicobacter pylori Эрадикация : рандомизированное двойное слепое исследование фазы III.Кишечник. 2016; 65: 1439–1446. DOI: 10.1136 / gutjnl-2015-311304. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 102. Ли М., Осима Т., Хорикава Т., Тозава К., Томита Т., Фукуи Х., Ватари Дж., Мива Х. Систематический обзор с метаанализом: вонопразан, мощный блокатор кислоты, превосходит протонный ингибиторы помпы для уничтожения устойчивых к кларитромицину штаммов Helicobacter pylori . Helicobacter. 2018; 23: e12495. DOI: 10.1111 / hel.12495. [PubMed] [CrossRef] [Google Scholar] 103. Танабэ Х., Yoshino K., Ando K., Nomura Y., Ohta K., Satoh K., Ichiishi E., Ishizuka A., Otake T., Kohgo Y., et al. Тройная терапия на основе вонопразана не уступает тройной терапии на основе ингибиторов протонной помпы на основе чувствительности для эрадикации Helicobacter pylori . Анна. Clin. Microbiol Antimicrob. 2018; 17:29. DOI: 10.1186 / s12941-018-0281-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 104. Судзуки С., Готода Т., Кусано К., Икехара Х., Итидзима Р., Охьяучи М., Ито Х., Кавамура М., Огата Ю., Отака М. и др. Семидневная двойная терапия фонопразаном и низкими дозами амоксициллина в качестве терапии первой линии Helicobacter pylori : многоцентровое рандомизированное исследование в Японии. Кишечник. 2020; 69: 1019–1026. DOI: 10.1136 / gutjnl-2019-319954. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 105. Ким Б.Дж., Ли Х., Ли Ю.С., Чон С.В., Ким Г.Х., Ким Х.С., Сунг Дж.К., Ли Д.Х., Ким Х.У., Пак М.И. и др. Десятидневная сопутствующая, 10-дневная последовательная и 7-дневная тройная терапия в качестве лечения первой линии для инфекции Helicobacter pylori : общенациональное рандомизированное исследование в Корее.Кишечник. Печень. 2019; 13: 531–540. DOI: 10.5009 / gnl19136. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 106. Zhou Y., Ye Z., Wang Y., Zhang Y., Tang Z., Yan W., Jiang Y., Huang Y. Сравнение четырех различных схем лечения против Helicobacter pylori в качестве лечения первой линии: перспектива , перекрестное, сравнительное, открытое испытание на китайских детях. Helicobacter. 2020; 25: e12679. DOI: 10.1111 / hel.12679. [PubMed] [CrossRef] [Google Scholar] 107. Банг К.С., Лим Х., Чон Х.М., Шин В.Г., Чой Дж. Х., Со Дж. С., Кан Х. С., Ян Й. Дж., Хонг Дж. Т., Шин С. П. и др. Амоксициллин или тетрациклин в висмутсодержащей четверной терапии в качестве лечения первой линии для инфекции Helicobacter pylori . Кишечные микробы. 2020; 11: 1314–1323. DOI: 10.1080 / 194.2020.1754118. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 108. Романо М., Гравина А.Г., Нардоне Г., Федерико А., Даллио М., Марторано М., Мучерино К., Ромити А., Аваллоне Л., Граната Л. и др. Четырехкратная терапия без висмута и висмута, основанная на предыдущем воздействии кларитромицина, столь же эффективна и безопасна в области высокой устойчивости к кларитромицину: исследование в реальной жизни.Helicobacter. 2020; 25: e12694. DOI: 10.1111 / hel.12694. [PubMed] [CrossRef] [Google Scholar] 109. Tai W.C., Liang C.M., Bi K.W., Kuo C.M., Lu L..S., Wu C.K., Yang S.C., Kuo Y.H., Lee C.H., Huang C.F. и др. Сравнение четырехкомпонентной (сопутствующей) терапии на основе декслансопразола с модифицированным высвобождением и на основе лансопразола для эрадикации первой линии Helicobacter pylori : проспективное рандомизированное исследование. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 2923–2931. DOI: 10.2147 / IDR.S213998. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 110.Hsu P.I., Tsay F.W., Kao J.Y., Peng N.J., Tsai K.W., Tsai T.J., Kuo C.H., Kao S.S., Wang H.M., Chen Y.H. и др. Эквивалентная эффективность обратного гибрида и сопутствующей терапии в лечении первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2020 doi: 10.1111 / jgh.15034. [PubMed] [CrossRef] [Google Scholar] 111. Myint N., Zaw T.T., Sain K., Waiyan S., Danta M., Cooper D., Aung N.M., Kyi M.M., Hanson J. Sequential Helicobacter pylori эрадикационная терапия в Мьянме; рандомизированное клиническое испытание эффективности и переносимости.J. Gastroenterol. Гепатол. 2020; 35: 617–623. DOI: 10.1111 / jgh.14942. [PubMed] [CrossRef] [Google Scholar] 112. Зулло А., Фиорини Г., Скаччаноче Г., Портинкаса П., Де Франческо В., Вассалло Р., Урбан Ф., Моника Ф., Могаверо Г., Амато А. и др. Последовательная терапия для эрадикации первой линии Helicobacter pylori : 10- или 14-дневный режим? J. Gastrointestin. Печень. Дис. 2019; 28: 11–14. DOI: 10.15403 / jgld.2014.1121.281.hpy. [PubMed] [CrossRef] [Google Scholar] 113. Цай Ф.В., Ву Д.С., Ю Х.С., Kao S.S., Lin K.H., Cheng J.S., Wang H.M., Chen W.C., Sun W.C., Tsai K.W. и др. Рандомизированное контролируемое исследование показывает, что как 14-дневная гибридная, так и четырехкомпонентная терапия висмутом излечивают большинство пациентов с инфекцией Helicobacter pylori в группах населения со средней устойчивостью к антибиотикам. Противомикробный. Агенты. Chemother. 2017; 61: e00140-17. DOI: 10.1128 / AAC.00140-17. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 114. Нисида Т., Цудзи Ю., Окамото А., Томита Р., Хигаки Ю., Осуги Н., Сугимото А., Такахаши К., Мукаи К., Накамацу Д. и др. Лекарство с тройным лекарством в блистерной упаковке с вонопразаном улучшает эрадикацию первой линии Helicobacter pylori у пожилых пациентов: когортное исследование с ретроспективной оценкой склонности. Пищеварение. 2019: 1–7. DOI: 10,1159 / 000501608. [PubMed] [CrossRef] [Google Scholar] 115. Луо Л., Хуанг Ю., Лян Х., Цзи Ю., Ю. Л., Лу Х. Терапия на основе чувствительности для Helicobacter pylori -инфицированных пациентов с аллергией на пенициллин: проспективное клиническое испытание терапии первой линии и терапии спасения .Helicobacter. 2020; 25: e12699. DOI: 10.1111 / hel.12699. [PubMed] [CrossRef] [Google Scholar] 116. Kim SG, Jung HK, Lee HL, Jang JY, Lee H., Kim CG, Shin WG, Shin ES, Lee YC, Korean College of Helicobacter and Upper Gastrointestinal Research Guidelines для диагностики и лечения инфекции Helicobacter pylori в Корее , Редакция 2013 г. J. Gastroenterol. Гепатол. 2014; 29: 1371–1386. DOI: 10.1111 / jgh.12607. [PubMed] [CrossRef] [Google Scholar] 117. Като М., Ота Х., Окуда М., Кикучи С., Сато К., Шимояма Т., Судзуки Х., Ханда О., Фурута Т., Мабе К. и др. Руководство по лечению инфекции Helicobacter pylori в Японии: пересмотренное издание 2016 г. Helicobacter. 2019; 24: e12597. DOI: 10.1111 / hel.12597. [PubMed] [CrossRef] [Google Scholar]
Лучшая стратегия ликвидации Helicobacter pylori в эпоху устойчивости к антибиотикам
Антибиотики (Базель). 2020 Aug; 9 (8): 436.
Су Ён Ким
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; мок.revan @ 2121ezeerb
Джун-Вон Чунг
2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдон-даэро 774beon-gil, Намдонг-гу, Инчхон 21565, Корея
1 Отделение гастроэнтерологии, отделение внутренней медицины, Медицинский колледж Вонджу Университета Йонсей, 20 Ильсан-ро, Вонджу 26426, Корея; moc.revan@2121ezeerb2 Отделение гастроэнтерологии, Отделение внутренней медицины, Университет Гачон, Медицинский центр Гиль, 21, Намдонг-даэро 774beon-gil, Namdong-gu, Инчхон 21565, Корея
Поступило 30 июня 2020 г .; Принята в печать 21 июля 2020 г.
Лицензиат MDPI, Базель, Швейцария. Эта статья — статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution (CC BY) (http://creativecommons.org/licenses/by/4.0/). Эта статья цитировалась другими статьями в PMC. .Abstract
Устойчивость к антибиотикам является основной причиной неэффективности лечения Helicobacter pylori , а учащение случаев устойчивости к антибиотикам является проблемой для клиницистов. Особую проблему представляет устойчивость к кларитромицину и метронидазолу.Стандартная тройная терапия (ингибитор протонной помпы, амоксициллин и кларитромицин) больше не подходит в качестве лечения первой линии в большинстве регионов. Недавние рекомендации по лечению инфекции H. pylori
рекомендуют четырехкратную схему лечения (висмут или невисмут) в качестве терапии первой линии. Эта стратегия лечения эффективна для областей с высокой резистентностью к кларитромицину или метронидазолу, но частота резистентности неизбежно возрастает в результате длительной терапии несколькими антибиотиками.Новая терапия на основе калий-конкурентных блокаторов кислоты может быть эффективной, но данные ограничены. Индивидуальная терапия, основанная на результатах теста на чувствительность к противомикробным препаратам, является идеальным вариантом. В этом обзоре обсуждались текущие важные схемы лечения H. pylori и оптимальная стратегия эрадикации H. pylori .Ключевые слова: Helicobacter pylori , устойчивость к антибиотикам, эрадикация
1. Введение
Helicobacter pylori — грамотрицательная, жгутиковая, спиралевидная бактерия, проникающая в слизистую оболочку верхнего отдела желудочно-кишечного тракта [1] , 2].Он вызывает пептические язвы, рак желудка и другие желудочные заболевания [3,4] и составляет 25% всех злокачественных новообразований, связанных с инфекциями; это также связано с повышенным риском рака желудочно-кишечного тракта [5]. Искоренение H. pylori облегчает язвенную болезнь и снижает риск рака желудка [6,7]. В глобальном масштабе рекомендации по лечению H. pylori постепенно меняются, а показания расширяются [4,8,9,10]. Кроме того, с экономическим развитием многих развивающихся стран и увеличением старения населения количество людей, получающих H.pylori увеличивается.
В 1990-х годах тройная терапия, состоящая из ингибитора протонной помпы (ИПП), кларитромицина и амоксициллина, была введена для искоренения инфекции H. pylori и в настоящее время является стандартом во всем мире [11,12]. С тех пор уровень искоренения тройной терапии во многих регионах заметно снизился [13,14]. Причины этого снижения включают бактериальные факторы, повторное инфицирование, генетический полиморфизм CYP2C19 и соблюдение пациентом режима лечения [15].Устойчивость к антибиотикам является наиболее важной причиной неудач лечения H. pylori [13,16]. Резистентность к кларитромицину H. pylori особенно серьезна; Схемы, содержащие кларитромицин, больше не подходят из-за степени эрадикации <80% [14,17]. Уровень устойчивости к метронидазолу и хинолонам (которые в основном используются в качестве схем второго или третьего ряда) во всем мире составляет> 15% [14,16]. Поскольку количество антибиотиков, подходящих для эрадикации H. pylori , ограничено (кларитромицин, амоксициллин, метронидазол, левофлоксацин, тетрациклин и рифабутин), повышение устойчивости к антибиотикам является серьезной проблемой.Следовательно, исключения кларитромицина недостаточно для предотвращения устойчивости к антибиотикам H. pylori .
Текущие руководства подчеркивают важность местной распространенности устойчивости к антибиотикам при выборе подходящей схемы лечения H. pylori [4,9,10]. В регионах с высокой устойчивостью к определенным антибиотикам успех лечения можно улучшить, отказавшись от использования таких антибиотиков. Однако, хотя новая комбинация антибиотиков может повысить скорость эрадикации, она может вызвать резистентность.Правительство Тайваня ограничило использование противомикробных препаратов, что привело к низкому уровню первичной устойчивости к кларитромицину и метронидазолу у H. pylori [18]. Однако частота первичной устойчивости к левофлоксацину увеличилась с 4,9% в 2000–2007 гг. До 13,4% в 2011–2012 гг. [18]. Кроме того, использование нескольких антибиотиков увеличивает частоту осложнений [4]. Поэтому важно определить оптимальную стратегию эрадикации H. pylori в соответствии с результатами теста на антибактериальную чувствительность (AST).Однако возможность ложноотрицательных результатов и возможность применения во всех медицинских учреждениях являются проблемой [19,20]. Мы рассмотрели наиболее важные схемы лечения против H. pylori , которые преодолевают устойчивость к антибиотикам, и стратегии, которые можно применять на практике.
2.
H. pylori Лечение на основе результатов ASTБактериальный посев обычно проводится перед выбором антибиотика, но посев H. pylori сложен и требует много времени. Исследование чувствительности к кларитромицину H.pylori улучшает скорость эрадикации [21,22]. Герритс и др. с помощью полимеразной цепной реакции (ПЦР) показали, что мутации A2142G и A2143G в 23S рРНК связаны с устойчивостью к антибиотикам [22]. ПЦР сравнительно прост и экономичен [21]. Следовательно, для H. pylori лечение на основе AST, такое как диагностический тест на устойчивость к кларитромицину, является полезным. Однако в некоторых случаях уровень эрадикации составляет <100%. Это связано с тем, что точечные мутации, отличные от A2142G или A2143G, приводят к ненадежным результатам, например.g., A2142C, A2115G, G2142T, A2142T и T2182C [23,24]. Кроме того, распространение мутаций отличается географически. Мутация A2142C встречается <10% в США и Европе, но не зарегистрирована в Японии [25,26,27,28]. В Гонконге частота мутации A2144G выше, чем в других регионах [29]. Различное распределение этих мутаций, вероятно, влияет на скорость эрадикации.
Терапия H. pylori , основанная на результатах AST, значительно улучшает скорость эрадикации.Однако, в отличие от других схем, мало исследований оценивали схемы первого ряда на основе АСТ. Уровень искоренения намерения лечить (ITT) для схемы первого ряда составляет> 90% [30,31,32]. В Южной Корее индивидуализированная терапия первой линии на основе ПЦР превосходит стандартную тройную терапию (STT; амоксициллин, кларитромицин и ИПП) [30,31]. В греческом исследовании тройная терапия на основе генотипической резистентности (определение чувствительности к кларитромицину и левофлоксацину с помощью анализа GenoType HelicoDR) позволила достичь высокого уровня H.pylori (90,2% по ITT и 97,8% по протоколу (PP) анализа) [32]. Кроме того, тройные схемы первой линии под контролем АСТ приводят к эрадикации> 90% у пациентов с H. pylori , устойчивым к двум антибиотикам [33]. Поскольку частота полирезистентности H. pylori увеличивается, это обнадеживающее открытие. Схемы первой линии эрадикации H. pylori на основе культивирования демонстрируют превосходный терапевтический эффект даже в регионах с высоким уровнем устойчивости к противомикробным препаратам [34].Общие показатели устойчивости к амоксициллину, кларитромицину, метронидазолу и моксифлоксацину составляют 6,7%, 31,0%, 41,8% и 39,2% соответственно. Однако уровень эрадикации составляет 93,1% (ITT) и 100,0% (PP) [34]. Chen et al. сообщили, что управляемый по чувствительности модифицированный четырехкратный режим висмута первой линии для H. pylori в регионе с высокой степенью устойчивости к противомикробным препаратам имел высокий уровень эрадикации [35].
Показатель успеха схем второго ряда / спасения под контролем AST ниже, чем у схем первого ряда.Уровень эрадикации низкий (68%), несмотря на тестирование чувствительности для лечения спасения [36]. Аналогичным образом, в Соединенных Штатах терапия с культуральным контролем показала 60% -ный успех у пациентов, у которых не удалось по крайней мере три лечения [37]. Даже если посев определяет чувствительность к кларитромицину, повторный анализ кларитромицина после неудачи лечения не рекомендуется [38]. Следовательно, одна только терапия под контролем АСТ не может достичь требуемой скорости эрадикации. Liou et al. показали, что терапия с учетом генотипа не была значительно более эффективной, чем эмпирическая терапия для стратегии спасательной терапии (78.0% против 72,2%, p = 0,170) [39]. Следовательно, соответствующая эмпирическая терапия является альтернативой индивидуализированной генотипической терапии рефрактерной инфекции H. pylori .
3. Четырехкратная терапия висмутом
Четырехкратная терапия висмутом (BQT) состоит из висмута, PPI, метронидазола и тетрациклина. Он рекомендован как схема первой линии Торонтским консенсусом, Маастрихтским V / Флорентийским консенсусом и рекомендациями Американского колледжа гастроэнтерологии (ACG) [4,9,10].На режим BQT не влияет резистентность к кларитромицину. Согласно сетевому метаанализу, BQT в течение 10 или 14 дней превосходит STT в течение 7 дней [40]. Более того, BQT очень эффективен в качестве эмпирической схемы первого ряда (уровень эрадикации PP и ITT составляет 98,8% и 92,7% соответственно) [41]. Рандомизированное контролируемое исследование (РКИ) на Тайване показало, что уровень эрадикации у пациентов, получавших BQT, составил 96,0%, хотя частота нежелательных явлений составила 47,7% [42]. BQT оказался высокоэффективным в качестве схемы первого ряда для H.pylori в проспективном исследовании в Испании (94,4% (ITT) и 96,2% (PP)) [43]. BQT имеет отличную скорость эрадикации H. pylori , но комплаентность пациента может быть снижена из-за большого количества лекарств. Кроме того, BQT вводят четыре раза в день, что также может снизить комплаентность пациента. Чтобы преодолеть это, были введены схемы приема BQT два раза в день, и исследования в Южной Корее продемонстрировали их эффективность [44,45]. Kim et al. продемонстрировали, что два раза в день BQT в течение 1 недели был так же эффективен и безопасен, как традиционный четырехкратный ежедневный BQT (93.9% против 92,9%) [45]. Кроме того, большинство пациентов демонстрируют хорошую комплаентность, а уровень эрадикации BQT два раза в день высок (88,2% (ITT) и 98,4% (PP)) [44]. Разработана единая капсула, содержащая висмут, метронидазол и тетрациклин. Xie et al. показали, что терапия BQT одной капсулой была эффективной для эрадикации H. pylori и хорошо переносилась (86,5% (ITT) и 94,6% (PP)) [46]. В итальянском исследовании однокапсульная терапия BQT позволила достичь уровня эрадикации 91% (ITT) и 97% (PP) [47].Согласно метаанализу, при терапии BQT с одной капсулой первого и второго ряда уровень эрадикации приближался к 90%. Даже это применимо, независимо от типа и дозы ИПП, у пациентов со штаммом, резистентным к антибиотикам, и у тех, кто ранее лечился кларитромицином [48]. При 7-дневной схеме лечения BQT второго ряда уровень эрадикации составляет 93,6% (PP). Скорость эрадикации 7-дневного BQT значительно выше, чем у 14-дневного моксифлоксацина, содержащего тройной режим (93,6% против 73,8% (PP), p <0.001) [49].
Неясно, улучшится ли скорость эрадикации при увеличении периода лечения с 7 до 14 дней. Маастрихтский V / Флорентийский консенсус рекомендует прием препарата в течение не менее 10 дней [10]. Сообщается, что уровень устойчивости к тетрациклину во всем мире низкий [50,51]. Следовательно, устойчивость к метронидазолу является основным фактором успеха эрадикации H. pylori . Устойчивость к метронидазолу можно преодолеть путем увеличения частоты, количества и продолжительности приема, поэтому лечение в течение ≥10 дней рекомендуется в регионах с высокой степенью устойчивости к метронидазолу [52].
BQT показал отличные результаты в различных исследованиях, и сфера его применения постепенно расширяется. Кроме того, BQT можно относительно безопасно применять у пациентов с аллергией на пенициллин [4]. Сообщается, что BQT имеет более высокий уровень нежелательных явлений, чем STT, но схожий уровень соблюдения пациентом режима лечения [53,54]. Однако, поскольку показания BQT расширяются в качестве лечения первой линии, также возникают опасения. Количество схем второго ряда, которые можно применять, значительно сокращается, когда эрадикация с помощью BQT не дает результатов по первой линии.Кроме того, в будущем может повыситься уровень устойчивости к тетрациклину, который в настоящее время является относительно низким. Для решения этой проблемы в будущем необходимы различные исследования.
4. Сопутствующая терапия
Рекомендуется одновременное введение трех антибиотиков (кларитромицин, метронидазол или нитроимидазол и амоксициллин) и ИПП в течение 10–14 дней [4,9,10]. Несколько метаанализов показали, что сопутствующая терапия превосходит STT [55,56,57].Кроме того, недавний метаанализ показал, что сопутствующая терапия в течение 5 или 10 дней превосходила STT в течение 5, 7 или 10 дней [58]. Испанское исследование продемонстрировало, что сопутствующая терапия была значительно лучше, чем тройная терапия (92% против 70% (ITT), p = 0,02 и 92% против 74% (PP), p = 0,05) и эрадикация Скорость сопутствующей терапии была выше, чем у последовательной терапии устойчивых к антибиотикам штаммов [59]. Кроме того, сопутствующая терапия и BQT в качестве схем первого ряда показали сходные результаты H.pylori в анализах PP (97,7% против 96,2%, p = 0,605) и ITT (98,0% против 94,4%, p = 0,346) [43]. Более того, сетевой метаанализ показал, что сопутствующая терапия имеет более высокую эффективность, чем несколько других схем [40,60].
Сопутствующая терапия предпочтительнее последовательной терапии (ИПП и амоксициллин в течение 5 дней, затем ИПП, кларитромицин и тинидазол в течение еще 5 дней), потому что это проще. Существуют разногласия по поводу того, превосходит ли сопутствующая терапия над последовательной терапией [61,62,63,64,65].В испанском РКИ сопутствующая терапия была незначительно лучше (~ 5%) по сравнению с последовательной терапией (87% против 81% (ITT), p = 0,15; 91% против 86% (PP), p = 0,131) [65]. Кроме того, два метаанализа не выявили значительной разницы в скорости эрадикации между сопутствующей терапией и последовательной терапией [66,67].
Маастрихтский / Флорентийский консенсус не рекомендует последовательную терапию, в отличие от предыдущих руководств [10]. Это связано с тем, что последовательная терапия имеет более низкий уровень эрадикации, чем сопутствующая терапия в случаях резистентности к кларитромицину и чувствительности к метронидазолу H.pylori . И наоборот, когда H. pylori чувствителен к кларитромицину и устойчив к метронидазолу, последовательная терапия показывает более низкий уровень эрадикации, чем STT [10]. Увеличение дозы или продолжительности лечения метронидазолом может привести к эрадикации метронидазол-резистентного H. pylori . Скорость эрадикации при последовательной терапии невысока, поскольку период приема метронидазола составляет всего 5 дней.
Сопутствующая терапия имеет несколько ограничений, таких как более высокая частота нежелательных явлений, чем последовательная терапия [68].Повышенная частота осложнений может повлиять на соблюдение режима лечения H. pylori [69,70]. Хотя частота нежелательных явлений относительно высока, период лечения составляет менее 2 недель, поэтому большинство пациентов завершают курс лечения. Кроме того, есть опасения, что устойчивость к антибиотикам может повыситься из-за чрезмерного воздействия ненужных антибиотиков [71]. Наконец, эффекты сопутствующей терапии ниже у H . pylori, устойчивы как к кларитромицину, так и к метронидазолу [72].
5. Гибридная терапия
Гибридная терапия — это комбинация последовательной и сопутствующей терапии. Гибридная терапия включает ИПП и амоксициллин в течение 7 дней, затем ИПП, амоксициллин, кларитромицин и метронидазол в течение 7 дней [4]. Хотя Торонтский консенсус и Маастрихтский / Флорентийский консенсус не рекомендуют гибридную терапию, в клинических рекомендациях ACG рекомендуется использовать ее в качестве лечения первой линии у пациентов без предварительного воздействия макролидов в регионах с низким уровнем устойчивости к кларитромицину.Несколько метаанализов сообщили об эффективности и переносимости гибридной терапии [40,67,73]. Wang et al. продемонстрировали, что гибридная терапия была альтернативой сопутствующей или последовательной терапии (уровни эрадикации ITT гибридной, сопутствующей и последовательной терапии составили 88,6%, 86,3% и 84,7% соответственно; частота эрадикации PP составила 92,1%, 92,5% и 87,5%. ) [73]. Кроме того, нет значительных различий в переносимости или комплаентности между гибридной терапией и STT, последовательными или сопутствующими схемами [40,67,73].
В проспективном многоцентровом исследовании гибридная терапия вылечила> 90% пациентов с инфекцией H. pylori в регионах с высокими показателями устойчивости к кларитромицину и метронидазолу; это похоже на скорость эрадикации сопутствующей терапии [74]. Кроме того, комплаентность к гибридной терапии выше, чем к сопутствующей терапии (98,8% против 95,2%, p = 0,05). Однако скорость искоренения гибридной терапии значительно ниже для H.pylori . В проспективном исследовании частота эрадикации у пациентов с двойной устойчивостью к антибиотикам (кларитромицину и метронидазолу) была заметно снижена (50%) по сравнению с пациентами с резистентностью только к кларитромицину (91,4%) или метронидазолу (90,5%) [75].
6. Терапия на основе левофлоксацина
Левофлоксацин активен в отношении большого спектра различных бактерий, и в некоторых исследованиях левофлоксацин используется в качестве средства первой линии лечения инфекции H. pylori [15]. Проспективное исследование в Китае показало, что цефуроксим, левофлоксацин, ИПП и висмут в качестве терапии первой линии позволили достичь H.pylori составляет 97,2% случаев чувствительности к левофлоксацину и 84,0% случаев резистентности к левофлоксацину [76]. Однако в случаях устойчивости к цефуроксиму и левофлоксацину уровень эрадикации составил 0%. 14- и 7-дневные режимы дозирования левофлоксацина (левофлоксацин, кларитромицин, рабепразол и висмут) один раз в сутки показали уровень эрадикации 94% и 84% соответственно [77]. Gan et al. сравнили эффективность различных доз левофлоксацина для эрадикации H.pylori [78]. Показатели эрадикации в группах, получавших один и два раза в день, составили 77,5% и 79,5% (ITT) и 82,9% и 86,4% (PP), соответственно [78]. Нет значительных различий в степени искоренения или соблюдения режима лечения. Бычий лактоферрин усиливает эффективность схем первой линии на основе левофлоксацина при инфекции H. pylori [79]. Успешная эрадикация составляет 96,1% для эзомепразола / амоксициллина / левофлоксацина / бычьего лактоферрина и 75% для эзомепразола / амоксициллина / левофлоксацина [79].Режим LOAD (левофлоксацин, омепразол, нитазоксанид и доксициклин) был введен недавно [71]. Basu et al. сообщили, что уровень эрадикации LOAD составил 89,4% по сравнению с 73,3% для STT ( p <0,05) [80].
Левофлоксацин представляет собой хинолон и широко используется во всем мире, например, при пневмонии, инфекции мочевыводящих путей, туберкулезе и H. pylori . Таким образом, многие пациенты в анамнезе принимали левофлоксацин. В большинстве руководств рекомендуется применять схемы на основе левофлоксацина в качестве экстренной помощи, а не в качестве терапии первой линии [81].Клинические рекомендации ACG слабо рекомендуют тройной (амоксициллин, левофлоксацин и ИПП), последовательный (5-7 дней ИПП и амоксициллин, затем 5-7 дней ИПП, нитроимидазол и левофлоксацин) или четырехкратный (амоксициллин, левофлоксацин и ИПП). ИПП, левофлоксацин, доксициклин и нитазоксанид в течение 7 или 10 дней) по схемам первого ряда [4].
Ситафлоксацин представляет собой фторхинолон четвертого поколения и обладает высокой активностью против штаммов gyr A с положительной мутацией H. pylori [82].Ситафлоксацин в основном используется с амоксициллином или метронидазолом в качестве экстренной помощи, а не терапии первой линии. Сообщается, что схемы третьей линии, содержащие ситафлоксацин, эффективны для эрадикации H. pylori (75,8% (ITT) и 83,3% (PP)) [83]. Фторхинолоны четвертого поколения, такие как ситафлоксацин и гареноксацин, могут преодолеть устойчивость к хинолонам H. pylori [84,85]. Среди 100 штаммов с высокими показателями устойчивости к кларитромицину, метронидазолу и левофлоксацину> 95% чувствительны к ситафлоксацину [86].Следует оценить эффективность схем, содержащих ситафлоксацин или гареноксацин, против gyr A с положительной мутацией H. pylori .
7. Терапия на основе рифабутина
Рифабутин — это производное рифамицина, структурно сходное с рифампицином (противотуберкулезным препаратом). Он в основном используется при атипичном туберкулезе, таком как Mycobacterium avium -intracellulare и M. tuberculosis , устойчивых к рифампицину [87]. Рифабутин подавляет синтез белка путем ингибирования бета-субъединицы ДНК-зависимой РНК-полимеразы Helicobacter , которая кодируется rpoB .Следовательно, мутация rpoB придает устойчивость к рифабутину [88]. Все существующие руководящие принципы предполагают, что схемы на основе рифабутина следует рассматривать только как терапию «спасения» при эрадикации H. pylori [81]. Согласно метаанализу, эффективность лечения на основе рифабутина второй, третьей и четвертой / пятой линий составляет 79%, 66% и 70% соответственно [87]. В итальянском исследовании тройная терапия на основе рифабутина (рифабутин, амоксициллин и ИПП) в течение 14 дней позволила достичь скорости эрадикации 72.7% (PP) и 71,5% (ITT) у пациентов, у которых эрадикация H. pylori оказалась неэффективной после лечения традиционными антибиотиками [89]. Рифабутин не обладает такой же устойчивостью к антибиотикам, как кларитромицин и амоксициллин, а также является жирорастворимым и легко всасывается после перорального приема [88, 90]. Кроме того, рифабутин стабилен в широком диапазоне значений pH и не разлагается желудочной кислотой, а уровень устойчивости у H. pylori низкий, поскольку он редко используется в клинических условиях [87,91]. Следовательно, схемы на основе рифабутина важны для спасательной терапии.Однако другое исследование показало, что уровень искоренения терапии на основе рифабутина был невысоким: 50,0% в анализе ITT и 54,5% в анализе PP [92]. Поскольку есть некоторые части, которые не достигают стабильной скорости эрадикации в качестве спасательной терапии, можно считать, что необходимы соответствующие исследования.
На сегодняшний день большинство исследований схем на основе рифабутина сосредоточено на спасательной терапии. Недавно Graham et al. показали, что тройная схема на основе рифабутина (амоксициллин, рифабутин и ИПП) имела более высокий уровень эрадикации, чем амоксициллин плюс ИПП в качестве эмпирического лечения первой линии H.pylori (83,8% против 57,7%, p <0,001) [93]. Это говорит о том, что рифабутин является революционным препаратом первой линии в эпоху устойчивости к антибиотикам. Однако он дороже других антибиотиков. Кроме того, он может вызвать устойчивость к режиму лечения туберкулеза [94]. Более того, поскольку использование рифампицина способствует точечной мутации rpoB и увеличивает минимальную ингибирующую концентрацию (МИК) рифабутина, перед назначением рифабутина необходимо определить предшествующее лечение рифампицином [95].Наконец, рифабутин имеет небольшой риск миелотоксичности [87].
8. Терапия на основе калий-конкурентных кислотных блокаторов
Калий-конкурентные кислотные блокаторы (P-CAB) — это ингибитор секреции кислоты желудочного сока, с более быстрым началом и более длительным действием подавления кислоты, и более эффективен, чем ИПП. [96,97]. Кроме того, P-CAB не требует активации желудочной кислотой, поэтому его можно принимать независимо от времени приема пищи. В обращении H . pylori, pH желудка должен поддерживаться выше определенного уровня, чтобы активировать антибиотик [98].P-CAB ингибирует опосредованную H + и K + -АТФазу секрецию кислоты желудочного сока и является кислотоустойчивым и менее подвержен влиянию системы CYP2C19, чем ИПП [71,99]. Поскольку ИПП имеют короткую продолжительность действия и на их эффективность влияют различные подтипы цитохрома Р450 (ИПП в основном метаболизируются CYP2C19 и CYP3A4), внимание привлекла новая схема лечения против H. pylori , содержащая PCAB [99,100]. Вонопразан в настоящее время продается в Японии, продвигая исследования P-CAB для H.pylori лечение.
По данным многоцентрового РКИ в Японии, частота эрадикации первой линии тройной терапии на основе фонопразана (фонопразан, амоксициллин и кларитромицин) составила 92,6% по сравнению с 75,9% для STT ( p <0,0001) [101]. Метаанализ японских исследований с участием 1599 пациентов показал, что тройная терапия на основе фонопразана значительно превосходила STT у пациентов с устойчивыми к кларитромицину штаммами (82,0% против 40,0%, p <0,0001) [102].Напротив, уровень эрадикации чувствительных к кларитромицину штаммов существенно не отличается. Если организм устойчив к кларитромицину, STT переключается на двойную терапию (ИПП + амоксициллин), и двойная терапия важна для поддержания pH желудочного сока на уровне ≥6. В этом отношении считается, что у вонопразана есть сильные стороны. Кроме того, тройная схема на основе фонопразана так же эффективна, как и STT на основе ИПП на основе чувствительности, для эрадикации H. pylori (97,4% против 95,7%) [103]. В исследовании эффективности двойной терапии 7-дневного фонопразана и низких доз амоксициллина в качестве препарата первой линии H.pylori , уровни эрадикации двойной (фонопразан и низкие дозы амоксициллина) и тройной терапии (фонопразан, амоксициллин с низкой дозой и кларитромицин) составили 84,5% и 89,2% ( p = 0,203) по ITT-анализу соответственно. и 87,1% и 90,2% ( p = 0,372) по данным PP-анализа, соответственно [104]. В реальности увеличения устойчивости к противомикробным препаратам можно сказать, что снижение общего количества антибиотиков с использованием вонопразана показывает положительный аспект в будущем лечении H.pylori .
В Японии схемы на основе P-CAB лицензированы в качестве лечения первого и второго ряда для эрадикации H. pylori . Мураками и др. продемонстрировали эффективность тройной схемы второго ряда на основе P-CAB (частота успеха 98,0%) [101]. Другое РКИ показало, что тройная терапия на основе фонопразана (фонопразан, амоксициллин и ситафлоксацин) была более эффективной, когда ИПП использовался с этими антибиотиками в качестве схемы лечения третьей линии для H. pylori (83,3% против 57.1% (PP), p = 0,043) [83]. Следовательно, терапия на основе P-CAB может быть жизнеспособной альтернативой схемам первого и второго ряда для эрадикации H. pylori .
9. Лечение при неэффективности первичной терапии
Все руководства рекомендуют избегать ранее принимаемых пациентом антибиотиков [4,8,9,10]. В частности, следует избегать повторного использования кларитромицина и левофлоксацина из-за высоких показателей устойчивости. Они также рекомендуют схему лечения тройной второй линии на основе BQT или левофлоксацина для H.pylori [81]. Если терапия первой или второй линии оказалась неэффективной, следует рассмотреть возможность проведения теста на восприимчивость к соответствующей терапии экстренной помощи [10,81].
Согласно Маастрихтскому / Флорентийскому консенсусу, после неэффективности BQT в качестве терапии первой линии рекомендуется трех- или четырехкратная терапия, содержащая хинолон [10]. После неэффективности четырехкомпонентного режима без висмута первой линии рекомендуется трех- или четырехкратный режим, содержащий BQT или хинолон [10]. BQT, четырехкомпонентная терапия без висмута и трехкомпонентная терапия, содержащая хинолоны, могут использоваться без перекрытия со схемами лечения второй или третьей линии [10].
Торонтский консенсус и рекомендации ACG, такие как Маастрихтский V / Флорентийский консенсус, подчеркивают важность BQT и левофлоксацин-содержащих схем лечения в качестве препаратов второго ряда [4,9]. Важным отличием от Маастрихтского V / Флорентийского консенсуса является возражение против использования четырехкратной схемы второго ряда без висмута, поскольку это менее эффективно, чем другие методы лечения [9]. Кроме того, схемы на основе рифабутина следует использовать только для пациентов, у которых в прошлом было не менее трех неудач лечения [9].В рекомендациях ACG указывается, что режим второго ряда следует выбирать на основе предыдущего воздействия антибиотиков и данных о местной устойчивости к антибиотикам [4].
10. Выводы
обобщает важные схемы лечения H. pylori . Лечение H. pylori — важная глобальная проблема, потому что оно было напрямую связано как причина нескольких желудочно-кишечных заболеваний. Существует явная озабоченность по поводу увеличения показателей устойчивости с течением времени, что подчеркивает необходимость использования подходящих антибиотиков в будущем, чтобы минимизировать дальнейший рост устойчивости к антибиотикам.Специальная терапия на основе AST показала хорошую скорость эрадикации при применении первой линии. Поскольку уровень устойчивости к антибиотикам H. pylori увеличивается, следует расширить роль индивидуализированных методов лечения. Однако, если индивидуальная терапия не может быть применена ко всем пациентам из-за реальных проблем, разумной альтернативой является использование высокоэффективного эмпирического режима на местном уровне. Кроме того, при использовании такой эмпирической схемы необходима простая и эффективная стратегия лечения H. pylori .Поэтому мы предлагаем BQT в качестве терапии первой линии, когда данные по AST или региональной резистентности недоступны (). Если BQT недоступен, мы предлагаем эмпирическую сопутствующую терапию. P-CAB может быть альтернативой, но данные немногочисленны и ограничены Восточной Азией.
Упрощенная стратегия лечения H. pylori .
Таблица 1
Схемы лечения инфекции Helicobacter pylori .
| Лечение | Схема | Продолжительность | Недавняя частота эрадикации первой линии (ITT) | Рекомендации в соответствии с Руководством | Примечания | |
|---|---|---|---|---|---|---|
| Стандартная тройная терапия (STT) | Стандартная тройная терапия (STT) | Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день | 7–14 дней | 63.9% [105], 74,1% [106] | Первая линия: необязательно рекомендована KCHUGR и JSHR Спасательная операция: ограничена рекомендована MAA | За последние 20 лет эффективность STT заметно снизилась, и STT обычно не рекомендуется в качестве схемы первого ряда |
| Квартальная терапия висмутом (BQT) | Стандартная доза ИПП 2 раза в день Стандартная доза висмута 4 раза в день Метронидазол 500 мг 3 раза в день Тетрациклин 500 мг 4 раза в день | 7–14 дней | .8% [107], 88,2% [44], 91,5% [108] Первая линия: рекомендовано ACG, MAA, TOR и KCHUGR (необязательно) Rescue: рекомендовано ACG, MAA, TOR и KCHUGR | BQT был предложен в качестве варианта лечения первой линии во многих руководствах, особенно для регионов с высокой устойчивостью к кларитромицину. | ||
| Сопутствующая терапия (четырехкратная терапия без висмута) | Стандартная доза ИПП 2 раза в день Кларитромицин 500 мг 2 раза в день Амоксициллин 1 г 2 раза в день Метронидазол 500 мг 2 раза в день | 10–14 дней | 84.6% [106], 90,1% [109], 93,5% [110] | Первая линия: рекомендовано ACG, MAA и TOR Спасение: рекомендовано ACG и MAA | Скорость искоренения превосходит это CTT, а метод введения прост по сравнению с последовательной терапией. Но побочные эффекты могут быть более вероятными при сопутствующей терапии. | |
| Последовательная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день (только первая половина) Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 10–14 д | 69.5% [106], 82,0% [111], 87,0% [112] | Первая линия: необязательно рекомендуется (не идеально) ACG Спасение: не рекомендуется во всех руководствах | В качестве терапии первой линии роль постепенно исчезает. Это обременительный способ снизить комплаентность пациента. | |
| Гибридная терапия | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Кларитромицин 500 мг 2 раза в день (только для второй половины) Метронидазол 500 мг 2 раза в день (только для второй половины) | 14 дней | 85.8% [75], 92,8% [113] | Первая линия: необязательно рекомендуется (не идеально) ACG Rescue: не рекомендуется во всех руководствах | Это метод, сочетающий последовательную терапию и сопутствующую терапию. | |
| Терапия на основе левофлоксацина | Левофлоксацин можно назначать в виде тройной или четырехкратной терапии. | 10–14 дней | 85,5% [76], 94,0% [77] | Первая линия: рекомендована ACG Rescue: рекомендована ACG, MAA и TOR | В большинстве руководств рекомендуется проводить терапию на основе левофлоксацина. применяется как терапия спасения, а не как первая линия.Он менее эффективен для областей с высокой устойчивостью к хинолонам. | |
| Терапия на основе рифабутина | Стандартная доза ИПП 2 раза в день Амоксициллин 1 г 2 раза в день Рифабутин 150 мг 2 раза в день | 10 дней | 83,8% [93] | Первая линия: не рекомендуется во всех рекомендациях Спасение: необязательно (третья или четвертая линия) по MAA и TOR | Все руководства рекомендуют терапию на основе рифабутина в качестве терапии спасения. Рифабутин имеет редкий риск миелотоксичности; поэтому требуется осторожное использование. | |
| Терапия на основе калий-конкурентных кислотных блокаторов | P-CAB можно назначать как тройную терапию или четырехкратную терапию, заменяя PPI на P-CAB. | 7–14 d | 89,2% [104], 90,2% [114] | Не указано в алгоритме руководящих принципов | Ожидается, что роль мощного подавления кислоты будет постепенно возрастать, и необходимы дополнительные исследования. | |
| Лечение H. pylori на основе теста на антибактериальную чувствительность | Индивидуальная терапия в соответствии с результатами AST | 7–14 дней | 92.7% [31], 92,9% [115] | MAA рекомендует проводить АСТ после неэффективности терапии второй линии. | Результаты индивидуализированной терапии на основе AST превосходны, и ожидается, что она сыграет роль в улучшении лечения H. pylori в будущем. Требуются усилия для облегчения применения AST в клинической практике. |
Индивидуальная терапия, согласно результатам AST, способствует лечению H. pylori без повышения устойчивости к антибиотикам, поэтому следует уделять особое внимание тестированию на чувствительность.Есть также дополнительные соображения; например, как установить продолжительность лечения при чувствительности к кларитромицину и как выбрать режим (BQT или амоксициллин-метронидазол-ИПП), если устойчивость к кларитромицину не изучалась. Дальнейшая работа должна быть сосредоточена на максимальном терапевтическом эффекте индивидуализированной терапии, основанной на результатах AST.
Вклад авторов
S.Y.K. написал рукопись, и J.-W.C. способствовал разработке концепции и дизайна исследования. Все авторы прочитали и согласились с опубликованной версией рукописи.
Финансирование
Это исследование было поддержано Программой фундаментальных научных исследований через Национальный исследовательский фонд Кореи (NRF), финансируемым Министерством образования (номер гранта: 2020R1I1A306686511) и Исследовательским фондом Кореи (NRF), финансируемым Министерством образования. Образование (номер гранта: 2020R1F1A1076839).
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
1. Кандульски А., Селград М., Малфертхайнер П. Инфекция Helicobacter pylori : клинический обзор. Копать землю. Печень. Дис. 2008. 40: 619–626. DOI: 10.1016 / j.dld.2008.02.026. [PubMed] [CrossRef] [Google Scholar] 2. Макколл К. Клиническая практика. Инфекция Helicobacter pylori . N. Engl. J. Med. 2010; 362: 1597–1604. DOI: 10.1056 / NEJMcp1001110. [PubMed] [CrossRef] [Google Scholar] 3. Пламмер М., Франчески С., Винья Дж., Форман Д., де Мартель С. Глобальное бремя рака желудка, связанное с Helicobacter pylori . Int.J. Рак. 2015; 136: 487–490. DOI: 10.1002 / ijc.28999. [PubMed] [CrossRef] [Google Scholar] 4. Чей В.Д., Леонтиадис Г.И., Хауден К.В., Мосс С.Ф. Клинические рекомендации ACG: Лечение инфекции Helicobacter pylori . Являюсь. J. Gastroenterol. 2017; 112: 212–239. DOI: 10.1038 / ajg.2016.563. [PubMed] [CrossRef] [Google Scholar] 5. Тестерман Т.Л., Моррис Дж. За пределами желудка: обновленный взгляд на патогенез, диагностику и лечение Helicobacter pylori . Мир J. Gastroenterol. 2014; 20: 12781–12808.DOI: 10.3748 / wjg.v20.i36.12781. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ли Ю.К., Чан Т.Х., Чжоу С.К., Ту Ю.К., Ляо В.С., Ву М.С., Грэм Д.Ю. Связь между Helicobacter pylori Эрадикация и заболеваемость раком желудка: систематический обзор и метаанализ. Гастроэнтерология. 2016; 150: 1113–1124. DOI: 10.1053 / j.gastro.2016.01.028. [PubMed] [CrossRef] [Google Scholar] 7. Судзуки Х., Нисидзава Т., Хиби Т. Эрадикационная терапия Helicobacter pylori . Будущее.Microbiol. 2010. 5: 639–648. DOI: 10.2217 / fmb.10.25. [PubMed] [CrossRef] [Google Scholar] 8. Ким С.Г., Юнг Х.К., Ли Х.Л., Чан Дж.Й., Ли Х., Ким С.Г., Шин В.Г., Шин Э.С., Ли Ю.С. Корейский колледж хеликобактер и исследований верхних отделов желудочно-кишечного тракта. Корейский J. Gastroenterol. 2013; 62: 3–26. DOI: 10.4166 / kjg.2013.62.1.3. [PubMed] [CrossRef] [Google Scholar] 9. Фаллон К.А., Чиба Н., ван Зантен С.В., Фишбах Л., Гисберт Дж. П., Хант Р. Х., Джонс Н. Л., Рендер К., Леонтиадис Г. И., Моайеди П. и др. Торонтский консенсус по лечению инфекции Helicobacter pylori у взрослых.Гастроэнтерология. 2016; 151: 51–69. DOI: 10.1053 / j.gastro.2016.04.006. [PubMed] [CrossRef] [Google Scholar] 10. Малфертхайнер П., Мегро Ф., О’Морайн С.А., Гисберт Дж. П., Койперс Э. Дж., Аксон А. Т., Баццоли Ф., Гасбаррини А., Атертон Дж., Грэм Д. Ю. и др. Управление инфекцией Helicobacter pylori — Маастрихт V / Флорентийский консенсусный доклад. Кишечник. 2017; 66: 6–30. DOI: 10.1136 / gutjnl-2016-312288. [PubMed] [CrossRef] [Google Scholar] 11. Гисберт Дж. П., Гонсалес Л., Кальвет X., Гарсия Н., Лопес Т., Roque M., Gabriel R., Pajares J.M. Ингибитор протонной помпы, кларитромицин и амоксициллин или нитроимидазол: метаанализ эрадикации Helicobacter pylori . Алимент. Pharmacol. Ther. 2000; 14: 1319–1328. DOI: 10.1046 / j.1365-2036.2000.00844.x. [PubMed] [CrossRef] [Google Scholar] 12. Современные европейские концепции лечения инфекции Helicobacter pylori Маастрихтский консенсусный доклад. Европейская группа по изучению Helicobacter pylori. Кишечник. 1997; 41: 8–13. DOI: 10.1136 / gut.41.1.8. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 13. Грэм Д.Ю., Фишбах Л. Лечение Helicobacter pylori в эпоху повышения устойчивости к антибиотикам. Кишечник. 2010; 59: 1143–1153. DOI: 10.1136 / gut.2009.1. [PubMed] [CrossRef] [Google Scholar] 14. Савольди А., Каррара Э., Грэм Д. Ю., Конти М., Такконелли Э. Распространенность устойчивости к антибиотикам у Helicobacter pylori : систематический обзор и метаанализ в регионах Всемирной организации здравоохранения. Гастроэнтерология.2018; 155: 1372–1382. DOI: 10.1053 / j.gastro.2018.07.007. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 15. Ким С.Ю., Чхве Д.Дж., Чунг Дж.В. Лечение антибиотиками от Helicobacter pylori : приближается конец? Мир J. Gastrointest. Pharmacol. Ther. 2015; 6: 183–198. DOI: 10.4292 / wjgpt.v6.i4.183. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 16. Тунг И., Арамин Х., Вавинская В., Гупта С., Парк Дж. Ю., Кроу С.Э., Валасек М.А. Обзорная статья: Глобальное появление устойчивости к антибиотикам Helicobacter pylori .Алимент. Pharmacol. Ther. 2016; 43: 514–533. DOI: 10.1111 / apt.13497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 17. Woo H.Y., Park D.I., Park H., Kim M.K., Kim D.H., Kim I.S., Kim Y.J. Мультиплексная ПЦР на основе олигонуклеотидов с двойным примированием для обнаружения Helicobacter pylori и определения устойчивости к кларитромицину с помощью биоптатов желудка. Helicobacter. 2009. 14: 22–28. DOI: 10.1111 / j.1523-5378.2009.00654.x. [PubMed] [CrossRef] [Google Scholar] 18. Лиу Дж. М., Чанг К.Y., Chen M.J., Chen C.C., Fang Y.J., Lee J.Y., Wu J., Luo J., Liou T., Chang W. и др. Первичная устойчивость Helicobacter pylori на Тайване после проведения национальной политики ограничения потребления антибиотиков и ее связи с факторами вирулентности — общенациональное исследование. PLoS ONE. 2015; 10: e0124199. DOI: 10.1371 / journal.pone.0124199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 19. Ли Дж.Й., Пак К.С. Оптимальное лечение первой линии для инфекции Helicobacter pylori : последние стратегии.Гастроэнтерол. Res. Практик. 2016; 2016: 81. DOI: 10.1155 / 2016/81. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 20. Альба К., Бланко А., Аларкон Т. Устойчивость к антибиотикам у Helicobacter pylori . Curr. Opin. Заразить. Дис. 2017; 30: 489–497. DOI: 10.1097 / QCO.0000000000000396. [PubMed] [CrossRef] [Google Scholar] 21. Hwang T.J., Kim N., Kim H.B., Lee B.H., Nam R.H., Park J.H., Lee M.K., Park Y.S., Lee D.H., Jung H.C. и др. Изменение устойчивости к антибиотикам штаммов Helicobacter pylori и влияние точечной мутации A2143G 23S рРНК на эрадикацию H.pylori в едином центре Кореи. J. Clin. Гастроэнтерол. 2010; 44: 536–543. DOI: 10.1097 / MCG.0b013e3181d04592. [PubMed] [CrossRef] [Google Scholar] 22. Герритс М.М., ван Влит А.Х., Кейперс Э.Дж., Кустерс Дж.Г. Helicobacter pylori и устойчивость к противомикробным препаратам: молекулярные механизмы и клинические последствия. Lancet Infect. Дис. 2006; 6: 699–709. DOI: 10.1016 / S1473-3099 (06) 70627-2. [PubMed] [CrossRef] [Google Scholar] 24. Халтен К., Гибриль А., Скольд О., Энгстранд Л. Устойчивость к макролидам у Helicobacter pylori : механизм и стабильность в штаммах от пациентов, получавших кларитромицин.Противомикробный. Агенты. Chemother. 1997; 41: 2550–2553. DOI: 10.1128 / AAC.41.11.2550. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 25. Стоун Г.Г., Шортридж Д., Версалович Дж., Бейер Дж., Фламм Р.К., Грэм Д.Ю., Гонейм А.Т., Танака С.К. ПЦР-анализ лигирования олигонуклеотидов для определения распространенности мутаций гена 23S рРНК у устойчивых к кларитромицину Helicobacter pylori . Противомикробный. Агенты Chemother. 1997. 41: 712–714. DOI: 10.1128 / AAC.41.3.712. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 26.Аларкон Т., Доминго Д., Прието Н., Лопес-Бреа М. Стабильность устойчивости к кларитромицину у Helicobacter pylori : влияние MIC и типа мутации в 23S рРНК. J. Antimicrob. Chemother. 2000. 46: 613–616. DOI: 10.1093 / jac / 46.4.613. [PubMed] [CrossRef] [Google Scholar] 27. Van Doorn LJ, Glupczynski Y., Kusters JG, Megraud F., Midolo P., Maggi-Solca N., Queiroz DM, Nouhan N., Stet E., Quint WG Точное прогнозирование устойчивости к макролидам у Helicobacter pylori с помощью Анализ зонда ПЦР для обнаружения мутаций в гене 23S рРНК: многоцентровое валидационное исследование.Противомикробный. Агенты Chemother. 2001; 45: 1500–1504. DOI: 10.1128 / AAC.45.5.1500-1504.2001. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 28. Като С., Фудзимура С., Удагава Х., Симидзу Т., Майсава С., Одзава К., Иинума К. Устойчивость к антибиотикам штаммов Helicobacter pylori у японских детей. J. Clin. Microbiol. 2002; 40: 649–653. DOI: 10.1128 / JCM.40.2.649-653.2002. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Ван В.Х., Вонг Б.С., Мукхопадхьяй А.К., Берг Д.Э., Чо К.Х., Лай К.С., Ху В.Х., Фунг Ф.М., Хуэй В.М., Лам С.К. Высокая распространенность инфекции Helicobacter pylori с двойной устойчивостью к метронидазолу и кларитромицину в Гонконге. Алимент. Pharmacol. Ther. 2000; 14: 901–910. DOI: 10.1046 / j.1365-2036.2000.00795.x. [PubMed] [CrossRef] [Google Scholar] 30. Ли Х. Дж., Ким Дж. И., Чунг Д. Ю., Ким Т. Х., Джун Э. Дж., О Дж. Х., Чунг В. К., Ким Б., Ким С. С., Пак С. и др. Искоренение Helicobacter pylori в соответствии с точечными мутациями 23S рибосомной РНК, связанными с устойчивостью к кларитромицину.J. Infect. Дис. 2013; 208: 1123–1130. DOI: 10.1093 / infdis / jit287. [PubMed] [CrossRef] [Google Scholar] 31. Чо Дж. Х., Чон С. Р., Ким Х. Г., Джин С. Ю., Пак С. Экономическая эффективность адаптированной стратегии ликвидации Helicobacter pylori , основанной на наличии точечной мутации 23S рибосомной РНК, которая вызывает устойчивость к кларитромицину у корейских пациентов. J. Gastroenterol. Гепатол. 2019; 34: 700–706. DOI: 10.1111 / jgh.14383. [PubMed] [CrossRef] [Google Scholar] 32. Папастержиу В., Мату Н., Ликуси С., Евгениди А., Параскева К.Д., Яннакопулос А., Ставру П., Платсука Э., Караджаннис Ю.А. Семидневная тройная эрадикационная терапия Helicobacter pylori на основе генотипической устойчивости может быть высокоэффективной. Анна. Гастроэнтерол. 2018; 31: 198–204. DOI: 10.20524 / aog.2017.0219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 33. Cosme A., Montes M., Ibarra B., Tamayo E., Alonso H., Mendarte U., Lizasoan J., Herreros-Villanueva M., Bujanda L. Тестирование на чувствительность к противомикробным препаратам перед лечением первой линии для Helicobacter pylori инфекция у пациентов с двойной или тройной устойчивостью к антибиотикам.Мир J. Gastroenterol. 2017; 23: 3367–3373. DOI: 10.3748 / wjg.v23.i18.3367. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 34. Ли Дж. У., Ким Н., Нам Р. Х., Ли С. М., Квон Ю. Х., Сон С. Д., Ким Дж. М., Ли Д. Х., Юнг Х. С. Благоприятные исходы эрадикационной терапии Helicobacter pylori на основе посева в регионе с высокой устойчивостью к противомикробным препаратам. Helicobacter. 2019; 24: e12561. DOI: 10.1111 / hel.12561. [PubMed] [CrossRef] [Google Scholar] 35. Чен К., Лонг X., Цзи Ю., Лян X., Ли Д., Гао Х., Сюй Б., Лю М., Чен Ю., Сунь Ю. Рандомизированное контролируемое исследование: терапия на основе чувствительности в сравнении с эмпирической четырехкратной терапией висмутом для лечения первой линии Helicobacter pylori . Алимент. Pharmacol. Ther. 2019; 49: 1385–1394. DOI: 10.1111 / apt.15273. [PubMed] [CrossRef] [Google Scholar] 36. Блюмель Б., Гёльц Х., Кист М., Глокер Э.О. Ретроспективное исследование результатов эрадикационной терапии «спасение» Helicobacter pylori на основе молекулярно-генетического тестирования чувствительности. Helicobacter.2018; 23: e12494. DOI: 10.1111 / hel.12494. [PubMed] [CrossRef] [Google Scholar] 37. Бхакта Д., Грэм Д. Ю., Чан Дж., Эль-Сераг Х. Б. Уроки использования культурального лечения после направления к специалисту по поводу множественной неудачи лечения инфекции, вызванной Helicobacter pylori . Clin. Гастроэнтерол. Гепатол. 2018; 16: 1531–1532. DOI: 10.1016 / j.cgh.2017.12.040. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Байлина М., Муньос Н., Санчес-Дельгадо Дж., Лопес-Гонгора С., Кальвет X., Пуч И. Систематический обзор: Достигнет ли лечение на основе чувствительности приемлемых показателей излечения для терапии второй линии Helicobacter pylori , как в настоящее время практиковал? Helicobacter.2019; 24: e12584. DOI: 10.1111 / hel.12584. [PubMed] [CrossRef] [Google Scholar] 39. Лиу Дж. М., Чен П. Ю., Ло Дж. К., Ли Дж. Ю., Чен К. С., Фанг Ю. Дж., Ян Т. Х., Чанг С. Ю., Баир М. Дж., Ченет М. Дж. И др. Эффективность управляемой генотипической резистентности по сравнению с эмпирической терапией рефрактерной инфекции Helicobacter pylori . Гастроэнтерология. 2018; 155: 1109–1119. DOI: 10.1053 / j.gastro.2018.06.047. [PubMed] [CrossRef] [Google Scholar] 40. Ли Б.З., Треэплтон Д.Э., Ван Дж.Й., Сюй Дж.М., Юань Дж.К., Чжан К., Ли П., Е К. Л., Го Б., Мао С. и др. Сравнительная эффективность и переносимость лечения Helicobacter pylori : систематический обзор и сетевой метаанализ. BMJ. 2015; 351: ч5052. DOI: 10.1136 / bmj.h5052. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 41. Лю К.С., Хунг И.Ф., Сето В.К., Тонг Т., Сюй А.С., Лам Ф.Й., Но Д.Й.К., Вонг С.Й., Люн В.К. Десятидневная последовательная и 10-дневная модифицированная четырехкратная терапия висмутом в качестве эмпирической терапии первой и второй линии для Helicobacter pylori у китайских пациентов: открытое рандомизированное перекрестное исследование.Кишечник. 2014; 63: 1410–1415. DOI: 10.1136 / gutjnl-2013-306120. [PubMed] [CrossRef] [Google Scholar] 42. Hsu P.I., Tsay F.W., Graham D.Y., Tsai T.J., Tsai K.W., Kao J.Y., Peng N.J., Kuo C.H., Kao S.S., Wang H.M. и др. Эквивалентная эффективность обратной гибридной и четверной терапии висмутом в искоренении инфекции Helicobacter pylori в рандомизированном контролируемом исследовании. Clin. Гастроэнтерол. Гепатол. 2018; 16: 1427–1433. DOI: 10.1016 / j.cgh.2018.03.031. [PubMed] [CrossRef] [Google Scholar] 43.Масиас-Гарсия Ф., Бастон-Рей И., де ла Иглесиа-Гарсия Д., Кальвино-Суарес К., Ньето-Гарсия Л., Домингес-Муньос Дж. Э. Висмутсодержащая четырехкратная терапия по сравнению с сопутствующей четырехкратной терапией в качестве лечения первой линии для инфекции Helicobacter pylori в области высокой устойчивости к кларитромицину: проспективное, перекрестное, сравнительное, открытое исследование. Helicobacter. 2019; 24: e12546. DOI: 10.1111 / hel.12546. [PubMed] [CrossRef] [Google Scholar] 44. Ким С.Дж., Чунг Дж.В., Ву Х.С., Ким С.Й., Ким Дж.Х., Ким Й.Дж., Ким К.О., Квон К.А., Пак Д.К. Двухнедельная четырехкратная терапия висмутом и сопутствующая терапия являются эффективными препаратами первой линии для эрадикации Helicobacter pylori : проспективное открытое рандомизированное исследование. Мир. J. Gastroenterol. 2019; 25: 6790–6798. DOI: 10.3748 / wjg.v25.i46.6790. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 45. Ким Дж.Й., Ли С.Й., Ким Дж.Х., Сунг И.К., Пак Х.С. Эффективность и безопасность четырехкратной висмутсодержащей терапии два раза в день с использованием высоких доз тетрациклина и метронидазола для эрадикации второй линии Helicobacter pylori .Helicobacter. 2020; 25: e12683. DOI: 10.1111 / hel.12683. [PubMed] [CrossRef] [Google Scholar] 46. Xie Y., Pan X., Li Y., Wang H., Du Y., Xu J., Wang J., Zeng Z., Chen Y., Zhang G. и др. Новая однократная капсула висмута, метронидазола и тетрациклина, вводимая с омепразолом, по сравнению с четырехкратной терапией, состоящей из висмута, омепразола, амоксициллина и кларитромицина для эрадикации Helicobacter pylori у пациентов с язвой двенадцатиперстной кишки: проспективное, многоцелевое исследование в Китае. J. Antimicrob.Chemother. 2018; 73: 1681–1687. [PubMed] [Google Scholar] 47. Фиорини Г., Зулло А., Сарачино И.М., Гатта Л., Павони М., Вайра Д. Пилера и последовательная терапия для эрадикации первой линии Helicobacter pylori : исследование на основе культуры в реальной клинической практике. Евро. J. Gastroenterol. Гепатол. 2018; 30: 621–625. DOI: 10.1097 / MEG.0000000000001102. [PubMed] [CrossRef] [Google Scholar] 48. Ниссен О.П., МакНичолл А.Г., Гисберт Дж.П. Метаанализ четырехкратной терапии, содержащей висмут, три-в-одной одной капсуле для уничтожения Helicobacter pylori .Helicobacter. 2019; 24: e12570. DOI: 10.1111 / hel.12570. [PubMed] [CrossRef] [Google Scholar] 49. Ким С.Э., Ро Дж. Х., Парк М. И., Пак С. Дж., Мун В., Ким Дж. Х., Юнг К., Хео Дж. Дж. Эффект 7-дневной четырехкратной терапии висмутом по сравнению с 14-дневной тройной терапией моксифлоксацином для второй линии Helicobacter pylori эрадикационной терапии. Корейский язык. J. Gastroenterol. 2019; 73: 26–34. DOI: 10.4166 / kjg.2019.73.1.26. [PubMed] [CrossRef] [Google Scholar] 50. Боянова Л., Митов И. Географическая карта и эволюция первичной устойчивости Helicobacter pylori к антибактериальным препаратам.Эксперт. Преподобный Anti. Заразить. Ther. 2010; 8: 59–70. DOI: 10.1586 / eri.09.113. [PubMed] [CrossRef] [Google Scholar] 51. Megraud F., Coenen S., Versporten A., Kist M., Lopez-Brea M., Hirschl AM, Andersen LP, Goossens H., Glupczynski Y., участники исследовательской группы Устойчивость Helicobacter pylori к антибиотикам в Европе и ее отношение к употреблению антибиотиков. Кишечник. 2013; 62: 34–42. DOI: 10.1136 / gutjnl-2012-302254. [PubMed] [CrossRef] [Google Scholar] 52. Фишбах Л., Эванс Э. Мета-анализ: влияние статуса устойчивости к антибиотикам на эффективность тройной и четверной терапии первой линии для Helicobacter pylori .Алимент. Pharmacol. Ther. 2007. 26: 343–357. DOI: 10.1111 / j.1365-2036.2007.03386.x. [PubMed] [CrossRef] [Google Scholar] 53. Venerito M., Krieger T., Ecker T., Leandro G., Malfertheiner P. Метаанализ четырехкратной терапии висмутом по сравнению с тройной терапией кларитромицином для эмпирического первичного лечения инфекции Helicobacter pylori . Пищеварение. 2013; 88: 33–45. DOI: 10,1159 / 000350719. [PubMed] [CrossRef] [Google Scholar] 54. Манцарис Г.Дж., Петраки К., Арчавлис Э., Амбериадис П., Христофоридис П., Kourtessas D., Chiotakakou E., Triantafyllou G. Тройная терапия омепразолом по сравнению с четырехкратной терапией омепразолом для заживления язвы двенадцатиперстной кишки и эрадикации инфекции Helicobacter pylori : последующее исследование через 24 месяца. Евро. J. Gastroenterol. Гепатол. 2002; 14: 1237–1243. DOI: 10.1097 / 00042737-200211000-00012. [PubMed] [CrossRef] [Google Scholar] 55. Gisbert J.P., Calvet X. Обзорная статья: Четырехкратная (сопутствующая) терапия без висмута для искоренения Helicobater pylori. Алимент. Pharmacol.Ther. 2011; 34: 604–617. DOI: 10.1111 / j.1365-2036.2011.04770.x. [PubMed] [CrossRef] [Google Scholar] 56. Essa A.S., Kramer J.R., Graham D.Y., Treiber G. Мета-анализ: «Сопутствующая терапия» с четырьмя лекарствами, тремя антибиотиками, без висмута по сравнению с тройной терапией для эрадикации Helicobacter pylori . Helicobacter. 2009. 14: 109–118. DOI: 10.1111 / j.1523-5378.2009.00671.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 57. Gisbert J.P., Calvet X. Последние данные о четырехкратной (сопутствующей) терапии без висмута для эрадикации Helicobacter pylori .Clin. Exp. Гастроэнтерол. 2012; 5: 23–34. [Бесплатная статья PMC] [PubMed] [Google Scholar] 58. Chen MJ, Chen CC, Chen YN, Chen CC, Fang YJ, Lin JT, Wu MS, Liou JM, Taiwan Gastrointestinal Disease Helicobacter Consortium Систематический обзор с метаанализом: сопутствующая терапия против тройной терапии для лечения первой линии Helicobacter pylori Инфекция. Являюсь. J. Gastroenterol. 2018; 113: 1444–1457. DOI: 10.1038 / s41395-018-0217-2. [PubMed] [CrossRef] [Google Scholar] 59. Молина-Инфанте Дж., Пазос-Пачеко К., Винагре-Родригес Г., Перес-Галлардо Б., Дуэнас-Садорнил К., Эрнандес-Алонсо М., Гонсалес-Гарсия Г., Матеос-Родригес Дж. М., Фернандес-Бермехо М., Гисберт Дж. П. Невисмут четырехкратная (сопутствующая) терапия: эмпирическая и индивидуализированная эффективность по сравнению со стандартной тройной терапией для чувствительных к кларитромицину Helicobacter pylori и по сравнению с последовательной терапией для устойчивых к кларитромицину штаммов. Helicobacter. 2012; 17: 269–276. DOI: 10.1111 / j.1523-5378.2012.00947.x. [PubMed] [CrossRef] [Google Scholar] 60.Jung Y.S., Park C.H., Park J.H., Nam E., Lee H.L. Эффективность эрадикационной терапии Helicobacter pylori в Корее: систематический обзор и сетевой метаанализ. Helicobacter. 2017; 22 DOI: 10.1111 / hel.12389. [PubMed] [CrossRef] [Google Scholar] 61. Чунг Дж. У., Хан Дж. П., Ким К. О., Ким С. Ю., Хонг С. Дж., Ким Т. Х., Ким С. В., Ким Дж. С., Ким Б. В., Банг Б. Десятидневная эмпирическая последовательная или сопутствующая терапия более эффективна, чем тройная терапия для эрадикации Helicobacter pylori : многоцентровое проспективное исследование.Копать землю. Печень. Дис. 2016; 48: 888–892. DOI: 10.1016 / j.dld.2016.05.005. [PubMed] [CrossRef] [Google Scholar] 62. Park S.M., Kim J.S., Kim B.W., Ji J.S., Choi H. Рандомизированное клиническое испытание, сравнивающее 10- или 14-дневную последовательную терапию и 10- или 14-дневную сопутствующую терапию для эмпирического лечения первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2017; 32: 589–594. DOI: 10.1111 / jgh.13510. [PubMed] [CrossRef] [Google Scholar] 63. Ким С. Ю., Ли С. В., Чхве Дж. В., Чон С. В., Хён Дж.J., Jung Y.K., Koo J.S., Yim H.J. Helicobacter pylori Показатели эрадикации сопутствующей и последовательной терапии в Корее. Helicobacter. 2017; 22: e12441. DOI: 10.1111 / hel.12441. [PubMed] [CrossRef] [Google Scholar] 64. Анг Т.Л., Фок К.М., Сонг М., Анг Д., Квек А.Б., Онг Дж., Тан Дж., Тео Е.К., Дхамодаран С. Десятидневная тройная терапия по сравнению с последовательной терапией по сравнению с сопутствующей терапией в качестве лечения первой линии для Helicobacter pylori инфекция. J. Gastroenterol. Гепатол. 2015; 30: 1134–1139.DOI: 10.1111 / jgh.12892. [PubMed] [CrossRef] [Google Scholar] 65. Макниколл А.Г., Марин А.С., Молина-Инфанте Дж., Кастро М., Баррио Дж., Дуконс Дж., Кальвет X., Коба К., Монторо М., Бори Ф. и др. Рандомизированное клиническое испытание, сравнивающее последовательную и сопутствующую терапию для эрадикации Helicobacter pylori в рутинной клинической практике. Кишечник. 2014; 63: 244–249. DOI: 10.1136 / gutjnl-2013-304820. [PubMed] [CrossRef] [Google Scholar] 66. Гатта Л., Вакил Н., Вайра Д., Скарпигнато С. Глобальные показатели эрадикации инфекции Helicobacter pylori : систематический обзор и метаанализ последовательной терапии.BMJ. 2013; 347: f4587. DOI: 10.1136 / bmj.f4587. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 67. Хе Л., Дэн Т., Луо Х. Мета-анализ последовательной, сопутствующей и гибридной терапии для эрадикации Helicobacter pylori . Междунар. Med. 2015; 54: 703–710. DOI: 10.2169 / internalmedicine.54.3442. [PubMed] [CrossRef] [Google Scholar] 68. Zullo A., Scaccianoce G., De Francesco V., Ruggiero V., D’Ambrosio P., Castorani L., Bonfrate L., Vannella L., Hassan C., Portincasa P. Сопутствующая, последовательная и гибридная терапия для ЧАС.pylori: пилотное исследование. Clin. Res. Гепатол. Гастроэнтерол. 2013; 37: 647–650. DOI: 10.1016 / j.clinre.2013.04.003. [PubMed] [CrossRef] [Google Scholar] 69. Ким С.Й., Ли С.В., Хён Дж.Дж., Юнг С.В., Ку Дж.С., Йим Х.Дж., Пак Дж.Дж., Чун Х.Дж., Чой Дж.Х. Сравнительное исследование степени эрадикации Helicobacter pylori с 5-дневной четырехкратной «сопутствующей» терапией и 7-дневной стандартной тройной терапией. J. Clin. Гастроэнтерол. 2013; 47: 21–24. DOI: 10.1097 / MCG.0b013e3182548ad4. [PubMed] [CrossRef] [Google Scholar] 70.Лим Дж. Х., Ли Д. Х., Чой К., Ли С. Т., Ким Н., Чон С. Х., Ким Дж. У., Хван Дж. Х., Пак Ю. С., Ли С. Х. и др. Клинические результаты двухнедельной последовательной и сопутствующей терапии для эрадикации Helicobacter pylori : рандомизированное пилотное исследование. Helicobacter. 2013. 18: 180–186. DOI: 10.1111 / hel.12034. [PubMed] [CrossRef] [Google Scholar] 71. Гевара Б., Когдилл А.Г. Helicobacter pylori : Обзор текущих стратегий диагностики и управления. Копать землю. Дис. Sci. 2020; 65: 1917–1931.DOI: 10.1007 / s10620-020-06193-7. [PubMed] [CrossRef] [Google Scholar] 72. Грэм Д.Ю., Ли Ю.С., Ву М.С. Рациональная терапия Helicobacter pylori : доказательная медицина, а не доказательная медицина. Clin. Гастроэнтерол. Гепатол. 2014; 12: 177–186. DOI: 10.1016 / j.cgh.2013.05.028. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 73. Wang B., Wang Y.H., Lv Z.F., Xiong H.F., Wang H., Yang Y., Xie Y. Обзор: Эффективность и безопасность гибридной терапии для инфекции Helicobacter pylori : систематический обзор и метаанализ.Helicobacter. 2015; 20: 79–88. DOI: 10.1111 / hel.12180. [PubMed] [CrossRef] [Google Scholar] 74. Молина-Инфанте Дж., Романо М., Фернандес-Бермехо М., Федерико А., Гравина А.Г., Поццати Л., Гарсия-Абадиа Э., Винагре-Родригес Г., Мартинес-Алькала К., Эрнандес-Алонсо М. , и другие. Оптимизированная четырехкомпонентная терапия без висмута излечивает большинство пациентов с инфекцией Helicobacter pylori в популяциях с высокими показателями устойчивости к антибиотикам. Гастроэнтерология. 2013; 145: 121–128. DOI: 10.1053 / j.gastro.2013.03.050. [PubMed] [CrossRef] [Google Scholar] 75. Georgopoulos SD, Papastergiou V., Martinez-Gonzalez B., Xirouchakis E., Familias I., Sgouras D., Mentis A., Karatapanis S. Гибридная терапия как схема первой линии для эрадикации Helicobacter pylori при высокой устойчивости к кларитромицину область: перспективное открытое испытание. Анна. Гастроэнтерол. 2018; 31: 205–210. DOI: 10.20524 / aog.2017.0221. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Сонг З., Фу В., Чжоу Л. Цефуроксим, левофлоксацин, эзомепразол и висмут в качестве терапии первой линии для ликвидации Helicobacter pylori у пациентов с аллергией на пенициллин.BMC Gastroenterol. 2019; 19: 132. DOI: 10.1186 / s12876-019-1056-3. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 77. Auttajaroon J., Vilaichone R.K., Chotivitayatarakorn P., Mahachai V. Рабепразол, левофлоксацин, кларитромицин-MR и висмут один раз в день для эрадикации Helicobacter pylori : рандомизированное исследование продолжительностью 7 или 14 дней (исследование ONCE) Helicobacter. 2019; 24: e12615. DOI: 10.1111 / hel.12615. [PubMed] [CrossRef] [Google Scholar] 78. Ган Х.Ю., Пэн Т.Л., Хуан Ю.М., Су К.Х., Чжао Л.Л., Яо Л.Ю., Ян Р.Дж. Эффективность двух различных доз левофлоксацина в лечении инфекции Helicobacter pylori : проспективное одноцентровое рандомизированное клиническое испытание. Sci. Отчет 2018; 8: 9045. DOI: 10.1038 / s41598-018-27482-2. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 79. Ciccaglione AF, Di Giulio M., Di Lodovico S., Di Campli E., Cellini L., Marzio L. Бычий лактоферрин повышает эффективность тройной терапии на основе левофлоксацина в качестве лечения первой линии инфекции Helicobacter pylori : An in vitro и in vivo исследования.J. Antimicrob. Chemother. 2019; 74: 1069–1077. DOI: 10,1093 / jac / dky510. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 80. Басу П.П., Раяпуди К., Пакана Т., Шах Н.Дж., Кришнасвами Н., Флинн М. Рандомизированное исследование, сравнивающее левофлоксацин, омепразол, нитазоксанид и доксициклин с тройной терапией для ликвидации Helicobacter pylori . Являюсь. J. Gastroenterol. 2011; 106: 1970–1975. DOI: 10.1038 / ajg.2011.306. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 81. Фэллон К.А., Мосс С.Ф., Малфертхайнер П. Согласование последних рекомендаций по лечению Helicobacter pylori во времена повышения устойчивости к антибиотикам. Гастроэнтерология. 2019; 157: 44–53. DOI: 10.1053 / j.gastro.2019.04.011. [PubMed] [CrossRef] [Google Scholar] 82. Мори Х., Судзуки Х. Обновленная информация о хинолон-содержащих терапии спасения от инфекции Helicobacter pylori . Мир J. Gastroenterol. 2020; 26: 1733–1744. DOI: 10.3748 / wjg.v26.i15.1733. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83.Sue S., Shibata W., Sasaki T., Kaneko H., Irie K., Kondo M., Maeda S. Рандомизированное испытание тройной терапии третьей линии на основе вонопразана и ингибитора протонной помпы с ситафлоксацином для Helicobacter pylori . J. Gastroenterol. Гепатол. 2019; 34: 686–692. DOI: 10.1111 / jgh.14456. [PubMed] [CrossRef] [Google Scholar] 84. Судзуки Х., Нишизава Т., Мураока Х., Хиби Т. Ситафлоксацин и гареноксацин могут преодолеть устойчивость к антибиотикам Helicobacter pylori с мутацией gyrA.Противомикробный. Агенты. Chemother. 2009; 53: 1720–1721. DOI: 10.1128 / AAC.00049-09. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 85. Miftahussurur M., Waskito LA, Syam AF, Nusi IA, Siregar G., Richardo M., Bakry AF, Rezkitha YAA, Wibawa IDN, Yamaoka Y. Альтернативные схемы эрадикации инфекции Helicobacter pylori в регионах Индонезии с высоким содержанием метронидазола и левофлоксина сопротивление. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 345–358. DOI: 10.2147 / IDR.S187063. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 86.Мифтахуссурур М., Афтаб Х., Шреста П.К., Шарма Р.П., Субсомвонг П., Васкито Л.А., Духан Д., Фаузия К.А., Ямаока Ю. Эффективные терапевтические схемы в двух странах Южной Азии с высокой устойчивостью к основным антибиотикам Helicobacter pylori . Противомикробный. Оказывать сопротивление. Заразить. Контроль. 2019; 8:40. DOI: 10.1186 / s13756-019-0482-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 87. Гисберт Дж. П., Кальвет X. Обзорная статья: Рифабутин в лечении рефрактерной инфекции Helicobacter pylori .Алимент. Pharmacol. Ther. 2012; 35: 209–221. DOI: 10.1111 / j.1365-2036.2011.04937.x. [PubMed] [CrossRef] [Google Scholar] 88. Хип М., Бек Д., Байердорфер Э., Лен Н. Механизм устойчивости к рифампину и рифабутину в Helicobacter pylori . Противомикробный. Агенты. Chemother. 1999; 43: 1497–1499. DOI: 10.1128 / AAC.43.6.1497. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 89. Рибалдоне Д.Г., Фагуни С., Астеджано М., Дураццо М., Моргандо А., Спруджевник Т., Джорданино К., Баронио М., Анжелис К.D., Saracco G.M. и др. Спасательная терапия на основе рифабутина для эрадикации Helicobacter pylori : долгосрочное проспективное исследование в большой когорте трудно поддающихся лечению пациентов. J. Clin. Med. 2019; 8: 199. DOI: 10,3390 / jcm8020199. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 90. Akada J.K., Shirai M., Fujii K., Okita K., Nakazawa T. Активность новых производных рифамицина, KRM-1648 и KRM-1657, in vitro против Helicobacter pylori in vitro. Противомикробный. Агенты. Chemother. 1999; 43: 1072–1076.DOI: 10.1128 / AAC.43.5.1072. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 91. Кунин С.М. Антимикробная активность рифабутина. Clin. Заразить. Дис. 1996; 22 (Дополнение 1: S3-13): 30. DOI: 10.1093 / Clinids / 22.Supplement_1.S3. [PubMed] [CrossRef] [Google Scholar] 92. Сунг Дж., Ким Н., Пак И. Х., Хван Ю. Дж., Квон С., На Г., Чой Дж. Ю., Кан Дж. Б., Ким Х. Р., Ким Дж. В. и др. Спасательная терапия четвертой и пятой линий на основе рифабутина у пациентов с неэффективностью эрадикации Helicobacter pylori . Корейский язык.J. Gastroenterol. 2017; 69: 109–118. DOI: 10.4166 / kjg.2017.69.2.109. [PubMed] [CrossRef] [Google Scholar] 93. Грэм Д.Ю., Ханаан Ю., Махер Дж., Винер Г., Халтен К.Г., Калфус И.Н. Тройная терапия на основе рифабутина (RHB-105) для ликвидации Helicobacter pylori : двойное слепое рандомизированное контролируемое исследование. Анна. Междунар. Med. 2020; 172: 795–802. DOI: 10.7326 / M19-3734. [PubMed] [CrossRef] [Google Scholar] 94. Бок Х., Куп Х., Лен Н., Хип М. Тройная терапия на основе рифабутина после неудачной эрадикационной терапии Helicobacter pylori : предварительный опыт.J. Clin. Гастроэнтерол. 2000. 31: 222–225. DOI: 10.1097 / 00004836-200010000-00007. [PubMed] [CrossRef] [Google Scholar] 95. Сузуки С., Сузуки Х., Нисидзава Т., Канеко Ф., Отани С., Мураока Х., Сайто Ю., Кобаяши И., Хиби Т. Прошлое дозирование рифампицина определяет устойчивость к рифабутину Helicobacter pylori . Пищеварение. 2009; 79: 1–4. DOI: 10,1159 / 0001. [PubMed] [CrossRef] [Google Scholar] 96. Скотт Дж. Я., Мансон К. Б., Маркус Э. А., Ламбрехт Н. В., Сакс Г. Селективность связывания фонопразана (TAK-438) с H +, K + -АТФазой желудка.Алимент. Pharmacol. Ther. 2015; 42: 1315–1326. DOI: 10.1111 / apt.13414. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 97. Park J.Y., Kim J.G. [New Helicobacter pylori Eradication Therapies] Корейский. J. Gastroenterol. 2018; 72: 237–244. DOI: 10.4166 / kjg.2018.72.5.237. [PubMed] [CrossRef] [Google Scholar] 99. Грэм Д.Ю., Дор М.П. Обновленная информация об использовании вонопразана: конкурентного блокатора кислоты. Гастроэнтерология. 2018; 154: 462–466. DOI: 10.1053 / j.gastro.2018.01.018. [PubMed] [CrossRef] [Google Scholar] 100.Лю Q.J., Пу Q.H., Чжун X.F., Чжан Дж. Эффективность и безопасность тройной терапии на основе вонопразана и ингибитора протонной помпы для искоренения Helicobacter pylori : метаанализ рандомизированных клинических испытаний. Биомед. Res. Int. 2019; 3: 1–8. DOI: 10.1155 / 2019/9781212. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 101. Murakami K., Sakurai Y., Shiino M., Funao N., Nishimura A., Asaka M. Vonoprazan, новый калий-конкурентный блокатор кислоты, в качестве компонента тройной терапии первой и второй линии против Helicobacter pylori Эрадикация : рандомизированное двойное слепое исследование фазы III.Кишечник. 2016; 65: 1439–1446. DOI: 10.1136 / gutjnl-2015-311304. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 102. Ли М., Осима Т., Хорикава Т., Тозава К., Томита Т., Фукуи Х., Ватари Дж., Мива Х. Систематический обзор с метаанализом: вонопразан, мощный блокатор кислоты, превосходит протонный ингибиторы помпы для уничтожения устойчивых к кларитромицину штаммов Helicobacter pylori . Helicobacter. 2018; 23: e12495. DOI: 10.1111 / hel.12495. [PubMed] [CrossRef] [Google Scholar] 103. Танабэ Х., Yoshino K., Ando K., Nomura Y., Ohta K., Satoh K., Ichiishi E., Ishizuka A., Otake T., Kohgo Y., et al. Тройная терапия на основе вонопразана не уступает тройной терапии на основе ингибиторов протонной помпы на основе чувствительности для эрадикации Helicobacter pylori . Анна. Clin. Microbiol Antimicrob. 2018; 17:29. DOI: 10.1186 / s12941-018-0281-х. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 104. Судзуки С., Готода Т., Кусано К., Икехара Х., Итидзима Р., Охьяучи М., Ито Х., Кавамура М., Огата Ю., Отака М. и др. Семидневная двойная терапия фонопразаном и низкими дозами амоксициллина в качестве терапии первой линии Helicobacter pylori : многоцентровое рандомизированное исследование в Японии. Кишечник. 2020; 69: 1019–1026. DOI: 10.1136 / gutjnl-2019-319954. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 105. Ким Б.Дж., Ли Х., Ли Ю.С., Чон С.В., Ким Г.Х., Ким Х.С., Сунг Дж.К., Ли Д.Х., Ким Х.У., Пак М.И. и др. Десятидневная сопутствующая, 10-дневная последовательная и 7-дневная тройная терапия в качестве лечения первой линии для инфекции Helicobacter pylori : общенациональное рандомизированное исследование в Корее.Кишечник. Печень. 2019; 13: 531–540. DOI: 10.5009 / gnl19136. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 106. Zhou Y., Ye Z., Wang Y., Zhang Y., Tang Z., Yan W., Jiang Y., Huang Y. Сравнение четырех различных схем лечения против Helicobacter pylori в качестве лечения первой линии: перспектива , перекрестное, сравнительное, открытое испытание на китайских детях. Helicobacter. 2020; 25: e12679. DOI: 10.1111 / hel.12679. [PubMed] [CrossRef] [Google Scholar] 107. Банг К.С., Лим Х., Чон Х.М., Шин В.Г., Чой Дж. Х., Со Дж. С., Кан Х. С., Ян Й. Дж., Хонг Дж. Т., Шин С. П. и др. Амоксициллин или тетрациклин в висмутсодержащей четверной терапии в качестве лечения первой линии для инфекции Helicobacter pylori . Кишечные микробы. 2020; 11: 1314–1323. DOI: 10.1080 / 194.2020.1754118. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 108. Романо М., Гравина А.Г., Нардоне Г., Федерико А., Даллио М., Марторано М., Мучерино К., Ромити А., Аваллоне Л., Граната Л. и др. Четырехкратная терапия без висмута и висмута, основанная на предыдущем воздействии кларитромицина, столь же эффективна и безопасна в области высокой устойчивости к кларитромицину: исследование в реальной жизни.Helicobacter. 2020; 25: e12694. DOI: 10.1111 / hel.12694. [PubMed] [CrossRef] [Google Scholar] 109. Tai W.C., Liang C.M., Bi K.W., Kuo C.M., Lu L..S., Wu C.K., Yang S.C., Kuo Y.H., Lee C.H., Huang C.F. и др. Сравнение четырехкомпонентной (сопутствующей) терапии на основе декслансопразола с модифицированным высвобождением и на основе лансопразола для эрадикации первой линии Helicobacter pylori : проспективное рандомизированное исследование. Заразить. Препарат, средство, медикамент. Оказывать сопротивление. 2019; 12: 2923–2931. DOI: 10.2147 / IDR.S213998. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 110.Hsu P.I., Tsay F.W., Kao J.Y., Peng N.J., Tsai K.W., Tsai T.J., Kuo C.H., Kao S.S., Wang H.M., Chen Y.H. и др. Эквивалентная эффективность обратного гибрида и сопутствующей терапии в лечении первой линии инфекции Helicobacter pylori . J. Gastroenterol. Гепатол. 2020 doi: 10.1111 / jgh.15034. [PubMed] [CrossRef] [Google Scholar] 111. Myint N., Zaw T.T., Sain K., Waiyan S., Danta M., Cooper D., Aung N.M., Kyi M.M., Hanson J. Sequential Helicobacter pylori эрадикационная терапия в Мьянме; рандомизированное клиническое испытание эффективности и переносимости.J. Gastroenterol. Гепатол. 2020; 35: 617–623. DOI: 10.1111 / jgh.14942. [PubMed] [CrossRef] [Google Scholar] 112. Зулло А., Фиорини Г., Скаччаноче Г., Портинкаса П., Де Франческо В., Вассалло Р., Урбан Ф., Моника Ф., Могаверо Г., Амато А. и др. Последовательная терапия для эрадикации первой линии Helicobacter pylori : 10- или 14-дневный режим? J. Gastrointestin. Печень. Дис. 2019; 28: 11–14. DOI: 10.15403 / jgld.2014.1121.281.hpy. [PubMed] [CrossRef] [Google Scholar] 113. Цай Ф.В., Ву Д.С., Ю Х.С., Kao S.S., Lin K.H., Cheng J.S., Wang H.M., Chen W.C., Sun W.C., Tsai K.W. и др. Рандомизированное контролируемое исследование показывает, что как 14-дневная гибридная, так и четырехкомпонентная терапия висмутом излечивают большинство пациентов с инфекцией Helicobacter pylori в группах населения со средней устойчивостью к антибиотикам. Противомикробный. Агенты. Chemother. 2017; 61: e00140-17. DOI: 10.1128 / AAC.00140-17. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 114. Нисида Т., Цудзи Ю., Окамото А., Томита Р., Хигаки Ю., Осуги Н., Сугимото А., Такахаши К., Мукаи К., Накамацу Д. и др. Лекарство с тройным лекарством в блистерной упаковке с вонопразаном улучшает эрадикацию первой линии Helicobacter pylori у пожилых пациентов: когортное исследование с ретроспективной оценкой склонности. Пищеварение. 2019: 1–7. DOI: 10,1159 / 000501608. [PubMed] [CrossRef] [Google Scholar] 115. Луо Л., Хуанг Ю., Лян Х., Цзи Ю., Ю. Л., Лу Х. Терапия на основе чувствительности для Helicobacter pylori -инфицированных пациентов с аллергией на пенициллин: проспективное клиническое испытание терапии первой линии и терапии спасения .Helicobacter. 2020; 25: e12699. DOI: 10.1111 / hel.12699. [PubMed] [CrossRef] [Google Scholar] 116. Kim SG, Jung HK, Lee HL, Jang JY, Lee H., Kim CG, Shin WG, Shin ES, Lee YC, Korean College of Helicobacter and Upper Gastrointestinal Research Guidelines для диагностики и лечения инфекции Helicobacter pylori в Корее , Редакция 2013 г. J. Gastroenterol. Гепатол. 2014; 29: 1371–1386. DOI: 10.1111 / jgh.12607. [PubMed] [CrossRef] [Google Scholar] 117. Като М., Ота Х., Окуда М., Кикучи С., Сато К., Шимояма Т., Судзуки Х., Ханда О., Фурута Т., Мабе К. и др. Руководство по лечению инфекции Helicobacter pylori в Японии: пересмотренное издание 2016 г. Helicobacter. 2019; 24: e12597. DOI: 10.1111 / hel.12597. [PubMed] [CrossRef] [Google Scholar]
Руководство по диагностике и лечению Helicobacter pylori
Причина и передача
Хотя путь передачи H pylori не совсем понятен, бактерия, похоже, перемещается к своему хозяину через прямой контакт с другим человеком или через зараженную среду. 4 H pylori инфицирует эпителиальную выстилку желудка и чаще всего заражается при межличностном контакте в детстве. 4,5 Передачу от человека к человеку можно разделить на вертикальную и горизонтальную. Многие исследования сосредоточены на вертикальной передаче, при которой H pylori передается между членами семьи. Исследования показывают, что передача H pylori между членами семьи является обычным явлением, поскольку члены семьи находятся в тесном контакте и могут иметь общий генетический состав, который предрасполагает их к инфекции H pylori .Кроме того, семьи часто подвергаются общему источнику инфекции и часто имеют одинаковый социально-экономический статус. В развитых странах, где частота инфицирования H pylori низкая, передача инфекции от матери детям считается основным источником инфекции. Однако в странах, где инфекция H pylori распространена, передача от матери менее вероятно будет основным путем передачи. Вместо этого высока распространенность передачи между братьями и сестрами и от горизонтальной передачи; то есть контакт человека с человеком вне дома. 4 Хотя считается, что все прямые передачи от человека к человеку происходят через желудочно-оральный, орально-оральный или фекально-оральный путь, преобладающий способ передачи неизвестен. 4 H pylori часто присутствует в больших количествах в рвотных массах и, по-видимому, выживает в желудочном соке вне организма, что свидетельствует о распространенности желудочно-оральной передачи, особенно в детстве и в сочетании с плохими гигиеническими условиями. 4 Однако H pylori может также колонизировать ротовую полость после рвоты или срыгивания, что делает слюну возможным носителем, а орально-оральный контакт — возможным путем передачи.Передача через рот часто происходит от матери к ребенку, но это не основной путь передачи у взрослых. 4 Кроме того, хотя попытки культивирования H pylori из фекалий были встречены с ограниченным успехом, ДНК H pylori была обнаружена в фекалиях человека, что указывает на то, что фекально-оральная передача может быть способом передачи H. pylori . . 4 Последний возможный способ передачи — окружающая среда; в этом случае загрязненные продукты питания и вода, вероятно, являются транспортными средствами. 4 Дети, живущие в домах с внешним водоснабжением, или те, кто потребляет те же сырые овощи, которые часто орошаются неочищенными сточными водами, демонстрируют высокие показатели инфекции H pylori . 4 Эффективные методы лечения могут защитить от этих многих способов передачи и предотвратить долгосрочные риски, которые представляет инфекция.
Заболеваемость и распространенность
Систематический обзор и метаанализ суммировали всеобъемлющую глобальную распространенность инфекции H. pylori и подсчитали, что более половины населения мира инфицировано. 5 Заболеваемость H pylori изменилась с течением времени с улучшением санитарных условий, но в некоторых областях его распространенность по-прежнему высока. 5 Африка, Южная Америка и Западная Азия — это регионы, где распространенность H pylori является самой высокой: 70,1%, 69,4% и 66,6% соответственно. 5 В Северной Америке распространенность среди белых неиспаноязычных людей ниже, чем среди афроамериканцев, латиноамериканцев, коренных американцев, коренных жителей Аляски и американцев корейского или китайского происхождения. 6 Распространенность H. pylori зависит от социально-экономического статуса, уровня гигиены и расы / этнической принадлежности. 5 К группам высокого риска относятся пожилые люди, люди, живущие в плохих гигиенических условиях, мигранты из районов с высокой распространенностью, лица, находящиеся в учреждениях, и, возможно, люди, живущие в сельской местности. 4 Несмотря на успехи в некоторых регионах, H pylori по-прежнему является серьезным бременем для большей части мира.
Диагноз
Крайне важно установить, у каких пациентов следует пройти тестирование на H pylori , поскольку всем пациентам с положительным тестом на активную инфекцию должно быть предложено лечение. 7 Клинические рекомендации Американского колледжа гастроэнтерологии (ACG) 2017 года рекомендуют пациентам с активной язвенной болезнью (ЯБ) в анамнезе (если не было документально подтверждено предыдущее излечение инфекции H pylori ), малозернистой лимфомой MALT , или история эндоскопической резекции раннего рака желудка (EGC) должна быть проверена на инфекцию H pylori . 7 Пациентам с новым диагнозом или анамнезом ЯБ следует использовать тест, который определяет активную инфекцию.Такие тесты включают дыхательные тесты на мочевину, тесты на фекальные антигены или, если выполняется эндоскопия, тесты на основе биопсии слизистой оболочки. В руководстве рекомендуется, чтобы пациенты с ЯБ в анамнезе, которые лечились от H pylori , прошли тест на эрадикацию с помощью дыхательного теста на мочевину или теста на фекальный антиген. 7 Исследования показывают, что эрадикация H pylori не эффективно предотвращает регрессию опухоли лимфомы MALT, но для подтверждения этого не проводились систематические обзоры или рандомизированные контролируемые испытания.Тем не менее, выявление новообразования лимфомы MALT остается ключевым показателем для тестирования и искоренения H pylori . 7 Для пациентов в возрасте до 60 лет с неисследованной диспепсией и без признаков тревоги следует рассмотреть неэндоскопическое тестирование; у пациентов с диспепсией, которым проводится эндоскопия верхних отделов желудка, исследование следует проводить на биопсийной ткани желудка. 7 В рандомизированном исследовании, проведенном в Великобритании, 90% взрослых с положительной реакцией на инфекцию H pylori , лечившихся от инфекции, достигли эрадикации, а также сообщалось о статистически значимом сокращении числа последующих консультаций по поводу диспепсии. 7 Причинно-следственная связь между H pylori и гастроэзофагеальной рефлюксной болезнью (ГЭРБ) не доказана; действительно, отрицательная связь между ними существует на географической основе, и лечение инфекции H pylori не улучшает симптомы ГЭРБ. 7 Следовательно, пациенты со стандартными симптомами ГЭРБ и без ЯБ в анамнезе не нуждаются в тестировании на H pylori . Однако, если обнаруживается, что пациенты инфицированы, следует предложить лечение. 7 Следует также рассмотреть возможность проведения анализов у пациентов, длительно принимающих низкие дозы аспирина, поскольку инфекция H pylori может вызвать язвы и кровотечения из язв в этой популяции.Эрадикационная терапия для тех, у кого положительный результат теста, может уменьшить кровотечение из язвы. 7 Пациенты, начинающие длительное лечение нестероидными противовоспалительными препаратами (НПВП), страдающие необъяснимой железодефицитной (ЖД) анемией или страдающие идиопатической тромбоцитопенической пурпурой (ИТП), также должны пройти обследование и, в случае положительного результата, предложить лечение. 7 Подобно пациентам, принимающим аспирин, пациенты, принимающие НПВП и положительные на H pylori , имеют более высокий риск развития язвенных осложнений. 7 Исследования показывают, что пациенты с инфекцией H pylori с большей вероятностью будут иметь анемию ID. 7 Количество тромбоцитов может также улучшиться после искоренения инфекции H pylori у некоторых взрослых с ИТП. 7 Руководство ACG не поддерживает рутинное тестирование и лечение H pylori у бессимптомных лиц с семейным анамнезом рака желудка или у пациентов с лимфоцитарным гастритом, гиперпластическими полипами желудка или гиперемезисом беременных. 7 Настоящее руководство расширяет список потенциальных пациентов для тестирования на H pylori по сравнению с руководством 2007 года, но не дает никаких оснований для универсального или популяционного скрининга в Северной Америке. 7
Методы диагностического тестирования, доступные для H pylori , включают неинвазивные и инвазивные методы. Неинвазивные методы, которые позволяют врачам легко обнаружить H pylori , включают серологию, дыхательный анализ мочевины и определение антигена в стуле. 8 Инвазивные методы включают использование эндоскопии для сбора биоптатов желудка и включают гистологию, посев и экспресс-тест на уреазу. 8 Серологический анализ — наименее чувствительный неинвазивный метод. Он имеет чувствительность от 75% до 85% по сравнению с более чем 95% для анализа дыхания на фекальный антиген и мочевину. Из-за этого и большого количества ложных срабатываний он больше не рекомендуется в США. 8 Дыхательные и фекальные тесты на мочевину выявляют активную инфекцию, имеют высокие отрицательные и положительные прогностические значения, отлично подходят для тестирования до или после лечения и являются высокоспецифичными.Недостатками этих тестов являются необходимость отмены пациентом ингибиторов протонной помпы (ИПП), висмута и антибиотиков, поскольку они могут подавлять жизнеспособность H pylori . 8 Инвазивное гистологическое исследование чувствительно от 60% до 86% и является наиболее дорогостоящим методом. Он предоставляет дополнительную информацию о слизистой оболочке желудка, но требует иммунохимии, что увеличивает стоимость. Посевы могут также проверить чувствительность к антибиотикам, но они имеют ограниченную доступность и чувствительность только 60%.
Наконец, экспресс-тест на уреазу имеет чувствительность от 80% до 95% и предлагает быстрое тестирование и точные результаты для пациентов, не принимающих ИПП. Однако тест может дать неоднозначные результаты и подвержен сильной систематической ошибке между наблюдателями. 8 Из-за ограничений культивирования и быстрого тестирования уреазы наиболее инвазивное тестирование на H pylori выполняется с помощью рутинной гистологии и дополнительной иммуногистохимии. 8 Клинические рекомендации ACG рекомендуют обследовать пациентов после лечения, чтобы гарантировать искоренение инфекции.Тестирование следует проводить с использованием дыхательного теста с мочевиной, теста на фекальный антиген или теста на основе биопсии, по крайней мере, через 4 недели после завершения антибактериальной терапии и после того, как терапия ИПП не проводилась в течение 1-2 недель. 7 Хотя обстоятельства могут сделать дополнительное тестирование нецелесообразным, и поставщики медицинских услуг или пациенты могут решить, что повторное тестирование не требуется, 7 подтверждение эрадикации с помощью теста после лечения позволяет определить показатели успеха и способствует раннему выявлению возникающих паттернов резистентности.Такое подтверждение может побудить к изменениям в терапии в будущем и предотвратить распространение резистентности. 8
Руководство по лечению ACG
Руководство по лечению ACG для терапии первой линии и терапии спасения последний раз обновлялось в 2017 году. Обычно H pylori лечится с помощью 2–3 антибиотиков и ИПП. 7
Терапия первой линии
В руководстве ACG от 2017 г. излагаются основанные на фактических данных стратегии первичного лечения для медицинских работников в Северной Америке.Они включают тройную терапию кларитромицином, четверную терапию висмутом, сопутствующую терапию, последовательную терапию, гибридную терапию, тройную терапию левофлоксацином и последовательную терапию фторхинолоном. 7 Тройная терапия кларитромицином включает лечение ИПП, кларитромицином и амоксициллином (метронидазолом, если у пациента аллергия на амоксициллин). В руководстве отмечается, что при использовании в Северной Америке курс лечения должен длиться 14 дней. 7 Успех тройной терапии кларитромицином зависит от степени устойчивости к кларитромицину.Действительно, метаанализ 2010 года показал, что уровень эрадикации составляет 22% для устойчивых к кларитромицину штаммов H pylori по сравнению с 90% для чувствительных к кларитромицину штаммов. 7 Маастрихтско-флорентийский консенсусный документ, опубликованный в 2012 году, рекомендовал отказаться от тройной терапии, когда уровень устойчивости к кларитромицину превышает 15–20%. 7 На момент публикации рекомендаций ACG в 2017 году данные предполагали, что уровни сопротивления в Северной Америке могут находиться в этом диапазоне. 7 В руководстве отмечено, что если резистентность к кларитромицину действительно превышает 15%, следует избегать тройной терапии кларитромицином. 7
Квартальная терапия висмутом состоит из антагониста рецепторов ИПП или гистамина-2, висмута, метронидазола и тетрациклина. 7 В руководстве ACG рекомендуется проводить это лечение в течение 10–14 дней. 7 Существуют ограниченные данные об эффективности или сравнительной эффективности четырехкратной терапии висмутом в Северной Америке, но данные со всего мира позволяют предположить, что четырехкратная терапия висмутом и тройная терапия кларитромицином имеют схожую эффективность, приверженность и переносимость .7 Таким образом, в регионах, где резистентность к кларитромицину является проблемой, четырехкратную терапию висмутом следует рассматривать как первоначальный выбор лечения, поскольку на нее не влияет резистентность к кларитромицину. 7
Сопутствующая терапия — это вариант первой линии для пациентов с непереносимостью висмута 8 и включает ИПП, амоксициллин, кларитромицин и нитроимидазол (тинидазол или метронидазол) вместе в течение 3–10 дней. 7 Признавая, что эффективность сопутствующей терапии не была хорошо изучена в Северной Америке, авторы рекомендаций ACG обратились к испытаниям из Европы, Азии и Латинской Америки, которые показывают, что сопутствующая терапия имеет более высокий уровень излечения от намерения к лечению, чем тройная терапия кларитромицином с коэффициентом излечения 90% по сравнению с 78%, соответственно. 7 Таким образом, руководство ACG рекомендует рассматривать сопутствующую терапию как многообещающий вариант лечения с высокими показателями излечения для Северной Америки. 7
Последовательная терапия состоит из ИПП плюс амоксициллин в течение 5 дней с последующим ИПП, кларитромицином и нитроимидазолом в течение дополнительных 5 дней. Принимая решение о целесообразности последовательной терапии в качестве терапии первой линии для инфекции H pylori , руководство ACG 2017 основывалось на недавнем обзоре и метаанализе, которые показали, что общий показатель успеха последовательной терапии составляет 84.3%. В руководстве признается, что последовательная терапия более эффективна, чем 7 дней тройной терапии на основе кларитромицина, но лишь немного лучше, чем 10 дней тройной терапии на основе кларитромицина, и не превосходит 14 дней тройной терапии на основе кларитромицина или 10-14 дней. четверной терапии висмутом. 7 Хотя в руководстве признается жизнеспособность последовательной терапии, в нем отмечается, что последовательная терапия не превосходит 14-дневную тройную терапию кларитромицином в условиях Северной Америки и что сложность последовательного лечения делает его менее желательным вариантом лечения первой линии. этот континент. 7
Гибридная терапия состоит из 7 дней приема ИПП и амоксициллина, а затем еще 7 дней лечения ИПП, амоксициллина, кларитромицина и нитроимидазола. 7 Поскольку в Северной Америке не проводились рандомизированные контролируемые испытания для оценки эффективности гибридной терапии, авторы рекомендаций ACG обратились к исследованиям из других стран, чтобы определить, что ее эффективность, переносимость или соблюдение не отличается от эффективности последовательной или последовательной терапии. сопутствующие терапии. 7 По этой причине руководство ACG предлагает гибридную терапию в качестве альтернативы тройной терапии кларитромицином. 7
Терапия на основе левофлоксацина в контексте первой линии включает тройную терапию с ИПП и амоксициллином; модифицированная последовательная терапия, состоящая из 5-7 дней приема ИПП, левофлоксацина и нитроимидазола; и четырехкратная терапия, состоящая из левофлоксацина, омепразола (ИПП), нитазоксанида и доксициклина (терапия НАГРУЗКОЙ) в течение 7 или 10 дней. 7 Как и в случае с другими препаратами H pylori , в руководстве ACG отмечается отсутствие данных в Северной Америке в отношении передовых методов лечения на основе левофлоксацина и обращаются к международным данным. 7 Отмечая, что тройная терапия левофлоксацином в течение 10-14 дней может быть альтернативой тройной терапии кларитромицином и что фторхинолон-содержащая последовательная терапия в течение 10-14 дней и терапия LOAD в течение 7-10 дней дают наиболее многообещающие результаты, руководство ACG Тем не менее авторы предупреждают, что устойчивость к фторхинолонам в Северной Америке может быть даже выше, чем устойчивость к кларитромицину. 7
Спасательная терапия
Поскольку от 10% до 30% лечения первой линии H pylori терпят неудачу, необходимо рассмотреть варианты спасательной терапии. 8 В своем руководстве от 2017 года ACG рекомендует, чтобы, если у пациента есть стойкая инфекция H pylori и ранее лечился антибиотиками, врачу следует избегать использования тех же антибиотиков в будущих терапиях. 7 Авторы рекомендаций рекомендуют выбирать наилучшее спасительное лечение из следующих вариантов на основании местных данных о резистентности к противомикробным препаратам и недавнего воздействия антибиотиков на пациента: четырехкратная терапия висмутом в течение 14 дней (рекомендуется), трехкратная схема лечения левофлоксацином в течение 14 дней (рекомендуется), сопутствующая терапия в течение 10–14 дней (рекомендуется), тройная схема приема рифабутина, состоящая из ИПП, амоксициллина и рифабутина в течение 10 дней (рекомендуется), и двойная терапия высокой дозой, состоящая из ИПП и амоксициллина в течение 14 дней (рекомендуется).Руководство ACG не рекомендует использовать тройную терапию кларитромицином в качестве схемы спасения. Если пациент получал лечение первой линии, содержащее кларитромицин, рекомендуется использовать четырехкратную терапию висмутом или левофлоксацин. Если пациенту была назначена четырехкратная терапия висмутом в качестве лечения первой линии, он должен получить схемы лечения, содержащие кларитромицин или левофлоксацин, в качестве альтернативного лечения. 7
Неудовлетворенные потребности
Руководства по лечению обсуждают устойчивость к антибиотикам, поскольку она относится к H pylori , но также может рассматриваться как непреднамеренно способствующая неправильному использованию. 9 H pylori — это высокоприоритетная устойчивая к антибиотикам бактерия, согласно определению Всемирной организации здравоохранения 9 , и включена в список соответствующих патогенов FDA, которые могут представлять серьезную угрозу для здоровья населения. 10 В ретроспективном исследовании пациентов в Китае исследователи оценили распространенность устойчивости к антибиотикам к H pylori у взрослых с или без предварительного лечения инфекции, у детей, ранее не получавших лечение, и у населения в целом. 11 Результаты показали высокую устойчивость к метронидазолу, кларитромицину и левофлоксацину. Эти показатели были самыми высокими у взрослых, ранее принимавших антибиотики, особенно метронидазол. 11 Португальские исследователи проанализировали механизмы устойчивости H pylori к кларитромицину и обнаружили множество мутаций в области 23S рРНК изолятов. 12 Поскольку кларитромицин ингибирует синтез белка путем связывания с петлей пептидилтрансферазы V-домена 23S рРНК, любая мутация в этой последовательности РНК будет ингибировать связывание и делать кларитромицин неактивным.12 В период с 2006 по 2016 год уровни устойчивости составляли от 21% до 30% для кларитромицина и левофлоксацина в США и от 10% до 20% для метронидазола в США и Канаде. 13 Чувствительность к антибиотикам является единственным наиболее важным предиктором успеха в клинических испытаниях эрадикации H pylori , но устойчивость к антибиотикам к кларитромицину, метронидазолу и левофлоксацину ограничивает успех обычных схем, используемых сегодня.
Тестирование на чувствительность к противомикробным препаратам
Тестирование на чувствительность к противомикробным препаратам неоценимо при выборе наиболее подходящей схемы лечения для инфицированных лиц. 7 Однако это не является широко распространенной практикой в Северной Америке. 6 Для получения изолятов культуры и тестирования чувствительности требуется эндоскопия верхних отделов желудочно-кишечного тракта, которая является дорогостоящей. 14 Кроме того, H pylori является микроаэрофилом, поэтому для его роста требуются определенные условия, что затрудняет культивирование и транспортировку. 15 Тем не менее, надзор за устойчивостью к антибиотикам следует отслеживать в течение долгого времени, чтобы направлять лечение. 15
Затраты на H. pylori
Инфекция H. pylori связана с риском развития язвенной болезни, гастрита и некардиального рака желудка. 1,2 Он отвечает за 90% язв двенадцатиперстной кишки и от 70% до 90% язв желудка. 16 В США ежегодные оценочные расходы на здравоохранение, связанные с гастродуоденальными язвами, в 2015 году составили 777 миллионов долларов. На лекарства, отпускаемые по рецепту, пришлось 189,6 миллиона долларов (24,4%) этих расходов. 17 В 2014 г. на гастрит и диспепсию приходилось около 2,8 миллиона обращений за амбулаторной помощью 17 , а на гастрит / дуоденит было госпитализировано более 58 000 отделений неотложной помощи. 17 В 2015 г. частота повторной госпитализации по всем причинам за 30 дней гастрита составила 14%, при среднем уровне платы в размере 28 349 долларов США за указанное пребывание и 31 111 долларов США за повторную госпитализацию. 17 Общие расходы на здравоохранение, связанные с гастритом и дуоденитом, составили почти 1,2 миллиарда долларов в 2015 году, в том числе 267 миллионов долларов (22,5%) на лекарства, отпускаемые по рецепту. 17 Огромные общие расходы на здравоохранение при желудочно-кишечных заболеваниях вносят существенный вклад в использование медицинских услуг в Соединенных Штатах, и расходы, вероятно, будут продолжать расти. 17
ССЫЛКИ
1. Moss SF. Клинические доказательства связи Helicobacter pylori с раком желудка. Клеточный Мол Гастроэнтерол Гепатол. 2016; 3 (2): 183-191. DOI: 10.1016 / j.jcmgh.2016.12.001
2. Кумар С., Мец, округ Колумбия, Элленберг С., Каплан Д.Е., Голдберг Д.С. Факторы риска и заболеваемость раком желудка после обнаружения инфекции Helicobacter pylori: крупное когортное исследование. Гастроэнтерология. 2020; 158 (3): 527-536.e7. DOI: 10.1053 / j. gastro.2019.10.019
3. Пламмер М., Франчески С., Винья Дж., Форман Д., де Мартель К.Глобальное бремя рака желудка, связанное с Helicobacter pylori. Int J Cancer. 2015; 136 (2): 487–490. DOI: 10.1002 / ijc.28999
4. Каяли С., Манфреди М., Гайани Ф. и др. Helicobacter pylori, пути передачи и рецидивы инфекции: современное состояние. Acta Biomed. 2018; 89 (приложение 8): 72-76. DOI: 10.23750 / abm.v89i8-S.7947
5. Hooi JKY, Lai WY, Ng WK, et al. Глобальная распространенность инфекции Helicobacter pylori: систематический обзор и метаанализ. Гастроэнтерология. 2017; 153 (2): 420-429.DOI: 10.1053 / j.gastro.2017.04.022
6. Салим Н., Хоуден CW. Обновленная информация о лечении инфекции Helicobacter pylori. Варианты лечения Curr Gastroenterol. 2020; 18: 476-487. DOI: 10.1007 / s11938-020-00300-3
7. Chey WD, Leontiadis GI, Howden CW, Moss SF. Клинические рекомендации ACG: лечение инфекции Helicobacter pylori. Am J Gastroenterol. 2017; 112 (2): 212-239. DOI: 10.1038 / ajg.2016.563
8. Сиддик О., Овалле А., Сиддик А.С., Мосс С.Ф. Инфекция Helicobacter pylori: новости для терапевтов в эпоху роста глобальной устойчивости к антибиотикам.Am J Med. 2018; 131 (5): 473-479. DOI: 10.1016 / j.amjmed.2017.12.024
9. Dang BN, Graham DY. Инфекция Helicobacter pylori и устойчивость к антибиотикам: высокий приоритет ВОЗ? Нат Рев Гастроэнтерол Гепатол. 2017; 14 (7): 383-384. DOI: 10.1038 / nrgastro.2017.57
10. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, Министерство здравоохранения и социальных служб США. Составление списка патогенов, отвечающих требованиям Закона о безопасности и инновациях Управления по санитарному надзору за качеством пищевых продуктов и медикаментов. Окончательное правило. Fed Regist. 2014; 79 (108): 32464-32481.
11. Лю Д.С., Ван Ю.Х., Чжу Чж.и др. Характеристики устойчивости к антибиотикам Helicobacter pylori: данные из четырех различных популяций. Противомикробная защита от инфекций. 2019; 8: 192. DOI: 10.1186 / s13756-019-0632-1
12. Маркес А.Т., Витор Ж.М.Б., Сантос А., Олеастро М., Вале Ф.Ф. Тенденции устойчивости Helicobacter pylori к кларитромицину: от фенотипического к геномному подходам. Microb Genom. 2020; 6 (3): e000344. DOI: 10.1099 / mgen.0.000344
13. Савольди А., Каррара Э, Грэм Д. Ю., Конти М., Такконелли Э.Распространенность устойчивости к антибиотикам у Helicobacter pylori: систематический обзор и метаанализ в регионах Всемирной организации здравоохранения. Гастроэнтерология. 2018; 155 (5): 1372-1382.e17. DOI: 10.1053 / j.gastro.2018.07.007
14. Gisbert JP. Рифабутин для лечения инфекции Helicobacter pylori: обзор. Возбудители. 2021; 10 (1): 15. doi: 10.3390 / pathogens10010015
15. Mégraud F, Hazell S, Glupczynski Y. Чувствительность и устойчивость к антибиотикам. В: Mobley HLT, Mendz GL, Hazell SL, ред.Helicobacter pylori: физиология и генетика. АСМ Пресс; 2001. Глава 42. По состоянию на 29 апреля 2021 г. https://www.ncbi.nlm. nih.gov/books/NBK2469/
16. Малик Т.Ф., Гнанапандитан К., Сингх К. Язвенная болезнь желудка. В: StatPearls. StatPearls Publishing; 2021. По состоянию на 29 апреля 2021 г. https://www.ncbi.nlm.nih.gov/books/NBK534792/
17. Peery AF, Crockett SD, Murphy CC, et al. Бремя и стоимость заболеваний желудочно-кишечного тракта, печени и поджелудочной железы в США: обновление 2018 г. Гастроэнтерология.2019; 156 (1): 254-272.e11. doi: 10.1053 / j.gastro.2018.08.063
Ликвидация Helicobacter pylori — обновленная информация о последних методах лечения
Джулиан Яксли
Бхаскар Чакраварти
Предпосылки
Ликвидация Helicobacter pylori (H. pylori) может быть сложной задачей при определенных обстоятельствах. В настоящее время не существует терапии первой линии, которая лечила бы всех пациентов.
Objective / s
В этой статье обобщается роль новых методов лечения в лечении H.pylori . Считается, что эти новые терапевтические стратегии, известные как последовательная терапия и терапия спасения, обеспечивают более высокую скорость эрадикации по сравнению с рекомендованными в настоящее время терапиями первой линии. В этой статье описывается растущий объем доказательств, подтверждающих их эффективность.
Обсуждение
Последовательная терапия и терапия спасения недавно появились в качестве альтернативных схем эрадикации H. pylori . Хотя текущие руководства по-прежнему рекомендуют традиционные методы лечения H.pylori , врачи общей практики должны знать об этих новых стратегиях, чтобы их можно было применять, когда традиционная терапия не помогает.
Связь между Helicobacter pylori ( H. pylori ) и пептическими язвами в настоящее время установлена. Колонизация H. pylori является основным признанным фактором риска развития язвенной болезни (PUD), и ее искоренение произвело революцию в современном лечении язвенной болезни. Примерно 15 лет назад основой терапии было кратковременное заживление язв и облегчение симптомов без уничтожения организма.Это потребовало длительной поддерживающей терапии и способствовало высокой частоте рецидивов.
Сегодня новые схемы эрадикации изменяют естественное течение язвенной болезни и все чаще предлагают долгосрочное лечение. Тем не менее, постоянно меняющееся лицо терапии H. pylori , вызванное устойчивостью организма к различным антибиотикам, по-прежнему представляет собой проблему для врачей.
Патогенез болезни, вызванной H. pylori
H.pylori — это грамотрицательная палочка, которая естественным образом колонизирует желудок человека не менее 50 000 лет. 1 Обычно он приобретается в детстве и в какой-то момент жизни колонизирует слизистую желудка около 50% населения мира. 1 В западных странах инфекция H. pylori имеет распространенность примерно 30%. 1
H. pylori был впервые идентифицирован и выделен из образца биопсии желудка в 1983 году. 2 Открытие было сделано в Австралии Маршаллом и Уорреном, которые осознали, что почти все пациенты с язвой желудка или двенадцатиперстной кишки, которых они наблюдали в период с 1979 по 1984 год, были инфицированы одним и тем же организмом. 3 H. pylori с тех пор превратился в важный патоген, связанный с гастродуоденальной областью, играющий важную роль в патогенезе большинства случаев ЯБД. 2
Инфекция H. pylori вызывает стойкий иммунный ответ.Поскольку организм обладает многочисленными адаптациями, предотвращающими обнаружение иммунной системы, выведение организмом никогда не бывает полным. В результате устойчивые воспалительные процессы в желудке вызывают сокращение популяции D-клеток, продуцирующих соматостатин. 1 Это вызывает последующее повышение секреции гастрина с последующим увеличением выделения кислоты желудочного сока, что может привести к пептической язве у некоторых пациентов.
Во всем мире более 80% язв двенадцатиперстной кишки и более 60% язв желудка связаны с H.pylori . 1 У большинства пациентов, инфицированных этим организмом, не развиваются пептические язвы, хотя у большинства разовьется гастрит. Риск возникновения язвы желудка или двенадцатиперстной кишки в течение жизни составляет всего 10%, 4 , что несколько меньше, чем риск колонизации H. pylori . Причина, по которой только у некоторых развиваются язвы, остается нерешенной, хотя комбинация различий в штаммах бактерий, восприимчивости хозяина и факторов окружающей среды, вероятно, сыграет свою роль. 1
Обследование и диагностика инфекции
Ретроспективное исследование, проведенное в Калифорнии в 1998 году, показало, что менее половины пациентов с диагнозом ЯБЛ прошли скрининг на H.pylori их терапевтом. 5 К счастью, по мере того, как растет понимание естественного течения язв желудка и двенадцатиперстной кишки, тестирование H. pylori стало более распространенным за последнее десятилетие.
Пептическая язва, связанная с H. pylori , должна рассматриваться у пациентов с болью в эпигастрии или диспепсией. Колонизацию также следует заподозрить и провести скрининг у пациентов с семейным анамнезом рака желудка или лимфоидной лимфомой, связанной со слизистой оболочкой желудка (MALT). 6 Также важно провести скрининг на инфекцию H. pylori у любого пациента, которому предстоит краткосрочная или длительная терапия нестероидными противовоспалительными препаратами (НПВП), поскольку эрадикация снижает частоту язвенной болезни у этих пациентов. . 7
Было бы неправильно исследовать H. pylori изначально при наличии тревожных симптомов, таких как потеря веса, кровотечение, дисфагия или симптомы у пациента старше 55 лет. 4 В этом контексте исследования в первую очередь должны быть направлены на исключение злокачественных новообразований, например, с помощью гастроскопии.
Исследования H. pylori в целом делятся на инвазивные и неинвазивные методы. У каждого метода есть свои преимущества и недостатки ( Таблица 1 ). Наиболее широко используемым неинвазивным тестом в общей практике является серологический тест. Если у пациента наблюдается высокий титр, это указывает на активную инфекцию, тогда как низкий титр может просто отражать предыдущее воздействие H.pylori . Дыхательный тест на мочевину — лучший тест для контроля успеха эрадикации после лечения, хотя он может быть доступен не всем врачам общей практики.
| Тест | Механизм | Примечания |
|---|---|---|
| Инвазивный | ||
| Быстрый тест на уреазу |
|
|
| Культура |
|
|
| Гистология |
|
|
| Неинвазивный | ||
| Серология |
|
|
| Дыхательный тест на мочевину |
|
|
| Анализ стула на антиген |
|
|
| IgG, иммуноглобулин G; СОЛОД, лимфоидная ткань, связанная со слизистой оболочкой | ||
Традиционные схемы ликвидации
Схемы ликвидации H. pylori продолжали развиваться в течение последних 20 лет.Первоначально основная терапия включала блокаторы гистаминовых рецепторов H 2 с антибиотиком. Уровень успешного искоренения составил 73–84%. 5 Со временем эта терапия использовалась все реже, так как появились новые схемы с лучшими результатами.
Примерно 15 лет назад были внедрены тройная терапия на основе висмута и двойная терапия на основе ингибиторов протонной помпы (ИПП). Они стали наиболее широко используемыми методами лечения в течение следующего десятилетия или около того, пока их не вытеснили более новые альтернативы.Двойная терапия на основе ИПП не имела адекватных показателей успеха, в то время как тройная и четверная терапия на основе висмута имела значительные побочные эффекты. Эти побочные эффекты часто наблюдались пожилыми пациентами, которые попадали в больницу в анекдотическом опыте одного из авторов.
Сегодня тройная терапия на основе ИПП является наиболее широко используемым методом во всем мире. 8 Эта схема включает использование ИПП в сочетании с амоксициллином и кларитромицином. Текущие терапевтические рекомендации в Австралии, пересмотренные в июле 2013 года, рекомендуют тройную терапию на основе ИПП в качестве меры первой линии для эрадикации H.pylori 9 ( Таблица 2 ).
| Эрадикационная терапия | Компоненты | Примечания |
|---|---|---|
| Тройная терапия на основе ИПП |
|
|
| Четверная терапия |
|
|
| ACG, Американский колледж гастроэнтерологии | ||
В этих рекомендациях указывается, что устойчивость к кларитромицину до лечения в Австралии составляет 5–7% и указывает на вероятность ее роста. 9 Следовательно, чтобы избежать неудачи лечения, было бы разумно рассмотреть рекомендацию Американского колледжа гастроэнтерологии (ACG) о том, что в областях с известной высокой устойчивостью к кларитромицину может быть предпочтительнее четырехкратная терапия на основе висмута. 10 Однако висмут доступен только в Австралии по схеме особого доступа. 9
Эффективность тройной терапии была широко проверена и не доказала превосходства схем, применяемых два десятилетия назад. 11,12 Стандартная тройная терапия на основе ИПП дает 70–85% успеха. 1 Кроме того, недавнее рандомизированное исследование 169 пациентов, которые испытали четырехкратную терапию после неудачной тройной терапии, показало, что четырехкратная терапия, рекомендованная при резистентности к кларитромицину, также не дает результатов в 20–25% случаев. 13 Сопоставимые результаты были получены в обширном шведском объединенном анализе, в котором тройная терапия на основе ИПП сравнивалась с различными другими традиционными методами лечения H.pylori . 14 Они включали четырехкратную терапию, терапию на основе висмута и двойную терапию на основе ИПП. Во всех группах лечения показатель успешной эрадикации был одинаковым. Вывод, который следует сделать из шведского исследования, заключается в том, что при всех традиционно прописываемых схемах эрадикация успешна лишь частично.
Доказательства для новых методов лечения
Последовательная терапия
В то время как стандартная тройная терапия остается протоколом первой линии для инфекции H. pylori , 15 растущая устойчивость к антибиотикам, используемым в этом лечении, вызывает озабоченность.В последнее время это привело к возрождению интереса к новым терапевтическим стратегиям, одной из которых является последовательная терапия.
Доказательства в пользу последовательной терапии обнадеживают: в ряде исследований сообщается, что уровень эрадикации выше, чем у любого широко используемого в настоящее время лечения. Последовательная терапия — это двухэтапная 10-дневная программа, состоящая из введения ИПП с амоксициллином в течение первых 5 дней с последующей тройной терапией, которая включает ИПП, кларитромицин и тинидазол в течение следующих 5 дней.
Примером схемы может быть эзомепразол 20 мг два раза в день в сочетании с амоксициллином 1 г два раза в день, назначаемый в течение 5 дней. Затем необходимо провести тройную терапию эзомепразолом 20 мг два раза в день, кларитромицином 500 мг два раза в день и тинидазолом 500 мг дважды в течение следующих 5 дней. 16
В январе 2013 г. Lancet опубликовал рандомизированное контролируемое исследование, в котором сравнивали последовательную терапию с тройной терапией на основе ИПП. Было обнаружено, что группа последовательного лечения давала более высокие показатели эрадикации по сравнению со стандартной терапией 87.0% и 82,3% соответственно. 17 В этом испытании также была протестирована 14-дневная последовательная терапия, которая оказалась еще более эффективной с показателем успеха 90,7%. 15
Последовательная терапия доказала свою высокую эффективность в других исследованиях. Недавний анализ намерения лечить 22 рандомизированных исследования последовательной терапии с участием 2388 пациентов показал уровень эрадикации порядка 91,3%. 18 Если этот ряд данных расширен до анализа протокола, последовательная терапия предвещает 93.7% Уровень эрадикации H. pylori . 18
Спасательная терапия
Несмотря на высокую эффективность последовательной терапии, некоторые пациенты не реагируют. Имеются некоторые данные по варианту второй линии для этой когорты, называемому «спасательной терапией». Спасательная терапия представляет собой тройную терапию, включающую ИПП, амоксициллин и левофлоксацин, вводимые в течение 10 дней. Предлагаемый рецепт будет включать эзомепразол 20 мг два раза в день, амоксициллин 500 мг два раза в день и левофлоксацин 500 мг два раза в день. 18
Ограниченные данные, основанные на доказательствах, доступные в настоящее время в Австралии, позволяют предположить, что терапия спасения достигает высоких показателей успеха. 9 ACG сообщает, что спасательная обработка эффективна на 76% при реализации после неудачного последовательного режима. 8 Небольшое проспективное пилотное исследование, проведенное Зулло и другими, также показало, что спасательная терапия является действенной альтернативой в случае неэффективности эрадикации при последовательной терапии. 19 В исследование были включены 35 пациентов, получавших 10-дневную тройную терапию рабепразолом, левофлоксацином и амоксициллином после неудачной последовательной терапии.При анализе намерения лечить это лечение было успешным в 85,7% случаев. 19
Решение проблемы устойчивости к антибиотикам
Устойчивость к противомикробным препаратам к антибиотикам является проблемой при эрадикационной терапии. Считается, что неэффективность лечения обычно происходит из-за роста устойчивости к противомикробным препаратам. Несколько исследований показали, что эрадикация H. pylori более успешна, если до начала лечения проводится тестирование чувствительности. 6 Это позволяет подбирать антибиотики в соответствии с восприимчивостью организма.
Также важно спросить пациентов о предыдущих лекарствах. Имеющиеся данные свидетельствуют о том, что предыдущее воздействие метронидазола или макролидных антибиотиков на пациента снижает успех эрадикации. 9 Если они подверглись подобному воздействию в прошлом, следует выбирать препараты замещающих классов, чтобы избежать неудачного лечения.
За последние 10 лет было отмечено снижение эффективности стандартной тройной терапии. 17 Хотя данные указывают на более низкую частоту неудач лечения с помощью новых методов лечения, вполне вероятно, что они также испытают подобное явление. 17 Поскольку развитие лекарственной устойчивости останется проблемой, новые методы лечения должны быть внедрены раньше, чем позже. Таким образом, важно подчеркнуть, что после первоначальной неудачи стандартной тройной терапии эту схему не следует повторять, 9 скорее следует уделить внимание испытаниям последовательной или спасательной терапии.
Соответствие требованиям
Хорошее соблюдение пациентом режима лечения также является важным предиктором результата. 10 Поэтому важно подчеркнуть его важность для пациентов.Плохое соблюдение не только способствует устойчивости к антибиотикам, но и пациенты, которые не завершили полный курс лечения антибиотиками, также с большей вероятностью не пройдут лечение. В Австралии неполное соблюдение режима лечения является наиболее частой причиной неудачной эрадикации. 9
Побочные эффекты являются основной причиной несоблюдения схем эрадикации. Хотя они встречаются примерно у 5–20% пациентов, 10 было бы разумно сообщить пациентам о возможных побочных эффектах до начала лечения.Важные побочные эффекты перечислены в , Таблица 3 . Профили побочных эффектов последовательной терапии и стандартной тройной терапии аналогичны. 16
Финансовые затраты на последовательную и спасительную терапию также являются проблемой, определяющей соблюдение пациентом режима лечения. Поскольку 10-дневная последовательная терапия дает результаты лишь незначительно хуже, чем 14-дневная последовательная терапия, экономически выгодно рекомендовать более короткое лечение. 9,16
| Противомикробное средство | Побочные эффекты | |
|---|---|---|
| Часто | Нечасто | |
| Ингибитор протонной помпы (ИПП) |
|
|
| Кларитромицин |
| |
| Амоксициллин | ||
| Метронидазол |
|
|
| Соли висмута |
|
|
| Тетрациклин | ||
| Тинидазол |
|
|
| Левофлоксацин |
|
|
Заключение
H.pylori остается важной причиной заболеваемости во всем мире. На сегодняшний день полностью успешная терапевтическая стратегия остается труднодостижимой, однако последовательная терапия и терапия спасения становятся эффективными альтернативами первой и второй линии. Хотя пока преждевременно рекомендовать их рутинное использование во всех случаях, эти новые варианты следует рассматривать для лечения инфекции H. pylori , когда стандартная тройная терапия не дает результата.
Конкурирующие интересы: Нет.
Происхождение и экспертная оценка: Не введен в эксплуатацию; внешняя экспертная оценка.
Список литературы
- Лонг Д., Фаучи А., Каспер Д. и др. Принципы внутренней медицины Харрисона. Нью-Йорк: McGraw Hill Companies; 2012.
- Феннерти М., Либерман Д., Вакил Н. и др. Эффективность лечения Helicobacter pylori в условиях клинической практики. Arch Intern Med 1999; 159: 1562–66.
- Уоррен Дж., Маршалл Б. Неопознанные изогнутые бациллы на эпителии желудка при активном хроническом гастрите.Ланцет 1983; 1: 1273–75.
- Рамакришнан К., Салинас Р. Язвенная болезнь. Am Fam Physician 2007; 76: 1005–12.
- Peura D. Helicobacter pylori: варианты рационального ведения. Am J Med 1998; 105: 424–30.
- Stenstroem B, Mendis A, Marshall B. Helicobacter pylori: новейшие достижения в диагностике и лечении. Врач Aust Fam, 2008; 37: 608–12.
- Талли Н., Вакил Н. Руководство по ведению диспепсии. Am J Gastroenterol 2005; 100: 2324–37.
- Malfertheiner P, Megraud F, O’Morain C, et al.Современные концепции лечения инфекции Helicobacter pylori: Маастрихтский консенсусный отчет III. Кишечник 2007; 56: 772–81.
- Группа экспертов по антибиотикам. Ликвидация Helicobacter pylori и заживление язв В: eTG Complete [Интернет] Мельбурн. ООО «Терапевтические рекомендации», 2013 г. Доступно на сайте www.tg.org.au [Доступно с 15 марта 2013 г.].
- Chey W, Wong B. Руководство Американского колледжа гастроэнтерологии по лечению инфекции Helicobacter pylori. Am J Gastroenterol 2007; 102: 1808–25.
- Лайне Л., Феннерти М., Осато М. и др. Эрадикационная терапия Helicobacter pylori на основе эзомепразола и эффект устойчивости к антибиотикам: результаты трех многоцентровых двойных слепых исследований в США. Am J Gastroenterol 2000; 95: 3393–98.
- Vakil N, Lanza F, Schwartz H, Barth J. Семидневная терапия Helicobacter pylori в Соединенных Штатах. Aliment Pharmacol Ther 2004; 20: 99–107.
- Юн Дж, Байк Дж, Ким Й и др. Сравнение скорости эрадикации между 1-недельной и 2-недельной висмутсодержащей четырехкратной спасательной терапией для эрадикации Helicobacter pylori.Кишечная печень 2012; 6: 434–39.
- Унге П. Какие еще схемы лечения инфекции Helicobacter pylori исследуются? Гастроэнтерол 1997; 113: 131–48.
- Эдвардс П. Искоренение Helicobacter pylori: какая последняя рекомендованная терапия? Curr Ther 1996; январь: 49–54.
- Кроу С. Схемы лечения Helicobacter pylori. Сан-Диего: UpToDate; 2013.
- Liou J, Chen C, Chen M и др. Последовательная и тройная терапия для лечения Helicobacter pylori первой линии: многоцентровое открытое рандомизированное исследование.Ланцет 2013; 381: 205–13.
- Vaira D, Zullo A, Hassan C, Fiorini G, Vakil N. Последовательная терапия для ликвидации Helicobacter pylori: время пришло! Ther Adv Gastroenterol 2009; 2: 317–22.
- Зулло А., Франческо В., Хассан С., Панелла С., Морини С., Иерарди Е. Лечение второй линии для эрадикации Helicobacter pylori после неудачной последовательной терапии: пилотное исследование. Future Med 2006; 3: 251–54.
- Ди Каро С., Францески Ф., Мариани А. и др. Тройные схемы на основе левофлоксацина второго ряда для эрадикации Helicobacter pylori.Dig Liver Dis 2009; 41: 480–85.
- Micomedix 2.0. 2013 г. [обновлено 13 марта 2013 г.] Доступно по адресу: http://healthcare.thomsonreuters.com/ micromedexMobile / [доступ 26 марта 2013 г.].
- Австралийский справочник по лекарственным средствам. Аделаида: Фармацевтическое общество Австралии; 2010.
Переписка [email protected]
Открытие или сохранение файлов
Файлы на веб-сайте можно открывать или загружать и сохранять на свой компьютер или устройство.
Чтобы открыть, щелкните ссылку, ваш компьютер или устройство попытается открыть файл с помощью совместимого программного обеспечения.
Чтобы сохранить файл, щелкните ссылку правой кнопкой мыши или щелкните ссылку и выберите «Сохранить как …». Следуйте подсказкам, чтобы выбрать место.
Типы файлов
PDF Большинство документов на веб-сайте RACGP имеют формат Portable Document Format (PDF). Эти файлы будут иметь «PDF» в скобках вместе с размером файла для загрузки. Чтобы открыть файл PDF, вам потребуется совместимое программное обеспечение, такое как Adobe Reader.Если у вас его нет, вы можете бесплатно загрузить Adobe Reader.
DOC Некоторые документы на этом сайте представлены в формате Microsoft Word.
