Низкий гемоглобин — что делать?
Гемоглобин — один из важнейших элементов крови, он выполняет функцию переноса кислорода к тканям и клеткам организма, забирая из них углекислый газ. Изменение показателей гемоглобина может быть следствием какого-либо заболевания.
Факторы, влияющие на развитие анемии:
- Разрушение эритроцитов быстрее нормы.
- Уменьшение объёма вырабатываемых эритроцитов.
- Потеря большого количества крови.
- Нарушение работы органов кроветворения.
- Наличие инфекционных заболеваний.
- Дефицит витаминов и микроэлементов. (особенно влияет количество железа в организме)
- Неблагоприятная экологическая обстановка.
Какие бывают уровни гемоглобина?
Уровень гемоглобина в крови можно определить с помощью анализа крови, который назначает ваш лечащий врач — гематолог.
Легкая степень недостаточности гемоглобина — определяется уровнем гемоглобина в крови до 90 г/ л.
Средняя степень недостаточности гемоглобина — определяется уровнем гемоглобина в диапазоне от 70 до 90 г/л. Распространенными признаками такой анемии бывает головная боль, головокружение, сухость и шершавость кожи, нарушения в работе системы пищеварения.
Тяжелая степень недостаточности гемоглобина — определяется уровнем гемоглобина ниже 70 г/л., часто наблюдается утомляемость, потеря сознания и головные боли. У женщин возникают сбои в менструальном цикле, вплоть до отсутствия менструации. Кожа бледнеет, состояние волос и ногтей ухудшается, они становятся ломкими. Появляется ощущение холодных рук и ног.
Низкий уровень гемоглобина влияет на работу всех органов, такое состояние опасно для жизни.
Если вы наблюдаете у себя симптомы анемии, ощущаете ухудшение состояния здоровья, обязательно обратитесь к врачу. Гематолог МЦ «САНАС» проведет осмотр и назначит необходимое обследование, по результатам которого назначит правильное лечение.
Гематолог МЦ «САНАС» проведет осмотр и назначит необходимое обследование, по результатам которого назначит правильное лечение.
Только профильный специалист — гематолог, может назначить правильное лечение, прописать диету для повышения уровня железа в крови.
Может быть рекомендовано добавление в рацион красного мяса, морепродуктов, гречихи и фруктов с высоким содержанием витамина C, а также назначит необходимые пациенту лекарственные препараты. Обычный курс лечения длится от нескольких недель до месяца.
Почему уровень гемоглобина в крови скачет то вверх, то вниз и как его держать в норме. — Верис
Гемоглобин в крови ниже нормы — это плохо. Выше нормы — ещё хуже. Почему его уровень в крови скачет и что делать, чтобы этот показатель всегда был в норме?
1. Главная функция гемоглобина — транспортировка кислорода во все органы и ткани. Понятия нормы гемоглобина у мужчин и женщин разнятся (для женщин нормальный уровень гемоглобина — 120-140 г/л, у мужчин — 130-160 г/л).
Для беременных женщин (организм которых работает за двоих) и для младенцев нормальным уровнем гемоглобина считается 110 г/л. Однако будущим мамам необходимо постоянно контролировать уровень гемоглобина. Его недостаток может вызвать преждевременные роды или задержку развития плода, а избыток — смерть ребёнка.
2. Умеренное снижение гемоглобина (анемия, малокровие) — явление обычное, особенно у женщин. Это объясняется физиологически обусловленной ежемесячной потерей крови. Если месячные обильные, уровень гемоглобина может опускаться до 90 г/л.
Нередко это отмечается у пациентов с воспалительными заболеваниями желудочно-кишечного тракта: воспалённая слизистая желудка не может полноценно усваивать железо.
Самые опасные состояния — внутренние кровотечения (язвы, эрозии, опухоли, в том числе злокачественные).
 Бледность — отличительная особенность пациентов, страдающих этими заболеваниями.
Бледность — отличительная особенность пациентов, страдающих этими заболеваниями. 4. У детей высокие показатели гемоглобина — косвенный признак болезни крови или онкологических заболеваний. Поэтому оставлять без внимания высокий гемоглобин крайне опасно: нужно обязательно выяснять причину.
5. Признаки низкого уровня гемоглобина
Непреходящая слабость, снижение аппетита, сонливость, головокружения, извращение вкуса, сухая кожа, ломкие ногти, выпадение волос, заеды в уголках рта.
6. Признаки высокого гемоглобина
Сдать анализ крови в лаборатории и оперативно получить консультацию врача-гематолога (взрослого или детского) можно у нас в Семейной клинике.
 Приемы ВЗРОСЛЫХ и ДЕТЕЙ! Запись по тел. 43-03-03 и 41-03-03.
Приемы ВЗРОСЛЫХ и ДЕТЕЙ! Запись по тел. 43-03-03 и 41-03-03.Анемия при сердечно-сосудистых заболеваниях
С.П. Сидорук, Е.Б. Петрова, Н.П. Митьковская
Госпиталь, Аль-Ахса, Саудовская Аравия, УО «Белорусский государственный медицинский университет»

ключевые слова: анемия, сердечно-сосудистые заболевания, ишемическая болезнь сердца, артериальная гипертензия, дефицит железа, карбоскимальтоза
для цитирования: Сидорук С.П., Петрова Е.Б., Митьковская Н.П. Анемия при сердечно-сосудистых заболеваниях. Неотложная кардиология и кардиооваскулярные риски, 2017, Т. 1, №1, С. 38-45.
Введение
Сердечно-сосудистые заболевания являются основной причиной смерти во всем мире. Многие пациенты с сердечно-сосудистой патологией страдают анемией в результате острых или хронических сопутствующих состояний. Согласно критериям Всемирной организации здравоохранения термин «анемия» раскрывается как состояние, при котором наблюдается согласно гендерной принадлежности снижение концентрации гемоглобина в крови: у женщин — менее 120 г/л и менее 130 г/л у мужчин. Анемия является важной проблемой практического здравоохранения, так как влияет на качество жизни, смертность и является частой причиной обращения к врачу.
Анемия является важной проблемой практического здравоохранения, так как влияет на качество жизни, смертность и является частой причиной обращения к врачу.
Во всем мире анемией страдают 1,62 миллиарда людей, что составляет 24,8% от общего населения планеты. Наиболее часто анемии подвержены дети дошкольного возраста (47%), а реже всего – мужчины (12,7%). В половине случаев причиной анемии является дефицит железа [1]. Недостаток железа не только нарушает образование эритроцитов, но и ухудшает клеточные функции, связанные с мышечным метаболизмом, влияет на функцию митохондрий, нейротрансмиттеров, синтез ДНК и иммунную систему [2]. Частота анемии увеличивается с возрастом, что делает ее частым спутником сердечно-сосудистых катастроф. Анализ литературных источников продемонстрировал, что анемия является независимым предиктором кардиоваскулярных заболеваний и неблагоприятных исходов [3].
Влияние анемии на сердечно-сосудистую систему
Для оценки патологического влияния снижения концентрации уровня гемоглобина в крови на кардиоваскулярные риски необходимо рассмотреть физиологическую реакцию организма на анемию. Основными факторами, ответственными за газообмен, выступают: интенсивность кровотока и его распределение, потребление кислорода клетками, оксигенация крови. Гипоксия при анемии компенсируется каскадом гемодинамических и гемодинамически не ассоциированных механизмов, таких как активация продукции эритропоэтина, повышение тканевой утилизации кислорода. Реализация основных гемодинамических факторов достигается путем повышения контрактильной способности миокарда, уменьшения постнагрузки, увеличения преднагрузки, реализацией положительного ино- и хронотропных эффектов. Повышение продукции оксида азота, индуцированная гипоксией вазодилатация и снижение вязкости крови являются причиной уменьшения сосудистого сопротивления и приводят к снижению постнагрузки. Хроническая анемия стимулирует ангиогенез и образование новых мелких сосудов. Развитие коллатералей и микроциркуляторного русла способствует снижению постнаргузки. Повышение венозного возврата (преднагрузки) и кровенаполнения левого желудочка способствуют увеличению конечного диастолического объема и фракции выброса левого желудочка.
Основными факторами, ответственными за газообмен, выступают: интенсивность кровотока и его распределение, потребление кислорода клетками, оксигенация крови. Гипоксия при анемии компенсируется каскадом гемодинамических и гемодинамически не ассоциированных механизмов, таких как активация продукции эритропоэтина, повышение тканевой утилизации кислорода. Реализация основных гемодинамических факторов достигается путем повышения контрактильной способности миокарда, уменьшения постнагрузки, увеличения преднагрузки, реализацией положительного ино- и хронотропных эффектов. Повышение продукции оксида азота, индуцированная гипоксией вазодилатация и снижение вязкости крови являются причиной уменьшения сосудистого сопротивления и приводят к снижению постнагрузки. Хроническая анемия стимулирует ангиогенез и образование новых мелких сосудов. Развитие коллатералей и микроциркуляторного русла способствует снижению постнаргузки. Повышение венозного возврата (преднагрузки) и кровенаполнения левого желудочка способствуют увеличению конечного диастолического объема и фракции выброса левого желудочка.
Увеличение сердечного выброса в свою очередь способствует развитию артериального ремоделирования центральных сосудов эластического типа, таких как аорта и общие сонные артерии, за счёт увеличения просвета и компенсаторного утолщения комплекса интима-медии. Как следствие — повышение систолического давления и инерции, большая масса крови попадает в дилатированную артериальную систему. Активация симпатической нервной системы усиливает контрактильность левого желудочка и увеличивает частоту сердечных сокращений. В присутствии хронических заболеваний сердца эти дополнительные эффекты, опосредованные анемией, способствуют увеличению частоты сердечно-сосудистых осложнений [4].
Анемия при артериальной гипертензии
Нормохромная анемия – нередкая находка у пациентов, страдающих артериальной гипертензией (АГ), и чаще встречается при неконтролируемой гипертензии. Низкий уровень гемоглобина ассоциируется с плохим контролем артериального давления и является индикатором повышенного сердечно-сосудистого риска [5]. Согласно литературным данным, пациенты, страдающие АГ с сопутствующей анемией, имеют более высокие значения среднесуточного, ночного и недостаточное снижение ночного систолического артериального давления по сравнению с теми, у которых наблюдался нормальный уровень гемоглобина. У пациентов с анемией также прослеживается тенденция к увеличению среднесуточных значений диастолического артериального давления [6]. У пациентов с изолированной систолической гипертензией и гипертрофией левого желудочка с сопутствующим снижением уровня гемоглобина наблюдается увеличение сердечно-сосудистой смертности и частоты развитий острых нарушений мозгового кровообращения [7].
Низкий уровень гемоглобина ассоциируется с плохим контролем артериального давления и является индикатором повышенного сердечно-сосудистого риска [5]. Согласно литературным данным, пациенты, страдающие АГ с сопутствующей анемией, имеют более высокие значения среднесуточного, ночного и недостаточное снижение ночного систолического артериального давления по сравнению с теми, у которых наблюдался нормальный уровень гемоглобина. У пациентов с анемией также прослеживается тенденция к увеличению среднесуточных значений диастолического артериального давления [6]. У пациентов с изолированной систолической гипертензией и гипертрофией левого желудочка с сопутствующим снижением уровня гемоглобина наблюдается увеличение сердечно-сосудистой смертности и частоты развитий острых нарушений мозгового кровообращения [7].
Изменение электрокардиограммы при анемии
Электрокардиографические реполяризационные изменения (депрессия сегмента ST, инверсия зубца Т, удлинение интервала QT) часто встречаются у пациентов с анемией как в покое, так и при нагрузке [8]. Было обнаружено, что уровень гемоглобина сильно коррелирует с изменениями на электрокардиограмме [9].
Было обнаружено, что уровень гемоглобина сильно коррелирует с изменениями на электрокардиограмме [9].
Удлинение интервала QT является предиктором желудочковой аритмии и внезапной смерти. Гипоксия и нарушение доставки кислорода у пациентов с анемией может быть причиной нарушения реполяризации миокарда. Согласно проведенным исследованиям, анемия, макроцитоз и анизоцитоз коррелируют с удлинением интервала QT у пациентов с артериальной гипертензией и могут учитываться в оценке риска внезапной смерти [10]. Низкий уровень железа в остальном у практически здоровых детей отрицательно коррелирует с интервалами QT и QTс и может указывать на дополнительный риск развития аритмии [11].
Mehta и соавт. продемонстрировал значимую и воспроизводимую депрессию сегмента ST у пациентов с железно-дефицитной анемией во время нагрузочных тестов. Эти электрофизиологические изменения исчезали после лечения препаратами железа ещё до нормализации уровня гемоглобина, что может объясняться эффектом железа на тканевом уровне [12].
Анемия при ишемической болезни сердца
Ишемия миокарда определяется степенью выраженности несоответствия потребности кардиомиоцитов в кислороде и возможностями его доставки. Определяющими факторами, влияющими на заинтересованность миокарда в кислороде, являются: частота сердечных сокращений, контрактильность миокарда и напряжение стенки сердца. Факторами, определяющими доставку кислорода к сердцу, являются содержание кислорода в крови и интенсивность коронарного кровотока. Увеличение доставки кислорода к миокарду в ответ на увеличение потребления происходит путем уменьшения сопротивления коронарного русла. Экстракция кислорода кардиомиоцитами даже в покое составляет около 90% [13]. У пациентов без коронарной патологии даже значительное снижение содержания кислорода в коронарном кровотоке может компенсироваться за счёт периферической вазодилатации. При коронарном стенозе этот механизм имеет ограниченные возможности. Согласно данным литературы, у животных с анемией при остром инфаркте миокарда увеличивалась зона инфарцирования, снижалась насосная функция сердца и выживаемость. Переливание крови животным с анемией до уровня гемоглобина 100 г/л уменьшало зону инфаркта и улучшало контрактильную возможность миокарда. Вместе с тем, переливание крови до уровня гемоглобина 120 г/л было связано с увеличением зоны инфаркта [14].
Переливание крови животным с анемией до уровня гемоглобина 100 г/л уменьшало зону инфаркта и улучшало контрактильную возможность миокарда. Вместе с тем, переливание крови до уровня гемоглобина 120 г/л было связано с увеличением зоны инфаркта [14].
Sabatine et al. обнаружил U-образную зависимость клинических событий при остром коронарном синдроме к 30-му дню: у пациентов с инфарктом миокарда с подъемом сегмента ST наблюдалось увеличение смертности при уровне гемоглобина ниже 140 г/л и выше 170 г/л, в то время как у пациентов с инфарктом миокарда без подъема сегмента ST смертность, размер инфаркта и ишемии увеличивались при уровне гемоглобина менее 110 г/л и более 160 г/л [15].
Анемия является весомым фактором риска при ишемической болезни сердца (ИБС). Пациенты с ишемической болезнью сердца и сопутствующей анемией имеют более выраженную степень коронарной патологии. Согласно ряду публикаций, у пациентов с ИБС и анемией уровень гемоглобина, сывороточного железа и общая железосвязывающая способность крови отрицательно коррелируют с тяжестью коронарной патологии [16]. У пациентов с ишемической болезнью сердца и сопутствующей анемией наблюдается увеличение смертности по сравнению с категорией лиц с изолированной ИБС, а анемия выступает независимым предиктором возникновения острого ишемического повреждения миокарда [17].
У пациентов с ишемической болезнью сердца и сопутствующей анемией наблюдается увеличение смертности по сравнению с категорией лиц с изолированной ИБС, а анемия выступает независимым предиктором возникновения острого ишемического повреждения миокарда [17].
Исследование Ferreira и соавт. выявило, что уровень гемоглобина менее 108 г/л являлся одним из наиболее сильных независимых предикторов смертности к концу первого года при остром коронарном синдроме. Он предложил включить уровень гемоглобина в оценку риска пациентов, госпитализированных с острым коронарным синдромом, так как это является доступным параметром и систематически оценивается при госпитализации [18].
В исследовании Cadilac анемия часто встречалась у пациентов, направленных на первичную ангиопластику по поводу острого инфаркта миокарда. Была продемонстрирована сильная корреляционная связь между снижением уровня гемоглобина и развитием неблагоприятных исходов, увеличением смертности. Сделан вывод, что анемия выступала независимым предиктором госпитальной и общей смертности к концу первого года постинфарктного периода [19].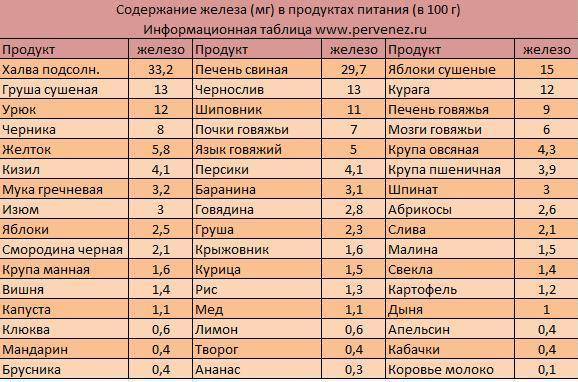 Тяжелая анемия может приводить к дисбалансу между доставкой и потреблением кислорода в миокарде даже при отсутствии гемодинамически значимого коронарного стенозирования. Bailey с соавт. описал пример развития острого коронарного синдрома с подъемом сегмента ST у пациента с тяжелой анемией в отсутствии ангиографически значимого коронарного стеноза, тромбоза или спазма [20].
Тяжелая анемия может приводить к дисбалансу между доставкой и потреблением кислорода в миокарде даже при отсутствии гемодинамически значимого коронарного стенозирования. Bailey с соавт. описал пример развития острого коронарного синдрома с подъемом сегмента ST у пациента с тяжелой анемией в отсутствии ангиографически значимого коронарного стеноза, тромбоза или спазма [20].
Таким образом, причины неблагоприятных исходов у пациентов с анемией и коронарной патологией многочисленны. Уменьшение кислородной емкости крови, а также активация симпатической нервной системы могут повышать потребность миокарда в кислороде и усугублять ишемию.
Анемия при сердечной недостаточности
Анемия – частое сопутствующее патологическое состояние при сердечной недостаточности (СН). У пациентов с сердечной недостаточностью и сопутствующей анемией прослеживается следующая тенденция: у них более выражены симптомы левожелудочковой недостаточности, выше частота госпитализаций по поводу декомпенсации хронической сердечной недостаточности (ХСН), среди них чаще встречаются женщины, пациенты представлены старшей возрастной группой, у них чаще диагностируется сахарный диабет, сопутствующая почечная недостаточность и артериальная гипертензия [21]. Анемия – мощный предиктор повторных госпитализаций и низкой выживаемости при хронической сердечной недостаточности [22]. Частота встречаемости анемии возрастает при увеличении степени тяжести сердечной недостаточности и может достигать 79.1% у пациентов с IV функциональным классом СН по классификации Нью-Йоркской Ассоциации Сердца [23].
Анемия – мощный предиктор повторных госпитализаций и низкой выживаемости при хронической сердечной недостаточности [22]. Частота встречаемости анемии возрастает при увеличении степени тяжести сердечной недостаточности и может достигать 79.1% у пациентов с IV функциональным классом СН по классификации Нью-Йоркской Ассоциации Сердца [23].
Этиология анемии при сердечной недостаточности является многофакторной, и множество механизмов ответственно за это состояние. Увеличение системного воспаления, нейрогуморальная активация, нарушение питания, дисфункция почек, снижение ответа костного мозга на запрос и эффект приема ряда лекарственных средств вносят вклад в ее развитие. Увеличение циркулирующих провоспалительных цитокинов при СН вызывает нарушение мобилизации железа, недостаточную продукцию эритропоэтина в ответ на активацию ренин-ангиотензин-альдостероновой системы и снижение почечного кровотока, снижение функции костного мозга. Использование ингибиторов ангиотензин-превращающего фермента может дополнительно уменьшать секрецию эритропоэтина. Нарушение питания вследствие отсутствия аппетита, желудочно-кишечная мальабсорбция, прием аспирина могут усугублять железодефицитную анемию. Гемоделюция также вносит дополнительный вклад в становление анемии [24].
Нарушение питания вследствие отсутствия аппетита, желудочно-кишечная мальабсорбция, прием аспирина могут усугублять железодефицитную анемию. Гемоделюция также вносит дополнительный вклад в становление анемии [24].
Дефицит железа
Дефицит железа (ДЖ) – наиболее частая причина анемии у пациентов с сердечной недостаточностью [25,26]. Дефицит железа может наблюдаться и при нормальном уровне гемоглобина, а железодефицитное состояние без анемии выявляется у 46% пациентов со стабильной сердечной недостаточностью [27]. ДЖ может быть представлен в абсолютной и функциональной формах. При абсолютном дефиците железа наступает истощение его запасов в организме, а железодефицитная анемия может рассматриваться как конечная стадия этого истощения. Функциональный дефицит железа связан с неадекватным его высвобождением из депо в ответ на потребности костного мозга и встречается при многих острых и хронических воспалительных состояниях. Дефицит железа ассоциируется с прогрессированием симптомов сердечной недостаточности, снижением качества жизни, увеличением смертности и госпитализаций [28-30].
Активация симпатической и ренин-ангиотензин-альдостероновой систем, хроническое воспаление, абсолютный и функциональный дефицит железа, нарушение образования и активности эритропоэтина, гемоделюция, почечная дисфункция ухудшают прогноз у пациентов с сердечной недостаточностью. Вероятно, анемия является как медиатором, так и маркером неблагоприятного прогноза у пациентов с сердечной недостаточностью.
Лечение анемии у пациентов с заболеваниями сердца
Лечение анемии при сердечной недостаточности и ишемической болезни сердца может включать прием эритропоэтинов, при наличии железодефицитных состояний с анемией или без нее — терапию препаратами железа, при тяжелом течении — переливание эритроцитарной массы.
Шестнадцать рандомизированных контролируемых исследований оценивало эффект эритропоэтинов у пациентов с сердечной недостаточностью. Большинство этих исследований включало пациентов с систолической сердечной недостаточностью. Полученные данные с умеренной степенью доказательности продемонстрировали отсутствие улучшения качества жизни и переносимости физических нагрузок при лечении эритропоэтинами. В то же время данные с высокой степенью доказательности продемонстрировали отсутствие снижения смертности при лечении эритропоэтинами. Среди серьезных побочных эффектов, связанных с их применением, выделили развитие сосудистых тромбозов [31].
В то же время данные с высокой степенью доказательности продемонстрировали отсутствие снижения смертности при лечении эритропоэтинами. Среди серьезных побочных эффектов, связанных с их применением, выделили развитие сосудистых тромбозов [31].
Несмотря на то, что анемия часто встречается у пациентов с хронической сердечной недостаточностью и ишемической болезнью сердца, лечение эритропоэтинами не уменьшало смертность, риск кардиоваскулярных событий или частоту госпитализаций [31]. Американский Колледж Врачей не рекомендует использование эритропоэтинов у пациентов с сердечной недостаточностью или коронарной болезнью сердца при незначительной или умеренной степени тяжести анемии [31].
Переливание крови было предложено для коррекции тяжелой анемии у пациентов с коронарной болезнью сердца, но результаты ее эффективности противоречивы. Большинство данных получено при использовании либеральных или рестриктивных протоколов гемотрансфузий. Либеральный подход к переливанию крови был определен как гемотрансфузия при уровне гемоглобина менее 90 г/л. Рестриктивная трансфунзионная стратегия — трансфузия с уровнем гемоглобина менее 70 г/л. Метаанализ 10 исследований, включавший 203,665 пациентов с острым коронарным синдромом выявил, что либеральная гемотрансфузия ассоциировалась с увеличением общей смертности по сравнению с рестриктивной гемотрансфузией или ведением пациентов без нее [32]. Но стоит отметить, что гемотрансфузия ассоциировалась со значимым увеличением риска смерти к 30-му дню только при показателе гематокрита более 25% [32].
Рестриктивная трансфунзионная стратегия — трансфузия с уровнем гемоглобина менее 70 г/л. Метаанализ 10 исследований, включавший 203,665 пациентов с острым коронарным синдромом выявил, что либеральная гемотрансфузия ассоциировалась с увеличением общей смертности по сравнению с рестриктивной гемотрансфузией или ведением пациентов без нее [32]. Но стоит отметить, что гемотрансфузия ассоциировалась со значимым увеличением риска смерти к 30-му дню только при показателе гематокрита более 25% [32].
На сегодняшний день нет единого мнения в отношении либеральной и рестриктивной гемотрансфузионной тактики у пациентов с ИБС. Ряд исследований с низкой степенью доказательности показывают, что ограничительная трансфузия не оказывает эффект на смертность у пациентов с коронарной патологией сердца по сравнению с либеральной трансфузией. Ряд исследований, основанных на клиническом наблюдении пациентов, выдвинули утверждение: гемотрансфузия не имеет практической пользы и может нанести вред пациентам с сердечно-сосудистой патологией при уровне гемоглобина более 100г/л [31]. Пилотное исследование, включавшее 110 пациентов с острым коронарным синдромом или стабильной стенокардией, которые подвергались коронарным вмешательствам, продемонстрировало, что гемоглобин менее 100г/л коррелировал с тенденцией к увеличению больших коронарных событий, включая смерть от сердечно-сосудистых причин у пациентов с либеральной по сравнению с рестриктивной стратегией гемотрансфузий [33].
Пилотное исследование, включавшее 110 пациентов с острым коронарным синдромом или стабильной стенокардией, которые подвергались коронарным вмешательствам, продемонстрировало, что гемоглобин менее 100г/л коррелировал с тенденцией к увеличению больших коронарных событий, включая смерть от сердечно-сосудистых причин у пациентов с либеральной по сравнению с рестриктивной стратегией гемотрансфузий [33].
Из-за противоречивых результатов исследований и недостатка полноценных рандомизированных контролируемых исследований рестриктивная гемотрансфузия может иметь место в условиях острого коронарного синдрома и у госпитализированных пациентов с коронарной болезнью сердца [31, 34].
Положительные эффекты лечения внутривенными препаратами железа при дефиците железа с анемией или без у пациентов с сердечной недостаточностью
Железо является жизненно необходимым элементом для организации целого ряда жизненно важных функций в организме. Оно служит переносчиком кислорода к клеткам, является частью важных ферментных систем в различных тканях. Железосодержащие ферменты выполняют функцию по переносу электронов внутри клетки, а их функция в окислительном метаболизме – перенос энергии внутри митохондрии. Другой ключевой функцией железосодержащих ферментов (например, цитохром Р450) является синтез стероидных гормонов и желчных кислот; обезвреживание токсинов в печени; контроль эффекта нейротрансмиттеров, таких как допамин, и серотониновых систем головного мозга [35].
Железосодержащие ферменты выполняют функцию по переносу электронов внутри клетки, а их функция в окислительном метаболизме – перенос энергии внутри митохондрии. Другой ключевой функцией железосодержащих ферментов (например, цитохром Р450) является синтез стероидных гормонов и желчных кислот; обезвреживание токсинов в печени; контроль эффекта нейротрансмиттеров, таких как допамин, и серотониновых систем головного мозга [35].
Несколько исследований были адресованы лечению пациентов с заболеваниями сердца внутривенными препаратами железа. Данные Fair-HF исследования, которое включало пациентов с анемией и без продемонстрировали: только 27,6% пациентов, получавших препарат карбоксимальтозы железа внутривенно, имели кардиоваскулярные события по сравнению с 50,2% пациентов, получавших плацебо (р=0.01). Внутривенное назначение карбоксимальтозы железа увеличивало переносимость и продолжительность физических нагрузок у пациентов со стабильной сердечной недостаточностью и хроническим заболеванием почек (ХБП), не выше 3 стадии ХБП. У большинства пациентов, включенных в исследование, уровень ферритина был менее 100 мг/л [36]. Это исследование показало, что назначение 200 мг препарата карбоксимальтозы железа внутривенно увеличивало дистанцию теста 6-минутной ходьбы (317 м против 277 м) по сравнению с внутривенным назначением физиологического раствора [36]. Данное исследование с умеренной степенью доказанности продемонстрировало, что внутривенный препарат железа улучшал качество жизни у пациентов с анемией или дефицитом железа со стабильным течением ХСН и хроническим заболеванием почек не выше 3 стадии. Fair-HF исследование показало, что лечение внутривенным препаратом железа улучшало функциональный класс сердечной недостаточности и показатели качества жизни независимо от того, присутствовали в пациента лабораторные признаки анемии или нет [36]. Это исследование также продемонстрировало отсутствие статистически значимой разницы в частоте существенных побочных эффектов между пациентами, принимавшими внутривенно карбосимальтозу железа, и контрольной группой [36].
У большинства пациентов, включенных в исследование, уровень ферритина был менее 100 мг/л [36]. Это исследование показало, что назначение 200 мг препарата карбоксимальтозы железа внутривенно увеличивало дистанцию теста 6-минутной ходьбы (317 м против 277 м) по сравнению с внутривенным назначением физиологического раствора [36]. Данное исследование с умеренной степенью доказанности продемонстрировало, что внутривенный препарат железа улучшал качество жизни у пациентов с анемией или дефицитом железа со стабильным течением ХСН и хроническим заболеванием почек не выше 3 стадии. Fair-HF исследование показало, что лечение внутривенным препаратом железа улучшало функциональный класс сердечной недостаточности и показатели качества жизни независимо от того, присутствовали в пациента лабораторные признаки анемии или нет [36]. Это исследование также продемонстрировало отсутствие статистически значимой разницы в частоте существенных побочных эффектов между пациентами, принимавшими внутривенно карбосимальтозу железа, и контрольной группой [36].
Целью CONFIRM-HF исследования было изучение долгосрочного эффекта от лечения препаратом карбоксимальтозой железа у пациентов с симптоматической сердечной недостаточностью и дефицитом железа. В исследование было включено 304 пациента со стабильной сердечной недостаточностью класса II или III согласно Нью-Йоркской Ассоциации Сердца (NYHA), с фракцией выброса левого желудочка ≤45%, повышенным уровнем натрийуритических пептидов (мозговой натрийуретический пептид >100 пг/мл и/или N-терминальный фрагмент натрийуритического пептида > 400 пг/мл), наличием дефицита железа (уровень сыворочного феритина < 100нг/мл, или от 100 до 300 нг/мл, если сатурация трансферрина < 20%) и гемоглобином до 15 г/дл.
В результате исследования было выявлено, что лечение стабильных симптоматических пациентов с сердечной недостаточностью и дефицитом железа внутривенным препаратом карбоксимальтозой железа приводит к устойчивому улучшению их функционального состояния согласно тесту 6-минутной ходьбы; улучшению качества жизни; значительному уменьшению риска госпитализаций вследствие прогрессирования сердечной недостаточности. Наблюдения за пациентами осуществлялось в течение одного года. Вышеперечисленные положительные эффекты были отмечены во всех подгруппах, включая пациентов с анемией или без нее [37].
Наблюдения за пациентами осуществлялось в течение одного года. Вышеперечисленные положительные эффекты были отмечены во всех подгруппах, включая пациентов с анемией или без нее [37].
Результаты CONFIRM-HF исследования по сравнению с Fair-HF имели более объективные первичную и конечную точки, показали более продолжительный положительный эффект от лечения карбоксимальтозой железа с хорошим профилем безопасности и продемонстрировали значительное снижение риска госпитализации вследствие ухудшения сердечной недостаточности [37].
Метаанализ всех рандомезированных контролируемых исследований, изучавших эффект лечения внутривенными препаратами железа у пациентов с систолической сердечной недостаточностью и дефицитом железа, показал, что ее применение у данной категории пациентов уменьшает риск комбинированных конечных точек: общей смертности и сердечно-сосудистых госпитализаций, сердечно-сосудистой смертности и госпитализации по поводу ухудшения сердечной недостаточности, и риск госпитализаций по причине декомпенсации ХСН. Не было выявлено значимого эффекта на общую и на смертность от сердечно-сосудистых причин. Вместе с тем, внутривенная терапия препаратами железа приводила к улучшению переносимости физических нагрузок, уменьшению симптомов сердечной недостаточности и улучшению качества жизни пациентов [38].
Не было выявлено значимого эффекта на общую и на смертность от сердечно-сосудистых причин. Вместе с тем, внутривенная терапия препаратами железа приводила к улучшению переносимости физических нагрузок, уменьшению симптомов сердечной недостаточности и улучшению качества жизни пациентов [38].
Внутривенное назначение препарата карбоксимальтозы железа должно рассматриваться в качестве лечения у симптомных пациентов с систолической сердечной недостаточностью и дефицитом железа для уменьшения клинических проявлений, повышения толерантности к физическим нагрузкам и улучшения качества жизни [39].
Заключение
Лечение анемии у пациентов с заболеваниями сердца может существенно отличаться от лечения анемии в общей популяции. Однако понимание доказательной базы и использование клинического суждения крайне необходимы для лечения данной категории лиц. Анемия коррелирует с ухудшением прогнозов у пациентов с кардиоваскулярной патологией и становится новой терапевтической мишенью для данной категории пациентов. Вопрос, является ли анемия причиной или маркером неблагоприятных исходов и отражает лишь тяжесть сердечно — сосудистого заболевания, остается актуальным по сей день.
Вопрос, является ли анемия причиной или маркером неблагоприятных исходов и отражает лишь тяжесть сердечно — сосудистого заболевания, остается актуальным по сей день.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов, способного повлиять на результаты исследования или их трактовку.
Introduction. Cardiovascular disease is a significant health problem around the world and accounts for the majority of deaths annually. Many of such patients have anemia due to acute blood loss (surgery or trauma) or chronic conditions such as renal failure or cancer.
According to the World Health Organization criteria anemia is defined in cases when hemoglobin is less than 120 g/l in females and less than 30 g/l in males. It is a major health problem that increases the mortality rate, affects physical status, and demands referral to health-care professionals. Globally, anemia affects 1.62 billion people, which corresponds to 24. 8% of the total population. The highest prevalence is in preschool-age children (47.4%), and the lowest prevalence is in men (12.7%). Half of the cases are due to iron deficiency [1] which affects not only red blood cell production but also cellular functions related to muscle metabolism, mitochondrial function, neurotransmitters, DNA synthesis, and the immune system [2].
8% of the total population. The highest prevalence is in preschool-age children (47.4%), and the lowest prevalence is in men (12.7%). Half of the cases are due to iron deficiency [1] which affects not only red blood cell production but also cellular functions related to muscle metabolism, mitochondrial function, neurotransmitters, DNA synthesis, and the immune system [2].
Prevalence of anemia increases with the advanced age making it a common associated comorbidity in patients with cardiovascular diseases. It has been established that anemia is an independent risk factor for cardiovascular diseases (CVD) outcomes [3].
Effects of anemia on the cardiovascular system. Understanding the physiologic response to anemia is important in order to take into account the implications of this state in regards to cardiac diseases. Three main factors are responsible for oxygen delivery to organs: blood flow and its distribution; the oxygen-carrying capacity of the blood, i. e. hemoglobin concentration; and oxygen extraction. Hypoxia in anemia is compensated through several non-hemodynamic (increased erythropoietin production to stimulate erythropoiesis, increased oxygen extraction) and hemodynamic mechanisms. The main hemodynamic factors are decreased afterload, increased preload, and positive inotropic and chronotropic effects. Enhanced nitric oxide activity, hypoxia-induced vasodilatation and lower blood viscosity are responsible for reduced vascular resistance and lead to the decreased afterload. Chronic anemia stimulates angiogenesis and recruitment of new microvessels. Enhanced venous return (preload) and left ventricular (LV) filling lead to the increased LV end-diastolic volume and cardiac output. Increased cardiac output is responsible for arterial remodeling of the central elastic arteries such as the aorta and common carotid artery through arterial enlargement and compensatory arterial intima-media thickening, leading to the elevated systolic pressure and high inertia due to higher blood mass in the dilated arterial system.
e. hemoglobin concentration; and oxygen extraction. Hypoxia in anemia is compensated through several non-hemodynamic (increased erythropoietin production to stimulate erythropoiesis, increased oxygen extraction) and hemodynamic mechanisms. The main hemodynamic factors are decreased afterload, increased preload, and positive inotropic and chronotropic effects. Enhanced nitric oxide activity, hypoxia-induced vasodilatation and lower blood viscosity are responsible for reduced vascular resistance and lead to the decreased afterload. Chronic anemia stimulates angiogenesis and recruitment of new microvessels. Enhanced venous return (preload) and left ventricular (LV) filling lead to the increased LV end-diastolic volume and cardiac output. Increased cardiac output is responsible for arterial remodeling of the central elastic arteries such as the aorta and common carotid artery through arterial enlargement and compensatory arterial intima-media thickening, leading to the elevated systolic pressure and high inertia due to higher blood mass in the dilated arterial system. Activation of sympathetic activity enhances LV contractility, and the heart rate. Short-lasting anemia is reversible but in chronic anemia hemodynamic changes lead to cardiac enlargement and development of eccentric LV hypertrophy (LVH). It also occurs in other forms of the volume overload. In case of heart diseases chronic anemia contributes to a high incidence of cardiovascular complications [4].
Activation of sympathetic activity enhances LV contractility, and the heart rate. Short-lasting anemia is reversible but in chronic anemia hemodynamic changes lead to cardiac enlargement and development of eccentric LV hypertrophy (LVH). It also occurs in other forms of the volume overload. In case of heart diseases chronic anemia contributes to a high incidence of cardiovascular complications [4].
Anemia in arterial hypertension
Normocytic anemia is common in hypertensive patients but more prevalent in uncontrolled hypertension. Lower hemoglobin is associated with poor blood pressure control, indicating a higher cardiovascular risk in uncontrolled hypertension [5]. It was noted that hypertensive patients with anemia had higher nocturnal systolic and mean blood pressure and a lower dipping status compared to the patients with normal hemoglobin levels. There was a trend for increased diastolic blood pressure [6].
In patients with isolated systolic hypertension and left ventricular hypertrophy lower hemoglobin was associated with the increased cardiovascular death or stroke [7].
Electrocardiographic changes in anemia.
Electrocardiographic (ECG) repolarization abnormalities (ST segment depression, T wave inversion, prolonged QT) are highly prevalent in anemic patients at rest and during the tests with physical loading [8]. It has been shown that the hemoglobin level is strongly correlated with ECG changes [9].
A long ECG QT interval duration is a predictor of ventricular arrhythmia and sudden cardiac death. Hypoxia and impaired oxygen supply in anemic patients may affect repolarization of the myocardium. It has been found that anemia, macrocytosis and anisocytosis are associated with prolonged QT intervals in hypertensive patients and may contribute to the risk of sudden cardiac death [10]. Low iron stores in otherwise healthy children negatively correlated with QT and QTc intervals and may indicate some risk in developing arrhythmias [11].
Mehta et al. showed significant reproducible ST depression in anemic patients with iron deficiency during the tests with physical loading. These electrophysiological changes were corrected after iron therapy, even before the rise of hemoglobin occurred, which may be explained by the effect of iron on the tissue level [12].
These electrophysiological changes were corrected after iron therapy, even before the rise of hemoglobin occurred, which may be explained by the effect of iron on the tissue level [12].
Anemia in Ischemic Heard Disease
Myocardial ischemia is defined as oxygen delivery that is insufficient to meet oxygen requirements. The determinants of myocardial oxygen demand are wall tension, heart rate and contractility. The determinants of myocardial oxygen delivery are arterial oxygen content and coronary arterial blood flow. The increase of oxygen delivery in response to the enhancement of oxygen demand occurs through the changes in coronary vascular resistance, as the extraction ratio of myocardium at rest is nearly 90% [13]. Patients without coronary artery disease, therefore, have a tremendous ability to compensate the decrease in coronary arterial oxygen content through distal vasodilatation but in the presence of coronary stenosis this compensatory mechanism has a limited ability.
It was proved that anemic animals have the increased infarct size, decreased cardiac function and the survival rate in case of acute myocardial infarction (MI). Transfusion of fresh blood to anemic animals up to 100 g/L Hb reduced the infarct size and improved the cardiac function. However, blood transfusion up to 120 g/L Hb was associated with larger infarcts [14].
Sabatine et al. found out a U-shaped relationship with clinical events by the 30th day: in patients with ST-elevation MI; the mortality rate was higher in those with the hemoglobin levels below 140g/L or above 170g/L, while in patients with non-ST elevation acute coronary syndrome (ACS), death, infarction and ischemia increased in case when hemoglobin levels were below 110g/L or above 160/L [15].
Anemia is a risk factor for ischemic heart disease. Patients with ischemic heard disease (IHD) and anemia have a more advanced degree of ischemic heart disease compared to patients with isolated IHD. In anemic patients with IHD the level of hemoglobin, serum iron and total iron-binding capacity negatively correlated with the severity of IHD [16]. The mortality rate in anemic patients with IHD was higher than in patients with isolated IHD [16]. Anemia was an independent predictor of acute coronary syndrome based on the hemoglobin level, while both anemia and a high hematocrit level were predictors of myocardial infarction based on hematocrit [17].
The mortality rate in anemic patients with IHD was higher than in patients with isolated IHD [16]. Anemia was an independent predictor of acute coronary syndrome based on the hemoglobin level, while both anemia and a high hematocrit level were predictors of myocardial infarction based on hematocrit [17].
The investigations made by Ferreira et al. revealed that hemoglobin<108g/L was one of the strongest independent predictors of one-year mortality in population with acute coronary syndrome (ACS). He suggested including the hemoglobin level in risk stratification scores of patients admitted for ACS, given that it is an easy parameter to measure and is systematically assessed at admission [18].
In the Cadilac trial anemia was common in patients with AMI who underwent primary PCI and was strongly associated with the adverse outcomes and increased mortality [19]. Anemia was an independent predictor of in-hospital mortality by the end of the first year [19].
Severe anemia can lead to disbalance between oxygen delivery and demand in the myocardium even in patients without coronary stenosis. Bailey D et al. reported a case of the ST segment elevation myocardial infarction (STEMI) secondary to severe anemia which occurred in the absence of angiographically significant coronary artery stenosis, thrombosis or coronary artery spasm [20].
Bailey D et al. reported a case of the ST segment elevation myocardial infarction (STEMI) secondary to severe anemia which occurred in the absence of angiographically significant coronary artery stenosis, thrombosis or coronary artery spasm [20].
Thus, there are a number of reasons for the worse outcomes in anemic patients with the obstructive coronary artery disease. Diminished oxygen-carrying capacity, activation of the sympathetic nervous system can increase myocardial oxygen demand and worsen ischemia.
Anemia in Heart Failure
Anemia is a very common comorbidity in chronic heart failure. Anemic patients are elderly women with more advanced symptoms and signs of heart failure, greater functional impairment and a higher hospitalization rate; they have a history of diabetes mellitus, renal insufficiency, and hypertension [21]. Anemia is a powerful predictor of rehospitalization rates and survival in case of chronic heart failure [22]. The prevalence of anemia increases with the severity of heart failure (HF) and can reach 79. 1% in those with Class IV according to the classification of the New York Heart Association [23].
1% in those with Class IV according to the classification of the New York Heart Association [23].
Etiology of anemia in HF may be multifactorial and a number of potential mechanisms may be responsible for such a condition in heart failure. Neurohormonal and inflammatory activation, renal dysfunction, bone marrow hyporesponsiveness, malnutrition, drug effects contribute to its development. Increased circulating proinflammatory cytokines enable defective iron mobilization, inappropriate erythropoietin production, depressed bone marrow function. Activation of the renin-angiotensin-aldosteron system, decreased renal perfusion caused by the low blood pressure and stroke volume stimulate the release of erythropoietin but the response is blunted due to effect of the circulatory cytokines. Poor nutrition due to anorexia, gastrointestinal malabsorbtion and aspirin use may precipitate iron deficiency anemia. Hemodilution can contribute to anemia. The use of the angiotensin-converting enzyme (ACE) inhibitor therapy may reduce secretion of erythropoietin [24].
Iron deficiency (ID) is the most frequent cause of anemia in patients with HF [25, 26] and can be revealed in ∼46% of non-anemic patients with stable systolic HF [27].
Iron deficiency may exist in absolute or functional forms. Absolute iron deficiency occurs when total body iron stores become exhausted and ID anemia can be considered as the final phase of iron stores depletion; functional iron deficiency refers to inadequate iron release in response to the demands of the bone marrow. Functional iron deficiency can be seen in many acute and chronic inflammatory states. ID is associated with the worsening of symptoms in patients with heart failure, impaired life quality, the increased mortality and hospitalization level [28, 29, 30].
Activation of sympathetic and renin-angiotensin-aldosteron systems, chronic inflammation, absolute and functional iron deficiency, impaired production and activity of erythropoietin, hemodilution, renal dysfunction impair prognosis in heart failure patients. Probably, anemia acts as a mediator and a marker of a poor prognosis in HF patients.
Probably, anemia acts as a mediator and a marker of a poor prognosis in HF patients.
Treatment of anemia in patients with heart diseases. Anemia treatment strategies in heart failure and CHD patients include erythropoiesis-stimulating agents (ESAs), red blood cell transfusions and iron replacement in iron deficient patients with or without anemia.
Sixteen randomized, controlled trials assessed the impact of ESAs in patients with heart disease. Most of these studies included patients with CHF and the reduced systolic function. Overall, moderate-quality evidence showed no benefit from ESAs in regard to improving exercise tolerance and duration or quality of life, and high-quality evidence showed no mortality benefit [31]. Serious harmful effects associated with the treatment include mortality and vascular thrombosis [31]. So, the damage outweighs the benefits in treatment of patients with mild to moderate anemia using ESAs. Although anemia is common in patients with CHF and CHD, treatment with ESAs did not decrease mortality, cardiovascular events or hospitalization rates [31]. The American College of Physicians does not recommend using erythropoiesis-stimulating agents to patients with mild to moderate anemia and congestive heart failure or coronary heart disease [31].
Blood transfusion has been suggested to correct severe anemia in patients with coronary artery disease, but data in regard to its effectiveness are contradictory. In the majority of studies investigating different transfusion protocols, a liberal blood transfusion strategy was defined as any red blood cell transfusion at a hemoglobin level up to 90 g/L, while a restrictive blood transfusion strategy was defined as any transfusion at a hemoglobin level up to 70 g/L. A meta-analysis of 10 studies totaling 203 665 patients with acute coronary syndrome (both STEMI and NSTEMI-ACS) reported that blood transfusion or a liberal transfusion strategy was associated with the increased all-cause mortality, compared with no blood transfusion or a restrictive transfusion strategy [32]. However, a transfusion or liberal transfusion strategy was associated with a significantly higher mortality risk by the 30th day only in case when a nadir hematocrit is more than 25% [32].
However, low-quality evidence data demonstrate that blood transfusion using restrictive compared with liberal transfusion protocols had no effect on mortality in patients with CHD. Observational studies suggested that transfusion is not beneficial and may be harmful for patients with heart disease and hemoglobin levels of more than 100 g/L (31). A pilot trial of 110 patients with acute coronary syndrome or stable angina undergoing cardiac catheterization and hemoglobin <100 g/L revealed a trend of fewer major cardiac events and deaths in patients with the liberal transfusion strategy as compared with a more restrictive strategy [33].
Due to inconsistent results of the studies and the lack of adequately powered RCTs restrictive red blood cell transfusion strategy may be considered in the settings of ACS and for hospitalized patients with coronary heart disease [31, 34]
Benefits of using intravenous iron injections in treatment of iron deficiency with or without anemia in HF patients.
Iron has several vital functions in the body. It serves as a carrier of oxygen to the tissues, a transport medium for electrons within cells, and an integrated part of important enzyme systems in various tissues. Several iron-containing enzymes act as electron carriers within the cell and their role in the oxidative metabolism is to transfer energy within the cell and mitochondria. Other key functions for the iron-containing enzymes (e.g. cytochrome P450) include synthesis of steroid hormones and bile acids; detoxification of foreign substances in the liver; and signal controlling in some neurotransmitters, such as the dopamine and serotonin systems in the brain [5].
Few studies addressed to intravenous iron therapy for patients with heart disease. Data from Fair-HF study, which included patients with and without anemia demonstrated, that 27.6% of patients treated with intravenous iron carboxymaltose had cardiovascular events compared with 50.2% of patients receiving placebo (p=0.01). Moderate-quality evidence showed that intravenous iron administration increased exercise tolerance and duration in patients with stable CHF including patients with Stage 3 chronic kidney disease. FAIR-HF trial (Ferinject Assessment in Patients with Iron Deficiency and Chronic Heart Failure) included anemic and nonanemic patients, with the majority of them having ferritin levels less than 100 µg/L [36]. This trial showed that 200 mg of intravenous ferric carboxymaltose (FCM) increased a 6-minute walk distance (313 m vs. 277 m) compared with intravenous saline [36]. Moderate-quality evidence showed that intravenous iron improved quality of life in patients with anemia or iron deficiency, stable CHF, and chronic kidney disease excluding the patients with the 4th and 5th stages. The FAIR-HF study showed that intravenous iron treatment improved Patient Global Assessment scores compared with control patients and the improved NYHA functional class, regardless of the anemia status (hemoglobin level ≤120 g/L) [36]. This trial also showed improved life quality. [36]. There was no statistically significant difference in serious harmful effects between the intravenous iron treatment and the control groups [36].
The CONFIRM-HF trial was aimed at studying effects of long-term intravenous iron therapy in ferric carboxymaltose inpatients with symptomatic heart failure and iron deficiency. Totally 304 patients with stable ambulatory HF (class II or III according to New York Heart Association (NYHA) classification) and left ventricular ejection fraction (LVEF) ≤45%, elevated natriuretic peptides (brain natriuretic peptide >100 pg/mL and/or N-terminal-pro-brain natriuretic peptide>400 pg/mL), presence of ID (defined as serum ferritin level <100 ng/mL, or between 100 and 300 ng/mL if transferrin saturation was <20%) and hemoglobin (Hb) up to15 g/L were enrolled in the study. This study showed that treatment of stable, symptomatic, ‘iron-deficient HF patients with intravenous iron (FCM) results in sustainable improvement of functional capacity as measured over a 1-year period using the 6-MWT walking test, improvement in quality of life, significantly reduced risk of hospital admission due to worsening of HF during a1-year follow-up period. These favorable results were consistent across all pre-specified subgroups including patients with and without anemia [37].
The results of CONFIRM-HF compared with FAIR-HF had a more objective primary end-point, documented longer-term sustainability of beneficial effects of treatment with FCM and the acceptable safety profile (i.e. 12 months compared with 6 months or less in previous studies) and provided data on significant risk reduction of the hospitalization due to HF worsening [37].
A meta-analysis of all randomized controlled trials that investigated the effects of intravenous iron therapy in iron-deficient patients with systolic HF (also analyzed separately in anemic and non-anemic subjects) showed that intravenous iron therapy in patients with systolic HF and ID reduced the risk of the combined endpoint of all-cause death or cardiovascular hospitalization, the risk of the combined endpoint of cardiovascular death or hospitalization due to advanced HF. However there was no effect on either all-cause or cardiovascular mortality, parenteral iron therapy resulted in the improved exercise capacity (as reflected by a longer 6MWT distance) and life quality, and also in alleviation of HF symptoms (reduction in the NYHA class) [38].
Intravenous FCM should be considered in symptomatic patients with systolic heart failure and iron deficiency (serum ferritin level <100 ng/mL, or between 100 and 300 ng/mL if transferrin saturation <20%) in order to alleviate HF symptoms, and improve exercise capacity and life quality [39].
Conclusion. Management of patients with heart disease and anemia might appropriately differ from that of the general population. Hence, clinical judgment and understanding the evidence base are critical when managing these patients. Anemia is associated with worse outcomes in patients with cardiovascular diseases. However, it is uncertain if anemia is the cause or the marker of poor outcomes and thus it only reflects advanced cardiovascular disease.
1. de Benoist B. et al., eds. Worldwide prevalence of anaemia 1993-2005. WHO Global Database on Anaemia Geneva, World Health Organization, 2008.
2. von DrygalskiA., Adamson J. W. Ironing out fatigue. Blood,2011, vol. 118, pp. 3191-3192.
3. Sarnak M. J., Tighiouart H., Manjunath G., MacLeod B., Griffith J., Salem D., Levey A. S. Anemia as a Risk Factor for Cardiovascular Disease in the Atherosclerosis Risk in Communities (ARIC) Study. J Am Coll Cardiology, 2002, vol. 40, no. 1, pp. 27-33.
4. Metivier F., Marchais S. J., Guerin A. P., Pannier B., London G. M. Pathophysiology of anaemia: focus on the heart and blood vessels, Nephrol Dial Transplant, 2000, vol. 15, no. 3, pp. 14-18.
5. Paul B., Wilfred N. C., Woodman R., Depasquale C. Prevalence and correlates of anaemia in essential hypertension. Clin Exp Pharmacol Physio, 2008, vol. 35, no. 12, pp. 1461-1464
6. Marketou M., Patrianakos A., Parthenakis F. Systemic blood pressure profile in hypertensive patients with low hemoglobin concentrations. Int J Cardiol, 2010, vol. 142, no. 1, pp. 95-96.
7. Marianne L. Smebye Emil K. Iversen A. H. Effect of Hemoglobin Levels on Cardiovascular Outcomes in Patients With Isolated Systolic Hypertension and Left Ventricular Hypertrophy (from the LIFE Study). Am J Cardiol, 2007, Sep 1, vol. 100, no. 5, pp. 747-912.
8. Stanojevic M., Stankov S. Electrocardiographic changes in patients with chronic anemia. Srp Arh Celok Lek, 1998, Nov-Dec. 126, no. 11-12, pp. 461-466.
9. Gv S., Pk S., Herur A., Chinagudi S., Patil S. S., Ankad R. B., Badami S. V. Correlation Between Haemoglobin Level and Electrocardiographic (ECG) Findings in Anaemia: A Cross-Sectional Study. J Clin Diagn Res, 2014, vol. 8, no.:4, doi: 10.7860/ JCDR/2014/8966.4202.
10. Mozos I., Serban C., Mihaescu R. Anemia and the QT interval in hypertensive patients. Int J Coiiabor Res Int Med Public Health, 2012, vol. 4, no 12, pp. 2084-2091.
11. Karadeniz C., Ozdemir R., Demirol M., Katipoglu N., Yozgat Y., Mege T., Onal N. Low Iron Stores in Otherwise Healthy Children Affect Electrocardiographic Markers of Important Cardiac events. Pediatr Cardiol, 2017, vol. 38, no. 5, pp. 909-914.
12. Mehta B. C., Panjwani D. D., Jhala D. A. Electrophysiologic abnormalities of heart in iron deficiency anemia. Effect of iron therapy. Acta Haematol, 1983, vol. 70, no. 3, pp. 189-193.
13. Hoffman J. I. Determinants and prediction of transmural myocardial perfusion. Circulation, 1978, vol. 58, pp. 381-339.
14. Hu H., Xenocostas A., Chin-Yee I., Lu X., Feng Q., Effects of anemia and blood transfusion in acute myocardial infarction in rats. Transfusion, 2010, vol. 50, no. 1. pp. 243-251.
15. Sabatine M. S., Morrow D. A., Giugliano R. P., Burton P. B., Murphy S. A., McCabe C.H., Gibson C. M., Braunwald E. Association of hemoglobin levels with clinical outcomes in acute coronary syndromes. Circulation, 2005, vol. 111, pp. 2042-2049.
16. Zeidman A., Fradin Z., Blecher A., Oster H. S., Avrahami Y., Mittelman M., Anemia as a risk factor for ischemic heart disease. Circulation. 2004, vol. 6, no. 1, pp. 16-18.
17. Mahmoodi M. R., Kimiagar S. M., Abadi A. R. Is anemia an independent predictor of occurrence of acute coronary syndrome? Results from the modares heart study. Am Heart Hosp J, 2007, vol. 5, no. 2, pp. 73-79.
18. Ferreira M., Antonio N., Gongalves F., Hemoglobina: um mero valor analitico ou um poderoso preditor de risco em doentes com sindromes coronarias agudas? Revista Portuguesa de Cardiologia, 2012, vol. 31, pp. 121-130.
19. Nikolsky E., Aymong E. D., Halkin A., Grines C. L., Cox D. A., Garcia E., Mehran R., Tcheng J. E., Griffin J. J., Guagliumi G., Stuckey T., Turco M., Cohen D. A., Negoita M., Lansky A. J., Stone G. W. Impact of anemia in patients with acute myocardial infarction undergoing primary percutaneous coronary intervention: Analysis from the controlled abciximab and device investigation to lower late angioplasty complications (cadillac) trial. J Am Coll Cardiol, 2004, Aug 4, vol. 44, no. 3, pp. 547-553.
20. Bailey D., Aude Y. W., Gordon P., Burtt D. ST-segment elevation myocardial infarction, severe anemia and nonobstructive coronary disease: case report and brief comment. Conn Med, 2003, vol. 67, no. 1, pp. 3-5.
21. Ezekowitz J. A., McAlister F.A., Armstrong P. W. Anemia is common in heart failure and is associated with poor outcomes: Insights from a cohort of 12,065 patients with new- onset heart failure. Circulation, 2003, vol. 107, pp. 223-225.
22. Mozaffarian D., Nye R., Levy W. C. Amemia predicts mortality in severe heart failure: The Prospective Randomized Amlodipine Survival Evaluation (PRAISE). J Am Coll Cardiol, 2003, vol. 41, pp. 1933-1939.
23. Silverberg D. S., Wexler D., Blum M., Keren G., Sheps D., Leibovitch E., Brosh D., Laniado S., Schwartz D., Yachnin T., Shapira I., Gavish D., Baruch R., Koifman B., Kaplan C., Steinbruch S., Iaina A. The use of subcutaneous erythropoietin and intravenous iron for the treatment of the anemia of severe, resistant congestive heart failure improves cardiac and renal function and functional cardiac class, and markedly reduces hospitalizations. J Am Coll Cardiol, 2000, vol. 35, no. 7, pp. 1737-1744.
24. Tang Y. D., Katz S. D. Anemia in chronic heart failure: Prevalence, etiology, clinical correlates and treatment options. Circulation, 2006, vol. 113, pp. 2454-2461.
25. Nanas J. N., Matsouka C., Karageorgopoulos D., Leonti A., Tsolakis E., Drakos S. G., Tsagalou E. P., Maroulidis G. D., Alexopoulos G. P., Kanakakis J. E., Anastasiou-Nana M. I. Etiology of anemia in patients with advanced heart failure. J Am Coll Cardiol, 2006, vol. 48, pp. 2485-2489.
26. Jankowska E. A., von Haehling S., Anker S. D., Macdougall I. C., Ponikowski P. Iron deficiency and heart failure: diagnostic dilemmas and therapeutic perspectives. Eur Heart J, 2013, vol. 34, pp. 816-829.
27. Klip I. T., Comin-Colet J., Voors A. A., Ponikowski P., Enjuanes C., Banasiak W., Lok D. J., Rosentryt P., Torrens A., Polonski L., van Veldhuisen D. J., van der Meer P., Jankowska E. A. Iron deficiency in chronic heart failure: an international pooled analysis. Am Heart J, 2013, vol. 165, pp. 575-582.e3.
28. Jankowska E. A., Rozentryt P., Witkowska A., Nowak J., Hartmann O., Ponikowska B., Borodulin-Nadzieja L., Banasiak W., Polonski L., Filippatos G., McMurray J.J., Anker S. D., Ponikowski P. Iron deficiency: an ominous sign in patients with systolic chronic heart failure. Eur Heart J, 2010, vol. 31, pp. 1872-1880.
29. Jankowska E. A., Rozentryt P., Witkowska A., Nowak J., Hartmann O., Ponikowska B., Borodulin-Nadzieja L., von Haehling S., Doehner W., Banasiak W., Polonski L., Filippatos G., Anker S. D., Ponikowski P. Iron deficiency predicts impaired exercise capacity in patients with systolic chronic heart failure. J Card Fail, 2011, vol. 17, pp. 899-906.
30. Enjuanes C., Klip I. T., Bruguera J., Cladellas M., Ponikowski P., Banasiak W., van Veldhuisen D. J., van der Meer P., Jankowska E. A., Comin-Colet J. Iron deficiency and health-related quality of life in chronic heart failure: results from a multicenter European study. Int J Cardiol, 2014, vol. 174, pp. 268-275. doi: 10.1016/j.ijcard.2014.03.169.
31. Qaseem A., Humphrey L. L., Fitterman N., Starkey M., Shekelle P. Clinical Guidelines Committee of the American College of Physicians.Treatment of Anemia in Patients With Heart Disease: A Clinical Practice Guideline From the American College of Physicians. Ann Intern Med, 2013, vol. 159, no. 11, pp. 770-779.
32. Chatterjee S., Wetterslev J., Sharma A., Lichstein E., Mukherjee D. Association of blood transfusion with increased mortality in myocardial infarction: a meta-analysis and diversity-adjusted study sequential analysis. JAMA Intern Med, 2013, vol. 173, pp. 132-139.
33. Carson J. L., Brooks M. M., Abbott J. D., Chaitman B., Kelsey S. F., Triulzi D. J., Srinivas V., Menegus M. A., Marroquin O. C., Rao S. V., Noveck H., Passano E., Hardison R. M., Smitherman T., Vagaonescu T., Wimmer N. J., Williams D. O. Liberal versus restrictive transfusion thresholds for patients with symptomatic coronary artery disease. Am Heart, 2013, vol. 165, no. 6, pp. 964-971.
34. Roffi M., Patron C. ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J, 2016, vol. 37, pp. 267-315. doi:10.1093/eurheartj/ehv320.
35. Gupta C. P. Role of Iron (Fe) in Body. J Appl Chem (IOSR-JAC), 2014, vol. 7, no. 11, pp. 38-46.
36. Anker S. D., Comin C. J., Filippatos G., Willenheimer R., Dickstein K., Drexler H., Luscher T. F., Bart B., Banasiak W., Niegowska J., Kirwan B. A., Mori C., von Eisenhart R. B., Pocock S. J., Poole-Wilson P.A., Ponikowski P. Ferric carboxymaltose in patients with heart failure and iron deficiency. N Engl J Med, 2009, vol. 361, no. 25, pp. 2436-2448.
37. Ponikowski P., van Veldhuisen D. J., Comin-Colet J., Ertl G., Komajda M., Mareev V., McDonagh T., Parkhomenko A., Tavazzi L., Levesque V., Mori C., Roubert B., Filippatos G., Ruschitzka F., Anker S. D. Beneficial effects of long-term intravenous iron therapy with ferric carboxymaltose in patients with symptomatic heart failure and iron deficiency. Eur Heart J, 2015, vol. 36, no. 11, pp. 657-658.
38. Jankowska E. A., Tkaczyszyn M., Suchocki T., Drozd M., von Haehling S., Doehner W., Banasiak W., Filippatos G., Anker S. D., Ponikowski P. Effects of intravenous iron therapy in iron-deficient patients with systolic heart failure: a meta-analysis of randomized controlled trials. Eur J Hearts Faii, 2016, vol. 18, no. 7, pp. 786-795. doi:10.1002/ejhf.473
39. Ponikowski P., Voors A. A., Anker S. D., Bueno H., Cleland J. G., Coats A. J., Falk V., Gonzalez-Juanatey J.R., Harjola V. P., Jankowska E. A., Jessup M., Linde C., Nihoyannopoulos P., Parissis J. T., Pieske B., Riley J. P., Rosano G. M., Ruilope L. M., Ruschitzka F., Rutten F. H., van der Meer P. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. RevEsp Cardiol (Engl Ed). 2016, vol. 69, no. 12, p. 1167. doi: 10.1016/j.rec.2016.11.005.
Анемия при беременности – железные аргументы и развеивание мифов
Анемия – одно из самых частых осложнений, возникающих во время беременности. В России этот диагноз ставится каждой третьей беременной женщине. Однако не все, столкнувшись с этим диагнозом понимают, о чём идёт речь и что надо делать, чтобы лечение было максимально эффективным.
Анемия – заболевание, при котором снижается уровень гемоглобина крови, часто при одновременном снижении числа эритроцитов. Основной причиной развития анемии является несоответствие между поступлением железа в организм и его затратами.
Во время беременности затраты на нужды растущего плода обуславливают значительное возрастание потребности в железе. Кроме того, более редкой, но возможной причиной анемии может быть недостаточное поступление фолиевой кислоты или витамина В12.
К факторам риска по развитию железодефицитной анемии во время беременности относятся:
- обильные менструации в анамнезе;
- заболевания желудочно-кишечного тракта;
- инфекционно-воспалительные заболевания;
- анемия в прошлом;
- короткий промежуток между беременностями, в том числе зачатие во время лактации;
- многоплодная беременность.
Поскольку главной задачей гемоглобина является доставка кислорода – жизненно важного элемента – ко всем тканям и клеткам женщины и плода, несложно представить какой вред наносит его снижение во время беременности. Однако и после родов вопрос нельзя считать закрытым. Доказано, что низкий уровень гемоглобина ассоциируется со снижением лактации, а так же с развитием анемии у ребенка.
Железодефицитная анемия проявляется слабостью, головокружением, патологической утомляемостью, извращенным восприятием вкусов и запахов, учащенным сердцебиением, отдышкой, головной болью, обмороками. Кожа становится сухой и бледной, а волосы и ногти ломкими.
Ставится диагноз анемии на основании оценки уровня гемоглобина в общем анализе крови. Нижняя граница нормы гемоглобина при беременности – 110 г/л. Однако, прежде чем снижается гемоглобин, происходит истощение запасов железа, что проявляется снижением уровня ферритина сыворотки крови. Это состояние носит название латентный дефицит железа и так же требует коррекции.
Лечение анемии и латентного дефицита железа проводят с помощью препаратов железа, которые чаще всего назначаются в виде таблеток или раствора для приёма внутрь, но иногда применяют растворы для внутривенного введения. Такая необходимость возникает, когда уровень гемоглобина очень низкий или в случае нарушения всасывания железа из желудочно-кишечного тракта.
Так же важно помнить о потенциале белковой диеты в коррекции железодефицита. Так как гемоглобин – это связь двух субъединиц – металлосодержащего гемма и белка глобина, — то при недостаточном поступлении белка даже адекватному количеству железа в организме связаться не с чем.
При диагнозе анемия пациенту важно помнить, что потребление продуктов с высоким содержанием железа поможет лишь поддержать имеющийся уровень гемоглобина, но не сможет повысить его уровень и насытить запасы железа в достаточной степени.
Отдельно хочется остановиться на том, в каких же продуктах содержание железа, действительно, высокое. Распространённым заблуждением является мнение, что при анемии нужно есть яблоки, свёклу и гранаты, а так же пить гранатовый сок. 100 грамм яблок содержат 0,5 — 2,2 мг железа; 100 грамм свёклы – 1,0 – 1,4 мг железа; 100 грамм гранатов — 0,78 мг железа. Примерно такое же количество железа содержат огурцы, клубника, тыква и другие фрукты и овощи. Для сравнения, гречка содержит 8 мг железа на 100 г продукта, сухофрукты (курага, чернослив, сушеные яблоки) — от 12 до 15 мг железа. Лидером по содержанию железа является свиная печень. Кроме того, высоко содержание этого микроэлемента в говяжьей печени, какао, чечевице, яичный желток, сердце.
Профилактикой железодефицитной анемии беременных является исследованием запасов железа и уровня гемоглобина на этапе планирования беременности, и при выявлении отклонений от нормы своевременная их коррекция, потребление продуктов с высоким содержанием железа, приём витаминно-минеральных комплексов, содержащих профилактические дозировки железа.
Врач акушер-гинеколог
женской консультации №14
Хиврич Е.Б.
Низкий гемоглобин может быть признаком рака или язвы желудка — Российская газета
Для нормальной работы иммунной системы человека необходимо железо. Нехватка этого микроэлемента может привести к возникновению проблем с потенцией у мужчин и нарушить менструальный цикл у женщин. Низкий уровень гемоглобина может предупреждать и о других серьезных заболеваниях.
Признаки нехватки железа в организме могут проявляться в упадке сил, депрессии, выпадении волос и сухости кожи, сонливости и раздражительности. Однако чтобы определить настоящую анемию и восполнить дефицит железа, необходимо провести развернутый анализ крови.
«Если у мужчины гемоглобин снижен хотя бы немного, допустим, до 120-110 г/л крови, то это уже красный флаг. Даже если он не испытывает при этом усталости и у него нет других симптомов анемии», — заявила изданию aif.ru руководитель Центра формирования здорового образа жизни Ирина Добрецова. Для мужчины норма гемоглобина — 130-160 г/л крови, для женщины — 120-140 г/л. Пониженный гемоглобин может говорить о наличии полипа, язвы желудка, эрозии и даже о начинающемся раке кишечника или желудка.
В зоне риска находятся вегетарианцы и любители жестких диет, подростки во время гормональной перестройки организма, дети-спортсмены, не принимающие дополнительно витаминно-минеральные комплексы. Если беременные женщины не принимают специальные поливитамины, то они также рискуют заболеть анемией.
Врач напоминает, что препараты для восполнения запасов гемоглобина и ферритина не стоит покупать самостоятельно в аптеке. Их назначают только медики. Кроме того, действие лекарств начинается лишь с шести месяцев и потому нельзя прерывать курс лечения.
Кстати
Важно помнить, что препараты, содержащие железо, нельзя совмещать с молочными продуктами. Нежелательно также запивать железосодержащие препараты черным чаем. Зато прекрасный результат даст апельсиновый сок, который помогает всасыванию железа. Помогут восстановить микроэлементы нежирное красное мясо (говядина и баранина), печень, гранат, морская капуста и тыквенные семечки.
Лечение железодефицитной анемии у женщин после родов
Анемия является состоянием, когда содержание гемоглобина в крови меньше нормы (низкий гемоглобин), что отражается в анализах крови. Гемоглобин это молекула в составе красных кровяных клеток, и для переноса кислорода ему требуется железо. Недостаточное потребление/поглощение железа и потеря железа (например, в результате кровотечения) могут привести к железодефицитной анемии. Симптомы анемии включают усталость/утомляемость, одышку и головокружение. Женщины могут потерять много крови во время родов, и у многих беременных женщин уже есть анемия, которая может прогрессировать в результате кровотечения. Тяжелая анемия может быть связана с материнской смертностью. Послеродовая железодефицитная анемия чаще встречается в странах с низким уровнем дохода.
Лечение железодефицитной анемии включает в себя таблетки, содержащие железо, или раствор,который вводят в вену (внутривенно). Другим вариантом лечения является восстановление красных кровяных клеток с помощью переливания крови от донора или стимулирование образования красных кровяных клеток с помощью эритропоэтина. Важно исследовать, какой метод является лучшим в уменьшении симптомов анемии, и являются ли эти варианты лечения безопасными.
Мы включили 22 рандомизированных контролируемых исследования с участием 2858 женщин и провели 13 сравнений, многие из которых были основаны только на небольшом числе исследований, включавших малое число женщин. В целом, качество доказательств было низким. Большинство клинических испытаний были проведены в странах с высоким уровнем дохода.
В 10 исследованиях, включающих 1553 женщины, сравнивали внутривенное железо с пероральным железом. Только в одном исследовании был показан временный положительный эффект в отношении усталости/утомляемости при внутривенном введении железа. О других симптомах анемии не сообщали. Одна женщина умерла от осложнений со стороны сердца в группе внутривенного введения железа. Только в двух исследованиях сообщали о материнских смертях. Аллергические реакции встречались у трех женщин, и осложнения со стороны сердца были у двух женщин в группе внутривенного введения препарата железа. Желудочно-кишечные симптомы были частыми в группе перорального приема препаратов железа (приема внутрь) и привели к отказу от лечения у некоторых участников.
в одном исследовании сравнивали переливание красных клеток крови с отсутствием переливания. Некоторые (но не все) показатели усталости/утомляемости временно улучшились в группе женщин с переливанием крови. О материнской смертности не сообщали.
При сравнении перорального железа с плацебо (три исследования) о симптомах анемии не сообщали. Остается неизвестным, перевешивает ли польза пероральных препаратов железа известный вред (неблагоприятные эффекты) со стороны желудочно-кишечного тракта.
В других исследованиях, в которых сравнивали другие варианты лечения, не изучали усталость/утомляемость.
В очень малом числе исследований сообщили об уменьшении симптомов анемии, хотя это, возможно, является самой важной целью лечения.
Существующие доказательства не позволяют нам в полной мере оценить эффективность лечения железодефицитной анемии после родов, и необходимы дальнейшие исследования.
Анемия
Анемия — это патологическое состояние, вызванное уменьшением количества эритроцитов в крови и/или снижением концентрации гемоглобина в самих эритроцитах.
Эритроциты (красные кровяные клетки, red blood cells, RBC) — самая многочисленная популяция клеток крови. Эритроциты содержат гемоглобин (Hb), который в легких присоединяет молекулы кислорода и доставляет их в ткани. В обратную сторону – из тканей к легким – гемоглобин переносит молекулы углекислого газа. Иными словами, гемоглобин обеспечивает процесс дыхания. Эритроцит имеет форму диска, вогнутого с обеих сторон. Такое устройство значительно увеличивает площадь поверхности, на которой происходит газообмен. Эритроциты имеют небольшой размер, что позволяет им проходить через самые узкие кровеносные сосуды (капилляры, артериолы, венулы). Один эритроцит в среднем живёт до 120 дней.
Низкий гемоглобин – один из критериев, на который необходимо обращать внимание не только при диагностике самих анемий, но и для оценки их степени тяжести. Снижение количества гемоглобина в эритроцитах возникает при недостаточном обеспечении железом в процессе созревания клеток в красном костном мозге.
Существует несколько классификаций анемий в зависимости от причин, от механизмов развития анемии и от выраженности изменений показателей крови. Они необходимы врачу для понимания, с чем связано текущее состояние. Это помогает выбрать наилучшую тактику дальнейшего обследования, провести дифференциальную диагностику и назначить эффективное лечение.
Диагностикой и лечением анемии занимаются врачи-терапевты, врачи общей практики, семейные врачи. В случае тяжелого или злокачественного течения болезни может потребоваться вмешательство врача-гематолога, а также проведение более подробного и специализированного обследования.
Причин для развития анемии множество. Часто анемия является осложнением основного хронического заболевания.
Железодефицитная анемия развивается либо при недостаточном поступлении железа в организм, либо при повышенной потребности организма в железе.
Часто в той или иной степени присутствуют оба фактора.
Причинами недостаточного поступления железа могут быть заболевания органов желудочно-кишечного тракта, при которых нарушаются процессы переваривания и всасывания пищи. Употребление продуктов, содержащих низкое количество железа или железо в трудно усваиваемой форме (исключительно растительный рацион). Некоторые пищевые продукты (алкоголь, молоко, кофе) или лекарственные средства (антибактериальные, антацидные препараты) препятствуют усвоению железа из пищи.
Потребности организма в железе («расход железа») существенно возрастают у детей в периоды активного роста, у женщин во время беременности и кормления грудью.
Анемии часто осложняют течение заболеваний, сопровождающихся длительной кровопотерей (особенно на фоне нарушения всасывания пищи):
- язвенная болезнь желудка и 12-перстной кишки;
- воспалительные заболевания кишечника;
- миома матки, эндометриоз;
- злокачественные новообразования;
- нарушения свертываемости крови;
- глистные инвазии.
Организм человека не может синтезировать железо! Железо мы получаем только с пищей. Значение имеет не только количество железа в продуктах, но и его доступность для усвоения организмом. В продуктах животного происхождения (говядина, баранина, печень) содержится гемовое железо. Оно усваивается организмом наиболее эффективно. В растительных продуктах (овощах, фруктах, крупах) содержится негемовое железо. Организм человека плохо усваивает негемовое железо.
Основная причина развития железодефицитной анемии, по мнению экспертов Всемирной организации здравоохранения (ВОЗ), — это неправильное (несбалансированное) питание. Если Вы не употребляете мясные продукты, то необходимо помнить, что из растительных продуктов железо усваивается значительно хуже. Разумно планируйте ваш рацион питания, чтобы не допустить дефицита железа.
Улучшают всасывание железа:
|
Ухудшают всасывание железа:
|
Другой вид анемии – заболевание, вызванное дефицитом витамина B12.
В12-дефицитная анемия развивается из-за недостатка цианокобаламина.
Причинами недостатка могут быть:
- Недостаточное поступление витамина В12 с пищей (строгое вегетарианство), так как цианокобаламин содержится только в мясных продуктах, молоке, яйцах, рыбе и морепродуктах.
- Нарушение секреции желудком «внутреннего фактора Кастла»;
- Нарушение всасывания витамина В12 в тонком кишечнике;
- Конкурентное расходование витамина В12;
- Повышенный расход витамина В12;
- Снижение запасов витамина В12;
- Нарушение транспорта витамина В12;
- Отсутствие транскобаламина или появление антител к нему.
Симптомы анемии:
- Бледность кожных покровов, трещинки, «заеды» в уголках рта
- Ломкость ногтей, истонченность и исчерченность ногтей
- Выпадение волос, ломкость, нарушение структуры
- Повышенная утомляемость, снижение работоспособности
- Учащенное сердцебиение, головокружение, одышка сопровождают даже небольшую физическую активность
Для железодефицитной анемии характерно
- Извращение вкуса: пристрастие к малосъедобным продуктам — сырому мясу, замороженным полуфабрикатам; желание употреблять в пищу несъедобные вещества — мел, землю, лёд, глину.
- Извращение обоняния: пристрастие к неприятным запахам, например, бензина, ацетона, краски и т. д.
Какие анализы можно сдать тем, кто подозревает у себя анемию? Самым доступным и простым является общий анализ крови
Если по результатам анализа будут выявлены изменения количества эритроцитов, гемоглобина, гематокрита, эритроцитарных индексов (MCV, MCH, MCHC, RDW), то необходимо проконсультироваться с врачом для назначения дальнейшего обследования и лечения.
Для справки:
Гематокрит (Ht) – показатель, который характеризует количество клеток в единице объема цельной крови. Величина гематокрита зависит от количества и формы эритроцитов. Снижение уровня гематокрита также характеризует снижение содержания эритроцитов в крови.
MCV (mean corpuscular volume) – средний объем эритроцита, отражает размер клеток. При наличии длительного дефицита железа, созревающие эритроциты становятся мелкими, в крови появляются микроциты, и показатель MCV снижается. При наличии дефицита витаминов В12 и В9 созревающие клетки становятся крупными, в крови появляются макроциты, и данный показатель увеличивается. Оба состояния негативно сказываются на главной функции эритроцитов – транспорте кислорода и углекислого газа. В случае макроцитарной анемии уменьшается их способность проходить по сосудам маленького диаметра, и уменьшается срок их жизни.
МСН (mean corpuscular hemoglobin) — среднее содержание гемоглобина в эритроците, отражает те же самые процессы, что и предыдущий показатель MCV. При длительном дефиците железа в кровоток выходят эритроциты, которым в процессе роста и созревания этого микроэлемента не хватало, и они становятся не только маленькими, но ещё и недостаточно насыщенными гемоглобином. MCH начинает снижаться, развивается состояние гипохромии. Эритроциты становятся бледными, ухудшается их функционирование. Раньше для оценки состояния насыщения гемоглобином эритроцитов рассчитывался цветовой показатель, MCH является его современным более точным аналогом и позволяет дифференцировать анемии на нормохромные, гипохромные и гиперхромные. В случае дефицита витаминов В12 и В9 происходит обратная ситуация. Созревающие эритроциты перенасыщены гемоглобином, данный показатель начинает увеличиваться, развивается состояние гиперхромии. В совокупности два этих показателя помогут врачу только лишь на основании результатов общего анализа крови предположить природу анемии.
MCHC (mean corpuscular hemoglobin concentration) средняя концентрация гемоглобина в эритроците. Отражает концентрацию гемоглобина в эритроците. Снижается при железодефицитных гипохромных анемиях и заболеваниях сопровождающихся нарушением синтеза гемоглобина на любом этапе. Повышается при гиперхромных В12 и В9 дефицитных анемиях.
RDW (red blood cell distribution width) ширина распределения эритроцитов по объему. Данный показатель зависит от среднего объема эритроцита, поэтому при повышении или снижении MCV, наблюдается его увеличение, что свидетельствует в пользу того, что в крови находятся клетки разного объема, например, макроциты и нормоциты, или микроциты и нормоциты.
Для комплексного обследования, когда причина анемии неизвестна, можно воспользоваться программой Биохимическая диагностика анемий в состав которой входят параметры отражающие обмен и запас железа в организме, запас витамина В9 (фолиевой кислоты) и витамина В12 (цианокобаламина), а так же эритропоэтин — гормон запускающий эритропоэз (созревание новых эритроцитов).
- Трансферрин — осуществляет внеклеточный транспорт железа во все клетки организма человека.
- Растворимые рецепторы трансферрина (sTfR). Один из важных диагностических критериев, на основании которого можно установить истинный дефицит железа. Поступление железа в клетку происходит после взаимодействия комплекса «железо-трансферрин» со специфическими белками — рецепторами на мембране клеток. Концентрация рецепторов трансферрина зависит от двух факторов – количества депонированного железа в составе ферритина и пролиферативной активности клетки. Количество растворимых трансферриновых рецепторов является чувствительным индикатором как активности эритропоэза, так и дефицита железа. При анемии, развившейся как осложнение хронических заболеваний, этот показатель не меняется (остается в норме). Это помогает установить основную причину анемии.
- Ферритин (Ferritin) – депонированная форма железа, отражающая его общий запас в организме. Понижение концентрации ферритина в крови — маркер железодефицитных состояний.
Источники:
- Федеральные клинические рекомендации по диагностике и лечению железодефицитной анемии Издание официальное Москва 2015
- Струтынский А.В Диагностика и лечение железодефицитных анемий РМЖ «Медицинское обозрение» №11 от 14.05.2014 стр. 839
- Анемии: железодефицитная, В12-дефитная и анемия хронических заболеваний. Информационное письмо для врачей-гематологов, терапевтов, врачей-интернов и врачей-ординаторов. г. Ростов-на-Дону, 2013 год.
Анемия — Симптомы и причины
Обзор
Анемия — это состояние, при котором вам не хватает здоровых эритроцитов, чтобы доставлять достаточное количество кислорода к тканям вашего тела. Анемия, также называемая низким гемоглобином, может вызывать у вас усталость и слабость.
Существует множество форм анемии, каждая из которых имеет свою причину. Анемия может быть временной или длительной и может варьироваться от легкой до тяжелой. В большинстве случаев анемия имеет несколько причин.Обратитесь к врачу, если подозреваете, что у вас анемия. Это может быть предупредительным признаком серьезного заболевания.
Лечение анемии, зависящее от причины, варьируется от приема добавок до медицинских процедур. Возможно, вы сможете предотвратить некоторые виды анемии, соблюдая здоровую и разнообразную диету.
Типы
Симптомы
Признаки и симптомы анемии различаются в зависимости от причины и тяжести анемии.В зависимости от причин анемии симптомы могут отсутствовать.
Признаки и симптомы, если они возникают, могут включать:
- Усталость
- Слабость
- Кожа бледная или желтоватая
- Нерегулярное сердцебиение
- Одышка
- Головокружение или дурноту
- Боль в груди
- Холодные руки и ноги
- Головные боли
Поначалу анемия может быть настолько легкой, что вы ее не замечаете.Но симптомы ухудшаются по мере обострения анемии.
Когда обращаться к врачу
Запишитесь на прием к врачу, если вы чувствуете усталость и не знаете, почему.
У усталости много причин, помимо анемии, поэтому не думайте, что если вы устали, значит, у вас анемия. Некоторые люди узнают, что у них низкий гемоглобин, что указывает на анемию, когда они сдают кровь. Если вам сказали, что вы не можете сдавать кровь из-за низкого уровня гемоглобина, запишитесь на прием к врачу.
Причины
Анемия может быть вызвана состоянием, присутствующим при рождении (врожденным), или состоянием, которое вы развиваете (приобретенным). Анемия возникает, когда в вашей крови недостаточно эритроцитов.
Это может произойти, если:
- Ваше тело не вырабатывает достаточно красных кровяных телец
- Кровотечение приводит к потере красных кровяных телец быстрее, чем они могут быть восполнены
- Ваше тело разрушает красные кровяные тельца
Что делают красные кровяные тельца
Ваше тело вырабатывает три типа кровяных телец: белые кровяные тельца для борьбы с инфекцией, тромбоциты для свертывания крови и красные кровяные тельца для переноса кислорода из легких в остальную часть тела и углерода диоксид из организма обратно в легкие.
Красные кровяные тельца содержат гемоглобин — богатый железом белок, придающий крови красный цвет. Гемоглобин позволяет эритроцитам переносить кислород из легких во все части тела и переносить углекислый газ из других частей тела в легкие для выдоха.
Большинство клеток крови, включая эритроциты, регулярно вырабатываются в костном мозге — губчатом материале, который находится в полостях многих крупных костей. Для производства гемоглобина и эритроцитов вашему организму необходимо железо, витамин B-12, фолиевая кислота и другие питательные вещества из продуктов, которые вы едите.
Причины анемии
У разных типов анемии разные причины. В их числе:
Железодефицитная анемия. Этот наиболее распространенный тип анемии вызван нехваткой железа в организме. Вашему костному мозгу нужно железо, чтобы производить гемоглобин. Без достаточного количества железа ваше тело не может производить достаточно гемоглобина для красных кровяных телец.
Без добавления железа этот тип анемии встречается у многих беременных.Это также вызвано кровопотерей, например, из-за обильного менструального кровотечения; язва желудка или тонкой кишки; рак толстой кишки; и регулярное использование некоторых болеутоляющих средств, доступных без рецепта, особенно аспирина, который может вызвать воспаление слизистой оболочки желудка, что приведет к потере крови. Важно определить источник дефицита железа, чтобы предотвратить рецидив анемии.
- Витаминодефицитная анемия. Помимо железа, вашему организму необходимы фолиевая кислота и витамин B-12 для производства достаточного количества здоровых эритроцитов.Диета, в которой отсутствуют эти и другие ключевые питательные вещества, может вызвать снижение выработки красных кровяных телец. Некоторые люди, потребляющие достаточное количество B-12, не могут усваивать витамин. Это может привести к витаминной анемии, также известной как злокачественная анемия.
- Анемия воспаления. Определенные заболевания, такие как рак, ВИЧ / СПИД , ревматоидный артрит, заболевание почек, болезнь Крона и другие острые или хронические воспалительные заболевания — могут препятствовать выработке красных кровяных телец.
- Апластическая анемия. Эта редкая, опасная для жизни анемия возникает, когда ваше тело не производит достаточного количества эритроцитов. Причины апластической анемии включают инфекции, некоторые лекарства, аутоиммунные заболевания и воздействие токсичных химикатов.
- Анемии, связанные с заболеванием костного мозга. Различные заболевания, такие как лейкемия и миелофиброз, могут вызывать анемию, влияя на производство крови в костном мозге. Последствия этих видов рака и раковых заболеваний варьируются от легких до опасных для жизни.
- Гемолитические анемии. Эта группа анемий развивается, когда эритроциты разрушаются быстрее, чем костный мозг может их заменить. Некоторые заболевания крови увеличивают разрушение красных кровяных телец. Вы можете унаследовать гемолитическую анемию или развить ее в более позднем возрасте.
- Серповидно-клеточная анемия. Это наследственное и иногда серьезное заболевание — гемолитическая анемия. Это вызвано дефектной формой гемоглобина, которая заставляет эритроциты принимать аномальную форму полумесяца (серпа).Эти нерегулярные кровяные тельца преждевременно умирают, что приводит к хронической нехватке красных кровяных телец.
Факторы риска
Эти факторы повышают риск анемии:
- Диета с недостатком определенных витаминов и минералов. Диета с постоянным низким содержанием железа, витамина B-12, фолиевой кислоты и меди увеличивает риск анемии.
- Кишечные расстройства. Наличие кишечного расстройства, которое влияет на всасывание питательных веществ в тонком кишечнике, например болезни Крона и целиакии, подвергает вас риску анемии.
- Менструация. В целом, женщины, у которых не было менопаузы, имеют больший риск железодефицитной анемии, чем мужчины и женщины в постменопаузе. Менструация вызывает потерю красных кровяных телец.
- Беременность. Беременность и отказ от приема поливитаминов с фолиевой кислотой и железом увеличивает риск анемии.
Хронические состояния. Если у вас рак, почечная недостаточность или другое хроническое заболевание, вы можете подвергаться риску хронической анемии.Эти условия могут привести к нехватке эритроцитов.
Медленная хроническая потеря крови из язвы или другого источника внутри вашего тела может истощить запасы железа в вашем организме, что приведет к железодефицитной анемии.
- Семейная история. Если в вашей семье в анамнезе была наследственная анемия, например серповидно-клеточная анемия, вы также можете подвергаться повышенному риску заболевания.
- Прочие факторы. Наличие в анамнезе определенных инфекций, заболеваний крови и аутоиммунных заболеваний увеличивает риск анемии.Алкоголизм, воздействие токсичных химикатов и использование некоторых лекарств могут повлиять на выработку эритроцитов и привести к анемии.
- Возраст. Люди старше 65 лет подвержены повышенному риску анемии.
Осложнения
При отсутствии лечения анемия может вызвать множество проблем со здоровьем, например:
- Сильная усталость. Тяжелая анемия может настолько утомить вас, что вы не сможете выполнять повседневные дела.
- Осложнения беременности. У беременных женщин с фолатодефицитной анемией могут быть более вероятны осложнения, такие как преждевременные роды.
- Проблемы с сердцем. Анемия может привести к учащенному или нерегулярному сердцебиению (аритмии). Когда вы страдаете анемией, ваше сердце перекачивает больше крови, чтобы восполнить недостаток кислорода в крови. Это может привести к увеличению сердца или сердечной недостаточности.
- Смерть. Некоторые наследственные анемии, такие как серповидноклеточная анемия, могут привести к опасным для жизни осложнениям.Потеря большого количества крови быстро приводит к острой, тяжелой анемии и может быть смертельной. У пожилых людей анемия связана с повышенным риском смерти.
Профилактика
Многие виды анемии невозможно предотвратить. Но вы можете избежать железодефицитной анемии и витаминно-дефицитной анемии, соблюдая диету, включающую множество витаминов и минералов, в том числе:
- Утюг. Продукты, богатые железом, включают говядину и другое мясо, бобы, чечевицу, обогащенные железом злаки, темно-зеленые листовые овощи и сушеные фрукты.
- Фолиевая кислота. Это питательное вещество и его синтетическая форма фолиевой кислоты можно найти во фруктах и фруктовых соках, темно-зеленых листовых овощах, зеленом горошке, фасоли, арахисе и продуктах из обогащенного зерна, таких как хлеб, крупы, макаронные изделия и рис.
- Витамин B-12. Продукты, богатые витамином B-12, включают мясо, молочные продукты, обогащенные злаки и соевые продукты.
- Витамин С. Продукты, богатые витамином С, включают цитрусовые фрукты и соки, перец, брокколи, помидоры, дыни и клубнику.Они также помогают увеличить усвоение железа.
Если вы беспокоитесь о том, чтобы получать достаточное количество витаминов и минералов из пищи, спросите своего врача, могут ли помочь поливитамины.
8 сентября 2021 г.
Анемия: причины, симптомы, диагностика, лечение
Что такое анемия?
Анемия определяется как низкое количество эритроцитов.При обычном анализе крови анемия определяется как низкий уровень гемоглобина или гематокрита. Гемоглобин — это основной белок в красных кровяных тельцах. Он переносит кислород и доставляет его по всему телу. Если у вас анемия, уровень гемоглобина тоже будет низким. Если он достаточно низкий, ваши ткани или органы могут не получать достаточно кислорода. Симптомы анемии, такие как усталость или одышка, возникают из-за того, что ваши органы не получают того, что им нужно для работы должным образом.
Анемия — наиболее распространенное заболевание крови в США.С. Поражает почти 6% населения. Женщины, маленькие дети и люди с хроническими заболеваниями чаще болеют анемией. Важно помнить следующее:
- Определенные формы анемии передаются через ваши гены, и у младенцев она может быть с рождения.
- Женщины подвержены риску железодефицитной анемии из-за потери крови во время менструации и повышенной потребности в кровоснабжении во время беременности.
- Пожилые люди подвержены большему риску анемии, потому что у них более высокая вероятность заболевания почек или других хронических заболеваний.
Существует много видов анемии. У всех разные причины и методы лечения. Некоторые формы — например, легкая анемия во время беременности — не вызывают серьезного беспокойства. Но некоторые типы анемии могут отражать серьезное основное заболевание.
Симптомы анемии
Признаки анемии могут быть настолько незначительными, что вы можете их даже не заметить. В определенный момент, когда количество клеток крови уменьшается, часто развиваются симптомы. В зависимости от причины анемии симптомы могут включать:
- Головокружение, легкость или ощущение, что вы собираетесь потерять сознание
- Быстрое или необычное сердцебиение
- Головная боль
- Боль, в том числе в костях, груди, животе, и суставов
- Проблемы с ростом, у детей и подростков
- Одышка
- Кожа бледная или желтая
- Холодные руки и ноги
- Усталость или слабость
Типы и причины анемии
Существует более 400 типов анемии, и они разделены на три группы:
- Анемия, вызванная кровопотерей
- Анемия, вызванная снижением или нарушением производства эритроцитов
- Анемия, вызванная разрушением эритроцитов
Анемия, вызванная кровью Потеря
Вы можете потерять эритроциты в результате кровотечения.Это может происходить медленно в течение длительного периода времени, и вы можете этого не заметить. Причины могут включать:
- Желудочно-кишечные заболевания, такие как язвы, геморрой, гастрит (воспаление желудка) и рак
- Нестероидные противовоспалительные препараты (НПВП), такие как аспирин или ибупрофен, которые могут вызывать язвы и гастрит
- Женские месячные, особенно если у вас обильные менструации (или обильные месячные). Это может быть связано с миомой.
- Посттравматический или послеоперационный период.
Анемия, вызванная снижением или нарушением выработки красных кровяных телец
При этом типе анемии ваше тело может не вырабатывать достаточное количество кровяных телец или они могут работать не так, как должны. Это может произойти из-за того, что с вашими эритроцитами что-то не так, или из-за того, что у вас недостаточно минералов и витаминов для нормального образования красных кровяных телец. Состояния, связанные с этими причинами анемии, включают:
Проблемы с костным мозгом и стволовыми клетками могут препятствовать выработке вашим организмом достаточного количества эритроцитов.Некоторые стволовые клетки в костном мозге, который находится в центре ваших костей, разовьются в красные кровяные тельца. Если стволовых клеток недостаточно, если они не работают должным образом или их заменяют другие клетки, например, раковые, у вас может развиться анемия. К анемии, вызванной проблемами костного мозга или стволовых клеток, относятся:
- Апластическая анемия возникает, когда у вас недостаточно стволовых клеток или их совсем нет. Вы можете получить апластическую анемию из-за ваших генов или из-за того, что ваш костный мозг был поврежден лекарствами, лучевой терапией, химиотерапией или инфекцией.Другие злокачественные новообразования, которые обычно поражают костный мозг, включают множественную миелому или лейкоз. Иногда явной причины апластической анемии нет.
- Отравление свинцом. Свинец токсичен для костного мозга, из-за чего в нем образуется меньше красных кровяных телец. Отравление свинцом может произойти, когда взрослые вступают в контакт со свинцом, например, на работе или если дети едят кусочки свинцовой краски. Вы также можете получить его, если ваша еда соприкасается с некоторыми видами глиняной посуды, которые не имеют должного глазурования.
- Талассемия возникает из-за проблемы с образованием гемоглобина (неправильно сформированы 4 цепи).Вы производите очень маленькие красные кровяные тельца — хотя вы можете вырабатывать их достаточно, чтобы протекать бессимптомно или они могут быть тяжелыми. Они передаются в ваших генах и обычно поражают людей средиземноморского, африканского, ближневосточного и юго-восточного азиатского происхождения. Это состояние может варьироваться от легкого до опасного для жизни; самая тяжелая форма называется анемией Кули.
Железодефицитная анемия возникает из-за недостатка минерального железа в организме. Вашему костному мозгу нужно железо, чтобы производить гемоглобин — часть красных кровяных телец, которая доставляет кислород к вашим органам.Железодефицитная анемия может быть вызвана:
- Диета без достаточного количества железа, особенно у младенцев, детей, подростков, веганов и вегетарианцев
- Определенные лекарства, продукты питания и напитки с кофеином
- Пищеварительные расстройства, такие как болезнь Крона или если вам удалили часть желудка или тонкой кишки
- Часто сдавали кровь
- Тренировки на выносливость
- Беременность и кормление грудью израсходовали железо в организме
- Ваши месячные
- Распространенной причиной является хроническое медленное кровотечение, обычно из-за Желудочно-кишечный источник.
Серповидно-клеточная анемия — это заболевание, которое в США поражает в основном афроамериканцев и латиноамериканцев. Ваши красные кровяные тельца, которые обычно имеют округлую форму, приобретают форму полумесяца из-за проблемы в ваших генах. Анемия возникает, когда красные кровяные тельца быстро разрушаются, поэтому кислород не попадает в ваши органы. Красные кровяные тельца в форме полумесяца также могут застревать в крошечных кровеносных сосудах и вызывать боль.
Витаминно-дефицитная анемия может возникнуть, когда вы не получаете достаточно витамина B12 и фолиевой кислоты.Эти два витамина нужны вам для образования красных кровяных телец. Этот вид анемии может быть вызван:
- Диетический дефицит: если вы едите мало или совсем не едите мяса, вы можете не получить достаточно витамина B12. Если вы переварите овощи или съедите их недостаточно, вы можете не получить достаточно фолиевой кислоты.
- Мегалобластная анемия: когда вы не получаете достаточного количества витамина B12, фолиевой кислоты или того и другого
- Пагубная анемия: когда ваше тело не усваивает достаточное количество витамина B12
Другие причины авитаминоза включают лекарства, злоупотребление алкоголем и кишечник. болезни, такие как тропический спру.
Анемия, связанная с другими хроническими состояниями обычно возникает, когда в вашем организме не хватает гормонов для выработки красных кровяных телец. К состояниям, вызывающим этот тип анемии, относятся:
Анемия, вызванная разрушением красных кровяных телец
Когда красные кровяные тельца хрупкие и не могут справиться со стрессом от путешествия по вашему телу, они могут лопнуть, вызывая то, что называется гемолитическим. анемия. У вас может быть это состояние при рождении, или оно может появиться позже.Иногда причины гемолитической анемии неясны, но они могут включать:
- Атака иммунной системы, как при волчанке. Это может случиться с кем угодно, даже с младенцем, находящимся в утробе матери, или с новорожденным. Это называется гемолитической болезнью новорожденного.
- Состояния, которые могут передаваться через ваши гены, такие как серповидноклеточная анемия, талассемия и тромботическая тромбоцитопеническая пурпура (ТТП)
- Увеличенная селезенка. В редких случаях это может захватить эритроциты и уничтожить их слишком рано.
- Что-то, что создает нагрузку на ваше тело, например, инфекции, лекарства, змеиный или паучий яд или определенные продукты
- Токсины от прогрессирующего заболевания печени или почек
- Сосудистые трансплантаты, протезы сердечных клапанов, опухоли, тяжелые ожоги, находящиеся поблизости химические вещества, тяжелая гипертензия и нарушения свертываемости крови
Диагностика анемии
Общий анализ крови (CBC) позволит измерить ваши эритроциты, гемоглобин и другие части вашей крови. Ваш врач спросит о вашей семейной истории и истории болезни после общего анализа крови.Они, вероятно, проведут несколько тестов, в том числе:
- Мазок крови или дифференциальный анализ для подсчета ваших лейкоцитов, проверки формы ваших эритроцитов и поиска необычных клеток
- Подсчет ретикулоцитов для проверки незрелых красных кровяных телец
Лечение анемии
Ваше лечение будет зависеть от вашего типа анемии. Причин много, поэтому существует множество способов лечения.
- Если у вас апластическая анемия, вам могут потребоваться лекарства, переливание крови (при котором вы получаете кровь от другого человека) или трансплантацию костного мозга (при которой вы получаете донорские стволовые клетки).
- Если у вас гемолитическая анемия, вам могут потребоваться лекарства, которые будут сдерживать вашу иммунную систему. Ваш лечащий врач может направить вас к врачу, специализирующемуся на сосудистых заболеваниях.
- Если это вызвано кровопотерей, вам может потребоваться операция, чтобы найти и исправить кровотечение. Если у вас железодефицитная анемия, вам, вероятно, придется принимать добавки железа и изменить свой рацион.
- Лечение серповидно-клеточной анемии включает обезболивающие, добавки фолиевой кислоты, периодические антибиотики или кислородную терапию.Препарат. так называемая гидроксимочевина (Droxia, Hydrea, Siklos) часто назначается для уменьшения серповидно-клеточных болевых кризов (сложный механизм). Лекарство, называемое voxelator (Oxbryta), может помочь вашим эритроцитам сохранить свою правильную форму. Crizanlizumab-tmca (Adakveo) может препятствовать слипанию клеток крови и закупорке сосудов. Порошок для перорального приема L-глутамина (Endari) может сократить ваши поездки в больницу из-за боли, а также защитить от состояния, называемого острым грудным синдромом.
- Если у вас дефицит витамина B12 или фолиевой кислоты, вам будут прописаны добавки..
- Талассемия обычно не требует лечения, но если ваш случай тяжелый, вам могут сделать переливание крови, трансплантацию костного мозга или операцию.
Анемия (для подростков) — Nemours Kidshealth
Что такое анемия?
Анемия — это когда количество красных кровяных телец в организме становится слишком низким. Красные кровяные тельца несут гемоглобин (произносится: HEE-muh-glow-bin), белок, переносящий кислород по всему телу. Без их достаточного количества кислород не попадает в органы тела.Без достаточного количества кислорода органы не могут нормально работать.
Существует много разных видов анемии, поэтому методы лечения различаются.
Какие бывают виды анемии?
Типы анемии зависят от их причины. В их числе:
- Анемии, возникающие при слишком быстром расщеплении эритроцитов , называемые гемолитическими анемиями. Они включают:
- аутоиммунная гемолитическая анемия: когда иммунная система организма разрушает собственные эритроциты
- наследственные гемолитические анемии: к ним относятся серповидноклеточная анемия, талассемия, дефицит G6PD и наследственный сфероцитоз
- Анемия вследствие кровотечения. Это может произойти из-за кровотечения из-за травмы, обильных менструаций, желудочно-кишечного тракта или другой проблемы со здоровьем.
- Анемия из-за слишком медленного образования красных кровяных телец , например:
- Апластическая анемия: когда организм перестает вырабатывать эритроциты в результате инфекции, болезни или другой причины
- железодефицитная анемия: когда в рационе человека не хватает железа
- анемия Дефицит B12: когда кто-то не получает достаточно B12 с пищей или организм не может усвоить B12
Каковы признаки и симптомы анемии?
У некоторых людей с анемией нет никаких симптомов.Тот, у кого есть симптомы, может:
- бледный
- казаться угрюмым
- очень устать
- головокружение или дурнота
- иметь учащенное сердцебиение
- имеют желтуху (желтую кожу и глаза), увеличенную селезенку и мочу темного цвета чая (при гемолитической анемии)
Как диагностировать анемию?
Обычно врачи диагностируют анемию по:
- задавая вопросы о симптомах
- спрашивают о диете
- спрашивают, есть ли у членов семьи анемия
- на медосмотре
- делает анализы крови на:
- Посмотрите на красные кровяные тельца под микроскопом, чтобы проверить их размер и форму
- проверить количество гемоглобина и железа в крови
- проверьте, насколько быстро производятся новые эритроциты
- проверка на наличие наследственной анемии
- проверяет другие клетки, производимые в костном мозге (например, лейкоциты)
Иногда врачи проводят анализы костного мозга.Костный мозг — это губчатая часть кости, в которой образуются клетки крови. Для этого теста врач вводит иглу в кость, чтобы взять небольшой образец костного мозга. Образец отправляется в лабораторию для специальных исследований.
Как лечится анемия?
Лечение анемии зависит от причины. Подросткам с анемией могут понадобиться:
- лекарства
- изменений в рационе
- переливание крови
- Лечение другого основного заболевания
- для приема к врачам (гематологам), специализирующимся на анемии и других проблемах с кровью
Если у вас железодефицитная анемия , ваш врач, вероятно, пропишет вам препараты железа, которые нужно принимать несколько раз в день.Ваш врач может сделать повторный анализ крови после того, как вы некоторое время принимаете добавку. Даже если тесты показывают, что анемия уменьшилась, вам, возможно, придется продолжать принимать железо в течение нескольких месяцев, чтобы пополнить запасы железа в вашем организме.
Чтобы получать достаточно железа, соблюдайте сбалансированную диету каждый день, начиная с завтрака, который включает источник железа, такой как обогащенные железом хлопья или хлеб. Постное мясо, изюм, мангольд, яйца, орехи, сушеные бобы, томатный соус и патока также являются хорошими источниками железа.
Если анемия вызвана другим заболеванием, врачи постараются устранить причину. Людям с некоторыми типами анемии необходимо будет обратиться к гематологу, который может предоставить необходимую медицинскую помощь в соответствии с их потребностями.
Хорошая новость в том, что для большинства людей анемия легко поддается лечению. И через несколько недель к ним вернется энергия!
Как справиться с анемией (низкий уровень эритроцитов)
Что такое анемия?
Анемия означает, что у вас меньше эритроцитов, чем обычно, или у вас недостаточно железа в крови.Когда это происходит, ваши красные кровяные тельца не могут переносить достаточно кислорода для остальной части вашего тела.
Симптомы включают:
Чувство сильной слабости, усталости или одышки
Чувство головокружения или головокружения
Бледные кожа, десны, ногтевые ложа или нижние веки.
Как лечится?
Анемию можно лечить с помощью:
Эти лекарства могут повысить уровень железа, помочь организму вырабатывать красные кровяные тельца или устранить причину анемии.
Тяжелая анемия требует переливания крови. В этом случае вы получите донорскую кровь через капельницу (небольшую трубку в вашей вене). Обычно это занимает от четырех до пяти часов. Вы можете получить кровь в одном из амбулаторных инфузионных центров Fairview.
Вам понадобится несколько анализов крови, чтобы убедиться, что ваше лечение работает.
Что еще я могу сделать для лечения или профилактики анемии?
Придерживайтесь здоровой диеты с большим количеством продуктов, богатых железом (например, говядина, печень, консервированный лосось, сухофрукты и обогащенные злаки).Пейте много жидкости.
Больше спать ночью и спать днем.
Планируйте свой день так, чтобы включать периоды отдыха. Не пытайтесь перегружать себя. Сохраняйте энергию для самых важных для вас вещей.
Старайтесь делать легкие упражнения каждый день. Избегайте тяжелых упражнений или активности.
Не бойтесь обращаться за помощью, когда она вам нужна. Семья и друзья могут помочь с уходом за ребенком, покупками, работой по дому или вождением.
Не вставайте слишком быстро, когда лежите или сидите. Это может вызвать у вас головокружение. Медленно меняйте позу.
Избегайте травм, которые могут вызвать кровотечение или синяки. Обеспечьте безопасность своего дома. Не пользуйтесь бритвами или острыми ножами.
Найдите время для занятий, которые помогут вам расслабиться (медитация, чтение, общение с друзьями, прослушивание музыки).
Когда мне следует позвонить в мою группу по уходу?
Позвоните в медицинскую бригаду, если:
Вы все время чувствуете себя очень слабым и усталым.
У вас проблемы с дыханием или вы чувствуете одышку.
У вас кружится голова или кружится голова.
Ваш пульс быстрее обычного.
У вас часто болит голова.
У вас сильное вагинальное кровотечение (замачивание одной прокладки в час) или изменение менструации. Это включает усиленное кровотечение или кровотечение между циклами.
Комментарии:
__________________________________________
__________________________________________
__________________________________________
__________________________________________
__________________________________________
__________________________________________
9000____________________________________________________
9000____________________________________________________
9000__________000 9 __________________________
Не заменять совет вашего врача. Авторское право © 2006 Fairview Health Services. Все права защищены. Клинически проверено Fairview Oncology. SMARTworks 520523 — РЕД. 19.04.Анемия у детей | Сидарс-Синай
Не то, что вы ищете?Что такое анемия у детей?
Анемия — распространенная проблема в дети. Около 20% детей в СШАв какой-то момент будет диагностирована анемия. Ребенку, страдающему анемией, не хватает эритроцитов или гемоглобина. Гемоглобин тип белка, который позволяет эритроцитам переносить кислород к другим клеткам в тело.
Есть много видов анемии. У вашего ребенка может быть 1 из них:
- Утюг дефицитная анемия. Это недостаточно железа в крови.Железо необходимо для образования гемоглобина. Это самая частая причина анемии.
- Мегалобластная анемия. Это когда красные кровяные тельца становятся слишком большими из-за недостатка фолиевой кислоты или витаминов. В-12. Один из видов мегалобластной анемии — злокачественная анемия. В этом типе есть проблема с усвоением витамина B-12, важного для создание красных кровяных телец.
- Гемолитик анемия. Это когда красные кровяные тельца разрушаются. Есть много разных причин, такие как серьезные инфекции или определенные лекарства.
- Серповидноклеточная анемия. Это тип гемоглобинопатии, наследственный тип анемии с эритроциты неправильной формы.
- Кули анемия (талассемия). Это еще один наследственный тип анемии с аномальные эритроциты.
- Апластический анемия. Это неспособность костного мозга вырабатывать клетки крови.
Что вызывает анемию у ребенка?
Анемия имеет 3 основные причины:
- Потеря эритроцитов
- Неспособность производить достаточное количество красных кровяных телец
- Разрушение красных кровяных телец
Снижение уровня эритроцитов или гемоглобина может быть связано с:
- Унаследованные дефекты эритроцитов
- Инфекции
- Некоторые болезни
- Некоторые лекарственные средства
- Недостаток некоторых витаминов или минералов в рационе
Какие дети подвержены риску анемии?
Факторы риска анемии включают:
- Недоношенность или низкая масса тела при рождении
- Живут в бедности или иммигрируют из развивающихся стран
- Раннее употребление коровьего молока
- Диета с низким содержанием железа или некоторых витаминов или минералов
- Операция или несчастный случай с кровопотерей
- Длительные болезни, такие как инфекции, болезни почек или печени
- В семейном анамнезе наследственный тип анемии, такой как серповидно-клеточная анемия
Каковы симптомы анемии у ребенка?
Большинство симптомов анемии возникает из-за недостаток кислорода в клетках.Многие симптомы не возникают при анемии легкой степени тяжести.
Это наиболее частые симптомы:
- Учащение пульса
- Одышка или затрудненное дыхание
- Недостаток энергии или быстрое утомление
- Головокружение или головокружение, особенно в положении стоя
- Головная боль
- Раздражительность
- Нерегулярные менструальные циклы
- Отсутствие или задержка менструации
- Болезненный или опухший язык
- Желтуха или пожелтение кожи, глаз и рта
- Увеличенная селезенка или печень
- Медленный или замедленный рост и развитие
- Плохое заживление ран и тканей
Симптомы анемии могут быть похожи на другие проблемы с кровью или состояние здоровья.Анемия часто бывает симптомом другого заболевания. Обязательно сообщайте о любых симптомах лечащему врачу. Всегда обращайтесь к врачу вашего ребенка для постановки диагноза.
Как диагностируют анемию у ребенка?
Поскольку анемия часто встречается у детей врачи проводят плановые обследования. К тому же у него часто нет симптомов. Самый анемия у детей диагностируется с помощью этих анализов крови:
- Гемоглобин и гематокрит. Это часто первый скрининговый тест на анемию в дети. Он измеряет количество гемоглобина и красных кровяных телец в крови.
- Завершено анализ крови (CBC). Общий анализ крови: красные и белые кровяные тельца, свертываемость крови клетки (тромбоциты), а иногда и молодые эритроциты (ретикулоциты). Это включает в себя гемоглобин и гематокрит, а также дополнительные сведения о красных кровяных тельцах.
- Периферийное мазок. Небольшой образец крови исследуют под микроскопом, чтобы увидеть, выглядят ли они обычный.
Для сдачи крови на анализ Медицинский работник вводит иглу в вену, обычно в руку или руку ребенка. А Жгут может быть обернут вокруг руки ребенка, чтобы помочь врачу найти вена. Кровь набирается в шприц или пробирку.В некоторых случаях можно взять кровь с помощью укола иглой.
Анализы крови могут дискомфорт при введении иглы. Это может вызвать синяк или опухоль. После кровь удалена, врач снимет жгут, окажет давление на область, и наложить повязку.
В зависимости от результатов анализы крови, вашему ребенку может быть сделана аспирация костного мозга, биопсия или и то, и другое.Это выполняется путем приема небольшого количества жидкости костного мозга (аспирация) или твердого костного мозга ткань (стержневая биопсия). Жидкость или ткань исследуются на количество, размер и зрелость. клеток крови или аномальных клеток.
Как лечится анемия у ребенка?
Лечение будет зависеть от симптомов, возраста и общего состояния вашего ребенка. Это также будет зависеть от степени тяжести состояния.
Лечение анемии зависит от причины.Некоторые виды не требуют лечения. Некоторым типам могут потребоваться лекарства, переливание крови, операция или пересадка стволовых клеток. Лечащий врач вашего ребенка может направить вас к гематологу. Это специалист по лечению заболеваний крови. Лечение может включать:
- Капли или пилюли витаминно-минеральные
- Изменение рациона вашего ребенка
- Прекращение приема лекарства, вызывающего анемию
- Медицина
- Операция по удалению селезенки
- Переливания крови
- Трансплантаты стволовых клеток
Какие возможные осложнения анемии у ребенка?
Осложнения анемии зависят от того, что ее вызывает.Некоторые типы имеют несколько осложнений, но другие имеют частые и серьезные осложнения. Некоторые анемии могут вызывать:
- Проблемы с ростом и развитием
- Боль и припухлость в суставах
- Недостаточность костного мозга
- Лейкемия или другие виды рака
Что я могу сделать, чтобы предотвратить анемию у моего ребенка?
Некоторые виды анемии передаются по наследству и предотвратить это невозможно.Железодефицитная анемия, распространенная форма анемии, может быть можно предотвратить, убедившись, что ваш ребенок получает достаточно железа в своем рационе. Для этого:
- Кормите ребенка грудью, если возможный. Он или она получит достаточно железа из грудного молока.
- Дайте формулу с железом. Если Ваш ребенок получает смесь, используйте смесь с добавлением железа.
- Не давайте коровье молоко до 1 год. В коровьем молоке недостаточно железа. Не следует давать младенцам до достижения им возраста 1 года, когда он или она ест достаточно другой пищи.
- Накормите ребенка железом продукты. Когда ваш ребенок ест твердую пищу, выбирайте продукты, которые являются хорошими источниками железо. К ним относятся обогащенные железом зерна и злаки, яичные желтки, красное мясо, картофель, помидоры и изюм.
Когда мне следует позвонить поставщику медицинских услуг для моего ребенка?
Позвоните лечащему врачу вашего ребенка, если вы заметили, что у вашего ребенка есть какие-либо симптомы анемии.И, если ваш ребенок не проверялся на анемию, поговорите с врачом о риске заболевания вашего ребенка.
Основные сведения об анемии у детей
- Анемия — это низкое количество эритроцитов или низкий уровень гемоглобина.
- Есть много разных причин анемии.
- Дети обычно проходят обследование на анемию. Часто симптомы отсутствуют.
- Лечение анемии зависит от того, что ее вызывает.
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от посещения лечащего врача вашего ребенка:
- Знайте причину визита и то, что вы хотите.
- Перед визитом запишите вопросы, на которые хотите получить ответы.
- Во время посещения запишите название нового диагноза и любые новые лекарства, методы лечения или тесты. Также запишите все новые инструкции, которые ваш поставщик дает вам для вашего ребенка.
- Узнайте, почему прописано новое лекарство или лечение и как они помогут вашему ребенку. Также знайте, каковы побочные эффекты.
- Спросите, можно ли вылечить состояние вашего ребенка другими способами.
- Знайте, почему рекомендуется тест или процедура и что могут означать результаты.
- Знайте, чего ожидать, если ваш ребенок не принимает лекарство, не проходит обследование или процедуру.
- Если вашему ребенку назначен повторный прием, запишите дату, время и цель этого визита.
- Узнайте, как можно связаться с лечащим врачом вашего ребенка в нерабочее время. Это важно, если ваш ребенок заболел и у вас есть вопросы или вам нужен совет.
Советы по низкому количеству эритроцитов
Анемия — это уменьшение количества красных кровяных телец (эритроцитов). Поскольку химиотерапия разрушает клетки, которые быстро растут, часто поражаются эритроциты.Пациенты, получающие комбинацию лучевой терапии и химиотерапии, подвержены большему риску анемии. Важной частью эритроцитов является гемоглобин — часть, которая переносит кислород по всему телу. Поэтому, когда у вас низкий гемоглобин, уровень кислорода снижается, и вашему организму приходится работать больше, чтобы компенсировать это. В конечном итоге ваше тело будет проявлять признаки сильной усталости.
Нормальный уровень гемоглобина у женщин обычно находится в диапазоне от 11,8 до 15,5 г / дл; для мужчин нормальный уровень от 13.От 5 до 17,5 г / дл. Во время химиотерапии / лучевой терапии ваш уровень гемоглобина может упасть ниже этих нормальных уровней, поэтому ваш уровень гемоглобина будет периодически проверяться на протяжении всего курса лечения. Каждый раз, когда уровень гемоглобина падает ниже 12,0 г / дл, считается, что вы страдаете анемией.
Признаки и симптомы анемии включают:
- слабость или утомляемость
- головокружение
- головная боль
- одышка или затрудненное дыхание
- Боль или сердцебиение в груди
- Раздражительность
- ощущение тяжести в верхней части ног
- звон в ушах
- ощущение холода
Что я могу сделать, чтобы предотвратить анемию?
Поскольку красные кровяные тельца разрушаются как побочный эффект химиотерапии / лучевой терапии, вы не можете ничего конкретно сделать, чтобы предотвратить развитие анемии.Анемия обычно вызывает у вас слабость и усталость; поэтому очень важно, чтобы при анемии вы старались не допускать сильной усталости своего тела. В противном случае вы можете заболеть. Конкретные действия, которые необходимо предпринять, включают:
Отдыхайте как можно больше для экономии энергии.
- Высыпайтесь.
- Избегайте длительной или напряженной деятельности.
- Двигайтесь сами. Отдыхайте во время занятий, от которых вы чувствуете усталость. При необходимости вздремните в течение дня.
- Расставьте приоритеты в своей деятельности, чтобы у вас было достаточно энергии для важных дел или занятий, которые вам нравятся больше всего.
- Попросите друзей и семью помочь вам приготовить еду или сделать работу по дому, когда вы устали.
Будьте осторожны, чтобы не получить травму, если почувствуете головокружение.
- Менять позу медленно, особенно при переходе из положения лежа в положение стоя.
- Вставая с постели, посидите несколько минут на краю кровати, прежде чем встать.
Соблюдайте сбалансированную диету.
- Ешьте продукты с высоким содержанием железа, включая зеленые листовые овощи, печень и приготовленное красное мясо.
- Пейте много жидкости.
- Избегайте кофеина и обильных приемов пищи в конце дня, если у вас проблемы со сном по ночам.
- Принимайте добавки железа только в том случае, если вам об этом сказал онколог или практикующая медсестра / фельдшер.
Когда мне позвонить своему врачу?
Немедленно позвоните своему врачу, если у вас есть одно или несколько из следующего:
- головокружение
- одышка или затрудненное дыхание
- чрезмерная слабость или утомляемость
- учащенное сердцебиение или боль в груди
Как лечится анемия?
В зависимости от причины и тяжести анемии существует несколько способов лечения анемии.Врач может посоветовать вам ежедневно принимать безрецептурные препараты железа или назначить переливание крови.
Ваш врач может также заказать инъекции «фактора роста» (Аранесп или Прокрит). Эти вещества действуют, стимулируя выработку организмом эритропоэтина. Важный фактор роста, используемый у онкологических больных, стимулирует рост красных кровяных телец. Увеличивая выработку эритроцитов вашим организмом, этот фактор роста может снизить риск развития анемии, а также уменьшить количество переливаний крови, которые могут потребоваться во время лечения.
Железодефицитная анемия | Институт заболеваний железа
: Что такое дефицит железа?
Дефицит железа — это состояние, вызванное недостатком железа в организме. Дефицит железа — это наиболее распространенная недостаточность питания и основная причина анемии в мире. В США, несмотря на обогащение пищевых продуктов, дефицит железа у некоторых групп населения растет. Дефицит железа в критические периоды роста и развития может привести к преждевременным родам, рождению детей с низкой массой тела, задержке роста и развития, задержке нормальной активности и движений ребенка.Дефицит железа может привести к плохой памяти или когнитивным навыкам (умственной функции), а также к плохой успеваемости в школе, на работе, в армии или на отдыхе. Более низкий IQ был связан с дефицитом железа, возникающим в критические периоды роста.
Признаки и симптомы дефицита железа
Человек с дефицитом железа может также страдать анемией и, как следствие, иметь один или несколько симптомов анемии. К ним могут относиться хроническая усталость, слабость, головокружение, головные боли, депрессия, болезненный язык, чувствительность к холоду (низкая температура тела), одышка при выполнении простых задач (подъем по лестнице, ходьба на короткие расстояния, выполнение работы по дому), синдром беспокойных ног, пика (желание жевать лед или непродовольственные товары) и потеря интереса к работе, отдыху, отношениям и близости.
Причины дефицита железа
Дефицит железа может быть результатом множества и множественных причин. Они делятся на две широкие категории: повышенная потребность в железе и / или снижение потребления или всасывания железа.
Повышенный спрос:
Дефицит железа может возникать в периоды быстрого роста. По этой причине природа следит за тем, чтобы развивающиеся плоды, новорожденные и младенцы в возрасте примерно до шести месяцев имели достаточный запас железа. Состояния, которые приводят к дефициту железа, включают потерю крови в результате обильных менструаций, беременность, частое или чрезмерное донорство крови, миомы, заболевания пищеварительного тракта (включая инфекции), а также операции и несчастные случаи.Дефицит железа также может быть вызван некоторыми лекарствами, некоторыми пищевыми добавками или веществами, вызывающими кровотечение, такими как обезболивающие с аспирином, а также в результате отравления свинцом, токсичными химическими веществами или злоупотреблением алкоголем.
Пониженное потребление или абсорбция
Пониженное потребление или абсорбция может происходить в диетах, которые не включают гемовое железо, железо, содержащееся в мясе и моллюсках.
