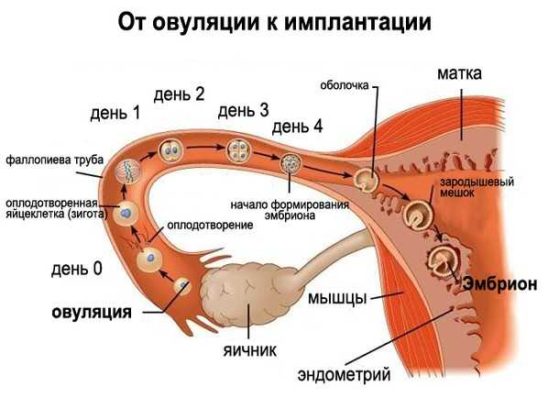
35.Сроки наступления имплантации зародыша человека, характеристика стадий.
Имплантация — внедрение зародыша в слизистую оболочку матки.
Различают две стадии имплантации: адгезию, когда зародыш прикрепляется к внутренней поверхности матки, и инвазию — внедрение зародыша в ткани слизистой оболочки матки. В трофобласте увеличивается количество лизосом с ферментами, тем самым способствующими внедрению зародыша в толщу слизистой оболочки матки. Зародышевый узелок уплощается и превращается в зародышевый щиток, начинается подготовка к первой стадии гаструляции. Имплантация продолжается около 40 ч. Одновременно с имплантацией происходит и начало гаструляции.
В первой стадии начинают дифференцироваться два слоя — цитотрофобласт и симпластотрофобласт. Во второй фазе протеолитические ферменты, разрушает слизистую оболочку матки. Ворсинки трофобласта, разрушают ее эпителий, подлежащую соединительную ткань и стенки сосудов. Образуется имплантационная ямка. Трофобластвначалепотребляет продукты распада материнских тканей, затем из материнской крови. Из крови матери зародыш получает питательные вещества, и кислород. В слизистой оболочке матки усиливается образование децидуальныхклеток. После полного погружения зародыша в имплантационную ямку отверстие, заполняется кровью и продуктами разрушения ткани слизистой оболочки матки. Слизистой оболочки покрывается регенерирующим эпителием.
36. Способы и особенности гаструляции у человека. Гипобласт, эпибласт.
Гаструляция — сложный процесс химических и морфогенетических изменений, сопровождающийся размножением, ростом, направленным перемещением и дифференцировкой клеток, в результате чего образуются зародышевые листки.
Гаструляция у человека осуществляется в две стадии. Первая стадия приходится на 7-е сутки, а вторая стадия — на 14—15-е сутки. При деламинации образуются два листка первичная эктодерма, или эпибласт и внутренний — гипобласт. Эпибласт в дальнейшем образует нижнюю стенку амниотического пузырька.
Гипобластверхнюю стенку начинающего формироваться желточного пузырька.
Затем выселение клеток из наружного и внутреннего листков в полость бластоцисты.
Мезенхима подрастает к трофобласту и внедряется в него. При этом формируется хорион.
Вторая стадия гаструляции происходит путем перемещения клеток в начале 3-й недели развития. Перемещение происходит в области дна амниотического пузырька. При этом образуется первичная полоска. В головном конце первичная полоска утолщается, образуя первичный, или головной, узелок, откуда берет свое начало головной отросток — хорда. В результате зародыш приобретает трехслойное строение в виде плоского диска, состоящего из эктодермы, мезодермы и энтодермы.
37.Внезародышевые органы, развитие, строение, их функции. Амнион, желточный мешок, аллантоис, пупочный канатик, хорион.
Внезародышевые органы, развивающиеся в процессе эмбриогенеза внетела зародыша, выполняют многообразные функции, обеспечивающие рост и развитие самого зародыша. Некоторые из этих органов, окружающих зародыш, называют также зародышевыми оболочками. К этим органам относятся амнион, желточный мешок, аллантоис, хорион, плацента.
Амнион— временный орган, обеспечивающий водную среду, он появляется на второй стадии гаструляции. Стенка пузырька образует внезародышевую эктодерму, соединяется с внезародышевой мезодермой.
Амнион быстро увеличивается, его соединительная ткань входит в контакт с соединительной тканью хориона. Амниона переходит на амниотическую ножку, превращающуюся пупочный канатик.
Основная функция амниотической оболочки — выработка околоплодных вод. Амнион выполняет также защитную функцию, предупреждая попадание в плод вредоносных агентов.
Эпителий амниона, образован крупными полигональными, тесно прилегающими друг к другу клетками. На 3-м месяце эпителий преобразуется в призматический. Эпителий амниона в области плацентарного диска, выполняет секреторную функцию, резорбцию околоплодных вод.
В соединительнотканной строме амниотической оболочки различают базальную мембрану, слой плотной волокнистой соединительной ткани и губчатый слой из рыхлой волокнистой соединительной ткани.
Желточный мешок— депонирующий питательные вещества, необходимые для развития зародыша. Он образован внезародышевой энтодермой мезодермой. Появившись на 2-й неделе. В стенке желточного мешка развиваются кровяные островки, формирующие первые клетки крови и первые кровеносные сосуды.
Над желточным мешком, формируется кишечная трубка. Связь зародыша с желточным мешком остается в виде полого канатика, называемого желточным стебельком.
Аллантоиссостоит из внезародышевой энтодермы и висцерального листка мезодермы по нему к хориону растут сосуды, располагающиеся в пупочном канатике. Это орган газообмена и выделения. По сосудам аллантоиса доставляется кислород, а в аллантоис выделяются продукты обмена веществ зародыша.
Пупочный канатикттяж, соединяющий зародыш (плод) с плацентой. Он покрыт амниотической оболочкой и рудиментами желточного мешка и аллантоиса.
Хорион, развивается из трофобласта и внезародышевой мезодермы. Первичные ворсинки выделяют протеолитические ферменты, с помощью которых разрушается слизистая оболочка матки и осуществляется имплантация. На 2-й неделе вторичные эпителиомезенхимальные ворсинки трофобласт превращается в хорион.
В начале 3-й недели в ворсинки хориона врастают кровеносные капилляры и формируются третичные ворсинки.
Имплантация зародыша это — Все о детях
В статье рассказывается о сроках, причинах и последствиях ранней имплантации эмбриона
Содержание статьи:
Сроки ранней имплантации эмбриона
Ранняя имплантация — это процесс внедрения эмбриона в маточный эндометрий по срокам ранее, чем физиологические нормы. Обычно эмбрион внедряется в матку на 7-10 день, если внедрение происходит на 6 день, говорят о ранней имплантации эмбриона. Ранняя имплантация эмбриона на 3-4-5 день после зачатия называется преждевременной.
Данный феномен является достаточной редкостью и в ряде случаев может характеризовать внематочную (трубную) беременность. Самая ранняя имплантация может произойти на 3-5 день после овуляции. В этом случае эмбрион преждевременно освобождается от своей защитной оболочки и может имплантироваться на поверхности слизистой оболочки фаллопиевой трубы.
Причины ранней имплантации эмбриона
Причиной ранней имплантации может быть:
- хорошая готовность эндометрия, которая дает все возможности для внедрения оплодотворенного эмбриона и нормального течения беременности;
- преждевременное удаление защитной оболочки эмбриона, при котором часто формируется эктопическая беременность.
Вылупление поздней бластоцисты из блестящей оболочки (хетчинг) обусловлено следующими процессами:
- накоплением в оболочке жидкости и, соответственно, увеличением давления внутри нее;
- совершением бластоцистой сокращающих движений;
- ферментативная активность эмбриона — выделение веществ, разрушающих «капсулу».
В свою очередь, преждевременный разрыв блестящей оболочки может быть спровоцирован:
- повышенным накоплением жидкости, которая продуцируется трофобластом;
- повышенным количеством протеолитических ферментов, которые растворяют оболочку.
Физиологически наступившая беременность может сопровождаться увеличенным накоплением жидкости, быстрым нарастанием давления и преждевременным разрывом блестящей оболочки. Причиной этого могут быть:
- гормональные нарушения;
- гипертермические реакции организма — состояния, при которых повышается температура тела;
- прием препаратов;
- воздействие вирусных агентов
К сожалению, при физиологической беременности у современной медицины нет прямых рычагов воздействия на хетчинг в утробе женщины. Единственное, что можно сделать – это пройти грамотную прегравидарную подготовку (обследоваться перед планированием беременности и провести терапию при необходимости) и во время зачатия беречь себя от контакта с больными. Это позволит исключить наличие гормонального дисбаланса, влияние вирусных агентов на развивающийся эмбрион в целом и на блестящую оболочку в частности.
Еще одной причиной преждевременной имплантации является вспомогательный хетчинг, применяемый в процедуре экстракорпорального оплодотворения. Речь идет об искусственном проколе блестящей оболочки в условиях эмбриологической лаборатории.
Вспомогательный хетчинг может быть:
- механическим — выполняется при помощи микроинструментария и микроиглы;
- химическим — выполняется при помощи специальных веществ, растворяющих оболочку;
- лазерным – предполагает выполнение надсечек на оболочке при помощи лазера.
В результате вышеуказанных действий в полость матки в протоколе ЭКО переносятся эмбрионы, которым не нужно время на освобождение от оболочки и которые могут имплантироваться сразу после процедуры подсадки.
Ранняя овуляция и ранняя имплантация
Ранняя овуляция – это преждевременный выход яйцеклетки из доминантного фолликула. Ранняя овуляция и ранняя имплантация не взаимосвязанные понятия. При преждевременной овуляции имплантация может происходить как в срок, так раньше или позже физиологических временных рамок. Ранняя имплантация совершенно не показатель преждевременного разрыва фолликула.
Как при нормальной, так и при ранней овуляции плодное яйцо может имплантироваться быстрее признанных норм. Сроки имплантации показывают, через какое время яйцеклетка внедрится в эндометрий после ее оплодотворения, независимо от того, когда она вышла из фолликула.
И ранняя овуляция, и ранняя имплантация могут иметь неблагоприятное влияние на беременность, так как они обе могут происходить на фоне гормонального сбоя. По причине ранней овуляции и имплантации может нужный слой эндометрия для нормального функционирования беременности может не успеть сформироваться.
Симптомы и ощущения женщины при ранней имплантации
Симптомы при ранней имплантации никаким образом не отличаются от таковых в нормальные физиологические сроки.
Первыми признаками может быть имплантационное кровотечение — выделения, которые имеют слизисто-кровянистый, алый характер в необильном количестве. Они беспокоят женщину в течение 1-3 дней. Эти выделения в обязательном порядке необходимо дифференцировать с другими патологическими состояниями гинекологической сферы.
Косвенным признаком имплантации являются:
- повышение базальной температуры;
- тянущие и острые боли внизу живота;
- нагрубание молочных желез;
- тошнота и рвота вследствие повышенного уровня прогестерона.
Для точного определения факта имплантации эмбриона необходимо сдать кровь на хорионический гонадотропин человека (ХГЧ).
Влияет ли ранняя имплантация на течение беременности?
Ранняя имплантация встречается редко и в большинстве случаев никак не влияет на беременность при условии, что она произошла именно в матке, а не в маточной трубе или в шейке матки. Беременность при ранних сроках имплантации никак не отличается от обычной беременности.
Гормональный сбой при имплантации чреват прерыванием беременности, так как при раннем и преждевременном прикреплении эндометрий не обладает нужными характеристиками, поэтому не является благоприятной средой для развития беременности.
Ранняя имплантация эмбриона после ЭКО
Имплантация при ЭКО почти никогда не бывает ранней, скорее, наоборот, для процесса экстракорпорального оплодотворения более характерна поздняя имплантация из-за потребности адаптации эмбриона в матке.
Ранняя имплантация может характеризовать тот протокол ЭКО, в котором был применен вспомогательный хэтчинг — разрез блестящей оболочки для более успешного процесса внедрения в полость матки.
Ирина Дроздова, акушер-гинеколог, специально для Mirmam.pro
Полезное видео
Source: mirmam.pro
Читайте также
Имплантация эмбриона — ♥ღ♥LOLO♥ღ♥ — BabyPlan
Блог в принципе сохраняю для себя, так как в дневнике не удобно.
Имплантация эмбриона в полости матки — сложный, многоступенчатый процесс, регуляция которого осуществляется при помощи большого количества гуморальных факторов и разнообразных межмолекулярных и межклеточных взаимодействий. Повышение результативности существующих методов лечения бесплодия, в том числе методов ВРТ, и разработка новых методов невозможны без изучения механизмов регуляции имплантации — одного из наиболее хрупких звеньев в становлении симбиотических взаимоотношений эмбриона и материнского организма.
Известно, что оплодотворенная яйцеклетка попадает в полость матки на стадии морулы на 4-й день после овуляции. На 5-й день морула развивается в бластоцисту [44]. Материнский эндометрий восприимчив к имплантирующейся бластоцисте только в пределах строго ограниченного во времени «окна имплантации» [5]. Наиболее вероятно, что у человека начало «окна имплантации» приходится на 7-й день после оплодотворения/овуляции [44]. Появление в эндометрии трансмембранного гликопротеина Muc 1 ограничивает временные рамки «окна имплантации» [12].
Во время фаз аппозиции и прикрепления на наружной мембране бластоцисты образуются многочисленные микровыпячивания, в результате чего она входит в тесный контакт с маточным эпителием, что знаменует собой переход в стадию адгезии (внедрения). Электроотрицательный заряд на поверхности эпителиальных клеток способствует сближению бластоцисты с поверхностью эндометрия [57]. Последующая стадия инвазии трофобласта завершает процесс имплантации и характеризуется глубоким проникновением бластоцисты в эпителий матки.
Синцитиотрофобласт эмбриона вторгается между эпителиальными клетками и прорастает в сторону базального слоя. Над погрузившейся в толщу эндометрия бластоцистой происходит полное смыкание покровного эпителия [5, 44].
Успех имплантации во многом зависит от синхронности обмена сигнальными молекулами между матерью и эмбрионом в ходе «диалога», который характеризуется интенсивными молекулярными взаимодействиями между клетками и тканями и экспрессией эффекторных молекул, факторов роста и цитокинов, осуществляющих паракринную, аутокринную и интракринную регуляцию столь сложного процесса [2, 69-71].
Межмолекулярные взаимодействия модулируют как дальнейшее развитие и «поведение» бластоцисты, так и распознавание беременности и адаптацию к ней организма матери.
Перед имплантацией ткани, составляющие секреторный эндометрий, в частности железистый эпителий, покровный эпителий, стромальные клетки, стромальные сосуды, внеклеточный матрикс, претерпевают различные морфологические, клеточные и молекулярные изменения, некоторые из них очень непродолжительные [31, 44].
Перед имплантацией ткани, составляющие секреторный эндометрий, в частности железистый эпителий, покровный эпителий, стромальные клетки, стромальные сосуды, внеклеточный матрикс, претерпевают различные морфологические, клеточные и молекулярные изменения, некоторые из них очень непродолжительные [31, 44].
В период имплантации митотическая активность клеток железистого эпителия увеличивается, что коррелирует с возрастающей концентрацией эстрадиола [64]. Секреторная активность желез достигает максимума. К характерным морфологическим изменениям желез эндометрия, наблюдающимся только в секреторную фазу, относятся образование гигантских митохондрий, отложение гликогена, формирование систем ядерных каналов [44].
Покровный эпителий матки первым контактирует с бластоцистой, в результате чего в нем происходят анатомические и молекулярные изменения, обеспечивающие восприимчивость эндометрия к нидации эмбриона. В период имплантации в нем образуются микровыпячивания (пиноподии) на апикальной поверхности эпителия, направленные к слизистой оболочки матки. Они появляются в середине секреторной фазы менструального цикла и сохраняются в течение 48-72 ч. Этот процесс стимулируется прогестероном и ингибируется эстрогенами [63]. Появление пиноподий соответствует по времени началу «окна имплантации», которое появляется в период максимальной рецепторной активности эндометрия [44].
Основными регуляторами морфологических изменений функционального слоя эндометрия в течение менструального цикла и в периимплантационном периоде считаются синтезируемые в яичниках стероиды [63, 66]. Только подготовленный циклическим стероидным воздействием эндометрий готов к приему бластоцисты и восприятию ее гуморальных сигналов [33].
Практически для всех видов млекопитающих в репродуктивном цикле характерны две следующие закономерности:
1) возрастающая секреция эстрогенов в фазу селекции и развития фолликулов, которая в хронологическом плане лишь косвенно влияет на имплантацию;
2) выработка значительных количеств прогестинов в секреторную фазу цикла, что совпадает по времени с имплантацией. Выраженная эстрогеновая секреция в эту фазу характерна далеко не для всех видов млекопитающих [25].
Считается, что в отличие от прогестерона эстрогены влияют на имплантацию опосредованно [37, 54].
Эстрадиол выступает в качестве пермиссивного агента, тогда как прямое действие оказывают локальные, регулируемые им факторы — цитокины, молекулы адгезии, факторы роста [41, 71, 75].
Установлено, что для полноценной пролиферации эндометрия в течение фолликулярной фазы нормального менструального цикла необходима концентрация эстрадиола в маточном кровотоке в пределах 200 — 400 пг/мл при одновременном содержании прогестерона не более 4 нг/мл [63]. Нормальная имплантация возможна при концентрации эстрадиола 50-100 пг/мл в сыворотке крови. Таким образом, уровень эстрадиола в периферической крови не всегда может являться прогностическим фактором в отношении успеха имплантации [66].
Более того, решающую роль в имплантации играет не столько абсолютное содержание стероидных гормонов, действующих на ткани-мишени органов репродуктивной системы, и морфологическая структура эндометрия, сколько его рецептивность, т.е. количество функционально полноценных рецепторов ткани эндометрия к соответствующим стероидным гормонам [4, 7].
Эстрогены одновременно с пролиферацией клеток эпителия стимулируют развитие секреторного аппарата клетки и синтез рецепторов к эстрогенам и прогестерону, посредством взаимодействия с которыми и осуществляется многогранное действие гормонов на клетки [4, 7].
Одной из причин низкого имплантационного потенциала эмбрионов, получаемых в программах ЭКО, считают нарушение экспрессии эмбриональных рецепторов ФРТ, в результате чего выживаемость эмбрионов понижается из-за дефицита аутокринной стимуляции [73]. Предполагают, что уровень секреции ФРТ может быть прогностическим маркером успешности имплантации и качества полученных эмбрионов в программе ЭКО [58].
При имплантации в клетках эндометрия выявлена экспрессия фактора роста кератиноцитов (ФРК). Последний принадлежит к семейству ФРФ, является выраженным паракринным регулятором, продуцируется стромальными клетками, но действует преимущественно на эпителиальные клетки эндометрия, которые имеют к нему соответствующие рецепторы.
Рецепторы этого фактора роста обнаруживаются также на бластоцисте и эмбрионах на более поздней стадии развития, имплантирующихся in vitro, что, по мнению авторов, подтверждает существование паракринного контроля имплантации [30].
В экспериментах in vitro показано, что ФРК является мощным митогеном, действующим как мезенхимальный медиатор роста, дифференцировки и морфогенеза эпителиальных клеток. Избыточная экспрессия ФРК in vivo вызывает гиперплазию эпителиальных тканей в различных органах. В репродуктивной системе уровень ФРК регулируется циркулирующими гормонами, в частности, его секреция увеличивается в периоды интенсивного роста клеток [30].
Однако собственно имплантации предшествуют определенные процессы, развивающиеся в эндометрии в секреторной фазе цикла. В соответствии с этим представлением, реакция эндометрия в ходе имплантации делится на три фазы [25]:
1. Первая фаза. Находится под контролем эстрогенов и прогестерона и характеризуется изменениями в покровных и железистых эпителиальных клетках эндометрия, результатом чего является подготовка к аппозиции и присоединению бластоцисты. Гормональные влияния на эндометрий зависят от присутствия ядерных рецепторов к стероидным гормонам. Нарастание концентрации рецепторов наблюдается в направлении от функционального слоя к базальному, что коррелирует с установлением максимальной рецептивности матки, необходимой для имплантации. Параллельно с изменениями в системе стероидных рецепторов клетки эпителия претерпевают изменения в структуре цитоскелета и профиле секреции белков. Эти изменения могут быть предотвращены антагонистами прогестероновых рецепторов в лютеиновой фазе цикла.
2. Вторая фаза. Модуляция гормональных стероидных эффектов эмбриональными факторами. Начало секреции бластоцистой хорионического гонадотропина и других белков ранней беременности вызывает дополнительные изменения в клетках эндометрия. В клетках покровного эпителия происходит эндорепликация, образуются «эпителиальные бляшки». Железистый эпителий отвечает на действие эмбриональных регуляторных факторов модификацией главного секреторного продукта — гликоделина, дающего иммунный протекторный эффект в отношении наступающей беременности. Стромальные фибробласты начинают процесс своей дифференцировки, приобретают децидуальный фенотип, начинают экспрессировать актиновые филаменты.
3. Третья фаза. Инвазия трофобласта и перестройка стромального компонента эндометрия, гладкомышечных клеток, эндотелия кровеносных сосудов. При этом на покровном эпителии исчезают «эпителиальные бляшки», железистый эпителий остается высоко секреторно активным. В этой фазе заканчивается трансформация фибробластов в децидуальные клетки, которые начинают экспрессировать весь комплекс ростовых факторов, свойственных ранней беременности.
Хорошими маркерами эндометриальной функции и готовности эндометрия к имплантации являются адгезионные молекулы, роль которых в регуляции имплантации стала интенсивно изучаться в последние годы.
К молекулам адгезии относятся 4 семейства белков: интегрины, кадгерины, селектины и семейство иммуноглобулинов.
В процессе имплантации обмен сигналами между эмбрионом и эндометрием осуществляется в том числе посредством молекул адгезии. Интересно, что добавление некоторых молекул адгезии в культуральную среду улучшало качество эмбрионов и повышало частоту имплантации и наступления беременности в программе ЭКО [26, 75].
Несмотря на достигнутые успехи в понимании некоторых механизмов имплантации, до сих пор остается невыясненным ряд вопросов, касающихся регуляции последовательности событий в секреторном эндометрии и установлении взаимодействия между развивающимся эмбрионом и рецептивным эндометрием. Мы только начинаем понимать механизмы действия ряда гуморальных факторов и эффекторных молекул в регуляции такого рода взаимоотношений. Несомненно, решение этих вопросов позволит значительно продвинуться в оптимизации существующих и создании новых методов преодоления бесплодия.
Имплантация зародыша
 |
ИМПЛАНТАЦИЯ ЧЕЛОВЕЧЕСКОГО ЗАРОДЫША НА РАННИХ СТАДИЯХ РАЗВИТИЯ: |
Имплантация зародыша (от лат.im… — в, внутрь и plantatio — посадка, пересадка), нидация зародыша — внедрение зародыша с помощью ворсинокхориона в слизистую оболочку матки. Происходит на стадии бластоцисты (см.Эмбриональное развитие) на 6—7-е сутки послеоплодотворения или 20—21-й деньменструального иикла преим. на задней стенке матки, в половине, соответствующей яичнику, из к-рого вышлаяйцеклетка. К концу 2-х суток от начала имплантации зародыш уже полностью погружается в слизистую оболочку матки.
У человека И. з. относится к интерстициальному типу, т. е. зародыш разрушает прилежащий участок слизистой с помощью протеолитич. ферментов и целиком погружается в её толщину, где и продолжает развиваться. Образующийся при этом имплантационный кратер закрывается восстановленной слизистой над погрузившимся зародышем. Важную роль в этом процессе играет трофобласт, к-рый усиленно разрастается. В начале И. з. зрелая бласто-циста прилегает к эпителию матки своим эмбриональным полюсом, покрытым цитотрофобластом.
Его поверхностный слой превращается в плазмодиотрофобласт, обладающий резко выраженными деструктивными и инфильтрирующими свойствами. Имплантационный плазмодий существует лишь непродолжительное врегйя и на 9-10-й день развития дегенерирует. Клетки цитотрофо,ласта, напротив, размножаются, образуя первичные ворсинки. В процессе И. з. слизистая оболочка матки претерпевает изменения, к-рые можно рассматривать как реакцию на внедрение зародыша на фоне гормонального влияния со стороны жёлтого тела.
Она выражается в расширении и многократном ветвлении спиральных артерий и появлении в их окружности крупных, богатых гликогеном децидуальных клеток. В период И. з. могут развиться аномалии прикрепления пуповины, формы плаценты, ведущие кплацентарной недостаточности.
имплантация и формирование хориона — жужа//
1. РАЗВИТИЕ ПЛАЦЕНТЫ ЧЕЛОВЕКА.
1.1. Гистофизиология трофобласта и динамика имплантации.
Для понимания процессов развития плаценты человека необходимо вспомнить некоторые детали раннего периода эмбриогенеза. Первая стадия эмбриогенеза — оплодотворение происходит в ампулярной части маточной трубы, после чего зародыш начинает перемещаться в направлении матки. Спустя 24-30 часов после оплодотворения, во время движения зародыша по маточной трубе, начинается процесс дробления с превращением зиготы в морулу, а затем в бластулу. Весь период движения с одновременным дроблением занимает 4-5 суток от момента оплодотворения, после чего зародыш попадает в матку. В течение всего этого времени зародыш окружен блестящей оболочкой, выполняющей двойную функцию. С одной стороны, она сдерживает прогрессивное увеличение размеров зародыша и предотвращает его внедрение в слизистую оболочку маточной трубы (трубную внематочную беременность). С другой стороны, в доимплантационный период блестящая оболочка защищает зародыш от иммунного конфликта с организмом матери. Это необходимо, так как зародыш является наполовину (отцовскую) генетически чужеродным организмом. Непосредственно перед попаданием в полость матки и в течение еще 1-2 дней после него зародыш превращается в зрелую бластоцисту. Через блестящую оболочку происходит всасывание маточного секрета с образованием полости бластоцисты. Бластомеры дифференцируются на 2 типа: темные и светлые. Скопление темных бластомеров (эмбриобласт) оттесняется на один полюс бластулы (бластоцисты), к ее эмбриональному полюсу. В последующем из эмбриобласта формируется тело зародыша и большинство внезародышевых органов и тканей. Светлые бластомеры окружают эмбриобласт и замыкают полость бластоцисты. Они формируют первичный трофобласт, который является источником развития эпителия хориона, а затем эпителия плацентарных ворсин. В течение 1-2 дней, когда зародыш находится в полости матки в состоянии свободной бластоцисты, в трофобласте происходят изменения, необходимые для внедрения зародыша в эндометрий — имплантации. Помимо внутреннего клеточного слоя — цитотрофобласта снаружи за счет слияния клеток цитотрофобласта и деления образуется многоядерный слой — синцитиотрофобласт (плазмодиотрофобласт). В этом слое увеличивается количество лизосом с гидролитическими ферментами. Непосредственно перед внедрением в эндометрий растворяется блестящая оболочка, что носит название стадии «вылупления» (hatching). На 6-7 сутки после оплодотворения начинается имплантация (нидация) зародыша. Процессы, происходящие при этом, могут быть разделены на 2 стадии: прилипания (адгезии) и проникновения (инвазии). В стадии адгезии бластоциста распластывается эмбриональным полюсом на поверхности эндометрия, что увеличивает площадь контакта синцитиотрофобласта со слизистой оболочкой матки. Обычным местом имплантации является передняя или задняя стенка матки, ближе к ее дну. Такое расположение обеспечивает не только правильное взаиморасположение плода, структур последа и частей матки, но и наилучшее кровоснабжение плаценты. Важно отметить, что в норме имплантация происходит эмбриональным полюсом бластоцисты. При имплантации строго противоположным полюсом зародыш погибает, а в случае неполной инверсии зародыша развиваются аномалии прикрепления пупочного канатика, которые тоже могут осложнить беременность и роды. В следующей стадии имплантации происходит массивный выброс гидролитических ферментов синцитиотрофобласта, что приводит к последовательному разрушению эпителия, собственной пластинки эндометрия с погружением в него зародыша. Кроме этого, разрушение эпителия происходит и за счет активизации его собственных лизосом. В среднем через 40 часов зародыш оказывается полностью погруженным в слизистую оболочку матки. Дефект в месте имплантации заполняется имплантационным коагулятом (кровь, фибрин, фрагменты тканей), который к 12-му дню полностью эпителизируется. За счет пролиферации трофобласта формируются клеточные тяжи, называемые первичными ворсинами. Эти выросты увеличивают глубину проникновения зародыша. Из первичного трофобласта формируется ворсинчатая оболочка -хорион. Бластоциста с момента образования первичных хориальных ворсин называется плодным пузырем. Между 8 и 9 днем внутриутробного развития (с момента оплодотворения) очаги расплавления эндометрия объединяются в сообщающиеся полости — лакуны. Они являются прообразами межворсинчатых пространств сформированной плаценты. Питание зародыша в этот короткий отрезок времени осуществляется за счет лизированных тканей эндометрия —гистиотрофно. Пролиферирующий трофобластический эпителий быстро внедряется в эндометриальные капилляры и материнская кровь свободно изливается в просвет лакун. Тип питания сменяется на гематотрофный, то есть за счет крови матери. На сроке 17-19 дней, как доказано в последнее сремя, происходит проникновение трофобласта до уровня спиральных сегментов эндометриальных артерий с их разрушением, вскрытием. Таким образом, с данного срока устанавливается маточно-плацентарное кровообращение. Этот факт доказан как морфологически, так и с помощью современных методов ультразвуковой диагностики. Все описанные структурные изменения после имплантации и до середины 2-й недели эмбриогенеза обозначаются как лакунарная стадия развития плаценты. В эти же сроки начинается усложнение структуры ворсин, которые первоначально состоят только из трофобластического эпителия. На 12-13 день из эмбриобласта выселяются клетки внезародышевой мезенхимы, которые изнутри врастают в трофобласт, в первичные ворсины. К 14-15 дню формируются вторичные (мезенхимальные) ворсины. Они состоят из центрально расположенной мезенхимальной стромы, покрытой снаружи двухслойным трофобластическим эпителием. Внутренний слой — цитотрофобласт состоит из крупных многоугольных клеток с оксифильной цитоплазмой и высокой митотической активностью. Наружный слой — синцитиотрофобласт представляет собой сплошную базофильную массу цитоплазмы с множеством удлиненных и интенсивно окрашенных ядер. Для зрелого трофобластического эпителия характерна высокая активность гидролитических, окислительных и других ферментов (щелочной и кислой фосфатазы, сукцинатдегидрогеназы, лактатдегидрогеназы, НАД-диафоразы и др.). В течение нормальной беременности цитотрофобласт должен практически полностью трансформироваться в синцитий. Имеются данные и о возможности формирования из цитотрофобласта соединительнотканных элементов ворсин. Отклонения в структуре трофобластического эпителия служат морфологическими маркерами патологии беременности. Клетки трофобластического эпителия образуют не только покров ворсин, но и располагаются отдельно в виде колонн или островков. Такой трофобласт, который обеспечивает дальнейшее внедрение ворсин в эндометрий, а также является гормонально активным, называется вневорсинчатым (периферическим). В процессе развития плацентарных ворсин трофобластический эпителий постоянно подвергается изменениям, в связи с чем формируется несколько типов синцитиотрофобласта, которые мы охарактеризуем при рассмотрении строения плаценты во второй половине беременности. Хорионический гонадотропин, интенсивная секреция которого устанавливается со 2-ой недели и удерживается до 4-го месяца беременности, поддерживает существование желтого тела беременности, продуцирующего прогестерон, пока плацента не возмет на себя эту функцию. Данный гормон является одним из основных гормонов плаценты, поддерживающим структурную и функциональную полноценность эндометрия. Элементы вневорсинчатого трофобласта имеются в составе материнской части плаценты, что представляет диагностическую ценность при исследовании эндометрия в ампутированной матке, при выскабливании полости матки, при биопсии эндометрия во время Кесарева сечения.
1.2. Формирование структуры плаценты в эмбриогенезе.
Все процессы, описанные выше, приводят к формированию вокруг зародыша ворсинчатой оболочки — хориона, который подразделяется на 2 части: ворсинчатый (chorion frondosum) и гладкий (chorion laeve). Ворсинчатый хорион формируется в области полюса имплантации и именно из него развивается плодная часть плаценты —хориальная пластинка и ворсины. На остальной площади ворсинчатые образования редуцируются, почему она и носит название гладкого хориона. В отдельных участках гладкого хориона сохраняются лишь остатки редуцированных ворсин. С 3-ей недели внутриутробного развития часть мезенхимных клеток стромы вторичных ворсин дифференцируется в клеточные элементы стенок кровеносных капилляров (аутохтонный ангиогенез). С этого времени условно исчисляется период плацентации. Одновременно происходит рост кровеносных сосудов со стороны аллантоиса. В среднем на 32-й день происходит соединение аллантоисных сосудов с капиллярами ворсин. Ворсины превращаются в третичные и устанавливается кровообращение между плодом и плацентой — фетоплацентарное кровообращение. Таким образом, после 3-й недели беременности большинство ворсин должны содержать кровеносные сосуды. При этом в период плацентации преобладают крупные стволовые (опорные) ворсины диаметром от 160 мкм до 2 мм. Их сосудистая сеть представлена как плодовыми артериями и венами, так и капиллярами. Мезенхима стромы ворсин дифференцируется с образованием тонких ретикулярных волокон, фибробластических клеток различной степени зрелости, макрофагов (клетки Кащенко-Гофбауэра). Период плацентации длится до 12 недели. В течение него наблюдается увеличение разветвленности ворсин, дальнейшая трансформация ворсинчатого цитотрофобласта в синцитий, дифференцировка соединительнотканной стромы ворсин и их сосудистого русла. На 5-6 неделе беременности синцитиотрофобласт составляет 2/3 эпителиального пласта ворсин. В период с 4 по 6, а затем с 8 по 12 неделю внутриутробного развития наблюдается волнообразное усиление притока материнской крови к плаценте. Происходит это за счет активности вневорсинчатого трофобласта. Часть его прикрепляет крупные ворсины к эндометрию. Такие ворсины называются якорными (ЯВ). Свободно расположенные островки трофобластического эпителия продолжают разрушение тканей эндометрия, что происходит за счет их пролиферации и ферментной активности как в строме эндометрия (интерстициальный трофобласт), так и внутри эндометриальных сосудов (внутрисосудистый трофобласт). В результате этого происходит вскрытие эндометриальных сегментов спиральных артерий эндометрия, после чего устанавливается постоянный маточно-плацентарный кровоток. Примерно с 8 недели беременности усложнение структуры ворсин сопровождается формированием структурных единиц плаценты — котиледонов, которые представляют собой участок хориальной пластинки с отходящей от него стволовой ворсиной со всеми ее ветвлениями. К концу периода плацентации (12 неделя) устанавливается окончательное количество котиледонов, которое достигает 200. Дальнейшие совершенствования в структуре плаценты, сменяющие период плацентации, характеризуются как период (стадия) фетализации плаценты и период (стадия) зрелой плаценты. Период фетализации длится в течение всего 2 триместра (4-6 месяцы) беременности до 35 недели 3 триместра и характеризуется дальнейшим ростом и усложнением ворсинчатого дерева. Существенным этапом в этот период является вторая волна внедрения вневорсинчатого трофобласта в эндометрий с вовлечением ближайших к эндометрию артерий мышечной оболочки матки. Это обеспечивает резкий прирост маточно-плацентарного кровотока. В период зрелой плаценты наблюдается не рост ворсинчатого дерева, а изменения его структуры в соответствии с метаболическими потребностями растущего плода.
Признаки имплантации эмбриона | Эмбриональное развитие
До рождения эмбрион проходит многосложный путь эволюции от одноклеточного организма до сформировавшегося ребенка. Процесс развития протекает в материнской утробе. Оплодотворение яйцеклетки — это начальный этап зарождения новой жизни. Одним из наиболее важных моментов является имплантация эмбриона. Признаки прикрепления зародыша можно определить по ощущениям. Оценивать объективно симптомы может женщина, имеющая понятие о беременности.
Как только у будущих родителей появилась уверенность в успешном зачатии, вдохновение к изучению приятного периода увеличивается. Будущая мама начинает наблюдать за каждым днем детально: прислушивается к симптомам, изучает совпадения и различия, подсчитывает сроки. Наибольшего внимания удостаиваются первые недели, когда происходит имплантация эмбриона. На какой день цикла случается внедрение зародыша в толщу маточной стенки и чем характеризуется данный процесс?
Эмбрион человека
Эмбрион – зародыш, развивающийся в материнской утробе. Статус эмбриона сохраняется восемь недель от начала зачатия. В течение этого времени оплодотворенная яйцеклетка проходит цикл развития, формируясь в тело, обладающее всеми морфологическими особенностями. Далее эмбрион принято называть плод. Эмбриональное развитие делят на периоды:
- Стадия одноклеточного организма. Период кратковременный, протекающий от оплодотворения до начала деления яйца.
- Дробление. Происходит образование бластомеров: формируется группа клеток – морула, затем однослойная бластула.
- Гаструляция. Образование зародышевых листков. В первой фазе цикла образуется эктодерма и эндодерма, а также закладка хориона. Вторая половина гаструляции характерна образованием хориона и плаценты. В период гаструляции закладывается нервная система, сколет, мускулатура.
- Обособление главных зачатков и их развитие.
Ближе к четвертой неделе беременности формируется сердце. При дальнейшем развитии сердечко становится четырехкамерным (восьмая неделя беременности). Сердце зародыша имеет особенность – овальный просвет между предсердиями и боталлов проток, расположенный между аортой и легочной артерией. Такое отверстие необходимо для снабжения организма кислородом в условиях отсутствия автономного дыхания. Иногда эмбрион отстает в развитии. Данная патология чаще заканчивается самопроизвольным абортом. Наиболее вероятные причины выкидышей – хромосомные дефекты.
Имплантация эмбриона. Признаки
Оплодотворение яйцеклетки – это зарождение организма. Другими словами – слияние мужской и женской половой клетки влечет за собой формирование плодного яйца, из которого развивается человек.
Наиболее популярным способом зачатия является эякуляция во время полового акта, происходящая одновременно с выходом яйцеклетки из фолликула. Завершается процесс оплодотворением. Когда зачатие естественным путем невозможно, то обращаются к вспомогательным способам репродукции.
При методике ЭКО яйцеклетку забирают из организма матери и оплодотворяют в пробирке. После этого эмбрион проводит некоторое время в инкубаторе. Через пять дней зародыш переносят в матку, где происходит имплантация эмбриона. На какой день зародыш закрепляется в матке? Момент прикрепления зародыша продолжается сорок часов, а имплантация эмбриона (признаки рассмотрим далее) происходит до 20 недели, пока не образуется плацента.
Перед тем, как пересадить эмбрион, репродуктологи его оценивают. Для имплантации отбираются качественные особи, не имеющие генетических отклонений, у которых высокие адаптационные возможности. Предимплантационная диагностика – это важный этап, позволяющий выявить наследственные заболевания и определить пол ребенка.
Период имплантации эмбриона разделяют на раннюю имплантацию и позднюю. Поздняя имплантация благоприятна при методике ЭКО (эмбриону необходимо больше времени для адаптации).
Беременность для организма – это значительная нагрузка. Из-за этого у женщины появляются признаки, свидетельствующие об имплантации эмбриона:
- Выделения. При имплантации эмбриона наблюдаются скудные выделения со светло-коричневым оттенком. Окрашенные бели являются нормой и возникают по причине повреждения мелких капилляров в процессе проникновения эмбриона в эпителий матки.
- Болезненность молочных желез.
- Боль внизу живота.
- Тошнота.
- Раздражительность, головокружение.
- Депрессия.
Отсутствие симптомов – не повод расстраиваться. Единственный надежный способ определить беременность – сделать исследование ХГЧ. Лабораторный тест беременности рекомендуют проводить не раньше пяти дней задержки менструального кровотечения. Норма ХГЧ при беременности – важный показатель благополучия. Любые отклонения свидетельствуют о патологии.
Если плодному яйцу удалось закрепиться, то он гарантированно преодолевает все трудности, которые могут возникнуть в период развития. Если эмбрион слабый, скорее всего, беременность прервется.
Выделения при имплантации эмбриона
Несмотря на то, что выделения при имплантации эмбриона являются своего рода правилом, однако, при появлении любых белей с розовым или красным оттенком женщина должна проинформировать врача.
Единственным допустимым признаком имплантации является капля светло- розовой или коричневой жидкости. Это объясняется тем, что плодное яйцо, достигнув матки, закрепляется в эпителиальном слое. Процесс постепенный. Во время проникновения зародыша в толщу эндометрия повреждаются мелкие кровеносные сосуды. Плодное яйцо настолько маленькое, что вызывать обильное кровотечение не способно. Если характер выделений настораживает: интенсивное кровотечение, которое длится долго, необходимо срочно обратиться к гинекологу, сделать УЗИ.
Благополучная имплантация
Удачная транспортировка эмбрионов в полость матки не гарантирует успешную имплантацию. Ни один специалист не может спрогнозировать, сколько зародышей имплантируется. Однако, в медицинских клиниках ЭКО разрабатываются и используются технологии, позволяющие увеличить результативность процедуры.
Помимо этого, после экстракорпорального оплодотворения с подсадкой эмбрионов женщина получает ряд рекомендаций относительно образа жизни:
- Исключить тяжелый физический труд
- В рационе питания должны присутствовать полезные продукты, содержащие витамины и минеральные вещества
- Избегать половых контактов
- Не переохлаждаться
- Кратковременные прогулки на природе
В целях безопасности лучше воздержаться от вождения автомобиля. Никогда не стоит отчаиваться при неудачных попытках зачатия. Даже если не происходит естественная имплантация эмбриона, просто необходимо обследоваться, выявить причины отторжения и постараться их вылечить. На сегодняшний день врачи успешно проводят процедуру ЭКО, итогом которой является беременность и рождение здорового малыша.