Гемофилия — Википедия
 Система для инъекций с раствором фактора VIII, способствующего свёртываемости крови; пригодна для самостоятельного введения препарата
Система для инъекций с раствором фактора VIII, способствующего свёртываемости крови; пригодна для самостоятельного введения препарата 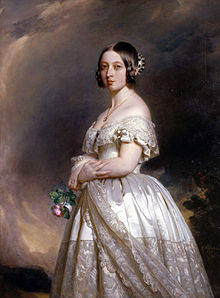
Гемофили́я (от др.-греч. αἷμα — «кровь» и др.-греч. φιλία, здесь — «склонность»[1]) — редкое наследственное заболевание, связанное с нарушением коагуляции (процессом свёртывания крови). При этом заболевании возникают кровоизлияния в суставы, мышцы и внутренние органы, как спонтанные, так и в результате травмы или хирургического вмешательства. При гемофилии резко возрастает опасность гибели пациента от кровоизлияния в мозг и другие жизненно важные органы, даже при незначительной травме. Больные с тяжёлой формой гемофилии подвергаются инвалидизации вследствие частых кровоизлияний в суставы (гемартрозы) и мышечные ткани (гематомы). Гемофилия относится к геморрагическим диатезам, обусловленным нарушением плазменного звена гемостаза (коагулопатия).
Гемофилия появляется из-за изменения одного гена в хромосоме X. Различают три типа гемофилии (A, B, C).
- Гемофилия A (рецессивная мутация в X-хромосоме) вызывает недостаточность в крови необходимого белка — так называемого фактора VIII (антигемофильного глобулина). Такая гемофилия считается классической, она встречается наиболее часто, у 80—90 %[1] больных гемофилией. Тяжёлые кровотечения при травмах и операциях наблюдаются при уровне VIII фактора — 5—20 %.
- Гемофилия B (рецессивная мутация в X-хромосоме) — недостаточность фактора плазмы IX (Кристмаса). Нарушено образование вторичной коагуляционной пробки.
- Гемофилия C (аутосомный рецессивный либо доминантный (с неполной пенетрантностью) тип наследования, то есть встречается как у мужчин, так и у женщин) — недостаточность фактора крови XI, известна в основном у евреев-ашкеназов. В настоящее время гемофилия С исключена из классификации, так как её клинические проявления значительно отличаются от А и В.
Ведущими симптомами гемофилии А и В являются повышенная кровоточивость с первых месяцев жизни; подкожные, межмышечные, субфасциальные, забрюшинные гематомы, обусловленные ушибами, порезами, различными хирургическими вмешательствами; гематурия; обильные посттравматические кровотечения; гемартрозы крупных суставов, с вторичными воспалительными изменениями, которые приводят к формированию контрактур и анкилозов.
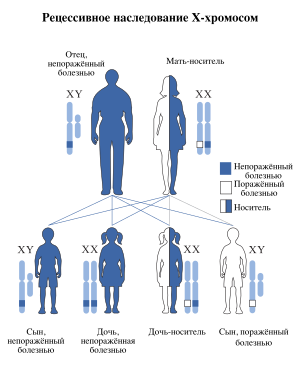
Обычно болезнью страдают мужчины (наследование, сцепленное с полом), женщины же обычно выступают как носительницы гемофилии и могут родить больных сыновей или дочерей-носительниц. Всего в мире задокументировано порядка 60 случаев гемофилии (типа A или B) у девочек. В связи с тем, что современная медицина существенно продлевает среднюю продолжительность жизни больных гемофилией, то определённо можно сказать, что случаи гемофилии у девочек будут встречаться всё чаще. Кроме того, примерно в 15-25 % случаев обследование матерей мальчиков, страдающих гемофилией, не выявляет указанных мутаций генов
Наиболее распространённое заблуждение о гемофилии — это то, что больной гемофилией может истечь кровью от малейшей царапины, что неверно. Проблему составляют крупные ранения и хирургические операции, удаление зубов, а также спонтанные внутренние кровоизлияния в мышцы и суставы, обусловленные, по-видимому, уязвимостью стенок сосудов у больных гемофилией.
Самой известной носительницей гемофилии в истории была королева Виктория; по-видимому, эта мутация произошла в её генотипе de novo, поскольку в семьях её родителей страдающие гемофилией не зарегистрированы. Теоретически, это могло бы произойти и в том случае, если бы биологическим отцом Виктории являлся не Эдуард Август, а какой-либо другой мужчина (больной гемофилией), однако никаких исторических свидетельств в пользу этого не существует. Гемофилией страдал один из сыновей Виктории (Леопольд, герцог Олбани), а также ряд внуков и правнуков (родившихся от дочерей или внучек), включая российского царевича Алексея Николаевича. По этой причине данное заболевание получило такие названия: «викторианская болезнь» и «царская болезнь». Также иногда в царских фамилиях для сохранения титула допускались браки между близкими родственниками, отчего частота встречаемости гемофилии была выше.
Для диагностики гемофилии применяется: коагулограмма, определение времени свёртываемости, добавление образцов плазмы с отсутствием одного из факторов свёртывания.
Хотя болезнь на сегодняшний день неизлечима, её течение контролируется с помощью инъекций недостающего фактора свёртываемости крови, чаще всего выделенного из донорской крови. Некоторые гемофилики вырабатывают антитела против замещающего белка, что приводит к увеличению необходимой дозы фактора или применению заменителей, таких как свиной фактор VIII. В целом современные гемофилики при правильном лечении живут столько же, сколько и здоровые люди.
На настоящий момент для лечения используются концентраты факторов свертывания как полученные из донорской крови, так и рекомбинантные (выращенные искусственным путём у животных).
Носительницы гена гемофилии на сегодня практически не имеют возможности заранее спланировать рождение больного или здорового ребёнка, за исключением, возможно, процедуры экстракорпорального оплодотворения (ЭКО) при соблюдении определённого ряда условий. Также, при соблюдении определённых условий, возможно диагностировать наличие гемофилии у плода с 8 недели беременности. Такое исследование можно провести в ряде медицинских учреждений России, однако самый большой опыт пренатальной диагностики гемофилии накоплен в НИИ акушерства и гинекологии им. Отта в Санкт-Петербурге.
Группе генетиков удалось вылечить лабораторных мышей от гемофилии при применении генотерапии[2]. Учёные для лечения использовали аденоассоциированные вирусы (AAV).
Принцип лечения заключается в вырезании мутированной последовательности ДНК с помощью фермента, носителем которого является AAV, и последующей вставке в это место здорового гена уже вторым вирусом AAV. Фактор свёртывания IX кодируется геном F9. Если исправить последовательность F9, то фактор свёртывания начнёт вырабатываться в печени, как у здоровой особи.
После генотерапии у мышей уровень фактора в крови вырос до нормы. За 8 месяцев не было выявлено никаких побочных эффектов.
Лечение проводится во время кровотечения:
- гемофилия А — переливание свежей плазмы, антигемофилийная плазма, криопреципитат;
- гемофилия В — свежезамороженная донорская плазма, концентрат фактора свёртывания;
- гемофилия С — свежезамороженная сухая плазма.
Далее проводится симптоматическое лечение.
По мнению С. И. Куцева, опубликованному в мае 2019 года, некоторые фармацевтические компании мира «очень близки» к началу лечения гемофилии с помощью редактирования генома и классической генной терапии
Методы лабораторной диагностики свертывающей системы крови[править | править код]
Регистрируют ее преимущественно у собак, свиней и лошадей. Диагноз устанавливают на основании повышенной кровоточивости, наличия случаев заболеваний по линии самцов, с учётом удлинения времени свёртывания крови. Пробы на ломкость сосудов при гемофилии отрицательные. Дифференциальную диагностику проводят с гиповитаминозами С, К, Р, тромбоцитопенией, апластической анемией и аллергией. Решающее значение в диагностике имеют данные биохимических, морфологических исследований крови и результаты постановки аллергических проб[4].
Болезнь несвертываемость крови: симптомы, диагностика и лечение

Несвертываемость крови уже давно известна медикам под названием «царской болезни». Этот недуг описывают, как склонность сосудов организма к повышенной кровоточивости. Безусловно, это заболевание несет серьезную угрозу не только для здоровья, но также и для жизни больного.
Как называется наследственная болезнь, вызывающая несвертываемость крови? Ее по-другому называют гемофилией и относят к геморрагическим патологиям, передающимся по наследству. Главная опасность кровяной несвертываемости заключается в том, что она может вызывать длительное и довольно интенсивное кровотечение.
Симптоматика у детей
Болезнь несвертываемость крови может быть обнаружена еще у новорожденного ребенка. У некоторых малышей вскоре после появления на свет отмечаются следующие признаки:
- Присутствие родовых гематом.
- Продолжительные кровотечения из пуповины.
- Возобновление кровотечений спустя несколько дней.
- Появление множественных синяков на теле.
- Формирование гематом.
Родители не всегда знают, как называется болезнь несвертываемости крови, и чем она опасна.
Даже простые прививки могут приводить к затяжному кровотечению у детей. По мере взросления ребенка интенсивность симптоматики, к сожалению, не уменьшится. По причине физического увеличения ткани, сосуды могут травмироваться, что приведет к увеличению кровоизлияний. Суставные кровотечения могут начинаться с двухлетнего возраста.
Следует отметить, что в том случае, если у ребенка была диагностирована эта патология, то об этом должны обязательно быть проинформированы школьные врачи, учителя и воспитатели в целях обеспечения безопасности.
Признаки в возрасте после 4 лет
Приблизительно после четырех лет у детей, которые страдают от гемофилии, могут развиваться такие симптомы:
- Появляется кровоточивость десен.
- Зачастую наблюдаются носовые кровотечения.
- Любая гематома становится обширнее и больше в своем объеме.
У детей проведение полной диагностики организма может показать наличие и других осложнений. Например, анализ мочи зачастую показывает гематурию, а именно присутствие в выделениях крови. В том случае, если происходит обострение, то весьма высок риск внутримозговых кровотечений, а кроме того, повреждений нервной системы и летального исхода в том числе.

После того как доктором будет поставлен точный диагноз — болезнь несвертываемости крови, ребенку потребуется постоянно принимать лекарственные средства, которые будут препятствовать развитию кровотечений. Очень важно оградить малыша от получения всяческих травм и проследить за тем, в какой форме он употребляет препараты. К примеру, из-за плохой кровяной свертываемости ему будут противопоказаны любые внутримышечные инъекции.
Симптомы у женщин
Гемофилия, или болезнь несвертываемости крови, у женщин является исключением из правил. За всю историю человечества было зарегистрировано только шестьдесят случаев этого заболевания у представительниц женского пола. В большинстве ситуаций передача гена от отца или матери, который поддался мутации, приводит к гибели плода женского пола. Правда, в редких случаях происходит и выживание. Не исключено генетическое изменение уже в процессе жизнедеятельности. Как правило, у женщин данная патология проходит в более легкой стадии, нежели у мужчин, и отличается следующими симптомами:
- Присутствие обильных менструаций.
- Продолжительные кровотечения непосредственно после удаления миндалин или зубов.
- Присутствие носовых кровотечений.

Необходимо отметить, что у женщин время от времени могут возникать кровотечения без каких-либо видимых причин и без предварительных травм при болезни крови. Несвертываемость крови чаще обнаруживается у мужчин.
Симптомы у мужчин
Жизнедеятельность с диагнозом «гемофилия» имеет свои особенности. У мужчин симптомы этой патологии в течение жизни возникают очень часто, а непосредственно с возрастом они становятся лишь сильнее и интенсивнее. Для того чтобы увеличить продолжительность жизни, требуется проводить постоянную профилактику и адекватное лечение. Симптоматика у мужчин наблюдается следующая:
- Появление обширных синяков в различных местах на теле.
- Возникновение обильных забрюшинных кровоизлияний.
- Присутствие кровоизлияний в костную ткань и суставные полости.
- Наличие защемления нервных окончаний вплоть до развития паралича вследствие уплотнения огромных гематом.
- Появление кровотечений из горла непосредственно после кашля или на фоне чихания.
Для того чтобы избавиться от гематом, больному необходимо проведение хирургического лечения. Оно проводится лишь после качественной подготовки пациента к оперативному вмешательству. Итак, мы выяснили, что название болезни несвертываемости крови – гемофилия.
Проведение диагностики
В целях подтверждения соответствующего диагноза такие пациенты должны пройти следующее обследование:
- Необходимо сдать анализ крови.
- Требуется выполнить исследование агрегации тромбоцитов. Эта диагностическая методика продемонстрирует способность клеток организма прикрепляться друг к другу.
- Также измеряется время, в течение которого кровь останавливается после прокола пальца пером.
Лечение недуга
В том случае, если заболевание возникло из-за какой-либо системной патологии, которая вызвала снижение скорости кровяного свертывания, то лечение должно направляться на устранение основных причин недуга. Так, когда в основе заболевания лежит лейкоз, пациентам показано облучение наряду с химиотерапией, а при наличии необходимости и трансплантация костного мозга.

Когда в том, что кровь не сворачивается, виновна печень, больным назначается медикаментозное лечение с применением гепатопротекторных препаратов. Зачастую ремиссию заболевания достигают путем обогащения питательного рациона необходимыми компонентами, дефицит которых довел до развития патологии. Для этого пациентам назначают фолиевую кислоту, кальций, витамин К, а кроме того, незаменимые аминокислоты. Повысить свертывание крови у ребенка или взрослого, который страдает от недуга, можно посредством применения определенных лекарственных средств.
Медикаменты
Лечение такого недуга, как гемофилия (в зависимости от факторов, вызвавших ее развитие), может включать в себя использование следующих медикаментов:
- Применение коагулянтов, полученных из плазмы донора. Они применяются с целью остановки кровотечения.
- Борьба с дефицитом фибриногена осуществляется путем внутривенного ввода препаратов с его большим содержанием.
- Лечение гемофилии, которая была вызвана болезнью Виллебранда, проводится инъекциями антигемофильной плазмы и криопреципитата.
- Отличное кровоостанавливающее воздействие демонстрируется «Контрикалом» и аминокапроновой кислотой. Эти лекарственные препараты осуществляют профилактику появления тромбов.

Вне зависимости от причин возникновения этого заболевания лечение обязательно предполагает использование препаратов с повышенным содержанием железа, а кроме того, переливание донорской крови. Что еще применяется в лечении болезни несвертываемости крови?
Народная медицина
Народной медициной рекомендуется дополнять лекарственное лечение описываемого недуга отварами из плодов аронии, барбариса, листьев земляники и смородины. Лечение народными методами допускается лишь в сочетании с медикаментозной терапией, которая должна назначаться врачом. Народные рецепты направлены на поддержку организма в целом и на увеличение иммунной защиты.
Профилактика
Лучший народный способ профилактики и поддержки организма при наличии болезни несвертываемости крови – это соблюдение диеты, которая должна быть бедна на полиненасыщенные жиры, но богата витамином D. Правильное питание даст возможность человеку поддерживать базовые жизненные процессы, при этом не снижая еще сильнее способность крови сворачиваться.
Несмотря на то что гемофилия является неизлечимым заболеванием, при условии правильного подхода и регулярного лечения можно значительно увеличить продолжительность жизни, а вместе с тем и сохранить относительно нормальное самочувствие пациента.

В случае отсутствия соответствующего лечения патологии могут быть спровоцированы обильные кровотечения, которые могут повлечь за собой смертельный исход. Плохая кровяная свертываемость при беременности является крайне серьезным заболеванием. В его основе лежат системные патологии наряду с дефицитом таких веществ, как протромбин, фибриноген, витамин К и кальций. В любом случае больным с этим недугом требуется своевременная медикаментозная терапия, направленная на ликвидацию причин заболевания и устранение его серьезных последствий. В противном случае болезнь может приводить к наступлению смерти больного.
Мы рассмотрели, как называется болезнь несворачиваемости крови, а также методы ее лечения и профилактики.
Свёртывание крови — Википедия
Свёртывание крови — это важнейший этап работы системы гемостаза, отвечающий за остановку кровотечения при повреждении сосудистой системы организма. Совокупность взаимодействующих между собой весьма сложным образом различных факторов свёртывания крови образует систему свёртывания крови.
Свёртыванию крови предшествует стадия первичного сосудисто-тромбоцитарного гемостаза. Этот первичный гемостаз почти целиком обусловлен сужением сосудов и механической закупоркой агрегатами тромбоцитов места повреждения сосудистой стенки. Характерное время для первичного гемостаза у здорового человека составляет 1—3 минуты. Собственно свёртыванием крови (гемокоагуляция, коагуляция, плазменный гемостаз, вторичный гемостаз) называют сложный биологический процесс образования в крови нитей белка фибрина, который полимеризуется и образует тромбы, в результате чего кровь теряет текучесть, приобретая творожистую консистенцию. Свёртывание крови у здорового человека происходит локально, в месте образования первичной тромбоцитарной пробки. Характерное время образования фибринового сгустка — около 10 минут. Свёртывание крови — ферментативный процесс.
Основоположником современной физиологической теории свёртывания крови является Александр Шмидт. В научных исследованиях XXI века, проведённых на базе Гематологического научного центра под руководством Атауллаханова Ф. И., было убедительно показано[1][2], что свёртывание крови представляет собой типичный автоволновой процесс, в котором существенная роль принадлежит эффектам бифуркационной памяти.
Фибриновый сгусток, полученный путём добавления тромбина в цельную кровь. Сканирующая электронная микроскопия.Процесс гемостаза сводится к образованию тромбоцитарно-фибринового сгустка. Условно его разделяют на три стадии[3]:
- временный (первичный) спазм сосудов;
- образование тромбоцитарной пробки за счёт адгезии и агрегации тромбоцитов;
- ретракция (сокращение и уплотнение) тромбоцитарной пробки.
Повреждение сосудов сопровождается немедленной активацией тромбоцитов. Адгезия (прилипание) тромбоцитов к волокнам соединительной ткани по краям раны обусловлена гликопротеином фактором Виллебранда[4]. Одновременно с адгезией наступает агрегация тромбоцитов: активированные тромбоциты присоединяются к повреждённым тканям и друг к другу, формируя агрегаты, преграждающие путь потере крови. Появляется тромбоцитарная пробка[3].
Из тромбоцитов, подвергшихся адгезии и агрегации, усиленно секретируются различные биологически активные вещества (АДФ, адреналин, норадреналин и другие), которые приводят к вторичной, необратимой агрегации. Одновременно с высвобождением тромбоцитарных факторов происходит образование тромбина[3], который воздействует на фибриноген с образованием сети фибрина, в которой застревают отдельные эритроциты и лейкоциты – образуется так называемый тромбоцитарно-фибриновый сгусток (тромбоцитарная пробка). Благодаря контрактильному белку тромбостенину тромбоциты подтягиваются друг к другу, тромбоцитарная пробка сокращается и уплотняется, наступает её ретракция[3].
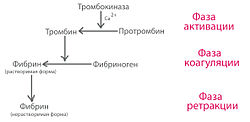 Классическая схема свёртывания крови по Моравицу (1905 год)
Классическая схема свёртывания крови по Моравицу (1905 год) 
Процесс свёртывания крови представляет собой преимущественно проферментно-ферментный каскад, в котором проферменты, переходя в активное состояние, приобретают способность активировать другие факторы свёртывания крови[3]. В самом простом виде процесс свёртывания крови может быть разделён на три фазы:
- фаза активации включает комплекс последовательных реакций, приводящих к образованию протромбиназы и переходу протромбина в тромбин;
- фаза коагуляции — образование фибрина из фибриногена;
- фаза ретракции — образование плотного фибринового сгустка.
Данная схема была описана ещё в 1905 году[5] Моравицем и до сих пор не утратила своей актуальности[6].
В области детального понимания процесса свёртывания крови с 1905 года произошёл значительный прогресс. Открыты десятки новых белков и реакций, участвующих в процессе свёртывания крови, который имеет каскадный характер. Сложность этой системы обусловлена необходимостью регуляции данного процесса.
Современное представление с позиций физиологии каскада реакций, сопровождающих свёртывание крови, представлено на рис. 2 и 3. Вследствие разрушения тканевых клеток и активации тромбоцитов высвобождаются белки фосфолипопротеины, которые вместе с факторами плазмы Xa и Va, а также ионами Ca2+ образуют ферментный комплекс, который активирует протромбин. Если процесс свёртывания начинается под действием фосфолипопротеинов, выделяемых из клеток повреждённых сосудов или соединительной ткани, речь идёт о внешней системе свёртывания крови (внешний путь активации свёртывания, или путь тканевого фактора). Основными компонентами этого пути являются 2 белка: фактор VIIа и тканевый фактор, комплекс этих 2 белков называют также комплексом внешней теназы.
Если же инициация происходит под влиянием факторов свёртывания, присутствующих в плазме, используют термин внутренняя система свёртывания. Комплекс факторов IXа и VIIIa, формирующийся на поверхности активированных тромбоцитов, называют внутренней теназой. Таким образом, фактор X может активироваться как комплексом VIIa—TF (внешняя теназа), так и комплексом IXa—VIIIa (внутренняя теназа). Внешняя и внутренняя системы свёртывания крови дополняют друг друга[5].
В процессе адгезии форма тромбоцитов меняется — они становятся округлыми клетками с шиповидными отростками. Под влиянием АДФ (частично выделяется из повреждённых клеток) и адреналина способность тромбоцитов к агрегации повышается. При этом из них выделяются серотонин, катехоламины и ряд других веществ. Под их влиянием происходит сужение просвета повреждённых сосудов, возникает функциональная ишемия. В конечном итоге сосуды перекрываются массой тромбоцитов, прилипших к краям коллагеновых волокон по краям раны[5].
На этой стадии гемостаза под действием тканевого тромбопластина образуется тромбин. Именно он инициирует необратимую агрегацию тромбоцитов. Реагируя со специфическими рецепторами в мембране тромбоцитов, тромбин вызывает фосфорилирование внутриклеточных белков и высвобождение ионов Ca2+.
При наличии в крови ионов кальция под действием тромбина происходит полимеризация растворимого фибриногена (см. фибрин) и образование бесструктурной сети волокон нерастворимого фибрина. Начиная с этого момента в этих нитях начинают фильтроваться форменные элементы крови, создавая дополнительную жёсткость всей системе, и через некоторое время образуя тромбоцитарно-фибриновый сгусток (физиологический тромб), который закупоривает место разрыва, с одной стороны, предотвращая потерю крови, а с другой — блокируя поступление в кровь внешних веществ и микроорганизмов. На свёртывание крови влияет множество условий. Например, катионы ускоряют процесс, а анионы — замедляют. Кроме того, существуют вещества как полностью блокирующие свёртывание крови (гепарин, гирудин и другие), так и активирующие его (яд гюрзы, феракрил).
Врождённые нарушения системы свёртывания крови называют гемофилией.
Методы диагностики свёртывания крови[править | править код]
Все многообразие клинических тестов свёртывающей системы крови можно разделить на две группы[7]:
- глобальные (интегральные, общие) тесты;
- «локальные» (специфические) тесты.
Глобальные тесты характеризуют результат работы всего каскада свёртывания. Они подходят для диагностики общего состояния свёртывающей системы крови и выраженности патологий, с одновременным учётом всех привходящих факторов влияний. Глобальные методы играют ключевую роль на первой стадии диагностики: они дают интегральную картину происходящих изменений в свёртывающей системе и позволяют предсказывать тенденцию к гипер- или гипокоагуляции в целом. «Локальные» тесты характеризуют результат работы отдельных звеньев каскада свёртывающей системы крови, а также отдельных факторов свёртывания. Они незаменимы для возможного уточнения локализации патологии с точностью до фактора свёртывания. Для получения полной картины работы гемостаза у пациента врач должен иметь возможность выбирать, какой тест ему необходим.
Глобальные тесты:
«Локальные» тесты:
Все методы, измеряющие промежуток времени с момента добавления реагента (активатора, запускающего процесс свёртывания) до формирования фибринового сгустка в исследуемой плазме, относятся к клоттинговым методам (от англ. сlot — сгусток).
Нарушения свёртываемости крови могут быть обусловлены дефицитом одного или нескольких факторов свёртывания крови, появлением в циркулирующей крови их иммунных ингибиторов
Примеры нарушений свёртывания крови:
- ↑ Атауллаханов Ф. И., Зарницына В. И., Кондратович А. Ю., Лобанова Е. С., Сарбаш В. И. Особый класс автоволн — автоволны с остановкой — определяет пространственную динамику свертывания крови (рус.) // УФН : журнал. — 2002. — Т. 172, № 6. — С. 671—690. — ISSN 0042-1294. — DOI:10.3367/UFNr.0172.200206c.0671.
- ↑ Атауллаханов Ф. И., Лобанова Е. С., Морозова О. Л., Шноль Э. Э., Ермакова Е. А., Бутылин А. А., Заикин А. Н. Сложные режимы распространения возбуждения и самоорганизация в модели свертывания крови (рус.) // УФН : журнал. — 2007. — Т. 177, № 1. — С. 87—104. — ISSN 0042-1294. — DOI:10.3367/UFNr.0177.200701d.0087.
- ↑ 1 2 3 4 5 Кузник Б. И. 6.4 Система гемостаза // Физиология человека / Под редакцией В. М. Покровского, Г. Ф. Коротько. — М.: Медицина, 2000. — Т. 1. — С. 313—325. — 448 с. — 3000 экз. — ISBN 5-225-00960-3.
- ↑ Walsh P. N. Platelet-mediated coagulant protein interactions in hemostasis // Semin. Hematol. — 1985. — № 22 (3). — С. 178—186. — PMID 3898383.
- ↑ 1 2 3 Вайс Х., Елькманн В. Глава 18. Функции крови. Раздел 6. Остановка кровотечения и свёртывание крови // Физиология человека / Под редакцией Р. Шмидта и Г. Тевса. — М.: Мир, 1996. — Т. 2. — С. 431—439. — ISBN 5-03-002544-8.
- ↑ Коагуляционный гемостаз (неопр.). Дата обращения 15 ноября 2012. Архивировано 20 ноября 2012 года.
- ↑ Пантелеев М. А., Васильев С. А., Синауридзе Е. И., Воробьёв А. И., Атауллаханов Ф. И. Практическая коагулология / Под ред. А. И. Воробьёва. — М.: Практическая медицина, 2011. — 192 с. — ISBN 978-5-98811-165-8.
причины, симптомы, диагностика и лечение
Гемофилия – наследственная патология системы гемостаза, в основе которой лежит снижение или нарушение синтеза VIII, IX или XI факторов свертывания крови. Специфическим проявлением гемофилии служит склонность больного к различным кровотечениям: гемартрозам, внутримышечным и забрюшинным гематомам, гематурии, желудочно-кишечным кровотечениям, длительным кровотечениям при операциях и травмах и др. В диагностике гемофилии первостепенное значение имеет генетическое консультирование, определение уровня активности факторов свертываемости, ДНК-исследование, анализ коагулограммы. Лечение гемофилии предполагает проведение заместительной терапии: трансфузии гемоконцентратов с факторами свертывания VIII или IX, свежезамороженной плазмы, антигемофильного глобулина и др.
Общие сведения
Гемофилия – заболевание из группы наследственных коагулопатий, обусловленное дефицитом факторов свертывания плазмы крови и характеризующееся повышенной склонностью к геморрагиям. Распространенность гемофилии А и В составляет 1 случай на 10000-50000 представителей мужского пола. Чаще всего дебют заболевания приходится на ранний детский возраст, поэтому гемофилия у ребенка является актуальной проблемой педиатрии и детской гематологии. Кроме гемофилии, у детей встречаются и другие наследственные геморрагические диатезы: геморрагическая телеангиэктазия, тромбоцитопатия, болезнь Гланцмана т. п.
Гемофилия
Причины гемофилии
Гены, обусловливающие развитие гемофилии, сцеплены с половой Х-хромосомой, поэтому заболевание наследуется по рецессивному признаку по женской линии. Наследственной гемофилией болеют практически исключительно лица мужского пола. Женщины являются проводниками (кондукторами, носителями) гена гемофилии, передающими заболевание части своих сыновей.
У здорового мужчины и женщины-кондуктора с одинаковой вероятностью могут родиться как больные, так и здоровые сыновья. От брака мужчины, больного гемофилией со здоровой женщиной рождаются здоровые сыновья или дочери-кондукторы. Описаны единичные случаи гемофилии у девочек, рожденных от матери-носителя и больного гемофилией отца.
Врожденная гемофилия встречается почти у 70 % пациентов. В этом случае наследуется форма и тяжесть гемофилии. Около 30% наблюдений приходится на спорадические формы гемофилии, связанные с мутацией в локусе, кодирующем синтез плазменных факторов свертывания крови на Х-хромосоме. В дальнейшем такая спонтанная форма гемофилии становится наследственной.
Свертываемость крови, или гемостаз, служит важнейшей защитной реакцией организма. Активизация системы гемостаза происходит в случае повреждения сосудов и начала кровотечения. Свертываемость крови обеспечивается тромбоцитами и особыми веществами – плазменными факторами. При дефиците того или иного фактора свертывания своевременный и адекватный гемостаз становится невозможным. При гемофилии в связи с дефицитом VIII, IX или других факторов нарушается первая фаза свертывания крови — образование тромбопластина. При этом увеличивается время свертывания крови; иногда кровотечение не останавливается в течение нескольких часов.
Классификация гемофилии
В зависимости от дефицита того или иного фактора свертываемости крови, различают гемофилию А (классическую), В (болезнь Кристмаса), С и др.
- Классическая гемофилия составляет подавляющее большинство (около 85%) случаев синдрома и связана с дефицитом VIII фактора свертывания (антигемофильного глобулина), приводящим к нарушению образование активной тромбокиназы.
- При гемофилии В, составляющей 13% случаев заболевания, имеет место недостаток IX фактора (плазменного компонента тромбопластина, фактора Кристмаса), также участвующего в образовании активной тромбокиназы в I фазе свертывания крови.
- Гемофилия С встречается с частотой 1-2% и обусловлена недостаточностью XI фактора свертывания крови (предшественника тромбопластина). На остальные разновидности гемофилии приходится менее 0,5% случаев; при этом может отмечаться дефицит различных плазменных факторов: V (парагемофилия), VII (гипопроконвертинемия), Х (болезнь Стюарта – Прауэр) и др.
Тяжесть клинического течения гемофилии зависит от степени недостаточности коагуляционной активности плазменных факторов свертывания крови.
- При гемофилии тяжелой степени уровень недостающего фактора составляет до 1%, что сопровождается развитием тяжелого геморрагического синдрома уже в раннем детском возрасте. У ребенка с тяжелой гемофилией возникают частые спонтанные и посттравматические кровоизлияния в мышцы, суставы, внутренние органы. Сразу после рождения ребенка могут обнаруживаться кефалогематомы, длительные кровотечения из пуповинного отростка, мелена; позднее — продолжительные кровотечения, связанные с прорезыванием и сменой молочных зубов.
- При среднетяжелой степени гемофилии у ребенка уровень плазменного фактора составляет 1-5%. Заболевание развивается в дошкольном возрасте; геморрагический синдром выражен умеренно, отмечаются кровоизлияния в мышцы и суставы, гематурия. Обострения случаются 2-3 раза в год.
- Легкая форма гемофилии характеризуется уровнем фактора выше 5%. Дебют заболевания возникает в школьном возрасте, часто в связи с травмами или операциями. Кровотечения более редкие и менее интенсивные.
Симптомы гемофилии
У новорожденных детей признаками гемофилии могут служить длительное кровотечение из культи пуповины, подкожные гематомы, кефалогематомы. Кровотечения у детей первого года жизни могут быть связаны с прорезыванием зубов, оперативными вмешательствами (инцизией уздечки языка, циркумцизио). Острые края молочных зубов могут стать причиной прикусывания языка, губ, щек и кровотечений из слизистых оболочек полости рта. Однако в грудном возрасте гемофилия дебютирует редко в связи с тем, что материнском молоке содержится достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений значительно возрастает, когда ребенок с гемофилией начинает вставать и ходить. Для детей после года характерны носовые кровотечения, подкожные и межмышечные гематомы, кровоизлияния в крупные суставы. Обострения геморрагического диатеза случаются после перенесенных инфекций (ОРВИ, ветрянки, краснухи, кори, гриппа и др.) вследствие нарушения проницаемости сосудов. В этом случае нередко возникают самопроизвольные диапедезные геморрагии. Ввиду постоянных и длительных кровотечений у детей с гемофилией имеется анемия различной степени выраженности.
По степени убывания частоты кровоизлияния при гемофилии распределяются следующим образом: гемартрозы (70—80%), гематомы (10-20%), гематурия (14-20%), желудочно-кишечные кровотечения (8%), кровоизлияния в ЦНС (5%).
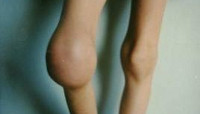
Гемартрозы являются наиболее частым и специфическим проявлением гемофилии. Первые внутрисуставные кровоизлияния у детей с гемофилией случаются в возрасте 1-8 лет после ушибов, травм или спонтанно. При гемартрозе выражен болевой синдром, отмечается увеличение сустава в объеме, гиперемия и гипертермия кожи над ним. Рецидивирующие гемартрозы приводят к развитию хронического синовита, деформирующего остеоартроза и контрактур. Деформирующий остеоартроз приводит к нарушению динамики опорно-двигательного аппарата в целом (искривлению позвоночника и таза, гипотрофии мышц, остеопорозу, вальгусной деформации стопы и др.) и к наступлению инвалидности уже в детском возрасте.
При гемофилии часто возникают кровоизлияния в мягкие ткани – подкожную клетчатку и мышцы. У детей обнаруживаются непроходящие синяки на туловище и конечностях, часто возникают глубокие межмышечные гематомы. Такие гематомы склонны к распространению, поскольку излившаяся кровь не сворачивается и, проникая вдоль фасций, инфильтрирует ткани. Обширные и напряженные гематомы могут сдавливать крупные артерии и периферические нервные стволы, вызывая интенсивные боли, паралич, атрофию мышц или гангрену.
Довольно часто при гемофилии возникают кровотечения из десен, носа, почек, органов ЖКТ. Кровотечение может быть инициировано любыми медицинскими манипуляциями (внутримышечной инъекцией, экстракцией зуба, тонзиллэктомией и др.). Крайне опасными для ребенка с гемофилией являются кровотечения из зева и носоглотки, поскольку могут привести к обструкции дыхательных путей и потребовать экстренной трахеостомии. Кровоизлияния в мозговые оболочки и головной мозг приводят к тяжелым поражениям ЦНС или летальному исходу.
Гематурия при гемофилии может возникать самопроизвольно или вследствие травм поясничной области. При этом отмечаются дизурические явления, при образовании кровяных сгустков в мочевыводящих путях — приступы почечной колики. У больных с гемофилией нередко обнаруживаются пиелоэктазия, гидронефроз, пиелонефрит.
Желудочно-кишечные кровотечения у пациентов с гемофилией могут быть связаны с приемом НПВС и др. лекарств, с обострением латентного течения язвенной болезни желудка и двенадцатиперстной кишки, эрозивным гастритом, геморроем. При кровоизлияниях в брыжейку и сальник развивается картина острого живота, требующая дифференциальной диагностики с острым аппендицитом, кишечной непроходимостью и др.
Характерным признаком гемофилии является отсроченный характер кровотечения, которое обычно развивается не сразу после травмы, а через некоторое время, иногда спустя 6-12 и более часов.
Диагностика гемофилии
Диагностика гемофилии проводится при участии ряда специалистов: неонатолога, педиатра, генетика, гематолога. При наличии у ребенка сопутствующей патологии или осложнений основного заболевания проводятся консультации детского гастроэнтеролога, детского травматолога-ортопеда, детского отоларинголога, детского невролога и др.
Супружеские пары, находящиеся в группе риска по рождению ребенка с гемофилией, должны пройти медико-генетическое консультирование еще на этапе планирования беременности. Выявить носительство дефектного гена позволяет анализ генеалогических данных и молекулярно-генетическое исследование. Возможно проведение пренатальной диагностики гемофилии с помощью биопсии хориона или амниоцентеза и исследования ДНК клеточного материала.
После рождения ребенка диагноз гемофилии подтверждается с помощью лабораторных исследований гемостаза. Основные изменения показателей коагулограммы при гемофилии представлены увеличением времени свертывания крови, АЧТВ, тромбинового времени, МНО, времени рекальцификации; уменьшением ПТИ и др. Решающее значение при диагностике формы гемофилии принадлежит определению снижения прокоагулянтной активности одного из факторов свертывания ниже 50%.
При гемартрозах ребенку с гемофилией проводится рентгенография суставов; при внутренних кровотечениях и забрюшинных гематомах – УЗИ брюшной полости и забрюшинного пространства; при гематурии – общий анализ мочи и УЗИ почек и т. д.
Лечение гемофилии
При гемофилии полное избавление от заболевания невозможно, поэтому основу лечения составляет заместительная гемостатическая терапия концентратами VIII и IX факторов свертывания крови. Необходимая доза концентрата определяется степенью выраженности гемофилии, тяжестью и видом кровотечения.
В лечении гемофилии выделяют два направления – профилактические и «по требованию», в период проявлений геморрагического синдрома. Профилактическое введение концентратов факторов свертывания крови показано пациентам с тяжелой формой гемофилии и проводится 2-3 раза в неделю для предупреждения развития гемофилической артропатии и прочих кровотечений. При развитии геморрагического синдрома требуются повторные трансфузии препарата. Дополнительно используются свежезамороженная плазма, эритромасса, гемостатики. Все инвазивные вмешательства у больных с гемофилией (наложение швов, удаление зубов, любые операции) проводятся под прикрытием гемостатической терапии.
При незначительных наружных кровотечениях (порезах, кровотечениях из полости носа и рта) может использоваться гемостатическая губка, наложение давящей повязки, обработка раны тромбином. При неосложненном кровоизлиянии ребенку необходим полный покой, холод, иммобилизация больного сустава гипсовой лонгетой, в дальнейшем – УВЧ, электрофорез, ЛФК, легкий массаж. Больным с гемофилией рекомендуется диета, обогащенная витаминами А, В, С, D, солями кальция и фосфора.
Прогноз и профилактика гемофилии
Длительная заместительная терапия приводит к изоиммунизации, образованию антител, блокирующих прокоагулянтную активность вводимых факторов, и неэффективности гемостатической терапии в обычных дозах. В таких случаях больному с гемофилией проводится плазмаферез, назначаются иммунодепрессанты. Поскольку больным с гемофилией проводится частое переливание компонентов крови, не исключается риск инфицирования ВИЧ-инфекцией, гепатитами В, С и D, герпесом, цитомегалией.
Легкая степень гемофилии не влияет на продолжительность жизни; при тяжелой гемофилии прогноз ухудшается при массивных кровотечениях, обусловленных операциями, травмами.
Профилактика предполагает проведение медико-генетического консультирования супружеских пар, имеющих отягощенный семейный анамнез по гемофилии. Дети, больные гемофилией, всегда должны иметь при себе специальный паспорт, где указан тип заболевания, группа крови и Rh-принадлежность. Им показан охранительный режим, профилактика травм; диспансерное наблюдение педиатра, гематолога, детского стоматолога и др. специалистов; наблюдение в условиях специализированного гемофильного центра.
Нарушение свертываемости крови
Некоторые люди ужасно боятся вида порезанного пальца, особенно собственного, — однако страх этот иррационален. Здоровый человек попросту не может истечь кровью через даже довольно крупные порезы, поскольку природа снабдила нас отличным механизмом свертывания крови. Но как понять, что свертывание ухудшилось?
Кто сворачивает кровь
Система гемостаза (остановки кровотечения) состоит из двух звеньев — сосудисто-тромбоцитарного и коагуляционного, он же плазменный.
Сосудисто-тромбоцитарное звено действует следующим образом: в момент ранения поврежденные клетки стенки сосуда выбрасывают ряд специальных веществ, которые активируют тромбоциты. В результате тромбоциты спутываются между собой, образуя рыхлую массу, и обретают способность к адгезии (прилипание к поврежденному месту сосуда) и агрегации (слипание в кучки). Так образуется первичный рыхлый тромб. Для капиллярного кровотечения (порезанный палец) его достаточно, но в крупных сосудах, где кровь движется с высокой скоростью, такую конструкцию просто «выбьет» напором.
Поэтому необходимо коагуляционное звено — это и есть собственно свертывание. Факторы свертывания (ФС) присутствуют в плазме крови постоянно, причем в таком количестве, что хватило бы практически на всю кровь разом (напрашивается сюжет для фильма ужасов). Но, как и тромбоциты, ФС находятся в неактивном состоянии, пока раненая сосудистая стенка не издаст свой биохимический «крик о помощи». После активации факторы свертывания образуют трехмерную сеть из фибрина, задача которой — укутать первичный тромб, укрепив его и крепко зафиксировав на поврежденном участке.
Нарушения в работе первого звена
Поскольку первое звено имеет два компонента, то и проблемы могут возникнуть с любым из них. Понижение свертываемости тромбоцитарного происхождения может иметь две причины: снижение числа тромбоцитов или их генетическая неполноценность. К кровоточивости приводит и повышенная ломкость сосудистой стенки (тоже, как правило, генетически обусловленная).

Любой из этих вариантов даст о себе знать легко возникающими синяками, которые берутся «неизвестно откуда», т. е. при таких легких ударах, которые человек даже не запоминает; также характерны частые носовые, десневые, у женщин — маточные кровотечения.
Читайте также:
Носовое кровотечение
Пробы, которые проводит врач при подозрении на поражение первого звена, настолько несложные, что часть из них можно выполнить самостоятельно. Например, щипковая проба: кожу под ключицей собирают в складку и делают щипок. Результат пробы оценивают через 24 часа — у здорового человека никаких видимых следов не останется.
Достаточно просты и лабораторные методы: это изучение количества тромбоцитов (составная часть общего анализа крови) и их формы, оценка времени кровотечения и вычисление индекса ретракции кровяного сгустка.
Нарушения в работе второго звена
Проблемы второго звена — это так называемые коагулопатии, т. е. генетическое отсутствие или недостаточная активность того или иного фактора свертывания. Коагуляционный каскад устроен как советская елочная гирлянда: если «ломается» какой-то один фактор, то «не горит» вся гирлянда, т. е. нарушается весь процесс.
Самым известным примером являются оба вида гемофилии — отсутствие в крови больного человека VIII или IX фактора. Как правило, это диагностируется еще в детстве, потому что очень сложно пропустить образование крупных гематом, беспричинное появление крови в моче, неостанавливающиеся кровотечения при травмах.
Для подтверждения диагноза используются тесты на время свертывания, тромбиновое время, активированное частичное тромбопластиновое время и прицельное исследование уровня того или иного ФС.
Нарушение коагуляции из-за лекарств

В отдельную группу стоит выделить пациентов, получающих пожизненную антикоагуляционную терапию — как правило, это варфарин. Список показаний для такого лечения очень широк — это различные тромбозы, профилактика осложнений после инфаркта миокарда, постоянная форма фибрилляции предсердий, протезированные клапаны сердца и многое другое.
Но с уменьшением способности крови к свертыванию увеличивается риск кровотечений. Именно поэтому жесткое условие успешного лечения антикоагулянтами — это регулярный контроль международного нормализованного отношения (МНО) крови. Это показатель одновременно и эффективности, и безопасности лечения. Если снизить свертываемость крови недостаточно — не будет эффекта; если перестараться — велик риск серьезных осложнений.
Контроль МНО должен проводиться как минимум раз в месяц. Сегодня существуют приборы для самостоятельного измерения МНО — они очень просты в обращении и позволяют гораздо лучше отслеживать свое состояние. На эффект варфарина влияют и другие лекарства, принимаемые одновременно с ним, и даже изменения в диете. Вы можете забыть упомянуть о них при посещении своего врача, но прибор поможет избежать последствий.
***
Так что если вас смущают синяки или частая кровь на зубной щетке — не стесняйтесь, расскажите об этом своему терапевту. А если вы точно знаете, что в вашу систему свертывания уже вмешались с помощью лекарств, то вам абсолютно необходимы регулярные проверки.
Будьте здоровы!
Лидия Куликова
Фото istockphoto.com
что это такое, болезнь, несвертываемость крови, у детей, лечение, клинические симптомы, причины, заболевание, больные, значит, новорожденных
Гемофилия — это тяжелое нарушение гемостаза, сопровождающееся снижением выработки факторов, отвечающих за свертывание крови. Патология является наследственной. Выраженные проявления возникают в детстве.

Несмотря на то что носителями патогенных генов выступают женщины, болеют преимущественно мужчины. У девочек гемофилия проявляется крайне редко и протекает в более легких формах. Это заболевание сопровождается частыми кровотечениями. Оно нередко приводит к ранней инвалидности больных и может становиться причиной летального исхода.
Причины
Когда речь идет о таком заболевании, как гемофилия, причины развития патологии уходят корнями в нарушения строения половой Х-хромосомы. Из-за этого болезнь передается рецессивно по женской линии. Наследственная разновидность этой патологии проявляется выраженной симптоматикой только у мальчиков. Женщины могут выступать кондукторами, т.е. носителями патологического гена. При этом сами они не болеют наследственной формой данного заболевания. Таким образом, причины гемофилии уходят корнями в передачу следующему поколению поврежденного гена.
Было зафиксировано всего несколько случаев рождения девочек, страдающих гемофилией в парах, где мужчина страдает гемофилией, а женщина является кондуктором. Однако вероятность такого исхода составляет менее 25%. Причина, почему крайне редко появляются на свет девочки, страдающие гемофилией, заключается в том, что для развития патологии у плода женского пола должны обе Х-хромосомы быть пораженными мутацией. Однако это невозможно.

Только по назначению лечащего врача 30%, 984 голоса
984 голоса 30%
984 голоса — 30% из всех голосов
Один раз в год и считаю этого достаточно 18%, 570 голосов
570 голосов 18%
570 голосов — 18% из всех голосов
Только когда болею 16%, 508 голосов
508 голосов 16%
508 голосов — 16% из всех голосов
Как минимум два раза в год 15%, 470 голосов
470 голосов 15%
470 голосов — 15% из всех голосов
Чаще чем два раза в год но меньше шести раз 11%, 354 голоса
354 голоса 11%
354 голоса — 11% из всех голосов
Я слежу за своим здоровьем и сдаю раз в месяц 6%, 204 голоса
204 голоса 6%
204 голоса — 6% из всех голосов
Боюсь эту процедуру и стараюсь не сдавать 4%, 143 голоса
143 голоса 4%
143 голоса — 4% из всех голосов
Всего голосов: 3233
21.10.2019
×
Вы или с вашего IP уже голосовали.В этом случае на 4 неделе беременности, когда у ребенка-девочки начинается выработка собственной крови, происходит выкидыш, т.к. такой плод является нежизнеспособным. У мальчиков присутствуют хромосомы Х и У. Таким образом, рецессивная хромосома Х, имеющая признаки мутации, может стать причиной появления выраженных симптомов данного заболевания.
На спорадические формы патологии, развивающиеся в результате спонтанных мутаций, приходится не более 30% случаев данного заболевания.
Классификация
Гемофилия — заболевание, которое может протекать в легкой, среднетяжелой и тяжелой форме. В первом случае уровень факторов достигает 5%. Клинические проявления появляются в школьном возрасте. Протекающее в этой форме расстройство почти не отражается на качестве жизни больного.
Болезнь гемофилия, протекающая в средней степени тяжести, сопровождается наличием 1-5% факторов. Из-за этого клинические симптомы возникают в 1-6 лет. При этом геморрагический синдром проявляется в умеренной форме. Нередко отмечаются примеси крови в моче. Обострения патологии наблюдаются 2-3 раза в год.
При тяжелой форме течения уровень факторов не превышает 1%. Это состояние проявляется тяжелым геморрагическим синдромом. Симптомы начинают возникать во младенчестве. В зависимости от недостаточности выработки тех или иных факторов выделяется гемофилия А, В и С типа.

Наиболее распространенной является гемофилия А типа. Она диагностируется примерно в 70% случаев. Данное расстройство характеризуется снижением выработки антигемофильного глобулина. Эта форма патологии сопряжена с нарушением формирования активной тромбокиназы.
Гемофилия В типа встречается не более чем в 13% случаев. Она сопровождается снижением выработки фактора Кристмаса и тромбопластина. Из-за данных изменений происходит нарушение формирования тромбокиназы на 1 фазе процесса свертывания гемолимфы.
Гемофилия С бывает выявлена не более чем в 2% случаев. Она обусловлена нарушением формирования предшественников тромбопластина.
Симптомы
Клинические симптомы, характерные для гемофилии, могут возникать как во младенчестве, так и в более позднем возрасте. Признаки заболевания могут проявляться в разной степени тяжести.
У мужчин
Симптомы гемофилии у мужчин, вызванные нарушением выработки факторов свертываемости, сохраняются с детского возраста. Учитывая, что болеют ею только мальчики, признаки патологии у взрослых мужчин выражены геморрагическим синдромом и осложнениями, вызванными кровотечениями во внутренние органы и суставы.
Мужчины, страдающие гемофилией с раннего детского возраста, в большинстве случаев отличаются низким ростом и сухопарым телосложением. Возможны нарушения подвижности суставов, в которые ранее не раз происходили кровоизлияния. При тяжелом течении возможны признаки кахексии. Данные нарушения нередко приводят к сокращению жизни пациентов даже при направленной терапии.
У женщин
У женщин гемофилия, симптомы которой проявились в выраженной форме, встречается крайне редко. Описано не более 60 случаев, т.к. для появления на свет такой девочки требуется стечение многих факторов. У женщин гемофилия проявляется той же симптоматикой, что и у мужчин.
У детей
Несвертываемость крови в большинстве случаев выражено проявляется у новорожденных, которые не находятся на грудном вскармливании. Гемофилия у детей, получающих грудное молоко, проявляется менее отчетливо. В молоке присутствуют все необходимые факторы свертывания. Могут присутствовать массированные кровотечения из пуповины. При легких надавливаниях появляются подкожные гематомы. Нередко гемофилия у новорожденных сопровождается кефалогематомами.

Обильные истечения крови у детей часто связаны с формированием молочного зубного ряда. Проявления несвертываемости крови усугубляются, когда ребенок учится ходить. Любые падения сопряжены с риском появления обширных гематом. У детей старше года на данное заболевание указывают частые носовые кровотечения.
Кроме того, с возрастом повышается риск развития кровоизлияний в мышцы и крупные составы. Обострения заболевания наблюдаются на фоне инфекций. Из-за частых случаев потери крови у детей развивается анемия, которая может быть выражена в различной степени тяжести. Нередко при этом заболевании развивается гематурия, т.е. появляются примести крови в моче. Кроме того, возможны кишечные кровотечения. В этом случае кровь будет определяться в кале.
Кровотечения внутрь суставов у детей от 1 до 8 лет могут носить спонтанный характер или быть результатом травмы. При кровоизлиянии в полость сустава появляются следующие симптомы:
- интенсивный болевой синдром;
- покраснение кожных покровов над суставом;
- повышение температуры кожи;
- увеличение сустава в размере.
В дальнейшем нарастает деформация сочленения и происходит развитие хронической формы синовита. Деформирующий остеоартроз провоцирует нарушение формирования всего опорно-двигательного аппарата у ребенка. Нередко это состояние провоцирует атрофию мышц, искривление тазовых костей и позвоночника, вальгусную деформацию стоп и т.д. Возможно появление остеопороза и формирование стойких контрактур. Это приводит к тому, что тяжелая инвалидность наступает в детском возрасте.
Диагностика
Сейчас существует возможность раннего выявления патологии у плода еще во время беременности. Парам, находящимся в группе риска рождения ребенка с гемофилией, рекомендовано прохождение медико-генетического консультирования еще в период подготовки к беременности. Для определения наличия патологии у плода проводится биопсия хориона и амниоцентез.
При появлении признаков развития данного нарушения ребенку требуется консультация неонатолога, гематолога и генетика. Комплексное обследование позволяет спрогнозировать течение заболевания. Кроме внешнего осмотра и определения протромбинового времени, назначается ряд специфичных исследований, в т.ч.:
- коагулограмма;
- АЧТВ;
- МНО.
Выполняются анализы для выявления прокоагулянтной активности фактора свертывания крови. Если данный показатель ниже 50%, это значит, что у ребенка гемофилия. Чтобы определить, есть или нет у пациента осложнения, назначается рентгенография суставов. Кроме того, часто выполняется УЗИ брюшной полости и почек.
Лечение
Это генетическое заболевание не лечится, но при правильном подходе к терапии удается добиться стабилизации состояния и снизить риск развития кровотечений. Лечение гемофилии у детей предполагает назначение пациентам гемостатических препаратов. Введение концентратов недостающих факторов позволяет компенсировать имеющийся дефицит. При таком заболевании, как гемофилия, лечение гемостатическими средствами подбирается пациентам индивидуально с учетом степени тяжести проявлений патологии и частоты возникновения кровотечений.
При тяжелом течении заболевания препараты концентратов факторов вводятся 2-3 раза в неделю для профилактики развития геморрагических осложнений. При легком течении данные лекарственные средства вводятся только при наличии признаков кровотечений.

Может требоваться и симптоматическая терапия. При легких наружных кровотечениях, возникших при небольших порезах или нарушении целостности сосудов в носу, рекомендуется использование гемостатической губки. При развитии внутрисуставного кровотечения требуется наложение гипсовой лонгеты. В дальнейшем назначаются физиопроцедуры, массаж и ЛФК. Людям, страдающим гемофилией, необходимы прием витаминных комплексов и специальная диета.
Возможные осложнения и прогноз на выздоровление
Больные гемофилией часто погибают из-за развития осложнений. Нередко наблюдаются нарушения работы почек. На фоне данного гематологического заболевания часто развиваются язва желудка или кишечника, а также геморрой и эрозивный гастрит. Поврежденные участки органов ЖКТ могут сильно кровоточить. Массированные кровотечения могут становиться причиной летального исхода.
Пропитывание мышечных тканей гемолимфой нередко приводит к гангрене. Кроме того, такие кровотечения могут становиться причиной передавливания нервных стволов и развития паралича или интенсивного болевого синдрома.

К наиболее опасным осложнениям данного гематологического заболевания относится внутримозговое кровотечение. Пропитывание мозговых оболочек кровью может привести к летальному исходу. Даже если пациент выживает, у него остаются тяжелые неврологические нарушения, которые почти не поддаются коррекции. Кровоизлияния в позвоночный канал могут приводить к нарушению работы спинного мозга. Последствия такой катастрофы зависят от объема вытекшей крови и расположения поврежденного участка.
Терапия приводит к тому, что в организме больного начинают вырабатываться особые антитела, которые блокируют активность введенных факторов. Это делает лечение малоэффективным. В этом случае требуется прием иммунодепрессантов. Кроме того, частое переливание факторов повышает риск заражения вирусными гепатитами, ВИЧ и другими инфекциями.
Прогноз заболевания зависит от тяжести его течения. При легкой форме патологии пациенты могут вести полноценный образ жизни. В этом случае болезнь не будет сказываться на продолжительности жизни и ее качестве. Средняя продолжительность жизни пациентов с тяжелой формой патологии составляет 14-16 лет.
Профилактика
Женщинам, имеющим в семейном анамнезе случаи развития гемофилии, требуется планировать беременность, пройдя со своим партнером все необходимые исследования. При появлении на свет больного ребенка нужно направить усилия на недопущение развития осложнений. Обязательна постановка больного на диспансерный учет. Пациентам с гемофилией необходимо придерживаться здорового образа жизни и соблюдать все рекомендации врача.
Больным требуются щадящая ЛФК и занятия плаваньем. Ребенок, страдающий этим заболеванием, должен быть освобожден от физкультуры в учебных учреждениях и прививок. С раннего детства пациент должен знать об опасности травм и кровотечений. Родственникам больного нужно знать все о гемофилии и специфике оказания первой помощи в случае кровотечения.
Несвертываемость крови Википедия
 Система для инъекций с раствором фактора VIII, способствующего свёртываемости крови; пригодна для самостоятельного введения препарата
Система для инъекций с раствором фактора VIII, способствующего свёртываемости крови; пригодна для самостоятельного введения препарата 

Гемофили́я (от др.-греч. αἷμα — «кровь» и др.-греч. φιλία, здесь — «склонность»[1]) — редкое наследственное заболевание, связанное с нарушением коагуляции (процессом свёртывания крови). При этом заболевании возникают кровоизлияния в суставы, мышцы и внутренние органы, как спонтанные, так и в результате травмы или хирургического вмешательства. При гемофилии резко возрастает опасность гибели пациента от кровоизлияния в мозг и другие жизненно важные органы, даже при незначительной травме. Больные с тяжёлой формой гемофилии подвергаются инвалидизации вследствие частых кровоизлияний в суставы (гемартрозы) и мышечные ткани (гематомы). Гемофилия относится к геморрагическим диатезам, обусловленным нарушением плазменного звена гемостаза (коагулопатия).
Гемофилия появляется из-за изменения одного гена в хромосоме X. Различают три типа гемофилии (A, B, C).
- Гемофилия A (рецессивная мутация в X-хромосоме) вызывает недостаточность в крови необходимого белка — так называемого фактора VIII (антигемофильного глобулина). Такая гемофилия считается классической, она встречается наиболее часто, у 80—90 %[1] больных гемофилией. Тяжёлые кровотечения при травмах и операциях наблюдаются при уровне VIII фактора — 5—20 %.
- Гемофилия B (рецессивная мутация в X-хромосоме) — недостаточность фактора плазмы IX (Кристмаса). Нарушено образование вторичной коагуляционной пробки.
- Гемофилия C (аутосомный рецессивный либо доминантный (с неполной пенетрантностью) тип наследования, то есть встречается как у мужчин, так и у женщин) — недостаточность фактора крови XI, известна в основном у евреев-ашкеназов. В настоящее время гемофилия С исключена из классификации, так как её клинические проявления значительно отличаются от А и В.

 Читайте также:
Читайте также: