Глиоз у ребенка — Неврология — 2.04.2018
анонимно, Мужчина, 5 лет
сыну 5 лет. особых жалоб и отклонений не наблюдается, очень живой, подвижный, развитый для своего возраста, в садике хвалят. 2 года наблюдаются единичные (1-2 раза в год) эпизоды с ухудшением самочувствия в виде светобоязни и тошноты, при этом нет ни температуры, ни инфекции. После сна все проходит. Обращались к невропатологу, получили направления к аллергологу и к окулисту — аномалий не нашли, как то забылось. В этом месяце после перенесенного ОРВИ было два небольших носовых кровотечения. Обратились к неврологу, получили направления на рэг головы и мрт. На рэг головы выявили ослабление венозного оттока во всех бассейнах, подозрение на гипертензию. На мрт написано следующее: в перивентрикулярном и в субкортикальном белом веществе лобных, теменных долей выявляются единичные мелкие очаги глиоза (гиперинтенсивные на Т2 ВИ и FLAIR IP) размерами 1,5-3 мм без перифокальной инфильтрации. Изменения мр сигнала в базальных ядрах, внутренней капсуле и в мозолистом теле не поределяются.
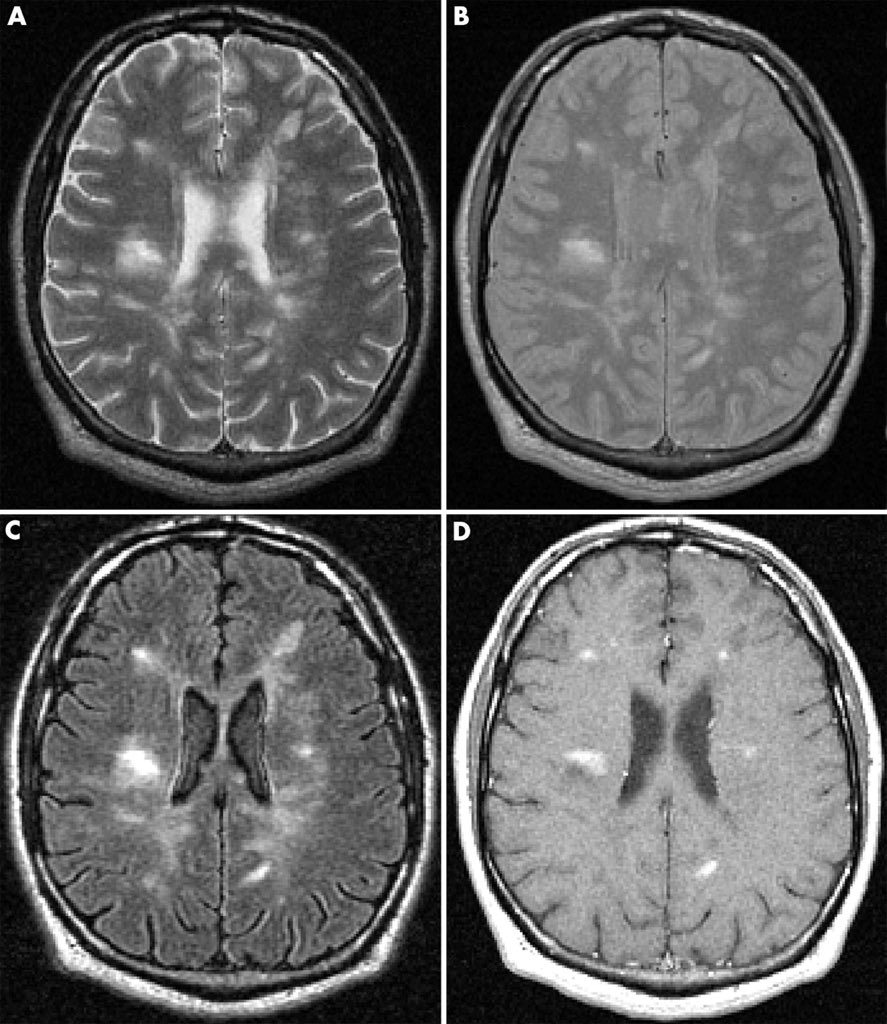
Повреждение головного мозга у злоупотребляющих алкоголем продолжает прогрессировать в течение 6 недель после прекращения употребления алкоголя
В журнале JAMA Psychiatry опубликованы результаты работы, посвященной оценке повреждения головного мозга у лиц, употребляющих алкоголь в больших количествах.
В исследование был включен 91 пациент; все они были госпитализированы с целью проведения дезинтоксикационной терапии в связи с предшествующим длительным употреблением больших доз алкоголя. Стационарный режим исключал возможность дальнейшего употребления алкоголя.
На момент госпитализации и в течение периода наблюдения повторно проводилась диффузионно-тензорная МРТ головного мозга. Метод позволяет производить прижизненную оценку микроструктуры белого вещества головного мозга (основываясь на характеристиках диффузии молекул воды в белом веществе).
Были продемонстрированы достоверные различия по числу микроповреждений белого вещества головного мозга у лиц, злоупотребляющих алкоголем, и здоровыми добровольцами. Большая часть подобных повреждений локализовалась в мозолистом теле, а также в своде головного мозга и бахромках гиппокампа. Повреждения также заметно чаще затрагивали правое полушарие ГМ, а также лобные доли. Аналогичные изменения выявлялись и у крыс, которым давался алкоголь в течение 30 дней. Степень повреждения белого вещества головного мозга напрямую зависела от количества алкоголя, употребляемого незадолго до исследования (и не зависела от иных клинических факторов).
Неожиданностью для исследователей стало то обстоятельство, что степень повреждения белого вещества продолжала нарастать уже после прекращения приема алкоголя еще в течение 2-6 недель. Математическое моделирование позволило предположить, что это связано как с продолжающейся демиелинизацией, так и с поражением аксонов.
Безусловно, столь выраженный резидуальный нейротоксический эффект алкоголя — еще один аргумент в пользу отказа от употребления больших доз алкогольных напитков.
По материалам:
De Santis S, Bach P, Pérez-Cervera L, et al. Microstructural White Matter Alterations in Men With Alcohol Use Disorder and Rats With Excessive Alcohol Consumption During Early
Abstinence. JAMA Psychiatry.Published online April 03, 2019. doi:10.1001/jamapsychiatry.2019.0318
https://www.medscape.com/
Текст: к.м.н. Шахматова О.О.
(PDF) Brain biopsy for diagnosis of chlamydia encephalitis
Клинический случай
ЖУРНАЛ ИНФЕКТОЛОГИИ Том 9, № 2, 2017 127
др. ] // Вестн. Рос. Воен.-мед. акад. – 2006. – № 1(15). – С.
] // Вестн. Рос. Воен.-мед. акад. – 2006. – № 1(15). – С.
42–48.
5. Almen L. (ed.). Barron Microbiology of Chlamydia.
Florida: CRC Press; 1988. р. 72–91.
6. Михайленко, А.А. Патология периферической нерв-
ной системы хламидийной природы / А.А. Михайленко [и
др.] // Неврол. вестн. им. В.М. Бехтерева. – 1996. – Т. 28,
№ 1-2. – С. 5-8.
7. Цинзерлинг, В.А. Инфекционные поражения нервной
системы: вопросы этиологии, патогенеза и диагностики: 2
изд. испр., доп. Руководство для врачей / В.А. Цинзерлинг,
М.Л. Чухловина. – СПб.: Элби, 2011. –583 с.
8. Одинак, М.М. Случай изолированной лимфомы го-
ловного мозга на фоне лейкоэнцефалита / М.М. Одинак
[и др.] // Нейроиммунология. – 2006. – Т.4, № 1–2. – С.
66–69.
9. Stratton C.W., Wheldon D.B. Multiple sclerosis: an infec-
tious syndrome involving Chlamydophila pneumonia. Trends.
Microbiol. 2006; 14(11): 474-479.
10. Fainardi E., et al. Under the microscope: focus on Chla-
mydia pneumoniae infection and multiple sclerosis. Curr. Neu-
rovasc. Res. 2008; 5(1):60-70.
11. Wagner A.D., Gerard H.C., Fresemann T. Detection of
Chlamydia pneumoniae in giant cell vasculitis and correlation
with the topographic arrangement of tissue-infiltrating dentrit-
ic cells. Arthrit. Rheum. 2000; 43(7):1543-1551.
12. Wohlschlaeger J., Wimmer M.L., Nagler D.K., et al.
Identification of Chlamydia pneumoniae in intracranial and ex-
tracranial arteries in patients with stroke and in controls: com-
bined immunohistochemical and polymerase chain reaction
analyses. Hum. Pathol. 2005; 36(4):395-402.
13. Серопегин, А.Д. Хламидийные поражения нервной
системы / А.Д. Серопегин [и др.] // Воен. – мед. журн. –
2006. – № 11. – С. 36–41.
14. Stratton C.W., Sriram S. Association of Chlamydia pneu-
moniae with central nervous system disease. Microbes. Infect.
Microbes. Infect.
2003; 5(13):1249-1253.
15. Grayston J.T., et al. Infection with Chlamydia pneu-
moniae as a cause of coronary heart disease: the hypothesis is
still untested. Patholog. Dis. 2015; 73(1):1-9.
16. Gieffers J., et al. Failure to detect Chlamydia pneumoni-
ae in brain sections of Alzheimer’s disease patients. J. Clin. Mi-
crobiol. 2000; (38):881-882.
17. Серопегин, А.Д. Неврологические аспекты хлами-
дийной инфекции: автореф. дис. … канд. мед. наук. / А.Д.
Серопегин. – СПб.: ВМедА, 1995. – 20 с.
18. Robertson D.K., et al. Inclusion biogenesis and reacti-
vation of persistent Chlamydia trachomatis requires host cell
sphingolipid biosynthesis. PLoS. Pathol. 2009. 5(11). Available
from: e1000664. doi: 10.1371/journal.ppat.1000664
19. Fukano H. Comparison of five PCR assays for detect-
ing Chlamydia pneumoniae DNA. Microbiol. Immunol. 2004;
48(1):441-448.
20. Меркулов, Г.А. Курс патологогистологической тех-
ники / Г.А. Меркулов. – Л.: Медицина, 1969. – 424 с.
21. Миронов, А.А. Методы электронной микроскопии в
биологии и медицине / А.А. Миронов, Я.Ю. Комиссарчик,
В.А. Миронов. – СПб.: Наука, 1994. – 400 с.
References
1. Vaynshenker, Yu.I. Khlamidioz tsentral’noy nervnoy
sistemy. Laboratornaya diagnostika i kliniko-morfologicheskie
osobennosti / Yu.I. Vaynshenker [i dr.] // Arkhiv patologii. –
2014. – T. 76, № 1. – S. 57-62.
2. Lobzin, Yu.V. Khlamidiynye infektsii: Rukovodstvo dlya
vrachey / Yu.V. Lobzin. – SPb.: OOO «Izd-vo FOLIANT»,
2003. – 399 s.
Таким образом, нами были учтены различные
инфекционные ассоциации, однако лишь санация
ЦНС от хламидий, обнаруженных при иммуноги-
стохимическом и электронно-микроскопическом
исследованиях, сопровождалась полной нормали-
зацией клинического состояния пациентки.
Заключение
Хроническая хламидийная инфекция в ЦНС
имеет ряд клинических особенностей, а также со-
провождается появлением в ликворе и сыворотке
крови таких маркеров иммунологически-опосре-
дованного демиелинизирующего поражения ЦНС,
как олигоклональные IgG и свободные легкие цепи
[3, 7, 17, 19]. В представленном клиническом слу-
чае при иммунологическом исследовании ликвора
были повышены свободные каппа- и лямбда-цепи
Ig, олигоклональный IgG в ликворе и сыворотке не
обнаружен, результат исследования ликвора мето-
дом ПЦР на хламидийную инфекцию был отрица-
тельным. Аналогичные результаты были получены
и в других работах [3, 17]. Ch. Trachomatis также
проявляла способность проникать в олигоден-
дроциты и репродуцироваться в астроглиальных
клетках головного мозга крыс [4]. В нашем иссле-
довании наличие хламидий в биоптате головного
мозга было установлено электронномикроскопи-
чески, что подтверждается полученными ранее
результатами экспериментальных исследований
[4, 8]. Важно отметить, что проведенная нами им-
Важно отметить, что проведенная нами им-
муногистохимическая реакция с антителами к Ch.
Trachomatis оказалась положительной, и это позво-
ляет с высокой степенью достоверности считать
диагноз энцефалита, ассоциированного с данным
видом хламидии, верифицированным. В связи с
этим выполненное этиопатогенетическое лечение
оказалось успешным.
Таким образом, комплексное изучение па-
тогенеза хронической хламидийной инфекции
нервной системы должно включать определение
клинических, лабораторных, нейровизуализаци-
онных паттернов в сочетании с иммуногистохими-
ческим и электронномикроскопическим исследо-
ваниями биопсийного материала.
Литература
1. Вайншенкер, Ю.И. Хламидиоз центральной нервной
системы. Лабораторная диагностика и клинико-морфоло-
гические особенности / Ю.И. Вайншенкер [и др.] // Архив
патологии. – 2014. – Т. 76, № 1. – С. 57–62.
2. Лобзин, Ю.В. Хламидийные инфекции: Руководство
для врачей / Ю.В. Лобзин. – СПб.: ООО «Изд-во ФОЛИ-
АНТ», 2003. – 399 с.
3. Мудрицкий, В.М. Клинико-лабораторная диагности-
ка менингитов и менингоэнцефалитов у больных, инфици-
рованных хламидиями : автореф. дис. … канд. мед. наук. /
В.М. Мудрицкий. – СПб.: ВМедА, 2002. – 22 с.
4. Одинак, М.М. Патология нервной системы при экс-
периментальной хламидийной инфекции / М.М. Одинак [и
Очаги Глиоза На Мрт

Очаговые изменения белого вещества головного мозга. МРТ диагностика
Глиоз — это итог восстановительных процессов нервной системы, суть которых заключается в заполнении свободного пространства, появившегося после гибели нейронов, глией — опорной тканью ЦНС. Они относятся к верхним отделам мозга в отличие от субтенториальных, включающих мозжечок и мозговой ствол. Расположенная над намётом затылочная доля страдает чаще всего при ушибах головы, родовых травмах из-за того, что со всех сторон окружена несжимаемой при ударе жидкостью ликворных пространств. В этой доле чаще всего возникают не связанные с травмами разрастания глии, имеющие сосудистый генез. Клиническая картина заболевания коррелирует с числом погибших нейронов и размером очага.youtube.com/embed/qoqgsxVImGY» frameborder=»0″ allowfullscreen=»»/>
Очаги глиоза в белом веществе головного мозга
Для быстрой передачи нервных импульсов от человеческого мозга к мышечным тканям и обратно, в тканях центральной нервной системы расположено огромное количество нейронов. В их функцию входит генерация и передача сигналов. Поддерживают и обеспечивают нормальную работу нейронов, расположенные в головном мозге глиальные клетки. Большинство специалистов неврологов сходятся во мнении, что глиозные изменения головного мозга не являются отдельным заболеванием, а скорее следствием других патологических изменений.
В статье обсуждаем глиоз головного мозга. Рассказываем о его видах, причинах образования, симптомах и диагностике.
Головной мозг человека представляет собой уникальную структуру, работа которой обеспечивает слаженное функционирование и единство всех внутренних систем.
Множественные супратенториальные очаги глиоза сосудистого генеза
Начнем с того, что многие специалисты, изучающие структуру нервной системы и ее патологии, уверены, что глиоз мозга — не самостоятельная болезнь. Она всегда вызвана серьезными нарушениями, которые возникли ранее. Из каких клеток построена нервная система? В нее входят не только нейроны нейроциты , но и другие элементы. Каждый из них имеет свое предназначение, например, нейроглия отвечает за метаболизм в других клетках и защищает нейроны.
youtube.com/embed/SLqHvnMX4rc» frameborder=»0″ allowfullscreen=»»/>
Очаги глиоза на мрт
Глиоз головного мозга: симптомы, лечение
Глиоз головного мозга — это процесс, который запускают ткани мозга, реагируя на разнообразные клеточные повреждения. Глиоз не является отдельной болезнью, он являет собой патологический процесс, который начинается после перенесенного заболевания мозга. Глиальные клетки замещают отмершие нейроны. Очаг глиоза в головном мозге не может заменить нормальную структуру мозговой ткани, в результате чего нарушается ее функция. Глиозные очаги — это патологическое разрастание глиальных клеток, которые замещают собой поврежденные погибшие нейроны. Группа таких клеток напоминает рубец или шрам на поверхности головного мозга, то есть этот участок ткани отличается от окружающей, как и шрамы на теле. Такой рубец не может справляться с возложенными на нее функциями, как другая мозговая ткань.
Глиальные клетки замещают отмершие нейроны. Очаг глиоза в головном мозге не может заменить нормальную структуру мозговой ткани, в результате чего нарушается ее функция. Глиозные очаги — это патологическое разрастание глиальных клеток, которые замещают собой поврежденные погибшие нейроны. Группа таких клеток напоминает рубец или шрам на поверхности головного мозга, то есть этот участок ткани отличается от окружающей, как и шрамы на теле. Такой рубец не может справляться с возложенными на нее функциями, как другая мозговая ткань.
Нервная система человека оснащена огромным объемом нейронов, их основная функция — это транспортирование импульсов и сигналов к мышцам и тканям. Полноценную работоспособность нейронов в головном мозге обеспечивают глиальные клетки.
Глиозные изменения?
Глиоз не является самостоятельным заболеванием.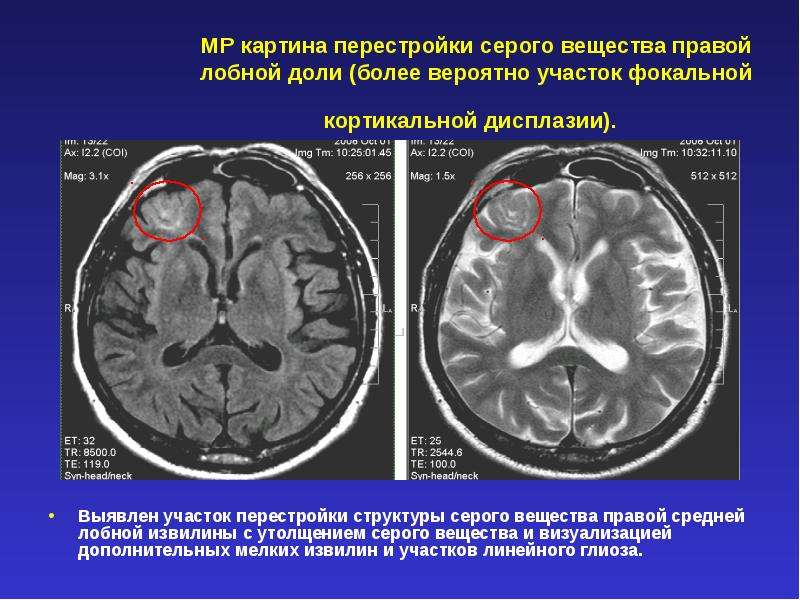 Суть его в изменении нормальных морфологических свойств вещества головного мозга. Таким образом, глиоз головного мозга является симптомом, возникающим при некоторых неврологических заболеваниях. При глиозе часть вещества головного мозга, подвергшегося атрофии при определенных обстоятельствах, замещается клетками особой соединительной ткани. Этот процесс можно сравнить с рубцеванием кожных повреждений — на месте глубокой раны появляется грубый рубец из соединительной ткани. То же наблюдается и в головном мозге при глиозе.
Суть его в изменении нормальных морфологических свойств вещества головного мозга. Таким образом, глиоз головного мозга является симптомом, возникающим при некоторых неврологических заболеваниях. При глиозе часть вещества головного мозга, подвергшегося атрофии при определенных обстоятельствах, замещается клетками особой соединительной ткани. Этот процесс можно сравнить с рубцеванием кожных повреждений — на месте глубокой раны появляется грубый рубец из соединительной ткани. То же наблюдается и в головном мозге при глиозе.
Глиоз клеток головного мозга — это вторичное состояние, провоцирующее патологию, при которой погибают клетки нервных волокон — нейроны. После гибели нейронов пустоты замещаются глиями. До того момента, пока в структуре клеток не происходит патологических процессов изменения, количество в мозге глии, не влияет на работоспособность всех мозговых функций. Нейроглия в мозгу выполняет определённые функции, которые становятся защитой клеток мозга от влияния на них инфекций, а также служат защитным балластом при травмировании головного мозга. Чем большее количество глии в здоровом мозге, тем мозговые органы лучше выполняют свои функциональные обязанности. Глиоз клеток мозга — это защита организма на повреждение волокон нервной системы. Когда происходит разрушение и гибель нейронов, клетки глии занимают их место и полностью стараются заменить нейроны по всем их функциям.
Нейроглия в мозгу выполняет определённые функции, которые становятся защитой клеток мозга от влияния на них инфекций, а также служат защитным балластом при травмировании головного мозга. Чем большее количество глии в здоровом мозге, тем мозговые органы лучше выполняют свои функциональные обязанности. Глиоз клеток мозга — это защита организма на повреждение волокон нервной системы. Когда происходит разрушение и гибель нейронов, клетки глии занимают их место и полностью стараются заменить нейроны по всем их функциям.
Вопрос от: Ирина — Клиника Здоровье 365 г. Екатеринбург
Вопрос Нейрохирургу
Вопрос от Ирина
Вопрос: 22 января 2009 года проведена операция «КПТЧ» по поводу тотального удаления объёмного образования (4.5*3.9*4.2 см) менингоматозная менингиома первой степени основания средней черепной ямки справа.Заключение МРТ от 17 августа 2010 года ,картина последствий КПТЧ с наличением постоперационных кистозно-глиозных атрофических изменений в области полюса височной,латеробазальных отделов лобнойи верхне-латеральных отделах теменной доли справа . Убедительных данных за рецедив опухоли на момент исследования не получено. Единичные очаговые изменения дистрофического (дисциркуляторного) характера.Арахноидальные изменения ликворокистозного характера.Риносинусопатия. Из исследовательской части следует ,что в зоне операционного вмешательства,в области передних отделах полюса височной и латеробазальных отделах лобных долей,проективно Сильвиевой щели справа ,определяется зона неправильной формы,общими приблизительными размерами до 4.5*3.9*4.2 см,имеющий неоднородно гиперинтенсивный сигнал по Т2 ВИ tirm,неоднородно гипоинтенсивный по Т1 ВИ,без признаков масс эффекта и перифокального отека -зона постоперационных кистозно-глиозных отрофических изменений .
Убедительных данных за рецедив опухоли на момент исследования не получено. Единичные очаговые изменения дистрофического (дисциркуляторного) характера.Арахноидальные изменения ликворокистозного характера.Риносинусопатия. Из исследовательской части следует ,что в зоне операционного вмешательства,в области передних отделах полюса височной и латеробазальных отделах лобных долей,проективно Сильвиевой щели справа ,определяется зона неправильной формы,общими приблизительными размерами до 4.5*3.9*4.2 см,имеющий неоднородно гиперинтенсивный сигнал по Т2 ВИ tirm,неоднородно гипоинтенсивный по Т1 ВИ,без признаков масс эффекта и перифокального отека -зона постоперационных кистозно-глиозных отрофических изменений .
В верхне-латеральных отделах правой теменной доли проективно костному дефекту,субкортикально,визуализируется небольшая зона глиозно-атрофических изменений,размерамидо 0,8*0,5 см. После введения контрастного вещества участков патологического изменения интенсивности сигнала убедительно не выявлено. Боковые желудочки мозга обычных размеров,несколько ассеметричны(D>S) с незначительными зонами глиозапо периферии ,в области передних и задних рогов.Субарахноидальные пространства вне зоны операционного доступа единично локально неравномерно расширенны преимущественно в области теменных долей.В белом веществе лобных долей определяются единичные мелкие очаги глиоза дистрофического характера,размером до 0.5 см,без перифакальных изменений.
Боковые желудочки мозга обычных размеров,несколько ассеметричны(D>S) с незначительными зонами глиозапо периферии ,в области передних и задних рогов.Субарахноидальные пространства вне зоны операционного доступа единично локально неравномерно расширенны преимущественно в области теменных долей.В белом веществе лобных долей определяются единичные мелкие очаги глиоза дистрофического характера,размером до 0.5 см,без перифакальных изменений.
В настоящее время у меня стало держаться давление диастолическое 140-160. Для меня это тяжело. Неустойчивость походки. Мне в октябре этого года(в данное время) сделали 8 капельниц винпоцетина,5 актовегина (струйно) , 7 сибазона (струйно) ,2 ниргоцелина( струйно) ,витамины В12 ставят в руку,ещё сегодня сделали блокаду в шею,(позвоночные артерии). Но я чувствую себя очень слабо,давление держится 140,утрами до 150.(при рабочем 120). Хотя гипертония у меня с подросткового возраста,но после операции это давление для меня высокое . Слабость сильная ,в руках,ногах. Аритмия . Тремор. (Хотя сахар в норме 3,9).Тяжесть в голове остается. Какое-то как внутреннее дрожание. Пролечилась полмесяца,а сил нет. Посоветуйте,пожалуйста, можно ли делать блокаду после такой операции и проводить лечение такими аппаратами?
Аритмия . Тремор. (Хотя сахар в норме 3,9).Тяжесть в голове остается. Какое-то как внутреннее дрожание. Пролечилась полмесяца,а сил нет. Посоветуйте,пожалуйста, можно ли делать блокаду после такой операции и проводить лечение такими аппаратами?
Ответ:
Здравствуйте, Ирина.
Невозможно заочно ответить на Ваши вопросы. Пожалуйста, смотрите правила онлайн консультации.
С уважением,
администрация
Назад
Болезнь белого вещества как биомаркер долгосрочных цереброваскулярных заболеваний и деменции
Варианты лечения Curr Cardiovasc Med. Авторская рукопись; доступно в PMC 2015 1 марта.
Опубликован в окончательной отредактированной форме как:
PMCID: PMC3964019
NIHMSID: NIHMS563166
, M.D., MSc. 1 and, MD, MPH 2Aurauma Chutinet
1 Отделение неврологии, Медицинский факультет, Университет Чулалонгкорна, Мемориальная больница Короля Чулалонгкорна, Красный Крест Таиланда, 1873, Рама IV Роуд, Бангкок , 10330 Таиланд
Наталья С.
 Rost
Rost2 J. Philip Kistler Stroke Research Center, Отдел неврологии, Массачусетская больница общего профиля, Гарвардская медицинская школа, 175 Cambridge Street, Suite 300, Boston, MA 02114 USA
1 Отделение неврологии, Департамент медицины , Медицинский факультет, Университет Чулалонгкорна, Мемориальная больница Короля Чулалонгкорна, Тайский Красный Крест, 1873, Рама IV Роуд, Бангкок, 10330 Таиланд
2 Центр исследования инсульта Дж. Филипа Кистлера, Отделение неврологии, Массачусетская больница общего профиля, Гарвардский медицинский центр School, 175 Cambridge Street, Suite 300, Boston, MA 02114 USA
Переписка и оттиски: Наталья С.Рост, доктор медицины, магистр здравоохранения, Центр исследования инсульта Дж. Филипа Кистлера, Центр генетических исследований человека, Массачусетская больница общего профиля, 175 Кембридж-стрит, офис 300, Бостон, Массачусетс, США 02114, США, тел .: (617) 643-3877 Факс: (617) 726-3939, gro. srentrap@tsorn Aurauma Chutinet, MD, MSc , 1873 Rama IV Road, Bangkok, 10330 Thailand., Тел .: (66) 81 256-4655, факс: (66) 81 256-4655, moc.oohay@amuarua Natalia S Rost, MD, MPH , 175 Cambridge Street, Suite 300, Boston MA 02114 USA, тел .: (617) 643-3877, факс: (617) 726-3939, gro .srentrap @ tsorn См. другие статьи в PMC, в которых цитируется опубликованная статья.
srentrap@tsorn Aurauma Chutinet, MD, MSc , 1873 Rama IV Road, Bangkok, 10330 Thailand., Тел .: (66) 81 256-4655, факс: (66) 81 256-4655, moc.oohay@amuarua Natalia S Rost, MD, MPH , 175 Cambridge Street, Suite 300, Boston MA 02114 USA, тел .: (617) 643-3877, факс: (617) 726-3939, gro .srentrap @ tsorn См. другие статьи в PMC, в которых цитируется опубликованная статья.Мнение
Болезнь белого вещества обычно выявляется на МРТ головного мозга у пожилых людей как гиперинтенсивность белого вещества (ГВН) или «лейкоареоз». С годами становится все более очевидным, что наличие и степень ВМГ является рентгенологическим маркером заболевания мелких сосудов головного мозга и важным предиктором пожизненного риска инсульта, когнитивных нарушений и функциональной инвалидности. В ряде крупных популяционных исследований подчеркивается значение ВМГ как биомаркера долгосрочных цереброваскулярных заболеваний и деменции, и в этом обзоре мы описываем концептуальную основу и методологию, которые поддерживают эту связь, и связывают существующие знания с будущими направлениями исследований. в поле.
в поле.
Ишемический инсульт и лейкоареоз — определение для 21
st век Определение «инсульт» претерпело значительную эволюцию на протяжении десятилетий исследований сосудов головного мозга. Совсем недавно в экспертном консенсусе Американской кардиологической ассоциации / Американской ассоциации инсультов подчеркивалась важность объективных клинических (нейровизуализационных) или лабораторных (патологических) свидетельств инфаркта головного мозга или гибели клеток головного мозга, связанной с ишемическим повреждением в определенном сосудистом распределении. присутствовать при диагностике ишемического инсульта, будь то симптоматический или бессимптомный.[1] Кроме того, обычным заболеванием, обнаруживаемым на МРТ головного мозга бессимптомных стареющих взрослых людей, является лейкоареоз, или лейкоареоз. Согласно определению Хачински в 1985 году, «лейкоареоз» подразумевает «пониженную плотность белого вещества, которая видна на компьютерной томографии головного мозга (КТ)», что, в свою очередь, является гиперинтенсивным при восстановлении после взвешивания по T2, плотности протонов и инверсии с ослаблением жидкости (FLAIR). последовательности МРТ головного мозга. [2–3] За прошедшие годы МРТ продемонстрировала более высокую чувствительность обнаружения аномального белого вещества, включая поражения, не видимые иным образом на КТ головы.[4
последовательности МРТ головного мозга. [2–3] За прошедшие годы МРТ продемонстрировала более высокую чувствительность обнаружения аномального белого вещества, включая поражения, не видимые иным образом на КТ головы.[4
Рентгенологическая оценка степени тяжести WMH
Существует два основных рентгенологических подхода к оценке степени тяжести WMH. Во-первых, оценочные шкалы визуальной оценки, которые используются для измерения поражения белого вещества (WML) на КТ или МРТ, основаны на локализации и тяжести заболевания белого вещества. Шкалы на основе МРТ, такие как шкала Фазекаса, оценивают WML как в перивентрикулярном (PVH), так и в глубоком белом веществе вещества (оценка 0–3). [5] По шкале Шелтенса добавлены расположение, размер и количество WML при PVH (оценка 0–6), WMH (оценка 0–24), гиперинтенсивности базальных ганглиев (BG) (оценка 0–30) и инфратенториальных очагах гиперинтенсивности. (ITF) (0–24 балла).[6] Шкала Роттердамского сканирующего исследования (RSS) оценивает WML в перивентрикулярной области (оценка 0–9) и подкорковую WML.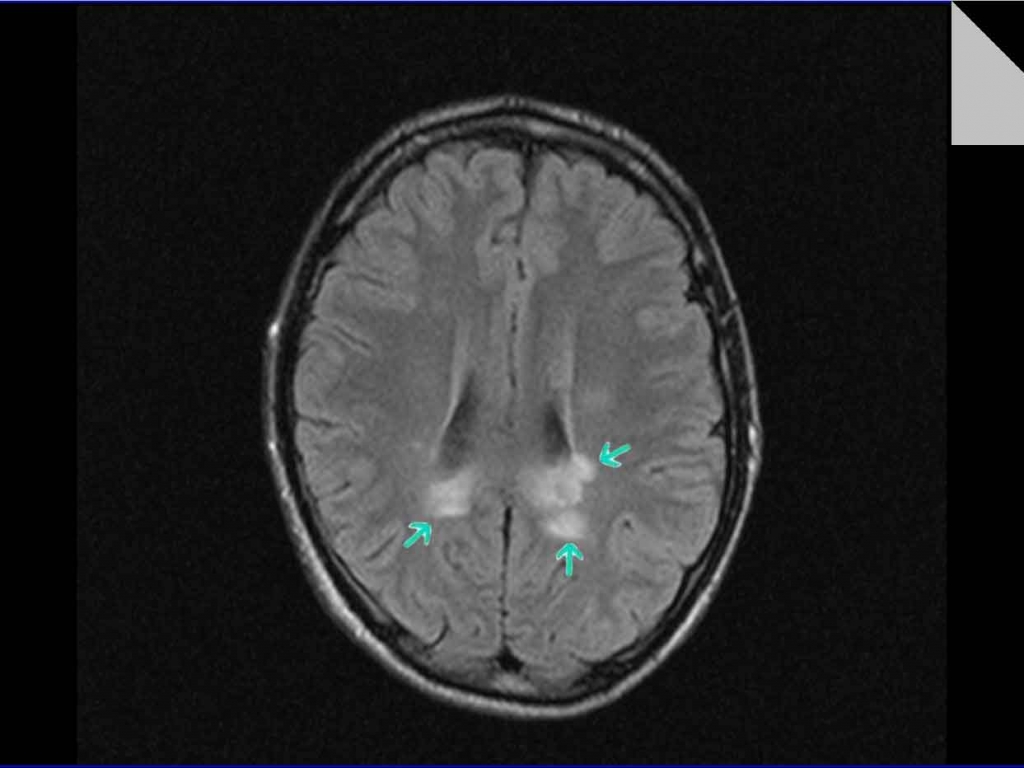 [7] Шкалы возрастных изменений белого вещества (ARWMC) для оценки WMH на КТ и МРТ включали место, размер и количество WML (0–3 балла) и поражений базальных ганглиев (0–3 балла) в 5 различных случаях. области (лобные, теменно-затылочные, височные, базальные ганглии и инфратенториальные) двусторонних полушарий [8]. Во-вторых, объемный подход к анализу WMH был основан на различных полуавтоматических протоколах с использованием аналитического программного обеспечения, такого как Sparc 5 (SUN, Пало-Альто, Калифорния) [9] или MRIcro (Школа психологии Ноттингемского университета, Ноттингем, Великобритания; www.mricro.com), которые определяют объем WMH (WMHv) на аксиальном FLAIR всего мозга или просто супратенториально. [10
[7] Шкалы возрастных изменений белого вещества (ARWMC) для оценки WMH на КТ и МРТ включали место, размер и количество WML (0–3 балла) и поражений базальных ганглиев (0–3 балла) в 5 различных случаях. области (лобные, теменно-затылочные, височные, базальные ганглии и инфратенториальные) двусторонних полушарий [8]. Во-вторых, объемный подход к анализу WMH был основан на различных полуавтоматических протоколах с использованием аналитического программного обеспечения, такого как Sparc 5 (SUN, Пало-Альто, Калифорния) [9] или MRIcro (Школа психологии Ноттингемского университета, Ноттингем, Великобритания; www.mricro.com), которые определяют объем WMH (WMHv) на аксиальном FLAIR всего мозга или просто супратенториально. [10
Хотя и более трудоемкие, но объемные методы обеспечивают большую точность и надежность при оценке тяжести WMH, особенно при оценке прогрессирования WMH, по сравнению с визуальными оценочными шкалами. [11–12] Некоторые шкалы прогрессии WMH, такие как шкалы Роттердамской прогрессии и шкалы прогрессии Шмидта, также чувствительны, согласованы и связаны с изменением объемного объема. [12]. Клиническое применение различных шкал может зависеть от их чувствительности к конкретному функциональному домену.Например, в исследовании лейкоареоза и инвалидности (LADIS) визуальная оценочная шкала и объемные методы продемонстрировали большую нагрузку на БГМ у субъектов с нарушенной физической работоспособностью и когнитивными способностями по сравнению с нормальной контрольной группой. [13] Однако объемная оценка была более чувствительной, чем визуальная оценка, при обнаружении симптомов памяти. [9] Во многих исследованиях использовали WMHv для оценки связи между лейкоареозом и риском инсульта, когнитивных нарушений, деменции, смертности, тяжести инсульта и других функциональных нарушений.
[12]. Клиническое применение различных шкал может зависеть от их чувствительности к конкретному функциональному домену.Например, в исследовании лейкоареоза и инвалидности (LADIS) визуальная оценочная шкала и объемные методы продемонстрировали большую нагрузку на БГМ у субъектов с нарушенной физической работоспособностью и когнитивными способностями по сравнению с нормальной контрольной группой. [13] Однако объемная оценка была более чувствительной, чем визуальная оценка, при обнаружении симптомов памяти. [9] Во многих исследованиях использовали WMHv для оценки связи между лейкоареозом и риском инсульта, когнитивных нарушений, деменции, смертности, тяжести инсульта и других функциональных нарушений.
Бремя WMH и риск инсульта
Риск первого в истории инсульта в популяционных исследованиях
Шесть крупных проспективных популяционных исследований предоставили решающие доказательства корреляции между WMH и риском первого в истории инсульта. Исследование риска атеросклероза в сообществах (ARIC) в 4 сообществах США, в котором наблюдали за 1684 людьми в течение 4,7 лет, показало, что у людей с WML кумулятивная частота клинического инсульта за 5 лет выше, чем у людей без WML (6,8% против 1,4%; ОР 3.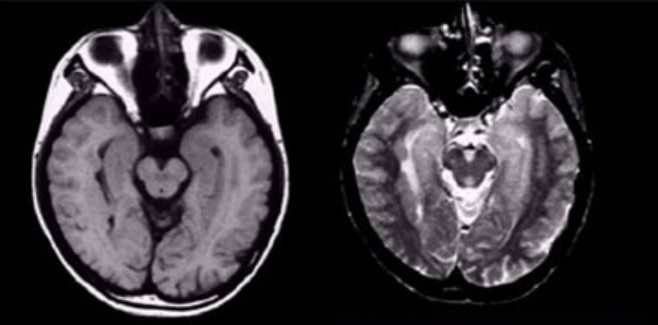 4; 95% ДИ 1,5–7,7), независимо от общих факторов риска инсульта. [14] Роттердамское сканирующее исследование в Нидерландах с участием 1077 участников в течение в среднем 4,2 года показало, что WML как в перивентрикулярных, так и в подкорковых областях значительно увеличивает риск инсульта. [15] Исследование сердечно-сосудистой системы (CHS) в 4 сообществах США включало 3293 человека, за которыми наблюдали в среднем в течение 7 лет, и показало, что риск инсульта увеличивался пропорционально увеличению степени WMH, независимо от обычных факторов риска инсульта.[16] Основываясь на результатах проспективного когортного исследования в Симане, Япония, выраженное бремя поливинилхлорида и подкоркового поражения белой матери (SWML) независимо увеличивало риск инсульта у 2684 пациентов, за которыми наблюдали в среднем 6,3 года. [17] Исследование, проведенное в 3 городах Дижон (Франция) с участием 1643 человек, за которыми в среднем наблюдали в течение 4,9 лет, показало значительное увеличение риска инсульта с увеличением WML.
4; 95% ДИ 1,5–7,7), независимо от общих факторов риска инсульта. [14] Роттердамское сканирующее исследование в Нидерландах с участием 1077 участников в течение в среднем 4,2 года показало, что WML как в перивентрикулярных, так и в подкорковых областях значительно увеличивает риск инсульта. [15] Исследование сердечно-сосудистой системы (CHS) в 4 сообществах США включало 3293 человека, за которыми наблюдали в среднем в течение 7 лет, и показало, что риск инсульта увеличивался пропорционально увеличению степени WMH, независимо от обычных факторов риска инсульта.[16] Основываясь на результатах проспективного когортного исследования в Симане, Япония, выраженное бремя поливинилхлорида и подкоркового поражения белой матери (SWML) независимо увеличивало риск инсульта у 2684 пациентов, за которыми наблюдали в среднем 6,3 года. [17] Исследование, проведенное в 3 городах Дижон (Франция) с участием 1643 человек, за которыми в среднем наблюдали в течение 4,9 лет, показало значительное увеличение риска инсульта с увеличением WML. [18] И, наконец, исследование Framingham Offspring Study, в котором систематически оценивали 2177 человек в течение 5,6 лет наблюдения, показало, что более высокий ВМГ был связан с повышенным риском инсульта (HR 2.28, 95% ДИ: 1,02–5,13), независимо от сосудистых факторов риска. [19] Метаанализ этих шести крупных популяционных когортных исследований продемонстрировал значительную связь WMH с риском инсульта (HR 3,1, 95% CI: 2,3–4,1, p <0,001). [20] Кроме того, объединенный популяционный анализ ARIC и CHS, который включал 4872 человека без инсульта, наблюдаемых в среднем в течение 13 лет, продемонстрировал, что более высокий уровень WMH на исходной МРТ является значимым предиктором спонтанного внутримозгового кровоизлияния (ICH). ) (p для тренда <0.0001). [21
[18] И, наконец, исследование Framingham Offspring Study, в котором систематически оценивали 2177 человек в течение 5,6 лет наблюдения, показало, что более высокий ВМГ был связан с повышенным риском инсульта (HR 2.28, 95% ДИ: 1,02–5,13), независимо от сосудистых факторов риска. [19] Метаанализ этих шести крупных популяционных когортных исследований продемонстрировал значительную связь WMH с риском инсульта (HR 3,1, 95% CI: 2,3–4,1, p <0,001). [20] Кроме того, объединенный популяционный анализ ARIC и CHS, который включал 4872 человека без инсульта, наблюдаемых в среднем в течение 13 лет, продемонстрировал, что более высокий уровень WMH на исходной МРТ является значимым предиктором спонтанного внутримозгового кровоизлияния (ICH). ) (p для тренда <0.0001). [21
Риск инсульта в группах высокого риска
Во многих проспективных исследованиях оценивали WMH и риск инсульта в группах высокого риска. Исследование с участием 89 японских участников, у которых был клинический лакунарный инфаркт и которые наблюдались в среднем в течение 51 месяца, показало, что обширный WMH на исходном уровне был значимым предиктором риска инсульта (ОР 1,60; 95% ДИ 1,02–2,54; p <0,05) [22 ] Исследование с участием 121 американского пациента с долевым ICH показало, что данные компьютерной томографии о повреждении белого вещества почти в четыре раза увеличивают риск рецидива ICH (HR 3.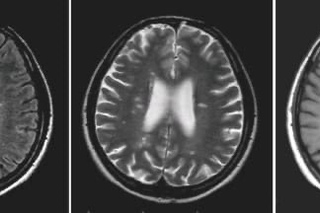 7, 95% ДИ 1,1–12,3, p = 0,02) через 2,7 года наблюдения. [10] Исследование 81 шведского пациента с лакунарным инфарктом показало, что тяжесть WML была предиктором повторного инсульта (OR 1,7, 95% CI 1,2–2,7) при длительном наблюдении (пять лет). [23] Точно так же обширная WML была связана с повторным инсультом в исследовании 228 китайских пациентов с инсультом (p = 0,0001). [24] Амстердамская группа сосудистой медицины в Нидерландах сообщила, что пациенты (n = 230) с подтвержденным атеросклеротическим заболеванием, включая недавно перенесенный инфаркт миокарда (ИМ), ишемический инсульт (ИИ), или заболевание периферических артерий (ЗПА), а также доказательства ПВГ при нейровизуализации. имеют более высокую частоту повторных ишемических инсультов в 3 года.5 лет по сравнению с лицами без ПВГ (18% против 5%, p = 0,001). [25] Исследование с участием 266 японских пациентов с ишемическим инсультом или ICH показало, что у пациентов с поздней стадией WMH, но без развития микрокровотечения, была самая высокая частота рецидивов ишемического инсульта среди 3 других подгрупп пациентов (10,5% в течение одного года и 17,4% в двух- год наблюдения, ОР 10,7, 95% ДИ 2,6–43,7).
7, 95% ДИ 1,1–12,3, p = 0,02) через 2,7 года наблюдения. [10] Исследование 81 шведского пациента с лакунарным инфарктом показало, что тяжесть WML была предиктором повторного инсульта (OR 1,7, 95% CI 1,2–2,7) при длительном наблюдении (пять лет). [23] Точно так же обширная WML была связана с повторным инсультом в исследовании 228 китайских пациентов с инсультом (p = 0,0001). [24] Амстердамская группа сосудистой медицины в Нидерландах сообщила, что пациенты (n = 230) с подтвержденным атеросклеротическим заболеванием, включая недавно перенесенный инфаркт миокарда (ИМ), ишемический инсульт (ИИ), или заболевание периферических артерий (ЗПА), а также доказательства ПВГ при нейровизуализации. имеют более высокую частоту повторных ишемических инсультов в 3 года.5 лет по сравнению с лицами без ПВГ (18% против 5%, p = 0,001). [25] Исследование с участием 266 японских пациентов с ишемическим инсультом или ICH показало, что у пациентов с поздней стадией WMH, но без развития микрокровотечения, была самая высокая частота рецидивов ишемического инсульта среди 3 других подгрупп пациентов (10,5% в течение одного года и 17,4% в двух- год наблюдения, ОР 10,7, 95% ДИ 2,6–43,7). [26
[26
Наконец, комбинированный анализ данных убедительно демонстрирует, что тяжесть WMH связана с риском повторного инсульта: метаанализ 3 исследований в группах высокого риска показал HR 7.4, 95% ДИ 2,4–22,9, p = 0,001, тогда как объединенные данные шести популяционных исследований и трех групп высокого риска показали HR 3,5, 95% ДИ 2,5–4,9, p <0,001. [20
Бремя WMH и риск сосудистых когнитивных нарушений и деменции
Риск сосудистых когнитивных нарушений
Во многих популяционных исследованиях оценивалась связь между лейкоареозом и риском когнитивных нарушений. В некоторых исследованиях использовалась исходная тяжесть ВМГ, но многие оценивали прогрессирование ВМГ в долгосрочном плане.
Исследование с участием 67 американских участников с нормальным когнитивным поведением показало, что высокий исходный уровень WMHv был связан с риском прогрессирования в легкое когнитивное нарушение (MCI) (HR 3,3; 95% CI 1,33–8,2, p = 0,01). [27] Тем не менее, Фрамингемское исследование потомства, в котором наблюдали 1694 человека в течение средней продолжительности 6,2 года, показало, что тяжесть ВГМ не коррелировала с риском всех MCI или амнезиальных MCI. [19] Точно так же австрийское исследование профилактики инсульта с участием 329 участников в течение 6 лет показало, что прогрессирование WMHv было связано с когнитивным снижением в некоторых областях, включая память, концептуализацию и зрительно-практические навыки.Однако изменения WMHV не были связаны со снижением когнитивных функций после корректировки на объем мозга. [28
[19] Точно так же австрийское исследование профилактики инсульта с участием 329 участников в течение 6 лет показало, что прогрессирование WMHv было связано с когнитивным снижением в некоторых областях, включая память, концептуализацию и зрительно-практические навыки.Однако изменения WMHV не были связаны со снижением когнитивных функций после корректировки на объем мозга. [28
Риск деменции
Связь между тяжестью лейкоареоза и риском деменции была изучена в ряде крупных проспективных популяционных исследований, включая когнитивное исследование здоровья сердечно-сосудистой системы, в котором у 480 из 3608 человек деменция развивалась в течение длительного периода. до 8 лет наблюдения. Это исследование показало, что обширная шкала WMH на начальном этапе исследования была значительным фактором риска развития деменции (HR 1.8) и болезнь Альцгеймера (БА). [29] Роттердамское сканирование продемонстрировало, что WML, преимущественно в перивентрикулярной области, независимо увеличивал риск деменции у 1077 когнитивно интактных участников через 5,2 года (отношение рисков 1,67; 95% доверительный интервал 1,25–2,24). [30] Аналогичным образом, проект Осаки-Тадзири в Японии наблюдал за 204 здоровыми взрослыми и 335 участниками с сомнительной деменцией в течение 5 лет и показал, что WML является предиктором прогрессирования сосудистой деменции (VaD). [31] Исследование Framingham Offspring Study (n = 2,013) показало, что тяжесть WMHv была значительно связана с повышенным риском деменции (HR 2.22; 95% ДИ 1,32–3,72 для WMHv, HR 3,97; 95% ДИ 1,10–14,3 для обширных WMHv) при среднем периоде наблюдения 5,9 лет. [19] Наконец, метаанализ трех популяционных исследований подтвердил значительную связь между WMH и риском всех типов деменции (HR 2,9; 95% CI 1,3–6,3, p = 0,008). [20
[30] Аналогичным образом, проект Осаки-Тадзири в Японии наблюдал за 204 здоровыми взрослыми и 335 участниками с сомнительной деменцией в течение 5 лет и показал, что WML является предиктором прогрессирования сосудистой деменции (VaD). [31] Исследование Framingham Offspring Study (n = 2,013) показало, что тяжесть WMHv была значительно связана с повышенным риском деменции (HR 2.22; 95% ДИ 1,32–3,72 для WMHv, HR 3,97; 95% ДИ 1,10–14,3 для обширных WMHv) при среднем периоде наблюдения 5,9 лет. [19] Наконец, метаанализ трех популяционных исследований подтвердил значительную связь между WMH и риском всех типов деменции (HR 2,9; 95% CI 1,3–6,3, p = 0,008). [20
WMH как биомаркер общего бремени цереброваскулярных заболеваний
Связь со смертностью
В нескольких крупных проспективных популяционных исследованиях оценивалась связь между WMH и смертностью.В когорте из 2684 неврологически нормальных японских субъектов, не имеющих инсульта, риск смерти через 6,3 года был значительно выше, если у субъектов был очевидный ЛВГ при визуализации головного мозга (OR 4,01; 95% ДИ 1,91–8,45). [17] Аналогичным образом, исследование Rotterdam Scan Study сообщило о повышенных показателях летальности среди 430 субъектов с WML [32], а также исследование Framingham Offspring с участием 2208 человек, которое показало, что тяжесть WMHv была связана с повышенным риском смерти (HR 1,38). 95% ДИ 1,13–1,69 для WMHv; HR 2.27, 95% ДИ 1,41–3,65 для обширного WMHv) в долгосрочном периоде наблюдения. [19] С другой стороны, в Исследовании здоровья сердечно-сосудистой системы 3245 участников с низкой степенью WMH продемонстрировали улучшение продолжительности жизни в течение 10–12 лет наблюдения. [33] Мета-анализ этих четырех популяционных исследований показал значительную корреляцию WMH с риском смерти (HR 2,3, 95% CI 1,9–2,8, p <0,001). [20
[17] Аналогичным образом, исследование Rotterdam Scan Study сообщило о повышенных показателях летальности среди 430 субъектов с WML [32], а также исследование Framingham Offspring с участием 2208 человек, которое показало, что тяжесть WMHv была связана с повышенным риском смерти (HR 1,38). 95% ДИ 1,13–1,69 для WMHv; HR 2.27, 95% ДИ 1,41–3,65 для обширного WMHv) в долгосрочном периоде наблюдения. [19] С другой стороны, в Исследовании здоровья сердечно-сосудистой системы 3245 участников с низкой степенью WMH продемонстрировали улучшение продолжительности жизни в течение 10–12 лет наблюдения. [33] Мета-анализ этих четырех популяционных исследований показал значительную корреляцию WMH с риском смерти (HR 2,3, 95% CI 1,9–2,8, p <0,001). [20
В некоторых исследованиях оценивалась связь лейкоареоза со смертностью в группах высокого риска. Исследование, проведенное в Южной Норвегии с участием 134 человек с первым в истории ВКГ, показало, что тяжелая ВГБ была независимо связана как с краткосрочной, так и с долгосрочной летальностью у 30-дневных выживших. [34] Точно так же выживаемость снизилась у 228 китайских субъектов с WML с первым в истории ишемическим инсультом при наблюдении в среднем 23 месяца (p = 0,007). [24
[34] Точно так же выживаемость снизилась у 228 китайских субъектов с WML с первым в истории ишемическим инсультом при наблюдении в среднем 23 месяца (p = 0,007). [24
Связь с тяжестью инсульта и исходами после инсульта
Тяжесть лейкоареоза была связана с плохим функциональным исходом после инсульта как в краткосрочных (90 дней), так и в долгосрочных исследованиях. У пациентов с острым ишемическим инсультом тяжесть WMH значительно связана с плохим функциональным исходом через 3 месяца [35–39] и позже.[39–40] Когда рассматривается топография WML, бремя PVH, но не подкорковое или глубокое WMH, по-видимому, связано с неблагоприятным клиническим исходом как в краткосрочных, так и в долгосрочных (более 90 дней) исследованиях. [35–36, 39] Исследование пациентов со спонтанным ВЧГ также показало, что более высокое бремя лейкоареоза было независимым маркером худшего функционального результата. [38
Помимо того, что он является предиктором функционального исхода после инсульта, тяжесть лейкоареоза была независимо связана с более крупными очагами инфаркта [41], большим увеличением объема инфаркта [42] и повышенным риском геморрагической трансформации и паренхиматозной гематомы после внутриартериальной тромбэктомии.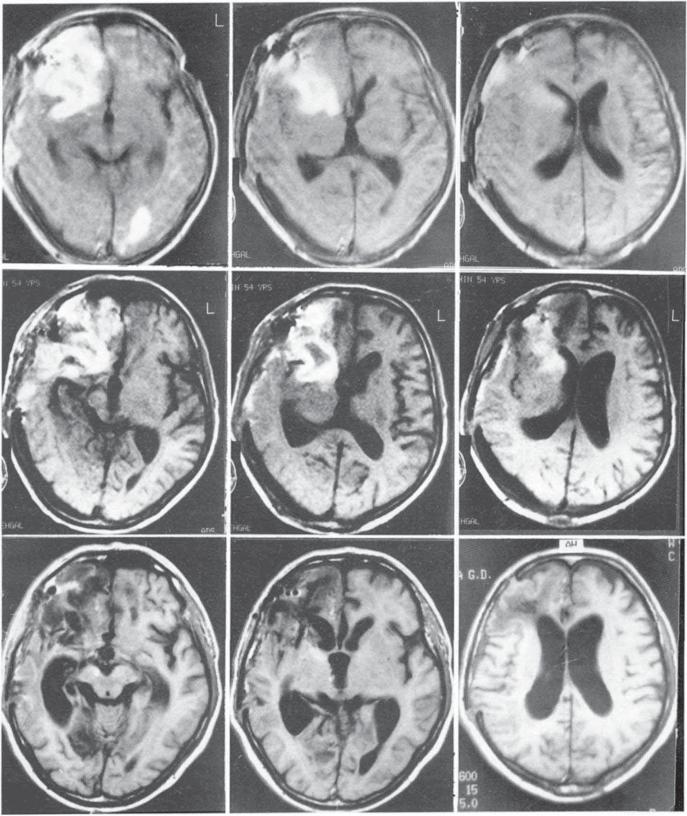 для лечения острого ишемического инсульта, особенно лейкоареоза в области глубокого белого вещества.[43
для лечения острого ишемического инсульта, особенно лейкоареоза в области глубокого белого вещества.[43
Связь с другими функциональными нарушениями
Лейкоареоз и инвалидность (LADIS) — это многоцентровое сотрудничество, оценивающее независимую роль изменения белого вещества с помощью нейровизуализации в определении инвалидности во многих клинических аспектах, таких как функциональный статус, когнитивные способности, настроение, двигательные функции. выступления и проблемы с мочеиспусканием. [44] В исследовании LADIS, проведенном среди 639 участников без инвалидности, умеренные и тяжелые изменения белого вещества были независимо связаны с ухудшением походки и равновесия [45], тогда как прогрессирование лейкоареоза было связано с постепенным снижением результатов теста управляющих функций.[46] Годовая переоценка 619 пожилых пациентов с LADIS с исходной функциональной независимостью показала, что тяжелая ВГМ подвергает их риску зависимости от моторных и когнитивных нарушений за короткий период времени. [47] Наконец, участники LADIS с тяжелым исходным прогрессированием WMH и WMH в течение 3-летнего периода наблюдения имели больший риск аномалий походки и стойки, верхних двигательных признаков и замедления постукивания пальцем (мелкая моторика), независимо от других сосудов. поражения. [48
[47] Наконец, участники LADIS с тяжелым исходным прогрессированием WMH и WMH в течение 3-летнего периода наблюдения имели больший риск аномалий походки и стойки, верхних двигательных признаков и замедления постукивания пальцем (мелкая моторика), независимо от других сосудов. поражения. [48
Аналогичным образом, Орегонское исследование старения мозга, в котором наблюдали 104 когнитивно интактных участников в течение до 13 лет, продемонстрировало, что увеличение общего и перивентрикулярного WMHv на исходном уровне и прогрессирование PVH коррелировали с постепенным ухудшением походки, тогда как прогрессирование подкоркового WMH было связано с при снижении памяти.[49
Наконец, в ряде исследований сообщается о связи между недержанием мочи и изменениями белого вещества. [50–52] Кроме того, неотложные позывы к мочеиспусканию были связаны с исходной тяжестью ВМГ среди участников LADIS, независимо от других факторов и сосудистого поражения головного мозга. [53
Будущие направления
Роль ВМГ как диагностического и прогностического биомаркера цереброваскулярных заболеваний в настоящее время общепринята; однако остается вопрос, играет ли WMH активную роль в патофизиологии церебральной дисфункции, связанной с тяжестью и прогрессированием лейкоареоза.Новые методы клинических исследований, включая полногеномные ассоциативные исследования (GWAS) и передовые методы нейровизуализации, могут предоставить доказательства биологии основного заболевания при WMH. Особый интерес представляет недавний отчет об общем генетическом вкладе между тяжестью ВМГ, оцененной на МРТ головного мозга здоровых пожилых людей, включенных в состав нескольких популяционных когорт консорциума CHARGE [54], и когорт пациентов с острым ишемическим инсультом в больницах. . [55] В метаанализе WMH GWAS у 9 361 человека европейского происхождения без инсульта, консорциум CHARGE идентифицировал 6 новых однонуклеотидных полиморфизмов (SNP) из локуса на хромосоме 17q25, связанных с бременем WMH.[54] Связь этих SNP, особенно rs9894383 (p = 0,0006) с WMHv у пациентов с ишемическим инсультом, была воспроизведена в исследовании International Stroke Genetics Consortium, [55] и представляет собой крупный прорыв в понимании общего генетического вклада в лейкоареоз по всему спектру заболеваний мелких сосудов головного мозга.
Ожидается, что в будущем прорывы произойдут также в области расширенной нейровизуализации белого вещества при здоровье и болезнях, среди которых наиболее многообещающими являются диффузионно-тензорная визуализация (DTI).DTI предоставляет подробные данные о структуре белого вещества, а в недавних исследованиях у здоровых взрослых изучалась связь между общими факторами риска сосудов, такими как гипертензия и липиды сыворотки крови, и показателями целостности белого вещества DTI [56–57]. Эти предварительные отчеты о влиянии артериального давления и ЛПНП в сыворотке на целостность белого вещества требуют дальнейшей оценки у субъектов с продвинутой стадией ВГБ.
Заключение
В литературе подтверждается роль ВМГ как биомаркера давних цереброваскулярных заболеваний.Продвинутая нейровизуализация и будущие исследования генетической архитектуры лейкоареоза позволят разгадать основную биологию заболевания белого вещества и его роль в патофизиологии инсульта, деменции и общего бремени цереброваскулярной дисфункции.
Степень тяжести гиперинтенсивности белого вещества при МРТ. Общее бремя болезни белого вещества значительно различается среди бессимптомных взрослых и пациентов с известным цереброваскулярным заболеванием. У лиц того же возраста объем гиперинтенсивности белого вещества (WMH) может варьироваться от легкой до очень тяжелой (, верхняя панель, ).Используя проверенный полуавтоматический объемный протокол, объем WMH может быть определен количественно ( нижняя панель, красного цвета, карты WMH получены из смежных супратенториальных аксиальных срезов T2-FLAIR MRI с использованием ранее опубликованного метода [10]) с высокой степенью тщательность и точность.
Таблица 1
Связь ВМГ с инсультом, повторным инсультом, внутримозговым кровоизлиянием, геморрагической трансформацией и смертностью
| Автор | Население | Результаты |
|---|---|---|
| Риск первого инсульта | ||
| Wong TY 2002 [14] | Исследование ARIC | 5-летняя кумулятивная частота клинического инсульта: WML по сравнению с WML: 6.8% против 1,4%; RR 3,4; 95% ДИ 1,5–7,7 |
| Vermeer SE 2003 [15] | Роттердамское сканирование, исследование | 3 rd по сравнению с 1 st PVH тертиль: HR 4,7; 95% ДИ 2,0–11,2 3 rd по сравнению с 1 st Тертиль SWML: HR 3,6; 95% ДИ 1,4–9,2 |
| Kuller LH 2004 [16] | CHS | классы WML ≥ 5 по сравнению с классами 0-1: 2,8% против 0,6%; HR 3,0; 95% ДИ 1,9–4,7 |
| Bokura H 2006 [17] | Shimane Study | отмеченный и мягкий PVH: OR 2.08; 95% ДИ 1,04–4,17. отмечены по сравнению с отсутствием SWML: OR 2,73; 95% ДИ 1,32–5,63 |
| Buyck JF 2009 [18] | 3-City Dijon Study | 4 th против 1 st общий квартиль WMHv: HR 5,7; 95% ДИ 2,0–16,4 4 th против 1 st квартиль объема PVH: HR 6,2; 95% ДИ 2,0–19,5 4 th против 1 st глубокий квартиль WMHv: HR 4,1; 95% ДИ 1,5–11,3 |
| Debette S 2010 [19] | Framingham Offspring Study | обширный WMHv: HR 2.28; 95% ДИ 1,02–5,13 |
| Debette S 2010 [20] | Мета-анализ | WMH: HR 3,1; 95% ДИ 2,3–4,1 |
| Folsom AR 2012 [21] | Исследование ARIC и CHS | Риск ICH: WMH степени 4–9 по сравнению с классом WMH 0–1: HR 3,96; 95% ДИ 1,90–8,27 WMH степени 3 по сравнению с WMH степени 0–1: HR 3,52; 95% ДИ 1,80–6,89 |
| Риск повторного инсульта | ||
| Yamauchi H 2002 [22] | Оценка HR 1 на исходном уровне | .60; 95% ДИ 1,02–2,54 |
| Appelros P 2005 [23] | Шведский | Оценка WML на исходном уровне: ОР 1,7 95% ДИ 1,2–2,7 |
| Fu JH 2005 [24] | Китайский | Степень серьезности WML: HR 4.18; 95% ДИ 2,0–8,6 |
| Gerdes VE 2006 [25] | Амстердамская группа сосудистой медицины | PVH в сравнении с PVH: HR 3,2; 95% ДИ 1,3–8,4 глубокий и без глубокого WML: ОР 1,5; 95% ДИ 0,6–3,8 |
| Naka H 2006 [26] | Японский | Для ишемического инсульта: продвинутый WMH: HR 10.7; 95% ДИ 2,6–43,7 |
| Debette S 2010 [20] | Мета-анализ | WMH: HR 7,4; 95% ДИ 2,4–22,9 |
| Риск ИЦГ и геморрагической трансформации | ||
| Smith EE 2004 [10] | для Америки CT WMH (степень 1) по сравнению с CT-WMH: HR 3,7; 95% ДИ 1,1–12,3 | |
| Naka H 2006 [26] | Японский | Для ICH: продвинутый WMH: HR 0.016; 95% ДИ 0,001–0,258 |
| Shi ZS 2012 [43] | Американский | Глубокий WMH умеренной или тяжелой степени на МРТ до вмешательства: Прогнозирование геморрагической трансформации: OR 3,43; 95% ДИ 1,23–9,57, после механической тромбэктомии Прогнозирование паренхиматозной гематомы: OR 6,26; 95% ДИ 1,74–22,45, после механической тромбэктомии |
| Смертность | ||
| Маркировка Bokura H 2006 [17] | в сравнении с исследованием Shimane .01; 95% ДИ 1,91–8,45. | |
| Ikram MA 2009 [32] | Роттердамское сканирование | Смертность от всех причин: 4 th vs 1 st Квартиль WMH: HR 2,05; 95% ДИ 1,32–3,20 WML на SD: HR 1,38; 95% ДИ 1,16–1,65 Для смертности от сердечно-сосудистых заболеваний: WML на SD: HR 2,52; 95% ДИ 1,65–3,84 |
| Debette S 2010 [19] | Framingham Offspring Study | Риск смерти: WMHv: HR 1.38; 95% ДИ 1,13–1,69 обширный WMHv: ОР 2,27; 95% ДИ 1,41–3,65 Риск сосудистой смерти: WMHv: HR 1,96; 95% ДИ 1,13–2,92 обширный WMHv: HR 4,18; 95% ДИ 1,72–10,15 Риск сердечно-сосудистой смерти: WMHv: HR 1,86; 95% ДИ 1,20–2,89 обширный WMHv: HR 3,49; 95% ДИ 1,30–9,37 |
| Kuller LH 2007 [33] | CHS | Желудочковый класс ≥ 6: HR 1,58; 95% ДИ 1,21–2,07 Степень белого вещества ≥ 5: ОР 1,87; 95% ДИ 1.43−2,32 |
| Tveiten A 2013 [34] | Norwegian | 30-дневная смертность: оценка WMH: OR 1,6; 95% ДИ 1,06–2,5 Долгосрочная смертность: оценка WMH: OR 1,6; 95% ДИ 1,2–2,1 |
| Fu JH 2005 [24] | Китайский | Выживаемость: степень тяжести WML: HR 2,02; 95% ДИ 1,032–3,960 |
| Debette S 2010 [20] | Мета-анализ | WMH: HR 2.3; 95% ДИ 1,9–2,8 |
Таблица 2
Связь ВГД с когнитивными нарушениями, деменцией, аномалиями походки и недержанием мочи
| Автор | Население | 12 |
|---|---|---|
| Smith EE 2008 [27] | American | High WMHv: HR 3.30; 95% ДИ 1,33–8,22 |
| Debette S 2010 [19] | Framingham Offspring Study | Для MCI WMHv: OR 1,06; 95% ДИ 0,83–1,36 обширный WMHv: OR 1,26; 95% ДИ 0,67–2,39 |
| Для амнезиаков MCI WMHv: OR 1,24; 95% ДИ 0,98–1,57 обширный WMHv: OR 1,67; 95% ДИ 0,96–2,93 | ||
| Для амнестических MCI, возраст ≥ 60 WMHv: OR 1,49; 95% ДИ 1,14–1,97 обширный WMHv: OR 2.47; 95% ДИ 1,31–4,66 | ||
| Schmidt R 2005 [28] | Австрийское исследование профилактики инсульта | WMHv: β -0,025; 95% ДИ от -0,047 до -0,004 (память) WMHv: β -0,022; 95% ДИ от -0,043 до 0,0004 (концептуализация) WMHv: β -0,035; 95% ДИ от -0,059 до -0,011 (зрительно-практические навыки) WMHv: β -0,017; 95% ДИ от -0,036 до -0,002 (внимание / скорость) |
| Риск деменции | ||
| Когнитивный LH14 2003 [2914] | Здоровье сердечно-сосудистых заболеваний WMH ≥ 3: HR 1.7; 95% ДИ 1,36–2,10 (полная деменция) WMH ≥ 3: HR 1,5; 95% ДИ 1,17–1,99 (AD) WMH ≥ 3: HR 2,1; 95% ДИ 1,36–3,11 (VaD / смешанная деменция) | |
| Prins ND 2004 [30] | Rotterdam Scan Study | PVH: HR 1,67; 95% CI 1,25–2,24 |
| Meguro K 2007 [31] | Проект Осаки-Тадзири | PVH: OR 0,78 (незначительно) (AD) Deep WMH: OR 1,07, 1,02 (справа, слева, не значимо) (AD) PVH: OR 4,14 (p <0,005) (VaD) Deep WMH: OR 4.04, 3,27 (справа, слева, p <0,05) (VaD) |
| Debette S 2010 [19] | Framingham Offspring Study | WMHv: HR 2,22; 95% ДИ 1,32–3,72 обширный WMHv: HR 3,97; 95% ДИ 1,10–14,30 |
| Debette S 2010 [20] | Мета-анализ | WMH: HR 2,9; 95% ДИ 1,3–6,3 |
| Нарушения походки | ||
| Kreisel SH 2013 [45] | LADIS Study 9014 SP14 901 9014 : Средняя степень ARWMC: −0.22; 95% ДИ от -0,35 до -0,09 Тяжелая степень ARWMC: -0,46; 95% ДИ от -0,63 до -0,28 | |
| Inzitari D 2007 [47] | Исследование LADIS | Для пациентов с 0 или 1 активностью, ограниченной на входе Тяжелая или легкая ARWMC: HR 2,38; 95% ДИ 1,29–4,38 Для пациентов без ограничения активности при входе Тяжелая или легкая ARWMC: ОР 3,02; 95% ДИ 1,34–6,78 |
| Poggesi A 2013 [48] | Исследование LADIS | Сильное или легкое изменение белого вещества: OR 2.34; 95% ДИ 1,52–3,60 |
| Silbert LC 2008 [49] | Oregon Brain Aging Study | Общий WMHv и скорость изменений во время ходьбы в секундах: 2 = 0,08, p = 0,0052 |
| Общий WMHv и количество шагов: R 2 = 0,12, p = 0,0125 | ||
| Повышенный PVH и скорость изменений во времени ходьбы в секундах: 2 R = 0,12, p = 0,0039 | ||
| Повышенный PVH и количество ступеней: R 2 = 0.13, p = 0,0075 | ||
| Недержание мочи | ||
| Poggesi A 2008 [53] | LADIS Study | 90 1.144; 95% ДИ 1,04–2,90|
Благодарности
Доктор Рост поддерживается Национальным институтом неврологических расстройств и инсульта (K23 NS064052 и R01 NS082285).
Сноски
Соблюдение этических норм
Конфликт интересов
Dr.Chutinet сообщает о неразглашении.
Права человека и животных и информированное согласие
Эта статья не содержит исследований с участием людей или животных, выполненных кем-либо из авторов.
Список литературы
* Важный
** Исключительно важный
1. Сакко Р.Л., Каснер С.Е., Бродерик Дж. П. и др. Обновленное определение инсульта для 21 века: заявление для медицинских работников Американской кардиологической ассоциации / Американской ассоциации инсульта.Инсульт. 2013; 44: 2064–2089. [PubMed] [Google Scholar] Это консенсусное заявление экспертов предоставляет самые последние данные в поддержку нового определения инсульта. Хачинский В.К., Поттер П., Мерски Х. Лейкоараиоз: древний термин для обозначения новой проблемы. Может J Neurol Sci. 1986; 13 (4 доп.): 533–534. [PubMed] [Google Scholar] 3. Хачинский В.К., Поттер П., Мерски Х. Лейкоараиоз. Arch Neurol. 1987. 44: 21–23. [PubMed] [Google Scholar] 4. Фазекас Ф., Баркхоф Ф., Валунд ЛО и др. Оценка поражений белого вещества при КТ и МРТ.Cerebrovasc Dis. 2002; 13 (Дополнение 2): 31–36. [PubMed] [Google Scholar] 5. Фазекас Ф., Чавлюк Дж. Б., Алави А. и др. Нарушения МР-сигнала при 1,5 Тл при деменции Альцгеймера и нормальном старении. AJR Am J Roentgenol. 1987. 149: 351–356. [PubMed] [Google Scholar] 6. Scheltens P, Barkhof F, Leys D, et al. Полуколичественная рейтинговая шкала для оценки гиперинтенсивности сигнала на магнитно-резонансной томографии. J Neurol Sci. 1993; 114: 7–12. [PubMed] [Google Scholar] 7. de Leeuw FE, de Groot JC, Achten E, et al. Распространенность поражений белого вещества головного мозга у пожилых людей: популяционное магнитно-резонансное исследование.Роттердамское сканирование. J Neurol Neurosurg Psychiatry. 2001; 70: 9–14. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Валунд Л.О., Баркхоф Ф., Фазекас Ф. и др. Новая шкала оценки возрастных изменений белого вещества, применимая к МРТ и КТ. Инсульт. 2001; 32: 1318–1322. [PubMed] [Google Scholar] 9. van Straaten EC, Fazekas F, Rostrup E et al. Влияние метода оценки гиперинтенсивности белого вещества на корреляцию с клиническими данными: исследование LADIS. Инсульт. 2006; 37: 836–840. [PubMed] [Google Scholar] 10.Smith EE, Gurol ME, Eng JA и др. Поражения белого вещества, когнитивные функции и рецидивирующие кровоизлияния при долевом внутримозговом кровоизлиянии. Неврология. 2004. 63: 1606–1612. [PubMed] [Google Scholar] 11. Prins ND, van Straaten EC, van Dijk EJ, et al. Измерение прогрессирования поражений белого вещества головного мозга на МРТ: визуальная оценка и волюметрия. Неврология. 2004. 62: 1533–1539. [PubMed] [Google Scholar] 12. Gouw AA, van der Flier WM, van Straaten EC, et al. Надежность и чувствительность визуальных шкал по сравнению с волюметром для оценки прогрессирования гиперинтенсивности белого вещества.Cerebrovasc Dis. 2008. 25: 247–253. [PubMed] [Google Scholar] 13. Gouw AA, Van der Flier WM, van Straaten EC, et al. Сравнение простой и комплексной оценки гиперинтенсивности белого вещества в зависимости от физической работоспособности и когнитивных способностей: исследование LADIS. J Neurol. 2006; 253: 1189–1196. [PubMed] [Google Scholar] 14. Вонг Т.Ю., Кляйн Р., Шарретт А.Р. и др. Поражения белого вещества головного мозга, ретинопатия и случайный клинический инсульт. ДЖАМА. 2002; 288: 67–74. [PubMed] [Google Scholar] 15. Vermeer SE, Hollander M, van Dijk EJ, et al.Тихие инфаркты головного мозга и поражения белого вещества увеличивают риск инсульта у населения в целом: исследование Rotterdam Scan Study. Инсульт. 2003. 34: 1126–1129. [PubMed] [Google Scholar] 16. Куллер Л.Х., Лонгстрет В.Т., мл., Арнольд А.М. и др. Гиперинтенсивность белого вещества на магнитно-резонансной томографии черепа: предиктор инсульта. Инсульт. 2004; 35: 1821–1825. [PubMed] [Google Scholar] 17. Бокура Х., Кобаяси С., Ямагути С. и др. Тихий инфаркт головного мозга и подкорковые поражения белого вещества увеличивают риск инсульта и смертности: проспективное когортное исследование.Журнал инсульта и цереброваскулярных заболеваний. 2006; 15: 57–63. [PubMed] [Google Scholar] 18. Buyck JF, Dufouil C, Mazoyer B, et al. Поражения белого вещества головного мозга связаны с риском инсульта, но не с другими сосудистыми событиями: исследование 3-City Dijon Study. Инсульт. 2009; 40: 2327–2331. [PubMed] [Google Scholar] 19. Дебетт С., Байзер А., ДеКарли С. и др. Ассоциация МРТ-маркеров сосудистого повреждения головного мозга с инсультом, умеренными когнитивными нарушениями, деменцией и смертностью: исследование Framingham Offspring.Инсульт. 2010. 41: 600–606. [Бесплатная статья PMC] [PubMed] [Google Scholar] 20. Дебетт С., Маркус Х.С. Клиническое значение гиперинтенсивности белого вещества на магнитно-резонансной томографии головного мозга: систематический обзор и метаанализ. BMJ. 2010; 341: c3666. [Бесплатная статья PMC] [PubMed] [Google Scholar] Этот метаанализ обеспечивает комплексный и систематический подход к оценке роли лейкоареоза в цереброловаскулярных заболеваниях. Фолсом А.Р., Яцуя Х., Мосли Т.Х., мл. И др. Риск внутрипаренхиматозного кровоизлияния при лейкоареозе и инфаркте головного мозга, определенном с помощью магнитно-резонансной томографии.Энн Нейрол. 2012; 71: 552–559. [Бесплатная статья PMC] [PubMed] [Google Scholar] 22. Ямаути Х., Фукуда Х., Оянаги С. Значение высокоинтенсивных поражений белого вещества как предиктора инсульта от артериолосклероза. J Neurol Neurosurg Psychiatry. 2002. 72: 576–582. [Бесплатная статья PMC] [PubMed] [Google Scholar] 23. Аппелрос П., Самуэльссон М., Линделл Д. Лакунарные инфаркты: функциональные и когнитивные результаты через пять лет в отношении результатов МРТ. Cerebrovasc Dis. 2005; 20: 34–40. [PubMed] [Google Scholar] 24.Fu JH, Lu CZ, Hong Z и др. Степень поражения белого вещества связана с острыми подкорковыми инфарктами и позволяет прогнозировать дальнейший риск инсульта у пациентов с первым в истории ишемическим инсультом. J Neurol Neurosurg Psychiatry. 2005. 76: 793–796. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Гердес В.Е., Ква В.И., тен Кейт Х. и др. Поражения белого вещества головного мозга позволяют прогнозировать как ишемический инсульт, так и инфаркт миокарда у пациентов с установленным атеросклеротическим заболеванием. Атеросклероз. 2006. 186: 166–172. [PubMed] [Google Scholar] 26.Нака Х., Номура Э., Такахаши Т. и др. Сочетание наличия или отсутствия церебральных микрокровоизлияний и повышенной гиперинтенсивности белого вещества в качестве предикторов последующих типов инсульта. AJNR Am J Neuroradiol. 2006. 27: 830–835. [Бесплатная статья PMC] [PubMed] [Google Scholar] 27. Смит Э.Е., Егорова С., Блэкер Д. и др. Магнитно-резонансная томография гиперинтенсивности белого вещества и объема мозга в прогнозировании легких когнитивных нарушений и деменции. Arch Neurol. 2008; 65: 94–100. [PubMed] [Google Scholar] 28.Шмидт Р., Ропель С., Энцингер С. и др. Прогрессирование поражения белого вещества, атрофия мозга и снижение когнитивных функций: австрийское исследование профилактики инсульта. Энн Нейрол. 2005. 58: 610–616. [PubMed] [Google Scholar] 29. Куллер Л.Х., Лопес О.Л., Ньюман А. и др. Факторы риска деменции в когнитивном исследовании сердечно-сосудистой системы. Нейроэпидемиология. 2003; 22: 13–22. [PubMed] [Google Scholar] 30. Принс Н.Д., ван Дейк Э.Дж., ден Хейер Т. и др. Поражения белого вещества головного мозга и риск деменции. Arch Neurol. 2004. 61: 1531–1534.[PubMed] [Google Scholar] 31. Мегуро К., Исии Х, Касуя М. и др. Заболеваемость деменцией и связанные с ней факторы риска в Японии: Проект Осаки-Тадзири. J Neurol Sci. 2007. 260: 175–182. [PubMed] [Google Scholar] 32. Икрам М.А., Верноой М.В., Врооман Х.А. и др. Объемы тканей головного мозга и заболевание мелких сосудов в зависимости от риска смерти. Neurobiol Aging. 2009. 30: 450–456. [PubMed] [Google Scholar] 33. Куллер Л.Х., Арнольд А.М., Лонгстрет В.Т., мл. И др. Уровень белого вещества и объем желудочков на МРТ головного мозга как маркеры долголетия в исследовании сердечно-сосудистой системы.Neurobiol Aging. 2007. 28: 1307–1315. [PubMed] [Google Scholar] 34. Tveiten A, Ljostad U, Mygland A, Naess H. Лейкоареоз связан с краткосрочной и долгосрочной смертностью у пациентов с внутримозговым кровоизлиянием. J Stroke Cerebrovasc Dis. 2013 21 февраля; pii: S1052-3057 (13) 00023-2. [Epub перед печатью] [PubMed] [Google Scholar] 35. Liou LM, Chen CF, Guo YC и др. Гиперинтенсивность белого вещества головного мозга позволяет прогнозировать исход функционального инсульта. Cerebrovasc Dis. 2010; 29: 22–27. [PubMed] [Google Scholar] 36.Киссела Б., Линдселл С.Дж., Клейндорфер Д. и др. Клиническое прогнозирование функционального исхода после ишемического инсульта: удивительная важность перивентрикулярной болезни белого вещества и расы. Инсульт. 2009. 40: 530–536. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Хеннингер Н., Лин Э., Бейкер С.П. и др. Лейкоареоз прогнозирует неблагоприятный исход через 90 дней после острой окклюзии крупной мозговой артерии. Cerebrovasc Dis. 2012; 33: 525–531. [PubMed] [Google Scholar] 38. Каприо Ф.З., Маас М.Б., Розенберг Н.Ф. и др. Лейкоареоз на магнитно-резонансной томографии коррелирует с худшими исходами после спонтанного внутримозгового кровоизлияния.Инсульт. 2013. 44: 642–646. [PubMed] [Google Scholar] 39. Канг Х.Дж., Стюарт Р., Парк М.С. и др. Гиперинтенсивность белого вещества и функциональные результаты через 2 недели и 1 год после инсульта. Cerebrovasc Dis. 2013; 35: 138–145. [PubMed] [Google Scholar] 40. Арсава Э.М., Рахман Р., Розанд Дж. И др. Тяжесть лейкоареоза коррелирует с клиническим исходом после ишемического инсульта. Неврология. 2009. 72: 1403–1410. [Бесплатная статья PMC] [PubMed] [Google Scholar] 42. Ай Х., Арсава Э.М., Розанд Дж. И др. Тяжесть лейкоареоза и предрасположенность к развитию инфаркта при остром инсульте.Инсульт. 2008; 39: 1409–1413. [PubMed] [Google Scholar] 43. Ши З.С., Ло Й., Либескинд Д.С. и др. Лейкоареоз позволяет прогнозировать паренхиматозную гематому после механической тромбэктомии при остром ишемическом инсульте. Инсульт. 2012; 43: 1806–1811. [Бесплатная статья PMC] [PubMed] [Google Scholar] 44. 2001–2011: десятилетие исследования LADIS (лейкоареоз и инвалидность): что мы узнали об изменениях белого вещества и болезни мелких сосудов? Cerebrovasc Dis. 2011; 32: 577–588. [PubMed] [Google Scholar] 45. Kreisel SH, Blahak C, Bazner H, et al.Ухудшение походки и равновесия с течением времени: эффекты возрастного изменения белого вещества — исследование LADIS. Cerebrovasc Dis. 2013; 35: 544–553. [PubMed] [Google Scholar] 46. Пантони Л., Подгези А., Базиль А.М. и др. Лейкоареоз позволяет прогнозировать скрытые глобальные функциональные нарушения у пожилых людей без инвалидности: исследование LADIS (лейкоареоз и инвалидность у пожилых людей). J Am Geriatr Soc. 2006; 54: 1095–1101. [PubMed] [Google Scholar] 47. Inzitari D, Simoni M, Pracucci G, et al. Риск быстрого глобального функционального снижения у пожилых пациентов с тяжелыми возрастными церебральными изменениями белого вещества: исследование LADIS.Arch Intern Med. 2007. 167: 81–88. [PubMed] [Google Scholar] 48. Поггези А., Гоу А., ван дер Флиер В. и др. Изменения белого вещества головного мозга связаны с отклонениями при неврологическом обследовании у пожилых людей без инвалидности: исследование LADIS. J Neurol. 2013; 260: 1014–1021. [PubMed] [Google Scholar] 49. Силберт Л.К., Нельсон С., Ховисон Д.Б. и др. Влияние увеличения объема гиперинтенсивного белого вещества на скорость когнитивного и моторного снижения. Неврология. 2008. 71: 108–113. [Бесплатная статья PMC] [PubMed] [Google Scholar] 50.Гото К., Исии Н., Фукасава Х. Диффузная болезнь белого вещества у пожилых людей. Клиническое, невропатологическое и КТ-исследование. Радиология. 1981; 141: 687–695. [PubMed] [Google Scholar] 51. Тарвонен-Шредер С., Ройтта М., Райха И. и др. Клинические особенности лейкоараиоза. J Neurol Neurosurg Psychiatry. 1996. 60: 431–436. [Бесплатная статья PMC] [PubMed] [Google Scholar] 52. Сито Ю.Ю., Сахадеван С. Клиническое значение поражений белого вещества головного мозга у пожилых азиатов с подозрением на деменцию. Возраст Старение.2004. 33: 67–71. [PubMed] [Google Scholar] 53. Поггези А., Пракуччи Г., Чабриат Н. и др. Жалобы на мочеиспускание у пожилых людей без инвалидности с возрастными изменениями белого вещества: исследование лейкоареоза и инвалидности (LADIS). J Am Geriatr Soc. 2008; 56: 1638–1643. [PubMed] [Google Scholar] 54. Fornage M, Debette S, Bis JC и др. Полногеномные исследования ассоциации бремени поражения белого вещества головного мозга: консорциум CHARGE. Энн Нейрол. 2011; 69: 928–939. [Бесплатная статья PMC] [PubMed] [Google Scholar] Это первая рукопись, в которой представлены доказательства связи между распространенными генетическими вариантами и тяжестью лейкоареоза.55. Адиб-Самии П., Рост Н., Трайлор М. и др. Локус 17q25 связан с объемом гиперинтенсивного белого вещества при ишемическом инсульте, но не со статусом лакунарного инсульта. Инсульт. 2013; 44: 1609–1615. [Бесплатная статья PMC] [PubMed] [Google Scholar] 56. Салат Д.Х., Уильямс В.Дж., Лериц Е.С. и др. Индивидуальные вариации артериального давления связаны с целостностью регионального белого вещества у здоровых пожилых людей. Нейроизображение. 2012; 59: 181–192. [Бесплатная статья PMC] [PubMed] [Google Scholar] 57. Уильямс В.Дж., Лериц Э.С., Шепель Дж. И др.Индивидуальные вариации уровня холестерина в сыворотке крови связаны с целостностью региональной ткани белого вещества у пожилых людей. Hum Brain Mapp. 2013; 34: 1826–1841. [Бесплатная статья PMC] [PubMed] [Google Scholar]Перивентрикулярные поражения белой материи
Тимоти К. Хейн, доктор медицины. • Последнее изменение страницы: 16 августа 2021 г.
| МРТ (магнитно-резонансное изображение) головного мозга.Это сечение в горизонтальной плоскости, чуть выше ушей. Перивентрикулярный можно увидеть поражения белого вещества (белые пятна внизу). Этот это умеренный случай. | МРТ показывает умеренную PVM. Умеренная ПВМ соответствует примерно 15% бремени лейкоариоза. | Тяжелый ПВМ. 90-летняя женщина. Происходит слияние (слияние), так что верхние желудочки окружает облако. (Чутье) |
МРТ-исследования пожилых лица с нарушением равновесия и походкой по неизвестной причине часто проявляют атрофия лобной части и гиперинтенсивные очаги Т2 подкоркового белого вещества.(Кербер и др. др., 1998). Патологические исследования, хотя и немногочисленные, предполагают атрофию лобной части (усыхание), вентрикуломегалию (то есть большее сжатие), реактивные астроциты в лобном перивентрикулярном белом веществе (т. е. рубцевание) и увеличиваются толщина стенки артериол (Whitman et al, 1999).
Есть несколько мест поражения белого вещества. Черные области вокруг центра называются «перивентрикулярными поражениями белого вещества». Те, которые расположены между корой и желудочками с некоторым промежутком между ними, называются просто «поражениями белого вещества».Есть также подтипы в «глубоком белом веществе», ниже желудочков, некоторые в мозжечке, а иногда они видны в стволе мозга. Эта страница посвящена более высоким поражениям желудочков.
Поражения белого вещества лучше всего видны на МРТ-последовательности изображений головного мозга «T2 FLAIR». КТ не так чувствительны. Чем лучше (сильнее) магнит МРТ, тем больше поражений видно. Таким образом, МРТ, сделанная на современных аппаратах 3T, выявляет больше и меньше поражений белого вещества, чем сканирование на «открытых» сканерах.Патологически ШИМ соответствуют областям истончения миелина и глиоза, и часто сопровождаются лакунарными (дырочками) инфарктами и мелкими сосудами. атеросклеротическое заболевание.
Поражения белого вещества головного мозга — обычное дело, вызывающее тревогу, и врачи часто называют его «случайным». Возможно, по этой причине автору этой страницы (д-ру Хейну) несколько раз писали по электронной почте с энергично сформулированными просьбами ослабить язык, касающийся когнитивных последствий поражений белого вещества.Я просто сообщаю то, что говорится в литературе, и, к сожалению, «это то, что есть». Тем не менее, в ответ я скорректировал язык в некоторых местах, чтобы использовать более «академические» термины для обозначения пониженной умственной функции.
Существует огромное количество литературы о поражениях белого вещества, и здесь мы обсуждаем лишь небольшую часть из этих тысяч статей. Поскольку существует так много статей, обычно можно найти статью, подтверждающую практически любую гипотезу — это хорошо иметь в виду, читая обзоры, подобные этому.
Что вызывает эти поражения белого вещества?
Короткий ответ заключается в том, что почти все, что повреждает мозг, может вызвать поражение белого вещества.
Обычно в этих поражениях связывают «болезнь мелких сосудов» (СВД), предполагая, что небольшой кровеносный сосуд закрывается. Термин расплывчатый и может применяться как к закрытию кровеносных сосудов, так и к кровотечению. В случае ишемического (закрытого) типа СВД мозг, снабжаемый этим кровеносным сосудом, поврежден, и на последовательности FLAIR МРТ появляется белое пятно.
Гипертония (высокое кровяное давление) является «основным фактором риска» ПВМ. Alateeq et al (2012) сообщили, что «метаанализ совместимых результатов показал дозозависимую зависимость, при которой каждое одно стандартное отклонение увеличения систолического АД (САД) выше 120 мм рт.ст. связано с 11,2% (95% ДИ 2,3, 19,9, p = 0,0128) увеличение WMLs и -0,13% (95% CI -0,25, -0,023, p = 0,0183) меньший объем гиппокампа ».
PVM также связаны с курением, диабетом 2 типа и недавним ожирением.В частности, висцеральное ожирение может увеличивать глубокие поражения белого вещества из-за воспаления (Lampe et al, 2018).
Поражения белого вещества часто встречаются у людей с ВИЧ-инфекцией, даже у людей с хорошим подавлением вируса (Su et al, 2016). Haddow et al (2014) сообщили, что WML были обнаружены у 161 из 254 ВИЧ-положительных пациентов, из которых 35% имели «диффузную аномалию сигнала WM», а 24% имели паттерн, указывающий на «болезнь мелких сосудов».
Эти два изображения показывают мозжечок.Слева — изображение Flair, а справа — изображение GRE. Черные пятна «цветут» из-за железа, полученного из продуктов распада крови. Другие причины повреждения головного мозга, которые можно обнаружить на МРТ, включают кровотечения, которые также вызывают повреждение головного мозга. Эти поражения встречаются примерно у 11-23% пожилых людей, проживающих в общинах. Поскольку они содержат железо из крови, их можно отличить на МРТ от других типов повреждений, рассматривая их с помощью «последовательности», чувствительной к железу, такой как градиентное эхо (GRE) (Greenberg et al, 2009).Церебральные микрокровотечения также могут возникать в белом веществе и могут быть вызваны травмой, гипертонией или церебральным амилоидом. Как показано выше, небольшие кровотечения могут быть очень сильными на GRE (справа), но не заметны на FLAIR. Из-за «цветения» размер черных пятен на МРТ может быть больше, чем реальная площадь отложения железа. Изображения GRE с более длительным временем эхо-сигнала (например, TE> 50) могут усиливать цветение (т.е. вызывать ложные срабатывания). Церебральные микрокровотечения связаны с ускоренным снижением когнитивных функций.(Динг и др., 2017)
Как количественно определяются поражения белого вещества на МРТ
Существует множество шкал, которые в основном используются в научных исследованиях для количественной оценки поражений белого вещества. Schelten и соавторы рассмотрели 26 различных шкал в 1998 г. (Scheltens et al, 1998). В настоящее время (2019 г.) термины «легкая», «умеренная» и «тяжелая» предпочтительны с клинической точки зрения, поэтому вы можете проигнорировать этот раздел, если хотите.
ARWMC — возрастные изменения белого вещества.
Эта шкала представляет собой 4-балльную шкалу, основанную на изображениях МРТ с протонной плотностью (PD), T2 или T2-FLAIR.Изменения белого вещества были определены как «нечеткая гиперинтенсивность> = 5 мм. Лакуны были определены как четко определенные области> 2 мм с такими же характеристиками сигнала на МРТ, что и спинномозговая жидкость» (Wahlund et al, 2001)
Рейтинговая шкала ARWMC Поражения белого вещества Фронтальные, теменно-затылочные, височные, инфратенториальные / мозжечок, базальные ганглии. Левое и правое полушария оцениваются отдельно 0 Нет очагов 1 Очаговые поражения 2 Начало впадения 3 Диффузное поражение всего региона Поражения базальных ганглиев 0 Нет очагов 1 1 очаговое поражение (> = 5 мм) 2 > 1 очаговое поражение 3 Конфлюэнтные очаги Затем эта шкала дает 10 различных чисел — это 5 областей * 2 стороны.Это делает шкалу непрактичной для клиницистов, у которых нет ресурсов для подсчета 10 различных областей мозга. Вероятно, поэтому он не так популярен, как две более простые шкалы, представленные ниже.
Весы Fazekas
Более простые, но похожие шкалы включают шкалу Фазекаса, которая учитывает только 2 области мозга — (Fazekas et al, 1998). Эта шкала была самой популярной по состоянию на 2016 год.
Рейтинговая шкала Fazekas Поражения белого вещества Перивентрикулярное белое вещество (PVWM) — в основном это заболевание мелких сосудов 0 Нет очагов 1 Колпачки или карандаш-тонкая подкладка 2 Гладкий ореол 3 Нерегулярный перивентрикулярный сигнал, распространяющийся в глубокое белое вещество Глубокое белое вещество Часто они не ишемические. 0 Нет очагов 1 пункт 2 начало слияния 3 Большие сливные участки Шкала Ван Свитена
Другой подобной шкалой для оценки поражений белого вещества является шкала Ван Свитена (van Swieten et al, 1990). Эта шкала требует классификации двух областей: одна включает переднее белое вещество в срезе сосудистого сплетения, а другая — заднее белое вещество.Для МРТ было три значения: 0 (ничего или одно поражение), 1 — множественные очаговые поражения, 2, множественные сливные очаги. Затем два региона и 2 числа были добавлены вместе, чтобы получить оценку от 0 до 4. Этот довольно близок к шкале Фазекаса — он не требует различать два разных типа слияния и исключает глубокое белое вещество. Однако это кажется довольно близким к клинической шкале (ничего, легкая, умеренная, тяжелая), а преимущество клинической системы в том, что она довольно очевидна даже для людей, не являющихся радиологами.
Распространенность поражений белого вещества.
| Lin et al (2017). WML (поражения белого вещества) у 4693 госпитализированных пациентов. Здесь процент положительных результатов — это все виды WML, маленькие или большие. Кроме того, эти пациенты не считаются здоровыми. | Chowdhury et al (2011). WML у пациентов без сосудистых факторов риска. DSWMH относится к некоторому слиянию WML. Обратите внимание, что это только сливные поражения, и «точечные» поражения исключаются.Таким образом, на этом графике ситуация будет лучше, чем в исследовании Lin et al слева, которое включает все типы WML у более больных пациентов. |
От трети до 80% МРТ, сделанных у людей старше 65 лет, имеют изменения в их мозговом белом веществе (Wong et al, 2002). Другие указывают на такую высокую распространенность, как 95% в возрасте старше 60 лет (например, Lampe et al, 2018).
Частота поражений белого вещества зависит от порога сообщения о них и исследуемой популяции.Линь и др. (2017) недавно сообщили о 4683 госпитализированных китайских пациентах. Они обнаружили довольно высокую распространенность, примерно 40% -80 у лиц от 50 лет и старше. Они включали как положительных пациентов, от легких (небольшие поражения) до тяжелых (большие сливные поражения). Распространенность была выше у лиц с гипертонией, диабетом и курильщиков.
Chowdhury et al (2011) сообщили о более здоровой группе — 1108 пациентов без факторов риска сосудистых заболеваний (то есть без диабета, гипертонии). Это были испытуемые в возрасте от 50 до 70 лет.В некоторой степени аналогично Lin et al, они обнаружили довольно высокую распространенность — 39,6% для «степени 1», то есть «точечный», что означает маленький, и только 0,4% для степени 4 (большой). Они обнаружили гораздо более низкую распространенность для степени 2-3, которые были определены как поражения, имеющие некоторое слияние (т. Е. Сливающиеся вместе). Это были пациенты без факторов риска сосудистых заболеваний, и их нельзя напрямую сравнивать с предметами Lin et al, у которых действительно были факторы риска сосудов.
Wen et al (2009) сообщили о 428 людях в возрасте от 44 до 48 лет, отобранных из исследования здорового сообщества.В целом у 50,9% были поражения белого вещества. Они отметили, что «мелкие точечные или очаговые WMH часто встречаются в мозгу людей в возрасте от 40 лет и могут представлять собой раннюю стадию развития этих поражений».
Объединив эти три исследования вместе, становится ясно, что небольшие (пунктированные) поражения белого вещества чрезвычайно распространены, они обнаруживаются примерно у половины здорового населения в возрасте от 40 до 40 лет, а WML увеличивается с возрастом. Кроме того, с возрастом у людей не только появляется больше поражений белого вещества, но и WML начинает сливаться в более крупные участки (слившиеся поражения белого вещества).У людей с сосудистыми факторами риска (такими как диабет, курение, гипертония) таких поражений больше.
Причины поражения перивентрикулярного белого вещества:
Основные причины поражения перивентрикулярного белого вещества (PWM) включают: нормальные изменения от старения (тогда они называются UBO, от «неопознанных ярких объектов»), небольшие инсульты и расстройства, связанные с рассеянным склерозом (РС). ШИМ также коррелирует с витамином B6 (пиридоксином). дефицит.Фраза «нормальные изменения в результате старения» на самом деле является синонимом «мы не знаем».
Старение: Возраст, безусловно, является самой распространенной ассоциацией ШИМ. Предположительно, это явление «износа». Вы стареете, а воды под мостом становится больше. Больше колебаний артериального давления, больше шансов на закрытие мелких кровеносных сосудов, больше шансов получить травму головы, больше шансов для маленьких эмболов.
Тем не менее, хотя клиницисты часто предполагают, что изменения в мозге, подобные изменениям в мозгу других людей того же возраста, не важны, и называют их «случайными», данные показывают, что даже некоторые из этих ШИМ снижают когнитивные способности (см. Ниже).
Малые инсульты : Период гипертонии — частая причина. По опыту авторов, может быть достаточно всего нескольких дней сильной гипертонии. Это связь типа «стресс вреден для вас». Прогрессирование этих поражений также связано с вариабельностью (Liu et al, 2016). Это может означать, что в некоторых случаях причиной являются небольшие кровотечения. Существует родственное заболевание, называемое «поверхностный сидероз», вызванное церебральными кровотечениями, а также церебральными микрокровотечениями, которые кратко обсуждались выше.
Клинические исследования ШИМ также показывают связь с диабет, но не всегда с атеросклерозом. ШИМ часто наблюдаются у людей с мигренью, и возникают особенно у женщин с мигренью и аурой. (Экерманн-Хэртер и Хуанг, 2021). ШИМ также чаще встречаются у лиц с частыми обмороками и ортостатической непереносимостью (Kruit et al, 2013)
ПораженияWM связаны с микрососудистыми аномалиями сетчатки. Люди с поражениями ВМ и ретинопатией имеют гораздо более высокий риск клинический инсульт (20% против 1.4%), (Wong et al, 2002).
РС и родственные состояния : Демиелинизирующие расстройства например, рассеянный склероз и родственники могут вызывать ШИМ. Обычно они выглядят иначе на МРТ, так как они часто напоминают «пальцы», указывающие на желудочки.
К более редким причинам заболевания белого вещества относятся: «Аутоиммунные процессы, включая рассеянный склероз и родственные заболевания: опухолевидные демиелинизирующие поражения, концентрический склероз Бало, варианты Марбурга и Шильдера, оптический нейромиелит (болезнь Девича), острый диссеминированный энцефаломиелит и острая геморрагическая лейкоэнцефалопатия» .Инфекционные процессы включают болезнь Лайма (нейроборрелиоз), прогрессирующую мультифокальную лейкоэнцефалопатию и энцефалопатию, вызванную вирусом иммунодефицита человека (ВИЧ). Сосудистые процессы включают различные типы заболеваний мелких сосудов: артериолосклероз, церебральную амилоидную ангиопатию, церебральную аутосомно-доминантную артериопатию с подкорковыми инфарктами и лейкоэнцефалопатией (CADASIL), первичный ангиит центральной нервной системы, синдром Сусака и нейролупус. Токсико-метаболические процессы включают осмотический миелинолиз, лейкоэнцефалопатию метотрексатом и синдром задней обратимой энцефалопатии.(Сарбу и др., 2016). По сути, это подробный список в основном редких состояний, которые имеют небольшие практические последствия, но дают понять, что существует множество возможностей.
Среди них есть невероятно редкий семейный вариант заболевания белого вещества, называемый CADASIL. Тестирование на Мутация notch-3, вызывающая CADASIL, была произведена Афиной, среди других лабораторий. Как и в случае с большинством генетических тестов, этот тест непомерно дорог, и его результат обычно не имеет клинических последствий.
PRES (синдром обратимой задней лейкоэнцефалопатии) может вызывать аналогичные поражения белого вещества, но это состояние является острым и имеет некоторую возможность обращения.
Серьезные последствия поражения перивентрикулярного белого вещества — это самое страшное.
Имеются убедительные доказательства того, что поражения белого вещества головного мозга нарушают функцию мозга и, в частности, ухудшают способность к мышлению и ходьбе.
Дебетт и Маркус (2010) провели метаанализ 22 исследований, в которых изучалась связь гиперинтенсивности белого вещества с инсультом, снижением когнитивных функций, деменцией и смертью.Они заявили: «Гиперинтенсивность белого вещества была связана с повышенным риском инсульта (отношение рисков 3,3, 95% доверительный интервал от 2,6 до 4,4), деменции (1,9, 1,3 до 2,8) и смерти (2,0, 1,6 до 2,7)».
Поражения белого вещества сильно коррелируют со снижением скорости ходьбы, как а также снижение умственных способностей (Starr et al, 2003; Guttman et al, 2000; Whitman et al, 2001; Bazner et al, 2008). Перивентрикулярное расположение белого вещества поражения, кажется, вызывают самые серьезные последствия.Здесь мы в основном говорим о более крупных поражениях белого вещества — тех, которые «сливаются», или степени 2-3 на графике выше. Считается, что люди с одним или двумя точечными поражениями белого вещества не имеют этих проблем. Есть также группы пациентов, которые не очень хорошо попадают в классы — возможно, у них около 40 точечных очагов. Вероятно, они принадлежат к группе степени 2 (частично сливной). Мы думаем, что есть место для разработки другого критерия — возможно, процента белого вещества, занятого поражениями.
Физические лица с Поражения ПВМ демонстрируют почти на 1 стандартное отклонение (СО) ниже среднего при выполнении заданий. вовлекающая психомоторную скорость. Лица с тяжелой перивентрикулярной WVL выполняют примерно на 1 стандартное отклонение ниже, чем средние субъекты, в задачах, связанных с психомоторной скоростью, и примерно на 0,5 SD ниже в отношении общей когнитивной функции (De Groot et al, 2000). Чтобы выразить это в более привычных терминах, по тесту IQ 1 стандартное отклонение составляет 15 баллов. Даже «тихие» поражения белого вещества у пациентов с гипертонией среднего возраста предсказывают снижение внимания (Sierra et al, 2014).Тяжелые поражения белого вещества указывают на плохую повседневную активность (Yamashita et al, 2016).
Лакуны (то есть дыры в мозгу) также связаны с когнитивными нарушениями (Jokinen et al, 2011).
Сообщается, что глубокие поражения белого вещества даже более обременительны для познания, чем поражения перивентрикулярного белого вещества (Soriano-Raya et al, 2012). К счастью, это относительно редко. Они больше связаны с висцеральным ожирением, чем с гипертонией (Lampe et al, 2018).
По данным Degroot et al (2002), «после поправки на возраст, пол, уровень образования, показатели депрессии, атрофии мозга и инфарктов, субъектов с тяжелыми перивентрикулярными поражениями белого вещества испытали когнитивное снижение почти в три раза быстрее», чем в среднем «. Это неудивительно, поскольку люди с тяжелой формой ПВМ испытали сильное повреждение головного мозга.
Ускорение бремени гиперинтенсивности белого вещества — это патологическое изменение, которое возникает на ранней стадии пресимптоматической фазы и приводит к легкому когнитивному ухудшению .Фактически, в среднем ускорение происходит за 10 лет до появления легких когнитивных нарушений. (Силберт и др., 2012). Достаточно всего 3% бремени лейкоариоза (процент поражения белого вещества мозга), чтобы снизить показатели рабочей памяти на 2 стандартных отклонения (Price et al, 2012). Нагрузка на 3% на МРТ — это количество ПВМ, обычно называемое «умеренным» в отчетах МРТ.
Если рассматривать походку и равновесие, большее количество поражений белого вещества прогнозирует снижение подвижности (Onen et al, 2004). Согласно недавнему исследованию Базнер, замедление ходьбы не экстремальное — пожилые люди примерно на 20% медленнее с большим # PVM, чем с маленьким #.Казалось бы нам, что люди могут просто быть более осторожными и идти медленнее, когда они более склонны к падению. (2008)
Обращение:
- Контролировать факторы риска сердечно-сосудистых заболеваний — особенно лабильную (вариабельную) артериальную гипертензию.
- Пиридоксин (витаминная) добавка (но будьте осторожны, потому что пиридоксин может вызвать невропатию)
- Профилактика мигрени — особенно «сосудистые» агенты, такие как верапамил и бета-адреноблокаторы
- «Познавательно-сложный» досуг.
- Физиотерапия — особенно консультирование по вопросам падения
- Корректировка медикаментов
На практике PVM, кажется, имеет серьезные последствия. В качестве когда они у вас есть, они остаются там на всю жизнь, профилактика — главное цель лечения.
Основные сосудистые факторы риска заболевания белого вещества включают:
- гипертония
- курение
- Сахарный диабет 2 типа
- ожирение, особенно висцеральное.
Мы призываем обратить внимание на снижение сосудистых факторов риска, и особенно контролируя как статическую (постоянную), так и лабильную (то есть быстро меняющуюся) артериальную гипертензию. Гипертоническая болезнь «белого халата » является разновидностью лабильной гипертонии . Таким образом, если ваше кровяное давление «только на приеме у врача», это не означает, что вы в безопасности от ПВМ. Может помочь бета-блокатор. Интенсивный контроль артериального давления (определяемый как «нацеливание» на АД <120) был связан с меньшим увеличением поражений белого вещества у 449 пациентов с гипертонией в возрасте старше 50 лет (Sprint group, 2019).Hughes et al (2020) сообщили, что снижение артериального давления с помощью гипотензивных средств по сравнению с контролем было значительно связано со снижением риска деменции или когнитивных нарушений. Согласно Croall et al (2018), «интенсивное снижение АД не снижает церебральную перфузию при тяжелой болезни мелких сосудов». По нашему мнению, интенсивный контроль артериального давления в целом является хорошей идеей, хотя применим не ко всем.
Возможно, поможет строгий контроль диабета. Это означает нормализацию гемоглобина A1C — скажем, около 6.5 или ниже.
Снижение количества потребляемых калорий до тех пор, пока ИМТ не станет нормальным, является разумным. Физическая подготовка слабо связана с улучшением состояния белого вещества (Sexton et al, 2016).
Редуктор повышенный холестерин, вероятно, тоже полезен.
Другие вещи, которые вы можете делать без особых доказательств, включают:
Малый количество добавок витамина b6 (пиридоксина) является разумным (т.е. 2 мг / день).
Познавательно сложный досуг (т.е. делать что-то сложное в свободное время) ассоциируется с лучшей умственной работоспособностью у людей с поражениями белого вещества (Saccynski et al, 2008). Безусловно, вашему мозгу лучше быть физически активным, и, вероятно, лучше поддерживать его в активном состоянии.
Неясно, полезно ли ежедневное потребление аспирина или вредны для людей с PVM, и, по нашему мнению, решение должно быть изготавливается в индивидуальном порядке. Людям с кровотечением, вероятно, не следует принимать аспирин.Другими словами, чтобы принять это решение, необходима МРТ. Бета-блокаторы, такие как пропранолол и родственные лекарства могут быть особенно подходящими для предотвращения спайков в артериальном давлении. Эти препараты также обладают кардиозащитным действием. Другими словами, если у кого-то есть «гипертония белого халата», стоит подумать о бета-блокаторах. Здесь было бы полезно больше данных, так как это просто предположение.
Людям с мигренью и большим количеством поражений белого вещества мы обычно предлагаем профилактический режим, например как комбинация низких доз аспирина и средства профилактики мигрени такие как верапамил.Неизвестно, подходит ли данная схема лечения. эффективный. Бета-блокаторы также кажутся очень разумными в этой ситуации.
Лечение демиелинизирующих заболеваний, таких как рассеянный склероз, может быть подходящим, но выходит за рамки этого краткого обзора.
Что касается распространенного симптома неустойчивости, эмпирическое лечение, включая физическое терапия. Однако физиотерапия не избавит от этих проблем.
Хотя обычно лекарства не помогают в ситуациях, когда клетчатка тракты или нейроны погибли (т.е. PVM), в отдельных случаях — испытания лекарства, такие как антидепрессанты или противопаркинсонические препараты, полезный. Опять же, лекарства не улучшат вашу МРТ или избавят от уже нанесенных повреждений.
Мы считаем маловероятным, что какое-либо лечение будет успешным в обращение вспять умственного замедления, связанного с ПВМ. Однако может быть немного места для корректировки лекарств, которые замедляют мышление самостоятельно — например, лекарства от головокружения (например,грамм. меклизин или клоназепам) и заменяя их лекарствами, которые не ухудшают мышление (например, бетагистин).
Артикул:
- Alateeq, K., et al. (2021 г.). «Повышенное кровяное давление связано с более серьезными поражениями белого вещества и атрофией мозга: систематический обзор с помощью метаанализа». J Clin Med 10 (4).
- Baszner H и многие другие. Связь нарушений походки и равновесия с возрастные изменения белого вещества. Исследование LADIS.Неврология 2008: 70: 935-942 (Комментарий: это очень большое исследование, показывающее, что ПВМ связаны с нарушением равновесия и снижением скорости ходьбы).
- Baloh RW, Sloane PD и Honrubia V: Количественное тестирование вестибулярной функции у пожилых пациентов с головокружением. Ухо, нос и горло 1989; 68: 935-939.
- Белал А., Глориг А. Нарушение равновесия старения (пресбиастаз). Дж Ларингол Отол 1986; 100: 1037-41.
- Чоудхури, М.H., et al. (2011). «Возрастные изменения в поражениях белого вещества, атрофии гиппокампа и церебральных микрокровотечениях у здоровых субъектов без основных факторов риска цереброваскулярных заболеваний». J Stroke Cerebrovasc Dis 20 (4): 302-309.
- Croall, I. D., et al. (2018). «Влияние стандартного и интенсивного контроля артериального давления на церебральный кровоток при заболевании мелких сосудов: рандомизированное клиническое испытание PRESERVE». JAMA Neurol 75 (6): 720-727.
- Де Гроот и другие. Поражения белого вещества головного мозга и когнитивные функции: исследование Rotterdam Scan.Энн Нейрол 2000: 47: 145-151.
- De Groot, J. C., et al. (2002). «Перивентрикулярные поражения белого вещества головного мозга предсказывают скорость снижения когнитивных функций». Энн Нейрол 52 (3): 335-341.
- Debette, S., et al. (2007). «Подкорковая гиперинтенсивность связана с когнитивным снижением у пациентов с легкими когнитивными нарушениями». Ход 38 (11): 2924-2930.
- Ding, J., et al. (2017). «Место и место возникновения церебральных микрокровоизлияний, снижения когнитивных способностей и деменции в обществе.»Неврология 88 (22): 2089-2097.
- Эйкерманн-Хэртер, К. и С. Ю. Хуанг (2021 г.). «Поражения белого вещества при мигрени». Am J Pathol.
- Fazekas, F., et al. (1998). «Спектр возрастных аномалий мозга: их измерение и гистопатологические корреляты». Приложение J Neural Transm 53: 31-39.
- Файф ТД, Балох RW. Нарушение равновесия у пожилых людей по неизвестным причинам. Анна Neurol 1993; 34: 594-702.
- Гринберг С.М. и др. Церебральные микрокровоизлияния: практическое руководство по их обнаружению и интерпретации, для группы изучения микрокровоизлияний Lancet Neurol.2009 фев; 8 (2): 165–174. DOI: [10.1016 / S1474-4422 (09) 70013-4] PMCID: PMC3414436 NIHMSID: NIHMS348039 PMID: 108
- Guttmann CRG и другие. Нарушения белого вещества с нарушением подвижности пожилые люди. Неврология 2000: 54, 1277-1283
- Haddow, L.J., et al. (2014). «Поперечное исследование необъяснимых поражений белого вещества у ВИЧ-положительных людей, которым проводится магнитно-резонансная томография головного мозга». Уход за больными СПИДом STDS 28 (7): 341-349.
- Hughes D и другие.Связь снижения артериального давления с деменцией или когнитивными нарушениями. Системный обзор и метаанализ. JAMA 2020; 323 (19) 1934-1944, 2020.
- Инзитари Д. Возрастные изменения белого вещества и когнитивные нарушения (От редакции). Энн Нейрол 47,2, 2000 г., стр. 141-142
- Йокинен Х и многие другие. Пробелы в происшествии влияют на снижение когнитивных функций. Кабинет Ладиса. Неврология 201: 76: 1872-1878
- Кербер К.А., Энриетто Дж. А., Якобсон Б. А., Бало Р. В..Нарушение равновесия у пожилых люди. Перспективное исследование. Неврология 1998: 51: 574-580
- Kruit MC и другие. Обморок и ортостатическая непереносимость повышают риск поражения головного мозга у мигрени и контрольной группы. Неврология 2013; 80: 1958-1965
- Lampe, L., et al. (2019). «Висцеральное ожирение связано с гиперинтенсивностью глубокого белого вещества через воспаление». Энн Нейрол 85 (2): 194-203.
- Lin, Q., et al. (2017). «Заболеваемость и факторы риска лейкоареоза у 4683 госпитализированных пациентов: перекрестное исследование.»Медицина (Балтимор) 96 (39): e7682.
- Liu, Z., et al. (2016). «Чрезмерная вариабельность систолического артериального давления, которое измеряется самостоятельно в домашних условиях, усугубляет прогрессирование поражения белого вещества мозга и когнитивных нарушений у пожилых людей». Hypertens Res 39 (4): 245-253.
- Миллер Дж. В., Грин Р., Мунгас Д. М. и др. Гомоцистеин, витамин B6 и сосудистые заболевание у пациентов с БА. Неврология, 2002, 58: 1471-1475
- Onen, F., et al. (2004). «Лейкоареоз и снижение подвижности: исследование магнитно-резонансной томографии высокого разрешения у пожилых людей с легкими когнитивными нарушениями.»Neurosci Lett 355 (3): 185-188.
- Цена CC и многие другие. Пороги МРТ-лейкоареоза и фенотипическое проявление деменции. Неврология 2012; 79: 734-740.
- Snakeskin, J. S., et al. (2008). «Повреждения белого вещества и когнитивные способности: роль когнитивно сложной досуговой деятельности». Дж. Геронтол Биол Науки Мед Науки 63 (8): 848-854.
- Sarbu, N., et al. (2016). «Болезни белого вещества с радиолого-патологической корреляцией». Радиография 36 (5): 1426-1447.
- Scheltens, P., et al. (1998). «Изменения белого вещества на КТ и МРТ: обзор шкал оценки зрения. Европейская целевая группа по возрастным изменениям белого вещества». Eur Neurol 39 (2): 80-89. Sexton, C.E., et al. (2016). «Систематический обзор исследований МРТ, изучающих взаимосвязь между физической подготовкой и активностью и белым веществом стареющего мозга». Нейроизображение 131: 81-90.
- Sierra, C., et al. (2004). «Бесшумные поражения белого вещества головного мозга и когнитивные функции у пациентов с гипертонической болезнью среднего возраста.»Am J Hypertens 17 (6): 529-534.
- Silbert LC и многие другие. Траектория бремени гиперинтенсивности белого вещества, предшествующей легкому когнитивному нарушению. Неврология 2012; 79: 741-47
- Сориано-Рая, Дж. Дж. И др. (2012). «Глубокие поражения белого вещества по сравнению с перивентрикулярными и когнитивные функции в выборке участников среднего возраста». J Int Neuropsychol Soc 18 (5): 874-885.
- Sprint MINDvestigators (2019). «Ассоциация интенсивного и стандартного контроля артериального давления с поражением белого вещества головного мозга.»JAMA 322 (6): 524-534.
- Старр JM, S A Leaper, A D Murray, H A Lemmon, R T Staff, I J Deary, L J Уолли. Поражения белого вещества головного мозга, обнаруженные с помощью магнитного резонанса визуализация связаны с балансом и скоростью походки. J Neurol Neurosurg Психиатрия 2003;
- Su, T., et al. (2016). «Изменения структуры белого вещества у ВИЧ-1-инфицированных мужчин с устойчивым подавлением виремии при лечении». СПИД 30 (2): 311-322.
- van Swieten, J. C., et al. (1990). «Оценка поражений белого вещества на КТ и МРТ: простая шкала.»J Neurol Neurosurg Psychiatry 53 (12): 1080-1083.
- Wahlund, L.O., et al. (2001). «Новая шкала оценки возрастных изменений белого вещества, применимая к МРТ и КТ». Ход 32 (6): 1318-1322.
- Wen, W., et al. (2009). «Гиперинтенсивность белого вещества в сороковых годах: их распространенность и топография в эпидемиологической выборке в возрасте 44-48 лет». Hum Brain Mapp 30 (4): 1155-1167.
- Whitman GT и другие. Невропатология у пожилых людей с нарушением равновесия по неизвестной причине.Неврология, 1999, 53, 375-382
- Whitman GT и другие. Проспективное исследование аномалий белого вещества головного мозга у пожилых людей с нарушением походки. Неврология 2001: 57: 990-994
- Wong TY et al. Поражения белого вещества головного мозга, ретинопатия и частота клинический инсульт. Джама 2002 288: 67-74
- Yamashita, Y., et al. (2016). «Влияние поражения белого вещества головного мозга на повседневную жизнь пожилых пациентов с легким инсультом.»Гериатр Геронтол Инт 16 (8): 942-947.
Соответствует ли гиперинтенсивность белого вещества мозга T2 / FLAIR потере миелина при нормальном старении? Рентгенологически-невропатологическое корреляционное исследование | Acta Neuropathologica Communications
Garde E, Mortensen EL, Krabbe K, Rostrup E, Larsson HB: Связь между возрастным снижением интеллекта и гиперинтенсивностью белого вещества головного мозга у здоровых восьмидесятилетних людей: продольное исследование. Lancet 2000, 356: 628–634.10.1016 / S0140-6736 (00) 02604-0
CAS Статья PubMed Google ученый
Ylikoski A, Erkinjuntti T, Raininko R, Sarna S, Sulkava R, Tilvis R: Гиперинтенсивность белого вещества на МРТ у неврологически здоровых пожилых людей. Анализ когорт последовательных субъектов в возрасте от 55 до 85 лет, живущих дома. Инсульт 1995, 26: 1171–1177. 10.1161 / 01.STR.26.7.1171
CAS Статья PubMed Google ученый
Debette S, Markus HS: Клиническое значение гиперинтенсивности белого вещества при магнитно-резонансной томографии головного мозга: систематический обзор и метаанализ. BMJ 2010, 341: c3666. 10.1136 / bmj.c3666
PubMed Central Статья PubMed Google ученый
Launer LJ: Эпидемиология поражений белого вещества. Верхняя магнитно-резонансная томография 2004, 15: 365–367.10.1097 / 01.rmr.0000168216.98338.8d
Артикул PubMed Google ученый
Xekardaki A, Santos M, Hof P, Kovari E, Bouras C, Giannakopoulos P: Невропатологические субстраты и структурные изменения депрессии позднего возраста: влияние сосудистой нагрузки. Acta Neuropathol 2012, 124 (4): 453. 10.1007 / s00401-012-1021-5
Артикул PubMed Google ученый
Сантос М., Ковари Э., Хоф П.Р., Голд Дж., Бурас С., Джаннакопулос P: Влияние сосудистой нагрузки на депрессию в позднем возрасте. Brain Res Rev. 2009, 62: 19–32. 10.1016 / j.brainresrev.2009.08.003
PubMed Central Статья PubMed Google ученый
Schmidt R, Berghold A, Jokinen H, Gouw AA, van der Flier WM, Barkhof F: Прогрессирование поражения белого вещества у женщин: частота, клинические эффекты и расчеты размера выборки. Ход поршня 2012, 43 (10): 2643. 10.1161 / STROKEAHA.112.662593
Артикул PubMed Google ученый
Kim JH, Hwang KJ, Kim JH, Lee YH, Rhee HY, Park KC: Региональная гиперинтенсивность белого вещества при нормальном старении, однодоменное амнестическое легкое когнитивное нарушение и легкая болезнь Альцгеймера. Дж. Clin Neurosci 2011, 18: 1101–1106. 10.1016 / j.jocn.2011.01.008
Артикул PubMed Google ученый
Smith EE, Salat DH, Jeng J, McCreary CR, Fischl B, Schmahmann JD: Корреляция между местоположением поражения белого вещества при МРТ и исполнительной функцией и эпизодической памятью. Неврология 2011, 76: 1492–1499. 10.1212 / WNL.0b013e318217e7c8
PubMed Central CAS Статья PubMed Google ученый
Yoshita M, Fletcher E, Harvey D, Ortega M, Martinez O, Mungas DM: Степень и распределение гиперинтенсивности белого вещества при нормальном старении, MCI и AD. Неврология 2006, 67: 2192–2198. 10.1212 / 01.wnl.0000249119.95747.1f
PubMed Central CAS Статья PubMed Google ученый
Кришнан М.С., О’Брайен Дж. Т., Фирбанк М. Дж., Пантони Л., Карлуччи Г., Эркинджунтти Т: Взаимосвязь между перивентрикулярными поражениями и поражениями глубокого белого вещества и депрессивными симптомами у пожилых людей.Исследование LADIS. Int J Geriatr Psychiatry 2006, 21: 983–989. 10.1002 / gps.1596
Артикул PubMed Google ученый
Херрманн Л.Л., Ле Мазурье М., Эбмайер КП: Гиперинтенсивность белого вещества при депрессии позднего возраста: систематический обзор. J Neurol Neurosurg Psychiatry 2008, 79: 619–624.
CAS Статья PubMed Google ученый
Gouw AA, Seewann A, van der Flier WM, Barkhof F, Rozemuller AM, Scheltens P: Гетерогенность болезни мелких сосудов: систематический обзор корреляций МРТ и гистопатологии. J Neurol Neurosurg Psychiatry 2011, 82: 126–135. 10.1136 / jnnp.2009.204685
Статья PubMed Google ученый
Ямамото Ю., Ихара М., Тхам С., Лоу RW, Слэйд Дж., Мосс T: Невропатологические корреляты гиперинтенсивности белого вещества височного полюса у CADASIL. Инсульт 2009, 40: 2004–2011. 10.1161 / STROKEAHA.108.528299
PubMed Central Статья PubMed Google ученый
Фолштейн М.Ф., Фолштейн С.Е., МакХью ПР: «Мини-психическое состояние». Практический метод оценки когнитивного состояния пациентов для клинициста. J Psychiatr Res 1975, 12: 189–198. 10.1016 / 0022-3956 (75) -6
CAS Статья PubMed Google ученый
Giannakopoulos P, Gold G, Kovari E, von Gunten A, Imhof A, Bouras C: Оценка когнитивного воздействия патологии болезни Альцгеймера и сосудистой нагрузки на стареющий мозг: опыт Женевы. Acta Neuropathol 2007, 113: 1–12.
Артикул PubMed Google ученый
Braak H, Braak E: Невропатологическая стадия изменений, связанных с болезнью Альцгеймера. Acta Neuropathol 1991, 82: 239–259.10.1007 / BF00308809
CAS Статья PubMed Google ученый
МакКейт И.Г., Галаско Д., Косака К., Перри Е.К., Диксон Д.В., Хансен Л.А.: Консенсусное руководство по клинической и патологической диагностике деменции с тельцами Леви (DLB): отчет консорциума о международном семинаре DLB . Неврология 1996, 47: 1113–1124. 10.1212 / WNL.47.5.1113
CAS Статья PubMed Google ученый
Fazekas F, Chawluk JB, Alavi A, Hurtig HI, Zimmerman RA: Нарушения сигнала MR при 1,5 Тл при деменции Альцгеймера и нормальном старении. AJR Am J Roentgenol 1987, 149: 351–356. 10.2214 / ajr.149.2.351
CAS Статья PubMed Google ученый
Ковари Э., Голд Дж., Херрманн Ф.Р., Кануто А., Хоф П.Р., Бурас С: Кортикальные микроинфаркты и демиелинизация влияют на когнитивные функции в случаях с высоким риском деменции. Неврология 2007, 68: 927–931. 10.1212 / 01.wnl.0000257094.10655.9a
CAS Статья PubMed Google ученый
Scheltens P, Barkhof F, Leys D, Wolters EC, Ravid R, Kamphorst W: Гистопатологические корреляты изменений белого вещества на МРТ при болезни Альцгеймера и нормальном старении. Неврология 1995, 45: 883–888. 10.1212 / WNL.45.5.883
CAS Статья PubMed Google ученый
Landis JR, Koch GG: Измерение согласия наблюдателя для категориальных данных. Биометрия 1977, 33: 159–174. 10.2307 / 2529310
CAS Статья PubMed Google ученый
Pantoni L, Garcia JH: Патогенез лейкоареоза: обзор. Инсульт 1997, 28: 652–659. 10.1161 / 01.STR.28.3.652
CAS Статья PubMed Google ученый
O’Sullivan M, Lythgoe DJ, Pereira AC, Summers PE, Jarosz JM, Williams SC: Паттерны снижения мозгового кровотока у пациентов с ишемическим лейкоареозом. Неврология 2002, 59: 321–326. 10.1212 / WNL.59.3.321
Артикул PubMed Google ученый
Topakian R, Barrick TR, Howe FA, Markus HS: Проницаемость гематоэнцефалического барьера увеличивается в нормальном белом веществе у пациентов с лакунарным инсультом и лейкоареозом. J Neurol Neurosurg Psychiatry 2010, 81: 192–197. 10.1136 / jnnp.2009.172072
CAS Статья PubMed Google ученый
Fazekas F, Kleinert R, Offenbacher H, Schmidt R, Kleinert G, Payer F: Патологические корреляты случайных гиперинтенсивностей сигналов МРТ белого вещества. Неврология 1993, 43: 1683–1689. 10.1212 / WNL.43.9.1683
CAS Статья PubMed Google ученый
Grafton ST, Sumi SM, Stimac GK, Alvord ECJ, Shaw CM, Nochlin D: Сравнение посмертной магнитно-резонансной томографии и невропатологических данных в белом веществе головного мозга. Arch Neurol 1991, 48: 293–298. 10.1001 / archneur.1991.00530150061019
CAS Статья PubMed Google ученый
van Swieten JC, van den Hout JH, van Ketel BA, Hijdra A, van Wokke JH, Gijn J: Перивентрикулярные поражения в белом веществе на магнитно-резонансной томографии у пожилых людей.Морфометрическая корреляция с артериолосклерозом и расширенными периваскулярными пространствами. Мозг 1991, 114: 761–774. 10.1093 / brain / 114.2.761
Статья PubMed Google ученый
Young VG, Halliday GM, Kril JJ: Невропатологические корреляты гиперинтенсивности белого вещества. Неврология 2008, 71: 804–811. 10.1212 / 01.wnl.0000319691.50117.54
Артикул PubMed Google ученый
Platt J: Последовательная минимальная оптимизация: быстрый алгоритм для обучения опорных векторных машин. Достижения в методах ядра — обучение векторов поддержки 1999, 208: 1-21.
Google ученый
Haller S, Lovblad KO, Giannakopoulos P: Принципы классификационного анализа при легких когнитивных нарушениях (MCI) и болезни Альцгеймера. J Alzheimers Dis 2011, 26 (Приложение 3): 389–394.
PubMed Google ученый
Дуэк П., Тернер Р., Пекар Дж., Ле Патронас Н., Бихан Д.: МР-цветовое картирование ориентации миелиновых волокон. J Comput Assist Tomogr 1991, 15: 923–929. 10.1097 / 00004728-19
CAS Статья PubMed Google ученый
Moseley ME, Cohen Y, Kucharczyk J, Mintorovitch J, Asgari HS, Wendland MF: Диффузионно-взвешенная МРТ-визуализация анизотропной диффузии воды в центральной нервной системе кошек. Радиология 1990, 176: 439–445.
CAS Статья PubMed Google ученый
Wolff SD, Balaban RS: Контраст переноса намагниченности (MTC) и релаксация протонов воды в тканях in vivo. Magn Reson Med 1989, 10: 135–144. 10.1002 / mrm.1
0113CAS Статья PubMed Google ученый
Murray ME, Senjem ML, Petersen RC, Hollman JH, Preboske GM, Weigand SD: Функциональное влияние гиперинтенсивности белого вещества у когнитивно нормальных пожилых людей. Arch Neurol 2010, 67: 1379–1385. 10.1001 / archneurol.2010.280
PubMed Central Статья PubMed Google ученый
Верноой М.В., Икрам М.А., Вроуман Х.А., Велополски П.А., Крестин Г.П., Хофман A: Микроструктурная целостность белого вещества и когнитивные функции у пожилого населения в целом. Arch Gen Psychiatry 2009, 66: 545–553. 10.1001 / archgenpsychiatry.2009.5
Статья PubMed Google ученый
de Groot JC, de Leeuw FE, Oudkerk M, Hofman A, Jolles J, Breteler MM: Поражения белого вещества головного мозга и депрессивные симптомы у пожилых людей. Arch Gen Psychiatry 2000, 57: 1071–1076. 10.1001 / archpsyc.57.11.1071
CAS Статья PubMed Google ученый
Schmidt R, Petrovic K, Ropele S, Enzinger C, Fazekas F: Развитие лейкоареоза и познание. Инсульт 2007, 38: 2619–2625. 10.1161 / STROKEAHA.107.489112
Артикул PubMed Google ученый
Повреждение белого вещества у доношенных новорожденных с неонатальной энцефалопатией
Индер Т.Э., Андерсон, Нью-Джерси, Спенсер С., Уэллс С., Вольпе Дж. . AJNR Am J Neuroradiol 24 : 805–809
PubMed Google ученый
Miller SP, Cozzio CC, Goldstein RB, Ferriero DM, Partridge JC, Vigneron DB, Barkovich AJ 2003 Сравнение диагностики повреждения белого вещества у недоношенных новорожденных с результатами серийной МРТ и трансфонтанальной ультрасонографии. AJNR Am J Neuroradiol 24 : 1661–1669
PubMed Google ученый
Miller SP, Ferriero DM, Leonard C, Piecuch R, Glidden DV, Partridge JC, Perez M, Mukherjee P, Vigneron DB, Barkovich AJ 2005 Раннее повреждение головного мозга у недоношенных новорожденных, обнаруженное с помощью магнитно-резонансной томографии, связано с неблагоприятными ранний исход нервного развития. J Pediatr 147 : 609–616
Артикул Google ученый
Maalouf EF, Duggan PJ, Counsell SJ, Rutherford MA, Cowan F, Azzopardi D, Edwards AD 2001 Сравнение результатов ультразвукового исследования черепа и магнитно-резонансной томографии у недоношенных детей. Педиатрия 107 : 719–727
CAS Статья Google ученый
Корнетт Л.Г., Таннер С.Ф., Раменги Л.А., Миалл Л.С., Чайлдс А.М., Артур Р.Дж., Мартинес Д., Левен М.И. 2002 Магнитно-резонансная томография головного мозга младенца: анатомические характеристики и клиническое значение точечных поражений. Arch Dis Child Fetal Neonatal Ed 86 : F171 – F177
CAS Статья Google ученый
Dyet LE, Kennea N, Counsell SJ, Maalouf EF, Ajayi-Obe M, Duggan PJ, Harrison M, Allsop JM, Hajnal J, Herlihy AH, Edwards B, Laroche S, Cowan FM, Rutherford MA, Edwards AD 2006 г. Естественная история поражений головного мозга у крайне недоношенных новорожденных, изученных с помощью серийной магнитно-резонансной томографии с рождения и оценки нервного развития. Педиатрия 118 : 536–548
Статья Google ученый
Woodward LJ, Anderson PJ, Austin NC, Howard K, Inder TE 2006 МРТ новорожденных для прогнозирования исходов развития нервной системы у недоношенных детей. N Engl J Med 355 : 685–694
CAS Статья Google ученый
McQuillen PS, Sheldon RA, Shatz CJ, Ferriero DM 2003 Избирательная уязвимость субпластинчатых нейронов после ранней неонатальной гипоксии-ишемии. J Neurosci 23 : 3308–3315
CAS Статья Google ученый
Follett PL, Rosenberg PA, Volpe JJ, Jensen FE 2000 NBQX ослабляет эксайтотоксическое повреждение в развивающемся белом веществе. J Neurosci 20 : 9235–9241
CAS Статья Google ученый
Back SA, Gan X, Li Y, Rosenberg PA, Volpe JJ 1998 Зависимая от созревания уязвимость олигодендроцитов к смерти, вызванной окислительным стрессом, вызванной истощением глутатиона. J Neurosci 18 : 6241–6253
CAS Статья Google ученый
Riddle A, Luo NL, Manese M, Beardsley DJ, Green L, Rorvik DA, Kelly KA, Barlow CH, Kelly JJ, Hohimer AR, Back SA 2006 Предсказывает пространственную неоднородность созревания линии олигодендроцитов, а не церебральный кровоток повреждение перивентрикулярного белого вещества у плода овцы. J Neurosci 26 : 3045–3055
CAS Статья Google ученый
Kinney HC, Panigrahy A, Newburger JW, Jonas RA, Sleeper LA 2005 Гипоксически-ишемическое повреждение головного мозга у младенцев с врожденным пороком сердца, умирающих после кардиохирургии. Acta Neuropathol 110 : 563–578
Статья Google ученый
Маккуиллен П.С., Баркович А.Дж., Хамрик С.Е., Перес М., Уорд П., Глидден Д.В., Азаки А., Карл Т., Миллер С.П. 2007 Профиль временного и анатомического риска повреждения головного мозга при неонатальном восстановлении врожденных пороков сердца. Инсульт 38 : 736–741
Артикул Google ученый
Galli KK, Zimmerman RA, Jarvik GP, Wernovsky G, Kuypers MK, Clancy RR, Montenegro LM, Mahle WT, Newman MF, Saunders AM, Nicolson SC, Spray TL, Gaynor JW 2004 Распространенная перивентрикулярная лейкомаляция операция на сердце. J Thorac Cardiovasc Surg 127 : 692–704
Артикул Google ученый
Miller SP, McQuillen PS, Hamrick S, Xu D, Glidden DV, Charlton N, Karl T., Azakie A, Ferriero DM, Barkovich AJ, Vigneron DB 2007 Аномальное развитие мозга у новорожденных с врожденным пороком сердца. N Engl J Med 357 : 1928–1938
CAS Статья Google ученый
Cowan F, Rutherford M, Groenendaal F, Eken P, Mercuri E, Bydder GM, Meiners LC, Dubowitz LM, de Vries LS 2003 Происхождение и время поражения головного мозга у доношенных детей с неонатальной энцефалопатией. Ланцет 361 : 736–742
Артикул Google ученый
Rutherford M, Counsell S, Allsop J, Boardman J, Kapellou O, Larkman D, Hajnal J, Edwards D, Cowan F 2004 Диффузионно-взвешенная магнитно-резонансная томография при перинатальной травме головного мозга: сравнение с местом поражения и время от рождения. Педиатрия 114 : 1004–1014
Статья Google ученый
Сарджент М.А., Поскитт К.Дж., Роланд Э.Х., Хилл А., Хендсон Г. 2004 Атрофия вермиана мозжечка после неонатальной гипоксически-ишемической энцефалопатии. AJNR Am J Neuroradiol 25 : 1008–1015
PubMed Google ученый
Chau V, Poskitt KJ, Sargent MA, Lupton BA, Hill A, Roland E, Miller SP Сравнение компьютерной томографии и МРТ на третий день жизни доношенных новорожденных с неонатальной энцефалопатией. Pediatrics , in press
Kaufman SA, Miller SP, Ferriero DM, Glidden DH, Barkovich AJ, Partridge JC 2003 Энцефалопатия как предиктор аномалий магнитно-резонансной томографии у новорожденных с асфиксией. Pediatr Neurol 28 : 342–346
Артикул Google ученый
Миллер С.П., Латал Б., Кларк Х., Барнуэлл А., Глидден Д., Баркович А.Дж., Ферриеро Д.М., Партридж Дж. К. 2004. Клинические признаки позволяют прогнозировать 30-месячный исход развития нервной системы после неонатальной энцефалопатии. Am J Obstet Gynecol 190 : 93–99
Артикул Google ученый
Miller SP, Weiss J, Barnwell A, Ferriero DM, Latal-Hajnal B, Ferrer-Rogers A, Newton N, Partridge JC, Glidden DV, Vigneron DB, Barkovich AJ 2002 Судорожно-мозговая травма у доношенных новорожденных при перинатальной асфиксии. Неврология 58 : 542–548
CAS Статья Google ученый
Луптон Б.А., Хилл А., Роланд Э.Х., Уитфилд М.Ф., Флодмарк О. 1988 Набухание мозга у доношенных новорожденных после асфиксии: патогенез и исход. Педиатрия 82 : 139–146
CAS PubMed Google ученый
Баркович А.Дж., Миллер С.П., Барта А., Ньютон Н., Хамрик С.Е., Мукерджи П., Гленн О.А., Сюй Д., Партридж Дж.С., Ферриеро Д.М., Vigneron DB 2006 МР-визуализация, МР-спектроскопия и диффузионно-тензорная визуализация последовательного исследования новорожденных с энцефалопатией. AJNR Am J Нейрорадиол 27 : 533–547
CAS Google ученый
Баркович А.Дж., Хайнал Б.Л., Виньерон Д., Сола А., Партридж Дж.К., Аллен Ф., Ферриеро Д.М. 1998 Прогнозирование нейромоторного исхода при перинатальной асфиксии: оценка систем оценки МРТ. AJNR Am J Neuroradiol 19 : 143–149
CAS PubMed Google ученый
Миллер С.П., Рамасвами В., Михельсон Д., Баркович А.Дж., Холшаузер Б., Уиклифф Н., Глидден Д.В., Деминг Д., Партридж Дж.С., Ву Ю.В., Ашвал С., Ферриеро Д.М. 2005 Паттерны черепно-мозговой травмы при неонатальной энцефалопатии. J Pediatr 146 : 453–460
Артикул Google ученый
Volpe JJ 2001 Неврология новорожденного. Филадельфия: W. B. Saunders Company
Maalouf EF, Duggan PJ, Rutherford MA, Counsell SJ, Fletcher AM, Battin M, Cowan F, Edwards AD 1999 Магнитно-резонансная томография головного мозга в группе чрезвычайно недоношенных младенцев. J Педиатр 135 : 351–357
CAS Статья Google ученый
Ramenghi LA, Fumagalli M, Righini A, Bassi L, Groppo M, Parazzini C, Bianchini E, Triulzi F, Mosca F 2007 Оценка созревания мозга недоношенных новорожденных с точечными поражениями белого вещества с помощью магнитно-резонансной томографии. Нейрорадиология 49 : 161–167
Статья Google ученый
Back SA, Luo NL, Borenstein NS, Levine JM, Volpe JJ, Kinney HC 2001 Поздние предшественники олигодендроцитов совпадают с периодом развития уязвимости для перинатального повреждения белого вещества человека. J Neurosci 21 : 1302–1312
CAS Статья Google ученый
Костович И., Иуда М., Радос М., Храбак П. 2002 Ламинарная организация головного мозга плода человека, выявленная с помощью гистохимических маркеров и магнитно-резонансной томографии. Cereb Cortex 12 : 536–544
Артикул Google ученый
Baud O, Daire JL, Dalmaz Y, Fontaine RH, Krueger RC, Sebag G, Evrard P, Gressens P, Verney C 2004 Гестационная гипоксия вызывает повреждение белого вещества у новорожденных крыс: новая модель перивентрикулярной лейкомаляции. Brain Pathol 14 : 1–10
Статья Google ученый
Svedin P, Kjellmer I, Welin AK, Blad S, Mallard C 2005 Эффекты созревания липополисахарида на повреждение белого вещества у плода овцы. J Детский нейрол 20 : 960–964
Артикул Google ученый
Qiao M, Meng S, Scobie K, Foniok T., Tuor UI 2004 Магнитно-резонансная томография дифференциального повреждения серого и белого вещества после легкого или умеренного гипоксически-ишемического инсульта у новорожденных крыс. Neurosci Lett 368 : 332–336
CAS Статья Google ученый
Triulzi F, Parazzini C, Righini A 2006 Типы повреждений зрелого неонатального мозга. Pediatr Radiol 36 : 608–620
Артикул Google ученый
Baenziger O, Martin E, Steinlin M, Good M, Largo R, Burger R, Fanconi S, Duc G, Buchli R, Rumpel H, Boltshauser E 1993 Раннее распознавание паттернов тяжелой перинатальной асфиксии: проспективное МРТ-исследование . Нейрорадиология 35 : 437–442
CAS Статья Google ученый
Sie LT, van der Knaap MS, Oosting J, de Vries LS, Lafeber HN, Valk J 2000 MR-модели гипоксически-ишемического повреждения мозга после пренатальной, перинатальной или послеродовой асфиксии. Нейропедиатрия 31 : 128–136
CAS Статья Google ученый
McKinstry RC, Miller JH, Snyder AZ, Mathur A, Schefft GL, Almli CR, Shimony JS, Shiran SI, Neil JJ 2002 Проспективное исследование повреждений головного мозга с помощью тензора продольной диффузии у новорожденных. Неврология 59 : 824–833
CAS Статья Google ученый
Graham EM, Holcroft CJ, Rai KK, Donohue PK, Allen MC 2004 Повреждение белого вещества головного мозга у недоношенных новорожденных связано с инфекциями с положительным посевом и лишь в редких случаях с метаболическим ацидозом. Am J Obstet Gynecol 191 : 1305–1310
Артикул Google ученый
Volpe JJ 2003 Повреждение белого вещества головного мозга у недоношенных детей — более распространенное явление, чем вы думаете. Педиатрия 112 : 176–180
Статья Google ученый
Miller SP, Vigneron DB, Henry RG, Bohland MA, Ceppi-Cozzio C, Hoffman C, Newton N, Partridge JC, Ferriero DM, Barkovich AJ 2002 МРТ с серийным количественным тензором диффузии недоношенного мозга: развитие у новорожденных с травмой и без нее. Дж Магнитно-резонансная томография 16 : 621–632
Артикул Google ученый
Пирсон CR, Folkerth RD, Billiards SS, Trachtenberg FL, Drinkwater ME, Volpe JJ, Kinney HC 2007 Повреждение серого вещества, связанное с перивентрикулярной лейкомаляцией у недоношенных детей. Acta Neuropathol 114 : 619–631
Статья Google ученый
% PDF-1.х ~ $ PL) г = Ԗc? 9w; ooz} 3ifjS1vZ2IhD | * Q8sD \ Rxl’8 ‘> Gq
Гиперинтенсивность белого вещества мозга на МРТ: современные концепции и терапевтическое значение — FullText — Цереброваскулярные заболевания 2006, Vol. 22, № 2-3
Абстрактные
Общие сведения: Гиперинтенсивность белого вещества (WMH) обычно наблюдаются при МРТ у пожилых людей, которые обычно отражают скрытое повреждение сосудов головного мозга. WMH в совокупности приводит к значительным неврологическим, психиатрическим и медицинским заболеваниям.В этом обзоре представлен обзор современных знаний о сосудистой БГМ и описаны некоторые фармакологические агенты, которые могут играть роль в смягчении этого состояния. Краткое содержание обзора: Этот обзор имеет две основные области. Первый — это обсуждение имеющихся в настоящее время знаний о бремени общественного здравоохранения, патогенезе и различных факторах риска, связанных с наличием сосудистых поражений белого вещества, отмеченных на МРТ головного мозга. Во втором разделе статьи подробно описываются механистические и клинические основы перспективных методов фармакологического лечения, которые потенциально могут предотвратить прогрессирование ишемического повреждения белого вещества головного мозга.Многие из этих методов лечения уже доказали свою эффективность в предотвращении повторного инсульта. Выводы: Лица с сосудистыми поражениями белого вещества на МРТ могут представлять потенциальную целевую группу, которая, вероятно, получит пользу от лечения вторичной профилактики инсульта.
© 2006 S. Karger AG, Базель
Текущие концепции
Бремя ишемических травм, вызванных белой материей, для общественного здравоохранения
Около 750 000 американцев ежегодно переносят первый или повторный инсульт [1, 2].Однако эти оценки отражают только клинически манифестные, симптоматические инсульты и не принимают во внимание ежегодные потери сосудистого повреждения белого вещества головного мозга среди населения Америки. Среди пожилых людей симптоматический инсульт имеет распространенность 4,7% [3], но гиперинтенсивность белого вещества при МРТ (WMH) обнаруживается у значительной части пожилого населения, проживающего в общинах, и частота этих поражений приближается к 100% к возрасту. 85 [4, 5]. Вначале WMH может не вызывать никаких симптомов или вызывать только легкие, неспецифические и / или нераспознанные симптомы, но в конечном итоге может привести к серьезным неврологическим, психиатрическим и медицинским заболеваниям.WMH связаны с когнитивной дисфункцией, явной деменцией, депрессией [6, 7], психозами, нарушением походки и падениями [8,9,10], нарушением координации движений рук [9, 10] и заметно повышенным риском симптоматического инсульта в будущем.
МРТ Гиперинтенсивность белого вещества
WMH — это области ярких сигналов с высокой интенсивностью, отмеченных на МРТ T 2 -взвешенных последовательностях и последовательностях плотности протонов, представляющих области рассеянной потери белого вещества мозга, связанной с локальным увеличением содержания воды в мозге.Эта гиперинтенсивность отражает лейкоареоз (от греческого leuko = белый, araios = разреженный), термин, введенный Hachinski et al. [11], чтобы указать на «уменьшение плотности изображения белого вещества» при нейровизуализации.
WMH сосудистого происхождения также можно разделить на точечную, раннюю сливающуюся и сливную гиперинтенсивности [12, 13]. Пунктированные поражения имеют тенденцию соответствовать периваскулярному снижению содержания миелина с атрофией нейропиля и, по-видимому, представляют собой незначительную степень повреждения ткани из-за низкой проницаемости через утолщенные стенки артериол.Однако ранние сливающиеся и сливающиеся (рис. 1) гиперинтенсивности указывают на более обширное ишемическое повреждение, согласующееся с развитой микроангиопатией. [12, 13].
Рис. 1
MRI T 2 -взвешенных последовательностей, показывающих сливающиеся WMH.
Прогрессирование ВГМ и явно высокий риск у субъектов со сливными поражениями
Было показано, что присутствие сливного ВМГ во время первоначального наблюдения является мощным предиктором последующего прогрессирования ВГБ [14].Ранние сливающиеся и сливные аномалии белого вещества прогрессируют и, вероятно, являются злокачественными. Два крупных популяционных исследования предоставили подробную информацию о резких различиях в скорости прогрессирования объема поражения у людей с разной степенью исходного уровня ВГМ (таблица 1). Исследователи Австрийского исследования профилактики инсульта провели популяционное исследование, в котором оценивали прогрессирование поражений белого вещества у местных добровольцев в возрасте 50–75 лет без психоневрологических заболеваний [15].МРТ были выполнены у 296 добровольцев на исходном уровне, 3 года и 6 лет, и был измерен общий объем поражений белого вещества. Участники без поражений и с точечными аномалиями на исходном уровне имели низкую тенденцию к прогрессированию поражений, тогда как участники с ранними сливающимися и сливающимися поражениями показали значительное медианное увеличение объема поражения через 6 лет. Было обнаружено, что степень поражения на исходном уровне является значимым предиктором прогрессирования поражения (p <0,0001) [15].
Таблица 1
Ежегодное увеличение объема поражения белого вещества (см. 3 ) у субъектов с разной степенью ВМГ на момент включения в исследование
В подисследовании PROGRESS MRI многоцентровая исследовательская группа во Франции получила исходные и трехлетние МРТ у пациентов с последовательным инсультом, включенных в международное исследование постинсультной гипотензивной терапии PROGRESS [16]. В группе плацебо степень поражения на исходном уровне сильно зависела от прогрессирования поражения, при этом прогрессирование не наблюдалось у легких исходных субъектов, и в пять раз большее прогрессирование наблюдалось у сливающихся субъектов по сравнению с ранними сливающимися субъектами.
Патогенез
Патологическая корреляция показала, что эти пятнистые поражения белого вещества соответствуют в первую очередь участкам ишемической демиелинизации и глиоза, а иногда и клинически бессимптомным инфарктам [17]. Хроническая сосудистая недостаточность слабой степени вызывает атрофическую периваскулярную демиелинизацию, а не острый некроз тканей, вызванный более тяжелой ишемией. Вероятно, в основном причиной ВМГ являются гипоперфузия и заболевание артериол [18]. Липогиалиноз средних и утолщение стенок сосудов сужают просвет мелких перфорирующих артерий и артериол, питающих глубокое белое вещество [19].Перфорирующие сосуды, берущие свое начало из кортикальных и лептоменингеальных артерий, имеют относительно слабую анастомотическую систему, что делает белое вещество уязвимым для церебральной ишемии. Патологоанатомические исследования показали, что ВМГ, обнаруживаемое на МРТ, связано с дегенеративными изменениями артериол, которые связаны с атеросклерозом, что позволяет предположить, что церебральный артериосклероз проникающих сосудов является основным фактором патогенеза ишемической ВМГ [19].
Факторы риска церебральной ишемической травмы белого вещества
Гипертония
Помимо возраста, гипертония постоянно считается наиболее частым фактором риска ВМГ головного мозга и повреждения спинного мозга [20,21,22].Связь между артериальной гипертензией и WMH была установлена в поперечных [19] и лонгитюдных исследованиях [20]. В нескольких исследованиях изучали распространенность ГМГ у лиц с гипертонией и высоким нормотензивным давлением [23,24,25]. Например, исследование ARIC [23] сообщило о 24,6% распространенности ВМГ среди людей в возрасте 55–72 лет, 49% из которых были гипертониками. Ранее повышенное артериальное давление может увеличить риск развития деменции, вызывая заболевание мелких сосудов и поражения белого вещества [26].Есть также предположение о большей ассоциации гипертонии с сливными поражениями белого вещества; van Swieten et al. [27] обнаружили, что диастолическое артериальное давление было выше у лиц с конфлюэнтными поражениями, чем у лиц без очаговых поражений 13 ± 9 лет назад.
Атеросклероз крупных сосудов
Breteler et al. [25] сообщили, что WMH были связаны с атеросклерозом, на что указывало увеличение общей толщины интима-медиа сонных артерий и каротидных бляшек. Аналогичным образом Manolio et al.[28] обнаружили, что инфаркты МРТ, расширение желудочков и борозд, а также оценка белого вещества были тесно связаны с толщиной интимы-медиальной артерии и степенью стеноза сонной артерии после поправки на возраст и пол (все p <0,01). Кроме того, de Leeuw et al. [29] показали, что наличие атеросклероза аорты в среднем возрасте, оцененное на рентгенограммах брюшной полости, было значительно связано с наличием перивентрикулярного ВМГ 20 лет спустя.
Эндотелиальная дисфункция
Несколько исследований показывают, что церебральный лейкоараоз связан с нарушением релаксации эндотелия и реактивности как сосудов головного мозга, так и системных сосудов.Транскраниальные ультразвуковые допплеровские исследования показали значительное нарушение вазомоторной реактивности у пациентов с перивентрикулярными поражениями белого вещества [30] и лакунарными инсультами [31]. Длительный артериовенозный церебральный транзит, указывающий на нарушение церебральной микроциркуляции, был продемонстрирован у субъектов с микроангиопатией и сосудистой деменцией [32].
Несколько авторов использовали эпидемиологические, патологические и экспериментальные исследования, чтобы предположить, что дисфункция эндотелия мелких сосудов головного мозга с утечкой компонентов плазмы в стенку сосуда и окружающую ткань мозга, приводящую к повреждению нейронов, может способствовать развитию лакунарного инсульта. лейкоареоз и деменция [33, 34].
Исследование Hassan et al. [35], измеряя уровни циркулирующих маркеров активации и повреждения эндотелия, молекулы межклеточной адгезии 1, тромбомодулина, тканевого фактора (TF) и ингибитора пути тканевого фактора (TFPI) в проспективной серии пациентов с лакунарным инсультом, было обнаружено, что группа пациентов с ишемическим лейкоареозом имела другой профиль эндотелиальных маркеров с более низкими уровнями TFPI (p = 0,01) и более высоким соотношением TF / TFPI (p = 0,01) по сравнению с группой изолированного лакунарного инфаркта.Уровни тромбомодулина были связаны с количеством лакун (p = 0,008) и баллом лейкоареоза (p = 0,03), но уровни TF и соотношение TF / TFPI были связаны только со степенью лейкоареоза (p ≤ 0,02). Эти результаты позволяют предположить, что существуют доказательства хронической эндотелиальной дисфункции при заболевании мелких сосудов головного мозга и что эндотелиальные протромботические изменения могут быть важны в опосредовании фенотипа ишемического лейкоареоза.
Диабет
Некоторые исследования показали, что ВМГ связаны с диабетом [12, 13].Однако другие исследования не подтвердили эту связь [27, 36]. Было высказано предположение, что причиной этих противоречивых результатов могут быть различия в размерах выборок, степенях WMH, тяжести диабета и продолжительности диабета в различных исследуемых популяциях [37]. Совсем недавно исследование недемментированных пожилых людей обнаружило значительную корреляцию Пирсона с WMH для повышенного уровня гемоглобина, индекса недавнего (предшествовавшего 3 мес) гликемического контроля [38]. Безусловно, необходимы дальнейшие исследования любой потенциальной связи между диабетом и ВМЗ.
Терапевтическое значение
Перспективные методы лечения для предотвращения прогрессирования ишемического поражения головного мозга белым веществом головного мозга
Антитромбоцитарные агенты
Антитромбоцитарные агенты играют признанную роль в снижении вторичного инсульта и первичного сердечного риска [39]. Однако до недавнего времени антитромбоцитарные препараты нельзя было рекомендовать для рутинного использования для первичной профилактики клинически манифестных цереброваскулярных заболеваний. Во многом это было связано с отсутствием высококачественных доказательств, подтверждающих эффективность, и потенциально повышенным риском геморрагического инсульта, как было отмечено при профилактическом применении аспирина для первичной профилактики инсульта [40].Результаты исследования здоровья женщин предполагают, что может быть роль стратегии первичной профилактики инсульта с использованием антитромбоцитарной терапии в отдельных группах населения [41]. Это исследование показало снижение риска ишемического инсульта на 24% (относительный риск 0,76; 95% ДИ 0,63–0,93; p = 0,009) и незначительное небольшое увеличение риска геморрагического инсульта в пользу аспирина (по сравнению с плацебо) среди женщин 45 лет и старше, без инсульта в анамнезе [41]. Результаты исследования здоровья женщин и доказанная эффективность различных антитромбоцитарных агентов, действующих через различные механизмы при вторичной профилактике инсульта (см. Ниже), могут подтвердить необходимость разработки исследований для оценки потенциала антитромбоцитарной терапии для смягчения неблагоприятных последствий ВГМ у пациентов. лица без клинических проявлений цереброваскулярных заболеваний.
Аспирин. Аспирин (ацетилсалициловая кислота) предотвращает активацию тромбоцитов, ингибируя фермент циклооксигеназу, что приводит к блокированию образования тромбоксана, и было показано, что он защищает большинство типов пациентов с повышенным риском окклюзионных сосудистых событий [39]. Циклооксигеназа также продуцирует супероксидные радикалы в эндотелиальных клетках сосудов. Уменьшение количества супероксидных радикалов устраняет опосредованную амилоидом вазоактивность и повреждение. Таким образом, аспирин может также уменьшить повреждение эндотелия за счет ингибирования циклооксигеназы [42].Другой механизм церебропротекторного действия аспирина может заключаться в его известном ингибировании активности матриксной металлопротеиназы [43]. Было высказано предположение, что продолжающееся повреждение белого вещества головного мозга связано с производством матриксной металлопротеиназы микроглией / макрофагами [44].
Дипиридамол. Дипиридамол, как хорошо известно, обладает антитромбоцитарной активностью [45]. Дипиридамол — это не только антиагрегант, оказывающий свое действие непосредственно на тромбоциты путем ингибирования захвата аденозина, но также и антитромботический агент, использующий другие механизмы [46].Одним из фармакологических эффектов дипиридамола является расширение сосудов, что, в свою очередь, может привести к снижению артериального давления [47]. Дипиридамол также напрямую стимулирует высвобождение эндотелиального PGI 2 , а также снижает тромбогенность субэндотелиальных структур за счет увеличения продуктивного медиатора 13-гидроксиоктадекадиеновой кислоты. Одно исследование показало, что дипиридамол может действовать в первую очередь на медиаторов воспаления (что определяется С-реактивным белком) и эндотелиальной дисфункции (оценивается с помощью фактора фон Виллебранда) [48].
Аспирин и дипиридамол. Доклинические исследования показали синергетический эффект дипиридамола и ацетилсалициловой кислоты в снижении тромбообразования [49]. Комбинация аспирина и дипиридамола превосходит любой агент по отдельности в предотвращении явного рецидивирующего ишемического инсульта. В крупном исследовании European Stroke Prevention Study 2 было обнаружено, что низкие дозы аспирина плюс дипиридамол более чем вдвое снижают риск инсульта, достигаемого с помощью одного аспирина, то есть снижение риска для комбинации на 37% по сравнению с 18.1% только для аспирина. Результаты также показали, что эффекты аспирина и дипиридамола являются аддитивными [50].
Клопидогрель. Клопидогрель является антагонистом рецептора аденозиндифосфата, который ингибирует индуцированное аденозиндифосфатом связывание фибриногена с тромбоцитами, что является необходимым этапом в процессе агрегации тромбоцитов. Исследование CAPRIE выявило небольшое преимущество клопидогреля перед аспирином в комбинированной конечной точке — ишемическом инсульте, инфаркте миокарда или смерти сосудов в когорте из 19 185 пациентов, недавно перенесших ишемический инсульт, инфаркт миокарда или заболевание периферических артерий [51, 52].
Антигипертензивные агенты
Субъекты, принимающие гипотензивные препараты и контролирующие артериальное давление, имеют пониженный риск тяжелой ВГМ [20]. Хотя среднее артериальное давление является важным предиктором событий инсульта, результаты недавних клинических испытаний, показывающих пользу снижения артериального давления даже у лиц с нормальным АД [53], указывают на то, что артериальное давление, вероятно, представляет собой континуум риска инсульта и что категориальное различие между артериальная гипертензия, вызванная нормотензией, в некоторой степени искусственна [54], что означает, что круг субъектов, которых можно лечить с помощью эффективных методов профилактики инсульта, может быть расширен, и укрепляет мнение о том, что использование гипотензивных средств должно определяться общим уровнем риска человека. а не только уровень артериального давления.
Наиболее важным в этой аргументации является недавний отчет о французском субисследовании МРТ клинического исследования PROGRESS, которое представляет собой первое клиническое испытание по изучению прогрессирования аномалий белого вещества у субъектов, получавших дополнительную антигипертензивную терапию. В исследовании PROGRESS пациенты с гипертонией и высоким нормальным давлением с инсультом в анамнезе получали дополнительную терапию тиазидным диуретиком и ингибитором ангиотензинпревращающего фермента (ИАПФ) (в дополнение к их существующему режиму артериального давления).Французская многоцентровая группа выполнила подисследование МРТ в исследовании PROGRESS, чтобы определить, привели ли активные диуретики в сочетании с терапией ИАПФ к снижению частоты новых ВМГ во время последующего наблюдения МРТ по сравнению с группой лиц, получавших плацебо. Dufouil et al. [16] получили исходную и 3-летнюю МРТ для измерения наличия и объема случайных поражений белого вещества у 225 человек с предшествующим цереброваскулярным заболеванием (инсульт или транзиторная ишемическая атака). Результаты продемонстрировали статистически значимый эффект диуретиков и ИАПФ в снижении частоты появления новых очагов поражения белого вещества, причем лечебный эффект наиболее выражен в подгруппе субъектов с запущенным лейкоареозом на момент включения в исследование.
Из тех субъектов в группе активного лечения, у которых были серьезные поражения белого вещества при входе, ни у одного не наблюдалось увеличения поражений. Результаты ясно показывают, что дополнительный режим снижения артериального давления у пациентов, перенесших инсульт, останавливает или отсрочивает дальнейшее скрытое ишемическое повреждение головного мозга. Однако эти многообещающие результаты у субъектов, которые уже перенесли явный клинический инсульт, необходимо распространить на субъектов, не имевших в анамнезе явного инсульта, у которых может быть разная скорость прогрессирования скрытого сосудистого повреждения.Примечательно, что результаты подисследования PROGRESS MRI предполагают, что только у субъектов с более поздним лейкоараозом на момент входа будет наблюдаться достаточно существенное прогрессирование, чтобы получить пользу от терапии для предотвращения прогрессирующего скрытого сосудистого повреждения головного мозга в течение нескольких лет после вмешательства.
По общему мнению, снижение артериального давления является наиболее важным фактором в профилактике инсульта, обеспечиваемой антигипертензивным лечением, независимо от класса гипотензивных средств, и что это должно быть в центре внимания любого лечения, направленного на снижение риска инсульта.Однако появляется все больше доказательств того, что определенные классы антигипертензивных средств могут дать клиническую пользу в профилактике инсульта за счет дополнительных механизмов [55].
Система ренин-ангиотензин-альдостерон-кинин
Блокаторы рецепторов ангиотензина II (БРА) и ИАПФ — это два класса гипотензивных препаратов, которые снижают активность системы ренин-ангиотензин II (РАС). Фармакологическая модуляция системы ренин-ангиотензин-альдостерон-кинин является привлекательной терапевтической мишенью для лечения скрытого сосудистого повреждения головного мозга, поскольку аномалии каскада ренин-ангиотензин-альдостерон-кинин участвуют в патогенезе и клинической экспрессии мелких сосудов головного мозга. болезнь [56, 57].ИАПФ, и БРА показали свою эффективность в предотвращении первого и повторного симптоматического инсульта [53, 58, 59]. Эти агенты также снижают кровяное давление, не уменьшая церебральную перфузию [60].
Исследования генетических ассоциаций в рамках Австрийского исследования по профилактике инсульта показали, что полиморфизмы в РАН повышают предрасположенность к прогрессированию болезни мелких сосудов головного мозга. Гомозиготность по аллелю T полиморфизма M235T гена ангиотензиногена была связана с 3.В 19 раз повышен риск прогрессирования поражения независимо от артериальной гипертензии. Эти данные позволяют предположить, что лекарственные препараты, влияющие на РАС, могут препятствовать неблагоприятному течению болезни мелких сосудов головного мозга [61].
Ангиотензин II (ANG II), главный эффекторный пептид РАС, участвует в развитии сосудистых патологий. Недавние исследования, которые считаются центральными для всего сосудистого континуума, также установили роль АНГ II в восстановлении мозга после церебрального инсульта.ANG II действует через два рецептора: ANG II типа 1 (AT1) и типа 2 (AT2). Препараты, активирующие рецепторы AT2, такие как БРА, всегда оказывались более эффективными для уменьшения инсульта, чем препараты, лишенные такой активации, несмотря на такое же падение артериального давления [62, 63]. Эти клинические и эпидемиологические наблюдения подтверждаются экспериментальными данными, документально подтверждающими большую церебропротекторную защиту с помощью БРА (которые повышают уровни АНГ II и стимулируют рецепторы АТ2), чем с ИАПФ [62].Среди многих потенциальных эффектов, опосредованных стимуляцией AT2, — регенерация нейронов после повреждения и ингибирование патологического роста. Действительно, экспериментальные данные показывают, что БРА обеспечивают двойную защиту, поскольку они ингибируют проатеротромботические эффекты, опосредованные рецептором AT1, и усиливают опосредованную рецептором AT2 защиту от ишемии за счет увеличения генерации ANG II, особенно в небольших артериях [62]. Этот последний эффект может дать БРА преимущество перед ИАПФ, потому что, хотя ИАПФ также ингибируют АТ1-опосредованные проатеротромботические эффекты, они также снижают уровни циркулирующего АНГ II и, таким образом, церебропротекцию, зависящую от рецептора АТ2 [62].Однако это потенциальное преимущество не было доказано в клинической практике. Текущее глобальное исследование конечных точек телмисартана в отдельности и в комбинации с рамиприлом (ONTARGET) — это продолжающееся двойное слепое рандомизированное исследование, в котором сравнивается эффективность и безопасность дополнительной терапии БРА и ИАПФ в профилактике сердечно-сосудистых событий, и оно подтвердит или опровергнуть любые дополнительные преимущества ARB перед ACEI [64].
Статины
Использование статинов (ингибиторов HMG-CoA редуктазы) интуитивно потенциально привлекательно для предотвращения травм, вызванных WMH.Многочисленные исследования показали, что лечение статинами связано со значительным снижением риска инсульта и транзиторной ишемической атаки у пациентов с симптоматической болезнью коронарных артерий или множественными факторами риска атеросклероза [65], а некоторые исследования показывают, что предварительное лечение статинами может привести к при инсульте меньшей степени тяжести [66]. Механизм, с помощью которого статины обеспечивают защиту сосудов, вероятно, является многофакторным и включает изменения липопротеинов (повышающая регуляция активности рецепторов липопротеинов низкой плотности и уменьшение поступления липопротеинов низкой плотности в кровоток), улучшение функции эндотелия (улучшение эндотелиальной синтазы оксида азота, ингибирование индуцируемой синтаза оксида азота), стабилизация бляшек, антитромбоз, ослабление воспалительных цитокиновых ответов и антиоксидантные эффекты [67].
Несмотря на все это, ни одно исследование еще не показало, что статины эффективны в предотвращении вторичного инсульта. В настоящее время этот вопрос исследуется в исследовании SPARCL [68]. Применительно к пациентам с ВМГ исследование здоровья сердечно-сосудистой системы изучало связь употребления статинов с изменениями показателей белого вещества на серийных снимках МРТ с интервалом в 5 лет и не обнаружило заметных различий в эволюции показателей белого вещества между лечением (статины и отсутствие данных). статин) группы [69]. Тем не менее, из этих данных МРТ в подгруппе исследования сердечно-сосудистого здоровья можно сделать лишь ограниченные выводы, поскольку исследование было наблюдательным, размер выборки был относительно скромным (n = 1730), а система оценок, использованная для измерения болезни белого вещества в исследовании, может не обладали достаточной чувствительностью или надежностью считывателя для обнаружения значительных изменений в пределах интервала исследования.В будущем потребуются более крупные рандомизированные исследования для изучения роли статинов, если таковые имеются, в уменьшении ишемического повреждения белого вещества головного мозга. Выводы. Для испытаний лечения с использованием только клинических конечных точек, вероятно, потребуются большие размеры выборки, и к тому времени, когда клинические конечные точки станут очевидными, бремя повреждения мозга, вызванного этими поражениями, будет значительным.Клинические конечные точки устанавливают окончательный стандарт для окончательных клинических испытаний, но более чувствительные суррогатные маркеры могут быть полезны при оценке эффективности новых методов лечения и выборе наиболее многообещающих методов лечения для крупных испытаний. Аналогия обеспечивается рассеянным склерозом, для которого обнаружение новых поражений с помощью МРТ с контрастным усилением было реализовано в качестве суррогатного маркера активности заболевания [70, 71], а обнаружение новых поражений было включено в рекомендации по мониторингу заболевания в терапевтических испытаниях. при рассеянном склерозе [71].Европейская рабочая группа по возрастным изменениям белого вещества недавно пришла к выводу, что поражения белого вещества при МРТ являются подходящим биометрическим маркером для использования в клинических испытаниях фазы 2 [72]. С появлением многообещающих новых (и не очень новых) методов лечения, которые могут ограничить снижение когнитивных функций у людей с МРТ ВМГ, могут появиться возможности для изучения путей уменьшения огромного общественного бремени ишемического повреждения белого вещества сосудов головного мозга.
Список литературы
- Broderick J, Miller R, Khoury JC, Alwell K, Kissela MB, Woo D, Shukla R, Moomaw C, Gebel J, Pancioli AM, Brott TG, Kothari RU: Заболеваемость инсультом у чернокожих и белых: предварительные результаты из большего Цинциннати / исследование инсульта на севере Кентукки.Инсульт 2001; 32: 320.
- Уильямс Дж .: Заболеваемость и характеристики общего инсульта в США. BMC Neurol 2001; 1: 2.
- Mittelmark M, Psaty BM, Rautaharju PM, Fried LP, Borhani NO, Tracy RP, Gardin JM, O’Leary DH: Распространенность сердечно-сосудистых заболеваний среди пожилых людей.Исследование здоровья сердечно-сосудистой системы. Am J Epidemiol 1993; 137: 311–317.
- Awad I, Johnson PC, Spetzler RF, Hodak JA: Случайные подкорковые поражения, выявленные на магнитно-резонансной томографии у пожилых людей. Патологические находки после смерти. Инсульт 1986; 17: 1090–1097.
- Кертес А., Блэк С.Е., Токар Г., Бенке Т., Карр Т., Николсон Л.: Перивентрикулярная и подкорковая гиперинтенсивность на магнитно-резонансной томографии.«Обода, колпачки и неопознанные яркие предметы». Arch Neurol 1988; 45: 404–408.
- Kidwell C, Saver JL: Причины и последствия лейкоареоза: обзор. Факты Res Gerontol 1996 (добавлено отрывок): 115–135.
- de Groot J, de Leeuw FE, Oudkerk M, Hofman A, Jolles J, Breteler MM: Поражения белого вещества головного мозга и депрессивные симптомы у пожилых людей.Arch Gen Psychiatry 2000; 57: 1071–1076.
- Baloh R, Yue Q, Socotch TM, Jacobson KM: Поражения белого вещества и нарушение равновесия у пожилых людей. 1. Сравнение случай-контроль. Arch Neurol 1995; 52: 970–974.
- Прайс Т., Манолио Т.А., Кронмал Р.А., Киттнер С.Дж., Юэ NC, Роббинс Дж., Антон-Калвер Х., О’Лири Д.: Тихий инфаркт мозга по данным магнитно-резонансной томографии и неврологические аномалии у пожилых людей, проживающих в сообществе.Исследование здоровья сердечно-сосудистой системы. Группа совместных исследований CHS. Инсульт 1997; 28: 1158–1164.
- Longstreth W: Нарушения головного мозга у пожилых людей: частота и предикторы в США (Исследование здоровья сердечно-сосудистой системы). Группа совместных исследований сердечно-сосудистых заболеваний.Журнал Neural Transm Suppl 1998; 53: 9–16.
- Хачинский В., Поттер П., Мерски Х .: Лейкоареоз: древний термин для обозначения новой проблемы. Can J Neurol Sci 1986; 13: 533–534.
- Schmidt R, Fazekas F, Kleinert G, Offenbacher H, Gindl K, Payer F, Freidl W., Niederkorn K, Lechner H: гиперинтенсивность сигнала магнитно-резонансной томографии в глубоком и подкорковом белом веществе.Сравнительное исследование пациентов, перенесших инсульт, и здоровых добровольцев. Arch Neurol 1992; 49: 825–827.
- Фазекас Ф., Нидеркорн К., Шмидт Р., Оффенбахер Х., Хорнер С., Берта Г., Лехнер Х. Аномалии сигнала белого вещества у нормальных людей: корреляция с ультразвуковым исследованием сонной артерии, измерениями церебрального кровотока и факторами риска цереброваскулярных заболеваний.Инсульт 1988; 19: 1285–1288.
- Schmidt R, Schmidt H, Kapeller P, Enzinger C, Ropele S, Saurugg R, Fazekas F: Естественное течение гиперинтенсивности белого вещества при МРТ. J Neurol Sci 2002; 203–204: 253–257.
- Schmidt R, Enzinger C, Ropele S, Schmidt H, Fazekas F: Прогрессирование поражений белого вещества головного мозга: 6-летние результаты австрийского исследования профилактики инсульта.Ланцет 2003; 361: 2046–2048.
- Dufouil C, Chalmers J, Coskun O, Besancon V, Bousser MG, Guillon P, MacMahon S, Mazoyer B, Neal B, Woodward M, Tzourio-Mazoyer N, Tzourio C: Влияние снижения артериального давления на гиперинтенсивность белого вещества головного мозга у пациентов с инсультом: подразделение магнитно-резонансной томографии PROGRESS (исследование защиты периндоприла от повторного инсульта).Тираж 2005; 112: 1644–1650.
- Фазекас Ф., Кляйнерт Р., Оффенбахер Х., Шмидт Р., Кляйнерт Г., Пайер Ф., Раднер Х., Лехнер Х .: Патологические корреляты случайных гиперинтенсивностей сигнала МРТ белого вещества. Неврология 1993; 43: 1683–1689.
- Liao D, Cooper L, Cai J, Toole J, Bryan N, Burke G, Shahar E, Nieto J, Mosley T., Heiss G: Распространенность и тяжесть поражений белого вещества, их связь с возрастом, этнической принадлежностью, полом и сердечно-сосудистыми заболеваниями. Факторы риска заболеваний: исследование ARIC.Нейроэпидемиология 1997; 16: 149–162.
- Пантони Л., Гарсия Дж. Х .: Значение аномалий белого вещества головного мозга через 100 лет после доклада Бинсвангера. Обзор. Инсульт 1995; 26: 1293–1301.
- Dufouil C, de Kersaint-Gilly A, Besancon V, Levy C, Auffray E, Brunnereau L, Alperovitch A, Tzourio C: Продольное исследование артериального давления и гиперинтенсивности белого вещества: когорта EVA-MRI.Неврология 2001; 56: 921–926.
- Lee S, Park SJ, Ki HK, Gwon HC, Chung CS, Byun HS, Shin KJ, Shin MH, Lee WR: Распространенность и факторы риска тихого инфаркта головного мозга у практически нормальных взрослых. Гипертония 2000; 36: 73–77.
- Longstreth WT Jr, Bernick C, Manolio TA, Bryan N, Jungreis CA, Price TR: Лакунарные инфаркты, определенные с помощью магнитно-резонансной томографии 3660 пожилых людей: исследование здоровья сердечно-сосудистой системы.Arch Neurol 1998; 55: 1217–1225.
- Liao D, Cooper L, Cai J, Toole JF, Bryan NR, Hutchinson RG, Tyroler HA: Наличие и тяжесть поражений белого вещества головного мозга и гипертонии, их лечение и контроль. Исследование ARIC. Риск атеросклероза в исследовании сообществ. Инсульт 1996; 27: 2262–2270.
- Longstreth W, Manolio TA, Arnold A, Burke GL, Bryan N, Jungreis CA, Enright PL, O’Leary D, Fried L: Клинические корреляты результатов исследования белого вещества на черепной магнитно-резонансной томографии 3301 пожилого человека. Исследование здоровья сердечно-сосудистой системы. Инсульт 1996; 27: 1274–1282.
- Breteler MM, van Swieten JC, Bots ML, Grobbee DE, Claus JJ, van den Hout JH, van Harskamp F, Tanghe HL, de Jong PT, van Gijn J, et al: Поражения белого вещества головного мозга, факторы риска сосудов и когнитивные функция в популяционном исследовании: Роттердамское исследование.Неврология 1994; 44: 1246–1252.
- Скуг И., Лернфельт Б., Ландаль С., Палмерц Б., Андреассон Л.А., Нильссон Л., Перссон Г., Оден А., Сванборг А.: 15-летнее продольное исследование артериального давления и деменции. Ланцет 1996; 347: 1141–1145.
- van Swieten J, Geyskes GG, Derix MM, Peeck BM, Ramos LM, van Latum JC, van Gijn J: Гипертония у пожилых людей связана с поражением белого вещества и снижением когнитивных функций.Энн Нейрол 1991; 30: 825–830.
- Manolio T, Burke GL, O’Leary DH, Evans G, Beauchamp N, Knepper L, Ward B: Связь результатов МРТ головного мозга с ультразвуковым атеросклерозом сонных артерий у пожилых людей: Исследование здоровья сердечно-сосудистой системы. Группа совместных исследований CHS. Arterioscler Thromb Vasc Biol 1999; 19: 356–365.
- de Leeuw FE, De Groot JC, Oudkerk M, Witteman JC, Hofman A, van Gijn J, Breteler MM: Атеросклероз аорты в среднем возрасте предсказывает поражение белого вещества головного мозга у пожилых людей. Инсульт 2000; 31: 425–429.
- Баккер С., де Леув Ф. Э., де Гроот Дж. К., Хофман А., Коудстал П. Дж., Бретелер М. М.: Церебральная вазомоторная реактивность и поражения белого вещества головного мозга у пожилых людей.Неврология 1999; 52: 578–583.
- Молина С., Сабин Дж. А., Монтанер Дж., Ровира А., Абиллейра С., Кодина А. Нарушение цереброваскулярной реактивности как маркер риска первого в истории лакунарного инфаркта: исследование случай-контроль. Инсульт 1999; 30: 2296–2301.
- Puls I, Hauck K, Demuth K, Horowski A, Schliesser M, Dorfler P, Scheel P, Toyka KV, Reiners K, Schoning M, Becker G: Диагностическое влияние времени мозгового транзита при выявлении микроангиопатии при деменции: транскраниальное ультразвуковое исследование учиться.Инсульт 1999; 30: 2291–2295.
- Уордлоу Дж., Сандеркок П.А., Деннис М.С., Старр Дж.: Является ли нарушение гематоэнцефалического барьера ответственным за лакунарный инсульт, лейкоареоз и деменцию? Инсульт 2003; 34: 806–812.
- Балох Р., Винтерс Х.В.: Поражения белого вещества и нарушение равновесия у пожилых людей.2. Клинико-патологическая корреляция. Arch Neurol 1995; 52: 975–981.
- Hassan A, Hunt BJ, O’Sullivan M, Parmar K, Bamford JM, Briley D, Brown MM, Thomas DJ, Markus HS: Маркеры эндотелиальной дисфункции при лакунарном инфаркте и ишемическом лейкоареозе. Мозг 2003; 126: 424–432.
- Bogousslavsky J, Regli F, Uske A: Лейкоэнцефалопатия у пациентов с ишемическим инсультом. Инсульт 1987; 18: 896–899.
- Фукуда Х., Китани М.: Различия между леченными и нелеченными гипертониками в степени перивентрикулярной гиперинтенсивности, наблюдаемой на МРТ головного мозга.Инсульт 1995; 26: 1593–1597.
- Murray A, Staff RT, Шенкин SD, Deary IJ, Starr JM, Whalley LJ: Гиперинтенсивность белого вещества мозга: относительная важность сосудистых факторов риска у недемольных пожилых людей. Радиология 2005; 237: 251–257.
- Совместный метаанализ рандомизированных исследований антитромбоцитарной терапии для предотвращения смерти, инфаркта миокарда и инсульта у пациентов с высоким риском.BMJ 2002; 324: 71–86.
- Rodondi N, Bauer DC: Оценка профиля риска / пользы перед тем, как рекомендовать аспирин для первичной профилактики сердечно-сосудистых событий. Am J Med 2004; 117: 528–530.
- Ridker P, Cook NR, Lee IM, Gordon D, Gaziano JM, Manson JE, Hennekens CH, Buring JE: рандомизированное испытание низких доз аспирина в первичной профилактике сердечно-сосудистых заболеваний у женщин.N Engl J Med 2005; 352: 1293–1304.
- Broe GA, Grayson DA, Creasey HM, Waite LM, Casey BJ, Bennett HP, Brooks WS, Halliday GM: Противовоспалительные препараты защищают от болезни Альцгеймера в низких дозах. Arch Neurol 2000; 57: 1586–1591.
- Jiang MC, Liao CF, Lee PH: Аспирин ингибирует активность матричной металлопротеиназы-2, увеличивает выработку E-кадгерина и ингибирует инвазию опухолевых клеток in vitro.Biochem Biophys Res Commun 2001; 282: 671–677.
- Розенберг Г.А., Салливан Н., Эсири М.М.: Повреждение белого вещества связано с матриксными металлопротеиназами при сосудистой деменции. Инсульт 2001; 32: 1162–1168.
- Эммонс PR, Харрисон MJ, Honor AJ, Митчелл JR: Влияние дипиридамола на поведение тромбоцитов человека.Lancet 1965; II: 603–606.
- Eisert WG: Усиление антитромботических эффектов дипиридамола в ближнем поле через клетки стенки сосудов. Неврология 2001; 57: S20 – S23.
- Aktas B, Utz A, Hoenig-Liedl P, Walter U, Geiger J: Дипиридамол усиливает NO / cGMP-опосредованное вазодилататор фосфорилирование и передачу сигналов в тромбоцитах человека: исследования in vitro и in vivo / ex vivo.Инсульт 2003; 34: 764–769.
- Zhao L, Leonardi-Bee J, Weaver C, Heptinstall S, Bath P: Влияние аспирина, клопидогреля и дипиридамола на растворимые маркеры сосудистого стресса у пациентов с предшествующим инсультом. 13-я Европейская конференция по инсульту, Мангейм-Гейдельберг, май 2004 г.
- Honor AJ, Hockaday TD, Mann JI: синергетический эффект аспирина и дипиридамола на тромбы тромбоцитов в живых кровеносных сосудах.Br J Exp Pathol 1977; 58: 268–272.
- Diener HC, Cunha L, Forbes C, Sivenius J, Smets P, Lowenthal A: Европейское исследование профилактики инсульта. 2. Дипиридамол и ацетилсалициловая кислота во вторичной профилактике инсульта. J Neurol Sci 1996; 143: 1–13.
- Ringleb PA, Bhatt DL, Hirsch AT, Topol EJ, Hacke W. Преимущество клопидогреля перед аспирином усиливается у пациентов с ишемическими событиями в анамнезе.Инсульт 2004; 35: 528–532.
- Хирш Дж., Бхатт Д.Л.: Сравнительные преимущества клопидогреля и аспирина в группах пациентов с высоким риском: уроки исследований CAPRIE и CURE. Arch Intern Med 2004; 164: 2106–2110.
- Рандомизированное исследование схемы снижения артериального давления на основе периндоприла среди 6105 человек, перенесших инсульт или транзиторную ишемическую атаку.Ланцет 2001; 358: 1033–1041.
- Горелик П.Б .: Новые горизонты профилактики инсульта: ПРОГРЕСС и НАДЕЖДА. Lancet Neurol 2002; 1: 149–156.
- Ruland S, Gorelick PB: Предотвращают ли холестерин-снижающие лекарства и гипотензивные средства инсульт другими способами, кроме как контролируя фактор риска? Curr Neurol Neurosci Rep 2003; 3: 21–26.
- Takami S, Imai Y, Katsuya T., Ohkubo T, Tsuji I, Nagai K, Satoh H, Hisamichi S, Higaki J, Ogihara T: Полиморфизм генов ренин-ангиотензиновой системы связан с риском лакунарного инфаркта. Исследование Охасамы. Am J Hypertens 2000; 13: 121–127.
- Hassan A, Lansbury A, Catto AJ, Guthrie A, Spencer J, Craven C, Grant PJ, Bamford JM: Генотип вставки / делеции ангиотензинпревращающего фермента связан с лейкоареозом при лакунарных синдромах.J Neurol Neurosurg Psychiatry 2002; 72: 343–346.
- Dahlof B, Devereux RB, Kjeldsen SE, Julius S, Beevers G, Faire U, Fyhrquist F, Ibsen H, Kristiansson K, Lederballe-Pedersen O, Lindholm LH, Nieminen MS, Omvik P, Oparil S, Wedel H: Сердечно-сосудистые заболевания и смертность в исследовании «Вмешательство лозартана для снижения конечной точки в исследовании гипертонии» (LIFE): рандомизированное испытание атенолола.Ланцет 2002; 359: 995–1003.
- Юсуф С., Слейт П., Погу Дж., Бош Дж., Дэвис Р., Дагене Г.: Влияние ингибитора ангиотензин-превращающего фермента, рамиприла, на сердечно-сосудистые события у пациентов с высоким риском. Исследователи оценочного исследования профилактики сердечных исходов. N Engl J Med 2000; 342: 145–153; исправления в N Engl J Med 2000; 342: 748 и N Engl J Med 2000; 342: 1376.
- Ванна P: Высокое кровяное давление как фактор риска и прогностический фактор острого ишемического инсульта: когда и как его лечить? Цереброваскский дис. 2004; 17 (приложение 1): 51–57.
- Schmidt R, Fazekas F, Enzinger C, Ropele S, Kapeller P, Schmidt H: Факторы риска и прогрессирование церебральных аномалий, связанных с заболеванием мелких сосудов.J Neural Transm Suppl 2002: 47–52.
- Fournier A, Messerli FH, Achard JM, Fernandez L: Церебропротекция, опосредованная ангиотензином II: гипотеза, подтвержденная недавними рандомизированными клиническими испытаниями. Дж. Ам Колл Кардиол 2004; 43: 1343–1347.
- Schrader J, Luders S, Kulschewski A, Hammersen F, Plate K, Berger J, Zidek W., Dominiak P, Diener HC: Заболеваемость и смертность после инсульта, эпросартан по сравнению с нитрендипином для вторичной профилактики: основные результаты проспективного рандомизированного контролируемого исследования ( МОИСЕЙ).Инсульт 2005; 36: 1218–1226.
- http://www.ontarget-micardis.com/studyprog/ontar/ontarget.htm). Последний доступ 16 ноября 2005 г.
- Ovbiagele B, Kidwell, CS, Saver JL: Расширение показаний к применению статинов при церебральной ишемии: количественное исследование.Arch Neurol 2005; 62: 67–72.
- Greisenegger S, Mullner M, Tentschert S, Lang W, Lalouschek W: Влияние предварительного лечения статинами на тяжесть острых ишемических цереброваскулярных событий. J Neurol Sci 2004; 221: 5–10.
- Давиньон Дж., Лааксонен Р.: Липопротеин-независимые эффекты низкой плотности статинов.Curr Opin Lipidol 1999; 10: 543–559.
- Amarenco P, Bogousslavsky J, Callahan AS, Goldstein L, Hennerici M, Sillsen H, Welch MA, Zivin J: Исследование дизайна и исходных характеристик профилактики инсульта путем агрессивного снижения уровня холестерина (SPARCL). Цереброваскский Дис. 2003; 16: 389–395.
- Берник С., Кац Р., Смит Н.Л., Рапп С., Бхаделия Р., Карлсон М., Куллер Л.: Статины и когнитивные функции у пожилых людей: исследование здоровья сердечно-сосудистой системы. Неврология 2005; 65: 1388–1394.
- Миллер Д., Баркхоф Ф., Наута Дж. Дж .: Повышение уровня гадолиния увеличивает чувствительность МРТ при обнаружении активности болезни при рассеянном склерозе.Мозг 1993; 116: 1077–1094.
- Miller D, Albert PS, Barkhof F, Francis G, Frank JA, Hodgkinson S, Lublin FD, Paty DW, Reingold SC, Simon J: Рекомендации по использованию методов магнитного резонанса в мониторинге лечения рассеянного склероза. Целевая группа Национального общества РС США.Энн Нейрол 1996; 39: 6–16.
- Schmidt R, Scheltens P, Erkinjuntti T., Pantoni L, Markus HS, Wallin A, Barkhof F, Fazekas F: Прогрессирование поражения белого вещества: суррогатная конечная точка для испытаний при заболеваниях мелких сосудов головного мозга. Неврология 2004; 63: 139–144.
Автор Контакты
Брюс Овбиагеле, доктор медицины
Центр инсульта и отделение неврологии Калифорнийского университета в Лос-Анджелесе
710 Westwood Plaza
Лос-Анджелес, Калифорния
(США)Тел.+1 310 794 6379, факс +1 310 267 2063, электронная почта [email protected]
Подробности статьи / публикации
Предварительный просмотр первой страницы
Получено: 28 сентября 2005 г.
Принято: 8 декабря 2005 г.
Опубликовано в Интернете: 14 июля 2006 г.
Дата выпуска: июль 2006 г.
Количество страниц для печати: 8
Количество рисунков: 1
Количество столов: 1
ISSN: 1015-9770 (печатный)
eISSN: 1421-9786 (онлайн)
Для дополнительной информации: https: // www.karger.com/CED
Авторские права / Дозировка препарата / Заявление об ограничении ответственности
Авторские права: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование, или какой-либо системой хранения и поиска информации, без письменного разрешения издателя. .
Дозировка лекарственного средства: авторы и издатель приложили все усилия для обеспечения того, чтобы выбор и дозировка лекарств, указанные в этом тексте, соответствовали текущим рекомендациям и практике на момент публикации.Однако ввиду продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю настоятельно рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новое и / или редко применяемое лекарство.
Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор (-ы) не несут ответственности за любой ущерб, причиненный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в контенте или рекламе.
Что такое болезнь белого вещества? Может быть причиной сосудистой деменции
Болезнь белого вещества изначально считалась нормальным явлением для стареющего мозга.Но доктор Дэниел Манделл и его исследовательская группа обнаружили, что на самом деле это может быть вызвано крошечными инсультами и способствовать сосудистой деменции. (Видео: UHN)
Деменция — это термин, обозначающий снижение умственных способностей, таких как проблемы с памятью, языковые проблемы и психологические нарушения, которые снижают способность человека выполнять повседневные действия. Есть несколько различных заболеваний головного мозга, вызывающих слабоумие; однако у них действительно есть две общие черты: причины этих заболеваний плохо изучены и есть несколько хороших методов лечения от них.
Но исследователи из Нейробиологического центра Крембил обнаружили возможную причину распространенного слабоумия, открытие, которое открывает возможности для лечения. Источник? Заболевание белого вещества (лейкоареоз).
Это ваш мозг в процессе старения.
Человеческий мозг имеет тонкий слой сложенного серого вещества на поверхности и белого вещества внутри. Белое вещество состоит из более чем 100 000 километров нервных волокон, которые соединяют части серого вещества друг с другом, со спинным мозгом и остальными частями тела.
С тех пор, как в 1980-х годах появились компьютерная томография (КТ) и магнитно-резонансная томография (МРТ), врачи заметили, что с возрастом белое вещество мозга обычно дегенерирует (и становится губчатым на вид). К 60 годам эта дегенерация, называемая болезнью белого вещества, присутствует более чем у половины населения.
Первоначально болезнь белого вещества считалась нормальным возрастным изменением. Но за последнее десятилетие медицинские эксперты пришли к пониманию того, что наличие обширных участков заболевания в белом веществе мозга связано со снижением когнитивных функций и деменцией у пациентов.
Бессимптомные инсульты
Это побудило доктора Дэниела Манделла, нейрорадиолога из Объединенного отделения медицинской визуализации (JDMI), и его исследовательскую группу выяснить, что вызывает заболевание белого вещества мозга с возрастом. Поскольку заболевание со временем нарастает, исследователи полагали, что причиной могут быть повторяющиеся крошечные недиагностированные инсульты — инсульт — это когда недостаток кровотока повреждает часть мозга.
Доктор Манделл и его команда выдвинули гипотезу, что каждый крошечный удар может быть достаточно маленьким, чтобы вызвать лишь незначительную потерю функции мозга.Ни пациент, ни его или ее врач не заметят проблемы, пока за многие годы не накопится достаточно крошечных инсультов, которые причинят пациенту достаточно вреда для развития деменции.
Чтобы проверить эту теорию, команда набрала пять взрослых в возрасте от 57 до 79 лет, у которых было заболевание белого вещества головного мозга от умеренной до тяжелой степени и не было доказательств ранее перенесенных инсультов. Каждую неделю в течение 16 недель они делали МРТ своего мозга.
Как они и предполагали, но все же обнаружили удивление, исследователи наблюдали новые крошечные штрихи, появляющиеся в белом веществе в ходе исследования (посмотрите видео выше, чтобы увидеть, как болезнь белого вещества прогрессирует в течение нескольких недель).Эти инсульты не имели явных симптомов, поскольку участники исследования не испытывали слабости, нарушений зрения, речевых или языковых проблем — все это признаки инсульта.
«Мы были удивлены, обнаружив инсульты у большинства участников нашего исследования», — сказал д-р Манделл, который является главным исследователем исследования. «Но что еще более интересно, мы заметили, что в ходе исследования ущерб от этих крошечных ударов стал неотличим от существующей болезни белого вещества участников.«
« Если бы участникам исследования сделали только два МРТ, один раз в начале исследования и еще раз через 16 недель, было бы невозможно сказать, что их обострение болезни белого вещества было вызвано инсультом », — добавил он.
Возможное лечение
Исследование доктора Манделла является первым убедительным доказательством того, что крошечные бесшумные инсульты являются причиной возрастной дегенерации белого вещества мозга, потенциально вызывающей тип деменции, которую можно предотвратить или остановить.
В отличие от большинства дегенеративных типов деменции, лечение которых очень ограничено, этот тип, основанный на сосудистых заболеваниях, потенциально более поддается лечению. Для подтверждения этих результатов необходимы дополнительные исследования, но обнаружение болезни белого вещества может в конечном итоге стать спусковым крючком для агрессивного лечения пациентов с факторами риска инсульта, такими как высокий уровень холестерина, отсутствие физических упражнений, высокое кровяное давление и т.
