Виды костей и их соединения — урок. Биология, Человек (8 класс).
Рис. \(1\). Скелет человека
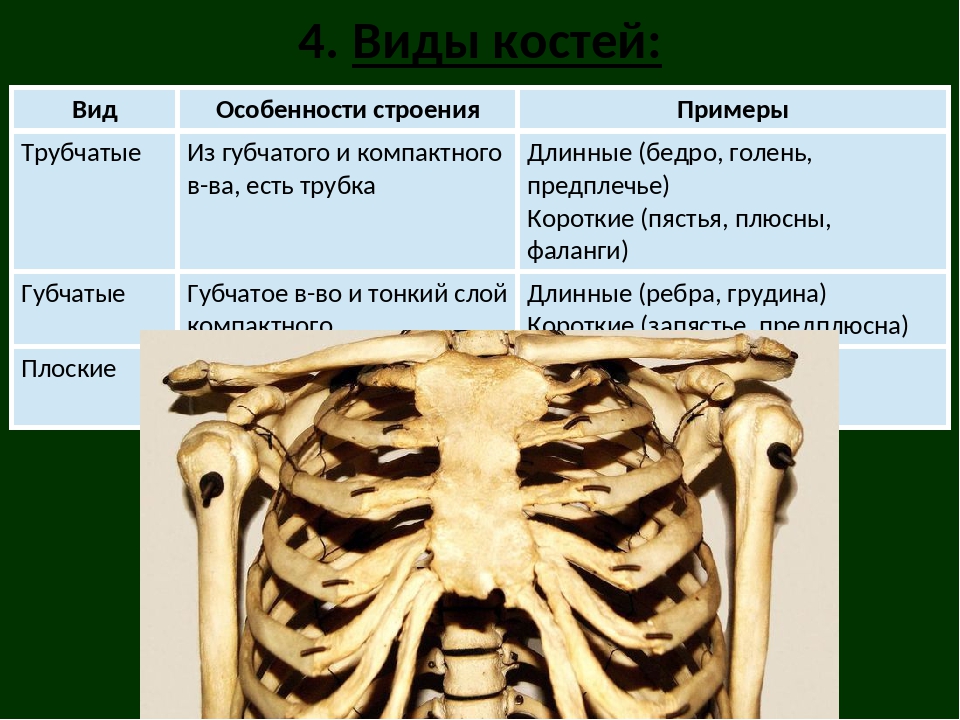
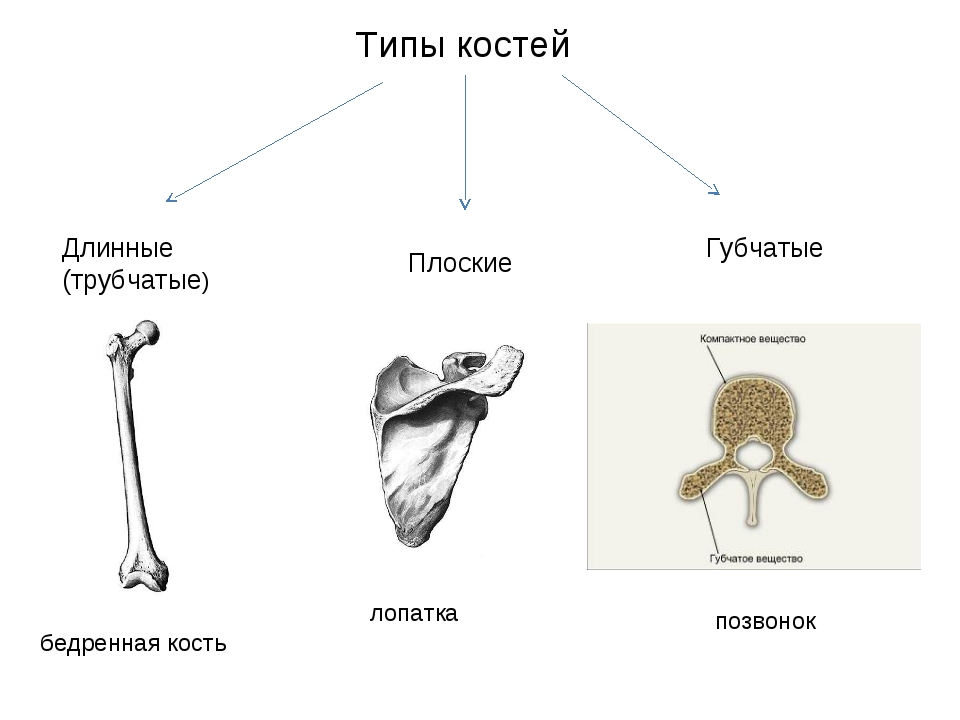
Все кости скелета по строению, происхождению и выполняемым функциям делят на четыре вида.
Трубчатые (плечевая, локтевая, лучевая, бедренная, большая берцовая, малоберцовая) — это длинные кости в форме трубки, имеющие внутри канал с жёлтым костным мозгом. Обеспечивают быстрые разнообразные движения конечностей.
Губчатые (длинные: рёбра, грудина; короткие: кости запястья, предплюсны) — кости, преимущественно содержат губчатое вещество, которое покрыто снаружи слоем компактного вещества. Содержат красный костный мозг, обеспечивающий функцию кроветворения.
Плоские (лопатки, кости черепа) — кости, ширина которых преобладает над толщиной для защиты внутренних органов. Состоят в основном из пластинок компактного вещества. Слой губчатого вещества в них тонкий.
Смешанные — образованы несколькими частями, имеющими разную форму, строение и функции (тело позвонка является губчатой костью, а его отростки — плоскими костями).

Рис. \(2\). Виды костей
Различные виды соединения костей обеспечивают функции частей скелета.
Неподвижное (непрерывное) соединение представляет собой срастание или скрепление соединительной тканью для выполнения защитной функции (соединение костей крыши черепа для защиты головного мозга).
Полуподвижное соединение с помощью небольших хрящевых дисков образуют кости, выполняющие и защитную, и двигательную функции (соединения позвонков межпозвоночными дисками, соединение грудины и рёбер).
Рис. \(3\). Соединения костей
В суставе выделяют:
- суставные поверхности костей;
- суставную сумку;
- суставную полость;
- суставную (синовиальную) жидкость.
Рис. \(4\). Строение сустава
Суставные поверхности соответствуют друг другу по форме и покрыты гиалиновым хрящом. Суставная сумка образует герметичную полость с синовиальной жидкостью. Это способствует скольжению и защищает кость от стирания.
Суставная сумка образует герметичную полость с синовиальной жидкостью. Это способствует скольжению и защищает кость от стирания.
Разные суставы обеспечивают различные направления движений.
Рис. \(5\). Суставы
Источники:
Рис. 1. Скелет человека. Автор: LadyofHats. Общественное достояние. https://upload.wikimedia.org/wikipedia/commons/thumb/5/5b/Human_skeleton_back_ru.svg/530px-Human_skeleton_back_ru.svg.png. 16.08.2021
Рис. 2. Виды костей: © ЯКласс
Рис. 3. Соединения костей: © ЯКласс
Рис. 4. Строение сустава: © ЯКласс
Рис. 5. Суставы: © ЯКласс
Отдел тела | Отдел скелета | Описание |
Голова, череп | Мозговой | Неподвижные кости, образующие сводчатую черепную коробку, в которой помещается мозг. |
Лицевой | Включает непарные (подвижную нижнюю челюсть, сошник, подъязычную кость) и парные (скуловые, носовые, нёбные) кости | |
Туловище | Позвоночник | Включает шейный (7 позвонков), грудной (12), поясничный (5), крестцовый (5) и копчиковый (3–5) отделы. Позвонки полуподвижные (соединены с помощью хрящевых прокладок), кроме крестца (сращён). Дуги позвонков образуют трубку, в которой находится спинной мозг |
Грудная клетка | Образована грудными позвонками и рёбрами, соединёнными спереди с грудиной. Всего 12 пар рёбер по числу позвонков. Передняя часть рёбер переходит в хрящевую ткань, чтобы обеспечивать подвижность при дыхании | |
Верхние конечности | Плечевой пояс | Состоит из лопаток, находящихся на стороне спины, и ключиц, выступающих спереди. |
Конечности | Состоят из плеча, предплечья и кисти. Плечо образовано плечевой костью, предплечье – локтевой и лучевой, кисть – запястьем, пястью, фалангами пальцев. Подвижны соединения в плече, локте, запястье и пальцах | |
Нижние конечности | Тазовый пояс | Состоит из тазовых костей, крестца и копчика. Тазовые кости образованы парными подвздошными, седалищными, лобковыми костями, которые соединены неподвижно в костное кольцо и вместе с крестцом образуют тазовую полость. Лобковые кости спереди соединены с помощью хряща и образуют лобок. Таз женщин шире, а тазовая полость больше, чем у мужчин |
Конечности | Состоят из бедра, голени и стопы. Бедро образовано бедренной костью, голень – большеберцовой и малоберцовой костями, стопа – предплюсной, плюсной и флангами. Спереди коленный сустав прикрывает наколенник или коленная чашечка |
Кости: строение, состав, типы костей, типы соединений и их характеристика | Биология.
 Реферат, доклад, сообщение, краткое содержание, конспект, сочинение, ГДЗ, тест, книга
Реферат, доклад, сообщение, краткое содержание, конспект, сочинение, ГДЗ, тест, книга1. Охарактеризуйте строение и состав костей.
В состав костей входят минеральные и органические вещества. Минеральные вещества (в костях содержится весь фосфор и кальций организма, 0,5% магния и натрия) придают кости твердость, составляют 70% от массы костей. Кости способны отдавать минеральные вещества в кровь. Органические вещества придают кости эластичность и упругость, составляют 30% от массы костей. Кость состоит из всех видов тканей, но костная преобладает. Костная ткань — соединительная ткань, состоит из клеток (остеоциты, остеобласты, остеокласты) и межклеточного вещества (коллагеновые и осеиновые волокна). Кость покрыта надкостницей (соединительно-тканной оболочкой). Наружный слой состоит из коллагеновых волокон (придают прочность), здесь проходят нервы и кровеносные сосуды. Внутренний слой — костная ткань. В нем находятся клетки костной ткани, за счет которых происходит развитие, рост в толщину и регенерация костей после повреждения.
Функции надкостницы:
б) трофическая;
в) костеобразующая.
Рост костей в толщину происходит за счет деления клеток внутренней поверхности надкостницы, в длину — за счет деления клеток хрящевых пластинок, расположенных вблизи концов костей.
На рост костей влияют гормоны роста, например гормоны, выделяемые гипофизом. Рост костей происходит до 22-25 лет. Замена старого костного вещества новым продолжается в течение всей жизни человека.
Чем больше нагрузка на скелет, тем активнее происходят процессы обновления костей и тем прочнее становится костное вещество.
2. Какие типы костей различают?
В зависимости от формы, строения, функции и развития выделяют 4 группы костей:
а) Трубчатые кости располагаются в отделах скелета, где совершаются движения с большой амплитудой (конечности). Делятся на длинные (плечо, предплечье, бедро, голень) и короткие (дистальная часть фаланги пальцев).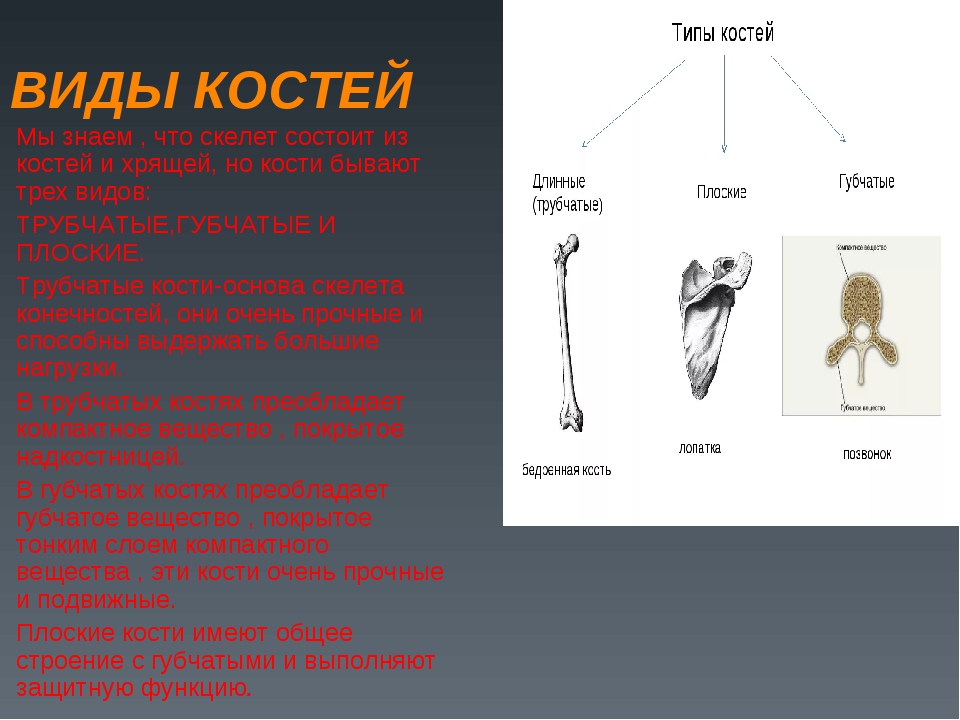 Трубчатая кость состоит из диафиза (тело кости) и эпифиза. Внутри диафиза — полость, заполненная желтым костным мозгом. В эпифизе — красный костный мозг — орган кроветворения.
Трубчатая кость состоит из диафиза (тело кости) и эпифиза. Внутри диафиза — полость, заполненная желтым костным мозгом. В эпифизе — красный костный мозг — орган кроветворения.
Трубчатые кости — основа скелета конечностей. Они очень прочны и способны выдерживать большую физическую нагрузку. Полость внутри костей, не снижая прочности, значительно уменьшает их массу.
б) Губчатые кости состоят из губчатого вещества, покрыты тонким слоем компактного. Длинные (ребра, грудина) и короткие (позвонки).
в) Плоские кости представляют собой 2 пластинки компактного костного вещества, между которыми — губчатое вещество (грудина, крыша черепа). Основная функция защитная.
г) Смешанные кости состоят из нескольких частей, имеющих разную функцию и развитие (кости основания черепа).
3. Какие типы соединения костей различают в скелете человека? Дайте характеристику каждому из них. Приведите примеры.
В скелете человека различают три типа соединения костей:
а) Неподвижные соединения образуются путем срастания костей (позвонки копчика).
б) Полуподвижные соединения. Многие кости соединены между собой хрящевыми прокладками, обладающими упругостью и эластичностью. Например, хрящевые прокладки между позвонками обеспечивают гибкость позвоночника. Материал с сайта //iEssay.ru
в) Подвижные соединения — суставы. Наиболее типичный план строения сустава таков: на одной из сочленяющихся костей находится суставная впадина, куда входит головка другой кости. Суставная впадина и головка соответствуют друг другу по форме и размеру, а их поверхность покрыта слоем гладкого хряща. Суставные поверхности костей тесно соприкасаются друг с другом. Это обеспечивается наличием внутрисуставных связок — прочных тяжей из соединительной ткани.
- строение и свойства костей типы их соеденений
- название костей и где они находятся
- кости и их типы костей
- реферат на тему строение костей и их состав
- типы строения костей
СКЕЛЕТ ПОЯСОВ КОНЕЧНОСТЕЙ –ДОБАВОЧНЫЙ СКЕЛЕТ. СОЕДИНЕНИЯ КОСТЕЙ
Урок биологии 8 класс Тема: СКЕЛЕТ ПОЯСОВ КОНЕЧНОСТЕЙ –ДОБАВОЧНЫЙ СКЕЛЕТ. СОЕДИНЕНИЯ КОСТЕЙ
Задачи: продолжить изучение строения и функций
опорно-двигательной
системы; выявить особенности скелета, связанные с прямохождением и
трудовой деятельностью; познакомить с типами соединения костей.
Оборудование: модели скелетов человека и млекопитающих, таблицы с изображением скелетов человека и млекопитающих, таблица с изображением типов соединения костей, презентация
Ход урока
1. Проверка знаний. Фронтальный опрос — Какое значение имеет скелет? — Что составляет осевой скелет и добавочный7 — Назовите отделы позвоночника и строение позвонка? -Определите, к каким отделам скелета относятся заданные кости:
1вариант Грудина, теменная кость,
верхнечелюстная кость, лобная кость, затылочная кость, грудной позвонок.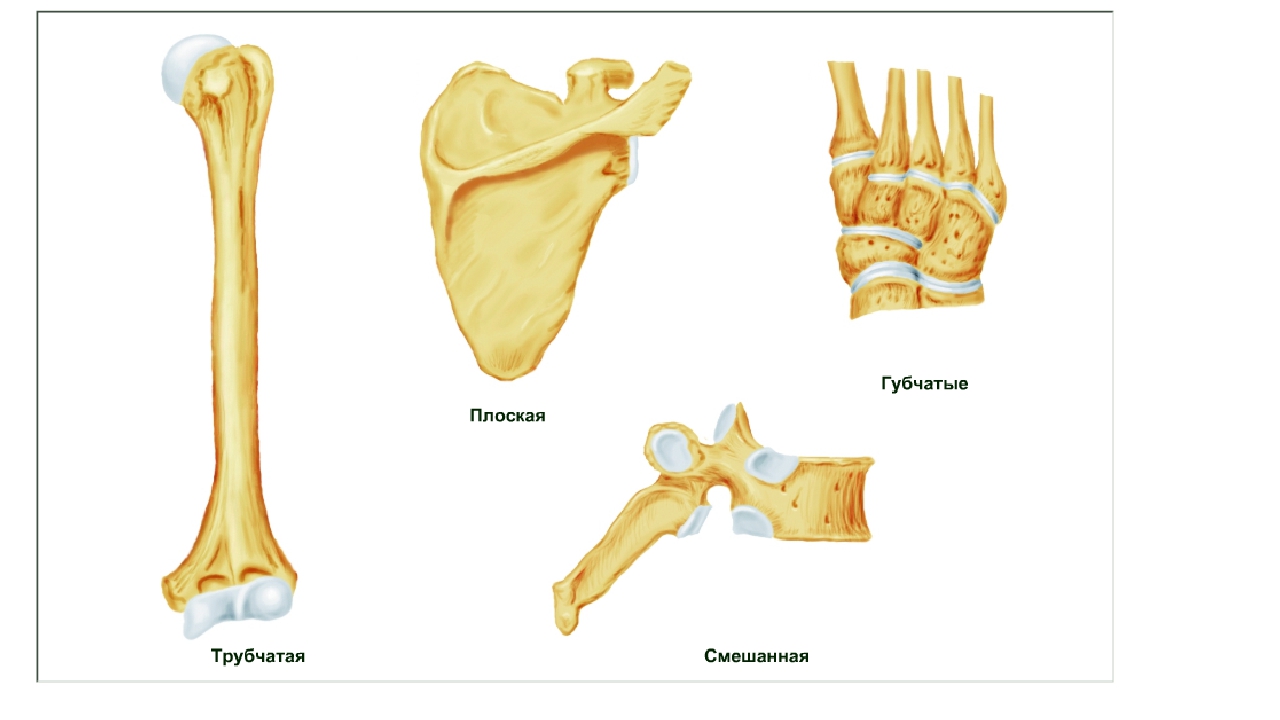
2 вариант Шейный позвонок, скуловая кость, носовая кость, крестцовый позвонок, поясничный позвонок, клиновидная кость II. Изучение нового материала. Скелет верхних конечностей: Плечевой пояс и скелет свободных верхних конечностей. Строение, функции. Продолжение заполнения таблицы
Отделы тела | Отделы скелета | Кости скелета | Тип костей | Характер соединения костей | Особенности скелета человека |
Верхняя конечность | Плечевой пояс | Две лопатки Две ключицы | Плоские (широкие) Длинные трубчатые | Подвижное | Плечевой пояс подвижный, обеспечивает большую подвижность руки |
Свободная конечность Плечо Предплечье Кисть
| -Плечевая кость -Локтевая и лучевая -Кости запястья, пястья, фаланги пальцев | Длинные трубчатые короткие губчатые короткие трубчатые | Подвижное | Облегченная конструкция скелета, высокая
подвижность в плечевом суставе. | |
Нижняя конечность | Тазовый пояс | Парные кости – подвздошные, седалищные, лобковые | Плоские | Неподвиж ное | Рсширенная форма таза,широкораставленные тазобедренные суставы. |
| Свободная конечность Бедро Голень Стопа | -Бедренная Большеберцовая малоберцовые предплюсны (таранная и пяточная) плюсны фаланги пальцев | Длинные трубчатые короткие губчатые короткие трубчатые |
| Мощное разв. костей ног, выпрямленность в коленном суставе,
мощное развитие связок Опорная стопа с мощным бол. |
Беседа с использованием рисунков 27, 28 нас. 57. и 29, 30 нас. 58.
3. Соединение костей.
Самостоятельная работа с учебником. Задание: используя текст на с. 59, составьте схему «Типы соединения костей».
Возможный вариант схемы
Типы соединения костей
неподвижные полуподвижные подвижные
костный шов с помощью хрящевых прокладок суставы
а) Неподвижные соединения: нахождение таких соединений, причины существования таких соединений. Беседа.
Неподвижное соединение костей происходит путем их срастания. Движения при этом ограничены или вовсе отсутствуют. Неподвижное соединение костей имеет защитное значение.
б) Полуподвижные соединения: нахождение таких соединений, причины
существования таких соединений. Беседа.
Беседа.
Полуподвижность достигается упругими хрящевыми прокладками между костями. Такие прокладки находятся между отдельными позвонками. При сокращении мышц эти прокладки сжимаются и позвонки сближаются. При ходьбе, беге, прыжках прослойки упругого хряща действуют как амортизаторы, смягчая резкие толчки и предохраняя тело от сотрясения. Такое соединение имеет опорное, защитное и двигательное значение.
в) Подвижные соединения костей. Строение сустава.
Объяснение учителя.
Подвижное соединение встречается чаще. Их называют суставами . Они обеспечивают условия для движение частей тела. Например, суставы: коленный, локтевой, лучезапястный.
Суставы бывают простыми и сложными. В простом соединяются две кости (между фалангами пальцев), а в сложном три и более (локтевой, коленный, голеностопный).
Строение сустава:
1. Суставные поверхности (покрыты гладким хрящем)
2. Суставная головка (выпуклая кость)
3. Суставная впадина (вогнутая кость)
Суставная впадина (вогнутая кость)
4. Суставная сумка ( заполненная суставной жидкостью)
5.Связки ( укрепляют суставы)
I II. Закрепление знаний.
Особенности строения скелета человека, связанные с трудовой деятельностью и прямохождением?
Выберите из каждой колонки по одному соответствующие ответы, начиная с первого.
1. Грудная клетка В. Сводчатая
2. Стопа Г. Широкий, как чаша
3. Позвоночник Д. Большой палец противопоставляется остальным
4. Верхняя конечность Е. Опора для внутренних органов
5. Таз Ж. Защита внутренних органов
А. Имеет изгибы З. Удерживание орудий труда
Б. Расширена в стороны И. Пружинит, смягчает толчки при движении
Ответы: 1 — Б, Ж 2 – В, И 3 — А, Е 4 — Д, З 5 — Г, Е
Задание
на дом: § 12, ответить на вопросы в конце параграфа; повторить из § 8 материал о
мышечных тканях.
Боль в пятке — причины появления, при каких заболеваниях возникает, диагностика и способы лечения
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Боль в пятке: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.Определение
Боль в пяточной области не только вызывает дискомфорт, но и лишает человека возможности долго стоять и нормально передвигаться. Боль обычно возникает вследствие воспалительных изменений тканей, окружающих пяточную кость, и часто носит длительный и рецидивирующий характер. Пяточная кость – наиболее крупная из всех костей стопы, и на нее приходится наибольшая нагрузка при ходьбе.
Разновидности боли в пятке
В зависимости от заболевания, которое сопровождается болью в пятке, характер болевого синдрома будет различаться. Возможна острая боль, возникающая при ходьбе и в положении стоя. Боль может появляться утром, когда человек встает после сна, затем она уменьшаться или проходить совсем. В других случаях боль в пятке носит ноющий характер и не связана с нагрузкой на ногу. При ряде заболеваний боль беспокоит не только при ходьбе, но и ночью, в покое. Иногда вместе с болью ощущается онемение, покалывания и «мурашки», кожа может краснеть, появляются отеки.
Боль может усиливаться при разгибании стопы, а в некоторых случаях вызывает ограничение подвижности в голеностопном суставе.
Возможные причины боли в пяткеПричины боли в пятке можно разделить на физиологические и патологические. К первым относится перенапряжение стопы из-за ношения неудобной обуви или обуви с плоской подошвой и без супинатора, из-за длительного стояния, из-за повышенной нагрузки на стопу во время беременности или при быстром наборе веса.
Патологическими причинами служат различные заболевания и травмы.
Тендинит ахиллова сухожилия и подошвенный фасцит (пяточная шпора). При физических нагрузках и перерастяжении сухожилий, прикрепленных к пяточной кости, возникает их воспаление, которое проявляется болью в пятке и в области сухожилия при физических нагрузках, локальным отеком по задней стороне пятки, чувством слабости в голеностопном суставе. Сгибание и разгибание стопы болезненно. Тендинит ахиллова сухожилия (ахиллодиния) часто бывает следствием спондилоартрита (заболевания межпозвоночных дисков), гипермобильности суставов (наследственного заболевания или предрасположенности), плоскостопия, укорочения одной из нижних конечностей вследствие перекоса таза при межпозвоночных грыжах.
Подошвенный фасциит, или пяточная шпора, также характеризуется воспалением подошвенного связочного аппарата. Следствие этого процесса – формирование пяточной шпоры, то есть краевых костных разрастаний (остеофитов). Пациенты отмечают боль при ходьбе и стоянии по всей подошвенной поверхности стопы.
Чаще всего боль дает о себе знать при первых шагах после ночного сна или длительного сидения.
Тарзальный туннельный синдром характеризуется поражением волокон большеберцового нерва вследствие его сдавления между связками голеностопа при травмах, костных разрастаниях и опухолях мягких тканей. Синдром сопровождается жгучей болью и покалыванием в области пятки, а иногда и всей подошвы. Боль усиливается при разгибании стопы. Возможно изменение чувствительности кожи в области подошвы. При тарзальном туннельном синдроме часто нарушаются функции стопы и походка.Травматические повреждения пяточной кости (ушиб, трещина, перелом). Травма пяточной кости чаще возникает при падении или прыжка с высоты в вертикальном положении. Сильный удар приводит к ушибу или нарушению целостности кости (часто сочетается с переломами других костей нижних конечностей) и вызывает резкую боль, невозможность опоры на пятку, отек, который охватывает стопу и нижнюю часть голени.
Повреждение пяточной кости редко сопровождается внешним нарушением целостности мягких тканей, чаще отмечаются гематомы на боковых поверхностях стопы.
Ахиллобурсит — заболевание характеризуется воспалением синовиальной сумки, которая располагается между пяточным сухожилием и пяточной костью, и проявляется болью внизу и сзади пятки, в месте прикрепления ахиллова сухожилия к пяточному бугру, покраснением и отеком в области пяточного бугра, а также частичным ограничением подвижности стопы. Причинами ахиллобурсита могут быть травматические повреждения вследствие ношения тесной обуви, избыточные физические нагрузки на голеностопный сустав, деформация Хаглунда. Реже заболевание обусловливают метаболические и гормональные нарушения, аллергические реакции, аутоиммунные заболевания, инфекции.Реактивный артрит — артрит суставов, частью которых является пяточная кость (сочленения пяточной кости с костями предплюсны – таранной и ладьевидной).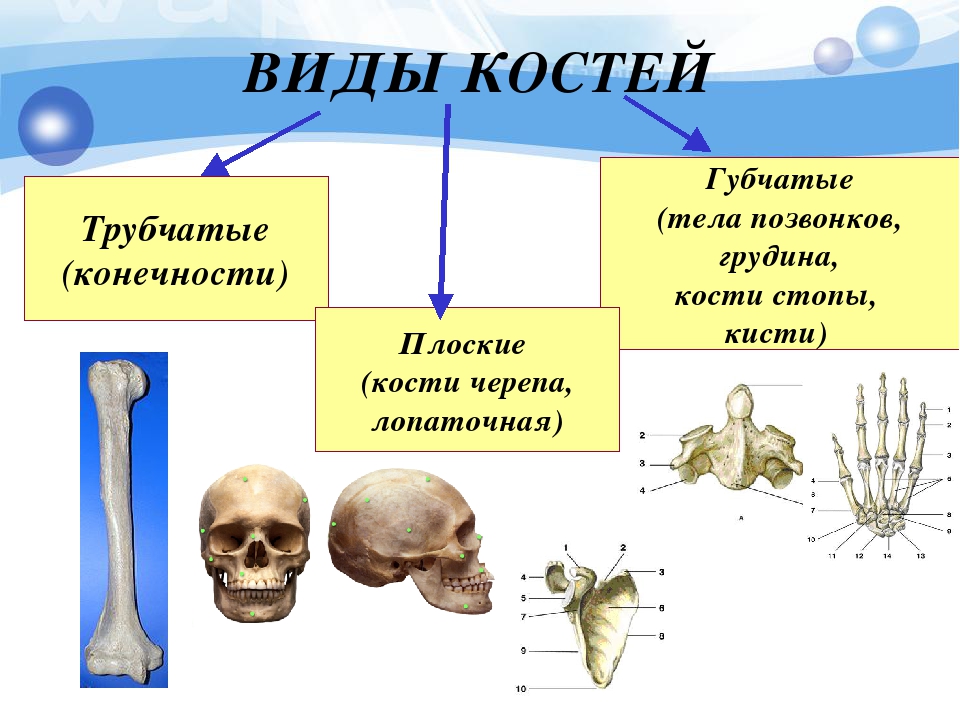
Болезнь развивается как следствие перенесенных инфекционных заболеваний (чаще всего – урогенитальных).
Болевой синдром появляется через две недели – месяц после перенесенной инфекции. Выраженная боль чувствуется не только при нагрузке, но и в покое. Могут поражаться обе пятки, отмечаются припухлость и покраснение.Инфекционные заболевания (туберкулез, гонококковая инфекция, остеомиелит пяточной кости) – довольно редкая причина возникновения боли в пятке. Микобактерии туберкулеза и гонококки могут развиваться в губчатых костях и эпифизах трубчатых костей, что приводит к их локальной деструкции. Процесс сопровождается болью, отеком в области голеностопного сустава и покраснением. Нарушается подвижность стопы.
Деформация Хаглунда — окостенение пяточной кости, при котором происходит костно- хрящевое разрастание в области пяточного бугра, сопровождающееся появлением нароста (остеофита) в области прикрепления ахиллова сухожилия.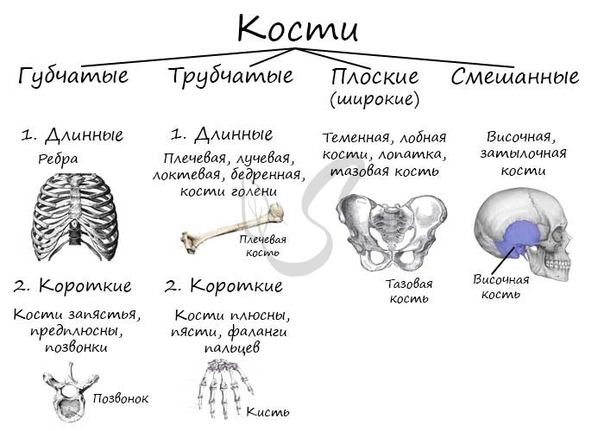 К такой патологии могут приводить высокий свод или плосковальгусная деформация стопы (сочетание плоскостопия и вальгусной деформации стопы – отклонения большого пальца в сторону остальных пальцев), снижение эластичности сухожилий.
К такой патологии могут приводить высокий свод или плосковальгусная деформация стопы (сочетание плоскостопия и вальгусной деформации стопы – отклонения большого пальца в сторону остальных пальцев), снижение эластичности сухожилий.
Вальгусная деформация обеих стоп
Постоянное трение ахиллова сухожилия приводит к развитию воспалительного процесса и изменению хряща, иногда с образованием острых шипов. Пациенты могут заметить твердый выступ на задней поверхности пятки. Функция стопы, как правило, не нарушается, но воспаление суставной сумки и оболочки сухожилия приводит к болевому синдрому при ходьбе, а иногда и в покое.
Заболевание чаще отмечается у женщин молодого возраста из-за ношения неудобной обуви на высоких каблуках.
Эпифизит пяточной кости — это заболевание развивается у детей в возрасте 8–15 лет из-за нарушения процессов оссификации (окостенения) пяточной кости. В норме пяточная кость формируется в результате деятельности двух центров окостенения. Один из них функционирует с рождения ребенка, другой – примерно с 8 лет. Между центрами окостенения располагается хрящевая ткань, которая со временем преобразуется в костную. В случае перегрузки хрящевой ткани между этими двумя участками возможна деградация хряща или частичный разрыв, что сопровождается воспалением и болью на задней и боковой поверхности пятки, усиливающейся при нагрузке. Наблюдается ограничение амплитуды движения, а при разрыве хряща – отек и покраснение.
Один из них функционирует с рождения ребенка, другой – примерно с 8 лет. Между центрами окостенения располагается хрящевая ткань, которая со временем преобразуется в костную. В случае перегрузки хрящевой ткани между этими двумя участками возможна деградация хряща или частичный разрыв, что сопровождается воспалением и болью на задней и боковой поверхности пятки, усиливающейся при нагрузке. Наблюдается ограничение амплитуды движения, а при разрыве хряща – отек и покраснение.Остеохондропатия апофиза бугра пяточной кости, или болезнь Хаглунда–Шинца — заболевание характеризуется асептическим (неинфекционным) омертвением бугра пяточной кости, которое возникает из-за ее травмы, ношения неудобной обуви, вследствие наследственной предрасположенности и нарушения гормонального баланса. Прикрепленные к бугру сухожилия при перенапряжении постоянно травмируют кость, что вызывает боль и отек, которые усиливаются после нагрузки и при разгибании стопы. Над пяточным бугром можно увидеть припухлость.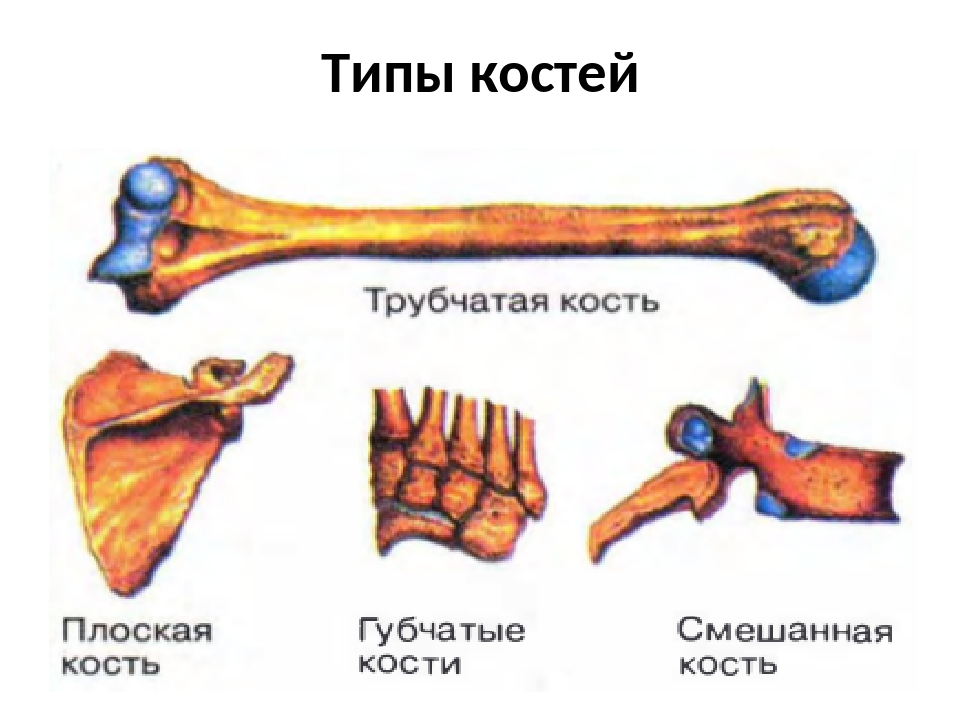 Замечено, что болезнь Хаглунда–Шинца чаще встречается у девочек в возрасте 12–16 лет.
Замечено, что болезнь Хаглунда–Шинца чаще встречается у девочек в возрасте 12–16 лет.
Чтобы уменьшить выраженность боли, пациенты при ходьбе опираются на носок.
Боль в пятке могут причинять дерматологические и сосудистые патологии, которые диагностируются у больных сахарным диабетом (трофические язвы при синдроме диабетической стопы), при варикозном расширении вен, тромбофлебите. Пациенты испытывают незначительную дергающую, тянущую боль, быструю утомляемость. Наблюдаются отеки стоп, перемежающаяся хромота.К каким врачам обращаться при боли в пятке
При боли в пятке, особенно в случае травмы, рекомендуется обратиться к травматологу-ортопеду. В некоторых случаях требуется консультация инфекциониста и других специалистов для определения заболеваний, которые вызвали появление боли.
Диагностика и обследования при боли в пятке
При появлении боли в области пятки необходимы тщательный сбор анамнеза и инструментальные исследования. В первую очередь назначают клинический анализ крови, а также анализы на инфекционные заболевания – хламидийную и гонококковую инфекции, туберкулез.
В первую очередь назначают клинический анализ крови, а также анализы на инфекционные заболевания – хламидийную и гонококковую инфекции, туберкулез.
Виды костей и их соединения. Строение плоских костей
Задание 1. Изучите строение различных видов костей в ходе лабораторной работы.
Пользуясь текстом параграфа 15 учебника, объясните, где находится губчатое вещество, а где компактное.
Наружный слой кости представлен толстой (в диафизах трубчатых костей) или тонкой (в эпифизах трубчатых костей, в губчатых и плоских костях) пластинкой компактного вещества. Под компактным веществом располагается губчатое (трабекулярное) вещество, пористое, построенное из костных балок с ячейками между ними, по виду напоминающие губку.
Назовите особенности строения плоских костей.
Плоские кости образованы двумя пластинами компактного костного вещества, между которыми располагается губчатое вещество. Служит защитой организма. Примеры: тазовые кости, свод черепа, ребра, лопатка, грудина.
Служит защитой организма. Примеры: тазовые кости, свод черепа, ребра, лопатка, грудина.
Сделайте вывод о взаимосвязи строения и функций костей.
Различают 4 вида костей:
Трубчатые — выглядят в форме трубки, внутри которых заполнены красным и желтым костным веществом. Необходима большая амплитуда движений (рычаги тела)
Губчатые кости участвуют в образовании стенок полостей, содержащих внутренние органы. Внутри губчатых костей располагается губчатое вещество кости, состоящее из костных перекладин.
Плоские кости образованы двумя пластинами компактного костного вещества, между которыми располагается губчатое вещество. Служит защитой организма.
Смешанные кости имеют сложную форму, так как состоят из нескольких частей, которые имеют разные очертания и различное строение. Такие особенности обусловлены различием функции частей этих костей.
Задание 2. Проверьте себя. Заполните таблицу.
Проверьте себя. Заполните таблицу.
Сравнительная характеристика различных видов костей
Составьте самостоятельно памятку для домашней аптечки, пользуясь текстом параграфа.
Первая помощь при повреждениях опорно-двигательного аппарата
6.3 Костная структура: Шон Маккарти (Песчаная яма)
AU_SANDPIT_1078466
6.3 Костная структура
перейти к содержанию Щиток приборовАвторизоваться
Панель приборов
Календарь
Входящие
История
Помощь
- Мой Dashboard
- AU_SANDPIT_1078466
- Страницы
- 6.
 3 Костная структура
3 Костная структура
- Дом
- Модули
- Тесты
- Файлы
- Чтения по курсу
- Инструментарий
- Значки
- SELT
Соответствующая анатомия, базовая биомеханика и перспективы визуализации
Радиология.Июль 2016 г .; 280 (1): 21–38.
От отделения радиологии (M.N.P.) и радиологической службы, VA San Diego Healthcare System (C.B.C.), UC San Diego Medical Center, 200 W Arbor Dr, San Diego, CA 92103; и отделение радиологии, UCSD Teleradiology and Education Center, La Jolla, Calif (D.L.R.).
Автор, ответственный за переписку. Авторское право, 2016 г., Радиологическое общество Северной Америки, Inc. Эта статья цитируется в других статьях в PMC.
Abstract
Знание макроскопической и микроскопической анатомии, а также базовой биомеханики кости обеспечивает основу для лучшего понимания того, как эта ткань реагирует на измененные механические силы, и проливает свет на визуальные эффекты, связанные с обоими острые и повторяющиеся травмы хряща, кортикального слоя и губчатого вещества кости.
Abstract
Кость или хрящ, или и то, и другое, часто травмируются в результате единичного эпизода травмы или повторяющегося чрезмерного использования. Возникающие в результате структурные повреждения различны, что определяется сложным макроскопическим и микроскопическим составом этих тканей. Кроме того, биомеханические свойства как хряща, так и кости неоднородны, что зависит от точного возраста и уровня активности человека, а также от конкретного анатомического расположения в скелете. Из различных гистологических компонентов, которые обнаруживаются в хрящах и костях, коллагеновые волокна и пучки наиболее влияют на передачу приложенных к ним сил, в значительной степени объясняя расположение и направление возникающих внутренних напряжений, которые развиваются в этих тканях. Следовательно, глубокое знание анатомии, физиологии и биомеханики нормальных костей и хрящей служит предпосылкой для полного понимания как того, как эти ткани адаптируются к физиологическим стрессам, так и паттернов тканевого разрушения, развивающегося в ненормальных условиях. Такие знания составляют основу для более точной оценки разнообразных особенностей визуализации, возникающих после острых травм и повреждений скелета, вызванных стрессом.
Следовательно, глубокое знание анатомии, физиологии и биомеханики нормальных костей и хрящей служит предпосылкой для полного понимания как того, как эти ткани адаптируются к физиологическим стрессам, так и паттернов тканевого разрушения, развивающегося в ненормальных условиях. Такие знания составляют основу для более точной оценки разнообразных особенностей визуализации, возникающих после острых травм и повреждений скелета, вызванных стрессом.
© RSNA, 2016
Цели обучения:
После прочтения статьи и прохождения теста читатель сможет:
■ Описать цикл микроповреждений и ремоделирования кости в ответ на ежедневная активность
■ Опишите нормальную морфологию суставного хряща и то, как он не работает при травме
■ Опишите анатомию и биомеханические свойства кортикальной кости и губчатой кости
■ Обсудите последовательность происходящих изменений в кости во время повторяющейся травмы
Заявление об аккредитации и назначении
RSNA аккредитована Советом по аккредитации непрерывного медицинского образования (ACCME) для обеспечения непрерывного медицинского образования врачей. RSNA назначает эту основанную на журнале деятельность SA-CME максимум на 1.0 AMA PRA Category 1 Credit ™ . Врачи должны претендовать только на заслугу, соизмеримую со степенью их участия в этой деятельности.
RSNA назначает эту основанную на журнале деятельность SA-CME максимум на 1.0 AMA PRA Category 1 Credit ™ . Врачи должны претендовать только на заслугу, соизмеримую со степенью их участия в этой деятельности.
Заявление о раскрытии информации
ACCME требует, чтобы RSNA, как аккредитованный поставщик CME, получила подписанные заявления о раскрытии информации от авторов, редакторов и рецензентов для этой деятельности. Для этой журнальной деятельности CME раскрытие информации об авторах перечислено в конце этой статьи.
Введение
Разрушение костей и хрящей может происходить только на микроскопическом уровне или на микроскопическом и макроскопическом уровнях. Такой отказ связан с несоответствием между силами, приложенными к ткани, и ее способностью противостоять таким силам, ее силой. Прочность скелета зависит от свойств материала его композитных тканей. Следовательно, чтобы понять, каким образом кость и хрящ перестают работать после острого эпизода травмы или повторяющегося стресса, необходим первоначальный краткий обзор эмбриологии и макроскопической и микроскопической анатомии.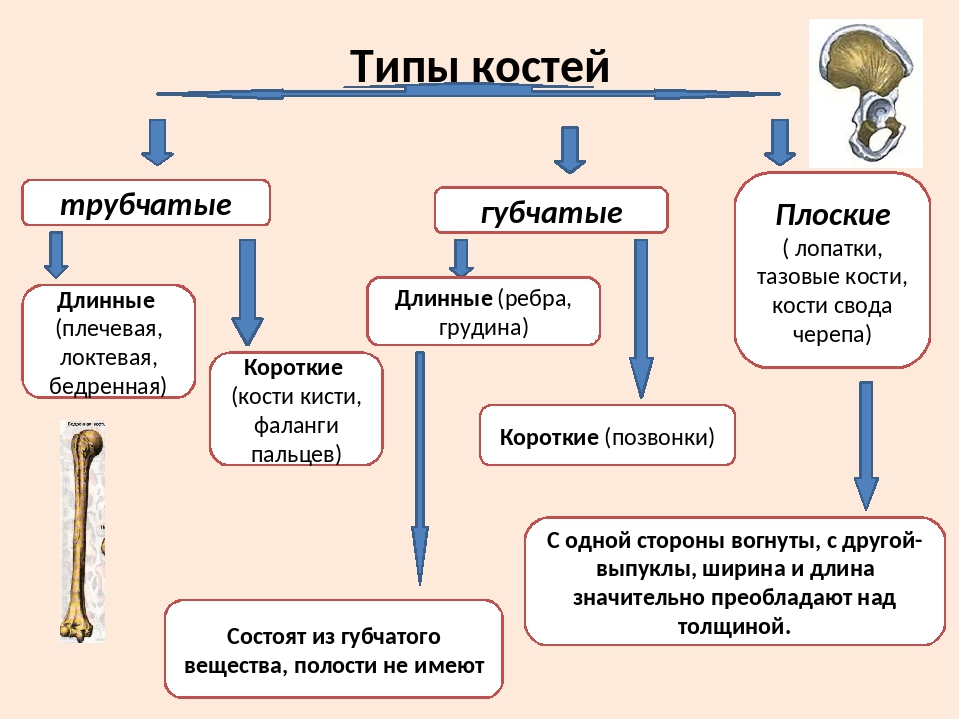 После этого рассматриваются основные биомеханические принципы, объясняющие паттерны разрушения хряща, субхондральной костной пластинки, кортикальной и губчатой кости, которые встречаются клинически.
После этого рассматриваются основные биомеханические принципы, объясняющие паттерны разрушения хряща, субхондральной костной пластинки, кортикальной и губчатой кости, которые встречаются клинически.
Развитие и рост скелета
Кость развивается в соответствии с двумя различными процессами: внутримембранозная оссификация и эндохондральная оссификация (1,2). Внутримембранозная оссификация включает образование кости, возникающее непосредственно в высокососудистых листах конденсированной примитивной мезенхимы.Формирование эндохондральной кости, которое является более доминирующим процессом, связано с упорядоченным и прогрессирующим окостенением матрицы, состоящей из хряща, с образованием первичных и вторичных центров окостенения, которые в конечном итоге сливаются в единую структуру.
Внутримембранозная оссификация инициируется пролиферацией слоев мезенхимальных клеток с последующим их преобразованием в клетки-остеопрогениторы, а затем в остеобласты, которые секретируют сеть, состоящую из коллагеновых волокон и аморфного основного вещества (1). Этот примитивный остеоид со временем характеризуется увеличением областей и слоев кальцинированной и окостеневшей ткани, которые в определенных областях поддерживают сосудистые пространства, которые становятся участками кроветворной ткани. Участки образования внутримембранозной кости включают кости свода черепа, хотя аналогичный процесс происходит на поверхности большинства костей, где покрывающая надкостница представляет собой мезенхимальную ткань, ответственную за развитие оболочки из компактной кортикальной кости. Наружная и внутренняя поверхности коры покрыты фиброзным и коллагеновым слоями ткани, обозначаемыми соответственно надкостницей и эндостом.Оба слоя содержат все клетки, необходимые для обновления костной ткани. Надкостничный слой более толстый, менее ячеистый и прочно прикреплен к кости за счет проникновения волокон коллагена. Надкостница более плотно прилегает к коре в зрелом скелете по сравнению с незрелым скелетом, что объясняет легкость, с которой надкостница поднимается кровоизлиянием, инфекционным экссудатом или новообразованием, и тем самым стимулирует образование новой кости в первые годы.
Этот примитивный остеоид со временем характеризуется увеличением областей и слоев кальцинированной и окостеневшей ткани, которые в определенных областях поддерживают сосудистые пространства, которые становятся участками кроветворной ткани. Участки образования внутримембранозной кости включают кости свода черепа, хотя аналогичный процесс происходит на поверхности большинства костей, где покрывающая надкостница представляет собой мезенхимальную ткань, ответственную за развитие оболочки из компактной кортикальной кости. Наружная и внутренняя поверхности коры покрыты фиброзным и коллагеновым слоями ткани, обозначаемыми соответственно надкостницей и эндостом.Оба слоя содержат все клетки, необходимые для обновления костной ткани. Надкостничный слой более толстый, менее ячеистый и прочно прикреплен к кости за счет проникновения волокон коллагена. Надкостница более плотно прилегает к коре в зрелом скелете по сравнению с незрелым скелетом, что объясняет легкость, с которой надкостница поднимается кровоизлиянием, инфекционным экссудатом или новообразованием, и тем самым стимулирует образование новой кости в первые годы. жизни.
жизни.
Эндохондральное (внутрихрящевое) окостенение заметно в костях аппендикулярного скелета, осевого скелета и основания черепа.В основе этого процесса лежит разрушение хрящевой ткани, происходящей из примитивной мезенхимы, и ее последующее замещение костью (1,2). Начальные участки этого процесса обозначаются центрами окостенения (первичными и вторичными), их количество и расположение варьируются от одной кости к другой. Хотя это обсуждение подчеркивает процесс эндохондрального окостенения, наблюдаемый в трубчатой кости, увеличенные ядра окостенения обнаруживаются также и в других костях, включая запястье, предплюсну и кости позвоночника.
В трубчатых костях первичный центр окостенения развивается в центре кости и вторичный центр (центры), на концах кости, в эпифизах или апофизах, или в обоих. Что касается первичного центра окостенения, центральный очаг оссификации развивается в результате последовательности гипертрофии и гибели хондроцитов, кальцификации и сосудистой инвазии, трансформации остеобластов и превращения в костные пространства, содержащие костный мозг (1). Затем окостенение переходит к концам кости.Мигрирующая граница эндохондрального окостенения, продвигающаяся к концу кости, становится лучше очерченной, в конечном итоге формируя пластинку роста, расположенную между диафизом и эпифизом трубчатой кости (). На концах трубчатых костей происходят те же морфологические изменения, ведущие к созданию увеличивающегося ядра окостенения, вторичного центра окостенения. Дальнейшее созревание приводит к постепенному превращению вторичного центра окостенения в кость, оставляя субхондральную костную пластинку на эпифизарной стороне у основания суставного хряща и физический рубец на метафизарной стороне пластинки.Хрящ, оставшийся на субхондральной поверхности, образует зрелый гиалиновый хрящ, который характеризует суставные поверхности.
Затем окостенение переходит к концам кости.Мигрирующая граница эндохондрального окостенения, продвигающаяся к концу кости, становится лучше очерченной, в конечном итоге формируя пластинку роста, расположенную между диафизом и эпифизом трубчатой кости (). На концах трубчатых костей происходят те же морфологические изменения, ведущие к созданию увеличивающегося ядра окостенения, вторичного центра окостенения. Дальнейшее созревание приводит к постепенному превращению вторичного центра окостенения в кость, оставляя субхондральную костную пластинку на эпифизарной стороне у основания суставного хряща и физический рубец на метафизарной стороне пластинки.Хрящ, оставшийся на субхондральной поверхности, образует зрелый гиалиновый хрящ, который характеризует суставные поверхности.
Продольный гистологический срез развивающейся проксимальной части бедренной кости у плода в третьем триместре, иллюстрирующий от верхнего до нижнего хрящевого эпифиза с развивающимся центром вторичного окостенения головки бедренной кости (изогнутая стрелка), всей пластиной роста (прямая стрелка) и метафизом и проксимальный диафиз, содержащий первичный центр окостенения (окраска гематоксилин-эозином, малое увеличение. )
)
Моделирование и ремоделирование
Как внутримембранозные, так и эндохондральные окостенения определяют продольный и радиальный рост и созревание скелета в детстве и подростковом возрасте. Два различных процесса необходимы для последовательных модификаций развития, которые имеют место в общей форме, размере и прочности кости: моделирование скелета и ремоделирование скелета.
Есть несколько типов костных клеток, которые различаются по происхождению и функциям, но взаимодействуют друг с другом или сигнализируют друг другу, чтобы контролировать и координировать процессы моделирования и ремоделирования.Функция одного из типов клеток, остеокласта, уникальна, поскольку его задача состоит в разрушении самой ткани, которая его содержит (3). Остеокласты происходят из одноядерных клеток-предшественников моноцитарно-макрофагальной линии (4). Два цитокина, активатор рецептора ядерного фактора, лиганда каппа-B, или RANKL, и фактор, стимулирующий колонии макрофагов, важны для образования остеокластов, а также для выживания и организации остеокластов (4,5). Остеокласты ответственны за подкисление резорбционного отсека, растворение минерального компонента костного матрикса и переваривание белкового матрикса (4,6).
Остеокласты ответственны за подкисление резорбционного отсека, растворение минерального компонента костного матрикса и переваривание белкового матрикса (4,6).
Резорбция кости, индуцированная остеокластами, стимулирует высвобождение факторов роста, которые приводят к привлечению клеток-предшественников остеопрогениторов, полученных из плюрипотентных мезенхимальных стволовых клеток, которые дифференцируются в остеобласты. Остеобласты синтезируют новый костный матрикс, секретируя коллаген 1 типа и другие матричные белки (4). Остеобласты обнаруживаются в изобилии по всей растущей или реконструирующейся кости, тогда как в покоящейся взрослой кости остеобласты концентрируются на эндостальной кортикальной поверхности и в эндостальной ткани, выстилающей гаверсовы каналы (1).
Остеоциты — это долгоживущие, терминально дифференцированные, непролиферативные клетки линии остеобластов, которые составляют основной тип клеток зрелой кости (7). Они заключены в остеоидном материале в небольших лакунарных пространствах, связанных между собой многочисленными дендритными цитоплазматическими процессами, и они не секретируют напрямую матрикс или резорбцию кости (7,8). Остеоциты взаимодействуют с остеобластами, высвобождая молекулы, которые подавляют функцию остеобластов и образование костей (9). Их секреция других веществ влияет на набор и функцию остеокластов, сигнализируя остеокластам о необходимости замены поврежденной кости (10,11).Благодаря этим взаимодействиям с остеобластами и остеокластами, когда кость повреждена, остеоциты передают сигналы, которые направляют соответствующую клеточную реакцию.
Остеоциты взаимодействуют с остеобластами, высвобождая молекулы, которые подавляют функцию остеобластов и образование костей (9). Их секреция других веществ влияет на набор и функцию остеокластов, сигнализируя остеокластам о необходимости замены поврежденной кости (10,11).Благодаря этим взаимодействиям с остеобластами и остеокластами, когда кость повреждена, остеоциты передают сигналы, которые направляют соответствующую клеточную реакцию.
Моделирование скелета приводит к изменениям общей формы и размера кости в ответ на физиологические воздействия и механические силы, которые действуют на нее (4,12). Это несвязанный процесс в том смысле, что образование кости и резорбция кости не взаимозависимы тесно, часто происходя в разных, а иногда и на удаленных участках скелета.Скорее, кости расширяются или сужаются, меняют оси и развиваются искривления из-за независимого действия остеобластов и остеокластов, как правило, во время роста скелета в детстве. Механические и молекулярные механизмы, объясняющие этот важный процесс, понятны лишь частично. Соответствующие роли играют системные регуляторы, особенно гормоны, на которые влияют возраст и половая зрелость (12). Процесс моделирования скелета обычно менее частый, чем процесс ремоделирования скелета у взрослых (13–15).
Соответствующие роли играют системные регуляторы, особенно гормоны, на которые влияют возраст и половая зрелость (12). Процесс моделирования скелета обычно менее частый, чем процесс ремоделирования скелета у взрослых (13–15).
При ремоделировании скелета сопряженная резорбция кости и формирование кости происходят в одном и том же участке скелета и хронологически и количественно сбалансированы (12). Этот процесс начинается до рождения и продолжается до смерти и включает в себя непрерывное удаление участков старой кости с заменой синтезированным белковым матриксом и последующей минерализацией этого матрикса с образованием новой кости (4). Юлиус Вольф, немецкий хирург и анатом, живший почти полностью в 19 веке, признал, что кость динамически реконструируется как по количеству, так и по архитектуре, чтобы функционально адаптироваться к изменениям нагрузки (16).Хотя точный перевод закона Вольфа найти трудно, он основан на концепции, согласно которой силы или механические сигналы, возникающие во время нагрузки, преобразуются в биохимические стимулы на клеточном уровне, которые влияют на ремоделирование кости (17,18).
Ремоделирование происходит в ответ на повышенную нагрузку и микроскопическое повреждение кортикальных остеонов или губчатых трабекул (19). Остеоциты являются неотъемлемой частью обнаружения повреждений и инициации цикла ремоделирования, но для успешного ремоделирования требуется скоординированная и синхронизированная деятельность множества клеточных участников, включая остеокласты, остеобласты, макрофаги, а также различные иммунные и гематопоэтические клетки (20).Совокупность таких клеток объединяется, чтобы сформировать микроскопическую временную блуждающую сборку, называемую базовой многоклеточной единицей, которая нацелена на дискретную область для ремонта (20,21). Основная многоклеточная единица устроена с остеокластами, ведущими к хвосту остеобластов, образуя цилиндрический туннель, известный как режущий конус внутри кортикальной кости или выемка, напоминающая канавку вдоль губчатой поверхности в губчатой кости (22). Стадии ремоделирования включают покой, активацию, резорбцию, обращение, формирование кости и прекращение (20) ().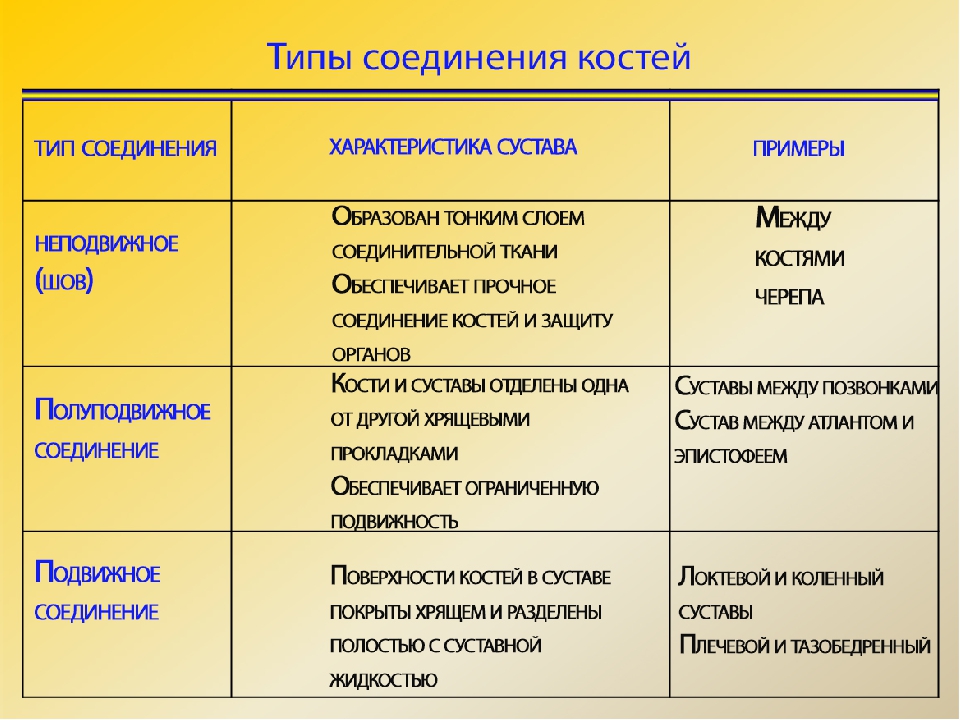 Нормальное ремоделирование прогрессирует медленно, полный цикл занимает несколько недель или месяцев.
Нормальное ремоделирование прогрессирует медленно, полный цикл занимает несколько недель или месяцев.
Последовательные фазы нормального цикла ремоделирования кости.
Основная многоклеточная единица может подавляться такими факторами, как пожилой возраст, хронические заболевания, лекарства, метаболическая или эндокринная дисфункция (23). Признанным последствием лекарственного подавления основных многоклеточных единиц является развитие атипичных переломов боковой коры бедренной кости в результате длительного лечения бисфосфоната алендронатом, мощным ингибитором метаболизма костной ткани (24) ().Бисфосфонаты ингибируют резорбцию кости за счет подавления остеокластов и индукции апоптоза остеокластов, нарушая цикл ремоделирования кости. Гистологически поверхность кости у пациентов с атипичными переломами бедренной кости лишена клеточных элементов и демонстрирует нарушение формирования матрикса, подобно адинамической кости, имеющейся у пациентов с хронической почечной недостаточностью (23).
Переднезадняя рентгенограмма проксимального отдела бедренной кости у 78-летней женщины демонстрирует перелом боковой коры проксимального отдела бедренной кости (стрелка), связанный с длительным применением бисфосфонатов.Обратите внимание на типичную поперечную ориентацию и надкостницу, связанную с этими переломами.
Костная анатомия
Макроскопическая анатомия
Состав костного матрикса можно разделить на два типа организации: тканая кость и пластинчатая кость. Тканая кость, состоящая из нерегулярного расположения коллагеновых волокон, которые различаются по диаметру и не ориентированы на напряжение в своем направлении, заметна только у плода и в ситуациях, требующих быстрого обновления костной ткани, например, во время фазы заживления переломов и при таких расстройствах, как гиперпаратиреоз и болезнь Педжета.Большая часть скелета у взрослых состоит из пластинчатой кости, которая более организована, прочна и менее гибка, чем тканая кость, с ориентацией коллагена, которая связана со стрессом.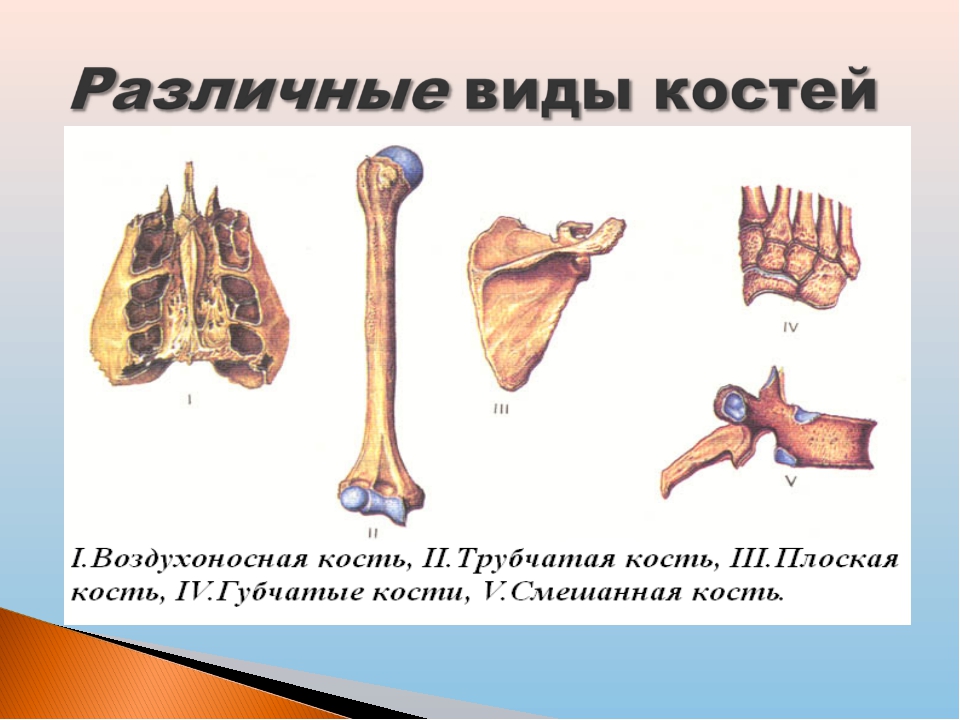 Пластинчатая архитектура обнаруживается как в кортикальной, так и в губчатой кости, хотя точное расположение ламелей варьируется между двумя (1).
Пластинчатая архитектура обнаруживается как в кортикальной, так и в губчатой кости, хотя точное расположение ламелей варьируется между двумя (1).
Скелет состоит как из плотной компактной кости, особенно на ее поверхности, известной как кортикальная кость, так и из сотового каркаса из пластин и стоек кости с промежуточными промежутками, известными как губчатая или губчатая кость.У взрослых кортикальная кость обычно составляет 80% от общей костной массы, хотя точная пропорция варьируется от одного человека к другому и от одного анатомического участка к другому. В длинных трубчатых костях периферическая оболочка кортикальной кости относительно толстая и включает центральную мозговую полость, состоящую из редких трабекул. Межтрабекулярные пространства содержат смесь кроветворного и жирового костного мозга, состав которой варьируется в зависимости от возраста и пола человека, точного расположения скелета и требований кроветворения, предъявляемых к скелету ().
(a) Корональный анатомический разрез и (b) соответствующая рентгенограмма проксимального отдела плечевой кости иллюстрируют жировой костный мозг, заполняющий пространства губчатой кости, расположенные в субхондральной и медуллярной областях. Обратите внимание на тонкую субхондральную костную пластину на головке плечевой кости (наконечники стрелок) и плотную кортикальную кость, образующую стержень плечевой кости (стрелка).
Обратите внимание на тонкую субхондральную костную пластину на головке плечевой кости (наконечники стрелок) и плотную кортикальную кость, образующую стержень плечевой кости (стрелка).
(a) Корональный анатомический разрез и (b) соответствующая рентгенограмма проксимального отдела плечевой кости иллюстрируют жировой костный мозг, заполняющий пространства губчатой кости, расположенные в субхондральной и медуллярной областях.Обратите внимание на тонкую субхондральную костную пластину на головке плечевой кости (наконечники стрелок) и плотную кортикальную кость, образующую стержень плечевой кости (стрелка).
К поверхности многих костей прикрепляются сухожилия и связки, а также капсульная ткань, связанная с близлежащими суставами, в местах, известных как энтезы (25). Было высказано предположение, что шероховатые отметины на поверхности кости в местах прикрепления сухожилий указывают на то, что окостенение распространилось от кости до концевых коллагеновых волокон сухожилия под влиянием силы и направления натяжения соответствующих мышц (1). Связки прикрепляются непосредственно к кортикальной поверхности или надкостнице через волокна, которые ориентированы либо перпендикулярно, либо наклонно к коре головного мозга. Анатомическая связь между мышцей и костью, которая влияет на растягивающие напряжения, прикладываемые к этой кости, связана не с прямым кортикальным проникновением мышечных волокон, а через соединительную ткань, которая инкапсулирует и пронизывает эти мышцы (1).
Связки прикрепляются непосредственно к кортикальной поверхности или надкостнице через волокна, которые ориентированы либо перпендикулярно, либо наклонно к коре головного мозга. Анатомическая связь между мышцей и костью, которая влияет на растягивающие напряжения, прикладываемые к этой кости, связана не с прямым кортикальным проникновением мышечных волокон, а через соединительную ткань, которая инкапсулирует и пронизывает эти мышцы (1).
Микроскопическая анатомия
Минерализованный внеклеточный компонент кости называется матрицей, которая частично состоит из бесчисленных коллагеновых волокон, встроенных в основное вещество.Коллагеновые волокна синтезируются остеобластами, тесно связаны с минеральным компонентом и обеспечивают структурную устойчивость к биомеханическим силам, что способствует удивительной прочности кости. Именно сила этих коллагеновых волокон в большей степени, чем любая другая составляющая, увеличивает количество энергии, которое должно быть поглощено, прежде чем кость сломается. Размер и ориентация фибрилл коллагена влияют на вероятность появления микроскопических трещин, когда кость подвергается напряжению, и на последующую величину и направление таких трещин по мере их распространения.Молекулы трехспирального коллагена в кости (чаще всего коллаген I типа) агрегированы вместе бесчисленными поперечными связями. Разрушение или расщепление этих поперечных связей при старении, травме или заболевании снижает общую прочность кости (26,27).
Размер и ориентация фибрилл коллагена влияют на вероятность появления микроскопических трещин, когда кость подвергается напряжению, и на последующую величину и направление таких трещин по мере их распространения.Молекулы трехспирального коллагена в кости (чаще всего коллаген I типа) агрегированы вместе бесчисленными поперечными связями. Разрушение или расщепление этих поперечных связей при старении, травме или заболевании снижает общую прочность кости (26,27).
Костные минералы также являются компонентом матрицы. Основным минеральным компонентом является гидроксиапатит с небольшим содержанием карбоната, магния и других минералов. Эти минералы способствуют прочности, жесткости и твердости кости и объясняют ее непрозрачность при рентгенографии.Средняя степень минерализации кости неодинакова в разных областях скелета, хотя она одинакова в губчатой и кортикальной костях, у мужчин и женщин и в разном возрасте (28). При расстройствах, характеризующихся повышенным уровнем и скоростью ремоделирования кости, остается меньше времени для завершения минерализации, что приводит к более низкой средней степени минерализации кости (27). И наоборот, более высокая средняя степень минерализации кости указывает на снижение скорости обновления костной ткани. Чрезмерная минерализация кости не укрепляет кость; хотя кость становится жестче, она также становится более хрупкой, что снижает энергию, необходимую для перелома (29,30).Проблема влияния минерализации на общую прочность кости усложняет дополнительное влияние размера кристаллов. Кости с более крупными кристаллами, такие как остеопоротические кости, более склонны к разрушению из-за их повышенной хрупкости (27,31).
И наоборот, более высокая средняя степень минерализации кости указывает на снижение скорости обновления костной ткани. Чрезмерная минерализация кости не укрепляет кость; хотя кость становится жестче, она также становится более хрупкой, что снижает энергию, необходимую для перелома (29,30).Проблема влияния минерализации на общую прочность кости усложняет дополнительное влияние размера кристаллов. Кости с более крупными кристаллами, такие как остеопоротические кости, более склонны к разрушению из-за их повышенной хрупкости (27,31).
Анатомия суставного хряща
Гиалиновый суставной хрящ — это узкоспециализированная соединительная ткань, которая покрывает поверхности тех костей, которые составляют диатродиальный сустав. Эта ткань бывает гипоцеллюлярной, аневральной, лимфатической и бессосудистой.Он состоит из небольшого количества клеток (хондроцитов), расположенных во внеклеточном матриксе, состоящем из воды и макромолекул, которые включают протеогликан, коллаген и неколлагеновые белки.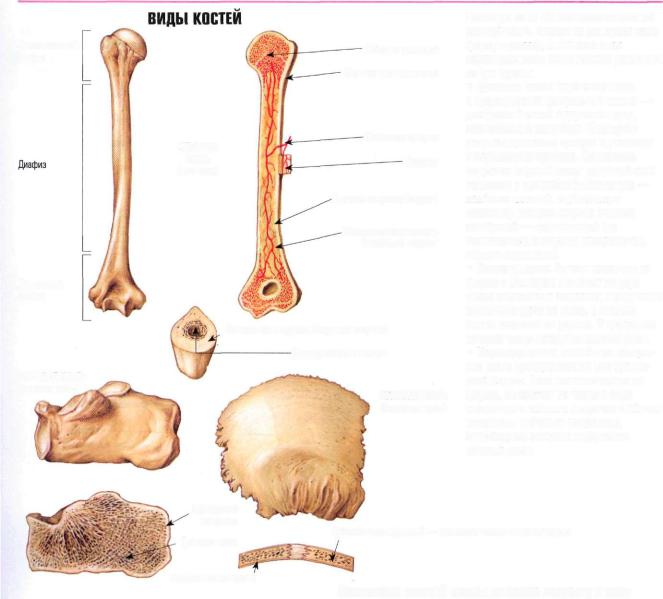 Хондроциты различаются по количеству, размеру и форме в зависимости от их местоположения или зоны (от глубокой до поверхностной), и они несут ответственность за производство, организацию и поддержание внеклеточного матрикса (32). Сложное взаимодействие между хондроцитами и внеклеточным матриксом поддерживает структурную целостность и придает биомеханические свойства этой ткани, включая прочность на разрыв и эластичность, которые облегчают ее способность поглощать и распределять нагрузку.Структура и функция становятся частью петли обратной связи с биосинтезом хондроцитов, управляемым, по крайней мере частично, стрессом и деформацией клетки (33,34).
Хондроциты различаются по количеству, размеру и форме в зависимости от их местоположения или зоны (от глубокой до поверхностной), и они несут ответственность за производство, организацию и поддержание внеклеточного матрикса (32). Сложное взаимодействие между хондроцитами и внеклеточным матриксом поддерживает структурную целостность и придает биомеханические свойства этой ткани, включая прочность на разрыв и эластичность, которые облегчают ее способность поглощать и распределять нагрузку.Структура и функция становятся частью петли обратной связи с биосинтезом хондроцитов, управляемым, по крайней мере частично, стрессом и деформацией клетки (33,34).
Суставной хрящ имеет зональную конфигурацию, состоящую из четырех основных горизонтальных слоев, которые различаются по клеточному профилю (размер, форма, метаболическая активность, плотность), концентрации протеогликана и организации коллагена. Их называют поверхностным, переходным, глубоким и кальцинированным слоями (). Поверхностный слой является самым тонким и состоит из уплощенных хондроцитов, протеогликана (низкая концентрация), коллагена (два плотно упакованных слоя с тонким диаметром) и воды (в самой высокой концентрации любого из слоев) (35). Переходная зона (промежуточная или средняя) характеризуется круглыми хондроцитами, случайной организацией коллагена и повышенной концентрацией протеогликана. Глубокая или радиальная зона имеет самый низкий объем клеток с столбчатой организацией хондроцитов. Здесь коллагеновые волокна ориентированы перпендикулярно субхондральной кости, концентрация протеогликана высокая, а концентрация воды низкая. Отметка прилива, полоса фибрилл, служащих якорем для коллагена, отделяет глубокий слой хряща от кальцинированного слоя.Зона обызвествления характеризуется наличием круглых хондроцитов и отсутствием протеогликанов. Это переход и точка соединения между поверхностным хрящом и субхондральной костью (32) ().
Переходная зона (промежуточная или средняя) характеризуется круглыми хондроцитами, случайной организацией коллагена и повышенной концентрацией протеогликана. Глубокая или радиальная зона имеет самый низкий объем клеток с столбчатой организацией хондроцитов. Здесь коллагеновые волокна ориентированы перпендикулярно субхондральной кости, концентрация протеогликана высокая, а концентрация воды низкая. Отметка прилива, полоса фибрилл, служащих якорем для коллагена, отделяет глубокий слой хряща от кальцинированного слоя.Зона обызвествления характеризуется наличием круглых хондроцитов и отсутствием протеогликанов. Это переход и точка соединения между поверхностным хрящом и субхондральной костью (32) ().
Микрофотография нормального суставного хряща ребенка иллюстрирует зональную организацию хряща и соединение хряща с субхондральной костной пластиной. Показаны приблизительные границы между тонким поверхностным слоем и переходным слоем (изогнутые стрелки), а также между переходным и более глубоким радиальными слоями (стрелки). Обратите внимание на кальцинированный хрящ (стрелка) на стыке хряща и субхондральной костной пластинки, который еще не полностью окостенел в этом образце. (Окраска гематоксилин-эозином, среднее увеличение.)
Обратите внимание на кальцинированный хрящ (стрелка) на стыке хряща и субхондральной костной пластинки, который еще не полностью окостенел в этом образце. (Окраска гематоксилин-эозином, среднее увеличение.)
Сагиттальное ультракороткое время эхо-сигнала (время повторения мсек / время эхо-сигнала мсек, 500 / 0,008) магнитно-резонансное (МР) изображение колена демаскирует короткую ткань Т2 (1 мс Т2 * ) нормально выглядящего кальцинированного слоя бедренного (изогнутая стрелка) и большеберцового (белая стрелка) хряща, а также показаны области бедренного (острие стрелки) и большеберцового (черная стрелка) кальцинированного хряща, представляющего дегенерацию.
Напряжения, силы и виды структурного разрушения
Биомеханические свойства любого вещества можно описать соотношением между его способностью воспринимать нагрузку (напряжение) и его способностью деформироваться (деформироваться) при приложении к нему силы. Нагрузка относится к сумме всех сил, действующих на вещество, тогда как деформация относится к любому изменению формы, которое происходит в этом веществе при приложении силы.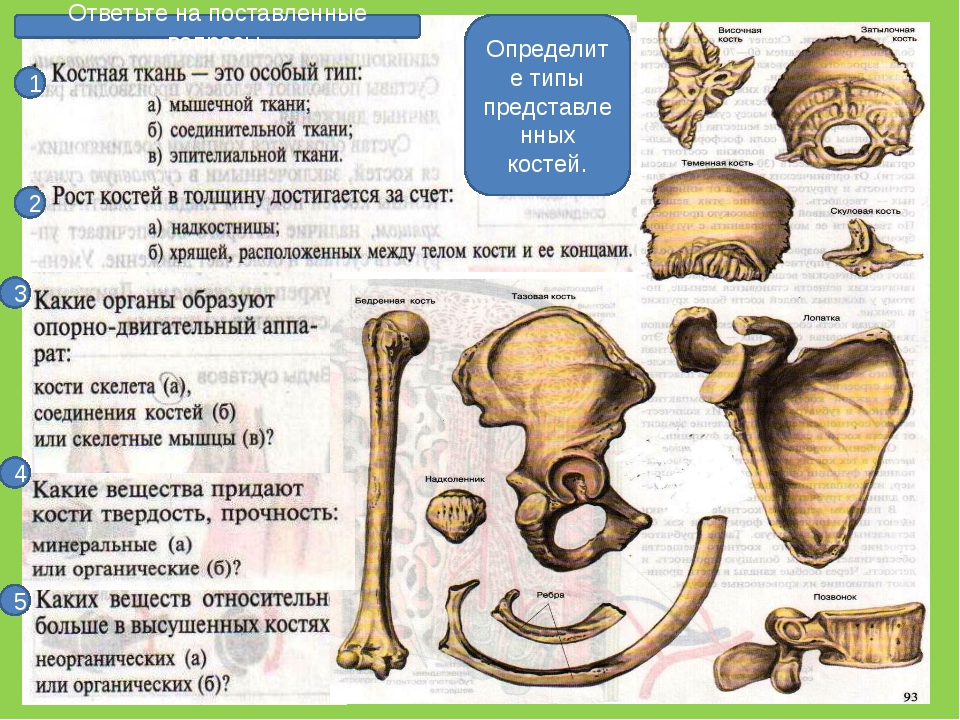 Эта взаимосвязь изображается графически в виде кривой напряжение-деформация (нагрузка-деформация) (), которая показывает реакцию однородного материала на внешнюю силу, иллюстрируя его жесткость (модуль упругости), а также его точки текучести и разрушения (36– 38).Материалы, которые могут выдерживать высокие нагрузки, но не могут деформироваться, например стекло, считаются хрупкими, а вещества, которые значительно деформируются до разрушения, считаются пластичными. Кости и хрящи ведут себя промежуточно: они способны выдерживать умеренную нагрузку, а также демонстрируют способность выдерживать умеренную нагрузку до отказа. Любая отдельная кривая нагрузка-деформация неадекватна для описания неоднородной ткани скелета человека, поскольку существуют значительные различия в структуре, составе и геометрии в различных анатомических областях.Сама кость состоит из двух совершенно разных тканевых фракций, при этом губчатая губчатая кость и кортикальная кость ведут себя по-разному при приложении силы.
Эта взаимосвязь изображается графически в виде кривой напряжение-деформация (нагрузка-деформация) (), которая показывает реакцию однородного материала на внешнюю силу, иллюстрируя его жесткость (модуль упругости), а также его точки текучести и разрушения (36– 38).Материалы, которые могут выдерживать высокие нагрузки, но не могут деформироваться, например стекло, считаются хрупкими, а вещества, которые значительно деформируются до разрушения, считаются пластичными. Кости и хрящи ведут себя промежуточно: они способны выдерживать умеренную нагрузку, а также демонстрируют способность выдерживать умеренную нагрузку до отказа. Любая отдельная кривая нагрузка-деформация неадекватна для описания неоднородной ткани скелета человека, поскольку существуют значительные различия в структуре, составе и геометрии в различных анатомических областях.Сама кость состоит из двух совершенно разных тканевых фракций, при этом губчатая губчатая кость и кортикальная кость ведут себя по-разному при приложении силы. Каркас также проявляет анизотропию, по-разному реагируя на напряжения в зависимости от направления нагрузки (37,38). Механические свойства кости также меняются с возрастом, так как кость у ребенка более податлива, чем кость взрослого, а хрящевая пластинка незрелой кости особенно уязвима для травм.
Каркас также проявляет анизотропию, по-разному реагируя на напряжения в зависимости от направления нагрузки (37,38). Механические свойства кости также меняются с возрастом, так как кость у ребенка более податлива, чем кость взрослого, а хрящевая пластинка незрелой кости особенно уязвима для травм.
Кривая напряжения-деформации для любого материала иллюстрирует взаимосвязь между величиной нагрузки, которую он может воспринимать, и деформацией, которую он может выдерживать до достижения предела текучести и, в конечном итоге, до точки разрушения.Наклон кривой (ε) определяется как модуль упругости для этого материала.
Структурная нагрузка может быть одноосной, при которой сила прилагается к веществу только в одном направлении, или может быть многоосной, при которой сила более сложна с геометрической точки зрения, при этом напряжение, прикладываемое к веществу в двух или более направлениях (38 ) (). Сжимающие, растягивающие и поперечные силы являются формами одноосной нагрузки. Проще говоря, сжимающие напряжения развиваются, когда прилагаемые силы действуют для уменьшения длины материала по оси приложенной нагрузки, а растягивающие напряжения развиваются, когда прилагаемые силы действуют для удлинения материала вдоль оси приложенной нагрузки.Напряжения сдвига действуют для отделения одного слоя материала от соседнего в одной плоскости. Изгиб — это режим разрушения, характерный для длинной тонкой колонны, когда сжимающие силы прикладываются к длинным концам, что приводит к боковому прогибу конструкции. Величина силы, приводящей к короблению, меньше максимальной сжимающей силы, которую может выдержать материал, и математически описывается законом Эйлера (39).
Проще говоря, сжимающие напряжения развиваются, когда прилагаемые силы действуют для уменьшения длины материала по оси приложенной нагрузки, а растягивающие напряжения развиваются, когда прилагаемые силы действуют для удлинения материала вдоль оси приложенной нагрузки.Напряжения сдвига действуют для отделения одного слоя материала от соседнего в одной плоскости. Изгиб — это режим разрушения, характерный для длинной тонкой колонны, когда сжимающие силы прикладываются к длинным концам, что приводит к боковому прогибу конструкции. Величина силы, приводящей к короблению, меньше максимальной сжимающей силы, которую может выдержать материал, и математически описывается законом Эйлера (39).
Показаны основные механизмы повреждения костей и хрящей.Сжатие, растяжение и сдвиг являются одноосными механизмами, в то время как изгиб, вращение и внеосевой сдвиг являются более сложными, когда сила прилагается в двух или более плоскостях.
Многоосное нагружение вещества происходит, когда сила действует в двух или более плоскостях одновременно. Типичные примеры многоосного нагружения включают изгиб и кручение (вращение). Изгибание приводит к тому, что одна сторона вещества испытывает сжатие, а другая сторона вещества испытывает растяжение, что приводит к отклонению, провисанию или боковому перемещению материала.Кручение возникает, когда один конец вещества вращается в одном направлении, а другой конец остается неподвижным или вращается в противоположном направлении, что приводит к скручиванию материала, что приводит к внутренним напряжениям сдвига в материале. Признаны более сложные формы применения силы, но они выходят за рамки данной статьи. Кроме того, может существовать комбинация нескольких различных типов стресса, применяемых одновременно, что усложняет анализ биомеханики скелета при нормальной нагрузке, перегрузке и травме (37,38).
Типичные примеры многоосного нагружения включают изгиб и кручение (вращение). Изгибание приводит к тому, что одна сторона вещества испытывает сжатие, а другая сторона вещества испытывает растяжение, что приводит к отклонению, провисанию или боковому перемещению материала.Кручение возникает, когда один конец вещества вращается в одном направлении, а другой конец остается неподвижным или вращается в противоположном направлении, что приводит к скручиванию материала, что приводит к внутренним напряжениям сдвига в материале. Признаны более сложные формы применения силы, но они выходят за рамки данной статьи. Кроме того, может существовать комбинация нескольких различных типов стресса, применяемых одновременно, что усложняет анализ биомеханики скелета при нормальной нагрузке, перегрузке и травме (37,38).
Хондральная и костно-хрящевая травма
Биомеханическое поведение суставного хряща определяется взаимодействием его преобладающих компонентов: коллагена, протеогликана и интерстициальной жидкости. Сети коллагеновых волокон вносят вклад в механику суставов напрямую, сопротивляясь растягивающим напряжениям, и косвенно, увеличивая давление поровой жидкости (40). В хрящевом матриксе объем, занимаемый агрегатом протеогликана, ограничен коллагеновой сетью. При сжатии отрицательно заряженные компоненты протеогликанов сдвигаются ближе друг к другу, увеличивая их силы отталкивания и увеличивая сжимающую жесткость хряща.Повреждение коллагеновой основы снижает жесткость ткани при сжатии, поскольку протеогликаны удерживаются менее эффективно. При хондральной деформации жидкость протекает через ткань и суставную поверхность, образуя тонкую пленку, которая смазывает эту поверхность и способствует эффективному движению суставов (41,42). Признание того, что поток жидкости и деформация ткани взаимозависимы, подчеркивает концепцию, согласно которой хрящ можно рассматривать как двухфазную смесь жидких и твердых компонентов, свойства материала которой включают жесткость и проницаемость (41).
Сети коллагеновых волокон вносят вклад в механику суставов напрямую, сопротивляясь растягивающим напряжениям, и косвенно, увеличивая давление поровой жидкости (40). В хрящевом матриксе объем, занимаемый агрегатом протеогликана, ограничен коллагеновой сетью. При сжатии отрицательно заряженные компоненты протеогликанов сдвигаются ближе друг к другу, увеличивая их силы отталкивания и увеличивая сжимающую жесткость хряща.Повреждение коллагеновой основы снижает жесткость ткани при сжатии, поскольку протеогликаны удерживаются менее эффективно. При хондральной деформации жидкость протекает через ткань и суставную поверхность, образуя тонкую пленку, которая смазывает эту поверхность и способствует эффективному движению суставов (41,42). Признание того, что поток жидкости и деформация ткани взаимозависимы, подчеркивает концепцию, согласно которой хрящ можно рассматривать как двухфазную смесь жидких и твердых компонентов, свойства материала которой включают жесткость и проницаемость (41).
Часто встречаются хрящевые и костно-хрящевые травмы, особенно в нижних конечностях из-за единичной чрезмерной ударной силы или повторяющихся подпороговых нагрузок. Результирующее структурное изменение включает три типа повреждения хряща: повреждение хряща без видимого разрушения ткани (хрящ в группе риска), разрушение только суставного хряща и разрушение суставного хряща и субхондральной кости вместе (повреждение костно-хрящевой ткани). Точная роль травмы в развитии остеоартроза, обнаруженная более чем в 60% артроскопий коленного сустава у взрослых, неясна (43–45).
Результирующее структурное изменение включает три типа повреждения хряща: повреждение хряща без видимого разрушения ткани (хрящ в группе риска), разрушение только суставного хряща и разрушение суставного хряща и субхондральной кости вместе (повреждение костно-хрящевой ткани). Точная роль травмы в развитии остеоартроза, обнаруженная более чем в 60% артроскопий коленного сустава у взрослых, неясна (43–45).
При острой травме травма связана с одним из трех типов силы: сжатием, сдвигом или растяжением (46,47). Сжимающие силы действуют перпендикулярно поверхности сустава, вызывая неравномерную деформацию суставного хряща. Пространственный профиль и величина деформации зависят от ряда переменных, включая величину и скорость нагрузки, геометрию сустава и механические свойства ткани (48). В пространственном отношении наибольшая деформация возникает в месте контакта поверхностно и уменьшается к глубокому слою (49).Скорость нагрузки также влияет на степень деформации хряща (50,51). При высокой скорости нагрузки относительно жесткий хрящ рассеивает энергию в своей поверхностной области, создавая поверхностные трещины (52,53) (). Более низкие уровни нагрузки приводят к передаче энергии в более глубокие слои ткани, вызывая очаговые потери хрящевой ткани. Компрессионная деформация до 30% может привести к гибели клеток, если скорость деформации достаточно высока (54,55). По мере увеличения силы воздействия снижается жизнеспособность хондроцитов и развиваются поражения хряща прогрессирующей тяжести (> 50%) (56–59).Следует отметить, что даже при отсутствии видимых структурных повреждений гибель клеток и повреждение матрикса может быть результатом сжатия, что приводит к сценарию «хрящ в зоне риска», который в конечном итоге приводит к повреждению ткани (60–64).
Более низкие уровни нагрузки приводят к передаче энергии в более глубокие слои ткани, вызывая очаговые потери хрящевой ткани. Компрессионная деформация до 30% может привести к гибели клеток, если скорость деформации достаточно высока (54,55). По мере увеличения силы воздействия снижается жизнеспособность хондроцитов и развиваются поражения хряща прогрессирующей тяжести (> 50%) (56–59).Следует отметить, что даже при отсутствии видимых структурных повреждений гибель клеток и повреждение матрикса может быть результатом сжатия, что приводит к сценарию «хрящ в зоне риска», который в конечном итоге приводит к повреждению ткани (60–64).
Сагиттальное средневзвешенное (2000/20) МРТ-изображение колена демонстрирует хрящевую щель на всю толщину (стрелка) в хряще надколенника.
Сдвиговые усилия прилагаются параллельно поверхности соединения. Скорость и энергия сдвигового усилия будут влиять на характер и степень разрушения хряща, что приводит к повреждениям хряща, которые различаются в зависимости от пораженной зоны хряща и наличия или отсутствия нарушения поверхности хряща (65). Чрезмерное усилие сдвига может вызвать разрывы поверхностного слоя хряща вдоль наклонно ориентированных волокон в переходной зоне или, при передаче на костно-хрящевое соединение, может отсоединить кальцинированный слой хряща от подлежащей костной пластинки (53) (). Силы растяжения обычно приводят к отрывным травмам, когда связки или сухожилия оказывают натяжение на свои костные места, а не повреждение хряща. Костно-хрящевые травмы затрагивают как хрящ, так и субхондральную кость и могут быть острыми, подострыми или хроническими, при этом более длительные аномалии обозначаются рассекающим остеохондритом (66).
Чрезмерное усилие сдвига может вызвать разрывы поверхностного слоя хряща вдоль наклонно ориентированных волокон в переходной зоне или, при передаче на костно-хрящевое соединение, может отсоединить кальцинированный слой хряща от подлежащей костной пластинки (53) (). Силы растяжения обычно приводят к отрывным травмам, когда связки или сухожилия оказывают натяжение на свои костные места, а не повреждение хряща. Костно-хрящевые травмы затрагивают как хрящ, так и субхондральную кость и могут быть острыми, подострыми или хроническими, при этом более длительные аномалии обозначаются рассекающим остеохондритом (66).
Сагиттальное Т2-взвешенное МР-изображение колена с подавлением жира (3200/65) показывает отделение бедренного суставного хряща от субхондральной кости (стрелка) без видимого распространения на поверхность суставного хряща. Эта аномалия представляет собой скрытое (не видимое при артроскопии) отслоение хряща от подлежащей кости.
При клинической оценке хрящевой и костно-хрящевой травм необходимо учитывать размер и глубину поражения, его расположение и любое связанное с этим поражение субхондральной кости. Распространенной системой клинической классификации, используемой для описания аномалии суставного хряща, является система Outerbridge (67), в которой повреждение суставного хряща варьируется между четырьмя степенями в зависимости от глубины хрящевой аномалии (68) (). Сообщается, что точность и воспроизводимость этой системы составляет от 22% до 100%, при этом поражения более низкой степени диагностируются с меньшей точностью, чем поражения более высокой степени (69). Совсем недавно получила признание Модифицированная система классификации хрящевых травм Международного общества по восстановлению хряща (70).Эта последняя система фокусируется на глубине поражения (от 0 до 4) и площади повреждения (от нормального до крайне ненормального). Международное общество восстановления хряща также разработало систему классификации костно-хрящевых повреждений, основанную на размере, глубине и стабильности аномалии (71).
Распространенной системой клинической классификации, используемой для описания аномалии суставного хряща, является система Outerbridge (67), в которой повреждение суставного хряща варьируется между четырьмя степенями в зависимости от глубины хрящевой аномалии (68) (). Сообщается, что точность и воспроизводимость этой системы составляет от 22% до 100%, при этом поражения более низкой степени диагностируются с меньшей точностью, чем поражения более высокой степени (69). Совсем недавно получила признание Модифицированная система классификации хрящевых травм Международного общества по восстановлению хряща (70).Эта последняя система фокусируется на глубине поражения (от 0 до 4) и площади повреждения (от нормального до крайне ненормального). Международное общество восстановления хряща также разработало систему классификации костно-хрящевых повреждений, основанную на размере, глубине и стабильности аномалии (71).
Сагиттальное Т2-взвешенное МРТ-изображение колена с подавлением жира (3200/65) демонстрирует очаговый хондральный дефект на всю толщину (стрелка) мыщелка бедренной кости, представляющий поражение внешнего моста 4 степени. Его узкая зона перехода с прилегающим хрящом свидетельствует о посттравматической этиологии.
Его узкая зона перехода с прилегающим хрящом свидетельствует о посттравматической этиологии.
Оценка и классификация хрящевых и костно-хрящевых повреждений с помощью МРТ не вызывает затруднений при наличии истинных морфологических изменений. В условиях острого повреждения более высокой степени изменение сигнала в суставном хряще хорошо заметно и часто связано с изменением интенсивности сигнала в прилегающем субхондральном костном мозге и смещением хряща (). Тем не менее, травма хряща низкой степени обычно сопровождается очень незначительными морфологическими изменениями.Традиционные системы оценки классически использовали измененный сигнал Т2 внутри хряща, чтобы сделать вывод о наличии повреждения инфраструктуры (72–74). Развитие методов количественной МРТ обеспечивает прямую оценку биохимии тканей в условиях травмы. Доступно несколько методов для оценки целостности гликозаминогликанов хряща, включая МРТ-визуализацию натрия, МРТ-визуализацию хряща с усилением гадолиния и визуализацию T1 ρ (75–78). Для оценки ориентации коллагена чаще всего используется количественное картирование Т2 (79) ().
Для оценки ориентации коллагена чаще всего используется количественное картирование Т2 (79) ().
Осевое средневзвешенное изображение коленного сустава с подавлением жира (2400/24) показывает костно-хрящевую травму (черная стрелка) на срединном гребне надколенника с сопутствующим отеком костного мозга. Фрагмент выпадения (белая стрелка) с линейной низкой интенсивностью сигнала на его краю представляет собой часть прикрепленной субхондральной костной пластинки.
Сагиттальное средневзвешенное (1800/20) МРТ-изображение пациента после разрыва передней крестообразной связки с наложенной цветной картой Т2 на латеральный бедренный суставной хрящ показывает очаговое повышение значения Т2 хряща борозды надколенника в области ушиба костного мозга .Хотя потери хрящевой ткани не отмечается, измененные значения Т2 представляют собой изменение коллагеновой инфраструктуры ткани.
Субхондральная кость
Анатомические и биомеханические аспекты
Сразу под кальцинированной зоной суставного хряща находится слой компактной кости, обозначенный как субхондральная костная пластинка, которая служит для разделения суставного хряща и субхондральных трабекул. Толщина субхондральной костной пластинки варьируется как внутри, так и между костями (80).Его форма обычно повторяет форму суставной поверхности конкретной кости, частью которой он является, и представляет собой важный компонент опорной системы, которая реагирует и сопротивляется силам, приложенным к суставной поверхности, силам, которые изменяются по мере движения сустава. (81,82). Эти напряжения внутри субхондральной костной пластинки частично передаются трабекулам, которые лежат под ней. Действительно, некоторые исследователи сообщили, что субхондральная костная пластинка и прилегающие трабекулы поглощают большую часть механических сил, передаваемых через сустав (81).
Толщина субхондральной костной пластинки варьируется как внутри, так и между костями (80).Его форма обычно повторяет форму суставной поверхности конкретной кости, частью которой он является, и представляет собой важный компонент опорной системы, которая реагирует и сопротивляется силам, приложенным к суставной поверхности, силам, которые изменяются по мере движения сустава. (81,82). Эти напряжения внутри субхондральной костной пластинки частично передаются трабекулам, которые лежат под ней. Действительно, некоторые исследователи сообщили, что субхондральная костная пластинка и прилегающие трабекулы поглощают большую часть механических сил, передаваемых через сустав (81).
Нормальная архитектура трабекул варьируется от одного анатомического участка к другому и состоит из групп линейных или дугообразных трабекул, которые в большинстве участков утолщены и ориентированы вдоль осей основных сжимающих и растягивающих напряжений внутри этой кости (83 ). Многие трабекулы в часто сдавленных областях сустава ориентированы почти под прямым углом к субхондральной костной пластинке, простираясь вниз в материнскую кость на различные расстояния. В другом месте трабекулы ориентированы наклонно.Пересекающиеся трабекулы пересекают эти вертикальные и наклонные трабекулы, в основном, ортогонально (84–87) (). Камеры образуются в субхондральной губчатой кости, состоящей из центральных областей, содержащих области костного мозга, и периферических стенок, состоящих из этих трабекул. Размер и форма этих камер варьируются от одной кости к другой и в разных областях одной кости.
В другом месте трабекулы ориентированы наклонно.Пересекающиеся трабекулы пересекают эти вертикальные и наклонные трабекулы, в основном, ортогонально (84–87) (). Камеры образуются в субхондральной губчатой кости, состоящей из центральных областей, содержащих области костного мозга, и периферических стенок, состоящих из этих трабекул. Размер и форма этих камер варьируются от одной кости к другой и в разных областях одной кости.
Графическое изображение трабекулярной организации иллюстрирует более толстые продольные трабекулы, соединенные поперечными трабекулами под разными углами.(Изменено с разрешения Marion Karl, Lure Animations, Reno, Nev.)
Наиболее изученными трабекулами в человеческом теле являются те, которые расположены в головке и шее бедренной кости, где выделяются пять основных групп трабекул: основные группы трабекул: основные сжимающие, основные группы растяжения, вторичного сжатия, вторичного растяжения и большие вертельные группы (88–90) (). Индекс Сингха, исторически используемый для оценки наличия и степени остеопороза, был основан на морфологии этих трабекулярных групп (91). К сожалению, проксимальный отдел бедренной кости представляет собой особенно сложную область из-за количества и сложности трабекулярных групп и их сложных взаимоотношений с корой и калькаром. По крайней мере, некоторые из трабекулярных пересечений в головке и шейке бедренной кости не ортогональны, и ориентация трабекул не обязательно соответствует направлениям основных направлений напряжения любого одного условия нагрузки (88,92,93).
К сожалению, проксимальный отдел бедренной кости представляет собой особенно сложную область из-за количества и сложности трабекулярных групп и их сложных взаимоотношений с корой и калькаром. По крайней мере, некоторые из трабекулярных пересечений в головке и шейке бедренной кости не ортогональны, и ориентация трабекул не обязательно соответствует направлениям основных направлений напряжения любого одного условия нагрузки (88,92,93).
Коронарное МРТ-изображение проксимального отдела бедренной кости с высоким разрешением толщиной 0,9 мм, полученное с помощью трехмерной последовательности спин-эхо, демонстрирует трабекулярный паттерн проксимального отдела бедренной кости.(Любезно предоставлено Thomas Link, MD, UCSF, Сан-Франциско, Калифорния)
Субхондральный ушиб (ушиб кости)
С развитием МРТ было обнаружено, что изменения сигнала костного мозга могут быть результатом травмы даже при отсутствии видимый перелом, явление, обозначенное как ушиб кости или ушиб кости (94). Распределение ушибов костей варьируется в зависимости от механизма повреждения, причем некоторые распределения характерны для повреждения конкретной связки, например передней крестообразной (95) ().Сжимающие силы, прикладываемые к суставной поверхности, передаются через хрящ субхондральным трабекулам, которые разрушаются и развивают микротрещины, поскольку они выгибаются под нагрузкой. Концептуально, сопровождая этот процесс или действуя независимо, кровоизлияние и отек внутри трабекулярных камер могут «оказывать давление» на костный мозг, тем самым увеличивая растягивающее напряжение на стенках этой камеры. Этот отклик аналогичен сжатой автомобильной шине, в которой нагрузка, приложенная к ее верхней и нижней части, сжимает воздух внутри, что, в свою очередь, создает большее растягивающее напряжение на ее боковых стенках.Подобные механизмы использовались для объяснения появления увеличивающихся кист субхондральной кости, особенно при остеоартрозе (96).
Распределение ушибов костей варьируется в зависимости от механизма повреждения, причем некоторые распределения характерны для повреждения конкретной связки, например передней крестообразной (95) ().Сжимающие силы, прикладываемые к суставной поверхности, передаются через хрящ субхондральным трабекулам, которые разрушаются и развивают микротрещины, поскольку они выгибаются под нагрузкой. Концептуально, сопровождая этот процесс или действуя независимо, кровоизлияние и отек внутри трабекулярных камер могут «оказывать давление» на костный мозг, тем самым увеличивая растягивающее напряжение на стенках этой камеры. Этот отклик аналогичен сжатой автомобильной шине, в которой нагрузка, приложенная к ее верхней и нижней части, сжимает воздух внутри, что, в свою очередь, создает большее растягивающее напряжение на ее боковых стенках.Подобные механизмы использовались для объяснения появления увеличивающихся кист субхондральной кости, особенно при остеоартрозе (96).
Сагиттальное средневзвешенное МРТ-изображение колена с подавленным жиром (2400/26) у женщины с острым разрывом передней крестообразной связки показывает отек костного мозга в дистальном отделе бедренной кости и проксимальном отделе большеберцовой кости (стрелки).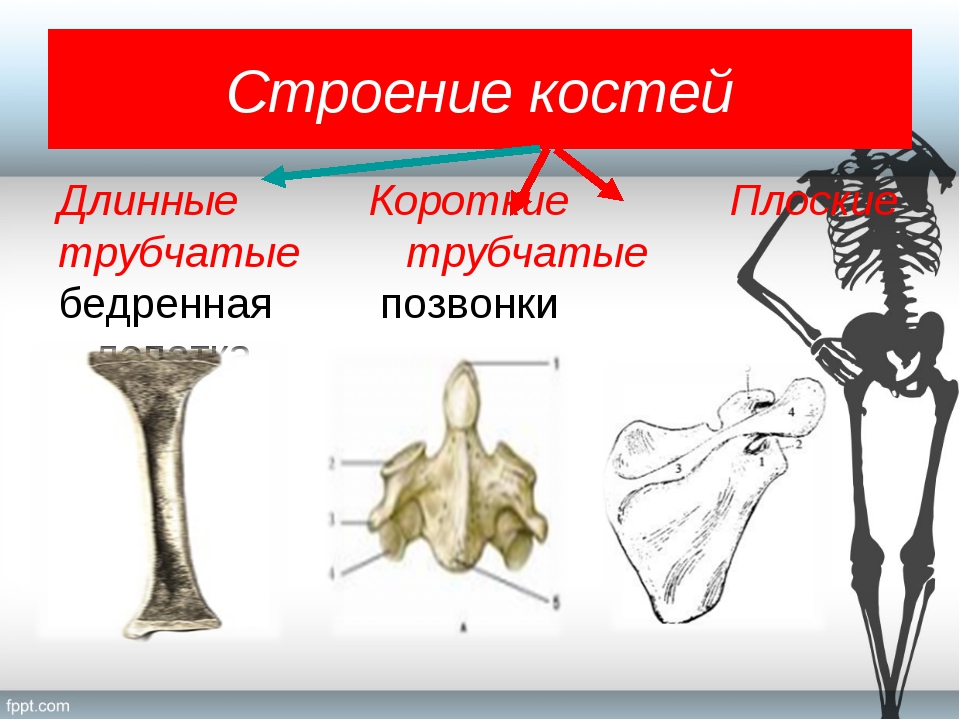 На бедренной кости имеется костно-хрящевой ударный перелом с углубленной латеральной насечкой (стрелка). Отек большеберцовой кости связан с контузией, но без разрушения хрящевой или костной ткани.
На бедренной кости имеется костно-хрящевой ударный перелом с углубленной латеральной насечкой (стрелка). Отек большеберцовой кости связан с контузией, но без разрушения хрящевой или костной ткани.
Существует мало сообщений о гистологических изменениях, которые характеризуют ушиб кости, хотя Rangger и его коллеги (97) обнаружили микротрещины губчатой кости и отек костного мозга, а также кровоизлияние в гистологическом исследовании ушибов костей колена у небольшой группы пациентов. образцы, полученные в результате артроскопии или патологоанатомического исследования. Недавнее исследование подчеркнуло другую форму ушиба кости, которая имеет характерный вид на МРТ-изображениях, связанных с разжиженным и некротическим жиром внутри или рядом с костной травмой, иногда окруженной тем, что кажется воспалительной реакцией (98) ().Жировые «шарики» могут мигрировать из одной камеры в другую, поскольку стенки трабекул нарушены травмой. Неизвестно, способствуют ли такие очаги разжиженного жира системной жировой эмболии, выявленной после серьезного повреждения скелета (99).
(a) Т1-взвешенное коронарное (600/20) и (b) средневзвешенное изображение МРТ с подавлением жира (3100/35) колена у пожилой женщины с недостаточным переломом (стрелки) На медиальном плато большеберцовой кости, связанном с остеопорозом, видны глобулярные скопления (стрелка) костного мозга, прилегающие к перелому.
(a) Т1-взвешенное коронарное (600/20) и (b) средневзвешенное изображение МРТ с подавлением жира (3100/35) колена у пожилой женщины с недостаточным переломом (стрелки) На медиальном плато большеберцовой кости, связанном с остеопорозом, видны глобулярные скопления (стрелка) костного мозга, прилегающие к перелому.
Кортикальная кость
Биомеханика кортикальной кости
Кортикальная кость значительно отличается от губчатой кости по анатомическому распределению, а также по составу и архитектуре.Разница в плотности кортикальной кости и губчатой кости является основным фактором, определяющим разные биомеханические свойства этих двух тканей (100). Кортикальная кость компактная и плотная, с пористостью 5–10% по сравнению с рыхлой трабекулярной архитектурой губчатого вещества кости, для которой типичная пористость составляет 50–90% (101) (). Потеря костной массы, связанная со старением, увеличивает пористость коры, снижая ее прочность и увеличивая риск переломов, в первую очередь за счет снижения способности коры головного мозга выдерживать стресс (102).Кортикальная кость прочнее и имеет более высокую способность воспринимать нагрузку, особенно при сжатии, чем губчатая кость, но демонстрирует более высокий модуль упругости, что указывает на то, что она более жесткая и менее гибкая, чем губчатая кость, которая может деформироваться в три-четыре раза и в большей степени. степень (38).
Кортикальная кость компактная и плотная, с пористостью 5–10% по сравнению с рыхлой трабекулярной архитектурой губчатого вещества кости, для которой типичная пористость составляет 50–90% (101) (). Потеря костной массы, связанная со старением, увеличивает пористость коры, снижая ее прочность и увеличивая риск переломов, в первую очередь за счет снижения способности коры головного мозга выдерживать стресс (102).Кортикальная кость прочнее и имеет более высокую способность воспринимать нагрузку, особенно при сжатии, чем губчатая кость, но демонстрирует более высокий модуль упругости, что указывает на то, что она более жесткая и менее гибкая, чем губчатая кость, которая может деформироваться в три-четыре раза и в большей степени. степень (38).
Продольно ориентированные остеоны — структурная единица пластинчатой кортикальной кости. Сагиттальная рентгенограмма коленного сустава показывает разницу во внешнем виде между плотной периферической кортикальной костью и пористой губчатой костью в костномозговом пространстве и субхондральной области. Биомеханические различия между этими двумя костными фракциями показаны в прилагаемой таблице.
Биомеханические различия между этими двумя костными фракциями показаны в прилагаемой таблице.
Микроструктура кортикальной кости подобна микроструктуре хряща и других армированных волокнами композитных материалов, при этом хрупкие минерализованные элементы усиливаются и укрепляются пластичными коллагеновыми компонентами (36). Остеоны — его основная структурная единица, имеющая характерное расположение, известное как гаверсовская система, с концентрическими цилиндрами минерализованного костного матрикса, которые окружают центральную область, содержащую сосудисто-нервные каналы, обозначенные гаверсовскими каналами.В скелете взрослого человека насчитывается примерно 21 миллион остеонов, средняя длина которых составляет 400 мкм, а диаметр варьируется от 100 до 400 мкм (1,4). Под микроскопом остеоны располагаются в виде параллельных пучков вдоль длинной оси стержня, между соседними остеонами располагаются интерстициальные пластинки. На стыке остеона и интерстициальных пластинок откладываются цементные полосы (). Цементная линия рассматривается как область с пониженной минерализацией, потенциально важная для зарождения и отклонения корковых трещин (103,104).
Цементная линия рассматривается как область с пониженной минерализацией, потенциально важная для зарождения и отклонения корковых трещин (103,104).
Одно полное сечение и одно частичное сечение кортикальных остеонов иллюстрируют центральные гаверсовские каналы, окруженные концентрическими пластинками. Тонкая линия цемента (стрелки) видна по краям всего остеона. За пределами этих двух остеонов отмечаются интерстициальные ламели. (Окраска гематоксилин-эозином, среднее увеличение.)
Кортикальная кость расположена преимущественно в стволах длинных костей, в меньших количествах — в виде тонкой внешней оболочки, окружающей губчатую кость плоских и неправильных костей.Диафиз длинных трубчатых костей представляет собой периферическое кольцо плотной кортикальной кости, которое окружает пористое центральное мозговое пространство. Эта трубчатая форма, аналогичная полому цилиндру, оптимальна для того, чтобы выдерживать множество внешних и внутренних сил, действующих на вал, поскольку полый цилиндр, если рассматривать его по весу, намного прочнее, чем твердый материал (105). Прочность стержня увеличивается по мере увеличения его внешнего диаметра и / или толщины стенки, причем только эти свойства составляют более 55% различий в прочности кортикальной кости (26).
Прочность стержня увеличивается по мере увеличения его внешнего диаметра и / или толщины стенки, причем только эти свойства составляют более 55% различий в прочности кортикальной кости (26).
Возникновение и отклонение трещины
Переломы кортикальной кости могут быть вызваны либо приложением одной силы высокой амплитуды (травматический перелом), либо подпороговой силой, приложенной к кости, ослабленной в результате патологического процесса, такого как новообразование (патологический перелом), или накопленные микроповреждения, связанные с повторяющейся травмой (стресс-перелом) (106). Паттерны разрушения кортикальной кости связаны с ее иерархической организацией, которую можно понять в микроскопическом масштабе, в котором развиваются отслоение коллагена, микроповреждения и микротрещины, и в макроскопическом масштабе, при котором встречаются клинически важные переломы (107,108) ().Зарождение трещины в кортикальном слое кости обычно происходит на ее поверхности или вблизи нее. Морфология микротрещины варьируется в зависимости от механизма нагружения, при этом трещины сжатия длиннее и имеют угол 30-40 ° относительно коры, а трещины растяжения меньше и ориентированы перпендикулярно растягивающей силе. В то время как трещины при растяжении могут вызвать более диффузное повреждение, последующее распространение до явного перелома чаще встречается при повреждении от сжатия (19).
Морфология микротрещины варьируется в зависимости от механизма нагружения, при этом трещины сжатия длиннее и имеют угол 30-40 ° относительно коры, а трещины растяжения меньше и ориентированы перпендикулярно растягивающей силе. В то время как трещины при растяжении могут вызвать более диффузное повреждение, последующее распространение до явного перелома чаще встречается при повреждении от сжатия (19).
Иерархическая масштабная модель кортикальной кости показывает различные масштабы длины тканей, составляющих кору.Остеон — это основная структурная единица кортикального слоя кости. (Изменено и перепечатано с разрешения ссылки 108.)
Механизмы упрочнения костей, такие как отклонение и перекрытие трещин коллагеном, пытаются сдержать повреждение коры и предотвратить распространение микроскопической трещины в макроскопическую трещину (106,107,109,110) . При низких уровнях силы распространение поперечных микротрещин в коре головного мозга тормозится концентрическим ламеллярным расположением минерализованного коллагена внутри остеона, а также цементными линиями, расположенными на поверхности плотно упакованных остеонов (111, 112).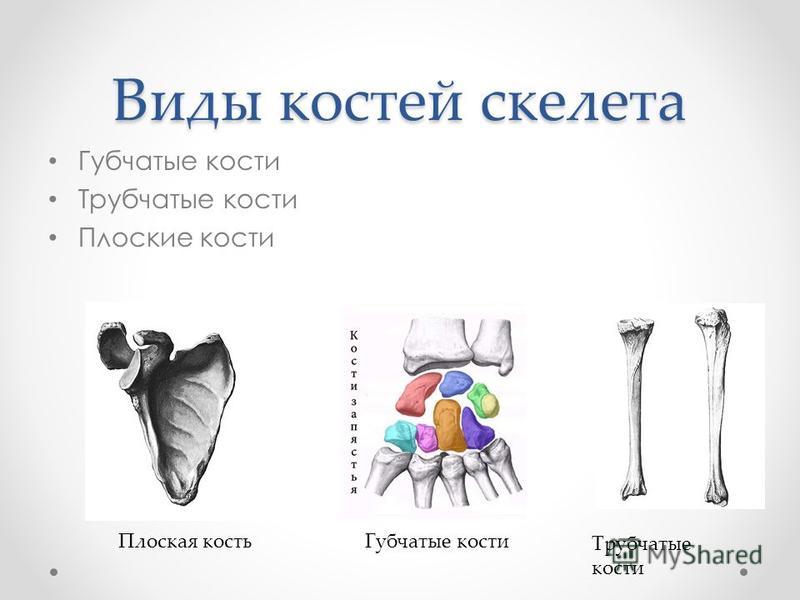 Эти продольно ориентированные границы раздела препятствуют поперечному распространению трещины, что приводит к продольному прогибу и извилистым траекториям трещины, поскольку трещина снова и снова отклоняется на этих границах раздела (109) (). При высоких уровнях силы механизмы упрочнения оказываются подавленными, и микротрещины распространяются поперечно по всей коре головного мозга, что приводит к явному перелому.
Эти продольно ориентированные границы раздела препятствуют поперечному распространению трещины, что приводит к продольному прогибу и извилистым траекториям трещины, поскольку трещина снова и снова отклоняется на этих границах раздела (109) (). При высоких уровнях силы механизмы упрочнения оказываются подавленными, и микротрещины распространяются поперечно по всей коре головного мозга, что приводит к явному перелому.
Путь трещины от выемки, образованной в образце кортикальной кости, демонстрирующий отклонения трещины, связанные с продольными границами, образованными цементными линиями и костными пластинами.(Изменено и перепечатано с разрешения ссылки 109.)
В то время как продольно ориентированные трещины коры головного мозга обычны на микроскопическом уровне (109), макроскопические продольные переломы коры головного мозга в клинической практике встречаются редко, особенно после единичного эпизода травмы. Этот необычный характер перелома чаще всего является результатом повторяющихся нагрузок, чаще всего наблюдаемых в большеберцовой кости, за которой следуют бедренная кость, малоберцовая кость, плечевая кость и надколенник (113–115).
Перелом кортикального слоя
Травматический перелом кортикальной кости возникает в результате внезапного приложения нагрузки, превышающей ее пороговое значение напряжения и / или деформации, при этом ориентация линии перелома отражает геометрическую ориентацию силы, приложенной к поверхности кости ( 100).Сдавливание кости, как видно после приземления при падении, приводит к вертикальному перелому, хотя стержень кости редко выходит из строя при сжатии, если нет дополнительной угловой силы (36). Скорее, компрессионная недостаточность обычно возникает в губчатых трабекулах, которые доминируют на конце кости. Повреждение кости при растяжении обычно приводит к отрывному перелому при энтезе; такие насадки сосредоточены на концах костей. Многоосные механизмы повреждения, такие как изгиб и скручивание, приводят к большинству переломов стержня кости, при этом изгиб вызывает поперечные или короткие косые переломы, а скручивание приводит к спиральным переломам стержня кости (36, 116, 117). Такие переломы часто наблюдаются в большеберцовой и малоберцовой коже после скручивания голеностопного сустава. Изгиб первоначально приводит к образованию поперечных трещин на растянутой стороне кости, хотя большинство травматических переломов, связанных с изгибом, на самом деле являются результатом комбинации изгиба и осевой нагрузки, что приводит к разрыву при растяжении выпуклой стороны и разрушению при сдвиге на стороне сжатия. создание наклонной линии перелома (36,38). Одновременное приложение силы с помощью комбинации этих механизмов происходит часто, что приводит к сложным трещинам, которые показывают особенности, отражающие более чем одну простую структуру трещин ().
Такие переломы часто наблюдаются в большеберцовой и малоберцовой коже после скручивания голеностопного сустава. Изгиб первоначально приводит к образованию поперечных трещин на растянутой стороне кости, хотя большинство травматических переломов, связанных с изгибом, на самом деле являются результатом комбинации изгиба и осевой нагрузки, что приводит к разрыву при растяжении выпуклой стороны и разрушению при сдвиге на стороне сжатия. создание наклонной линии перелома (36,38). Одновременное приложение силы с помощью комбинации этих механизмов происходит часто, что приводит к сложным трещинам, которые показывают особенности, отражающие более чем одну простую структуру трещин ().
Переднезадняя рентгенограмма правой большеберцовой и малоберцовой костей демонстрирует оскольчатый перелом большеберцовой кости с фрагментом «бабочка» (стрелка) и поперечный перелом дистального диафиза малоберцовой кости. Обратите внимание на измельчение, смещение и угловую деформацию переломов, что указывает на то, что во время травмы к ним были приложены сложные силы.
Прямая сила, приложенная к кости, является менее частой причиной травматических переломов, чем косвенная сила. Прямая сила небольшой величины, такая как удар предметом с низкой скоростью, например кулаком, приводит к поперечному перелому в месте приложения силы, как это видно на переломе локтевой кости от дубинки.Прямая сила более высокой величины, например, столкновение с движущимся транспортным средством, приводит к более сложной картине разрушения, обычно связанной с измельчением (37,117).
Стрессовое повреждение кости
Стрессовое повреждение кости включает в себя спектр аномалий, которые возникают, когда кость подвергается повторяющейся нагрузке, причем каждое событие нагрузки само по себе ниже порога разрушения кости (118). В отличие от травматического перелома, при котором кость разрушается из-за одного эпизода нагрузки, стрессовое повреждение возникает из-за совокупного дисбаланса между развитием микроповреждений и способностью кости к самовосстановлению. Стрессовое повреждение приводит к многочисленным формам нарушения цикла ремоделирования кости, которые неточно определены и не поддаются четкому разделению, что приводит к путанице в терминологии и классификации этих повреждений (118, 119). Стресс-перелом является конечной точкой непрерывного спектра морфологических изменений, которые варьируются от бессимптомного ремоделирования до различных стадий связанных со стрессом изменений в архитектуре кости, включая микроповреждения, образование и распространение микротрещин, очаговую резорбцию кости и макротрещины (120).
Стрессовое повреждение приводит к многочисленным формам нарушения цикла ремоделирования кости, которые неточно определены и не поддаются четкому разделению, что приводит к путанице в терминологии и классификации этих повреждений (118, 119). Стресс-перелом является конечной точкой непрерывного спектра морфологических изменений, которые варьируются от бессимптомного ремоделирования до различных стадий связанных со стрессом изменений в архитектуре кости, включая микроповреждения, образование и распространение микротрещин, очаговую резорбцию кости и макротрещины (120).
Стресс-переломы традиционно делятся на подтипы недостаточности и усталости. Переломы недостаточности являются результатом повторяющихся нагрузок в пределах нормального диапазона действий, применяемых к кости, что само по себе является аномальным, тогда как усталостные переломы являются результатом повторяющихся избыточных нагрузок, прикладываемых к нормальной кости. Форма утомления обычно наблюдается у молодых людей, особенно у тех, кто занимается спортом.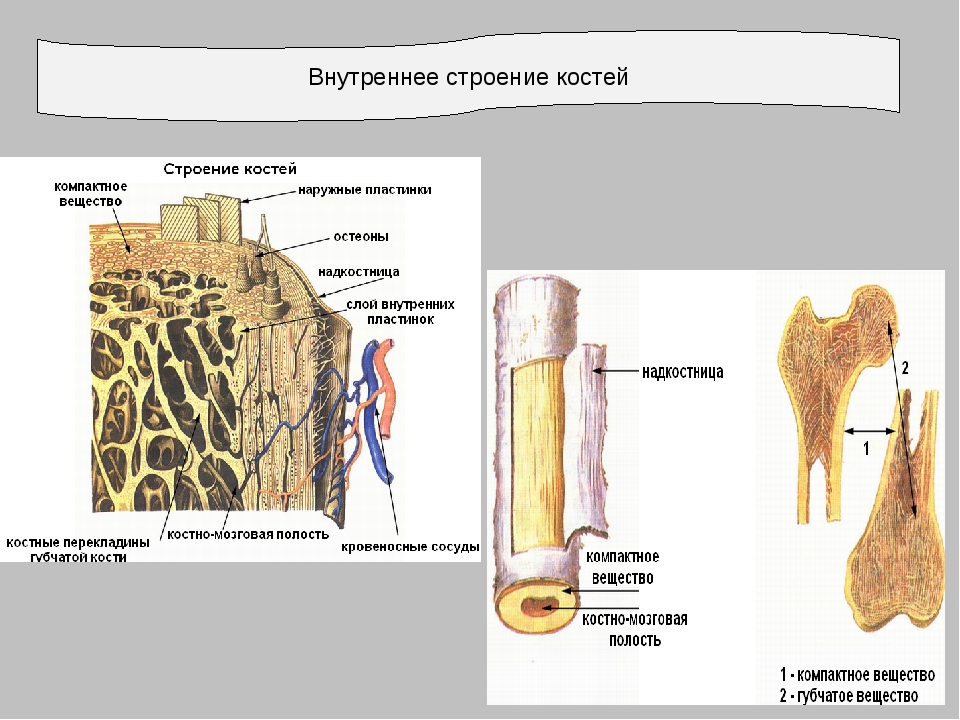 Повреждения, вызванные недостаточностью, обычно связаны с метаболическими заболеваниями костей, такими как остеопороз, и обычно возникают у людей старше тех, кто страдает усталостными травмами (120).Однако есть много людей, у которых стрессовая травма не совсем вписывается в категорию усталости или недостаточности, а скорее имеет компоненты и того, и другого. В связи с тем, что в настоящее время делается упор на поддержание хорошего здоровья и «поддержание формы», люди среднего и пожилого возраста с большей вероятностью будут заниматься активными физическими упражнениями и развлекательными видами спорта, что объясняет учащение случаев усталости костей у пожилых людей. И наоборот, наличие нарушений питания или метаболизма у молодых может привести к недостаточной прочности костей и развитию переломов недостаточности.Классическим примером последней ситуации является «триада спортсменки», синдром трех частично совпадающих состояний, включающий дефицит энергии с нарушением питания или без него, нарушение менструального цикла и потерю минералов в костях.
Повреждения, вызванные недостаточностью, обычно связаны с метаболическими заболеваниями костей, такими как остеопороз, и обычно возникают у людей старше тех, кто страдает усталостными травмами (120).Однако есть много людей, у которых стрессовая травма не совсем вписывается в категорию усталости или недостаточности, а скорее имеет компоненты и того, и другого. В связи с тем, что в настоящее время делается упор на поддержание хорошего здоровья и «поддержание формы», люди среднего и пожилого возраста с большей вероятностью будут заниматься активными физическими упражнениями и развлекательными видами спорта, что объясняет учащение случаев усталости костей у пожилых людей. И наоборот, наличие нарушений питания или метаболизма у молодых может привести к недостаточной прочности костей и развитию переломов недостаточности.Классическим примером последней ситуации является «триада спортсменки», синдром трех частично совпадающих состояний, включающий дефицит энергии с нарушением питания или без него, нарушение менструального цикла и потерю минералов в костях. Наличие одного или нескольких компонентов этой триады увеличивает риск стрессового перелома у молодой спортсменки (111, 120).
Наличие одного или нескольких компонентов этой триады увеличивает риск стрессового перелома у молодой спортсменки (111, 120).
Недостаточный перелом
Существует целый ряд аномалий, которые могут ослабить саму кость, связанных с пониженной минерализацией, снижением прочности и прочности костей, потерей эластического сопротивления или недостаточной архитектурой кости, или их комбинациями, или, альтернативно, связанными с ними. к нарушению нормальных механизмов восстановления костей (26,108,112).В клинической практике остеопороз, остеомаляция и предшествующее облучение кости являются наиболее частыми нарушениями, которые приводят к недостаточной способности кости выдерживать обычную нагрузку (112). В то время как остеопороз обычно считается основной причиной недостаточности повреждения костей, только измерения минеральной плотности костей объясняют только 70–75% различий в прочности костей (121).
Нарушения метаболизма костей преимущественно поражают губчатую кость, у которой отношение площади поверхности к массе в 10 раз выше, чем у кортикальной кости, что подвергает большие площади этой поверхности метаболическим стимулам и региональному кровотоку. Потеря костной массы, наблюдаемая в губчатых трабекулах, неоднородна, с преимущественной потерей вторичных трабекул, а не первичных продольно ориентированных несущих трабекул, что приводит к нарушению костной архитектуры, которая легко терпит неудачу даже при физиологической нагрузке (121). Способность первичных продольных трабекул без опоры воспринимать сжимающую нагрузку сильно снижается из-за потери опорных вторичных трабекул, что приводит к разрушению изгиба, как это предсказано законом Эйлера.Нарушение выпучивания смежных первичных трабекул объясняет типичную ориентацию недостаточных переломов, которые распространяются перпендикулярно оси первичных трабекул.
Потеря костной массы, наблюдаемая в губчатых трабекулах, неоднородна, с преимущественной потерей вторичных трабекул, а не первичных продольно ориентированных несущих трабекул, что приводит к нарушению костной архитектуры, которая легко терпит неудачу даже при физиологической нагрузке (121). Способность первичных продольных трабекул без опоры воспринимать сжимающую нагрузку сильно снижается из-за потери опорных вторичных трабекул, что приводит к разрушению изгиба, как это предсказано законом Эйлера.Нарушение выпучивания смежных первичных трабекул объясняет типичную ориентацию недостаточных переломов, которые распространяются перпендикулярно оси первичных трабекул.
Переломы недостаточности обычно поражают те области кости, где имеется высокая фракция губчатого вещества, такие как тела позвонков, плоские кости таза (особенно области крестцового крыла), субхондральные области длинных трубчатых костей и небольшие кости стопы неправильной формы (например, пяточная кость).Коллапс субхондральной кости приводит к визуализации, имитирующей остеонекроз. Например, перегрузка субхондральной кости вокруг колена, обычно сопровождающаяся аномалиями прилегающего мениска и хондры, приводит к коллапсу субхондральной костной пластинки бедренной или большеберцовой кости, состоянию, ранее ошибочно обозначенному спонтанным остеонекрозом (122) ( ).
Например, перегрузка субхондральной кости вокруг колена, обычно сопровождающаяся аномалиями прилегающего мениска и хондры, приводит к коллапсу субхондральной костной пластинки бедренной или большеберцовой кости, состоянию, ранее ошибочно обозначенному спонтанным остеонекрозом (122) ( ).
(a) Корональное T1-взвешенное (600/20) и (b) средневзвешенное МРТ с подавлением жира (3100/30) колена у женщины среднего возраста с переломом субхондральной недостаточности медиальный мыщелок бедра (прямая стрелка) с вторичным коллапсом опорной поверхности.Имеется периферическое выдавливание мениска (изогнутая стрелка), связанное с разрывом заднего корня мениска (не показано), что приводит к механической перегрузке вышележащей кости и хряща. Обратите внимание на хрящевую потерю медиальной части бедренной кости и сильный отек костного мозга в области перелома, а также на выпот и жидкость, раздувающую большеберцовую коллатеральную сумку внутри медиальной коллатеральной связки.
(a) Корональное T1-взвешенное (600/20) и (b) средневзвешенное МРТ с подавлением жира (3100/30) колена у женщины среднего возраста с переломом субхондральной недостаточности медиальный мыщелок бедра (прямая стрелка) с вторичным коллапсом опорной поверхности.Имеется периферическое выдавливание мениска (изогнутая стрелка), связанное с разрывом заднего корня мениска (не показано), что приводит к механической перегрузке вышележащей кости и хряща. Обратите внимание на хрящевую потерю медиальной части бедренной кости и сильный отек костного мозга в области перелома, а также на выпот и жидкость, раздувающую большеберцовую коллатеральную сумку внутри медиальной коллатеральной связки.
Усталостный перелом
Усталостное повреждение кости наиболее часто встречается в кортикальной кости нижних конечностей, особенно в шейке второй и третьей плюсневых костей, средней и дистальной части голени и шейке бедренной кости, прилегающей к малому вертлугу. возле стыка диафиза и бедренной кости ().Роль мышечной активности в создании сжимающих, сдвигающих и крутящих сил в кости подчеркивалась в предыдущих описаниях усталостных переломов, предполагая, что дисбаланс между прочностью кости и мышечной силой способствует развитию таких травм (123). Вначале усталостное повреждение кортикального слоя кости проявляется в виде микротрещин на поверхности кости. Их можно идентифицировать гистологически и с помощью таких методов, как микрокомпьютерная томография высокого разрешения (121), но они не видны с помощью обычных методов визуализации, пока они не станут достаточно обширными, чтобы вызвать ответ надкостницы.По мере прогрессирования травмы продольное отклонение микротрещин приводит к внутрикортикальным резорбционным полостям различного размера и ориентации, образуя рентгенопрозрачные области и, в конечном итоге, к реактивному отеку костного мозга по мере приближения повреждения к мозговому пространству (119). Развитие стрессового повреждения приводит к распространению этих внутрикортикальных микротрещин на кору эндоста и, в конечном итоге, к развитию поперечно ориентированной прямой линии перелома, которая входит в костномозговое пространство.
возле стыка диафиза и бедренной кости ().Роль мышечной активности в создании сжимающих, сдвигающих и крутящих сил в кости подчеркивалась в предыдущих описаниях усталостных переломов, предполагая, что дисбаланс между прочностью кости и мышечной силой способствует развитию таких травм (123). Вначале усталостное повреждение кортикального слоя кости проявляется в виде микротрещин на поверхности кости. Их можно идентифицировать гистологически и с помощью таких методов, как микрокомпьютерная томография высокого разрешения (121), но они не видны с помощью обычных методов визуализации, пока они не станут достаточно обширными, чтобы вызвать ответ надкостницы.По мере прогрессирования травмы продольное отклонение микротрещин приводит к внутрикортикальным резорбционным полостям различного размера и ориентации, образуя рентгенопрозрачные области и, в конечном итоге, к реактивному отеку костного мозга по мере приближения повреждения к мозговому пространству (119). Развитие стрессового повреждения приводит к распространению этих внутрикортикальных микротрещин на кору эндоста и, в конечном итоге, к развитию поперечно ориентированной прямой линии перелома, которая входит в костномозговое пространство.
(a) Переднезадняя рентгенограмма и (b) МРТ-снимок со средневзвешенной коронкой (3100/35) с подавлением жира у бегуна с болью в левом бедре демонстрируют усталостный перелом шейки бедра (стрелка), расположенный на медиальная (компрессионная) сторона шейки бедра.
(a) Переднезадняя рентгенограмма и (b) МРТ-снимок со средневзвешенной коронкой (3100/35) с подавлением жира у бегуна с болью в левом бедре демонстрируют усталостный перелом шейки бедра (стрелка), расположенный на медиальная (компрессионная) сторона шейки бедра.
Резюме
В заключение, знание макроскопической и микроскопической анатомии, а также базовой биомеханики кости и хряща обеспечивает основу для лучшего понимания того, как эта ткань реагирует на измененные механические силы и проливает свет на визуализация, связанная как с острой, так и с повторяющейся травмой.
Essentials
■ Состав костного матрикса можно разделить на два типа организации: кортикальная кость и губчатая кость; эти две фракции существенно различаются по своим анатомическим и биомеханическим свойствам.

■ Травматическое повреждение костей и хрящей может принимать форму однократного чрезмерного сильного удара или повторяющихся нагрузок ниже порогового значения травмы, каждая из которых может вызвать перегрузку ткани, приводящую к повреждению.
■ Нормальные биомеханические свойства и паттерны разрушения хрящей и костей связаны с их анатомией и организацией тканей, которые можно понять в нескольких масштабах длины.
Благодарности
Мы благодарим Парвиса Хагиги, доктора медицины, профессора клинической патологии в UCSD и директора отделения анатомической патологии в Медицинском центре штата Вирджиния в Сан-Диего за предоставленные гистологические материалы. Вон Бэ, доктор философии, научный сотрудник, UCSD MSK Лаборатория исследования изображений для обзора частей этой рукописи, посвященных биомеханике, и Дебора Труделл, RT, для подготовки анатомических разделов.
Сноски
C.B.C. при поддержке Национальных институтов здравоохранения (гранты R01DE022068 и R01AR064321) и Департамента США по делам ветеранов, клинических научных исследований и разработок (Merit Award I01CX000625).
Поступило 10.10.2014 г .; доработка запрошена 1 декабря; окончательная доработка получена 27 апреля 2015 г .; принято 11 мая; окончательная версия принята 4 июня; Окончательная проверка 20 января 2016 г.
Раскрытие конфликта интересов: M.Н.П. не раскрыл никаких соответствующих отношений. C.B.C. не раскрыл никаких соответствующих отношений. D.L.R. не раскрыл никаких соответствующих отношений.
Список литературы
1. Стандринг С. Функциональная анатомия опорно-двигательного аппарата. В кн .: Standring S, ed. Анатомия Грея: анатомическая основа клинической практики. 40-е изд. Филадельфия, Пенсильвания: Черчилль Ливингстон Эльзевьер, 2008; 81–97. [Google Scholar] 2. Кини У, Нандиш Б.Н. Физиология костеобразования, ремоделирования и обмена веществ.В: Fogelman I, Gnanesegaran G, van der Wall H, ред. Радионуклидная и гибридная визуализация костей. Берлин, Германия: Springer-Verlag, 2012; 29–57. [Google Scholar] 3. Карсенти Г., Ури Ф. Биология без стен: новая эндокринология кости. Анну Рев Физиол 2012; 74: 87–105. [PubMed] [Google Scholar] 6. Бойл В.Дж., Саймонет В.С., Лейси Д.Л. Дифференциация и активация остеокластов. Nature 2003; 423 (6937): 337–342. [PubMed] [Google Scholar] 7. Когианни Г, Благородный BS. Биология остеоцитов. Curr Osteoporos Rep 2007; 5 (2): 81–86.[PubMed] [Google Scholar] 8. van der Plas A, Aarden EM, Feijen JH, et al. . Характеристики и свойства остеоцитов в культуре. J Bone Miner Res 1994; 9 (11): 1697–1704. [PubMed] [Google Scholar] 9. van Bezooijen RL, ten Dijke P, Papapoulos SE, Löwik CW. SOST / склеростин, негативный регулятор костеобразования, происходящий из остеоцитов. Фактор роста цитокинов Rev 2005; 16 (3): 319–327. [PubMed] [Google Scholar] 10. Благородный BS. Линия остеоцитов. Arch Biochem Biophys 2008; 473 (2): 106–111. [PubMed] [Google Scholar] 11.Мари ПиДжей. Ремоделирование костей: социальная сеть клеток. Medicographia 2012; 34: 149–154. [Google Scholar] 12.
[Google Scholar] 3. Карсенти Г., Ури Ф. Биология без стен: новая эндокринология кости. Анну Рев Физиол 2012; 74: 87–105. [PubMed] [Google Scholar] 6. Бойл В.Дж., Саймонет В.С., Лейси Д.Л. Дифференциация и активация остеокластов. Nature 2003; 423 (6937): 337–342. [PubMed] [Google Scholar] 7. Когианни Г, Благородный BS. Биология остеоцитов. Curr Osteoporos Rep 2007; 5 (2): 81–86.[PubMed] [Google Scholar] 8. van der Plas A, Aarden EM, Feijen JH, et al. . Характеристики и свойства остеоцитов в культуре. J Bone Miner Res 1994; 9 (11): 1697–1704. [PubMed] [Google Scholar] 9. van Bezooijen RL, ten Dijke P, Papapoulos SE, Löwik CW. SOST / склеростин, негативный регулятор костеобразования, происходящий из остеоцитов. Фактор роста цитокинов Rev 2005; 16 (3): 319–327. [PubMed] [Google Scholar] 10. Благородный BS. Линия остеоцитов. Arch Biochem Biophys 2008; 473 (2): 106–111. [PubMed] [Google Scholar] 11.Мари ПиДжей. Ремоделирование костей: социальная сеть клеток. Medicographia 2012; 34: 149–154. [Google Scholar] 12. Тети А. Развитие костей: обзор костных клеток и передачи сигналов. Curr Osteoporos Rep 2011; 9 (4): 264–273. [PubMed] [Google Scholar] 13. Кобаяси С., Такахаши Х.Э., Ито А. и др. . Минимоделирование трабекул в подвздошной кости человека. Кость 2003; 32 (2): 163–169. [PubMed] [Google Scholar] 14. Убара Ю., Фусими Т., Тагами Т. и др. . Гистоморфометрические особенности кости у пациентов с первичным и вторичным гипопаратиреозом.Kidney Int 2003; 63 (5): 1809–1816. [PubMed] [Google Scholar] 15. Убара Ю., Тагами Т., Наканиши С. и др. . Значение минимоделирования у диализных пациентов с адинамической болезнью костей. Kidney Int 2005; 68 (2): 833–839. [PubMed] [Google Scholar] 16. Вольф Дж. Классика: о внутренней архитектуре костей и ее важности для роста костей. 1870. Clin Orthop Relat Res 2010; 468 (4): 1056–1065. [Бесплатная статья PMC] [PubMed] [Google Scholar] 17. Дункан Р.Л., Тернер С.Х. Механотрансдукция и функциональный ответ кости на механическое напряжение.Calcif Tissue Int 1995; 57 (5): 344–358. [PubMed] [Google Scholar] 18. Frost HM. A. Обновление физиологии костей и закона Вольфа для клиницистов в 2003 г. Угол Ортод 2004; 74 (1): 3–15. [PubMed] [Google Scholar] 19. Чапурлат Р.Д., Дельмас П.Д. Микроповреждения костей: клиническая перспектива. Остеопорос Инт 2009; 20 (8): 1299–1308. [PubMed] [Google Scholar] 21. Отт С.М. Гистоморфометрический анализ ремоделирования кости. В: Билезикян Дж. П., Райс Л. Г., Родан Г. А., ред. Принципы костной биологии. Сан-Диего, Калифорния: Academic Press, 2002; 303–319.[Google Scholar] 22. Эрнандес CJ, Beaupré GS, Carter DR. Модель механобиологических и метаболических влияний на адаптацию костей. J. Rehabil Res Dev 2000; 37 (2): 235–244. [PubMed] [Google Scholar] 23. Odvina CV, Zerwekh JE, Rao DS, Maalouf N, Gottschalk FA, Pak CY. Сильно подавленный метаболизм костной ткани: потенциальное осложнение терапии алендронатом. J Clin Endocrinol Metab 2005; 90 (3): 1294–1301. [PubMed] [Google Scholar] 24. Goh SK, Yang KY, Koh JS, et al. . Подвертельная недостаточность переломов у пациентов, получающих алендронат: с осторожностью.J Bone Joint Surg Br 2007; 89 (3): 349–353. [PubMed] [Google Scholar] 25. Benjamin M, Toumi H, Ralphs JR, Bydder G, Best TM, Milz S. Место соединения сухожилий и связок с костью: места прикрепления («энтезы») в зависимости от упражнений и / или механической нагрузки. Журнал Анат 2006; 208 (4): 471–490. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Дэвисон К.С., Симиноски К., Адачи Дж. Д. и др. . Сила костей: целое больше, чем сумма его частей. Semin Arthritis Rheum 2006; 36 (1): 22–31. [PubMed] [Google Scholar] 27.Oxlund H, Mosekilde L, Ortoft G. Снижение концентрации восстанавливаемых коллагеном поперечных связей в губчатой кости человека с учетом возраста и остеопороза. Кость 1996; 19 (5): 479–484. [PubMed] [Google Scholar] 28. Boivin G, Meunier PJ. Степень минерализации костной ткани измеряется компьютерной количественной контактной микрорентгенографией. Calcif Tissue Int 2002; 70 (6): 503–511. [PubMed] [Google Scholar] 29. Currey JD, Brear K, Zioupos P. Эффекты старения и изменения содержания минералов в снижении прочности бедер человека.J Biomech 1996; 29 (2): 257–260. [PubMed] [Google Scholar] 30. Риггс Б.Л., Ходжсон С.Ф., О’Фаллон В.М. и др. . Влияние лечения фтором на частоту переломов у женщин в постменопаузе с остеопорозом. N Engl J Med 1990; 322 (12): 802–809. [PubMed] [Google Scholar] 31. Фриман Дж. Дж., Вопенка Б., Сильва М. Дж., Пастерис Дж. Д.. Рамановское спектроскопическое обнаружение изменений биоапатита в бедрах мышей в зависимости от возраста и лечения фторидом in vitro. Calcif Tissue Int 2001; 68 (3): 156–162. [PubMed] [Google Scholar] 32. Хубер М., Траттниг С., Линтнер Ф.Анатомия, биохимия и физиология суставного хряща. Инвест Радиол 2000; 35 (10): 573–580. [PubMed] [Google Scholar] 33. Фриман П.М., Натараджан Р.Н., Кимура Дж. Х., Андриакчи Т.П. Клетки хондроцитов механически реагируют на сжимающие нагрузки. J Orthop Res 1994; 12 (3): 311–320. [PubMed] [Google Scholar] 34. Glaser C, Putz R. Функциональная анатомия суставного хряща при сжимающей нагрузке: количественные аспекты глобальных, локальных и зональных реакций коллагеновой сети в отношении целостности поверхности.Хрящевой остеоартрит 2002; 10 (2): 83–99. [PubMed] [Google Scholar] 35. Вайс С., Розенберг Л., Хелфет А.Дж. Ультраструктурное исследование нормального суставного хряща молодого взрослого человека. J Bone Joint Surg Am 1968; 50 (4): 663–674. [PubMed] [Google Scholar] 37. Нордин М., Франкель В.Х. Биомеханика кости. В: Нордин М., Франкель В.Х., ред. Базовая биомеханика опорно-двигательного аппарата. 2-е изд. Балтимор, Мэриленд: Липпинкотт Уильямс и Уилкинс, 2001; 26–59. [Google Scholar] 39. Dempster DW. Микроархитектура и прочность костей.Osteoporos Int 2003; 14 (Приложение 5): S54 – S56. [PubMed] [Google Scholar] 40. Ширази Р., Ширази-Адл А., Хуртиг М. Роль сетей коллагеновых фибрилл хряща в биомеханике коленного сустава при сжатии. J Biomech 2008; 41 (16): 3340–3348. [PubMed] [Google Scholar] 41. Линн Ф.К., Соколов Л. Движение и состав интерстициальной жидкости хряща. Arthritis Rheum 1965; 8: 481–494. [PubMed] [Google Scholar] 42. Моу В.К., Холмс М.Х., Лай В.М. Транспорт жидкости и механические свойства суставного хряща: обзор.Дж. Биомех 1984; 17 (5): 377–394. [PubMed] [Google Scholar] 43. Ароен А., Лёкен С., Наследник С. и др. . Поражения суставного хряща при 993 последовательных артроскопиях коленного сустава. Am J Sports Med 2004; 32 (1): 211–215. [PubMed] [Google Scholar] 44. Hjelle K, Solheim E, Strand T, Muri R, Brittberg M. Дефекты суставного хряща при артроскопии 1000 коленного сустава. Артроскопия 2002; 18 (7): 730–734. [PubMed] [Google Scholar] 45. Curl WW, Krome J, Gordon ES, Rushing J, Smith BP, Poehling GG. Повреждения хряща: обзор 31 516 артроскопий коленного сустава.Артроскопия 1997; 13 (4): 456–460. [PubMed] [Google Scholar] 46. Моу В.К., Чжу В., Рэтклифф А. Структура и функция суставного хряща и мениска. В: Mow VC, Hayes WC, eds. Основы ортопедической биомеханики. Нью-Йорк, Нью-Йорк: Рэйвен, 1991; 143–198. [Google Scholar] 47. Фермер Дж. М., Мартин Д. Ф., Болес, Калифорния, Керл, WW. Хондральные и костно-хрящевые травмы. Диагностика и лечение. Clin Sports Med 2001; 20 (2): 299–320. [PubMed] [Google Scholar] 48. Боррелли Дж. Младший, Риччи ВМ. Острые последствия воздействия на хрящи. Clin Orthop Relat Res 2004; (423): 33–39.[PubMed] [Google Scholar] 49. Бэ WC, Льюис CW, Левенстон, штат Мэн, Южная Африка. Тестирование вдавливания суставного хряща человека: влияние геометрии наконечника зонда и глубины вдавливания на деформацию внутри ткани. J Biomech 2006; 39 (6): 1039–1047. [PubMed] [Google Scholar] 50. Моу В.К., Куэй СК, Лай В.М., Армстронг К.Г. Двухфазная ползучесть и расслабление суставного хряща при сжатии? Теория и эксперименты. J Biomech Eng 1980; 102 (1): 73–84. [PubMed] [Google Scholar] 51. Франк EH, Grodzinsky AJ. Электромеханика хряща.II. Континуальная модель электрокинетики хряща и корреляция с экспериментами. J. Biomech, 1987; 20 (6): 629–639. [PubMed] [Google Scholar] 52. Эверс BJ, Jayaraman VM, Banglmaier RF, Haut RC. Скорость тупой ударной нагрузки влияет на изменения ретропателлярного хряща и подлежащей кости надколенника кролика. J Biomech 2002; 35 (6): 747–755. [PubMed] [Google Scholar] 53. Галло Р.А., Мошер Т.Дж. Визуализация повреждений хряща и костно-хрящевой ткани: обзор конкретных случаев. Clin Sports Med 2013; 32 (3): 477–505. [PubMed] [Google Scholar] 54.Loening AM, James IE, Levenston ME, et al. . Повреждающее механическое сжатие суставного хряща крупного рогатого скота вызывает апоптоз хондроцитов. Arch Biochem Biophys 2000; 381 (2): 205–212. [PubMed] [Google Scholar] 55. Д’Лима Д.Д., Хашимото С., Чен П.С., Колвелл К.В., младший, Лотц М.К. Апоптоз хондроцитов человека в ответ на механическое повреждение. Хрящевой остеоартрит 2001; 9 (8): 712–719. [PubMed] [Google Scholar] 56. Курц Б., Джин М., Патвари П., Ченг Д.М., Ларк М.В., Гродзинский А.Дж. Биосинтетический ответ и механические свойства суставного хряща после травматической компрессии.J Orthop Res 2001; 19 (6): 1140–1146. [PubMed] [Google Scholar] 57. Клементс К.М., Би З.С., Кроссингем Г.В., Адамс М.А., Шариф М. Насколько серьезной должна быть повторяющаяся нагрузка, чтобы убить хондроциты в суставном хряще? Хрящевой остеоартрит 2001; 9 (5): 499–507. [PubMed] [Google Scholar] 58. Quinn TM, Allen RG, Schalet BJ, Perumbuli P, Hunziker EB. Повреждение матрикса и клеток из-за субударной нагрузки эксплантатов суставного хряща взрослого крупного рогатого скота: влияние скорости деформации и пикового напряжения. J Orthop Res 2001; 19 (2): 242–249.[PubMed] [Google Scholar] 59. Патвари П., Гашен В., Джеймс И. Е. и др. . Ультраструктурная количественная оценка гибели клеток после травматического сжатия суставного хряща теленка крупного рогатого скота. Хрящевой остеоартрит 2004; 12 (3): 245–252. [Бесплатная статья PMC] [PubMed] [Google Scholar] 60. Дуда Г. Н., Эйлерс М., Лох Л., Хоффман Дж. Э., Кеб М., Шейзер К. Смерть хондроцитов предшествует структурному повреждению при травме от тупого удара. Clin Orthop Relat Res 2001; (393): 302–309. [PubMed] [Google Scholar] 61. Чен К. Т., Бхаргава М., Лин П. М., Торзилли ПА.Гибель хондроцитов и повреждение коллагена в циклически нагруженном суставном хряще зависят от времени, стресса и местоположения. J Orthop Res 2003; 21 (5): 888–898. [PubMed] [Google Scholar] 62. Ли X, Куо Д., Теологис А. и др. . Хрящ в коленях, реконструированных с помощью передней крестообразной связки: МРТ T1rho и T2 — первоначальный опыт с последующим наблюдением в течение 1 года. Радиология 2011; 258 (2): 505–514. [Бесплатная статья PMC] [PubMed] [Google Scholar] 63. Potter HG, Jain SK, Ma Y, Black BR, Fung S, Lyman S. Повреждение хряща после острого изолированного разрыва передней крестообразной связки: немедленный и продольный эффект с последующим клиническим наблюдением / МРТ.Am J Sports Med 2012; 40 (2): 276–285. [PubMed] [Google Scholar] 64. Tiderius CJ, Olsson LE, Nyquist F, Dahlberg L. Потеря гликозаминогликанов хряща в острой фазе после повреждения передней крестообразной связки: отсроченная магнитно-резонансная томография хряща с усилением гадолиния и анализ синовиальной жидкости. Arthritis Rheum 2005; 52 (1): 120–127. [PubMed] [Google Scholar] 65. Томацу Т., Имаи Н., Такеучи Н., Такахаши К., Кимура Н. Экспериментально полученные переломы суставного хряща и кости: влияние сил сдвига на колено свиньи.J Bone Joint Surg Br 1992; 74 (3): 457–462. [PubMed] [Google Scholar] 66. Mosher TJ. МРТ костно-хрящевых повреждений колена и голеностопа у спортсмена. Clin Sports Med 2006; 25 (4): 843–866. [PubMed] [Google Scholar] 67. Аутербридж RE. Этиология хондромаляции надколенника. J Bone Joint Surg Br 1961; 43-B: 752–757. [PubMed] [Google Scholar] 68. Нойес Ф. Р., Бассет Р. В., Груд Е. С., Батлер Д. Л.. Артроскопия при остром травматическом гемартрозе коленного сустава: частота передних крестообразных разрывов и других травм. J Bone Joint Surg Am 1980; 62 (5): 687–695, 757.[PubMed] [Google Scholar] 69. Кэмерон М.Л., Бриггс К.К., Стедман-младший. Воспроизводимость и надежность классификации внешнего моста для артроскопической классификации хондральных поражений коленного сустава. Am J Sports Med 2003; 31 (1): 83–86. [PubMed] [Google Scholar] 70. Бриттберг М. Оценка повреждений хряща и восстановление хряща. Osteologie 2000; 9: 17–25. [Google Scholar] 71. Бриттберг М, Винальски К.С. Оценка повреждений и ремонта хрящей. J Bone Joint Surg Am 2003; 85-A (Приложение 2): 58–69. [PubMed] [Google Scholar] 72.Кийовски Р., Бланкенбейкер Д.Г., Дэвис К.В., Шинки К., Каплан Л.Д., Де Смет А.А. Сравнение магнитно-резонансной томографии 1,5 и 3,0 Тл для оценки суставного хряща коленного сустава. Радиология 2009; 250 (3): 839–848. [PubMed] [Google Scholar] 73. Бределла М.А., Тирман П.Ф., Петерфи К.Г. и др. . Точность Т2-взвешенного быстрого спин-эхо МРТ с насыщением жира при обнаружении дефектов хряща в колене: сравнение с артроскопией у 130 пациентов. AJR Am J Roentgenol 1999; 172 (4): 1073–1080. [PubMed] [Google Scholar] 74.Петерфи К.Г., Гермази А., Заим С. и др. . Оценка всего органа с помощью магнитно-резонансной томографии (WORMS) колена при остеоартрите. Хрящевой остеоартрит 2004; 12 (3): 177–190. [PubMed] [Google Scholar] 76. Голд Г.Е., Бурштейн Д., Дарзински Б., Ланг П., Боада Ф., Мошер Т. МРТ суставного хряща при ОА: новые импульсные последовательности и композиционные / функциональные маркеры. Остеоартрозный хрящ 2006; 14 (Приложение A): A76 – A86. [PubMed] [Google Scholar] 77. Уильямс А., Гиллис А., Маккензи С. и др. . Распределение гликозаминогликанов в хрящах, определенное с помощью отсроченной МРТ хряща с усилением гадолиния (dGEMRIC): потенциальные клинические применения.AJR Am J Roentgenol 2004; 182 (1): 167–172. [PubMed] [Google Scholar] 78. Уитон AJ, Dodge GR, Borthakur A, Kneeland JB, Schumacher HR, Reddy R. Выявление изменений протеогликана суставного хряща с помощью магнитно-резонансной томографии T (1rho). J Orthop Res 2005; 23 (1): 102–108. [Бесплатная статья PMC] [PubMed] [Google Scholar] 79. Xia Y, Moody JB, Burton-Wurster N, Lust G. Количественная корреляция in situ между исследованиями суставного хряща с помощью микроскопической МРТ и микроскопии поляризованного света. Хрящевой остеоартрит 2001; 9 (5): 393–406.[PubMed] [Google Scholar] 80. Мадри Х., ван Дейк К.Н., Мюллер-Гербль М. Основы науки о субхондральной кости. Коленная хирургия Sports Traumatol Arthrosc 2010; 18 (4): 419–433. [PubMed] [Google Scholar] 81. Радин Е.Л., Роза Р.М. Роль субхондральной кости в инициации и прогрессировании повреждения хряща. Clin Orthop Relat Res 1986; (213): 34–40. [PubMed] [Google Scholar] 82. Херт Дж. Новая попытка интерпретации функциональной архитектуры губчатой кости. Дж. Биомех 1994; 27 (2): 239–242. [PubMed] [Google Scholar] 83.Барак М.М., Либерман Д.Е., Хублин Дж. Дж. Вольф в овечьей шкуре: адаптация губчатой кости в ответ на изменение ориентации суставной нагрузки. Кость 2011; 49 (6): 1141–1151. [PubMed] [Google Scholar] 84. Ланьон LE. Анализ деформации поверхности пяточной кости овцы при нормальном движении: анализ деформации пяточной кости. J Biomech 1973; 6 (1): 41–49. [PubMed] [Google Scholar] 85. Ланьон LE. Экспериментальное подтверждение траекторной теории строения кости. J Bone Joint Surg Br 1974; 56 (1): 160–166.[PubMed] [Google Scholar] 86. Бувье М. Применение методов измерения деформации костей in vivo для решения проблем адаптации скелета. Am J Phys Anthropol 1985; 28 (Приложение 6): 237–248. [Google Scholar] 87. Su SC, Skedros JG, Bachus KN, Bloebaum RD. Условия нагружения и конструкция кортикальной кости парнокопытной пяточной кости. J Exp Biol 1999; 202 (Pt 22): 3239–3254. [PubMed] [Google Scholar] 88. Скедрос JG, Baucom SL. Математический анализ трабекулярных «траекторий» в видимых траекторных структурах: неудачный исторический акцент на проксимальном отделе бедренной кости человека.Журнал J Theor Biol 2007; 244 (1): 15–45. [PubMed] [Google Scholar] 89. Бек TJ, Ruff CB, Warden KE, Scott WW, Jr, Rao GU. Прогнозирование прочности шейки бедра на основе данных о минералах костей: структурный подход. Инвест Радиол 1990; 25 (1): 6–18. [PubMed] [Google Scholar] 90. Кристофолини Л., Висконти М., Каппелло А., Тони А. Механическая проверка композитных моделей бедренной кости из цельной кости. J Biomech 1996; 29 (4): 525–535. [PubMed] [Google Scholar] 91. Pramudito JT, Soegijoko S, Mengko TR, Muchtadi FI, Wachjudi RG. Анализ трабекулярных паттернов на рентгенограммах проксимального отдела бедренной кости для выявления остеопороза.J Biomed Pharm Eng 2007; 1 (1): 45–51. [Google Scholar] 92. Чан И.Г., Ким И.Ю. Вычислительное исследование закона Вольфа с трабекулярной архитектурой проксимального отдела бедренной кости человека с использованием оптимизации топологии. J Biomech 2008; 41 (11): 2353–2361. [PubMed] [Google Scholar] 93. Картер Д.Р., Орр Т.Э., Фихри Д.П. Связь между историей нагружения и архитектурой губчатой кости бедренной кости. Дж. Биомех 1989; 22 (3): 231–244. [PubMed] [Google Scholar] 94. Deutsch AL, Mink JH, Shellock FG. Магнитно-резонансная томография повреждений костей и суставных хрящей: акцент на рентгенологически скрытых аномалиях.Ортоп Рев 1990; 19 (1): 66–75. [PubMed] [Google Scholar] 95. Мерфи Б.Дж., Смит Р.Л., Урибе Дж.В., Янеки С.Дж., Хехтман К.С., Мангасарян Р.А. Аномалии костного сигнала в задне-боковой большеберцовой кости и латеральном мыщелке бедренной кости при полном разрыве передней крестообразной связки: конкретный признак? Радиология 1992; 182 (1): 221–224. [PubMed] [Google Scholar] 96. Cox LG, Lagemaat MW, van Donkelaar CC и др. . Роль жидкости под давлением в росте кисты субхондральной кости. Кость 2011; 49 (4): 762–768. [PubMed] [Google Scholar] 97.Rangger C, Kathrein A, Freund MC, Klestil T, Kreczy A. Костный ушиб колена: гистология и криосрезы в 5 случаях. Acta Orthop Scand 1998; 69 (3): 291–294. [PubMed] [Google Scholar] 98. Wong A, Grando H, Fliszar E, Pathria M, Chang EY, Resnick D. Интрамедуллярные жировые глобулы, связанные с травмой кости: новое открытие МРТ. Скелетная радиология 2014; 43 (12): 1713–1719. [PubMed] [Google Scholar] 100. Гупта Х.С., Зиупос П. Перелом костной ткани: «как» и «почему». Med Eng Phys 2008; 30 (10): 1209–1226.[PubMed] [Google Scholar] 101. Добларе М., Гарсия Дж. М., Гомес М. Дж. Моделирование (sic) перелома и заживления костной ткани: обзор. Eng Fract Mech 2004; 71 (13-14): 1809–1840. [Google Scholar] 102. Бэ В.К., Чен ПК, Чунг С.Б., Масуда К., Д’Лима Д., Ду Дж. Количественная МРТ с ультракоротким временем эхо-сигнала (UTE) кортикальной кости человека: корреляция с пористостью и биомеханическими свойствами. Журнал J Bone Miner Res 2012; 27 (4): 848–857. [Бесплатная статья PMC] [PubMed] [Google Scholar] 103. Burr DB, Schaffler MB, Frederickson RG. Состав цементной линии и ее возможная механическая роль в качестве локального интерфейса в компактной кости человека.Дж. Биомех 1988; 21 (11): 939–945. [PubMed] [Google Scholar] 104. Скедрос Дж. Г., Холмс Дж. Л., Вайда Э. Г., Блубаум Р. Д.. Цементные линии вторичных остеонов в кости человека не страдают дефицитом минералов: новые данные в исторической перспективе. Anat Rec A Discov Mol Cell Evol Biol 2005; 286 (1): 781–803. [PubMed] [Google Scholar] 105. Steiniche T, Hauge EM. Нормальное строение и функция костей. В: An YH, Martin KL, ред. Справочник по методам гистологии костей и хрящей. Тотова, Нью-Джерси: Humana, 2003; 59–72. [Google Scholar] 106.Ричи Р.О., Кинни Дж.Х., Крузич Дж.Дж., Налла Р.К. Механика перелома и механистический подход к разрушению кортикальной кости. Fatigue Fract Engng Mater Struct 2005; 28 (4): 345–371. [Google Scholar] 107. Ричи Р.О., Бюлер М.Дж., Хансма П. Пластичность и прочность кости. Phys Today 2009; 62 (6): 41–46. [Google Scholar] 108. Лони М.Э., Бюлер М.Дж., Ричи Р.О. О механистических источниках прочности кости. Annu Rev Mater Res 2010; 40: 25–53. [Google Scholar] 109. Кестер KJ, Ager JW, 3-е место, Ричи RO. Истинная прочность кортикальной кости человека, измеренная по реально коротким трещинам.Nat Mater 2008; 7 (8): 672–677. [PubMed] [Google Scholar] 110. Fratzl P. Перелом костей: когда начинают проявляться трещины. Nat Mater 2008; 7 (8): 610–612. [PubMed] [Google Scholar] 111. Пеграм Дж., Крисп Т., Падиар Н. Диагностика и лечение травм нижних конечностей от напряжения костей у спортсменов. BMJ 2012; 344 (7854): e2511. [PubMed] [Google Scholar] 112. Seeman E, Delmas PD. Качество костей: материальная и структурная основа прочности и хрупкости костей. N Engl J Med 2006; 354 (21): 2250–2261. [PubMed] [Google Scholar] 113.Уманс Х.Р., Кэй Дж.Дж. Продольные стрессовые переломы большеберцовой кости: диагностика с помощью магнитно-резонансной томографии. Скелетная радиология 1996; 25 (4): 319–324. [PubMed] [Google Scholar] 114. Уильямс М., Ларедо Дж. Д., Сетбон С. и др. . Необычные продольные стресс-переломы диафиза бедренной кости: отчет о пяти случаях. Скелетная радиология 1999; 28 (2): 81–85. [PubMed] [Google Scholar] 115. Craig JG, Widman D, van Holsbeeck M. Продольный стресс-перелом: характер отека и важность питательного отверстия. Скелетная радиология 2003; 32 (1): 22–27.[PubMed] [Google Scholar] 116. Pathria MN. Радиологический анализ травмы. В: Naham A, Melvin JW, ред. Случайная травма: биомеханика и профилактика. 2-е изд. Нью-Йорк, штат Нью-Йорк: Springer-Verlag, 2001; 103–120. [Google Scholar] 117. Роджерс Л.Ф. Скелетная биомеханика. В: Роджерс Л.Ф., изд. Радиология травм скелета. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон, 1992; 19–28. [Google Scholar] 118. Андерсон М.В., Гринспен А. Стресс-переломы. Радиология 1996; 199 (1): 1–12. [PubMed] [Google Scholar] 119. Бек Б.Р., Бергман А.Г., Майнер М. и др.. Стрессовое повреждение большеберцовой кости: взаимосвязь рентгенографии, сканирования костей с помощью ядерной медицины, МРТ и КТ степени тяжести с клинической тяжестью и временем до заживления. Радиология 2012; 263 (3): 811–818. [PubMed] [Google Scholar] 120. Пеппер М., Акутота В., Маккарти Э. Патофизиология стрессовых переломов. Clin Sports Med 2006; 25 (1): 1–16, vii. [PubMed] [Google Scholar] 121. Burghardt AJ, Link TM, Majumdar S. Компьютерная томография высокого разрешения для клинической визуализации микроархитектуры кости. Clin Orthop Relat Res 2011; 469 (8): 2179–2193.[Бесплатная статья PMC] [PubMed] [Google Scholar] 122. Ямамото Т., Буллоу П.Г. Спонтанный остеонекроз коленного сустава: результат перелома субхондральной недостаточности. J Bone Joint Surg Am 2000; 82 (6): 858–866. [PubMed] [Google Scholar] 123. Попп К.Л., Хьюз Дж. М., Смок А. Дж. И др. . Геометрия, сила и размер костей у бегунов с историей стрессовых переломов. Med Sci Sports Exerc 2009; 41 (12): 2145–2150. [PubMed] [Google Scholar]
Тети А. Развитие костей: обзор костных клеток и передачи сигналов. Curr Osteoporos Rep 2011; 9 (4): 264–273. [PubMed] [Google Scholar] 13. Кобаяси С., Такахаши Х.Э., Ито А. и др. . Минимоделирование трабекул в подвздошной кости человека. Кость 2003; 32 (2): 163–169. [PubMed] [Google Scholar] 14. Убара Ю., Фусими Т., Тагами Т. и др. . Гистоморфометрические особенности кости у пациентов с первичным и вторичным гипопаратиреозом.Kidney Int 2003; 63 (5): 1809–1816. [PubMed] [Google Scholar] 15. Убара Ю., Тагами Т., Наканиши С. и др. . Значение минимоделирования у диализных пациентов с адинамической болезнью костей. Kidney Int 2005; 68 (2): 833–839. [PubMed] [Google Scholar] 16. Вольф Дж. Классика: о внутренней архитектуре костей и ее важности для роста костей. 1870. Clin Orthop Relat Res 2010; 468 (4): 1056–1065. [Бесплатная статья PMC] [PubMed] [Google Scholar] 17. Дункан Р.Л., Тернер С.Х. Механотрансдукция и функциональный ответ кости на механическое напряжение.Calcif Tissue Int 1995; 57 (5): 344–358. [PubMed] [Google Scholar] 18. Frost HM. A. Обновление физиологии костей и закона Вольфа для клиницистов в 2003 г. Угол Ортод 2004; 74 (1): 3–15. [PubMed] [Google Scholar] 19. Чапурлат Р.Д., Дельмас П.Д. Микроповреждения костей: клиническая перспектива. Остеопорос Инт 2009; 20 (8): 1299–1308. [PubMed] [Google Scholar] 21. Отт С.М. Гистоморфометрический анализ ремоделирования кости. В: Билезикян Дж. П., Райс Л. Г., Родан Г. А., ред. Принципы костной биологии. Сан-Диего, Калифорния: Academic Press, 2002; 303–319.[Google Scholar] 22. Эрнандес CJ, Beaupré GS, Carter DR. Модель механобиологических и метаболических влияний на адаптацию костей. J. Rehabil Res Dev 2000; 37 (2): 235–244. [PubMed] [Google Scholar] 23. Odvina CV, Zerwekh JE, Rao DS, Maalouf N, Gottschalk FA, Pak CY. Сильно подавленный метаболизм костной ткани: потенциальное осложнение терапии алендронатом. J Clin Endocrinol Metab 2005; 90 (3): 1294–1301. [PubMed] [Google Scholar] 24. Goh SK, Yang KY, Koh JS, et al. . Подвертельная недостаточность переломов у пациентов, получающих алендронат: с осторожностью.J Bone Joint Surg Br 2007; 89 (3): 349–353. [PubMed] [Google Scholar] 25. Benjamin M, Toumi H, Ralphs JR, Bydder G, Best TM, Milz S. Место соединения сухожилий и связок с костью: места прикрепления («энтезы») в зависимости от упражнений и / или механической нагрузки. Журнал Анат 2006; 208 (4): 471–490. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26. Дэвисон К.С., Симиноски К., Адачи Дж. Д. и др. . Сила костей: целое больше, чем сумма его частей. Semin Arthritis Rheum 2006; 36 (1): 22–31. [PubMed] [Google Scholar] 27.Oxlund H, Mosekilde L, Ortoft G. Снижение концентрации восстанавливаемых коллагеном поперечных связей в губчатой кости человека с учетом возраста и остеопороза. Кость 1996; 19 (5): 479–484. [PubMed] [Google Scholar] 28. Boivin G, Meunier PJ. Степень минерализации костной ткани измеряется компьютерной количественной контактной микрорентгенографией. Calcif Tissue Int 2002; 70 (6): 503–511. [PubMed] [Google Scholar] 29. Currey JD, Brear K, Zioupos P. Эффекты старения и изменения содержания минералов в снижении прочности бедер человека.J Biomech 1996; 29 (2): 257–260. [PubMed] [Google Scholar] 30. Риггс Б.Л., Ходжсон С.Ф., О’Фаллон В.М. и др. . Влияние лечения фтором на частоту переломов у женщин в постменопаузе с остеопорозом. N Engl J Med 1990; 322 (12): 802–809. [PubMed] [Google Scholar] 31. Фриман Дж. Дж., Вопенка Б., Сильва М. Дж., Пастерис Дж. Д.. Рамановское спектроскопическое обнаружение изменений биоапатита в бедрах мышей в зависимости от возраста и лечения фторидом in vitro. Calcif Tissue Int 2001; 68 (3): 156–162. [PubMed] [Google Scholar] 32. Хубер М., Траттниг С., Линтнер Ф.Анатомия, биохимия и физиология суставного хряща. Инвест Радиол 2000; 35 (10): 573–580. [PubMed] [Google Scholar] 33. Фриман П.М., Натараджан Р.Н., Кимура Дж. Х., Андриакчи Т.П. Клетки хондроцитов механически реагируют на сжимающие нагрузки. J Orthop Res 1994; 12 (3): 311–320. [PubMed] [Google Scholar] 34. Glaser C, Putz R. Функциональная анатомия суставного хряща при сжимающей нагрузке: количественные аспекты глобальных, локальных и зональных реакций коллагеновой сети в отношении целостности поверхности.Хрящевой остеоартрит 2002; 10 (2): 83–99. [PubMed] [Google Scholar] 35. Вайс С., Розенберг Л., Хелфет А.Дж. Ультраструктурное исследование нормального суставного хряща молодого взрослого человека. J Bone Joint Surg Am 1968; 50 (4): 663–674. [PubMed] [Google Scholar] 37. Нордин М., Франкель В.Х. Биомеханика кости. В: Нордин М., Франкель В.Х., ред. Базовая биомеханика опорно-двигательного аппарата. 2-е изд. Балтимор, Мэриленд: Липпинкотт Уильямс и Уилкинс, 2001; 26–59. [Google Scholar] 39. Dempster DW. Микроархитектура и прочность костей.Osteoporos Int 2003; 14 (Приложение 5): S54 – S56. [PubMed] [Google Scholar] 40. Ширази Р., Ширази-Адл А., Хуртиг М. Роль сетей коллагеновых фибрилл хряща в биомеханике коленного сустава при сжатии. J Biomech 2008; 41 (16): 3340–3348. [PubMed] [Google Scholar] 41. Линн Ф.К., Соколов Л. Движение и состав интерстициальной жидкости хряща. Arthritis Rheum 1965; 8: 481–494. [PubMed] [Google Scholar] 42. Моу В.К., Холмс М.Х., Лай В.М. Транспорт жидкости и механические свойства суставного хряща: обзор.Дж. Биомех 1984; 17 (5): 377–394. [PubMed] [Google Scholar] 43. Ароен А., Лёкен С., Наследник С. и др. . Поражения суставного хряща при 993 последовательных артроскопиях коленного сустава. Am J Sports Med 2004; 32 (1): 211–215. [PubMed] [Google Scholar] 44. Hjelle K, Solheim E, Strand T, Muri R, Brittberg M. Дефекты суставного хряща при артроскопии 1000 коленного сустава. Артроскопия 2002; 18 (7): 730–734. [PubMed] [Google Scholar] 45. Curl WW, Krome J, Gordon ES, Rushing J, Smith BP, Poehling GG. Повреждения хряща: обзор 31 516 артроскопий коленного сустава.Артроскопия 1997; 13 (4): 456–460. [PubMed] [Google Scholar] 46. Моу В.К., Чжу В., Рэтклифф А. Структура и функция суставного хряща и мениска. В: Mow VC, Hayes WC, eds. Основы ортопедической биомеханики. Нью-Йорк, Нью-Йорк: Рэйвен, 1991; 143–198. [Google Scholar] 47. Фермер Дж. М., Мартин Д. Ф., Болес, Калифорния, Керл, WW. Хондральные и костно-хрящевые травмы. Диагностика и лечение. Clin Sports Med 2001; 20 (2): 299–320. [PubMed] [Google Scholar] 48. Боррелли Дж. Младший, Риччи ВМ. Острые последствия воздействия на хрящи. Clin Orthop Relat Res 2004; (423): 33–39.[PubMed] [Google Scholar] 49. Бэ WC, Льюис CW, Левенстон, штат Мэн, Южная Африка. Тестирование вдавливания суставного хряща человека: влияние геометрии наконечника зонда и глубины вдавливания на деформацию внутри ткани. J Biomech 2006; 39 (6): 1039–1047. [PubMed] [Google Scholar] 50. Моу В.К., Куэй СК, Лай В.М., Армстронг К.Г. Двухфазная ползучесть и расслабление суставного хряща при сжатии? Теория и эксперименты. J Biomech Eng 1980; 102 (1): 73–84. [PubMed] [Google Scholar] 51. Франк EH, Grodzinsky AJ. Электромеханика хряща.II. Континуальная модель электрокинетики хряща и корреляция с экспериментами. J. Biomech, 1987; 20 (6): 629–639. [PubMed] [Google Scholar] 52. Эверс BJ, Jayaraman VM, Banglmaier RF, Haut RC. Скорость тупой ударной нагрузки влияет на изменения ретропателлярного хряща и подлежащей кости надколенника кролика. J Biomech 2002; 35 (6): 747–755. [PubMed] [Google Scholar] 53. Галло Р.А., Мошер Т.Дж. Визуализация повреждений хряща и костно-хрящевой ткани: обзор конкретных случаев. Clin Sports Med 2013; 32 (3): 477–505. [PubMed] [Google Scholar] 54.Loening AM, James IE, Levenston ME, et al. . Повреждающее механическое сжатие суставного хряща крупного рогатого скота вызывает апоптоз хондроцитов. Arch Biochem Biophys 2000; 381 (2): 205–212. [PubMed] [Google Scholar] 55. Д’Лима Д.Д., Хашимото С., Чен П.С., Колвелл К.В., младший, Лотц М.К. Апоптоз хондроцитов человека в ответ на механическое повреждение. Хрящевой остеоартрит 2001; 9 (8): 712–719. [PubMed] [Google Scholar] 56. Курц Б., Джин М., Патвари П., Ченг Д.М., Ларк М.В., Гродзинский А.Дж. Биосинтетический ответ и механические свойства суставного хряща после травматической компрессии.J Orthop Res 2001; 19 (6): 1140–1146. [PubMed] [Google Scholar] 57. Клементс К.М., Би З.С., Кроссингем Г.В., Адамс М.А., Шариф М. Насколько серьезной должна быть повторяющаяся нагрузка, чтобы убить хондроциты в суставном хряще? Хрящевой остеоартрит 2001; 9 (5): 499–507. [PubMed] [Google Scholar] 58. Quinn TM, Allen RG, Schalet BJ, Perumbuli P, Hunziker EB. Повреждение матрикса и клеток из-за субударной нагрузки эксплантатов суставного хряща взрослого крупного рогатого скота: влияние скорости деформации и пикового напряжения. J Orthop Res 2001; 19 (2): 242–249.[PubMed] [Google Scholar] 59. Патвари П., Гашен В., Джеймс И. Е. и др. . Ультраструктурная количественная оценка гибели клеток после травматического сжатия суставного хряща теленка крупного рогатого скота. Хрящевой остеоартрит 2004; 12 (3): 245–252. [Бесплатная статья PMC] [PubMed] [Google Scholar] 60. Дуда Г. Н., Эйлерс М., Лох Л., Хоффман Дж. Э., Кеб М., Шейзер К. Смерть хондроцитов предшествует структурному повреждению при травме от тупого удара. Clin Orthop Relat Res 2001; (393): 302–309. [PubMed] [Google Scholar] 61. Чен К. Т., Бхаргава М., Лин П. М., Торзилли ПА.Гибель хондроцитов и повреждение коллагена в циклически нагруженном суставном хряще зависят от времени, стресса и местоположения. J Orthop Res 2003; 21 (5): 888–898. [PubMed] [Google Scholar] 62. Ли X, Куо Д., Теологис А. и др. . Хрящ в коленях, реконструированных с помощью передней крестообразной связки: МРТ T1rho и T2 — первоначальный опыт с последующим наблюдением в течение 1 года. Радиология 2011; 258 (2): 505–514. [Бесплатная статья PMC] [PubMed] [Google Scholar] 63. Potter HG, Jain SK, Ma Y, Black BR, Fung S, Lyman S. Повреждение хряща после острого изолированного разрыва передней крестообразной связки: немедленный и продольный эффект с последующим клиническим наблюдением / МРТ.Am J Sports Med 2012; 40 (2): 276–285. [PubMed] [Google Scholar] 64. Tiderius CJ, Olsson LE, Nyquist F, Dahlberg L. Потеря гликозаминогликанов хряща в острой фазе после повреждения передней крестообразной связки: отсроченная магнитно-резонансная томография хряща с усилением гадолиния и анализ синовиальной жидкости. Arthritis Rheum 2005; 52 (1): 120–127. [PubMed] [Google Scholar] 65. Томацу Т., Имаи Н., Такеучи Н., Такахаши К., Кимура Н. Экспериментально полученные переломы суставного хряща и кости: влияние сил сдвига на колено свиньи.J Bone Joint Surg Br 1992; 74 (3): 457–462. [PubMed] [Google Scholar] 66. Mosher TJ. МРТ костно-хрящевых повреждений колена и голеностопа у спортсмена. Clin Sports Med 2006; 25 (4): 843–866. [PubMed] [Google Scholar] 67. Аутербридж RE. Этиология хондромаляции надколенника. J Bone Joint Surg Br 1961; 43-B: 752–757. [PubMed] [Google Scholar] 68. Нойес Ф. Р., Бассет Р. В., Груд Е. С., Батлер Д. Л.. Артроскопия при остром травматическом гемартрозе коленного сустава: частота передних крестообразных разрывов и других травм. J Bone Joint Surg Am 1980; 62 (5): 687–695, 757.[PubMed] [Google Scholar] 69. Кэмерон М.Л., Бриггс К.К., Стедман-младший. Воспроизводимость и надежность классификации внешнего моста для артроскопической классификации хондральных поражений коленного сустава. Am J Sports Med 2003; 31 (1): 83–86. [PubMed] [Google Scholar] 70. Бриттберг М. Оценка повреждений хряща и восстановление хряща. Osteologie 2000; 9: 17–25. [Google Scholar] 71. Бриттберг М, Винальски К.С. Оценка повреждений и ремонта хрящей. J Bone Joint Surg Am 2003; 85-A (Приложение 2): 58–69. [PubMed] [Google Scholar] 72.Кийовски Р., Бланкенбейкер Д.Г., Дэвис К.В., Шинки К., Каплан Л.Д., Де Смет А.А. Сравнение магнитно-резонансной томографии 1,5 и 3,0 Тл для оценки суставного хряща коленного сустава. Радиология 2009; 250 (3): 839–848. [PubMed] [Google Scholar] 73. Бределла М.А., Тирман П.Ф., Петерфи К.Г. и др. . Точность Т2-взвешенного быстрого спин-эхо МРТ с насыщением жира при обнаружении дефектов хряща в колене: сравнение с артроскопией у 130 пациентов. AJR Am J Roentgenol 1999; 172 (4): 1073–1080. [PubMed] [Google Scholar] 74.Петерфи К.Г., Гермази А., Заим С. и др. . Оценка всего органа с помощью магнитно-резонансной томографии (WORMS) колена при остеоартрите. Хрящевой остеоартрит 2004; 12 (3): 177–190. [PubMed] [Google Scholar] 76. Голд Г.Е., Бурштейн Д., Дарзински Б., Ланг П., Боада Ф., Мошер Т. МРТ суставного хряща при ОА: новые импульсные последовательности и композиционные / функциональные маркеры. Остеоартрозный хрящ 2006; 14 (Приложение A): A76 – A86. [PubMed] [Google Scholar] 77. Уильямс А., Гиллис А., Маккензи С. и др. . Распределение гликозаминогликанов в хрящах, определенное с помощью отсроченной МРТ хряща с усилением гадолиния (dGEMRIC): потенциальные клинические применения.AJR Am J Roentgenol 2004; 182 (1): 167–172. [PubMed] [Google Scholar] 78. Уитон AJ, Dodge GR, Borthakur A, Kneeland JB, Schumacher HR, Reddy R. Выявление изменений протеогликана суставного хряща с помощью магнитно-резонансной томографии T (1rho). J Orthop Res 2005; 23 (1): 102–108. [Бесплатная статья PMC] [PubMed] [Google Scholar] 79. Xia Y, Moody JB, Burton-Wurster N, Lust G. Количественная корреляция in situ между исследованиями суставного хряща с помощью микроскопической МРТ и микроскопии поляризованного света. Хрящевой остеоартрит 2001; 9 (5): 393–406.[PubMed] [Google Scholar] 80. Мадри Х., ван Дейк К.Н., Мюллер-Гербль М. Основы науки о субхондральной кости. Коленная хирургия Sports Traumatol Arthrosc 2010; 18 (4): 419–433. [PubMed] [Google Scholar] 81. Радин Е.Л., Роза Р.М. Роль субхондральной кости в инициации и прогрессировании повреждения хряща. Clin Orthop Relat Res 1986; (213): 34–40. [PubMed] [Google Scholar] 82. Херт Дж. Новая попытка интерпретации функциональной архитектуры губчатой кости. Дж. Биомех 1994; 27 (2): 239–242. [PubMed] [Google Scholar] 83.Барак М.М., Либерман Д.Е., Хублин Дж. Дж. Вольф в овечьей шкуре: адаптация губчатой кости в ответ на изменение ориентации суставной нагрузки. Кость 2011; 49 (6): 1141–1151. [PubMed] [Google Scholar] 84. Ланьон LE. Анализ деформации поверхности пяточной кости овцы при нормальном движении: анализ деформации пяточной кости. J Biomech 1973; 6 (1): 41–49. [PubMed] [Google Scholar] 85. Ланьон LE. Экспериментальное подтверждение траекторной теории строения кости. J Bone Joint Surg Br 1974; 56 (1): 160–166.[PubMed] [Google Scholar] 86. Бувье М. Применение методов измерения деформации костей in vivo для решения проблем адаптации скелета. Am J Phys Anthropol 1985; 28 (Приложение 6): 237–248. [Google Scholar] 87. Su SC, Skedros JG, Bachus KN, Bloebaum RD. Условия нагружения и конструкция кортикальной кости парнокопытной пяточной кости. J Exp Biol 1999; 202 (Pt 22): 3239–3254. [PubMed] [Google Scholar] 88. Скедрос JG, Baucom SL. Математический анализ трабекулярных «траекторий» в видимых траекторных структурах: неудачный исторический акцент на проксимальном отделе бедренной кости человека.Журнал J Theor Biol 2007; 244 (1): 15–45. [PubMed] [Google Scholar] 89. Бек TJ, Ruff CB, Warden KE, Scott WW, Jr, Rao GU. Прогнозирование прочности шейки бедра на основе данных о минералах костей: структурный подход. Инвест Радиол 1990; 25 (1): 6–18. [PubMed] [Google Scholar] 90. Кристофолини Л., Висконти М., Каппелло А., Тони А. Механическая проверка композитных моделей бедренной кости из цельной кости. J Biomech 1996; 29 (4): 525–535. [PubMed] [Google Scholar] 91. Pramudito JT, Soegijoko S, Mengko TR, Muchtadi FI, Wachjudi RG. Анализ трабекулярных паттернов на рентгенограммах проксимального отдела бедренной кости для выявления остеопороза.J Biomed Pharm Eng 2007; 1 (1): 45–51. [Google Scholar] 92. Чан И.Г., Ким И.Ю. Вычислительное исследование закона Вольфа с трабекулярной архитектурой проксимального отдела бедренной кости человека с использованием оптимизации топологии. J Biomech 2008; 41 (11): 2353–2361. [PubMed] [Google Scholar] 93. Картер Д.Р., Орр Т.Э., Фихри Д.П. Связь между историей нагружения и архитектурой губчатой кости бедренной кости. Дж. Биомех 1989; 22 (3): 231–244. [PubMed] [Google Scholar] 94. Deutsch AL, Mink JH, Shellock FG. Магнитно-резонансная томография повреждений костей и суставных хрящей: акцент на рентгенологически скрытых аномалиях.Ортоп Рев 1990; 19 (1): 66–75. [PubMed] [Google Scholar] 95. Мерфи Б.Дж., Смит Р.Л., Урибе Дж.В., Янеки С.Дж., Хехтман К.С., Мангасарян Р.А. Аномалии костного сигнала в задне-боковой большеберцовой кости и латеральном мыщелке бедренной кости при полном разрыве передней крестообразной связки: конкретный признак? Радиология 1992; 182 (1): 221–224. [PubMed] [Google Scholar] 96. Cox LG, Lagemaat MW, van Donkelaar CC и др. . Роль жидкости под давлением в росте кисты субхондральной кости. Кость 2011; 49 (4): 762–768. [PubMed] [Google Scholar] 97.Rangger C, Kathrein A, Freund MC, Klestil T, Kreczy A. Костный ушиб колена: гистология и криосрезы в 5 случаях. Acta Orthop Scand 1998; 69 (3): 291–294. [PubMed] [Google Scholar] 98. Wong A, Grando H, Fliszar E, Pathria M, Chang EY, Resnick D. Интрамедуллярные жировые глобулы, связанные с травмой кости: новое открытие МРТ. Скелетная радиология 2014; 43 (12): 1713–1719. [PubMed] [Google Scholar] 100. Гупта Х.С., Зиупос П. Перелом костной ткани: «как» и «почему». Med Eng Phys 2008; 30 (10): 1209–1226.[PubMed] [Google Scholar] 101. Добларе М., Гарсия Дж. М., Гомес М. Дж. Моделирование (sic) перелома и заживления костной ткани: обзор. Eng Fract Mech 2004; 71 (13-14): 1809–1840. [Google Scholar] 102. Бэ В.К., Чен ПК, Чунг С.Б., Масуда К., Д’Лима Д., Ду Дж. Количественная МРТ с ультракоротким временем эхо-сигнала (UTE) кортикальной кости человека: корреляция с пористостью и биомеханическими свойствами. Журнал J Bone Miner Res 2012; 27 (4): 848–857. [Бесплатная статья PMC] [PubMed] [Google Scholar] 103. Burr DB, Schaffler MB, Frederickson RG. Состав цементной линии и ее возможная механическая роль в качестве локального интерфейса в компактной кости человека.Дж. Биомех 1988; 21 (11): 939–945. [PubMed] [Google Scholar] 104. Скедрос Дж. Г., Холмс Дж. Л., Вайда Э. Г., Блубаум Р. Д.. Цементные линии вторичных остеонов в кости человека не страдают дефицитом минералов: новые данные в исторической перспективе. Anat Rec A Discov Mol Cell Evol Biol 2005; 286 (1): 781–803. [PubMed] [Google Scholar] 105. Steiniche T, Hauge EM. Нормальное строение и функция костей. В: An YH, Martin KL, ред. Справочник по методам гистологии костей и хрящей. Тотова, Нью-Джерси: Humana, 2003; 59–72. [Google Scholar] 106.Ричи Р.О., Кинни Дж.Х., Крузич Дж.Дж., Налла Р.К. Механика перелома и механистический подход к разрушению кортикальной кости. Fatigue Fract Engng Mater Struct 2005; 28 (4): 345–371. [Google Scholar] 107. Ричи Р.О., Бюлер М.Дж., Хансма П. Пластичность и прочность кости. Phys Today 2009; 62 (6): 41–46. [Google Scholar] 108. Лони М.Э., Бюлер М.Дж., Ричи Р.О. О механистических источниках прочности кости. Annu Rev Mater Res 2010; 40: 25–53. [Google Scholar] 109. Кестер KJ, Ager JW, 3-е место, Ричи RO. Истинная прочность кортикальной кости человека, измеренная по реально коротким трещинам.Nat Mater 2008; 7 (8): 672–677. [PubMed] [Google Scholar] 110. Fratzl P. Перелом костей: когда начинают проявляться трещины. Nat Mater 2008; 7 (8): 610–612. [PubMed] [Google Scholar] 111. Пеграм Дж., Крисп Т., Падиар Н. Диагностика и лечение травм нижних конечностей от напряжения костей у спортсменов. BMJ 2012; 344 (7854): e2511. [PubMed] [Google Scholar] 112. Seeman E, Delmas PD. Качество костей: материальная и структурная основа прочности и хрупкости костей. N Engl J Med 2006; 354 (21): 2250–2261. [PubMed] [Google Scholar] 113.Уманс Х.Р., Кэй Дж.Дж. Продольные стрессовые переломы большеберцовой кости: диагностика с помощью магнитно-резонансной томографии. Скелетная радиология 1996; 25 (4): 319–324. [PubMed] [Google Scholar] 114. Уильямс М., Ларедо Дж. Д., Сетбон С. и др. . Необычные продольные стресс-переломы диафиза бедренной кости: отчет о пяти случаях. Скелетная радиология 1999; 28 (2): 81–85. [PubMed] [Google Scholar] 115. Craig JG, Widman D, van Holsbeeck M. Продольный стресс-перелом: характер отека и важность питательного отверстия. Скелетная радиология 2003; 32 (1): 22–27.[PubMed] [Google Scholar] 116. Pathria MN. Радиологический анализ травмы. В: Naham A, Melvin JW, ред. Случайная травма: биомеханика и профилактика. 2-е изд. Нью-Йорк, штат Нью-Йорк: Springer-Verlag, 2001; 103–120. [Google Scholar] 117. Роджерс Л.Ф. Скелетная биомеханика. В: Роджерс Л.Ф., изд. Радиология травм скелета. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон, 1992; 19–28. [Google Scholar] 118. Андерсон М.В., Гринспен А. Стресс-переломы. Радиология 1996; 199 (1): 1–12. [PubMed] [Google Scholar] 119. Бек Б.Р., Бергман А.Г., Майнер М. и др.. Стрессовое повреждение большеберцовой кости: взаимосвязь рентгенографии, сканирования костей с помощью ядерной медицины, МРТ и КТ степени тяжести с клинической тяжестью и временем до заживления. Радиология 2012; 263 (3): 811–818. [PubMed] [Google Scholar] 120. Пеппер М., Акутота В., Маккарти Э. Патофизиология стрессовых переломов. Clin Sports Med 2006; 25 (1): 1–16, vii. [PubMed] [Google Scholar] 121. Burghardt AJ, Link TM, Majumdar S. Компьютерная томография высокого разрешения для клинической визуализации микроархитектуры кости. Clin Orthop Relat Res 2011; 469 (8): 2179–2193.[Бесплатная статья PMC] [PubMed] [Google Scholar] 122. Ямамото Т., Буллоу П.Г. Спонтанный остеонекроз коленного сустава: результат перелома субхондральной недостаточности. J Bone Joint Surg Am 2000; 82 (6): 858–866. [PubMed] [Google Scholar] 123. Попп К.Л., Хьюз Дж. М., Смок А. Дж. И др. . Геометрия, сила и размер костей у бегунов с историей стрессовых переломов. Med Sci Sports Exerc 2009; 41 (12): 2145–2150. [PubMed] [Google Scholar]Анатомия и физиология нормальной кости
Clin J Am Soc Nephrol.2008 ноя; 3 (Дополнение 3): S131 – S139.
Барт Кларк
Отделение эндокринологии, диабета, метаболизма и питания, Клиника Мэйо, Рочестер, Миннесота
Отделение эндокринологии, диабета, метаболизма и питания, Клиника Майо, Рочестер, Миннесота
Адрес для корреспонденции: Барт Кларк, отдел эндокринологии, диабета, метаболизма и питания, клиника Мэйо, W18-A, 200 1st Street SW, Rochester, MN 55905; Телефон: 507-266-4322; Факс: 507-284-5745; Электронная почта удэ[email protected] Авторские права © 2008 Американского общества нефрологов Эта статья цитируется в других статьях в PMC.Abstract
Этот обзор описывает анатомию и физиологию нормальной кости как введение к последующим статьям в этом разделе, в которых обсуждаются клинические применения биопсии гребня подвздошной кости. Сначала рассматриваются нормальная анатомия и функции скелета, после чего дается общее описание процессов моделирования и ремоделирования костей. Процесс ремоделирования кости регулирует увеличение и уменьшение минеральной плотности костной ткани в скелете взрослого человека и напрямую влияет на прочность кости.Тщательное понимание процесса ремоделирования кости имеет решающее значение для оценки ценности и интерпретации результатов гистоморфометрии гребня подвздошной кости. Рекрутирование, активация и резорбция остеокластов обсуждается довольно подробно с последующим обзором рекрутирования остеобластов и процесса образования новой кости. Затем суммируются коллагеновые и неколлагеновые белковые компоненты и функция внеклеточного матрикса кости, после чего дается описание процесса минерализации вновь образованного костного матрикса.Воздействие биомеханических сил на кость воспринимается синцитием остеоцитов в кости через канальцевую сеть и межклеточные щелевые соединения. Наконец, концепции, касающиеся ремоделирования кости, функции остеокластов и остеобластов, внеклеточного матрикса, минерализации матрикса и функции остеоцитов, синтезируются в кратком изложении понятных в настоящее время функциональных детерминант прочности кости. Эта информация закладывает основу для понимания полезности и клинического применения биопсии гребня подвздошной кости.
Скелет
Скелет взрослого человека состоит всего из 213 костей, не считая сесамовидных костей (1). Аппендикулярный скелет состоит из 126 костей, осевого скелета — 74, а слуховых косточек — 6 костей. Каждая кость постоянно подвергается моделированию в течение жизни, чтобы помочь ей адаптироваться к изменяющимся биомеханическим силам, а также ремоделированию для удаления старой, микроповрежденной кости и замены ее новой, механически более прочной костью, чтобы помочь сохранить прочность кости.
Четыре основные категории костей: длинные, короткие, плоские и неправильные кости.Длинные кости включают ключицы, плечевые кости, радиусы, локтевые кости, пястные кости, бедренные кости, голени, малоберцовые кости, плюсневые кости и фаланги. Короткие кости включают запястные и предплюсневые кости, надколенники и сесамовидные кости. Плоские кости включают череп, нижнюю челюсть, лопатки, грудину и ребра. Кости неправильной формы включают позвонки, крестец, копчик и подъязычную кость. Плоские кости образуются за счет образования перепончатой кости, тогда как длинные кости образуются путем сочетания эндохондрального и перепончатого образования кости.
Каркас выполняет множество функций.Кости скелета обеспечивают структурную поддержку для остального тела, позволяют движение и передвижение, обеспечивая рычаги для мышц, защищают жизненно важные внутренние органы и структуры, обеспечивают поддержание минерального гомеостаза и кислотно-щелочного баланса, служат резервуаром для роста. факторов и цитокинов, а также обеспечивают среду для кроветворения в костном мозге (2).
Длинные кости состоят из полого стержня или диафиза; расширяющиеся конусообразные метафизы под пластинками роста; и округлые эпифизы над пластинками роста.Диафиз состоит в основном из плотной кортикальной кости, тогда как метафиз и эпифиз состоят из кости трабекулярной сети, окруженной относительно тонкой оболочкой из плотной кортикальной кости.
Скелет взрослого человека состоит из 80% кортикальной кости и 20% губчатой кости в целом (3). Различные кости и участки скелета внутри костей имеют разное соотношение кортикальной и губчатой кости. Позвонок состоит из кортикальной и губчатой кости в соотношении 25:75. Это соотношение составляет 50:50 в головке бедренной кости и 95: 5 в лучевом диафизе.
Кортикальная кость плотная и твердая и окружает костный мозг, тогда как губчатая кость состоит из сотовой сети трабекулярных пластин и стержней, вкрапленных в компартменте костного мозга. И кортикальная, и губчатая кость состоят из остеонов.
Кортикальные остеоны называются гаверсовыми системами. Гаверсовы системы имеют цилиндрическую форму, примерно 400 мм в длину и 200 мм в ширину в основании и образуют разветвленную сеть внутри кортикальной кости (3). Стены гаверсовских систем образованы концентрическими пластинками.Кортикальная кость обычно менее метаболически активна, чем губчатая кость, но это зависит от вида. У здоровых взрослых людей примерно 21 × 10 6 кортикальных остеонов с общей площадью ремоделирования по Гаверсу примерно 3,5 м 2 . Пористость кортикальной кости обычно составляет <5%, но это зависит от соотношения активно ремоделирующих гаверсовских систем и неактивных кортикальных остеонов. Увеличение кортикального ремоделирования вызывает увеличение кортикальной пористости и уменьшение корковой костной массы.Здоровые стареющие взрослые обычно испытывают истончение коры и увеличение пористости коры.
Кортикальная кость имеет внешнюю надкостничную поверхность и внутреннюю эндостальную поверхность. Поверхностная активность надкостницы важна для аппозиционного роста и заживления переломов. Костеобразование обычно превышает резорбцию кости на периостальной поверхности, поэтому кости обычно увеличиваются в диаметре с возрастом. Поверхность эндоста имеет общую площадь приблизительно 0,5 м 2 , с более высокой активностью ремоделирования, чем поверхность надкостницы, вероятно, в результате большего биомеханического напряжения или большего воздействия цитокинов из соседнего компартмента костного мозга.Резорбция кости обычно превышает образование кости на эндостальной поверхности, поэтому костный мозг обычно расширяется с возрастом.
Трабекулярные остеоны называются пакетами. Трабекулярная кость состоит из пластин и стержней толщиной от 50 до 400 мм (3). Трабекулярные остеоны имеют полулунную форму, обычно примерно 35 мм толщиной, и состоят из концентрических пластинок. Подсчитано, что у здоровых взрослых людей имеется 14 × 10 6 трабекулярных остеонов с общей площадью трабекулярной поверхности приблизительно 7 м 2 .
Кортикальная кость и губчатая кость обычно образуются пластинчатым узором, в котором коллагеновые фибриллы располагаются в чередующейся ориентации (3). Пластинчатая кость лучше всего видна при микроскопическом исследовании в поляризованном свете, во время которого виден пластинчатый узор в результате двойного лучепреломления. Механизм, с помощью которого остеобласты откладывают фибриллы коллагена в виде пластин, неизвестен, но пластинчатая кость имеет значительную прочность в результате чередования ориентаций фибрилл коллагена, как у фанеры.В тканой кости отсутствует нормальный пластинчатый узор, в котором коллагеновые фибриллы располагаются неорганизованным образом. Плетеная кость слабее пластинчатой. Плетеная кость обычно образуется во время образования первичной кости, а также может наблюдаться при состояниях с высоким метаболизмом костной ткани, таких как кистозный остеит, в результате гиперпаратиреоза и болезни Педжета, или во время высокого костеобразования во время раннего лечения фтором.
Надкостница — это волокнистая соединительнотканная оболочка, которая окружает внешнюю кортикальную поверхность кости, за исключением суставов, где кость выстлана суставным хрящом, который содержит кровеносные сосуды, нервные волокна, остеобласты и остеокласты.Надкостница плотно прикреплена к внешней кортикальной поверхности кости толстыми коллагеновыми волокнами, называемыми волокнами Шарпейса, которые проникают в подлежащую костную ткань. Эндост представляет собой мембранную структуру, покрывающую внутреннюю поверхность кортикальной кости, губчатой кости и каналы кровеносных сосудов (каналы Фолькмана), присутствующие в кости. Эндост находится в контакте с пространством костного мозга, губчатой костью и каналами кровеносных сосудов и содержит кровеносные сосуды, остеобласты и остеокласты.
Рост, моделирование и ремоделирование костей
Кость подвергается продольному и радиальному росту, моделированию и ремоделированию в течение жизни.Продольный и радиальный рост во время роста и развития происходит в детском и подростковом возрасте. Продольный рост происходит в пластинах роста, где хрящ разрастается в эпифизарной и метафизарной областях длинных костей, прежде чем впоследствии подвергнется минерализации с образованием первичной новой кости.
Моделирование — это процесс, с помощью которого кости изменяют свою общую форму в ответ на физиологические воздействия или механические силы, что приводит к постепенной адаптации скелета к силам, с которыми он сталкивается.Кости могут расширяться или изменять ось за счет удаления или добавления кости к соответствующим поверхностям за счет независимого действия остеобластов и остеокластов в ответ на биомеханические силы. Кости обычно расширяются с возрастом в ответ на надкостницу новой кости и эндостальную резорбцию старой кости. Закон Вольфа описывает наблюдение, что длинные кости меняют форму, чтобы приспособиться к действующим на них нагрузкам. Во время моделирования кости образование и резорбция кости не взаимосвязаны. Моделирование кости у взрослых происходит реже, чем ремоделирование (4).Моделирование может быть усилено при гипопаратиреозе (5), почечной остеодистрофии (6) или лечении анаболическими средствами (7).
Ремоделирование кости — это процесс обновления кости для поддержания прочности кости и минерального гомеостаза. Ремоделирование включает непрерывное удаление отдельных пакетов старой кости, замену этих пакетов вновь синтезированным белковым матриксом и последующую минерализацию матрицы с образованием новой кости. Процесс ремоделирования резорбирует старую кость и формирует новую кость, чтобы предотвратить накопление микроповреждений кости.Ремоделирование начинается до рождения и продолжается до смерти. Блок ремоделирования кости состоит из тесно связанной группы остеокластов и остеобластов, которые последовательно выполняют резорбцию старой кости и образование новой кости. Ремоделирование костей увеличивается у женщин в перименопаузе и в раннем постменопаузе, а затем замедляется с дальнейшим старением, но продолжается более быстрыми темпами, чем у женщин в пременопаузе. Считается, что ремоделирование костей у стареющих мужчин происходит умеренно.
Цикл ремоделирования состоит из четырех последовательных фаз.Активация предшествует резорбции, предшествующей обращению, предшествующей формированию. Сайты ремоделирования могут развиваться случайным образом, но также нацелены на участки, требующие ремонта (8,9). Считается, что сайты ремоделирования развиваются в основном случайным образом.
Активация включает привлечение и активацию мононуклеарных моноцитов-макрофагов-предшественников остеокластов из кровотока (10), отрыв эндоста, который содержит выстилающие клетки от поверхности кости, и слияние нескольких мононуклеарных клеток с образованием многоядерных преостеокластов.Преостеокласты связываются с костным матриксом посредством взаимодействий между рецепторами интегрина в их клеточных мембранах и RGD (аргинин, глицин и аспарагин) -содержащими пептидами в матричных белках с образованием кольцевых герметизирующих зон вокруг резорбируемых костью компартментов под многоядерными остеокластами.
Опосредованная остеокластами резорбция кости занимает всего около 2–4 недель в течение каждого цикла ремоделирования. Образование, активация и резорбция остеокластов регулируются соотношением активатора рецептора лиганда NF-κB (RANKL) к остеопротегерину (OPG;), IL-1 и IL-6, колониестимулирующему фактору (CSF), паратиреоидному гормону, 1 , 25-дигидроксивитамин D и кальцитонин (11,12).Резорбирующиеся остеокласты секретируют ионы водорода через протонные насосы H + -АТФазы и хлоридные каналы в своих клеточных мембранах в отсек резорбции, чтобы снизить pH внутри отсека резорбции кости до 4,5, что помогает мобилизовать минералы кости (13 ). Резорбирующиеся остеокласты выделяют устойчивую к тартрату кислую фосфатазу, катепсин К, матриксную металлопротеиназу 9 и желатиназу из цитоплазматических лизосом (14) для переваривания органического матрикса, в результате чего образуются блюдцеобразные лакуны Ховшипа на поверхности трабекулярной кости () и гаверсовских каналов. в кортикальном слое кости.Фаза резорбции завершается мононуклеарными клетками после того, как многоядерные остеокласты подвергаются апоптозу (15,16).
Регулирование остеокластогенеза с помощью активатора рецептора лиганда NF-κB (RANKL) и остеопротегерина (OPG): колониестимулирующий фактор 1 (CSF-1) обычно стимулирует рекрутирование остеокластов. Две формы RANKL продуцируются остеобластами и предшественниками остеобластов для стимуляции рекрутирования и активации остеокластов. Мембраносвязанная форма напрямую взаимодействует с мембраносвязанными молекулами RANK на соседних предшественниках остеокластов.Растворимая форма высвобождается из остеобластов или предшественников остеобластов, чтобы диффундировать через межклеточное пространство и взаимодействовать с мембраносвязанными молекулами RANK на соседних предшественниках остеокластов. OPG действует как ловушка-рецептор, предотвращая взаимодействие RANKL или sRANKL с RANK. Соотношение между RANKL и OPG, продуцируемыми остеобластами и предшественниками остеобластов, контролирует стимулированный RANKL остеокластогенез.
Многоядерные остеокласты рассасывают кость с образованием ямок для рассасывания, известных как лакуны Ховшипа.
Во время фазы обращения резорбция кости переходит в формирование кости. По завершении резорбции кости резорбционные полости содержат множество мононуклеарных клеток, включая моноциты, остеоциты, высвобождаемые из костного матрикса, и преостеобласты, привлекаемые для начала образования новой кости. Связанные сигналы, связывающие конец резорбции кости с началом образования кости, пока неизвестны. Предполагаемые кандидаты для связывающего сигнала включают факторы, производные от костного матрикса, такие как TGF-β, IGF-1, IGF-2, костные морфогенетические белки, PDGF или фактор роста фибробластов (17-19).Концентрация TGF-β в костном матриксе коррелирует с гистоморфометрическими показателями обновления костной ткани, а также с остеокальцином в сыворотке крови и костной специфической щелочной фосфатазой. TGF-β, высвобождаемый из костного матрикса, снижает резорбцию остеокластов за счет ингибирования продукции RANKL остеобластами. Было высказано предположение, что фаза обращения опосредуется градиентом деформации в лакунах (20,21). Поскольку остеокласты резорбируют кортикальный слой кости в режущем конусе, деформация уменьшается спереди и увеличивается сзади, а в лакунах Ховшипа деформация наиболее высока у основания и меньше — в окружающей кости по краям лакун.Градиент штамма может привести к последовательной активации остеокластов и остеобластов, при этом остеокласты активируются уменьшенным напряжением, а остеобласты — повышенным напряжением. Было высказано предположение, что сам остеокласт играет роль во время обращения (22).
Формирование кости занимает от 4 до 6 месяцев. Остеобласты синтезируют новый коллагеновый органический матрикс () и регулируют минерализацию матрикса, высвобождая небольшие мембраносвязанные матричные везикулы, которые концентрируют кальций и фосфат и ферментативно разрушают ингибиторы минерализации, такие как пирофосфат или протеогликаны (23).Остеобласты, окруженные матриксом и погребенные в нем, становятся остеоцитами с обширной канальцевой сетью, соединяющей их с клетками выстилки поверхности кости, остеобластами и другими остеоцитами, поддерживаемыми щелевыми соединениями между цитоплазматическими процессами, отходящими от остеоцитов (24). Сеть остеоцитов в кости служит функциональным синцитием. По завершении формирования кости примерно от 50 до 70% остеобластов подвергаются апоптозу, при этом остальная часть становится остеоцитами или клетками выстилки кости.Клетки, выстилающие костную ткань, могут регулировать приток и отток минеральных ионов в костную внеклеточную жидкость и из нее, тем самым выступая в качестве гемато-костного барьера, но сохраняя способность повторно дифференцироваться в остеобласты при воздействии паратиреоидного гормона или механических сил (25). Клетки, выстилающие костную ткань эндоста, отрываются от поверхности кости перед резорбцией кости, чтобы сформировать дискретные компартменты ремоделирования кости со специализированным микроокружением (26). У пациентов с множественной миеломой клетки выстилки могут быть индуцированы экспрессией устойчивой к тартрату кислой фосфатазы и других классических маркеров остеокластов.
Остеобласты синтезируют белковый матрикс, состоящий в основном из коллагена I типа, для заполнения ямок резорбции. Белковый матрикс постепенно минерализуется, образуя новую кость.
Конечным результатом каждого цикла ремоделирования кости является производство нового остеона. Процесс ремоделирования в кортикальной и губчатой кости по существу одинаков, при этом единицы ремоделирования кости в губчатой кости эквивалентны единицам ремоделирования кортикальной кости, разделенным пополам в продольном направлении (27). Костный баланс — это разница между резорбированной старой костью и новой сформированной костью.Баланс надкостницы умеренно положительный, тогда как балансы эндостальной и губчатой костей умеренно отрицательны, что приводит к истончению кортикального и трабекулярного слоев с возрастом. Эти относительные изменения происходят при эндостальной резорбции, опережающей периостальное образование.
Основные признанные функции ремоделирования кости включают сохранение механической прочности кости путем замены старой, микроповрежденной кости на более новую, более здоровую кость, а также гомеостаз кальция и фосфата. Относительно низкая скорость обновления кортикального слоя кости у взрослых, составляющая от 2 до 3% в год, достаточна для поддержания биомеханической прочности кости.Скорость обновления губчатой кости выше, чем требуется для поддержания механической прочности, что указывает на то, что обновление губчатой кости более важно для метаболизма минералов. Повышенная потребность в кальции или фосфоре может потребовать увеличения единиц ремоделирования кости, но во многих случаях эта потребность может быть удовлетворена за счет увеличения активности существующих остеокластов. Повышенная потребность в кальции и фосфоре скелета частично удовлетворяется за счет резорбции остеокластов и частично за счет притока и оттока неостеокластического кальция.Постоянная деятельность по ремоделированию кости обеспечивает непрерывное поступление вновь сформированной кости, которая имеет относительно низкое содержание минералов и способна легче обмениваться ионами с внеклеточной жидкостью. Единицы ремоделирования кости, по-видимому, в основном случайным образом распределены по скелету, но могут быть вызваны образованием микротрещин или апоптозом остеоцитов. Пространство ремоделирования кости представляет собой сумму всех активных единиц ремоделирования кости в скелете в данный момент времени.
Остеокласты
Остеокласты — единственные клетки, которые, как известно, способны резорбировать кость ().Активированные многоядерные остеокласты происходят из мононуклеарных клеток-предшественников моноцитарно-макрофагальной линии (11). Мононуклеарные клетки-предшественники моноцитов-макрофагов были идентифицированы в различных тканях, но считается, что клетки-предшественники моноцитов-макрофагов костного мозга дают начало большинству остеокластов.
RANKL и макрофагальный CSF (M-CSF) — два цитокина, которые имеют решающее значение для образования остеокластов. И RANKL, и M-CSF продуцируются в основном стромальными клетками костного мозга и остеобластами в мембраносвязанных и растворимых формах, а для остеокластогенеза необходимо присутствие стромальных клеток и остеобластов в костном мозге (28).RANKL принадлежит к суперсемейству TNF и имеет решающее значение для образования остеокластов. M-CSF необходим для пролиферации, выживания и дифференцировки предшественников остеокластов, а также для выживания остеокластов и перестройки цитоскелета, необходимых для резорбции кости. OPG представляет собой мембраносвязанный и секретируемый белок, который связывает RANKL с высоким сродством, чтобы ингибировать его действие на рецептор RANK (29).
Резорбция кости зависит от секреции остеокластами ионов водорода и фермента катепсина К. Ионы H + подкисляют отсек резорбции под остеокластами, растворяя минеральный компонент костного матрикса, тогда как катепсин К переваривает белковый матрикс, который в основном состоит из коллагена I типа (11).
Остеокласты связываются с костным матриксом через рецепторы интегрина в мембране остеокластов, связываясь с пептидами костного матрикса. Семейство β1 рецепторов интегрина в остеокластах связывается с коллагеном, фибронектином и ламинином, но основным рецептором интегрина, способствующим резорбции кости, является интегрин α v β 3 , который связывается с остеопонтином и костным сиалопротеином (30).
Связывание остеокластов с костным матриксом заставляет их поляризоваться, при этом на резорбирующей кость поверхности образуется взъерошенная граница, которая образуется, когда подкисленные везикулы, содержащие металлопротеиназы матрикса и катепсин К, транспортируются через микротрубочки для слияния с мембраной.Рифленая граница секретирует ионы H + через H + -АТФазные и хлоридные каналы и вызывает экзоцитоз катепсина К и других ферментов в подкисленных везикулах (31).
При контакте с костным матриксом фибриллярный актиновый цитоскелет остеокласта организуется в актиновое кольцо, которое способствует образованию зоны уплотнения по периферии прикрепления остеокласта к матрице. Зона уплотнения окружает и изолирует подкисленный отсек резорбции от окружающей поверхности кости (32).Нарушение взъерошенной границы или актинового кольца блокирует резорбцию кости. Активно резорбирующиеся остеокласты образуют подосомы, которые прикрепляются к костному матриксу, а не к фокальным спайкам, которые образуются большинством клеток. Подосомы состоят из актинового ядра, окруженного интегринами α v β 3 и ассоциированными белками цитоскелета.
Остеобласты
Остеопрогениторные клетки образуют и поддерживают остеобласты, которые синтезируют новый костный матрикс на костеобразующих поверхностях (), остеоциты внутри костного матрикса, поддерживающие структуру кости, и клетки защитной оболочки, покрывающие поверхность покоящейся кости.Внутри линии остеобластов субпопуляции клеток по-разному реагируют на различные гормональные, механические или цитокиновые сигналы. Остеобласты осевой и аппендикулярной кости по-разному реагируют на эти сигналы.
Самообновляющиеся плюрипотентные стволовые клетки дают начало клеткам-остеопрогениторам в различных тканях при правильных условиях окружающей среды. Костный мозг содержит небольшую популяцию мезенхимальных стволовых клеток, которые способны давать начало костной, хрящевой, жировой или волокнистой соединительной ткани, отличной от популяции гемопоэтических стволовых клеток, дающей начало клонам клеток крови (33).Клетки со свойствами, характерными для мезенхимальных стволовых клеток костного мозга взрослых, были выделены из периферической крови и пульпы зуба взрослых, а также из пуповинной крови плода, печени, крови и костного мозга. Также были идентифицированы мультипотенциальные миогенные клетки, которые способны дифференцироваться в кости, мышцы или адипоциты. Мезенхимные клетки, принадлежащие к одному фенотипу, могут дедифференцироваться во время пролиферации и развить другой фенотип, в зависимости от местной тканевой среды. Перициты кровеносных сосудов могут развить остеобластический фенотип во время дедифференцировки при определенных обстоятельствах (34).
Приверженность мезенхимальных стволовых клеток к клону остеобластов требует канонического пути Wnt / β-catenin и ассоциированных белков (35). Идентификация фенотипа с высокой костной массой, связанного с активирующими мутациями белка, связанного с рецепторами LDL 5, подчеркнула важность канонического пути Wnt / β-catenin в формировании паттерна эмбрионального скелета, развитии скелета плода и ремоделировании скелета взрослых (36,37). Система Wnt также важна в хондрогенезе и гематопоэзе и может быть стимулирующей или ингибирующей на разных стадиях дифференцировки остеобластов.
Сглаженные клетки выстилки кости считаются покоящимися остеобластами, которые образуют эндост на трабекулярной и эндостальной поверхностях и лежат в основе надкостницы на минерализованной поверхности. Остеобласты и клетки выстилки находятся в непосредственной близости и соединяются сращениями. Кадгерины — это кальций-зависимые трансмембранные белки, которые являются неотъемлемой частью адгезивных соединений и вместе с плотными контактами и десмосомами соединяют клетки вместе, связывая их цитоскелеты (38).
Предшественники остеобластов изменяют форму от веретеновидных остеопрогениторов до больших кубовидных дифференцированных остеобластов на поверхности костного матрикса после того, как преостеобласты перестают пролиферировать.Преостеобласты, которые находятся рядом с функционирующими остеобластами в модуле ремоделирования кости, обычно распознаются из-за экспрессии в них щелочной фосфатазы. Активные зрелые остеобласты, которые синтезируют костный матрикс, имеют большие ядра, увеличенные структуры Гольджи и обширный эндоплазматический ретикулум. Эти остеобласты секретируют коллаген I типа и другие матричные белки векторно по направлению к поверхности образования кости.
Популяции остеобластов гетерогенны, разные остеобласты экспрессируют разные репертуары генов, что может объяснять гетерогенность трабекулярной микроархитектуры в разных участках скелета, анатомические сайт-специфические различия в болезненных состояниях и региональные различия в способности остеобластов реагировать на используемые агенты. для лечения заболеваний костей.
Костный внеклеточный матрикс
Костный белок на 85–90% состоит из коллагеновых белков (). Костный матрикс в основном состоит из коллагена I типа (39) со следовыми количествами коллагенов III и V типов и FACIT на определенных этапах формирования кости, что может помочь определить диаметр коллагеновых фибрилл. Коллагены FACIT являются членами семейства ассоциированных с фибриллами коллагенов с прерывистыми тройными спиралями, группы нефибриллярных коллагенов, которые служат в качестве молекулярных мостиков, важных для организации и стабильности внеклеточных матриксов.Члены этого семейства включают коллагены IX, XII, XIV, XIX, XX и XXI. Неколлагеновые белки составляют от 10 до 15% от общего костного белка. Примерно 25% неколлагенового белка происходит экзогенно, включая сывороточный альбумин и α2-HS-гликопротеин, которые связываются с гидроксиапатитом из-за своих кислотных свойств. Неколлагеновые белки сыворотки могут помочь регулировать минерализацию матрикса, а α2-HS-гликопротеин, который является человеческим аналогом фетуина, может регулировать пролиферацию костных клеток. Остальные неколлагеновые белки, полученные экзогенно, состоят из факторов роста и большого количества других молекул в следовых количествах, которые могут влиять на активность костных клеток.
Таблица 1.
Белки внеклеточного матрикса a
| Белок (расположение хромосомы) | Функция | Болезнь человека | ||||
|---|---|---|---|---|---|---|
| Белки, связанные с коллагеном | тип | |||||
| Самый распространенный белок костного матрикса | Несовершенный остеогенез | |||||
| тип X (6q21) | Обнаружен в гипертрофическом хряще | Неизвестен | ||||
| 905 тип III (248q21) Следы в костях; может регулировать диаметр коллагеновых фибрилл | Синдром Элерса-Данлоса | |||||
| тип V (9q34.2-34,3; 2q24.3-31; 19q13.2) | Следы в кости; может регулировать диаметр коллагеновых фибрилл | |||||
| Сывороточные белки в костном матриксе | ||||||
| альбумин (4q11-13) | Уменьшает рост кристаллов гидроксиапатита | αHS | (3q27) | Аналогом крупного рогатого скота является фетуин | Нет | |
| Гликоаминогликан-содержащие белки и повторяющиеся белки с высоким содержанием лейцина | ||||||
| аггрекан (15q26.1) | Организация матрицы, удержание кальция / фосфора | Нет | ||||
| версикан (5q14.3) | Определяет пространство, предназначенное для превращения в кость | Нет | ||||
| Декорин (12q21.347) Регулирует коллаген | 905 диаметр фибриллы; связывает TGF-βПрогероидная форма синдрома Элерса-Данлоса с двойным нокаутом декорина / бигликана | |||||
| бигликан (Xq28) | Связывает коллаген; связывает TGF-β; генетическая детерминанта пика костной массы | |||||
| гиалуронан (мультигенный комплекс) | Может работать с версиканом для определения пространства, предназначенного для превращения в кость .1-p34) | Гидролизует ингибиторы отложения минералов | Гипофосфатазия | |||
| остеонектин (5q31.3-32) | Регулирует диаметр коллагеновых фибрилл | Нет | ||||
| SIBLING 905 4q21) | Подавляет минерализацию и ремоделирование | Нет | ||||
| Костный сиалопротеин (4q21) | Инициирует минерализацию | Нет | ||||
| MEPE (4q21.1) | Регулятор фосфатного обмена | Опухоль-индуцированная остеомаляция | ||||
| RGD-содержащие гликопротеины | ||||||
| тромбоспондины (15q15, 6q13545 | , 6q275 Нет||||||
| фибронектин (2q34) | Связывается с клетками | Нет | ||||
| витронектин (17q11) | Прикрепление клеток | Нет | .1, 5q23-31) | Регулирует образование эластичных волокон | Фибриллин 1: синдром Марфана | |
| белки, содержащие гамма-карбоксиглутаминовую кислоту | ||||||
| матричный белок Gla12 (12p13.1-p ) | Подавляет минерализацию | Нет | ||||
| остеокальцин (1q25-q31) | Регулирует остеокласты; подавляет минерализацию | Нет | ||||
| протеин S (3p11.2) | Печеночный продукт, может быть произведен остеобластами | Остеопения |
Остеобласты синтезируют и выделяют столько же неколлагенового молярного белка, сколько не коллаген.Неколлагеновые белки в целом делятся на несколько категорий, включая протеогликаны, гликозилированные белки, гликозилированные белки с потенциальной активностью прикрепления клеток и γ-карбоксилированные (gla) белки. Роли каждого из костных белков в настоящее время четко не определены, и многие из них, по-видимому, выполняют несколько функций, включая регулирование отложения и обмена костных минералов, а также регуляцию активности костных клеток. Ранее считалось, что остеокальцин в сыворотке, синтезируемый остеобластами, действует как промотор или инициатор отложения кальция в очаге между концами коллагеновых фибрилл и, следовательно, рассматривается как маркер образования кости.Наблюдение, что мышь с нокаутом остеокальцина имеет фенотип с высокой костной массой, предполагает, что остеокальцин обычно ингибирует образование кости. Поскольку сывороточный остеокальцин образуется как в результате высвобождения матрикса за счет активности остеокластов, так и в результате синтеза остеобластов, в настоящее время он рассматривается как маркер обновления костной ткани, а не как специфический маркер образования кости.
Основным гликозилированным белком, присутствующим в кости, является щелочная фосфатаза. Щелочная фосфатаза в кости связана с поверхностями клеток остеобластов через фосфоинозитольную связь, а также находится в свободном состоянии в минерализованном матриксе.Щелочная фосфатаза играет пока еще неопределенную роль в минерализации костей (40). Наиболее распространенным неколлагеновым белком в кости является остеонектин, составляющий примерно 2% от общего белка в развивающейся кости. Считается, что остеонектин влияет на рост и / или пролиферацию остеобластов и минерализацию матрикса.
Минерализация костного матрикса
Кость состоит из 50–70% минералов, 20–40% органического матрикса, 5–10% воды и <3% липидов. Минеральный состав кости состоит в основном из гидроксиапатита [Ca 10 (PO 4 ) 6 (OH) 2 ] с небольшими количествами карбоната, магния и кислого фосфата с отсутствующими гидроксильными группами, которые обычно присутствуют. .По сравнению с геологическими кристаллами гидроксиапатита, костные кристаллы гидроксиапатита очень малы, их наибольший размер составляет всего около 200 Å. Эти маленькие, малокристаллические, карбонат-замещенные кристаллы более растворимы, чем кристаллы геологического гидроксиапатита, что позволяет им поддерживать минеральный метаболизм.
Созревание матрикса связано с экспрессией щелочной фосфатазы и нескольких неколлагеновых белков, включая остеокальцин, остеопонтин и костный сиалопротеин.Считается, что эти связывающие кальций и фосфат белки помогают регулировать упорядоченное отложение минералов, регулируя количество и размер образующихся кристаллов гидроксиапатита.
Костный минерал придает кости механическую жесткость и несущую способность, а органический матрикс обеспечивает эластичность и гибкость. Костный минерал изначально откладывается в зонах «дырок» между концами коллагеновых фибрилл (41). Этому процессу могут способствовать везикулы внеклеточного матрикса в кости, такие как кальцификация хряща и минерализация сухожилий индейки (23).Внеклеточные везикулы матрикса синтезируются хондроцитами и остеобластами и служат защищенным микроокружением, в котором концентрации кальция и фосфата могут увеличиваться в достаточной степени, чтобы ускорить образование кристаллов. Внеклеточная жидкость обычно не перенасыщена гидроксиапатитом, поэтому гидроксиапатит не осаждается самопроизвольно. Внеклеточные везикулы матрицы содержат ядро ядра, которое состоит из белков и комплекса кислых фосфолипидов, кальция и неорганического фосфата, которого достаточно для осаждения кристаллов гидроксиапатита.Пока неясно, как внеклеточные везикулы матрикса вносят вклад в минерализацию в определенных местах на концах фибрилл коллагена, потому что везикулы, по-видимому, не нацелены непосредственно на концы фибрилл (23).
Нет никаких доказательств того, что кластеры некристаллического фосфата кальция (аморфный фосфат кальция) образуются в кости до того, как он превращается в гидроксиапатит (42). По мере созревания костей кристаллы гидроксиапатита увеличиваются в размерах и снижают уровень примесей. Увеличение кристаллов происходит как за счет роста кристаллов, так и за счет агрегации.Макромолекулы костного матрикса могут способствовать начальному зарождению кристаллов, секвестрировать ионы минералов для увеличения локальной концентрации кальция и / или фосфора или способствовать гетерогенному зарождению. Макромолекулы также связываются с поверхностями растущих кристаллов, чтобы определить размер, форму и количество образующихся кристаллов.
Подтвержденные промоторы минерализации (нуклеаторы) включают белок 1 матрикса дентина и сиалопротеин кости. Коллаген I типа не способствует минерализации костей. Фосфопротеинкиназы и щелочная фосфатаза регулируют процесс минерализации.Костная щелочная фосфатаза может увеличивать локальную концентрацию фосфора, удалять фосфатсодержащие ингибиторы роста кристаллов гидроксиапатита или изменять фосфопротеины, чтобы контролировать их способность действовать как нуклеаторы.
Витамин D играет косвенную роль в стимуляции минерализации неминерализованного костного матрикса. После абсорбции или выработки кожей витамина D печень синтезирует 25-гидроксивитамин D, а почки впоследствии производят биологически активный 1,25-дигидроксивитамин D [1,25- (OH) 2 D].Сыворотка 1,25- (OH) 2 D отвечает за поддержание сывороточного кальция и фосфора в адекватных концентрациях, позволяющих пассивную минерализацию неминерализованного костного матрикса. Сыворотка 1,25- (OH) 2 D делает это в первую очередь за счет стимуляции кишечного всасывания кальция и фосфора. Сыворотка 1,25- (OH) 2 D также способствует дифференцировке остеобластов и стимулирует экспрессию остеобластами специфической для кости щелочной фосфатазы, остеокальцина, остеонектина, OPG и ряда других цитокинов.Сыворотка 1,25- (OH) 2 D также влияет на пролиферацию и апоптоз других скелетных клеток, включая гипертрофические хондроциты.
Остеоциты
Остеоциты представляют собой терминально дифференцированные остеобласты и функционируют в синцитиальных сетях, поддерживая структуру кости и метаболизм. Остеоциты лежат в лакунах в минерализованной кости () и имеют обширные филиподиальные отростки, которые лежат внутри канальцев в минерализованной кости (43). Остеоциты обычно не экспрессируют щелочную фосфатазу, но экспрессируют остеокальцин, галектин 3 и CD44, рецептор клеточной адгезии для гиалуроната, а также несколько других белков костного матрикса.Остеоциты экспрессируют несколько матричных белков, которые поддерживают межклеточную адгезию и регулируют обмен минералов в костной жидкости в лакунах и канальцевой сети. Остеоциты активны во время остеолиза и могут функционировать как фагоцитарные клетки, поскольку содержат лизосомы.
Остеоциты поддерживают связь друг с другом и с поверхностью кости посредством своих множественных филиподиальных клеточных отростков. Коннексины — это интегральные клеточные белки, которые поддерживают щелевые контакты между клетками, чтобы обеспечить прямую связь через межклеточные каналы.Остеоциты метаболически и электрически связаны через щелевые соединения, состоящие в основном из коннексина 43 (44). Щелевые соединения необходимы для созревания, активности и выживания остеоцитов.
Основная функция синцития остеоцитов-остеобластов / выстилающих клеток — механочувствительность (45). Остеоциты преобразуют сигналы напряжения от изгиба или растяжения кости в биологическую активность. Поток канальцевой жидкости в ответ на внешние силы вызывает множество реакций внутри остеоцитов.Считается, что быстрые потоки костного кальция через щелевые соединения филиподий стимулируют передачу информации между остеобластами на поверхности кости и остеоцитами внутри кости (46). Сигнальные механизмы, участвующие в механотрансдукции, включают простагландин E2, циклооксигеназу 2, различные киназы, Runx2 и закись азота.
Остеоциты могут десятилетиями жить в неперевёрнутой кости человека. Присутствие пустых лакун в стареющей кости указывает на то, что остеоциты могут подвергаться апоптозу, вероятно, вызванному нарушением их межклеточных щелевых контактов или взаимодействий клетка-матрица (47).Апоптоз остеоцитов в ответ на дефицит эстрогена или лечение глюкокортикоидами вредит структуре кости. Терапия эстрогенами и бисфосфонатами, а также физиологическая нагрузка на кость могут помочь предотвратить апоптоз остеобластов и остеоцитов (48).
Детерминанты прочности кости
Костная масса составляет от 50 до 70% прочности кости (49). Однако геометрия и состав костей важны, потому что более крупные кости прочнее, чем более мелкие кости, даже при эквивалентной минеральной плотности костей.По мере того как диаметр кости увеличивается в радиальном направлении, прочность кости увеличивается на радиус пораженной кости, увеличенный до четвертой степени. Количество и пропорция трабекулярной и кортикальной кости в данном участке скелета независимо влияет на прочность кости. Свойства костного материала важны для прочности кости. У некоторых пациентов с остеопорозом аномальный костный матрикс. Мутации в некоторых белках могут вызывать слабость костей (, например, , дефекты коллагена вызывают снижение прочности костей при несовершенном остеогенезе, нарушение γ-карбоксилирования белков Gla).На прочность костей могут влиять остеомаляция, терапия фтором или состояния гиперминерализации. Микроструктура костей также влияет на прочность костей. Низкий костный обмен приводит к накоплению микротрещин. Высокий метаболизм кости, при которой резорбция кости выше, чем образование кости, является основной причиной ухудшения микроархитектуры.
Выводы
Каркас выполняет несколько функций. Моделирование и ремоделирование костей сохраняют функцию скелета на протяжении всей жизни. Блок ремоделирования кости обычно сочетает резорбцию и формирование кости.Костный матрикс регулирует минерализацию костей. Прочность костей зависит от костной массы, геометрии и состава, свойств материала и микроструктуры.
Список литературы
1. Опорно-двигательный аппарат. В: Анатомия Грея, 39-е изд., Под редакцией Standring S, New York, Elsevier, 2004. , стр83 –135
2. Тайчман Р.С.: Кровь и кость: две ткани, судьбы которых переплетаются, чтобы создать нишу для гемопоэтических стволовых клеток. Кровь 105 : 2631 –2639,2005 [PubMed] [Google Scholar]3. Эриксен Э. Ф., Аксельрод Д. В., Мельсен Ф.Костная гистоморфометрия, Нью-Йорк, Raven Press, 1994. , pp1 –12
4. Кобаяси С., Такахаши Х.Э., Ито А., Сайто Н., Навата М., Хориучи Х., Охта Х., Ито А., Иорио Р., Ямамото Н., Такаока К.: Трабекулярное минимальное моделирование подвздошной кости человека. Кость 32 : 163 –169,2003 [PubMed] [Google Scholar] 5. Убара Ю., Тагами Т., Наканиси С., Сава Н., Хосино Дж., Сувабе Т., Кайтори Н., Такемото Ф., Хара С., Такаичи К.: Значение минимального моделирования у диализных пациентов с адинамической болезнью костей. Почки Инт 68 : 833 –839,2005 [PubMed] [Google Scholar] 6.Ubara Y, Fushimi T, Tagami T., Sawa N, Hoshino J, Yokota M, Kaitori H, Takemoto F, Hara S: гистоморфометрические особенности кости у пациентов с первичным и вторичным гиперпаратиреозом. Почки Инт 63 : 1809 –1816,2003 [PubMed] [Google Scholar] 7. Линдси Р., Косман Ф., Чжоу Х., Бостром М., Шен В., Круз Дж., Ньевес Дж. В., Демпстер Д. В.: Новый график маркировки тетрациклинов для продольной оценки краткосрочных эффектов анаболической терапии с помощью биопсии одного гребня подвздошной кости: Ранние действия терипаратида.J Bone Miner Res 21 : 366 –373,2006 [PubMed] [Google Scholar] 9. Parfitt AM: Целевое и нецелевое ремоделирование кости: связь с возникновением и развитием основных многоклеточных единиц. Кость 30 : 5 –7,2002 [PubMed] [Google Scholar] 10. Рудман Г.Д .: Клеточная биология остеокластов. Опыт Гематол 27 : 1229 –1241,1999 [PubMed] [Google Scholar] 11. Бойл В.Дж., Симонет В.С., Лейси Д.Л.: дифференциация и активация остеокластов. Природа 423 : 337 –342,2003 [PubMed] [Google Scholar] 12. Блэр ХК, Атанасу Н.А.: Последние достижения в биологии остеокластов и патологической резорбции кости.Гистол Гистопатол 19 : 189 –199,2004 [PubMed] [Google Scholar] 13. Silver IA, Murrills RJ, Etherington DJ: Микроэлектродные исследования кислотного микроокружения под прилипшими макрофагами и остеокластами. Exp Cell Res 175 : 266 –276,1988 [PubMed] [Google Scholar] 14. Delaisse JM, Andersen TL, Engsig MT, Henriksen K, Troen T, Blavier L: Матричные металлопротеиназы (MMP) и катепсин K по-разному влияют на активность остеокластов. Microsc Res Tech 61 : 504 –513,2003 [PubMed] [Google Scholar] 15. Эриксен Э.Ф .: Нормальное и патологическое ремоделирование губчатой кости человека: Трехмерная реконструкция последовательности ремоделирования в норме и при метаболическом заболевании костей.Endocr Ред. 7 : 379 –408,1986 [PubMed] [Google Scholar] 16. Редди С.В.: Регуляторные механизмы, действующие в остеокластах. Crit Rev Eukaryot Gene Expr 14 : 255 –270,2004 [PubMed] [Google Scholar] 17. Боневальд Л., Манди Г. Р.: Роль трансформирующего фактора роста бета в ремоделировании костей. Clin Orthop Rel Res 2S : 35 –40,1990 [Google Scholar] 18. Hock JM, Centrella M, Canalis E: инсулиноподобный фактор роста I (IGF-I) оказывает независимое влияние на формирование костного матрикса и репликацию клеток. Эндокринология 122 : 254 –260,2004 [PubMed] [Google Scholar] 19.Locklin RM, Oreffo RO, Triffitt JT: Эффекты TGFbeta и bFGF на дифференцировку стромальных фибробластов костного мозга человека. Cell Biol Int 23 : 185 –194,1999 [PubMed] [Google Scholar] 20. Smit TH, Burger EH, Huyghe JM: Является ли BMU-сцепление явлением, регулируемым деформацией? Анализ методом конечных элементов. J Bone Miner Res 15 : 301 –307,2002 [PubMed] [Google Scholar] 21. Smit TH, Burger EH, Huyghe JM: случай, когда поток жидкости, индуцированный деформацией, используется в качестве регулятора BMU-сцепления и выравнивания костной ткани. J Bone Miner Res 17 : 2021 –2029,2002 [PubMed] [Google Scholar] 22.Мартин Т.Дж., Симс Н.А.: Активность остеокластов в сочетании образования кости с резорбцией. Тренды Мол Мед 11 : 76 –81,2005 [PubMed] [Google Scholar] 23. Андерсон ХК: Матричные везикулы и кальцификация. Curr Rheumatol Rep 5 : 222 –226,2003 [PubMed] [Google Scholar] 24. Burger EH, Klein-Nuland J, Smit TH: Поток канальцевой жидкости, полученный из деформации, регулирует активность остеокластов в ремоделирующем остеоне: предложение. Дж Биомех 36 : 1452 –1459,2003 [PubMed] [Google Scholar] 25. Добниг Х., Тернер Р.Т.: Доказательства того, что периодическое лечение паратироидным гормоном увеличивает образование костной ткани у взрослых крыс за счет активации клеток выстилки костей.Эндокринология 136 : 3632 –3638,1995 [PubMed] [Google Scholar] 26. Hauge EM, Qvesel D, Eriksen EF, Mosekilde L, Melsen F: Ремоделирование злокачественной кости происходит в специализированных отсеках, выстланных клетками, экспрессирующими маркеры остеобластов. J Bone Miner Res 16 : 1575 –1582,2001 [PubMed] [Google Scholar] 27. Парфитт AM: Остеональное и гемиостеональное ремоделирование: пространственные и временные рамки для передачи сигналов в кости взрослого человека. J Cell Biochem 55 : 273 –276,1994 [PubMed] [Google Scholar] 28. Тейтельбаум С.Л., Росс Ф.П.: Генетическая регуляция развития и функции остеокластов.Нат Рев Жене 4 : 638 –649,2003 [PubMed] [Google Scholar] 29. Коэн М.М.-младший: Новая биология костей: патологические, молекулярные, клинические корреляты. Am J Med Genet A 140 : 2646 –2706,2006 [PubMed] [Google Scholar] 30. Росс Ф.П., Тейтельбаум SL: α v β 3 и фактор, стимулирующий колонию макрофагов: партнеры в биологии остеокластов. Иммунол Рев 208 : 88 –105,2005 [PubMed] [Google Scholar] 31. Teitelbaum SL, Abu-Amer Y, Ross FP: Молекулярные механизмы резорбции кости. J Cell Biochem 59 : 1 –10,1995 [PubMed] [Google Scholar] 32.Vaananen HK, Zhao H, Mulari M, Halleen JM: клеточная биология функции остеокластов. J Cell Sci 113 : 377 –381,2000 [PubMed] [Google Scholar] 33. Pittenger MF, Mackay AM, Beck SC, Jaiswal RK, Douglas R, Mosca JD, Moorman MA, Simonetti DW, Craig S, Marshak DR: Многолинейный потенциал мезенхимальных стволовых клеток взрослого человека. Наука 284 : 143 –147,1990 [PubMed] [Google Scholar] 34. Доэрти М.Дж., Эштон Б.А., Уолш С., Бересфорд Дж. Н., Грант М.Э., Кэнфилд А.Е.: Сосудистые перициты выражают остеогенный потенциал in vitro и in vivo.J Bone Miner Res 13 : 828 –838,1998 [PubMed] [Google Scholar] 35. Логан CY, Nusse R: Путь передачи сигналов Wnt в развитии и болезни. Анну Rev Cell Dev Biol 20 : 781 –810,2004 [PubMed] [Google Scholar] 36. Boyden LM, Mao J, Belsky J, Mitzner L, Farhi A, Mitnick MA, Wu D, Insogna K, Lifton RP: Высокая плотность костей из-за мутации в связанном с рецептором ЛПНП протеине 5. N Engl J Med 346 : 1513 –1521,2002 [PubMed] [Google Scholar] 37. Литтл Р.Д., Реккер Р.Р., Джонсон М.Л.: Высокая плотность костей из-за мутации белка 5, связанного с рецептором ЛПНП.N Engl J Med 347 : 943 –944,2002 [PubMed] [Google Scholar] 38. Shin CS, Lecanda F, Sheikh S, Weitzmann L, Cheng SL, Civitelli R: Относительное количество различных кадгеринов определяет дифференциацию мезенхимальных предшественников в остеогенные, миогенные или адипогенные пути. J Cell Biochem 78 : 566 –577,2000 [PubMed] [Google Scholar] 39. Бродский Б., Персиков А.В.: Молекулярная структура тройной спирали коллагена. Adv Protein Chem 70 : 301 –339,2005 [PubMed] [Google Scholar] 40. Уайт М.П .: Гипофосфатазия и роль щелочной фосфатазы в минерализации скелета.Endocr Ред. 15 : 439 –461,1994 [PubMed] [Google Scholar] 41. Ландис У. Дж .: Прочность кальцинированной ткани частично зависит от молекулярной структуры и организации составляющих ее минеральных кристаллов в их органической матрице. Кость 16 : 533 –544,1995 [PubMed] [Google Scholar] 42. Вайнер С., Саги И., Аддади Л.: Структурная биология: выбор менее пройденного пути кристаллизации. Наука 309 : 1027 –1028 [PubMed] 43. Bonewald LF: Создание и характеристика остеоцитоподобной клеточной линии MLO-Y4. Джей Боун Майнер Метаб 17 : 61 –65,1999 [PubMed] [Google Scholar] 44.Плоткин Л.И., Manolagas SC, Bellido T: Трансдукция сигналов выживания клеток с помощью полуканалов коннексина-43. J Biol Chem 277 : 8648 –8657,2002 [PubMed] [Google Scholar] 45. Rubin CT, Lanyon LE: Остеорегуляторная природа механических стимулов: функция как детерминант адаптивного ремоделирования кости. J Orthop Res 5 : 300 –310,1987 [PubMed] [Google Scholar] 46. Jorgensen NR, Teilmann SC, Henriksen Z, Civitelli R, Sorensen OH, Steinberg TH: Активация кальциевых каналов L-типа необходима для опосредованной щелевыми соединениями межклеточной передачи сигналов кальция в остеобластных клетках.J Biol Chem 278 : 4082 –4086,2003 [PubMed] [Google Scholar] 47. Xing L, Boyce BF: Регулирование апоптоза в остеокластах и остеобластических клетках. Биохимия Биофиз Рес Коммуна 328 : 709 –720,2005 [PubMed] [Google Scholar] 48. Плоткин Л.И., Агирре Дж.И., Кустени С., Манолагас С.К., Беллидо Т. Бисфосфонаты и эстрогены ингибируют апоптоз остеоцитов через различные молекулярные механизмы, расположенные ниже по ходу активации регулируемой внеклеточными сигналами киназы. J Biol Chem 280 : 7317 –7325,2005 [PubMed] [Google Scholar] 49. Покок Н.А., Эйсман Дж. А., Хоппер Дж. Л., Йейтс М. Г., Сэмбрук PH, Эберл С.: Генетические детерминанты костной массы у взрослых: исследование близнецов.J Clin Invest 80 : 706 –710,1987 [Бесплатная статья PMC] [PubMed] [Google Scholar]Ушиб кости — Physiopedia
Ушиб кости — это разновидность травмы кости.
- Другие примеры травм костей включают стрессовые переломы, костно-хрящевые переломы и различные виды переломов костей. [1]
- Ушиб кости характеризуется тремя различными видами повреждений кости, включая: поднадкостничную гематому, межкостный синяк и субхондральное поражение или их комбинацию. [2]
- Ушиб кости отличается от альтернативных типов перелома тем, что сломаны только некоторые трабекулы. [3]
Клинически значимая физиология [редактировать | править источник]
Костная ткань — это особая форма соединительной ткани, состоящая из органического матрикса (коллагена и гликозаминогликанов) и неорганических минералов (кальция и фосфата). [4] Скелет взрослого человека содержит 80% кортикальной кости и 20% губчатой кости.Оба типа костей состоят из остеонов. Кортикальная кость представляет собой твердый тип кости, а губчатая кость напоминает соты, которые состоят из сети трабекулярных пластин и стержней. Подробнее о гистологии и физиологии костей читайте здесь.
Наиболее частой причиной ушиба кости является травма, однако это состояние также может быть связано с нормальной стрессовой нагрузкой и гемофилией A и B. [5]
Чаще всего поражается нижняя конечность. [6]
Пациенты с ушибом кости, как правило, имеют длительное клиническое выздоровление с большим выпотом и более медленным возвращением движений. [1]
У пациентов с разрывом ПКС существует 80% -ная вероятность сопутствующего синяка кости в мыщелке бедренной кости или плато большеберцовой кости. [1] [4] Согласно Boks et al. 2007, наличие ушиба кости в этих зонах является наиболее важным вторичным признаком в диагностике травмы ПКС.
МРТ с белой стрелкой, указывающей на наличие ушиба кости в области постлатеральной таранной кости (а) и эпифизе хвостовой большеберцовой кости (б).
| Тип костной травмы | Характеристики | Типичный механизм травмы |
|---|---|---|
| Поднадкостничная гематома | Концентрированное скопление крови под надкостницей кости. | Прямая травма кости с высокой силой |
| Межкостный синяк | Поражение костного мозга.Кровоснабжение кости нарушается, что вызывает внутреннее кровотечение. | Повторяющееся сжимающее усилие на кость (чрезмерное давление на обычное основание). |
| Субхондральное поражение | Поражение происходит под хрящевым слоем сустава. | Чрезвычайная сила сжатия или вращательный механизм, такой как испытание (сила сдвига), который буквально раздавливает клетки Сила вызывает разделение хряща (или связки) и подлежащей кости, а также кровотечение, когда энергия удара распространяется на кость. |
Уровень заболеваемости всеми травмами костей, как правило, выше среди профессиональных спортсменов и тех, кто часто бегает и прыгает по твердым покрытиям, например футболистов и баскетболистов. [1] [2]
Хотя рентген должен определить, есть ли перелом кости, ушиб кости не может быть диагностирован с помощью рентгеновского изображения. В настоящее время «золотым стандартом» диагностического метода визуализации ушибов костей является МРТ, в частности Т2-взвешенные изображения с подавлением жира или Т1-взвешенные изображения. [4]
[1] [2] [7]
Управление физиотерапией [править | править источник]
Лечение ушиба кости состоит из риса, обезболивающих и / или противовоспалительных средств в соответствии с предписаниями практикующего врача и ограничения нагрузки в зависимости от обстоятельств травмы. [8] Время разрешения ушиба кости варьируется. Литература предполагает, что время заживления для полного устранения этой травмы может занять от трех недель до двух лет после травмы. [1] [2]
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 V. Mandalia, A.J.B. Fogg, R. Chari, J. Murray, A. Beale, J.H.L. Хенсон. Костный ушиб колена. Клиническая радиология 2005; 60, 627–636 Степени рекомендации: A
- ↑ 2,0 2,1 2.2 2,3 В. Мандалия, J.H.L. Хенсон. Травматический ушиб кости — обзорная статья, Европейский журнал радиологии, 2008 г .; 67; 54–61 Степени рекомендации A
- ↑ Дженис Поландит, 5 фактов о костном ушибе, которые нужно знать, 2011 г .; http://www.livestrong.com/article/5521-need-bone-bruise/ Уровни рекомендации F
- ↑ 4.0 4,1 4,2 L.C. Джунгейра и Дж. Карнейро, «Функциональная гистология» 2010; 167
- ↑ Проф. Д-р С. Ван Кревельд и д-р М. Кингма Поднадкостничное кровоизлияние при гемофилии А и Б. Нед. Т. Генееск. 105. I. 22. 1961; 1095-1098 Степени рекомендации F
- ↑ Christoph Rangger, Anton Kathrein, Martin C Freund и др. Костный ушиб колена. Acta Orthop Scand 1998; 69 (3): 291-294.Степени рекомендации B
- ↑ Симона С. Бокс, Даммис Вроэгиндевей, Барт В. Коес и др. Последующее наблюдение МРТ посттравматических костных ушибов колена в общей врачебной практике. AJR 2007; 189: 556–562 Степени рекомендации B
- ↑ Основы ушибов костей; Степени рекомендации F http: // синяки.knowfirstaid.com/permalink.php?article=Bone%20Bruises.txt
Минеральная плотность проксимальной большеберцовой губчатой кости связана с болью у пациентов с остеоартритом | Исследования и терапия артрита
Hawker GA, Stewart L, French MR, Cibere J, Jordan JM, March L, et al. Понимание боли при остеоартрите тазобедренного и коленного суставов — инициатива OARSI / OMERACT. Osteoarthr Cartil. 2008; 16: 415–22.
CAS Статья PubMed Google ученый
Хантер DJ, Felson DT. Остеоартроз. Br Med J. 2006; 332: 639–42.
Артикул Google ученый
Дьепп П., Ломандер Л. Патогенез и лечение боли при остеоартрите. Ланцет. 2005; 365: 965–73.
CAS Статья PubMed Google ученый
Lo GH, Harvey WF, McAlindon TE. Связь варусного толчка и выравнивания с болью при остеоартрите коленного сустава.Ревматоидный артрит. 2012; 64: 2252–9.
Артикул PubMed PubMed Central Google ученый
Lo GH, McAlindon TE, Niu J, Zhang Y, Beals C., Dabrowski C, et al. Поражения костного мозга и суставной выпот тесно и независимо связаны с болью при нагрузке на коленный сустав при остеоартрите коленного сустава: данные из инициативы по остеоартриту. Osteoarthr Cartil. 2009; 17: 1562–9.
CAS Статья PubMed PubMed Central Google ученый
Kornaat PR, Bloem JL, Ceulemans RYT, Riyazi N, Rosendaal FR, Nelissen RG, et al. Остеоартрит коленного сустава: связь между клиническими данными и результатами МРТ. Радиология. 2006; 239: 811–7.
Артикул PubMed Google ученый
Бакленд-Райт С. Изменения субхондральной кости при остеоартрите кисти и колена, обнаруженные с помощью рентгенографии. Остеоартроз Хрящ. 2004; 12: 10.
Артикул Google ученый
Bobinac D, Spanjol J, Zoricic S, Maric I. Изменения гистоморфометрии суставного хряща и субхондральной кости в коленных суставах при остеоартрите у людей. Кость. 2003. 32: 284–90.
Артикул PubMed Google ученый
Zysset PK, Sonny M, Hayes WC. Взаимосвязь морфологии и механических свойств губчатой кости проксимального отдела большеберцовой кости, пораженной остеоартритом. J Артропластика. 1994; 9: 203–16.
CAS Статья PubMed Google ученый
Mach DB, Роджерс С.Д., Сабино М.С., Люгер Н.М., Швай М.Дж., Помонис Д.Д. и др. Причины скелетной боли: сенсорная и симпатическая иннервация бедренной кости мыши. Неврология. 2002. 113: 155–66.
CAS Статья PubMed Google ученый
Радин Э.Л., Пол ИЛ, Роуз РМ. Роль механических факторов в патогенезе первичного остеоартроза. Ланцет. 1972; 1: 519–22.
CAS Статья PubMed Google ученый
Акамацу Ю., Мицуги Н., Таки Н., Аши Х. К., Сайто Т. Соотношение минеральной плотности медиальной и латеральной мыщелковой кости в поперечном исследовании: потенциальный маркер тяжести медиального остеоартрита коленного сустава. Arthritis Care Res. 2012; 64: 1036–45.
Google ученый
Бернетт В.Д., Контулайнен С., МакЛеннан С., Хейзел Д., Талмо К., Хантер Д. и др. У пациентов с остеоартритом коленного сустава с сильной ночной болью изменилась минеральная плотность субхондральной большеберцовой кости.Osteoarthr Cartil. 2015; 23: 1483–90.
CAS Статья PubMed Google ученый
Ding M, Danielsen CC, Hvid I. Плотность кости не отражает механических свойств при ранней стадии артроза. Acta Orthop Scand. 2001; 72: 181–5.
CAS Статья PubMed Google ученый
Day JS, Ding M, van der Linden JC, Hvid I., Sumner DR, Weinans H.Снижение модуля упругости субхондральной губчатой костной ткани связано с преартритным повреждением хряща. J Orthop Res. 2001; 19: 914–8.
CAS Статья PubMed Google ученый
Беннелл К.Л., Creaby MW, Wrigley TV, Hunter DJ. Субхондральная трабекулярная объемная плотность кости большеберцовой кости при остеоартрозе медиального коленного сустава с использованием технологии периферической количественной компьютерной томографии. Ревматоидный артрит. 2008. 58: 2776–85.
Артикул PubMed Google ученый
Амини М., Наземи С.М., Лановаз Дж., Контулайнен С., Масри Б.А., Уилсон Д.Р. и др. Индивидуальные и комбинированные эффекты связанных с ОА изменений субхондральной кости на жесткость проксимальной большеберцовой поверхности: исследование параметрического моделирования методом конечных элементов. Med Eng Phys. 2015; 37: 783–91.
Артикул PubMed Google ученый
Картер Д.Р., Хейс У.С.Сжимающее поведение кости как двухфазной пористой структуры. J Bone Joint Surg Am. 1977; 59: 954–62.
CAS Статья PubMed Google ученый
Неоги Т. Клиническое значение костных изменений при остеоартрозе. Ther Adv Musculoskelet Dis. 2012; 4: 259–67.
Артикул PubMed PubMed Central Google ученый
Келлгрен Дж. Х., Лоуренс Дж. С..Радиологическая оценка остеоартроза. Ann Rheum Dis. 1957; 16: 494–502.
CAS Статья PubMed PubMed Central Google ученый
Беллами Н., Бьюкенен WW, Голдсмит СН, Кэмпбелл Дж., Ститт Л.В. Валидационное исследование WOMAC: инструмент состояния здоровья для измерения клинически значимых исходов противоревматической лекарственной терапии у пациентов с остеоартритом тазобедренного или коленного сустава. J Rheumatol. 1988; 15: 1833–40.
CAS PubMed Google ученый
Санга О., Штуки Дж., Лян М. Х., Фоссель А. Х., Кац Дж. Н.. Анкета самоуправляемой коморбидности: новый метод оценки коморбидности для клинических исследований и исследований служб здравоохранения. Ревматоидный артрит. 2003. 49: 156–63.
Артикул PubMed Google ученый
Kontulainen SA, Johnston JD, Liu D, Leung C, Oxland TR, McKay HA.Индексы силы на основе изображений pQCT предсказывают до 85% отклонений в свойствах костной недостаточности на эпифизе и диафизе большеберцовой кости. J Musculoskelet Nueronal Взаимодействие. 2008; 8: 401–9.
CAS Google ученый
Отчет НКДАР ООН 2000 Генеральной Ассамблее — Приложение B: Облучение от естественных источников излучения. Научный комитет ООН по действию атомной радиации.
Ljunggren AE. Вариации во взаимоотношениях диафиза и эпифизов большеберцовой кости.Acta Morphol Neerl Scand. 1976; 14: 101–37.
CAS PubMed Google ученый
Джонстон Дж. Д., МакЛеннан К. Э., Хантер Д. Д., Уилсон Д. Р.. Точность in vivo метода топографического картирования с учетом глубины при КТ-анализе остеоартрита и нормальной плотности проксимальной части большеберцовой субхондральной кости. Skelet Radiol. 2010; 40: 1057–64.
Артикул Google ученый
Glüer CC, Blake G, Lu Y, Blunt BA, Jergas M, Genant HK. Точная оценка ошибок точности: как измерить воспроизводимость методов костной денситометрии. Osteoporos Int. 1995; 5: 262–70.
Артикул PubMed Google ученый
Джонстон Д.Д., Масри Б.А., Уилсон Д.Р. Компьютерная томография, топографическое картирование субхондральной плотности (CT-TOMASD) при остеоартрите и нормальных коленях: методологическая разработка и предварительные результаты.Osteoarthr Cartil. 2009; 17: 1319–26.
CAS Статья PubMed Google ученый
Spoor CF, Zonneveld FW, Macho GA. Линейные измерения кортикального слоя кости и зубной эмали с помощью компьютерной томографии: приложения и проблемы. Am J Phys Anthropol. 1993; 91: 469–84.
CAS Статья PubMed Google ученый
Чен Й, Хуанг И-С, Лу WW.Связана ли минеральная плотность субхондральной кости с ночной болью у пациентов с остеоартритом коленного сустава? Остеоартроз Хрящ. 2015; 23: 2297–8.
CAS Статья Google ученый
Чиба К., Бургхардт А.Дж., Осаки М., Маджумдар С. Трехмерный анализ субхондральных кист при остеоартрите тазобедренного сустава: исследование ex vivo HR-pQCT. Кость. 2014; 66: 140–5.
Артикул PubMed PubMed Central Google ученый
Франк А.В., Лабас М.С., Джонстон Д.Д., Контулайнен С.А. Локально-зависимые различия лучевой кости и прочности большеберцовой кости, определяемые размером мышц и массой тела. Physiother Can. 2012; 64: 292–301.
Артикул PubMed PubMed Central Google ученый
Шнайдер А., Хоммель Г., Блеттнер М. Анализ линейной регрессии. Dtsch Arztebl Int. 2010; 107: 776–82.
PubMed PubMed Central Google ученый
Томпсон Р. Примечание об ограниченной оценке максимального правдоподобия с альтернативной моделью выбросов. J R Stat Soc B Methodol. 1985; 47: 53–5.
Google ученый
Dore D, Ding C, Jones G. Пилотное исследование воспроизводимости и достоверности измерения плотности субхондральной кости колена в большеберцовой кости. Остеоартроз Хрящ. 2008; 16: 1539–44.
CAS Статья Google ученый
Бернетт В., Контулайнен С., МакЛеннан С., Хейзел Д., Талмо С., Хантер Д. и др. Ответ на письмо редактору: «Связана ли минеральная плотность субхондральной кости с ночной болью у пациентов с остеоартритом коленного сустава?». Остеоартроз Хрящ. 2015; 23: 2299–301.
CAS Статья Google ученый
Seah S, Wheaton D, Li L, Dyke JP, Talmo C, Harvey WF и др. Взаимосвязь перфузии большеберцовой кости при остеоартрозе коленного сустава.Osteoarthr Cartil. 2012; 20: 1527–33.
CAS Статья PubMed Google ученый
Lowitz T, Museyko O, Bousson V, Laouisset L, Kalendar WA, Laredo JD, et al. Поражения костного мозга, выявленные с помощью МРТ при остеоартрите коленного сустава, связаны с местным повышением минеральной плотности костной ткани, измеренной с помощью QCT. Osteoarthr Cartil. 2013; 21: 957–64.
CAS Статья PubMed Google ученый
Venäläinen MS, Mononen ME, Jurvelin JS, Töyräs J, Virén T., Korhonen RK. Важность свойств материала и пористости кости на механическую реакцию суставного хряща в коленном суставе человека: двухмерное исследование методом конечных элементов. J Biomech Eng. 2014; 136: 121005.
Артикул PubMed Google ученый
Гц VHH. Uber die Berührung fester elastischer Körper. J Reine Angew Math. 1882; 92: 156–71. Немецкий.
Wada M, Maezawa Y, Baba H, Shimada S, Sasaki S, Nose Y. Взаимосвязь между минеральной плотностью костной ткани, статическим выравниванием и динамической нагрузкой у пациентов с остеоартритом медиального отдела коленного сустава. Ревматология (Оксфорд). 2001; 40: 499–505.
Артикул Google ученый
Ли Дж., Чжэн К., Ландао-Бассонга Е., Ченг Т.С., Павлос, Нью-Джерси, Ма И и др. Влияние возраста и пола на микроархитектуру и ремоделирование кости в субхондральной кости головки бедренной кости с остеоартрозом.Кость. 2015; 77: 91–7.
Артикул PubMed Google ученый
Perilli E, Baleani M, Ohman C, Baruffaldi F, Viceconti M. Структурные параметры и механическая прочность губчатой кости головки бедренной кости при остеоартрозе не зависят от возраста. Кость. 2007; 41: 760–8.
CAS Статья PubMed Google ученый
Мазесс РБ. При старении потеря костной массы.Clin Orthop Relat Res. 1982; 165: 239–52.
Google ученый
Peduzzi P, Concato J, Kemper E, Holford TR, Feinstein AR. Имитационное исследование количества событий на переменную в логистическом регрессионном анализе. J Clin Epidemiol. 1996; 49: 1373–9.
CAS Статья PubMed Google ученый
Miranda H, Viikari-Juntra E, Martikainen R, Riihimaki H.Проспективное исследование боли в коленях и ее факторов риска. Остеоартроз Хрящ. 2002; 10: 623–30.
CAS Статья Google ученый
Wesseling J, Welsing PMJ, Bierma-Zeinstra SMA, Dekker J, Gorter KJ, Kloppenburg M, et al. Влияние самооценки сопутствующей патологии на физическое и психическое состояние здоровья при раннем симпотматическом остеоартрите: исследование CHECK (Cohort Hip and Cohort Knee). Ревматология. 2013; 52: 180–8.
Артикул PubMed Google ученый
Ранталайнен Т., Никандер Р., Дали Р.М., Хейнонен А., Сиванен Х.Нагрузка при физической нагрузке и распределение кортикальной кости на диафизе большеберцовой кости. Кость. 2011; 48: 786–91.
CAS Статья PubMed Google ученый
Вассерштейн Р., Лазар Н. Заявления ASA о p-значениях: контекст, процесс и цель. Am Stat. 2016; 70: 129–33.
Артикул Google ученый
Angst F, Aeschlimann A, Stucki G. Наименьшие выявляемые и минимальные клинически важные различия реабилитационных вмешательств с их последствиями для требуемых размеров выборки с использованием инструментов измерения качества жизни WOMAC и SF-36 у пациентов с остеоартритом нижних конечностей .Arthritis Care Res (Хобокен). 2001; 45: 384–91.
CAS Статья Google ученый
Петерсен М.М., Нильсен П.Т., Лебек А., Токсвиг-Ларсен С., Лунд Б. Предоперационная минеральная плотность кости проксимального отдела большеберцовой кости и миграция большеберцового компартмента после несцементированной тотальной артропластики коленного сустава. J Артропластика. 1999; 14: 77–81.
CAS Статья PubMed Google ученый
Levitz CL, Lotke PA, Karp JS.Долгосрочные изменения минеральной плотности костной ткани после полной замены коленного сустава. Clin Orthop Relat Res. 1995. 321: 68–72.
Google ученый
Mavrogenis AF, Dimitriou R, Parvizi J, Babis GC. Биология остеоинтеграции имплантата. J Musculoskelet Nueronal Взаимодействие. 2009; 9: 61–71.
CAS Google ученый
Шарки П.Ф., Хозак В.Дж., Ротман Р.Х., Шастри С., Якоби С.М.Почему тотальные артропластики коленного сустава сегодня терпят неудачу? Clin Orthop Relat Res. 2002; 404: 7–13.
Артикул Google ученый
Риттер М.А., Дэвис К.Э., Смолл С.Р., Мерчун Дж.Г., Фаррис А. Плотность трабекулярной кости проксимального отдела большеберцовой кости, связанная с неудачей тотального эндопротезирования коленного сустава. Bone Joint J. 2014; 96-B: 1503–9.
CAS Статья PubMed Google ученый
Части кости
Части кости
Большинство людей представляют себе кость однородно твердой, но ничто не может быть дальше от истины.Во-первых, как вы увидите позже в этом разделе, кости бывают разных форм: длинные, короткие, плоские, неправильные, червячные и сесамовидные, которые имеют много общего, несмотря на их различия. Типичную кость можно разбить на несколько частей, каждая из которых выполняет определенную функцию:
- Epiphysis . Эта часть находится на крайних концах кости ( epi = выше), где образуются суставы (сочленения).
- Суставной хрящ . Слой гиалинового хряща, называемый суставной хрящ , существует для уменьшения трения и поглощения ударов в синовиальных суставах (см. Суставы).
- Диафиз . Древко длинной кости — это направление, в котором кость может выдержать наибольшую нагрузку.
- Метафиз . Метафиз — это место, где диафиз встречается с эпифизом. Здесь происходит основной рост костей, а также там, где кровь попадает в кость.
- Надкостница . Тонкая мембрана, которая покрывает внешнюю сторону кости, где к кости прикрепляются сухожилия и связки. Внешний фиброзный слой — это место, где кровеносные сосуды, нервы и лимфатические сосуды соединяются с костью, в то время как внутренний остеогенный слой содержит костные клетки, необходимые для роста и восстановления костей.
- Медуллярная (или костномозговая) полость . Эта полая полость в диафизе предназначена для хранения желтого костного мозга.
- Эндост . Эта мембрана выстилает мозговую полость и содержит клетки-остеопрогениторы (неспециализированные костные клетки, как вы скоро увидите).
Вверх, вниз и посередине
Как вы можете видеть на Рисунке 5.1, стержень длинной кости называется диафизом. Центральная жировая полость костного мозга находится внутри диафиза.На каждом конце кости, в месте синовиального сустава, есть область, называемая эпифизом. На стыке между ними есть область, называемая метафизом.
Рисунок 5.1 Множество частей типичной длинной кости. Показанный здесь пример — бедренная кость. (2003 www.clipart.com)
Общая картина
Определенное заболевание гипофиза связано с гиперпродукцией человеческого гормона роста или чГР. У ребенка это приводит к гигантизму, тогда как слишком малое количество гормона роста приводит к одной форме карликовости (другие формы вызываются либо крайним недоеданием, либо, в случае ахондроплазии , доминантным геном).У взрослого человека из-за образования эпифизарной линии кости лица, рук и ног резко увеличиваются. Это состояние, которое наблюдается у некоторых злодеев кино, называется акромегалия .
Помните, что органам, включая кости, необходимы три соединения: кровеносные сосуды (артерии и вены), лимфатические сосуды и нервы. Эти структуры входят в кость через маленькие отверстия, называемые отверстиями . Отверстие, специально предназначенное для кровеносных сосудов, называется питательным отверстием (единственная форма отверстия ).Любой студент может определить, настоящий ли скелет, просто посмотрев на отверстия вокруг метафиза. Еще одна подсказка — это вес: настоящие кости легче твердых моделей из-за отверстий для красного и желтого костного мозга.
Помимо входящих и выходящих нервов и сосудов, в метафизе также находятся эпифизарные пластинки , которые являются первичными центрами роста длинной кости. В эпифизарной пластинке четыре зоны. Зона покоя хряща не участвует в росте, но она прикрепляет пластину к остальной части кости.Зона пролиферирующего хряща и зона гипертрофического хряща обе участвуют в производстве хондроцитов (хрящевых клеток), но в последней зоне происходит созревание клеток. Последняя зона, где фактически формируется кость, известна как зона кальцинированного хряща .
По мере старения эпифизарные пластинки, которые менее плотны, чем кость и выглядят темнее на рентгеновском снимке, окостенят (превратятся в кость), после чего они появятся в виде светлой линии (называемой эпифизарная линия ).Это знаменует конец способности кости расти длиннее; это окостенение обычно завершается к началу-середине двадцатых годов (хотя грудина заканчивается только после 30 лет). Однако лицевые кости и часто руки и ноги не перестают расти, что объясняет, почему молодой Джимми Стюарт выглядел совсем иначе, чем в старину.
Чем они сложнее
Компактная кость отличается большим расстоянием между ячейками внутри твердой кристаллической матрицы (см. Рис. 5.2). Вы можете помнить, что и широкое расстояние, и матрица были характеристиками соединительной ткани.Главная особенность компактной кости — ее прочность. Он обеспечивает защиту мест за пределами мягкой структуры, например, в плоских костях черепа. Компактная кость также выдерживает нагрузку на нее. В длинной кости напряжение лучше всего поглощается вдоль продольной оси диафиза. Такое расположение отлично подходит для такой кости, как бедренная кость, которая поглощает напряжение в этом направлении, но этого нельзя сказать о ключице, которая может быть легко сломана, если она получает удар вниз перпендикулярно диафизу.
Микроскопически компактная (или плотная) кость отличается расположением остеоцитов (костных клеток) в концентрических кругах матрикса. Подобно тому, как люди селятся вокруг источников воды, эти кольца или концентрические ламели расположены вокруг центрального гаверсовского канала, по которому проходят кровеносные сосуды. Комбинация концентрических пластинок и гаверсова канала называется остеоном или гаверсовской системой. Помимо гаверсовского канала, существуют перпендикулярные каналы, называемые перфорирующими каналами, которые соединяют гаверсовы каналы и помогают снабжать кровью не только более глубокие гаверсовские системы, но и полость костного мозга.
Остеоциты немного похожи на муравьев из-за расположения небольших каналов, называемых канальцами, вокруг каждой клетки; эти canaliculi, название которых всегда заставляет меня думать об итальянском десерте, являются местом, где находится интерстициальная жидкость. Канальцы выходят наружу во всех направлениях от лакуны, в которой находится остеоцит.
Рисунок 5.2 Это диаграмма гаверсовых систем в компактной кости. Обратите внимание, что организация кости основана на расположении кровеносных сосудов.(LifeART1989-2001, Lippincott Williams & Wilkins)
Не только для удаления разливов
Губчатая или губчатая кость очень отличается по внешнему виду. Вместо жестких концентрических систем губчатая кость выглядит губчатой. Внешний вид обусловлен нерегулярным набором перекрывающихся и соединенных между собой спиц, называемых трабекулами (см. Рисунок 5.2). Чтобы понять функцию губчатой кости, обратите внимание, что она чаще всего появляется в эпифизе, прямо под защитным компактным слоем.Компактный слой обеспечивает прочное прикрепление к суставному хрящу, что помогает защитить от трения в каждом синовиальном суставе.
Так почему губчатая часть? Что касается нагрузки на сустав, представьте, что подпрыгиваете в воздухе и тяжело приземляетесь на ступни, держа ноги прямыми; Большое напряжение будет ощущаться не только в коленях, но и в местах сочленения бедренной кости с тазом, не говоря уже о спине. Вы можете легко уменьшить напряжение, согнув ноги в коленях и лодыжках; такой изгиб поглощает ударную нагрузку.Теперь вы знаете причину образования губчатой кости? Верно, чтобы поглотить часть ударов по синовиальным суставам.
Завинчивающиеся разнонаправленные трабекулы позволяют поглощать напряжение с разных сторон. Кроме того, промежутки между трабекулами делают губчатую кость намного легче, что делает скелет в целом намного легче. Эти пространства служат другой цели; они заполнены красным костным мозгом, местом кроветворения.
Выдержки из The Complete Idiot’s Guide to Anatomy and Physiology 2004 Майкл Дж.Виейра Лазарофф. Все права защищены, включая право на полное или частичное воспроизведение в любой форме. Используется по договоренности с Alpha Books , членом Penguin Group (USA) Inc.
Чтобы заказать эту книгу непосредственно у издателя, посетите веб-сайт Penguin USA или позвоните по телефону 1-800-253-6476. Вы также можете приобрести эту книгу на Amazon.com и Barnes & Noble.
Блок ремоделирования кости — обзор
Стимуляция образования кости
Что касается гомеостаза кальция, стимуляция образования кости с помощью ПТГ выполняет функцию связывания образования новой кости с резорбцией кости, таким образом восстанавливая кости, принесенные в жертву требованиям гипокальциемии.В классической модели ремоделирования кости вещества, резорбирующие кости, активируют новые группы остеокластов для резорбции кости. После того, как эти остеокласты выкопали яму, наступает фаза обращения, а затем образование новой кости в вырытом пространстве (см. Главу 2). Сигналы, которые привлекают остеобласты к участку ремоделирования и контролируют их активность, не были идентифицированы, но, как полагают, являются хемотаксическими сигналами, генерируемыми высвобождением факторов из резорбированного костного матрикса. Формирование кости связано во времени и пространстве с предшествующей резорбцией кости.
Стимуляция образования кости при первичном гиперпаратиреозе не может быть полностью объяснена активацией единиц ремоделирования кости [231]. На уровне блока ремоделирования кости не только увеличивается частота активации (что можно объяснить первичным действием ПТГ на активацию резорбции кости), но также увеличивается скорость аппозиции минералов, увеличивается продолжительность периода активного формирования, а средняя толщина стенки увеличивается [232, 233]. ПТГ увеличивает ежедневную продуктивность остеобластов и продлевает их активную трудовую жизнь, делая каждый остеобласт более продуктивным, добавляя больше остеобластов, или и то, и другое.В результате масса губчатой кости сохраняется и может даже увеличиваться при первичном гиперпаратиреозе, несмотря на выраженную резорбцию кости [234, 235].
Анаболический эффект ПТГ заметно усиливается, когда гормон вводится один раз в день — наблюдение [236], которое привело к введению ПТГ для терапии остеопороза. Ежедневное подкожное введение ПТГ (1–34) вызывает быстрое, резкое увеличение массы губчатой и кортикальной кости у животных [191, 237–240] и людей [192, 241–243], увеличивает прочность костей [244–246] и заметно снижает заболеваемость. новых переломов у женщин в постменопаузе [192].Неизвестно, почему периодическое воздействие ПТГ имеет анаболический эффект, тогда как постоянное воздействие высоких доз ПТГ часто вызывает чистый катаболизм кости [247]. Возможно, что постоянное воздействие ПТГ вызывает подавление рецепторов и, таким образом, снижает стимуляцию анаболического пути.
Прерывистое лечение ПТГ увеличивает частоту активации костных многоклеточных единиц и значительно увеличивает поверхность остеобластов [231,248–250]. Увеличение количества остеобластов или минерализующей поверхности количественно больше, чем увеличение суточной скорости минерализации [248–250]; то есть работает больше остеобластов и / или они работают дольше, но они также работают больше.Увеличивая образование костной ткани, лечение ПТГ и эстрогеном вызывает увеличение связности губчатой кости, чего не происходит при лечении только антирезорбтивными агентами [249, 251], и в высоких дозах может фактически заменить костное пространство губчатой костью. Таким образом, лечение ПТГ один раз в день усиливает все эффекты первичного гиперпаратиреоза на функцию остеобластов. Также имеются предварительные данные о том, что лечение ПТГ, помимо активации единиц ремоделирования кости, может вызывать образование кости на ранее покоящихся поверхностях кости [252].
Клеточные эффекты ПТГ на остеобласты многочисленны [46] (Таблица 2), и нелегко синтезировать согласованное представление о биохимической и клеточной основе для общих эффектов ПТГ на рекрутирование остеобластов или функцию остеобластов. Учитывайте синтетическую активность остеобластов. ПТГ индуцирует экспрессию семейств непосредственных ранних генов c- fos (c- fos, fra-1 и fra-2 ) и c- jun (c- jun и junD ) [253–256].Это опосредуется фосфорилированием фактора транскрипции CREB с помощью PKA [257–259], чтобы индуцировать связывание с CRE в промоторе c- fos [257, 258]. ПТГ также вызывает цАМФ-зависимое фосфорилирование фактора транскрипции cbfa1 [260]. Как эти транскрипционные эффекты связаны с увеличением синтетической функции остеобластов, неясно, поскольку прямой эффект острого введения ПТГ заключается в ингибировании транскрипции гена коллагена типа I, основного белка костного матрикса [46, 261, 262].
ТАБЛИЦА 2. Действие ПТГ на костные клетки.
Трансформирующий фактор роста β
Семейство цитокинов интерлейкина-6
Другие цитокины и простагландины
Инактивация калиевых каналов, чувствительных к хинину Поступление кальция через потенциалзависимые кальциевые каналы L-типа Открытые кальций-чувствительные калиевые каналы
Щелевые соединения
|
ПТГ также увеличивает количество остеобластов на поверхности кости — по крайней мере, при применении в анаболических режимах. ПТГ может увеличивать рост предшественников остеобластов в костном мозге, пролиферацию предшественников остеобластов или привлечение предшественников остеобластов на формирующуюся поверхность. Прерывистый ПТГ может увеличивать проникновение стромальных клеток в клон остеобластов [263], хотя клетку-мишень для ПТГ еще предстоит найти.Транскрипты рецептора PTH / PTHrP отсутствуют или их не хватает в STRO-1-положительных, отрицательных по щелочной фосфатазе стромальных клетках костного мозга [264, 265], которые, как полагают, представляют собой ранние предшественники остеобластов. Прерывистый ПТГ не увеличивает пролиферацию предшественников остеобластов: ни уровень мРНК маркера пролиферации гистона h5 [266], ни количество [ 3 H] ядер, меченных тимидином, на поверхности кости не увеличиваются [267]. Периодическое воздействие ПТГ, однако, может увеличивать возвращение на поверхность кости поздних постмитотических предшественников остеобластов в костном мозге, которые имеют рецепторы ПТГ [217, 222].
ПТГ увеличивает продолжительность жизни активного остеобласта [231]. У мышей периодическое лечение высокой дозой ПТГ снижает скорость апоптоза остеобластов [268], хотя лечение ПТГ фактически увеличивает количество апоптотических остеобластов в метафизарной кости молодых крыс [269]. Хотя ингибирование апоптоза способствует анаболическому эффекту ПТГ, неясно, является ли снижение гибели клеток количественно достаточным, чтобы объяснить все это. Если продолжительность жизни активного остеобласта составляет несколько месяцев [231], то скорость обновления остеобластов, приводящая к снижению скорости апоптоза, будет слишком медленной, чтобы учесть быстрое расширение пула остеобластов, которое происходит в течение 1 недели. начала введения ПТГ на моделях грызунов.Например, если продолжительность жизни остеобластов составляет 100 дней, скорость оборота составляет 1% в день, а максимальное увеличение размера пула остеобластов, ожидаемое от полной отмены апоптоза, также составляет 1% в день. Если бы снижение скорости апоптоза было основным эффектом ПТГ, можно было бы ожидать увеличения не только средней толщины стенки, но и продолжительности периода активного формирования. Достаточно ясно, что средняя толщина стенки увеличивается при применении анаболических режимов ПТГ или при первичном гиперпаратиреозе, но вопрос о том, увеличивается ли также продолжительность периода активного формирования, не решено [233, 248].
Помимо увеличения скорости образования предшественников остеобластов, выхода из пула преостеобластов на поверхность кости или увеличения продолжительности активной жизни рабочих остеобластов, лечение ПТГ может также привлекать остеобласты из выстилающих клеток, покрывающих покоящиеся поверхности кости [267 ]. Набор из этой популяции будет вызывать образование кости на ранее покоящихся поверхностях [252]. Относительно небольшое количество ячеек подкладки необходимо для покрытия больших площадей неподвижной поверхности, поскольку ячейки являются плоскими; однако кажется маловероятным, что имеется достаточно клеток, чтобы объяснить увеличение количества остеобластов после лечения ПТГ.
Тот факт, что существует так много возможностей анаболического действия ПТГ, является симптомом нашего глубокого невежества в отношении базовой клеточной кинетики популяции остеобластов. Чтобы более точно определить механизмы, с помощью которых ПТГ оказывает анаболическое действие, мы должны узнать гораздо больше о происхождении, продолжительности жизни и судьбе остеобластов.
Другие цитокины могут опосредовать эффекты ПТГ на формирование кости [46,191,231]. Непрерывное воздействие ПТГ подавляет синтез коллагена изолированным сводом черепа крысы, но воздействие ПТГ в течение первых 24 часов 72-часового эксперимента заметно увеличивает синтез коллагена [270].Стимуляция синтеза коллагена с помощью ПТГ блокируется антителами к инсулиноподобному фактору роста-1 (IGF-1), но не пролиферация [271]. Обработка интактных крыс ПТГ увеличивает мРНК IGF-1 [272] и содержание IGF-1 в костном матриксе [272a]. ПТГ также регулирует экспрессию связывающих IGF белков в кости [273]. Разгрузка скелета вызывает устойчивость in vitro к IGF-1 и к анаболическому эффекту ПТГ, предполагая, что устойчивость к IGF-1 может быть причиной устойчивости к ПТГ [274]. Однако условный мутагенез гена рецептора IGF-1 в кости вызывает состояние высокого оборота с заметно увеличенным количеством остеобластов, а не угнетение обмена костной ткани, которое можно было бы ожидать при блокаде действия ПТГ [275].
Прерывистая обработка крыс ПТГ увеличивает содержание TGF-β в костном матриксе 1 [272], повышая вероятность того, что анаболические эффекты ПТГ, наблюдаемые при прерывистом введении, также могут быть опосредованы, по крайней мере частично, повышенной секрецией это мощный фактор роста и дифференцировки остеобластов. Эффект ПТГ на TGF-β 1 может быть опосредован PKC, тогда как его действие на TGF-β 2 опосредовано PKA [276].
Роль PTH в костях не будет понятна, пока не будет определена роль PTHrP.PTHrP экспрессируется в зрелых остеобластах [217, 277], периостальных клетках [278], выстилающих клетках [217] и преостеобластах [279–281]. Тесная взаимосвязь между паракринными эффектами PTHrP и эндокринными эффектами PTH, вероятно, происходит через их общий рецептор.

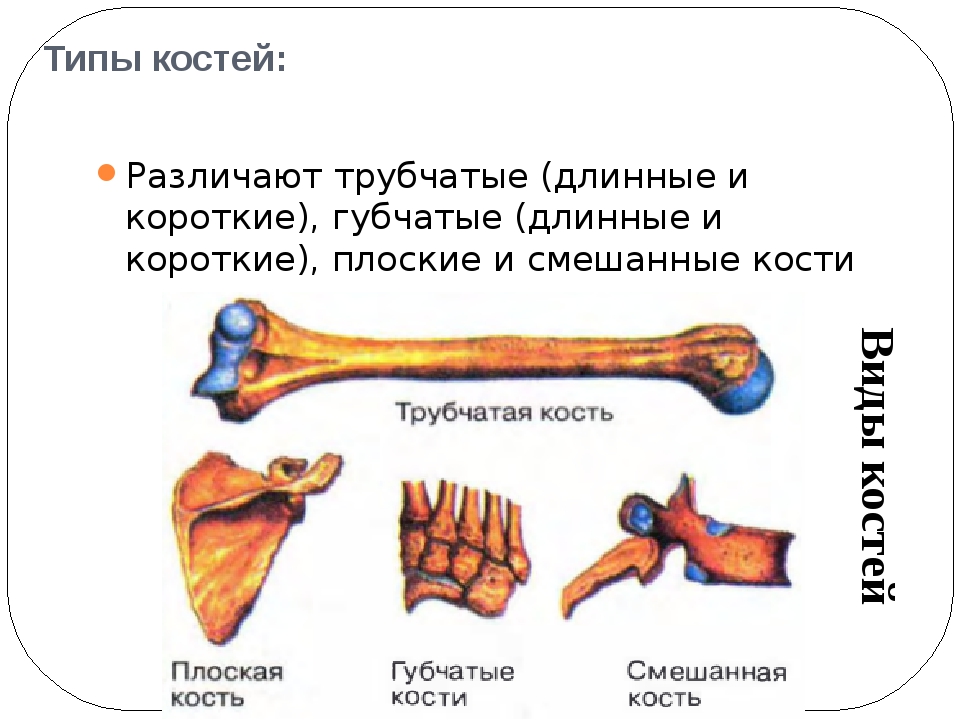 Состоит из парных (теменных и височных) и непарных (лобная, затылочная, решетчатая, клиновидная) костей
Состоит из парных (теменных и височных) и непарных (лобная, затылочная, решетчатая, клиновидная) костей Лопатка соединяет плечевую кость с ключицей
Лопатка соединяет плечевую кость с ключицей Большая подвижность большого пальца и
способность его противопоставляться всем остальным
Большая подвижность большого пальца и
способность его противопоставляться всем остальным пальцем. Пружинящий свод
стопы.
пальцем. Пружинящий свод
стопы. 3 Костная структура
3 Костная структура