Питание при хроническом колите. Болезни желудка и кишечника
Питание при хроническом колите
Данная диета способствует обеспечению полноценного питания при имеющейся недостаточности функции кишечника. По содержанию белков, жиров и углеводов она относится к полноценным (но с ограничением поваренной соли до нижних границ нормы). Белки – 100—120 г, жиры – 100—120 г, углеводы – 400—500 г. Рекомендованы витамины А, В1, В2, С и РР, из минеральных веществ необходимы кальций, фосфор, железо.
В диете отсутствуют продукты и блюда, которые могу раздражать слизистую оболочку и нервно-рецепторный аппарат органов пищеварения, усиливать двигательную функцию, процессы брожения и гниения в кишечнике.
Пища должна быть приготовлена в вареном, паровом, жареном без панировки, тушеном или запеченном виде из неизмельченных продуктов. Питание дробное, не реже 4—5 раз в день.
Рекомендованные продукты
Больным хроническим колитом предлагают нежирные сорта говядины, телятины, крольчатины без сухожилий.
Для супов выбирают слабые обезжиренные бульоны (мясной, мясо-костный, рыбный). После приготовления с их поверхности снимают жир, процеживают, разводят водой в пропорции 2 : 1 и доводят до кипения. Бульоны заправляют крупами (за исключением пшена) и овощами: картофелем, морковью, цветной капустой, кабачками, тыквой. Для заправки также используют вермишель и лапшу. В супы добавляют фрикадельки, кнели.
В рацион входят различные рассыпчатые каши (кроме пшенной и перловой). Их готовят на воде с добавлением трети молока или 10% сливок.
Цельное молоко показано только в случае его хорошей переносимости и обязательно в блюдах. Из молочных продуктов рекомендованы ряженка, кефир, ацидофилин, а также свежий творог и творожная масса, сырники, паровые или запеченные пудинги, неострый сыр. Сметану можно использовать как приправу к блюдам. Сливочное масло – в бутерброде и в блюдах не более 6—15 г на один прием.
В день можно употреблять 1—2 яйца, паровой омлет.
Овощи рекомендованы в отварном, паровом непротертом виде. Не исключены пюре, запеканки, суфле из свеклы, моркови с творогом.
В диету также включены фрукты (сырые и печеные). Это яблоки, груши (без кожицы), апельсины и мандарины. Из ягод – клубника, земляника, малина, виноград (без кожуры). Хороши фруктовые и ягодные соки (яблочный, мандариновый, малиновый, клубничный, томатный), отвар шиповника.
Из напитков для рациона выбраны некрепкие чай, кофе, какао. Перед сном актуален стакан кефира.
Хлебобулочные изделия представлены в диете пшеничным хлебом (вчерашней выпечки или подсушенным), несдобными сортами печенья, сухарями. В ограниченном количестве можно употреблять пироги с творогом, яблоками, повидлом, джемом, яйцами, мясом.
В ограниченном количестве можно употреблять пироги с творогом, яблоками, повидлом, джемом, яйцами, мясом.
Запрещенные продукты
Жирные сорта мяса, гусь, утка.
Копченые колбасы, консервы; жирная соленая и копченая рыба.
Крепкие жирные бульоны, борщи, рассольники, щи, супы из бобовых и грибов, а также молочные.
Жареные и сваренные вкрутую яйца.
Жирные молочные продукты с повышенной кислотностью, острые сыры.
Тугоплавкие жиры: бараний, говяжий, свиной и кулинарный.
Из овощей – брюква, репа, огурцы, щавель, шпинат, редис, редька, лук, чеснок, грибы, бобовые.
Из фруктов – абрикосы, сливы, финики, инжир, ягоды с грубой кожицей. Из соков – абрикосовый, сливовый и виноградный.
Перец, хрен, горница, жирные и острые соусы.
Ржаной и свежий пшеничный хлеб, изделия из сдобного и слоеного теста.
Также необходимо ограничить потребление грубой клетчатки, цельного молока, острых блюд, закусок и пряностей.
Примерное меню диеты
1-й завтрак: рисовая каша на молоке, белковый омлет, чай с молоком, сухарики.
2-й завтрак: нежирный сыр, сухарик, чай.
Обед: лапша на курином бульоне, отварное мясо с морковным пюре, яблочный компот.
Полдник: отвар шиповника.
Ужин: отварное куриное мясо с картофельными котлетами, черничный сок.
На ночь: стакан кефира, сухарик.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Советыпри хроническом, спастическом и язвенном колите — симптомы. Вот уже на протяжении 20 лет мне ставят диагноз хронический спастический колит. Но чем старше становлюсь (мне 60 лет), тем сильнее боли и постоянные позывы в туалет. Все оспастическом колите: Медицина: : Медицинские статьи Все о спастическом колите. Всю жизнь ваш организм работал как часы: кишечник опорожнялся каждый день.. Поскольку колит — заболевание хроническое, большинство страдающих им людей могут успешно бороться с приступами, соблюдаяРеферат:Хронический колит — BestReferat.ru — Банк рефератов. Хронический колит, характеризующийся нарушением тонуса толстой кишки (спастический компонент), следует дифференцировать со спастической колопатией. При хроническом колите без резкого усиления бродильных и гнилостных процессов назначают диету № 4..
Колит, язвенный колит — Симптомы и лечение народными средствами. Пьют по 1/3–1/2 стакана 3 раза в день при хронических спастических колитах. При обострении колита При хроническом колите без резкого усиления бродильных и гнилостных процессов назначают диету № 4..
Колит, язвенный колит — Симптомы и лечение народными средствами. Пьют по 1/3–1/2 стакана 3 раза в день при хронических спастических колитах. При обострении колита . Основной диетой для больных . Основной диетой для больных Лечебное питаниепри хроническом колите Лечебное питание при хроническом колите. Неспецифический язвенный колит. Страница 1 из 2.. В ряде случаев могут образовываться язвы (эрозии) на слизистой оболочке толстой кишки (язвенный колит).. Хронический колит При спастическом колите, особенно при вовлечении в процесс дистальных отделов толстой кишки, каловые массы имеют фрагментированный вид («овечий кал»). Лечениеколита кишечника народными средствами Хронический спастический колит.. Народное лечение колита. Колит требует длительного лечения, в основе которого лежит строгая .
Хронический колит / Большая Медицинская Энциклопедия При спастическом колите, особенно при вовлечении в процесс дистальных отделов толстой. Боли при хроническом колите имеют ряд особенностей.. При наличии сопутствующих заболеваний (холецистит, панкреатит, атеросклероз) в .
Хронический колит / Большая Медицинская Энциклопедия При спастическом колите, особенно при вовлечении в процесс дистальных отделов толстой. Боли при хроническом колите имеют ряд особенностей.. При наличии сопутствующих заболеваний (холецистит, панкреатит, атеросклероз) в .%2Fbnoonies-6-nbank%2F6.html%22+style%3D%22font-size%3A+12pt%22%3E%D0%BF%D0%B8%D1%82%D1%8C%D0%B5%D0%B2%D0%B0%D1%8F+%D0%B4%D0%B8%D0%B5%D1%82%D0%B0+%D0%BA%D0%B3%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-11-nbank%2F9.html%22+style%3D%22font-size%3A+12pt%22%3E%D0%BA%D0%B0%D0%BA+%D0%BF%D0%BE%D0%B4%D1%82%D1%8F%D0%BD%D1%83%D1%82%D1%8C+%D0%BA%D0%BE%D0%B6%D1%83+%D0%BF%D0%BE%D1%81%D0%BB%D0%B5+%D0%BF%D0%BE%D1%85%D1%83%D0%B4%D0%B5%D0%BD%D0%B8%D1%8F+%D1%84%D0%BE%D1%80%D1%83%D0%BC%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-2-nbank%2F3.html%22+style%3D%22font-size%3A+12pt%22%3E%D1%81%D0%B5%D0%BA%D1%80%D0%B5%D1%82%D1%8B+%D0%BF%D0%BE%D1%85%D1%83%D0%B4%D0%B5%D0%BD%D0%B8%D1%8F+%D0%B2%D0%B5%D1%80%D1%8B+%D0%B1%D1%80%D0%B5%D0%B6%D0%BD%D0%B5%D0%B2%D0%BE%D0%B9%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-8-nbank%2F4.html%22+style%3D%22font-size%3A+12pt%22%3E%D0%B0%D0%BB%D0%BB%D0%B0+%D0%BF%D1%83%D0%B3%D0%B0%D1%87%D0%B5%D0%B2%D0%B0+%D0%BE%D1%84%D0%B8%D1%86%D0%B8%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9+%D1%81%D0%B0%D0%B9%D1%82+%D0%B4%D0%B8%D0%B5%D1%82%D0%B0%3C%2Fa%3E%3Ca+href%3D%22.  .%2Fbnoonies-3-nbank%2F1.html%22+style%3D%22font-size%3A+12pt%22%3E%D1%81%D1%80%D0%B5%D0%B4%D1%81%D1%82%D0%B2%D0%B0+%D0%B4%D0%BB%D1%8F+%D0%BF%D0%BE%D1%85%D1%83%D0%B4%D0%B5%D0%BD%D0%B8%D1%8F+%D0%BA%D1%83%D0%BF%D0%B8%D1%82%D1%8C+%D0%B2+%D0%BA%D0%B8%D0%B5%D0%B2%D0%B5%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-5-nbank%2F8.html%22+style%3D%22font-size%3A+12pt%22%3E%D0%B0%D0%BA%D0%B2%D0%B0%D0%B0%D1%8D%D1%80%D0%BE%D0%B1%D0%B8%D0%BA%D0%B0+%D0%B4%D0%BB%D1%8F+%D0%BF%D0%BE%D1%85%D1%83%D0%B4%D0%B5%D0%BD%D0%B8%D1%8F+%D0%B2+%D0%BA%D1%80%D0%B0%D1%81%D0%BD%D0%BE%D1%8F%D1%80%D1%81%D0%BA%D0%B5%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-8-nbank%2F6.html%22+style%3D%22font-size%3A+12pt%22%3E%D1%82%D0%B2%D0%BE%D1%80%D0%BE%D0%B6%D0%BD%D0%B0%D1%8F+%D0%B4%D0%B8%D0%B5%D1%82%D0%B0+%D0%BD%D0%B0+2+%D0%B4%D0%BD%D1%8F%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-1-nbank%2F4.html%22+style%3D%22font-size%3A+12pt%22%3E%D0%BA%D0%B5%D0%B9%D1%82+%D0%BC%D0%B8%D0%B4%D0%B4%D0%BB%D1%82%D0%BE%D0%BD+%D0%B4%D0%BE+%D0%B8+%D0%BF%D0%BE%D1%81%D0%BB%D0%B5+%D0%B4%D0%B8%D0%B5%D1%82%D1%8B%3C%2Fa%3E%3C%2Ftags%3E»> .%2Fbnoonies-3-nbank%2F1.html%22+style%3D%22font-size%3A+12pt%22%3E%D1%81%D1%80%D0%B5%D0%B4%D1%81%D1%82%D0%B2%D0%B0+%D0%B4%D0%BB%D1%8F+%D0%BF%D0%BE%D1%85%D1%83%D0%B4%D0%B5%D0%BD%D0%B8%D1%8F+%D0%BA%D1%83%D0%BF%D0%B8%D1%82%D1%8C+%D0%B2+%D0%BA%D0%B8%D0%B5%D0%B2%D0%B5%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-5-nbank%2F8.html%22+style%3D%22font-size%3A+12pt%22%3E%D0%B0%D0%BA%D0%B2%D0%B0%D0%B0%D1%8D%D1%80%D0%BE%D0%B1%D0%B8%D0%BA%D0%B0+%D0%B4%D0%BB%D1%8F+%D0%BF%D0%BE%D1%85%D1%83%D0%B4%D0%B5%D0%BD%D0%B8%D1%8F+%D0%B2+%D0%BA%D1%80%D0%B0%D1%81%D0%BD%D0%BE%D1%8F%D1%80%D1%81%D0%BA%D0%B5%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-8-nbank%2F6.html%22+style%3D%22font-size%3A+12pt%22%3E%D1%82%D0%B2%D0%BE%D1%80%D0%BE%D0%B6%D0%BD%D0%B0%D1%8F+%D0%B4%D0%B8%D0%B5%D1%82%D0%B0+%D0%BD%D0%B0+2+%D0%B4%D0%BD%D1%8F%3C%2Fa%3E%3Ca+href%3D%22..%2Fbnoonies-1-nbank%2F4.html%22+style%3D%22font-size%3A+12pt%22%3E%D0%BA%D0%B5%D0%B9%D1%82+%D0%BC%D0%B8%D0%B4%D0%B4%D0%BB%D1%82%D0%BE%D0%BD+%D0%B4%D0%BE+%D0%B8+%D0%BF%D0%BE%D1%81%D0%BB%D0%B5+%D0%B4%D0%B8%D0%B5%D1%82%D1%8B%3C%2Fa%3E%3C%2Ftags%3E»>2013 hasy. |
Пройти диагностику и лечение хронического колита в Москве, цена
02.11.2021Статья проверена врачом-гастроэнтерологом, эндоскопистом Кондрашовой Е.А., носит общий информационный характер, не заменяет консультацию специалиста.
Для рекомендаций по диагностике и лечению необходима консультация врача.
Хронический колит — воспалительное заболевание слизистой оболочки толстой кишки. Это заболевание достаточно распространено, встречается у мужчин чаще в возрасте 40–60 лет, а у женщин — в возрасте от 20 до 60 лет.
В отделении гастроэнтерологии Клинического госпиталя на Яузе врачи проводят тщательную диагностику и назначают лечение, учитывая индивидуальные особенности каждого пациента.
Хронический колит может появляться при других заболеваниях желудочно-кишечного тракта: гастрит, панкреатит, хронический энтерит. Также выделяют хронический колит аллергической природы.
Также выделяют хронический колит аллергической природы.
Причины и патогенез хронического колита
К факторам, вызывающим развитие заболевания, относят:
- острые кишечные инфекции
- дисбактериоз
- вирусные инфекции (например, ротавирус)
- паразитарные инвазии
- продолжительные нарушения режима питания
- длительный бесконтрольный прием некоторых лекарственных препаратов, например, антибиотиков
- хронические интоксикации промышленными ядами
- вредные привычки (в частности, курение)
- анатомические особенности кишечника
- длительное лучевое воздействие
Симптомы хронического колита
В результате длительного воздействия раздражающих факторов на слизистую кишечника нарушается ее всасывающая функция. Одновременно страдает моторика кишечника. Все это приводит к нарушениям стула: это и является главным проявлением хронического колита.
Во время обострения заболевания больных может мучить упорный понос, до 10–15 раз в сутки.
После дефекации у больного остается ощущение неполного опорожнения кишечника. На смену поносам могут приходить запоры, а также возникают ложные позывы к дефекации, во время которых выделяется только слизь. При запорах отмечается метеоризм.
Еще один характерный симптом хронического колита —тупые ноющие боли в животе, в основном. в нижней части, иногда по всему животу; при левостороннем колите — в левой подвздошной области, при правостороннем — в правой.
Также больные хроническим колитом жалуются на тошноту, метеоризм, неприятный привкус во рту, слабость, раздражительность, быструю утомляемость. При длительном течении заболевания наблюдаются ломкость ногтей, выпадение волос, сухость кожи и разнообразные кожные и аллергические проявления.
Если хронический колит своевременно не выявить и не лечить, могут возникнуть осложнения: кишечные кровотечения, некроз участка кишки с развитием перитонита, сужение просвета кишки, спаечный процесс.
Диагностика хронического колита в Клиническом госпитале на Яузе
В первую очередь врачи отделения гастроэнтерологии исключают колиты инфекционного или паразитарного происхождения. Диагноз подтверждается по результатам лабораторных исследований (общий анализ крови, копрограмма, возможно, кал на дисбактериоз). Большое диагностическое значение имеют эндоскопические исследования — ректороманоскопия и колоноскопия, при необходимости с биопсией. Также важную роль в диагностике хронического колита играют рентгенологическое (ирригоскопия) и ультразвуковое (УЗИ брюшной полости) исследования.
Гастроэнтеролог может направить пациента на консультацию к хирургу.
Лечение хронического колита в Клиническом госпитале на Яузе
Амбулаторное лечение подразумевает прием лекарств строго по назначению врача.
Гастроэнтеролог Клинического госпиталя на Яузе подберет необходимое вам медикаментозное лечение и диетотерапию.
Профилактика заболевания включает предупреждение и своевременное лечение кишечных инфекций, разумное применение антибактериальных препаратов и соблюдение режима питания..gif)
Стоимость услуг
Цены на услуги Вы можете посмотреть в прайсе или уточнить по телефону, указанному на сайте.
Литература:
Белоусов С.С., Муратов С.В., Ахмад А.М. Гастроэзофагеальная рефлюксная болезнь и дуоденогастральный рефлюкс // НГМА. 2005.
Калинина А.В., Хазанова А.И. Гастроэнтерология и гепатология: диагностика и лечение: руководство для врачей // М.: Миклош. 2007.
Ивашкин В.Т., Лапина Т.Л., Охлобыстин А.В., Буеверов А.О. Наиболее распространенные заболевания желудочно-кишечного тракта и печени: справ. для практикующих врачей // Литтерра. 2008.
Правильная диета при колите
Колит (воспаление толстой кишки) – достаточно распространенное заболевание ЖКТ, сопровождающееся частыми тягостными, с сильными болями в животе, позывами на стул. При колите наблюдается расстройство пищеварительного тракта, в результате чего в экскрементах имеются частички непереваренной пищи и сгустки слизи. К возникновению колита могут привести инфекции (сальмонеллы, дизентерийная палочка, балантидии, амебы и др.), нехватка желудочных кислот и даже обычная простуда. Проходя курс лечения колита кишечника следует придерживаться диеты, без этого выздоровление невозможно.
При колите наблюдается расстройство пищеварительного тракта, в результате чего в экскрементах имеются частички непереваренной пищи и сгустки слизи. К возникновению колита могут привести инфекции (сальмонеллы, дизентерийная палочка, балантидии, амебы и др.), нехватка желудочных кислот и даже обычная простуда. Проходя курс лечения колита кишечника следует придерживаться диеты, без этого выздоровление невозможно.
Диета при колите заключается в полном исключении из рациона белков. На замену им приходят углеводы и жиры: каши, молоко, картофель. Суточные нормы определенных продуктов разбиваются на 5-6 приемов пищи, при этом порции должны быть небольшими. Сухие или твердые продукты способны повредить стенки кишечника, поэтому следует вести контроль над консистенцией употребляемой пищи. Насколько быстро человек избавится от колита непосредственно зависит от того, насколько правильно он питается.
Подготовка к диете
Перед тем, как остановиться на диете подробнее, следует рассказать о процедурах, которые ей предшествуют. Клизма и 2-дневное воздержание от пищи – это начало пути к выздоровлению. В эти дни больному рекомендовано употреблять много жидкости. Лучше выпивать 6-8 стаканов теплого чая с лимоном или соком черники, допускается небольшое количество сахара в напитке. Желательно также добавлять в питье столовую ложку красного вина. Такие меры восстановят обезвоженный после частого стула и рвоты организм.
Клизма и 2-дневное воздержание от пищи – это начало пути к выздоровлению. В эти дни больному рекомендовано употреблять много жидкости. Лучше выпивать 6-8 стаканов теплого чая с лимоном или соком черники, допускается небольшое количество сахара в напитке. Желательно также добавлять в питье столовую ложку красного вина. Такие меры восстановят обезвоженный после частого стула и рвоты организм.
Вместо чая можно употреблять теплый отвар шиповника или черники (либо чередовать их). Эти ягоды насыщены витамином C, который отлично очищает организм от токсинов. С этой целью рекомендуется также употреблять компот из сухофруктов – яблок, груш, добавлять замороженную или свежую черную смородину. Такое питье, благодаря вяжущему действию, нормализует стул.
Особенности диеты
В первый день диета при колите очень строгая – только жидкость. На второй – можно употребить яблоки. Это должны быть некислые, мягкие, очищенные и перетертые плоды. Не более 1,5 кг яблок допустимо съесть за 6 приемов. Эти фрукты помогут остановить гнилостные процессы в кишечнике.
Эти фрукты помогут остановить гнилостные процессы в кишечнике.
В последующие дни рацион пополняется продуктами, которые не являются агрессивными для кишечника. Не будут раздражать кишечник, вызывать движение кишок и повышенную секрецию слизистые отвары. Именно они рекомендованы при колите. Для приготовления нужно использовать манную, рисовую или овсяную крупу. Допустимо употребление небольшого количества сливочного масла. Мясное пюре также разрешено при такой диете.
Из молочных продуктов положено включить в рацион кефир, простоквашу, нежирный творог. Разнообразить меню с пользой можно киселями из малины, вишни, смородины, клубники. Удовлетворить потребность в сладком можно пудингом с апельсиновым, мандариновым или гранатовым соком.
Дальше состояние здоровья улучшается, а вместе с этим расширяется список допустимых продуктов, которые рекомендует диета при колите. Сюда входят паровые тефтели и котлеты, вареная рыба, протертые каши. Продолжать питаться следует по-прежнему 6 раз в день. Важно ежедневное употребление творога и неострого протертого сыра. Эти продукты окажут противовоспалительный и вяжущий эффект.
Важно ежедневное употребление творога и неострого протертого сыра. Эти продукты окажут противовоспалительный и вяжущий эффект.
Конечно, много продуктов оказывается под запретом. Диета при колите исключает из рациона молоко, многие фрукты и овощи, мучные изделия, консервацию, мед, «газировки». Нельзя также употреблять соленую, холодную, острую и жареную пищу. Не лишне начать принимать аскорбиновую кислоту и циацин для восстановления нарушенных функций.
При спастическом колите, который сопровождается запором и вздутием, следует отказаться от молочных продуктов. Голодная или полуголодная диета при спастическом колите поможет полностью избавиться от заболевания.
Когда болезнь переходит в хроническую форму (язвенный колит), требуется составление особого рациона питания.
Во время обострения начинать день можно с рисовой, манной или овсяной каши с галетным печеньем и соком из моркови или апельсина. На протяжении дня можно употребить крупяной суп на некрепком мясном бульоне, нежирное отварное мясо, рыбу или паровые кнели, тефтели. После снятия обострения питание при язвенном колите предполагает расширение рациона с избеганием пряных, острых и сладких блюд.
После снятия обострения питание при язвенном колите предполагает расширение рациона с избеганием пряных, острых и сладких блюд.
Строгая диета при колите не даст заболеванию перерасти в хроническую форму.
Исследование диеты для поддержания ремиссии при воспалительном заболевании кишечника
Abstract
Предполагается, что диета является фактором патогенеза воспалительного заболевания кишечника и может быть важным фактором в лечении симптомов заболевания. Пациенты манипулируют своим питанием, пытаясь контролировать симптомы, что часто приводит к принятию неуместно ограничивающих диет, что подвергает их риску пищевых осложнений. Медицинские работники изо всех сил стараются предоставить пациентам рекомендации по питанию, основанные на фактических данных, из-за общего отсутствия единообразия или ясности в научных исследованиях.Срочно необходимы хорошо продуманные исследования диеты, чтобы лучше понять роль диеты в лечении воспалительных заболеваний кишечника. Целью этого обзора является обобщение имеющихся данных по диетическому лечению воспалительных заболеваний кишечника и демонстрация того, что изменение режима питания может быть важным фактором при лечении заболеваний. Обращая внимание на важность диеты при воспалительном заболевании кишечника, специалисты здравоохранения могут лучше поддерживать пациентов и сотрудничать с диетологами для улучшения лечебного питания.
Обращая внимание на важность диеты при воспалительном заболевании кишечника, специалисты здравоохранения могут лучше поддерживать пациентов и сотрудничать с диетологами для улучшения лечебного питания.
Ключевые слова: диета, диетотерапия, питание, диетотерапия, воспалительное заболевание кишечника, язвенный колит, болезнь Крона
1. Введение
Воспалительное заболевание кишечника (ВЗК) — хроническое воспалительное состояние, которое включает язвенный колит (ЯК) и болезнь Крона (CD). CD представляет собой трансмуральное воспалительное заболевание слизистой оболочки желудочно-кишечного тракта, которое может поражать любой компонент желудочно-кишечного тракта, включая тонкий и / или толстый кишечник, полость рта, пищевод, желудок и задний проход.ЯК не является трансмуральным и в основном затрагивает только слизистую оболочку толстой кишки. Пациенты с ВЗК испытывают периоды рецидива (активное заболевание) и клинической ремиссии [1]. Клиническими симптомами ВЗК являются диарея и / или запор, выделение крови или слизи в стуле и спазмы в животе. Кроме того, пациенты с CD могут также испытывать непроходимость кишечника, стриктуры и абсцессы.
Кроме того, пациенты с CD могут также испытывать непроходимость кишечника, стриктуры и абсцессы.
Лекарства — это первая линия терапии при лечении ВЗК. Хирургия обычно предназначена для тех пациентов, которые не переносят лекарства или страдают рефрактерным заболеванием.Основные классы препаратов, используемых при лечении ВЗК, включают 5-аминосалицилаты (5-ASA) (например, сульфасалазин и месаламин), кортикостероиды (например, гидрокортизон, преднизон и преднизолон), иммуномодуляторы (например, азатиоприн, 6-меркаптопурин. , метотрексат и циклоспорин) и биопрепараты (например, инфликсимаб, адалимумаб и ведолизумаб). Хотя многие пациенты хорошо реагируют на фармакотерапию, лекарства могут иметь серьезные побочные эффекты. Среди побочных эффектов, о которых сообщалось, являются гиперчувствительность к лекарствам, нефротоксичность, лихорадка, сыпь, лимфаденопатия, гепатит, панкреатит, обострение диареи, тошнота, рвота, боль в животе, миалгия и повышенный риск лимфомы.Кроме того, приверженность к лечению вызывает беспокойство, поскольку недавнее исследование показало, что примерно четверть пациентов с ВЗК, посещающих клинику третичного уровня, не принимали прописанные лекарства, специфичные для ВЗК [2]. Совершенно очевидно, что внедрение новых стратегий и профилактической медицины имеет решающее значение для благополучия пациентов с ВЗК, чтобы избежать осложнений и побочных эффектов, связанных как с заболеванием, так и с лечением.
Совершенно очевидно, что внедрение новых стратегий и профилактической медицины имеет решающее значение для благополучия пациентов с ВЗК, чтобы избежать осложнений и побочных эффектов, связанных как с заболеванием, так и с лечением.
Эксклюзивное энтеральное питание — это лечебное питание, при котором 100% потребностей пациента в питании удовлетворяются с помощью жидкой формулы питания и вводятся перорально или через зонд для кормления.Обеспечивается исключительно энтеральное питание в течение 6–8 недель, затем постепенно возвращается пероральная диета [3]. У детей с активной БК вместо кортикостероидной терапии можно использовать исключительно энтеральное питание, и было показано, что время до рецидива сокращается [4]. Также было показано, что этот подход положительно влияет на воспалительные изменения, заживление слизистых оболочек, ускоряет рост и общий статус питания у детей [4]. За пределами Японии эксклюзивное энтеральное питание обычно не используется в качестве терапии первой линии у взрослых.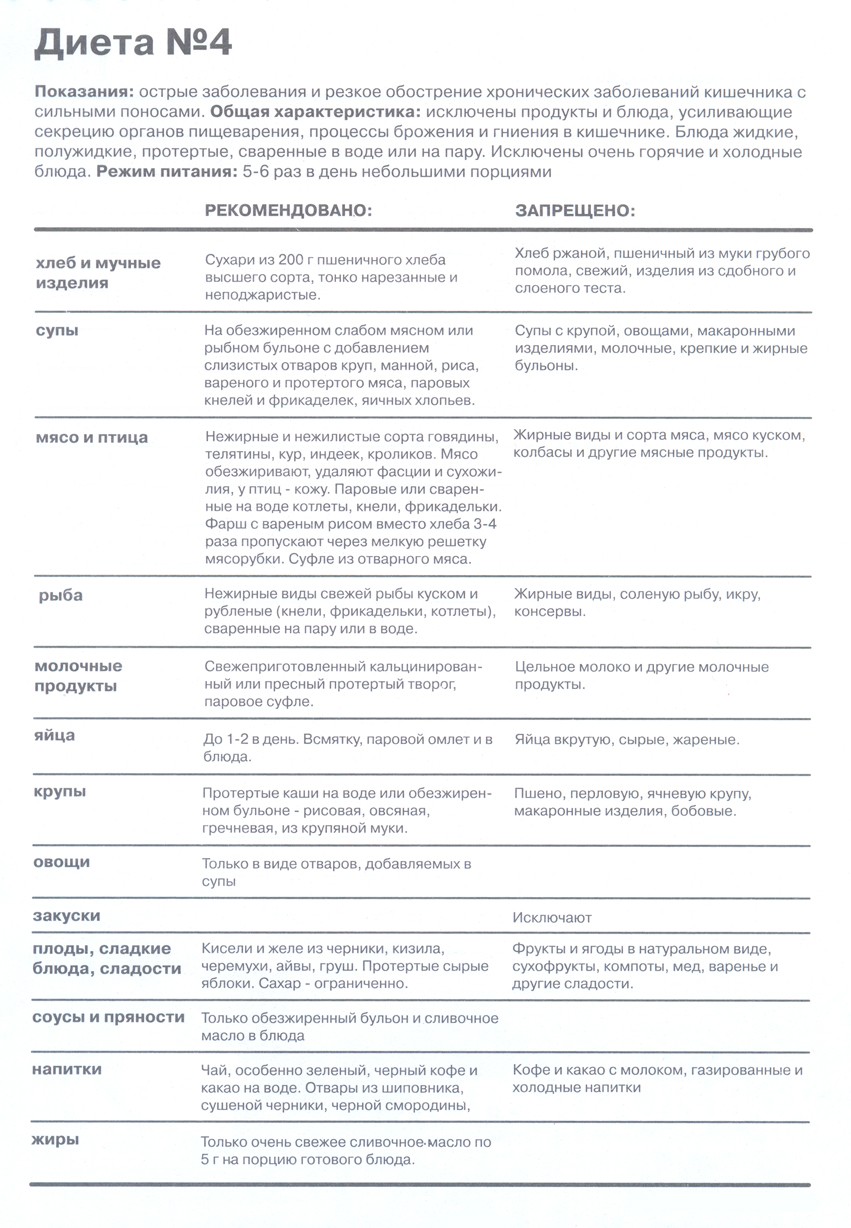 Имеются некоторые доказательства в поддержку использования эксклюзивного энтерального питания в качестве метода лечения у избранной группы взрослых пациентов с БК, особенно у тех, у кого новый диагноз БК, у пациентов с поражением подвздошной кишки и у тех, у кого есть мотивация придерживаться исключительно энтерального питания. режим питания [5].
Имеются некоторые доказательства в поддержку использования эксклюзивного энтерального питания в качестве метода лечения у избранной группы взрослых пациентов с БК, особенно у тех, у кого новый диагноз БК, у пациентов с поражением подвздошной кишки и у тех, у кого есть мотивация придерживаться исключительно энтерального питания. режим питания [5].
ВЗК связана с пищевыми осложнениями как во время рецидива, так и во время клинической ремиссии. Некоторые из пищевых осложнений включают снижение потребления пищи, нарушение всасывания питательных веществ, дефицит макро- или микронутриентов, потерю веса и остеопороз [6,7,8,9,10].Пациенты с ВЗК озабочены едой и диетой [11,12] и используют различные диетические стратегии, пытаясь контролировать или минимизировать желудочно-кишечные расстройства [13], а также улучшить общее состояние здоровья. До 71% пациентов с ВЗК считают, что диета влияет на симптомы их заболевания, при этом 90% пациентов с БК и 71% пациентов с ЯК применяют элиминационную диету в период ремиссии [14,15]. Модификация диеты может вызывать беспокойство, если пациенты резко сокращают или полностью избегают важных с точки зрения питания продуктов / групп продуктов, поскольку это может подвергнуть их повышенному риску развития дефицита питательных веществ [16], а также ухудшить качество жизни.До 77,1% пациентов с ВЗК отказываются от определенных продуктов [14]. Исследование случай-контроль показало значительно более низкое среднесуточное потребление углеводов, мононенасыщенных жиров, клетчатки, кальция и витаминов C, D, E и K по сравнению с контрольной группой в результате исключения молочных продуктов, овощей и фруктов [17 ].
Модификация диеты может вызывать беспокойство, если пациенты резко сокращают или полностью избегают важных с точки зрения питания продуктов / групп продуктов, поскольку это может подвергнуть их повышенному риску развития дефицита питательных веществ [16], а также ухудшить качество жизни.До 77,1% пациентов с ВЗК отказываются от определенных продуктов [14]. Исследование случай-контроль показало значительно более низкое среднесуточное потребление углеводов, мононенасыщенных жиров, клетчатки, кальция и витаминов C, D, E и K по сравнению с контрольной группой в результате исключения молочных продуктов, овощей и фруктов [17 ].
В Интернете имеется огромное количество информации, которая утверждает, что определенные диеты улучшают или усугубляют симптомы, однако лишь несколько тщательных исследований питания изучали определенные диетические факторы как вредные или защищающие от ЯК или БК.Внедрение диетических стратегий и подходов в клиническую практику идет медленно и ограниченно. Общие препятствия на пути реализации на практике включают проблемы, связанные с управлением знаниями, такие как доступ к источникам данных исследований, время для анализа источников, основанных на фактах, и отсутствие навыков для оценки и понимания данных исследований [18]. Помимо управления знаниями, финансовые барьеры, несоответствующий набор навыков и проблемы, связанные с работой с профессиональными дисциплинами и между ними, способствуют отставанию в трансляции знаний [18].В этом обзоре предпринята попытка консолидировать существующие данные о диете / фармокопании и поддержании ремиссии при ВЗК, включая исследования, в которых оценивается связь между потреблением питательных веществ до болезни и группами пищевых продуктов и риском последующего диагноза ВЗК, исследования диетических вмешательств для поддержания ремиссия при ВЗК, а также существующие руководства [19, 20, 21], в свете самых современных ограничений в доказательствах и практике. Основанные на фактических данных диетические рекомендации для пациентов с ВЗК кратко изложены в и и.
Помимо управления знаниями, финансовые барьеры, несоответствующий набор навыков и проблемы, связанные с работой с профессиональными дисциплинами и между ними, способствуют отставанию в трансляции знаний [18].В этом обзоре предпринята попытка консолидировать существующие данные о диете / фармокопании и поддержании ремиссии при ВЗК, включая исследования, в которых оценивается связь между потреблением питательных веществ до болезни и группами пищевых продуктов и риском последующего диагноза ВЗК, исследования диетических вмешательств для поддержания ремиссия при ВЗК, а также существующие руководства [19, 20, 21], в свете самых современных ограничений в доказательствах и практике. Основанные на фактических данных диетические рекомендации для пациентов с ВЗК кратко изложены в и и.
Краткое изложение практических рекомендаций по питанию для поддержания ремиссии при ВЗК.
Таблица 1
Доказательные рекомендации по диете для поддержания ремиссии при ВЗК.
| Заявление | Рекомендация |
|---|---|
| Поощрять высокое потребление клетчатки из пищевых продуктов, особенно из фруктов и овощей [22,23,24,25] | Настоятельно рекомендовать * |
| Избегать n -6 ПНЖК (сафлоровое масло, кукурузное масло, маргарин) и потребление транс-ненасыщенных жирных кислот [23,24,26,27] | Настоятельно рекомендую |
| Поощрять потребление молочных продуктов [28,29] | Рекомендовать † (если переносится) |
| Ограничьте / избегайте рафинированных углеводов, особенно подслащенных и безалкогольных напитков [30] | Рекомендовать |
| Ограничить потребление красного мяса, особенно из говядины, свинины, баранины и мясных продуктов [22,31] | Рекомендовать |
| FODMAP Diet [32,33,34] | Дополнительно ‡ (для управления IBS-overlay) |
| Средиземноморская диета [35,36,37] 9 0040 | Необязательно |
| Конкретная углеводная диета [38,39,40,41] | Нет рекомендаций β |
| Диета с низким содержанием остатков [42] | |
| Полувегетарианская диета [43] | |
| Элиминационная диета на основе IgG4 [44] | |
| IBD-AID [45] | |
| Палеодиета | Нет рекомендаций |
Таблица 2
Рекомендации по питанию для добавок для поддержания ремиссии в IBD.
| Заявление | Тип ВЗК | Рекомендация |
|---|---|---|
| Витамин D (минимум 1200 МЕ / день) [47,48,49,50,51] | Оба | Настоятельно рекомендую * (цель для уровней сыворотки 25 (OHD)> 75 нмоль / л |
| Подорожник (минимум 4 грамма / день) [52,53] | UC | Рекомендовать † |
| Куркумин (1 грамм два раза в день) [54 , 55,56] | UC | Дополнительно ‡ |
| Добавка из овсяных отрубей (20 г / день) [57] | UC | Дополнительно |
| Продовольственный продукт из проросшего ячменя (минимум 20 г / день) [58 , 59,60] | UC | Дополнительно |
| Пшеничные отруби (1/2 стакана в день) [61] | CD | Дополнительно |
2.
 Поиск литературы
Поиск литературыСистематический поиск литературы проводился с использованием PubMed, EMBASE и Medline с 1966 по октябрь 2016 года с использованием терминов в медицинских предметных заголовках (MeSH) «воспалительное заболевание кишечника», «болезнь Крона», «язвенный колит», «питание», «Диетотерапия», «диета» и «диетотерапия». Также использовались поиски, содержащие релевантные синонимы и комбинации вышеуказанных терминов. Мы рассмотрели интервенционные исследования, систематические обзоры, а также соответствующие обзорные статьи, содержащие практические рекомендации с акцентом на взрослых.Исследования, посвященные активной ВЗК, энтеральному / парентеральному питанию и ВЗК с колэктомией / стомией, были исключены из обзора.
3. Диета в этиологии ВЗК
ВЗК традиционно считалась болезнью Западного полушария, однако заболеваемость растет в Японии, Гонконге, Корее и Восточной Европе [62,63]. Хотя все еще реже, рост заболеваемости ВЗК также выявляется в Южной Африке, Южной Америке и Саудовской Аравии [64, 65, 66]. Резкий рост заболеваемости ВЗК, особенно в Южной Азии, Индии и Японии, где заболеваемость традиционно была низкой, предполагает, что факторы окружающей среды, такие как западная диета, играют важную роль в патогенезе болезни [67, 68, 69 ].Эта гипотеза дополнительно подтверждается ростом заболеваемости иммигрантами в Западном полушарии. Миграция из страны с низкой заболеваемостью в страну с более высокой заболеваемостью увеличивает риск развития ВЗК, особенно у детей первого поколения [70]. Долгое время считалось, что состав диеты способствует развитию ВЗК. Таким образом, диета и нутриенты являются важными факторами окружающей среды, которые необходимо учитывать в этиологии ВЗК [22,71].
Резкий рост заболеваемости ВЗК, особенно в Южной Азии, Индии и Японии, где заболеваемость традиционно была низкой, предполагает, что факторы окружающей среды, такие как западная диета, играют важную роль в патогенезе болезни [67, 68, 69 ].Эта гипотеза дополнительно подтверждается ростом заболеваемости иммигрантами в Западном полушарии. Миграция из страны с низкой заболеваемостью в страну с более высокой заболеваемостью увеличивает риск развития ВЗК, особенно у детей первого поколения [70]. Долгое время считалось, что состав диеты способствует развитию ВЗК. Таким образом, диета и нутриенты являются важными факторами окружающей среды, которые необходимо учитывать в этиологии ВЗК [22,71].
3.1.Схема западной диеты
Современная диета значительно отличается от традиционной диеты предыдущих поколений, когда распространенность ВЗК была значительно ниже. В западной диете преобладает повышенное потребление рафинированного сахара, полиненасыщенных жиров омега-6 и фаст-фуда в сочетании с диетой с дефицитом фруктов, овощей и клетчатки [72]. Большая часть сегодняшних продуктов питания обрабатывалась, изменялась, хранилась и транспортировалась на большие расстояния, в отличие от традиционной диеты, когда продукты местного производства потреблялись вскоре после сбора урожая.Предполагается, что этот переход к западной диете увеличивает провоспалительные цитокины, модулирует кишечную проницаемость и изменяет микробиоту кишечника, способствуя хроническому воспалению в кишечнике слабой степени [73]. Диета, содержащая провоспалительные продукты, является важным фактором риска развития ЯК. Исследование случай-контроль, проведенное в Иране с участием недавно диагностированных пациентов с ЯК ( n = 62 пациента с ЯК, 124 контрольной группы), показало, что у субъектов, у которых был более высокий диетический воспалительный индекс (провоспалительная диета), был повышенный риск развития ЯК (шансы Соотношение (OR): 1.55, 95% доверительный интервал (ДИ): 1,04–2,32) [23]. Авторы пришли к выводу, что поощрение потребления большего количества противовоспалительных диетических факторов, таких как продукты на растительной основе, богатые клетчаткой и фитохимическими веществами, и сокращение потребления провоспалительных факторов, таких как жареные или обработанные продукты, богатые трансжирными кислотами, могут быть потенциальная стратегия снижения риска ЯК.
Большая часть сегодняшних продуктов питания обрабатывалась, изменялась, хранилась и транспортировалась на большие расстояния, в отличие от традиционной диеты, когда продукты местного производства потреблялись вскоре после сбора урожая.Предполагается, что этот переход к западной диете увеличивает провоспалительные цитокины, модулирует кишечную проницаемость и изменяет микробиоту кишечника, способствуя хроническому воспалению в кишечнике слабой степени [73]. Диета, содержащая провоспалительные продукты, является важным фактором риска развития ЯК. Исследование случай-контроль, проведенное в Иране с участием недавно диагностированных пациентов с ЯК ( n = 62 пациента с ЯК, 124 контрольной группы), показало, что у субъектов, у которых был более высокий диетический воспалительный индекс (провоспалительная диета), был повышенный риск развития ЯК (шансы Соотношение (OR): 1.55, 95% доверительный интервал (ДИ): 1,04–2,32) [23]. Авторы пришли к выводу, что поощрение потребления большего количества противовоспалительных диетических факторов, таких как продукты на растительной основе, богатые клетчаткой и фитохимическими веществами, и сокращение потребления провоспалительных факторов, таких как жареные или обработанные продукты, богатые трансжирными кислотами, могут быть потенциальная стратегия снижения риска ЯК. Это было одно из первых исследований, в которых изучали диетический воспалительный индекс как результат развития ЯК. В нескольких крупномасштабных исследованиях была предпринята попытка выяснить, какие диетические компоненты связаны с риском ВЗК [22,24,26,27].В целом это говорит о том, что западная диета является фактором риска ВЗК.
Это было одно из первых исследований, в которых изучали диетический воспалительный индекс как результат развития ЯК. В нескольких крупномасштабных исследованиях была предпринята попытка выяснить, какие диетические компоненты связаны с риском ВЗК [22,24,26,27].В целом это говорит о том, что западная диета является фактором риска ВЗК.
3.2. Потребление углеводов как фактор риска ВЗК
Систематический обзор ( n = 19 исследований с 2609 субъектами ВЗК) сообщил об отрицательной связи между диетической клетчаткой (OR 0,12, 95% CI: 0,04–0,37) и потреблением фруктов (OR: 0,2, 95% ДИ: 0,1–0,9) и риск БК [22]. Растворимая клетчатка из фруктов может оказывать защитное действие на БК [24]. Высокое потребление овощей может быть связано со снижением риска ЯК (диапазон OR 0.32–0,75) [22]. Европейское исследование рака и питания ( n = 366 351 с 256 случаями UC и 117 CD, и четыре соответствующих контроля на случай) показало, что повышенное потребление сахара и безалкогольных напитков с низким потреблением овощей было положительно связано с Риск ЯК (ОШ 1,31, 95% ДИ: 0,85–2,02; p = 0,05) [25]. Повышенное потребление сладкого положительно связано с CD (OR: 2,83, 95% CI: 1,38–5,83) и UC (OR: 2,86, 95% CI: 1,24–6,57) [30].В целом это говорит о том, что, хотя рафинированные и обработанные углеводы и потребление подслащенных напитков являются факторами риска ВЗК, сложные углеводы, включая фрукты, овощи и клетчатку, должны быть включены в рацион для лечения ВЗК.
Повышенное потребление сладкого положительно связано с CD (OR: 2,83, 95% CI: 1,38–5,83) и UC (OR: 2,86, 95% CI: 1,24–6,57) [30].В целом это говорит о том, что, хотя рафинированные и обработанные углеводы и потребление подслащенных напитков являются факторами риска ВЗК, сложные углеводы, включая фрукты, овощи и клетчатку, должны быть включены в рацион для лечения ВЗК.
3.3. Потребление белка как фактор риска ВЗК
Большое проспективное когортное исследование ( n = 67 581), завершенное в течение 10,5-летнего периода, показало, что высокое потребление белка, особенно животного белка (мяса, а не молочных продуктов), было положительно связано с повышенный риск ВЗК [31].Систематический обзор ( n = 2609 пациентов с ВЗК; 19 исследований) сообщил о связи высокого общего потребления белка с развитием ЯК (диапазон OR 0,2–3,7) и CD (диапазон OR 0,45–3,34) [22]. Высокое потребление белка было связано с 3,3-кратным повышением риска ВЗК, что позволяет предположить, что диета с высоким содержанием животного белка является основным фактором риска развития ВЗК.
3.4. Потребление молочных продуктов как фактор риска ВЗК
Европейское исследование рака и питания обнаружило, что у людей, потреблявших молоко, вероятность развития БК значительно снижалась (ОШ: 0.30, 95% ДИ: 0,13–0,65), что свидетельствует о защитном эффекте при потреблении молочных продуктов [28]. Отдельные молочные продукты состояли из молока, йогурта и сыра с различным содержанием жира (например, жирные, обезжиренные, полуобезжиренные и неуточненные). Это подтверждается исследованием типа случай-контроль у детей ( n = 130 пациентов с БК и n = 202 контрольной группы), которое продемонстрировало, что потребление молочных продуктов не было связано с CD (OR: 0,86, 95% CI: 0,42– 1,76, p = 0,65) [29].В целом потребление молочных продуктов не является фактором риска ВЗК.
3.5. Потребление жиров с пищей как фактор риска ВЗК
Существуют противоречивые данные о связи между потреблением жиров с пищей и развитием ВЗК, поскольку многие исследования являются ретроспективными и используют небольшие размеры выборки. Однако в очень большом долгосрочном проспективном исследовании ( n = 170 805), завершенном более 26 лет, не было обнаружено значимой связи повышенного риска развития БК или ЯК с общим потреблением жиров, насыщенных жирных кислот (НЖК) и мононенасыщенные жирные кислоты (MUFA) [26], что было хорошо подтверждено другими исследованиями [74,75,76].Растущее количество научных данных указывает на то, что тип средиземноморской диеты связан со значительным улучшением состояния здоровья [77,78] и снижением маркеров воспаления у людей [79]. Предполагается, что защитный эффект обусловлен балансом жиров, который включает MUFA, SFA и потребление рыбы [80]. Хотя несколько исследований действительно показывают, что МНЖК полезны при колите, исследования влияния НЖК и ПНЖК на здоровье кишечника противоречивы.
Однако в очень большом долгосрочном проспективном исследовании ( n = 170 805), завершенном более 26 лет, не было обнаружено значимой связи повышенного риска развития БК или ЯК с общим потреблением жиров, насыщенных жирных кислот (НЖК) и мононенасыщенные жирные кислоты (MUFA) [26], что было хорошо подтверждено другими исследованиями [74,75,76].Растущее количество научных данных указывает на то, что тип средиземноморской диеты связан со значительным улучшением состояния здоровья [77,78] и снижением маркеров воспаления у людей [79]. Предполагается, что защитный эффект обусловлен балансом жиров, который включает MUFA, SFA и потребление рыбы [80]. Хотя несколько исследований действительно показывают, что МНЖК полезны при колите, исследования влияния НЖК и ПНЖК на здоровье кишечника противоречивы.
Диетические n -6 ПНЖК, в частности линолевая кислота, вовлечены в этиологию ВЗК.Диетические n -6 ПНЖК представляют собой незаменимые жирные кислоты, в большом количестве присутствующие в красном мясе, кулинарных маслах (сафлоровом и кукурузном масле) и маргаринах. Проспективное когортное исследование ( n = 203 193), проведенное в течение четырех лет, показало, что потребление линолевой кислоты было связано с повышенным риском ЯК (OR: 2,49, 95% ДИ: 1,23–5,07, p = 0,01) [27 ]. Дальнейший анализ исследования Европейского исследования рака и питания ( n = 260 686) за пять лет выявил повышенный риск ЯК при более высоком общем потреблении ПНЖК (тенденция по квартилям OR = 1.19 (95% ДИ: 0,99–1,43) p = 0,07) [74], что также было подтверждено систематическим обзором ( n = 2609 пациентов с ВЗК), в котором изучалось потребление питательных веществ до болезни и последующее развитие UC [22]. Исследование случай-контроль при БК показало, что повышенное общее потребление ПНЖК было положительно связано с риском БК (ОШ: 2,31, 95% ДИ: 1,12–4,79) [30].
Проспективное когортное исследование ( n = 203 193), проведенное в течение четырех лет, показало, что потребление линолевой кислоты было связано с повышенным риском ЯК (OR: 2,49, 95% ДИ: 1,23–5,07, p = 0,01) [27 ]. Дальнейший анализ исследования Европейского исследования рака и питания ( n = 260 686) за пять лет выявил повышенный риск ЯК при более высоком общем потреблении ПНЖК (тенденция по квартилям OR = 1.19 (95% ДИ: 0,99–1,43) p = 0,07) [74], что также было подтверждено систематическим обзором ( n = 2609 пациентов с ВЗК), в котором изучалось потребление питательных веществ до болезни и последующее развитие UC [22]. Исследование случай-контроль при БК показало, что повышенное общее потребление ПНЖК было положительно связано с риском БК (ОШ: 2,31, 95% ДИ: 1,12–4,79) [30].
Когорты исследования здоровья медсестер ( n = 170 805 женщин с 269 случаями БК и 338 случаями ЯК) сообщили о высоком, долгосрочном потреблении транс-ненасыщенных жирных кислот, связанных с тенденцией к увеличению заболеваемости. UC (HR 1.34, 95% ДИ: 0,94–1,92), но не CD [26]. Повышенный относительный риск развития ВЗК также был связан с частым употреблением фаст-фуда (фаст-фуд богат транс-ненасыщенными жирными кислотами) [81,82]. Относительный риск, связанный с потреблением фаст-фуда не менее двух раз в неделю, оценивался в 3,4 (95% ДИ: 1,3–9,3) для БК и 3,9 (95% ДИ: 1,4–10,6) для ЯК [82]. Частое употребление фаст-фуда, определяемое как более чем один раз в неделю, было значительно связано с риском ЯК (43%, OR: 5.78, 95% ДИ: 2,38–14,03) и CD (27%, ОШ: 2,84, 95% ДИ: 1,21–6,64) [81].
UC (HR 1.34, 95% ДИ: 0,94–1,92), но не CD [26]. Повышенный относительный риск развития ВЗК также был связан с частым употреблением фаст-фуда (фаст-фуд богат транс-ненасыщенными жирными кислотами) [81,82]. Относительный риск, связанный с потреблением фаст-фуда не менее двух раз в неделю, оценивался в 3,4 (95% ДИ: 1,3–9,3) для БК и 3,9 (95% ДИ: 1,4–10,6) для ЯК [82]. Частое употребление фаст-фуда, определяемое как более чем один раз в неделю, было значительно связано с риском ЯК (43%, OR: 5.78, 95% ДИ: 2,38–14,03) и CD (27%, ОШ: 2,84, 95% ДИ: 1,21–6,64) [81].
Было высказано предположение, что прием длинноцепочечных n -3 ПНЖК (докозапентаеновая кислота, эйкозапентаеновая кислота, докозагексаеновая кислота), известных как омега-3, может быть полезным для пациентов с ВЗК. Считается, что положительный эффект обусловлен противовоспалительными свойствами ПНЖК n -3; однако клинические и экспериментальные исследования показали противоречивые результаты [83]. Мета-анализы не показали положительного эффекта приема добавок рыбьего жира в поддержании ремиссии при БК и ЯК [84,85,86]. Потребление с пищей n -3 ПНЖК было обратно пропорционально связано с риском ЯК, тогда как связи с БК не обнаружено [26]. Европейское исследование рака и питания ( n = 203 193) обнаружило отрицательную связь с развитием ЯК с увеличением потребления с пищей n -3 ПНЖК, в частности докозагексаеновой кислоты (OR: 0,23, 95% ДИ: 0,06). до 0,97) [27], и подтверждается европейским исследованием рака и питания — Норфолк ( n = 26 639) (OR: 0.43, 95% ДИ: 0,22–0,86) [57]. Два исследования случай-контроль в CD сообщают, что диета с регулярным потреблением рыбы оказывала защитный эффект на развитие CD (OR 0,52, 95% CI: 0,33–0,80, p = 0,003) и (OR 0,46, 95% ДИ: 0,20–1,06, p = 0,02) [29,69].
Потребление с пищей n -3 ПНЖК было обратно пропорционально связано с риском ЯК, тогда как связи с БК не обнаружено [26]. Европейское исследование рака и питания ( n = 203 193) обнаружило отрицательную связь с развитием ЯК с увеличением потребления с пищей n -3 ПНЖК, в частности докозагексаеновой кислоты (OR: 0,23, 95% ДИ: 0,06). до 0,97) [27], и подтверждается европейским исследованием рака и питания — Норфолк ( n = 26 639) (OR: 0.43, 95% ДИ: 0,22–0,86) [57]. Два исследования случай-контроль в CD сообщают, что диета с регулярным потреблением рыбы оказывала защитный эффект на развитие CD (OR 0,52, 95% CI: 0,33–0,80, p = 0,003) и (OR 0,46, 95% ДИ: 0,20–1,06, p = 0,02) [29,69].
Было выдвинуто предположение, что общее соотношение n -3 ПНЖК: n -6 PUFA, обнаруженных в пище, является важным фактором. Одно проспективное когортное исследование [87] и одно исследование случай-контроль [29] сообщают, что высокое соотношение n -3PUFA: n -6 PUFA в рационе обратно связано с риском ВЗК. В поддержку этого объяснения было обнаружено, что исследование диетических вмешательств, направленное на увеличение соотношения n -3 ПНЖК: n -6 ПНЖК, было эффективным в поддержании ремиссии заболевания у пациентов как с ЯК, так и с БК, за счет увеличения n. -3 Потребление ПНЖК [88]. В целом не похоже, что следует избегать полножирных диет, однако следует употреблять жиры, включая диеты, богатые оливковым маслом, молочными продуктами и рыбой, но не таблетки рыбьего жира, избегая при этом большого потребления растительных масел, богатых n -6 ПНЖК. .
В поддержку этого объяснения было обнаружено, что исследование диетических вмешательств, направленное на увеличение соотношения n -3 ПНЖК: n -6 ПНЖК, было эффективным в поддержании ремиссии заболевания у пациентов как с ЯК, так и с БК, за счет увеличения n. -3 Потребление ПНЖК [88]. В целом не похоже, что следует избегать полножирных диет, однако следует употреблять жиры, включая диеты, богатые оливковым маслом, молочными продуктами и рыбой, но не таблетки рыбьего жира, избегая при этом большого потребления растительных масел, богатых n -6 ПНЖК. .
Таким образом, несколько эпидемиологических исследований предоставляют убедительные доказательства роли пищи в патогенезе ВЗК. Более того, рост заболеваемости ВЗК в странах, в которых ранее была очень низкая заболеваемость, предполагает, что индустриализация и переход на западную диету могут быть фактором риска развития ВЗК. Снижение потребления фруктов и, возможно, овощей, приводящее к снижению общего потребления клетчатки, с высоким потреблением мяса, фаст-фуда и трансжирных кислот, по-видимому, связано с общим повышением риска развития ВЗК [71].
4. Диетические вмешательства и ВЗК
Диетические вмешательства изучались при ВЗК в попытке управлять активным заболеванием или поддерживать ремиссию. Было показано, что некоторые из них эффективны, однако точные компоненты, которые важны для каждой диеты, четко не определены или часто противоречат друг другу. В отсутствие золотого стандарта рекомендации по питанию, предоставляемые в настоящее время специалистами здравоохранения, основаны на «наилучших имеющихся данных».
4.1. Диета с низким содержанием остатков
Диета с низким содержанием остатков часто рекомендуется для лечения острого обострения ВЗК, особенно у пациентов со стриктурами или сужением кишечника.Хотя диета с низким содержанием остатков назначается для краткосрочного использования, в клинической практике пациенты часто придерживаются диеты в течение длительного времени. Основная цель диеты с низким содержанием остатков — уменьшить частоту и объем стула и снизить риск кишечной непроходимости [89]. В литературе имеются разночтения относительно фактического состава диет с низким содержанием клетчатки и / или остатков. Диета с низким содержанием остатков требует отказа от цельнозерновых, бобовых и всех фруктов и овощей (кроме бананов и картофеля без кожицы), молочных продуктов и клетчатки [89].Это не то же самое, что диета с низким содержанием клетчатки, которая исключает только нерастворимую клетчатку. Проспективное исследование с участием субъектов с активной CD ( n = 70), которое сравнивало диету с низким содержанием остатков и неограниченную диету, не обнаружило различий в результатах, включая симптомы, потребность в госпитализации, потребность в хирургии, новые осложнения, статус питания или послеоперационный период. рецидив [42]. Из-за отсутствия доказательств, по-видимому, нет причин ограничивать остатки из рациона, однако, по некоторым данным, пациенты с БК с обструктивными симптомами и стриктурами сообщают об улучшении симптомов при соблюдении диеты с пониженным содержанием клетчатки (общее суточное потребление клетчатки <10 г) [89 , 90].
В литературе имеются разночтения относительно фактического состава диет с низким содержанием клетчатки и / или остатков. Диета с низким содержанием остатков требует отказа от цельнозерновых, бобовых и всех фруктов и овощей (кроме бананов и картофеля без кожицы), молочных продуктов и клетчатки [89].Это не то же самое, что диета с низким содержанием клетчатки, которая исключает только нерастворимую клетчатку. Проспективное исследование с участием субъектов с активной CD ( n = 70), которое сравнивало диету с низким содержанием остатков и неограниченную диету, не обнаружило различий в результатах, включая симптомы, потребность в госпитализации, потребность в хирургии, новые осложнения, статус питания или послеоперационный период. рецидив [42]. Из-за отсутствия доказательств, по-видимому, нет причин ограничивать остатки из рациона, однако, по некоторым данным, пациенты с БК с обструктивными симптомами и стриктурами сообщают об улучшении симптомов при соблюдении диеты с пониженным содержанием клетчатки (общее суточное потребление клетчатки <10 г) [89 , 90].
Исследования все еще находятся в зачаточном состоянии, однако появляется все больше доказательств связи между ВЗК и изменением микробиоты кишечника. Западная диета, характеризующаяся повышенным потреблением ПНЖК, животного белка и сахара, а также пониженным потреблением клетчатки, считается фактором, способствующим дисбактериозу [91,92,93]. Небольшое пилотное исследование CD ( n = 6) сообщило о заметном снижении микробного разнообразия при диете с низким содержанием остатков [94]. Это вызывает беспокойство, учитывая, что низкое разнообразие микробиоты связано с множеством хронических заболеваний [95].Более того, улучшение маркеров воспаления не было продемонстрировано при диете с низким содержанием остатков при БК [96]. Требуются дополнительные исследования; однако диета с низким содержанием остатков потенциально может иметь негативные последствия для ВЗК, поэтому длительный отказ от клетчатки не рекомендуется [90].
4.2. Полувегетарианская диета
Проспективное исследование, проведенное в Японии на госпитализированных пациентах с CD ( n = 22), изучало влияние полувегетарианской диеты на поддержание ремиссии [43]. Диета была лакто-ово-вегетарианской, при которой разрешались яйца и молоко, небольшие порции мяса предлагались раз в две недели, а рыба — еженедельно. Уровень ремиссии, достигнутый при использовании полувегетарианской диеты, составил 100% через год и 92% через два года. Полувегетарианская диета показала значительную профилактику рецидивов по сравнению с людьми, соблюдающими всеядную диету ( p = 0,003 логарифмического критерия). Основываясь на этих наблюдениях, полувегетарианская диета может быть очень эффективным способом поддержания ремиссии БК.Хотя это исследование является многообещающим, необходимы крупные рандомизированные контрольные исследования для подтверждения эффективности этого типа диеты для пациентов с ВЗК.
Диета была лакто-ово-вегетарианской, при которой разрешались яйца и молоко, небольшие порции мяса предлагались раз в две недели, а рыба — еженедельно. Уровень ремиссии, достигнутый при использовании полувегетарианской диеты, составил 100% через год и 92% через два года. Полувегетарианская диета показала значительную профилактику рецидивов по сравнению с людьми, соблюдающими всеядную диету ( p = 0,003 логарифмического критерия). Основываясь на этих наблюдениях, полувегетарианская диета может быть очень эффективным способом поддержания ремиссии БК.Хотя это исследование является многообещающим, необходимы крупные рандомизированные контрольные исследования для подтверждения эффективности этого типа диеты для пациентов с ВЗК.
4.3. FODMAPs Diet
Диета с низким содержанием ферментируемых олигосахаридов, дисахаридов, моносахаридов и полиолов (FODMAP) состоит из исключения продуктов с высоким содержанием ферментируемых, но плохо усваиваемых углеводов и полиолов в течение шести-восьми недель [97]. FODMAP включают фруктозу, лактозу, фрукто- и галактоолигосахариды (фруктаны и галактаны) и полиолы (сорбит, маннит, ксилит и мальтит) [97].
FODMAP включают фруктозу, лактозу, фрукто- и галактоолигосахариды (фруктаны и галактаны) и полиолы (сорбит, маннит, ксилит и мальтит) [97].
Общие пищевые источники продуктов, содержащих FODMAPS, следующие: (1) фруктаны: лук, чеснок и пшеница; (2) фруктоза: фрукты и фруктовые продукты, мед и продукты с добавлением подсластителей с высоким содержанием фруктозы; (3) лактоза: в основном молочные продукты; (4) олигосахариды: бобовые, орехи, семена, некоторые зерна; и (5) полиолы: фрукты и овощи и продукты без сахара. После исчезновения симптомов диетолог направляет пациентов, как постепенно возвращать продукты с высоким содержанием ферментируемых углеводов, чтобы определить индивидуальную переносимость определенных FODMAP.
Достоверные данные подтверждают эффективность диеты с низким содержанием FODMAP для лечения симптомов синдрома раздраженного кишечника (СРК), особенно уменьшения вздутия живота, боли и диареи [98,99]. Симптомы, подобные СРК, распространены при ВЗК и были зарегистрированы у 57% пациентов с БК и у 33% пациентов с ЯК [100], поэтому диета с низким содержанием FODMAP была предложена для ведения пациентов с ВЗК с СРК. наложение. Было проведено три ретроспективных исследования по оценке диеты с низким содержанием FODMAP при ВЗК [32,33,34].Ретроспективное исследование 72 пациентов с ВЗК, получавших диетическое вмешательство с упором на диету с низким содержанием FODMAP, показало, что каждый второй пациент сообщил о значительном улучшении абдоминальных симптомов, боли в животе, вздутие живота, ветра и диареи ( p <0,02 для всех симптомов) [ 32]. Во-вторых, анализ электронных историй болезни 88 пациентов с ВЗК с функциональными кишечными симптомами, которые получали рекомендации по диете с низким содержанием FODMAP, выявил значительное уменьшение симптомов любой степени тяжести (легкой, средней или тяжелой) боли в животе ( p <0.001), вздутие живота ( p <0,001), метеоризм ( p = 0,041), отрыжка ( p = 0,001), неполное опорожнение ( p = 0,012), тошнота ( p = 0,011) и изжога ( p = 0,035) [33]. Наблюдалось улучшение консистенции и частоты стула, включая увеличение «нормальной» формы стула ( p = 0,002) и «нормальной» частоты стула ( p <0,001) [33].
наложение. Было проведено три ретроспективных исследования по оценке диеты с низким содержанием FODMAP при ВЗК [32,33,34].Ретроспективное исследование 72 пациентов с ВЗК, получавших диетическое вмешательство с упором на диету с низким содержанием FODMAP, показало, что каждый второй пациент сообщил о значительном улучшении абдоминальных симптомов, боли в животе, вздутие живота, ветра и диареи ( p <0,02 для всех симптомов) [ 32]. Во-вторых, анализ электронных историй болезни 88 пациентов с ВЗК с функциональными кишечными симптомами, которые получали рекомендации по диете с низким содержанием FODMAP, выявил значительное уменьшение симптомов любой степени тяжести (легкой, средней или тяжелой) боли в животе ( p <0.001), вздутие живота ( p <0,001), метеоризм ( p = 0,041), отрыжка ( p = 0,001), неполное опорожнение ( p = 0,012), тошнота ( p = 0,011) и изжога ( p = 0,035) [33]. Наблюдалось улучшение консистенции и частоты стула, включая увеличение «нормальной» формы стула ( p = 0,002) и «нормальной» частоты стула ( p <0,001) [33]. Ретроспективное перекрестное исследование ( n = 49) было проведено для изучения долгосрочной приверженности и влияния на течение заболевания у пациентов с ВЗК, получавших диету с низким содержанием FODMAP [34].Сорок три процента пациентов с ВЗК сообщили о полной эффективности ( p = 0,08) с наибольшим уменьшением боли в животе (63%) и вздутия живота (83%) при диете с низким содержанием FODMAP. Доля пациентов с нормальным стулом увеличилась на 66% в группе ВЗК ( p < 0,001). У 24% пациентов с ВЗК симптомы исчезли при соблюдении диеты. Таким образом, хотя не было завершено никаких проспективных исследований по вмешательству при ВЗК, ретроспективные данные свидетельствуют о том, что диета с низким содержанием FODMAP может быть стратегией для лечения сопутствующих функциональных симптомов кишечника в этой популяции.
Ретроспективное перекрестное исследование ( n = 49) было проведено для изучения долгосрочной приверженности и влияния на течение заболевания у пациентов с ВЗК, получавших диету с низким содержанием FODMAP [34].Сорок три процента пациентов с ВЗК сообщили о полной эффективности ( p = 0,08) с наибольшим уменьшением боли в животе (63%) и вздутия живота (83%) при диете с низким содержанием FODMAP. Доля пациентов с нормальным стулом увеличилась на 66% в группе ВЗК ( p < 0,001). У 24% пациентов с ВЗК симптомы исчезли при соблюдении диеты. Таким образом, хотя не было завершено никаких проспективных исследований по вмешательству при ВЗК, ретроспективные данные свидетельствуют о том, что диета с низким содержанием FODMAP может быть стратегией для лечения сопутствующих функциональных симптомов кишечника в этой популяции.
4.4. Диеты исключения
Энтеральное питание часто используется в качестве дополнительной терапии для поддержания ремиссии при БК, особенно в Японии. В рандомизированном контрольном исследовании половину потребности в питании испытуемые получали с помощью элементарной формулы (принимаемой перорально ( n = 21) или через назогастральный зонд ( n = 5)), а оставшиеся 50% потребности в питании. соблюдается за счет неограниченной диеты [101]. Частота рецидивов в группе полуэлементной диеты была значительно ниже (34.6% против 64,0%; многомерное отношение рисков 0,40 (95% ДИ: 0,16–0,98)), чем в контрольной группе, после среднего периода наблюдения 11,9 месяцев. В последующем отчете по этому исследованию говорилось, что элементарная диета в качестве поддерживающей терапии БК способствовала поддержанию пациентов в клинически стабильном состоянии, не влияя на качество их жизни и не приводя к дополнительным медицинским расходам [102].
В рандомизированном контрольном исследовании половину потребности в питании испытуемые получали с помощью элементарной формулы (принимаемой перорально ( n = 21) или через назогастральный зонд ( n = 5)), а оставшиеся 50% потребности в питании. соблюдается за счет неограниченной диеты [101]. Частота рецидивов в группе полуэлементной диеты была значительно ниже (34.6% против 64,0%; многомерное отношение рисков 0,40 (95% ДИ: 0,16–0,98)), чем в контрольной группе, после среднего периода наблюдения 11,9 месяцев. В последующем отчете по этому исследованию говорилось, что элементарная диета в качестве поддерживающей терапии БК способствовала поддержанию пациентов в клинически стабильном состоянии, не влияя на качество их жизни и не приводя к дополнительным медицинским расходам [102].
Исключающие диеты могут быть неприятными и трудными для соблюдения, поэтому в двойном слепом рандомизированном контрольном исследовании оценивалась эффективность исключающей диеты с контролем IgG4 у субъектов с CD [44]. Цель исследования состояла в том, чтобы определить, каких компонентов рациона следует избегать из-за индукции IgG4, антитела, вырабатываемого в ответ на хроническое воздействие антигенного стимула, такого как пищевой антиген. Предполагается, что диетические белковые антигены могут способствовать сохранению воспаления при БК в результате предшествующей сенсибилизации. Титры IgG4 были протестированы для 16 распространенных типов пищи. Субъекты в группе лечения удаляли четыре типа пищи с наивысшим титром антител в течение четырех недель, тогда как в контрольной группе удаляли четыре типа пищи с самым низким титром антител.Исследователи обнаружили значительное улучшение качества жизни, измеренное с помощью краткого опросника по воспалительным заболеваниям кишечника (3,05 (0,01–6,11) p <0,05), и показателей активности заболевания, измеренных с помощью индекса активности болезни Крона (41 (10,4–71,5) ). p = 0,009). Сорок один процент субъектов, получавших лечение, испытали улучшение индекса активности болезни Крона> 100, тогда как 16% участников контрольной группы испытали улучшение.
Цель исследования состояла в том, чтобы определить, каких компонентов рациона следует избегать из-за индукции IgG4, антитела, вырабатываемого в ответ на хроническое воздействие антигенного стимула, такого как пищевой антиген. Предполагается, что диетические белковые антигены могут способствовать сохранению воспаления при БК в результате предшествующей сенсибилизации. Титры IgG4 были протестированы для 16 распространенных типов пищи. Субъекты в группе лечения удаляли четыре типа пищи с наивысшим титром антител в течение четырех недель, тогда как в контрольной группе удаляли четыре типа пищи с самым низким титром антител.Исследователи обнаружили значительное улучшение качества жизни, измеренное с помощью краткого опросника по воспалительным заболеваниям кишечника (3,05 (0,01–6,11) p <0,05), и показателей активности заболевания, измеренных с помощью индекса активности болезни Крона (41 (10,4–71,5) ). p = 0,009). Сорок один процент субъектов, получавших лечение, испытали улучшение индекса активности болезни Крона> 100, тогда как 16% участников контрольной группы испытали улучшение. Исключение молока, свинины, говядины и яиц сильнее всего ассоциировалось с улучшением.Это исследование было недостаточно мощным, однако оно продемонстрировало клинические улучшения, и этот новый подход к диетическому лечению ВЗК действительно требует дальнейших исследований.
Исключение молока, свинины, говядины и яиц сильнее всего ассоциировалось с улучшением.Это исследование было недостаточно мощным, однако оно продемонстрировало клинические улучшения, и этот новый подход к диетическому лечению ВЗК действительно требует дальнейших исследований.
4.5. Новые противовоспалительные диетические методы лечения
Хотя точная этиология ВЗК остается неясной, все больше данных свидетельствует о том, что микробиом желудочно-кишечного тракта играет решающую роль в патогенезе заболевания [103,104]. Манипулирование микробиомом желудочно-кишечного тракта с помощью диетических вмешательств в попытке уменьшить системное воспаление все чаще рекомендуется в качестве дополнения к продолжающейся медикаментозной терапии.Противовоспалительная диета (IBD-AID) — это диетический подход, разработанный для решения проблемы адекватности питательных веществ, мальабсорбции и симптомов [45]. IBD-AID ограничивает потребление определенных углеводов (лактозы, рафинированных и обработанных сложных углеводов), включает потребление пре- и пробиотических продуктов и изменяет потребление жирных кислот с пищей, в частности, уменьшая общее количество жиров, насыщенных жиров, устраняя гидрогенизированные масла, и поощрение увеличения потребления продуктов, богатых n -3 ПНЖК. Ретроспективная серия случаев с использованием IBD-AID показала, что у субъектов, которые пытались соблюдать диету ( n = 40), 60% сообщили об уменьшении симптомов, включая снижение частоты стула (самоотчет пациента). Небольшая группа субъектов ( n = 7) смогла прекратить прием по крайней мере одного из своих лекарств от ВЗК. Для дальнейшей оценки эффективности необходимо интервенционное испытание со строгим дизайном исследования, в котором изучаются как биомаркеры воспаления, так и гистологические изменения.
Ретроспективная серия случаев с использованием IBD-AID показала, что у субъектов, которые пытались соблюдать диету ( n = 40), 60% сообщили об уменьшении симптомов, включая снижение частоты стула (самоотчет пациента). Небольшая группа субъектов ( n = 7) смогла прекратить прием по крайней мере одного из своих лекарств от ВЗК. Для дальнейшей оценки эффективности необходимо интервенционное испытание со строгим дизайном исследования, в котором изучаются как биомаркеры воспаления, так и гистологические изменения.
4.6. Добавки с клетчаткой
Преимущества клетчатки при ВЗК чаще проявляются при использовании добавок, а не диетических вмешательств, а также при лечении ЯК и БК [105].Хотя доказательства все еще не ясны, вмешательства с клетчаткой могут облегчить симптомы и / или поддерживать ремиссию заболевания у пациентов с ВЗК. Тип волокна может быть важным фактором.
4.6.1. Овсяные отруби
Контролируемое интервенционное исследование с добавлением 60 граммов овсяных отрубей в день (эквивалент 20 граммов овсяных волокон в день) к диете субъектов ( n = 22) с покоящимся ЯК не выявило признаков или симптомов рецидива колита после 12 недель [57]. Подгруппа испытуемых отметила уменьшение боли в животе, рефлюкса и диареи ( p <0.05). Наибольшее влияние вмешательство овсяных отрубей было замечено на концентрации короткоцепочечных жирных кислот в кале (SCFA), обнаруженных в стуле. Пятнадцать субъектов продемонстрировали 36% -ное увеличение концентрации бутирата в кале в течение четырех недель ( p <0,01) вмешательства, которое сохранялось на протяжении 12-недельного вмешательства. Это открытие важно, поскольку все больше данных свидетельствует о том, что SCFAs играют важную роль в поддержании здоровья слизистой оболочки толстой кишки, поскольку бутират является основным энергетическим субстратом для колоноцитов [106].Бутират также играет важную роль в профилактике и лечении дистального ЯК [107]. Добавление овсяных отрубей в эту популяцию требует дальнейшего исследования с большим размером выборки в долгосрочной перспективе для определения общей пользы в качестве поддерживающей терапии ЯК.
Подгруппа испытуемых отметила уменьшение боли в животе, рефлюкса и диареи ( p <0.05). Наибольшее влияние вмешательство овсяных отрубей было замечено на концентрации короткоцепочечных жирных кислот в кале (SCFA), обнаруженных в стуле. Пятнадцать субъектов продемонстрировали 36% -ное увеличение концентрации бутирата в кале в течение четырех недель ( p <0,01) вмешательства, которое сохранялось на протяжении 12-недельного вмешательства. Это открытие важно, поскольку все больше данных свидетельствует о том, что SCFAs играют важную роль в поддержании здоровья слизистой оболочки толстой кишки, поскольку бутират является основным энергетическим субстратом для колоноцитов [106].Бутират также играет важную роль в профилактике и лечении дистального ЯК [107]. Добавление овсяных отрубей в эту популяцию требует дальнейшего исследования с большим размером выборки в долгосрочной перспективе для определения общей пользы в качестве поддерживающей терапии ЯК.
4.6.2. Пшеничные отруби
Рандомизированное контрольное испытание, завершенное в CD ( n = 7), где испытуемым было рекомендовано придерживаться диеты с высоким содержанием клетчатки, включая потребление цельнозерновых отрубей (1/2 стакана в день) и ограничивать количество рафинированных углеводов, сообщалось об улучшении связанное со здоровьем качество жизни, измеренное с помощью опросника по воспалительным заболеваниям кишечника ( p = 0. 028) [61]. Значительные улучшения были замечены в показателях клинической активности заболевания, измеренных с помощью частичного индекса Харви-Брэдшоу ( p = 0,008). Это было технико-экономическое обоснование с очень небольшим размером выборки ( n = 4 получавших вмешательства), которое не включало субъектов, получающих биологическую терапию. Для проверки результатов этого исследования требуется гораздо больший размер выборки в долгосрочной перспективе, включая субъектов, принимающих различные лекарства.
028) [61]. Значительные улучшения были замечены в показателях клинической активности заболевания, измеренных с помощью частичного индекса Харви-Брэдшоу ( p = 0,008). Это было технико-экономическое обоснование с очень небольшим размером выборки ( n = 4 получавших вмешательства), которое не включало субъектов, получающих биологическую терапию. Для проверки результатов этого исследования требуется гораздо больший размер выборки в долгосрочной перспективе, включая субъектов, принимающих различные лекарства.
4.6.3. Псиллиум
Сообщается о рандомизированном контрольном исследовании субъектов с ЯК в стадии ремиссии ( n = 105), в котором сравнивали клетчатку псиллиума (10 г 2 раза в день) с месаламином (500 мг 3 раза в день) и волокном псиллиума плюс месаламин (10 г 2 раза в день + 500 мг 3 раза в день). продолжалась ремиссия через 12 месяцев и несколько ниже частота рецидивов в группе мезаламин плюс волокна псиллиума [52].Вероятность продолжения ремиссии была одинаковой во всех трех группах (тест Mantel-Cox, p = 0,67; анализ намерения лечить). Hallert et al. (1991) провели рандомизированное контрольное исследование с ремиссией ЯК в течение четырех месяцев ( n = 29), обнаружив, что псиллиум (7 г / день Testa ispaghula) превосходит плацебо в облегчении желудочно-кишечных симптомов ( p <0,001), особенно при диарее и запоре [53]. Хотя дозировка псиллиума требует уточнения, слабые данные свидетельствуют о том, что клетчатка псиллиума может быть эффективной в поддержании ремиссии при ЯК.
Hallert et al. (1991) провели рандомизированное контрольное исследование с ремиссией ЯК в течение четырех месяцев ( n = 29), обнаружив, что псиллиум (7 г / день Testa ispaghula) превосходит плацебо в облегчении желудочно-кишечных симптомов ( p <0,001), особенно при диарее и запоре [53]. Хотя дозировка псиллиума требует уточнения, слабые данные свидетельствуют о том, что клетчатка псиллиума может быть эффективной в поддержании ремиссии при ЯК.
4.6.4. Пищевой продукт из пророщенного ячменя
Пищевой продукт из пророщенного ячменя представляет собой нерастворимое пищевое волокно, получаемое путем измельчения и просеивания отработанного зерна пивоваренными заводами [108]. Пищевой продукт из пророщенного ячменя имеет пребиотические свойства, он содержит богатый глутамином белок и богатую гемицеллюлозой клетчатку, которая, как было показано, снижает клиническую активность и продлевает ремиссию при ЯК [58,59,60]. Открытое испытание с участием 41 пациента (21 контрольная группа, 20 вмешательств в отношении пищевых продуктов из проросшего ячменя) с ЯК в стадии ремиссии получало 30 г (три раза в день) пищевых продуктов из проростков ячменя в дополнение к обычным лекарствам в течение двух месяцев [59]. Статистически значимое снижение среднего CRP было замечено в группе вмешательства по выращиванию проросшего ячменя ( p = 0,017), а также значительное уменьшение боли в животе и спазмов ( p = 0,017). Аналогичное исследование показало, что 20 граммов проросшего ячменя ( n = 41) снижали уровни TNF-, α , IL-6 и IL-8, со значительным снижением уровня IL-6 ( p = 0,034). и ИЛ-8 ( p = 0,013) [60]. Продолжительность ремиссии также увеличивалась при длительном приеме (12 месяцев) 20 граммов пищевых продуктов проросшего ячменя [58].Пищевые продукты из пророщенного ячменя представляют собой безопасную и эффективную поддерживающую терапию для продления ремиссии у пациентов с ЯК.
Статистически значимое снижение среднего CRP было замечено в группе вмешательства по выращиванию проросшего ячменя ( p = 0,017), а также значительное уменьшение боли в животе и спазмов ( p = 0,017). Аналогичное исследование показало, что 20 граммов проросшего ячменя ( n = 41) снижали уровни TNF-, α , IL-6 и IL-8, со значительным снижением уровня IL-6 ( p = 0,034). и ИЛ-8 ( p = 0,013) [60]. Продолжительность ремиссии также увеличивалась при длительном приеме (12 месяцев) 20 граммов пищевых продуктов проросшего ячменя [58].Пищевые продукты из пророщенного ячменя представляют собой безопасную и эффективную поддерживающую терапию для продления ремиссии у пациентов с ЯК.
4.7. Роль жира в диете
Систематические обзоры эффективности добавок n -3 ПНЖК в поддержании ремиссии при ВЗК не показали четких доказательств их эффективности [84,85,109]. Тем не менее, тип жирных кислот, потребляемых с пищей, может иметь важное значение для поддержания ремиссии. Uchiyama et al. внедрила диетическую терапию для пациентов с ВЗК ( n = 230), которая включала использование «таблицы пищевого обмена n -3 ПНЖК» (план диеты n -3 ПНЖК)) для достижения диеты n — 3/ n -6 отношение [почти равно] 1 [88].В этом режиме для достижения соотношения n -3 / n -6, равного ~ 1, потребление n -6 ПНЖК было ограничено до 50% от среднего потребления, а потребление n -3 ПНЖК. был увеличен. Испытуемым было запрещено употреблять основные источники пищевых продуктов n -6 ПНЖК, то есть растительное масло; приправы, такие как маргарин, заправки и майонез; пища, приготовленная на растительном масле; и закуски. В подгруппе субъектов среднее соотношение n -3 / n -6 значительно увеличилось после вмешательства.Среднее соотношение n -3 / n -6 в ремиссии было значительно выше, чем в группах рецидивов (0,65 ± 0,28 и 0,53 ± 0,18, p <0,001) и увеличение в n -3 / n.
Uchiyama et al. внедрила диетическую терапию для пациентов с ВЗК ( n = 230), которая включала использование «таблицы пищевого обмена n -3 ПНЖК» (план диеты n -3 ПНЖК)) для достижения диеты n — 3/ n -6 отношение [почти равно] 1 [88].В этом режиме для достижения соотношения n -3 / n -6, равного ~ 1, потребление n -6 ПНЖК было ограничено до 50% от среднего потребления, а потребление n -3 ПНЖК. был увеличен. Испытуемым было запрещено употреблять основные источники пищевых продуктов n -6 ПНЖК, то есть растительное масло; приправы, такие как маргарин, заправки и майонез; пища, приготовленная на растительном масле; и закуски. В подгруппе субъектов среднее соотношение n -3 / n -6 значительно увеличилось после вмешательства.Среднее соотношение n -3 / n -6 в ремиссии было значительно выше, чем в группах рецидивов (0,65 ± 0,28 и 0,53 ± 0,18, p <0,001) и увеличение в n -3 / n. Соотношение -6 наблюдалось в мембране эритроцитов субъектов с ВЗК. Это исследование пришло к выводу, что соотношение n -3 / n -6 может влиять на активность заболевания у субъектов с ВЗК.
Соотношение -6 наблюдалось в мембране эритроцитов субъектов с ВЗК. Это исследование пришло к выводу, что соотношение n -3 / n -6 может влиять на активность заболевания у субъектов с ВЗК.
Средиземноморская диета может оказывать защитное действие на ВЗК, поскольку заболеваемость ВЗК на юге Европы ниже, чем в Северной Европе [110].Средиземноморская диета — это диета с высоким содержанием богатых клетчаткой растительных продуктов (например, злаков, фруктов, овощей, бобовых, орехов, семян и оливок), с оливковым маслом в качестве основного источника добавленных жиров, наряду с высоким содержанием жира. умеренное потребление рыбы и морепродуктов, умеренное потребление яиц, птицы, молочных продуктов (сыр и йогурт), вина и низкое потребление красного мяса [111]. Растущее количество научных данных указывает на то, что тип средиземноморской диеты связан со значительным улучшением состояния здоровья и [77,78] снижением маркеров воспаления [79].Предполагается, что защитный эффект обусловлен балансом соотношения омега-6 / омега-3 в средиземноморской диете (35% общего жира: 15% MUFA (в основном из оливкового масла), 13% SFA и 6% PUFA. [80]. Механизмы того, как MUFA могут быть полезными при колите, неизвестны, хотя было показано, что соблюдение средиземноморской диеты благотворно влияет на микробиом кишечника и метаболиты кишечника (метаболом) [35]. n = 264 пациента с ВЗК и 203 контрольной группы) обнаружили, что низкая приверженность средиземноморской диете была значительным фактором риска в развитии педиатрического ЯК (OR: 2.3; 1.2–4.5) [36]. Интервенционное исследование, изучающее влияние модели средиземноморской диеты на CD ( n = 8), продемонстрировало тенденцию к снижению воспалительных биомаркеров ( p = 0,39) и тенденцию к «нормализации» микробиоты кишечника [37]. Проблемой этого исследования было отсутствие статистически значимых результатов и небольшой размер выборки. Хотя необходимо более четкое понимание роли средиземноморской диеты и ее влияния на ВЗК, средиземноморская диета может предложить многообещающий подход к снижению маркеров воспаления и нормализации микробиоты, но это необходимо будет подтвердить в будущих клинических испытаниях.
[80]. Механизмы того, как MUFA могут быть полезными при колите, неизвестны, хотя было показано, что соблюдение средиземноморской диеты благотворно влияет на микробиом кишечника и метаболиты кишечника (метаболом) [35]. n = 264 пациента с ВЗК и 203 контрольной группы) обнаружили, что низкая приверженность средиземноморской диете была значительным фактором риска в развитии педиатрического ЯК (OR: 2.3; 1.2–4.5) [36]. Интервенционное исследование, изучающее влияние модели средиземноморской диеты на CD ( n = 8), продемонстрировало тенденцию к снижению воспалительных биомаркеров ( p = 0,39) и тенденцию к «нормализации» микробиоты кишечника [37]. Проблемой этого исследования было отсутствие статистически значимых результатов и небольшой размер выборки. Хотя необходимо более четкое понимание роли средиземноморской диеты и ее влияния на ВЗК, средиземноморская диета может предложить многообещающий подход к снижению маркеров воспаления и нормализации микробиоты, но это необходимо будет подтвердить в будущих клинических испытаниях. .
.
4.8. Популярные диеты для пациентов
Specific Carbohydrate Diet ™ — одна из самых популярных диет в непрофессиональной литературе, которую используют пациенты с ВЗК. К сожалению, опубликованных данных об этой диете, основанных на доказательствах, недостаточно. На сегодняшний день доказательства этой диеты основаны на ретроспективных опросах и отчетах о случаях заболевания. Согласно книге «Прерывание вязкого цикла», диета представляет собой строгий режим без зерна, сахара и сложных углеводов [112]. Интернет-опрос ( n = 451), в ходе которого изучалось восприятие пациентом с ВЗК специальной углеводной диеты ™, показал, что симптомы уменьшились (боль в животе, диарея и кровь в стуле) [38].Сорок два процента пациентов считают, что диета помогла им достичь ремиссии. Небольшой интернет-опрос ( n = 51) пациентов, которые использовали Specific Carbohydrate Diet ™ для лечения ВЗК, сообщил, что у 84% улучшилось соблюдение диеты, а у 75% улучшились симптомы [113]. Пятьдесят четыре процента сообщили, что они поддерживали ремиссию благодаря использованию специальной углеводной диеты ™. В отчете о серии случаев ( n = 50) тридцать три субъекта (66%) отметили полное исчезновение симптомов при среднем значении 9.9 месяцев (от 1 до 60 месяцев) после начала Specific Carbohydrate Diet ™ [41]. Самостоятельный отчет пациентов об эффективности Specific Carbohydrate Diet ™ был оценен как в среднем 91,3% для контроля симптомов обострения (диапазон от 30% до 100%) и в среднем 92,1% для поддержания ремиссии (диапазон = От 53% до 100%). Было проведено два ретроспективных исследования с участием педиатров, в которых изучались результаты применения Specific Carbohydrate Diet ™ по клиническим исходам и лабораторным параметрам при ВЗК [39,40].Было проанализировано 26 пациентов с ВЗК ( n = 20 с CD, 6 с UC) плюс 10 контрольных пациентов [39]. Сравнительный анализ субъектов, соблюдающих Specific Carbohydrate Diet ™ с контрольной группой, выявил значительное улучшение индекса активности болезни Крона у детей, CRP и калпротектина с течением времени для обеих групп ( p = 0,03, 0,03 и 0,03, соответственно).
Пятьдесят четыре процента сообщили, что они поддерживали ремиссию благодаря использованию специальной углеводной диеты ™. В отчете о серии случаев ( n = 50) тридцать три субъекта (66%) отметили полное исчезновение симптомов при среднем значении 9.9 месяцев (от 1 до 60 месяцев) после начала Specific Carbohydrate Diet ™ [41]. Самостоятельный отчет пациентов об эффективности Specific Carbohydrate Diet ™ был оценен как в среднем 91,3% для контроля симптомов обострения (диапазон от 30% до 100%) и в среднем 92,1% для поддержания ремиссии (диапазон = От 53% до 100%). Было проведено два ретроспективных исследования с участием педиатров, в которых изучались результаты применения Specific Carbohydrate Diet ™ по клиническим исходам и лабораторным параметрам при ВЗК [39,40].Было проанализировано 26 пациентов с ВЗК ( n = 20 с CD, 6 с UC) плюс 10 контрольных пациентов [39]. Сравнительный анализ субъектов, соблюдающих Specific Carbohydrate Diet ™ с контрольной группой, выявил значительное улучшение индекса активности болезни Крона у детей, CRP и калпротектина с течением времени для обеих групп ( p = 0,03, 0,03 и 0,03, соответственно). Успешное поддержание ремиссии с помощью специальной углеводной диеты ™ позволило некоторым субъектам прекратить прием лекарств и сохранить контроль над заболеванием только с помощью специальной углеводной диеты ™.Небольшой ретроспективный обзор диаграммы ( n = 11), где педиатрические пациенты соблюдали Specific Carbohydrate Diet ™ в течение одного года, обнаружил значительное улучшение гематокрита, альбумина и СОЭ ( p = 0,006, 0,002, 0,002, соответственно) [40]. У десяти детей увеличился процентиль веса, а у девяти детей увеличился процентиль роста при соблюдении строгой специфической углеводной диеты ™. Чтобы определить достоинства этой диеты для лечения ВЗК, необходимы тщательные проспективные рандомизированные контролируемые исследования в педиатрии и у взрослых.
Успешное поддержание ремиссии с помощью специальной углеводной диеты ™ позволило некоторым субъектам прекратить прием лекарств и сохранить контроль над заболеванием только с помощью специальной углеводной диеты ™.Небольшой ретроспективный обзор диаграммы ( n = 11), где педиатрические пациенты соблюдали Specific Carbohydrate Diet ™ в течение одного года, обнаружил значительное улучшение гематокрита, альбумина и СОЭ ( p = 0,006, 0,002, 0,002, соответственно) [40]. У десяти детей увеличился процентиль веса, а у девяти детей увеличился процентиль роста при соблюдении строгой специфической углеводной диеты ™. Чтобы определить достоинства этой диеты для лечения ВЗК, необходимы тщательные проспективные рандомизированные контролируемые исследования в педиатрии и у взрослых.
Палеодиета — еще одна популярная диета среди пациентов с ВЗК. Он рекомендует избегать обработанных пищевых продуктов, рафинированного сахара, бобовых, молочных продуктов, зерновых и круп, а вместо этого выступает за мясо откорма травой, дикую рыбу, фрукты, овощи, орехи и «здоровые» насыщенные жиры [114]. Хотя логично, что диета, которая способствует отказу от рафинированного и дополнительного сахара, а также высококалорийной пищи, будет иметь последствия для здоровья, клинических испытаний, которые бы изучали эффективность этой диеты при ВЗК, не проводилось.Требуются рандомизированные контролируемые исследования, чтобы определить, оказывает ли палеодиета положительное влияние по сравнению с другими советами по диете.
Хотя логично, что диета, которая способствует отказу от рафинированного и дополнительного сахара, а также высококалорийной пищи, будет иметь последствия для здоровья, клинических испытаний, которые бы изучали эффективность этой диеты при ВЗК, не проводилось.Требуются рандомизированные контролируемые исследования, чтобы определить, оказывает ли палеодиета положительное влияние по сравнению с другими советами по диете.
5. Pharmaconutrition
5.1. Куркумин (куркума)
Куркумин — это активный ингредиент, содержащийся в куркуме, распространенной индийской специи. Куркума обычно используется в аюрведической медицине для лечения различных воспалительных заболеваний. Было показано, что желтый пигмент (куркумин), присутствующий в куркуме, проявляет многочисленные противовоспалительные свойства [115].Куркумин в основном применяется перорально в виде капсул, заполненных его порошком. Рандомизированное контролируемое исследование 82 пациентов с ЯК продемонстрировало, что куркумин в дозе 2 г / день (1 г / день после завтрака и 1 г / день после ужина) при добавлении к стандартной терапии значительно снижает частоту рецидивов [54]. У двух субъектов случился рецидив в течение 6 месяцев терапии с одновременной терапией куркумином (4,65%), тогда как у 8 из 39 субъектов (20,51%) в группе плацебо произошел рецидив ( p = 0,040).Индекс клинической активности и индексы эндоскопической активности в группе куркумина значительно улучшились через шесть месяцев у субъектов с ЯК в стадии ремиссии (индекс клинической активности: p = 0,038 и индексы эндоскопической активности: p = 0,0001). В систематическом обзоре [55] и в одном Кокрановском обзоре [56] делается вывод, что куркумин может быть эффективным и безопасным средством для поддержания ремиссии при ЯК на срок до шести месяцев при условии его стандартной терапии (сульфасалазин и месаламин). Необходимы более обширные, хорошо контролируемые клинические испытания, чтобы подтвердить преимущества куркумина, в настоящее время он представляется безопасным и недорогим вариантом для поддержания ремиссии при ЯК при добавлении к стандартной медикаментозной терапии.
5.2. Пробиотики
Использование пробиотиков для поддержания ремиссии при ВЗК было исследовано в нескольких клинических испытаниях, однако результаты противоречивы. Клинические исследования имеют значительную неоднородность, включая множество различных родов, видов, штаммов и доз пробиотиков, которые были исследованы, что затрудняет однозначные выводы об эффективности. Мета-анализ пробиотического штамма Escherichia coli Nissle 1917 для поддержания ремиссии при ЯК показал, что E.coli Nissle 1917 поддержала ремиссию, как и стандартная терапия месалазином (OR = 1,07, 95% ДИ: 0,70–1,64) [116]. Аналогичным образом, другой метаанализ показал, что пробиотики могут предотвращать рецидив ЯК так же эффективно, как месалазин ( n = 638; 316 группа пробиотиков, 322 группа месалазина; RR = 1,0, 95% ДИ: 0,79–1,26) [117]. Эффективными штаммами были E. coli Nissle 1917, E. coli (серотип O6: K5: h2), Lactobacillus GG и Probio-Tec AB-25 ( L.s acidophilus La-5 и Bifidobacterium animalis subsp. lactis BB-1). Шен и др. (2013) также обнаружили, что пробиотики были сопоставимы с 5-АСК в поддерживающей терапии при ЯК ( p = 0,69, ОР = 0,96) [118]. Напротив, Кокрановское сотрудничество не обнаружило разницы между пробиотиками и месалазином для поддержания ремиссии при ЯК (3 исследования; 555 пациентов: ОШ 1,33; 95% ДИ: 0,94–1,90) [119]. Прием пробиотиков для поддержания ремиссии при БК также неблагоприятен.Два метаанализа показали, что пробиотические штаммы Lactobacillus GG и Lactobacillus johnsonii LA1 не могут предотвратить рецидив БК (ОР = 1,18, 95% ДИ: 0,81–1,70) [118,120], и пришли к выводу, что пробиотики не оказывают значительного воздействия на CD с добавкой пробиотиков ( p = 0,71, RR = 1,09) [120]. Было показано, что пробиотический штамм Lactobacillus GG значительно улучшает рецидив по сравнению с плацебо (ОР 1,68, 95% ДИ: от 1,07 до 2,64) [118].В будущих исследованиях, посвященных изучению пробиотиков в поддержании ремиссии при ВЗК, необходимо сосредоточить внимание на эффектах различных штаммов пробиотиков и различных дозировках, а также на однородных популяциях пациентов, чтобы определить, какие пациенты с наибольшей вероятностью получат пользу от лечения пробиотиками.
5.3. Витамин D
Дефицит витамина D часто встречается у пациентов с ВЗК с частотой от 16% до 95% [121]. В одном исследовании сообщается, что у пациентов с ЯК шансы дефицита витамина D более чем в два раза выше по сравнению с нормальной контрольной группой (OR = 2.28; 95% ДИ: 1,18–4,41; I = 41%; p = 0,01) [47]. Есть также данные, позволяющие предположить, что дефицит витамина D может влиять на тяжесть воспаления при ВЗК [48,49,50]. Поперечное исследование показало, что пациенты с активной болезнью чаще имели низкий уровень витамина D (80% против 50,4%, p = 0,005) по сравнению с пациентами в стадии ремиссии [49]. Большая проспективно собранная когорта из 230 субъектов продемонстрировала обратную связь между концентрацией 25 (OH) D в сыворотке и воспалением слизистой оболочки, как оценивалось по шкале эндоскопии Майо ( p = 0.01), активность заболевания, на которую указывает общий балл Mayo ( p = 0,001), и гистологическая активность ( p = 0,02) у субъектов с UC [48]. Было обнаружено, что концентрации 25 (OH) D в сыворотке обратно коррелируют с калпротектином ( r = -0,207, p = 0,030), особенно среди пациентов с БК в клинической ремиссии ( r = -0,242, p ). = 0,022) [50]. Кроме того, большая когорта из более чем 3200 пациентов с ВЗК продемонстрировала, что низкий уровень 25 (OH) D в плазме (<50 нмоль / л) независимо связан с повышенным риском последующей операции (OR: 1.76; 95% ДИ: 1,24–2,51) и госпитализация (ОШ: 2,07; 95% ДИ: 1,59–2,68) при БК с аналогичными результатами, полученными при ЯК [51]. Исследование, в котором наблюдали за пациентами с ВЗК в течение пяти лет ( n = 965), показало, что пациенты с низким средним уровнем витамина D (<50 нмоль / л) имели более сильную боль, показатели активности заболевания, степень обращения за медицинской помощью и качество жизни ( p <0,05) по сравнению с пациентами с нормальным средним уровнем витамина D (> 75 нмоль / мл) [122]. Большая группа пациентов с ВЗК, состоящая из нескольких учреждений, обнаружила, что пациенты с дефицитом витамина D (<50 нмоль / л) имеют повышенный риск рака (ОШ: 1.82; 95% ДИ: 1,25–2,65) по сравнению с пациентами, у которых был достаточный уровень [123].
Учитывая, что статус витамина D, по-видимому, является независимым фактором риска для потенциально худших исходов ВЗК, добавление витамина D в эту популяцию является разумным. Пациенты с CD, у которых был дефицит витамина D (<75 нмоль / л) и нормализовался уровень 25 (OH) D, имели меньшую вероятность хирургического вмешательства (OR: 0,56; 95% CI: 0,32–0,98) по сравнению с пациентами, у которых оставался дефицит [ 51]. Проспективное исследование в UC ( n = 70) продемонстрировало, что низкие уровни витамина D (<88 нмоль / л) увеличивают риск клинического рецидива в течение 12 месяцев, а также связаны с увеличением наличия эндоскопического воспаления (OR: 1 .29; 95% ДИ: 1,07–1,85; p <0,01) или гистологическое воспаление (OR: 1,46; 95% ДИ: 1,13–1,88; p = 0,005) [124]. Оптимальная концентрация для пациентов с ВЗК остается неизвестной, но нацеливание на концентрацию 25 (OH) D в сыворотке выше 75 нмоль / л кажется безопасным и может иметь преимущества для активности заболевания ВЗК, улучшения здоровья костей, предотвращения колоректального рака и облегчения депрессии [125 ]. Вероятно, необходимы ежедневные дозы 1800–10 000 МЕ витамина D3 (холекальциферол), в зависимости от исходной концентрации витамина D в сыворотке крови, вовлеченности подвздошной кишки в CD и индекса массы тела [125].В клиническом исследовании Jorgensen et al. (2010) ( n = 108), при БК пероральное лечение витамином D3 1200 МЕ в день увеличивало уровень 25 (OH) D в сыворотке со среднего значения 69 нмоль / л до среднего значения 96 нмоль / л после трех месяцев лечения ( p <0,001) [126].
6. Проблемы при создании руководств, основанных на фактах
Несмотря на то, что есть испытания диетических вмешательств, которые показывают многообещающие результаты в поддержании ремиссии, их эффективность остается под вопросом. Короткая продолжительность вмешательств (менее 12 недель), отсутствие надлежащей контрольной группы в некоторых случаях и небольшие размеры выборки (менее 20 человек) затрудняют для клиницистов сделать твердые выводы на основе имеющихся данных.В целом отсутствуют объективные клинические и эндоскопические маркеры заболевания. Например, многие исследования завершаются ретроспективно и основываются на анкетах пациентов в отношении симптомов заболевания, таких как боль и частота стула. Срочно необходимы хорошо спланированные клинические испытания ВЗК, чтобы точно определить роль каждой из этих диет в профилактике или лечении ВЗК. До сих пор роль диеты при ВЗК сильно подрывается сообщениями непрофессионалов и анекдотами без достаточных научных доказательств.
Высококачественные интервенционные исследования диет для лечения ВЗК должны включать следующее: (1) количественное определение исходного уровня привычного рациона; (2) мониторинг соблюдения диеты посредством отзыва продуктов; (3) крупные проспективные контрольные испытания в долгосрочной перспективе; (4) использование контрольной диеты для определения специфичности наблюдаемых эффектов вмешательства; (5) использование различных конечных точек (симптомы, качество жизни, клинические биомаркеры, эндоскопические индексы, диета и оценка кала) для мониторинга реакции на диетические вмешательства; и (6) рассмотреть возможность использования животных моделей ВЗК (например,g., модель гнотобиотической мыши), чтобы обнаружить механизмы патогенеза.
По мере того, как исследования в этой области продвигаются вперед, следующим рубежом может стать индивидуальный подход к питанию для отдельных лиц или отдельных групп пациентов. Индивидуальный подход может быть полезен не только для первичной профилактики ВЗК, но и для лечения заболеваний. Мы должны помнить, что общее диетическое лечение для всех пациентов может не сработать. Безусловно, мы наблюдаем новые исследования, которые предполагают, что подходы, ориентированные на микробиоту, продемонстрировали некоторые перспективы в борьбе с хроническими заболеваниями [127].
Лучшие продукты, которые следует есть и которых следует избегать при воспалительном заболевании кишечника
Воспалительное заболевание кишечника (ВЗК) — это излечимое, но хроническое заболевание, продолжающееся всю жизнь. ВЗК — это широкий термин, который относится к воспалению желудочно-кишечного тракта и включает определенные состояния, такие как язвенный колит и болезнь Крона.
Нет доказательств того, что план по предотвращению или контролю ВЗК отсутствует. Но соблюдение диеты может помочь справиться с болезнью во время обострений и периодов ремиссии.Обязательно поговорите со своим врачом или диетологом о своих потребностях в питании и ведении ВЗК.
Вот рекомендации по диете для лечения обострений и ремиссий ВЗК от службы амбулаторного питания UH.
Что есть во время вспышек болезни
Уменьшите потребление клетчатки — Продукты с низким содержанием клетчатки легче перевариваются и меньше раздражают кишечник, особенно с такими симптомами, как боль в животе или диарея. Выберите:
- Зерна / крахмалы: Белые продукты вместо пшеницы или цельнозерновых продуктов, а также продукты, содержащие менее 2 граммов клетчатки на порцию
- Приготовленные овощи: Хорошо прожаренные овощи, такие как стручковая фасоль, морковь, картофельное пюре без кожи, тушеные кончики спаржи и протертые тыквенные пюре.Используйте свежие или замороженные.
- Консервы или мягкие фрукты: Очищенные яблоки, спелые бананы, дыня, медвяная роса, арбуз и консервированные фрукты в фруктовом соке или легком сиропе
Обязательно ешьте достаточно белка — Воспаление вызывает повышенную потребность в белке. Выберите:
- Нежное, хорошо прожаренное мясо: Птица, лосось или другая рыба, нежирная говядина и свинина, приготовленные без добавления жира
- Мясные деликатесы: С низким содержанием натрия и нежирными сортами
- Яйца: Хорошо прожаренные
- Тофу
- Масло из гладких орехов и семян: Арахис, миндаль или семена подсолнечника
Пейте много жидкости — Старайтесь выпивать восемь чашек в день и при необходимости рассмотрите возможность использования напитков для пероральной регидратации.Постарайтесь ограничить употребление напитков с кофеином, сахаром и напитков с заменителями сахара.
Ограничьте количество добавляемых жиров и масел — Сосредоточьтесь на маслах, а не на твердых жирах, и ограничьте потребление до менее восьми чайных ложек в день.
Потребляйте достаточное количество кальция, витамина D, пробиотиков и пребиотиков — Источники включают:
- Сгущенное обезжиренное 1-процентное и 2-процентное молоко
- Молоко без лактозы
- Обогащенное немолочное молоко, такое как миндальное, кешью, кокосовое или рисовое молоко — эти варианты не содержат много белка
- Обогащенное гороховое и соевое молоко — они могут вызывать газы и вздутие живота
- Йогурт / йогурт без лактозы
Что есть во время ремиссии
Увеличьте количество клетчатки и повторно введите цельнозерновые — Медленно добавляйте продукты с высоким содержанием клетчатки, когда желудочно-кишечные симптомы уменьшаются.
Потребляйте омега-3 жирные кислоты — Подумайте о том, чтобы есть больше свежей или консервированной жирной рыбы или принимать добавки из рыбы или льняного масла.
Сосредоточьтесь на здоровых продуктах питания в их естественном состоянии — Сюда входят продукты с минимальной обработкой и минимальным количеством ингредиентов.
Молочные и лактозные продукты переносятся лучше — Если у вас непереносимость лактозы, избегайте молочных продуктов или ешьте продукты с низким содержанием лактозы или безлактозные продукты.
Добавленные жиры будут лучше переноситься — Продолжайте сосредотачиваться на использовании масел, таких как оливковое масло или масло канолы, вместо твердых жиров.
Продолжайте уделять внимание белковой пище — Употребляйте говядину, яйца, птицу и другое нежирное мясо или растительные белки, такие как соевые продукты.
Обязательно пейте много воды — Пейте воду вместо фруктовых соков, безалкогольных напитков, алкоголя и напитков с кофеином, таких как кофе или чай.
Ссылки по теме
Амбулаторное питаниеUH доступно в медицинском центре UH Cleveland, медицинском центре UH Ahuja, UH Minoff в Chagrin Highlands, Landerbrook, Medina, Solon и Westlake в медицинских центрах и W.Центр О. Уокера. Позвоните по телефону 216-844-1499, чтобы записаться на прием.
Что есть и чего избегать для лечения ВЗК
Некоторые продукты ухудшают симптомы ВЗК. Составление противовоспалительной диеты, уникальной для вашего состояния, может помочь вам уменьшить обострения.
Опубликовано on Пятница, Сентябрь 4, 2020
Диета важна для всех.Употребление правильных продуктов в нужных количествах обеспечивает ваше тело питательными веществами, необходимыми для поддержания здоровья.
При воспалительном заболевании кишечника получить правильное питание может быть непросто. Тонкая кишка поглощает питательные вещества из пищи, которую вы едите. Когда у вас хроническое воспаление и другие симптомы ВЗК, вы можете не усваивать все питательные вещества или переваривать пищу. Это может привести к серьезным проблемам, таким как недоедание, потеря веса и дефицит питательных веществ.
Чтобы предотвратить эти осложнения и сделать прием пищи приятным, вам нужно уделять пристальное внимание тому, что вы вводите в свое тело, и как реагирует ваша пищеварительная система.
Что входит в план диеты при ВЗК?
Составление диеты, подходящей для вашего состояния, будь то болезнь Крона, язвенный колит или воспалительное заболевание кишечника, не подходящее ни к одной из категорий, является сложной задачей. Не существует ни одной диеты при болезни Крона или язвенном колите. Продукты, которые вызывают симптомы болезни Крона или колита, могут отличаться от продуктов, вызывающих проблемы у кого-то другого. Но есть несколько ключевых ингредиентов для создания собственной диеты при воспалительном заболевании кишечника:
- Прием пищи небольшими порциями — Ешьте меньше, чаще.Небольшие приемы пищи — скажем, шесть приемов пищи в день вместо традиционного завтрака, обеда и ужина — помогают снизить нагрузку на пищеварительный тракт.
- Жидкости и электролиты — Частые приступы диареи истощают ваш организм водой и питательными веществами. Выпивайте половину своего веса в унциях воды и восполняйте запасы натрия, калия и электролитов с помощью спортивных напитков.
- Витамины и минералы — Люди с болезнью Крона подвергаются большему риску дефицита питательных веществ.Люди с язвенным колитом чаще страдают анемией. Возможно, вам придется ежедневно принимать поливитамины или добавки, чтобы дополнить хорошо сбалансированную, богатую питательными веществами диету.
- Белок — Хотя многие думают о витаминах и минералах, белок также является питательным веществом. Ешьте свой вес в килограммах белка и увеличивайте потребление, чтобы восстановить потери после обострения.
- Более высокое содержание калорий — Когда ваш организм испытывает проблемы с переработкой пищи, вам, возможно, придется увеличить их количество, чтобы восполнить это.Потребление большего количества калорий особенно важно для восстановления после обострения и восстановления потерянного веса.
- Вызвать отказ от еды — Некоторые вещи могут усугубить ваши симптомы. Всегда следите за своими симптомами после еды, чтобы избежать употребления этих продуктов в будущем.
Шесть экспертов IBD в одном удобном месте
Наш центр IBD координирует комплексное лечение вашего хронического заболевания кишечника.
Узнать больше
Какие продукты уменьшают воспаление и другие симптомы ВЗК?
Целью лечения воспалительного синдрома кишечника является уменьшение воспаления, а в идеале — полное избавление от него.Когда воспаление находится под контролем, исчезают и другие проблемы с пищеварением.
Возможно, вы слышали о противовоспалительных диетах или противовоспалительных продуктах. Хорошая диета для ВЗК — это тип противовоспалительной диеты, включающий большинство стандартных рекомендаций по здоровому питанию. Хотя вам все еще необходимо составить собственный список продуктов, которые нужно есть, и продуктов, которых следует избегать, на основе триггеров, определенных вами и вашими врачами, есть несколько общих рекомендаций, которым вы можете следовать.
Продукты, которые нужно включить в диету с ВЗК
Ваши триггеры неизбежно уменьшат ваш выбор продуктов питания. Но вы все равно должны стремиться к разнообразной и богатой питательными веществами диете, чтобы контролировать воспалительное заболевание кишечника. Ваш рацион должен включать здоровую смесь:
- Волокно — Волокно может быть проблемным питательным веществом. Это важная часть здорового питания, но обычно она вызывает симптомы во время обострения. Сосредоточьтесь на источниках растворимой клетчатки (которые помогают уменьшить диарею), таких как бобы, мясистые фрукты, овес и ячмень, и ешьте другие цельнозерновые и продукты с высоким содержанием клетчатки, насколько сможете.
- Постные белки — Слишком много жира может привести к плохому усвоению белка и ухудшить ваши симптомы. Придерживайтесь источников белка с низким содержанием жира, таких как курица, индейка, рыба, яйца и тофу.
- Фрукты и овощи — Употребление в пищу разноцветных растений обеспечивает разнообразное сочетание витаминов и минералов. Если волокнистая кожура и семена вызывают проблемы с пищеварением, удалите их перед едой.
- Продукты, богатые кальцием — ВЗК и особенно болезнь Крона могут привести к непереносимости лактозы.Таким образом, вам может потребоваться получать кальций из немолочных источников, консервов из рыбы или темно-зеленых овощей. Что касается молочных продуктов, вы можете выбрать безлактозные или немолочные альтернативы молоку, йогурту и сыру.
- Пробиотики — Воспалительное заболевание кишечника может вымывать «хорошие» бактерии из кишечника. Йогурт, кимчи, мисо, квашеная капуста, темпе и другие источники живых бактерий могут помочь восстановить баланс кишечных бактерий.
Продукты, которых следует избегать при IBD
Нет причин избегать еды, если она не вызывает или не ухудшает ваши симптомы.Вы хотите получать как можно больше питательных веществ из самых разных источников. Но если вы еще не определили продукты, которые вызывают у вас обострения болезни Крона, язвенного колита или ВЗК, наиболее частыми виновниками являются
- Жирные, жирные или жареные продукты
- Горячие или острые продукты
- Сырые фрукты и овощи с высоким содержанием клетчатки
- Орехи, семена и бобы
- Напитки с кофеином или сладкие напитки
- Напитки алкогольные
- Конфеты, сладости и другие источники добавленного сахара
Алкоголь, кофеин и острая пища могут вызвать раздражение толстой кишки.Так что проблемы могут усугубиться, если у вас воспалительное заболевание кишечника. Жир, сахар и клетчатка усваиваются труднее. Поэтому вам, возможно, придется придерживаться продуктов с низким содержанием этих категорий или есть продукты с более высоким содержанием в умеренных количествах.
Что есть во время обострения болезни Крона или колита
Некоторые продукты вызывают спазмы, вздутие живота или диарею — все, чего следует избегать, если обостряется воспалительное заболевание кишечника. Когда симптомы вернутся, лучше придерживаться основ.Держитесь подальше от всего, что может усугубить из списка «Продукты, которых следует избегать». Вместо этого ешьте эти продукты без примесей и используйте кипячение, жарение на гриле и приготовление на пару в качестве основных методов приготовления:
- Овощи: Морковь, шпинат, спаржа, картофель
- Фрукты: Яблочное пюре, консервированные груши или персики, бананы, дыни, авокадо
- Очищенные зерна: Белый рис, хлеб и макаронные изделия
- Белки: Арахисовое масло, лосось, вареные яйца, курица или индейка без добавок
Как только обострение ВЗК будет под контролем, вы можете постепенно возвращать продукты в свой обычный рацион, по одной или две за раз каждые несколько дней.Начните с вещей, которые, как вы знаете, вы можете терпеть — сначала жидкости, а затем мягкие твердые вещества. И постепенно увеличивайте количество калорий, белков и клетчатки, чтобы вернуться к здоровой диете, которая, возможно, страдала от плохого аппетита или потери веса.
Независимо от того, находитесь ли вы в стадии ремиссии или в разгаре обострения, ваша диета является одним из ключей к лечению воспалительного заболевания кишечника. Но, как и любую диету, придерживаться ее не всегда легко. Когда вы работаете с опытной командой экспертов по ВЗК и диетологов, вы можете разработать план диеты, чтобы получить адекватное питание, избегая при этом триггеров, и при этом есть многие из любимых продуктов.
Вся информация, представленная на веб-сайте клиники Айовы, предназначена только для использования в качестве общей образовательной информации. Любой контент, продукт или услуга не предназначены для замены профессиональных медицинских консультаций, диагностики или лечения. Если вы считаете, что у вас есть проблема со здоровьем, всегда обращайтесь за индивидуальной консультацией к своему врачу или квалифицированному поставщику медицинских услуг.
Клиника Айовы может предоставлять ссылки на внешние источники для получения дополнительных ресурсов или информации и никоим образом не несет ответственности за информацию, предоставленную другими организациями или источниками.© Клиника Айовы, 2021
Что нужно знать о диете и питании при язвенном колите
Продукты, которые нужно есть при обострении болезни Во время обострения болезни часто бывает полезно придерживаться мягких продуктов, которые легко перевариваются, по мнению Крона. И Фонд колита.Вы можете попробовать следующие продукты:
- Бананы
- Белый хлеб или хлеб на закваске
- Крекеры из белой муки (не из цельнозерновой муки)
- Белый рис (не коричневый рис)
- Сыр (если вы не страдаете непереносимостью лактозы)
- Разбавленные фруктовые соки и спортивные напитки
- Яблочное пюре
- Фруктовые консервы
- Арахисовое масло гладкое
- Простые хлопья
- Рафинированные макаронные изделия (не цельнозерновые)
- Бульон
- Приготовленные овощи без кожи
- Жареная или приготовленная на пару рыба
- Индейка, курица или яйца
Ведение журнала питания поможет вам выяснить, какие продукты вас беспокоят, а какие нет.
По данным Калифорнийского университета в Сан-Франциско, потребление большего количества жирных кислот омега-3 может помочь уменьшить воспаление при язвенном колите.К продуктам с высоким содержанием омега-3 жирных кислот относятся следующие продукты:
Каких продуктов следует избегать при язвенном колите?Хотя однозначно не обнаружено, что продукты питания усугубляют воспаление или изъязвление при язвенном колите, некоторые продукты могут усугубить такие симптомы, как спазмы и диарея.
Во время обострения часто лучше избегать продуктов с высоким содержанием клетчатки, которые сложнее переваривать, чем продукты с низким содержанием клетчатки.К продуктам с высоким содержанием клетчатки относятся следующие продукты:
- Свежие фрукты
- Бобовые, такие как сушеные бобы и чечевица
- Орехи
- Семена
- Сырые овощи или овощи с кожицей
- Цельные овощи, такие как брокколи и капуста 95 Зерновые
Жирные, жареные или жирные продукты, такие как масло, маргарин и сливки, также могут вызывать диарею.
С осторожностью относитесь к некоторым другим продуктам питания и напиткам:
- Алкогольные напитки Употребление алкоголя может усугубить диарею.
- Кофеин Это вещество, содержащееся в кофе, чае, шоколаде и многих безалкогольных напитках, может вызвать диарею.
- Газированные напитки Газированные напитки могут вызывать вздутие живота и газы у некоторых людей.
- Зерна Некоторые зерна могут вызывать дискомфорт в животе и диарею, особенно если вы чувствительны к глютену.
- Молочные продукты Эти продукты могут вызвать вздутие живота и диарею, особенно если у вас непереносимость лактозы. Но они могут быть хорошим источником белка и других питательных веществ.
- Spicy Foods Эти продукты могут вызвать диарею.
- Сладости Продукты и напитки с высоким содержанием сахара, такие как конфеты и соки, могут способствовать потере воды и обезвоживанию.
- Сверхобработанные продукты питания К этой категории относятся безалкогольные напитки, рафинированные подслащенные продукты, соленые закуски и обработанное мясо.
Некоторые люди будут иметь больше проблем с некоторыми продуктами и напитками, чем другие. Важно выяснить, какие продукты вызывают у вас дискомфорт при пищеварении, а затем избегать их.
Получение достаточного количества жидкости при язвенном колитеТолстая кишка поглощает воду из переваренной пищи и выводит твердые отходы из организма. Когда ваша толстая кишка воспаляется во время активного приступа язвенного колита, она не поглощает воду должным образом, что может привести к диарее и обезвоживанию.
Вот почему так важно пить достаточно жидкости, когда у вас активен язвенный колит.
По данным Калифорнийского университета в Сан-Франциско, хорошее практическое правило — потреблять половину унции (унции) жидкости на фунт (фунт) веса тела в день.Если вы весите, например, 150 фунтов, вам нужно как минимум 75 унций жидкости в день или более 9 чашек. Большинство напитков и даже некоторые продукты с высоким содержанием воды, такие как арбузы и огурцы, учитываются в этой сумме.
Поскольку питье ледяной жидкости или употребление слишком большого количества жидкости за один раз может усугубить диарею, лучше всего в течение дня делать глотки теплых или прохладных напитков.
Избегайте глотания жидкости, так как это может усугубить диарею и привести к глотанию воздуха вместе с жидкостью, что приведет к отрыжке.
Хороший способ измерить потребление жидкости — это следить за цветом мочи. Если он бледный или прозрачный, вероятно, вы пьете достаточно жидкости. Получение достаточного количества питательных веществ при язвенном колитеЯзвенный колит может затруднить получение необходимого питания — с точки зрения как основных компонентов вашего рациона, таких как белок, так и определенных витаминов и минералов.
Возможно, вам потребуется принимать витаминные или минеральные добавки, чтобы восполнить дефицит питательных веществ, вызванный язвенным колитом, вашим питанием или лекарствами, которые вы принимаете для лечения болезни.
Поговорите со своим врачом или диетологом о том, какие добавки, если таковые имеются, вам могут понадобиться.
Сосредоточьтесь на двух основных категориях питания:
- Всего калорий Поскольку язвенный колит может снизить аппетит и увеличить потребность в калориях, вам может потребоваться больше калорий, чем вы привыкли.
- Белок Когда вы находитесь в стадии ремиссии, адекватным потреблением белка обычно считается 1 грамм (г) в день на каждый килограмм (кг) — примерно 2.2 фунта — веса тела.
Это означает, что если вы весите 150 фунтов (68 кг), вы должны потреблять 68 г белка в день.
По данным Калифорнийского университета в Сан-Франциско, ваши потребности в белке могут увеличиться на 50 процентов сразу после обострения.Люди с язвенным колитом подвержены повышенному риску дефицита следующих витаминов и минералов:
- Фолиевая кислота, особенно если вы принимаете сульфасалазин (азульфидин)
- Магний, особенно если у вас хроническая диарея
- Кальций, особенно если вы принимаете преднизон (Deltasone)
- Железо, особенно при большей кровопотере из-за тяжелого заболевания
- Калий, повышенный риск хронической рвоты или диареи, или если вы принимаете преднизон
Прием пищи во время обострения болезни может вызвать спазмы в животе .Один из способов свести к минимуму этот дискомфорт — часто есть мягкую пищу небольшими порциями.
Если у вас возникли проблемы с поиском продуктов, которые не ухудшают ваши симптомы, или если вы теряете вес из-за этих трудностей, проконсультируйтесь с диетологом, который знает о воспалительных заболеваниях кишечника.
Ваш диетолог может порекомендовать жидкие добавки, если вы не переносите твердую пищу.Дополнительная информация Али Макферсон и Куинн Филлипс.
Питание в раннем возрасте влияет на восприимчивость к хроническому воспалительному колиту в более позднем возрасте
Рост щенков и состав тела
Для исследования влияния питания в раннем возрасте на созревание и функциональность кишечника мы использовали мышиную модель PNGR, вызванную недостаточным питанием во время период лактации за счет увеличения размера помета (рис.1а). Поскольку кишечник созревает в послеродовой период за относительно короткое время 14 , модели новорожденных грызунов представляют ценность для изучения влияния питания в раннем возрасте на созревание кишечника и связанные с ним кишечные расстройства.
Рис. 1ПНГ повлияла на рост и состав тела щенков. () Опытный образец. (b ) Кривые массы тела и (c ) прибавка массы тела после отъема в контрольной (CTRL) (n = 7 помётов) и постнатальной группе ограничения роста (PNGR) (n = 6 помётов) группах. (d ) Состав тела (фиолетовый = масса висцерального жира; зеленый = масса подкожного жира; синий = мышечная масса), (e ) жировая масса и (f ) мышечная масса у взрослых мышей с PNGR (n = 12 из 5 пометов) и мышей CTRL (n = 10 из 3 пометов) оценивали с помощью компьютерного томографа. Результаты представляют 3 независимых эксперимента. * P <0,05; ** P <0,01; *** P <0,001.
Щенки были случайным образом отнесены на четвертый постнатальный день (PN) либо к контрольному (CTRL) помету (8 детенышей), либо к большому помету (LL, 15 детенышей).Масса тела у всех детенышей в PN4 была одинаковой. Щенки из LL показали значительно меньшую массу тела из PN6 и в течение всего раннего постнатального периода ( P — значения в диапазоне PN6 и PN21 = 0,001–0,004) (рис. 1b). Масса тела детенышей с PNGR была ниже 10 -го перцентиля распределения массы тела в группе CTRL от PN6 до PN21. После отлучения от груди детеныши с PNGR демонстрировали догоняющий рост, обозначенный более высокой прибавкой массы тела (рис. 1c), тем самым достигая нормальной массы тела во взрослом возрасте (рис.1б). Несмотря на нормальную массу тела в зрелом возрасте, состав тела, измеренный с помощью компьютерной томографии, отличался в группах PNGR и CTRL (рис. 1d). Взрослые из PNGR показали более низкую массу общего, висцерального и подкожного жира ( P = 0,0003, P = 0,0004 и P = 0,0008, соответственно, рис. 1e), тогда как мышечная масса была выше ( P = 0,016 , Рис. 1е).
PNGR изменяет созревание кишечника
Чтобы исследовать влияние PNGR на созревание кишечника, мы исследовали морфогенез и функциональность кишечника в подвздошной и толстой кишке у детенышей при отъеме (PN21).
PNGR изменяет постнатальный морфогенез кишечника
PNGR был связан с незрелым эпителием подвздошной кишки в PN21, характеризуемым присутствием вакуолизированных энтероцитов ворсинок (рис. 2а), которые обычно исчезают в течение третьей недели жизни у грызунов. Глубина крипты подвздошной кишки была ниже у детенышей с PNGR ( P = 0,0005, рис. 2б). Разницы в высоте ворсинок подвздошной кишки не было ( P = 0,08, рис. 2c). Глубина крипт толстой кишки была меньше ( P = 0,04, рис.2d, e), а также толщину слизистой оболочки ( P = 0,004, рис. 2d, f) у детенышей с PNGR при PN21. Количество бокаловидных клеток на крипту толстой кишки было уменьшено у детенышей с PNGR ( P = 0,004, фиг. 2g).
Рисунок 2PNGR изменил созревание кишечника у детенышей при отъеме. (a ) Типичное окрашивание гематоксилином и эозином (HE) срезов подвздошной кишки от контрольных (CTRL) и постнатальных детенышей с ограничением роста (PNGR). (b ) Глубина крипты и высота ворсинок (c ) в подвздошной кишке на 21-й постнатальный день (PN21) в группах CTRL (n = 12 из 4 пометов) и PNGR (n = 11 из 4 пометов). (d ) Репрезентативное окрашивание HE срезов толстой кишки от CTRL и PNGR детенышей. (e ) Глубина крипты, (f ) толщина слизистой оболочки и (g ) количество бокаловидных клеток в толстой кишке при PN21 в CTRL (n = 12 из 4 пометов) и PNGR (n = 11 из 4 пометов) группы. Репрезентативное окрашивание сиалированных гликанов (h ) лектином MAA и фукозилированных гликанов (i ) лектином UEA1 в подвздошной и толстой кишке при PN21 в CTRL (n = 11 из 4 пометов) и PNGR (n = 10 из 4 пометов) группы. (j ) Репрезентативное иммуноокрашивание окклюдина в подвздошной и толстой кишке при PN21 в группах CTRL (n = 9–11 из 4 пометов) и PNGR (n = 8–9 из 4 пометов). (k ) Репрезентативное иммуноокрашивание claudin7 в подвздошной и толстой кишке на PN21 в группах CTRL (n = 9 из 4 пометов) и PNGR (n = 11 из 4 пометов). (l ) In vivo параклеточная проницаемость кишечника для FITC-декстрана 4 кДа при PN21 в группах CTRL (n = 12 из 4 пометов) и PNGR (n = 8 из 4 пометов). (m – r ) Экспрессия цитокинов в толстой кишке в PN21 в группах CTRL (n = 9–14 из 4 пометов) и PNGR (n = 9–11 из 4 пометов). Результаты являются репрезентативными для 2–3 независимых экспериментов. * P <0,05; ** P <0,01; *** P <0,001.
PNGR нарушает экспрессию ферментов щеточной каймы у детенышей при отъеме от груди
Для изучения пищеварительной и детоксицирующей способности подвздошной кишки были проанализированы характер экспрессии и уровень активности основных ферментов щеточной каймы дипептидилпептидазы IV (DPPIV) и кишечной щелочной фосфатазы (IAP) .Экспрессия DPPIV и IAP на щеточной кайме, по-видимому, снижена в подвздошной кишке детенышей с PNGR при PN21, как показывает иммуногистохимия ( P <0,0001 и P = 0,0003, соответственно, Suppl. Fig. S1a). Однако DPPIV экспрессировался в цитоплазме вакуолизированных энтероцитов ворсинок детенышей с PNGR (Suppl. Fig. S1a). Уровень активности DPPIV в подвздошной кишке был одинаковым в обеих группах при PN21 ( P = 0,95, Suppl. Fig. S1b). Напротив, уровень активности ВБД в подвздошной кишке увеличился на 2.6 раз у детенышей с PNGR при PN21 ( P = 0,04, дополнительный рис. S1c). Более высокая активность IAP в группе PNGR может быть компенсирующим эффектом для увеличения детоксикационной способности LPS 15 .
PNGR вызывает изменения в паттерне гликозилирования кишечного эпителия у детенышей при отъеме от груди
Гликозилирование тканей хозяина регулируется диетой и микробиотой. В свою очередь, кишечный гликом может модулировать состав микробиоты, предоставляя питательные вещества, которые способствуют росту определенных бактерий 16,17 .Чтобы определить, может ли PNGR влиять на гликозилирование O , мы исследовали с помощью иммунофлуоресценции экспрессию сиалилированных и фукозилированных гликанов, оцениваемую с помощью иммуноокрашивания на PN21 с помощью агглютинина Maackia amurensis (MAA) и Ulex europaeus aglutin (Ulex europaeus, aglutin). соответственно. Окрашивание MAA было ниже в подвздошной и толстой кишке детенышей с PNGR ( P = 0,0005 и P <0,0001, соответственно, рис. 2h), в то время как при использовании UEA1 различий между двумя группами не было обнаружено ( P = 0.97 и P = 0,47 соответственно, рис. 2i).
PNGR изменяет кишечный барьер у детенышей при отъеме от груди
Чтобы оценить влияние PNGR на функцию эпителиального барьера, мы измерили с помощью иммунофлуоресцентного окрашивания на срезах подвздошной и толстой кишки экспрессию двух основных белков плотного соединения, клаудина7 и окклюдина. PNGR был связан с нарушением экспрессии белков плотных контактов в обеих тканях на PN21. Экспрессия окклюдина была ограничена криптами подвздошной кишки детенышей с PNGR (рис.2j), тогда как у крысят CTRL окрашивание окклюдином наблюдалось в криптах и вдоль ворсинок. В толстой кишке окклюдин был менее экспрессирован у детенышей с PNGR по сравнению с CTRL ( P = 0,001, фиг. 2j). Количественная оценка окрашивания Claudin7 была сходной в криптах и ворсинах подвздошной кишки в обеих группах. Однако экспрессия claudin7 была искажена в эпителии ворсинок детенышей с PNGR, где claudin7 в основном экспрессировался на базолатеральной стороне энтероцитов (Fig. 2k). В толстой кишке распределение claudin7 выглядело одинаковым в обеих группах ( P = 0.75, рис. 2к). Чтобы оценить, влияет ли паттерн экспрессии белков плотных контактов на целостность кишечного барьера, мы затем измерили in vivo кишечную проницаемость для декстрана, меченного FITC 4 кДа, в PN21. У детенышей с PNGR обнаружена повышенная парацеллюлярная проницаемость кишечника ( P <0,0001, рис. 2l).
PNGR вызывает увеличение экспрессии провоспалительных цитокинов у детенышей при отъеме от груди
Чтобы проверить, связана ли повышенная кишечная проницаемость с провоспалительным ответом иммунной системы слизистой оболочки, мы измерили несколько уровней цитокинов в образцах подвздошной и толстой кишки.Уровень IFNγ был сходным в обеих группах в толстой кишке при PN21 ( P = 0,98, рис. 2m). Экспрессия на уровне белка провоспалительных цитокинов TNF-α ( P <0,0001, фиг. 2n), интерлейкина (IL) -1β ( P = 0,01, фиг. 2o) и IL-6 ( P = 0,003, рис. 2p), был увеличен в толстой кишке у детенышей с PNGR. Экспрессия цитокинов, связанных с Th27 (IL-17) и регуляторным (IL-10) иммунным ответом, была сходной в обеих группах ( P = 0.44, рис. 2q и P = 0,35, рис. 2r соответственно). В подвздошной кишке экспрессия TNF-α была выше у детенышей с PNGR ( P <0,0001, Suppl. Fig. S2). Уровни IFN-γ, IL-1β, IL-17A, IL-6 и IL-10 были одинаковыми в обеих группах (дополнительный рис. S2).
Взятые вместе, эти данные показывают, что PNGR отрицательно влиял на статус созревания кишечника и целостность кишечного барьера, что было связано с провоспалительным статусом слизистой оболочки кишечника в раннем возрасте.
PNGR вызывает изменения функций кишечника у взрослых мышей
Чтобы изучить, могут ли изменения, обнаруженные в тканях кишечника детенышей с PNGR, повлиять на взрослый возраст, морфологию и функции кишечника в подвздошной и толстой кишке у взрослых мышей исследовали при PN60.
Глубина крипты подвздошной кишки ( P = 0,002, рис. 3a, b) и высота ворсинок ( P = 0,001, рис. 3a, c) были увеличены у взрослых мышей с PNGR по сравнению со взрослыми мышами CTRL. Точно так же в двоеточии глубина крипты ( P = 0.0005, фиг. 3d, e) и толщина слизистой оболочки ( P = 0,002, фиг. 3d, f) были увеличены у взрослых мышей PNGR по сравнению со взрослыми мышами CTRL. Кроме того, количество бокаловидных клеток в толстой кишке не различалось в обеих группах ( P = 0,25, фиг. 3g).
Рисунок 3PNGR оказал долгосрочное влияние на состояние здоровья кишечника взрослых мышей. (a ) Типичное окрашивание гематоксилином и эозином (HE) срезов подвздошной кишки от контрольных (CTRL) и постнатальных мышей с ограничением роста (PNGR) взрослых мышей. (b ) Глубина крипты и высота ворсинок (c ) в подвздошной кишке на 60-й постнатальный день (PN60) в группах CTRL (n = 12 из 4 пометов) и PNGR (n = 12 из 4 пометов). (d ) Типичное окрашивание HE срезов толстой кишки взрослых мышей CTRL и PNGR. (e ) Глубина крипты, (f ) толщина слизистой оболочки и (g ) количество бокаловидных клеток в толстой кишке при PN60 в группах CTRL (n = 12 из 4 пометов) и PNGR (n = 12 из 4 пометов) . Типичное окрашивание сиалированных гликанов (h ) лектином MAA и фукозилированных гликанов (i ) лектином UEA1 в подвздошной и толстой кишке при PN60 в CTRL (n = 12 из 4 пометов) и PNGR (n = 12 из 4 пометов) группы. (j ) Репрезентативное иммуноокрашивание окклюдина в подвздошной и толстой кишке при PN60 в группах CTRL (n = 6 из 3 пометов) и PNGR (n = 6 из 3 пометов). (k ) Репрезентативное иммуноокрашивание claudin7 в подвздошной и толстой кишке при PN60 в группах CTRL (n = 12 из 4 пометов) и PNGR (n = 12 из 4 пометов). (l ) In vivo парацеллюлярная проницаемость кишечника для FITC-декстрана 4 кДа при PN60 в группах CTRL (n = 12 из 4 пометов) и PNGR (n = 10 из 4 пометов). Результаты являются репрезентативными для 2–3 независимых экспериментов.* P <0,05; ** P <0,01; *** P <0,001.
Экспрессия белков DPPIV и IAP на щеточной кайме в подвздошной кишке была сходной в обеих группах при PN60 ( P = 0,24 и P = 0,35, соответственно, Suppl. Fig. S3a). Тем не менее, на уровне активности фермента DPPIV и IAP были снижены в 1,4 раза во взрослой подвздошной кишке с PNGR ( P = 0,003 и P = 0,02, соответственно, дополнительные рис. S3b и S3c) по сравнению со взрослыми мышами CTRL. .
Иммуноокрашивание лектином MAA для оценки сиалирования показало меньшее количество сиалированных гликанов в подвздошной кишке взрослых мышей с PNGR по сравнению с CTRL ( P = 0,02, рис. 3h). Фукозилированные гликаны, оцененные с помощью иммуноокрашивания лектином UEA1, были одинаковыми в обеих группах в подвздошной и толстой кишке при PN60 ( P = 0,35 и P = 0,07, соответственно, рис. 3i).
Что касается целостности эпителиального барьера, экспрессия окклюдина не различалась ни в подвздошной кишке, ни в толстой кишке между взрослыми группами PNGR и CTRL при PN60 ( P = 0.25 и P = 0,48 соответственно, рис. 3j). Экспрессия Claudin7 в подвздошной кишке взрослых мышей PNGR была снижена по всей крипте-ворсинке по сравнению с мышами CTRL ( P = 0,03 в ворсинках и P = 0,005 в криптах, рис. 3k), но не в толстой кишке ( P ). = 0,07, рис. 3к). Наконец, парацеллюлярная проницаемость кишечника, измеренная через четыре часа после орогастрального зондирования мышей раствором декстрана, меченного FITC 4 кДа, не увеличивалась у взрослых мышей с PNGR по сравнению с CTRL ( P = 0.23, рис. 3л).
PNGR изменяет бактериальную колонизацию кишечника
Поскольку кишечная микробиота имеет решающее значение для созревания и защиты эпителиального барьера и образования иммунной системы, мы изучили богатство и состав микробиоты из образцов фекалий в PN21 и PN60 с использованием бактериальной 16S рРНК секвенирование генного ампликона (Illumina MiSeq). Среднее число прочтений на выборку составило 66 397 (58 818–76 509), разделенных на 2 075 операционных таксономических единиц (OTU).Α-разнообразие показало увеличение богатства микробиоты между PN21 и PN60 в обеих группах (рис. 4a) и, что интересно, меньшее богатство у детенышей с PNGR ( P = 0,0014, рис. 4a). При PN60 больше не было разницы между двумя группами ( P = 0,70, рис. 4a). Общий состав фекальной микробиоты, измеренный с помощью взвешенного расстояния Unifrac, показал небольшое разделение групп вдоль ПК1 в анализе основных координат (PCoA) на PN21 (рис. 4b), что свидетельствует о различии между группами CTRL и PNGR.Однако образцы PN60 не были разделены на графике PCoA и перекрывались (рис. 4c), что позволяет предположить, что фекальная микробиота была более схожей во взрослом возрасте. Различия, обнаруженные в относительных уровнях численности родов, соответствовали более отчетливой микробиоте в PN21 по сравнению с PN60, поскольку 21 род значительно различались между двумя исследуемыми группами в PN21 и только одним родом в PN60 (Таблица 1). Со временем тридцать два рода развивались одинаково в обеих группах между PN21 и PN60 (Таблица 1).Семь родов показали противоположное развитие во времени между двумя группами. Odoribacter spp. и несколько членов Firmicutes, в основном принадлежащих к семейству Lachnospiraceae, имели более низкие значения PN21 в PNGR по сравнению с CTRL, а затем повышались до PN60 у мышей с PNGR (рис. 4d). Несколько родов не увеличились в группе PNGR между PN21 и PN60, тогда как они увеличились со временем в группе CTRL: Atopobium spp., Несколько некультивируемых членов семейства Ruminococcaceae (группа NK4A214, UCG-005, UCG-010 и UCG- 013), Turicibacter spp., и Bilophila spp. (Таблица 1). Candidatus Arthromitus spp. увеличилось с PN21 до PN60 только в группе PNGR (рис. 4d) и группе Firmicutes Family XIII Eubacterium nodatum , а также в группе Desulfovibrio spp. (Proteobacteria) уменьшилось только в группе PNGR (Таблица 1). Шесть родов были высокоспецифичными для PNGR в PN21 и показали высокие уровни численности только в этой группе и в определенный момент времени: Parabacteroides spp., Erysipelatoclostridium spp., Eubacterium coprostanoligenes spp., Enterococcus spp., Staphylococcus spp. И Escherichia-Shigella spp. (Рис. 4e). Эти данные демонстрируют, что PNGR повлиял на состав и состав микробиоты в раннем возрасте у детенышей.
Рис. 4PNGR измененная бактериальная колонизация кишечника. (a ) α-разнообразие фекальной микробиоты в группах контроля (CTRL, n = 18 из 6 пометов) и постнатального ограничения роста (PNGR, n = 17–18 из 6 пометов) на 21-й день (PN21) и в постнатальный день 60 (PN60).Филогенетическое расстояние между образцами фекальной микробиоты на (b ) PN21 и (c ) PN60 в группах CTRL и PNGR. Бактериальные роды с низкой численностью (d ) и высокой численностью (e ) в PN21 у детенышей с PNGR по сравнению с CTRL. Результаты представляют 3 независимых эксперимента. * P <0,05; ** P <0,01; *** P <0,001.
Таблица 1 Таксономический профиль фекальной микробиоты.PNGR влияет на восприимчивость к колиту у взрослых мышей
Чтобы исследовать, оказывает ли PNGR долгосрочное влияние на иммунный гомеостаз кишечника, мы вызвали хронический колит пероральным введением 3% декстрансульфата натрия (DSS) взрослым мышам.Взрослые мыши CTRL и PNGR получали питьевую воду (CTRL-H 2 O; PNGR-H 2 O) или 3% DSS в питьевой воде в течение трех циклов, состоящих из пяти дней DSS с последующими семью днями обычной питьевой воды ( CTRL-DSS; PNGR-DSS). Гистологическую тяжесть колита, длину толстой кишки и экспрессию цитокинов оценивали в конце трех циклов.
Взрослые мыши PNGR, не подвергавшиеся воздействию DSS (PNGR-H 2 O), экспрессировали более высокие уровни провоспалительных цитокинов в слизистой оболочке кишечника, что указывает на то, что PNGR приводил к измененному иммунному статусу у взрослых мышей без предварительного заражения DSS.В подвздошной кишке экспрессия провоспалительного цитокина IL-1β была увеличена у взрослых мышей с PNGR ( P = 0,007, Suppl. Fig. S4a), как и уровни экспрессии цитокинов IL-10 ( P ). = 0,004, дополнительный рисунок S4b) и IL-17 ( P = 0,01, дополнительный рисунок S4c). Уровни IFN-γ, TNF-α и IL-6 были одинаковыми в обеих группах (Дополнение, Рис. S4d-f). В толстой кишке экспрессия цитокинов Th2 IFN-γ ( P = 0,009, фиг. 5a) и TNF-α ( P = 0,02, фиг. 5b) была увеличена у взрослых мышей с PNGR, как и экспрессия цитокина IL-17 Th27 ( P = 0.02, фиг. 5c), и регуляторный иммунный ответ, связанный с цитокином IL-10 ( P = 0,02, фиг. 5d). Экспрессия цитокина IL-6, связанного с иммунным ответом Th3 ( P = 0,22, фиг. 5e), и IL-1β ( P = 0,56, фиг. 5f) была сходной в обеих группах.
Фигура 5PNGR индуцировал более высокую восприимчивость к хроническому химически индуцированному колиту у взрослых мышей. Контрольные (CTRL) взрослые мыши и мыши с ограничением послеродового роста (PNGR) получали питьевую воду (CTRL-H 2 O, n = 6 из 3 пометов; PNGR-H 2 O, n = 6 из 3 пометов) или 3%. декстран-сульфат натрия (DSS) в питьевой воде в течение трех циклов, состоящих из пяти дней DSS с последующими семью днями обычного питья воды (CTRL-DSS, n = 19 из 6 пометов; PNGR-DSS, n = 15 из 4 пометов). (a – f ) Экспрессия цитокинов в толстой кишке в группах CTRL и PNGR. (г ) Изменение массы тела. * P <0,05; ** P <0,01, PNGR-DSS по сравнению с CTRL-DSS. $$ P <0,01; $$$ P <0,001, PNGR-DSS по сравнению с PNGR-H 2 O. §§ P <0,01; §§§ P <0,001, CTRL-DSS vs. CTRL-H 2 O. (h ) Длина двоеточия. ** P <0.01; *** P <0,001. (i ) Типичное окрашивание гематоксилином и эозином срезов толстой кишки после трех циклов DSS и гистологическая оценка тяжести колита (j ). * P <0,05; ** P <0,01; *** P <0,001. * P <0,05; *** P <0,001. Результаты являются репрезентативными для 2 независимых экспериментов.
Колит DSS вызвал значительную потерю массы тела в обеих группах. Потеря массы тела была максимальной на 9-й день острой фазы колита и была менее выраженной в группе PNGR ( P = 0.03, рис. 5ж). После 9-го дня животные в обеих группах выздоровели, достигнув своей исходной массы тела к 25-му дню в контрольной группе и к 13-му дню в группе PNGR (фиг. 5g). Хроническое введение DSS вызывало более выраженное уменьшение длины толстой кишки в группе PNGR ( P = 0,006, фиг. 5h). Гистологическая оценка тяжести была выше у мышей PNGR ( P = 0,02, рис. 5i, j). После трех циклов DSS TNF-α был единственным цитокином, который был повышен в толстой кишке в группе CTRL (CTRL-H 2 O vs.CTRL-DSS: P = 0,02, рис. 5б). Экспрессия в толстой кишке провоспалительных цитокинов TNF-α, IL-1β и IL-17 была выше у мышей PNGR, чем у CTRL (CTRL-DSS по сравнению с PNGR-DSS: P = 0,006, рис. 5b; P = 0,04, рис. 5f и P = 0,04, рис. 5c, соответственно). Экспрессия связанного с регуляторным иммунным ответом цитокина IL-10 снизилась в группе PNGR после трех циклов DSS (PNGR-H 2 O по сравнению с PNGR-DSS: P = 0,01, рис.5г). Повышенная гистологическая оценка тяжести, более выраженное укорочение толстой кишки, стойкая повышенная экспрессия провоспалительных цитокинов и снижение регуляторного иммунного ответа предполагают более высокую восприимчивость к хроническому химически индуцированному колиту у взрослых мышей PNGR.
Язвенный колит и диета — Gastrointestinal Society
Язвенный колит и диетаGIS2020-04-01T13: 36: 32-07: 00Что такое язвенный колит?
Язвенный колит — хроническое воспалительное заболевание, поражающее слизистую оболочку толстой и прямой кишки.Причина неизвестна, и хотя она не имеет наследственной составляющей, в некоторых семьях она может быть более частой. Слизистая оболочка кишечника изъязвляется, как правило, первоначально от нижнего конца толстой кишки. Симптомы включают диарею, кровь в стуле, спазмы, лихорадку и / или потерю веса.
Как диагностируется?
Язвенный колит диагностируется с помощью клинических, колоноскопических и гистологических исследований. Колоноскоп / сигмоидоскоп вводится в толстую кишку, а затем образец биопсии подтверждает диагноз.Клинические симптомы и анализы крови могут помочь оценить кровопотери и дефицит питательных веществ у пациентов.
Как лечится язвенный колит?
Язвенный колит лечится медикаментами, а иногда и хирургическим путем. Чтобы уменьшить воспаление, часто используются такие лекарства, как сульфасалазин, месаламин, олсалазин и кортикостероиды. Другие лекарства, которые могут быть эффективными, — это будесонид, азатиоприн и некоторые антибиотики. Людям с тяжелым заболеванием, не поддающимся медицинскому лечению, может потребоваться операция по удалению части (или всей) толстой кишки.
Какие рекомендации по диете при язвенном колите?
- Люди с язвенным колитом часто страдают дефицитом железа в результате кровопотери. Это можно исправить с помощью добавок железа или употребления продуктов с высоким содержанием железа, таких как печень, говядина, индейка, баранина, тофу, шпинат, патока, овсянка и яйца.
- Достаточное количество жидкости и продукты с низким содержанием клетчатки могут быть полезными при лечении диареи.
- Стимуляторы и раздражители следует избегать в соответствии с индивидуальной переносимостью, e.грамм. жирная пища, кофеин, острая пища и / или продукты из отрубей.
- Не было доказано, что парентеральное питание и элементарная диета более эффективны, чем пероральная диета для предотвращения хирургического вмешательства или содействия ремиссии.
Продукты с низким содержанием клетчатки
| Хлеб и злаки (размер порции: 1 ломтик или 1/2 стакана) |
| Печенье Arrowroot (2), бублик, хлеб (белый, цельнозерновой, изюм, мультизерновой, лаваш), Cheerios, кукурузные хлопья, овсянка, макаронные изделия, воздушная пшеница, рис (белый, коричневый), рисовые криспи, Special K, Total |
| Фрукты (размер порции: 1 маленькая или 1/2 чашки) |
| Яблоко, абрикос, банан, дыня, вишня, фруктовый салат (консервированный), грейпфрут, виноград, дыня, сок, мандарин, манго, персик, слива, ананас, клубника, мандарин |
| Овощи (размер порции: 1 маленькая или 1/2 стакана) |
| Артишок, спаржа, ростки фасоли, свекла, капуста, цветная капуста, сельдерей, огурец, салат, грибы, лук, картофель, зеленый перец, редис, кабачки, помидоры |
Заключение
Многие люди, страдающие язвенным колитом, могут пережить ремиссию своего заболевания, и в это время им не нужно соблюдать специальную диету.Медикаменты являются основным методом лечения в периоды активного заболевания, а диета может помочь облегчить некоторые симптомы. Если у вас возникнут дополнительные вопросы о язвенном колите, проконсультируйтесь с врачом.
Мэри Флешер , клинический диетолог, больница Ричмонда
Впервые опубликовано в выпуске 142 информационного бюллетеня
Inside Tract® — март / апрель 2004 г.Изображение: Энгин Акюрт с сайта Pexels.com
Противовоспалительная диета как лечение воспалительного заболевания кишечника: отчет о серии случаев | Журнал питания
Day AS, Ledder O, Leach ST, Lemberg DA: болезнь Крона и колит у детей и подростков. Мир Дж. Гастроэнтерол. 2012, 18: 5862-5869. 10.3748 / wjg.v18.i41.5862.
Артикул PubMed PubMed Central Google ученый
Brown AC, Rampertab SD, Mullin GE: Существующие диетические рекомендации при болезни Крона и язвенном колите. Эксперт Рев Гастроэнтерол Гепатол. 2011, 5: 411-425. 10.1586 / например.11.29.
Артикул PubMed Google ученый
Balfour Sartor R: UpToDate 2013. Пробиотики при желудочно-кишечных заболеваниях. 2013, UpToDate 2013. Расположение: 95 Sawyer Rd. Уолтем, Массачусетс, 02453-
Google ученый
Bl AO: Трансплантация фекальной микробиоты. Курр Опин Гастроэнтерол. 2013, 29 (1): 79-84. 10.1097 / MOG.0b013e32835a4b3e.
Артикул Google ученый
Roses RE, Rombeau JL: Последние тенденции в хирургическом лечении воспалительных заболеваний кишечника.Мир Дж. Гастроэнтерол. 2008, 14: 408-412. 10.3748 / wjg.14.408.
Артикул PubMed PubMed Central Google ученый
Fazio VW, Ziv Y, Church JM, Oakley JR, Lavery IC, Milsom JW, Schroeder TK: Осложнения и функции анастомозов подвздошной кишки и анального анастомоза у 1005 пациентов. Ann Surg. 1995, 222: 120-127. 10.1097 / 00000658-199508000-00003.
CAS Статья PubMed PubMed Central Google ученый
Hahnloser D, Pemberton JH, Wolff BG, Larson DR, Crownhart BS, Dozois RR: Результаты в срок до 20 лет после анастомоза подвздошно-анального мешка при хроническом язвенном колите. Br J Surg. 2007, 94: 333-340. 10.1002 / bjs.5464.
CAS Статья PubMed Google ученый
Басси А., Додд С., Уильямсон П., Боджер К.: Стоимость воспалительного заболевания кишечника в Великобритании: ретроспективное исследование одного центра. Кишечник. 2004, 53: 1471-1478.10.1136 / gut.2004.041616.
CAS Статья PubMed PubMed Central Google ученый
Картер М.Дж., Лобо А.Дж., Трэвис С.П., Секция ВЗК, Британское общество гастроэнтерологии: Рекомендации по ведению воспалительного заболевания кишечника у взрослых. Кишечник. 2004, 53 (Приложение 5): V1-V16.
Артикул PubMed PubMed Central Google ученый
Ямамото Т .: Питание и диета при воспалительном заболевании кишечника.Курр Опин Гастроэнтерол. 2013, 29: 216-221. 10.1097 / MOG.0b013e32835b9a40.
CAS Статья PubMed Google ученый
Triggs CM, Munday K, Hu R, Fraser AG, Gearry RB, Barclay ML, Ferguson LR: Диетические факторы при хроническом воспалении: пищевая толерантность и непереносимость новозеландской популяции с кавказской болезнью Крона. Mutat Res. 2010, 690: 123-138. 10.1016 / j.mrfmmm.2010.01.020.
CAS Статья PubMed Google ученый
Пирсон М., Тиахон К., Леви А.Дж., Бьярнасон I. Пищевая непереносимость и болезнь Крона. Кишечник. 1993, 34: 783-787. 10.1136 / gut.34.6.783.
CAS Статья PubMed PubMed Central Google ученый
Хаас С.В., Хаас МП: Лечение целиакии. 1951, Липпинкотт, Филадельфия
Google ученый
Shivappa N, Steck SE, Hurley T.G., Hussey JR, Hebert JR: Разработка и разработка основанного на литературе популяционного диетического воспалительного индекса.Public Health Nutr. 2013, 14: 1-8.
Google ученый
Cavicchia PP, Steck SE, Hurley TG, Hussey JR, Ma Y, Ockene IS, Hebert JR: новый диетический воспалительный индекс предсказывает интервальные изменения в сыворотке высокочувствительного С-реактивного белка. J Nutr. 2009, 139: 2365-2372. 10.3945 / jn.109.114025.
CAS Статья PubMed PubMed Central Google ученый
Lichtiger S, Present DH, Kornbluth A, Gelernt I, Bauer J, Galler G, Michelassi F, Hanauer S: циклоспорин при тяжелом язвенном колите, резистентном к стероидной терапии. N Engl J Med. 1994, 330: 1841-1845. 10.1056 / NEJM199406303302601.
CAS Статья PubMed Google ученый
Vermeire S, Schreiber S, Sandborn WJ, Dubois C, Rutgeerts P: Корреляция между активностью болезни Крона и индексами Харви-Брэдшоу при оценке тяжести болезни Крона.Clin Gastroenterol Hepatol. 2010, 8: 357-363. 10.1016 / j.cgh.2010.01.001.
Артикул PubMed Google ученый
Tamboli CP, Neut C, Desreumaux P, Colombel JF: Дисбактериоз при воспалительном заболевании кишечника. Кишечник. 2004, 53: 1-4. 10.1136 / gut.53.1.1.
CAS Статья PubMed PubMed Central Google ученый
О’Флаэрти С., Солнье Д.М., Пот Б., Версалович Дж .: Как пробиотики и пребиотики могут влиять на иммунитет слизистой оболочки ?.Кишечные микробы. 2010, 1: 293-300. 10.4161 / gmic.1.5.12924.
Артикул PubMed PubMed Central Google ученый
Fujimori S, Gudis K, Mitsui K, Seo T, Yonezawa M, Tanaka S, Tatsuguchi A, Sakamoto C: рандомизированное контролируемое испытание эффективности синбиотиков по сравнению с пробиотиками или пребиотиками для улучшения качества жизни у больных язвенным колитом. Питание (Бербанк, округ Лос-Анджелес, Калифорния, 2009 г., 25: 520-525.10.1016 / j.nut.2008.11.017.
Артикул Google ученый
Bosscher D, Breynaert A, Pieters L, Hermans N: пищевые стратегии для изменения состава кишечной микробиоты и связанных с ними последствий для здоровья. J. Physiol Pharmacol. 2009, 60 (Прил. 6): 5-11.
PubMed Google ученый
Цзя В., Уайтхед Р.Н., Гриффитс Л., Доусон С., Уоринг Р.Х., Рамсден Д.Б., Хантер Дж.О., Коул Дж.А.: Имеет ли отношение обилие Faecalibacterium prausnitzii к болезни Крона?Письма по микробиологии FEMS. 2010, 310: 138-144. 10.1111 / j.1574-6968.2010.02057.x.
CAS Статья PubMed PubMed Central Google ученый
McFarland LV: Систематический обзор и метаанализ Saccharomyces boulardii у взрослых пациентов. Мир Дж. Гастроэнтерол. 2010, 16 (18): 2202-2222. 10.3748 / wjg.v16.i18.2202.
Артикул PubMed PubMed Central Google ученый
Furrie E, Macfarlane S, Kennedy A, Cummings JH, Walsh SV, O’Neil DA, Macfarlane GT: терапия синбиотиками (Bifidobacterium longum / Synergy 1) инициирует разрешение воспаления у пациентов с активным язвенным колитом: рандомизированное контролируемое пилотное исследование. Кишечник. 2005, 54: 242-249. 10.1136 / gut.2004.044834.
CAS Статья PubMed PubMed Central Google ученый
Лореа Бароя М., Кирьявайнен П.В., Хекмат С., Рид Г.: Противовоспалительные эффекты пробиотического йогурта у пациентов с воспалительными заболеваниями кишечника.Clin Exp Immunol. 2007, 149: 470-479. 10.1111 / j.1365-2249.2007.03434.x.
CAS Статья PubMed PubMed Central Google ученый
Хоу Дж. К., Абрахам Б., Эль-Сераг Х: Диетическое питание и риск развития воспалительного заболевания кишечника: систематический обзор литературы. Am J Gastroenterol. 2011, 106: 563-573. 10.1038 / ajg.2011.44.
CAS Статья PubMed Google ученый
Геррейро С.С., Феррейра П., Таварес Л., Сантос П.М., Невес М., Брито М., Краво М.: Полиморфизмы жирных кислот, IL6 и TNFalpha: пример нутригенетики при болезни Крона. Am J Gastroenterol. 2009, 104: 2241-2249. 10.1038 / ajg.2009.313.
Артикул PubMed Google ученый
Triantafillidis JK, Merikas E, Georgopoulos F: Текущие и новые препараты для лечения воспалительных заболеваний кишечника. Drug Des Devel Ther.2011, 5: 185-210.
CAS Статья PubMed PubMed Central Google ученый
Wall R, Ross RP, Fitzgerald GF, Stanton C: Жирные кислоты из рыбы: противовоспалительный потенциал длинноцепочечных жирных кислот омега-3. Обзоры питания. 2010, 68: 280-289. 10.1111 / j.1753-4887.2010.00287.x.
Артикул PubMed Google ученый
Guijarro LG, Mate J, Gisbert JP, Perez-Calle JL, Marin-Jimenez I, Arriaza E, Olleros T, Delgado M, Castillejo MS, Prieto-Merino D, Gonzalez Lara V, Pena AS: N -ацетил-L-цистеин в сочетании с месаламином в лечении язвенного колита: рандомизированное плацебо-контролируемое пилотное исследование.Мир Дж. Гастроэнтерол. 2008, 14: 2851-2857. 10.3748 / wjg.14.2851.
CAS Статья PubMed PubMed Central Google ученый
Choi JH, Chung KM, Park K: Психосоциальные предикторы четырех видов поведения, способствующих укреплению здоровья, для профилактики рака с использованием стадии изменения транстеоретической модели. Психоонкология. 2013, 29 (22): 2253-2261.
Google ученый
Подольский Д.К .: Будущее лечения ВЗК. J Gastroenterol. 2003, 38 (Приложение 15): 63-66.
CAS PubMed Google ученый
Шейл Б., Шанахан Ф., О’Махони Л.: Пробиотические эффекты при воспалительном заболевании кишечника. J Nutr. 2007, 137: 819С-824С.
CAS PubMed Google ученый
Schwiertz A, Jacobi M, Frick JS, Richter M, Rusch K, Kohler H: Микробиота при воспалительных заболеваниях кишечника у детей.J Pediatr. 2010, 157: 240-244.e1. 10.1016 / j.jpeds.2010.02.046.
Артикул PubMed Google ученый
Галланд Л: Ракель: Интегративная медицина. 2007, Филадельфия: Сондерс Эльзевир, 2
Google ученый
Paturi G, Mandimika T, Butts CA, Zhu S, Roy NC, McNabb WC, Ansell J: Влияние диетической черники и брокколи на активность микробиоты слепой кишки и морфологию толстой кишки у мышей mdr1a (- / -), a модель воспалительных заболеваний кишечника.Питание. 2012, 28 (3): 324-330. 10.1016 / j.nut.2011.07.018.
CAS Статья PubMed Google ученый
Остерман М: Заживление слизистой оболочки при воспалительном заболевании кишечника. J Clin Gastroenterol. 2013, 47 (3): 212-221. 10.1097 / MCG.0b013e3182732ff5.
Артикул PubMed Google ученый
Massironi S, Rossi R, Cavalcoli F, Della Valle S, Fraquell IM, Conte D: Дефицит питательных веществ при воспалительном заболевании кишечника: терапевтические подходы.Clin Nutr. 2013, S0261-5614 (13): 00098-8.
Google ученый
Donnellan C, Yann L, Lal S: Управление питанием при болезни Крона. Therap Adv Гастроэнтерол. 2013, 6 (3): 231-242. 10.1177 / 1756283X13477715.
Артикул PubMed PubMed Central Google ученый
Thia KT, Sandborn WJ, Harmsen WS, Zinsmeister AR, Loftus EV: Факторы риска, связанные с прогрессированием кишечных осложнений болезни Крона в популяционной когорте.Гастроэнтерология. 2010, 139: 1147-1155. 10.1053 / j.gastro.2010.06.070.
Артикул PubMed PubMed Central Google ученый
Хаас С.В., Хаас М.П.: лечение целиакии с помощью специальной углеводной диеты; сообщают о 191 дополнительном случае. Am J Gastroenterol. 1955, 23: 344-360.
CAS PubMed Google ученый
Gottschall E: Разорвать порочный круг: здоровье кишечника с помощью диеты.2004, Балтимор, Онтарио: Kirkton Press Ltd
Google ученый
Роберфроид М: Пребиотики: новая концепция. J Nutr. 2007, 137: 830S-837S.
CAS PubMed Google ученый
Comino I, Real A, de Lorenzo L, Cornell H, Lopez-Casado MA, Barro F, Lorite P, Torres MI, Cebolla A, Sousa C: Разнообразие потенциальной иммуногенности овса: основа для выбора сорта овса, не токсичные при глютеновой болезни.Кишечник. 2011, 60: 915-922. 10.1136 / gut.2010.225268.
CAS Статья PubMed PubMed Central Google ученый
Харди Х, Харрис Дж, Лайон Э, Бил Дж, Фоуи А.Д.: Пробиотики, пребиотики и иммуномодуляция защитных функций слизистой оболочки кишечника: гомеостаз и иммунопатология. Питательные вещества. 2013, 5: 1869-1912. 10.3390 / nu5061869.
CAS Статья PubMed PubMed Central Google ученый
Tilg H: Диета и иммунитет кишечника. N Engl J Med.

 narod.ru/blog Диета при хроническом спастическом колите
narod.ru/blog Диета при хроническом спастическом колите