Диетическое питание при повреждении, воспалении пищевода — эзофагите
вопрос:
Лежу в больнице — выпила уксус как, чем мне питаться?
Что и как можно есть после ожога пищевода и при воспалении пищевода
Эзофагит — воспаление пищевода, возникающее вследствие разных причин. После отравления кислотами: азотной, серной, хлористоводородной, уксусной, щавелевой, а также щелочами происходит химический ожог пищевода. После приема очень горячей пищи или жидкости может быть термический ожог. Возможности и особенности питания будут различаться в зависимости от степени поражения оболочек пищевода.Но общие принципы питания одинаковы:
1) пища должна быть примерно температуры тела, ни в коем случае не горячая и не холодная
2) пища должна быть максимально щадящей консистенции, жидкая или полужидкая, приготовленная на пару или отваренная в воде с минимальным содержанием пищевых волокон
3) абсолютно исключается острая, жирная, жареная пища
Если было выпито небольшое количество химиката и после обследования разрешено амбулаторное лечение
 Начиная с 4-5 дня можно переходить на обычное питание.
Начиная с 4-5 дня можно переходить на обычное питание.При сильном ожеге — 2 степень, грубом повреждении стенок пищевода выбор способов питания нужно предоставить специалистам, и лечение этих состояний проводится
Обычно в первые сутки-двое (а при выраженных ожегах и более продолжительное время — до 5-6 суток) назначается голодание, еду не рекомендуют из-за ее механически раздражающего воздействия и возможного дальнейшего повреждения и разрыва обожженного пищевода. Питательные вещества в этот период заболевания вводят внутривенно. Если в течении этого времени выясняется, что выраженных повреждений пищевода нет, то могут разрешить энтеральное питание. В первые сутки возможно назначение через рот жидкой антибактериальной смеси, содержащей некоторое количество питательных веществ (эмульгированного растительного масла) и антибиотиков.
По мере стихания воспалительных явлений обычно разрешают и даже рекомендуют начинать принимать сначала прохладную, потом теплую жидкую и полужидкую — кашицеобразную пищу.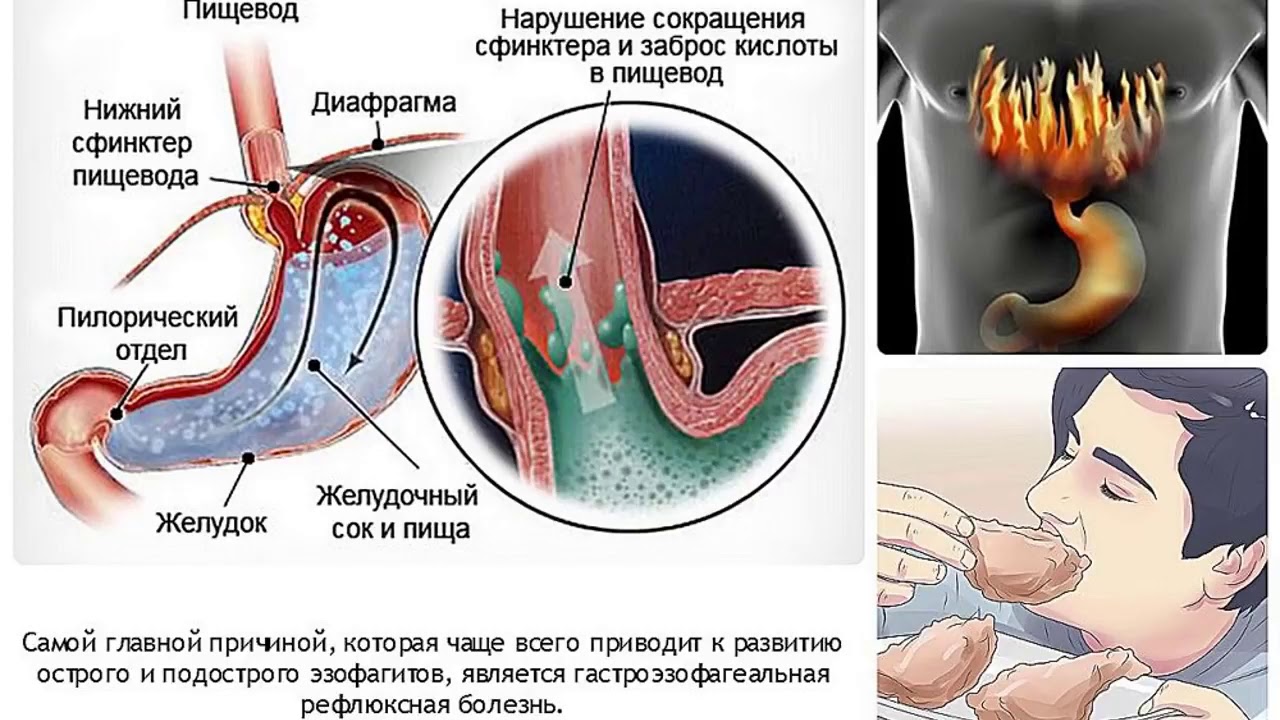 Считается, что процесс глотания и проведения пищи по пищеводу препятствует образованию грубых рубцов при заживлении.
Считается, что процесс глотания и проведения пищи по пищеводу препятствует образованию грубых рубцов при заживлении.
При очень сильных, глубоких ожогах III степени, а также если нарушается физиологический процесс глотания и больной не может есть, то необходимо хирургическое лечение, обычно это определяется к 5-10 дню заболевания — накладывается гастростома или энтеростома, и питание осуществляется непосредственно через стому — прямо в желудок или в кишечник.
Питание через стому должно быть небольшими порциями, 5-6 раз в день.
При поражениях пищевода можно есть:
— супы, сваренные на мясных, птичьих, рыбных, овощных, крупяных бульонах (без кубиков и приправ)
— каши, лучше — овсяная, можно гречневая, рисовая, сваренные на воде или с добавлением молока, кроме пшеничной, пшенной и перловой
— нежирные сорта мяса — курица, индюшатина без кожи, нежирная свинина, телятина. Мясо должно быть хорошо отварено, пропущено через мясорубку и разведено бульоном, или в виде суфле, приготовленного на пару.
— нежирные сорта рыбы в отварном, измельченном виде. В более поздние периоды, когда больной уже привык к жидой и полужидкой пище, мясо и рыбу можно после отваривания немного обжаривать
— яйца всмятку, можно омлет, приготовленный на пару
— сливочное и растительное масла добавлять в небольшом количестве к готовым блюдам
— молочные и кисломолочные продукты: молоко, кефир, простокваша, ряженка, сметана, сырки, творог желательно не кислый, а свежий, блюда из творога, сыр
— овощные блюда — тушеные или отварные и на первое время измельченные морковь, свекла, кабачки, тыква. Нежелательно в первое время помидоры, томатный сок. Можно в небольшом количестве тушеный или вареный картофель, хорошо вымоченную тушеную квашеную капусту.
Из питания на первое время нужно исключить: хлеб, жареные, жирные и острые блюда, грибы, подливки, соусы, копчености, маринады, соленья, газированные напитки, сырые овощи и фрукты, шоколад, орехи, кофе, какао, крепкий чай.
При хронических эзофагитах
При рефлюкс-эзофагите — забросе кислого желудочного содержимого в пищевод и раздражении последнего рекомендуется не ложиться спать после еды 2-3 часа, не работать внаклон после еды, пищу принимать в вертикальном положении туловища, избегать обильного приема пищи, не носить стягивающие ремни и пояса на талии, не поднимать тяжести, исключить работу, связанную с напряжением мышц брюшного пресса. После еды, для более быстрого освобождения желудка хорошо немного погулять. Есть ограничения по приему лекарственных препаратов, снижающих тонус нижнего пищеводного сфинктера, об этом нужно консультироваться с лечащим врачом. Курение также снижает тонус сфинктера.
—
Вопрос:
При эзофагите может быть жжение во рту (языка)?
Ответ:
Эзофагиту может сопутствовать жжение языка. Но нередко этот симптом может быть признаком другого заболевания, например, глоссит — воспаление языка. Может наблюдаться жжение языка при хроническом воспалительном заболевании ЖКТ — гастрите. При гастрите может нарушаться всасывание питательных веществ в желудочно-кишечном тракте, в том числе витаминов. Из-за недостатка витамина В12 развивается В12-дефицитная анемия, при которой часто атрофируются сосочки языка. При этом возникают боли, жжение, язык становится ярко-красным, очень гладким. Для диагностики заболевания необходимо сдать анализ крови и обратиться к своему врачу за помощью.
Может наблюдаться жжение языка при хроническом воспалительном заболевании ЖКТ — гастрите. При гастрите может нарушаться всасывание питательных веществ в желудочно-кишечном тракте, в том числе витаминов. Из-за недостатка витамина В12 развивается В12-дефицитная анемия, при которой часто атрофируются сосочки языка. При этом возникают боли, жжение, язык становится ярко-красным, очень гладким. Для диагностики заболевания необходимо сдать анализ крови и обратиться к своему врачу за помощью.
Вопрос:
При РЭ (рефлюкс-эзофагите) возможны боли в горле и сухость во рту и на языке?
Ответ:
Симптомы эзофагита: изжога, отрыжка, подташнивание, рвота, ощущение инородного тела в горле, боли при глотании, сухость в горле и во рту. Может возникнуть охриплость голоса, обложенность языка. Изжога возникает или усиливается после обильной еды, алкогольных и газированных напитков, углеводистой пищи, курения. Изжога усиливается в положении лежа, уменьшается после приема соды и антацидов.
Вопрос:
Можно ли заниматься фитнесом с диагнозом рефлюкс-эзофагит?
Можно ли заниматся дома гантелями при рефлюкс-езофагите, при этом исключить упражнения на брюшную полость и заниматься по 2 часов от еды?
Ответ:
Фитнесом заниматься можно, но упражнения, связанные с напряжением мышц брюшного пресса нужно исключить. Лучше делать специальный комплекс упражнений, предварительно специально посоветовавшись с врачом лечебной физкультуры. Такие специалисты обычно работают в санаториях по лечению проблем ЖКТ.
Вопрос:
Может ли при эзофагите пропасть аппетит?
Ответ:
Вопрос:
Уже незнаю к кому обратиться за помощью. Вот уже семь месяцев нахожусь в полном аду. Сначала почувствовала, что в горле что-то мешает, затем начались жжения за грудиной. Сразу поехала сделала эндоскопию. Диагноз: атрофический эзофагит, недостаточность кардии. Гастрит. Проходила лечение на протяжении 3 месяцев. Резултат оказался маленьким: прошли боли за грудиной, а ощущение инородного тела не проходят до сих пор. Обследована ЛОР врачами, в этом плане все нормально. Отправили к невропатологу, диагноз остеохандроз шейного отдела. Два месяца лечусь, «комок» не проходит. В горле постоянно першит, чувство стянутости, комок, П О М О Г И Т Е!!!! Незнаю к кому обратиться. Мне 39 лет.
Сразу поехала сделала эндоскопию. Диагноз: атрофический эзофагит, недостаточность кардии. Гастрит. Проходила лечение на протяжении 3 месяцев. Резултат оказался маленьким: прошли боли за грудиной, а ощущение инородного тела не проходят до сих пор. Обследована ЛОР врачами, в этом плане все нормально. Отправили к невропатологу, диагноз остеохандроз шейного отдела. Два месяца лечусь, «комок» не проходит. В горле постоянно першит, чувство стянутости, комок, П О М О Г И Т Е!!!! Незнаю к кому обратиться. Мне 39 лет.
Ответ:
Описанные вами симптомы встречаются при гастритах, эзофагитах, рефлюкс-эзофагитах, недостаточности кардиального отднла желудка и некоторых других. Недостаточность кардии — хроническое состояние, может быть врожденным или развивается годами, и за два месяца не лечится. Вероятно, боли возникали из-за воспаления пищевода, симптомы которого можно значительно уменьшить правильным лечением и питанием, в чем вы добились успеха — боли прошли. Недостаточность кардии может быть останется с вами надолго и необходимо предпринимать меры, чтобы вновь не возникало воспаление пищевода.

Обратный заброс может быть при частом переедании, ожирении, у любителей полежать после сытной еды и обильного питья, обильном газообразовании при брожении пищи, а также при хроническом воспалении слизистой желудка и при расширении пищеводного отверстия диафрагмы — грыжа. Для устранения заболевания необходимо выяснить его причину. Если это грыжа — необходима операция по ушиванию, если гастрит — нужна диета, лечение и изменение некоторых привычек. Для уменьшения давления на желудок нужно носить более свободную одежду, снизить избыточный вес, больше ходить, двигаться, есть чаще и малыми порциями, пища должна быть легкой, нежирной и неострой, последний прием пищи перед сном должен быть не менее, чем за 1,5-2 часа.
 При появлении болезненных ощущений необходима консультация врача-гастроэнтеролога.
При появлении болезненных ощущений необходима консультация врача-гастроэнтеролога.Вопрос:
Подскажите сколько грамм составляет разовый прием пищи при эзофагите?
Ответ:
Количество потребляемой за один прием пищи не является строго регламентируемым и зависит от состояния пищевода и желудка. Рекомендуется уменьшить объем пищи при каждом ее приеме и есть почаще, примерно, два-три раза — легкие перекусы и три раза — основное питание.
Вопрос:
У меня боли при глотании и чувствую как пища проходит и доходит до желудка. При прохождении между желудком и пищеводом боль усиливается. Желудок не болит. Удален желчный пузырь 10 лет назад.
Ответ:
Чего вы ждете? Если есть боли, то в первую очередь нужно немедленно обратиться к врачу, сделать фиброгастроскопию, и в последующем лечение проводить в зависимости от диагноза. В интернете правильный диагноз никто не поставит.
Вопрос:
Рефлюкс-эзафогит 2 степени, эрозивный А. Пъю париет 1т 2раза в день, денол 4 раза в день, тримедат 3 раза в день. Возможноли заживление эрозий за 14 дней?
Пъю париет 1т 2раза в день, денол 4 раза в день, тримедат 3 раза в день. Возможноли заживление эрозий за 14 дней?
Ответ:
При соответствии лечения диагнозу, уменьшении негативного воздействия на организм (ограничение воздействия острой, горячей, жареной пищи, курения, соблюдение рационального режима питания) вполне возможно заживление эрозий за 14 дней. Для закрепления эффекта рекомендуется санаторно-курортное лечение. например, хороши для желудочных проблем минеральные воды в Болгарии в Хисаре и в Велинграде.
Вопрос:
После еды я всегда лежу на кровати, 4 недели назад ощутились изжоги и постоянные отрыжки в области грудины, сделал ФГДС. Диагноз — недостаточность кардии, катаральный эзофагит легкой степени. Как можно вылечиться и можно ли делать физические упражнения?
Ответ:
Вполне вероятно, что недостаточность кардии явилась прямым следствием вашего образа жизни. После еды не желательно ложиться. Для того, чтобы пищевой комок прошел пищевод и желудок нормально, нужно находиться в вертикальном положении хотя бы полчаса-час. Изжога и отрыжка появились, вероятно, вследствии присоединения к недостаточности кардии воспалительного процесса в пищеводе. Чтобы воспалительный процесс не усилился и не перешел в язвенную стадию, необходимо пройти курс лечения (не обязательно таблетки). Для начала достаточно соблюдения режима питания (см. выше), диеты с соблюдением температурного режима пищи (близкая к температуре тела), тщательного неспешного пережевывания (каждый кусочек прожевывать 20-30 раз). Физические упражнения делать можно, но не после еды и с ограничением нагрузок на брюшной пресс. Если есть возможность съездить в санаторий на минеральные воды — оптимально. Опытный инструктор вас ознакомит с рекомендуемым в вашем случае комплексом упражнений.
Изжога и отрыжка появились, вероятно, вследствии присоединения к недостаточности кардии воспалительного процесса в пищеводе. Чтобы воспалительный процесс не усилился и не перешел в язвенную стадию, необходимо пройти курс лечения (не обязательно таблетки). Для начала достаточно соблюдения режима питания (см. выше), диеты с соблюдением температурного режима пищи (близкая к температуре тела), тщательного неспешного пережевывания (каждый кусочек прожевывать 20-30 раз). Физические упражнения делать можно, но не после еды и с ограничением нагрузок на брюшной пресс. Если есть возможность съездить в санаторий на минеральные воды — оптимально. Опытный инструктор вас ознакомит с рекомендуемым в вашем случае комплексом упражнений.
Вопрос:
01479 Мед можно есть при эзофагите?
Ответ:
При остром эзофагите или обострении воспалительного процесса мед может усилить раздражение слизистой пищевода, поэтому нежелательно его применение в острой фазе заболевания. При хроническом эзофагите без обострения умеренное употребление меда полезно.
—
Рекомендации разработаны на основе стандартных диет номерной системы (диеты №№ 1-15).
См. также:
Отравление столовым уксусом и уксусной кислотой, помощь
последние изменения статьи 13янв2011, 14апр2013
Перепечатка (кроме материалов под «стандартным копирайтом» — знаком ©) и цитирование приветствуются, если указываются:
в любых гипертекстовых документах — прямая гиперссылка на автора и на страницу-источник;
в обычных документах — указание автора, название материала, источник (например, FAQ-for-FAQ.NetNotebook.Net).
Авторские права, интеллектуальная собственность:
Статьи: указанный в статье автор или правообладатель
Вебдизайн и структуры: © Astrela Ltd., 2010-2018; 2019-2021 Вадим Шулман
лицензировано под Creative Commons Attribution-Share Alike 3.0 License,
если не указано иное.
Внешние элементы: их соответствующие правообладатели и лицензии.
(С), (TM): их соответствующие правообладатели.
Питание при рефлюкс-гастрите — Вести-Кузбасс
Питание при рефлюкс-гастрите составляет основу эффективного лечения. Из меню убирают острое, жирное, копченое. Рацион должен быть сбалансированным, еда — готовиться на пару, вариться или запекаться.
Из меню убирают острое, жирное, копченое. Рацион должен быть сбалансированным, еда — готовиться на пару, вариться или запекаться.
Правильно подобранное питание при рефлюкс-гастрите купирует тошноту, уберет отрыжку и изжогу после приемов пищи. Строгое следование диете, назначенной лечащим врачом, выступает залогом выздоровления, однако не отменяет приема медикаментозных препаратов. При составлении меню также нужно учитывать индивидуальную непереносимость продуктов и стадию развития заболевания.
Диета: как питаться при рефлюкс-гастрите?
Основные правила
Переедание и голодание негативно сказываются на состояние ЖКТ, поэтому рацион больного должен быть богат микро-, макроэлементами, витаминами и содержать достаточное количество калорий.
Оптимальный рацион при эзофагите и гастрите поможет составить диетолог либо можете ознакомится на сайте https://etozheludok.ru/, однако, если такой возможности нет, необходимо следовать следующим рекомендациям врачей:
- Показано дробное питание 4—5 раз в сутки небольшими порциями.
 Количество калорий рассчитывается на основе физических параметров.
Количество калорий рассчитывается на основе физических параметров. - Ночью есть нельзя.
- Если у больного диагностировано ожирение, то количество получаемых калорий должно быть меньше, чем затрачиваемых. Для этого рекомендуется завести специальный блокнот.
- Рацион составляется из жидких или измельченных блюд, чтобы уменьшить нагрузку на ЖКТ.
- Пища варится, тушится или готовится на пару. Жареные и копченые блюда исключаются.
- При появлении даже слабого чувства голода необходимо немедленно перекусить, чтобы не провоцировать выработку желудочного сока.
- Оптимальная температура — теплая. Горячая и холодная еда, а также напитки плохо сказываются на желудке.
- Перед едой рекомендуется выпивать 1 стакан воды, чтобы уменьшить концентрацию соляной кислоты желудка. Можно пить также сок картофеля.
- После приема пищи лучше пройтись, но ни в коем случае не ложиться.
- В стадии обострения стоит носить одежду, не стесняющую движений. Ремень лучше снять.
Примерное количество необходимых элементов представлено в таблице: Питательные вещества Норма, г/сут. Белок 80—90 Углеводы 310—350 Жиры 70—80
Что можно есть?
Согласно рекомендациям врачей, диета при рефлюкс-гастрите желудка базируется на таких блюдах, которые действуют, как щелочь:
- любые полностью разваренные крупы;
- супы: молочные, на основе овощей, с добавлением круп;
- мясные, рыбные суфле;
- говядина, курица, индейка;
- судак, хек, карп;
- запеченный и отварной картофель;
- белый хлеб, сухари;
- яичное суфле и воздушный омлет;
- нежирный творог, молоко, кефир, простокваша;
- перебитые в блендере овощи;
- яблоки, груши;
- свекла, морковь.
Во время приготовления не нужно добавлять специи, соль — в минимальном количестве. Можно пить кисель, слабый черный чай с добавлением молока, отвар из шиповника и ягод, компот. Наиболее полезна минеральная вода, понижающая кислотность желудка. Хорошо влияют на ЖКТ травяные настойки на основе ромашки, одуванчика, подорожника, пустырника. Их лучше принимать перед сном, так как они дают расслабляющий эффект.
Что нельзя есть?
Диета при рефлюкс-эзофагите, особенно в период обострения, полностью исключает употребление таких блюд:
- жирные бульоны на основе мяса и рыбы;
- свежие хлебобулочные изделия;
- жирные, покупные соусы;
- кислые фрукты: цитрусовые, киви, ананас;
- соленые, копченые, маринованные, острые блюда;
- овощи, провоцирующие газы: капуста, редиска, редька, лук, артишок;
- кисломолочная продукция;
- мед, варенье;
- орехи;
- фастфуд;
- газированная вода;
- кофеиносодержащие напитки.
После выздоровления и в период ремиссии можно включать некоторые блюда из красного списка в меню, однако в маленьких дозировках. Важно помнить, что запущенный рефлюкс-гастрит чреват такими осложнениями, как перфорация пищевода или эрозивный эзофагит, которые не выявить при поверхностном осмотре. Поэтому даже после выздоровления необходимо следить за питанием. При появлении изжоги, отрыжки или болей в желудке следует вновь вернуться к строгой диете. Фрукты и овощи с повышенной кислотностью есть категорически запрещается.
При появлении негативных симптомов врачи рекомендуют быстро съесть сладкий фрукт: банан, грушу, яблоко. Тошнота и изжога пройдут через 5—10 мин.
Примерное меню
Диета при эзофагите может включать такие блюда на каждый день:
- Первый завтрак:
- овсянка;
- отвар шиповника.
- Второй завтрак:
- запеченная груша с творогом.
- Обед:
- овощной суп с гречкой;
- рыбное суфле;
- картофельное пюре.
- Полдник:
- салат из морковки и яблока.
- Ужин:
- карп на пару;
- разваренный рис;
- травяная настойка.
- Второй ужин:
- стакан домашнего йогурта.
Примерный рацион не учитывает индивидуальных особенностей больного и возможные негативные реакции на отдельные ингредиенты. Лечение билиарного рефлюкс-гастрита занимает длительное время, так что рекомендуется заранее распланировать рацион на несколько недель вперед, чтобы сохранить разнообразие блюд. При ухудшении состояния необходимо немедленно обратиться к врачу.
Рекомендации по питанию при ахалазии кардии
Дата публикации: .
Климович А.Е., Жартун С.А.
Ахалазия кардии – хроническое нервно-мышечное заболевание, при котором нарушается прохождение пищевых масс по пищеводу и из пищевода в желудок вследствие патологических изменений пищеводной перистальтики и отсутствия рефлекторного расслабления нижнего пищеводного сфинктера во время глотания.
Больным с ахалазией кардии необходимо соблюдать определённый режим питания и особые рекомендации относительно приёма пищи.
Рекомендации по питанию:
- Большое значение имеет регулярное питание (5–6 раз в день).
- Исключить переедание и закуски перед сном. Последний прием пищи не позднее, чем за 2 часа до сна.
- Во время сна строго горизонтальное положение тела также не показано, так как пища может задерживаться в пищеводе до нескольких часов, а верхний пищеводный сфинктер во время сна расслабляется, что создаёт предпосылки для аспирации. Лучше спать на высоких подушках или с приподнятым головным концом кровати.
- Не лежать после еды в течение 2 часов.
- Прекратить употребление алкоголя.
- Принимать пищу необходимо медленно, тщательно её пережёвывая.
- Умеренно щадящая диета: избегать острой, жирной, горячей, очень холодной пищи, которая оказывает повреждающее действие на слизистую пищевода.
- Исключить газированные напитки, повышающие внутрижелудочное давление.
- Ограничить употребление кислых продуктов, продуктов, содержащих грубые виды клетчатки (капуста, яблоки др.), свежей выпечки и хлеба.
- Исключить или уменьшить потребление жиров, которые угнетают двигательную активность желудка.
- При формировании белково-энергетической недостаточности показано искусственное питание.
Диетический стол N 5 — « С 56 до 53 кг за 2 недели. Одна диета, одна история победы над собой и болезнями ЖКТ. Ошибки, взлеты и падения. Как ВКУСНО КУШАТЬ на диете 5 стол и РАЗНООБРАЗИТЬ ПИТАНИЕ.»
Всем привет!
К сожалению, мне пришлось сесть на долгосрочную диету по состоянию ЖКТ и если вы читаете эти строки, значит мы в одной лодке.
Немного вводной части.
Меня беспокоили голодные боли по ночам около 5 лет.
По началу они почти не беспокоили, но со временем усилились, стали ежедневными, появилось постоянное жжение в эпигастрии, изжога и тяжесть в желудке.
Все врачи на свой лад ставили мне совершенно разные диагнозы, назначали лечение, которое не помогает, а лишь облегчает мое самочувствие. Меня закормили таблетками, что я только не принимала.
По результатам обследования особых проблем не было замечено.
Гастрит в стадии ремиссии, несущественная недостаточность кардии и загиб желчного пузыря, который у каждого второго встречается, но проблема существует уже не первый год.
Диагноз: недостаточность кардии, диспепсия и возможно дискинезия желчевыводящих путей.
Лишь придерживаясь диеты я добилась ощутимого результата. Без нее медикаментозное лечение оказалось малоэффективным.
Диета № 5 считается самой долгой и может длиться до двух лет. Многие люди придерживаются этой диеты всю жизнь, так как заболевания протекают хронически. В случае обострения заболевания меню диеты не изменяется.
Диета разработана врачами-диетологами и направлена на людей с болезными ЖКТ, она разгружает и очищает организм, улучшает отток желчи, восстанавливает печень, ну и по собственному опыту скажу — снижает вес.
За первые две недели я скинула 3 кг, с 56 до 53 кг, что при моем росте (169) — предел.
Полностью здоровым людям держать ее не рекомендуют, так как она подразумевает ощутимые ограничения и поэтому далека от ПП диеты, к примеру.
памятка от врача
Основные принципы диеты 5 стол:
1) Главное наладить правильный режим питания.
Кушать по часам, в одно и тоже время.
Питаться дробно, маленькими порциями 5-6 раз в день,но не более 200 грамм за один прием, учитывая жидкость. Нужно стараться не наедаться до отвала и вставать из-за стола с небольшим чувством голода.
Это нужно чтобы не нагружать желудок, особенно актуально при болезнях желчного пузыря и недостаточности кардии.
Этот пункт для меня был самым сложным. Ведь что такое 200 грамм- уже полноценная чашка чая, которую я всегда выпивала после ужина, теперь же приходится пить чай лишь во время перекуса, иначе изжога и тяжесть в желудке дают о себе знать.
2) Щадящее питание.
Пища должна быть не холодной и не слишком горячей.
К этому быстро привыкаешь, не так сложно лишь слегка разогреть еду в микроволновке.
Даже плюс не нужно долго ждать))))
3) А что нужно, так это отказаться от жирного, жаренного,кислого, соленого, острого, сладостей.
Разрешается исключительно вареное, запеченное, на пару и редко тушенное.
С точки зрения большой семьи, отдельно каждому не приготовишь итп это кажется проблематичным, но разница может быть лишь в способе приготовления, не обязательно готовить разные продукты. Например сделав фарш для котлет, какую-то часть можно пожарить для счастливчиков, а для 5 стола сделать тефтели на пару, или запечь в духовке.
4) Не рекомендуются продукты вызывающие вздутие ( капуста белокочанная, бобовые, грубая клетчатка)
Кушать неторопясь, хорошо пережевывая пищу. Во время трапезы стараться сидеть с ровной спиной без прогибов в районе талии. Это касается тех у кого частым спутником бывает изжога.
Мой случай. Сидеть с прямой спиной мне довольно трудно было по началу, но иначе ощущалось неприятное жжение.
Начать- это самое сложное.
Я не сразу начала соблюдать диету, а постепенно убирала запрещенные продукты один за одним. Думала, что будет достаточно если я просто исключу из рациона жирное, жаренное, соленое и начну питаться по часам, но нет, не свезло.
По мне, так диета бьет по самому больному, пришлось отказаться от кофе, какао и крепкого черного чая. Я тот еще кофеман и при виде вкусного латте с пышной пенкой теперь чуть ли не в обморок падаю, я без него уже пол года. Кофе…люблю, скучаю, надеюсь увидеться в будущем)
Шоколад. Отдельная песня.
Никогда я не замечала за собой сильную страсть к сладкому. Но с такой диетой, когда нельзя вкусного и жирного навернуть, я стала смотреть на шоколад, как маньяк на жертву. Как много нарушений диеты связано с ним. Открывала плитку, убежденная, что съем всего один квардратик, но в конечном счете не могла остановиться не слопав все до последней крошки. Шо-ко-лааааад!
Да, по началу очень сложно сопротивляться внешнему миру, где друзья тянут в бар, домашние уплетают котлеты за обе щеки и на каждом углу продаются вкусняшки.
Первое время я только и думала, что о борще, пицце, мысленно падая в голодный обморок.
Но я постепенно приняла такое положение вещей как должное, сделав диету образом жизни и мышления. Пусть и временное.
Ведь нельзя на утро съесть овсяную кашу, на обед молочный суп, а вечером наесться шашлыка и считать, что держишь диету. Это так не работает и ждать результат придется долго.
Нарушала — проверено =)
В целом, мне как любителю правильного питания было не так сложно держать диету, как тем кому с жаренных котлет слазить приходилось.
Основная проблема была в режиме и дробности питания и в отказе от вкусняшек)
Итак, начнем.
ЗАВТРАК
За полчаса до завтрака врачи советуют выпивать стакан воды.
Если по утрам ныл желудок вода реально спасала на некоторое время,например пока готовила завтрак.
Вода способствует выработке желудочного сока и разбавляет его, понижая кислотность и регулируя работу кишечника. Особенно полезно пить сырую или кипяченую воду людям с гастритами или язвами.
Оптимальный вариант: овсяная, гречневая, манная, рисовые каши, омлет, сырники , варенные яйца всмятку. Разрешены бутерброды из вчерашнего хлеба (ржаной нельзя) с сыром.
Одна из ошибок.
Я все лето ела овсяную кашу, лишь изредка для разнообразия делала омлет, совершенно не понимая, что врежу организму.
К концу лета я заметила, что у меня начали шататься передние зубы. Боже, что за дичь!!
Несильно и лишь во время поглощения твердой пищи. Как выяснилось, именно эта каша способствует выведению кальция из организма и ее можно включать в рацион лишь 2-3 раза в неделю, как и манную кстати.
Симптомы ушли как только я внесла таки разнообразие и перестала есть ежедневно овсянку.
ОБЕД
Это нельзя, то нельзя, а чем же тогда питаться? На самом деле вариантов очень много!
Рекомендуется отдавать предпочтение легкоусвояемым, протертым, слизистым продуктам.
Поэтому, на обед я предпочитаю овощные супчики-пюре.
Называю эти супы «назад в детство». Овощные пюрешки…за маму, за папу!
Вариантов таких супов масса: тыквенные, кабачковые, из цветной капусты, свеклы, картофельные,брокколи,морковные, думаю это не предел)
При этом нежелательно переваривать овощи, тем самым разрушая содержащиеся в них витамины. Правильно приготовленные супы-пюре очень полезны и вкусные)
Тыквенный суп-пюре
овощной крем суп- пюре (кабачки, цв. капуста, морковь)
крем суп- пюре из брокколи
Так же можно приготовить молочные супы с лапшой или овощами.
Супы на основе овощных бульонов.
А вот наваристые на мясном бульоне есть нельзя.
Под запетом щи, борщ, окрошка, харчо и прочие.
Суп обязательно должен ежедневно присутствовать в меню, особенно для гастритострадальцев.
С думами, что приготовить на обед у меня не было никаких проблем, ввиду богатого разнообразия, к тому же я и до диеты любила легкие супчики и супы-пюре.
овощной суп с курицей
УЖИН
индейка и овощи на пару
ленивые варенники
С ужином уже немного сложнее.
Я частенько ломаю голову над тем что приготовить.
Ведь хочется покушать вкусно, но не нарушая диету, а это не так уж и просто.
Но даже сидя на такой строгой диете как 5 стол, можно получить гастрономическое удовольствие, если как следует подумать ну и погуглить, конечно)
Тут на помощь мне приходят овощные котлеты , овощи измельчаются варятся и запекаются в духовке. Их можно сделать практически из любого овоща, но место моего полноправного фаворита занимают морковно- тыквенные. Они сладкие и правда очень вкусные.
Отлично сочетаются с рисом, и думаю жаренные на сковороде они были бы просто обалденными, но проверю я это еще не скоро)
Временами я даже рада, что приходится соблюдать 5 стол, из него я заберу не мало рецептов в свою повседневную жизнь, когда ЖКТ перестанет портить мне жизнь.
морковно-тыквенная котлета
цветная капуста тушеная с яйцом
Основу моего рациона по большей части составляют вареные блюда, но изредка можно тушить или же запекать.
Запекать мясо\рыбу\курицу рекомендуется после предварительной варки, ну или же запекать в фольге без масла.
отварная курица запеченная в молочном соусе
запеченный в фольге окунь
фаршированный брокколи картофель
Ужин- это последний прием пищи, так как есть за 3-4 часа до сна не рекомендуется, особенно тем у кого расшатана кардия желудка. Иначе можно заработать ночную изжогу и новый рецидив.
Но если что можно выпить стакан молока или кефира.
ПЕРЕКУСЫ ( второй завтрак и полдник)
льняные сырники в духовке
На перекус я предпочитаю бутерброды из цельнозернового хлеба с зеленью и овощами, с сыром. Можно любые блюда из творога: запеканки, сырники, желе.
Мне очень понравилось желе из творога и банана.
Желе легко усваивается организмом, это вкусный, воздушный десерт. Главное, что и желудок доволен и внутренний ребенок-сладкоежка.
Понравился он и всем моим домашним.
Разрешены любые сладкие фрукты : яблоки, груши, виноград, бананы, но в разумных пределах ,1-2 фрукта в день. Кислое- табу!
Сухое печенье, галеты,мед, пастила и зефир.
Конечно, не увлекаясь, разрешено есть не более 30 грамм сладкого в день.
Нужно смотреть на реакцию организма, ведь все индивидуально. Бананы моему желудку не сильно то и нравятся, ощущается дискомфорт, их я не ем.
К зефиру и пастиле так же отношусь скептически, но когда сильно хочется чего то сладкого, нет-нет да наверну с чайком.
Сухие зерновые галеты
Творожный десерт с желатином.
- Одна пачка творога
- Банан
- Желатин 15 г
- Ванилин
- Сахар по вкусу
- 250 мл молока
1) Смешиваем молоко с желатином и даем ему набухнуть, подогреть на водяной бане до полного растворения желатина.
2) Банан растереть в блендере вместе с творогом с небольшим добавлением молока + ванилин и сахар.
3) Смешать обе части, перелить в форму или любую емкость, по желанию можно на дно формы положить любые фрукты и поставить в холодильник до полного застывания.
Творожно-банановый десерт с желатином
Иногда делаю домашнее галетное печенье Мария.
Оно сухое, хрустящее и его можно кушать даже соблюдая диету № 1.
Делается оно совсем просто.
- Яйцо 1шт
- Сахар 1,5 ст. л
- Подсолнечное масло 1 ст. л
- Молоко 1 ст. л
- Мука 1 стак.
- Сода — 0,25 ч. л.
Все смешать, замесить тесто. Раскатать, вырезать печеньки, запекать при температуре 220 градусов 5-8 минут.
Домашнее печенье Мария
Результат.
Диету в общей сложности я держу уже пол года, совмещая ее с медикаментозной терапией.
Но так как постепенно отказывалась от запрещенных продуктов и постоянно нарушала по незнанию основные правила это время можно не считать, лучше мне не было.
В чистом виде выйдет 1.5 месяца.
Дело в том, что я постоянно ела на ночь, боясь голодных болей. Могла проснуться среди ночь и сточив бутерброд, лечь обратно спать.
Боли проходили и я думала в этом нет ничего страшного, но именно эти действия привели к ухудшению ситуации.
Кроме этого я постоянно переедала, не держала принцип дробности питания, то есть просто считала что нужно есть разрешенные продукты 5-6 раз в сутки, не контролирую общий объем съеденного учитывая чай и прочее. Помню собираясь на дачу, я так боялась голодных болей по пути, что сильно переела, так что чуть ли обратно не лезло. После этого у меня и случилось сильное ухудшение самочувствия, постоянная изжога и диспепсия стали моими постоянными спутниками и не проходили.
Да, очень сложно держать диету когда кругом столько соблазнов. Сложно держать диету летом ведь столько вкусного: малина, клубника, потом смородина созревает, персики. Но ничего нельзя.
А как же хотелось шашлыка. Я срывалась, ела и потом ругала себя за это.
Но когда я набила все возможные шишки и встала на верный путь, приняла основные принципы питания, постепенно, благодаря диете 5 стол, мое состояние начало улучшаться.
Это небыстрый процесс, нужно запастись терпением, постепенно шаг за шагом, двигаясь к заветной целе.
И мне удалось заметно улучшить свое состояние.
Состояние до диеты:
— Изжога до горла, постоянная и ежедневная;
— Сильные голодные боли каждую ночь;
— Тяжесть в желудке.
Спустя 2 недели снизилась интенсивность изжоги и тяжести в желудке.
Симптомы как бы угасают, но постепенно…
Где- то через месяц наступил тот счастливый день когда я не почувствовала присутствия моих постоянных спутников, но увы периодически изжога все же меня навещает.
На данный момент я держу диету ровно 1.5 месяца. Голодные боли, которые беспокоили меня ежедневно, теперь практически отсутствуют, а если и приходят то уже не такие злые.
Не скажу, что теперь я в рядах полностью здоровых людей, но я добилась значительных улучшений.
Диету я буду держать до состояния стойкой ремиссии. Когда она наступит я обязательно напишу.
Думаю, осталось недолго, а потом начну плавно переходить на правильное питание,забрав с собой несколько рецептов 5 стола)
Дополнение 15.12.18
Итак, диету я все еще держу, но пришлось перейти на стол №1 так как мне наконец-то был поставлен правильный диагноз — рефлюксная болезнь. Чтобы войти в стойкую ремиссию эту пакость надо лечить очень долго и упорно.
Диета действительно эффективна, гастрит с ее помощью можно вылечить очень быстро.
А мне же нужно стойко держаться и дальше.
___________________________________________________________________
Тыква. Что из нее приготовить
Гастроскопия
Рентген желудка с барием
симптомы и причины развития, диета, лечение
Пищеварительный тракт человека — сложная система, состоящая из множества элементов. Важную роль в работе основных органов ЖКТ играют сфинктеры — клапаны, регулирующие процесс перехода содержимого пищеварительного тракта из одной его части в другую. Если функция одного сфинктера нарушена, это может отразиться на работе всех связанных с ним органов.
Недостаточность кардии желудка представляет собой нарушение смыкания нижнего сфинктера пищевода, расположенного на входе в желудок.
Стоит ли пугаться, если врач-гастроэнретолог поставил вам соответствующий диагноз, и существует ли эффективная методика лечения такой патологии?
Что значит диагноз «недостаточность кардии желудка»?
Сама по себе халазия (именно так называется состояние недостаточности функции клапана) в клиническом понимании болезнью не является, как и результат несмыкания — рефлюкс (заброс пищи вместе с желудочным соком и соляной кислотой обратно в пищевод). Даже у здоровых людей время от времени может наблюдаться такое явление.
Но если функция кардии сильно нарушается, забросы пищи вверх становятся слишком частыми, слизистая пищевода повреждается кислотой и не успевает полноценно восстанавливаться.
Со временем на ней появляются изъязвления и эрозии, а человек начинает испытывать заметный дискомфорт, проявляющийся следующими симптомами:
- постоянными приступами изжоги;
- болью в пищеводе;
- срыгиванием желудочного содержимого;
- ощущением переполненности желудка;
- отрыжкой воздухом;
- тошнотой, иногда — рвотой;
- урчанием в животе.
Если игнорировать симптомы и не начинать лечение недостаточности кардии желудка, развивается гастроэзофагиальная рефлюксная болезнь (ГЭРБ) — неприятное хроническое заболевание, часто сопровождающееся болью за грудиной и диспептическими явлениями.
Симптомы ГЭРБ могут проявляться в виде одышки и кашля, возникающих в положении лежа, охриплостью голоса и сухостью в горле, хроническим тонзиллитом и синуситом.
Анализируя жалобы и анамнез пациентов, страдающих ГЭРБ, врачи отмечают, что во многих случаях причиной ее развития становятся вредные привычки: переедание, неправильное питание (еда непосредственно перед сном, редкие приемы пищи), лишний вес и малоподвижный образ жизни (гиподинамия).
Иногда недостаточность кардии желудка проявляется на фоне других заболеваний органов ЖКТ, в том числе хронического гастрита.
Почти в половине случаев причиной развития рефлюкс-эзофагита служит грыжа пищеводного отверстия диафрагмы — распространенная, но трудно диагностируемая патология. Это не значит, что пациенты, у которых диагностирована ГЭРБ, должны смириться с дискомфортом: на сегодняшний день медицина предлагает эффективные способы лечения недостаточности кардии желудка.
Для постановки правильного диагноза необходимо пройти обследование в условиях клиники: врач-гастроэнтеролог может назначить ряд исследований — эндоскопию, пищеводную манометрию, контрастную рентгеноскопию пищевода и желудка, суточную pH-метрию пищевода, сцинтиграфию или импедансометрию пищевода. Только после тщательного обследования и определения степени недостаточности кардии назначается лечение.
Лечение недостаточности кардии желудка: медикаменты и народные средства
Чаще всего ГЭРБ лечат таблетками и суспензиями, а на операцию могут направить при диагностированной грыже пищеводного отверстия диафрагмы, когда единственным способом лечения становится ушивание ткани.
Современная медицина располагает широким ассортиментом традиционных средств для борьбы с проявлениями ГЭРБ: лекарствами можно не только нормализовать кислотность желудка, тем самым снизив урон, который наносится пищеводу при забросе его содержимого, но и улучшить моторику ЖКТ.
Как правило, стандартный набор медикаментов, выписанных пациенту с рефлюкс-эзофагитом, содержит:
- антациды;
- прокинетики;
- антисекреторные средства;
- витаминные препараты.
Выбор конкретных средств зависит от стадии развития заболевания, имеющихся у пациента противопоказаний и решения врача. Назначая лекарственные препараты, гастроэнтерологи не устают повторять, что таблетками мы только устраняем последствия заболевания, а чтобы разом преодолеть такие проявления, надо от многого отказаться и завести новые полезные привычки.
Народная медицина предлагает лечение недостаточности кардии желудка средствами растительного происхождения: центральное место среди них занимают сок подорожника, корень болотного аира и сироп из одуванчиков.
- Сок подорожника отжимают из свежих зеленых листьев растения и выпивают каждый день по 1 столовой ложке непосредственно перед приемом пищи. Для лечения в холодное время года сок разводят со спиртом в пропорции 4:1 — в таком виде препарат хранится несколько месяцев;
- Измельченный корень аира болотного необходимо залить стаканом кипятка и пить в теплом виде за полчаса до приема пищи — примерно по полчашки за один раз;
- Свежие цветки одуванчика перекладывают слоями с сахаром, а затем тщательно перетирают до получения сиропа. Затем отфильтрованный сироп разводят теплой отфильтрованной водой и выпивают незадолго до еды.
Перед тем, как воспользоваться народными рецептами, не забудьте посоветоваться с врачом, особенно если у вас есть другие заболевания или аллергия на любые виды растений.
Питание, рекомендуемое при недостаточности кардии желудка
Диета — одно из условий эффективного лечения пациентов, страдающих от проявлений ГЭРБ. Питание должно быть регулярным, пищу лучше дробить на множество приемов, чтобы не переполнять желудок.
- Некоторые продукты способны ухудшать состояние больных, поэтому диета при выявлении недостаточности кардии желудка подразумевает отказ от жирной и острой пищи, шоколада и алкоголя в любом виде, крепкого черного или зеленого чая, кофе, кислых фруктов и цитрусовых, лука и чеснока, а также любых продуктов, повышающих газообразование — бобовых, капусты, ржаного хлеба, газированных напитков.
- Последний вечерний прием пищи нужно завершать минимум за три часа до сна. Кроме того, врач может посоветовать изменить привычки, напрямую не связанные с питанием.
Облегчают состояние при рефлюкс-эзофагите:
- нормализация массы тела;
- приподнятое положение тела во время сна, при котором головная часть кровати приподнимается примерно на локоть;
- исключение нагрузок, повышающих давление в брюшине;
- отказ от ношения тесных корсетов, тугих поясов и ремней, юбок с завышенной талией;
- отказ от курения;
- правильная осанка и регулярное выполнение упражнений для поддержания общего мышечного тонуса организма.
Внимательное отношение к своему здоровью и образу жизни позволяет если не забыть навсегда о проявлениях болезни, то, по крайней мере, добиться минимизации ее симптомов и возвратиться к обычной жизни без боли, изжоги и постоянного дискомфорта.
Материалы, размещённые на данной странице, носят информационный характер и предназначены для образовательных целей. Посетители сайта не должны использовать их в качестве медицинских рекомендаций. Определение диагноза и выбор методики лечения остаётся исключительной прерогативой вашего лечащего врача.
причины болезни, симптомы, лечение и диета
Организм человека представляет собой сложную конструкцию, которая имеет разные механизмы, обеспечивающие жизнедеятельность человека. Один из них — кардиальный сфинктер на границе желудка и пищевода. Он играет роль клапана и не позволяет поступившей в желудок еде выйти назад. По разным причинам происходит неполное смыкание сфинктера — недостаточность кардии желудка.
Описание заболевания
Патология среди всех проблем с ЖКТ занимает ведущее место. Причина кардиальной недостаточности заключается в несмыкании гастроэзофагеального сфинктера. Он представляет собой мышечное образование (иногда еще называют «розеткой»).
При нормальном состоянии, после поступления пищи по пищеводной трубке он полностью смыкается. Его работу можно сравнить с обязанностью привратника: открыть и закрыть двери для гостей. Это необходимо для того, чтобы содержимое желудка не поступали обратно в пищеводную трубку.
Нарушение этой функции в медицине называется халазией (в народе его иногда называют мышечным жомом). Болезнь развивается последовательно и имеет 3 степени:
- Мышечное кольцо смыкается не полностью, зияние отверстия не более 1/3 от диаметра пищеводной трубки. Недостаточность кардии 1 степени у больных людей проявляется в частой отрыжке воздухом.
- При глубоком вдохе отверстие кардии зияет наполовину или больше. Помимо отрыжки, наблюдается пролапс слизистой желудка. В пищеводе происходит раздражение слизистой стенки, что приводит к выраженному дискомфорту при 2-й степени.
- Полная несмыкаемость мышечного кольца, происходит выброс желудочного сока в пищевод, из-за чего воспаляется слизистая стенка пищевода — эзофагита.
Этиология болезни
Причинами недостатка функциональной работы кардии являются:
- Гипотония.
- Отсутствие физических нагрузок, малоподвижный образ жизни.
- Переедание перед сном.
- Неправильная организация приема еды.
- Лишний вес.
- Другие заболевания ЖКТ.
- Как следствие различных хирургических вмешательств.
- Грыжи. Возникает механическое сдавление.
- Внутрибрюшное давление.
Недостаточность розетки кардии может привести к более тяжелым последствиям. Соблюдение здорового образа жизни поможет избежать заболевание.
Характерные симптомы
Признаки проявления связаны непосредственно со степенью заболевания и ярко выражены на 3-й стадии:
- Изжога. В начале болезни наблюдается взаимосвязь с приемом пищи, затем это проходит. Затем изжога носит постоянный характер.
- Появляются отрыжки воздухом, при этом может выходить наружу принятая пища.
- Тошнота, часто сопровождаемая рвотой.
- Боли в грудной области.
- Головная боль, сонливость и снижение работоспособности.
Симптомы проявляются одиночно и в совокупности. Наличие нескольких признаков может означать недостаточность в работе кардия. При прогрессировании заболевания симптомы становятся более выраженными.
Лечение кардиальной недостаточности
Сфинктер желудка плохо закрывается. Для выбора методов лечения необходимо сдать анализы и пройти обследование (ФГДС и т. д. ). Терапия проводится комплексно. Снимаются не только симптомы, но и причина возникновения. Такой подход возможен только после постановки точного диагноза. При самолечении можно нанести вред здоровью.
Вначале необходимо скорректировать режим и рацион. Прием пищи осуществляется 4−5 раз в день маленькими порциями. При этом важно соблюдать режим, нельзя лежать после этого 2 часа. Важно удалить из рациона продукты, которые могут раздражать слизистую желудка (острое, соленое, копченое, алкоголь и т. д). Желательно употреблять супы и жидкие каши.
Назначаются препараты для устранения неприятных симптомов (Церукал, Бимарал, Реглан и т. д).
Необходимо соблюдать простые правила:
- Избегать тяжелых физических нагрузок.
- Не носить сильно обтягивающую одежду. Не затягивать туго поясные ремни.
- Как можно меньше наклоняться.
- Кровать должна быть устроена так, чтобы верхняя часть туловище пациента была выше нижней.
Иногда, при медикаментозном лечении мышцы кардия смыкаются не полностью. Как лечить дальше, решает хирург. Трансхиатальный метод лечения применяется при запущенных формах заболевания или при наличии грыжи. Если лечение назначено правильно и пациент соблюдает все назначения, то патологию можно полностью вылечить.
Народные средства
Допускается применение отваров следующих растений и трав: мяты, ромашки, подорожника, зверобоя, пустырника, тысячелистника. Они снижают и нормализуют кислотность, ускоряют процессы восстановления клеток тканей желудка и пищевода. Также снимают воспалительные процессы.
Народные средства применять только после консультации с лечащим врачом.
Прогулки на свежем воздухе и легкий бег укрепят организм. Можно заниматься дыхательной гимнастикой, упражнения улучшают работу дыхательных мышц и сфинктера.
Гастроэзофагеальный рефлюкс › Болезни › ДокторПитер.ру
Рефлюкс (позднелат. refluxus обратное течение) — передвижение жидкого содержимого полых органов в обратном (антифизиологическом) направлении. В отличие от регургитации, при которой обратное передвижение содержимого совершается путем активного забрасывания, рефлюкс представляет собой пассивное затекание, обусловленное разностью давления жидкости в сообщающихся полых органах или действием силы тяжести при недостаточности либо отсутствии клапанного аппарата, препятствующего затеканию. Рефлюкс нередко наблюдается при заболевании органов пищеварения и мочевыделения. Поступление в полый орган содержимого, которое ему несвойственно, может вызвать в нем патологические изменения
Признаки
Клинические проявления соответствуют картине эзофагита, но их интенсивность не всегда соответствует степени воспаления по морфологическим признакам. В некоторых случаях течение гастроэзофагального рефлюкса клинически бессимптомно, а почти в половине случаев — малосимптомно. Наиболее характерным симптомом является изжога, ощущаемая в подложечной области и за грудиной. По мере прогрессирования процесса она становится интенсивнее и продолжительнее и может стать постоянной, мучительной, заставляющей больного ограничивать движения, прибегать к питью холодной воды, щелочей и другим попыткам ее устранения. К другим частым проявлениям относятся боль и тяжесть за грудиной, иногда требующие дифференциальной диагностики со стенокардией. В отличие от последней ощущения за грудиной при гастроэзофагальном рефлюксе появляются или усиливаются в основном после еды и в горизонтальном положении, а также при повышении внутрибрюшного давления (вздутие живота, наклоны, статическая нагрузка), не купируются нитроглицерином. При формировании недостаточности кардии возможны отрыжка, срыгивание, а при выраженном отеке слизистой оболочки или осложнении гастроэзофагального рефлюкса стенозом пищевода отмечается затруднение прохождения пищи по пищеводу, что проявляется дисфагией.
Описание
Гастроэзофагеальный рефлюкс, то есть затекание желудочного содержимого в пищевод, встречается наиболее часто и имеет самостоятельное клиническое значение, так как сопровождается мучительными для больного ощущениями и приводит к развитию таких серьезных осложнений как эзофагит, рецидивирующая язва пищевода и сужение пищевода. Возникает этот рефлюкс в основном из-за несостоятельности функции области пищеводно-желудочного перехода — нижнего пищеводного сфинктера, хотя могут иметь значение также патология диафрагмально-пищеводной связки, слизистой розетки, снижение тонуса диафрагмального жома, стенки внутрибрюшной части пищевода и круговых мышц желудка. Возникновению гастроэзофагального рефлюкса и задержке содержимого желудка в пищеводе способствуют расстройство перистальтики пищевода, повышенное внутрижелудочное и внутрибрюшное давление. Тонус нижнего пищеводного сфинктера, зависимый от состояния мышцы и контролируемый нервными и гормональными влияниями, снижается и приводит к гастроэзофагальному рефлюксу при язвенной болезни желудка и двенадцатиперстной кишки, после операций на желудке и пищеводе, при сахарном диабете, болезнях пищевода, врожденной неполноценности соединительной ткани, при длительном применении холинолитиков и щелочей, употреблении избыточной жирной пищи, алкоголя, под влиянием никотина. Вследствие раздражения слизистой оболочки пищевода содержимым желудка (особенно при высокой его кислотности) возникает ее воспаление — рефлюкс-эзофагит.
Диагностика
Диагноз гастроэзофагеального рефлюкса при выраженной картине рефлюкс-эзофагита устанавливают по клиническим симптомам. При бессимптомном и малосимптомном течении установить диагноз и уточнить его помогают дополнительные исследования. Рентгенологически гастроэзофагальный рефлюкс может быть установлен по перемещению из желудка в пищевод бариевой взвеси, но отсутствие этого перемещения при исследовании в вертикальном положении больного не исключает гастроэзофагального рефлюкса. Эзофагоскопия с биопсией является основным методом диагностики начальных стадий рефлюкс-эзофагита; косвенными признаками гастроэзофагального рефлюкса служат пролапс складок желудка в пищевод, наличие хиатальной грыжи, зияние кардии. Эзофагоманометрия позволяет обнаружить пониженное давление дистального сфинктера пищевода, а место, в котором гастроэзофагальный рефлюкс может быть установлен с наибольшей вероятностью, можно определить с помощью рН-электрода, введенного в пищевод, по периодическому появлению в этом месте кислой реакции при суточном измерении рН. Этот наиболее точный метод диагностики применяется в стационарных условиях; другие перечисленные методы исследования могут быть проведены в поликлинике.
Лечение
Лечение больных с гастроэзофагеальным рефлюксом комплексное; оно включает диетотерапию, медикаментозную коррекцию нарушений моторной и секреторной функции желудка, тонуса пищевода, физиотерапию, при необходимости также хирургическое вмешательство. Ограничивают употребление жирных продуктов и разовый объем принимаемой пищи (с целью уменьшения давления в желудке) при 4—6-разовом питании, причем последний прием пищи должен быть не позже чем за 3—4 ч до сна. Исключают отдых в горизонтальном положении после еды. С целью повышения тонуса нижнего пищеводного сфинктера назначают метоклопрамид курсами по 3—4 недели. Исключают или резко сокращают прием холинолитиков. При возникновении рефлюкс-эзофагита показаны алмагель или фосфалюгель, которые следует принимать, не разводя водой, вскоре после еды; облепиховое масло внутрь по 1—2 чайных ложки 2—3 раза день после еды в течение 10—15 дней. При значительной гиперсекреции соляной кислоты в желудке целесообразно назначать блокаторы Н2-рецепторов. Используя иглотерапию или фотолазерное воздействие на биологически активные точки, определяемые индивидуально. Показаниями к хирургическому лечению являются отсутствие эффекта от консервативной терапии в случаях, когда рефлюкс обусловлен наличием параэзофагальной грыжи, а также осложнения незаживающей язвой или стенозом пищевода.
© Медицинская энциклопедия РАМН
диета и ГЭРБ | Общество желудочно-кишечного тракта
Диета и ГЕРДГИС2020-07-29T10: 57: 43-07: 00Что такое ГЭРБ?
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) — это обратный поток содержимого желудка в пищевод. Это происходит в результате грыжи пищеводного отверстия диафрагмы (выпячивание части желудка через диафрагму в область пищевода), рефлюкс-эзофагита, абдоминального давления, связанного с ожирением, или изжоги во время беременности. Мышечное кольцо, называемое нижним сфинктером пищевода (LES), окружает пищевод у входа в желудок.LES расслабляется, чтобы пища попала в желудок, а затем закрывается после того, как еда прошла, тем самым предотвращая отток содержимого желудка. ГЭРБ вызывается длительным расслаблением нижнего сфинктера пищевода и задержкой опорожнения желудка, вызывая раздражение пищевода желудочной кислотой, желчью и пепсином.
Каковы симптомы ГЭРБ?
Самый частый симптом ГЭРБ — изжога. Другие симптомы включают кислый привкус с кислотной регургитацией, отрыжку и вздутие живота.Хотя рекомендации по диете направлены на уменьшение причины ГЭРБ, есть также некоторые продукты, которые могут раздражать уже поврежденный из-за рефлюкса пищевод или усугублять эти симптомы.
Как лечится ГЭРБ?
Лечение ГЭРБ требует изменения диеты и образа жизни, медикаментозной терапии и, в тяжелых случаях, хирургического вмешательства. Лечение включает не только то, что едят, но и то, как и когда едят.
Образ жизни
Некоторые рекомендуемые изменения образа жизни включают:
- Сохранять вертикальное положение во время еды и в течение 45-60 минут после еды (чтобы избежать обратного потока содержимого желудка)
- Достижение и поддержание здоровой массы тела (добавленный вес увеличивает внутрижелудочное давление)
- Поднимите изголовье кровати примерно на 6 дюймов во время сна
- Бросьте курить (курение расслабляет нижний сфинктер пищевода)
- Не ешьте в течение 2–3 часов перед сном
- Избегайте одежды, которая плотно прилегает к области живота
Диетическое
Рекомендации по диетическому лечению ГЭРБ включают:
- Ограничьте употребление продуктов с высоким содержанием жира, e.грамм. жареные продукты, выпечка с высоким содержанием жира, сливки, мороженое, сыры с высоким содержанием жира, колбасы, бекон, картофельные чипсы и т. д. Было обнаружено, что жирная пища задерживает опорожнение желудка и снижает давление LES, тем самым продлевая время воздействия желудочной кислоты и желудочного сока на пищевод. объем, доступный для рефлюкса.
- Обеспечьте адекватное потребление белка. Ранние исследования показали, что белок увеличивает давление LES, тем самым обеспечивая закрытие сфинктера и уменьшая рефлюкс. Несмотря на то, что более поздние исследования не подтверждают это мнение, соблюдение диеты с адекватным потреблением белка с низким содержанием жира все же может помочь в заживлении раздраженной слизистой оболочки или язв.
- Ограничьте количество шоколада и кофе. Оба содержат метилксантин, который заставляет мышцы расслабляться и снижает давление LES. Кроме того, кофе может стимулировать секрецию желудка, что может способствовать рефлюксу. При раздражении слизистой оболочки пищевода необходимо определить индивидуальную переносимость кофе (обычного или без кофеина).
- Ограничьте или избегайте употребления алкоголя, мяты, цитрусовых, помидоров и / или газированных напитков в соответствии с индивидуальной переносимостью. Эти продукты могут вызвать дополнительное раздражение поврежденной слизистой оболочки пищевода, но не было обнаружено, что они сами вызывают рефлюкс.
Заключение
Гастроэзофагеальная рефлюксная болезнь возникает, когда содержимое желудка контактирует с пищеводом. Симптомы включают изжогу, отрыжку и / или срыгивание. Лечение ГЭРБ может включать изменение диеты, образа жизни, прием лекарств и иногда хирургическое вмешательство. Проконсультируйтесь с врачом для составления индивидуального плана лечения.
Мэри Флешер , клинический диетолог, больница Ричмонд
Впервые опубликовано в информационном бюллетене
Inside Tract ®, выпуск 135 — январь / февраль 2003 г.Изображение: GBALLGIGGSPHOTO | bigstockphoto.com
Питание пациентов с раком желудка: обновление
Опухоли желудочно-кишечного тракта. 2016 May; 2 (4): 178–187.
Rosa Rosania
a Отделения гастроэнтерологии, гепатологии и инфекционных заболеваний, Магдебург, Германия
Костанза Чиаппони
b Отделения общей, висцеральной и сосудистой хирургии, Отто-фон-Герике, Университет Магдебурга, Магдебург, Магдебург, Германия
Peter Malfertheiner
a Отделение гастроэнтерологии, гепатологии и инфекционных заболеваний, Магдебург, Германия
Marino Venerito
a Отделение гастроэнтерологии, гепатологии и инфекционных заболеваний Отделение гастроэнтерологии, гепатологии и инфекционных болезней Отделение гастроэнтерологии, Магдебург, Германия
, Гепатология и инфекционные заболевания, Магдебург, Германияb Отделения общей, висцеральной и сосудистой хирургии, Университет Отто-фон-Герике, Магдебург, Магдебург, Германия
* Проф.Д-р Петер Мальфертхайнер, отделение гастроэнтерологии, гепатологии и инфекционных заболеваний, Университет Отто-фон-Герике, Магдебург, Leipziger Strasse 44, DE – 39120 Магдебург (Германия), электронная почта [email protected]Получено в марте 2016 г. 3; Принято 3 марта 2016 г.
Эта статья цитировалась в других статьях в PMC.Реферат
Предпосылки
Управление питанием пациентов с раком желудка (РЖ) представляет собой сложную задачу.
Резюме
В этом обзоре представлен обзор имеющихся данных о нутритивной поддержке у пациентов с ГК, перенесших операцию, а также у пациентов с запущенным заболеванием
Ключевое сообщение
Для пациентов, перенесших операцию, предоперационное состояние питания напрямую влияет на послеоперационный прогноз , общая выживаемость и выживаемость при конкретном заболевании.Периоперационная нутритивная поддержка, обогащенная иммуностимулирующими питательными веществами, снижает общие осложнения и время пребывания в больнице, но не смертность после обширных плановых операций на желудочно-кишечном тракте. Раннее энтеральное питание после операции улучшает состояние питания в раннем и отдаленном послеоперационном периоде, а также сокращает продолжительность госпитализации. Витамин B 12 и дефицит железа являются частыми метаболическими последствиями после гастрэктомии и требуют соответствующей замены. У истощенных пациентов с поздними стадиями ГК краткосрочное домашнее дополнительное парентеральное питание улучшает качество жизни, нутритивный статус и функциональный статус.Полное парентеральное питание в домашних условиях представляет собой единственный способ потребления калорий для пациентов с поздними стадиями ГК, которые не могут принимать пероральное или энтеральное питание. операбельное и запущенное заболевание.
Ключевые слова: Рак желудка, Управление питанием
Введение
Несмотря на снижение заболеваемости за последние несколько десятилетий, рак желудка (РЖ) остается пятым по распространенности злокачественным новообразованием в мире и третьим по значимости причиной смерти от рака в мире. оба пола во всем мире [1].ГК часто протекает бессимптомно или может вызывать только неспецифические симптомы на ранних стадиях, что является одной из основных причин часто поздней диагностики [2] и относительно плохого прогноза [3].
Снижение веса отмечается у 31–87% пациентов при первом диагнозе злокачественного новообразования, и масштабы потери веса напрямую зависят от типа рака [4]. В частности, потеря веса> 10% в течение предыдущих 6 месяцев наблюдается у 15% пациентов с диагнозом гастроэзофагеальный рак, тогда как недоедание встречается у 80% пациентов с РЖ на поздней стадии [5,6].
Синдром анорексии-кахексии [7,8], обычно описываемый у пациентов с запущенным раком, характеризуется снижением потребления пищи, гипоальбуминемией, потерей веса и истощением мышечной ткани и связан с повышенной заболеваемостью и смертностью [9,10,11 ]. У пациентов с GC это состояние в основном вызвано обструкцией верхних отделов пищеварительного тракта из-за механического воздействия опухоли [12]. Могут последовать дисфагия, преждевременное насыщение, тошнота и рвота. У пациентов с ГК синдром анорексии-кахексии связан с сокращением общей выживаемости [13].Вместе с такими симптомами, как тошнота, рвота, преждевременное насыщение и дисфагия после химиотерапии, лучевой терапии или хирургического вмешательства, это состояние может способствовать недоеданию, связанному с раком [14,15,16]. Таким образом, выявление и лечение недостаточности питания на ранних этапах ГК имеет решающее значение для улучшения результатов лечения пациентов.
Диетологическое лечение
Целью диетотерапии является улучшение статуса питания, обмена веществ, приверженности к противоопухолевой терапии, качества жизни и течения заболевания [17].Нутритивная поддержка рекомендуется как пациентам с ГК, подвергшимся хирургическому вмешательству, так и пациентам с неоперабельным заболеванием, и может осуществляться пероральным, энтеральным (EN) и парентеральным (PN) питанием. Пероральное питание включает диету и пероральные добавки. После резекции желудка рекомендуется диета, основанная на частом приеме пищи небольшими порциями с ограничением простых углеводов, чтобы предотвратить демпинг-синдром. EN (питание в кишечнике) определяется по-разному и может включать диету, пероральные добавки и кормление через зонд.В настоящем обзоре ЭП определяется как питание через зонд и включает чрескожную эндоскопическую гастростомию, чрескожную радиологическую гастростомию и чрескожную эндоскопическую еюностомию. ЭН сохраняет структурную и функциональную целостность желудочно-кишечного тракта и представляет собой действенный вариант питания для пациентов с дисфагией или обструкцией, когда пероральный прием не удовлетворяет потребности в питании [18]. ЭП безопаснее, дешевле и физиологичнее ПП. Однако у пациентов с нарушением функции желудочно-кишечного тракта ПН является обязательным.Хотя PN (питание центральными и периферическими венами) обеспечивает оптимальное питание, оно увеличивает риск инфекций по сравнению с EN [19]. Инфекция кровотока, связанная с катетером, является наиболее частым и серьезным осложнением у взрослых пациентов, получающих PN. В систематическом обзоре 39 исследований общая частота инфицирования кровотока, связанного с катетером, варьировала от 0,4 до 4,6 эпизодов на 1000 катетер-дней (медиана 1,3) у пациентов с домашним PN (HPN) и в основном была связана с грамположительными бактериями кожная флора человека [20].Таким образом, при терминальной стадии болезни польза от нутритивной поддержки может быть ограничена и связана с повышенным риском осложнений. Как следствие, недавние немецкие рекомендации S3 рекомендуют нутритивную поддержку только в том случае, если преимущества преобладают над любыми возможными осложнениями или по желанию пациентов [17].
Оценка состояния питания
Оценка состояния питания, приема пищи и тяжести заболевания должна проводиться, начиная с первого контакта, на регулярной основе и через короткие промежутки времени (не реже, чем каждые 4-8 недель), чтобы распознать любое заболевание. снижение нутритивного статуса как можно раньше [17].Было разработано несколько анкет для раннего выявления и лечения недоедающих пациентов больниц [21,22]. В частности, повышение баллов по инструменту «Скрининг пищевых рисков 2002» (NRS 2002) связано с увеличением частоты послеоперационных осложнений и увеличением продолжительности пребывания в стационаре [23]. Кроме того, в недавнем исследовании, посвященном оценке эффективности Краткого вопросника оценки питания (SNAQ) в прогнозировании риска послеоперационной смертности после операции GC, оценка SNAQ ≥1 была связана с повышенным уровнем смертности по сравнению с оценкой SNAQ, равной 0 (ИЛИ = 5.1; 95% ДИ: 1,01–23,8) [24].
В недавнем ретроспективном исследовании 775 пациентов, перенесших гастрэктомию по поводу GC, только индекс массы тела (ИМТ) не повлиял на периоперационную заболеваемость, безрецидивную или общую выживаемость [25]. Однако у пациентов с ИМТ <18,5 и низким уровнем альбумина до операции значительно снизилась общая выживаемость после гастрэктомии.
Были предложены различные индексы для прогнозирования прогноза пациентов со злокачественными новообразованиями желудочно-кишечного тракта [26,27].В частности, прогностический индекс питания (ПНИ) получил широкое распространение благодаря его эффективности, простоте и удобству [28]. PNI рассчитывается по следующей формуле: 10 × значение сывороточного альбумина (г / дл) + 0,005 × количество лимфоцитов в периферической крови. Оценка <45 указывает на серьезное нарушение питания, тогда как PNI ≥45 связано с нормальным статусом питания. В недавнем метаанализе PNI был связан с глубиной инвазии и метастазами в лимфатические узлы в GC [29]. Сакураи и др.[30] показали, что у пациентов с ГК предоперационный PNI является независимым прогностическим фактором как для общей выживаемости, так и для выживаемости при конкретном заболевании. Примечательно, что пациенты с заболеванием UICC стадии 1 и 2 имели значительно худшие результаты в группе с низким PNI, чем в группе с высоким PNI. Подводя итог, можно сказать следующее:
Предоперационная нутритивная поддержка может улучшить послеоперационный исход у пациентов, перенесших операцию по поводу GC
Имеется несколько проверенных вопросников для раннего выявления и лечения истощенных пациентов больниц
PNI или комбинация предоперационного ИМТ <18.5 и низкий уровень альбумина является прогностическим признаком снижения общей выживаемости после гастрэктомии
Предоперационное питание
Для пациентов, перенесших серьезную операцию, предоперационное недоедание связано с повышенной заболеваемостью (т.е. респираторный дистресс-синдром) и смертность [31,32,33]. Таким образом, улучшение нутритивного статуса перед операцией может улучшить послеоперационный результат у пациентов с ГК.Немецкие рекомендации S3 рекомендуют нутритивную поддержку всем пациентам с недостаточным питанием [17]. Это состояние определяется как потребление пероральной пищи <500 ккал / день или ≤75% от потребности в течение более 1-2 недель [34]. В интактном желудочно-кишечном тракте ЭП так же эффективна, как и ПП [35]. ЭП можно проводить через назогастральный или назоэнтериальный зонд в течение коротких периодов времени, тогда как прямой доступ к кишечнику, например через еюностомию, должен быть предпочтительным, если ЭП вводится более 3 недель [36].Недавно рандомизированное контролируемое исследование (РКИ) с участием 106 пациентов, перенесших гастрэктомию по поводу ГК, продемонстрировало, что предоперационная ЭП улучшает послеоперационный нутритивный статус, уменьшает воспалительную реакцию и способствует выздоровлению пациентов [37]. Пациентам с нефункциональным или недоступным желудочно-кишечным трактом может потребоваться нутритивная поддержка через ПП [38].
Пероральное или энтеральное введение питательного раствора, обогащенного иммуностимулирующими питательными веществами (аргинин, ω-3 жирные кислоты и нуклеотиды), называется иммунным питанием (ИН) [39].В недавнем метаанализе 9 исследований иммунологическое влияние энтерального ИН было оценено у пациентов, перенесших операцию по поводу ГК [40]. По сравнению со стандартным EN, IN усиливает иммунитет хозяина за счет увеличения уровня иммуноглобулинов, Т-хелперов 17 и естественных клеток-киллеров и снижения уровня провоспалительных цитокинов, таких как IL-6 и TNF-α. В другом метаанализе, основанном на 21 РКИ, периоперационная ИН сравнивалась со стандартной ЭП у пациентов, перенесших обширные плановые операции на желудочно-кишечном тракте.Периоперационная ИН значительно снизила общие осложнения и продолжительность госпитализации, но не смертность [41]. Соответственно, ESPEN Guidelines, German S3 Guidelines [17] для GC и Североамериканский саммит по хирургическому питанию [42] рекомендуют пероральные / энтеральные IN для пациентов с раком верхних отделов желудочно-кишечного тракта за 5-7 дней до операции и в послеоперационный период. На рисунке показан алгоритм доставки периоперационного питания у пациентов, перенесших операцию по поводу GC.
Алгоритм принятия решения о маршруте доставки периоперационного питания у пациентов, перенесших операцию по поводу GC.* Пероральный прием пищи <500 ккал / день или ≤75% от потребности в течение более 1-2 недель [17]. GI = желудочно-кишечный тракт; PEJ = чрескожная эндоскопическая нейностомия.
Независимо от статуса питания, группа улучшенного восстановления после операции (ERAS) недавно предоставила рекомендации по периоперационному комплексному ведению пациентов с опухолями верхних отделов желудочно-кишечного тракта. Они рекомендуют предоперационную углеводную нагрузку (800 мл напитка с 12,5% углеводов за ночь перед операцией и 400 мл на следующее утро за 2 часа до индукции анестезии), чтобы (1) снизить резистентность к инсулину и гликозилирование тканей, вызванное операцией. , (2) помогают в послеоперационном контроле уровня глюкозы и (3) поддерживают нормальную функцию кишечника [43].Подводя итоги, можно констатировать следующее:
Периоперационная ИН снижает общие осложнения и продолжительность госпитализации, но не снижает смертность после обширных плановых операций на желудочно-кишечном тракте
Предоперационная углеводная нагрузка в ночное время перед операцией снижает резистентность к инсулину и гликозилирование тканей, вызванное хирургия, помогает в послеоперационном контроле уровня глюкозы и поддерживает нормальную функцию кишечника
Послеоперационное питание
Роль послеоперационной нутритивной поддержки заключается в поддержании нутритивного статуса в катаболический период после операции.В проспективном исследовании, оценивающем периоперационный статус питания 435 пациентов с ГК, распространенность тяжелого недоедания значительно увеличилась после операции (2,3 и 26,3% до и после операции, соответственно) [44]. Пожилой возраст, предоперационная потеря веса и открытая операция были определены как факторы риска тяжелой послеоперационной недостаточности питания.
После хирургического лечения снижение аппетита и диеты во время выздоровления и восстановление нутритивного статуса может занять до 1 года [45].Функции тонкого кишечника восстанавливаются между 6 и 12 часами после операции, что указывает на то, что в это время можно начать поддержку ЭП. В соответствии с этим представлением, исследование Gabor et al. [46] показали, что через 6 ч после операции можно начинать ЭП. Соответственно, пациенты, перенесшие операцию на верхних отделах желудочно-кишечного тракта, обычно получают чрескожную еюностомическую трубку для послеоперационной ЭП, которую можно продолжить также после выписки в зависимости от потребностей пациента. Раннее пероральное питание после операции по поводу ГК также безопасно и не увеличивает частоту послеоперационных осложнений по сравнению с ЭП через назогастральный зонд [47].В РКИ с участием 105 пациентов, перенесших операцию по поводу рака желудочно-кишечного тракта, ранняя послеоперационная нутритивная поддержка снизила высокий метаболизм, связанный с хирургической травмой, поддержала функцию слизистого барьера кишечника и снизила частоту кишечных инфекций, улучшив выздоровление пациентов [48] . Периоперационное питание эффективно снижает частоту послеоперационных осложнений у истощенных пациентов с РЖ. В другом РКИ 468 пациентов с умеренной или тяжелой недостаточностью питания с ГК или колоректальным раком были случайным образом распределены на 7-дневное предоперационное и 7-дневное послеоперационное искусственное питание (ЭП или ПП) и сравнивались с простой контрольной группой.Среди пациентов, получавших периоперационное питание, наблюдалось двукратное снижение послеоперационных осложнений и трехкратное снижение смертности. Наиболее резко снизилось количество серьезных септических осложнений (14,9 против 27,9%, p = 0,011), таких как пневмония и раневая инфекция [49]. Общая продолжительность госпитализации и послеоперационного пребывания в контрольной группе была значительно больше (29 против 22 дней, p = 0,014), чем у исследуемых пациентов. В заключение можно сказать следующее:
EN можно безопасно начать через 6 часов после операции через чрескожную еюностомическую трубку
Раннее послеоперационное питание снижает высокий метаболизм, связанный с хирургической травмой, поддерживает функцию барьера слизистой оболочки кишечника и снижает частоту кишечных инфекций, улучшая выздоровление пациентов
Пищевые добавки после гастрэктомии
Анемия является частым осложнением после гастрэктомии, а дефицит железа, витамина B 12 или фолиевой кислоты после желудочной операция.Анемия развивается у 50% пациентов, перенесших тотальную резекцию желудка [50]. Плохой статус питания и пониженное потребление железа с пищей могут привести к истощению запасов железа после операции на желудке [51]. Повышенное истощение запасов железа также может быть результатом желудочно-кишечной кровопотери в месте анастомоза [52] или избыточного бактериального роста в слепых петлях [53]. Однако изменения в пищеварении и нарушение всасывания железа считаются ведущими факторами, способствующими дефициту железа после гастрэктомии [54]. Нарушение всасывания пищевого железа, возможно, является результатом снижения секреции желудочной кислоты и обхода двенадцатиперстной кишки.Пониженная кислотность желудочного сока ухудшает превращение негемового железа (Fe 3+ ) в более усваиваемую форму двухвалентного железа (Fe 2+ ) [55]. Реконструкция после резекции желудка может снизить абсорбцию железа из-за обхода основных участков абсорбции железа: двенадцатиперстной кишки и проксимального отдела тощей кишки.
В ретроспективном исследовании 119 пациентов, перенесших дистальную гастрэктомию с реконструкциями по Бильроту I или Roux-en-Y для стадии I GC, одномерный и многомерный анализ показал, что реконструкция Roux-en-Y является единственным фактором риска (p = 0 .0487; ИЛИ = 2,755; 95% ДИ: 1,01–7,91) для снижения гемоглобина [56]. Сообщалось также о более высокой частоте анемии и дефицита железа после тотальной гастрэктомии по сравнению с субтотальной гастрэктомией [57].
Лечение железодефицитной анемии после гастрэктомии требует коррекции дефицита циркулирующего гемоглобина, восполнения дефицита накопления и коррекции любого излечимого источника аномальной кровопотери. Также обычно эффективно профилактическое лечение ожидаемого дефицита простыми препаратами в форме сульфата железа или глюконата [17].
Дефицит витамина B 12 может развиться уже через 1 год после тотальной резекции желудка [58]. Внутренний фактор, который в основном продуцируется париетальными клетками кислородных желез желудка, необходим для энтерального поглощения витамина B 12 [59]. Fischermann et al. [60] показали, что тип реконструкции не влияет на всасывание витамина B 12 . Таким образом, прохождение пищи через двенадцатиперстную кишку не является необходимым для энтерального всасывания витамина B 12 . Однако клинические проявления дефицита витамина B 12 после гастрэктомии не были четко определены, а роль дополнительной терапии витамином B 12 не была стандартизирована.В немецком руководстве S3 [17] после операции рекомендуется принимать добавки с витамином B 12 . Введение витамина B 12 эффективно как подкожно, так и перорально [61]. Действительно, в исследовании Adachi et al. [62] пероральный прием витамина B 12 был эффективным в увеличении концентрации витамина B 12 в сыворотке с быстрым исчезновением симптомов, связанных с дефицитом витамина B 12 . Kim et al. [63] продемонстрировали, что пероральная заместительная терапия витамином B 12 обеспечивает безопасное и эффективное лечение дефицита витамина B 12 после тотальной гастрэктомии у пациентов с РЖ.Обоснованием этого подхода является наличие второй, менее эффективной транспортной системы для витамина B 12 , которая не требует внутреннего фактора или функционирующего терминального отдела подвздошной кишки, но использует пассивную диффузию. Таким образом, профилактическое энтеральное введение витамина B 12 после тотальной гастрэктомии является хорошей и удобной альтернативой подкожному пути для предотвращения симптомов, связанных с дефицитом витамина B 12 .
Недостаточность поджелудочной железы была предложена как возможная причина мальабсорбции после тотальной гастрэктомии [64].Хотя внешнесекреторная недостаточность поджелудочной железы была продемонстрирована после гастрэктомии, ключевым вопросом остается вопрос о том, могут ли добавки ферментов поджелудочной железы улучшить клинический результат у пациентов с РЖ. В проспективном двойном слепом рандомизированном параллельном плацебо-контролируемом многоцентровом исследовании добавление ферментов поджелудочной железы не привело к значительным различиям между плацебо и группой, получавшей ферменты, в отношении привычек кишечника или недостаточной ассимиляции жира [65]. Влияние высоких доз ферментов поджелудочной железы на симптомы и стеаторею после тотальной гастрэктомии было незначительным и не оправдывало рутинного использования.Таким образом, можно сказать следующее:
Анемия развивается у 50% пациентов, перенесших тотальную резекцию желудка
Нарушение всасывания пищевого железа из-за снижения секреции желудочной кислоты и обхода двенадцатиперстной кишки является основной причиной анемия после гастрэктомии
Лечение железодефицитной анемии требует коррекции дефицита циркулирующего гемоглобина, восполнения дефицита накопления и коррекции любого излечимого источника аномальной кровопотери
Может развиться дефицит витамина B 12 уже через 1 год после тотальной гастрэктомии
Текущие руководства рекомендуют добавление витамина B 12 после гастрэктомии
Влияние высоких доз ферментов поджелудочной железы на симптомы и стеаторею после тотальной гастрэктомии незначительно и не оправдывает себя рутинное использование
Nutritio n у пациентов с Advanced GC
Когда показана нутритивная поддержка, пероральный и энтеральный пути введения предпочтительнее парентерального.У пациентов с ГК со стенозом кардии или привратника установка стента может позволить оральное питание, улучшающее качество жизни. Руководства Европейского общества клинического питания и метаболизма рекомендуют применение ПП, когда «можно ожидать неадекватного приема пищи менее 60% от расчетного потребления энергии в течение более десяти дней» [19]. Пациентам, получающим химиотерапию, у которых наблюдаются связанные с химиотерапией побочные эффекты со стороны желудочно-кишечного тракта (например, анорексия, тошнота, рвота, запор и диарея), рекомендуется дополнительная HPN для стабилизации веса и продолжения терапии [17].Кроме того, исходя из нашего опыта, краткосрочная дополнительная HPN может быть безопасно и эффективно предоставлена пациентам с потерей веса, несмотря на адекватное пероральное потребление или пероральные добавки (например, раковая кахексия), а также в случаях непереносимости EN (например, тошнота, боль в животе и понос).
Для пациентов с карцинозом брюшины и тяжелым нарушением функции желудочно-кишечного тракта обязательна общая HPN [15]. Синдром короткой кишки из-за обширного хирургического вмешательства является еще одним показанием для HPN [66].Успех ПП зависит от соблюдения пациентом режима лечения, поддержки со стороны профессионального и преданного диетолога и сотрудничества между пациентом, диетологом, врачом и поставщиком медицинских услуг на дому [67]. В многочисленных исследованиях PN не удалось снизить токсичность химиотерапии [68] и улучшить скорость ответа [69]. Особенно для пациентов с поздними стадиями ГК и для тех, кто не страдает от истощения или гипофагии, риски ПП могут перевешивать преимущества [70]. С другой стороны, у пациентов с прогрессирующим раком и недостаточностью питания средней и тяжелой степени HPN улучшает качество жизни, пищевой статус и функциональный статус независимо от типа опухоли [71].Наибольший эффект был отмечен у пациентов, получавших дополнительную HPN в течение 3 месяцев, хотя пациенты, получавшие HPN в течение 1 или 2 месяцев, также продемонстрировали значительные улучшения. Подводя итог, можно сказать следующее:
Для пациентов с поздними стадиями ГК, которые не могут принимать пероральное питание или ЭП, обязательна общая HPN.
риски PN могут перевешивать преимущества
У истощенных пациентов с запущенным раком краткосрочная дополнительная HPN связана с улучшением качества жизни, статуса питания и функционального статуса
Будущие направления
Современная терапия пациентов с локализованными ГК, подходящими для хирургии, включают неоадъювантную радиохимиотерапию и периоперационную химиотерапию, которые представляют собой источники катаболического стресса и недоедания.Роль нутритивной поддержки во время неоадъювантного / периоперационного лечения пациентов с РЖ еще предстоит определить. В Европе в рамках контролируемого исследования фазы III в настоящее время проверяется, может ли ИН улучшить качество жизни пациентов, получавших неоадъювантную радиохимиотерапию и периоперационную химиотерапию по поводу рака пищевода и желудка ({«type»: «клиническое испытание», «attrs»: {«text «:» NCT01423799 «,» term_id «:» NCT01423799 «}} NCT01423799).
Заявление о раскрытии информации
R.R., C.C., P.M. И м.В. нечего раскрывать.
Справочные документы
2. Вадхва Р., Такета Т., Судо К., Блум М.А., Аджани Дж.А. Современные онкологические подходы к аденокарциноме желудка. Гастроэнтерол Clin North Am. 2013; 42: 359–369. [PubMed] [Google Scholar] 4. Гупта Д., Лис К. Г., Граник Дж., Груч Дж. Ф., Ваши П. Г., Ламмерсфельд, Калифорния. Недоедание было связано с низким качеством жизни при колоректальном раке: ретроспективный анализ. J Clin Epidemiol. 2006; 59: 704–709. [PubMed] [Google Scholar] 5. Deans DA, Tan BH, Wigmore SJ, Ross JA, de Beaux AC, Paterson-Brown S, Fearon KCD.Влияние системного воспаления, рациона питания и стадии заболевания на скорость потери веса у пациентов с раком желудочно-пищеводного тракта. Br J Рак. 2009. 100: 63–69. [Бесплатная статья PMC] [PubMed] [Google Scholar] 6. Раваско П., Монтейро-Грилло И., Видаль П.М., Камило М.Э. Рак: болезнь и питание являются ключевыми детерминантами качества жизни пациентов. Поддержка лечения рака. 2004. 12: 246–252. [PubMed] [Google Scholar] 7. Динс С., Вигмор С. Системное воспаление, кахексия и прогноз у больных раком.Curr Opin Clin Nutr Metab Care. 2005. 8: 265–269. [PubMed] [Google Scholar] 8. фон Хелинг С., Анкер С.Д. Кахексия как серьезная недооцененная и неудовлетворенная медицинская потребность: факты и цифры. J Cachexia Sarcopenia Muscle. 2010; 1: 1–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 9. Фирон К., Штрассер Ф., Анкер С.Д., Босэус I, Брюра Э., Файнсингер Р.Л., Ятой А., Лопринци К., Макдональд Н., Мантовани Дж., Дэвис М., Мускаритоли М., Оттери Ф, Радбрух Л., Раваско П., Уолш Д., Уилкок А. , Kaasa S, Baracos VE. Определение и классификация раковой кахексии: международный консенсус.Ланцет Онкол. 2011; 12: 489–495. [PubMed] [Google Scholar] 10. Тан ЧР, Яффи П.М., Джамиль Л.Х., Ло СК, Ниссен Н., Пандол С.Дж., Тули Р., Хендифар А.Е. Кашексия рака поджелудочной железы: обзор механизмов и терапии. Front Physiol. 2014; 5: 88. [Бесплатная статья PMC] [PubMed] [Google Scholar] 11. Эванс В.Дж., Морли Дж. Э., Аргилес Дж., Бейлс К., Баракос В., Гаттридж Д., Ятой А., Калантар-Заде К., Лохс Х., Мантовани Дж., Маркс Д., Митч В.Е., Мускаритоли М., Наджанд А., Пониковски П., Росси Фанелли Ф. , Шамбелан М., Шолс А., Шустер М., Томас Д., Вулф Р., Анкер С.Д.Кахексия: новое определение. Clin Nutr. 2008. 27: 793–799. [PubMed] [Google Scholar] 13. Дьюис У.Д., Бегг С., Лавин П.Т., Band PR, Беннетт Дж. М., Бертино Дж. Р., Коэн М. Х., Дуглас Х.о., младший, Энгстром П. Ф., Эздинли Э. З., Хортон Дж., Джонсон Дж. Дж., Мёртель К. Г., Окен М. М., Перлия К., Розенбаум К., Сильверштейн М.Н., Скил Р.Т., Спонзо РВ, Торми, округ Колумбия. Прогностический эффект снижения веса до химиотерапии у онкологических больных. Восточная кооперативная онкологическая группа. Am J Med. 1980; 69: 491–497. [PubMed] [Google Scholar] 14. Тонг Х., Изенринг Э., Йейтс П.Распространенность симптомов воздействия питания и их связь с качеством жизни и клиническими исходами у онкологических пациентов. Поддержка лечения рака. 2009; 17: 83–90. [PubMed] [Google Scholar] 15. Шахморади Н., Кандиа М., Пэн Л. Влияние статуса питания на качество жизни больных раком на поздних стадиях при уходе на дому в хосписе. Азиатский Pac J Cancer Prev. 2009; 10: 1003–1009. [PubMed] [Google Scholar] 16. Ван Катсем Э., Арендс Дж. Причины и последствия недоедания, связанного с раком. Eur J Oncol Nurs.2005; 9 (приложение 2): S51 – S63. [PubMed] [Google Scholar] 17. Arends J, Bertz H, Bischoff SC, Fietkau R, Herrmann HJ, Holm E, Horneber M, Hütterer E, Körber J, Schmid I, DGEM Steering, Комитет S3-Руководство Немецкого общества диетологии (DGEM) Aktuelle Ernahrungsmed. 2015; 40: 1–74. [Google Scholar] 18. Weimann A, Braga M, Harsanyi L, Laviano A, Ljungqvist O, Soeters P, DGEM (Немецкое общество диетической медицины) Jauch KW, Kemen M, Hiesmayr JM, Horbach T, Kuse ER, Vestweber KH, ESPEN (Европейское общество парентерального питания) и энтеральное питание) Руководство ESPEN по энтеральному питанию: хирургия, включая трансплантацию органов.Clin Nutr. 2006. 25: 224–244. [PubMed] [Google Scholar] 19. Бозцетти Ф., Арендс Дж., Лундхольм К., Миклрайт А., Цурчер Дж., Мускаритоли М.; ESPEN. Руководство ESPEN по парентеральному питанию: нехирургическая онкология. Clin Nutr. 2009. 28: 445–454. [PubMed] [Google Scholar] 20. Dreesen M, Foulon V, Spriet I, Goossens G, Hiele M, De Pourcq L, Willems L. Эпидемиология катетерных инфекций у взрослых пациентов, получающих парентеральное питание в домашних условиях: систематический обзор. Clin Nutr. 2013; 32: 16–26. [PubMed] [Google Scholar] 21.Kruizenga H, Seidell J, de Vet H, Wierdsma N, van Bokhorst-de van der Schueren MA. Разработка и валидация больничного скрининга на недостаточность питания: краткий опросник для оценки питания (SNAQ ©) Clin Nutr. 2005. 24: 75–82. [PubMed] [Google Scholar] 22. van Venrooij LM, van Leeuwen PA, Hopmans W, Borgmeijer-Hoelen MM, de Vos R, De Mol BA. Точность быстрых и простых инструментов скрининга недостаточности питания — краткого вопросника оценки питания, универсального инструмента скрининга недоедания и модифицированного универсального инструмента скрининга недоедания — у пациентов, перенесших кардиохирургические операции.J Am Diet Assoc. 2011; 111: 1924–1930. [PubMed] [Google Scholar] 23. Guo W, Ou G, Li X, Huang J, Liu J, Wei H. Скрининг пищевого риска у пациентов с карциномой желудка перед операцией NRS 2002 и его связь с послеоперационными результатами. J Gastroenterol Hepatol. 2010. 25: 800–803. [PubMed] [Google Scholar] 24. Тегельс Дж., Де Маат М., Хулсеве К., Хофвейк А., Стоут Дж. Значение гериатрической слабости и оценки нутритивного статуса в прогнозировании послеоперационной смертности при хирургии рака желудка.J Gastrointest Surg. 2014; 18: 439–445. [PubMed] [Google Scholar] 25. Ejaz A, Spolverato K, Poultsides G, Fields R, Bloomston M, Cho C, Votanopoulos K, Maithel S, Pawlik T. Влияние индекса массы тела на периоперационные исходы и выживаемость после резекции по поводу рака желудка. J Surg Res. 2015; 195: 74–82. [PubMed] [Google Scholar] 26. Ашер В., Ли Дж., Иннама А. Предоперационное соотношение лимфоцитов тромбоцитов как независимый прогностический маркер рака яичников. Clin Transl Oncol. 2011; 13: 499–503. [PubMed] [Google Scholar] 27.Чуа В., Чарльз К.А., Баракос В.Е., Кларк С.Дж. Отношение нейтрофилов / лимфоцитов позволяет прогнозировать результаты химиотерапии у пациентов с распространенным колоректальным раком. Br J Рак. 2011; 104: 1288–1295. [Бесплатная статья PMC] [PubMed] [Google Scholar] 28. Онодера Т., Госеки Н., Косаки Г. Прогностический индекс питания в желудочно-кишечной хирургии у истощенных онкологических больных (на японском языке) Нихон Гека Гаккай Засси. 1984; 85: 1001–1005. [PubMed] [Google Scholar] 29. Нозоэ Т., Ниномия М., Маэда Т., Мацукума А., Накашима Х., Эзаки Т.Прогностический пищевой индекс: инструмент для прогнозирования биологической агрессивности рака желудка. Хирург сегодня. 2010; 40: 440–443. [PubMed] [Google Scholar] 30. Сакураи К., Охира М., Тамура Т., Тойокава Т., Амано Р., Кубо Н., Танака Х, Мугурума К., Яширо М., Маеда К., Хиракава К. Прогностический потенциал предоперационного статуса питания в долгосрочных прогнозах исходов для пациентов с раком желудка . Энн Сург Онкол. 2016; 23: 525–533. [PubMed] [Google Scholar] 31. Рей-Ферро М., Кастаньо Р., Ороско О, Серна А., Морено А.Нутритивная и иммунологическая оценка пациентов с раком желудка до и после операции. Питание. 1997; 13: 878–881. [PubMed] [Google Scholar] 32. Сунгуртекин Х., Сунгуртекин У., Балчи С., Зенцир М., Эрдем Э. Влияние нутритивного статуса на осложнения после обширных внутрибрюшных операций. J Am Coll Nutr. 2004. 23: 227–232. [PubMed] [Google Scholar] 33. Кузу М.А., Терзиоглу Х., Генч В., Эркек А.Б., Озбан М., Сонюрек П., Эльхан А.Х., Торун Н. Предоперационная оценка риска питания для прогнозирования послеоперационного исхода у пациентов, перенесших серьезную операцию.Мир J Surg. 2006. 30: 378–390. [PubMed] [Google Scholar] 34. Арендс Дж., Бодоки Дж., Бозцетти Ф., Фирон К., Мускаритоли М., Сельга Дж., Ван Бокхорст-де ван дер Шуерен М. А., фон Мейенфельдт М., DGEM (Немецкое общество диетологии) Цюрхер Г., Фиткау Р., Аульберт Э, Фрик Б. , Holm M, Kneba M, Mestrom HJ, Zander A, ESPEN (Европейское общество парентерального и энтерального питания) Руководство ESPEN по энтеральному питанию: нехирургическая онкология. Clin Nutr. 2006. 25: 245–259. [PubMed] [Google Scholar] 35. Бозцетти Ф.Нутритивная поддержка пациентов с раком пищевода. Поддержка лечения рака. 2010; 18: S41 – S50. [PubMed] [Google Scholar] 36. Мариетт С., Де Боттон М., Писсен Г. Хирургия у пациентов с раком пищевода и желудка: какова роль нутритивной поддержки в вашей повседневной практике? Энн Сург Онкол. 2012; 19: 2128–2134. [PubMed] [Google Scholar] 37. Ding D, Feng Y, Song B, Gao S, Zhao J. Влияние предоперационного и послеоперационного энтерального питания на послеоперационный статус питания и иммунную функцию пациентов с раком желудка.Turk J Gastroenterol. 2015; 26: 181–185. [PubMed] [Google Scholar] 38. Липман Т. Зерна или вены: действительно ли энтеральное питание лучше парентерального? Посмотрите на доказательства. JPEN J Parenter Enteral Nutr. 1998. 22: 167–182. [PubMed] [Google Scholar] 39. Heyland DK, Novak F, Drover JW, Jain M, Su X, Suchner U. Должно ли иммунное питание стать обычным делом для тяжелобольных пациентов? Систематический обзор доказательств. ДЖАМА. 2001; 286: 944–953. [PubMed] [Google Scholar] 40. Серантола Ю., Хюбнер М., Грасс Ф., Демартинес Н., Шефер М.Иммунное питание в хирургии желудочно-кишечного тракта. Br J Surg. 2011; 98: 37–48. [PubMed] [Google Scholar] 41. Джанотти Л., Брага М., Несполи Л., Радаэлли Дж., Бенедуче А., Ди Карло В. Рандомизированное контролируемое исследование предоперационного перорального приема добавок со специальной диетой у пациентов с раком желудочно-кишечного тракта. Гастроэнтерология. 2002; 122: 1763–1770. [PubMed] [Google Scholar] 42. McClave SA, Kozar R, Martindale RG, Heyland DK, Braga M, Carli F, Drover JW, Flum D, Gramlich L, Herndon DN, Ko C, Kudsk KA, Lawson CM, Miller KR, Taylor B, Wischmeyer PES.Сводные моменты и согласованные рекомендации Североамериканского саммита по хирургическому питанию. JPEN J Parenter Enteral Nutr. 2013; 37 (доп.): 99С – 105С. [PubMed] [Google Scholar] 43. Мариетт К. Роль нутритивной поддержки в программе ERAS. J Visc Surg. 2015; 152 (приложение 1): S18 – S20. [PubMed] [Google Scholar] 44. Shim H, Cheong JH, Lee KY, Lee H, Lee JG, Noh SH. Периоперационные изменения нутритивного статуса у больных раком желудочно-кишечного тракта. Йонсей Мед Дж. 2013; 54: 1370–1376. [Бесплатная статья PMC] [PubMed] [Google Scholar] 45.Ryu SW, Kim IH. Сравнение различных оценок питания при выявлении недоедания у пациентов с раком желудка. Мир Дж. Гастроэнтерол. 2010. 16: 3310–3317. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Габор С., Реннер Х., Маци В., Ратценхофер Б., Линденманн Дж., Санкин О., Пинтер Х., Майер А., Смолле Дж., Смолле-Юттнер Ф.М. Раннее энтеральное питание по сравнению с парентеральным питанием после резекции и реконструкции пищевода или пищевода. Br J Nutr. 2005; 93: 509–513. [PubMed] [Google Scholar] 47.Hur H, Si Y, Kang WK, Kim W, Jeon HM. Влияние раннего перорального кормления на хирургические результаты и восстановление после излечивающей операции по поводу рака желудка: результаты пилотного исследования. Мир J Surg. 2009. 33: 1454–1458. [PubMed] [Google Scholar] 48. Хуан Д., Сунь З., Хуанг Дж., Шен З. Раннее энтеральное питание в сочетании с парентеральным питанием у пожилых пациентов после операции из-за рака желудочно-кишечного тракта. Int J Clin Exp Med. 2015; 15: 13937–13945. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. У GH, Лю Чж, Ву Чж, Ву ZG.Периоперационное искусственное питание у истощенных больных раком желудочно-кишечного тракта. Мир Дж. Гастроэнтерол. 2006; 12: 2441–2444. [Бесплатная статья PMC] [PubMed] [Google Scholar] 50. Келли В.Д., Маклин Л.Д., Перри Дж. Ф., Вангенстин, Огайо. Исследование пациентов после тотальной и почти тотальной гастрэктомии. Операция. 1953; 35: 964–982. [PubMed] [Google Scholar] 51. Хайнс Дж. Д., Хоффбранд А. В., Моллин Д. Л.. Гематологические осложнения после частичной гастрэктомии. Обследовано 292 пациента. Am J Med. 1967. 43: 555–569. [PubMed] [Google Scholar] 52.Кимбер С., Паттерсон Дж. Ф., Вайнтрауб Л. Р.. Патогенез железодефицитной анемии после частичной гастрэктомии. Исследование баланса железа. ДЖАМА. 1967; 202: 935–938. [PubMed] [Google Scholar] 53. Тоскес ПП. Гематологические аномалии после резекции желудка. Major Probl Clin Surg. 1976; 20: 119–128. [PubMed] [Google Scholar] 54. Тови Ф, Кларк С. Анемия после частичной гастрэктомии: запущенное излечимое состояние. Ланцет. 1980; 1: 956–958. [PubMed] [Google Scholar] 56. Имамура Т., Комацу С., Итикава Д., Косуга Т., Окамото К., Кониси Х., Сиодзаки А., Фудзивара Х., Оцудзи Э.Реконструктивный метод как независимый фактор риска послеоперационного снижения гемоглобина при I стадии рака желудка. J Gastroenterol Hepatol. 2015 Epub опережает печать. [PubMed] [Google Scholar] 58. Пэ Дж. М., Пак Дж. У., Ян Х. К., Ким Дж. П. Состояние питания больных раком желудка после тотальной гастрэктомии. Мир J Surg. 1998. 22: 254–260. обсуждение 260-261. [PubMed] [Google Scholar] 59. Окуда К. Открытие витамина B 12 в печени и фактора его абсорбции в желудке: исторический обзор.J Gastroenterol Hepatol. 1999; 14: 301–308. [PubMed] [Google Scholar] 60. Fischermann K, Harly S, Worning H, Zacho A. Функция поджелудочной железы и усвоение жира, железа, витамина B 12 и кальция после тотальной гастрэктомии при раке желудка. Кишечник. 1967. 8: 260–266. [Бесплатная статья PMC] [PubMed] [Google Scholar] 61. Брэдли Э.Л., Айзекс Дж. Пострезекционная анемия. Предотвратимое осложнение тотальной гастрэктомии. Arch Surg. 1976; 111: 844–848. [PubMed] [Google Scholar] 62. Адачи С., Кавамото Т., Оцука М., Тодороки Т., Фукао К.Энтерально витамин B 12 дополняет обратную постгастрэктомию B 12 дефицит. Ann Surg. 2000; 232: 199–201. [Бесплатная статья PMC] [PubMed] [Google Scholar] 63. Kim HI, Hyung WJ, Song KJ, Choi SH, Kim CB, Noh SH. Пероральная замена витамина B 12 : эффективное лечение дефицита витамина B 12 после тотальной гастрэктомии у пациентов с раком желудка. Энн Сург Онкол. 2011; 18: 3711–3717. [PubMed] [Google Scholar] 64. Гулло Л. Показания для лечения ферментами поджелудочной железы при непанкреатических заболеваниях пищеварительной системы.Пищеварение. 1993; 54 (приложение 2): 43–47. [PubMed] [Google Scholar] 65. Brägelmann R, Armbrecht U, Rosemeyer D, Schneider B, Zilly W., Stockbrügger R. Влияние добавок ферментов поджелудочной железы у пациентов со стеатореей после тотальной гастрэктомии. Eur J Gastroenterol Hepatol. 1999; 11: 231–237. [PubMed] [Google Scholar] 66. Винклер М.Ф., Смит К.Э. Клинические, социальные и экономические последствия зависимости от парентерального питания в домашних условиях при синдроме короткой кишки. JPEN J Parenter Enteral Nutr. 2014; 38 (доп.): 32С – 37С. [PubMed] [Google Scholar] 67.Рихтер Э., Денеке А., Клапдор С., Клапдор Р. Поддержка парентерального питания для пациентов с раком поджелудочной железы — улучшение нутритивного статуса и терапевтического результата. Anticancer Res. 2012; 32: 2111–2118. [PubMed] [Google Scholar] 68. Де Чикко М., Панарелло Г., Фантин Д., Веронези А., Пинто А., Загонель В., Монфардини С., Теста В. Парентеральное питание онкологических больных, получающих химиотерапию: влияние на токсичность и статус питания. JPEN J Parenter Enter Nutr. 1993; 17: 513–518. [PubMed] [Google Scholar] 69.Серру Б., Куписсоль Д., Плань Р., Бутен П., Шоле П., Каркассон И., Мишель Ф. Б. Последующее наблюдение за рандомизированным исследованием овсяноклеточной карциномы, оценивающим эффективность периферического внутривенного питания (PIVN) в качестве дополнительного лечения. Последние результаты Cancer Res. 1982; 80: 246–253. [PubMed] [Google Scholar] 70. Корец Р.Л., Липман Т.О., Кляйн С; Американская гастроэнтерологическая ассоциация. Технический обзор парентерального питания AGA. Гастроэнтерология. 2001; 121: 970–1001. [PubMed] [Google Scholar] 71. Ваши П.Г., Дальк С., Попил Б., Ламмерсфельд, Калифорния, Иретон-Джонс С., Гупта Д.Продольное исследование качества жизни и результатов питания у больных раком на поздних стадиях, получающих парентеральное питание в домашних условиях. BMC Рак. 2014; 14: 593. [Бесплатная статья PMC] [PubMed] [Google Scholar]Аденокарциномы пищевода и кардии желудка: заболевания, табак, алкоголь и социально-экономические факторы
Заболеваемость аденокарциномами пищевода и кардии желудка в западных странах за последние 10-15 лет увеличилась.Причина увеличения заболеваемости до сих пор неизвестна. Наше исследование было разработано для изучения потенциальных факторов риска аденокарциномы пищевода и кардии желудка, а также для сравнения профилей риска для группы пациентов с этим раком и пациентов с дистальным раком желудка. Мы изучили 95 случайных случаев с патологическим диагнозом аденокарциномы пищевода и кардии желудка, 67 пациентов с аденокарциномами дистального отдела желудка и 132 контрольной группы без рака. Пациенты наблюдались в Мемориальном онкологическом центре Слоуна-Кеттеринга с 1 ноября 1992 года по 1 ноября 1994 года.Эпидемиологические данные были собраны с помощью модифицированного опросника истории привычек Национального института рака. Факторы риска были проанализированы с использованием методов Mantel-Haenszel и модели логистической регрессии. Гипертония была связана с двукратным повышением риска аденокарциномы пищевода и кардии желудка после учета возраста, пола, расы, образования, количества лет курения, употребления алкоголя, индекса массы тела и общего количества калорий с пищей. Повышенный риск аденокарциномы пищевода и кардии желудка был связан с возрастом, мужским полом и европеоидной расой.Табакокурение было связано со умеренным риском аденокарциномы пищевода и кардии желудка. Напротив, риск рака дистального отдела желудка был связан с язвой желудка и годами курения сигарет. Дефицит железа был значительно связан с повышенным риском как аденокарцином пищевода и кардии желудка, так и аденокарцином дистального отдела желудка. Не было выявлено очевидных ассоциаций между профессиональным воздействием, семейным анамнезом рака и физической активностью.Это исследование предполагает, что такие заболевания, как гипертония и дефицит железа, могут быть связаны с риском развития аденокарциномы пищевода и кардии желудка, и подтверждает умеренный риск, связанный с курением табака. Наши результаты указали на этиологическую гетерогенность в отношении факторов риска, выявленных между аденокарциномами пищевода и кардии желудка и аденокарциномами дистального отдела желудка.
Питание пациентов с раком желудка: обновление — FullText — опухоли желудочно-кишечного тракта 2015, Vol.2, №4
Аннотация
Справочная информация: Управление питанием пациентов с раком желудка (РЖ) представляет собой сложную задачу. Резюме: В этом обзоре представлен обзор имеющихся данных о нутритивной поддержке у пациентов с ГК, перенесших операцию, а также у пациентов с запущенным заболеванием. Ключевое сообщение: Для пациентов, перенесших операцию, предоперационное состояние питания напрямую влияет на послеоперационный прогноз, общую выживаемость и выживаемость при конкретном заболевании.Периоперационная нутритивная поддержка, обогащенная иммуностимулирующими питательными веществами, снижает общие осложнения и время пребывания в больнице, но не смертность после обширных плановых операций на желудочно-кишечном тракте. Раннее энтеральное питание после операции улучшает состояние питания в раннем и отдаленном послеоперационном периоде, а также сокращает продолжительность госпитализации. Витамин B 12 и дефицит железа являются частыми метаболическими последствиями после гастрэктомии и требуют соответствующей замены. У истощенных пациентов с поздними стадиями ГК краткосрочное домашнее дополнительное парентеральное питание улучшает качество жизни, нутритивный статус и функциональный статус.Полное парентеральное питание в домашних условиях представляет собой единственный способ потребления калорий для пациентов с поздними стадиями ГК, которые не могут принимать пероральное или энтеральное питание. Практическое значение: Ранняя оценка нутритивного статуса и нутриционной поддержки представляют собой ключевые аспекты ведения пациентов с РЖ как с операбельным, так и с запущенным заболеванием.
© 2016 S. Karger AG, Базель
Введение
Несмотря на снижение заболеваемости за последние несколько десятилетий, рак желудка (РЖ) остается пятым по распространенности злокачественным новообразованием в мире и третьим по значимости причиной смерти от рака у обоих полов во всем мире [1].ГК часто протекает бессимптомно или может вызывать только неспецифические симптомы на ранних стадиях, что является одной из основных причин часто поздней диагностики [2] и относительно плохого прогноза [3].
Снижение веса отмечается у 31–87% пациентов при первом диагнозе злокачественного новообразования, и масштабы потери веса напрямую зависят от типа рака [4]. В частности, потеря веса> 10% в течение предыдущих 6 месяцев наблюдается у 15% пациентов с диагнозом гастроэзофагеальный рак, тогда как недоедание встречается у 80% пациентов с РЖ на поздней стадии [5,6].
Синдром анорексии-кахексии [7,8], обычно описываемый у пациентов с запущенным раком, характеризуется снижением потребления пищи, гипоальбуминемией, потерей веса и истощением мышечной ткани и связан с повышенной заболеваемостью и смертностью [9,10,11 ]. У пациентов с GC это состояние в основном вызвано обструкцией верхних отделов пищеварительного тракта из-за механического воздействия опухоли [12]. Могут последовать дисфагия, преждевременное насыщение, тошнота и рвота. У пациентов с ГК синдром анорексии-кахексии связан с сокращением общей выживаемости [13].Вместе с такими симптомами, как тошнота, рвота, преждевременное насыщение и дисфагия после химиотерапии, лучевой терапии или хирургического вмешательства, это состояние может способствовать недоеданию, связанному с раком [14,15,16]. Таким образом, выявление и лечение недостаточности питания на ранних этапах ГК имеет решающее значение для улучшения результатов лечения пациентов.
Диетологическое лечение
Целью диетотерапии является улучшение статуса питания, обмена веществ, приверженности к противоопухолевой терапии, качества жизни и течения заболевания [17].Нутритивная поддержка рекомендуется как пациентам с ГК, подвергшимся хирургическому вмешательству, так и пациентам с неоперабельным заболеванием, и может осуществляться пероральным, энтеральным (EN) и парентеральным (PN) питанием. Пероральное питание включает диету и пероральные добавки. После резекции желудка рекомендуется диета, основанная на частом приеме пищи небольшими порциями с ограничением простых углеводов, чтобы предотвратить демпинг-синдром. EN (питание в кишечнике) определяется по-разному и может включать диету, пероральные добавки и кормление через зонд.В настоящем обзоре ЭП определяется как питание через зонд и включает чрескожную эндоскопическую гастростомию, чрескожную радиологическую гастростомию и чрескожную эндоскопическую еюностомию. ЭН сохраняет структурную и функциональную целостность желудочно-кишечного тракта и представляет собой действенный вариант питания для пациентов с дисфагией или обструкцией, когда пероральный прием не удовлетворяет потребности в питании [18]. ЭП безопаснее, дешевле и физиологичнее ПП. Однако у пациентов с нарушением функции желудочно-кишечного тракта ПН является обязательным.Хотя PN (питание центральными и периферическими венами) обеспечивает оптимальное питание, оно увеличивает риск инфекций по сравнению с EN [19]. Инфекция кровотока, связанная с катетером, является наиболее частым и серьезным осложнением у взрослых пациентов, получающих PN. В систематическом обзоре 39 исследований общая частота инфицирования кровотока, связанного с катетером, варьировала от 0,4 до 4,6 эпизодов на 1000 катетер-дней (медиана 1,3) у пациентов с домашним PN (HPN) и в основном была связана с грамположительными бактериями кожная флора человека [20].Таким образом, при терминальной стадии болезни польза от нутритивной поддержки может быть ограничена и связана с повышенным риском осложнений. Как следствие, недавние немецкие рекомендации S3 рекомендуют нутритивную поддержку только в том случае, если преимущества преобладают над любыми возможными осложнениями или по желанию пациентов [17].
Оценка состояния питания
Оценка состояния питания, приема пищи и тяжести заболевания должна проводиться, начиная с первого контакта, на регулярной основе и через короткие промежутки времени (не реже, чем каждые 4-8 недель), чтобы распознать любой как можно более раннее снижение нутритивного статуса [17].Было разработано несколько анкет для раннего выявления и лечения недоедающих пациентов больниц [21,22]. В частности, повышение баллов по инструменту «Скрининг пищевых рисков 2002» (NRS 2002) связано с увеличением частоты послеоперационных осложнений и увеличением продолжительности пребывания в стационаре [23]. Кроме того, в недавнем исследовании, посвященном оценке эффективности Краткого вопросника оценки питания (SNAQ) в прогнозировании риска послеоперационной смертности после операции GC, оценка SNAQ ≥1 была связана с повышенным уровнем смертности по сравнению с оценкой SNAQ, равной 0 (ИЛИ = 5.1; 95% ДИ: 1,01–23,8) [24].
В недавнем ретроспективном исследовании 775 пациентов, перенесших гастрэктомию по поводу GC, только индекс массы тела (ИМТ) не повлиял на периоперационную заболеваемость, безрецидивную или общую выживаемость [25]. Однако у пациентов с ИМТ <18,5 и низким уровнем альбумина до операции значительно снизилась общая выживаемость после гастрэктомии.
Были предложены различные индексы для прогнозирования прогноза пациентов со злокачественными новообразованиями желудочно-кишечного тракта [26,27].В частности, прогностический индекс питания (ПНИ) получил широкое распространение благодаря его эффективности, простоте и удобству [28]. PNI рассчитывается по следующей формуле: 10 × значение сывороточного альбумина (г / дл) + 0,005 × количество лимфоцитов в периферической крови. Оценка <45 указывает на серьезное нарушение питания, тогда как PNI ≥45 связано с нормальным статусом питания. В недавнем метаанализе PNI был связан с глубиной инвазии и метастазами в лимфатические узлы в GC [29]. Сакураи и др.[30] показали, что у пациентов с ГК предоперационный PNI является независимым прогностическим фактором как для общей выживаемости, так и для выживаемости при конкретном заболевании. Примечательно, что пациенты с заболеванием UICC стадии 1 и 2 имели значительно худшие результаты в группе с низким PNI, чем в группе с высоким PNI. Подводя итог, можно сказать следующее:
• Предоперационная нутриционная поддержка может улучшить послеоперационный результат у пациентов, перенесших операцию по поводу GC
• Доступно несколько проверенных вопросников для раннего выявления и лечения истощенных пациентов больниц
• PNI, или комбинация предоперационного ИМТ <18.5 и низкий уровень альбумина, является прогностическим фактором снижения общей выживаемости после гастрэктомии
Предоперационное питание
Для пациентов, перенесших серьезную операцию, предоперационное недоедание связано с повышенной заболеваемостью (т. синдром) и смертность [31,32,33]. Таким образом, улучшение нутритивного статуса перед операцией может улучшить послеоперационный результат у пациентов с ГК.Немецкие рекомендации S3 рекомендуют нутритивную поддержку всем пациентам с недостаточным питанием [17]. Это состояние определяется как потребление пероральной пищи <500 ккал / день или ≤75% от потребности в течение более 1-2 недель [34]. В интактном желудочно-кишечном тракте ЭП так же эффективна, как и ПП [35]. ЭП можно проводить через назогастральный или назоэнтериальный зонд в течение коротких периодов времени, тогда как прямой доступ к кишечнику, например через еюностомию, должен быть предпочтительным, если ЭП вводится более 3 недель [36].Недавно рандомизированное контролируемое исследование (РКИ) с участием 106 пациентов, перенесших гастрэктомию по поводу ГК, продемонстрировало, что предоперационная ЭП улучшает послеоперационный нутритивный статус, уменьшает воспалительную реакцию и способствует выздоровлению пациентов [37]. Пациентам с нефункциональным или недоступным желудочно-кишечным трактом может потребоваться нутритивная поддержка через ПП [38].
Пероральное или энтеральное введение питательного раствора, обогащенного иммуностимулирующими питательными веществами (аргинин, ω-3 жирные кислоты и нуклеотиды), называется иммунным питанием (ИН) [39].В недавнем метаанализе 9 исследований иммунологическое влияние энтерального ИН было оценено у пациентов, перенесших операцию по поводу ГК [40]. По сравнению со стандартным EN, IN усиливает иммунитет хозяина за счет увеличения уровня иммуноглобулинов, Т-хелперов 17 и естественных клеток-киллеров и снижения уровня провоспалительных цитокинов, таких как IL-6 и TNF-α. В другом метаанализе, основанном на 21 РКИ, периоперационная ИН сравнивалась со стандартной ЭП у пациентов, перенесших обширные плановые операции на желудочно-кишечном тракте.Периоперационная ИН значительно снизила общие осложнения и продолжительность госпитализации, но не смертность [41]. Соответственно, ESPEN Guidelines, German S3 Guidelines [17] для GC и Североамериканский саммит по хирургическому питанию [42] рекомендуют пероральные / энтеральные IN для пациентов с раком верхних отделов желудочно-кишечного тракта за 5-7 дней до операции и в послеоперационный период. На рисунке 1 показан алгоритм доставки периоперационного питания у пациентов, перенесших операцию по поводу GC.
Фиг.1
Алгоритм выбора пути доставки периоперационного питания у пациентов, перенесших операцию по поводу GC. * Пероральный прием пищи <500 ккал / день или ≤75% от потребности в течение более 1-2 недель [17]. GI = желудочно-кишечный тракт; PEJ = чрескожная эндоскопическая нейностомия.
Независимо от статуса питания, группа улучшенного восстановления после операции (ERAS) недавно предоставила рекомендации по периоперационному комплексному ведению пациентов с опухолями верхних отделов желудочно-кишечного тракта.Они рекомендуют предоперационную углеводную нагрузку (800 мл напитка с 12,5% углеводов за ночь перед операцией и 400 мл на следующее утро за 2 часа до индукции анестезии), чтобы (1) снизить резистентность к инсулину и гликозилирование тканей, вызванное операцией. , (2) помогают в послеоперационном контроле уровня глюкозы и (3) поддерживают нормальную функцию кишечника [43]. Подводя итоги, можно констатировать следующее:
• Периоперационная ИН снижает общие осложнения и продолжительность госпитализации, но не снижает смертность после обширных плановых операций на желудочно-кишечном тракте
• Предоперационная углеводная нагрузка в ночь перед операцией снижает резистентность к инсулину и гликозилирование тканей, вызванное операцией , помогает в послеоперационном контроле уровня глюкозы и поддерживает нормальную функцию кишечника
Послеоперационное питание
Роль послеоперационной нутритивной поддержки заключается в поддержании нутритивного статуса в катаболический период после операции.В проспективном исследовании, оценивающем периоперационный статус питания 435 пациентов с ГК, распространенность тяжелого недоедания значительно увеличилась после операции (2,3 и 26,3% до и после операции, соответственно) [44]. Пожилой возраст, предоперационная потеря веса и открытая операция были определены как факторы риска тяжелой послеоперационной недостаточности питания.
После хирургического лечения снижение аппетита и диеты во время выздоровления и восстановление нутритивного статуса может занять до 1 года [45].Функции тонкого кишечника восстанавливаются между 6 и 12 часами после операции, что указывает на то, что в это время можно начать поддержку ЭП. В соответствии с этим представлением, исследование Gabor et al. [46] показали, что через 6 ч после операции можно начинать ЭП. Соответственно, пациенты, перенесшие операцию на верхних отделах желудочно-кишечного тракта, обычно получают чрескожную еюностомическую трубку для послеоперационной ЭП, которую можно продолжить также после выписки в зависимости от потребностей пациента. Раннее пероральное питание после операции по поводу ГК также безопасно и не увеличивает частоту послеоперационных осложнений по сравнению с ЭП через назогастральный зонд [47].В РКИ с участием 105 пациентов, перенесших операцию по поводу рака желудочно-кишечного тракта, ранняя послеоперационная нутритивная поддержка снизила высокий метаболизм, связанный с хирургической травмой, поддержала функцию слизистого барьера кишечника и снизила частоту кишечных инфекций, улучшив выздоровление пациентов [48] . Периоперационное питание эффективно снижает частоту послеоперационных осложнений у истощенных пациентов с РЖ. В другом РКИ 468 пациентов с умеренной или тяжелой недостаточностью питания с ГК или колоректальным раком были случайным образом распределены на 7-дневное предоперационное и 7-дневное послеоперационное искусственное питание (ЭП или ПП) и сравнивались с простой контрольной группой.Среди пациентов, получавших периоперационное питание, наблюдалось двукратное снижение послеоперационных осложнений и трехкратное снижение смертности. Наиболее резко снизилось количество серьезных септических осложнений (14,9 против 27,9%, p = 0,011), таких как пневмония и раневая инфекция [49]. Общая продолжительность госпитализации и послеоперационного пребывания в контрольной группе была значительно больше (29 против 22 дней, p = 0,014), чем у исследуемых пациентов. В заключение можно сказать следующее:
• ЭН можно безопасно начать через 6 часов после операции через чрескожную еюностомическую трубку
• Раннее послеоперационное питание снижает высокий метаболизм, связанный с хирургической травмой, поддерживает функцию слизистого барьера кишечника и снижает частота кишечных инфекций, улучшение выздоровления пациентов
Пищевые добавки после гастрэктомии
Анемия является частым осложнением после гастрэктомии, и после хирургических вмешательств на желудке сообщалось о дефиците железа, витамина B 12 или фолиевой кислоты.Анемия развивается у 50% пациентов, перенесших тотальную резекцию желудка [50]. Плохой статус питания и пониженное потребление железа с пищей могут привести к истощению запасов железа после операции на желудке [51]. Повышенное истощение запасов железа также может быть результатом желудочно-кишечной кровопотери в месте анастомоза [52] или избыточного бактериального роста в слепых петлях [53]. Однако изменения в пищеварении и нарушение всасывания железа считаются ведущими факторами, способствующими дефициту железа после гастрэктомии [54]. Нарушение всасывания пищевого железа, возможно, является результатом снижения секреции желудочной кислоты и обхода двенадцатиперстной кишки.Пониженная кислотность желудочного сока ухудшает превращение негемового железа (Fe 3+ ) в более усваиваемую форму двухвалентного железа (Fe 2+ ) [55]. Реконструкция после резекции желудка может снизить абсорбцию железа из-за обхода основных участков абсорбции железа: двенадцатиперстной кишки и проксимального отдела тощей кишки.
В ретроспективном исследовании 119 пациентов, перенесших дистальную гастрэктомию с реконструкциями по Бильроту I или Roux-en-Y для стадии I GC, одномерный и многомерный анализ показал, что реконструкция Roux-en-Y является единственным фактором риска (p = 0 .0487; ИЛИ = 2,755; 95% ДИ: 1,01–7,91) для снижения гемоглобина [56]. Сообщалось также о более высокой частоте анемии и дефицита железа после тотальной гастрэктомии по сравнению с субтотальной гастрэктомией [57].
Лечение железодефицитной анемии после гастрэктомии требует коррекции дефицита циркулирующего гемоглобина, восполнения дефицита накопления и коррекции любого излечимого источника аномальной кровопотери. Также обычно эффективно профилактическое лечение ожидаемого дефицита простыми препаратами в форме сульфата железа или глюконата [17].
Дефицит витамина B 12 может развиться уже через 1 год после тотальной резекции желудка [58]. Внутренний фактор, который в основном продуцируется париетальными клетками кислородных желез желудка, необходим для энтерального поглощения витамина B 12 [59]. Fischermann et al. [60] показали, что тип реконструкции не влияет на всасывание витамина B 12 . Таким образом, прохождение пищи через двенадцатиперстную кишку не является необходимым для энтерального всасывания витамина B 12 . Однако клинические проявления дефицита витамина B 12 после гастрэктомии не были четко определены, а роль дополнительной терапии витамином B 12 не была стандартизирована.В немецком руководстве S3 [17] после операции рекомендуется принимать добавки с витамином B 12 . Введение витамина B 12 эффективно как подкожно, так и перорально [61]. Действительно, в исследовании Adachi et al. [62] пероральный прием витамина B 12 был эффективным в увеличении концентрации витамина B 12 в сыворотке с быстрым исчезновением симптомов, связанных с дефицитом витамина B 12 . Kim et al. [63] продемонстрировали, что пероральная заместительная терапия витамином B 12 обеспечивает безопасное и эффективное лечение дефицита витамина B 12 после тотальной гастрэктомии у пациентов с РЖ.Обоснованием этого подхода является наличие второй, менее эффективной транспортной системы для витамина B 12 , которая не требует внутреннего фактора или функционирующего терминального отдела подвздошной кишки, но использует пассивную диффузию. Таким образом, профилактическое энтеральное введение витамина B 12 после тотальной гастрэктомии является хорошей и удобной альтернативой подкожному пути для предотвращения симптомов, связанных с дефицитом витамина B 12 .
Недостаточность поджелудочной железы была предложена как возможная причина мальабсорбции после тотальной гастрэктомии [64].Хотя внешнесекреторная недостаточность поджелудочной железы была продемонстрирована после гастрэктомии, ключевым вопросом остается вопрос о том, могут ли добавки ферментов поджелудочной железы улучшить клинический результат у пациентов с РЖ. В проспективном двойном слепом рандомизированном параллельном плацебо-контролируемом многоцентровом исследовании добавление ферментов поджелудочной железы не привело к значительным различиям между плацебо и группой, получавшей ферменты, в отношении привычек кишечника или недостаточной ассимиляции жира [65]. Влияние высоких доз ферментов поджелудочной железы на симптомы и стеаторею после тотальной гастрэктомии было незначительным и не оправдывало рутинного использования.Таким образом, можно сказать следующее:
• Анемия развивается у 50% пациентов, перенесших тотальную резекцию желудка
• Нарушение всасывания пищевого железа из-за снижения секреции желудочного сока и обхода двенадцатиперстной кишки является основной причиной анемии после гастрэктомия
• Лечение железодефицитной анемии требует коррекции дефицита циркулирующего гемоглобина, восполнения дефицита накопления и коррекции любого излечимого источника аномальной кровопотери
• Дефицит витамина B 12 может развиться уже в 1 год после тотальной гастрэктомии
• Текущие руководства рекомендуют добавление витамина B 12 после гастрэктомии
• Влияние высоких доз ферментов поджелудочной железы на симптомы и стеаторею после тотальной гастрэктомии незначительно и не оправдывает рутинного использования
Питание у пациентов с Advanced GC
Каждый раз, когда показана нутритивная поддержка пероральный и энтеральный пути предпочтительнее парентерального.У пациентов с ГК со стенозом кардии или привратника установка стента может позволить оральное питание, улучшающее качество жизни. Руководства Европейского общества клинического питания и метаболизма рекомендуют применение ПП, когда «можно ожидать неадекватного приема пищи менее 60% от расчетного потребления энергии в течение более десяти дней» [19]. Пациентам, получающим химиотерапию, у которых наблюдаются связанные с химиотерапией побочные эффекты со стороны желудочно-кишечного тракта (например, анорексия, тошнота, рвота, запор и диарея), рекомендуется дополнительная HPN для стабилизации веса и продолжения терапии [17].Кроме того, исходя из нашего опыта, краткосрочная дополнительная HPN может быть безопасно и эффективно предоставлена пациентам с потерей веса, несмотря на адекватное пероральное потребление или пероральные добавки (например, раковая кахексия), а также в случаях непереносимости EN (например, тошнота, боль в животе и понос).
Для пациентов с карцинозом брюшины и тяжелым нарушением функции желудочно-кишечного тракта обязательна общая HPN [15]. Синдром короткой кишки из-за обширного хирургического вмешательства является еще одним показанием для HPN [66].Успех ПП зависит от соблюдения пациентом режима лечения, поддержки со стороны профессионального и преданного диетолога и сотрудничества между пациентом, диетологом, врачом и поставщиком медицинских услуг на дому [67]. В многочисленных исследованиях PN не удалось снизить токсичность химиотерапии [68] и улучшить скорость ответа [69]. Особенно для пациентов с поздними стадиями ГК и для тех, кто не страдает от истощения или гипофагии, риски ПП могут перевешивать преимущества [70]. С другой стороны, у пациентов с прогрессирующим раком и недостаточностью питания средней и тяжелой степени HPN улучшает качество жизни, пищевой статус и функциональный статус независимо от типа опухоли [71].Наибольший эффект был отмечен у пациентов, получавших дополнительную HPN в течение 3 месяцев, хотя пациенты, получавшие HPN в течение 1 или 2 месяцев, также продемонстрировали значительные улучшения. Подводя итог, можно констатировать следующее:
• Для пациентов с поздними стадиями ГК, которые не могут принимать пероральное питание или ЭП, обязательна полная ХПН. PN может перевесить преимущества
• У истощенных пациентов с распространенным раком краткосрочная дополнительная HPN связана с улучшением качества жизни, нутритивного статуса и функционального статуса
Будущие направления
Современная терапия пациентов с локализованным ГК, подходящая для хирургия включает неоадъювантную радиохимиотерапию и периоперационную химиотерапию, которые представляют собой источники катаболического стресса и недоедания.Роль нутритивной поддержки во время неоадъювантного / периоперационного лечения пациентов с РЖ еще предстоит определить. В Европе в рамках контролируемого исследования фазы III в настоящее время проверяется, может ли ИН улучшить качество жизни пациентов, получавших неоадъювантную радиохимиотерапию и периоперационную химиотерапию при раке пищевода и желудка (NCT01423799).
Заявление о раскрытии информации
R.R., C.C., P.M. и М.В. нечего раскрывать.
Список литературы
- Международное агентство по изучению рака: GLOBOCAN 2012: оценка заболеваемости, смертности и распространенности рака во всем мире в 2012 году.http://globocan.iarc.fr/Pages/fact_sheets_cancer.aspx.
- Wadhwa R, Taketa T, Sudo K, Blum MA, Ajani JA: Современные онкологические подходы к аденокарциноме желудка. Gastroenterol Clin North Am 2013; 42: 359-369.
- Cancer Research UK: Статистика и перспективы рака желудка.2014. http://www.cancerresearchuk.org/about-cancer/type/stomach-cancer/treatment/statistics-and-outlook-for-stomach-cancer.
- Гупта Д., Лис К. Г., Граник Дж., Груч Дж. Ф., Ваши П. Г., Ламмерсфельд К. А.: Недоедание было связано с низким качеством жизни при колоректальном раке: ретроспективный анализ.J Clin Epidemiol 2006; 59: 704-709.
- Deans DA, Tan BH, Wigmore SJ, Ross JA, de Beaux AC, Paterson-Brown S, Fearon KCD: Влияние системного воспаления, диетического питания и стадии заболевания на скорость потери веса у пациентов с раком желудочно-пищеводного тракта. Br J Cancer 2009; 100: 63-69.
- Раваско П., Монтейро-Грилло И., Видаль П.М., Камило М.Э .: Рак: болезнь и питание являются ключевыми определяющими факторами качества жизни пациентов. Поддержите лечение рака 2004; 12: 246-252.
- Deans C, Wigmore S: Системное воспаление, кахексия и прогноз у больных раком.Курр Опин Clin Nutr Metab Care 2005; 8: 265-269.
- фон Хелинг С., Анкер С.Д .: Кахексия как серьезная недооцененная и неудовлетворенная медицинская потребность: факты и цифры. J Cachexia Sarcopenia Muscle 2010; 1: 1-5.
- Фирон К., Штрассер Ф., Анкер С.Д., Босэус I, Брюра Э., Файнсингер Р.Л., Ятой А., Лопринци К., Макдональд Н., Мантовани Дж., Дэвис М., Мускаритоли М., Оттери Ф, Радбрух Л., Раваско П., Уолш Д., Уилкок А. , Kaasa S, Baracos VE: Определение и классификация раковой кахексии: международный консенсус.Ланцет Онкол 2011; 12: 489-495.
- Тан CR, Yaffee PM, Jamil LH, Lo SK, Nissen N, Pandol SJ, Tuli R, Hendifar AE: кахексия рака поджелудочной железы: обзор механизмов и терапии. Front Physiol 2014; 5: 88.
- Эванс В.Дж., Морли Дж. Э., Аргилес Дж., Бейлс С., Баракос В., Гаттридж Д., Ятой А., Калантар-Заде К., Лохс Х., Мантовани Дж., Маркс Д., Митч В.Е., Мускаритоли М., Наджанд А., Пониковски П., Росси Фанелли Ф. , Шамбелан М., Схолс А., Шустер М., Томас Д., Вулф Р., Анкер С.Д.: Кахексия: новое определение.Clin Nutr 2008; 27: 793-799.
- Донохо С., Райан А., Рейнольдс Дж. Раковая кахексия: механизмы и клинические последствия. Гастроэнтерол Рес Прак 2011; 2011: 601434.
- Dewys WD, Begg C, Lavin PT, Band PR, Bennett JM, Bertino JR, Cohen MH, Douglass HO Jr, Engstrom PF, Ezdinli EZ, Horton J, Johnson GJ, Moertel CG, Oken MM, Perlia C, Rosenbaum C, Silverstein MN, Skeel RT, Sponzo RW, Tormey DC: Прогностический эффект потери веса до химиотерапии у онкологических больных.Восточная кооперативная онкологическая группа. Am J Med 1980; 69: 491-497.
- Тонг Х., Изенринг Э., Йетс П.: Распространенность симптомов воздействия питания и их связь с качеством жизни и клиническими исходами у онкологических пациентов. Поддержка лечения рака 2009; 17: 83-90.
- Шахморади Н., Кандиа М., Пэн Л.: Влияние статуса питания на качество жизни больных раком на поздних стадиях при уходе на дому в хосписе.Азиатский Pac J Cancer Prev 2009; 10: 1003-1009.
- Ван Катсем Э., Арендс Дж .: Причины и последствия недоедания, связанного с раком. Eur J Oncol Nurs 2005; 9 (приложение 2): S51-S63.
- Арендс Дж., Бертц Х., Бишофф С. К., Фиткау Р., Херрманн Х. Дж., Хольм Э., Хорнебер М., Хюттерер Э., Кербер Дж., Шмид И.; Руководящий комитет DGEM: S3-Руководство Немецкого общества диетологии (DGEM).Aktuelle Ernahrungsmed 2015; 40: 1-74.
- Вейманн А., Брага М., Харшани Л., Лавиано А., Юнгквист О., Соетерс П.; DGEM (Немецкое общество диетологии), Jauch KW, Kemen M, Hiesmayr JM, Horbach T., Kuse ER, Vestweber KH; ESPEN (Европейское общество парентерального и энтерального питания): Руководство ESPEN по энтеральному питанию: хирургия, включая трансплантацию органов.Clin Nutr 2006; 25: 224-244.
- Бозцетти Ф., Арендс Дж., Лундхольм К., Миклрайт А., Цурчер Дж., Мускаритоли М.; ESPEN: Руководство ESPEN по парентеральному питанию: нехирургическая онкология. Clin Nutr 2009; 28: 445-454.
- Dreesen M, Foulon V, Spriet I, Goossens G, Hiele M, De Pourcq L, Willems L: Эпидемиология катетерных инфекций у взрослых пациентов, получающих парентеральное питание в домашних условиях: систематический обзор.Clin Nutr 2013; 32: 16-26.
- Kruizenga H, Seidell J, de Vet H, Wierdsma N, van Bokhorst-de van der Schueren MA: Разработка и валидация больничного скринингового инструмента для выявления недоедания: краткая анкета для оценки питания (SNAQ ©). Clin Nutr 2005; 24: 75-82.
- van Venrooij LM, van Leeuwen PA, Hopmans W, Borgmeijer-Hoelen MM, de Vos R, De Mol BA: Точность быстрых и простых инструментов скрининга недостаточности питания — Краткая анкета оценки питания, Универсальный инструмент скрининга недоедания и модифицированный Универсальный инструмент скрининга недоедания — у пациентов, перенесших кардиохирургические операции.J Am Diet Assoc 2011; 111: 1924-1930.
- Guo W, Ou G, Li X, Huang J, Liu J, Wei H: Скрининг пищевого риска у пациентов с карциномой желудка перед операцией NRS 2002 и его связь с послеоперационными результатами. J Gastroenterol Hepatol 2010; 25: 800-803.
- Тегельс Дж., Де Маат М., Хулсеве К., Хофвейк А., Стоот Дж .: Значение гериатрической слабости и оценки нутритивного статуса в прогнозировании послеоперационной смертности при хирургии рака желудка.Журнал Gastrointest Surg 2014; 18: 439-445.
- Ejaz A, Spolverato K, Poultsides G, Fields R, Bloomston M, Cho C, Votanopoulos K, Maithel S, Pawlik T: Влияние индекса массы тела на периоперационные исходы и выживаемость после резекции по поводу рака желудка. J Surg Res 2015; 195: 74-82.
- Ашер В., Ли Дж., Иннама А. Предоперационное соотношение лимфоцитов тромбоцитов как независимый прогностический маркер рака яичников.Клин Транс Онкол 2011; 13: 499-503.
- Чуа В., Чарльз К.А., Баракос В.Е., Кларк С.Дж.: Соотношение нейтрофилов / лимфоцитов позволяет прогнозировать результаты химиотерапии у пациентов с распространенным колоректальным раком. Br J Cancer 2011; 104: 1288-1295.
- Онодера Т., Госеки Н., Косаки Г.: Прогностический индекс питания в желудочно-кишечной хирургии больных раком, страдающих от недоедания (на японском языке).Нихон Гека Гаккаи Засси 1984; 85: 1001-1005.
- Nozoe T, Ninomiya M, Maeda T., Matsukuma A, Nakashima H, Ezaki T: Прогностический индекс питания: инструмент для прогнозирования биологической агрессивности рака желудка. Surg Today 2010; 40: 440-443.
- Сакураи К., Охира М., Тамура Т., Тойокава Т., Амано Р., Кубо Н., Танака Х, Мугурума К., Яширо М., Маэда К., Хиракава К.: Прогностический потенциал предоперационного статуса питания в долгосрочных прогнозах исходов для пациентов с раком желудка .Энн Сург Онкол 2016; 23: 525-533.
- Рей-Ферро М., Кастаньо Р., Ороско О, Серна А., Морено А. Нутритивная и иммунологическая оценка пациентов с раком желудка до и после операции. Питание 1997; 13: 878-881.
- Сунгуртекин Х., Сунгуртекин У., Бальчи С., Зенцир М., Эрдем Э. Влияние нутритивного статуса на осложнения после обширной интраабдоминальной хирургии.J Am Coll Nutr 2004; 23: 227-232.
- Кузу М.А., Терзиоглу Х., Генч В., Эркек А.Б., Озбан М., Сонюрек П., Эльхан А.Х., Торун Н.: Предоперационная оценка риска питания при прогнозировании послеоперационного исхода у пациентов, перенесших серьезную операцию. Мировой журнал J Surg 2006; 30: 378-390.
- Арендс Дж., Бодоки Дж., Бозцетти Ф., Фирон К., Мускаритоли М., Селга Дж., Ван Бокхорст-де ван дер Шуерен М. А., фон Мейенфельдт М; DGEM (Немецкое общество диетологии), Zürcher G, Fietkau R, Aulbert E, Frick B, Holm M, Kneba M, Mestrom HJ, Zander A; ESPEN (Европейское общество парентерального и энтерального питания): Руководство ESPEN по энтеральному питанию: нехирургическая онкология.Clin Nutr 2006; 25: 245-259.
- Бозцетти Ф: Нутриционная поддержка пациентов с раком пищевода. Поддержка лечения рака 2010; 18: S41-S50.
- Мариетт С., Де Боттон М., Писсен Г. Хирургия у пациентов с раком пищевода и желудка: какова роль нутритивной поддержки в вашей повседневной практике? Энн Сург Онкол 2012; 19: 2128-2134.
- Ding D, Feng Y, Song B, Gao S, Zhao J: Влияние предоперационного и послеоперационного энтерального питания на послеоперационный статус питания и иммунную функцию пациентов с раком желудка. Turk J Gastroenterol 2015; 26: 181-185.
- Липман Т .: Зерна или вены: действительно ли энтеральное питание лучше парентерального? Посмотрите на доказательства.JPEN J Parenter Enteral Nutr 1998; 22: 167-182.
- Heyland DK, Novak F, Drover JW, Jain M, Su X, Suchner U: Должно ли иммунное питание стать обычным делом для тяжелобольных пациентов? Систематический обзор доказательств. JAMA 2001; 286: 944-953.
- Серантола Ю., Хюбнер М., Грасс Ф., Демартинес Н., Шефер М.: Иммунное питание в желудочно-кишечной хирургии.Br J Surg 2011; 98: 37-48.
- Gianotti L, Braga M, Nespoli L, Radaelli G, Beneduce A, Di Carlo V: рандомизированное контролируемое исследование предоперационных пероральных добавок со специальной диетой у пациентов с раком желудочно-кишечного тракта. Гастроэнтерология 2002; 122: 1763-1770.
- McClave SA, Kozar R, Martindale RG, Heyland DK, Braga M, Carli F, Drover JW, Flum D, Gramlich L, Herndon DN, Ko C, Kudsk KA, Lawson CM, Miller KR, Taylor B, Wischmeyer PES: Итоговые баллы и согласованные рекомендации Североамериканского саммита по хирургическому питанию.JPEN J Parenter Enteral Nutr 2013; 37 (доп.): 99S-105S.
- Мариетт К. Роль нутритивной поддержки в программе ERAS. J Visc Surg 2015; 152 (приложение 1): S18-S20.
- Shim H, Cheong JH, Lee KY, Lee H, Lee JG, Noh SH: Периоперационные изменения нутритивного статуса у пациентов с раком желудочно-кишечного тракта.Йонсей Мед Журнал 2013; 54: 1370-1376.
- Ryu SW, Kim IH: Сравнение различных оценок питания при выявлении недоедания у пациентов с раком желудка. Всемирный журнал J Gastroenterol 2010; 16: 3310-3317.
- Gabor S, Renner H, Matzi V, Ratzenhofer B, Lindenmann J, Sankin O, Pinter H, Maier A, Smolle J, Smolle-Jüttner FM: раннее энтеральное питание по сравнению с парентеральным питанием после резекции и реконструкции пищевода или пищеводно-желудочного сока.Br J Nutr 2005; 93: 509-513.
- Hur H, Si Y, Kang WK, Kim W, Jeon HM: Влияние раннего перорального кормления на хирургические результаты и восстановление после лечебной операции по поводу рака желудка: результаты пилотного исследования. Мировой журнал J Surg 2009; 33: 1454-1458.
- Хуан Д., Сунь З., Хуанг Дж., Шен З .: Раннее энтеральное питание в сочетании с парентеральным питанием у пожилых пациентов после операции из-за рака желудочно-кишечного тракта.Int J Clin Exp Med 2015; 15: 13937-13945.
- Wu GH, Liu ZH, Wu ZH, Wu ZG: Периоперационное искусственное питание у истощенных пациентов с раком желудочно-кишечного тракта. Всемирный журнал J Gastroenterol 2006; 12: 2441-2444.
- Kelly WD, MacLean LD, Perry JF, Wangensteen OH: исследование пациентов после тотальной и почти тотальной гастрэктомии.Хирургия 1953; 35: 964-982.
- Хайнс Дж. Д., Хоффбранд А. В., Моллин Д. Л.: Гематологические осложнения после частичной гастрэктомии. Обследовано 292 пациента. Am J Med 1967; 43: 555-569.
- Kimber C, Patterson JF, Weintraub LR: Патогенез железодефицитной анемии после частичной гастрэктомии.Исследование баланса железа. JAMA 1967; 202: 935-938.
- Тоскес П.П.: Гематологические аномалии после резекции желудка. Майор Пробл Clin Surg 1976; 20: 119-128.
- Тови Ф, Кларк С: Анемия после частичной гастрэктомии: запущенное излечимое состояние.Ланцет 1980; 1: 956-958.
- Муньос М., Вильяр I, Гарсия-Эрсе Х.А.: Обновленная информация о физиологии железа. Всемирный журнал J Gastroenterol 2009; 15: 4617-4626.
- Имамура Т., Комацу С., Итикава Д., Косуга Т., Окамото К., Кониси Х., Сиодзаки А., Фудзивара Х., Оцудзи Е. Метод реконструкции как независимый фактор риска послеоперационного снижения гемоглобина при раке желудка I стадии.J Gastroenterol Hepatol 2015, Epub перед печатью.
- Geokas M, McKenna RD: Железодефицитная анемия после частичной гастрэктомии. Can Med Assoc J 1967; 96: 411-417.
- Bae JM, Park JW, Yang HK, Kim JP: Состояние питания пациентов с раком желудка после тотальной гастрэктомии.World J Surg 1998; 22: 254-260; обсуждение 260-261.
- Окуда К: открытие витамина B 12 в печени и его фактора абсорбции в желудке: исторический обзор. J. Gastroenterol Hepatol 1999; 14: 301-308.
- Fischermann K, Harly S, Worning H, Zacho A: Функция поджелудочной железы и усвоение жира, железа, витамина B 12 и кальция после тотальной гастрэктомии при раке желудка.Gut 1967; 8: 260-266.
- Брэдли Э.Л., Исаакс Дж .: Пострезекционная анемия. Предотвратимое осложнение тотальной гастрэктомии. Arch Surg 1976; 111: 844-848.
- Адачи С., Кавамото Т., Оцука М., Тодороки Т., Фукао К. Энтеральный витамин B 12 дополняет обратную постгастрэктомию B 12 дефицит.Энн Сург 2000; 232: 199-201.
- Kim HI, Hyung WJ, Song KJ, Choi SH, Kim CB, Noh SH: Пероральная замена витамина B 12 : эффективное лечение дефицита витамина B 12 после тотальной гастрэктомии у пациентов с раком желудка. Энн Сург Онкол 2011; 18: 3711-3717.
- Gullo L: Показания для лечения ферментами поджелудочной железы при заболеваниях пищеварительной системы, отличных от поджелудочной железы. Пищеварение 1993; 54 (приложение 2): 43-47.
- Brägelmann R, Armbrecht U, Rosemeyer D, Schneider B, Zilly W., Stockbrügger R: Влияние добавок ферментов поджелудочной железы у пациентов со стеатореей после тотальной гастрэктомии.Eur J Gastroenterol Hepatol 1999; 11: 231-237.
- Винклер М.Ф., Смит К.Э .: Клинические, социальные и экономические последствия зависимости от парентерального питания в домашних условиях при синдроме короткой кишки. JPEN J Parenter Enteral Nutr 2014; 38 (доп.): 32S-37S.
- Рихтер Э., Денеке А., Клапдор С., Клапдор Р.: Поддержка парентерального питания для пациентов с раком поджелудочной железы — улучшение состояния питания и терапевтического результата.Anticancer Res 2012; 32: 2111-2118.
- Де Чикко М., Панарелло Г., Фантин Д., Веронези А., Пинто А., Загонель В., Монфардини С., Тест V: Парентеральное питание онкологических больных, получающих химиотерапию: влияние на токсичность и статус питания. JPEN J Parenter Enter Nutr 1993; 17: 513-518.
- Serrou B, Cupissol D, Plagne R, Boutin P, Chollet P, Carcassonne Y, Michel FB: продолжение рандомизированного исследования овсяноклеточной карциномы, оценивающее эффективность периферического внутривенного питания (PIVN) в качестве дополнительного лечения. Недавние результаты Cancer Res 1982; 80: 246-253.
- Корец Р.Л., Липман Т.О., Кляйн С; Американская гастроэнтерологическая ассоциация: технический обзор парентерального питания AGA.Гастроэнтерология 2001; 121: 970-1001.
- Vashi PG, Dahlk S, Popiel B, Lammersfeld CA, Ireton-Jones C, Gupta D: продольное исследование, посвященное изучению качества жизни и исходов питания у больных раком на поздних стадиях, получающих парентеральное питание на дому. BMC Рак 2014; 14: 593.
Автор Контакты
Проф. Д-р Петер Мальфертхайнер
Отделение гастроэнтерологии, гепатологии и инфекционных заболеваний
Университет Отто-фон-Герике Магдебург, Лейпцигер-штрассе 44
DE-39120 Магдебург (Германия)
E-Mail [email protected]
Подробности статьи / публикации
Предварительный просмотр первой страницы
Получено: 3 марта 2016 г.
Принято: 3 марта 2016 г.
Опубликовано в Интернете: 13 апреля 2016 г.
Дата выпуска: май 2016 г.
Количество страниц для печати: 10
Количество рисунков: 1
Количество столов: 0
ISSN: 2296-3774 (печатный)
eISSN: 2296-3766 (онлайн)
Для дополнительной информации: https: // www.karger.com/GAT
Авторские права / Дозировка препарата / Заявление об ограничении ответственности
Авторские права: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование, или какой-либо системой хранения и поиска информации, без письменного разрешения издателя. .
Дозировка лекарств: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор и дозировка лекарств, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, ввиду продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новое и / или редко применяемое лекарство.
Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор (-ы) не несут ответственности за любой ущерб, причиненный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в контенте или рекламе.
младенцев срыгивают — в большинстве случаев нормально
Español
Любой, кто когда-либо ухаживал за младенцем, знает, что младенцы срыгивают.И срыгнул. А потом снова срыгнул.
Легко понять, почему обеспокоены некоторые родители и другие опекуны. Достаточно ли питания ребенок? Является ли частое срыгивание признаком более серьезного заболевания? Нужны ли ребенку лекарства для лечения проблемы?
По словам Эндрю Э. Мулберга, доктора медицины, педиатра и детского гастроэнтеролога Управления по контролю за продуктами и лекарствами (FDA), частые срыгивания в большинстве случаев являются абсолютно нормальным явлением и не являются признаком плохого состояния здоровья.По его словам, пока ребенок бодр, достаточно доволен, набирает вес и не проявляет других признаков болезни.
Так что же заставляет ребенка так часто возвращаться к еде?
У младенцев мышечное кольцо между пищеводом и желудком — нижний сфинктер пищевода (LES) — не полностью созрело, что позволяет содержимому желудка течь назад, объясняет Mulberg. Со временем LES созреет и откроется только тогда, когда ребенок проглотит, и будет оставаться плотно закрытым все остальное время, сохраняя содержимое желудка на своем месте.
«К тому времени, когда ребенку исполнится 18 месяцев или меньше, проблема, известная как гастроэзофагеальный рефлюкс (ГЭР), обычно проходит сама собой», — говорит Малберг.
В небольшом количестве случаев может иметь место более серьезное заболевание, известное как ГЭРБ (гастроэзофагеальная рефлюксная болезнь). ГЭРБ также может вызывать чрезмерную срыгивание, но требует лечения, чтобы избежать дополнительных осложнений со здоровьем, таких как повреждение тканей слизистой оболочки пищевода. По словам Мюлберга, следует немедленно проконсультироваться со специалистом в области здравоохранения, если у ребенка проявляются такие симптомы, как срыгивание крови, кровь в стуле, потеря веса, задержка развития, в том числе отсутствие набора веса и постоянный кашель или хрипы.
PPI: да или нет?
Многие родители достаточно обеспокоены, чтобы попробовать лекарства, отпускаемые без рецепта (OTC), включая ингибиторы протонной помпы (ИПП), такие как Prilosec. ИПП работают за счет уменьшения количества желудочной кислоты, вырабатываемой железами, выстилающими слизистую оболочку желудка, и часто используются взрослыми для лечения ГЭРБ, широко известной как изжога.
Однако ИПП, продаваемые без рецепта, не одобрены FDA для лечения рефлюкса у младенцев, говорит Мулберг.
Консультативный комитет FDA собрался в ноябре 2010 года для обсуждения четырех клинических испытаний, посвященных изучению эффектов лечения ГЭРБ младенцев с помощью ИПП.Комитет пришел к выводу, что ИПП не следует назначать в качестве терапии для здоровых детей младше 1 года, говорит Мулберг, если нет доказательств эрозии тканей пищевода.
Что касается того, какие лекарства могут понадобиться, а какие нет, это решение должен принять медицинский работник после проведения тщательного медицинского осмотра. Малберг предлагает родителям быть готовыми обсудить детальное поведение ребенка во время еды, а также общее настроение ребенка.Перед приемом родители должны быть готовы ответить на такие вопросы, как:
- Срыгивает ли ребенок при каждом кормлении?
- Сколько жидкости срыгивает ребенок?
- Вы кормите грудью?
- Если вы не кормите грудью, какую смесь вы используете?
- Вы недавно меняли формулы?
Способы справиться с нормальным срыгиванием
После того, как медицинский работник исключил более серьезное заболевание, родители и другие лица, осуществляющие уход, могут предпринять ряд мер, чтобы предотвратить постоянное срыгивание младенцев.К ним относятся:
- Держите ребенка в вертикальном положении во время кормления.
- Кормление ребенка небольшими порциями за раз.
- Переход на другую формулу.
«Понятно, почему молодые родители особенно обеспокоены, когда кажется, что их ребенок срыгивает безостановочно», — говорит Малберг. «Как правило, родители тоже изрядно недосыпают, что не помогает ситуации».
к началу
Большая внутрибрюшная грыжа пищеводного отверстия диафрагмы как редкая причина одышки
Гигантские грыжи пищеводного отверстия диафрагмы, обычно наблюдаемые в пожилом возрасте, редко могут вызывать сердечные симптомы, такие как одышка и боль в груди.Здесь мы стремились представить случай с большой грыжей пищеводного отверстия диафрагмы, которая в значительной степени выступала во внутригрудную полость и вызывала одышку, особенно в постпрандиальном периоде, из-за сдавливания левого предсердия и правой легочной вены. Мы рассмотрели этот случай, так как большая грыжа пищеводного отверстия диафрагмы является редкой интраабдоминальной причиной одышки.
1. Введение
Грыжа пищеводного отверстия диафрагмы определяется как аномальное выпячивание желудка другим внутрибрюшным органом, в некоторых случаях над диафрагмой из пищеводного отверстия.Сообщалось, что его распространенность составляет 0,8–2,9% при эндоскопии верхних отделов желудочно-кишечного тракта. Симптомы часто связаны с гастроэзофагеальной рефлюксной болезнью при грыже пищеводного отверстия диафрагмы, которая обычно протекает бессимптомно. Однако, хотя и редко, грыжа пищеводного отверстия диафрагмы может вызывать атипичные симптомы, такие как боль в груди или одышка, из-за протяженности грыжи и выступающих органов в полость грудной клетки. Здесь мы стремились представить случай грыжи пищеводного отверстия диафрагмы, которая в значительной степени выступала в полость грудной клетки и сдавливала левое предсердие, вызывая одышку.
2. Описание клинического случая
84-летняя женщина поступила в поликлинику с нарастающей утомляемостью, одышкой и почерневшим стулом в течение 1 месяца. Она отметила, что одышка усиливается при физической нагрузке и после приема пищи. Пациент не описал основное хроническое заболевание и не принимал никаких лекарств в течение предыдущих 6 месяцев. При физикальном обследовании жизненно важные функции были стабильными, конъюнктива бледность.Никаких отклонений от нормы при физикальном обследовании у пациента не наблюдалось, кроме систолического шума на вершине при кардиологическом обследовании. При лабораторных исследованиях были получены следующие результаты: WBC, 7400 / мм 3 ; Hgb, 10,9 г / дл; MCV, 72,3 фЛ; Plt, 376,000 / мм 3 ; железо, 18 мкм г / дл; железосвязывающая способность 350 мкм г / дл; ферритин, 3,7 нг / мл. Анализ кала на скрытую кровь положительный. Биохимические показатели были в пределах нормы. На задне-передней рентгенограмме грудной клетки наблюдались повышение кардиоторакального индекса, увеличенное средостение и образование массы с уровнем воздух-жидкость, наложенным на контуры сердца (рис. 1).Пациенту была выполнена компьютерная томография торакоабдоминальной области, включая аксиальный и коронарный срезы, в связи с подозрением на большую грыжу пищеводного отверстия диафрагмы с доступным изображением. Было обнаружено, что большая часть желудка была образована грыжей в средостение без каких-либо признаков ущемления и желудочно-кишечной непроходимости, и что грыжа пищеводного отверстия диафрагмы сдавила заднюю стенку левого предсердия и правую легочную вену (рис. 2).
При эндоскопии верхних отделов желудочно-кишечного тракта были обнаружены линейные эрозии в области пищеводно-желудочного перехода, где произошла грыжа пищеводного отверстия диафрагмы и сдавление диафрагмы.Активных желудочно-кишечных кровотечений не наблюдалось. Колоноскопия считалась нормальной. проводилась по поводу этиологии железодефицитной анемии. При трансторакальной эхокардиографии было обнаружено, что систолическая и диастолическая функции левого желудочка были нормальными, в то время как задняя стенка левого предсердия была сильно сдавлена большой массой (рис. 3 (а)). Систолическое давление в легочной артерии было оценено как высокое (42 мм рт. Ст.) При эхокардиографии. Поскольку согласно анамнезу наблюдалось усиление одышки после тяжелой еды, была проведена постпрандиальная трансторакальная эхокардиография, которая выявила усиление компрессии левого предсердия из-за грыжи пищеводного отверстия диафрагмы (Рисунок 3 (b)).Увеличение одышки после приема пищи было связано с застоем в легких, вызванным сдавлением левого предсердия и правой легочной вены. Пациентам, отказавшимся от хирургического вмешательства из-за преклонного возраста, были даны рекомендации по питанию. Назначены ингибитор протонной помпы и регулятор моторики. Гемограмма была нормальной через 3 месяца после заместительной терапии железом, и пациент протекал без осложнений.
3. Обсуждение
Грыжа пищеводного отверстия диафрагмы определяется как патологическое выпячивание желудка другим внутрибрюшным органом, в некоторых случаях над диафрагмой из пищеводного отверстия диафрагмы [1].Грыжа пищеводного отверстия диафрагмы I типа (скользящий тип) является наиболее часто наблюдаемым типом, при котором гастроэзофагеальный переход скользит вместе с частью желудка [2]. Хотя причина развития грыжи пищеводного отверстия диафрагмы неизвестна, частота ее возникновения увеличивается с возрастом [3]. Считается, что расслабление ножек диафрагмы в результате процесса старения является причиной более частых и крупных грыж пищеводного отверстия диафрагмы у пожилых людей [4]. Симптомы часто связаны с гастроэзофагеальной рефлюксной болезнью. Грыжи пищеводного отверстия диафрагмы обычно протекают бессимптомно.Как правило, пожилые люди не могут описать типичные симптомы рефлюкса, такие как жжение в груди, кислотная регургитация и боль в эпигастрии. Желудочно-кишечные кровотечения, связанные с язвой или эрозией, железодефицитной анемией, выпадением слизистой оболочки, ущемлением и заворотом пищевода, являются основными осложнениями грыжи пищеводного отверстия диафрагмы. В частности, наиболее пугающими осложнениями являются развитие ущемления или заворота [2].
Железодефицитная анемия — одно из часто встречающихся осложнений при грыже пищеводного отверстия диафрагмы. Связь между железодефицитной анемией и грыжей пищеводного отверстия диафрагмы известна с начала 1930-х годов [5]. Основной причиной железодефицитной анемии при грыже пищеводного отверстия диафрагмы является кровоизлияние в результате линейных язв и эрозий (поражение Камерона) в складках слизистой оболочки, где происходит сжатие диафрагмы [6, 7]. Кровотечение — не единственный фактор , ответственный за анемию у пациентов с грыжей пищеводного отверстия диафрагмы. Одна из причин железодефицитной анемии при грыже пищеводного отверстия диафрагмы — хронический гастрит со всеми последствиями.Сегодня, хотя их часто не замечают, эти поражения, являющиеся одной из скрытых причин как желудочно-кишечного кровотечения, так и железодефицитной анемии [8], регистрируются у 5% пациентов с грыжей пищеводного отверстия диафрагмы и у 20% пациентов со стойкой анемией и рецидивирующей анемией. кровотечение [9]. Бернардо и др. заявили, что поражения Кэмерона не были редкостью причиной хронических желудочно-кишечных кровотечений и их следует учитывать при исследовании пациентов с железодефицитной анемией [10]. В нашем случае во время предыдущих обследований считалось, что хроническая железодефицитная анемия объяснялась пожилым возрастом и нарушением орального приема пищи в результате скрытого кровоизлияния, вызванного грыжей пищеводного отверстия диафрагмы.
Хотя большие грыжи пищеводного отверстия диафрагмы встречаются нечасто, они могут приводить к атипичным симптомам, таким как боль в груди и одышка, и к редким осложнениям, таким как отек легких и сердечная недостаточность, из-за большой грыжи и сдавления сердца и легочных вен органами, выступающими в грудную клетку. полость. Siu et al. сообщили, что большая грыжа пищеводного отверстия диафрагмы вызвала сердечную недостаточность из-за сдавления левого предсердия в случае повторяющихся приступов острой сердечной недостаточности [11]. В другом отчете о случае Chau et al.продемонстрировали большую грыжу пищеводного отверстия диафрагмы как причину боли в груди у пациента, поступившего в отделение неотложной помощи с острой стенокардией [12]. Грыжа пищеводного отверстия диафрагмы при эхокардиографии может проявляться новообразованием в левом предсердии. Это может вызвать отек легких и сердечную недостаточность из-за обструкции легочных вен [13].
В нашем случае хроническая усталость и одышка при физической нагрузке особенно усиливаются в постпрандиальном периоде. Повышенное давление в легочной артерии в нашем случае было связано со сдавлением левого предсердия и правой легочной вены, так как другой очевидной причины не было.По имеющимся данным, считалось, что одышка, усиливающаяся после обильной еды, составляет из-за закупорки легких, из — сдавление левого предсердия и правой легочной вены.
4. Заключение
В заключение, большие грыжи пищеводного отверстия диафрагмы следует рассматривать при дифференциальной диагностике как редкую внутрибрюшную причину стойкой железодефицитной анемии и одышки. Следует иметь в виду, что большие грыжи пищеводного отверстия диафрагмы могут привести к сердечным симптомам и осложнениям из-за сдавления.Случаи с большими грыжами пищеводного отверстия диафрагмы должны быть оценены с помощью физического обследования и методов визуализации, таких как эхокардиография .
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации данной статьи.
Авторские права
Авторские права © 2015 Cem Sahin et al. Это статья в открытом доступе, распространяемая под лицензией Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Маразм: история болезни, патофизиология, состав тела
Скримшоу Н.С., Витери Ф.Э. INCAP изучает квашиоркор и маразм. Пищевой Нутер Бык . 2010 31 марта (1): 34-41. [Медлайн].
Spoelstra MN, Mari A, Mendel M, Senga E, van Rheenen P, van Dijk TH, et al. Квашиоркор и маразм связаны с нарушением клиренса глюкозы, связанным с дисфункцией ß-клеток поджелудочной железы. Метаболизм . 2 марта 2012 г. [Medline].
Данные Глобальной обсерватории здравоохранения (GHO): недостаточный вес у детей. Всемирная организация здравоохранения. Доступно по адресу http://www.who.int/gho/mdg/poverty_hunger/underweight_text/en/. 2016; Доступ: 4 октября 2016 г.
[Рекомендации] РЕКОМЕНДАЦИИ: ОБНОВЛЕНИЯ ПО ВЕДЕНИЮ ОСТРОГО НЕДОСТАТОЧНОГО ПИТАНИЯ У МЛАДЕНЦЕВ И ДЕТЕЙ. 2013. [Medline].
Pelletier DL, Frongillo EA Jr, Schroeder DG, Habicht JP. Влияние недоедания на детскую смертность в развивающихся странах. Бык Всемирная организация здравоохранения . 1995. 73 (4): 443-8. [Медлайн].
Joosten KF, Hulst JM. Распространенность недоедания у пациентов детских больниц. Curr Opin Педиатр . 2008 20 октября (5): 590-6. [Медлайн].
Павеллек И., Докупил К., Колецко Б. Распространенность недоедания у пациентов детских больниц. Clin Nutr . 2008 27 февраля (1): 72-6. [Медлайн].
Jeyaseelan V, Jeyaseelan L, Yadav B.Заболеваемость и факторы риска недоедания среди детей в возрасте 5-7 лет в Южной Индии. J Biosoc Sci . 2016 май. 48 (3): 289-305. [Медлайн].
Akuyam SA, Isah HS, Ogala WN. Липидный профиль сыворотки у голодающих нигерийских детей в заре. Niger Postgrad Med J . Сентябрь 2008. 15 (3): 192-6.
Чанд С., Шах Д. Окружность средней части плеча для выявления тяжелой острой недостаточности питания у младенцев в возрасте от одного до шести месяцев. Индийский педиатр . 2015 июн. 52 (6): 528-9. [Медлайн].
Эмери PW. Метаболические изменения при неправильном питании. Глаз . Октябрь 2005. 19 (10): 1029-32. [Медлайн].
Данные ЮНИСЕФ: мониторинг положения детей и женщин. ЮНИСЕФ. Доступно по адресу http://data.unicef.org/nutrition/malnutrition.html. 2016; Доступ: 4 октября 2016 г.
Lazzerini M, Ronfani L. Цинк для перорального применения для лечения диареи у детей. Кокрановская база данных Syst Rev . 2008. (3): CD005436. [Медлайн].
Spoelstra MN, Mari A, Mendel M, Senga E, van Rheenen P, van Dijk TH, et al. Квашиоркор и маразм связаны с нарушением клиренса глюкозы, связанным с дисфункцией β-клеток поджелудочной железы. Метаболизм . 2012 Сентябрь 61 (9): 1224-30. [Медлайн].
Алтинкайнак С., Селимоглу М.А., Эртекин В., Киликарслан Б. Уровни грелина в сыворотке крови у детей с первичной белково-энергетической недостаточностью питания. Педиатр Интерн. . 2008 50 августа (4): 429-31. [Медлайн].
Kilic M, Taskin E, Ustundag B, Aygun AD. Оценка уровня лептина в сыворотке крови и других гормональных показателей у детей с тяжелой недостаточностью питания. Clin Biochem . 2004 Май. 37 (5): 382-7. [Медлайн].
Bartz S, Mody A, Hornik C, Bain J, Muehlbauer M, Kiyimba T. и др. Тяжелое острое недоедание в детстве: гормональный и метаболический статус на момент обращения, ответ на лечение и предикторы смертности. Дж. Клин Эндокринол Метаб . 2014 июн.99 (6): 2128-37. [Медлайн].
Million M, Diallo A, Raoult D. Микробиота кишечника и недоедание. Микроб Патог . 2016 г. 4 февраля [Medline].
Международный научно-исследовательский институт продовольственной политики, Вашингтон, округ Колумбия. Глобальный доклад по питанию 2016 г .: от обещаний к результату: покончить с недоеданием к 2030 году. Глобальный отчет по питанию 2016 г .: от обещаний к результатам: покончить с недоеданием к 2030 г. .2016.
Хендрикс К.М., Дагган С., Галлахер Л. и др. Недоедание у госпитализированных педиатрических больных. Текущая распространенность. Арх Педиатр Адолеск Мед . 1995 Октябрь 149 (10): 1118-22. [Медлайн].
Cameron JW, Rosenthal A, Olson AD. Недоедание у госпитализированных детей с врожденными пороками сердца. Арх Педиатр Адолеск Мед . 1995 Октябрь 149 (10): 1098-102. [Медлайн].
Fisberg M, Nobrega FJ.Disturbios da nutricao. Ревинтер . 1998. 140-4.
Могила Manejo da desnutricao: um manual para profissionals de saude de nivel superior (medicos, enfermeiros, nutricionistas e outros) и suaas equipes auxillares. Organizacao Mundial da Saude, Бразилиа . 1999.
Роча Г.А., Роча Е.Дж., Мартиньш CV. Влияние госпитализации на состояние питания детей. Дж. Педиатр (Рио Дж.) . 2006 янв-фев.82 (1): 70-4. [Медлайн].
Мартелетти О., Калдари Д., Гимбер Д., Упоминание К., Мишо Л., Готтранд Ф. [Скрининг недоедания у госпитализированных детей: влияние отделения больницы на его управление]. Арх. Педиатр . 2005 12 августа (8): 1226-31. [Медлайн].
Озтюрк Й, Бююкгебиз Б., Арслан Н., Эллидокуз Х. Влияние пребывания в больнице на антропометрические данные о питании турецких детей. Дж. Троп Педиатр . 2003 июн. 49 (3): 189-90.[Медлайн].
Питер С.Дж., Фишер Л.К., Кундакович М., Гарг П., Яковцевски М., Динсер А. и др. Сигнатуры метилирования ДНК при недоедании в раннем детстве, связанном с нарушениями внимания и познания. Биологическая психиатрия . 2016 26 марта. [Medline].
Waber DP, Bryce CP, Fitzmaurice GM, et al. Нейропсихологические результаты в среднем возрасте после умеренного и тяжелого недоедания в младенчестве. Нейропсихология . 2014 17 марта.[Медлайн].
Фрэнсис-Эммануэль П.М., Томпсон Д.С., Барнетт А.Т. и др. Метаболизм глюкозы у взрослых, переживших тяжелое острое недоедание. Дж. Клин Эндокринол Метаб . 2014 11 февраля. Jc20133511. [Медлайн].
Agarwal E, Miller M, Yaxley A, Isenring E. Недоедание у пожилых людей: обзорный обзор. Maturitas . 2013 декабрь 76 (4): 296-302. [Медлайн].
Санчес Саплана I, Маэстре Гонсалес Э.[Питание и старение]. Рев. Энферм . 2013 июн. 36 (6): 8-15. [Медлайн].
Alcoba G, Kerac M, Breysse S и др. Нужны ли антибиотики детям с неосложненной тяжелой острой недостаточностью питания? Систематический обзор и метаанализ. PLoS Один . 2013. 8 (1): e53184. [Медлайн].
Пико Дж., Хартвелл Д., Харрис П. и др. Эффективность вмешательств для лечения тяжелой острой недостаточности питания у детей раннего возраста: систематический обзор. Оценка медицинских технологий . 2012. 16 (19): 1-316. [Медлайн].
Trehan I, Goldbach HS, LaGrone LN, et al. Антибиотики как часть лечения тяжелой острой недостаточности питания. N Engl J Med . 2013 31 января. 368 (5): 425-35. [Медлайн].
Million M, Lagier JC, Raoult D. Мета-анализ эффективности амоксициллина при неосложненной тяжелой острой недостаточности питания. Микроб Патог . 2016 29 июня. [Medline].
Всемирная организация здравоохранения.Глобальная база данных ВОЗ по детскому росту и недоеданию. Женева: ВОЗ . 1996.
Kim Y, Hahn S, Garner P. Раствор для пероральной регидратации с пониженной осмолярностью для лечения обезвоживания, вызванного острой диареей у детей. Кокрановская база данных Syst Rev . 2001. (2): CD002847. [Медлайн].
ЮНИСЕФ. Новая формула солей для пероральной регидратации (ORS) с пониженной осмолярностью. Детский фонд ООН. Доступно по адресу http: // www.supply.unicef.dk/catalogue/bulletin9.htm.
Пухлый орех. Доступно на http://en.wikipedia.org/wiki/Plumpy’nut.
Совместное заявление Всемирной организации здравоохранения, Мировой продовольственной программы, Постоянного комитета системы Организации Объединенных Наций по питанию и Детского фонда Организации Объединенных Наций. Управление тяжелой острой недостаточностью питания на уровне общины. Май 2007г.
[Рекомендации] Всемирная гастроэнтерологическая организация (WGO).Практическое руководство WGO: острая диарея. Март 2008 г. [Полный текст].
Stanga Z, Brunner A, Leuenberger M, et al. Питание в клинической практике — синдром возобновления питания: наглядные примеры и рекомендации по профилактике и лечению. евро J Clin Nutr . 2008 июнь 62 (6): 687-94. [Медлайн].
Шварц С.М., Корредор Дж., Фишер-Медина Дж., Коэн Дж., Рабиновиц С. Диагностика и лечение нарушений питания у детей с отклонениями в развитии. Педиатрия . 2001 сентябрь 108 (3): 671-6. [Медлайн].
Bhutta ZA, Ahmed T, Black RE, Cousens S, Dewey K, Giugliani E. Что работает? Вмешательства для материнского и детского недоедания и выживания. Ланцет . 2008 г. 2 февраля. 371 (9610): 417-40. [Медлайн].
Adhisivam B, Srinivasan S, Soudarssanane MB, et al. Кормление младенцев и маленьких детей в деревнях Пондичерри, пострадавших от цунами. Индийский педиатр .2006 г., 43 (8): 724-7. [Медлайн].
Вентилятор CN. [Распространенность и профилактика общих рисков для питания детей после землетрясения]. Чжунго Данг Дай Эр Кэ За Чжи . 2013 июн.15 (6): 427-30. [Медлайн].
Чапарро С.М., Дьюи К.Г. Использование пищевых добавок на липидной основе (LNS) для повышения адекватности питательных веществ в общих рационах распределения продовольствия для уязвимых подгрупп в условиях чрезвычайных ситуаций. Детский нутер Matern .2010, 6 января, Приложение 1: 1-69. [Медлайн].
[Руководство] Глобальные рекомендации Всемирной гастроэнтерологической организации: острая диарея у взрослых и детей: глобальная перспектива. Доступно на https://guideline.gov/summaries/summary/47569.
Эшворт А., Джексон А., Ханум С., Скофилд С. Десять шагов к выздоровлению. Диалог о здоровье детей . 1996. 10-2. [Медлайн].
Barennes H, Kahiatani F, Pussard E, et al.Интраректальный Quinimax (ассоциация алкалоидов Cinchona) для лечения малярии Plasmodium falciparum у детей в Нигере: эффективность и фармакокинетика. Транс Р Соц Троп Мед Хиг . 1995 июль-авг. 89 (4): 418-21. [Медлайн].
Beaufrere B, Bresson JL, Briend A, et al. Потребности в белке и энергии у детей с тяжелым недоеданием. Применение в условиях стационара для лечения недоедания, вызванного недостаточным потреблением. Арх. Педиатр .1998. 5 (7): 763-71. [Medline].
Беркли Дж., Мванги И., Гриффитс К. и др. Оценка тяжелого недоедания среди госпитализированных детей в сельской Кении: сравнение веса с ростом и средней окружностью плеча. ЯМА . 2005 3 августа. 294 (5): 591-7. [Медлайн].
Briend A, Wojtyniak B, Rowland MG. Окружность руки и другие факторы у детей с высоким риском смерти в сельских районах Бангладеш. Ланцет . 1987 26 сентября.2 (8561): 725-8. [Медлайн].
Бьюкенен Н. Лекарственная кинетика при белково-энергетической недостаточности. S Afr Med J . 1978 г. 4. 53 (9): 327-30. [Медлайн].
Бьюкенен Н. Влияние белково-энергетической недостаточности на метаболизм лекарств у человека. Диета Мира Рев Нутра . 1984. 43: 129-39. [Медлайн].
Бьюкенен Н., Эйберг С., Дэвис, Мэриленд. Фармакокинетика изониазида в Квашиоркоре. Южная Африка Мед J . 1979 г.56 (8): 299-300. [Медлайн].
Buchanan N, Robinson R, Koornhof HJ, Eyberg C. Фармакокинетика пенициллина в квашиоркоре. Ам Дж. Клин Нутр . 1979, ноябрь 32 (11): 2233-6. [Медлайн].
Эль-Сайед Х.Л., Нассар М.Ф., Хабиб Н.М. и др. Структурные и функциональные поражения сердца у пациентов с белково-энергетической недостаточностью при поступлении и после восстановления питания. евро J Clin Nutr . 2006 апр. 60 (4): 502-10. [Медлайн].
Финч РГ.Побочные реакции на антибиотики. Гринвуд Д., изд. Антимикробная химиотерапия . 4-е изд. Оксфорд, Англия: Издательство Оксфордского университета; 2000. 200-11.
Голден М. Влияние неправильного питания на обмен веществ у детей. Транс Р Соц Троп Мед Хиг . 1988. 82 (1): 3-6. [Медлайн].
Гомес Ф., Рамос Гальван Р., Френк С. и др. Смертность при недоедании второй и третьей степени. В: Bull World Health Organ. 2000; 78 (10): 1275-80. J Trop Ped and Afr Child Health . 1956. 2:77. [Медлайн].
Grantham-McGregor S. Обзор исследований влияния тяжелого недоедания на умственное развитие. Дж Нутрь . 1995. 125: 2233-8 S. [Medline].
Кришнасвами К. Метаболизм и фармакокинетика лекарств у детей с недостаточным питанием. Клин Фармакокинет . 1989. 17 Suppl 1: 68-88. [Медлайн].
Листерник Р., Кристоффель К., Пейс Дж., Кьярамонте Дж.Тяжелое первичное недоедание у детей в США. Ам Дж. Дис Детский . 1985 ноябрь 139 (11): 1157-60. [Медлайн].
Long J, Всемирная организация здравоохранения. Управление тяжелым недоеданием: руководство для врачей и старших медицинских работников. 1999.
Martorell R, Habicht JP, Rivera JA. История и дизайн продольного исследования INCAP (1969-77) и его продолжение (1988-89). Дж Нутрь . 1995. 125: 1027-41 S. [Medline].
Mazouni SM, Guignard JP.[Недоедание у детей и вариабельность эффектов лекарств]. Rev Med Suisse Romande . 1996 декабрь 116 (12): 965-9. [Медлайн].
Мехта С. Метаболизм лекарств у недоедающего ребенка. Мастерская Nestle Nutr ser . 1988. 19: 329-38.
Mehta S, Nain CK, Sharma B, Mathur VS. Распоряжение четырьмя препаратами для детей с недостаточным питанием. Лекарство Нутр Взаимодействие . 1982. 1 (3): 205-11. [Медлайн].
Мехта С., Наин С.К., Ядав Д. и др.Распределение парацетамола у детей с белково-калорийной недостаточностью. Int J Clin Pharmacol Ther Toxicol . 1985 июня 23 (6): 311-5. [Медлайн].
Merritt RJ, Suskind RM. Обследование питания госпитализированных педиатрических больных. Ам Дж. Клин Нутр . 1979 июн. 32 (6): 1320-5. [Медлайн].
Polasa K, Murthy KJ, Krishnaswamy K. Кинетика рифампицина при недостаточном питании. Бр. Дж. Клин Фармакол . 1984 апр. 17 (4): 481-4.[Медлайн].
Поллитт Э. Развитие последствий раннего дефицита питания: окончательные и вероятностные суждения. Дж Нутрь . 2000, февраль 130 (2S Suppl): 350S-353S. [Медлайн].
Rumack BH, Holtzman J, Chase HP. Метаболизм лекарств в печени и белковая недостаточность. J Pharmacol Exp Ther . 1973 Сентябрь 186 (3): 441-6. [Медлайн].
Сет В., Беотра А., Багга А., Сет С. Лекарственная терапия при недоедании. Индийский педиатр . 1992 29 ноября (11): 1341-6. [Медлайн].
Taketomo CK, Hodding JH, Kraus DM. Справочник по дозировке для детей . 12-е изд. Хадсон, Огайо: Lexi Comp Inc; 2005.
Tolboom JJ. Управление тяжелым истощением и диареей. Дж Педиатр Гастроэнтерол Нутр . 2000 марта 30 (3): 346-8. [Медлайн].
Waterlow JC. Классификация и определение белково-калорийной недостаточности. Br Med J . 1972 г. 2. 3 (826): 566-9. [Медлайн].
Ядав Д. Распределение парацетамола у детей с белково-калорийной недостаточностью. Clin Pharmacol Ther . 1985. 23: 311-5.

 Количество калорий рассчитывается на основе физических параметров.
Количество калорий рассчитывается на основе физических параметров.