Антибиотикоассоциированный колит: симптомы и лечение
Антибиотики надо принимать строго по назначению врача и с большой осторожностью. Помимо того, что они убивают плохие бактерии, и вирусы, они могут нанести значительный урон хорошим и полезным бактериям. После приема антибиотиков возникает псевдомембранозный (антибиотикоассоциированный) колит.
Антибиотикоассоциированный колит – это воспаление кишечника, носящее очень тяжелый характер, возникающее после длительного приема антибиотиков. Для подобного вида колита характерен специфический дисбактериоз и фиброзные налеты. Фиброзные налеты по-другому называют псевдомембранами, отсюда и название псевдомембранозный колит.
В тяжелых случаях у сильно ослабленных больных наблюдается интоксикационный синдром, обезвоживание с нарушением электролитов, развитие грубых поражений кишечных стенок, что в результате приводит к прободению.
Содержание статьи
Подробнее о заболевании
Не так давно получены доказательства того, что использование антибиотиков широкого спектра действия может привести к острой воспалительной реакции со стороны толстой кишки.
Антибиотикоассоциированный колит — воспалительное заболевание толстой кишки, обусловленное приемом антибиотиков и варьирующее от кратковременной диареи до тяжелых форм с образованием фибринозных бляшек на слизистой оболочке кишки, возбудителем патологии являются С. Perfringes, С. Difficile, Staphylococuss aureus, С. Clebsiella oxytoca, Salmonella spp., Candida spp.
Классификация заболевания
В практическом отношении антибиотик-ассоциированный колит (ААК) подразделяется на две группы: колит, вызванный ампициллином и его дериватами, и колит, вызванный линкомицином или клиндамицином. Колит, вызванный ампициллином, представляет собой, как правило, геморрагический колит, проявления которого быстро стихают после отмены этого антибиотика. Тем не менее, имеются неединичные сообщения о случаях псевдомембранозного колита, вызванных ампициллином.

В Японии причиной возникновения большинства случаев ААК оказалось назначение ампициллина или его дериватов. Totani обобщил сведения о 35 случаях ААК, имевших место в отделении заразных заболеваний центрального госпиталя. В 80% случаев симптоматика развивалась в течение трёх дней с момента назначения антибиотика.
Totani сообщает о наличии Klebsiella oxytoca практически в чистой культуре в фекалиях пациентов с заболеванием в ранней стадии развития. Klebsiella oxytoca представляет собой новый биологический тип Klebsiella pneumoniae . Данная бацилла рассматривается не в качестве возбудителя, а как суперинфекция.
Колит, вызванный линко- или клиндамицином, отличается более тяжёлым течением и как правило, проявляется в виде псевдомембранозного колита. К возникновению заболевания может приводить как энтеральный, так и парентеральный способ введения антибиотика.
Исследования последних лет показали, что главной причиной псевдомембранозного колита является токсинообразующая Clostridium difficile. C. difficile выделена из фекалий большинства больных псевдомембранозным ААК, но редко обнаруживается в фекалиях здоровых людей. C.difficile представляет собой крупную неспорообразующую Грам-отрицательную облигатно-анаэробную бациллу с сужением на конце.
Tedesco разделяет клиндамицин-ассоциированный колит на две клинические группы. К первой группе относится колит, диагностированный в ранней стадии, когда антибиотик-терапия немедленно отменялась, а благодаря адекватной поддерживающей терапии симптомы колита купировались без смертельного исхода. Ко второй группе относятся пациенты, у которых диарея и колит развились после полного курса антибиотик-терапии, а также те, которым введение антибиотика продолжалось, несмотря на явное наличие диареи и симптомокомплекса колита. У этих больных длительно сохранялась диарея с выраженным болевым синдромом, иногда наступал летальный исход.
Патоморфология
ААК может поражать различные сегменты толстой кишки. В случае применения ампициллина чаще всего развивается острый геморрагический колит с локализацией в проксимальных сегментах толстой кишки, тогда как прямая кишка нередко свободна от поражения. Тонкая кишка вовлекается в процесс редко. Характер поражения при остром геморрагическом колите, как правило, отличается равномерностью и сегментарностью, а прерывисто-пятнистое или скачкообразное поражение в пределах сегмента встречается редко.
Иногда сегментарное поражение имеет псевдомембранозный характер, и прямая кишка не является исключением. Спектр гистологических изменений распространяется от признаков незначительного воспаления до проявлений псевдомембранозного колита. При наличии слабовыраженного неспецифического воспаления локализация основных изменений ограничивается поверхностным межжелезистым эпителием и расположенной ниже собственной пластинкой.
Сохраняется почти правильное расположение тубулярных желез на фоне сокращения популяции бокаловидных клеток. Собственная пластинка инфильтрирована полиморфными и лимфо-плазматическими клетками. Характерным признаком являются внутрислизистые кровоизлияния, которые нередко обширные, несмотря на незначительные воспалительные изменения. В более выраженных случаях заболевания наиболее характерными являются деструкция желез и распространённая воспалительно-клеточная инфильтрация.
В тяжёлых случаях ампициллин-ассоциированного колита встречаются также псевдомембранозные образования или структурный некроз.
По распространённости поражения псевдомембранозный колит может быть местно-очаговым или же охватывать значительные по протяжённости сегменты кишки. Price и Devis описали три патогистологические модели псевдомембранозного колита. Ранние признаки поражения заключаются в фокальном эпителиальном некрозе поверхностного эпителия в межжелезистом пространстве. Второй тип поражения характеризуется типичным формированием псевдомембран.
При поражении третьего типа наблюдается полный структурный некроз слизистой с немногими сохранившимися железами, покрытыми воспалительно-клеточным детритом, включающим муцин и фибрин. Наиболее показательные случаи характеризуются наличием патологического слоя, напоминающего древесную кору с мшистым покрытием.
Сама по себе псевдомембрана состоит из смеси фибрина, детрита, слизи и воспалительных клеток и часто содержит колонии бактерий. Подобная мембрана прочно связана с некротизированой слизистой и повреждёнными, обращёнными в просвет железами. Глубже расположенные железы нередко остаются интактными. Под псевдомембраной отмечается дилатация желез. Отёчная собственная пластинка инфильтрирована нейтрофилами, лимфоцитами и плазматическими клетками.

Отмечается значительный отёк подслизистого слоя, однако, клеточная инфильтрация его минимальная. В конечном итоге, если больной не погибает, повреждённая слизистая оболочка отторгается и в результате полного слущивания отторгнутой слизистой могут образовываться язвы.
Имеет место также ряд изменений, наблюдаемых в фазе разрешения процесса или выздоровления и заключающихся в признаках регенерации и восстановления поражённой слизистой оболочки из сохранившихся крипт. Может наблюдаться деформация сохранившихся желез, но встречается также полное восстановление слизистой оболочки.
Причины антибиотикоассоциированного колита
Основная причина возникновения колита после приема антибиотиков – это сама длительная терапия данными препаратами. Существует даже распределение лекарств, которые, так или иначе, влияют на появление колита. К самым опасным относят: Клиндамицин, Линкомицин. Наименее опасны: Тетрациклин, Цефалоспорин, Ампициллин, Эритромицин, Левомицетин, Пенициллин.
Но даже здесь существуют разногласия между специалистами. Некоторые из них считают, что такой колит могут провоцировать все антибиотики и к тому же к ним еще добавляют слабительные средства и ряд цитостатиков. Специфический дисбактериоз – основная характерная черта. Развивается дисбактериоз с преобладанием микроорганизма – Clostridium difficile. Такая патогенная бактерия обнаруживается у 3% здорового населения разных возрастов. По большей части этот процент делят между собой дети и новорожденные. Подтверждение этому 50% инфицированных – это дети младшей возрастной группы.
Самое интересное, что подобная бактерия свойственна не только человеческому организму, но и животным, независимо от того, домашние это животные или дикие. А еще она может находиться даже в обычной почве.
То, что антибиотики способствуют развитию колита, это мы выяснили, а вот какая форма опаснее? По многим данным выясняется, что лекарства, которые были получены инъекционным путем, намного опаснее.
Самая опасная причина – это наличие бактерии Clostridium difficile. Эта бактерия, находясь в организме, выделяет токсины, которые плохо влияют на эпительный покров кишечной стенки. Влияние подобных токсинов усиливают антибиотики.
Факторы, которые повышают вероятность возникновения антибиотик-ассоциированного колита:
- использование антибиотиков;
- возраст: пожилой;
- длительная госпитализация или лечение;
- тяжелая болезнь.
Другие возможные факторы риска включают:
- энтеральное питание;
- прием лекарств, снижающих кислотность желудка;
- желудочно-кишечная хирургия (операции желудка или кишечника ) или желудочно-кишечные заболевания, такие как болезнь Крона или неспецифический язвенный колит;
- беременность;
- химиотерапия;
- пересадка костного мозга.
Потенциальный риск развития ААК при использовании различных антибактериальных препаратов:
| Вид антибиотика | Риск развития ААК | ||
| умеренный | высокий | очень высокий | |
| Клиндамицин | ● | ||
| Цефалоспорины | ● | ||
| Аминопенициллины | ● | ||
| Макролиды | ● | ||
| Хинолоны | ● | ||
| Тетрациклины | ● | ||
| Пенициллины | ● | ||
| Триметоприм / сульфаметоксазол | ● | ||
| Сульфаниламиды | ● | ||
| Рифампицин | ● | ||
| Метронидазол | ● | ||
Клиническая картина ААК может варьировать от легкой преходящей диареи до тяжелых фатальных форм колита. Течение заболевания зависит от вида возбудителя, характера антибактериальной терапии, ее длительности, применения комбинированной противомикробной терапии, возраста пациента, наличия иммунокомпрометированного статуса, коморбидных состояний, хирургических операций на органах ЖКТ, применения антисекреторных и антиперистальтических средств, зондового питания.
Критерии тяжести Clostridium dificile-ассоциированного колита
| Легкое течение: | диарея до 5-7 раз в сутки, умеренная боль в животе, отсутствие лихорадки, отсутствие лейкоцитоза |
| Средне-тяжелое течение: | диарея 10-15 раз в сутки, боль в животе, лихорадка <38,50С, умеренная дегидратация, умеренный лейкоцитоз |
| Тяжелое течение ААК или ПМК: | гектическая лихорадка ≥38,50С, тяжелый интоксикационный синдром, гемодинамические нарушения (включая признаки инфекционного шока), признаки перитонита (включая ослабление кишечных шумов, напряжение передней брюшной стенки), признаки кишечной непроходимости (включая рвоту, отсутствие стула), выраженный лейкоцитоз со сдвигом лейкоцитарной формулы влево, повышение уровня сывороточного креатинина, повышение уровня лактата, наличие псевдомембран (эндоскопически), признаки токсического мегаколона, утолщение стенок кишечника, гипоальбуминемия, признаки асцита, выраженная дегидратация, электролитные нарушения |
Симптоматика заболевания
Комплекс клинических симптомов может варьировать от легкого течения в виде водянистой диареи до 5–7 раз в сутки без системных проявлений. При среднетяжелом течении водянистая диарея достигает 10–15 раз в сутки, сопровождается болями в животе, лихорадкой до 38 °C, умеренной дегидратацией, лейкоцитозом крови. Развитие диареи возможно как в первые дни приема антибиотиков, так и в последние дни курса лечения антибиотиками.
При тяжелом течении заболевания диарея — до 20 раз в сутки, иногда с примесью крови, сопровождается лихорадкой до 39–40 °C, тяжелой дегидратацией — обезвоживанием, астенизацией — ослаблением, высоким лейкоцитозом крови. Вариантом течения является псевдомембранозный колит, который наблюдается у 1 % больных с колитом, вызванным инфекцией С. Difficile который имеет эндоскопическую особенность — образование плотных связанных с подлежащими тканями фибринозных наложений на слизистой оболочке толстой кишки.
Несвоевременное лечение псевдомембранозного колита может привести к летальным осложнениям — развитию токсического мегаколона (гигантской толстой кишки), перфорации кишки.
Основан диагноз колита, ассоциированного с С. Difficile, на анамнезе — прием антибиотиков в течение последних 8 недель. Клинические данные о частоте диареи, примесь крови в кале, лихорадка, степень дегидратации предполагают тяжесть заболевания. Лабораторные исследования: обнаружение в кале лейкоцитов и эритроцитов, при тяжелом течении — лейкоцитоз, анемия, электролитные нарушения, снижение уровня альбумина и сывороточного железа.
Стандартом диагностики служит определение в кале токсинов А и В, С. Difficile методом иммуноферментного анализа, который обеспечивает результат в течение нескольких часов, чувствительность и специфичность метода приближается к 100 %. Микробиологический метод диагностики с выявлением культуры С. Difficile и оценкой ее токсичности применяется редко из-за большей длительности проведения. При колоноскопии в случае легкого течения болезни эндоскопическая картина неспецифична.
Диагноз псевдомембранозного колита подтверждается при эндоскопическом исследовании: на слизистой оболочке толстой кишки, в частности в дистальных отделах, наблюдаются типичные псевдомембраны, представляющие собой небольшие — 2–8 мм в диаметре — налеты кремового цвета, сливающиеся между собой, состоящие из фибрина, некротизированных эпителиальных клеток и лейкоцитов.
Осложнения заболевания
Осложнения псевдомембранозного колита — электролитные нарушения, артериальная гипотония, дегидратация, токсический мегаколон; при токсическом мегаколоне, если не проводится лечение, летальность составляет 30 %, при своевременной терапии — 4 %. При токсическом мегаколоне происходит дилатация толстой кишки, истончение ее стенок и избыточное накопление газа в просвете, что создает высокий риск перфорации.
Клинически токсический мегаколон проявляется общим тяжелым состоянием, нередко с нарушением сознания, высокой лихорадкой, тяжелым обезвоживанием, электролитными расстройствами, нейтрофильным лейкоцитозом, анемией. Главный критерий диагностики — увеличение диаметра просвета толстой кишки более 6 см. При отсутствии положительной динамики на фоне лечения в течение 24 часов предполагают рефрактерное течение заболевания, таким больным необходимо экстренное выполнение тотальной колэктомии.
Диагностика заболевания
Сравнительная характеристика различных методов диагностики Clostridium difficile–ассоциированного колита
| Метод | Цель | Время, ч | Чувствительность, % | Специфичность, % | Достоинства | Недостатки |
| Цитопатогенный тест (ЦПТ) (на культуре клеток) «Золотой стандарт» | Токсин В | 28–48 | 67–100 | 85–100 | • Высокая чувствительность. • Возможно полуколичественное определение путем титрования проб. • Высокая чувствительность. | Рекомендуется использовать в сочетании с бактериологическим исследованием |
| Реакция нейтрализации токсина (на культуре фибробластов) | Токсин В | 28–48 | – | – | Хорошие чувствительность и специфичность. | Рекомендуется использовать в сочетании с ЦПТ |
| Латекс-агглютинация | Глутамат-дегидрогеназа | 0,5 | 58–92 | 80–96 | Быстрота получения результата исследования | Невысокие чувствительность и спе-цифичность. Используется только для экспресс-диагностики |
| Иммуноферментный анализ (ИФА) | Токсин А или оба токсина А и В | 2–4 | 63–99 | 75–100 | Хорошие специфичность и чувствительность. | Может потребоваться 2–3 кратное повторение исследования |
| Дот-иммуноблотинг | Токсин А | 0,5 | – | – | – | – |
| Полимеразная цепная реакция (ПЦР) | Ген, кодирующий токсин В, ген, кодирующий токсин А, или оба гена | 2–4 | – | – | Хорошая чувствительность,высокая специфичность | – |
| Культуральный метод | Микроорганизм и его токсигенность in vitro | 24–72 | 89–100 | 84–99 | Хорошая чувствительность | Низкая специфичность в связи с высокой частотой носительства у госпитализированных пациентов, особенно получающих антибиотики |
| Эндоскопия | Диагностика ПМK | – | 51 | ≈100 | – | – |
Дифференциальная диагностика
Диагноз ампициллин-ассоциированного колита правомочен тогда, когда в анамнезе больного имеется назначение данного препарата. Наличие в кале Klebsiella oxytoca в практически чистой культуре является существенным диагностическим подспорьем в случае ампициллин-ассоциированного колита, так как при других патологических состояниях этого не отмечается. Обнаружение в кале патогенных бацилл обусловливает правильную диагностику инфекционного колита. Ишемический колит является преимущественно возрастной патологией, развивающейся, как правило, на фоне сердечно-сосудистых заболеваний. Течение ИК может быть продолжительным. При негангренозной форме ИК часто наступает выздоровление, сопровождающееся образованием рубцов и/или псевдодивертикулов, которые нехарактерны для ампициллин-ассоциированного колита.
Последний характеризуется также быстро наступающим выздоровлением. Поэтому тотальная колоноскопия, проведённая как можно раньше с момента появления симптоматики, облегчает постановку диагноза.
Симптоматика ампициллин-ассоциированного колита кое-чем напоминает таковую при НЯК. Тем не менее, НЯК характеризуется поражением прямой кишки, а в большинстве случаев ампициллин-ассоциированного колита дистальные отделы толстой кишки остаются интактными на фоне сегментарного поражения ободочной кишки. Течение НЯК хроническое непрерывное или рецидивирующее. Ампициллин-ассоциированный колит напротив характеризуется острым и преходящим течением без обострений.
Колит Крона — хроническое заболевание с сегментарным поражением кишки, характер которого, как правило, скачкообразный. Неизъязвлённые участки зачастую выглядят интактными, а кровоточивость слизистой оболочки не является характерным признаком данного заболевания. Поэтому клиническая и морфологическая дифференцировка БКТК и ААК не представляет затруднений.
Псевдомембранозный колит — неспецифическое поражение, характеризующееся образованием псевдомембран. Это полиэтиологичное заболевание, хотя термин «псевдомембранозный колит» Morson использовал только в отношении случаев острого ишемического некроза. Некоторые авторы считают, что все случаи данного заболевания возникают по причине назначения антибиотиков или обусловлены стафилококком. В то же время имеются сообщения, основанные на обширном материале и сделанные ещё до эры применения антибиотиков.
Стафилококк же обнаруживается не во всех случаях псевдомембранозного колита. Сверхрост стафилококка, зачастую рассматриваемый в качестве причины ААК, можно исключить с помощью изучения выделенных из кала культур после окраски по Граму. Рентгенологические проявления псевдомембранозного колита характеризуются наличием при ирригоскопии множественных дефектов наполнения. Дифференциальная диагностика в данном случае должна проводиться с воспалительными полипами, «булыжной мостовой» и семейным полипозом.
Лечение антибиотик-ассоциированного колита
Лечение включает следующее:
Первый шаг — прекращение приема антибиотиков и возмещение потерянной жидкости. Перед прекращением приема антибиотиков необходимо посоветоваться с врачом. Колит обычно проходит в течение двух недель после отмены антибиотиков.
Пациенту назначают антибиотики, которые убивают Clostridium difficile. Также можно принимать пробиотики, которые помогают восстановить нормальный уровень полезных бактерий в кишечнике.
Не рекомендуется использовать антидиарейные препараты (например, лоперамид и опиаты).
В очень редких случаях может понадобиться операция. Хирург может вывести тонкую кишку через отверстие в брюшной полости. При этом стул будет отводиться, минуя толстый кишечник и прямую кишку. Эта операция называется илеостомия.
Хирург может также удалить толстую кишку. Эта операция называется колэктомия.
Профилактика антибиотикассоциированного колита
Лучший способ предотвратить это заболевание — снижение использования антибиотиков. Антибиотики следует применять только когда врач подтвердил наличие бактериальной инфекции.
При назначении антибиотиков нужно спросить у врача о возможности приема пробиотиков, которые помогают восстановлению полезных бактерий в кишечнике.
Прогноз заболевания
Прогноз зависит от степени тяжести Clostridium difficile–ассоциированной диареи/колита, характера течения, наличия осложнений. При легком и средне-тяжелом течении ― прогноз благоприятный. Лихорадка обычно исчезает в течение 1-2 сут., а диарея купируется через 5-7 дней от начала этиотропной терапии. При отсутствии серьезных осложнений (перфорация кишки, кишечная непроходимость, токсический мегаколон), практически все пациенты отвечают на проводимое лечение.
К неблагоприятным прогностическим факторам относятся: кишечная непроходимость, псевдомембранозный колит, почечная недостаточность.
Антибиотик-ассоциированная диарея — причины, симптомы, диагностика и лечение

Антибиотик-ассоциированная диарея — это заболевание, которое характеризуется появлением неоформленного стула во время или после приема антибактериальных препаратов. Болезнь сопровождается диспепсической симптоматикой (послаблением стула, газообразованием). В тяжелых случаях появляются интенсивные боли в животе, слабость, лихорадка. Диагностика основывается на установлении связи приема АБ с развитием диареи. Дополнительно проводят анализ кала, эндоскопическое исследование кишечника. Лечение предполагает отмену АБ, назначение пробиотиков и дезинтоксикационных препаратов. При выявлении возбудителя болезни проводят этиотропную антибактериальную терапию.
Общие сведения
Антибиотик-ассоциированная диарея (ААД, нозокомиальный колит) — три и более эпизода жидкого стула, повторяющиеся на протяжении не менее двух дней и связанные с приемом антибактериальных препаратов (АБ). Расстройство может проявляться в течение 4-х недель после отмены АБ. В развитых странах поражение кишечника является наиболее частой реакцией на антибиотикотерапию: у лиц, принимающих антибиотики, ААД встречается в 5-30% случаев. Патология протекает как в легкой самокупирующейся форме, так и в виде тяжелого затяжного колита. В современной гастроэнтерологии не менее 70% случаев заболевания приходится на идиопатическую ААД, 30% — на Clostridium difficile-ассоциированную диарею. Болезнь в равной степени поражает мужчин и женщин.

Антибиотик-ассоциированная диарея
Причины ААД
Антибиотик-ассоциированная диарея чаще развивается после назначения антибиотиков пенициллинового ряда, тетрациклинов, цефалоспоринов. Способ введения лекарств практически не влияет на вероятность появления диареи. При пероральном приеме медикаменты воздействуют на слизистый слой ЖКТ. При парентеральном пути введения метаболиты АБ выделяются с желчью и слюной, оказывая влияние на облигатную микрофлору. С учетом причин возникновения болезни различают 2 формы ААД:
- Идиопатическая (ИААД). Развивается в результате негативного воздействия АБ на эубиоз желудочно-кишечного тракта. Влияние патогенных микроорганизмов на ЖКТ является одной из возможных причин развития данного заболевания. Среди многообразия возбудителей часто встречаются стафилококки, протеи, энтерококки, клостридии, грибы. Риск возникновения ААД увеличивается при длительном (более 10 дней), частом и неправильном приеме АБ (превышении дозы).
- Clostridium difficile-ассоциированная диарея (C. difficile-АД). Этиологически связана с нарушением микрофлоры и избыточным заселением ЖКТ условно-патогенными бактериями Clostridium difficile. Дисбактериоз возникает в результате приема АБ из группы цефалоспоринов, амоксициллина, линкомицина. Известны случаи развития внутригоспитальной антибиотик-ассоциированной инфекции путем передачи возбудителя через средства личной гигиены (полотенца, мыло, посуда), медицинский инструментарий при некачественной обработке.
Патогенез
Противомикробные препараты уменьшают рост и размножение не только патогенных, но и симбионтных микроорганизмов. Происходит уменьшение облигатной микрофлоры кишечника, развивается дисбактериоз. Данный факт лежит в основе патогенеза обоих видов антибиотик-ассоциированной диареи. При идиопатической форме также играет роль усиление моторики кишечника, токсическое поражение слизистой оболочки или нарушение обменных процессов в кишечнике.
Антибиотик-ассоциированный клостридиальный колит возникает вследствие изменения состава эндогенной нормофлоры ЖКТ при приеме цефалоспоринов III и IV поколения, фторхинолонов, пенициллинов. Дисбактериоз способствует размножению C. Difficile, которые в большом количестве выделяют 2 вида токсинов (А и В). Находясь в просвете ЖКТ, энтеротоксины разрушают эпителиоциты и вызывают воспалительные изменения стенки кишечника. Колит преимущественно поражает толстый кишечник с формированием диффузной гиперемии и отечности слизистой. Стенка ЖКТ утолщается, образуются налеты фибрина, имеющие вид желтоватых бляшек (псевдомембраны).
Классификация
Выделяют две формы идиопатической антибиотик-ассоциированной диареи: инфекционную и неинфекционную. Среди возбудителей инфекционной формы ААД часто встречаются клостридии перфрингенс, золотистый стафилококк, сальмонеллы, клебсиеллы, грибы рода Кандида. Неинфекционная ИААД представлена следующими видами:
- Гиперкинетическая. Клавуланат и его метаболиты увеличивают двигательную активность ЖКТ, прием макролидов вызывает сокращение 12-перстной кишки и антрального отдела желудка. Данные факторы способствуют появлению неоформленного стула.
- Гиперосмолярная. Развивается за счет частичного всасывания АБ (цефалоспоринов) или при нарушении углеводного обмена. В просвете кишечника накапливаются метаболиты углеводов, которые вызывают повышенную секрецию электролитов и воды.
- Секреторная. Формируется за счет нарушения эубиоза кишечника и деконъюгации желчных кислот. Кислоты стимулируют выделение воды и солей хлора в просвет кишки, следствием этих процессов является частый неоформленный стул.
- Токсическая. Формируется из-за негативного воздействия метаболитов пенициллинов и тетрациклинов на слизистую кишечника. Развивается дисбактериоз и диарея.
Проявления C. difficile-АД могут варьировать от бессимптомного носительства до молниеносно развивающихся и тяжелых форм. В зависимости от клинической картины, данных эндоскопии выделяют следующие виды антибиотик-ассоциированной клостридиальной инфекции:
- Диарея без колита. Проявляется неоформленным стулом без интоксикационного и абдоминального синдромов. Слизистая оболочка кишечника не изменена.
- Колит без псевдомембран. Характеризуется развёрнутой клинической картиной с умеренной дегидратацией и интоксикацией. При эндоскопическом исследовании наблюдаются катаральные воспалительные изменения в слизистой оболочке.
- Псевдомембранозный колит (ПМК). Данное заболевание характеризуется выраженной интоксикацией, дегидратацией, частым водянистым стулом и болями в животе. При колоноскопии определяется фибринозный налет и эрозивно-геморрагические изменения слизистой.
- Фульминантный колит
Симптомы ААД
При идиопатической антибиотик-ассоциированной диарее симптоматика возникает во время (у 70% пациентов) или после прекращения лечения антибиотиками. Основным, иногда единственным, проявлением болезни служит неоформленный стул до 3-7 раз в сутки без примесей крови и гноя. Редко отмечаются боли и чувство распирания в животе, метеоризм вследствие усиленной работы ЖКТ. Заболевание протекает без повышения температуры тела и симптомов интоксикации.
В отличие от идиопатической формы, клинический спектр проявлений Clostridium difficile-АД варьирует от бессимптомного колита до тяжелых фатальных форм болезни. Бактерионосительство выражается отсутствием симптоматики и выделением в окружающую среду клостридий с калом. Легкое течение заболевания характеризуется только жидким стулом без лихорадки и выраженного абдоминального синдрома. Чаще наблюдается C. difficile-ассоциированный колит средней степени тяжести, который проявляется повышением температуры тела, периодическими схваткообразными болями в околопупочной области, многократной диареей (10-15 раз/сутки).
Тяжелое течение болезни (ПМК) характеризуется частым (до 30 раз/сутки) обильным водянистым стулом, имеющим зловонный запах. Кал может содержать примеси слизи и крови. Болезнь сопровождается интенсивными абдоминальными болями, которые исчезают после акта дефекации. У пациентов отмечается ухудшение общего состояния, выраженная слабость и повышение температуры до 38-39°С. В 2-3% случаев регистрируется фульминантная форма заболевания, которая проявляется стремительным нарастанием симптомов, выраженной интоксикацией и появлением ранних тяжелых осложнений антибиотик-ассоциированной диареи.
Осложнения
Идиопатическая ААД хорошо поддается лечению и не вызывает осложнений у пациентов. Диарея, вызванная С.difficile, приводит к стойкому снижению артериального давления, развитию электролитных нарушений и обезвоживанию организма. Потери белка и воды способствуют возникновению отеков нижних конечностей и мягких тканей. Дальнейшее развитие болезни провоцирует появление мегаколона, изъявлений слизистой оболочки ЖКТ вплоть до перфорации толстой кишки, перитонита и сепсиса. Отсутствие своевременной диагностики и патогенетического лечения в 15-30% случаев приводит к летальному исходу.
Диагностика
При появлении обильного жидкого стула и дискомфорта в животе, вызывающих подозрение на развитие антибиотик-ассоциированной диареи, требуется консультация гастроэнтеролога. Специалист с помощью изучения анамнеза жизни и заболевания, физикального осмотра, данных лабораторных и инструментальных обследований составит соответствующее заключение.
Для диагностики идиопатической антибиотик-ассоциированной диареи достаточно выявить связь между приемом АБ и началом диареи, исключить сопутствующую патологию ЖКТ. В этом случае лабораторные показатели остаются нормальными, изменения слизистой оболочки кишечника отсутствуют. При подозрении на Clostridium difficile-ассоциированную диарею для подтверждения диагноза используются следующие методы:
- Лабораторные анализы крови. В общем анализе крови отмечается лейкоцитоз, увеличение СОЭ, анемия; в биохимическом — гипопротеинемия.
- Исследование кала. В копрограмме обнаруживаются лейкоциты и эритроциты. Основным диагностическим критерием заболевания служит выявление возбудителя в кале. Диагностикой выбора являются цитопатогенный тест (ЦТ) и реакция нейтрализации токсина (РНТ), которые определяют токсин В. Метод иммуноферментного анализа (ИФА) чувствителен к А и В-эндотоксинам. Полимеразная цепная реакция (ПЦР) используется для идентификации генов, кодирующих токсины. Культуральный метод позволяет обнаружить клостридии в посеве кала.
- Эндоскопия толстой кишки. Колоноскопию выполняют для визуализации патологических изменений кишечника (псевдомембран, фибриновых пленок, эрозий). Эндоскопическая диагностика при тяжелом колите может представлять опасность в связи с риском прободения кишки.
Диагностика антибиотик-ассоциированного расстройства стула обычно не вызывает трудностей. Идиопатическую форму болезни дифференцируют с пищевыми токсикоинфекциями легкой степени. Клиника C. difficile-ассоциированной диареи, а именно псевдомембранозного колита, может напоминать течение холеры, болезни Крона, язвенного колита и тяжелого пищевого отравления. Дополнительно проводят обзорную рентгенографию брюшной полости, КТ толстого кишечника.
Лечение ААД
Лечение неклостридиальной антибиотик-ассоциированной диареи предполагает отмену или снижение дозы антибактериального средства, назначение противодиарейных препаратов (лоперамид), эубиотиков и пробиотиков (лактобактерии, бифидобактерии). При многократных эпизодах жидкого стула целесообразно проводить нормализацию водно-солевого баланса.
Выявление клостридий диффициле является показанием для отмены АБ и назначения этиотропной, симптоматической и дезинтоксикационной терапии. Препаратом выбора для лечения заболевания является метронидазол. В тяжелых случаях и при непереносимости метронидазола назначают ванкомицин. Коррекция дегидратации и интоксикации осуществляется парентеральным введением водно-солевых растворов (ацесоль, р-р Рингера, регидрон и др.).
В комплексную терапию клостридиального колита входит использование энтеросорбентов, пробиотиков. Последние назначаются после проведения этиотропной терапии для восстановления нормофлоры кишечника курсом на 3-4 месяца. При осложнениях ПМК (перфорация кишки, мегаколон, рецидивирующее прогрессирующее течение колита) показано хирургическое лечение. Выполняют резекцию части или всей толстой кишки (гемиколэктомию, колэктомию).
Прогноз и профилактика
Прогноз идиопатической ААД благоприятный. Заболевание может купироваться самостоятельно после отмены антибиотиков и не требовать специфического лечения. При своевременной диагностике и адекватном лечении псевдомембранозного колита удается добиться полного выздоровления. Тяжелые формы диареи, игнорирование симптомов болезни могут повлечь осложнения как со стороны ЖКТ, так и всего организма.
Рациональная антибиотикотерапия предполагает прием медикаментов по строгим показаниям только при назначении врачом и под его тщательным контролем. Профилактика антибиотик-ассоциированной диареи включает применение пробиотиков для поддержания нормальной микрофлоры ЖКТ, рациональное питание и ведение активного образа жизни.
Антибиотикоассоциированный колит, тяжелого течения. Разбор клинического случая
Авторы клинического разбора:
Корнеева Ольга Николаевна — кандидат медицинских наук, врач клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии Первого МГМУ им И.М. Сеченова
Ивашкин Владимир Трофимович – академик РАМН, профессор, заведующий кафедрой проведевтики внутренних болезней и директор клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии Первого МГМУ им И.М. Сеченова.
В клинику обратился пожилой мужчина 62 лет с жалобами на жидкий стул до 8 раз в сутки, повышение температуры тела до 38-39С, боль в околопупочной области спастического характера, общую слабость и похудание на 7 кг в течение месяца.
Из анамнеза известно, что за 20 дней до момента поступления лечился в районной больнице по поводу бронхопневмонии. Проводилась антибиотикотерапия цефалоспорином III поколения. На фоне лечения пневмония разрешилась, и больной был выписан в удовлетворительном состоянии. Через 3 дня после окончания приема антибиотика отметил появление частого водянистого стула, появилась общая слабость. Пациент самостоятельно начал прием левомицетина и лоперамида. После чего наступило резкое ухудшение состояния — появилась лихорадка до 39С с ознобом, выраженная общая слабость, сохранялась диарея. Больной обратился к врачу поликлиники, где было рекомендовано исследование кала для исключения кишечных инфекций. Исследование кала на дизгруппу возбудителей кишечных инфекций не выявило. В связи с сохранением вышеперечисленных жалоб больной был госпитализирован в нашу клинику.
При объективном осмотре состояние средней тяжести, 38С, кожа и видимые слизистые бледные, язык сухой, живот увеличен в объеме за счет метеоризма, при пальпации умеренно болезненный по ходу толстой кишки.
Требовалось установить предварительный диагноз. Отрицательные результаты исследования кала на дизгруппу ставили под сомнение наличие кишечной инфекции, дебют воспалительных заболеваний кишечника у мужчины в 62 года представлялся маловероятным. Имеющиеся факторы риска антибиотикоассоциированного колита – прием антибиотиков, пожилой возраст, наличие сопутствующей патологии (ишемическая болезнь сердца, гипертоническая болезнь) свидетельствовали с высокой вероятностью о наличии антибиотикассоциированного колита, тяжелого течения (псевдомембранозный?).
Было начато обследование. В анализах крови обращали на себя внимание нормохромная железодефицитная анемия, лейкоцитоз со сдвигом лейкоцитарной формулы влево вплоть до миелоцитов, тромбоцитоз и ускорение СОЭ. Также выявлена гипонатриемия, гипоальбуминемия, снижение уровня железа, резкое повышение уровня С-реактивного белка, реакция кала на скрытую кровь с бензидином – положительная. При исследовании кала методом ИФА обнаружены токсины А и В C.difficile. Для исключения дилатации толстой кишки был сделан обзорный снимок брюшной полости в положении лежа – ширина петель в пределах нормы. При ультразвуковом исследовании брюшной полости обращало на себя внимание утолщение стенок толстой кишки до 10 мм. Утолщение стенок толстой кишки, сужение просвета кишки отмечалось и при компьютерной томографии органов брюшной полости.
При сигмоскопии: аппарат введен в сигмовидную кишку, на осмотренных участках слизистая умеренно гиперемирована, с множественными белесоватыми включениями. Слизистая прямой кишки гиперемирована, отёчна. Заключение: антибиотикоассоциированный колит (псевдомембранозный). (Рис. 2).

Рис. 2. Сигмоскопия
Морфологическая картина соответствовала псевдомембранозному колиту: выявлялся некроз эпителия, фибриновый выпот с нейтрофилами, типичные изъязвления слизистой напоминающие извержения вулкана, формирование псевдомембран (Рис.3).
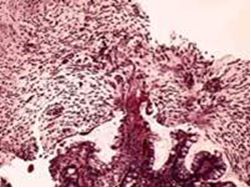
Рис. 3. Морфологическая картина псевдомембранозного колита
Таким образом, был установлен следующий клинический диагноз: Антибиотикоассоциированный колит, тяжелого течения (псевдомембранозный). Синдром нарушенного всасывания: железодефицитная анемия. Гипоальбуминемия.
Лечение больного включало регидратационную терапию, парентеральное питание, с дальнейшим переводом на энтеральное питание, метронидазолом 500 мг в/в каждые 6 ч, ванкомицином 250 мг 4 раза в сутки. Пробиотические препараты не назначались. На фоне лечения состояние больного улучшилось, нормализовалась температура тела, постепенно уменьшилась частота стула и общая слабость, больной прибавил в весе и был выписан в удовлетворительном состоянии.
Через 2 недели после выписки из стационара больному была назначена антибиотикотерапия после экстракции зуба, которая была прервана на 2-е сутки в связи с возникновением диареи. Больной обратился в нашу клинику. Был заподозрен рецидив C.difficile-ассоциированного колита, что было подтверждено обнаружением токсинов C.difficile в кале. Назначена терапия ванкомицином в начальной дозе 500 мг 2 раза в сутки с последующим постепенным снижением дозы в комбинации с пробиотическим препаратом Флорасан А по 1 капсуле 3 раза в день на 14 дней. Состояние больного быстро улучшилось, в течение 1 года наблюдения рецидивов диареи не отмечалось.
Пробиотические препараты (Флорасан А) оказывают отчетливый эффект в лечении антибиотикоассоциированного колита, что делает актуальным включение пробиотиков в схемы лечения. Важными элементами профилактики антибиотикоассоциированных поражений кишечника служат дифференцированное назначение антибиотиков под строгим и обязательным контролем врача, а также обязательное назначение пробиотиков одновременно с началом антибактериальной терапии.
Антибиотикоассоциированный колит: клинические рекомендации
Инфекция толстого кишечника, вызванная бактериями Clostridium difficile. Характеризуется воспалением толстого кишечника и формированием фибринозных пленок. Развивается у пациентов, у которых нормальная микрофлора кишечника была изменена в результате приема антибиотиков. Также известна как псевдомембранозный колит или заболевание, вызванное Clostridium difficile. В разделе описано методы диагностики и лечения только взрослых пациентов.
В 2018 году Институт клинических и лабораторных стандартов США сообщил об изменении названий вида бактерии, а именно с Clostridium difficile на Clostridioides difficile; однако это изменение еще не принято повсеместно.
Это раздел посвящен методам диагностики и лечения С. difficile инфекции лишь у взрослых пациентов.
Антибиотики широкого спектра действия нарушают нормальную микрофлору кишечника, наиболее частыми причинными агентами являются ампициллин, цефалоспорины, карбапенемы, клиндамицин, фторхинолоны. Колонизация Clostridium difficile происходит после такого нарушения нормальной микрофлоры кишечника путем перорального попадания внутрь термостойких спор, которые конвертируются в вегетативные формы в толстой кишке.
Передача в больничных условиях скорее всего является результатом распространения от человека к человеку орально-фекальным путем (например, через руки медицинских работников), через предметы (например, не тщательно очищенные подкладные судна или ректальные термометры) либо же непосредственно через зараженную среду. Пациенты с колонизацией (носительством), у которых не наблюдаются симптомы, также могут способствовать распространению возбудителя.
Патофизиология
Инкубационный период в общем составляет 2–3 дня, но может занимать также более недели. Clostridium difficile являются грамположительными анаэробными спорообразующими палочками, которые продуцируют токсины A и B. Эти токсины вызывают воспалительные реакции в толстой кишке, приводя к увеличению сосудистой проницаемости и формированию псевдомембраны. Псевдомембрана в толстом кишечнике имеет характерный внешний вид приподнятого желтого и белого налета, который обладает определенной адгезией, располагается на воспаленной слизистой оболочке, и состоит из нейтрофилов, фибрина, муцина и остатков разрушенных клеток.
Считается, что токсин A играет более важную роль в патогенезе по сравнению с токсином B, поскольку в экспериментальных моделях на животных было установлено, что токсин А провоцирует большее повреждение тканей и накопление жидкости. Считается, что токсин B выполняет свою роль только после того, как слизистая оболочка кишечника уже повреждена токсином A.
В зависимости от характера иммунной реакции организма хозяина и от того, является ли штамм Clostridium difficile токсикогенным, развивается либо бессимптомное состояние носительства, либо ассоциированное с Clostridium difficile заболевание. У бессимптомных носителей вероятность образования токсинов довольно низкая.
Клинические проявления обычно наблюдаются с 4-го по 9-й день антибактериальной терапии, но могут возникать и до 8-й недели после прекращения приема антибиотиков.
Организм ослабленных пациентов может быть не в состоянии проявить иммунный ответ в виде выработки иммуноглобулинов на воздействие токсина А.
Диагностика
Диагноз основан на точном анамнезе, физикальном осмотре и подтверждении соответствующими тестами. Диагноз следует рассматривать у пациентов с анамнезом недавнего применения антибиотиков, у которых есть диарея. Тестирование должно ограничиваться пациентами с недавно возникшей или диареей неясной этиологии (определяемой как 3 и более эпизода неоформленного кала в течение 24 часов). Молекулярное тестирование самостоятельно или в рамках многоэтапного алгоритма рекомендовано в зависимости от местных институциональных протоколов.
Анамнез
Пациенты пожилого возраста, у которых в анамнезе есть указание на лечение антибиотиками, сопутствующие заболевания (например, воспалительное заболевание кишечника, хроническая болезнь почек, ВИЧ-инфекция), длительная госпитализация, пребывание в доме престарелых, использование препаратов для понижения кислотности, трансплантация паренхиматозных органов или пересадка кроветворных стволовых клеток либо Clostridium difficile инфекция, подвержены особому риску.
Наиболее распространенными антибиотиками являются ампициллин, цефалоспорины, клиндамицин, карбапенемы и фторхинолоны, особенно в предшествующие 3 месяца. Пациенты часто жалуются на лихорадку, диарею, боль в брюшной полости, тошноту или рвоту.
Физикальное обследование
Возможно выявление признаков от незначительной или неадекватной абдоминальной чувствительности до признаков острой брюшной полости.
Системные симптомы шока, включая гипотонию и тахикардию, с сильной абдоминальной болью и чувствительностью указывают на молниеносный колит. Фульминантное заболевание определяется как сложный тяжелый случай заражения Clostridium difficile с высоким риском смерти.
Первоочередные тесты
При первичном обследовании нужно проводить общий анализ крови с лейкограммой, при котором обычно обнаруживают лейкоцитоз. Если уровень лейкоцитов очень высокий (30 000–50 000/мм³), пациент подвергается риску развития фульминантного колита.
Рентген брюшной полости следует проводить у пациентов со вздутием живота или симптомами и признаками, указывающими на инфекцию. Это может выявить расширение толстой кишки.
Образцы стула следует собирать в ходе первичного исследования и проверять на наличие скрытой крови.
Довольно сложно отличить Clostridium difficile инфекцию и бактериальную колонизацию, поэтому нет конечных сведений относительно лучшего диагностического метода. Тест позволяет обнаружить сам микроорганизм (например, метод амплификации нуклеиновых кислот, в частности ПЦР кала, иммуноанализ на глутаматдегидрогеназу [ГДГ], либо токсиногенную культуру) или основные токсины (например, иммунологический анализ на токсин А и В фермент, тест на нейтрализацию цитотоксичности клеточной культуры) непосредственно в фекалиях. Молекулярная диагностика, наиболее распространенный метод, не позволяет дифференцировать инфекцию с бактериальной колонизацией). Он отличается высокой чувствительностью и низкой/средней специфичностью. Таким образом, с целью корректной диагностики, необходимо применять тест пациентам с недавно возникшей диареей неясной этиологии (3 и более эпизодов неоформленного кала в течение 24 часов) которые не принимают слабительные препараты; однако нет достаточных сведений относительно целесообразности этой рекомендации. В случае согласия медицинских работников и представителей лаборатории относительно критериев отбора фекалий, рекомендовано проведение лишь МАНК, поскольку это наиболее чувствительный метод диагностики образцов кала для пациентов с C. difficile инфекцией (согласно клиническим симптомам). Однако если нет заранее согласованного критерия для исследования фекалий, в качестве этапа многостадийного алгоритма рекомендовано исследование на токсины в кале (например, ГДГ плюс токсин; ГДГ плюс токсин с помощью МАНК; либо же МАНК плюс токсин) , а не просто МАНК. Не следует повторять исследование в течение 7 дней такого же эпизода диареи, исследование бессимптомных пациентов не требуется.
Согласно европейским рекомендациям следует применять двухэтапный алгоритм, начиная с высокочувствительного теста (например, МАНК или ГДГ иммуноферментный анализ), и в случае положительного результата требуется подтверждение с помощью высокоспецифичных тестов (иммуноферментный анализ на токсин А/В). В качестве альтернативы образцы могут быть исследованы с помощью иммуноферментного анализа на ГДГ и токсин А/В.
Последующие исследования
Сигмоидоскопия или колоноскопия показаны пациентам в случае неэффективности терапии либо же отрицательного результата иммуноферментного анализа, или когда подозревают другие причины, такие как ишемический колит.
КТ брюшной полости показана пациентам со вздутием живота, усилением боли, отсутствием перистальтики.
Неотложные исследования
С целью дифференцирования воспалительной и не воспалительной этиологии диареи на данный момент активно используют фекальные биомаркеры, в частности кальпротектин и лактоферрин. Пока недостаточно сведений относительно рекомендации использования этих биомаркеров в диагностике C. difficile инфекции.
Дифференциальная диагностика
| Заболевание | Дифференциальные признаки/симптомы | Дифференциальные обследования |
|
|
|
|
|
|
|
| |
|
|
|
Лечение
Основная цель лечения — прекратить применение противомикробного агента и начать соответствующую терапию.
Все пациенты, которые еще не госпитализированы, должны быть госпитализированы, если у них нет системных клинических проявлений и органной дисфункции, когда их можно было лечить в амбулаторном режиме. Большинство рекомендаций, содержащихся в этом разделе, основано на рекомендациях Общества инфекционных болезней США (IDSA)/Американского общества эпидемиологии здравоохранения, опубликованных в начале 2018 года.
Профилактика инфекции и контроль
Госпитализированные пациенты с подтвержденной инфекцией либо с подозрением на инфекцию должны быть изолированы в отдельной комнате с отдельным туалетом для предотвращения заражения других пациентов. В учреждениях с недостаточным количеством отдельных комнат принимать должны в первую очередь пациентов с симптомами недержания стула. Важно применять меры контактной предосторожности в отношении пациентов с подозрением на инфекцию, аж до получения результатов исследований. Меры контактной предосторожности следует применять на протяжении 48 часов после прекращения диареи и аж до выписки, если уровень заражения Clostridium difficile остается высоким.
Медицинским работниками следует использовать халаты и перчатки для входа в палату, при уходе за пациентами. Следует соблюдать гигиену рук перед и после контакта с пациентом, а также после снятия перчаток. Следует применять мыло и воду, либо моющее средство на основе этилового спирта. Также следует поощрять пациентов мыть руки, и принимать душ с целью уменьшения количества спор возбудителя на коже. При лечении пациента следует использовать одноразовое приспособление (ректальные термометры не рекомендованы).
ВОЗ (Всемирна организация здравоохранения) утвердила инструкции относительно правильной техники мытья рук. Было обнаружено, что поэтапная техника мытья рук более эффективна при борьбе с Clostridium difficile, чем неструктурированная техника.
Прекращение приема провоцирующего препарата
При первом же предположении относительно диагноза следует как можно скорее прекратить прием провоцирующих антибиотиков. Если антибиотики не могут быть отменены, следует заменить препарат, который менее вероятно вызовет инфекцию Clostridium difficile. В особенности следует избегать применения ампициллина, цефалоспоринов, клиндамицина, карбапенемов, а также фторхинолонов.
Симптоматическая терапия
Первоначально следует оценить уровень гидратации пациента, особенно в случае госпитализации. При необходимости следует использовать заместительную терапию с целью восстановления жидкостного и электролитного баланса. Следует избегать применения антиперистальтических препаратов, в частности опиоидов и лоперамида, хотя и нет данных относительно этой рекомендации.
Антибиотикотерапия
В случае отложенного получения результатов лабораторного анализа (>48 часов) либо при фульминантном колите следует применять эмпирическую антибиотикотерапию. В иных случаях антибиотикотерапию следует начинать после постановки диагноза с целью ограничения чрезмерного использования антибиотиков. Рекомендованные схемы лечения зависят от тяжести заболевания, а также от того, является это первичным эпизодом или рецидивом.
Согласно рекомендациям США в качестве препарата первой линии следует принимать пероральный ванкомицин или фидаксомицин в случае первичного эпизода C. difficile инфекции. Ранее антибиотиком первого выбора был пероральный метронидазол; однако теперь его применение рекомендовано лишь в случае невозможности использования препаратов первой линии.
- Первичный эпизод: не тяжелое течение
- Поддерживающие клинические данные: лейкоцитоз с уровнем лейкоцитов ≤15 000 клеток/ мл и креатинин сыворотки <0,13 ммоль/л (<1,5 мг/дл)
- Лечение первой линии: пероральный ванкомицин или фидаксомицин в течение 10 дней.
- Альтернативная терапия: пероральный метронидазол в течение 10 дней
- Первичный эпизод: тяжелое течение
- Поддерживающие клинические данные: лейкоцитоз с уровнем лейкоцитов ≥15 000 клеток/ мл и креатинин сыворотки >0,13 ммоль/л (>1,5 мг/дл)
- Лечение первой линии: пероральный ванкомицин или фидаксомицин в течение 10 дней.
- Первичный эпизод: молниеносное течение (тяжелая, осложненная инфекция).
- Поддерживающие клинические данные: гипотензия, шок, кишечная непроходимость или мегаколон
- Терапия первой линии: пероральный ванкомицин (доза выше, чем при не молниеносном течении) Если есть кишечная непроходимость, следует рассмотреть ректальное введение ванкомицина. Внутривенное вливание метронидазола следует проводить параллельно с пероральным/ректальным приемом ванкомицина, особенно в случае кишечной непроходимости, поскольку это может препятствовать поступлению перорального ванкомицина в толстый отдел кишечника.
- Альтернативное лечение: тигециклин или иммуноглобулины применяли у пациентов с неэффективной терапией первой линии, но пока еще не проводили контролируемых клинических исследований относительно такого подхода.
Международные принципы все так же могут рекомендовать метронидазол в качестве препарата первой линии при неосложненном течении. Например, согласно Европейским рекомендациям, метронидазол следует принимать в качестве препарата первой линии при не осложненном течении заболевания (наряду с ванкомицином или фидаксомицином как альтернативными агентами) и ванкомицин в качестве препарата первой линии при тяжелом течении. Министерство здравоохранения Англии в Великобритании также поддерживает эти рекомендации.
Эти рекомендации предшествовали руководствам IDSA/SHEA, опубликованным в начале 2018 года. Следует руководствоваться местными клиническими рекомендациями. Согласно метаанализу установлены достоверные данные относительно значительного превосходства фидаксомицина над ванкомицином в достижении стойкого разрешения симптоматики (определяется как количество пациентов с прекращением диареи минус количество пациентов с рецидивом или летальным исходом) у взрослых с не умноженной рекуррентной инфекцией. Таким образом, этот препарат считается лучшим чем ванкомицин в качестве терапевтического агента во всех случаях, кроме тяжелых инфекций. Показатели эффективности лечения метронидазолом были значительно меньше по сравнению с ванкомицином и фидаксомицином.
Согласно одному из Кокрановских обзоров установлено, что применение ванкомицина превосходит применение метронидазола, а фидаксомицин лучше ванкомицина по достижению симптоматического эффекта у пациентов с C. difficile инфекцией, хоть разница в эффективности этих препаратов незначительна. Не было сделано никаких окончательных выводов относительно эффективности лечения антибиотиками при тяжелых заболеваниях, поскольку большинство исследований исключали этих пациентов. Нет никаких выводов относительно необходимости лечения антибиотиками у пациентов с легкой инфекцией помимо потребности в прекращении приема этиологически значимого антибиотика, их нельзя сделать из-за отсутствия в обзоре контрольных исследований без лечения.
Данные свидетельствуют о том, что фидаксомицин эффективней в лечении легкой либо умеренной формы C. difficile инфекции, и что этот препарат лучше, чем пероральный ванкомицин, из-за устойчивости клинической реакции и снижения частоты рецидивов.
У пациентов с ВЗК (воспалительным заболеванием кишечника) на фоне инфекции следует применять ванкомицин или фидаксомицин. Также необходимо госпитализировать таких пациентов и проводить агрессивную терапию. Решение относительно прекращения или продолжения приема иммунодепрессантов у пациентов с ВЗК во время острой инфекции следует принимать в зависимости от конкретного случая.
Применение нитазоксанида и фузидиевой кислоты оказалось эффективным в лечении первичного эпизода C. difficile инфекции, однако пока недостаточно поддерживающих данных. Нет данных, поддерживающих применение рифаксимина, тигециклина или бацитрацина в лечении первичного эпизода заболевания.
Хирургическое вмешательство
У пациентов, которые не реагируют на антибиотикотерапию при фульминантной форме болезни, может быть оправдана хирургия.
Фульминантное заболевание часто недооценивают по причине недостаточной осведомленности о его тяжести и неспецифическом клиническом синдроме, а ведь оно является опасным для жизни. Своевременная диагностика и лечение являются ключевыми факторами положительного исхода, а раннее хирургическое вмешательство должно рассматриваться в случаях неэффективности терапии либо при повышении уровня лейкоцитов и лактата. Хирургической процедурой выбора является субтотальная колэктомия с сохранением прямой кишки. Илеостомия по Торнболлу (с последующим лаважем толстого кишечника при помощи антеградного промывания ванкомицином) является альтернативным подходом к лечению.
Рецидивирующая инфекция
Частота рецидивов варьирует от 5 до 50%, хотя одно исследование показало, что как минимум один рецидив заболевания отмечается в 21% случаев госпитальных инфекций, и в 14% случаев внегоспитальных инфекций.
Приблизительно у 25% пациентов, которым проводили лечение ванкомицином при первичном эпизоде, отмечался рецидив.
Выбор подхода к лечению зависит от терапии первичного эпизода. Первый рецидив могут лечить с помощью таких режимов антибиотикотерапии:
- Пролонгированная, с импульсным и постепенным снижением дозы, пероральная антибиотикотерапия с помощью ванкомицина (если пероральный ванкомицин использовался при первичном эпизоде).
- Стандартный 10-дневный курс фидаксомицина (если пероральный ванкомицин использовали при лечении первичного эпизода).
- Стандартный 10-дневный курс перорального ванкомицина (если метронидазол использовали при лечении первичного эпизода).
Исследования показали возможное снижение вероятности рецидива у пациентов с не-B1/NAP1 штаммом при лечении фидаксомицином по сравнению с ванкомицином.Лечение последующих рецидивов возможно при использовании следующих режимов антибиотикотерапии:
- Пролонгированный, с постепенным снижением и импульсным дозированием перорального ванкомицина.
- Стандартный 10-дневный курс перорального ванкомицина с последующим приемом рифаксимина на протяжении 20 дней.
- Стандартный 10-дневный курс фидаксомицина.
Трансплантация фекальной микробиоты (ТФМ) является альтернативным подходом к лечению пациентов с двумя случаями рецидива и при неэффективности антибиотикотерапии.
Процедура состоит из имплантации обработанных фекалий здорового донора в кишечный тракт инфицированного пациента с целью корректирования кишечного дисбактериоза. Применение непродолжительного вступительного курса перорального ванкомицина может быть целесообразным для снижения нагрузки C. difficile у пациентов, которым не проводят антибиотикотерапию до запланированного ТФМ (трансплантация фекальной микробиоты). Рандомизированные контролируемые клинические испытания показали высокий уровень эффективности.
Согласно систематическому обзору рандомизированных клинических исследований достаточно достоверно установлено, что ТФМ эффективней, чем ванкомицин или плацебо. Замороженная ТФМ обладает такой же эффективностью по прекращению диареи как трансплантация свежей фекальной микробиоты. Трансплантация в нижней части ЖКТ может быть таким же эффективным как в верхний. ТФМ в общем хорошо переносится организмом, но среди побочных явлений могут наблюдаться лихорадка, абдоминальная чувствительность или дискомфорт, вздутие, тошнота/рвота, диарея/запор, а также инфекционные осложнения. Долгосрочные последствия неизвестны. Недостаточно данных относительно рекомендаций ТФМ при тяжелом течении болезни.
Британское общество гастроэнтерологии/Общество инфекционных болезней поддерживают текущее руководство прибегать к ТФМ в качестве лечения второй линии. В частности, они рекомендуют проведение ТФМ в следующих случаях:
- Пациенты с рекуррентной инфекцией, у которых отмечались по крайней мере два рецидива.
- Пациенты с рекуррентной инфекцией, которые имели один рецидив, а также с факторами риска возникновения таких эпизодов в дальнейшем (например, тяжелая/осложненная инфекция).
- Рефрактерное инфекционное заболевание
Однако они добавили, что ТФМ следует рассматривать только после разрешения первичного эпизода, который лечили с помощью по крайней мере 10-дневного курса корректно подобранных антибиотиков, также перед ТФМ рекомендовано проведение пролонгированной/с импульсным дозированием режима ванкомицина и/или фидаксомицина. Кроме того, пациентам с тяжелым либо осложненным течением инфекции перед ТФМ должен быть предложен препарат, который мене вероятно вызовет рецидив в дальнейшем (например, фидаксомицин, безлотоксумаб). Его следует использовать с осторожностью у пациентов с ослабленным иммунитетом. Замороженная ТФМ предпочтительнее свежей, а повторное лечение может быть предложено в случае неэффективности первоначального Следует избегать применения у пациентов с анафилактической пищевой аллергией.
Безлотоксумаб, человеческое моноклональное антитело, которое связывается с токсином В Clostridium difficile, одобрен в США и Европе, чтобы уменьшить рецидив инфекции Clostridium difficile у взрослых, которые получают антибактериальное лечение от инфекции Clostridium difficile и имеют высокий риск рецидива. Тем не менее, его место в терапии в настоящее время неясно, и он по-прежнему считается новым видом лечения.
Колит после приема антибиотиков, антибиотикоассоциированный, спаечный
Опубликовано: 29 сентября 2015 в 14:23  Как известно многим, антибиотики надо принимать строго по назначению врача и с большой осторожностью. Помимо того, что они убивают плохие бактерии, и вирусы, они могут нанести значительный урон хорошим и полезным бактериям. После приема антибиотиков возникает псевдомембранозный (антибиотикоассоциированный) колит.
Как известно многим, антибиотики надо принимать строго по назначению врача и с большой осторожностью. Помимо того, что они убивают плохие бактерии, и вирусы, они могут нанести значительный урон хорошим и полезным бактериям. После приема антибиотиков возникает псевдомембранозный (антибиотикоассоциированный) колит.
Антибиотикоассоциированный колит – это воспаление кишечника, носящее очень тяжелый характер, возникающее после длительного приема антибиотиков. Для подобного вида колита характерен специфический дисбактериоз и фиброзные налеты. Фиброзные налеты по-другому называют псевдомембранами, отсюда и название псевдомембранозный колит.
В тяжелых случаях у сильно ослабленных больных наблюдается интоксикационный синдром, обезвоживание с нарушением электролитов, развитие грубых поражений кишечных стенок, что в результате приводит к прободению.
Причины антибиотикоассоциированного колита
 Основная причина возникновения колита после приема антибиотиков – это сама длительная терапия данными препаратами. Существует даже распределение лекарств, которые, так или иначе, влияют на появление колита. К самым опасным относят: Клиндамицин, Линкомицин. Наименее опасны: Тетрациклин, Цефалоспорин, Ампициллин, Эритромицин, Левомицетин, Пенициллин.
Основная причина возникновения колита после приема антибиотиков – это сама длительная терапия данными препаратами. Существует даже распределение лекарств, которые, так или иначе, влияют на появление колита. К самым опасным относят: Клиндамицин, Линкомицин. Наименее опасны: Тетрациклин, Цефалоспорин, Ампициллин, Эритромицин, Левомицетин, Пенициллин.
Но даже здесь существуют разногласия между специалистами. Некоторые из них считают, что такой колит могут провоцировать все антибиотики и к тому же к ним еще добавляют слабительные средства и ряд цитостатиков. Специфический дисбактериоз – основная характерная черта. Развивается дисбактериоз с преобладанием микроорганизма – Clostridium difficile. Такая патогенная бактерия обнаруживается у 3% здорового населения разных возрастов. По большей части этот процент делят между собой дети и новорожденные. Подтверждение этому 50% инфицированных – это дети младшей возрастной группы.
Самое интересное, что подобная бактерия свойственна не только человеческому организму, но и животным, независимо от того, домашние это животные или дикие. А еще она может находиться даже в обычной почве.
То, что антибиотики способствуют развитию колита, это мы выяснили, а вот какая форма опаснее? По многим данным выясняется, что лекарства, которые были получены инъекционным путем, намного опаснее.
Самая опасная причина – это наличие бактерии Clostridium difficile. Эта бактерия, находясь в организме, выделяет токсины, которые плохо влияют на эпительный покров кишечной стенки. Влияние подобных токсинов усиливают антибиотики.
Факторы, способствующие развитию колита после антибиотиков:
- Возрастная группа более 65 лет;
- Имеющиеся тяжелые патологии, например, онкология;
- Почечная недостаточность;
- Обширные хирургические вмешательства;
- Лечение в отделениях интенсивной терапии.
Симптомы колита после антибиотиков
 В легких случаях специфическая диарея возникает после приема антибиотиков. При этом симптоматика полностью исчезает, если полностью отменить прием этих лекарств.
В легких случаях специфическая диарея возникает после приема антибиотиков. При этом симптоматика полностью исчезает, если полностью отменить прием этих лекарств.
В среднетяжелых и тяжелых случаях симптоматика продолжает проявляться даже после отмены антибиотикотерапии еще в течение 10 дней.
Главный симптом, свойственный псевдомембранозному колиту – это водянистая диарея. При тяжелых формах развития диарея может принимать вид рисового отвара. Вследствие такой водянистой диареи развиваются сопутствующие клинические проявления: тахикардия, парестезия, судороги и сниженный тонус мышц.
Кровавые выделения (кровавый понос) могут появляться только в тяжелых случаях колита. Обезвоживание и длительная диарея после антибиотиков также сопровождается рядом симптомов интоксикации:
- Повышенная температура тела (часто не более 38 градусов).
- Головная боль.
- Снижение аппетита.
- Общая слабость.
- Схваткообразные боли.
Локализуется схваткообразная боль чаще в месте нахождения сигмовидной кишки. Это левая нижняя часть живота.
Лечение колита после приема антибиотиков
 Начальный диагноз антибиотикоассоциированного колита ставится на основании анамнеза. Анамнез включает в себя перечень жалоб пациента и выявление симптомов. Основными направляющими являются появление диареи, с выраженной интоксикацией, после прекращения приема антибиотиков.
Начальный диагноз антибиотикоассоциированного колита ставится на основании анамнеза. Анамнез включает в себя перечень жалоб пациента и выявление симптомов. Основными направляющими являются появление диареи, с выраженной интоксикацией, после прекращения приема антибиотиков.
После анамнеза для утверждения начального диагноза проводят лабораторные и другие исследования. Общий анализ крови должен выявить высокий лейкоцитоз. При тяжелой форме копрологическое исследование обнаружит наличие крови в кале, положительную реакцию на белок и большое количество лейкоцитов и слизи. При исследовании кала на бактерии обнаруживается бактерия Clostridium difficile, если нет, то это еще не значит, что антибиотикоассоциированный колит отсутствует.
Эндоскопия при диагностике колита – обязательный этап исследования. Если воспалились нижние отделы кишечника, то можно ограничиться ректороманоскопией. Что можно обнаружить? Такое исследование даст точную картину по воспалению, а точнее воспалена ли слизистая кишечника, существует ли налет?
Лечение колита после приема антибиотиков включает несколько этапов:
- Диета – обязательное условие в лечении антибиотикоассоциированного колита. Первые дни, возможно, придется поголодать, после потихоньку включать в рацион продукты, разрешенные врачом.
- Этиотропное лечение. Обязательно следует прекратить прием антибиотиков. Основное направление – это уничтожение бактерии, провоцирующей развитие заболевания.
- Коррекция дисбактериоза. Чтобы не усугублять положение больного, следует немедленно остановить диарею бактериальными препаратами.
- Патогенетическая терапия. Эта терапия направлена на лечение и предотвращение основных синдромов болезни: обезвоживание, интоксикация, нарушение белкового и электролитного обмена.
- Симптоматическая терапия – направлена на ослабление и полное уничтожение симптомов болезни.
- Хирургическое вмешательство. Возможно только в серьезных, тяжелых случаях течения болезни. Например, в случае сильных осложнений: прободение, токсическое расширение кишечника и прочие.
Спаечный колит
 Спаечный колит – это воспаление кишечника, вызванное в результате образования – спаек. Спайки в большинстве случаев находятся в брюшной полости между органами или петлями кишечника. Спаечный колит характеризуется тем, что эти образования спаивают серозные оболочки между собой.
Спаечный колит – это воспаление кишечника, вызванное в результате образования – спаек. Спайки в большинстве случаев находятся в брюшной полости между органами или петлями кишечника. Спаечный колит характеризуется тем, что эти образования спаивают серозные оболочки между собой.
Заболевание появляется:
- После беременности.
- После хирургических операций.
- После травм живота и органов, находящихся в брюшной полости.
- После острых, хронических и воспалительных заболеваний.
Симптомы болезни:
- Может протекать бессимптомно.
- Возможен дискомфорт, вроде болевых ощущений, похожих на язву. Часто боль возникает после тяжелых, физических нагрузок.
- При остром течении предполагается непроходимость тонкого кишечника. По-другому, ее называют спаечной непроходимостью: боль в животе, рвота, отсутствие стула, вздутие из-за невозможности газам выйти наружу.
Такой вид колита предполагает длительную терапию. В зависимости от формы развития болезни ее можно лечить как дома, так и в больнице (стационаре). При легких формах развития пациентам рекомендуют прибегать к самолечению народными способами и никаких антибиотиков. Даже доктора считают этот способ более безопасным, нежели использование медикаментов. В тяжелых случаях без операции не обойтись. Удалять спаечные образования обязательно. При этом операция проводится через большой разрез или лапараскопическую операцию.
Антибиотик-ассоциированная диарея — Медицинский справочник
Антибиотик-ассоциированная диареяАнтибиотик-ассоциированная диарея — заболевание, которое характеризуется появлением неоформленного стула во время или после приема антибактериальных препаратов. Болезнь сопровождается диспепсической симптоматикой (послаблением стула, газообразованием). В тяжелых случаях появляются интенсивные боли в животе, слабость, лихорадка. Диагностика основывается на установлении связи приема АБ с развитием диареи. Дополнительно проводят анализ кала, эндоскопическое исследование кишечника. Лечение предполагает отмену АБ, назначение пробиотиков и дезинтоксикационных препаратов. При выявлении возбудителя болезни проводят этиотропную антибактериальную терапию.
Антибиотик-ассоциированная диареяАнтибиотик-ассоциированная диарея
Антибиотик-ассоциированная диарея (ААД, нозокомиальный колит) — три и более эпизода жидкого стула, повторяющиеся на протяжении не менее двух дней и связанные с приемом антибактериальных препаратов (АБ). Расстройство может проявляться в течение 4-х недель после отмены АБ. В развитых странах поражение кишечника является наиболее частой реакцией на антибиотикотерапию: у лиц, принимающих антибиотики, ААД встречается в 5-30% случаев. Патология протекает как в легкой самокупирующейся форме, так и в виде тяжелого затяжного колита. В гастроэнтерологии не менее 70% случаев заболевания приходится на идиопатическую ААД, 30% — на Clostridium difficile-ассоциированную диарею. Болезнь в равной степени поражает мужчин и женщин.
Причины антибиотик-ассоциированной диареи
Заболевание чаще развивается после назначения антибиотиков пенициллинового ряда, тетрациклинов, цефалоспоринов. Способ введения лекарств практически не влияет на вероятность появления диареи. При пероральном приеме медикаменты воздействуют на слизистый слой ЖКТ. При парентеральном пути введения метаболиты АБ выделяются с желчью и слюной, оказывая влияние на облигатную микрофлору. С учетом причин возникновения болезни различают 2 формы ААД:
- Идиопатическая (ИААД). Развивается в результате негативного воздействия АБ на эубиоз желудочно-кишечного тракта. Влияние патогенных микроорганизмов на ЖКТ является одной из возможных причин развития данного заболевания. Среди многообразия возбудителей часто встречаются стафилококки, протеи, энтерококки, клостридии, грибы. Риск возникновения ААД увеличивается при длительном (более 10 дней), частом и неправильном приеме АБ (превышении дозы).
- Clostridium difficile-ассоциированная диарея (C. difficile-АД). Этиологически связана с нарушением микрофлоры и избыточным заселением ЖКТ условно-патогенными бактериями Clostridium difficile. Дисбактериоз возникает в результате приема АБ из группы цефалоспоринов, амоксициллина, линкомицина. Известны случаи развития внутригоспитальной антибиотик-ассоциированной инфекции путем передачи возбудителя через средства личной гигиены (полотенца, мыло, посуда), медицинский инструментарий при некачественной обработке.
Помимо прямого воздействия антибактериальных средств на стенку кишечника, существуют факторы риска, увеличивающие вероятность развития болезни. К ним относят детский и пожилой возраст, наличие тяжелой соматической патологии (сердечная, почечная недостаточность), бесконтрольный прием антацидных препаратов, врожденные и приобретенные иммунодефицитные состояния, хирургические вмешательства на брюшной полости, зондовое питание. Хронические заболевания ЖКТ (болезнь Крона, неспецифический язвенный колит) также способствуют возникновению антибиотик-ассоциированного колита.
Патогенез
Противомикробные препараты уменьшают рост и размножение не только патогенных, но и симбионтных микроорганизмов. Происходит уменьшение облигатной микрофлоры кишечника, развивается дисбактериоз. Данный факт лежит в основе патогенеза обоих видов антибиотик-ассоциированной диареи. При идиопатической форме также играет роль усиление моторики кишечника, токсическое поражение слизистой оболочки или нарушение обменных процессов в кишечнике.
Антибиотик-ассоциированный клостридиальный колит возникает вследствие изменения состава эндогенной нормофлоры ЖКТ при приеме цефалоспоринов III и IV поколения, фторхинолонов, пенициллинов. Дисбактериоз способствует размножению C. Difficile, которые в большом количестве выделяют 2 вида токсинов (А и В). Находясь в просвете ЖКТ, энтеротоксины разрушают эпителиоциты и вызывают воспалительные изменения стенки кишечника. Колит преимущественно поражает толстый кишечник с формированием диффузной гиперемии и отечности слизистой. Стенка ЖКТ утолщается, образуются налеты фибрина, имеющие вид желтоватых бляшек (псевдомембраны).
Классификация
Выделяют две формы идиопатической антибиотик-ассоциированной диареи: инфекционную и неинфекционную. Среди возбудителей инфекционной формы ААД часто встречаются клостридии перфрингенс, золотистый стафилококк, сальмонеллы, клебсиеллы, грибы рода Кандида. Неинфекционная ИААД представлена следующими видами:
- Гиперкинетическая. Клавуланат и его метаболиты увеличивают двигательную активность ЖКТ, прием макролидов вызывает сокращение 12-перстной кишки и антрального отдела желудка. Данные факторы способствуют появлению неоформленного стула.
- Гиперосмолярная. Развивается за счет частичного всасывания АБ (цефалоспоринов) или при нарушении углеводного обмена. В просвете кишечника накапливаются метаболиты углеводов, которые вызывают повышенную секрецию электролитов и воды.
- Секреторная. Формируется за счет нарушения эубиоза кишечника и деконъюгации желчных кислот. Кислоты стимулируют выделение воды и солей хлора в просвет кишки, следствием этих процессов является частый неоформленный стул.
- Токсическая. Формируется из-за негативного воздействия метаболитов пенициллинов и тетрациклинов на слизистую кишечника. Развивается дисбактериоз и диарея.
Проявления C. difficile-АД могут варьировать от бессимптомного носительства до молниеносно развивающихся и тяжелых форм. В зависимости от клинической картины, данных эндоскопии выделяют следующие виды антибиотик-ассоциированной клостридиальной инфекции:
- Диарея без колита. Проявляется неоформленным стулом без интоксикационного и абдоминального синдромов. Слизистая оболочка кишечника не изменена.
- Колит без псевдомембран. Характеризуется развёрнутой клинической картиной с умеренной дегидратацией и интоксикацией. При эндоскопическом исследовании наблюдаются катаральные воспалительные изменения в слизистой оболочке.
- Псевдомембранозный колит (ПМК). Характеризуется выраженной интоксикацией, дегидратацией, частым водянистым стулом и болями в животе. При колоноскопии определяется фибринозный налет и эрозивно-геморрагические изменения слизистой.
- Фульминантный колит. Наиболее тяжелая форма антибиотик-ассоциированного расстройства ЖКТ. Развивается молниеносно (от нескольких часов до суток). Вызывает серьезные гастроэнтерологические и септические нарушения.
Симптомы антибиотик-ассоциированной диареи
При ИААД симптоматика возникает во время (у 70% пациентов) или после прекращения лечения антибиотиками. Основным, иногда единственным, проявлением болезни служит неоформленный стул до 3-7 раз в сутки без примесей крови и гноя. Редко отмечаются боли и чувство распирания в животе, метеоризм вследствие усиленной работы ЖКТ. Заболевание протекает без повышения температуры тела и симптомов интоксикации.
В отличие от идиопатической формы, клинический спектр проявлений Clostridium difficile-АД варьирует от бессимптомного колита до тяжелых фатальных форм болезни. Бактерионосительство выражается отсутствием симптоматики и выделением в окружающую среду клостридий с калом. Легкое течение заболевания характеризуется только жидким стулом без лихорадки и выраженного абдоминального синдрома. Чаще наблюдается C. difficile-ассоциированный колит средней степени тяжести, который проявляется повышением температуры тела, периодическими схваткообразными болями в околопупочной области, многократной диареей (10-15 раз/сутки).
Тяжелое течение болезни (ПМК) характеризуется частым (до 30 раз/сутки) обильным водянистым стулом, имеющим зловонный запах. Кал может содержать примеси слизи и крови. Болезнь сопровождается интенсивными абдоминальными болями, которые исчезают после акта дефекации. У пациентов отмечается ухудшение общего состояния, выраженная слабость и повышение температуры до 38-39°С. В 2-3% случаев регистрируется фульминантная форма заболевания, которая проявляется стремительным нарастанием симптомов, выраженной интоксикацией и появлением ранних тяжелых осложнений антибиотик-ассоциированной диареи.
Осложнения
Идиопатическая ААД хорошо поддается лечению и не вызывает осложнений у пациентов. Диарея, вызванная С.difficile, приводит к стойкому снижению артериального давления, развитию электролитных нарушений и обезвоживанию организма. Потери белка и воды способствуют возникновению отеков нижних конечностей и мягких тканей. Дальнейшее развитие болезни провоцирует появление мегаколона, изъявлений слизистой оболочки ЖКТ вплоть до перфорации толстой кишки, перитонита и сепсиса. Отсутствие своевременной диагностики и патогенетического лечения в 15-30% случаев приводит к летальному исходу.
Диагностика
При появлении обильного жидкого стула и дискомфорта в животе необходимо посетить гастроэнтеролога. Специалист с помощью изучения анамнеза жизни и заболевания, физикального осмотра, данных лабораторных и инструментальных обследований составит соответствующее заключение. Для диагностики идиопатической антибиотик-ассоциированной диареи достаточно выявить связь между приемом АБ и началом диареи, исключить сопутствующую патологию ЖКТ. В этом случае лабораторные показатели остаются нормальными, изменения слизистой оболочки кишечника отсутствуют.
При подозрении на Clostridium difficile-ассоциированную диарею для подтверждения диагноза используются следующие методы:
- Лабораторные анализы крови. В общем анализе крови отмечается лейкоцитоз, увеличение СОЭ, анемия; в биохимическом — гипопротеинемия.
- Исследование кала. В копрограмме обнаруживаются лейкоциты и эритроциты. Основным диагностическим критерием заболевания служит выявление возбудителя в кале. Диагностикой выбора являются цитопатогенный тест (ЦТ) и реакция нейтрализации токсина (РНТ), которые определяют токсин В. Метод иммуноферментного анализа (ИФА) чувствителен к А и В-эндотоксинам. Полимеразная цепная реакция (ПЦР) используется для идентификации генов, кодирующих токсины. Культуральный метод позволяет обнаружить клостридии в посеве кала.
- Эндоскопия толстой кишки. Колоноскопию выполняют для визуализации патологических изменений кишечника (псевдомембран, фибриновых пленок, эрозий). Эндоскопическая диагностика при тяжелом колите может представлять опасность в связи с риском прободения кишки.
Диагностика антибиотик-ассоциированного расстройства стула обычно не вызывает трудностей. Идиопатическую форму болезни дифференцируют с пищевыми токсикоинфекциями легкой степени. Клиника C. difficile-ассоциированной диареи, а именно псевдомембранозного колита, может напоминать течение холеры, болезни Крона, язвенного колита и тяжелого пищевого отравления. Дополнительно проводят обзорную рентгенографию брюшной полости, КТ толстого кишечника.
Лечение антибиотик-ассоциированной диареи
Лечение идиопатической ААД предполагает отмену или снижение дозы антибактериального средства, назначение противодиарейных препаратов (лоперамид), эубиотиков и пробиотиков (лактобактерии, бифидобактерии). При многократных эпизодах жидкого стула целесообразно проводить нормализацию водно-солевого баланса.
Выявление клостридий диффициле является показанием для отмены АБ и назначения этиотропной, симптоматической и дезинтоксикационной терапии. Препаратом выбора для лечения заболевания является метронидазол. В тяжелых случаях и при непереносимости метронидазола назначают ванкомицин. Коррекция дегидратации и интоксикации осуществляется парентеральным введением водно-солевых растворов (ацесоль, р-р Рингера, регидрон и др.). В комплексную терапию клостридиального колита входит использование энтеросорбентов, пробиотиков. Последние назначаются после проведения этиотропной терапии для восстановления нормофлоры кишечника курсом на 3-4 месяца. При осложнениях ПМК (перфорация кишки, мегаколон, рецидивирующее прогрессирующее течение колита) показано хирургическое лечение. Выполняют резекцию части или всей толстой кишки (гемиколэктомию, колэктомию).
Прогноз и профилактика
Прогноз идиопатической ААД благоприятный. Заболевание может купироваться самостоятельно после отмены антибиотиков и не требовать специфического лечения. При своевременной диагностике и адекватном лечении псевдомембранозного колита удается добиться полного выздоровления. Тяжелые формы диареи, игнорирование симптомов болезни могут повлечь осложнения как со стороны ЖКТ, так и всего организма. Рациональная антибиотикотерапия предполагает прием медикаментов по строгим показаниям только при назначении врачом и под его тщательным контролем. Профилактика антибиотик-ассоциированной диареи включает применение пробиотиков для поддержания нормальной микрофлоры ЖКТ, рациональное питание и ведение активного образа жизни.
Вконтакте
Google+
LiveJournal
Одноклассники
Мой мир
симптомы, проведение диагностических исследований и лечение
Закодированная как К98.1 в МКБ 10, антибиотикоассоциированная диарея (ААД) – это нарушение стула, не связанное с инфекцией или иными причинами. Предшествует такому состоянию прием антибактериальных препаратов. О диарее говорят, если неоформленный стул наблюдается трижды два дня подряд или чаще. Иногда ААД фиксируется спустя некоторое время после прохождения терапевтического курса – до восьми недель.
Общее представление
Зашифрованная символами К98.1 в МКБ антибиотикоассоциированная диарея в редких случаях может развиться на фоне инфицирования, но чаще объясняется прямым эффектом медикаментов на кишечную моторику либо опосредованным влиянием. Кроме того, препараты достаточно сильно воздействуют на разные части пищеварительной системы, что также может стать причиной неоформленного патологического стула. Хороший пример – макролиды, оказывающие мотилиноподобный эффект. Курс лечения препаратами с цефтриаксоном может спровоцировать сладж-синдром. Проявления патологического состояния при такой форме расстройства самостоятельно исчезают спустя некоторое время после прекращения приема препарата. Специфической программы коррекции состояния пациента не требуется.
К98.1 – код в МКБ 10 антибиотикоассоциированной диареи, то есть расстройства стула из-за терапевтического курса антимикробными препаратами. Как видно из клинических данных, медицинской статистики, практически 37% пациентов, вынужденных принимать медикаменты этой группы, сталкиваются с проявлениями ААД, что фиксируется в личной истории болезни. Указанная частота – это минимальная оценка страдающих от расстройств ЖКТ, но некоторые специалисты убеждены, что проблема гораздо более распространена. Не совсем точная оценка числа случаев связана с толерантной оценкой проявлений – и больные, и доктора не воспринимают феномен как патологию. Особенно характерно это, если нарушение стула наблюдается в легкой форме или средней по уровню тяжести течения.
Формы и нюансы
Используемый в МКБ код антибиотикоассоциированной диареи К98.1 включает в себя несколько клинических форм патологического состояния. В последнее время широкое применение получила система классификации, предполагающая оценку проявлений. Бывает ААД без признаков колита, АА колит и псевдомембранозный. При заражении определенными формами клостридий ААД классифицируют на не имеющую признаков колита, а также выделяют три разновидности такового: фульминантный, псевдомембранозный и форму без псевдомембран.
До 20% всех случаев объясняются клостридиями вида difficile. Применяемый в МКБ к антибиотикоассоциированной диарее код К98.1 также включает прочие случаи, на долю которых приходится (суммарно) около 80% всех пациентов. Это ситуации, при которых нарушение стула связано с иными формами клостридий, грибковой микрофлорой, кокками, сальмонеллами, клебсиеллами. Последние, как установлено, чаще всего становятся причиной сегментарного геморрагического патологического состояния ЖКТ.
Диагнозы и классификация
В 2009 году специалисты по инфекционным заражениям, микробиологи, входящие в Европейский союз врачей, опубликовали актуальные при антибиотикоассоциированной диарее клинические рекомендации. Внушительных объемов научная работа была посвящена в первую очередь самым распространенным формам микрофлоры – клостридиям difficile. Рассматривались проблемы диагностики и терапии таких случаев. Особенное внимание специалисты уделили оценке тяжести состояния больного, формулировке прогноза. Эпидемиологи Америки годом позже выпустили практические рекомендации по наблюдению, лечению пациентов с ААД, при которой доминирует указанная форма микрофлоры.
Актуальность проблемы диареи после антибиотиков у взрослых и детей связана с недостаточной изученностью вопроса. В частности, для упомянутого выше вида патологической формы жизни только недавно выявили новый штамм, которому свойственно существенно более активное продуцирование отравляющих компонентов в сравнении с известными прежде. Разница достигает 23 раз. Заражение таким штаммом становится причиной тяжело протекающей ААД. Среди генерируемых микрофлорой веществ – бинарный токсин. Проведенные мероприятия до настоящего момента не позволили уточнить, какое влияние на человека оказывает это вещество. Специфическая особенность выявленного типа – повышенная стойкость к фторхинолонам. Из этого врачи заключили, что применение фторхинолонов может быть одним из провоцирующих ААД факторов.
Нюансы и проявления
Антибиотикоассоциированный дисбактериоз, ААД могут развиваться в разных формах. У некоторых пациентов отмечается легкая диарея, быстро проходящая. У других диагностируют тяжелый колит, сопряженный с опасностью летального исхода. В преимущественном проценте случаев манифестация выражена послаблением выделений, слабыми проявлениями колита. Общая симптоматика отсутствует. Стул в сутки бывает до четырех раз, сопровождается умеренной болезненностью, напоминающей схватки, в области живота. Температура сохраняется нормальной. При пальпации можно определить повышенную чувствительность, но не всегда. Газообразование также активнее нормы, но разница от здорового состояния не очень большая.
Антибиотикоассоциированная диарея у детей и взрослых не проявляет себя маркерами воспаления в кровеносной системе. Симптоматику обычно купируют приемом специфических препаратов, отменой курса антимикробных средств. Для быстрого улучшения состояния рекомендовано применять пробиотики, средства против диареи. Врачами установлено точно: такое состояние связано с дисбалансом состава микрофлоры кишечника, нарушением функциональности полезных бактерий. Пролиферации патологических микроскопических форм жизни не происходит.
Случаи: иногда – сложнее
Существенно отличается лечение диареи после антибиотиков, если беспокоят клинические проявления ААД, ассоциированной с клостридиями difficile, в случае колита. Заподозрить такое состояние можно по сильно, неприятно пахнущим выделениям, в которых заметны слизистые включения. Стул профузный. Опорожнение кишечника сопровождается тенезмами. Больного беспокоят боли, напоминающие схватки, в области живота. При пальпации этот участок мягкий, отдельные области отзываются повышенной чувствительностью (ободочная кишка). Прослушивание позволяет определить: шумы в кишечнике существеннее нормы.
Если диарея после приема антибиотиков связана с указанной формой жизни, больного лихорадит (состояние умеренного уровня тяжести). Наблюдается общее обезвоживание организма, пациента тошнит, рвет. Анализ крови показывает несущественный лейкоцитоз даже в случае, если типичных проявлений диареи нет. Колит чаще всего локализован в правой части толстой кишки, указывает на себя очагами боли, повышением содержания лейкоцитов в крови, лихорадочным состоянием. Диарея умеренная либо вовсе отсутствует.
Варианты и случаи
Иногда диарея после приема антибиотиков протекает в тяжелой форме. Токсический мегаколон сопровождаете редким стулом. В клинической практике известны случаи неадекватной оценки такого прогресса состояния больного – иногда врачи (и сами пациенты) принимают симптом за признак улучшения. При этом в кишечном тракте задерживаются газы, брюшинная область раздражена, человека лихорадит, исследования выявляют дистензию ободочной кишки. Детальное изучение состояния пациента помогает обнаружить выпот в области брюшины, малого таза. В кровеносной системе устанавливают повышенный уровень содержания лейкоцитов, а концентрация альбуминов, наоборот, ниже нормы. Кроме того, выявляется гиповолемия. Указанные проявления – типичная клиническая картина.

Если антибиотикоассоциированная диарея прогрессирует в такой форме, следует направить пациента на рентгеновский снимок. При отравляющем мегаколоне расширяется ободочная кишка. Исследования помогают выявить кишечный пневматоз. Проведя КТ, можно установить утолщение кишечной стенки, сужение просветов, уплотнение жировых структур, окружающих кишку, а также асцит. Состояние достаточно тяжелое, поэтому следует избегать ухудшения до такого уровня диареи после антибиотиков. Что делать, если прогресс все же достиг этой стадии, знают квалифицированные врачи: больному показана срочная операция. Впрочем, как видно из медицинской практики, преимущественный процент больных сталкивается с достаточно тяжелыми осложнениями, негативными последствиями вмешательства. Повышен процент летальных исходов.
Проблема: типичные случаи
Если ранее антибиотикоассоциированные диареи преимущественно объяснялись относительно безопасными формами патологической микрофлоры, в последнее время участились случаи встречаемости самого опасного штамма клостридий – BI/NAPI. Чаще всего вспышки такого рода ААД наблюдаются в больничных стенах, где пациенты вынуждены проходить продолжительные курсы лечения антимикробными препаратами. Протекают такие ААД существенно тяжелее прочих типов и форм патологии.
Обычно симптоматика начинает выявляться на пятый день с момента старта антимикробной программы, иногда до первичных проявлений проходит вдвое больше времени. Известны единичные случаи выявления симптомов ААД уже на второй день приема лекарств, но бывают и поздние варианты, когда первые проявления приходились на десятую неделю с момента завершения курса лечения антибиотиками.
BI/NAPI: ААД в легкой форме
Антибиотикоассоциированная диарея такого типа проявляется понижением функциональности тонкой кишки и контаминацией этого органа. Полостное переваривание пищи ослабевает, брожение, гниение с участием бактерий активизируются. Кислотность содержимого кишечного тракта падает, вследствие чего активность липазы сбивается. У больного наблюдается стеаторея, в кишечном тракте формируются мыльные соединения, жирные структуры. Жирорастворимые витаминные вещества всасываются значительно хуже, что провоцирует полигиповитаминоз эндогенного типа.
Поскольку адсорбция и пищеварительные процессы в тонком кишечнике нарушаются, антибиотикоассоциированная диарея становится причиной активного газообразования и дисбаланса кишечной моторики, что выливается в стойкий синдромный комплекс диспепсии. Слишком активное продуцирование органических кислот из-за реакций, активизируемых микрофлорой, приводит к росту осмолярности одержимого ЖКТ. Следствия явления – вздутие живота, метеоризм, диарея, распирающая болезненность, приходящая приступами. Дисбиоз провоцирует высокий уровень проницаемости барьера кишечника, что инициирует аллергический ответ организма. Избыточное развитие микрофлоры в тонком кишечнике может стать причиной ослабевания функциональности других отделов ЖКТ, как следствие – повышения давления, дуоденостаза, СРК, псевдообструкции. Возможен старт воспалительных процессов из-за продолжительной контаминации, деконъюгации. В карте пациента фиксируют энтерит или дуоденит.
Продолжая рассмотрение
Лечения антибиотикоассоциированная диарея, ассоциированная с клостридиями difficile, не требует, если протекает в легкой форме. Не нужно корректировать состояние больного, если болезненность умеренная, а дефекация фиксируется в день до четырех раз, при этом общая симптоматика отсутствует, лабораторные исследования показывают, что значительных сдвигов нет. Если указанное состояние развивается дома, строго запрещено использовать антибактериальные препараты для избавления от ААД.
Как правило, диарея полностью проходит самостоятельно, когда пациент завершает терапевтический курс, ее вызвавший. В ряде случаев врач может порекомендовать принимать пробиотики. Без врачебной рекомендации никакие медикаменты использовать не стоит, чтобы не спровоцировать ухудшение состояния.
BI/NAPI: ААД в тяжелой форме
В некоторых случаях ААД протекает по более негативному сценарию, развивается колит. Выделяют две основные формы: с псевдомембранами и без таковых. Без псевдомембран процесс обычно системный. ААД проявляет себя лихорадочным состоянием, общим отравлением организма, болью в животе. Больного тошнит и рвет. Стул частый, водянистый. В сутки возможно опорожнение до двадцати раз. Наблюдается обезвоживание.
Псевдомембранозный колит поначалу указывает на себя сходными симптомами. Проведение колоноскопии позволяет выявить псевдомембраны. В ходе копроскопии можно обнаружить эритро-, лейкоциты. Анализ на скрытую кровь в преимущественном проценте случаев дает положительный результат. Иногда наблюдается гематохезия.
Самый тяжелый вариант патологического состояния – колит фульминантного типа. Встречается приблизительно у 3% пациентов. Состояние может стать причиной непроходимости кишечного тракта, мегаколона на фоне отравления, кишечной перфорации, воспаления в брюшной полости, заражения крови. Заподозрить фульминантный колит можно, если пациент страдает от яркой, четко выраженной боли в области желудка и вздутиея живота. Колит сопровождается обезвоживанием, лихорадочным состоянием, гипотонией, угнетенностью сознания либо возбужденностью. Токсин А, генерируемый патологической микрофлорой, напрямую отравляет ЦНС, что сможет стать причиной тяжелой энцефалопатии.
Развитие случая: внимание нюансам
При ААД могут наблюдаться проявления, позволяющие заподозрить раздражение тканей брюшины. Возможно мышечное напряжение в отдельных областях. Такие явления – основание предположить кишечную перфорацию. При лабораторных исследованиях можно установить повышенную концентрацию лейкоцитов в крови, азотемию.
Непроходимость ЖКТ, токсический мегаколон, в которые может прогрессировать состояние, приводят к более редкому стулу. Иногда колит проявляется абдоминальным синдромом в острой форме, но не сопровождается диареей. Это возможно и при мегаколоне на фоне отравления организма.
Не всегда по шаблону
Возможно развитие атипичной ААД. При такой форме заболевания больной страдает колитом, нарушается целостность и здоровье тонкого кишечника. Наблюдается потеря белковых структур, энтеропатия. Наблюдение за состоянием пациента позволяет выявить экстраинтестинальные симптомы.
Уточнение
При симптомах ААД, колита, включая подозрение на случаи, связанные с новыми и самыми опасными штаммами клостридий, следует изучить историю болезни. Если в последние два месяца человек использовал антимикробные препараты, нужно исходить из того, что вероятность ААД существенно выше среднего. При дифференциальной диагностике нужно определить нюансы течения случая. Важно взять на исследование образцы кала, крови, урины, провести лабораторную диагностику. Необходимо проверить факт клостридиальной инфекции. На ААД указывают недостаток альбуминов, азотемия, содержание лейкоцитов – 15-16 тысяч на мм куб.
При подозрении на колит в первую очередь необходимо сделать рентгеновский снимок, оценить состояние органов брюшной полости. Диагноз подтверждают при обнаружении перфорации, мегаколона, пневматоза, илеуса. КТ может показать увеличенную толщину кишечных стенок в отдельных участках, асцит. Несколько реже выявляются облитерция, перфорация кишечника.
Самый точный и быстрый метод постановки диагноза – анализ кала на наличие возбудителей. Для этого проводят исследования, позволяющие выявить содержание токсина А. Используют иммунологические ферменты. Точность и чувствительность современных систем тестирования оценивается в среднем в 75-85%. Разработаны методы выявления одновременно токсинов А, В. Этот подход считается более точным.
Эндоскоп для уточнения состояния
Наиболее осторожно проводят такое исследование, если есть основания предположить, что требуется лечение антибиотикоассоциированной диареи, прогрессировавшей в колит. При подобном прогрессе процедура считается опасной, поскольку увеличивает вероятность кишечной перфорации. В большей степени это свойственно тяжелым случаям.
Если развился псевдомембранозный колит, самым надежным способом окончательного подтверждения диагноза признана колоноскопия. Учитывая высокие риски, связанные с таким мероприятием, обследование проводят только в случае, когда нужно крайне быстро и предельно точно определить диагноз, а также при илеусе. Колоноскопия необходима, чтобы дифференцировать состояние и исключить иные патологические состояния кишечного тракта, угрожающие жизни пациента.
Что делать?
Лучше всего знают, как лечить диарею после антибиотиков, квалифицированные доктора. Преимущественный процент людей сталкивается с легкой формой ААД, поэтому специфического терапевтического курса не полагается. Симптомы сами исчезают, когда завершается антимикробный курс. Иногда назначают симптоматическую терапию для предупреждения обезвоживания, коррекции баланса электролитов в организме. Если симптоматика указывает на колит, положены антибактериальные препараты.
Формулируя рекомендации о том, как лечить диарею после антибиотиков при носительстве клостридий рода difficile без типичной симптоматики, врачи из Американского союза заключили, что не нужно давать пациенту препараты для специфической корректировки состояния. В общем случае завершают антибактериальный курс и не используют средства для предупреждения секреторной активности, перистальтики кишечного тракта – они могут спровоцировать активное размножение патологической микрофлоры.

Основное лечение – использование пробиотиков, то есть живых микроорганизмов, восстанавливающих баланс микрофлоры в кишечном тракте. Это разнообразные бактерии: лакто-, бифидо-, палочки, кокки, грибковые культуры. Ряд ученых убежден, что пробиотики можно применять для профилактики ААД. Этот вопрос в настоящее время открыт, проводятся многочисленные исследования для подтверждения гипотезы или ее опровержения.
