ФГДС желудка, описание и подготовка к процедуре
ФГДС (фиброэзофагогастродуоденоскопия) – это специальная медицинская процедура, в ходе которой выполняется исследование пищевода, желудка и начального отдела кишечника с помощью специального прибора-эндоскопа. Врачи сокращенно называют ее эндоскопией, а те пациенты, которым пришлось ее пройти – зондированием. Такое слово они объясняют тем, что в ходе процедуры в пищевод вводится эндоскоп («глотают зонд»).
Содержание:
ФГДС
Как подготовиться к ФГДС?
Порядок проведения процедуры
Что бывает после ФГДС?
Другие методы исследования желудка
ФГДС желудка
Записаться на процедуру (м. Озерки, м. Просвещения)
Онлайн запись на прием
Телефоны:
+7 (812) 30-888-03
+7 (812) 242-53-50
Адрес клиники: Санкт-Петербург, Выборгский район, ул. Асафьева, 9, к 2, лит. А (ст. м. Озерки, ст. м. Проспект Просвещения)
ЦЕНЫ
Обратите внимание! Цены указаны для взрослых пациентов. Стоимость детских приёмов смотрите, пожалуйста, в разделе «Педиатрия».
Стоимость детских приёмов смотрите, пожалуйста, в разделе «Педиатрия».
| ФГДС (без хеликобактерного теста ) | 4 200 |
| Определение секреторной функции желудка | 450 |
| Биопсия желудка с помощью эндоскопии (во время ФГДС, без стоимости лаб. исследования) | 600 |
| Helicobacter pylori, ДНК [реал-тайм ПЦР] | 850 |
ФГДС желудка позволяет подробно изучить состояние слизистой оболочки и выявить некоторые заболевания на ранних стадиях, когда они еще легко поддаются лечению. Кроме того, в ходе проведения процедуры врач может выполнить забор материала для последующего исследования в лаборатории. Иногда это является едва ли не единственным методом достоверно диагностики болезни, что особенно актуально для лечения злокачественных опухолей.
Наконец, еще одна сфера применения ФГДС заключается в ее использовании в качестве терапевтической процедуры. Например, этим способом успешно лечат химические ожоги пищевода и стенок желудка, а также внутренние кровотечения из пищеводных вен. Из остальных преимуществ можно отметить эффективное определение кровоточащих мест в желудке, выявление причин появление тошноты и изжоги, а также вообще, любое изучение патологий желудочно-кишечного тракта.
Из остальных преимуществ можно отметить эффективное определение кровоточащих мест в желудке, выявление причин появление тошноты и изжоги, а также вообще, любое изучение патологий желудочно-кишечного тракта.
Как подготовиться к процедуре?
Обо всех правилах подготовки к ФГДС желудка подробно расскажет врач-гастроэнтеролог, а здесь мы остановимся на самых важных из них. Итак, за два дня до процедуры следует полностью отказаться от алкоголя и острой пищи. А вот курильщики могут вздохнуть с облегчением, так как на их привычку это правило не распространяется. Отказаться от курения нужно только лишь за несколько часов до визита к врачу. Курение непосредственно перед процедурой провоцирует выделение желудочного сока, что может стать причиной неверной диагноза.
Еще одно важное правило: ФГДС должна проводиться на полностью пустой желудок. Если процедура назначена наутро, пациенту нельзя есть после 20.00 предыдущего дня, а если она планируется после обеда, с утра допускается легкий завтрак. Пренебрежение этим правилом может вызвать дискомфорт и рвоту у пациента, а для врача – затруднит изучение стенок желудка. Оптимальной едой считаются блюда из овощей, фруктов, рыбы и курицы. Орехи и шоколад есть не рекомендуется, так как в больном желудке они перерабатываются очень долго.
Пренебрежение этим правилом может вызвать дискомфорт и рвоту у пациента, а для врача – затруднит изучение стенок желудка. Оптимальной едой считаются блюда из овощей, фруктов, рыбы и курицы. Орехи и шоколад есть не рекомендуется, так как в больном желудке они перерабатываются очень долго.
Порядок проведения процедуры
ФГДС желудка занимает совсем немного времени – не более 10 минут. Если есть необходимость взятия материала для исследований (биопсия), это время увеличивается до 15 минут. Перед процедурой пациент должен пройти тестирование на устойчивость к вводимому материалу (он не должен вызывать аллергические реакции).
Все начинается с того, что врач укладывает пациента набок и обрызгивает ротовую полость анестезирующим средством, которое помогает минимизировать рвотный рефлекс и избавиться от дискомфорта. Затем врач вставляет в рот пластиковый загубник, который нужен на тот случай, если пациент вдруг рефлекторно сожмет зубы. После этого в отверстие загубника вводится эндоскоп, который врач постепенно продвигает в пищевод, и далее – в желудок. Как правило, пациентом процедура переносится спокойно, хотя неприятные ощущения, конечно же, присутствуют. В крайнем случае врач может назначить наркоз, но этот вопрос обсуждается заранее.
Как правило, пациентом процедура переносится спокойно, хотя неприятные ощущения, конечно же, присутствуют. В крайнем случае врач может назначить наркоз, но этот вопрос обсуждается заранее.
В ходе проведения ФГДС врач наблюдает изображение внутренних стенок желудка на экране монитора в режиме реального времени. Современная аппаратура для диагностики позволяет получить качественные снимки с высоким разрешением, которые затем могут быть распечатаны и приложены к медицинской карте больного. Также с помощью эндоскопа можно вводить лекарственные препараты, удалять наросты и останавливать внутренние кровотечения на стенках пищевода. В этом случае процедура занимает чуть большее время. После извлечения эндоскопа пациент чувствует себя нормально и сразу же может идти домой.
Что бывает после процедуры?
Введение эндоскопа в желудок вызывает дискомфортные ощущения, которые могут сохраняться пару дней в горле, но не более того. Также у пациентов может слегка болеть живот, но это тоже быстро проходит.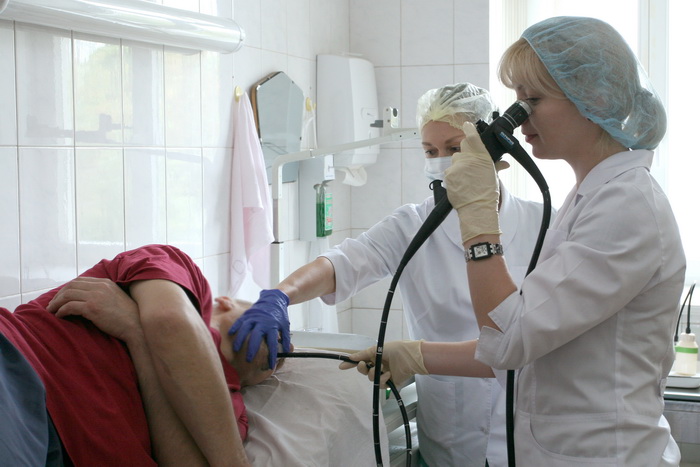 Крайне редко из-за повреждения эндоскопом может открыться кровотечение в стенке внутреннего органа, а в остальных случаях осложнений практически не бывает.
Крайне редко из-за повреждения эндоскопом может открыться кровотечение в стенке внутреннего органа, а в остальных случаях осложнений практически не бывает.
Намного серьезнее последствия будут тогда, когда пациенты пренебрегают указаниями врача и идут на процедуру после еды. В этом случае остатки пищи могут переместиться выше, в дыхательные пути, что, в свою очередь, приводит к приступу удушья. Если же человек строго соблюдал все правила, ни у него, ни у врача, не возникнет проблем во время ФГДС желудка. Специалист получит четкие и полные изображения внутренних стенок, что поможет ему точнее определить диагноз. В частности, ФГДС позволяет определить:
- Объемные образования в органах ЖКТ
- Проходимость пищевода, желудка и некоторых отделов кишечника
- Грыжу в пищеводном отверстии диафрагмы
- Заболевания ЖКТ на разных стадиях
- Изменения состояния слизистой оболочки
- Выпячивание мышечной стенки и другие патологии и болезни
При отсутствии в пищеводе пищи и воды все эти проблемы хорошо видны на экране монитора. Благодаря ФГДС, врач может назначить своевременное лечение и побороть болезнь на ранней стадии.
Благодаря ФГДС, врач может назначить своевременное лечение и побороть болезнь на ранней стадии.
Другие методы исследования желудка
Хотя ФГДС желудка – довольно простая и эффективная процедура, ее применяют далеко не всегда. Обычно это связано с непереносимостью материала эндоскопа или ослабленными стенками внутренних органов, у которых эндоскоп может вызвать кровотечение. Крайне редко, но все же случается, что пациенты панически бояться данной процедуры. Если провести ФГДС желудка невозможно, применяются следующие альтернативные методы диагностики:
- Компьютерная томография
- Магнитно-резонансная томография
- Рентген-исследование. Как известно, рентген применяется, в основном, для выявления переломов, так как кости намного плотнее остальных тканей, поэтому хорошо видны на снимке. Для изучения ЖКТ пациент принимает сульфат бария, который виден в рентгеновских лучах, и помогает определить патологические изменения в желудке.
- Капсульная эндоскопия.
 Как и при ФГДС, пациент глотает прибор с камерой, которая передает врачу изображения внутренних стенок ЖКТ (точнее, записывает их на носитель). Однако такая капсула проглатывается полностью и путешествует по кишечнику долгое время, пока не выведется из организма естественным путем. Преимущество данного метода заключается в том, что он позволяет получить полную картину состояния ЖКТ.
Как и при ФГДС, пациент глотает прибор с камерой, которая передает врачу изображения внутренних стенок ЖКТ (точнее, записывает их на носитель). Однако такая капсула проглатывается полностью и путешествует по кишечнику долгое время, пока не выведется из организма естественным путем. Преимущество данного метода заключается в том, что он позволяет получить полную картину состояния ЖКТ. - Дуоденальное зондирование. При этой процедуре пациент медленно заглатывает тонкую резиновую трубку. Через нее наружу поступает желчь и другие вещества, вырабатываемые органами желудочно-кишечного тракта.
Все указанные методы позволяют получить довольно достоверную картину состояния пищевода, желудка и кишечника, однако, ни один из них не является столь же хорошим, как ФГДС желудка. Обычно врачи назначают эти варианты диагностики в качестве вспомогательных методов, так как единственно верным средством исследования они быть не могут. Кроме того, они только лишь показывают картину внутренних органов, в то время как с помощью ФГДС желудка можно проводить многие важные лечебные процедуры, когда диагноз уже определен.
Сделать ФГДС (гастроскопию) в СПб. Цена, подготовка, как проходит. / Клиника ЭКСПЕРТ
ЭГДС — Эзофагогастроскопия (ФГДС) — это один из самых распространенных и современных методов исследования органов пищеварения (пищевода, желудка и 12-перстной кишки), который всегда применяется для подтверждения или опровержения предварительного диагноза и дополнительной диагностики. Для большинства пациентов эта процедура достаточно неприятна, однако ее результаты позволяют своевременно и точно поставить правильный диагноз и предотвратить развитие тяжелых осложнений.
Назначение процедуры
Диагностическая ЭГДС – это высокоинформативный метод, который позволяет:
- оценить анатомическое строение исследуемых органов и состояние их слизистых
- выявить наличие и определить степень тяжести различных дефектов (язв, эрозий)
- обнаружить участки аномального разрастания тканей
- установить месторасположение новообразований различной этиологии.

Практически любое заболевание органов желудочно-кишечного тракта (ЖКТ) окончательно подтверждается только результатами гастроскопии. ФГДС также применяется для забора материала на анализ на Helicobacter Pylori, гистологическое или морфологическое исследование (биопсия). Также сделать фиброгастроскопию направляют для мониторинга состояния поврежденного органа и оценки эффективности проводимого лечения.
Показания к ЭГДС
Сделать ЭГДС с целью диагностики заболеваний ЖКТследует при любых тревожных симптомах со стороны пищеварительной системы. Это:
- боли в эпигастрии (область желудка)
- постоянная тошнота
- периодическая рвота
- отрыжка, срыгивание после еды
- частая изжога
- горечь и неприятный привкус во рту
- признаки интоксикации (отравления).
Но чаще всего фиброгастродуоденоскопию назначают специалисты при наличии определенных показаний (даже при отсутствии ярко выраженной симптоматики):
- нарушение аппетита
- нестабильность массы тела или резкое похудение
- стойкая и продолжительная анемия (снижение гемоглобина)
- наследственная предрасположенность к патологиям пищеварительного тракта
- подготовка к хирургическому вмешательству на желудке, пищеводе или 12-перстной кишке
- диспансерное обследование больных, стоящих на учете у гастроэнтеролога
- оценка состояния органов пищеварения после оперативного лечения.

Противопоказания к гастроскопии
Делать фиброгастроскопию можно только при отсутствии абсолютных и относительных противопоказаний. В противном случае можно не только не получить ожидаемого диагностического или терапевтического результата, но и столкнуться с неприятными осложнениями. Перед назначением ЭГДС квалифицированный специалист обязательно проверит наличие у пациента ограничений к процедуре.
Абсолютные противопоказания
- патология свертывающей системы крови (гемофилия)
- увеличение размеров щитовидной железы
- некроз участка сердечной мышцы ишемического характера – инфаркт миокарда (в течение недели после приступа)
- острое нарушение мозгового кровообращения (инсульт)
- гипертонический криз (повышение артериального давления до индивидуально высоких цифр)
- обострение бронхиальной астмы
- общее тяжелое состояние больного.
Относительные противопоказания
Список ограничений может быть дополнен относительными противопоказаниями, при которых гастроскопия проводится только в случае крайней необходимости:
- острые воспалительные процессы, локализованные в области глотки и гортани
- гипертоническая болезнь и стенокардия
- увеличение размеров шейных лимфоузлов
- психические расстройства.

Подготовка к процедуре эзофагогастроскопии (ЭГДС)
За 1-2 суток до назначенной даты проведения ЭГДС больному следует перейти на легкоусвояемую пищу, отказаться от жирных, жареных и острых блюд, исключить употребление алкоголя и временно отменить лекарственные препараты в случае их постоянного применения (только после консультации со специалистом).
За 12 часов до обследования необходимо соблюдать режим голодания. Если гастроскопия назначена на утро, то накануне с 19-20 часов и до утра следующего дня нужно воздержаться от приема еды, на процедуру прийти строго натощак. Утром следут отказаться от любых напитков, включая воду.
Методика проведения ЭГДС и результаты
Гастроскопия предполагает введение желудочного зонда в пищевод и желудок больного через ротовую полость. В течение нескольких минут врач проводит визуальный осмотр внутренних органов, а затем извлекает зонд.
Процедура сама по себе безболезненна, но все врачебные манипуляции неприятны для пациента, поэтому для облегчения рвотных позывов, которые возникают при введении трубки в желудок, и уменьшения общего дискомфорта при фиброгастродуоденоскопии необходимо внимательно слушать и следовать всем рекомендациям врача. Также предварительно горло пациента может быть обработано обезболивающим спреем.
Также предварительно горло пациента может быть обработано обезболивающим спреем.
Где можно сделать ЭГДС в Санкт-Петербурге?
В Клинике ЭКСПЕРТ гастроскопия проводится квалифицированными специалистами, которые стремятся обеспечить максимальный комфорт пациенту и произвести все необходимые диагностические манипуляции как можно быстрее, но без ущерба для качества и информативности исследования. Высокотехнологичное оборудование только способствует оперативному и результативному обследованию пациента методом ЭГДС.
В нашей клинике после проведения ЭГДС вам выдадут на руки заключение врача-эндоскописта, с которым вы можете обратиться за медицинской помощью к своему лечащему врачу или к участковому терапевту по месту жительства.
При желании вы можете проконсультироваться с врачом гастроэнтерологом Клиники ЭКСПЕРТ. В этом случае у вас будет возможность получить не только необходимую и важную по вашему заболеванию информацию, но и составить индивидуальную программу лечения.
Обращаем ваше внимание, что наблюдение у одного специалиста (с момента первого визита и до выздоровления) позволяет достичь видимого положительного результата в короткие сроки, повышает комфорт лечения и улучшает взаимодействие между врачом и пациентом.
Перед процедурой требуется сделать ЭКГ, чтобы убедиться в безопасности проведения процедуры.
Важно: Если возраст пациента старше 55 лет и/или пациент имеет тяжелое сопутствующее заболевание, для проведения ФГДС необходим допуск врача.
Процедура ФГС. Когда и в каких случаях делать
Правильное название исследования желудка — эзофагогастродуоденоскопия (ЭФГДС). И оно является единственным информативным методом, способным дать сведения о состоянии органов пищеварительной системы от пищевода до тонкого кишечника. Этот безопасный метод диагностики подходит даже детям, главное, правильно настроиться и выполнять все рекомендации специалиста.
ЭФГДС назначается людям при подозрении на язву, онкологические процессы органов ЖКТ, гастрит, а также при отсутствии аппетита; резком похудении; жжении в горле, грудине; ощущении кислоты, горечи, тошноты, рвотных позывов; анемии; затруднениях при глотании; боли, тяжести в эпигастральной зоне. В ходе исследования можно выявить новообразования, скрытые кровотечения, изъязвления слизистой в области пищевода, желудка, двенадцатиперстной кишки.
В ходе исследования можно выявить новообразования, скрытые кровотечения, изъязвления слизистой в области пищевода, желудка, двенадцатиперстной кишки.
Исследование выполняется эндоскопом. Он представляет собой гибкую длинную трубку до одного сантиметра в диаметре. На конце прибора находится источник света и миниатюрная камера, которая передаёт изображение на монитор. Продолжительность манипуляции — не более 10 минут. Расшифровка обследования выдаётся в течение 15—20 минут.
Когда надо побороть внутренний страх, пациенту обезболивают глотку и корень языка. Очень редко прибегают к общему наркозу.
Через ротовую полость, глотку и пищевод трубка эндоскопа постепенно продвигается в желудок. В этот момент необходимо стараться вдыхать воздух. При необходимости в зоне повреждения тканей производится забор маленького кусочка для дальнейшего гистологического исследования.
Правильная подготовка к ЭФГДС имеет решающее значение, так как остатки пищи, брожение или повышенная кислотность из-за курения, могут исказить картину и дать ложный результат.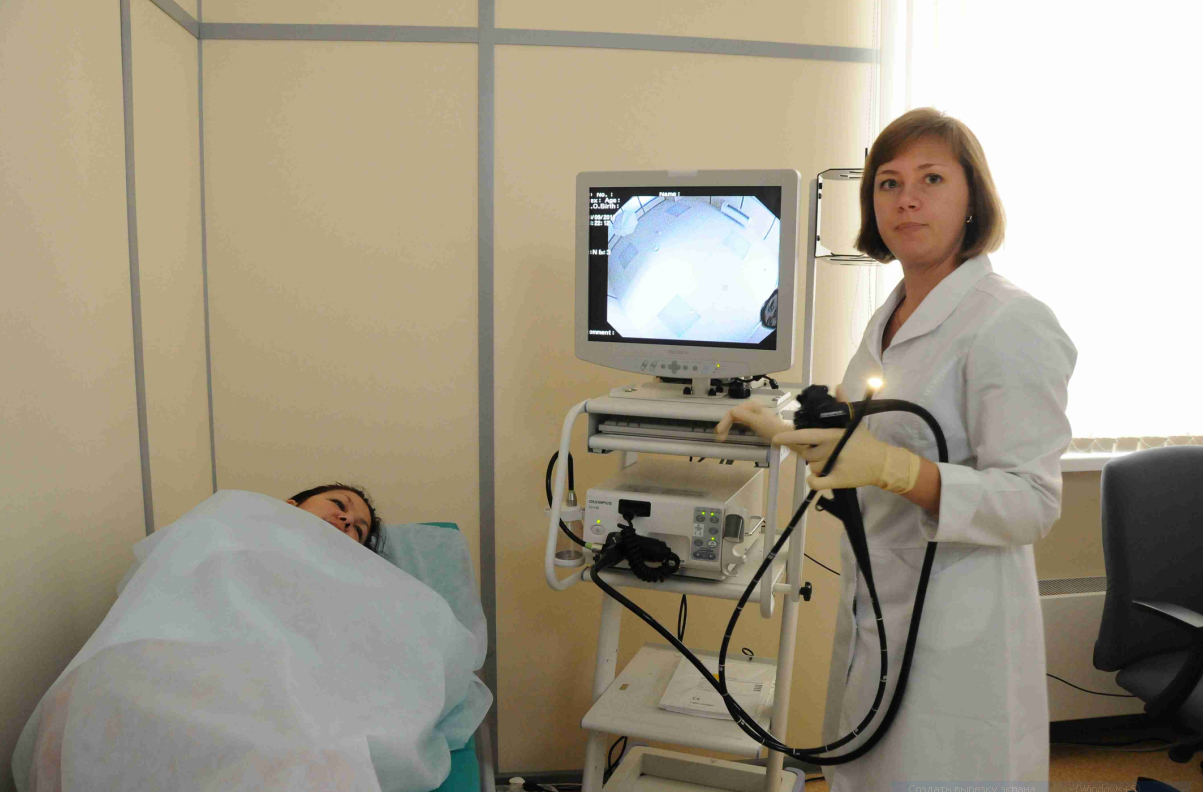
Обычно советуют не есть 10—12 часов до обследования. При проблемах, когда длительное голодание вредно пациенту, хотя бы восемь часов нужно оставаться без пищи. Когда гастроскопия назначается на утро, последний раз кушать вечером можно не позднее 18—19 часов. Пища должна легко усваиваться, это может быть манная каша на воде, картофельное пюре, перемолотое нежирное отварное мясо. Пить можно до 22 часов. Если процедура проводится после обеда, то, помимо лёгкого ужина, пациент может рассчитывать на небольшой завтрак. Например, кашу на воде, отварное яйцо.
Кушать после ЭФГДС не следует в течение двух часов. При взятии биопсии этот промежуток голодания может увеличиться до шести часов. Воду без газа можно употреблять сразу, а от чая и кофе лучше на сутки отказаться.
Чтобы не повредить слизистые, первые несколько дней следует потреблять лишь перетёртую тёплую пищу, можно есть каши, овощные пюре, супчики, некислые кисели, нежирные бульоны. Не следует злоупотреблять молоком, яйцами, мясом. Строгий температурный режим блюд не менее важен, так как горячее и холодное будет раздражать стенки.
Колоноскопия — это разновидность эндоскопического исследования с целью выявления патологий толстого кишечника. Проводится с помощью колоноскопа — специального оптического прибора, который представляет собой длинную трубку с камерой и рабочим каналом. Он выводит изображение на экран, а также позволяет проводить манипуляции в кишечнике: забор участка ткани для биопсии или одномоментное удаление патологических образований, например полипов.
Любой больной с жалобами на проблемы с толстым кишечником должен быть обследован этим методом.
Два важных момента при подготовке к колоноскопии: диета и очищение. Важно перед процедурой освободить кишечник от пищевых, фекальных масс. Иначе будет нарушено проведение исследования и резко снизится его качество. Чтобы этого не случилось, за три дня из питания исключают свежие овощи и фрукты; каши из цельнозерновых круп; бобовые; мучные изделия; жирное и жёсткое мясо; молоко; копчёные, солёные, жареные блюда; магазинные йогурты с кусочками фруктов и орехов; продукты с пищевыми красителями; кофе, крепкий чёрный чай.
Иначе будет нарушено проведение исследования и резко снизится его качество. Чтобы этого не случилось, за три дня из питания исключают свежие овощи и фрукты; каши из цельнозерновых круп; бобовые; мучные изделия; жирное и жёсткое мясо; молоко; копчёные, солёные, жареные блюда; магазинные йогурты с кусочками фруктов и орехов; продукты с пищевыми красителями; кофе, крепкий чёрный чай.
Колоноскопия — процедура довольно неприятная, поэтому её сегодня зачастую проводят с обезболиванием, в настоящее время это либо седацию, либо общий наркоз. Седация — это не совсем наркоз, но приближенное к этому состояние. Для этого внутривенно вводится специальный препарат, вызывающий сон.
После 50 лет повышается риск возникновения рака кишечника, поэтому в этом возрасте рекомендуется проводить эндоскопическое исследование толстой кишки каждые пять лет, чтобы выявить заболевание на ранних стадиях развития.
Очень важно научиться контролировать свои эмоции перед выполнением и во время процедуры. Чем спокойнее пациент, тем легче врачу. Те, кто впервые идёт на обследование, испытывают множество страхов, в том числе и за свою жизнь. Бытует мнение, что можно задохнуться в момент нахождения эндоскопа в пищеварительном тракте. Это совершенно неверное и безосновательное суждение. Трубка совершенно не граничит с дыхательными путями.
Чем спокойнее пациент, тем легче врачу. Те, кто впервые идёт на обследование, испытывают множество страхов, в том числе и за свою жизнь. Бытует мнение, что можно задохнуться в момент нахождения эндоскопа в пищеварительном тракте. Это совершенно неверное и безосновательное суждение. Трубка совершенно не граничит с дыхательными путями.
Опубликовано 1 год, 6 месяцев назад, 22 февраля 2020 г. 20:00
Подготовка к проведению ФГДС (гастроскопии)
Одним из важных факторов, обеспечивающих полноценное и безопасное эндоскопическое исследование, является правильная подготовка пациента .
Всю подготовку к эндоскопии можно разделить на общую и местную.
Общая подготовка к эндоскопическим исследованиям (проводится по трём направлениям):
Психологическая подготовка. Включает разъяснение пациенту целей и задач предстоящего исследования, необходимости его проведения для постановки правильного диагноза и дальнейшего успешного лечения; у людей с лабильной психикой для снятия отрицательных эмоций, чувства страха и нормализации сна показано назначение успокаивающих препаратов, снотворных и седативных средств, транквилизаторов (вы можете попросить назначить эти препараты своего лечащего врача). Коррекция нарушенных параметров гомеостаза. В первую очередь это относится к сердечно-сосудистой и дыхательной системам, со стороны которых можно ожидать во время исследования наиболее тяжёлых осложнений.
Коррекция нарушенных параметров гомеостаза. В первую очередь это относится к сердечно-сосудистой и дыхательной системам, со стороны которых можно ожидать во время исследования наиболее тяжёлых осложнений.
Такие состояния, как тяжёлая стенокардия, различные виды аритмий, высокие цифры артериального давления, тяжёлая дыхательная недостаточность требуют обязательной грамотной коррекции в течение нескольких дней перед исследованием. Обязательно предупреждайте доктора о наличие заболеваний и состояний, которые могут повлиять на выбор средств для подготовки к исследованию. Это — повышенная чувствительность, аллергия к лекарственным препаратом, которые применяются в эндоскопии (местные анестетики), наличие глаукомы (противопоказан атропин), желчнокаменной болезни (противопоказано применение в качестве солевого слабительного раствора сернокислый магнезии), беременности и др.
Местная подготовка к эндоскопии (включает два основных направления): Поскольку относительным противопоказанием для ФГДС являются воспалительные заболевания верхних дыхательных путей (ОРЗ. тонзиллит, трещины, заеды и др.). Сначала необходимо полечиться, а потом делать ФГДС.
тонзиллит, трещины, заеды и др.). Сначала необходимо полечиться, а потом делать ФГДС.
Очищение полых органов. Недостаточное очищение желудчно-кишечного тракта от содержимого затрудняет полноценный осмотр исследуемых органов, необходимый для оценки характера патологического процесса и его протяжённости, что имеет принципиальное значение для постановки диагноза и проведения лечебных манипуляций. Гастроскопия проводится обязательно, натощак. При проведении исследования утром последний приём пищи — лёгкий ужин накануне исследования не позднее 19 часов. Если исследование проводится во второй половине дня, ужин так же должен быть не позднее 20.00 и не обильным; утром в день исследования — легкий завтрак (чай, каша, булочка) и спустя 6 — 8 часов возможно проведение исследования (то есть, в течение 6 — 8 часов до исследования не принимать пищу и не пить жидкость).
Как подготовиться морально?
Это может прозвучать странно, но накануне вечером перед процедурой можно мысленно «поговорить с собой».
Скажите себе, что вас ждет неприятная процедура, что возможен рвотный рефлекс, попросите свой организм подготовиться к тому, что в горло будут запихивать трубку с камерой. Разъясните себе, что это необходимость для качественного обследования. Это нужно для того, чтобы для вашего тела и организма данная процедура не была неожиданностью. Попросите свое тело подготовиться морально и физически к этой процедуре.
Если вам страшно, то подумайте о том, чего вы боитесь. Мне кажется, что большинство страхов связано:
1. С болью при самой процедуре ФГДС. Самый неприятный момент при обследовании ФГДС это введение трубки через горло. В этот момент вы не чувствуете боли потому что вам обработают горло лидокаином. Это обезболивающее, оно довольно эффективное. Единственное, что вы можете почувствовать — это давление на ваше горло, которое длится не более двух секунд.
2. С рвотными позывами при обследовании. Увы, скорее всего этот момент будет для вас неизбежен. Но сразу можем заверить, что рвоты у вас точно не будет, при условии соблюдения рекомендаций перед подготовкой. Здесь все просто, желудок пуст. Вас может немного подташнивать во время процедуры, это нормально. Представьте, что вы отравились и вас чуть-чуть подташнивает. Примерно такие ощущения. Иногда у вас будут возникать рвотные рефлексы, это тоже нормально. Представьте, что вы надавили чем-то на корень языка и у вас появились позывы к рвоте. Примерно такие же ощущения. Но они не постоянные. Рвотные позывы, думаю, всем нам знакомы. Здесь не будет каких-то новых ощущений. Вы все знаете, что в этом нет боли. Просто неприятно.
Здесь все просто, желудок пуст. Вас может немного подташнивать во время процедуры, это нормально. Представьте, что вы отравились и вас чуть-чуть подташнивает. Примерно такие ощущения. Иногда у вас будут возникать рвотные рефлексы, это тоже нормально. Представьте, что вы надавили чем-то на корень языка и у вас появились позывы к рвоте. Примерно такие же ощущения. Но они не постоянные. Рвотные позывы, думаю, всем нам знакомы. Здесь не будет каких-то новых ощущений. Вы все знаете, что в этом нет боли. Просто неприятно.
По сути в этом и заключается вся неприятность процедуры. Во время обследования у вас могут появиться слезы. Это не страшно. Вы просто будете лежать и в какое-то время заметите, что у вас покатилась слеза. Это не сопровождается ни болями, ни жжением в глазах. Слезы текут от того, что затрагиваются рецепторы.
3. Со страхом нехватки кислорода. В данном случае точно нет повода для беспокойства. У вас будет достаточно кислорода в любую секунду вашего времени. Можно дышать и через нос, и через рот, можно проглатывать слюну.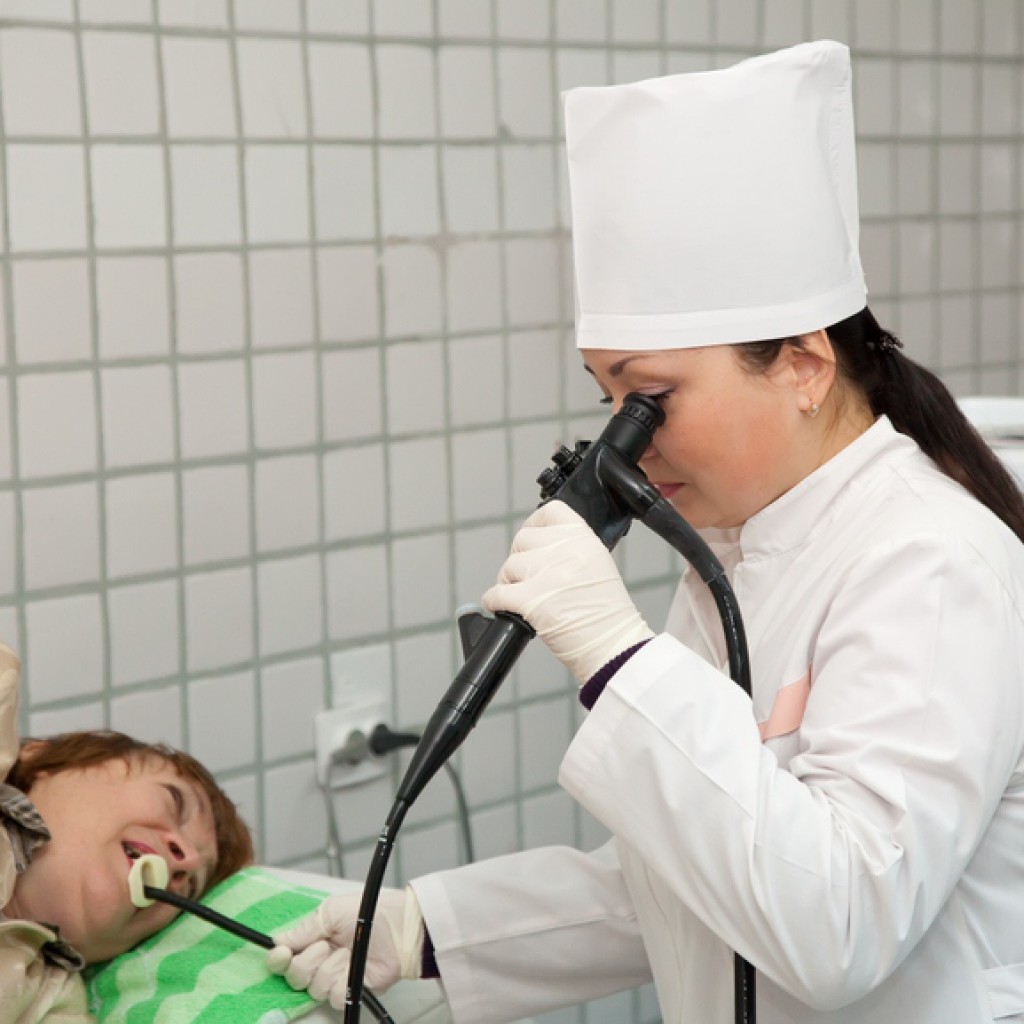 Но проглатывание будет сопровождаться с неприятным ощущением трубки в горле.
Но проглатывание будет сопровождаться с неприятным ощущением трубки в горле.
Важные рекомендации для подготовки к ФГДС желудка
Мы уже неоднократно писали, что гастроскопия – одно из важнейших обследований при заболеваниях желудочно-кишечного тракта. Однако ее проведение связано для пациента с определенным дискомфортом.
Нет, речь не о боли, болезненных ощущений при ФГДС как раз не бывает. Но из-за того, что трубка гастроскопа вводится в желудок через пищевод, начинается обильное слюноотделение и могут возникнуть рвотные позывы. Причем процедура требует от пациента определенной подготовки. Если он не сможет соблюсти несколько условий, то гастроскопию придется переделывать и снова оказываться в не самой комфортной для себя обстановке.
Поэтому, если врач назначил вам ФГДС, то внимательно выслушайте (а лучше запишите), какие требования нужно выполнить перед процедурой. В этой статье мы расскажем о самых общих принципах подготовки к фиброгастроскопии, но в каждом отдельном случае могут быть некоторые отличия, поэтому советы лечащего врача нужно соблюдать в первую очередь.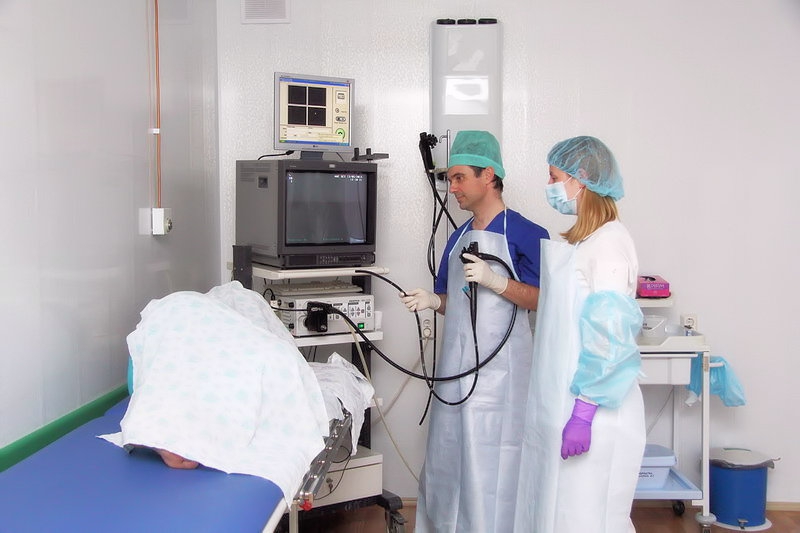
Как подготовиться к гастроскопии
Основные рекомендации касаются питания. ФГДС должна проводиться на голодный желудок, поэтому, как правило, обследование назначают на утренние часы.
Ужинать нужно за 3-4 часа до сна (чтобы последний прием пищи был за 10-12 часов до процедуры). Желательно воздержаться от тяжелой пищи (жареное мясо, орехи, шоколад, грибы). Также следует исключить и продукты, вызывающие повышенное газообразование (молоко, бобовые, капуста, виноград, яблоки, газированные напитки).
В рамках подготовки к гастроскопии за несколько дней следует отказаться от алкоголя и острой пищи. Непосредственно в день процедуры не рекомендуется курить – курение способствует выработке слизи в желудке, а это может привести к обострению рвотного рефлекса. Но строгого запрета нет, вы сами решаете – отказываться от табака или нет.
Также необходимо заранее сообщить врачу о всех медикаментах, которые вы регулярно принимаете. Возможно, некоторые из них необходимо будет на время исключить.
Что можно есть и пить перед ФГДС
Несмотря на существенные ограничения в еде, совсем голодать не придется. Например, можно спокойно перекусить отварной куриной грудкой, рыбой, гречкой или рисом.
Ограничения на напитки не такие строгие – воду можно пить вплоть до двух часов до начала гастроскопии, но только в небольшом количестве. Если речь идет о других напитках, то, например, вместо завтрака за 4 часа до процедуры можно выпить некрепкий сладкий чай. А вот молоко и газировку употреблять запрещается.
Как глотать зонд
Этот вопрос уже не имеет непосредственного отношения к подготовке к фиброгастроскопии желудка, однако поможет вам лучше понять, как проходит процедура.
Чтобы пациент случайно не сдавил шланг зубами, в рот вставляется специальный нагубник. Дальше следует самый неприятный для многих момент – проглатывание шланга. Однако с появлением местной анестезии этот процесс перестал быть столь уж дискомфортным — перед началом процедуры гортань обрабатывается раствором лидокаина..jpg)
После окончание ФГДС еще некоторое время нельзя будет есть, и, возможно, будут неприятные ощущения в животе.
В целом же гастроскопия – широко применяемая и отработанная диагностика, которая помогает эффективно лечить множество заболеваний. В сети клиник «Медицентр» все эндоскопические обследования проводят врачи высшей квалификационной категории. Процедура проходит максимально комфортно для пациента. В том числе есть возможно сделать ФГДС под наркозом.
Наши клиники в Санкт-Петербурге
Получить подробную информацию и записаться на прием Вы можете по телефону +7 (812) 640-55-25
Разница ФГДС и ФКС
Гастроскопия – основное обследование для диагностики заболеваний ЖКТ. В свою очередь она подразделяется на две процедуры: ФГС (фиброгастроэндоскопию) и ФГДС (фиброгастродуоденоскопию).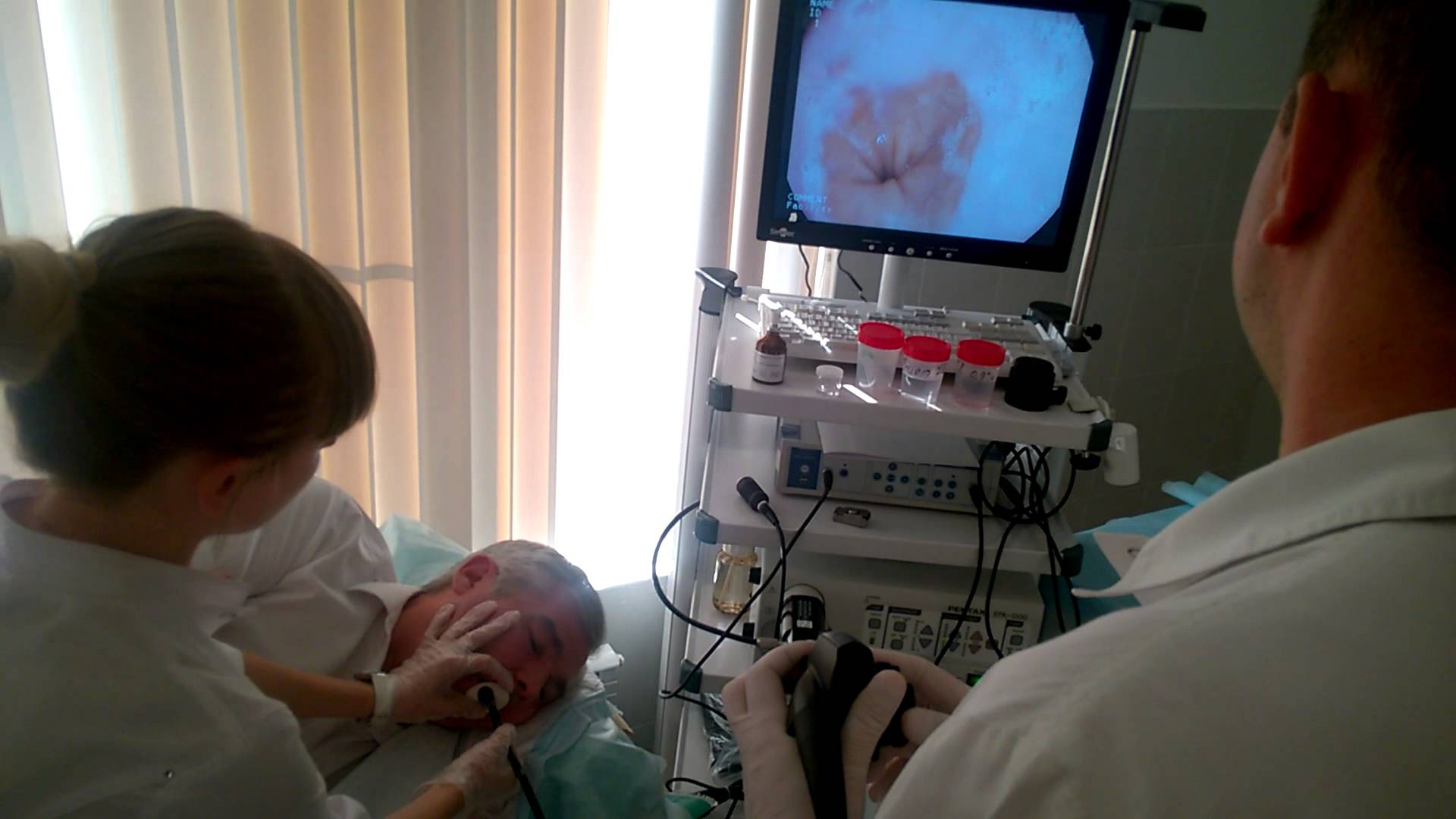 С точки зрения пациента оба этих исследования проводятся одинаково: в обоих случаях гастроскоп вводится внутрь пищевода, и врач осматривает стенки желудка. Однако разница все же присутствует.
С точки зрения пациента оба этих исследования проводятся одинаково: в обоих случаях гастроскоп вводится внутрь пищевода, и врач осматривает стенки желудка. Однако разница все же присутствует.
Во время ФГС обследуется только состояние желудка (слизистой, стенок, эпителиального слоя). При необходимости с помощью эндоскопа врач может взять биопсию и анализ на наличие бактерий Хеликобактер Пилори. ФГС назначает гастроэнтеролог при подозрении на язвенную болезнь, воспаление и наличие новообразований.
ФГДС – это расширенная версия ФГС, когда эндоскоп проникает не только в желудок, но и продвигается глубже, в двенадцатиперстную кишку. Это позволяет оценить желчевыводящие пути, обнаружить язву, опухоль или другие повреждения в верхнем отделе кишечника.
Для пациента ощущения при ФГДС и ФКС никак не отличаются – в желудке и кишечнике нет нервных окончаний, поэтому обе процедуры проходят безболезненно. Но все же они причиняют некоторый дискомфорт (повышенное слюноотделение, рвотные позывы). Поэтому иногда врачи даже рекомендуют проходить гастроскопию под наркозом.
Поэтому иногда врачи даже рекомендуют проходить гастроскопию под наркозом.
Как проводится ФГС и ФГДС
Гастроскопия – безболезненная, но крайне неприятная процедура. При глотании трубки эндоскопа может возникнуть рвотный рефлекс. Это естественная реакция, и, чтобы ее избежать, полость рта и гортань обрабатывают местным анестетиком.
Во время обследования пациент лежит на боку, а зонд постепенно вводится в пищевод. Неприятные ощущения вызывают обильное выделение слюны, но это нормальный процесс, поэтому не стоит из-за этого переживать.
Процедура занимает в среднем от 5 до 20 минут. При этом ФГДС длится несколько дольше, чем ФКС. Это объясняется тем, что при ФГДС обследование состоит из двух этапов. Сначала врач оценивает состояние желудка, а затем изучает двенадцатиперстную кишку. Но это единственное отличие в проведении процедуры, которое может заметить пациент. Поэтому на практике оба этих обследования принято называть одним словом – гастроскопия.
Есть ли разница в подготовке к ФКС и ФГДС
Никаких специфических различий при подготовке к этим обследованиям нет. Обе процедуры проводятся на голодный желудок, в течение нескольких дней до гастроскопии нельзя употреблять алкоголь, острые и «тяжелые» блюда. Также нужно заранее известить гастроэнтеролога о наличии хронических заболеваний.
Обе процедуры проводятся на голодный желудок, в течение нескольких дней до гастроскопии нельзя употреблять алкоголь, острые и «тяжелые» блюда. Также нужно заранее известить гастроэнтеролога о наличии хронических заболеваний.
В сети клиник «Медицентр» можно пройти оба этих обследования. Причем предусмотрено проведение ФГДС в состоянии медикаментозного сна.
Наши клиники в Санкт-Петербурге
Получить подробную информацию и записаться на прием Вы можете по телефону +7 (812) 640-55-25
ФГС желудка в Новосибирске — ЕвроМед клиника
ФГС (фиброгастроскопия) — широко распространенный и один из наиболее информативных диагностических методов исследования органов желудочно-кишечного тракта: пищевода, желудка и двенадцатиперстной кишки. Кроме того, ФГС дает возможность осуществлять наблюдение динамики развития заболевания.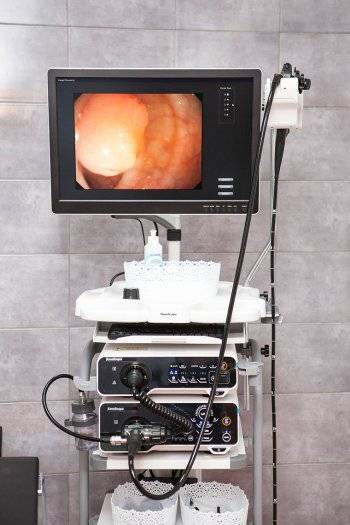
Также процедуру часто называют ФГДС (фиброгастродуоденоскопия) – по сути, разницы между ФГС и ФГДС нет, так как врач-эндоскопист при осмотре в любом случае осмотрит не только желудок, но и пищевод, и двенадцатиперстную кишку.
Показания к проведению ФГС
Фиброгастроскопия — это исследование высокой точности, которое позволяет подробно изучить состояние внутренней поверхности желудка, пищевода и кишечника и при необходимости взять образцы тканей из этих органов.
С помощью ФГС проводится диагностика заболеваний:
- дуоденит,
- различные эрозии,
- гастрит,
- язва желудка и двенадцатиперстной кишки,
- полипы желудка
и многие другие заболевания органов пищеварительной системы.
Также ФГС — самый точный метод диагностики рака желудка на ранней стадии.
Подготовка к ФГС
Гастроскопия проводится на голодный желудок в утренние часы. Вечером накануне исследования можно принимать пищу до 19 часов. За сутки стоит исключить потребление мяса, рыбы, бобовых и прочей трудно перевариваемой пищи. Утром перед проведением процедуры нельзя пить, есть, курить и жевать резинку.
Вечером накануне исследования можно принимать пищу до 19 часов. За сутки стоит исключить потребление мяса, рыбы, бобовых и прочей трудно перевариваемой пищи. Утром перед проведением процедуры нельзя пить, есть, курить и жевать резинку.
Методика проведения ФГС
Во время проведения ФГС гибкий шланг с лампочкой и видеокамерой на конце (фиброгастроскоп) вводится в пищеварительные органы пациента через рот. Уменьшить появление неприятных ощущений помогает местная анестезия: зев обрабатывают спреем с содержанием лидокаина. Во время проведения процедуры пациент находится на кушетке лежа на боку, зажав во рту пластиковый мундштук-загубник, при помощи которого вводится фиброгастроскоп. Для правильного введения аппарата пациенту необходимо совершить глотательное движение.
При проведении всех эндоскопических исследований мировые медицинские стандарты обязывают специалистов брать у пациента биоптаты (образцы тканей) для гистологического исследования. Гистология — самый точный метод выявления онкологических заболеваний на начальной стадии, морфологического подтверждения диагнозов, определения активности воспалительного процесса и т.д. Необходимо отметить, что взятие биоптатов не вызывает никаких неприятных или болезненных ощущений у пациента, поскольку в исследуемых органах отсутствуют нервные окончания. Более того – дискомфорт настолько незначителен, что процедуру легко переносят даже маленькие дети.
Гистология — самый точный метод выявления онкологических заболеваний на начальной стадии, морфологического подтверждения диагнозов, определения активности воспалительного процесса и т.д. Необходимо отметить, что взятие биоптатов не вызывает никаких неприятных или болезненных ощущений у пациента, поскольку в исследуемых органах отсутствуют нервные окончания. Более того – дискомфорт настолько незначителен, что процедуру легко переносят даже маленькие дети.
Продолжительность ФГС желудка не более 10-15 минут.
Безопасность ФГС
ФГС в «ЕвроМед клинике» в Новосибирске – процедура, совершенно безопасная для здоровья пациента. Все детали фиброгастроскопа, контактирующие с организмом пациента, проходят полный цикл стерилизации и очистки в автоматическом режиме. Это полностью исключает возможность передачи любых видов инфекции.
Хирургия под контролем флуоресценции
Abstract
Хирургическая резекция рака остается важным методом лечения.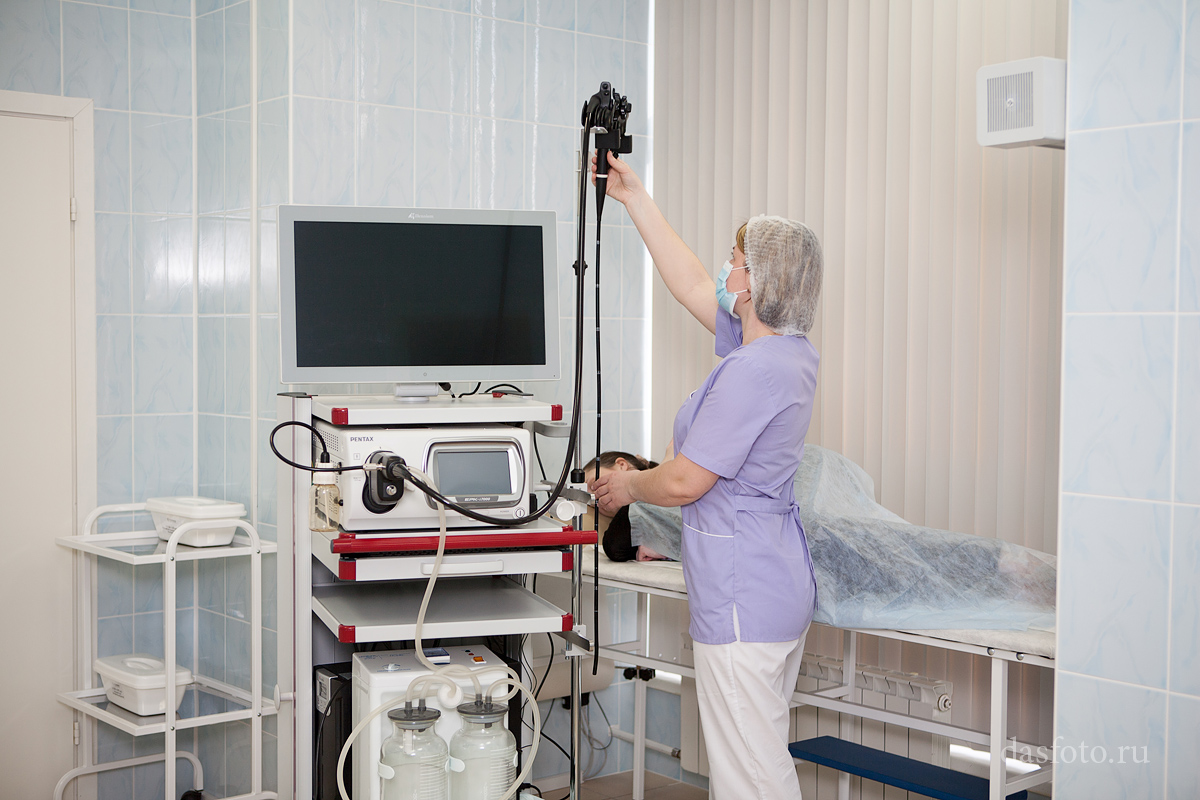 Несмотря на успехи в предоперационной визуализации, сама операция в первую очередь определяется способностью хирурга локализовать патологию с помощью обычной визуализации в белом свете. Хирургия под контролем флуоресценции (FGS) может использоваться для определения местоположения опухоли и ее границ во время процедуры. Интраоперационная визуализация опухолей может не только позволить более полные резекции, но и повысить безопасность, избегая ненужного повреждения нормальных тканей, что также может сократить время операции и уменьшить потребность в повторных операциях.Недавно был разработан ряд новых датчиков для визуализации FGS, которые дополняют небольшое, но полезное количество существующих датчиков. В этом обзоре мы описываем существующие и новые флуоресцентные зонды, которые могут помочь в FGS.
Несмотря на успехи в предоперационной визуализации, сама операция в первую очередь определяется способностью хирурга локализовать патологию с помощью обычной визуализации в белом свете. Хирургия под контролем флуоресценции (FGS) может использоваться для определения местоположения опухоли и ее границ во время процедуры. Интраоперационная визуализация опухолей может не только позволить более полные резекции, но и повысить безопасность, избегая ненужного повреждения нормальных тканей, что также может сократить время операции и уменьшить потребность в повторных операциях.Недавно был разработан ряд новых датчиков для визуализации FGS, которые дополняют небольшое, но полезное количество существующих датчиков. В этом обзоре мы описываем существующие и новые флуоресцентные зонды, которые могут помочь в FGS.
Ключевые слова: Хирургия под контролем флуоресценции, активируемый зонд, моноклональные антитела, молекулярная визуализация, постоянно активный зонд
Введение
Хирургия является основным методом лечения многих злокачественных новообразований. Например, 63–98% пациентов с раком легких, груди, мочевого пузыря и колоректального рака будут подвергаться хирургическому вмешательству (1).Цель операции — безопасно удалить как можно больше раковых опухолей. Степень удаления рака тесно связана с прогнозом. Однако возможность резекции опухоли в настоящее время зависит от визуальной локализации опухоли и / или возможности ее пальпировать. Первое ограничено низким контрастом между опухолями и фоновой тканью, и многие небольшие опухоли могут быть пропущены. Более того, определение границ опухоли часто должно проводиться вслепую с последующим патологическим анализом замороженных срезов.
Например, 63–98% пациентов с раком легких, груди, мочевого пузыря и колоректального рака будут подвергаться хирургическому вмешательству (1).Цель операции — безопасно удалить как можно больше раковых опухолей. Степень удаления рака тесно связана с прогнозом. Однако возможность резекции опухоли в настоящее время зависит от визуальной локализации опухоли и / или возможности ее пальпировать. Первое ограничено низким контрастом между опухолями и фоновой тканью, и многие небольшие опухоли могут быть пропущены. Более того, определение границ опухоли часто должно проводиться вслепую с последующим патологическим анализом замороженных срезов.
Наличие остаточных опухолевых клеток после резекции считается сильным предиктором рецидива опухоли и, следовательно, выживаемости.Многие исследования показывают, что положительные границы, определяемые как идентификация опухолевых клеток на переднем крае хирургического образца, связаны с увеличением местного рецидива и указывают на плохой прогноз при большинстве типов рака, включая рак головы и шеи (2), рак груди ( 3, 4), немелкоклеточный рак легкого (5), колоректальный рак (6), рак мочевого пузыря (7) и рак простаты (8). Несмотря на достижения в области предоперационной визуализации, такие как компьютерная томография (КТ), магнитно-резонансная томография (МРТ) и позитронно-эмиссионная томография, показатель положительности хирургического края существенно не изменился за последние несколько десятилетий (9), с показателем положительного края 15-60 % по всем видам рака (10–16).В настоящее время стандарт ухода за отрицательными краями основан на визуальном осмотре, пальпации и интраоперационном гистопатологическом анализе замороженных краев опухоли, каждый из которых имеет серьезные ограничения. Невооруженный глаз ограничен в способности обнаруживать небольшие опухоли. Чувствительность пальпации ограничена, и она все чаще не используется из-за более широкого использования роботизированной лапароскопической хирургии. Интраоперационный анализ замороженных срезов ограничен определенными типами тканей, занимает много времени и подвержен ошибкам при взятии проб.Анализ замороженных срезов не соответствует стойкой патологии в 5–15% случаев (17).
Несмотря на достижения в области предоперационной визуализации, такие как компьютерная томография (КТ), магнитно-резонансная томография (МРТ) и позитронно-эмиссионная томография, показатель положительности хирургического края существенно не изменился за последние несколько десятилетий (9), с показателем положительного края 15-60 % по всем видам рака (10–16).В настоящее время стандарт ухода за отрицательными краями основан на визуальном осмотре, пальпации и интраоперационном гистопатологическом анализе замороженных краев опухоли, каждый из которых имеет серьезные ограничения. Невооруженный глаз ограничен в способности обнаруживать небольшие опухоли. Чувствительность пальпации ограничена, и она все чаще не используется из-за более широкого использования роботизированной лапароскопической хирургии. Интраоперационный анализ замороженных срезов ограничен определенными типами тканей, занимает много времени и подвержен ошибкам при взятии проб.Анализ замороженных срезов не соответствует стойкой патологии в 5–15% случаев (17).
Во время операции был предложен ряд неоптических методов визуализации. Как правило, эти методы не нацелены на опухоль как таковую , а полагаются на анатомические аномалии для определения опухоли. Например, интраоперационная КТ и МРТ сыграли значительную роль в области нейрохирургического контроля изображений (18–20). Однако интраоперационные системы дороги, сложны и требуют места.Более того, их использование прерывает нормальный рабочий процесс хирургической процедуры, увеличивая время операции / анестезии. Эти методы в основном используются в нейрохирургии в крупных медицинских центрах.
Следовательно, необходимы практические методы увеличения способности хирурга удалять опухоли. Одним из таких методов является хирургия под контролем флуоресценции (FGS). Первое использование флуоресцентной визуализации в хирургии относится к 1948 году, когда хирурги использовали внутривенный флуоресцеин для усиления внутричерепных новообразований во время нейрохирургии (21). С тех пор дополнительные флуоресцентные агенты стали использоваться в различных хирургических операциях (22–24). Интраоперационная флуоресцентная визуализация предлагает преимущества высокой контрастности и чувствительности, низкой стоимости, отсутствия ионизирующего излучения, простоты использования, безопасности и высокой специфичности (25, 26). По сравнению со стандартным невооруженным зрением с использованием визуализации в белом свете, флуоресцентная визуализация в реальном времени помогает идентифицировать раковые ткани и очертить границы опухоли. Более того, улучшенная визуализация рака может уменьшить повреждение важных нормальных структур, таких как нервы, кровеносные сосуды, мочеточники и желчные протоки.
С тех пор дополнительные флуоресцентные агенты стали использоваться в различных хирургических операциях (22–24). Интраоперационная флуоресцентная визуализация предлагает преимущества высокой контрастности и чувствительности, низкой стоимости, отсутствия ионизирующего излучения, простоты использования, безопасности и высокой специфичности (25, 26). По сравнению со стандартным невооруженным зрением с использованием визуализации в белом свете, флуоресцентная визуализация в реальном времени помогает идентифицировать раковые ткани и очертить границы опухоли. Более того, улучшенная визуализация рака может уменьшить повреждение важных нормальных структур, таких как нервы, кровеносные сосуды, мочеточники и желчные протоки.
В этой обзорной статье мы сосредоточимся на используемых в настоящее время флуоресцентных датчиках, одобренных Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), и новых типах датчиков флуоресцентной визуализации для FGS, которые находятся в стадии разработки.
Текущий FGS
Экспоненциальный рост в области FGS демонстрируется количеством опубликованных статей в этой области, которое выросло с менее 50 в год в 1995 году до почти 500 в год в 2015 году (27). Кроме того, FGS добился ряда предварительных успехов (23, 28), а некоторые методы FGS уже достигли клинического успеха (29).FGS может улучшить скорость резекции опухоли при минимизации резекции нормальной ткани (9, 30, 31). Это может привести к улучшению клинических результатов.
По сравнению с дорогими традиционными методами визуализации оптические методы менее затратны и занимают меньше места. Одна оценка стоимости системы резекции и исследования с использованием флуоресценции (FLARE) составляет 120 000 долларов США и 40 000 долларов США для mini-FLARE (32, 33). Конечно, это не включает стоимость самого оптического зонда, но общие затраты намного ниже, чем при традиционной визуализации.Более того, поскольку он портативный, один инструмент может использоваться в нескольких операционных.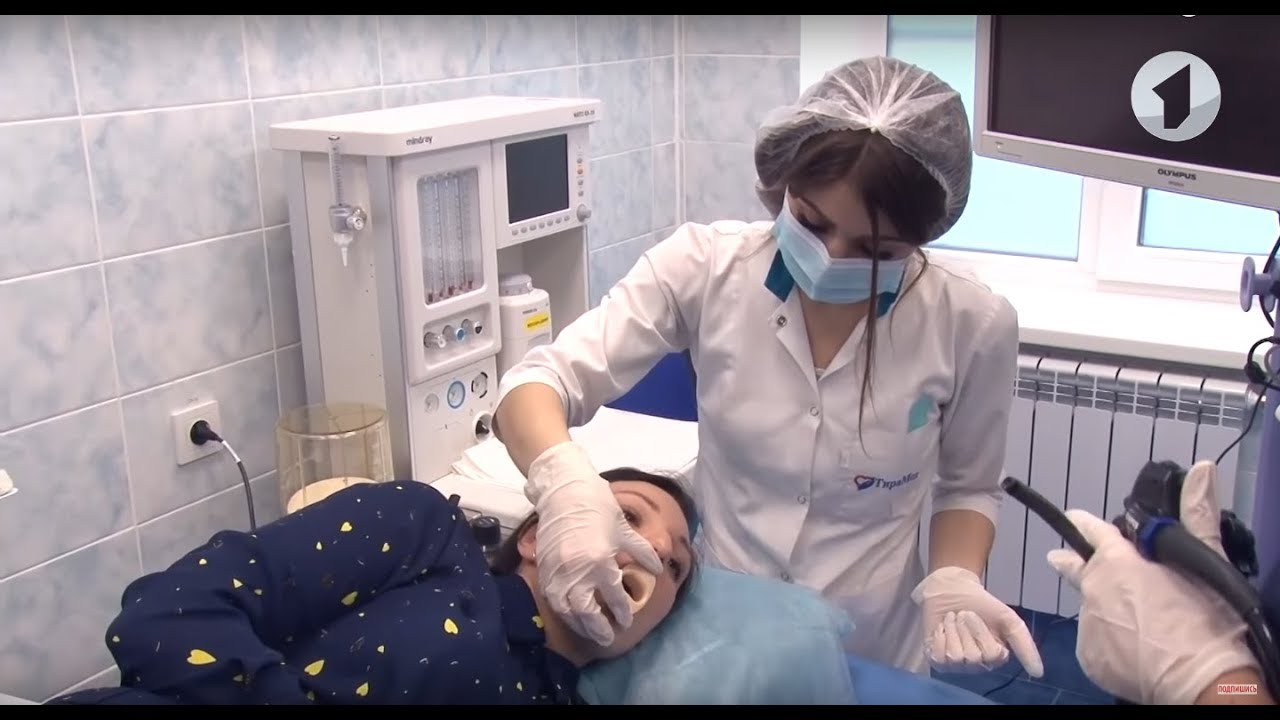
Хирургия под контролем флуоресценции в настоящее время используется для множества хирургических ситуаций, включая картирование сторожевых лимфатических узлов (СЛУ), идентификацию солидных опухолей, лимфографию, ангиографию и анатомическую визуализацию во время операции. Важно отметить, что FGS можно беспрепятственно использовать во время процедуры, не прерывая рабочий процесс хирурга. Это интегрирует FGS в хирургию, создавая многочисленные возможности для ее использования.Мы суммируем текущие клинические и доклинические методы FGS в таблице.
Таблица 1
Современные методы клинической и доклинической хирургии под контролем флуоресценции.
| Применение | Типы | Контрастное вещество | Статус | |
|---|---|---|---|---|
| Картирование контрольных лимфатических узлов | Рак груди | Индоцианин зеленый (ICG) (34–37) | Клинический | |
| Метилен синий (MB) (38, 39) | Клинический | |||
| Меланома | ICG (40, 41) | Клинический | ||
| Рак головы и шеи | ICG (42) | Клинический | ||
| Рак легкого | ICG (43) | Клинический | ||
| Рак пищевода | ICG (44, 45) | Клинический | ||
| Рак желудка | ICG (46, 47 ) | Клинический | ||
| Колоректальный рак | ICG (48) | Клинический | ||
| 9005 2 | Рак анального канала | ICG (49) | Клинический | |
| Рак простаты | ICG (50–52) | Клинический | ||
| Рак полового члена | ICG (51, 52) | Клиническая | ||
| Лимфография | Лимфоток | ICG (53–55) | Клиническая | |
| Ангиография | Церебральная аневризма | Флюоресцеин натрия (56–58) | Клиническая | |
| Коронарная артерия шунтирование | ICG (59, 60) | Клиническая | ||
| Аневризма брюшной аорты | ICG (61) | Клиническая | ||
| Абдоминальная хирургия | ICG (62, 63) | Клиническая | ||
| Реконструктивная хирургия | ICG (64–70) | Клиническая | ||
| Анатомическая визуализация | Холангиография | ICG (71, 72) | Клиническая | |
| Поджелудочная железа | MB (73) | Доклиническая | ||
| T700-F (74) | Доклиническая | |||
| Мочеточники | MB (75) | Доклинические исследования | ||
| Нервы | Различные флуоресцентно меченые пептиды (NP) (76, 77) | Доклинические исследования | ||
| Паратироидные и тироидные гранты | T700 и T700 fluorophores800 (78) | Доклинический | ||
| Гранты эндокринной системы | Различные флуорофоры ближнего инфракрасного диапазона (79–81) | Доклинические исследования | ||
| Визуализация опухоли | Злокачественная глиома | 5-ALA (82–86) | Клинический | |
| Флуоресцеин натрия (87–89) | Клинический | |||
| 90 052 | BLZ-100 (90) | Клинический | ||
| GB119 (91) | Доклинический | |||
| Метастазы в мозг | Флюоресцеин натрия (92, 93) | Клинический | ||
| Рак головы и шеи | Конъюгат IRDye800CW (94, 95) | Клинический | ||
| Конъюгат IRDye700DX (96) | Клинический | |||
| Гепатоцеллюлярная карцинома | ICG (97–100) | |||
| Метастазы в печени | ICG (99) | Клинический | ||
| Рак груди | MB (101) | Клинический | ||
| EC17 (102) | Клинический | |||
| Конъюгат IRDye800CW (102) | Клинический | |||
| LUM015 (103) | Клинический | |||
| AVB-620 (104) | Клинический | |||
| Образования в легких и грудной клетке | ICG (105) | Клинические | ||
| Фолат-флуоресцеина изотиоцианат (FITC) (106) | Клинический | |||
| EC17 (107) | Клинический | |||
| OTL38 (108) | Клинический | |||
| Рак яичников | ICG (109) | Клинический | ||
| Фолат-FITC (28) | Клинический | |||
| EC17 (110) | Клинический | |||
| OTL38 ( 111) | Клинический | |||
| gGlu-HMRG (112) | Доклинический | Рак поджелудочной железы | Зеленый конъюгат флуорофора (113, 114) | Доклинический |
| IRDye800CW конъюгат (102) | Доклинический | |||
| Инсулинома | MB (73 73 | Инсулинома | MB (73) Доклиническая | |
| Солитарная фиброзная опухоль (поджелудочная железа) | MB (115) | Доклиническая | ||
| Почечно-клеточная карцинома | EC17 (116) | Клиническая | ||
| OTL38 ( 102) | Клинический | |||
| Рак мочевого пузыря | 5-ALA / HAL (117–120) | Клинический | ||
| Рак простаты | Конъюгат ICG (121) | Доклинический | ||
| 5-ALA (122) | Клинический | |||
| G рак астры | ICG (123–125) | Клинический | ||
| Колоректальный рак | Зеленый конъюгат флуорофора (113) | Доклинический | ||
| Конъюгат IRDye800CW | ||||
| gGlu-HMRG (127) | Доклинический | |||
| Базальноклеточный рак | 5-ALA (128) | Клинический | ||
| GB119 (129) | Доклинический | |||
| Саркома | LUM015 (103) | Клиническая | ||
| Аденома паращитовидной железы | МБ (130) | Клиническая | ||
| Лапароскопическая и роботизированная хирургия | Нефрэктомия (131)Клинический | |||
| Холецистэктомия 9005 2 | ICG (72, 132) | Клиническая | ||
| Эзофагэктомия | ICG (133) | Клиническая | ||
| Гастрэктомия | ICG (134) | Клиническая | ||
| Адреналэктомия | ICG (135, 136) | Клиническая | ||
| Флуоресцентная эндоскопия | Аневризма головного мозга | ICG (137–139) | Клиническая | |
| Эндоназальная хирургия | ICG (140–142) | Клиническая | ||
| Ангиография | ICG (142, 143) | Клиническая | ||
| Опухоль головного мозга | ICG (140, 144, 145) | Клиническая | ||
| Опухоль головы и шеи | ICG (146) | Клинический | ||
| Рак желудка | ICG (123–125) | Clin ical | ||
| Маркировка опухоли | Татуировка толстой кишки | ICG (147–149) | Клиническая |
Клинически доступная флуоресцентная визуализация
Интерес к FGS резко возрос, что привело к устойчивому спросу для новых устройств и датчиков флуоресцентной визуализации. В настоящее время большая часть изображений FGS выполняется с помощью системы Novadaq SPY, которая была первой одобренной FDA в 2005 году; однако несколько новых систем флуоресцентной визуализации были впоследствии одобрены FDA, как показано в таблице. Эти системы одобрены для различных процедур, включая визуализацию кровотока, перфузию тканей и кровообращение в свободных лоскутах, пластическую хирургию и реконструктивную хирургию. Эти системы портативны, что позволяет полностью адаптировать их расположение в комнате к ситуации.Например, портативные камеры PDE и Fluobeam обладают тем преимуществом, что они компактны и удобны для получения флуоресцентных изображений в реальном времени. Другие камеры, такие как Quest Spectrum и VS3 Iridium, одновременно показывают изображение в белом свете и наложение изображения флуоресцентного датчика, что снижает отвлекающие факторы для хирурга (150, 151). В области онкологии груди система SPY применялась для мониторинга перфузии кожи при мастэктомиях с сохранением сосков с использованием ICG в качестве зонда для визуализации.
В настоящее время большая часть изображений FGS выполняется с помощью системы Novadaq SPY, которая была первой одобренной FDA в 2005 году; однако несколько новых систем флуоресцентной визуализации были впоследствии одобрены FDA, как показано в таблице. Эти системы одобрены для различных процедур, включая визуализацию кровотока, перфузию тканей и кровообращение в свободных лоскутах, пластическую хирургию и реконструктивную хирургию. Эти системы портативны, что позволяет полностью адаптировать их расположение в комнате к ситуации.Например, портативные камеры PDE и Fluobeam обладают тем преимуществом, что они компактны и удобны для получения флуоресцентных изображений в реальном времени. Другие камеры, такие как Quest Spectrum и VS3 Iridium, одновременно показывают изображение в белом свете и наложение изображения флуоресцентного датчика, что снижает отвлекающие факторы для хирурга (150, 151). В области онкологии груди система SPY применялась для мониторинга перфузии кожи при мастэктомиях с сохранением сосков с использованием ICG в качестве зонда для визуализации. Этот метод может определять расположение разрезов при мастэктомии и минимизировать ишемические осложнения (152).
Этот метод может определять расположение разрезов при мастэктомии и минимизировать ишемические осложнения (152).
Таблица 2
Доступные в клинической практике системы флуоресцентной визуализации, одобренные Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов.
| Система визуализации | Компания | Длина волны возбуждения (нм) | Источник света | Рабочее расстояние (см) | Поле зрения (см) | Наложение в реальном времени |
|---|---|---|---|---|---|---|
| SPY | Novadaq Technologies | 805 | Laser | ~ 30 | 19 × 14 | Нет |
| PDE | Hamamatsu Photonics | 760 | LED | ~ 20 | 5 × 5 до 10 × 6. 7 7 | Нет |
| Fluobeam 700 (800) | Fluoptics Minatec | 680 (750) | Laser | 15 ~ 25 | 2,2 × 1,5 до 20 × 14 | Нет |
| Quest Spectrum | Quest Medical Imaging | 400–1,000 | Laser | 5 ~ | 2,25 × 2,25 (расстояние 5 см) | Да |
| VS3 Iridium system | VisionSense | 805 | Laser | ~ 30 | 19 × 14 | Да |
Успешное устройство должно быть способно отображать изображения в белом свете RGB, флуоресцентные изображения и наложения изображений.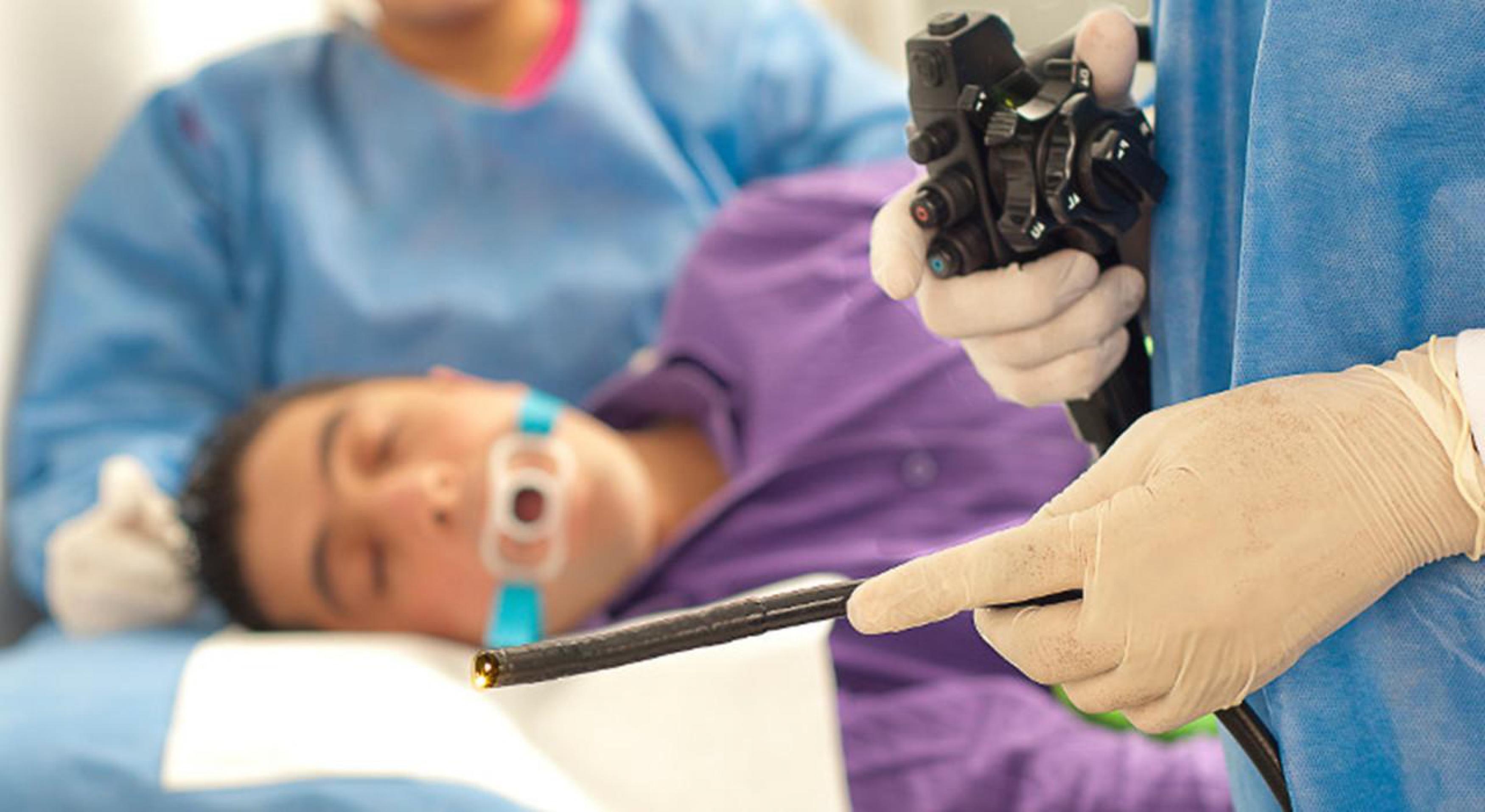 Устройство должно позволять количественно определять интенсивность света, насколько это возможно. Количественное определение позволяет использовать FGS в многоцентровых исследованиях и позволяет проводить сравнение в разные моменты времени у одного и того же пациента. Необходимы дальнейшие исследования, чтобы установить надежный количественный анализ флуоресцентной визуализации.
Устройство должно позволять количественно определять интенсивность света, насколько это возможно. Количественное определение позволяет использовать FGS в многоцентровых исследованиях и позволяет проводить сравнение в разные моменты времени у одного и того же пациента. Необходимы дальнейшие исследования, чтобы установить надежный количественный анализ флуоресцентной визуализации.
Текущее клиническое использование датчиков флуоресцентной визуализации
Биомедицинская флуоресцентная визуализация работает в длинах волн видимого спектра (400–700 нм), расширяясь до ближнего инфракрасного (NIR) спектра (700–900 нм).Доступно большое количество коммерчески доступных флуорофоров; однако немногие из них одобрены клинически. Хотя большинство флуоресцентных зондов излучают свет в видимом диапазоне, это, вероятно, наименее желательная часть спектра из-за перекрытия с аутофлуоресценцией тканей и высокого поглощения света тканями в видимом спектре. Флуорофоры NIR лучше подходят для визуализации in vivo .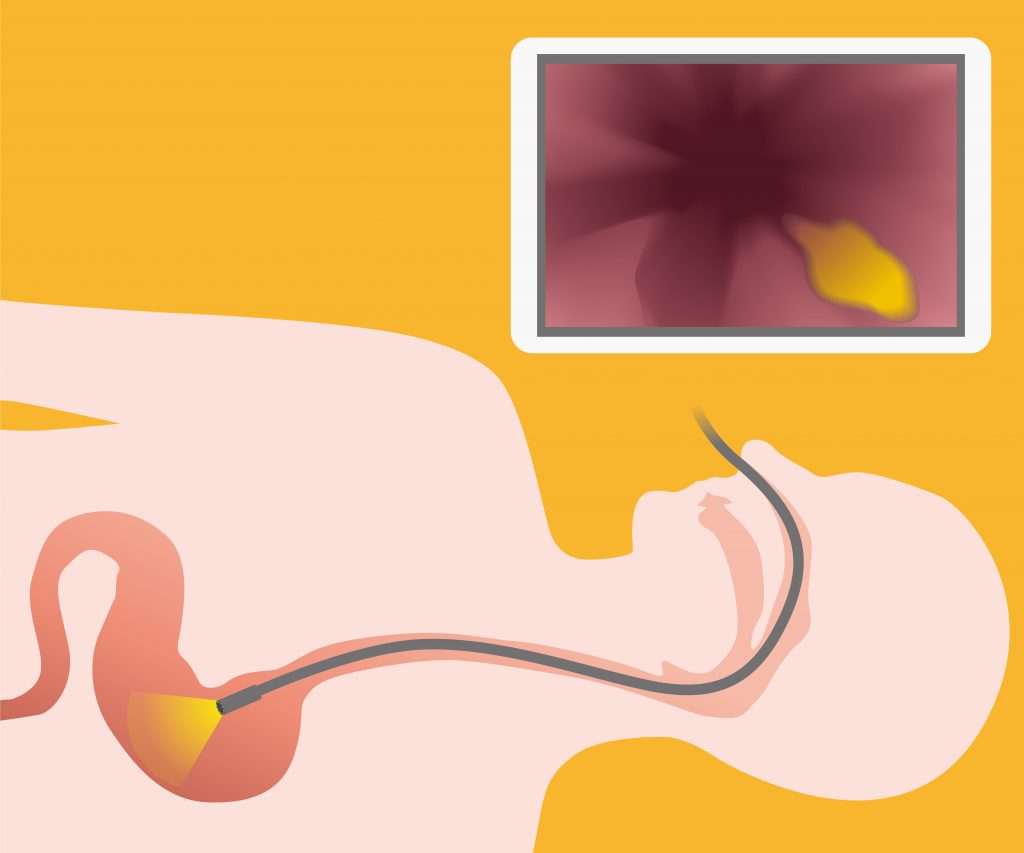 В то время как длины волн ниже 700 нм сильно поглощаются тканями эндогенными молекулами, такими как гемоглобин и миоглобин, длины волн выше 900 нм ограничиваются длинами волн поглощения воды и липидов (153–155).Поэтому флуорофоры, излучающие свет <700 или> 900 нм, ограничены в своей способности проникать в ткань (156). «Окно NIR» от 700 до 900 нм возникает из-за меньшего поглощения в тканях, что позволяет получать более глубокие изображения и обнаружение (153, 154). Таким образом, флуорофоры в ближнем инфракрасном диапазоне обладают отличным потенциалом для ФГС. Флуоресцентная визуализация с использованием NIR-флуорофоров улучшает навигацию при онкологической хирургии и обеспечивает более высокую чувствительность по сравнению с предоперационной визуализацией, визуальным осмотром и пальпацией во время операции (157).Далее мы сосредоточимся на используемых в настоящее время датчиках флуоресцентной визуализации в хирургической онкологии (таблица).
В то время как длины волн ниже 700 нм сильно поглощаются тканями эндогенными молекулами, такими как гемоглобин и миоглобин, длины волн выше 900 нм ограничиваются длинами волн поглощения воды и липидов (153–155).Поэтому флуорофоры, излучающие свет <700 или> 900 нм, ограничены в своей способности проникать в ткань (156). «Окно NIR» от 700 до 900 нм возникает из-за меньшего поглощения в тканях, что позволяет получать более глубокие изображения и обнаружение (153, 154). Таким образом, флуорофоры в ближнем инфракрасном диапазоне обладают отличным потенциалом для ФГС. Флуоресцентная визуализация с использованием NIR-флуорофоров улучшает навигацию при онкологической хирургии и обеспечивает более высокую чувствительность по сравнению с предоперационной визуализацией, визуальным осмотром и пальпацией во время операции (157).Далее мы сосредоточимся на используемых в настоящее время датчиках флуоресцентной визуализации в хирургической онкологии (таблица).
Таблица 3
Используемые в настоящее время флуоресцентные датчики, одобренные Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов.
| Зонд флуоресценции | Возбуждение | Излучение | Тип флуоресценции |
|---|---|---|---|
| Индоцианин зеленый | 780 нм | 820 нм | Индоцианин зеленый |
| Метиленовый синий (MB70) | 690 нм | MB | |
| 5-аминолевулиновая кислота (5-ALA) | 380–440 нм | 620 нм (щелочной pH) 634 нм (кислый pH) | Порфирин |
| Флюоресцеин натрия | 494 нм | 512 нм | Флуоресцеин |
| Фолат | 495 нм (фолат-FITC) | 520 нм (фолат-FITC) | Флуоресцеин-изотиоцианат (FITC) |
| IRDye800CW конъюгат | нм796 нм | IRDye800 | |
| Конъюгат IRDye700DX | 680 нм | 687 нм | IRDye700 900 52 |
| Активируемые зонды | Разные | Разные | Разные |
Индоцианин зеленый (ICG)
В настоящее время ICG является одним из наиболее часто используемых NIR-флуорофоров для FGS. ICG представляет собой водорастворимый анионный амфифильный трикарбоцианиновый зонд с молекулярной массой 776 Да (158, 159), который быстро связывается с белками плазмы в организме. Пик возбуждения составляет 780 нм, а пик излучения — 820 нм, что выходит за пределы диапазона автофлуоресценции большинства тканей. ICG был впервые произведен в 1955 году исследовательскими лабораториями Kodak, а в 1959 году он был одобрен FDA для ангиографии сетчатки. Исторически его использовали в клинических условиях для измерения сердечного выброса (160), функции печени (161) и ангиографии сетчатки (162).
ICG представляет собой водорастворимый анионный амфифильный трикарбоцианиновый зонд с молекулярной массой 776 Да (158, 159), который быстро связывается с белками плазмы в организме. Пик возбуждения составляет 780 нм, а пик излучения — 820 нм, что выходит за пределы диапазона автофлуоресценции большинства тканей. ICG был впервые произведен в 1955 году исследовательскими лабораториями Kodak, а в 1959 году он был одобрен FDA для ангиографии сетчатки. Исторически его использовали в клинических условиях для измерения сердечного выброса (160), функции печени (161) и ангиографии сетчатки (162).
На протяжении всей своей истории ICG поддерживала высокий индекс безопасности (25, 163, 164), поскольку количество аллергических реакций очень низкое (1: 10 000, по данным производителя) (165). ICG также допускает многократное повторное использование из-за его короткого периода полураспада от 150 до 180 с и выводится исключительно печенью (166).
Картирование SNL под контролем ICG в ближней инфракрасной области было выполнено при различных раковых заболеваниях, как показано в таблице. ICG также использовался для лимфографии (167), ангиографии (61, 168), реконструктивной хирургии (65, 67), холангиографии (71) и визуализации опухолей (99) и т. Д.Использование ICG для определения опухолей оказалось успешным. Например, флуоресцентная визуализация ICG выявила 100% первичных гепатоцеллюлярных карцином (ГЦК), а в 40% случаев также выявила дополнительные небольшие (3–6 мм) ГЦК, которые в противном случае остались бы незамеченными (98).
ICG также использовался для лимфографии (167), ангиографии (61, 168), реконструктивной хирургии (65, 67), холангиографии (71) и визуализации опухолей (99) и т. Д.Использование ICG для определения опухолей оказалось успешным. Например, флуоресцентная визуализация ICG выявила 100% первичных гепатоцеллюлярных карцином (ГЦК), а в 40% случаев также выявила дополнительные небольшие (3–6 мм) ГЦК, которые в противном случае остались бы незамеченными (98).
Метиленовый синий (MB)
Метиленовый синий представляет собой гетероциклическое ароматическое соединение с молекулярной массой 320 Да (51). Это одобренный FDA видимый (темно-синий) контрастный агент. При достаточном разбавлении МБ действует как флуоресцентный краситель ближнего инфракрасного диапазона, который действует в оптическом окне NIR с пиком поглощения при 670 нм и пиком эмиссии при 690 нм и естественным образом выводится с мочой (51).МБ был первым полностью синтетическим лекарством, используемым в медицине и использовался для лечения малярии еще в 1891 году Гутманном и Эрлихом (169). МБ по-прежнему применяется и исследуется для лечения различных медицинских применений в клинических условиях, включая метгемоглобинемии и энцефалопатию, вызванную ифосфамидом (170, 171). МБ также использовался для выявления рака груди (101) и нейроэндокринных опухолей (73) и обычно используется для картирования СЛУ (38, 39), а также для идентификации урологических опухолей (51, 52) и опухолей паращитовидной железы. железы (130).
МБ по-прежнему применяется и исследуется для лечения различных медицинских применений в клинических условиях, включая метгемоглобинемии и энцефалопатию, вызванную ифосфамидом (170, 171). МБ также использовался для выявления рака груди (101) и нейроэндокринных опухолей (73) и обычно используется для картирования СЛУ (38, 39), а также для идентификации урологических опухолей (51, 52) и опухолей паращитовидной железы. железы (130).
Метиленовый синий относительно безопасен; однако использование МБ потенциально может привести к сердечным аритмиям, коронарной вазоконстрикции, снижению сердечного выброса, снижению почечного кровотока и брыжеечного кровотока, а также повышению легочного сосудистого давления (172). Хотя МБ накапливается в большинстве опухолей, количество накопления зависит от типа опухоли. Следовательно, требуется соответствующая концентрация красителя для каждого типа опухоли (38).
5. -Аминолевулиновая кислота (5-ALA)
5-ALA является основным субстратом для синтеза протопорфирина и клинически используется для обнаружения опухолей и лечения опухолей (фотодинамическая терапия; PDT) в качестве вещества, одобренного FDA. 5-ALA, обычно вводимая в форме местного или перорального применения, индуцирует синтез и накопление флуоресцентной молекулы протопорфирина IX (PpIX) в эпителии и опухолевых тканях (83, 85, 86). PpIX, индуцированный 5-ALA, проявляет несколько физико-химических состояний в зависимости от микроокружения. Одним из наиболее важных параметров, влияющих на состояние PpIX, является pH. В диапазоне pH от 3 до 11,5 есть два различных состояния: пики эмиссии при 620 нм в щелочной среде и пики эмиссии при 634 нм в кислой среде после возбуждения видимым синим светом с длиной волны 380-440 нм (173, 174).
5-ALA, обычно вводимая в форме местного или перорального применения, индуцирует синтез и накопление флуоресцентной молекулы протопорфирина IX (PpIX) в эпителии и опухолевых тканях (83, 85, 86). PpIX, индуцированный 5-ALA, проявляет несколько физико-химических состояний в зависимости от микроокружения. Одним из наиболее важных параметров, влияющих на состояние PpIX, является pH. В диапазоне pH от 3 до 11,5 есть два различных состояния: пики эмиссии при 620 нм в щелочной среде и пики эмиссии при 634 нм в кислой среде после возбуждения видимым синим светом с длиной волны 380-440 нм (173, 174).
Онкоспецифический FGS с 5-ALA был успешно применен для резекции злокачественных глиом в Европе после того, как исследования четко продемонстрировали клинические преимущества в отношении полноты удаления опухоли (полная резекция с 5-ALA на 65% по сравнению с 36% в белом свете. группа) и выживаемость без прогрессирования с его использованием (83). 5-ALA и его производные также описаны при раке мочевого пузыря (117, 118, 120) и раке простаты (122).
Использование 5-ALA ограничено его относительно высокой стоимостью и неудобным методом введения (его вводят перорально за несколько часов до его использования).Высокий риск сенсибилизации кожи в течение 24 часов после операции (пациент не должен подвергаться воздействию солнечных лучей или сильного искусственного света) также представляет проблему для его использования (175).
Флуоресцеин натрия
Флуоресцеин натрия — это флуоресцентный препарат, который можно использовать внутривенно для улучшения визуализации опухолевой ткани головного мозга, главным образом на основе неспецифической сосудистой утечки. Он также используется для ангиографии сетчатки (56–58). Флуоресцеин натрия представляет собой натриевую соль и органический флуоресцентный краситель с пиком возбуждения при 494 нм и пиком эмиссии при 512 нм.Он безопасно используется у людей в течение многих лет, преимущественно в офтальмологии для ангиографии сетчатки, а стоимость флуоресцеина натрия относительно невысока по сравнению со стоимостью 5-ALA (176). Флуоресцеин натрия обычно виден невооруженным глазом при высоких дозах (20 мг / кг массы тела) и наблюдается через желтый фильтр 560 нм при более низких дозах, что позволяет лучше различать ткани с более естественными цветами (177, 178).
Флуоресцеин натрия обычно виден невооруженным глазом при высоких дозах (20 мг / кг массы тела) и наблюдается через желтый фильтр 560 нм при более низких дозах, что позволяет лучше различать ткани с более естественными цветами (177, 178).
Использование флуоресцеина натрия для идентификации внутричерепных опухолей известно с 1947 г. (179).В качестве агента ФГС флуоресцеин натрия обычно используется для идентификации глиобластомы (88) и метастатических опухолей головного мозга (92, 93). Его также использовали для внутричерепной ангиографии (56–58).
Новые датчики флуоресцентной визуализации
Идеальный датчик флуоресцентной визуализации должен обеспечивать отличный контраст между опухолью или пораженным лимфатическим узлом и здоровой тканью (180). Поэтому актуальной проблемой является создание зондов для флуоресцентной визуализации с высокой селективностью в отношении опухолей, высоким соотношением опухоли к фону и минимальной токсичностью (155).
Текущие клинические исследования основаны на уже одобренных контрастных веществах. Наиболее часто используемые флуорофоры — это агенты пула крови (включая ICG), которые не обладают специфической специфичностью для опухолей или нормальных тканей и, следовательно, не являются идеальными флуорофорами для FGS. В настоящее время исследуется ряд новых агентов, в том числе несколько красителей из семейства цианинов, таких как Cy5.5, Cy7, Cy7.5, ИК-красители, составы наночастиц и красители видимого спектра (181). Большинство исследований сосредоточено на увеличении доступности новых флуоресцентно меченных агентов для определения важных ориентиров, таких как границы опухоли, лимфатические узлы и жизненно важные структуры, представляющие интерес для хирургов.Новое поколение агентов, нацеленных на специфические антигены, основано на антителах (113, 182, 183), нанотелах (184), аптамерах и пептидах (77). Другие подходы используют ферменты для активации флуоресценции (185–189).
Наиболее часто используемые флуорофоры — это агенты пула крови (включая ICG), которые не обладают специфической специфичностью для опухолей или нормальных тканей и, следовательно, не являются идеальными флуорофорами для FGS. В настоящее время исследуется ряд новых агентов, в том числе несколько красителей из семейства цианинов, таких как Cy5.5, Cy7, Cy7.5, ИК-красители, составы наночастиц и красители видимого спектра (181). Большинство исследований сосредоточено на увеличении доступности новых флуоресцентно меченных агентов для определения важных ориентиров, таких как границы опухоли, лимфатические узлы и жизненно важные структуры, представляющие интерес для хирургов.Новое поколение агентов, нацеленных на специфические антигены, основано на антителах (113, 182, 183), нанотелах (184), аптамерах и пептидах (77). Другие подходы используют ферменты для активации флуоресценции (185–189).
В следующих разделах мы суммируем прогресс, достигнутый в нескольких конкретных целевых агентах оптической визуализации для FGS.
Фолат-нацеленный FGS
Фолатный рецептор обычно активируется на опухолевых клетках и, следовательно, является хорошим кандидатом для флуоресцентно меченого целевого агента общего назначения.Примером является фолиевая флюоресцеина изотиоцианат (фолат-FITC), который возбуждает на длине волны 495 нм и излучает на длине волны 520 нм (190). Фолат и эти аналоги фолиевой кислоты интернализуются в клетке посредством эндоцитоза, опосредованного рецептором , в течение 2 часов (191). Попав внутрь эндосомы, конъюгат остается неповрежденным и, следовательно, может оставаться флуоресцентным после интернализации (191, 192). Эта стабильность привела к разработке широкого спектра конъюгатов, нацеленных на фолат. van Dam et al. использовали изотиоцианат фолиевой кислоты для идентификации опухолевых имплантатов у пациентов с раком яичников, перенесших абдоминальную операцию (28).Также известно, что аденокарцинома легкого экспрессирует высокий уровень фолатного рецептора α (193, 194). Это было использовано Okusanya et al. которые продемонстрировали, что аденокарциномы легких демонстрируют флуоресценцию у 92% (46/50) пациентов с фолат-FITC (106). Другой аналог фолиевой кислоты, EC17, также использовался для визуализации почечно-клеточного рака, хотя были обнаружены только два из четырех видов рака (116). В другом исследовании с использованием EC17 для интраоперационного выявления рака яичников Tummers et al. показали, что добавление FGS привело к увеличению резекции злокачественных опухолей на 16% по сравнению с визуальным осмотром и пальпацией (110).Конечно, клиническое значение этого увеличения все еще остается неопределенным. Другой аналог фолиевой кислоты, OTL38, использовался для определения границ почечно-клеточной карциномы во время частичной нефрэктомии (102) и для выявления рака яичников (111). Hoogstins et al. также сообщили, что OTL38 накапливается в α-положительных опухолях и метастазах по фолатному рецептору у 12 пациентов с раком яичников, что позволяет хирургу резектировать дополнительно 29% злокачественных новообразований, которые не были идентифицированы при осмотре и / или пальпации (111).
Это было использовано Okusanya et al. которые продемонстрировали, что аденокарциномы легких демонстрируют флуоресценцию у 92% (46/50) пациентов с фолат-FITC (106). Другой аналог фолиевой кислоты, EC17, также использовался для визуализации почечно-клеточного рака, хотя были обнаружены только два из четырех видов рака (116). В другом исследовании с использованием EC17 для интраоперационного выявления рака яичников Tummers et al. показали, что добавление FGS привело к увеличению резекции злокачественных опухолей на 16% по сравнению с визуальным осмотром и пальпацией (110).Конечно, клиническое значение этого увеличения все еще остается неопределенным. Другой аналог фолиевой кислоты, OTL38, использовался для определения границ почечно-клеточной карциномы во время частичной нефрэктомии (102) и для выявления рака яичников (111). Hoogstins et al. также сообщили, что OTL38 накапливается в α-положительных опухолях и метастазах по фолатному рецептору у 12 пациентов с раком яичников, что позволяет хирургу резектировать дополнительно 29% злокачественных новообразований, которые не были идентифицированы при осмотре и / или пальпации (111). Недавно и EC17, и OTL38 также использовались для интраоперационной визуализации опухоли легкого (107, 108). Как и все нацеленные агенты, фолат-FITC ограничен для использования только в опухолях, экспрессирующих фолатный рецептор, и, благодаря видимому свету, излучаемому FITC, агент имеет ограниченную глубину проникновения.
Недавно и EC17, и OTL38 также использовались для интраоперационной визуализации опухоли легкого (107, 108). Как и все нацеленные агенты, фолат-FITC ограничен для использования только в опухолях, экспрессирующих фолатный рецептор, и, благодаря видимому свету, излучаемому FITC, агент имеет ограниченную глубину проникновения.
Флуоресцентные зонды на основе моноклональных антител
Возможно, наиболее распространенные зонды FGS основаны на моноклональных антителах (mAb), конъюгированных с флуоресцентным красителем. Существует как минимум два сценария, в которых флуоресцентные зонды на основе mAb могут стать клинически полезными.Один из них — это навигация под контролем флуоресценции, которая помогает хирургам обнаруживать крошечные поражения и определять границу между раком и нормальной тканью. Другой заключается в отборе пациентов, чьи раковые клетки экспрессируют достаточное количество мишени для молекулярно-направленной терапии, такой как конъюгаты антитело-лекарство или конъюгаты антитело-фотоабсорбент.
Многообещающие доклинические примеры направленных флуоресцентно меченных зондов включают антиканцерогенный антиген при раке поджелудочной железы и колоректальном раке, конъюгированный с зеленым флуорофором (113), антиуглеводный антиген 19-9 при раке поджелудочной железы, конъюгированный с зеленым флуорофором (114), эпидермальный фактор роста рецептор (EGFR) и EGFR типа 2 (HER2) при раке груди (195–197) и простатоспецифический мембранный антиген (PSMA) при раке простаты, конъюгированный с ICG (121).Большинство флуоресцентных зондов на основе mAb предназначены для системного введения. По сравнению с другими способами введения, такими как пероральная или внутриопухолевая инъекция, системное введение обеспечивает более однородное микрораспределение. Более того, системное введение позволяет пройти достаточное время вымывания, чтобы устранить неспецифическую флуоресценцию крови и мочевыводящих путей (22). В отличие от внутриопухолевой инъекции системное введение также позволяет обнаруживать ранее нераспознанные опухолевые очаги или метастазы.
Немногие из этих флуоресцентных зондов на основе mAb прошли клинические испытания. Одно из них — первое клиническое испытание на людях флуоресцентной навигации для помощи при хирургических вмешательствах при раке головы и шеи. В этом исследовании используется конъюгат анти-EGFR-антитела цетуксимаб-IRDye800CW для лечения рака головы и шеи (94, 95). В этом исследовании Rosenthal et al. продемонстрировали, что конъюгат EGFR mAb-флуорофор был безопасным и эффективным. Отношение целевого показателя к фоновому значению (TBR), достигнутое в этом исследовании (среднее TBR, равное 5.2 в максимальном диапазоне доз) повысили точность принятия хирургических решений (95). Недавно цетуксимаб-IRDye800CW или бевацизумаб-IRDye800CW (нацеленный на фактор роста эндотелия сосудов) также прошел клинические испытания, направленные на аденокарциному поджелудочной железы, рак толстой кишки и рак груди (102, 126). Было отмечено, что конъюгация IRDye800CW значительно сокращает период полувыведения цетуксимаба в кровотоке, несмотря на низкое соотношение конъюгации антитело-краситель (примерно 1) (95). Быстрый клиренс конъюгатов mAb-краситель может помочь снизить фоновый сигнал; тем не менее, это может одновременно поставить под угрозу накопление опухоли.В совокупности эти изменения могут снизить общую производительность агента.
Быстрый клиренс конъюгатов mAb-краситель может помочь снизить фоновый сигнал; тем не менее, это может одновременно поставить под угрозу накопление опухоли.В совокупности эти изменения могут снизить общую производительность агента.
Еще одно интересное достижение с потенциальными последствиями для FGS — это метод, называемый «фотоиммунотерапия в ближнем инфракрасном диапазоне» (NIR-PIT) (96). NIR-PIT основан на антителе, которое нацелено на антиген клеточной поверхности, но конъюгировано с фотопоглощающим красителем (IRDye700DX), который обладает как флуоресцентными характеристиками, так и способностью повреждать клетки, с которыми оно конъюгировано. Таким образом, NIR-PIT обладает двойной способностью локализовать опухоли и избирательно устранять раковые клетки.Цитотоксические эффекты NIR-PIT наблюдаются только тогда, когда конъюгат mAb-IR700 связывается с рецепторами на клеточной мембране; фототоксичность не наблюдается, когда конъюгат присутствует, но еще не связан (96). Таким образом, NIR-PIT обеспечивает тщательно отобранное целевое уничтожение раковых клеток. Было показано, что NIR-PIT эффективен в отношении множества различных типов раковых клеток, проявляющих ряд поверхностных антигенов, таких как EGFR, CD20, мезотелин и PSMA (198–202). Кроме того, недавно было завершено первое на людях исследование фазы 2 NIR-PIT у пациентов с неоперабельным раком головы и шеи, и этот агент коммерциализируется.NIR-PIT имеет большой потенциал в качестве нового метода лечения рака для многих типов опухолей в сочетании с FGS.
Было показано, что NIR-PIT эффективен в отношении множества различных типов раковых клеток, проявляющих ряд поверхностных антигенов, таких как EGFR, CD20, мезотелин и PSMA (198–202). Кроме того, недавно было завершено первое на людях исследование фазы 2 NIR-PIT у пациентов с неоперабельным раком головы и шеи, и этот агент коммерциализируется.NIR-PIT имеет большой потенциал в качестве нового метода лечения рака для многих типов опухолей в сочетании с FGS.
Эти датчики флуоресцентной визуализации, в том числе IRDye700DX и IRDye800CW, обычно дают сигнал флуоресценции «всегда включен». Следовательно, флуоресценция в раковых тканях примерно связана с количеством конъюгированных mAb, связанных с опухолью. Демонстрируя достаточную экспрессию молекул-мишеней, активируемые флуоресцентные зонды могут быть полезны для отбора подходящих пациентов, которых можно было бы эффективно лечить с помощью FGS.
Активируемые флуоресцентные зонды
Исходя из фармакокинетики, «идеальный» нацеливающий агент in vivo еще не разработан. Основным недостатком «постоянно включенных» зондов является то, что они излучают сигнал независимо от их близости или взаимодействия с тканями-мишенями. В результате возникает значительный фоновый сигнал, с которым нужно бороться. Чтобы разработать превосходные зонды для молекулярной визуализации, нужно либо (1) максимизировать сигнал от мишени, (2) минимизировать сигнал от фона, либо (3) сделать и то, и другое.Все это приводит к улучшению TBR, что, в свою очередь, повышает чувствительность и специфичность обнаружения опухолей с помощью визуализации (203).
Основным недостатком «постоянно включенных» зондов является то, что они излучают сигнал независимо от их близости или взаимодействия с тканями-мишенями. В результате возникает значительный фоновый сигнал, с которым нужно бороться. Чтобы разработать превосходные зонды для молекулярной визуализации, нужно либо (1) максимизировать сигнал от мишени, (2) минимизировать сигнал от фона, либо (3) сделать и то, и другое.Все это приводит к улучшению TBR, что, в свою очередь, повышает чувствительность и специфичность обнаружения опухолей с помощью визуализации (203).
Активируемые флуоресцентные зонды («умные зонды») нацелены на опухолевые клетки, используя преимущества физиологических различий между раковыми и нормальными клетками, тем самым улучшая обнаружение границ опухоли (204). Поскольку активируемые зонды не излучают сигналы до контакта с целью, несвязанные зонды не выдают сигнал. Следовательно, меньше фонового сигнала, что снижает чувствительность и специфичность, что приводит к абсолютному увеличению TBR (205). Следовательно, по сравнению с «постоянно включенными» флуоресцентными зондами активируемые флуоресцентные зонды имеют более высокий TBR (203). Доклинические исследования показали достоинства этого подхода (206–208). Например, при использовании антитела в качестве платформы для активируемых зондов для визуализации активируемые зонды на основе IgG обычно дают как самый высокий сигнал (из-за высокого связывания), так и самый высокий TBR (из-за отсутствия фонового сигнала) по сравнению с «всегда включенным». ”Зонды (203, 209, 210) (рисунок).
Следовательно, по сравнению с «постоянно включенными» флуоресцентными зондами активируемые флуоресцентные зонды имеют более высокий TBR (203). Доклинические исследования показали достоинства этого подхода (206–208). Например, при использовании антитела в качестве платформы для активируемых зондов для визуализации активируемые зонды на основе IgG обычно дают как самый высокий сигнал (из-за высокого связывания), так и самый высокий TBR (из-за отсутствия фонового сигнала) по сравнению с «всегда включенным». ”Зонды (203, 209, 210) (рисунок).
Сравнение флуоресцентных зондов с молекулярной направленностью, использующих стратегии постоянной и активируемой флуоресценции.Радиоактивно меченый трастузумаб, нацеленный на HER2 с постоянно включенными флуорофорами, показывает как связанные, так и несвязанные агенты (левая и правая опухоли), что приводит к плохому соотношению мишени к фону (TBR). Напротив, активируемый флуоресцентный зонд, трастузумаб, меченный индоцианиновым зеленым (ICG), отображает только HER2-экспрессирующие опухоли (правая опухоль) без фонового сигнала, приводящего к более высокой TBR.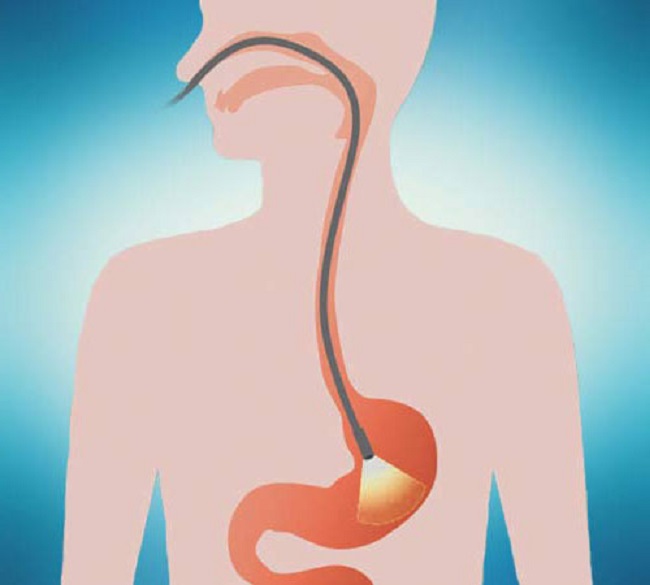 Перепечатано из публикации (210) с разрешения Elsevier.
Перепечатано из публикации (210) с разрешения Elsevier.
Существует два основных типа активируемых флуоресцентных зондов (рисунок) (203, 207, 211).Один из типов — это активируемые ферментативно активируемые флуоресцентные зонды, которые существуют в гашеном состоянии до тех пор, пока они не активируются ферментативным расщеплением в основном вне клеток (212, 213) (рисунок). Хорошо известными целевыми ферментами являются катеспсин, матриксные металлопротеиназы (MMP), γ-глутамилтрансфераза (GGT) и бета-галактозидазы. Некоторые из активируемых ферментативно активируемых флуоресцентных зондов можно применять местно или местно.
Схематическое объяснение двух типов активируемых флуоресцентных зондов.Активация флуоресценции молекулярно-направленных активируемых зондов происходит внутриклеточно (слева), тогда как реактивная активация ферментов обычно происходит во внеклеточной среде (справа). Печатается с разрешения Ref. (203). Авторское право 2011 г., Американское химическое общество.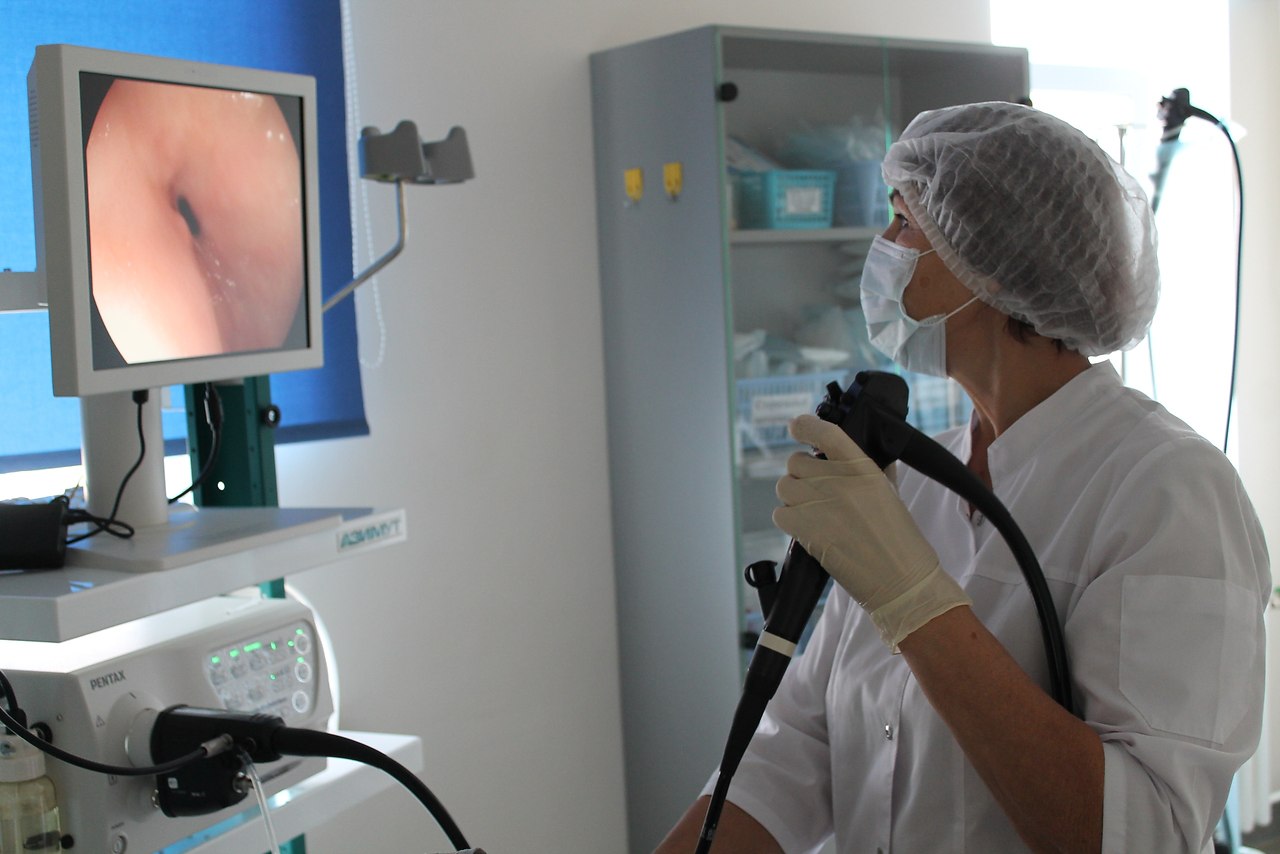
Другой тип активируемых флуоресцентных зондов — это активируемые молекулярным связыванием флуоресцентные зонды, которые блокируются до тех пор, пока не активируются в клетках-мишенях посредством эндолизосомной обработки (рисунок). Внутри лизосомы катаболизм может происходить в таких условиях, как низкий pH, протеазная активность или окисление, что может высвободить флуорофор из его гашеного состояния.Например, pH-активируемый флуоресцентный зонд излучает свет только в опухолях из-за их кислого микроокружения, что приводит к высокому TBR, тогда как контрольные «постоянно включенные» зонды производят более низкий TBR из-за более высокого фонового сигнала (рисунок) (155, 214). Этот тип активируемого флуоресцентного зонда вводится систематически посредством внутривенной инъекции .
Обнаружение опухоли in vivo с помощью активируемых флуоресцентных зондов на HER2-положительной модели метастазов в легкие.Флуоресцентный зонд, активируемый pH, излучает свет только в опухолях легких. Однако контрольный зонд «всегда включен» производит флуоресцентный сигнал как от опухолей, так и от нормального легкого и сердца, снижая соотношение опухоли к фону. Печатается с разрешения Ref. (155). Авторское право Американского химического общества, 2010 г.
Однако контрольный зонд «всегда включен» производит флуоресцентный сигнал как от опухолей, так и от нормального легкого и сердца, снижая соотношение опухоли к фону. Печатается с разрешения Ref. (155). Авторское право Американского химического общества, 2010 г.
У обоих методов есть свои преимущества и недостатки. При ферментативной активации один фермент-мишень может активировать множество различных флуоресцентных молекул, тем самым усиливая сигнал от ткани-мишени.Однако недостатком ферментативной активации является то, что активация происходит во внеклеточном пространстве, и фермент может диффундировать от мишени, внося вклад в фоновый сигнал. Кроме того, этому типу зонда не хватает специфичности, поскольку ни один из используемых в настоящее время ферментов для активации флуоресценции не является специфичным для канцерогенеза. Напротив, зонды, которые активируются эндолизосомным процессингом, являются высокоспецифичными для рака и обычно остаются локализованными на мишени, поскольку активация зависит от связывания зонда со специфическими рецепторами клеточной поверхности и их интернализации. Однако молекулярное связывание специфических активируемых флуоресцентных зондов требует биологического и катаболического процесса для достижения достаточной TBR. Нацеленные активируемые флуоресцентные зонды должны сначала вытекать из сосудистой сети, связывать клетки-мишени, а затем интернализоваться в клетке-мишени для активации зонда. Процесс активации часто требует дней, что снижает их практичность для повседневного клинического использования (214). Новые активируемые флуоресцентные зонды, нацеленные на дополнительные физиологические характеристики раковых клеток, такие как деградация мицелл, концентрация тиолов, поверхностные лектины и связывание антител, также в настоящее время находятся в разработке (159, 207, 211, 215–218).Использование этих активируемых флуоресцентных зондов в клинических исследованиях может значительно увеличить количество и качество инструментов интраоперационной визуализации, доступных во время удаления рака.
Однако молекулярное связывание специфических активируемых флуоресцентных зондов требует биологического и катаболического процесса для достижения достаточной TBR. Нацеленные активируемые флуоресцентные зонды должны сначала вытекать из сосудистой сети, связывать клетки-мишени, а затем интернализоваться в клетке-мишени для активации зонда. Процесс активации часто требует дней, что снижает их практичность для повседневного клинического использования (214). Новые активируемые флуоресцентные зонды, нацеленные на дополнительные физиологические характеристики раковых клеток, такие как деградация мицелл, концентрация тиолов, поверхностные лектины и связывание антител, также в настоящее время находятся в разработке (159, 207, 211, 215–218).Использование этих активируемых флуоресцентных зондов в клинических исследованиях может значительно увеличить количество и качество инструментов интраоперационной визуализации, доступных во время удаления рака.
Активируемые флуоресцентные зонды сильно различаются по механизму гашения флуоресценции. Наиболее известным механизмом гашения является резонансный перенос энергии Фёстера (флуоресценция) (FRET), при котором энергия от одного флуорофора передается другой молекуле, когда две молекулы находятся в непосредственной близости (<10 нм).Пара FRET может состоять из двух флуорофоров (самотушение) или флуорофора и молекулы тушителя (203, 219). Образование гомодимера (H или J-димера) является другим методом тушения. Например, известно, что производные ксантена образуют H-димеры при более высоких концентрациях (~ мМ), что вызывает сдвиги спектров поглощения, полностью гася флуоресценцию (195, 203). Фундаментальным для образования как FRET, так и H-димера является межфлуорофорный процессинг, который происходит, когда две молекулы находятся рядом друг с другом.
Другой механизм гашения, индуцированный фотонами перенос электрона (PeT), происходит, когда электрон передается от донора PeT к возбужденному флуорофору, уменьшая сигнал флуоресценции. Когда донор PeT отщепляется от флуорофора или инактивируется, происходит активация. В отличие от FRET и образования H-димера, PeT происходит внутри одной молекулы флуорофора и не требует присутствия второго флуорофора (203, 220). Механизм PeT имеет особенно высокое соотношение светоотдачи и закалки.
Еще один механизм расщепления гена заключается в удерживании двух флуорофоров в непосредственной близости друг от друга с использованием пептидного остова. В присутствии фермента каркас пептида расщепляется, высвобождая и активируя флуорофоры.
Первым активируемым флуоресцентным зондом, прошедшим клинические испытания, был LUM015. Активация LUM015 зависит от расщепления протеазой катепсина, фермента, обычно сверхэкспрессируемого опухолями (221). LUM015 оптически неактивен при нормальных условиях, но при протеолитическом расщеплении высвобождается ковалентно присоединенная молекула гасителя, и сигнал флуоресценции значительно усиливается (103).Впервые он был оценен Whitley et al. в когорте из 15 пациентов с раком груди или саркомой мягких тканей (103). Внутривенная инъекция этого активируемого протеазой флуоресцентного зонда для визуализации перед операцией хорошо переносилась, а визуализация резецированных тканей человека показала, что флуоресценция опухоли была значительно выше, чем флуоресценция нормальных тканей (103).
Недавно были протестированы несколько других механизмов. Блокированный активируемый, проникающий в клетки пептид, AVB-620, был протестирован в первом клиническом испытании на людях, в котором 27 пациентов с раком груди получили инфузию с последующим хирургическим удалением.Инфузия AVB-620 была безопасной и улучшила обнаружение рака во время операции (104). Другой новый подход — использование пептида, конъюгированного с ICG. В этом случае агент BLZ-100 использует хлортоксин (пептид из 36 аминокислот) в качестве целевого фрагмента и конъюгирует его с ICG. Этот агент использовался для визуализации глиомы (90).
Распыляемые активируемые флуоресцентные зонды
Во многих случаях процесс расхолаживания занимает от нескольких часов до нескольких дней, что затрудняет его интеграцию в хирургические рабочие процессы.Например, активируемые зонды, использующие катепсин D и MMP2 / 9 (222, 223), следует систематически вводить, по крайней мере, за день до операции, чтобы довести их до рака и полностью активировать из-за множественных участков расщепления. Однако кинетика некоторых других ферментативно-реактивных зондов намного быстрее, особенно когда они активируются однократным расщеплением. Следовательно, такие ферментативно активируемые флуоресцентные зонды могут быть настолько быстрыми, что их можно будет использовать по мере необходимости во время хирургической процедуры. Например, Urano et al. разработали активируемый флуоресцентный зонд, γ-глутамилгидроксиметилродамин зеленый (gGlu-HMRG).GGlu-HMRG полностью подавляется спироциклическим каркасом, но быстро активируется с помощью одностадийной ферментативной реакции в присутствии GGT, который часто присутствует на клеточных мембранах клеток рака шейки матки и яичников. В результате этот зонд активируется в течение 10 минут после распыления. В модели рака яичников человека на мышах Urano et al. опрыскали брюшную полость зондом gGlu-HMRG и продемонстрировали, что небольшие опухолевые узелки можно было визуализировать в течение 10 минут после введения и оставались помеченными в течение как минимум 1 часа (рисунок) (112).Mitsunaga et al. использовали gGlu-HMRG во время колоноскопии, чтобы дифференцировать долгосрочный колит от рака, ассоциированного с ранним колитом, на мышиной модели рака толстой кишки. Они смогли визуализировать рак и дисплазию через 5–30 минут после распыления gGlu-HMRG на поверхность толстой кишки. Более того, сигнал от рака / дисплазии был в 10 раз выше, чем фоновая флуоресценция, несмотря на наличие колита (127). Зонд gGlu-HMRG недавно был протестирован на свежих человеческих хирургических образцах колоректальной опухоли (224) и рака груди (225) для обнаружения границ опухоли и метастатических лимфатических узлов в качестве предшественника его, вводимого в клинические испытания.Точно так же эти зонды показали, что местное введение агента на аспирированные образцы от пациентов с опухолями поджелудочной железы приводит к опухолеспецифическому усилению (226).
Спектрально-флуоресцентные изображения четырех перитонеальных опухолей яичников с использованием gGlu-HMRG. In vivo Интенсивность флуоресценции распыляемого зонда. Через 10 и 60 минут после внутрибрюшинного введения gGlu-HMRG оценивали каждую из четырех моделей перитонеальных опухолей яичников: SHIN3, OVCAR4, OVCAR5 и OVCAR8.Желтые стрелки указывают местоположение опухоли. Шкала шкалы 1 см. Перепечатано из публикации (112) с разрешения AAAS.
Другие активируемые зонды, которые можно распылять, находятся в стадии разработки. Они активируются ферментами путем однократного расщепления, такими как катепсин (91, 129), бета-галактозидаза (227), эндоаминопептидазы (228) и НАДФН (229).
Различные типы недавно разработанных активируемых флуоресцентных зондов имеют тенденцию превосходить постоянно включенные зонды; однако их безопасность для пациентов еще предстоит определить.Учитывая относительно небольшой рынок, провести таких агентов через процесс утверждения заявки на новый лекарственный препарат будет непросто.
Сокращения
AAA, аневризма брюшной аорты; ALA, аминолевулиновая кислота; ADC, конъюгат антитело-лекарственное средство; APC, конъюгат антитело-фотоабсорбент; CA, углеводный антиген; АКШ, аортокоронарное шунтирование; СЕА, карциноэмбриональный антиген; КТ, компьютерная томография; рецептор эпидермального фактора роста; FDA, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов; ФГС — хирургия под контролем флуоресценции; FITC, флуоресцеинизотиоцианат; FLARE, резекция и исследование с использованием флуоресценции; FRET, резонансный перенос энергии Фёстера (флуоресценция); gGlu, γ-глутамил; GGT, γ-глутамилтрансфераза; H-димеры, гомодимеры; HLA, гексаминолевулинат; HMRG, гидроксиметилродамин зеленый; ICG, индоцианин зеленый; mAb, моноклональные антитела; МБ, метиленовый синий; ММП, матриксная металлопротеиназа; МРТ, магнитно-резонансная томография; NDA, New Drug Application, NIR, ближний инфракрасный диапазон; ПЭТ, позитронно-эмиссионная томография; PeT — перенос электрона, индуцированный фотонами; ПИТ, фотоиммунотерапия; Pp, протопорфирин; PSMA, простатоспецифический мембранный антиген; SLN, сторожевой лимфатический узел; TBR — отношение целевого значения к фоновому; VEGF, фактор роста эндотелия сосудов.
Носимая система флуоресцентного контроля REVEAL FGS
Designs for Vision представляет REVEAL TM FGS, первую НОСИТЕЛЬНУЮ систему для хирургии с флуоресцентным контролем, предоставляющую хирургам свободу движений и позиционирования во время процедур FGS.
Designs for Vision Новая система REVEAL TM FGS сочетает в себе синий возбуждающий свет и очки с фильтром излучения, обеспечивающие яркую флуоресцентную визуализацию.Система REVEAL TM FGS позволяет использовать различные увеличения. Эта портативная носимая система предлагает ту же визуализацию, что и другие подходы к флюоресцентной хирургии, с несколькими явными преимуществами, включая возможность изменять перспективу, просто изменяя линию обзора.
REVEAL TM Система FGS
Улучшенная визуализация за счет фильтрации излучения как в увеличении, так и в оптике очковых линз, откалиброванной в соответствии с REVEAL TM FGS Tribeam HDi TM Фара
TriBeam HDi TM Фара объединяет три светодиода HDi TM (High Definition Imaging), позволяя хирургу выбирать между двумя настройками возбуждения и белым светом
Беспроводная ножная педаль с синими зубьями позволяет хирургу легко управлять настройками освещения
Полная мобильность , позволяющая хирургам перемещаться и просматривать место операции под разными углами
Светопропускание Более 91% позволяет хирургам визуализировать более яркую флуоресценцию с большей детализацией
Увеличение Custom Fit для хирурга, никаких специальных оптических регулировок не требуется
ПАТЕНТЫ
ОЧКИ REVEAL TM FGS: 10 215 977 • 10 895 735
REVEAL TM FGS TriBeam ФАРЫ: США 11099376 B1
ХИРУРГИЧЕСКИЕ ИССЛЕДОВАНИЯ / РАЗРЕШЕНИЯ
Светодиод DayLite HDi TM LEDSC
Блоки питания / фонари:
IEC 60601 Третье издание, электрическое
Безопасность и 4-е место по безопасности EMC
МЭК 62133
МЭК 62366-1
ISO 14971
ОЧКИ REVEAL TM FGS:
EN207 (только зона обзора)
Эндоскопия — Фиброгастроскопия (ФГС)
Сделать фиброгастроскопию в Харькове
При подозрении на появление или обострение заболеваний верхних отделов пищеварительной системы проводится фиброгастроскопия (ФГС), диагностическая процедура, которая проводится с использованием может потребоваться эндоскоп.Во время исследования оптоволоконная трубка с линзой на конце и каналами для вспомогательных инструментов вставляется в полость аппарата. пищеварительный тракт. На мониторе эндоскопа врач, выполняющий ФГС, видит состояние слизистых оболочек пищевода и желудка, может провести визуальный осмотр. оценка тканей этих органов и, при необходимости, выполнение биопсии для гистологического исследования.
Точность результатов фиброгастроскопии в Харькове и самочувствие пациента во время процедуры во многом определяются качественными показателями используемого оборудования и квалификация специалиста, проводящего обследование.В OK Center процедуры фиброгастроскопии проводят врачи с многолетним опытом. опыт диагностики и лечения на самом современном оборудовании. Благодаря этому пациентам гарантируется возможность пройти обследование в комфортных условиях. окружающей среды и получить точные результаты.
Показания к фиброгастроскопии
Инструментальная диагностика ЖКТ назначается гастроэнтерологом для подтверждения (опровержения) предполагаемого диагноза и выбора наиболее эффективной лечебной тактики.Процедура ФГС назначается при появлении следующих симптомов:
- боль в верхней части живота, свидетельствующая о развитии эрозивных процессов слизистой оболочки желудка или прогрессировании воспалительного процесса
- изжога и частая отрыжка — состояния, часто связанные с возникновением язвенной болезни
- потеря аппетита или его полное отсутствие
- постоянная тошнота
- Расстройство глотания
- необоснованное похудание, которое может быть показателем развития злокачественного опухолевого процесса
Противопоказаниями к гастроскопии в Харькове являются гипертонический криз, нарушение свертываемости крови, инсульт или инфаркт, бронхиальная астма и ряд других патологических состояний. состояния, о течении которых следует сообщить лечащему врачу перед назначением процедуры.Это будет способствовать принятию разумного решение и поиск оптимальной тактики диагностики.
Техника фиброгастроскопии в ОК Центре
Процедуре предшествует подготовительный период, в течение которого пациенту рекомендуется пересмотреть диету за 2-3 дня до обследования (исключить трудноперевариваемые продукты из меню), полностью отказаться от еды за 6-8 часов до ФГС.
Подготовка к ФГС (фиброгастроскопия)
Непосредственно перед фиброгастроскопией полость рта пациента обрабатывается аэрозольным анестетиком для уменьшения рвотного рефлекса и устранения боли.Установлен мундштук между зубами, после чего эндоскоп осторожно вводят в полость рта и перемещают по пищеварительному тракту. Обследование проводится от 1,5 до 10 часов. минут, по истечении которых диагноз подтверждается и обсуждается тактика лечения.
Подробную информацию о фиброгастроскопии в Харькове и подготовке к процедуре можно узнать у специалистов OK Center во время записи к врачу. к гастроэнтерологу или позвонив по контактным телефонам на сайте.
Clinic OK Center — отличный выбор для проведения ФГС. В Харькове работает не один медцентр, но, тем не менее, местные жители выбирают OK Center как место, где квалифицированные специалисты предоставляют качественные услуги. В цена FGS указана на нашем сайте, как и все наши контакты.
Центр флюоресцентной хирургии | Калифорнийский университет в Сан-Диего Здоровье
Технология на основе флуоресценции — это спасательный инструмент для визуализации, который освещает опухоли и раковые клетки, а также нервы и другие анатомические особенности для более легкой идентификации и точного удаления или сохранения во время операций.Этот подход меняет то, как хирургическое вмешательство может быть более безопасным и точным для пациентов.
Калифорнийский университет в Сан-Диего Health предлагает высокоточную хирургическую технику в своем новом Центре хирургии под контролем флуоресценции под руководством Сантьяго Хорган, доктор медицины, директор центра и Майкл Буве, доктор медицины, содиректор.
Что такое флуоресцентная визуализация?
Флуоресцентная визуализация позволяет врачам лечить пациентов с опухолями и сложными заболеваниями всех типов с точностью, подобной GPS, выявляя раковые или злокачественные ткани по всему телу, потому что они буквально светятся.
Калифорнийский университет в Сан-Диего Health использует эту форму визуализации для оптимизации различных операций, от обычных процедур, таких как удаление желчного пузыря и операции по снижению веса, до самых сложных нейрохирургических процедур.
Непосредственно перед операцией под контролем флуоресценции (FGS) в кровоток пациента обычно вводят контрастные вещества или зонды для направленной визуализации. Затем раковые клетки освещаются специальными камерами и источниками света, используемыми хирургами, что позволяет им точно визуализировать и маркировать местоположение опухоли, анатомию, края или другие важные структуры в режиме реального времени для более точной операции и резекции.
Эта улучшенная визуализация может использоваться при открытых, лапароскопических и роботизированных операциях для выявления критических или важных структур и кровотока в тканях. И это помогает уменьшить повреждение нормальных структур, таких как нервы, кровеносные сосуды, мочеточники и желчные протоки.
Как мы связаны с флуоресцентной визуализацией?
Наш новый центр основан на работе и наследии Нобелевского лауреата Роджер Цзянь, доктор философии, Калифорнийский университет в Сан-Диего. Он помог произвести революцию в области хирургии, разработав серию светящихся пептидов, которые однажды осветят раковые клетки для облегчения идентификации и удаления во время операции.
Развитие работы доктора Цзяня в лаборатории до наших операционных в UC San Diego Health — это сочетание трансляционной и персонализированной медицины в лучшем виде.
Мы сотрудничаем в междисциплинарной атмосфере и обеспечиваем высочайший уровень знаний, предлагаемый единственной академической системой здравоохранения Сан-Диего.
FAQ: Гендерная хирургия лица | Центр здоровья трансгендеров Джонса Хопкинса
Что такое хирургия лица по половому признаку?
Гендерная хирургия лица (FGS) — это комбинация процедур, которые позволяют пациенту иметь лицо, более подтверждающее пол.
Какие процедуры включены в ФГО?
Мы предлагаем как хирургические, так и консервативные методы лечения. Типы процедур FGS, которые мы предлагаем, включают, но не ограничиваются:
Пример хирургических процедур феминизации лица.Как выбрать наиболее подходящую для меня операцию?
Хирургическое планирование зависит от ваших хирургических целей. Только вы можете выбрать, какие участки лица вы хотите исправить хирургическим путем. Вам не нужно выбирать одну операцию; Чаще всего для достижения ваших целей можно рассмотреть несколько процедур и вмешательств.Вы и ваш хирург можете обсудить свои цели и приоритеты при совместной разработке хирургического плана.
Все ли можно сделать за одну операцию?
Предпочтительный подход с точки зрения безопасности пациентов и ограничений страхования — поэтапный подход. Это позволяет нам расставлять приоритеты и адаптировать планы к исцелению и выздоровлению. Это самый безопасный подход, поэтому вы не находитесь под наркозом в течение небезопасного периода времени.
Как долго длится операция?
Хирургическая длина зависит от типа вашей процедуры.Чем сложнее процедура, тем дольше она длится.
Нужна ли мне предоперационная визуализация?
Да. Каждый случай FGS требует 3D-компьютерной томографии лица, чтобы мы могли оценить кости и создать 3D-модели для хирургического планирования. Перед операцией будет проведено сканирование мягких тканей, а также послеоперационная визуализация.
Эти трехмерные компьютерные томографии следует делать либо в амбулаторном центре Джонса Хопкинса, либо в отделении Johns Hopkins Green Spring.
Придется ли мне оставаться в больнице?
Большинство операций включают в себя 23-часовое наблюдение, чтобы убедиться, что все хорошо заживает после операции.
Когда мне нужно будет следить?
Последующие действия зависят от процедуры (процедур). Большинство первичных посещений после операции происходит в течение 5 дней после операции и назначается до выписки из больницы.
Будет ли у меня сильная боль после операции?
Вы можете испытывать некоторый дискомфорт в течение нескольких дней после операции, но обычно через 4-5 дней после операции ваша боль начнет уменьшаться, и вы сможете вернуться к некоторым нормальным занятиям с ограничениями.
Могу ли я принять душ после операции?
В первые несколько дней после операции вам следует избегать душа и обмывать остальную часть тела губкой. После первого приема в послеоперационный период вы сможете принять душ. При купании важно использовать мыло без запаха и никогда не опрыскивать место операции водой.
Какой послеоперационный уход требуется после бритья трахеи?
У вас будет разрез на шее, который зашивают нерастворимыми швами.Эти швы будут сняты примерно через 10 дней после операции. Разрез и швы должны быть закрыты куском марли и прозрачной ленты, например, тегадерм. Не снимайте эту повязку до первого посещения клиники.
Могу ли я побрить шею после бритья трахеи?
Не брейте место операции в течение как минимум 4 недель, чтобы кожа и разрез зажили. Особенно важно не сбривать швы, так как бритва может выдернуть швы слишком рано, и рана откроется.
Какой послеоперационный уход требуется после контурной пластики челюсти?
Эта операция требует выполнения разреза во рту, который закрывается рассасывающимися швами. В течение нескольких недель после операции вам придется чистить внутреннюю часть рта специальным средством для полоскания рта.
Вам также придется носить специальную компрессионную повязку на челюсти в течение нескольких недель после операции. Эта повязка будет предоставлена вам во время операции.
Могу ли я говорить после контурной пластики челюсти?
Да.После контурной пластики челюсти следует поговорить, но рекомендуется не переусердствовать. Разговоры приветствуются, но только в том случае, если они терпимы.
Есть ли специальная диета после контурной пластики челюсти?
После операции в течение 3-4 дней следует есть мягкую пищу, так как во рту будет болезненно ощущаться боль и твердую пищу будет трудно есть. Если вам кажется, что вы едите недостаточно, вы можете дополнить свой рацион пищевыми коктейлями, например Ensure. Как только вы почувствуете себя готовым, можно начинать вводить более твердую пищу.Вам следует избегать горячих напитков, таких как чай или кофе, в течение 1-2 недель, пока разрез заживает.
Что произойдет, если я кашляю / чихаю после контурной пластики челюсти?
Не паникуйте. Кашель или чихание после коррекции контура челюсти являются нормальным явлением, и это не повлияет на место операции.
Какой послеоперационный уход требуется после реконструкции лба?
Для этой процедуры требуется разрез, проходящий через голову от уха до уха. В конце процедуры разрез зашивается скобами.Эти скобы будут удалены примерно через 2 недели после операции.
Есть ли у меня хирургические дренажи после реконструкции лба?
Если вам предстоит реконструкция лба, у вас будет дренаж, который останется на месте во время вашего пребывания в больнице. Этот слив будет удален перед вашей выпиской.
Могу ли я сделать подтяжку бровей одновременно с реконструкцией лба?
Да. Во время реконструкции лба мы можем сделать небольшую подтяжку бровей, чтобы переместить брови в более удобное место.
Какой послеоперационный уход требуется после ринопластики?
После ринопластики вы вернетесь домой с внутренней и внешней шиной носа и наложите несколько швов на нижнюю часть носа. Все эти повязки остаются на месте примерно в течение 1 недели после операции.
Будет ли у меня опухоль и подбитые глаза после ринопластики?
Появление синяков и отеков под глазами после ринопластики — это нормально. Через 4-6 недель и опухоль, и синяки станут менее заметными.
Что будет, если я чихну после ринопластики?
Если вам нужно чихнуть после ринопластики, важно чихать с открытым ртом. Если вы чихнули с закрытым ртом, не паникуйте. Убедитесь, что носовые шины остались на месте и не расшатались.
Что такое жировая трансплантация?
Пересадка жира включает взятие жира в одном месте вашего тела, обычно в желудке, и нанесение его на лицо, чтобы заполнить области, которые могут быть впалыми или вдавленными.
Жировая трансплантация — это то же самое, что липосакция?
Несмотря на то, что трансплантация жира происходит по тому же процессу, что и липосакция, мы берем достаточно жира только для заполнения необходимых областей на вашем лице — обычно этого недостаточно, чтобы заметить большие изменения в вашем теле.
Где я могу получить инъекции и наполнители?
Есть множество областей, в которых мы можем использовать инъекции для достижения благоприятных результатов. Эти достопримечательности включают, среди прочего, мышцы челюсти, вокруг глаз, наполнители для губ.Имейте в виду, что страховые компании обычно не покрывают эти услуги, и их цена варьируется от 1500 до 3500 долларов, в зависимости от местоположения; но эти уколы очень легко сделать в клинике. Продолжительность их действия зависит от каждого пациента и продукта, который мы используем, но обычно от 6 до 12 месяцев или даже дольше.
Загрузите ответы на часто задаваемые вопросы о половой хирургии лица в формате PDF.
Лицевая половая хирургия: обзор процесса пациента
Запланировать прием …
Позвоните 844-546-5645.
Чтобы назначить консультацию …
Нам потребуется:
- Компьютерная томография завершена
- 1 письмо с оценкой психического здоровья предпочтительнее, чтобы показать медицинскую необходимость в вашей страховой компании
Чтобы назначить операцию …
Нам потребуется:
- Предварительное разрешение на страхование
Послеоперационный уход …
Будет назначено на дату завершения операции. Если у вас есть какие-либо вопросы, свяжитесь с нашей командой через MyChart.
Лечение женского генитального шистосомоза (FGS) празиквантелом: экспериментальное исследование — полный текст
Женский генитальный шистосомоз (FGS) — частое проявление инфекции Schistosoma haematobium или mansoni. Он встречается у женщин всех возрастных групп, включая молодых девушек, и связан с серьезными, часто изнурительными и стигматизирующими заболеваниями. Это может перерасти в опасное для жизни состояние. ФГС, вероятно, является самым запущенным гинекологическим заболеванием в тропиках.
В зависимости от места выброса яиц клиническая патология развивается в вульве и влагалище, шейке матки, матке, фаллопиевых трубах и яичниках. Могут быть поражены все половые органы одновременно. Женщины с ФГС сообщают о спонтанном или посткоитальном кровотечении, выделениях из влагалища, боли во время полового акта, боли в области таза, нерегулярных менструациях и бесплодии. Выделения из влагалища и зуд, боль во время полового акта, спонтанное + посткоитальное кровотечение, а также нарушения менструального цикла женщины приписывают ИППП.Это приводит к стыду, психологическому перенапряжению и страданиям, в конечном итоге вызывает стигматизацию и социальную изоляцию, что приводит к ухудшению качества жизни.
Клинические, гистопатологические, иммунологические и эпидемиологические данные свидетельствуют о наличии причинно-следственной связи между ФГС и ВИЧ-инфекцией. Есть намеки на причинно-следственную связь между ФГС и ВПЧ. Связь ФГС с инфекцией ВИЧ / ВПЧ подчеркивает решающее значение для эффективного лечения ФГС.
Клиническая патология является результатом сложной воспалительной реакции на антигены, выделяемые взрослыми червями и жизнеспособными яйцами.Воспаление генитальной ткани сохраняется до тех пор, пока в кровообращении присутствуют взрослые черви, а новые яйца высвобождаются и застревают. Следовательно, поражения могут зажить только в том случае, если воспаление уменьшится и восстановится нормальный иммунный ответ. Это означает, что необходимо уничтожить всех гельминтов и предотвратить повторное заражение в течение некоторого времени, чтобы обеспечить полное заживление половых органов.
Исходя из этого, пять доз празиквантела будут введены в течение 10 недель, чтобы гарантировать уничтожение всех существующих гельминтов.Первые три дозы направлены на то, чтобы убить всех взрослых червей. Четвертая доза убьет шистосомулу, которая созреет в следующие недели. Последняя доза предотвратит повторное заражение женщины.
Будет проведено рандомизированное контролируемое исследование для сравнения эффективности стандартного лечения и повторных доз празиквантела. Поскольку плацебо недоступно, исследование не будет слепым. Конечным результатом является исчезновение / регресс клинической патологии шейки матки, влагалища / вульвы.
Результат этого исследования имеет важное значение для сексуального здоровья миллионов женщин в странах Африки к югу от Сахары.
Целью исследования является сравнение стандартного лечения шистосомоза, рекомендованного ВОЗ (разовая доза празиквантела 40 мг / кг), с лечением, основанным на новом обосновании: пять доз празиквантела 40 мг / кг
- 1 x 40 мг / кг после включения в исследование (D1, H0) плюс две однократные дозы (40 мг / кг) через 12 и 24 часа после первого лечения
- 1 x 40 мг / кг через пять недель после первой обработки PZQ
- 1 x 40 мг / кг через десять недель после первой обработки PZQ
Тенденции и проблемы для клинического внедрения хирургии под контролем флуоресценции
См. Соответствующую статью на стр. 758.
Оптическая визуализация без посторонней помощи глаза, наряду с пальпацией, является основным руководством для хирургических онкологов. Вместе с субъективными суждениями хирурга эти сенсорные сигналы будут по-прежнему служить основой для процедур резекции опухоли. Тем не менее, очевидно, что существует потребность во вспомогательных технологиях для обеспечения большей точности резекции за счет большей чувствительности обнаружения опухоли, более высокого пространственного разрешения или увеличения количественного определения и воспроизводимости. Современные рентгенографические подходы, такие как КТ и МРТ, в настоящее время обычно используются для проведения процедур, требующих высокой точности, таких как нейрохирургическая резекция, либо с помощью предоперационной визуализации в сочетании с методами навигации в реальном времени, либо с помощью интраоперационной визуализации (1).Однако применимость этих методов ограничена из-за высокой стоимости и сложности таких рентгенографических подходов, а также их ограниченного разрешения и чувствительности, особенно для принятия оперативных решений на хирургических границах, где опухолевая нагрузка низкая или пространственно распространенная. Здесь ценность оптического изображения самая высокая, поскольку, хотя способность света проникать глубоко внутрь тканей мала, прекрасная чувствительность и пространственное разрешение, которые могут быть достигнуты на поверхностных глубинах (например.g., около краев окончательной резекции) имеет большое значение в хирургическом арсенале.
Недавнее раннее клиническое технико-экономическое обоснование, проведенное van Keulen et al. в этом выпуске журнала The Journal of Nuclear Medicine (2) приводятся конкретные примеры того, как хирургия под контролем флуоресценции (FGS) может повлиять на принятие хирургических решений. Первый и наиболее очевидный пример — это визуализация остаточной опухоли в основании («глубокий край») резекционной полости после того, как хирург определил, что резекция завершена, на основе обычных средств (т.е.е., визуальная и тактильная обратная связь). Другой пример — выявление непредвиденного вторичного поражения, которое не обнаруживается при стандартном визуальном осмотре.
Смешивающий фактор, упомянутый van Keulen et al. (2) — это органоспецифическое определение приемлемого края доброкачественной ткани, который должен существовать между иссеченной опухолью и поверхностью хирургического края (то есть «отмеченный краем»). Здесь следует признать, что современные критерии границ были частично разработаны, чтобы компенсировать ограничения традиционной послеоперационной гистологии, при которой небольшое количество срезов тонких тканей визуализируется в вертикальном (по глубине) направлении, часто с интервалами в несколько миллиметров. (я.э., батон). Следовательно, возможность комплексного изображения всей поверхности хирургического края с помощью FGS должна стимулировать новые индивидуальные критерии полноты хирургического вмешательства. Такие критерии неизменно будут оптимизироваться и адаптироваться с течением времени, чтобы отразить наше развивающееся понимание лежащей в основе биологии и пространственных характеристик конкретного заболевания, а также по мере того, как клинические исследования показывают преимущества результатов (3). Центральное место в этом анализе занимает также понимание целевого поведения конкретного используемого флуоресцентного контрастного вещества.
Точно так же, как критерии хирургической границы нельзя обобщить для разрозненных заболеваний, для решения конкретных клинических задач был разработан широкий спектр технологий FGS. Как описано у van Keulen et al. (2), флуоресцентная хирургическая микроскопия с низким разрешением является наиболее популярным методом FGS, в котором сейчас доступны многочисленные платформы для визуализации (4). Эти системы обеспечивают преимущество широкого обзора, часто всего операционного поля, но ограничены с точки зрения чувствительности обнаружения и субъективного характера считывания изображений (5).Портативные устройства для спектроскопии и зонды для визуализации с высоким разрешением жертвуют полем обзора, но обеспечивают большую чувствительность обнаружения и количественное определение контрастных веществ, специфичных для опухоли, в локализованных областях ткани (5). В случае микроскопов in vivo с высоким разрешением, детали микроархитектуры, приближающиеся к золотому стандарту гистопатологии, могут быть визуализированы в реальном времени как с помощью экзогенных агентов, так и без них (5). В конечном итоге комбинация методов обнаружения с низким разрешением (широкая область) и локализованного высокого разрешения может иметь значение для многих процедур резекции.Например, объемная опухоль и некритические области могут быть резецированы более агрессивно при обширной FGS, тогда как области, которые жизненно важны для косметических или функциональных целей, могут быть резецированы с большей точностью с использованием методов локального зондирования. Наконец, существует важная роль технологий визуализации ex vivo «замкнутого поля» для FGS, которые, в отличие от вышеупомянутых подходов к визуализации in vivo, позволяют лучше контролировать оптические параметры, такие как интенсивность и геометрию освещения, а также уменьшать помехи от окружающей среды. светлый фон, что в конечном итоге позволяет более точно и количественно визуализировать морфологию тканей и контраст флуоресценции.К недостаткам можно отнести увеличение времени процедуры и возможное ухудшение контраста изображения и качества ткани после удаления пациента. В недавнем исследовании той же группы под руководством доктора Эбена Розенталя была сделана попытка сравнить несколько платформ FGS in vivo и ex vivo (6).
По мере того, как подходы FGS достигают различных уровней зрелости, улучшения в обработке изображений и аналитике, вероятно, будут играть огромную роль в их успехе и влиянии. Первоначальные усилия были сосредоточены на повышении надежности регистрации сигнала при наличии мешающих факторов, таких как загрязнение окружающего света, а также вводящих в заблуждение источников контраста изображения, таких как изменения оптических свойств ткани, вариации сигнала из-за геометрии ткани (т.е. рабочее расстояние и угол падения), а также неспецифическое накопление контрастных веществ из-за пассивных механизмов. Методы смягчения этих проблем включают творческие комбинации аппаратного обеспечения и методов обработки изображений, такие как мультиспектральное обнаружение (7) и ратиометрические методы «парного агента», в которых неспецифический контрольный агент одновременно отображается с целевым агентом для обеспечения средств для нормализации для вводящих в заблуждение источников контраста, перечисленных выше (8). Необходимы дальнейшие усилия в области вычислительного анализа и машинного обучения, чтобы помочь в клинической интерпретации данных FGS.Например, van Keulen et al. (2) наблюдают различия как в средней интенсивности флуоресценции, так и в пространственной неоднородности изображений FGS, полученных для доброкачественных и злокачественных типов тканей. Автоматизированные алгоритмы сегментации и классификации, идеально обученные и проверенные с помощью исследований, основанных на результатах, могут помочь в решении тонких задач распознавания образов, но столкнутся с проблемами, аналогичными другим, стремящимся внедрить искусственный интеллект в здравоохранение (9).
Клиническая валидация и принятие — окончательные критерии успеха FGS и других инновационных подходов в медицине.Первые успехи должны проложить путь к ускоренному внедрению последующих технологий. В качестве эталонного примера Stummer et al. Опубликовали клиническое исследование фазы 3 по использованию 5-ALA для FGS глиом высокой степени злокачественности. в 2006 г. (10) и привело к его одобрению регулирующими органами в Европейском Союзе в 2007 г. Однако последующее одобрение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов в США произошло только через десять лет, в 2017 г. Хотя разрешение регулирующих органов представляет собой реальную и сложную проблему, Адекватное возмещение затрат на методы FGS является равной, если не большей, проблемой для широкого клинического применения всеми, кроме наиболее академически мотивированных учреждений.Здесь перед переводчиками и коммерческими организациями стоит задача разработать реалистичные финансовые модели, чтобы продемонстрировать плательщикам убедительное ценностное предложение. Такие модели должны выходить за рамки непосредственной финансовой выгоды от сокращения количества повторных операций для пациентов с положительной маржой (например, лампэктомия при раке груди) и включать долгосрочный анализ результатов лечения пациентов, таких как прогрессирование до прогрессирования метастатического заболевания, что приводит к экспоненциальному увеличению в стоимости лечения, а также в финансовых последствиях побочных эффектов, вызванных чрезмерным лечением (например,ж., неврологическая заболеваемость при резекции опухоли головного мозга). В статье van Keulen et al. (2) относится к концепции клинически значимых изменений, вызванных ФГС. В конечном итоге стратегии возмещения затрат потребуют тщательного и точного определения этих клинически значимых изменений, а также сопутствующих преимуществ и рисков для пациента, если смотреть через призму экономики ухода.
РАСКРЫТИЕ ИНФОРМАЦИИ
Доктор Джонатан Лю является соучредителем и акционером LightSpeed Microscopy Inc., который лицензировал интеллектуальную собственность, созданную лабораторией доктора Лю в Вашингтонском университете. О другом потенциальном конфликте интересов, имеющем отношение к этой статье, не сообщалось.
- © 2019 Общество ядерной медицины и молекулярной визуализации.
- Принята к публикации 4 марта 2019 г.
- Принята к публикации 7 марта 2019 г.

 Как и при ФГДС, пациент глотает прибор с камерой, которая передает врачу изображения внутренних стенок ЖКТ (точнее, записывает их на носитель). Однако такая капсула проглатывается полностью и путешествует по кишечнику долгое время, пока не выведется из организма естественным путем. Преимущество данного метода заключается в том, что он позволяет получить полную картину состояния ЖКТ.
Как и при ФГДС, пациент глотает прибор с камерой, которая передает врачу изображения внутренних стенок ЖКТ (точнее, записывает их на носитель). Однако такая капсула проглатывается полностью и путешествует по кишечнику долгое время, пока не выведется из организма естественным путем. Преимущество данного метода заключается в том, что он позволяет получить полную картину состояния ЖКТ.

.jpg)