Карбонат кальция — Википедия
Карбона́т ка́льция (углеки́слый кальций) — неорганическое химическое соединение, соль угольной кислоты и кальция. Химическая формула CaCO3{\displaystyle {\mathsf {CaCO_{3}}}}.
В природе встречается в виде многочисленных минералов, например, кальцита, арагонита и ватерита, является главной составной частью известняка, мрамора, мела, входит в состав скорлупы яиц птиц.
Нерастворим в воде и этаноле.
Зарегистрирован как белый пищевой краситель (E170).
Используется как белый пищевой краситель Е170. Являясь основой мела, используется для письма на досках. Используется в быту для побелки потолков, покраски стволов деревьев, для подщелачивания почвы в садоводстве.
Массовое производство/использование[править | править код]
 Таблетки из карбоната кальция
Таблетки из карбоната кальцияПри производстве бумаги карбонат кальция применяют одновременно в качестве отбеливателя, наполнителя, а также раскислителя.
Используется при производстве силикатного стекла, — материала для производства оконного стекла, стеклянных бутылок, стекловолокна.
Применяется при производстве предметов гигиены (например, зубной пасты), в медицине.
В пищевой промышленности часто используется в качестве препарата препятствующего слеживанию и для препятствования слипания в комки сухих молочных продуктах.
При употреблении сверх рекомендованной дозы (1,5 г в день) может вызывать молочно-щелочной синдром (синдром Бернетта). Рекомендован при болезнях костных тканей[источник не указан 439 дней].
Производители пластмассы — одни из основных потребителей чистого карбоната кальция (более 50% всего потребления). Используемый в качестве наполнителя и красителя, карбонат кальция необходим при производстве поливинилхлорида (PVC), полиэфирных волокон (кримплен, лавсан, и т. п.), полиолефинов. Изделия из данных видов пластмасс распространены повсеместно — это трубы, сантехника, кафельная плитка, черепица, линолеум, ковровые покрытия, и т.п. Карбонат кальция составляет порядка 20% красящего пигмента, используемого при производстве красок
В строительстве[править | править код]
Строительство — ещё один из основных потребителей карбоната кальция. Например, в качестве наполнителя шпаклёвок и герметиков.
Также карбонат кальция является важным составным элементом при производстве продукции бытовой химии — средств для чистки сантехники, кремов для обуви.
Карбонат кальция широко применяется для раскисления кислых почв.
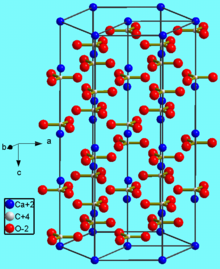
Карбонат кальция находится в минералах в виде полиморфов:
Тригональная кристаллическая структура кальцита является наиболее распространенной.
Минералы карбоната кальция находятся в следующих горных породах:
Залежи карбоната кальция в виде меловых пластов — отложений известковых раковин моллюсков, в основном, мелового периода является распространенным минералом на всех континентах.
В природе встречаются три кристаллические модификации (минералы с одинаковым химическим составом, но с различной кристаллической структурой): кальцит, арагонит и фатерит (ватерит).
Некоторые горные породы (известняк, мел, мрамор, травертин и другие известковые туфы) практически полностью состоят из карбоната кальция с различными примесями.
Кальцит является устойчивой кристаллической модификацией карбоната кальция и встречается в самых разнообразных геологических условиях: в осадочных, метаморфических и магматических горных породах.
Около 10 % всех осадочных пород составляют известняки, сложенные преимущественно кальцитовыми остатками раковин морских организмов. Арагонит является второй по распространённости кристаллической модификацией CaCO3 и в основном формируется в раковинах моллюсков и скелетах некоторых других организмов[каких?].
Также арагонит может образовываться и в неорганических процессах, например в карстовых пещерах или гидротермальных источниках.
Фатерит является наименее стабильной разновидностью этого карбоната, и очень быстро превращается в воде либо в кальцит, либо в арагонит. В природе встречается относительно редко, когда его кристаллическая структура стабилизирована теми или иными примесями.
Подавляющее количество карбоната кальция, добывающееся из полезных ископаемых, используется в промышленности. Чистый карбонат кальция (например, для производства продуктов питания или использования в фармацевтических целях), может быть изготовлен из природного минерала с малым количеством вредных примесей, например, из мрамора.
В лаборатории карбонат кальция может быть приготовлен предварительным гашением оксида кальция — негашеной извести. При этом образуется гидроксид кальция, и затем в суспензию продувается углекислый газ для получения карбоната кальция
- CaO+h3O⟶Ca(OH)2,{\displaystyle {\mathsf {CaO+H_{2}O\longrightarrow Ca(OH)_{2}}},}
- Ca(OH)2+CO2⟶CaCO3+h3O.{\displaystyle {\mathsf {Ca(OH)_{2}+CO_{2}\longrightarrow CaCO_{3}+H_{2}O}}.}
При нагревании до 900—1000 °C разлагается на кислотный оксид — углекислый газ CO2 и основный оксид — негашёную известь CaO:
- CaCO3⟶CaO+CO2↑.{\displaystyle {\mathsf {CaCO_{3}\longrightarrow CaO+CO_{2}\uparrow }}.}
Растворяется в воде при избытке углекислого газа образуя кислую соль — гидрокарбонат кальция Ca(HCO3
- CaCO3+CO2+h3O⟶Ca(HCO3)2.{\displaystyle {\mathsf {CaCO_{3}+CO_{2}+H_{2}O\longrightarrow Ca(HCO_{3})_{2}}}.}.
Из-за этой реакции образуются сталактиты, сталагмиты. Природные подземные воды, обильные углекислом газом, растворяют плохо растворимый карбонат кальция с образованием много лучше растворимого в воде гидрокарбоната кальция, при выделении подземной воды в виде капель с потолков пещер при попадании в воздух с низкой концентрацией углекислого газа происходит обратная реакция превращения гидрокарбоната кальция в плохо растворимый осадок карбоната кальция, образующего красивые природные формы в пещерах, и из-за этого же механизма образуются карстовые пещеры.
При обжиге с температурой свыше 1500 °C с углеродом, например, в форме кокса, образует карбид кальция и угарный газ:
- CaCO3+4C⟶CaC2+3CO↑{\displaystyle {\mathsf {CaCO_{3}+4C\longrightarrow CaC_{2}+3CO\uparrow }}}.
Карбонат кальцію — Вікіпедія
Матеріал з Вікіпедії — вільної енциклопедії.

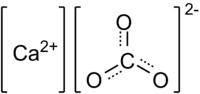
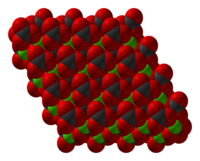
Карбона́т ка́льцію — найважливіша і найпоширеніша сполука кальцію. Хімічна формула СаСО3. В природі він зустрічається у вигляді кількох різновидів: вапняк, крейда, мармур, кальцит, арагоніт. У харчовій промисловості зареєстрований як харчова добавка Е170, та використовується як поверхневий барвник.
Усі різновидності карбонату кальцію, крім гідрокарбонату Са(НСО3)2, нерозчинні у воді. Однак гідрокарбонат кальцію є речовиною нестійкою. При тривалому перебуванні на повітрі, а також при кип’ятінні його розчину Са(НСО3)2 розкладається з виділенням вуглекислого газу, утворенням води і середньої солі:
- Са(НСО3)2 = СаСО3 + Н2О + СО2
У природних умовах гідрокарбонат кальцію утворюється при взаємодії розчиненого в природній воді вуглекислого газу з вапняками:
- СаСО3 + Н2О + СО2 = Са(НСО3)2
Завдяки цій реакції і розчинності гідрокарбонату у воді відбувається постійне переміщення карбонатів у природі. Просочуючись крізь ґрунт і шари вапняку, природні води, які завжди містять у собі розчинний вуглекислий газ, розчиняють карбонати кальцію і виносять його у вигляді гідрокарбонату в річки й моря. Там СаСО3 іде на побудову скелету живих морських організмів, а після їх відмирання нагромаджується на дні морів. Разом з тим у теплих місцях гідрокарбонат розкладається і у вигляді середньої солі осідає на дні моря.
Кислотами карбонат і гідрокарбонат кальцію легко розкладається, наприклад:
- СаСО3 + 2HCl = CaCl2 + Н2О + СО2
- Са(НСО3)2 + 2HCl = CaCl2 + 2Н2О + 2СО2
При нагріванні карбонат кальцію, не плавлячись, розкладається з утворенням оксиду кальцію і діоксиду вуглецю:
- СаСО3 = СаО + СО2
- Деркач Ф. А. Хімія. — Львів : Львівський університет, 1968. — 312 с.
Карбонат Кальция: формула, цена, что это такое, инструкция по применению
Закрыть- Болезни
- Инфекционные и паразитарные болезни
- Новообразования
- Болезни крови и кроветворных органов
- Болезни эндокринной системы
- Психические расстройства
- Болезни нервной системы
- Болезни глаза
- Болезни уха
- Болезни системы кровообращения
- Болезни органов дыхания
- Болезни органов пищеварения
- Болезни кожи
- Болезни костно-мышечной системы
- Болезни мочеполовой системы
- Беременность и роды
- Болезни плода и новорожденного
- Врожденные аномалии (пороки развития)
- Травмы и отравления
- Симптомы
- Системы кровообращения и дыхания
- Система пищеварения и брюшная полость
- Кожа и подкожная клетчатка
- Нервная и костно-мышечная системы
- Мочевая система
- Восприятие и поведение
- Речь и голос
- Общие симптомы и признаки
- Отклонения от нормы
- Диеты
- Снижение веса
- Лечебные
- Быстрые
- Для красоты и здоровья
- Разгрузочные дни
- От профессионалов
- Монодиеты
- Звездные
- На кашах
- Овощные
- Детокс-диеты
- Фруктовые
- Модные
- Для мужчин
- Набор веса
- Вегетарианство
- Национальные
- Лекарства
- Антибиотики
- Антисептики
- Биологически активные добавки
- Витамины
- Гинекологические
- Гормональные
- Дерматологические
- Диабетические
- Для глаз
- Для крови
- Для нервной системы
- Для печени
- Для повышения потенции
- Для полости рта
- Для похудения
- Для суставов
- Для ушей
- Желудочно-кишечные
- Кардиологические
- Контрацептивы
- Мочегонные
- Обезболивающие
- От аллергии
- От кашля
- От насморка
- Повышение иммунитета
- Противовирусные
- Противогрибковые
- Противомикробные
- Противоопухолевые
- Противопаразитарные
- Противопростудные
- Сердечно-сосудистые
- Урологические
- Другие лекарства
- Врачи
- Клиники
- Справочник
- Аллергология
- Анализы и диагностика
- Беременность
- Витамины
- Вредные привычки
- Геронтология (Старение)
- Дерматология
- Дети
- Женское здоровье
- Инфекция
- Контрацепция
- Косметология
- Народная медицина
- Обзоры заболеваний
- Обзоры лекарств
- Ортопедия и травматология
- Питание
- Пластическая хирургия
- Процедуры и операции
- Психология
- Роды и послеродовый период
- Сексология
- Стоматология
- Травы и продукты
- Трихология
- Другие статьи
- Словарь терминов
- [А] Абазия .. Ацидоз
- [Б] Базофилы .. Булимия
- [В] Вазектомия .. Выкидыш
- [Г] Галлюциногены .. Грязи лечебные
- [Д] Дарсонвализация .. Дофамин
- [Е] Еюноскопия
- [Ж] Железы .. Жиры
- [З] Заместительная гормональная терапия
- [И] Игольный тест .. Искусственная кома
- [К] Каверна .. Кумарин
- [Л] Лапароскоп .. Люмбальная пункция
- [М] Магнитотерапия .. Мутация
- [Н] Наркоз .. Нистагм
- [О] Общий анализ крови .. Отек
- [П] Паллиативная помощь .. Пульс
- [Р] Реабилитация .. Родинка (невус)
- [С] Секретин .. Сыворотка крови
- [Т]
Карбонат кальция — это… Что такое Карбонат кальция?
Карбонат кальция (углекислый кальций) — неорганическое химическое соединение, соль угольной кислоты и кальция. Химическая формула — . В природе встречается в виде минералов — кальцита, арагонита и ватерита, является главной составной частью известняка, мрамора. Нерастворим в воде и этаноле.
Зарегистрирован как белый пищевой краситель (E170).
Применение
Используется как белый пищевой краситель Е170. Являясь основой мела, используется для письма на досках. Используется в быту для побелки потолков, покраски стволов деревьев, для подщелачивания почвы в садоводстве.
Массовое производство/использование
 Таблетки из карбоната кальция
Таблетки из карбоната кальцияОчищенный от посторонних примесей, карбонат кальция широко используется в бумажной и пищевой промышленности, при производстве пластмасс, красок, резины, продукции бытовой химии, в строительстве. Производители бумаги используют карбонат кальция одновременно в качестве отбеливателя, наполнителя (заменяя им дорогостоящие волокна и красители), а также раскислителя. Производители стеклянной посуды, бутылок, стекловолокна используют карбонат кальция в огромных количествах в качестве источника кальция — одного из основных элементов, необходимых для производства стекла. Широко используется при производстве продукции личной гигиены (например, зубной пасты), и в медицинской промышленности. В пищевой промышленности часто используется в качестве антислеживающего агента и разделителя в сухих молочных продуктах. При употреблении сверх рекомендованной дозы (1,5 г в день) может вызывать молочно-щелочной синдром (синдром Бернетта). Рекомендован при болезнях костных тканей.
Производители пластмассы — одни из основных потребителей карбоната кальция (более 50 % всего потребления). Используемый в качестве наполнителя и красителя, карбонат кальция необходим при производстве поливинилхлорида (PVC), полиэфирных волокон (кримплен, лавсан, и т. п.), полиолефинов. Изделия из данных видов пластмасс распространены повсеместно — это трубы, сантехника, кафельная плитка, черепица, линолеум, ковровые покрытия, и т. п. Карбонат кальция составляет порядка 20 % красящего пигмента, используемого при производстве красок.
Строительство
Строительство — еще один из основных потребителей карбоната кальция. Шпатлевки, различные герметики — все они содержат карбонат кальция в значительных количествах. Также, карбонат кальция является важнейшим составным элементом при производстве продукции бытовой химии — средств для чистки сантехники, кремов для обуви.
Карбонат кальция также широко используется в очистительных системах, как средство борьбы с загрязнением окружающей среды, при помощи карбоната кальция восстанавливают кислотно-щелочной баланс почвы.
Нахождение в природе
Карбонат кальция находится в минералах в виде полиморфов:
Тригональная кристаллическая структура кальцита является наиболее распространенной.
Минералы карбоната кальция находятся в следующих горных породах:
Геология
Карбонат часто встречается в геологической среде. Он находится как полиморф. Полиморфами являются минералы с той же химической формулой, но разной химической структуры. Арагонит, кальцит, известняк, мел, мрамор, травертин, туф и др. — все они имеют формулу CaCO3, но каждый из них имеет несколько иной химический состав. Кальцит, как карбонат кальция, геологи обычно находят в морских условиях. Также кальцит, как правило, находится около теплых тропических условий. Это связано с его химией и свойствами. Кальцит может выпадать чаще как осадок в теплой среде, чем в холодной, поскольку теплая среда не дает улетучиваться в больших объемах CO2. Это аналогично тому как CO2 растворяется в воде. Когда вы открываете крышку пластиковой бутылки происходит выделение CO2. Из-за того что сода нагревается, выделяется углекислый газ. Этот же принцип может быть применен к кальциту и в океане. Карбонаты данного вещества в холодной воде существуют в более высоких широтах, но имеют очень медленный темп роста.
В тропических условиях вода теплая и чистая. Таким образом, вы можете увидеть много кораллов в данной среде по сравнению с холодной, где вода холодная. Производители карбоната кальция, такие как кораллы, водоросли и микроорганизмы, которые обычно встречаются в мелководных водоемах, как фильтраторы, требуют солнечный свет для производства карбоната кальция.
Изготовление
Подавляющее большинство карбоната кальция, добывающееся из полезных ископаемых, используется в промышленности. Чистый карбонат кальция (например, для производства продуктов питания или использования в фармацевтических целях), может быть изготовлен из чистого источника (как правило, мрамор).
В качестве альтернативы карбонат кальция может быть приготовлен кальцинацией оксида кальция. Вода добавляется к этому оксиду, давая гидроксид кальция, и затем проводится углекислый газ, который проходит через этот раствор для осаждения желаемого карбоната кальция[1]:
Химические свойства
При нагревании до 900−1000 °C расщепляется на кислотный оксид — углекислый газ CO2 и оксид — негашёную известь CaO по уравнению:
- .
В воде с углекислым газом растворяется, образуя кислую соль — гидрокарбонат кальция Ca(HCO3)2:
- .
Существование именно этой реакции дает возможность образовываться сталактитам, сталагмитам и прочим красивейшим формам, да и вообще развиваться карсту.
При 1500 °C вместе с углеродом образует карбид кальция и оксид углерода (II)
- .
Примечания
Ссылки
Шаблон:АТХ код A02
Польза и вред карбоната кальция
Чтобы понять, наносит ли карбонат кальция вред или дает пользу, важно разобраться в особенностях его состава. Природный минерал, известный всем нам как белый мел, химическая наука относит к красящим веществам неорганического происхождения. В действующей классификации пищевых добавок карбонату кальция присвоен код Е 170.

В естественных условиях вещество:
- встречается в трех кристаллических модификациях (состав единый, кристаллические решетки различаются) — арагонит, фатерит (ватерит), кальцит;
- присутствует в составе мрамора, доломита, известняка, травертита, меловых отложений и других пористых горных пород.
Кроме того, кальций является частью яичной скорлупы, а также беспозвоночных организмов: губок, моллюсков и пр. Собственно, окаменевшие останки этих животных считаются основным источником образования карбоната в природной среде.
Е170 — что за состав?
По химическому составу карбонат кальция относится к солям угольной кислоты. Лабораторный процесс получения этого вещества двухступенчатый:
- 1)гашение негашеной извести, в результате чего образуется гидроксид;
- 2)продувание полученной суспензии углекислым газом.
Очищенный кальций, т. е. краситель Е 170, — белый порошок, который не растворяется в воде и этиловом спирте.
Где добывают карбонат кальция?
Залежи карбоната кальция в форме меловых отложений имеются на всех континентах. Добычей занимается множество компаний, но 70 % производства принадлежит десятку фирм из Европы, среди которых лидируют швейцарская Omya и французская Imerys. Однако около 10 лет назад добычей природных карбонатов и изготовлением Е 170 активно занялись китайские предприятия. Сейчас их доля на рынке постоянно растет, постепенно сужая сбыт европейской продукции.

Меловые пласты, пригодные для добычи карбоната кальция, есть и на российской территории, например, в Белгороде и Воронеже.
Лучший порошок получается в результате промышленной обработки мрамора. Для изготовления фармацевтического компонента и пищевого красителя Е 170 камень подвергается измельчению и многоступенчатой очистке.
Применение карбоната кальция в промышленности
Физико-химические свойства карбоната кальция обусловили широкий потенциал его применения в разных отраслях промышленности. Мел используется при производстве:
- бытовой химии — чистящих средств для сантехники, труб, посуды, обуви;
- бумажных материалов — как отбеливающий компонент при изготовлении мелованной бумаги, картона, бумвинила;
- гигиенических средств — зубных паст, специализированных составов для отбеливания зубов;
- стройматериалов — стекла, керамической плитки, линолеума, пластиковых конструкций, герметиков, шпаклевок, лакокрасочной продукции.

Также природный карбонат кальция задействуется в разнообразных промышленных системах очистки. Он эффективно заменяет опасные синтетические препараты, чем помогает сохранять экологию. Углекислый кальций полезен для сельхозугодий — с его помощью восстанавливают и поддерживают кислотно-щелочной баланс почвы.
Применение в продуктах питания
При производстве продуктов питания очищенный карбонат кальция играет тройную роль:
- 1)краситель, улучшающий товарный вид ;
- 2)регулятор кислотности, повышающий вкусовые и ароматические свойства;
- 3)разрыхлитель, предотвращающий слеживание и комкование пищевой продукции, продляющий срок ее хранения.

Помимо карбоната производители продуктов питания используют для улучшения их свойств цитрат (соль лимонной кислоты) и другие добавки, закодированные буквой Е и цифровыми обозначениями.
Вреден или нет краситель Е170 (карбонат кальция) в пище?
Поступающий в нормальных количествах в организм вместе с пищей карбонат кальция вреда не наносит. Потенциальная опасность существует только при значительной передозировке вещества. Переизбыток Е 170, т. е. гиперкальцемия, может выражаться приступами рвоты и тошноты, болями в животе, раздражительностью, нарушением координации движений. Но повторимся — это редчайшие ситуации, когда человек существенно злоупотреблял пищевой добавкой.

Разрешенная медиками доза углекислого кальция составляет 1,2–1,5 грамма. В продуктах питания количество добавки Е 170 значительно меньше, поэтому она считается максимально безопасной. О безвредности этого компонента пищи свидетельствует тот факт, что вещество законодательно разрешено к использованию практически во всех странах, включая РФ.
Фармацевтическая польза и вред карбоната кальция для организма человека
Карбонат кальция способен положительно влиять на состояние человеческого организма, обеспечивая комплексную пользу:
- улучшает свертываемость крови;
- участвует в нормализации внутриклеточных процессов;
- способствует стабильности осмотического давления крови (оно обеспечивает нормальный водный обмен между тканями организма и кровью).
Благодаря этим свойствам карбонат используют в составе фармацевтических биоактивных добавок. Правильно дозированное применение таких препаратов помогает компенсировать дефицит кальция. Однако польза обеспечивается только качественным, хорошо очищенным веществом природного происхождения.

Вред от использования меловых добавок, напомним, может быть связан только с передозировкой.
- ВАЖНО. Поскольку организм каждого человека индивидуален, необходимо точно знать его состояние, чтобы без опасности для здоровья принимать БАДы. Перед использованием карбоната кальция в пищу лучше проконсультироваться с врачом.
Карбонат кальция, фомула, получение, применение, температурные показатели
Характеристика карбонат кальция
Кальция карбонат представляет собой твердые белые кристаллы без запаха и вкуса нерастворимые в воде, этаноле и легко растворимые в кислотах с выделением углекислого газа. Это неорганическое химическое соединение, соль угольной кислоты и кальция. В природе встречается в виде минералов, различающиеся кристаллической структурой — широко распространённый кальцит, арагонит и ватерит, является главной составной частью известняка, мела и мрамора, одно из самых распространенных на Земле соединений.
Плотность карбоната кальция
Плотность (кальцит) 2,74 г/см³, (арагонит) 2,83 г/см³.
Температура плавления карбонат кальция
Температура плавления (кальцит) 825° C, (арагонит) 1339° C,
Температура разложения карбоната кальция
Температура разложения 900-1000° C.
Формула карбоната кальция
Химическая формула: CaCO3.
Получение карбоната кальция
Кальция карбонат получают взаимодействием известкового молока с углекислотой или хлоридом кальция (СаСl2) с карбонатом натрия (Na2CO3) в водном растворе.
Применение карбоната кальция
Кальция карбонат (углекислый кальций, мел, кальциевая соль угольной кислоты) применяется:
- в лакокрасочной промышленности, в производстве красок и отделочных материалов;
- в химической промышленности при производстве карбида кальция;
- в стекольной промышленности при изготовлении стекла;
- в строительстве при производстве шпатлевок, различных герметиков и др.;
- в сельском хозяйстве, как известковое удобрение и для комплексного агрохимического окультуривания полей;
- в качестве наполнителя для резиновых смесей, бумаги, линолеума;
- в медицине как антацидное, противоязвенное, восполняющее дефицит кальция средство;
- в косметической промышленности при производстве зубного порошка, как наполнитель косметических средств;
- в пишевой промышленности, как пищевая добавка краситель E170.
Таблица 1. Физико-химические показатели карбоната кальция
| Наименование показателя | Норма |
|---|---|
| Содержание хлоридов, %, не более | 0,033 |
| Содержание cульфатов, %, не более | 0,25 |
| Содержание мышьяка (As), %, не более | 0,0001 |
| Содержание бария (Ba), %, не более | 0,0001 |
| Содержание железа (Fe), %, не более | 0,01 |
| Содержание фтора (F), %, не более | 0,005 |
| Содержание ртути (Hg), %, не более | 0,00005 |
| Содержание свинца (Pb), %, не более | 0,0003 |
| Содержание тяжелых металлов, %, не более | 0,002 |
Электрические свойства наполнителей на основе карбоната кальция (2 таблицы):
Таблица 2.
| Диэлектрическая проницаемость (при 17-22°C) при 104 Гц: | |
|---|---|
| кальцит в направлении, перпендикулярном оптической оси | 8,5 |
| кальцит в направлении параллельном оптической оси | 8,0 |
| Диэлектрическая проницаемость (при 17-22°C) при 108 Гц: | |
| доломит, в направлении, перпендикулярном оптической оси | 8,0 |
| доломит, в направлении параллельном оптической оси | 6,8 |
Таблица 3.
| Удельное электрическое сопротивление мрамора при 20°C: | |
|---|---|
| объемное, Ом·см | 109-1011 |
| поверхностное при 50%-ной отн. влажности, Ом | (3-8)·109 |
| поверхностное при 90%-ной отн. влажности, Ом | (1-3)·107 |
| Удельное электрическое сопротивление дисперсии 5г CaCO3 в 100 мл воды при 23 °C, Ом: | |
| кальцит (CaCO3) | 17 000-25 000 |
| доломит (CaCO3·MgCO3) | 3 000-5 000 |
| pH кальцита | 9,0-9,5 |
| pH доломита | 9-10 |
| Удельное объемное электрическое сопротивление ПВХ композиции электроизоляционного назначения при 50°C, Ом·см | >4·1014 |
Таблица 4. Физические свойства различных типов карбонатов.
| Показатели | Кальцит CaCO3 (наиболее устойчивая модификация) | Арагонит CaCO3 (метастабильная модификация, переходит в кальцит) | Доломит CaCO3-MgCO3 (45% масс. MgCO3) | Магнезит MgCO3 |
|---|---|---|---|---|
| Плотность, кг/м3 | 2600 — 2750 | 2920 — 2940 | 2800 — 2900 | 3000 — 3100 |
| Твердость по Мосу | 3,0 | 3,5 — 4,0 | 3,5 — 4,0 | 3,5 — 4,5 |
| Содержание растворимых фракций | 0,99·10-8 (при 15°C)0,87·10-8 (при 25°C) | — | — | 2,6·10-5 (при 12°C) |
| Растворимость при 18°С | ||||
| г/100 г воды | 0,0013 | 0,0019 | 0,032 | 0,0106 |
| г/100 г водного раствора СО2 | 0,13 | 0,19 | 3,2 | 1,06 |
| Температура разложения, °C | 900 | 825, переходит в кальцит при Т>400°C | 730-760 | 350 |
| Природные источники | Известняк, мрамор, известковый шпат, яичная скорлупа, кости (с примесью фосфата кальция), горные породы (в сочетании с доломитом) | Панцири моллюсков, кораллы.Образуется при Т>30°C; переходит в кальцит при Т>400°C и Т<30°C | — | — |
Карбонат кальция — инструкция, показания, применение

Карбонат кальция — антацидный, противоязвенный, восполняющий дефицит кальция препарат.
Фармакологическое действие Карбоната кальция
Карбонат кальция ослабляет или полностью нейтрализует повреждающее действие соляной кислоты на слизистые оболочки пищевода и желудка. После приема препарата уменьшается кислотность желудочного сока, нормализуется электролитный баланс.
Кальций, как макроэлемент, необходим для формирования костной ткани, стабильной работы сердца, нормальной передачи нервных импульсов. Кроме того, кальций участвует в процессе свертывания крови.
Существует еще один препарат с таким же, как у Карбоната кальция, антацидным действием. Это — Кальция карбонат + магния карбонат – препарат, снижающий кислотность желудка, уменьшающий расщепление белков (пептическую активность желудочного сока).
Действие препарата не вызывает изменения кислотно-щелочного равновесия, а также повышенного выделения соляной кислоты после приема лекарства. Магний — один из действующих компонентов препарата — помогает активизировать процессы обмена, оказывает спазмолитическое, антиаритмическое, антиагрегантное действия. Кроме того, микроэлемент принимает участие в регулировании синтеза нуклеиновых кислот и белка, отвечает за процессы переноса, хранения и утилизации энергии.
Форма выпуска
Препараты выпускают в виде таблеток и порошка Карбоната кальция, а также в виде обычных и жевательных таблеток кальция с магнием.
Показания к применению Карбоната кальция
Карбонат кальция применяют: при рефлюкс-эзофагите, расстройствах пищеварения, метеоризме, дискомфорте и болях в эпигастрии, при повышенной кислотности желудочного сока, для профилактики остеопороза у пожилых, кариеса и рахита у детей.
Прием препарата Кальция карбонат + магния карбонат необходим при заболеваниях пищеварительного тракта, сопровождающихся повышенной секрецией и кислотностью желудочного сока.
Препарат, кроме того, назначают в случае дефицита магния, определяемого по таким признакам, как: нарушение сна, утомляемость, мышечные спазмы, миалгия. Прием комплекса дает неплохой эффект во время быстрого роста детей, интенсивных занятий спортом.
Препарат полезен для профилактики оксалатного нефроуролитиаза. Разрешается назначение беременным женщинам, но только после консультации гинеколога, наблюдающего за течением беременности.
Лекарственное взаимодействие Карбоната кальция
Одновременный прием внутрь Карбоната кальция с другими лекарственными средствами может замедлить их абсорбцию. Прием препарата вместе с антибиотиками, принадлежащими к группе тетрациклинов, приводит к уменьшению концентрации тетрациклинов в плазме крови и снижению их клинической эффективности.
Карбонат кальция, принимаемый одновременно с тиазидными диуретиками, увеличивает риск развития метаболического алкалоза и гиперкальциемии.
Одновременный прием препарата с индометацином уменьшает абсорбцию вещества и его негативное раздражающее действие на желудочно-кишечный тракт.
Клиническая эффективность левотироксина также уменьшается, если его принимать вместе с Карбонатом кальция.
Способ применения Карбоната кальция
Для взрослых доза таблеток и порошка Карбоната кальция, принимаемая с целью нейтрализации соляной кислоты, составляет от 0,5 до 1 грамма в сутки. С целью профилактики остеопороза — от 0,6 до 1, 2 грамма в сутки.
Детям для лечения рахита и кариеса рекомендуется принимать препарат от трехсот до шестисот миллиграммов в сутки.
Кальция карбонат, магния карбонат назначают взрослым и детям, начиная с двенадцатилетнего возраста, по две таблетки на один прием. Препарат принимают в момент возникновения симптомов заболевания, либо после еды. В сложных ситуациях допустим прием лекарства каждые два часа. Таблетки не рекомендуется глотать, их нужно держать во рту до полного растворения (рассасывания). Максимальная доза — двенадцать таблеток в сутки.
Побочные действия Карбоната кальция
В результате длительного применения Карбоната кальция в организме могут накапливаться щелочные вещества, что, в свою очередь, вызывает повышение уровня pH в крови и тканях.
При передозировке (больше двух граммов кальция в сутки) возникает гиперкальциемия или молочно-щелочной синдром, сопровождающийся головной болью, слабостью, нарушением аппетита (иногда приводящего к анорексии), тошнотой, рвотой, запором, болью в животе, жаждой, полиурией, вялостью, болью в мышцах и суставах, нарушением сердечного ритма, поражением почек.
При появлении вышеперечисленных симптомов обязательно нужно сделать промывание желудка, принять активированный уголь. Также необходима симптоматическая терапия с поддержанием жизненно важных функций.
Кальций с магнием способен вызвать диарею, аллергические реакции, гипермагниемию, гиперкальциемию (особенно у больных, страдающих почечной недостаточностью). Все симптомы проходят после прекращения приема препарата.
Противопоказания к применению Карбоната кальция
Таблетки и порошок Карбоната кальция не рекомендуются в случаях: тромбоза, тяжелого атеросклероза, гиперкальциемии, а так же гиперчувствительности к лекарственному средству.
Таблетки Карбоната кальция, предназначенные для профилактики и лечения остеопороза, кариеса и рахита, не следует принимать для понижения кислотности. В качестве антацидного средства Кальция карбонат не рекомендуется принимать более шестнадцати таблеток в день.
Запрещено принимать препарат в максимальной дозе больше двух недель без осмотра врача. Если же по показаниям необходим длительный прием в высоких дозах, требуется регулярный контроль показателей функции почек и концентрации кальция в крови.
Кальций с магнием запрещен к применению детям, не достигшим двенадцатилетнего возраста, а так же пациентам с такими заболеваниями, как: фенилкетонурия, серьезные заболевания почек, гиперкальциемия, гиперчувствительность к компонентам препарата.
Не рекомендуется назначение Карбоната кальция для длительного применения. С осторожностью назначают прием препарата пациентам с сахарным диабетом, так как в одной таблетке содержится 475 миллиграммов сахарозы.
Условия хранения
Для хранения препаратов необходимо сухое место с температурой не более +25 °С.








