Применение коллоидного субцитрата висмута в альтернативных схемах эрад
Эпохальное и давно ожидаемое событие для всей гастроэнтерологической общественности произошло в 2005 году – Нобелевская премия по физиологии и медицине присуждена двум австралийским врачам – гастроэнтерологу Бэрри Маршаллу и патоморфологу Робину Уоррену – за открытие Helicobacter pylori и ее роли при гастрите и язвенной болезни.
А.И. Головченко, д.м.н.
В мировых научных кругах так и не сформировалось единое мнение по поводу этого микроорганизма: одни недооценивают роль H. pylori в развитии патологических процессов, другие ее преувеличивают. В любом случае значение открытия Уоррена и Маршалла трудно переоценить: оно потребовало пересмотра традиционных взглядов на возникновение, развитие и терапию весьма широкого круга заболеваний, а также существенно обогатило собственно бактериологическую методологию.
 С момента открытия микроорганизма появились принципиально новые подходы к лечению гастрита и язвенной болезни, которые обеспечили потрясающие результаты, но с течением лет все больше ранее нерешенных и вновь возникших вопросов предстает перед исследователями и практическими специалистами. Изучение особенностей Helicobacter pylori и модификация схем терапии в ответ на изменения микроорганизма продолжаются.
С момента открытия микроорганизма появились принципиально новые подходы к лечению гастрита и язвенной болезни, которые обеспечили потрясающие результаты, но с течением лет все больше ранее нерешенных и вновь возникших вопросов предстает перед исследователями и практическими специалистами. Изучение особенностей Helicobacter pylori и модификация схем терапии в ответ на изменения микроорганизма продолжаются.
Украинские врачи, не только гастроэнтерологи, терапевты, но и представители других специальностей, принявшие участие в научно-практическом симпозиуме «Новейшие перспективные технологии диагностики и контроля лечения заболеваний органов пищеварения», который проходил в Виннице 22-23 марта, проявляют большой интерес к современным методикам терапии при патологии желудочно-кишечного тракта. Именно поэтому высокую оценку аудитории получил доклад начальника клиники гастроэнтерологии Военно-медицинского центра воздушных сил Вооруженных сил Украины, доктора медицинских наук Александра Ивановича Головченко о применении альтернативных схем эрадикационной терапии.
– Согласно международным нормам, указанным в Маастрихтском консенсусе (Рим, 21-22 ноября 2000 года), показания к эрадикации Helicobacter pylori подразделяются на абсолютные и относительные. Среди абсолютных показаний – дуоденальная язва желудка или двенадцатиперстной кишки (активная, неактивная), MALT-лимфома, атрофический гастрит, состояние после резекции желудка по поводу рака, первая линия родства с больными раком желудка, желание пациента (после консультации с врачом). К относительным показаниям относятся функциональная диспепсия, гастроэзофагеальная рефлюксная болезнь и лечение нестероидными противовоспалительными препаратами. Основные направления Маастрихтского консенсуса-III (2005) сформулированы в следующих тезисах.
- Кого лечить?
- Как выявлять и устранять Helicobacter pylori?
- Профилактика рака желудка путем эрадикации Helicobacter pylori.
Инфицированность людей H. pylori в настящее время очень велика. По данным некоторых авторов, она достигает 80%. Однако частота хеликобактерассоциированных заболеваний варьирует в зависимости от страны (чем ниже экономический уровень страны, тем чаще отмечается хеликобактериоз), возраста больного (наиболее часто заражаются H. pylori в возрасте 18-23 лет в развитых странах и 5-10 лет в экономически неблагоприятных странах). Передача Helicobacter pylori происходит в основном от человека к человеку орально-оральным и фекально-оральным путем. Наиболее часто этот микроорганизм передается внутри семьи через предметы гигиены, посуду, при поцелуях. В большинстве случаев колонизация желудочно-кишечного тракта микроорганизмом не приводит к развитию патологического процесса.
Ответ организма на Helicobacter pylori зависит от многих факторов: состояния иммунитета человека, состава слизи в желудке и двенадцатиперстной кишки, а также уменьшения количества рецепторов на поверхности желудка, способствующих адгезии микроорганизма и вирулентности штамма H. pylori (способности продуцировать вакуолизирующий токсин (VacA), а также цитотоксинассоциированный протеин (CagA), которые обусловливают быструю деструкцию эпителиальных клеток с разрушением субэпителиальных тканей и экстрацеллюлярного матрикса). Патологический процесс в желудке запускается в случаях нарушения гомеостаза защитных систем и агрессивных факторов. При этом появляются показания для назначения антихеликобактерной терапии, которая состоит из антимикробных препаратов и средств, снижающих кислотопродуцирующую функцию желудка.
Существует несколько рекомендованных к применению схем эрадикации.
Терапия первой линии включает ингибиторы протонной помпы (ИПП) 2 раза в сутки, кларитромицин – 500 мг 2 раза в сутки, если для региона характерна первичная резистентность к кларитромицину более 15-20% – применяется амоксициллин в дозе 1000 мг 2 раза в сутки либо схема с использованием ИПП, кларитромицина в таких же дозах и метронидазола в дозе 500 мг дважды в сутки. Длительность лечения составляет 14 дней.
Терапия второй линии состоит из ИПП – 2 раза в сутки, висмута субцитрата – 120 мг 4 раза в сутки или 240 мг 2 раза в сутки, метронидазола по 500 мг 2 раза в сутки и тетрациклина – 500 мг 4 раза в сутки.
Лечение третьей линии после двух курсов различной эрадикационной терапии предусматривает определение чувствительности к антибиотикам. Первичная резистентность к кларитромицину составляет 15-20% и зависит от популяции, географического положения, а также проведенных курсов эрадикационной терапии.
В клинической практике хорошо зарекомендовала себя методика эрадикации Helicobacter pylori с применением ИПП. Флемоксина Солютаб по одной таблетке 500 мг 4 раза в день через 15 мин после еды, Де-Нола по 1 таблетке 120 мг 3 раза в день за час до еды и перед сном. Длительность курса терапии составляет 7 дней.
Препараты висмута для лечения заболеваний пищеварительного тракта начали использовать в далекие времена. Еще за много сотен лет до открытия Helicobacter pylori лекари прописывали это вещество при боли в области желудка. Но, как показали современные исследования, антихеликобактерный эффект оказывают лишь коллоидные соли висмута, которые обладают однородностью со слизью, хорошо перемешиваются с ней, а за счет адгезивных свойств способны длительно фиксироваться на слизистой оболочке. Препараты висмута практически не всасываются в кровь и выделяются кишечником, окрашивая испражнения в темный цвет. Побочные эффекты при их применении сравнительно редки. Кроме способности к эрадикации Helicobacter pylori, субцитрат висмута позитивно влияет на восстановление соотношения между уровнями соматостатина и гастрина, улучшая процессы репарации и регенерации поврежденной слизистой оболочки желудка. В глобальном масштабе препараты висмута обладают уникальным свойством – к ним отсутствует резистентность штаммов Helicobacter pylori.
Формирование устойчивости Helicobacter pylori к антибактериальным препаратам создает большую угрозу для медицины. Основными причинами появления резистентных штаммов Helicobacter pylori являются неполноценные схемы антихеликобактерной терапии, нарушение больными режима приема препаратов. По мнению G. Tytgat, в настоящее время лишь меньшая часть пациентов с язвенной болезнью получает адекватную антихеликобактерную терапию. В связи с этим в ряде стран ведутся динамические наблюдения за ростом уровня резистентности H. pylori к антибактериальным препаратам, которые входят в схемы антихеликобактерной терапии на популяционном уровне, и предпринимаются адекватные меры для предотвращения этого роста. К этим мерам относится включение коллоидных препаратов висмута в современные схемы эрадикационной терапии.
В последние годы установлена еще одна особенность Helicobacter pylori – под влиянием неблагоприятных условий, в т. ч. и неадекватной антибактериальной терапии, переходить из вегетативной формы в кокковую. При этом микроорганизм редуцирует ферментативную активность, и его трудно обнаружить с помощью уреазных тестов.
Характеризуя осложнения, обусловленные альтернативными схемами антихеликобактерной терапии, можно отметить формирование дисбиотических изменений толстой кишки. Среди побочных эффектов – аллергические реакции, активация моторики кишечника и прямое токсическое действие препаратов на слизистую оболочку.
Резюмируя вышесказанное, следует отметить, что ни одна из приведенных выше схем лечения не обеспечивает 100% эрадикации Helicobacter pylori, что может быть объяснено различными факторами. Однако эффективность рекомендуемых схем терапии в настоящее время составляет не менее 80%. Основываясь на этом, врачам необходимо продолжать назначать эрадикационное лечение и контролировать его результаты у конкретных пациентов.
Подготовила Елена Семиног
Читайте также
www.health-ua.org
Висмута субцитрат :: Инструкция :: Цена :: Описание препарата
Висмута субцитрат (Bismuth! subnitras)Противоязвенное средство с бактерицидной (уничтожающей бактерии) активностью в отношении Helicobacter pylori -микроорганизмов, которые, по-видимому, в ряде случаев способствуют возникновению хронического гастрита (воспаления слизистой оболочки желудка) и рецидивирующей (Периодически повторяющейся) язвенной болезни.
В кислой среде желудка и двенадцатиперстной кишки образует защитную пленку на поверхности язв и эрозий (дефекта слизистой оболочки), что способствует их рубцеванию, повышает устойчивость слизистой оболочки к воздействию пепсина (фермента, разлагающего пептиды и белки), соляной кислоты и ферментов. Повышает активность цитопротективных (защищающих клетки) механизмов, увеличивая синтез простагландина ei и секрецию (выделение) бикарбонатов.
Язвенная болезнь желудка и двенадцатиперстной кишки. Обострение гастродуоденита (воспаления желудка и двенадцатиперстной кишки) у больных язвенной болезнью. Гастрит (воспаление слизистой оболочки желудка), вызванный Helicobacter pylori.
Препарат назначают по 1 таблетке 3 раза в сутки за 30 минут до завтрака, обеда и ужина и на 4-й раз перед сном. Таблетку запивают 1-2 глотками воды (но не молока). Лечение проводят в течение 4-6 недель. При необходимости оно может быть продлено до 8 недель. После этого следует сделать перерыв на 8 недель, в течение которого не следует принимать другие препараты, содержащие висмут.
При обнаружении у больного бактерии Helicobacter pylori рационально сочетать лечение препаратом с приемом внутрь метронидазола по 0,25 г 4 раза в сутки в течение 10 дней и/или амоксициллина по 0,25 г 4 раза в сутки в течение 10 дней. С целью закрепления ремиссии (временного ослабления или исчезновения проявлений болезни) заболеваний, связанных с Helicobacter pylori, а также стойкой санации (устранения и профилактики заболеваний) слизистой оболочки, целесообразно проведение в течение первого года 3-4-х двухнедельных курсов антибактериальной терапии (висмута субцитрат + амоксициллин, или висмута субцитрат + метронидазол, или висмута субцитрат + фуразолидон).
За 30 мин до и после приема препарата следует воздерживаться от приема пиши, жидкостей и антацидньгх (понижающих кислотность желудка) средств.
Препарат уменьшает всасывание тетрациклина.
При совместном применении с другими препаратами, содержащими висмут, повышается риск увеличения концентрации висмута в плазме крови.
Возможно появление тошноты, рвоты, более частого стула. На фоне приема препарата возможно окрашивание кала в темный цвет, а также незначительное потемнение языка. При длительном приеме препарата в высоких дозах возможно развитие энцефалопатии (болезней головного мозга, связанных с накоплением висмута в центральной нервной системе, характеризующихся его дистрофическими изменениями).
Выраженное нарушение функции почек, беременность, кормление грудью. Препарат не назначают детям.
Таблетки по 0,12 г висмута субцитрата.
В плотно укупоренных упаковках в защищенном от света месте.
Биснол, Вентрисол, Трибимол, Де-Нол, Бисколвдтрат, Де-Нолтал, Дуозол, Ульцерон, Бизмат.
Смотрите также список аналогов препарата Висмута субцитрат.висмута субцитрат коллоидный
Инструкция составлена коллективом авторов и редакторов сайта Piluli. Список авторов справочника лекарств представлен на странице редакции сайта: Редакция сайта.
Ссылки на использованные источники информации.
Описание препарата «Висмута субцитрат» на данной странице является упрощённой и дополненной версией официальной инструкции по применению. Перед приобретением или использованием препарата вы должны проконсультироваться с врачом и ознакомиться с утверждённой производителем аннотацией.
Информация о препарате предоставлена исключительно с ознакомительной целью и не должна быть использована как руководство к самолечению. Только врач может принять решение о назначении препарата, а также определить дозы и способы его применения.
Количество просмотров: 67275.
www.piluli.kharkov.ua
Сравнительное исследование эффективности и безопасности использования препаратов коллоидного висмута трикалия дицитрата у больных с язвенной болезнью желудка и двенадцатиперстной кишки | Павлов А.И., Кириллов С.М., Пономаренко Д.С., Хаваншанов А.К., Фадина Ж.В., Бобкова И.В., Саввин В.Ю.
В статье представлено исследование препаратов коллоидного висмута трикалия дицитрата у больных с язвенной болезнью
Среди кислотозависимых заболеваний верхних отделов ЖКТ одно из ведущих мест занимает язвенная болезнь (ЯБ). Актуальность проблемы обусловлена высоким уровнем распространенности болезни и ее «омоложением». ЯБ страдают приблизительно 10% населения. Язвенные поражения являются не только медицинской, но и социальной проблемой в связи с широкой распространенностью заболевания, высокой стоимостью обследования и лечения таких больных. В настоящее время наблюдается утяжеление течения ЯБ с частыми рецидивами, нивелирование сезонности обострений, появление атипичных и бессимптомных форм. В отношении больших и длительно не рубцующихся язв до сих пор не определен подход к выбору лечения: хирургическое или консервативное [1, 2].Большое клиническое значение имеет растущая устойчивость Н. pylori к антибиотикам. Требуются определенные навыки по выбору для каждого конкретного больного наиболее оптимального плана диагностики и лечения [3–5].
Согласно рекомендациям Маастрихта-IV, для эрадикации H. pylori следует использовать схему квадротерапии, которая включает, помимо ингибиторов протонного насоса и антибиотиков, препараты висмута трикалия дицитрата (ВТД).
Соединения висмута вошли в медицинскую практику со времен средневековья, а первый научный доклад о содержащем висмут препарате для лечения диспепсии был сделан в 1786 г. На сегодняшний день самое широкое применение соединения висмута нашли в гастроэнтерологии, а наиболее часто используемыми среди них являются субсалицилат и коллоидный субцитрат – ВТД (табл. 1) [6].

Висмута субсалицилат во многих странах используется в качестве безрецептурного препарата для быстрого купирования изжоги, тошноты и диареи.
Коллоидный висмута субцитрат нашел применение в первую очередь в лечении заболеваний, ассоциированных с H. pylori-инфекцией, а также как пленкообразующий гастропротектор. Именно этот препарат представляет наибольший интерес с точки зрения фармакологических свойств и клинического применения [7, 8].
Механизм антибактериального действия ВТД связан не только с нарушением адгезии микроорганизмов к эпителию слизистой оболочки, но и с нарушением синтеза АТФ в бактериальной клетке. Так, в исследовании in vitro инкубация H. pylori с ВТД приводила к выраженному угнетению роста микроорганизма и его последующей гибели [6, 9–11]. Благодаря антихеликобактерной активности препараты коллоидного висмута позволяют повысить или сохранить эффективность эрадикационной терапии, особенно в условиях растущей антибиотикорезистентности H. рylori. Антихеликобактерный моноэффект ВТД составляет в среднем 14–40% [7]. Преимущество препарата состоит в том, что не существует естественной или приобретенной резистентности H. рylori к ионам висмута. Сочетание с антибиотиками увеличивает степень эрадикации до 50%, а сочетание 2-х базисных препаратов – ингибитора протонной помпы (ИПП) и ВТД – с двумя антибиотиками позволяет преодолеть резистентность штаммов H. pylori к производным нитримидазолов либо кларитромицину (рис. 1) [8].

В оригинальной работе Е.Ю. Плотниковой и А.С. Сухих (2016) сравнивались характеристики инфракрасных спектров 2-х готовых, наиболее востребованных лекарственных форм ВТД, а именно препаратов Де-Нол® и Новобисмол®. Спектральные характеристики изучались на инфракрасном фурье-спектрометре ФСМ-1202 (Россия). Данное исследование показало практически полную фармацевтическую эквивалентность исследованных препаратов Де-Нол® и Новобисмол® (рис. 2) [12].


Нами было проведено открытое сравнительное проспективное исследование препаратов Де-Нол® и Новобисмол®.
Цель исследования: сравнение эффективности и безопасности двух препаратов коллоидного висмута: Де-Нол® (Нидерланды) и Новобисмол® (Россия) в лечении ЯБ желудка и двенадцатиперстной кишки.
В ходе исследования были поставлены следующие задачи:
1) установить эффективность применения препаратов висмута в лечении ЯБ желудка и двенадцатиперстной кишки: сравнить сроки эпителизации (рубцевания) язвенных дефектов, оценить динамику клинических синдромов и жалоб больных;
2) оценить целесообразность применения исследуемых препаратов коллоидного субцитрата висмута в схемах эрадикации H. pylori;
3) оценить безопасность применения изучаемых препаратов путем оценки частоты и выраженности неблагоприятных реакций (побочных эффектов).
Обследовано 212 пациентов с ЯБ желудка (ЯБЖ) и ЯБ двенадцатиперстной кишки (ЯДК). Группа пациентов с ЯБЖ включала 83 пациента – 27 женщин и 56 мужчин. Группа с ЯДК включала 129 пациентов – 47 женщин и 82 мужчины. Возраст пациентов обеих групп составил от 19 до 67 лет (средний возраст 43,1±23,8 года), основные клинические и лабораторные показатели в группах статистически не различались. На рисунке 3 представлена структура пациентов с ЯБЖ и ЯДК, принимавших ВДТ.
Всем пациентам проводилось стандартное обследование и лечение согласно Маастрихтскому соглашению – IV [5, 6, 13]. Обследование включало опрос относительно жалоб, анамнеза, физикальных данных, сопутствующих патологий, а также общеклинические анализы крови и мочи, биохимический анализ крови, УЗИ брюшной полости по стандартной методике. Эзофагофиброгастродуоденоскопия (ЭГДС) также проводилась по стандартной методике на аппарате OLIMPUS EXERA – 160/190. ЭГДС проводилась при поступлении и на 10–14-е сутки нахождения пациента в стационаре. При отсутствии рубцевания (эпителизации) язвенного дефекта повторная ЭГДС выполнялась вновь через каждые 7–10 дней.
Наличие H. pylori определяли при помощи следующих методов:
– гистологический – «золотой стандарт» диагностики и степени обсемененности;
– уреазный тест – определение уреазной активности в биоптате слизистой оболочки желудка;
– дыхательный уреазный тест с применением мочевины, меченной изотопами 13С или 14С, – только для контроля эрадикации H. pylori через 1,0–1,5 мес. после окончания лечения.
В процессе обследования выявлены 3 пациента – мужчины старше 55 лет – с гигантскими язвами желудка. Они не вошли в группы исследования, т. к. при их лечении значительно увеличивались сроки и использовались дополнительные лекарственные препараты и хирургические методы.
Пациентам с ЯБЖ независимо от локализации язвенного дефекта выполнялась биопсия для исключения малигнизации. У всех этих больных злокачественные опухолевые клетки при биопсии не обнаружены. В обеих группах для лечения (рубцевания) язвенных дефектов помимо ИПП применялись препараты ВТД как для основной терапии (для рубцевания язвенного дефекта), так и для эрадикации H. pylori. Для эрадикации H. pylori использовалась, согласно рекомендациям Маастрихта-IV, квадротерапия в течение 10 дней: омепразол 20 мг 2 раза в день; ВТД 120 мг 4 раза в день; кларитромицин 500 мг 2 раза в день; амоксициллин 1000 мг 2 раза в день [13–15].
Болевой абдоминальный синдром при неэффективности терапии купировали спазмолитиками и холинолитиками в стандартных дозах. В 1-й группе из препаратов коллоидного висмута применялся Де-Нол® 120 мг 4 раза в день, во 2-й группе – Новобисмол® 120 мг 4 раза в день. Клинические показатели и осложнения в группах пациентов представлены в таблице 2.

Интенсивность болевого синдрома измерялась в баллах от 0 до 5. Динамика изменения боли представлена на диаграммах (рис. 4 и 5).
Диспепсический синдром характеризовался изжогой, тошнотой, горечью во рту, запахом изо рта, отрыжкой. Интенсивность синдрома суммарно оценивалась в баллах от 0 до 5 и представлена на диаграммах (рис. 6 и 7).

На фоне лечения болевой абдоминальный синдром значительно снижался уже на 3-и сутки, а полностью купировался при ЯБЖ на 6-е сутки, при ЯДК на 7-е сутки. Ночные боли прекратились на 7-е сутки при ЯБЖ, при ЯДК – на 8-е сутки (рис. 8 и 9).

Явления диспепсии на фоне лечения значительно уменьшались на 3–6-е сутки у всех пациентов с ЯБ. Полностью прекратились на 10-е сутки при ЯБЖ и на 11-е сутки – при ЯДК.
Контроль эпителизации (рубцевания) язвенных дефектов осуществлялся при помощи контрольных ЭГДС (табл. 3; рис. 10 и 11). Динамика рубцевания язвенных дефектов в 1-й и 2-й группах достоверно не различалась (р<0,05).


Эрадикационную терапию по квадросхеме проводили всем пациентам, у которых выявлялся H. pylori. Нежелательные явления при проведении эрадикации H. pylori развились у 7 (3,3%) пациентов. У 1 пациента (мужчина, 21 год) в 1-й группе была диагностирована аллергическая сыпь на препарат коллоидного висмута (Де-Нол®). Еще у 6 (2,8%) пациентов развилась антибиотикоассоциированная диарея легкой степени тяжести (4 пациента в 1-й группе и 2 – во 2-й группе). В результате этого пациенту с аллергической реакцией эрадикация H. pylori была прекращена, а пациентам с диареей эрадикация H. pylori – сокращена до 7 сут. Других осложнений не отмечалось.
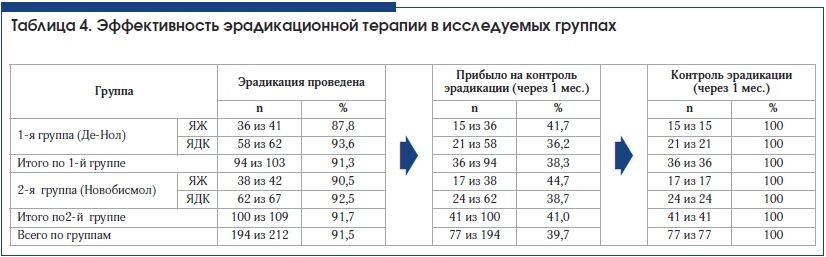
По парамедицинским причинам и из-за низкой комплаентности пациентов контроль эрадикации H. pylori был проведен в 1-й группе у 36 пациентов, во 2-й группе – у 41 пациента, т. е. от 38,3 до 41,0%. У всех пациентов, прошедших контроль, через месяц после эрадикации по квадросхеме, H. pylori не определялся, т. е. была достигнута 100% эрадикация. Результаты эрадикационной терапии представлены в таблице 4.
Выводы
1. Результаты проведенного исследования свидетельствуют об отсутствии достоверных различий в обеих группах пациентов с применением препаратов Де-Нол® и Новобисмол® по показателям сроков рубцевания язвенных дефектов желудка и двенадцатиперстной кишки, динамики разрешения болевого абдоминального и диспепсического синдромов.2. Достоверных различий в группах больных язвенной болезнью желудка и двенадцатиперстной кишки при проведении эрадикации H. pylori по квадросхеме с применением препаратов Де-Нол® и Новобисмол® не отмечалось. Эрадикация Н. рylori была достигнута сразу после курса приема препаратов в 1-й группе у 38,3%, во 2-й группе – у 41,0% пациентов. У всех пациентов, которым был осуществлен контроль через месяц после эрадикации, H. pylori не определялся, т. е. была достигнута 100% эрадикация патогена.
3. В ходе применения препаратов коллоидного висмута трикалия дицитрата (Де-Нол® и Новобисмол®) у пациентов с язвенной болезнью желудка и двенадцатиперстной кишки серьезных побочных эффектов не отмечалось.
www.rmj.ru
Висмута субцитрат — это… Что такое Висмута субцитрат?
Противоя́звенные препара́ты и препара́ты для лече́ния гастроэзофагеа́льного ре́флюкса (англ. Drugs for peptic ulcer and gastro-oesophageal reflux disease (GORD)) — группа лекарственных препаратов A02B Анатомо-терапевтическо-химической классификации (АТХ).
- В данной статье свойства лекарственных препаратов даются только в отношении их использования в терапии кислотозависимых заболеваний.
- Все упоминаемые в статье лекарственные препараты называются только по их действующим веществам (международным непатентованным названиям). Торговые наименования конкретных лекарств, при необходимости, можно уточнить по «Реестру лекарственных средств»[1] или по базе данных ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора РФ[2].
Состав группы «Противоязвенные препараты и препараты для лечения гастроэзофагеального рефлюкса»
По классификации АТХ в группу A02B «Противоязвенные препараты и препараты для лечения гастроэзофагеального рефлюкса» входят пять подгрупп:
Антисекреторные препараты
В 1910 году Карл Шварц выдвинул постулат: «Нет кислоты — нет язвы»[3]. В соответствии с этим постулатом многие из противоязвенных препаратов тем или иным способом снижают кислотность желудочного содержимого: или путём нейтрализации уже секретированной кислоты (такие препараты относятся к группе антацидов), или воздействуя угнетающим образом на механизмы секреции соляной кислоты. В гастроэнтерологии антисекреторными препаратами принято называть ингибиторы протонного насоса, Н2-блокаторы и периферические М-холинолитики[4].
Механизмы секреции соляной кислоты и её ингибирования
Секреция соляной кислоты в желудке происходит в париетальной клетке. Противоположные мембраны этой клетки функционально резко отличаются.
Процесс секреции соляной кислоты происходит на апикальной (направленный в просвет желудка) мембране, он основан на трансмембранном переносе протонов и непосредственно осуществляется специфическим протонным насосом — Н+/К+-АТФазой. При активизации молекулы Н+/К+-АТФазы встраиваются в мембрану секреторных канальцев париетальной клетки и переносят ионы водорода H+ из клетки в просвет железы, обменивая их на ионы калия K+ из внеклеточного пространства. Этот процесс предваряет выход из цитозоля париетальной клетки ионов хлора Cl–, таким образом в просвете секреторного канальца париетальной клетки и образуется соляная кислота.
На противоположной, базолатеральной мембране, располагается группа рецепторов, которые регулируют секреторную активность клетки: гистаминовые Н2, гастриновые CCKB и ацетилхолиновые М3. В результате их воздействия в париетальных клетках увеличивается концентрация кальция Ca2+ и циклического аденозинмонофосфата (цАМФ), что приводит к активации тубуловезикул, содержащих Н+/К+-АТФазы. На базолатеральной мембране также расположены рецепторы ингибиторов секреции соляной кислоты — простагландинов Е2 и соматостатина, эпидермального фактора роста и другие.
Действие антисекреторных препаратов основано либо на блокаде стимулирующих воздействий на уровне рецепторов, либо на блокаде внутриклеточных ферментов, участвующих в продукции соляной кислоты Н+/К+-АТФазы. Разные группы антисекреторных препаратов (М-холинолитики, H2-блокаторы, ингибиторы протонного насоса и другие) воздействуют на разные элементы париетальной клетки.
М-холинолитики
М-холинолитики (синонимы: антихолинергические средства, М-холиноблокаторы) подразделяются на неселективные (или системные) и селективные. Неселективные воздействуют на все типы М-холинорецепторов, а селективные — только на определённые.
М-холинолитики являются одними из самых старых протовоязвенных средств. Исторически первые из них — препараты белладонны и атропин. Последний в прошлом был основным лекарством для лечения кислотозависимых заболеваний, однако его неизбирательное воздействие на имеющиеся во многих органах М-холинорецепторы порождает множество серьезных побочных эффектов (тахикардия, сухость во рту, расстройства аккомодации, раздражительность, головная боль, нарушения сна). Не имеющий такого количества недостатков платифиллин заметно менее эффективен. Другие неселективные периферические М-холинолитики, такие как метоциния йодид, тоже обладают большим количеством побочных эффектов.
Из М-холинолитиков наиболее эффективным является селективный М1-холинолитик пирензепин, который блокирует М1-холинорецепторы на уровне интрамуральных ганглиев и, таким образом, тормозит стимулирующего влияние блуждающего нерва на секрецию соляной кислоты и пепсина, не оказывая ингибирующего воздействия на М-холинорецепторы слюнных желез, сердца и других органов. Пирензепин (единственный из М-холинолитиков) включён в рассматриваемую в данной статье группу A02B (код АТХ A02BX03). Однако по своим кислотоблокирующим свойствам он сильно проигрывает не только ингибиторам протонного насоса, но и Н2-блокаторам и, не имея перед ними никаких преимуществ, он, как и другие М-холинолитики, в терапии кислотозависимых заболеваний применяются всё реже[4].
H2-блокаторы
H2-блокаторы (синоним: блокаторы H2-гистаминовых рецепторов) конкурентным образом воздействуют на гистаминовые Н2-рецепторы, блокируя, тем самым, стимулирующее действие гистамина. Наиболее известны H2-блокаторы: циметидин, ранитидин и фамотидин.
- См. основную статью «Блокаторы h3-гистаминовых рецепторов».
Ингибиторы протонного насоса
Ингибиторы протонного насоса, встраиваясь в Н+/К+-АТФазу, блокируют транспортировку ею ионов водорода Н+ в просвет желудка. Наиболее известный ингибитор протонного насоса — омепразол.
- См. основную статью «Ингибиторы протонного насоса».
Блокаторы гастриновых рецепторов
Несмотря на многолетний поиск ингибиторов гастриновых рецепторов и создание нескольких препаратов этого типа, до широкого их использования в практической медицине далеко. Неселективный блокатор гастриновых рецепторов проглумид[5], код A02BX06, блокирует оба подтипа гастриновых рецепторов: CCKA и CCKB. По степени угнетения кислотопродукции он эквивалентен первому поколению Н2-блокаторов, но не имеет такого числа побочных эффектов. Селективные антагонисты гастриновых рецепторов лорглумид и девазипид[6], позиционированные при разработке как противоязвенные препараты, пока на нашли своего применения в клинической практике. В России ни один из перечисленных препаратов—блокаторов гастриновых рецепторов не зарегистрирован[1][2].
Новые классы антисекреторных средств
В настоящее время ведутся исследовательские работы, направленные на создание новых антисекреторных средств:
- новый тип блокаторов Н+/К+-АТФазы, так называемые антагонисты кислотного насоса (англ. acid pump antagonist), которые, в отличие от ингибиторов протонного насоса, блокируют механизм транспортировки Н+/К+-АТФазой ионов калия К+[7],
- блокаторов и стимуляторов мембранных рецепторов Ca2+[8].
Простагландины

Мизопростол — синтетический аналог простагландина Е1

Энпростил — синтетический аналог простагландина Е2
- В данной статье рассматриваются простагландины — противоязвенные препараты, простагландины — липидные физиологически активные вещества описываются в статье «Простагландины».
Простагландины в широком смысле — гормоноподобные вещества, которые синтезируются почти во всех тканях организма. Они участвуют в регуляции кровяного давления, сокращениях матки, снижают секрецию желудочного сока и уменьшают его кислотность, являются медиаторами воспаления и аллергических реакций, принимают участие в деятельности различных звеньев репродуктивной системы, играют важную роль в регуляции деятельности почек, оказывают влияние на различные эндокринные железы и ряде других физиологических процессов. В зависимости от химической структуры, простагландины относятся к той или иной серии: A, B, C, D, E, F, G, H, I.
Без участия простагландинов серии Е (Е1 и Е2) невозможна продукция адекватной по количеству и качеству гастродуоденальной слизи, секреция в просвет желудка бикарбонатов, сохранение достаточного объемного кровотока в слизисто–подслизистом слое, обеспечение восстановления слизистой[9]. Недостаток простагландинов Е1 и Е2 решающим образом снижает защитные свойства гастродуоденальной слизистой оболочки.
Нестероидные противовоспалительные препараты (синоним: нестероидные противовоспалительные средства, часто употребляемая аббревиатура: НПВС) — класс широко применяемых лекарств, без которых невозможна терапия многих заболеваний. Наиболее известным представителем НПВС является аспирин. НПВС, несмотря на различия химического строения, имеют общий механизм действия всех эффектов (болеутоляющего, противовоспалительного, жаропонижающего, десенсибилизирующего), в основе которого лежит угнетающее влияние на биосинтез простагландинов, в том числе простогландинов Е1 и Е2. Приём НПВС нередко является причиной изъязвления гастродуоденальной зоны, в том числе наиболее частой причиной возникновения язв желудка и двенадцатиперстной кишки для неинифицированных Helicobacter pylori[10].
Часто, когда терапия НПВС необходима, для компенсации ингибированных НПВС простогландинов применяются лекарственные средства — химические аналоги природных простагландинов. Они оказывают избирательное воздействие и не вызывают ряд серьезных побочных эффектов, а также не инактивируются столь быстро, как природные. Группу противоязвенных лекарственных препаратов «A02BB Простагландины» составляют мизопростол и энпростил — синтетические аналоги простагландинов, соответственно, Е1 и Е2.
Мизопростол и энпростил обладают антисекреторными и цитопротекторными свойствами. Связываясь с рецепторами париетальных клеток желудка, они угнетают базальную, стимулированную и ночную секрецию желудочного сока и соляной кислоты, усиливают образование бикарбоната и слизи, улучшает кровоток. Уменьшают базальную (но не стимулированную гистамином) продукцию пепсина. Повышают устойчивость слизистой оболочки желудка и предупреждают развитие эрозивно-язвенных поражений, способствует заживлению пептических язв. У больных, принимающих НПВС, уменьшают частоту развития язв желудка и двенадцатиперстной кишки, снижают риск язвенного кровотечения.
Побочные действия мизопростола и энпростила: преходящая диарея, легкая тошнота, головная боль, боль в животе.
В педиатрии простагландины применяются в исключительных случаях[11].
Мизопростол в увеличенной дозе используется при медикаментозных абортах.
Существуют другие противоязвенные препараты — аналоги природных простагландинов: риопростил (аналог Е1), арбапростил и тимопростил (аналоги Е2). Из всех перечисленных в данной статье простагландинов в России разрешён к применению только мизопростол[12]. (государственный орган США) мизопростол одобрен к применению, как рецептурное средство, только для профилактики НПВС-индуцированных язв.
Кроме простагландинов — противоязвенных препаратов, существуют иные синтетические аналоги простагладинов, предназначенные для других медицинских применений и не относящиеся к группе «A02BB Простагландины»: алпростадил (аналог простагландина Е1), динпрост (аналог F2) и другие[13].
Гастропротектроры, обволакивающие, вяжущие средства

Сукралфат
Сукралфат
Сукралфат (другое написание: сукральфат), код АТХ A02BX02. По «Фармакологическому указателю» относится к группе «Антациды и адсорбенты»[14]. При попадании в желудок, под действим кислоты желудочного сока, сукралфат образует пастообразную массу, выполняющую для язвы роль протектора. Антацидными свойствами не обладает[15].
Висмута трикалия дицитрат
Висмута трикалия дицитрат (синоним: висмута субцитрат), код АТХ A02BX05. По «Фармакологическому указателю» относится к группе «Антациды и адсорбенты»[16]. Цитопротектор. Увеличивает синтез простагландина Е2, стимулирующего образование слизи и секрецию бикарбоната. Оказывает местное бактерицидное действие на Helicobacter pylori, нарушая целостность стенки микробных клеток, препятствуя адгезии Helicobacter pylori на эпителиальных клетках, ингибируют его уреазу, фосфолипазу и протеолитическую активность. Сочетание обволакивающих, цитопротективных и антибактериальных свойств висмута трикалия дицитрата позволяет использовать его в схеме эрадикационной терапии[17].
Висмута субнитрат
Висмута субнитрат, код АТХ A02BX12. По «Фармакологическому указателю» относится к группам «Антациды и адсорбенты» и «Антисептики и дезинфицирующие средства»[18]. Цитопротектор. Вяжущее. Антисептическое средство. Применяется при лечении гастродуоденита, язвенной болезнь желудка и двенадцатиперстной кишки, рефлюкс-эзофагита, энтерита, колита. Подавляет рост и развитие Helicobacter pylori (эффективность подавления небольшая). Слабый антацид[19]. Применяется также при лечении воспалений кожи.
Альгиновая кислота
Альгиновая кислота, код АТХ A02BX13. По «Фармакологическому указателю» альгинаты относятся к группам «Антациды и адсорбенты». Антирегургитант. При взаимодействии препарата с кислотой желудочного сока, под действием альгинатов происходит нейтрализация последней, образуются гель, который предохраняет слизистую пищевода, предохраняя ее от дальнейшего воздействия соляной кислоты и пепсина, что проявляется в значительном ослаблении диспепсических и болевых ощущений. Одновременно обеспечивает защиту от щелочных рефлюксов желудочного содержимого в пищевод[20].
- См. основную статью «Альгиновая кислота».
Комбинации препаратов для эрадикации Helicobacter pylori
Состав группы «A02BD Комбинации препаратов для эрадикации Helicobacter pylori» отражает классический подход к эрадикации Helicobacter pylori, заключающийся в том, что для эрадикации необходимо использование «тройной терапии», включающей ингибитор протонного насоса и два антибиотика, однако современный подход («Маастрихтские консенсусы») к эрадикации Helicobacter pylori допускает применение в основных схемах и иных препаратов, например, ранитидина висмута цитрат[21]. Эрадикационная терапия отличаются довольно высокой агрессивностью, поскольку включают не менее двух антибактериальных препаратов. Подобное вмешательство небезразлично для детского или ослабленного организма и нередко сопровождается развитием побочных эффектов[17]. Кроме того, применение стандартных схем часто оказывается недостаточно эффективным в связи с широко распространенной и постоянно растущей резистентностью штаммов Helicobacter pylori к применяемым антибактериальным препаратам, в первую очередь, к метронидазолу и кларитромицину[22]. Поэтому круг применяемых на практике препаратов для эрадикации Helicobacter pylori заметно шире представленных в группе A02BD.
- См. основную статью «Эрадикация Helicobacter pylori».
Сравнение препаратов для лечения кислотозависимых заболеваний
Для заживления язвы желудка или двенадцатиперстной кишки необходимо поддержание рН в желудке больше 3 не менее 18 часов в сутки в течение 3 — 6 недель. Для заживления эрозии пищевода — рН в пищеводе должно быть более 4 в течение 16 часов от 8 до 12 недель[4]. Оптимальное значение рН (в течение не менее 16 часов в сутки) для функциональной диспепсии и поддерживающей терапии ГЭРБ — не менее 3, при эрозивной ГЭРБ и повреждениях слизистой оболочки желудка, вызванной НПВС — не менее 4, при тройной антихеликобактерной терапии язвенной болезни — не менее 5, при язвенном кровотечении и экстрапищеводных проявлениях ГЭРБ — не менее 6[10].
Препараты базисной и поддерживающей терапии
Единственным классом препаратов, способными обеспечить требуемое кислотоподавление, являются ингибиторы протонного насоса (ИПП). Поэтому они, в значительно большей степени, чем другие препараты могут претендовать на роль основных препаратов базисной терапии кислотозависимых заболеваний. Среди ИПП наибольший антисекреторный эффект дают эзомепразол и рабепразол[4][10][23]. Кроме ИПП, согласно современным взглядам, в качестве основного препарата базисной терапии допускается применение Н2-блокатора фамотидина[24]. Циметидин и ранитидин, не имея никаких преимуществ перед фамотидином, обладают заметно большим числом побочных эффектов. Н2-блокаторы 4-го и 5-го поколений не превосходят фамотидин по кислотоподавляющему действию[25].
В составе антихеликобактерной терапии ИПП также имеют преимущество перед остальными антисекреторными средствами[10]. При этом разница по эффективности действия между различными ингибиторами протонного насоса при эрадикации Helicobacter pylori не обнаружена[22].
При поддерживающей терапии в качестве основного средства также рекомендуются ингибиторы протонного насоса, обычно в половинной дозе по отношению к базисной[10].
Препараты «дополняющие» и «по требованию»
Однако ингибиторы протонного насоса имеют целый ряд недостатков. Большой латентный период (начало действия препарата после приёма), эффект «ночного кислотного прорыва», индивидуальная и расовая резистентность к различным ИПП (особенно «омепразоловая резистентность») доходящая, в отдельных ситуациях, до 40 % пациентов[15]. Поэтому приходится применять препараты других классов: при резистентности к ИПП — Н2-блокатор фамотидин, для коррекции ночного кислотного прорыва — дополнительная к ИПП вечерняя доза Н2-блокатора[21]. Для профилактики язв, вызываемых приёмом нестероидных противовоспалительных препаратов — простагландины и т.д.
Отдельный класс составляют «препараты по требованию» — при возникновении симптомов того или иного заболевания: изжоги, болей в животе для их купирования применяют не препараты базисной терапии (в связи большим латентым периодом последних), а антациды или прокинетики (стимуляторы моторики ЖКТ) типа домперидона или метоклопрамида.
В настоящее время в клинической практике для лечения только язвенной болезни желудка и двенадцатиперстной кишки применяется более 500 различных препаратов[26].
Препараты из группы A02BX, не зарегистрированные в России
В группу «A02BX Прочие противоязвенные препараты и препараты для лечения гастроэзофагеального рефлюкса», кроме тех, кто уже упомянут выше, входит целый ряд препаратов, созданных более 25 лет назад, не способных конкурировать по своим свойствам с современными антисекреторными препаратами и хотя часть из них еще используется в некоторых странах, сегодня они представляют не более, чем исторический интерес. В России все перечисленные в этом разделе препараты не зарегистрированы[1][2]. Ниже даны их краткие характеристики:

Карбеноксолон
Карбеноксолон
Карбеноксолон, код АТХ A02BX01. Синтетическое производное глицирризиновой кислоты, в природе получаемой из корня солодки; противовоспалительное средство для лечения изъязвлений и воспалений слизистой оболочки рта, пищевода. Иногда рассматривается как цитопротектроное средство[11]. В Великобритании рекомендован для лечения язв и воспалений пищевода (эзофагита).
Ацетоксолон
Ацетоксолон, код АТХ A02BX09. Ацетат глицирризиновой кислоты (англ. acetylglycyrrhetinic acid), противоязвенное средство[27].

Метиосульфония хлорид
Метиосульфония хлорид
Метиосульфония хлорид (метил-метионин-сульфоний), код АТХ A02BX04. Обладает выраженным цитопротективным действием на слизистую желудка и двенадцатиперстной кишки, способствует заживлению язвенных и эрозивных поражений.
В «натуральной медицине» метиосульфония хлорид называют витамином U и считают, что недостаток этого витамина ведёт к образованию язв[28]. Имеется, в том числе, в капусте, люцерне, сельдерее, непастеризованном молоке[29], яичном желтке. Современная наука[30] не относит метиосульфония хлорид к витаминам.
Гефарнат
Гефарнат, код АТХ A02BX07. Антацидное, спазмолитическое средство[31]. Российская регистрация аннулирована в 1996 году[32].
Сулгликотид
Сулгликотид, код АТХ A02BX08. Цитопротектор. Производится из двенадцатиперстных кишок свиней[33].
Золмидин
Золмидин (вариант наименования: золимидин), код АТХ A02BX10. Цитопротектор, применяемый при лечении дуоденальных язв[34].
Троксипид
Троксипид, код АТХ A02BX11. Используется при лечении гастроэзофагеальной рефлюксной болезни.
Препараты группы А02B в перечне «Жизненно необходимые и важнейшие лекарственные средства»
Три препарата из данной группы: омепразол, рабепразол и фамотидин включены в «Перечень жизненно необходимых и важнейших лекарственных средств» (в подраздел «Антациды и другие противоязвенные средства» раздела «XIII. Средства для лечения заболеваний желудочно-кишечного тракта»).
См. также
Источники
- Энциклопедия лекарств rlsnet.
- Статьи Википедии: en:Carbenoxolone, en:Cholecystokinin antagonist, en:Misoprostol, en:Proglumide, en:S-Methylmethionine, en:Troxipide
Примечания
- ↑ 1 2 3 Реестр лекарственных средств. Алфавитный список действующих веществ. Проверено 13 августа 2008.
- ↑ 1 2 3 ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора РФ. Поиск по базе данных лекарственных средств. Проверено 15 августа 2008.
- ↑ Кислотозависимые состояния у детей. Под ред. акад. РАМН В. А. Таболина. М., 1999, 120 с.
- ↑ 1 2 3 4 Калинин А. В. Кислотозависимые заболевания верхних отделов желудочно-кишечного тракта. Медикаментозная коррекция секреторных расстройств. Клинические перспективы в гастроэнтерологии и гепатологии. — 2002. — № 2. — С. 16–22.
- ↑ Bunney B. S., Chiodo L. A., Freeman A. S. Further studies on the specificity of proglumide as a selective cholecystokinin antagonist in the central nervous system. Annals of the New York Academy of Sciences. 1985;448:345-51.
- ↑ González-Puga C., García-Navarro A., Escames G., León J., López-Cantarero M., Ros E., Acuña-Castroviejo D. Selective CCK-A but not CCK-B receptor antagonists inhibit HT-29 cell proliferation: synergism with pharmacological levels of melatonin. Journal of Pineal Research. 2005 Oct;39(3):243-50. PMID 16150104.
- ↑ Yeo. M et all. The Novel Acid Pump Antagonists for Anti-secretory Actions with Their Peculiar Application Biyond Acid Suppression. J. Clin. Biobem. Nutr., 38, 1—8, Jan 2006.
- ↑ Коротько Г. Ф. Желудочное пищеварение. Краснодар, 2007. — 256 с. ISBN 5-93730-003-3.
- ↑ Евсеев М. А. НПВП–индуцированные гастродуоденальные язвы, осложненные кровотечением. Лекция. РМЖ, 2006, т. 15, № 16.
- ↑ 1 2 3 4 5 Исаков В. А. Терапия кислотозависимых заболеваний ингибиторами протонного насоса в вопросах и ответах. Consilium Medicum. 2006, №7, c 3-7.
- ↑ 1 2 Приворотский В. Ф., Луппова Н. Е. Кислотозависимые заболевания у детей (клиническая картина, диагностика, лечение). Учебное пособие. 2-ое изд. С-Пб., Издательский дом СПбМАПО, 2005.
- ↑ Поиск по базе данных ЛС, опции поиска: МНН — Мизопростол, флаги «Искать в реестре зарегистрированных ЛС», «Показывать лекформы». Обращение лекарственных средств. ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора РФ (27.03.2008). — Повторить поиск для энпростила, риопростила, арбапростила и тимопростила. Проверено 11 августа 2008.
- ↑ Реестр лекарственных средств. Простагландины, тромбоксаны, лейкотриены и их антагонисты.
- ↑ Реестр лекарственных средств. Фармакологический указатель. Сукральфат.
- ↑ 1 2 Бельмер С. В. Медикаментозная коррекция кислотозависимых состояний. Сукральфат. Кислотозависимые состояния у детей. Под ред. акад. РАМН В. А. Таболина. М., 1999, 120 с.
- ↑ Реестр лекарственных средств. Фармакологический указатель. Висмута трикалия дицитрат.
- ↑ 1 2 Потапов А. С., Пахомовская Н. Л., Дублина Е. С., Щербаков П. Л. Оценка эффективности и безопасности тройной эрадикационной терапии хеликобактериоза у детей препаратами хелол, де-нол и флемоксин солютаб. Альманах клинической медицины. 2006, том XIV, с. 87-94.
- ↑ Реестр лекарственных средств. Фармакологический указатель. Висмута субнитрат.
- ↑ Нижевич А. А., Щербаков П.Л., Кашников В. В., Татаринов П. А., Белоусов В.Б., Дюков И. В. Препараты висмута в детской гастроэнтерологии. Лечащий врач, 2007, № 6.
- ↑ Пахомова И.Г., Ткаченко Е.И., Успенский Ю.П. Первый в России опыт использования «Гевискона» в лечении гастроэзофагеальной рефлюксной болезни. РМЖ. 2007, том 15, № 22 с. 1639-1642.
- ↑ 1 2 Пасечников В. Д. Основные принципы проведения эрадикационной терапии при Helicobacter pylori-ассоциированных гастродуоденальных заболеваниях. Consilium-Medicum. Т. 4, №6, 2002.
- ↑ 1 2 Ивашкин В. Т., Лапина Т. Л. Лечение язвенной болезни: новый век — новые достижения — новые вопросы. Болезни органов пищеварения. — Том 4, № 1, 2002.
- ↑ Маев И.В., Кучерявый Ю. А., Пирогова А.И., Овсянникова Е. В. Эффективность париета в комплексной терапии обострения хронического панкреатита. Клинические перспективы гастроэнтерологии, гепатологии. № 3, 2003, с. 18-24.
- ↑ Калмыкова Е.А., Лучинкин И.Г., Сардаров Р.Ш., Силуянов С.В., Сохикян М.Б., Ступин В.А., Токарева Е.Ю. Инъекционные формы блокаторов желудочной секреции в профилактике рецидивов язвенных кровотечений. РМЖ, 2007, т. 15, № 29.
- ↑ Белоусова Е. А., Логинов А. Ф. Возможности блокаторов Н2-гистаминовых рецепторов в современной гастроэнтерологии. Consilium Medicum. Том 5, № 10, 2003.
- ↑ Гастроэнтерологический портал России. Язвенная болезнь желудка и 12-перстной кишки. Часть 2..
- ↑ Marshall Sittig. Pharmaceutical manufacturing encyclopedia. Acetoxolone Aluminum Salt. 1988 — Science. P. 19. ISBN 0815511442.
- ↑ Cheney G (1954). «Vitamin U concentrate therapy of peptic ulcer». American Journal of Gastroenterology 21 (3): 230–250. PMID 13138563.
- ↑ The Every Vitamin Page.
- ↑ Vitamins and minerals — names and facts
- ↑ Фармакологический информационный сайт Recipe. Гефарнат (Gefarnate).
- ↑ ФГУ «Научный центр экспертизы средств медицинского применения» Росздравнадзора РФ. Гефарнил.
- ↑ Gentium SpA. Sulglicotide.
- ↑ Belohlavek D., Malfertheiner P. The effect of zolimidine, imidazopyridine-derivate, on the duodenal ulcer healing. Scandinavian journal of gastroenterology. Supplement. 1979;54:44, PMID: 161649.
Wikimedia Foundation. 2010.
dic.academic.ru
инструкция по применению, показания и противопоказания.
Язвенная болезнь желудка поражает людей вне зависимости от их возраста, пола или социального статуса. Поэтому крайне важно иметь возможность решить проблему без серьезных побочных эффектов. Одним из таких решений можно считать висмута субцитрат, который не только уничтожает бактерию-возбудителя язвы желудка, но и защищает его поверхность, образуя на ней пленку.
Фармакологическое действие
Основное действие препарата направлено на устранение инфицирования бактерией хеликобактер пилори, вызывающей на поверхности желудка и двенадцатиперстной кишки язвы и эрозии. Кроме того, в кислой среде желудка висмута субцитрат образует защитную пленку, предохраняющую желудок от повреждений.
Помимо этого, он способствует активизации собственных цитопротекторных механизмов, увеличивает синтез простагландинов и бикарбонатов. В результате после приема препарата не только устраняется причина язвы, но и усиливается защита ЖКТ. Для преобразования висмута в защитную пленку обязательна сильнокислая среда желудочного сока.
Показания
Основное показания для приема висмута субцитрата — язвенная болезнь желудка и двенадцатиперстной кишки, вызванная влиянием бактерии хеликобактер пилори. Также препарат показан для приема при гастритах (как ассоциированных с бактериальной инфекцией, так и нет), наружно при кожных заболеваниях и экземах.
Препарат хорошо показал себя в терапии воспалений ЖКТ, появившихся из-за долгого приема лекарств из группы нестероидных противовоспалительных препаратов.
Введение препаратов с висмутом в терапевтическую схему помогает также улучшить общие защитные функции желудка при наличии у пациента риска развития повреждений.
При лечении язвы желудка и двенадцатиперстной кишки медикаментами препарат входит как в состав набора для комплексной терапии заболевания, так и используется как монопрепарат. Однако рекомендуется, все же, комбинировать его с другими средствами. Это повысит шанс на быстрое излечение.
Инструкция по применению
Согласно инструкции по применению субцитрата висмута, кратность приема таблеток зависит от возраста пациента. Взрослому необходимо принимать по таблетке четырежды в день, тогда как ребенку от 8 до 12 лет — по таблетке дважды в день.
После приема следует запить таблетку водой в небольшом количестве. Продолжительность курса приема составляет от 4 до 8 недель, после чего нужно сделать не менее 8 недель перерыва, во время которого не рекомендуется принимать препараты, содержащие висмут.
При наличии повреждений, вызванных хеликобактер пилори, лекарства с висмутом используются в составе комбинированной терапии и применяются строго по схеме: 1 таблетка висмута субцитрата дважды в день, 1 таблетка кларитромицина дважды в день и 1 таблетка амоксициллина дважды в день. Также в терапии рекомендуется использовать ингибиторы протонной помпы. Благодаря такой форме лечения препараты висмута способствуют максимальной защите желудка и двенадцатиперстной кишки.
После успешно пройденного лечения следует продолжить прием препарата висмута, чтобы исключить вероятность рецидива и предохранить желудок от возможных повреждений. Применение лекарственного средства желательно ограничить 6 неделями, так как длительный прием лекарственного средства может вызывать негативные побочные эффекты.
Противопоказания
Несмотря на то, что висмута субцитрат считается безопасным лекарственным препаратом, его не следует принимать пациентам с диагностированными нарушениями функций почек. Также необходимо по возможности заменить лекарственное средство, если пациент младше 14 лет. При беременности или кормлении грудью применение лекарственного средства разрешено с осторожностью.
Аналоги
Висмута субцитрат представлен на фармацевтическом рынке такими препаратами, как «Де-Нол», «Вис-Нол». Также сходными по действию являются препараты из группы антацидов, так как они также обеспечивают защиту желудка при помощи пленки на его внутренней поверхности. К ним относятся препараты «Альмагель», «Маалокс», «Ренни» и многие другие.

Особые указания
Применение может вызывать окрашивание кала в черный цвет. Висмута субцитрат и аналоги требуют исключения из рациона жидкости и пищи, способствующей снижению кислотности желудочного сока, а также антацидных препаратов. Делается это потому, что кислый желудочный сок необходим препарату для формирования защитной пленки для гастропротекторного действия.
Крайне нежелательно долгое (более двух месяцев) применение препарата, так как существует риск развития энцефалопатии. Однако подобный эффект является маловероятным при соблюдении верных дозировок.
Существует небольшая вероятность развития побочных эффектов, мешающих концентрации и вниманию, поэтому следует с осторожностью подходить к управлению транспортными средствами во время лечения препаратами, содержащими висмут.
При приеме какого-либо медикамента с висмутом следует воздерживаться от применения других средств, содержащих то же вещество. Применение нескольких аналогов может повлечь за собой повышение количества висмута в крови и, как следствие, риска развития нежелательных побочных эффектов, в том числе и воздействия на нервную систему.
fb.ru
Схемы антихеликобактерной терапии на основе коллоидного субцитрата висмута (Де-Нола)
В.А. Исаков
МОНИКИ, г. Москва
В настоящее время существуют два направления в лечении заболеваний, ассоциированных с Н. pylori: использование схем тройной терапии на основе блокаторов протонного насоса и тройной или квадро-терапии на основе коллоидного субцитрата висмута (Де-Нола). К настоящему времени опубликовано значительное число работ, свидетельствующих, что эффективность схем лечения на основе препаратов висмута эквивалентна таковой на основе блокаторов протонного насоса [1-3]. Конечный результат терапии зависит в основном от антибиотиков, входящих в схему лечения, и резистентности штаммов Н.pylori к ним в данной конкретной популяции.
Wink de Boer в своей передовой статье в Европейском журнале гастроэнтерологии и гепатологии справедливо отмечал, что «тройная терапия на основе препаратов висмута, пожалуй, наиболее широко используется в мире, так как это единственная эффективная антихеликобактерная терапия, доступная по экономическим соображениям в развивающихся странах мира, в которых сосредоточено большинство населения планеты» [4]. В связи с этим неудивительно, что схемы на основе препаратов висмута входят наряду со схемами на основе блокаторов протонного насоса в национальные рекомендации по лечению Н. pylori-ассоциированных заболеваний многих развивающихся стран. Следует также отметить, что наиболее интересные и впечатляющие результаты по использованию схем антихеликобактерной терапии, не содержащих производные нитроимидазола, были получены при применении в качестве базисного препарата солей висмута.
Так, успешно в сочетании с коллоидным субцитратом висмута и различными антибиотиками был использован фуразолидон [5-8]. В целом, учитывая, что проблема резистентных штаммов Н.pylori не решена, было бы разумным расширить спектр схем лечения первой линии с использованием двух базисных препаратов — блокатора протонного насоса или препарата висмута, а не ограничиваться использованием препарата висмута только в квадро-терапии, как предлагают авторы Маастрихтского соглашения-2, принятого в октябре 2000 года в Риме. В нем квадро-терапия (классическая тройная терапия — висмут + тетрациклин + метронидазол с добавлением блокатора протонного насоса) остается терапией второй линии, или резервной. В случае ее неудачи дальнейшая терапия должна определяться индивидуально.
С нашей точки зрения, в таких случаях разумнее использовать схемы лечения, содержащие резервные антибиотики, и в этом смысле более широкие возможности представляют схемы на основе препарата висмута (табл.
1), так как из схем на основе блокаторов протонного насоса используется лишь ограниченный спектр антибиотиков (производные нитроимидазола, макролиды и синтетические пенициллины). Схемы на основе Де-Нола дают большую гибкость врачу в составлении схем терапии, так как помимо указанных выше антибиотиков с ним удачно сочетаются тетрациклин и фуразолидон — антибиотики, к которым резистентность у Н.pylori вырабатывается медленно.Из нерешенных проблем применения схем на основе Де-Нола следует отметить, что использование таких антибиотиков, как тетрациклин и фуразолидон в высших суточных дозировках, которые рекомендуются к использованию, в настоящее время сопряжено с выраженными побочными действиями, поэтому следует определить оптимальные дозы указанных антибиотиков, что, безусловно, будет задачей контролируемых клинических исследований. В пользу того, что такие схемы лечения, безусловно, можно оптимизировать, свидетельствует тот факт, что в схемах Де-Нол + тетрациклин + метронидазол удавалось снижать дозу тетрациклина без ущерба для эрадикации, но побочные действия уменьшались значительно [9].
Приведенные данные свидетельствуют, что антихеликобактерная тройная терапия с препаратом Де-Нол остается одной из наиболее широко использующихся в настоящее время, а с новыми модификациями схем лечения будет связан прогресс в лечении больных с заболеваниями, ассоциированными с Н.pylori, особенно инфицированных штаммами Н.pylori, резистентными к производным нитроимидазола или макролидам.
Таблица 1. Схемы на основе коллоидного субцитрата висмута (Де-Нола)
Базисный препарат Антибактериальные препараты Коллоидный субцитрат
висмута (Де-Нол)
240 мг 2 раза в сутки тетрациклин 2000 мг/сут +
метронидазол (тинидазол) 1000-1600 мг/сут
или
амоксициллин 2000 мг/сут +
метронидазол (тинидазол) 1000-1600 мг/сут
или
амоксициллин 2000 мг/сут +
кларитромицин 500 мг/сут
или
кларитромицин 500 мг/сут +
метронидазол 1000-1600 мг/сут
или
амоксициллин 2000 мг/сут +
фуразолидон 400 мг/сут
или
кларитромицин 500 мг/сут +
фуразолидон 400 мг/сут
Литература
1. van der Hulst R.W., Keller J.J., Rauws E.A., et al. Treatment of
Helicobacter pylori infection: a review of the world literature. //
Helicobacter. — 1996. -Vol. 1. -P.6-19.
2. Unge P. Review of Helicobacter pylori eradication regimens. // Scand J
Gastroenterol. — 1996. -Vol.215 (Suppl.215.) -P.74-81.
3. Wang W. H., Wong B.C. Lam S.K. Pooled analysis of Helicobacter pylori
eradication regimes in Asia // J Gastroenterol Hepatol. — 2000. — Vol.15. — P.
1007-1017.
4. de Boer W.A. Bismuth triple therapy: still a very important drug regimen for
curing Helicobacter pylori infection//EurJ Gastroenterol Hepatol. — 1999. -Vol.
11. -P.697-700
5. Segura A.M., Gutierrez O., Otero W. et al. Furazolidone, amoxycillin, bismuth
triple therapy for Helicobacter pylori infection // Alimentary Pharmacology and
Therapeutics. — 1997. — Vol.11. — P.529-532.
6. Абдулхаков P.A., Гриневич В.Б., Иваников И.О. и др. Схемы тройной терапии
язвенной болезни луковицы двенадцатиперстной кишки на основе препарата Де-Нол
(Результаты мультицентрового исследования). — Российский журнал
гастроэнтерологии, гепатологии, колопроктологии. — 2000. — Том X. — N2. —
С.26-30
7. Liu W.Z., Xiao S.D., Shi Y. et al. Furazolidone-containing short-term triple
therapies are effective in the treatment of Helicobacter pylori infection //
Aliment Pharmacol Ther. — 1999. -Vol.13. -P.317-322
8. Xiao S.D., Liu W.Z., Hu P.J. et al. High cure rate of Helicobacter pylori
infection using tripo-tassium dicitrato bismuthate, furazolidone and
clarithromycin triple therapy for 1 week // Aliment Pharmacol Ther. — 1999.
-Vol. 13. -P.311-315
9. Roghani H.S., Massarrat S., Pahlewanzadeh M.R., Dashti M. Effect of two
different doses of metronidazole and tetracycline in bismuth triple therapy on
eradication of Helicobacter pylori and its resistant strains // Eur J
Gastroenterol Hepatol. — 1999. -Vol.11. — P.709-712.
Источник: http://medi.ru
www.medcentre.com.ua
коллоидный+субцитрат+висмута — с английского на русский
1. растворение 2. растворaddition solid solution твёрдый раствор внедрения
aggressive solution агрессивный раствор
buffer solution буферный раствор, буфер
Clerici solution раствор Клеричи
colloidal solution коллоидный раствор, золь
complete solution совершенный раствор
conjugate solutions сопряжённые растворы
cotectic solution котектический раствор
defect-lattice solid solution кристалл, в котором не завершено заполнение некоторых атомных позиций
differential solution внутрипластовое растворение
equilibrium solution равновесный раствор
gravity solution тяжёлый раствор
growth solution раствор выращивания, раствор роста
Hoyer’s solution раствор Хойера
hydrosaline solution водный раствор большой солёности
ideal solution идеальный раствор
incongruent solution инконгруэнтное растворение
interstitial solid solution твёрдый раствор внедрения
intrastratal solution внутрипластовое растворение
Klein solution раствор Клейна (тяжёлая жидкость)
Lemberg solution раствор Лемберга
meteoric solution метеорный раствор
omission solution раствор вычитания
omission solid solution см. defect-lattice solid solution
ore solution рудный раствор
original solution исходный [начальный] раствор
perfect solution идеальный раствор
phreatic solution фреатическое растворение (ниже зеркала грунтовых вод)
pressure solution растворение под давлением
soil solution почвенный раствор, жидкая фаза почвы
solid solution твёрдый раствор
Sonstadt solution жидкость Туле
substitution solid solution s твёрдые растворы замещения
supergene solution супергенный раствор
supersaturated solution пересыщенный раствор
Sushin solution жидкость Сушина
Thoulet solution жидкость Туле
vadose solution вадозное растворение
* * *
translate.academic.ru
