Воспаление желчного пузыря. Причины. Диагностика. Лечение.
Что такое воспаление желчного пузыря
Воспалительное заболевание, характеризующееся протеканием патологических процессов в слизистой плеве желчного пузыря, чаще всего попадается в пожилом возрасте после 50-60 лет. Воспаление желчного пузыря наиболее распространено среди женщин, нежели пациентов мужского пола. Согласно статистике, на втором месте среди общих хирургических патологий занимает именно данная болезнь.
Симптомы воспаления желчного пузыря:
Зачастую, проявление симптомов у каждого больного происходит индивидуально, однако к наиболее распространенным относят:
- тупые сильные боли, локализующиеся справа под ребрами;
- горечь во рту и отрыжка;
- расстройства стула всевозможных проявлений;
- тошнота, реже рвота;
- преобладание в оттенке лица желтого цвета;
- повышение температуры тела до 39, сопровождающееся ознобом;
- стремительные изменения в весе;
- головные боли.

Если наблюдаются повышенные физические нагрузки, застолья, сопровождающиеся поеданием жирной пищи в больших количествах, употребление алкоголя, а также психические и эмоциональные расстройства, это приводит к усилению болевых вспышек.
Консультацию можно получить по телефону: +7(495) 961-27-67
Причины возникновения заболевания
К появлению и дальнейшему развитию воспалительных процессов зачастую приводят паразитирования на слизистой, то есть условно-патогенные проявления микрофлоры, которые активизируются при ослаблении иммунитета. Попадая из кишечника в желчный пузырь лямблии, аскариды, кишечные палочки или бактерии, вызывают начало протекания воспаления.- Пародонтоз.
- Заболевания дыхательной системы, типа синусита.
- Воспалительные процессы в ЖКТ: аппендицит, дисбактериоз.
- Простатит или женская форма аднексит.

- Инфекции мочевыводящих путей.
- Вирусные образования в печени.
- Наличие паразитов в желчевыводящих путях.
Существуют также второстепенные причины воспаления желчного пузыря:
- возрастные изменения;
- генетическая отягощенная предрасположенность;
- обменные нарушения;
- застой желчи;
- диетические злоупотребления, в том числе переедание и нарушение режима;
- малоподвижный способ жизнедеятельности;
- гормональные сбои, беременность, прием гормонов;
- наличие иммунодефицита;
- хронические инфекции.
Диагностирование болезни
Выявление заболевания начинается с традиционной пальпации и внешнего осмотра на наличие желтушности и прочих кожных проявлений. Кроме этого врач выпишет направление на:
Если данных исследований будет недостаточно для постановки диагноза, наш специалистпредложит пройти дополнительную диагностику, результаты которой позволят максимально точно увидеть состояние желчного пузыря:
- Радиоизотопное сканирование.

- Рентген.
- Дуоденальное зондирование.
Методы лечения болезни
Излечение воспалительных процессов без сочетания различных видов лечения остается маловероятным, поэтому помимо консервативного метода,применять диету, а также вспомогательные методики.
На первоочередном месте стоит строгое следование режиму питания и диете, которая включает в себя прием продуктов, обработанных паровым способом, либо же варкой. Диета носит щадящий характер, потому как соединяет оптимальное число углеводов и белком, с минимальным количественным составом жиров, соли, клетчатки и холестерина. Происходит также разделение приема пищи на порции, до шести раз в сутки.
Что касается медикаментозного сопровождения, то наши врачи выделяют данные направления терапии:
-
прием спазмолитиков;
-
если наблюдается присутствие инфекционных паразитов, то назначение антибиотиков;
-
определяются противовоспалительные рекомендации;
-
дезинтоксикация и дегельминтизация;
-
антиоксидантная практика при кризовых ситуациях;
-
восстановление иммунитета;
-
приведение в нормальное функционирование функций желчевыводящих путей.

Такая терапия оптимальна для лечения не острых форм заболевания, а лечение воспаления желчного пузыря при острых болях и коликах происходит с применением хирургического вмешательства или литотрипсии.
Консультацию можно получить по телефону: +7(495) 961-27-67
Почему же наши гастроэнтерологи лучше других?
-
Знания и опыт врачей нашей клиники позволяют добиться поразительных успехов в лечении гастроэнтерологических заболеваний.
-
В Клинике Здоровья самое современное диагностическое оборудование, которое позволяет поставить точный диагноз и начать лечение.
-
Расположение в самом центре Москвы, в шаговой доступности от двух станций метро.
-
Привлекательные цены
-
Удобное время для посещения врача.

Мы работаем для того, что бы вы были здоровы.
Консультацию можно получить по телефону: +7(495) 961-27-67
Холецистит: признаки, как лечат | МРТ Эксперт
С патологией желчевыводящих путей современной медицине приходится сталкиваться довольно часто. И число таких заболеваний продолжает расти. Сегодня мы поговорим о холецистите: что это за заболевание, каковы его симптомы, причины появления, как его выявляют и лечат.
— Николай Борисович, есть данные, что сегодня холециститом страдает 10-20 % взрослого населения, и отмечается тенденция к дальнейшему росту этой патологии. Расскажите, пожалуйста, что она собой представляет?
— Если одной фразой, то холецистит – это воспаление желчного пузыря. Патология желчевыводящих путей остается актуальной проблемой для сегодняшней медицины.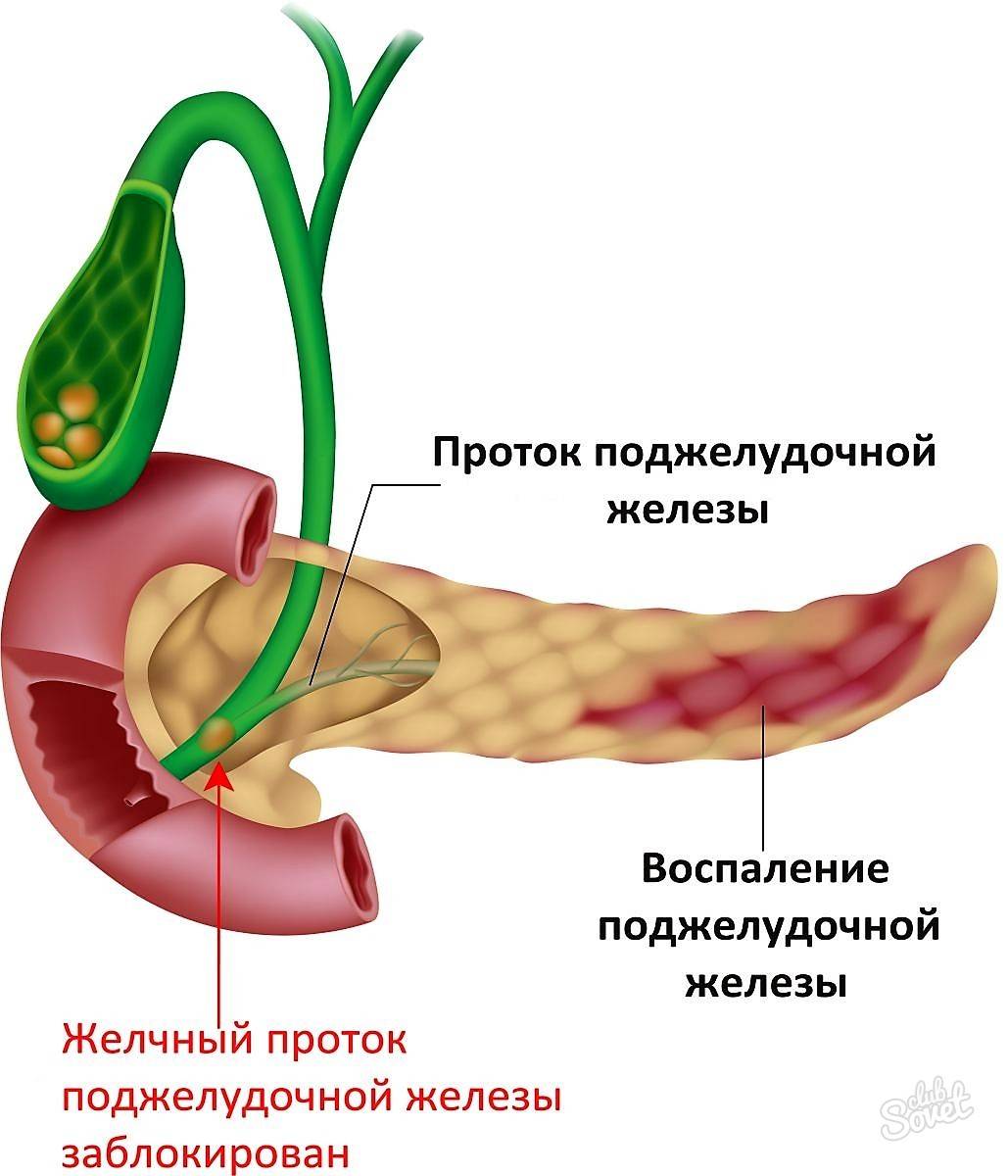 Да, тенденция к росту заболеваемости есть. Более того: по прогнозам учёных число заболеваний пищеварительной системы (куда относится и патология желчевыводящих путей) в ближайшие 15-20 лет вырастет в мире на 30-50 %.
Да, тенденция к росту заболеваемости есть. Более того: по прогнозам учёных число заболеваний пищеварительной системы (куда относится и патология желчевыводящих путей) в ближайшие 15-20 лет вырастет в мире на 30-50 %.
— Какие виды холецистита известны современной медицине?
— Их два: острый и хронический холецистит. Первый развивается быстро, на фоне полного благополучия. Появляется болевой синдром в животе, боль локализуется в правом подреберье. Может появиться тошнота, рвота, может повыситься температура. Как правило, острый холецистит наиболее часто является проявлением желчнокаменной болезни. Такие больные госпитализируются по линии скорой помощи в хирургический стационар.
Подробнее о желчнокаменной болезни читайте здесь: Удалить или оставить? Что делать, если обнаружены камни в желчном пузыре?
Хронический холецистит изначально развивается как самостоятельный процесс, исподволь, незаметно. Зачастую диагноз «холецистит» пациенту ставят при обследовании по поводу совершенно других заболеваний.
Надо учитывать и то, что болезням желчного пузыря и желчевыводящих путей свойственно разнообразие клинических проявлений, длительность течения, затяжные обострения – это обуславливает частую обращаемость за медицинской помощью, делает эти недуги социальной проблемой.
— Каковы причины холецистита? Из-за чего он возникает?
— В развитии этой патологии участвуют различные факторы. На первое место я бы поставил нарушение сократительной функции желчного пузыря. Это приводит к застою желчи, замедлению её эвакуации из желчного пузыря. Чаще всего на сократительную функцию желчного пузыря влияют психоэмоциональные перегрузки, невротические реакции и длительные стрессовые ситуации, гиподинамия.
Имеет значение и инфекционный фактор. Инфекционные агенты проникают в желчный пузырь из хронических очагов воспаления в организме – например, при болезнях ЛОР-органов, желудка, двенадцатиперстной кишки, из других отделов кишечной трубки.
Вносят свою лепту в развитие холецистита и глистные инвазии – скажем, описторхоз.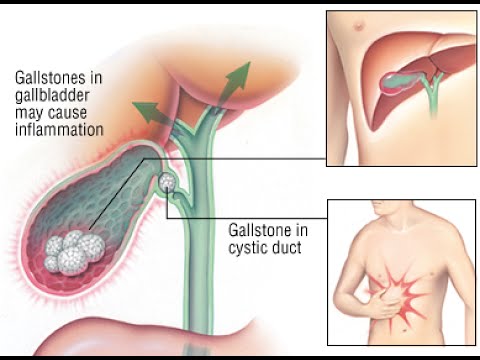
Также это заболевание могут спровоцировать забросы сока поджелудочной железы в полость желчного пузыря – возникает так называемый химический ожог слизистой желчного пузыря, что может привести к его воспалению.
Читайте материалы по теме:
Как уберечься от болезни Боткина?
Существует ли прививка от стресса?
Детство – для движения! К чему приводит гиподинамия?
— Расскажите, пожалуйста, о признаках холецистита. Как он проявляется?
— Холецистит может протекать с разной степенью тяжести. От этого, а также от стадии заболевания, будут зависеть симптомы. В первую очередь, патология проявляется болевым синдромом. Возникают эти боли за счёт спазма желчного пузыря или за счёт его растяжения.
Боль появляется в правом подреберье, как правило, через 40 минут – 1,5 часа после погрешности в диете (например, при употреблении острой, жирной пищи, жареных блюд, переедании).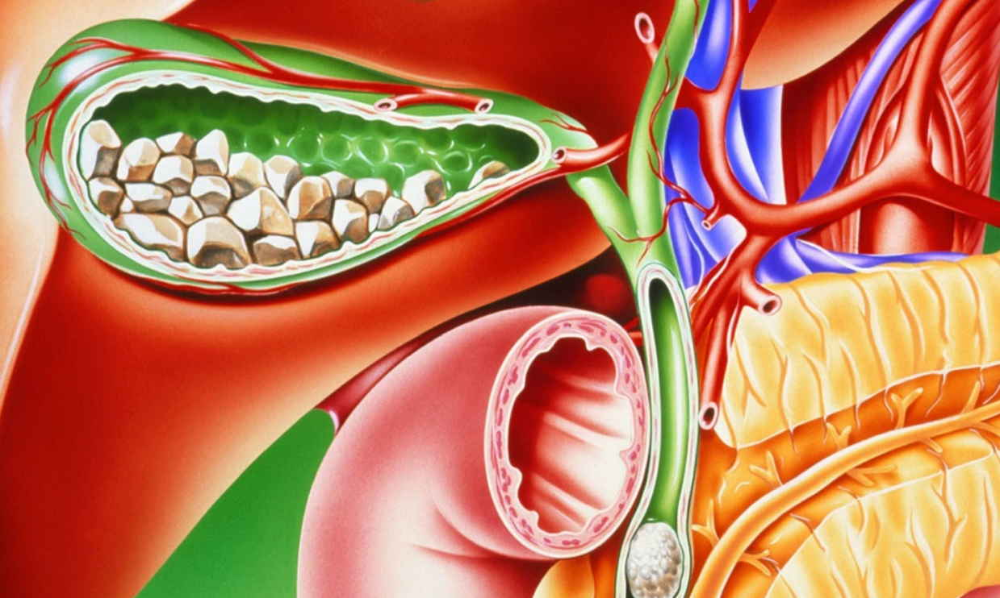 Боль ощущается примерно полчаса и при лёгкой форме проходит самостоятельно. При тяжёлых формах боли носят более интенсивный и длительный характер.
Боль ощущается примерно полчаса и при лёгкой форме проходит самостоятельно. При тяжёлых формах боли носят более интенсивный и длительный характер.
Ещё боль может провоцироваться длительным пребыванием человека в положении сидя – за рулём автомобиля, за компьютером. Из правого подреберья такие боли могут отдавать вверх – в правое плечо, шею, правую лопатку.
Кроме болевого синдрома, пациента могут беспокоить так называемые диспепсические расстройства: отрыжка, тошнота, металлический привкус во рту, иногда рвота (если она возникает неоднократно, в ней может появиться желчь). Могут наблюдаться вздутие живота, чередование запоров и поносов.
Также холецистит может сопровождаться раздражительностью, бессонницей, снижением работоспособности.
Чем тяжелее форма холецистита, тем ярче и длительнее будут выражены перечисленные симптомы.
— А бывает бессимптомный холецистит? То есть человека ничего не беспокоит, и болезнь выявляется только при проведении каких-либо диагностических исследований – например, в рамках профилактического обследования
— Да, такое бывает.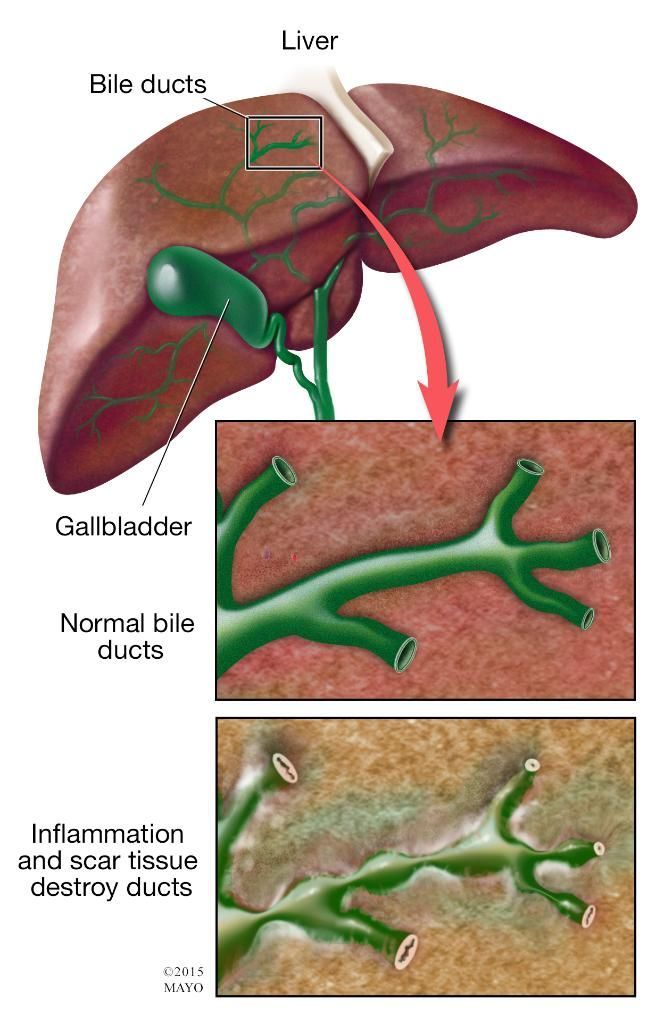 В 50 % случаев холецистит протекает скрыто, бессимптомно. На признаки патологии желчного пузыря до клинических проявлений заболевания могут указывать только данные ультразвукового исследования. Поэтому это исследование надо обязательно включать в программу обследования заболеваний пищеварительной системы.
В 50 % случаев холецистит протекает скрыто, бессимптомно. На признаки патологии желчного пузыря до клинических проявлений заболевания могут указывать только данные ультразвукового исследования. Поэтому это исследование надо обязательно включать в программу обследования заболеваний пищеварительной системы.
Кроме того, существуют атипичные клинические формы, которые могут вводить врача в заблуждение, симулируя различные заболевания других органов и систем, например, сердечно-сосудистой, эндокринной и других (так называемые «маски»). А когда начинаем разбираться, выясняется, что речь идёт о патологии именно желчного пузыря. Наиболее известна и изучена так называемая кардиальная маска холецистита (или холецисто-кардиальный синдром): каждый третий-второй больной холециститом может жаловаться на проблемы с сердцем. Это учащённое сердцебиение, одышка, боли в области сердца. Электрокардиограмма у таких больных без каких-либо отклонений.
Холецистит также может протекать под маской патологии щитовидной железы – здесь жалобы пациента будут как при тиреотоксикозе (раздражительность, чрезмерная потливость, то же учащённое сердцебиение, дрожание пальцев рук, повышение температуры тела до значений 37-37,5 градуса). При этом щитовидная железа может оказаться несколько увеличенной, и здесь надо разбираться, вызваны ли симптомы именно её патологией, или проблема всё же в желчном пузыре.
При этом щитовидная железа может оказаться несколько увеличенной, и здесь надо разбираться, вызваны ли симптомы именно её патологией, или проблема всё же в желчном пузыре.
Ещё у холецистита может быть аллергическая маска, и ряд других. Чтобы разобраться в этом, врач должен обладать немалым практическим опытом, правильно выстроить диагностический поиск.
— Давайте поговорим о диагностике холецистита. Что в неё входит? Как доктор может обнаружить эту патологию?
— Сегодня самый доступный и распространённый метод диагностики холецистита – это УЗИ брюшной полости. Ультразвуковая диагностика позволяет оценить состояние стенок желчного пузыря: если они утолщены более чем на 4 мм, это уже явный признак холецистита, если меньше – возможно, патология только в начале развития. Врач оценивает также сократительную способность желчного пузыря.
УЗИ поможет выявить и камни в желчном пузыре. Если они обнаружены и также имеется холецистит, то говорят о каменном (калькулёзном) холецистите.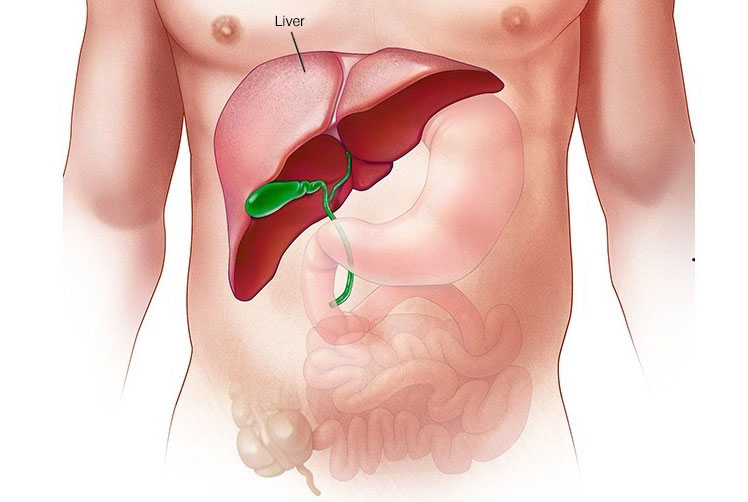
Записаться на УЗИ органов брюшной полости можно здесь
ВНИМАНИЕ: услуга доступна не во всех городах
Есть и другие методы исследования. Например, зондирование двенадцатиперстной кишки (дуоденальное зондирование). Оно позволяет оценить биохимический состав желчи, посеять её на наличие инфекции и выявить микробы, которые вызывают воспаление в желчном пузыре.
— Чем могут помочь врачи пациенту с этим недугом? Как лечат холецистит?
— Помочь мы можем только после того, когда в ходе полноценного обследования максимально полно выясним все причины, которые привели к появлению у пациента холецистита. Программа лечения строится следующим образом. На первом месте – лечебное питание. Прежде всего, это дробный приём пищи, пять-шесть раз в день. Желчный пузырь «любит», чтобы пищу мы принимали в одни и те же часы: этим мы его тренируем и предупреждаем застой желчи в нём. Важно, чтобы пища была не в горячем или холодном виде, а в тёплом.
Подбор лекарственных препаратов осуществляется с учётом функции желчного пузыря, в частности, его сократительной способности. Если функция повышена, если присутствуют резкие спастические боли, рекомендуются препараты спазмолитического действия. Когда при нормальной сократительной функции органа мы находим признаки вязкой, застойной желчи, используются средства с желчегонным действием.
Если исследования показывают плохую сократимость пузыря, тогда в программу лечения включаются препараты, стимулирующие его функцию, помогающие ему работать правильно.
В определённых случаях используются противопаразитарные, антибактериальные, противовоспалительные средства. Всё это решает доктор, в зависимости от результатов исследования.
Не будем забывать и о других методах лечения холецистита – о том же санаторно-курортном. Хроническим больным надо хотя бы года три-четыре подряд ездить на курорты – как раньше говорили, «на воды». Это очень полезно. Но ехать туда надо со всеми медицинскими документами, тогда пациенту там правильно подберут диету, режим приемы воды (её тип, количество и температурный режим).
— Что можно есть при холецистите, а что нельзя?
— Белков, жиров и углеводов должно быть ровно столько, сколько необходимо для нормального функционирования организма. В рацион следует включать нежирные сорта мяса (говядина, крольчатина), рыбу (лучше отварную или приготовленную на пару), обезжиренный творог, пшеничные отруби. Среди круп предпочтение отдаётся овсяной и гречневой.
Не будем забывать о свежих овощах и фруктах (лучше пусть это будут дыня, тыква, арбуз, морковь, яблоки).
Исключаются жирные, жареные блюда, копчёности, маринады, соленья, спиртные напитки, включая пиво. В этот же список включаем газированные напитки, острые приправы и яичные желтки (последние – на период обострения).
Не помешают разгрузочные дни (1-3 в неделю): это могут быть рисово-компотные, творожные, арбузные дни. Кроме того, рекомендуется обильное питьё.
— Как предотвратить развитие холецистита? Расскажите, пожалуйста, о профилактике
— Наверное, многое понятно уже из вышесказанного. Основная профилактика мало отличается от профилактики многих других заболеваний. Это здоровый образ жизни, рациональное питание – едим часто, не на бегу, пищу пережёвываем тщательно, не спеша.
Основная профилактика мало отличается от профилактики многих других заболеваний. Это здоровый образ жизни, рациональное питание – едим часто, не на бегу, пищу пережёвываем тщательно, не спеша.
Согласитесь, казалось бы, простые, прописные истины. Но, поверьте, прежде всего именно они важны в плане профилактики холецистита.
Беседовал Игорь Чичинов
Если вам нужна консультация врача-гастроэнтеролога, записаться на приём можно здесь
ВНИМАНИЕ: услуга доступна не во всех городах
Редакция рекомендует:
Дискинезия желчевыводящих путей: что скрывается за этим диагнозом?
Отчего люди желтеют?
МРТ печени: за и против
Для справки:
Патрушев Николай Борисович
Врач-гастроэнтеролог, кандидат медицинских наук
Выпускник Пермского государственного института 1988 г.
Первичная специализация по гастроэнтерологии – 1995 г.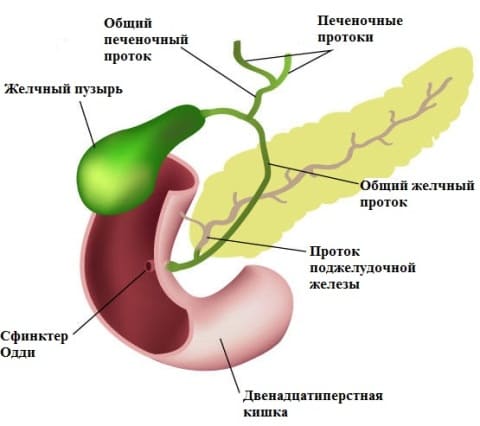
С 2005 по 2014 гг. работал в Центральном научно-исследовательском институте гастроэнтерологии (г. Москва). Сначала – врач отделения хронических заболеваний печени, затем заведующий консультативно-диагностическим отделением института.
С 2020 г. – врач-гастроэнтеролог в «Клиника Эксперт» Пермь.
Принимает по адресу: г. Пермь, ул. Монастырская, 42а.
Статьи медицинского центра в Краснодаре
Выделяют острый и хронический холециститы. Калькулезный (с наличием камней) и некалькулезный. Причинами могут быть: недостаточное употребление жидкости, эндокринные нарушения, генетическая предрасположенность, беременность, прием эстрогенов (контрацептивов), не правильное питание (прием большого количества жирной и жареной пищи) или голодание, малоподвижный образ жизни, анатомические особенности желчного пузыря, прием некоторых препаратов, а так же врожденные нарушения обмена веществ. Женщины болеют этим заболеванием чаще.
В механизме развития холецистита играет большую роль нарушение функции желчного пузыря, нарушение состава желчи (много холестерина и мало желчных кислот), сопутствующие воспалительные заболевания органов желудочно-кишечного тракта (панкреатит, дуоденит, дисбиозы, патология кишечника и т. д). До появления камней – образуется «песок» в желчном пузыре, а, в последствие – камни. Существуют 3 вида камней: холестериновые, пигментные, смешанные.
д). До появления камней – образуется «песок» в желчном пузыре, а, в последствие – камни. Существуют 3 вида камней: холестериновые, пигментные, смешанные.
Простым, доступным и точным методом диагностики камней в желчном пузыре и состояния желчевыводящих протоков является ультразвуковое исследование (УЗИ). Метод позволяет определить работу желчного пузыря, его размеры, наличие воспалительных изменений и размер камней. Применяется у всех пациентов без исключения, не противопоказан при беременности (II-III триместр). Так же существуют другие методы диагностики: магниторезонансная томография, компьютерная томография, ретроградная холангиопанкреатография (при попадании камней в желчные протоки), холецистография.
Жалобы пациента с острым холециститом и при обострении желчнокаменной болезни, очень похожи: боли или тяжесть в правом подреберье, боль может отдавать в правую руку, лопатку, спину. Провоцирующим фактором может являться погрешность в питании, нервный стресс, тяжелые физические нагрузки.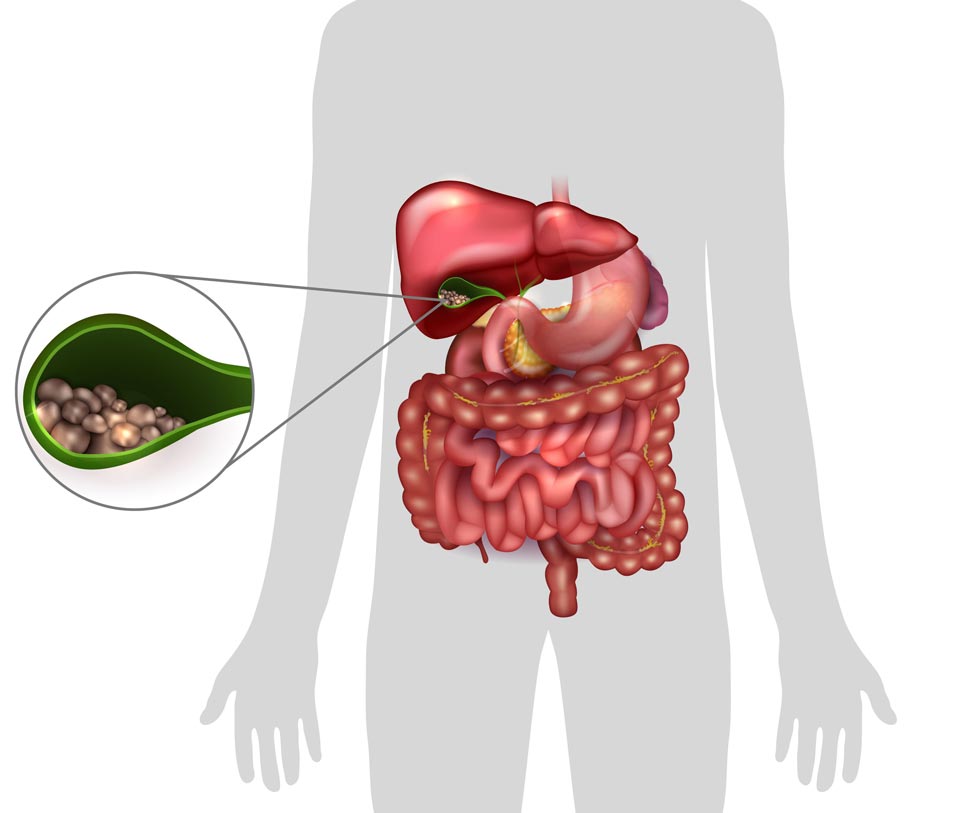 Так же симптомами обострения болезни могут быть тошнота, рвота, иногда повышение температуры тела (чаще при развитии осложнений), вздутие и отрыжка, чувство тяжести или распирания в желудке, желтуха (осветленный стул, темная моча).
Так же симптомами обострения болезни могут быть тошнота, рвота, иногда повышение температуры тела (чаще при развитии осложнений), вздутие и отрыжка, чувство тяжести или распирания в желудке, желтуха (осветленный стул, темная моча).
В общем анализе крови — повышение количества лейкоцитов, повышение скорости оседания эритроцитов (СОЭ), в биохимических анализах — повышение биллирубина, печеночных проб.
Острый некалькулезный холецистит лечится, как правило, консервативно амбулаторно или в дневном стационаре, врачами хирургами и гастроэнтерологами, если не возникли осложнения.
К осложнениям холецистита относятся: гангрена, эмпиема, водянка, абсцессы, перфорация желчного пузыря, перитонит и сепсис, требующие безотлагательной помощи хирурга и проведению холецистэктомии (удаление желчного пузыря).
Основным методом лечения хронического калькулезного холецистита и осложнений острых состояний является холецистэктомия. В современных клиниках используется малоинвазивное вмешательство – лапароскопическая холецистэктомия, в том числе из одного доступа, что менее травматично для организма пациента, позволяет быстрее вернуться к привычному образу жизни и сохраняет эстетику кожи живота.
В современных клиниках используется малоинвазивное вмешательство – лапароскопическая холецистэктомия, в том числе из одного доступа, что менее травматично для организма пациента, позволяет быстрее вернуться к привычному образу жизни и сохраняет эстетику кожи живота.
После проведения лапароскопической холецистэктомии пациент проводит в среднем 1-2 дня в стационаре и выписывается с рекомендациями по питанию, привычный образ жизни не меняется. Оперативное лечение, проведенное высококвалифицированными специалистами, современным хирургическим оборудованием, круглосуточное наблюдение заботливых врачей и медицинского персонала позволяет достичь максимальных результатов, без осложнений в послеоперационном периоде. Лапароскопические операции в срочном порядке — проводятся при обострении хронического калькулезного холецистита, острого холецистита и его осложнений. В случае серьезных тяжелых нарушений и состояния пациента, для снижения риска послеоперационных осложнений первично проводится дренирование желчевыводящих путей и желчного пузыря для снятия острого воспаления и в дальнейшем – проведения плановой лапароскопической холецистэктомии.
Своевременное обращение и диагностика заболеваний желчного пузыря позволяет каждому пациенту сохранить высокий уровень качества жизни и продолжить привычную активность.
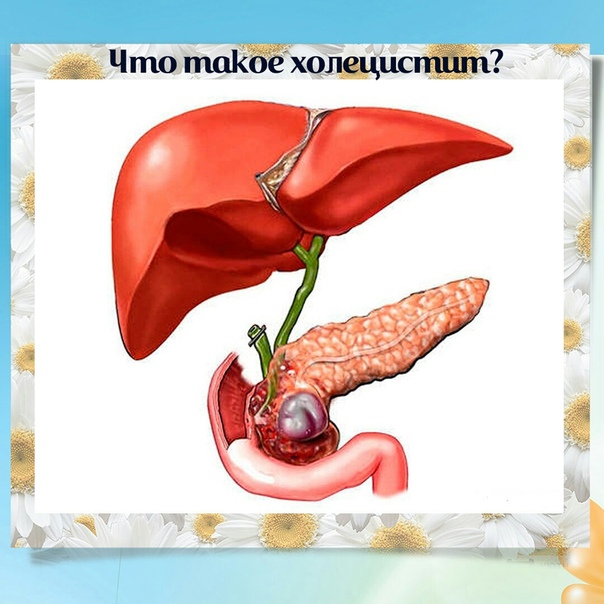
Холецистит, симптомы — Клиника Здоровье 365 г. Екатеринбург
Холецистит — воспаление желчного пузыря. К признакам и симптомам холецистита относятся:
- сильная непрерывная боль в верхней части брюшной полости, которая без медицинского вмешательства может длиться на протяжении нескольких часов и даже дней и усиливаться при глубоком дыхании;
- боль распространяется от брюшной полости до правого плеча или спины;
- болезненные ощущения при надавливании на брюшную полость;
- потеря аппетита;
- повышенная или высокая температура, озноб;
- вздутие живота
Симптомы холецистита часто появляются или усиливаются после обильного приема пищи, особенно жирной.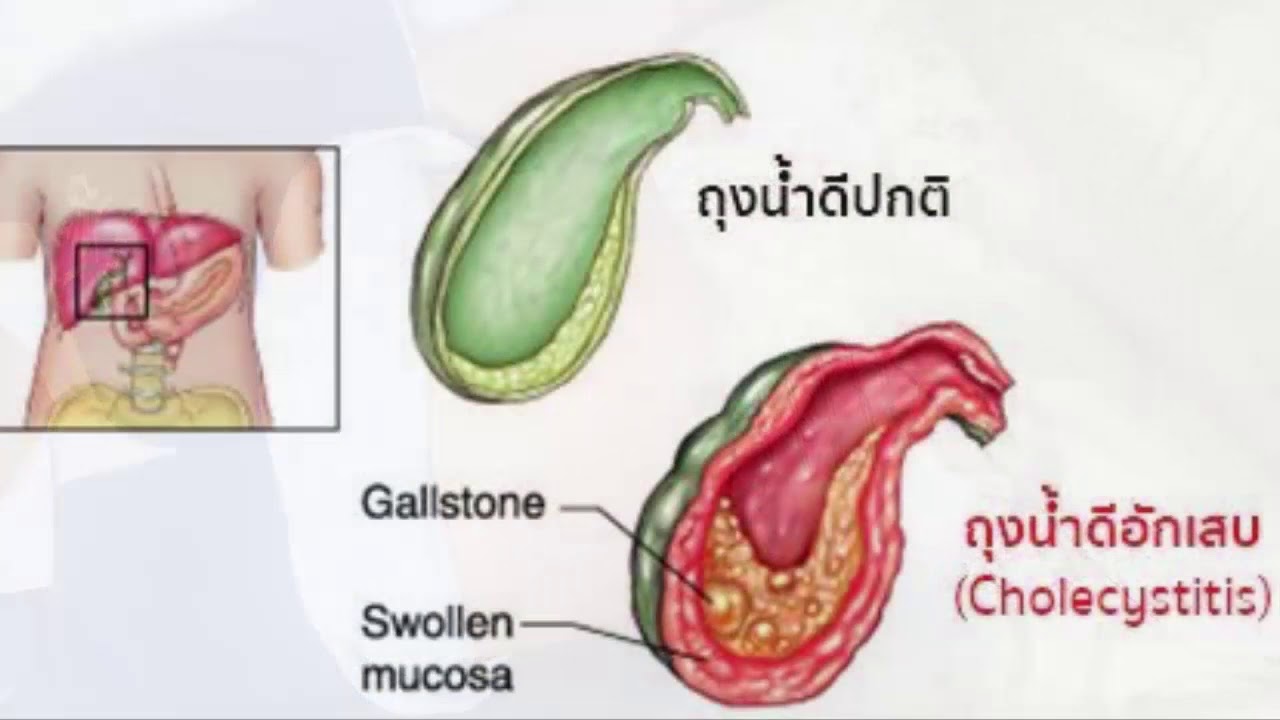
Желчный пузырь представляет собой небольшой грушеобразный орган, расположенный непосредственно под печенью в правой части брюшной полости. В желчном пузыре накапливается желчь — жидкость, которая поступает в тонкий кишечник и принимает участие в процессе пищеварения.
Во многих случаях холецистит возникает вследствие образования желчных камней, которые закупоривают выводной желчный проток. В результате происходит застой желчи, который может стать причиной воспаления. Другими причинами возникновения холецистита являются инфекции, травмы и опухоли.
Без принятия своевременных мер холецистит может привести к таким серьезным осложнениям, как, например, разрыв желчного пузыре и возникновение инфекций, которые могут распространиться на другие части тела. После обнаружения холецистита необходима госпитализация. Лечение холецистита часто сопровождается удалением желчного пузыря.
Когда обращаться врачу
При обнаружении у себя любых симптомов холецистита, немедленно обратитесь к врачу. Холецистит не всегда требует экстренной медицинской помощи, однако если своевременно не обратиться к врачу, болезнь может дать серьезные, а иногда и опасные для жизни осложнения. Пациентам с приступом холецистита обычно требуется госпитализация в хирургический стационар.
Холецистит не всегда требует экстренной медицинской помощи, однако если своевременно не обратиться к врачу, болезнь может дать серьезные, а иногда и опасные для жизни осложнения. Пациентам с приступом холецистита обычно требуется госпитализация в хирургический стационар.
Связанные статьи:
Боль в животе
Боль внизу живота
Аппендицит
УЗИ брюшной полости
Видеоэзофагогастродуоденоскопия (ФГС)
МР — холангиография (см. МРТ брюшной полости)
Желчный пузырь
Язва желудка
Гастрит
Панкреатит
Поджелудочная железа
Синдром раздраженного кишечника (СРК)
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ)
Неспецифический язвенный колит
Болезнь Крона.
Гастроэнтерит
ЧУЗ «КБ «РЖД-Медицина» им. Н.А. Семашко»
Холециститом называют воспаление желчного пузыря
Причины
Основной причиной холецистита является проникновение инфекции в желчный пузырь. Инфекция может попадать с током крови или лимфы, а так же восходящим путем из кишечника. Способствующими факторами являются дискинезии желчных путей, врожденные аномалии желчного пузыря, желчекаменная болезнь, злоупотребление жирной, острой пищей, алкоголем, гиподинамия, ожирение.
Инфекция может попадать с током крови или лимфы, а так же восходящим путем из кишечника. Способствующими факторами являются дискинезии желчных путей, врожденные аномалии желчного пузыря, желчекаменная болезнь, злоупотребление жирной, острой пищей, алкоголем, гиподинамия, ожирение.
Классификация
- По течению:
- Острый
- Хронический
- По наличию конкрементов:
- Бескаменный
- Калькулезный
- Клинико-морфологические формы:
- Катаральный
- Флегмонозный
- Гангренозный
Клиника
Симптомами холецистита являются боли в правом подреберье, тошнота, рвота, вздутие живота, повышение температуры, озноб. Может развиться желтушность кожных покровов.
Диагностика
Диагноз холецистита устанавливается на основе клинических данных, результатов лабораторного исследования, эндоскопического (ЭГДС) и рентгенологического исследования, данных УЗИ, компьютерной томографии.
Осложнения
К осложнениям холецистита относят околопузырный инфильтрат, перитонит, механическую желтуху, холангит и др.
Лечение
- Консервативное лечение холецистита включает антибактериальную терапию (антибиотики) и средства, улучшающие отхождение желчи (спазмолитики, желчегонные препараты).
При желчекаменной болезни были предприняты попытки терапевтического решения проблемы — поиска методов химического растворения желчных камней. Однако, имеющиеся в настоящее время препараты не универсальны, их литолитический эффект ограничен, как правило, холестериновыми конкрементами, при их пероральном приеме необходим длительный курс лечения, который плохо переносится рядом больных из-за побочного токсического действия. Литолитическая терапия имеет еще один существенный недостаток — даже полная ликвидация камней в желчном пузыре не означает излечения больного от желчнокаменной болезни, так как сохраняются патологические изменения желчного пузыря наряду с теми факторами, которые уже ранее привели к образованию конкрементов.
Большие надежды возлагались на экстракорпоральное ультразвуковое разрушение конкрементов в желчном пузыре. Многочисленные клинические наблюдения показали, что с помощью направленной ультразвуковой волны можно добиться разрушения желчных камней на мелкие фрагменты, способные удаляться через пузырный проток в общий желчный проток, а затем оттуда в двенадцатиперстную кишку. При использовании усовершенствованных литотриптеров процедура является в достаточной степени безболезненной, и при единичных камнях в желчном пузыре терапевтический успех достигается в течение нескольких сеансов. Метод экстракорпоральной литотрипсии начал довольно широко применяться в развитых странах, однако клинические наблюдения выявили и ряд негативных последствий этого метода: достаточно крупные фрагменты, мигрируя из пузыря, могут обусловить возникновение обтурационного холецистита, механической желтухи или панкреатита, требующих выполнения срочной полостной или эндоскопической операции.
- При остром флегмонозном, гангренозном холецистите, а также при хроническом калькулезном холецистите показано хирургическое лечение.

Эндовидеохирургические технологии за последние годы позволили широко внедрить в клиническую практику лапароскопическую холецистэктомию. Эта операция признана «Золотым стандартом» во всем мире. Лапароскопическая холецистэктомия сочетает в себе радикальность (удаляется патологически измененный желчный пузырь с конкрементами) с малой травматичностью (почти полностью сохраняется целостность мягких тканей брюшной стенки, прежде всего апоневроза и мышц, что практически исключает опасность формирования послеоперационных вентральных грыж), благодаря чему значительно сокращаются сроки восстановления трудоспособности пациентов, со значительным экономическим эффектом. Основным результатом применения данной технической методики является значительное сокращение времени оперативного вмешательства, в основном за счет быстроты и эффективности дифференцировки анатомически структур, минимальной кровопотери, и соответственно сокращения времени на адекватный гемостаз, особенно в отношении ложа желчного пузыря.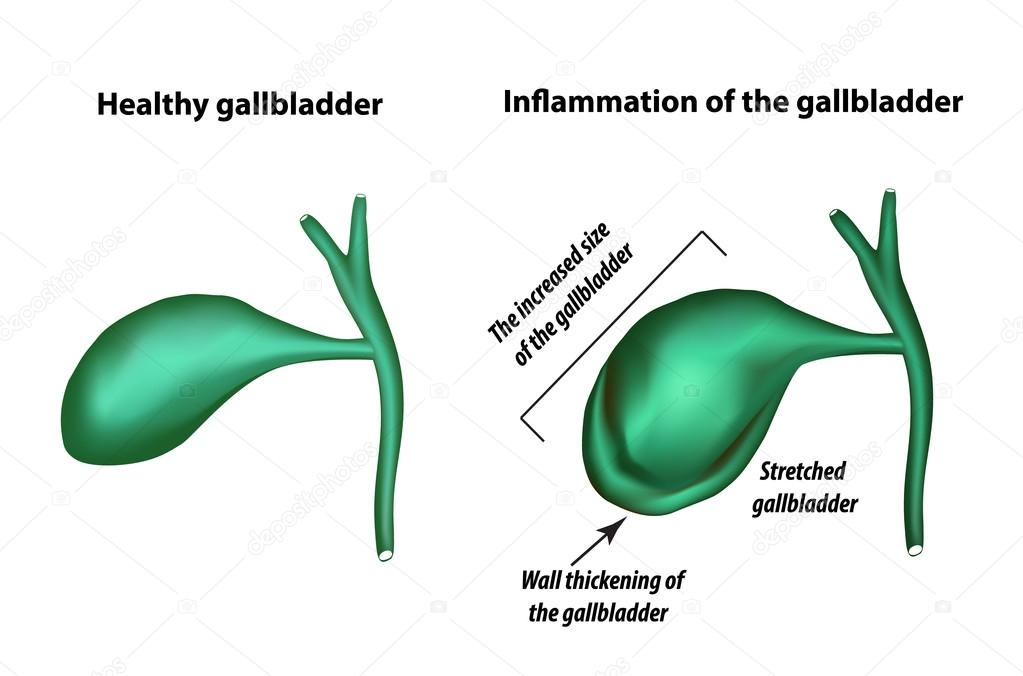 Сроки восстановительного периода после перенесенной операции занимают минимальный период времени.
Сроки восстановительного периода после перенесенной операции занимают минимальный период времени.
Распространенное воспаление желчного пузыря — фактор риска перфорации желчного пузыря у пациентов с острым холециститом | World Journal of Emergency Surgery
В этом исследовании изучалась степень воспаления желчного пузыря у пациентов, перенесших экстренную или неотложную операцию по поводу APC. Пятьдесят пациентов с подтвержденным APC после интраоперационного и гистологического диагноза были сравнены со 150 случайно выбранными пациентами, перенесшими LC по поводу AC без перфорации. Распространенное воспаление желчного пузыря с эмпиематозным и гангренозным холециститом регистрировалось значительно чаще в группе APC по сравнению с контролем.Пациенты с APC были значительно старше и имели значительно более высокий уровень СРБ по сравнению с контрольной группой. Операция длилась значительно дольше; частота разговоров, заболеваемость и смертность были значительно выше в группе APC. В группе APC лечение в ОИТ требовалось значительно чаще, а общий LOS был значительно дольше в группе APC по сравнению с группой без перфорации.
В группе APC лечение в ОИТ требовалось значительно чаще, а общий LOS был значительно дольше в группе APC по сравнению с группой без перфорации.
Перфорация желчного пузыря при остром холецистите была предложена в нашем недавно опубликованном исследовании регистров как фактор риска неблагоприятного исхода у пациентов, перенесших холецистэктомию по поводу АК [1].Результаты 5704 случаев с APC, подвергшихся экстренной или срочной холецистэктомии, сравнивались с результатами 39 661 пациента без перфорации. Продолжительность операции, частота разговоров, заболеваемость и смертность были значительно выше у пациентов с APC по сравнению с пациентами без APC. Результаты настоящего исследования согласуются с результатами, представленными в вышеупомянутом исследовании.
Большой недостаток исследования регистров, проведенного Jansen et al. что было четко указано авторами в разделе ограничений, это неспособность охарактеризовать степень воспаления желчного пузыря, потому что регистрационные данные, использованные в их исследовании, не содержали результатов гистологии. Этот недостаток исследован в настоящем исследовании. Осложненный холецистит, определяемый как прогрессирующее воспаление желчного пузыря в форме эмпиематозного или гангренозного холецистита, был подтвержден в значительной части группы APC по сравнению с контрольной группой.
Этот недостаток исследован в настоящем исследовании. Осложненный холецистит, определяемый как прогрессирующее воспаление желчного пузыря в форме эмпиематозного или гангренозного холецистита, был подтвержден в значительной части группы APC по сравнению с контрольной группой.
Пожилой возраст> 65 лет и повышенный CRP были определены как факторы риска APC. Эти факторы были дополнительно подтверждены многомерным анализом как независимые факторы риска APC. Эти же факторы были ранее описаны в связи с другими формами тяжелого холецистита и поэтому не специфичны для APC [18, 19].
Значительно более длительная продолжительность хирургического вмешательства и более высокий уровень конверсии в открытое хирургическое вмешательство после попытки LC в группе APC по сравнению с группой без перфорации являются фактическими аргументами в пользу хирургической проблемы, связанной с ведением пациентов с APC. Кроме того, частота повреждения желчных протоков в 8% и частота образования послеоперационных внутрибрюшных абсцессов в группе APC свидетельствует о серьезности этого заболевания. Смертность в этом исследовании составила 8%. Этот показатель почти вдвое превышает показатель, сообщаемый Jansen et al.[1], но сравнимо с показателем смертности 9,5%, сообщенным в ретроспективном анализе 137 пациентов с APC, проведенном Ausania et al. в 2015 г. [20]. Неоднородность сообщаемого риска смерти в этой, а также в предыдущих публикациях должна интерпретироваться в контексте исследуемой популяции. Кроме того, значительно более высокие показатели лечения в отделениях интенсивной терапии, а также значительно более длительный период LOS следует интерпретировать как индикаторы вяжущего характера APC.
Смертность в этом исследовании составила 8%. Этот показатель почти вдвое превышает показатель, сообщаемый Jansen et al.[1], но сравнимо с показателем смертности 9,5%, сообщенным в ретроспективном анализе 137 пациентов с APC, проведенном Ausania et al. в 2015 г. [20]. Неоднородность сообщаемого риска смерти в этой, а также в предыдущих публикациях должна интерпретироваться в контексте исследуемой популяции. Кроме того, значительно более высокие показатели лечения в отделениях интенсивной терапии, а также значительно более длительный период LOS следует интерпретировать как индикаторы вяжущего характера APC.
Еще одним интересным открытием в этом исследовании стало то, что четыре пациента (8%) в группе APC перенесли первичную открытую холецистэктомию по сравнению с никем в контрольной группе.Этим пациентам была выполнена диагностическая лапаротомия по поводу острого живота с перитонитом, диагноз APC был поставлен во время операции. Перфорация I типа с желчным перитонитом была очевидна во время лапаротомии у этих пациентов. Это открытие следует интерпретировать как дополнительную демонстрацию тяжелой клинической природы APC.
Это открытие следует интерпретировать как дополнительную демонстрацию тяжелой клинической природы APC.
Ретроспективный дизайн исследования и небольшой размер исследуемой популяции должны быть указаны как возможные ограничения этого исследования. Таким образом, для дальнейшего изучения тенденций, показанных здесь, потребуются дальнейшие исследования с более крупными популяциями.Кроме того, результаты, представленные в этом исследовании, могут быть вторичными по сравнению с глубоким опытом лапароскопической хирургии в нашем отделении. Следовательно, результаты этого исследования не могут быть легко спроецированы на другие учреждения. Все случаи, включенные в это исследование, лечились хирургическим путем. Интервенционное лечение, такое как чрескожная холецистостомия, в нашем центре обычно не проводится. Хотя текущая литература о роли чрескожной холецистостомии не является окончательной [21,22,23,24,25], остается спорным, могли ли результаты, зарегистрированные в этом исследовании, быть изменены таким интервенционным лечением.
Хирурги и клиницисты должны знать о серьезном характере APC, связанном с высокими рисками заболеваемости и смертности. Хирургическое лечение таких пациентов требует глубокого опыта, и переход от лапароскопической операции к открытой никогда не следует рассматривать как неудачу. В таких случаях следует рассмотреть возможность бдительного послеоперационного ухода, включая использование широкополосных антибиотиков и тщательный мониторинг, например, в отделении интенсивной терапии.
В совокупности результаты этого исследования подтверждают, что APC является тяжелым осложнением AC со значительно более высокими показателями заболеваемости и смертности.Распространенное воспаление желчного пузыря, включая эмпиематозный и гангренозный холецистит, значительно чаще наблюдалось у пациентов с APC, чем у пациентов без перфорации. Таким образом, перфорация желчного пузыря в APC должна быть вторичной по отношению к развитому воспалению желчного пузыря.
Боль в желчном пузыре: причины, симптомы, лечение
Желчный пузырь — это небольшой орган грушевидной формы, расположенный под печенью. Вы, наверное, особо не задумываетесь об этом — пока не станет больно.
Вы, наверное, особо не задумываетесь об этом — пока не станет больно.
Ваш желчный пузырь выделяет зеленоватую жидкость, называемую желчью, каждый раз, когда вы едите, чтобы помочь вашему организму переваривать жиры и витамины.Желчь течет в тонкую кишку по трубкам, называемым протоками. Когда что-то идет не так с желчным пузырем или желчевыводящими путями, может болеть верхняя правая сторона живота. Вы также можете почувствовать:
- Боль в спине или груди, особенно при глубоком вдохе
- Лихорадка
- Как рвота
- Вздутие живота
- Зуд
- Усталость
Другие общие симптомы включают пожелтение кожи и глаз ( известная как желтуха), похудание и изменение цвета мочи или фекалий.
Причины
Желчные камни . Это основная причина боли в желчном пузыре. Вы получаете их, когда желчь сливается в твердые массы. Камни в желчном пузыре могут быть крошечными пятнышками или размером с мяч для гольфа. Если они станут достаточно большими, эти камни могут заблокировать выход желчи. Это может привести к приступу желчнокаменной болезни — внезапной боли в верхней правой части живота.
Если они станут достаточно большими, эти камни могут заблокировать выход желчи. Это может привести к приступу желчнокаменной болезни — внезапной боли в верхней правой части живота.
Эти приступы часто случаются после обильного стейка или другой жирной пищи и могут длиться в течение многих часов.Но большинство людей с камнями в желчном пузыре этого не знают. Эти «тихие» камни не вызывают проблем в ваших органах. Диагностические тесты, такие как УЗИ, магнитно-резонансная холангиопанкреатография (MRCP), эндоскопическая ретроградная холангиопанкреатография (ERCP), анализ крови или другие методы визуализации, могут показать, есть ли у вас камни в желчном пузыре. Ваш врач может избавиться от них с помощью операции, лекарств или даже ударных волн.
Камни желчных протоков . Это либо камни, застрявшие в желчных протоках, либо камни, которые там образуются.Они могут не доставить вам хлопот, пока не заблокируют желчные протоки. Тогда у вас может возникнуть серьезная боль в животе, которая приходит и уходит часами. Ваша кожа и глаза могут пожелтеть, и вы можете почувствовать рвоту. Врач может удалить камни, продев тонкую трубку со светом на конце, называемым эндоскопом, через ваш рот к желчным протокам.
Ваша кожа и глаза могут пожелтеть, и вы можете почувствовать рвоту. Врач может удалить камни, продев тонкую трубку со светом на конце, называемым эндоскопом, через ваш рот к желчным протокам.
Перфорированный желчный пузырь . Это может произойти, если камни в желчном пузыре со временем образовывают отверстие в стенках органа.Это редко, но может быть смертельно опасным. Может болеть верхняя правая часть живота. У вас также может быть высокая температура, тошнота и рвота. Вам срочно понадобится лечение или операция.
Абсцесс желчного пузыря (эмпиема). Это вызвано инфекцией, вызванной выделением желчного пузыря из-за непроходимости протока (включая камни в желчном пузыре). Инфекция может не поддаваться лечению антибиотиками, и ее необходимо удалить. Серьезный абсцесс может привести к разрыву, в результате чего инфекция может проникнуть на внутреннюю поверхность живота (перитонит).
Воспаление желчного пузыря. Также называется холециститом. Это может произойти по нескольким причинам, включая травму, болезнь, инфекцию, опухоли или скопление желчи в желчном пузыре из желчных камней. Реже другие виновники могут включать опухоли, определенные бактерии или проблемы с желчевыводящими путями. Когда ваш желчный пузырь воспаляется и опухает, симптомы включают боль в животе, в том числе в области чуть выше живота. Вы также можете почувствовать боль в спине или правой лопатке.
Это может произойти по нескольким причинам, включая травму, болезнь, инфекцию, опухоли или скопление желчи в желчном пузыре из желчных камней. Реже другие виновники могут включать опухоли, определенные бактерии или проблемы с желчевыводящими путями. Когда ваш желчный пузырь воспаляется и опухает, симптомы включают боль в животе, в том числе в области чуть выше живота. Вы также можете почувствовать боль в спине или правой лопатке.
Обычно это можно диагностировать с помощью ультразвукового исследования и других методов визуализации. Вам может потребоваться операция по удалению желчного пузыря. (Ваше тело может нормально работать и без него.) Без лечения орган может лопнуть.
Первичный склерозирующий холангит (ПСХ). Это заболевание печени, при котором поражаются желчные протоки. Это прогрессирует, то есть со временем становится только хуже. Около 4 из 5 человек с ПСХ также страдают воспалительным заболеванием кишечника. ПСХ может привести к печеночной недостаточности. У многих людей симптомы отсутствуют.Или вы можете чувствовать усталость, боль в верхней правой части живота или зуд кожи. Это состояние часто обнаруживается, когда обычные анализы крови показывают, что ваша печень не работает.
У многих людей симптомы отсутствуют.Или вы можете чувствовать усталость, боль в верхней правой части живота или зуд кожи. Это состояние часто обнаруживается, когда обычные анализы крови показывают, что ваша печень не работает.
Рак желчного пузыря . Это редко и трудно диагностировать. Чаще всего симптомы не проявляются, пока рак не распространился. Признаки могут включать боль в животе, особенно в правом верхнем углу, а также потерю веса, желтуху и вздутие живота. Семейный анамнез камней в желчном пузыре; быть старше, женским или страдающим ожирением; а употребление нездоровой пищи может повысить вероятность заболевания раком желчного пузыря.
Рак желчных протоков . На ранних стадиях рака у вас может не быть симптомов. Если да, то это часто происходит из-за закупорки желчного протока. Желтуха — самый распространенный симптом, наряду с кожным зудом и светлыми или жирными фекалиями. Если ваши опухоли достаточно большие, у вас может возникнуть боль в животе, особенно под ребрами с правой стороны. Хирургия дает вам наилучшие шансы на излечение. Но большинство случаев рака желчных протоков обнаруживается слишком поздно. В этом случае вам может потребоваться лучевая или химиотерапия, чтобы сначала уменьшить опухоль.
Хирургия дает вам наилучшие шансы на излечение. Но большинство случаев рака желчных протоков обнаруживается слишком поздно. В этом случае вам может потребоваться лучевая или химиотерапия, чтобы сначала уменьшить опухоль.
Рубцы желчных протоков . Суженные желчные протоки из рубцовой ткани могут препятствовать выходу желчи из печени и желчного пузыря в тонкий кишечник. Это может вызвать боль в правой части живота, где находятся органы. У вас также может быть зуд или усталость, отсутствие аппетита, желтуха, ночная потливость или лихорадка.
Шрамы могут быть вызваны рядом причин, включая камни желчных протоков, травмы, инфекции, алкоголь и наркотики. Ваш врач может подтвердить это с помощью процедуры, называемой эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ), которая позволяет им заглянуть внутрь вашей желчи и протоков поджелудочной железы.
Осложнения
Боль в желчном пузыре выходит за рамки беспокойства. Некоторые из более мелких осложнений включают:
- дискомфорт во время еды
- потеря веса
- электролитные нарушения
- потребление обезболивающих
- нарушение повседневной активности.

Более серьезные осложнения заболевания желчного пузыря включают
- закупорку желчных протоков,
- серьезные инфекции (эмпиема и гангрена желчного пузыря)
- панкреатит,
- перитонит
- нечасто рак желчного пузыря
Что вы можете сделать
Изменения образа жизни могут помочь сохранить желчный пузырь в тонусе.
Увеличьте потребление клетчатки и сократите потребление сахара и углеводов. Проблемы с желчным пузырем часто связаны с избытком холестерина — жира из мясных, молочных и других источников животного происхождения. Но не бойтесь хороших ненасыщенных жиров из таких продуктов, как оливковое и рапсовое масло, лосось и другая жирная рыба, а также орехи.
Регулярно тренируйтесь . Стремитесь к 30-минутной быстрой ходьбе и другим умеренным тренировкам каждый день.
Поддерживайте здоровый вес .Если вы тяжелый, стремитесь худеть медленно и избегайте голодания.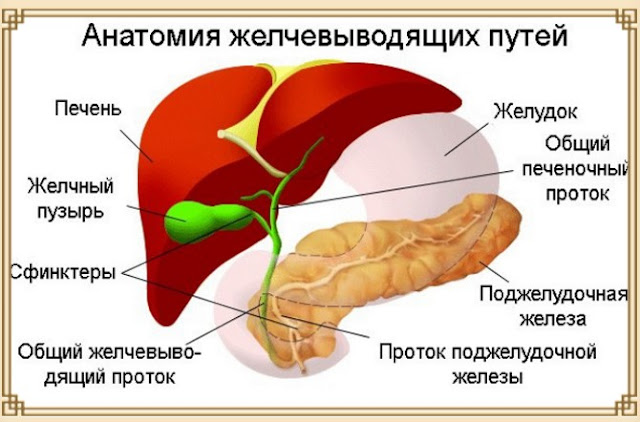 В противном случае это может привести к повышению уровня холестерина в желчном пузыре.
В противном случае это может привести к повышению уровня холестерина в желчном пузыре.
Когда звонить врачу
Необходимо проверить проблемы с желчным пузырем или желчевыводящими путями. Немедленно обратитесь к врачу, если вы:
- Чувствуете сильную боль в животе в течение многих часов
- Тошноту или рвоту
- Потный
- Озноб или жар
- Желтая кожа или глаза
- Обратите внимание на свое моча темнее или ваши фекалии светлее, чем обычно
Воспалительное начало рака желчного пузыря
Biochim Biophys Acta.Авторская рукопись; доступно в PMC 2018, 10 декабря.
Опубликован в окончательной редакции как:
PMCID: PMC6287912
NIHMSID: NIHMS997979
Хайме Эспиноза
департамент биологии и биологии SciLifeLab Медицинской биохимии и биофизики, Каролинский институт, Сольна, Стокгольм SE171 76, Швеция
Каролина Бизама
b Отделение патологии, Расширенный центр хронических заболеваний (ACCDiS), UC-Центр исследовательской онкологии (CITO), Школа Медицина, Папский католический университет Чили, Сантьяго 8330024, Чили
Патрисия Гарсия
b Отделение патологии, Расширенный центр хронических заболеваний (ACCDiS), UC-Центр исследовательской онкологии (CITO), Медицинский факультет Университета Пондифиса Católica de Chile, Santiago 8330024, Chile
Catterina Ferreccio
c Государственный департамент H ealth, Advanced Center for Chronic Diseases (ACCDiS), School of Medicine, Pontificia Universidad Católica de Chile, Santiago 8330024, Chile
Milind Javle
d Отделение онкологии желудочно-кишечного тракта, Онкологический центр им. М. Д. Андерсона Техасского университета , TX 77030, США
М. Д. Андерсона Техасского университета , TX 77030, США
Хуан Ф.Miquel
e Отделение гастроэнтерологии, Школа медицины, Папский католический университет Чили, Сантьяго 8330024, Чили
Джилл Кошиол
f Отдел эпидемиологии и генетики рака, Национальный институт рака США, США 20850, Бетесда, США
Хуан К. Роа
b Отделение патологии, Расширенный центр хронических заболеваний (ACCDiS), UC-Центр исследовательской онкологии (CITO), Школа медицины, Папский католический университет в Чили, Сантьяго 8330024, Чили
a SciLifeLab, Отдел трансляционной медицины и химической биологии, Отдел медицинской биохимии и биофизики, Каролинский институт, Сольна, Стокгольм, SE171 76, Швеция
b Отделение патологии, Расширенный центр хронических заболеваний (ACCDiS), UC- Центр исследовательской онкологии (CITO), Школа медицины, Папский католический университет Чили, Сантьяго 8330024, Чили
c Департамент общественного здравоохранения, Расширенный центр хронических заболеваний (ACCDiS), Школа медицины, Католический университет Чили, Сантьяго 8330024, Чили
d Департамент гастроинтестинальной медицинской онкологии Техасского университета Андерсона Онкологический центр, Хьюстон, Техас 77030, США
e Отделение гастроэнтерологии, Школа медицины, Папский католический университет Чили, Сантьяго 8330024, Чили
f Отдел эпидемиологии и генетики рака, Национальный институт рака 20850, , Мэриленд, США
Отчет о вкладе авторов
Статья написана JAE, JK и JCR.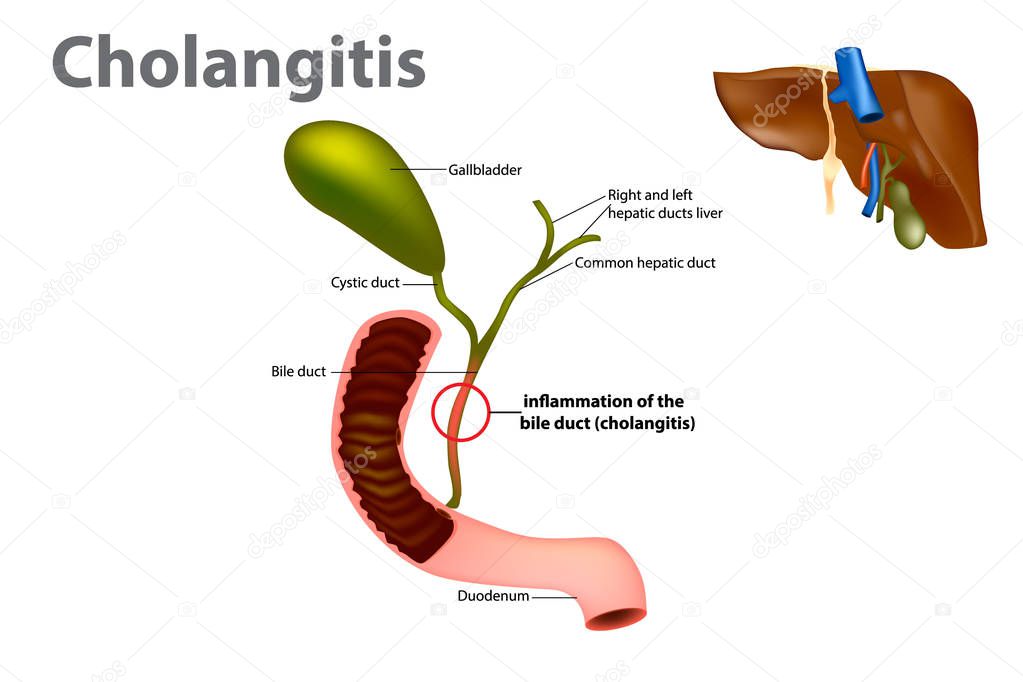 CB, PG, CF, MJ и JFM просмотрели и отредактировали рукопись. * Автор, ответственный за переписку: Папский университет Католики Чили, Марколета 377, 7-й этаж, Сантьяго, Чили. lc.cup.dem@aorcj (J.C. Roa). См. другие статьи в PMC, в которых цитируется опубликованная статья.
CB, PG, CF, MJ и JFM просмотрели и отредактировали рукопись. * Автор, ответственный за переписку: Папский университет Католики Чили, Марколета 377, 7-й этаж, Сантьяго, Чили. lc.cup.dem@aorcj (J.C. Roa). См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Рак желчного пузыря — это смертельное заболевание с заметными географическими вариациями по всему миру и склонностью к женщинам. Его основной фактор риска — длительное воздействие камней в желчном пузыре, хотя с ним также связаны бактериальные инфекции и другие воспалительные состояния.Повторяющиеся циклы повреждения и восстановления эпителия желчного пузыря создают хроническую воспалительную среду, которая способствует прогрессирующему морфологическому нарушению через метаплазию-дисплазию-карциному, наряду с кумулятивной нестабильностью генома. Инактивация TP53 , который мутирует более чем в 50% случаев GBC, по-видимому, является самым ранним и одним из наиболее важных канцерогенных путей. Повышенный оборот клеток и окислительный стресс способствуют раннему изменению TP53 , нарушению регуляции клеточного цикла, апоптозу и репликативному старению.В этом обзоре мы обсудим доказательства роли воспаления в канцерогенезе желчного пузыря, полученные в результате эпидемиологических исследований, полногеномных ассоциативных исследований, экспериментального канцерогенеза, морфогенетических исследований и сравнительных исследований с другими злокачественными новообразованиями, вызванными воспалением. Доказательства убедительно подтверждают, что хроническое неразрешенное воспаление является основным канцерогенным механизмом рака желчного пузыря, независимо от первоначального этиологического триггера. Учитывая эту центральную роль воспаления, может быть оправдана оценка потенциала профилактики GBC, устраняющего причины воспаления, или использования противовоспалительных препаратов в группах высокого риска.
Повышенный оборот клеток и окислительный стресс способствуют раннему изменению TP53 , нарушению регуляции клеточного цикла, апоптозу и репликативному старению.В этом обзоре мы обсудим доказательства роли воспаления в канцерогенезе желчного пузыря, полученные в результате эпидемиологических исследований, полногеномных ассоциативных исследований, экспериментального канцерогенеза, морфогенетических исследований и сравнительных исследований с другими злокачественными новообразованиями, вызванными воспалением. Доказательства убедительно подтверждают, что хроническое неразрешенное воспаление является основным канцерогенным механизмом рака желчного пузыря, независимо от первоначального этиологического триггера. Учитывая эту центральную роль воспаления, может быть оправдана оценка потенциала профилактики GBC, устраняющего причины воспаления, или использования противовоспалительных препаратов в группах высокого риска.
Ключевые слова: Рак желчного пузыря, камни в желчном пузыре, хроническое воспаление, метаплазия, Salmonella Typhi, TP53
1.
 Введение
ВведениеРак желчного пузыря (GBC) является наиболее распространенным злокачественным новообразованием желчного дерева. В глобальном масштабе показатели GBC демонстрируют заметную региональную изменчивость, достигая уровней эпидемии для некоторых регионов и этнических групп, особенно в таких странах, как Чили, Боливия, Перу, Эквадор, Индия и Польша. Основание для этой вариации, вероятно, кроется в различиях в воздействии окружающей среды, взаимодействующих с генетической предрасположенностью к модуляции канцерогенеза.Риск GBC увеличивается с возрастом, и женщины поражаются в 2-6 раз чаще, чем мужчины [1,2].
Основным фактором риска GBC является желчнокаменная болезнь (GSD), которая приводит к постоянному воспалительному состоянию, стимулируемому повторяющимися циклами гибели клеток и регенерации эпителиального слоя [3,4]. Связь между GSD и GBC подтверждается доказательствами уровня II (многокомпонентные исследования) [5]. У субъектов с GSD риск развития GBC увеличивается в 21–57 раз [6]. Часто заболеваемость GSD коррелирует с заболеваемостью GBC географически, и оба состояния имеют общие факторы риска, такие как возраст, женский пол, паритет и этническая принадлежность [1], факторы, которые могут ускорить образование желчных камней [7].Еще одним важным фактором риска для GBC является хроническое носительство Salmonella Typhi (OR 4.0), особенно для эндемичных регионов, таких как южно-центральная и юго-восточная Азия [8], где и инфекция, и рак коррелируют. Важно отметить, что недавние экспериментальные данные очерчивают механизм GBC, индуцированного Salmonella [9], подтверждая роль этих бактерий в этиологии части случаев GBC во всем мире. Кроме того, другие патологические состояния, такие как первичный склерозирующий холангит, аномальное расположение панкреатобилиарного протока (AAPBD) и бактериальные инфекции, связаны с возникновением GSD и GBC, и все они имеют сильный хронический воспалительный компонент [1].
Часто заболеваемость GSD коррелирует с заболеваемостью GBC географически, и оба состояния имеют общие факторы риска, такие как возраст, женский пол, паритет и этническая принадлежность [1], факторы, которые могут ускорить образование желчных камней [7].Еще одним важным фактором риска для GBC является хроническое носительство Salmonella Typhi (OR 4.0), особенно для эндемичных регионов, таких как южно-центральная и юго-восточная Азия [8], где и инфекция, и рак коррелируют. Важно отметить, что недавние экспериментальные данные очерчивают механизм GBC, индуцированного Salmonella [9], подтверждая роль этих бактерий в этиологии части случаев GBC во всем мире. Кроме того, другие патологические состояния, такие как первичный склерозирующий холангит, аномальное расположение панкреатобилиарного протока (AAPBD) и бактериальные инфекции, связаны с возникновением GSD и GBC, и все они имеют сильный хронический воспалительный компонент [1].
GBC уже давно представляет интерес как модель для понимания связи между хроническим воспалением и раком. В 20-е годы Арчибальд Лейтч решил изучать GBC из-за его связи с «… особым эндогенным раздражителем», желчным камнем. Лейтч имплантировал желчные камни, камешки и гранулы смолы в желчный пузырь морских свинок и наблюдал прогрессирование от десквамации эпителия до все более тяжелых поражений и, в конечном итоге, инвазивных аденокарцином, в зависимости от продолжительности жизни животных.Напротив, расплавленный ланолин, мягкий материал, не способный вызывать повторное повреждение клеток, не вызывает никаких изменений в желчном пузыре. Лейтч предположил, что это повреждение, вызванное инородным телом, а не его состав, создал «… патологическое состояние тканей», подходящее для развития рака [10]. Сегодня мы знаем, что хроническое воспаление — это «патологическое состояние», которое связывает повреждение и рак, что приводит к признанию того, что «желчные пути являются ярким примером связанной с воспалением карциномы» [11].Здесь мы рассматриваем доказательства связи воспаления с образованием GBC, чтобы пролить свет на малоизученный феномен и обозначить его значение для канцерогенеза и профилактики рака.
В 20-е годы Арчибальд Лейтч решил изучать GBC из-за его связи с «… особым эндогенным раздражителем», желчным камнем. Лейтч имплантировал желчные камни, камешки и гранулы смолы в желчный пузырь морских свинок и наблюдал прогрессирование от десквамации эпителия до все более тяжелых поражений и, в конечном итоге, инвазивных аденокарцином, в зависимости от продолжительности жизни животных.Напротив, расплавленный ланолин, мягкий материал, не способный вызывать повторное повреждение клеток, не вызывает никаких изменений в желчном пузыре. Лейтч предположил, что это повреждение, вызванное инородным телом, а не его состав, создал «… патологическое состояние тканей», подходящее для развития рака [10]. Сегодня мы знаем, что хроническое воспаление — это «патологическое состояние», которое связывает повреждение и рак, что приводит к признанию того, что «желчные пути являются ярким примером связанной с воспалением карциномы» [11].Здесь мы рассматриваем доказательства связи воспаления с образованием GBC, чтобы пролить свет на малоизученный феномен и обозначить его значение для канцерогенеза и профилактики рака.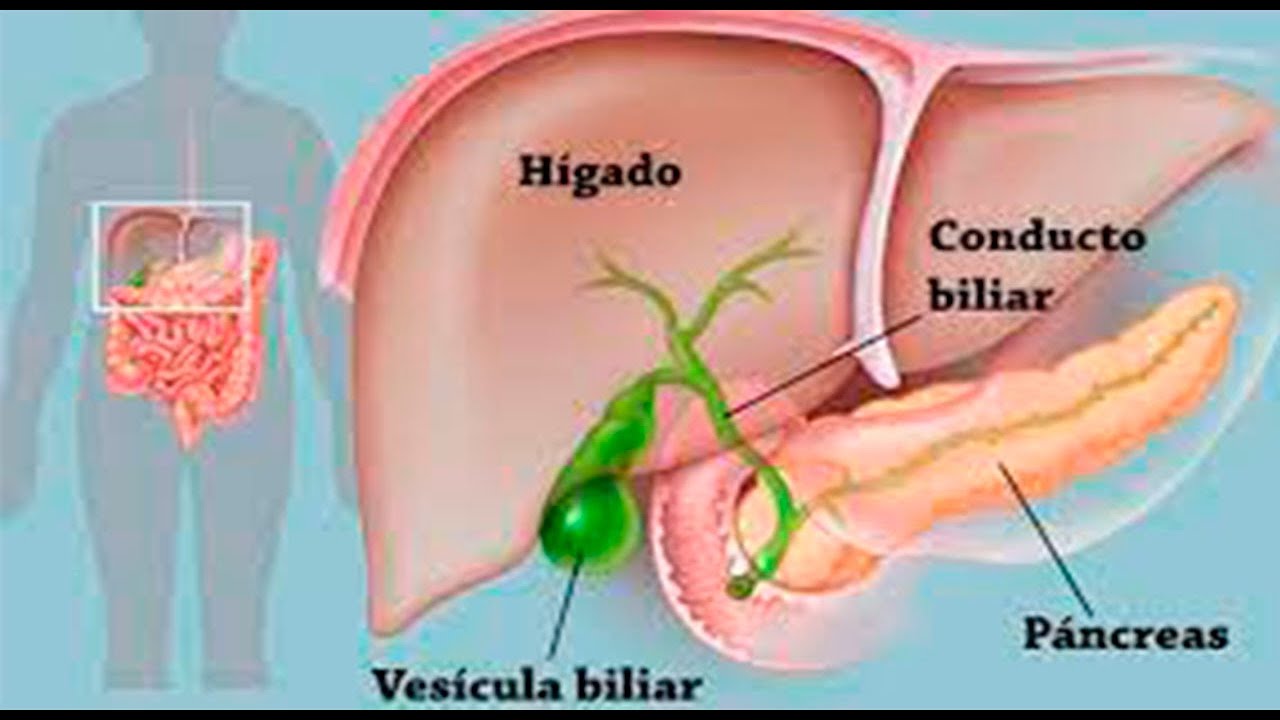
2. Воспаление и рак
Физиологическая цель воспаления — сдерживание и искоренение инфекции с последующим процессом разрешения, направленным на восстановление функции пораженных участков. В контексте повреждения ткани с повышенной гибелью клеток воспаление опосредует реакцию восстановления ткани, чтобы стимулировать пролиферацию и регенерацию [12].Однако, когда инициирующий стимул сохраняется во времени, процесс переходит в хроническое, неразрешимое воспаление. Хотя воспаление является необходимым процессом для восстановления гомеостаза, его постоянство способствует повреждению нормальных тканей и, в свою очередь, гибель клеток стимулирует усиление воспаления. Несколько патологий имеют общий компонент неразрешенного воспаления, среди которых ожирение, астма, хроническая обструктивная болезнь легких, рассеянный склероз, воспалительное заболевание кишечника, ревматоидный артрит и рак [13].
Иммунная система эволюционировала, чтобы определять гибель некротических клеток как способ косвенного обнаружения распространения инфекции.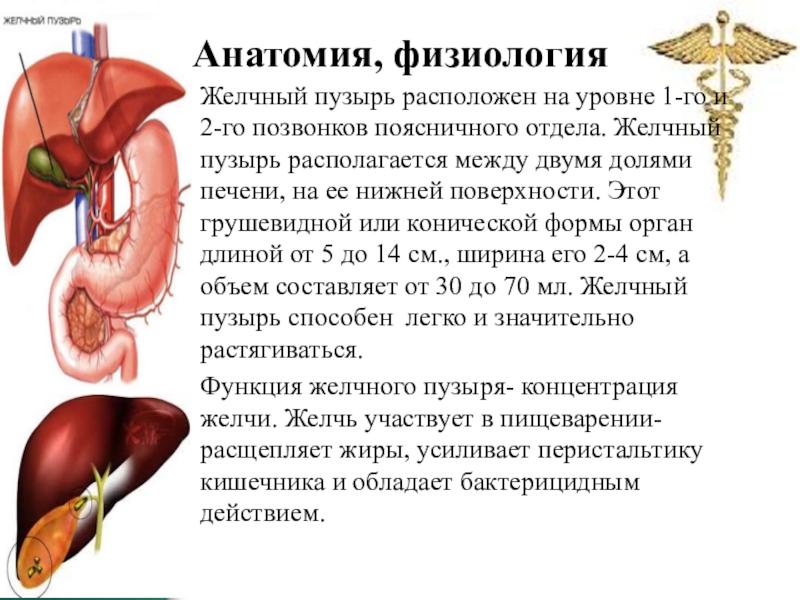 По этой причине иммунная система может реагировать как на инфекционные (вирусы, бактерии), так и на неинфекционные (опухоли, травмы) сценарии некроза [14]. Во время некроза, который часто является результатом нефизиологического повреждения, умирающие клетки высвобождают эндогенные молекулы, называемые молекулярными паттернами, связанными с повреждениями, которые способны стимулировать Т и дендритные клетки и обеспечивать воспалительную реакцию, расширяя артериолы и венулы для утечки жидкости и рекрутирования лейкоцитов из крови. в ткани, что приводит к нагреванию и отеку, классическим признакам воспалительной реакции [15].Было высказано предположение, что хроническое повреждение тканей может привести к аберрантному заживлению и регенеративному ответу, который в конечном итоге способствует расширению и прогрессированию инициированных клеток через механизмы, тесно связанные с воспалительными процессами. Если воспаление хронически спровоцировано повторяющимися травмами, гибелью клеток или другими факторами, возникающий в результате процесс может способствовать образованию рака [16].
По этой причине иммунная система может реагировать как на инфекционные (вирусы, бактерии), так и на неинфекционные (опухоли, травмы) сценарии некроза [14]. Во время некроза, который часто является результатом нефизиологического повреждения, умирающие клетки высвобождают эндогенные молекулы, называемые молекулярными паттернами, связанными с повреждениями, которые способны стимулировать Т и дендритные клетки и обеспечивать воспалительную реакцию, расширяя артериолы и венулы для утечки жидкости и рекрутирования лейкоцитов из крови. в ткани, что приводит к нагреванию и отеку, классическим признакам воспалительной реакции [15].Было высказано предположение, что хроническое повреждение тканей может привести к аберрантному заживлению и регенеративному ответу, который в конечном итоге способствует расширению и прогрессированию инициированных клеток через механизмы, тесно связанные с воспалительными процессами. Если воспаление хронически спровоцировано повторяющимися травмами, гибелью клеток или другими факторами, возникающий в результате процесс может способствовать образованию рака [16]. Как описывает Гарольд Дворжак, «… опухоли предстают перед хозяином в виде ран или, вернее, нескончаемой серии ран, которые постоянно инициируют заживление, но никогда не заживают полностью» [17].В этом случае воспалительная реакция не устраняет первичный стимул, как это обычно происходит в большинстве случаев инфекции или травмы, и, таким образом, возникает хроническая форма воспаления, которая в конечном итоге способствует повреждению тканей.
Как описывает Гарольд Дворжак, «… опухоли предстают перед хозяином в виде ран или, вернее, нескончаемой серии ран, которые постоянно инициируют заживление, но никогда не заживают полностью» [17].В этом случае воспалительная реакция не устраняет первичный стимул, как это обычно происходит в большинстве случаев инфекции или травмы, и, таким образом, возникает хроническая форма воспаления, которая в конечном итоге способствует повреждению тканей.
Доказательства роли воспаления в развитии опухоли накапливались в течение некоторого времени [18], и сегодня большой объем данных поддерживает гипотезу о том, что воспаление является связующим звеном между повреждением ткани и происхождением рака. Это прораковое воспаление можно отделить от воспаления, вызванного опухолью, которое возникает, когда инвазивная опухоль уже сформировалась и вызывает инвазию и метастатические процессы [16].Существуют убедительные доказательства того, что химические и физические повреждения способствуют развитию рака желудочно-кишечного тракта и печени, вызывая хроническое воспаление [19], а примеры воспалительных состояний, способствующих развитию рака, можно найти во многих органах, включая яичники, поджелудочную железу, пищевод, желудок. , печень, мочевой пузырь, толстая кишка, легкие и эндометрий [20–22].
, печень, мочевой пузырь, толстая кишка, легкие и эндометрий [20–22].
Воспаление может способствовать раннему изменению TP53 , возможно, за счет увеличения клеточного обмена и окислительного стресса, хотя точные механизмы неизвестны.Инактивация гена TP53 путем делеции или мутации является наиболее частым генетическим изменением, наблюдаемым при раке в различных анатомических участках [23], включая GBC [24,25]. TP53 Изменения наблюдаются даже в гистологически нормальном эпителии у пациентов с GDS с хроническим холециститом, а частота изменений TP53 увеличивается по мере того, как нарушение эпителиальной архитектуры прогрессирует от метаплазии до инвазивной карциномы [26,27]. Воздействие окружающей среды может привести к мутациям TP53 и повлиять на воспалительные и другие иммунные реакции.Например, воздействие афлатоксина B1 (AFB1) приводит к специфическим соматическим мутациям в TP53 с высокой частотой трансверсий в кодоне 249 [28], а исследования на животных показали, что воздействие AFB1 приводит к увеличению провоспалительных цитокинов и регуляторных цитокинов.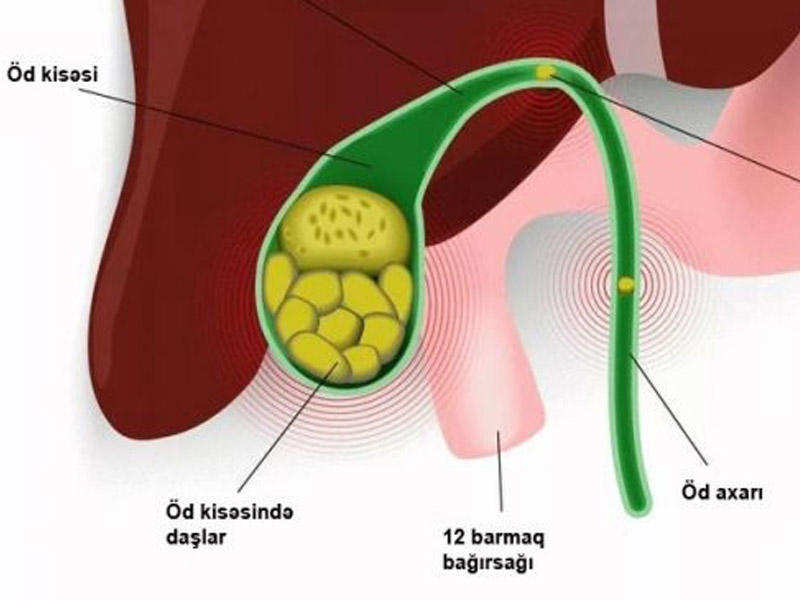 экспрессия при уменьшении пролиферации лимфоцитов [29,30]. В недавнем коротком отчете было обнаружено, что в случаях GBC в 13 раз чаще обнаруживались аддукты афлатоксина с альбумином, чем в нормальной контрольной группе (OR, 13,2; 95% CI, 4.3–47.9) [31]. Хотя открытие необходимо воспроизвести в других исследованиях, оно представляет интерес из-за связи между афлатоксином, мутациями TP53 и воспалением.
экспрессия при уменьшении пролиферации лимфоцитов [29,30]. В недавнем коротком отчете было обнаружено, что в случаях GBC в 13 раз чаще обнаруживались аддукты афлатоксина с альбумином, чем в нормальной контрольной группе (OR, 13,2; 95% CI, 4.3–47.9) [31]. Хотя открытие необходимо воспроизвести в других исследованиях, оно представляет интерес из-за связи между афлатоксином, мутациями TP53 и воспалением.
Утрата функции TP53 наблюдается при других пренеоплазиях, связанных с вызывающими воспаление состояниями и повреждением тканей. Например, потеря функции TP53 обычна для пищевода Барретта, метаплазии, которая возникает в ответ на хронический желудочный рефлюкс с хроническим эзофагитом и является предшественником аденокарциномы пищевода [32].Аналогичным образом, изменение TP53 считается ранним событием для связанного с язвенным колитом (т.е. связанного с воспалением) колоректального рака [33], тогда как оно является поздним событием для спорадического колоректального рака. Гистологическое прогрессирование ассоциированного с колитом и спорадического колоректального рака также отличается; в то время как спорадический колоректальный рак проявляется прогрессированием от полипа к карциноме, связанный с язвенным колитом рак включает увеличение гистологической степени дисплазии, которая достигает кульминации в инвазивной карциноме [34] с морфогенетическим прогрессированием, аналогичным GBC.Кроме того, инфекция Helicobacter pylori и мультиатрофический гастрит, связанный с кишечной метаплазией желудка, предшественником рака желудка кишечного типа, часто проявляются мутациями, делециями и сверхэкспрессией IHC TP53 [35–37]. В печени самая высокая частота мутаций TP53 обнаруживается при гепатоцеллюлярных карциномах [38] и внутрипеченочных холангиокарциномах, связанных с гепатитом B [39]. Взятые вместе, эти наблюдения предполагают, что независимо от конкретных этиологических агентов, вовлеченных в развитие вышеупомянутых видов рака, хроническое воспаление и стойкое повреждение тканей вносят свой вклад в канцерогенез первоначально через инактивацию TP53 .
Интересно, что при холангиокарциноме, связанной с двуустками, рак, в основном вызванный колонизацией желчевыводящих путей Opisthorchis viverrini или Clonorchis sinensis двуустки, TP53 мутирует в 40–44% случаев по сравнению с ~ 10% в обычных случаях. -инфекционная холангиокарцинома [40,41]. Эта высокая частота мутаций TP53 вместе с низкой частотой активации онкогенов, обобщенная в другом месте [42], аналогична той, что наблюдается в GBC [24]. Это сходство между этими двумя типами рака желчных путей можно частично объяснить повреждением тканей и воспалительным процессом, вызванным определенными факторами (паразитами или желчными камнями) внутри желчных путей.Это представление поддерживает идею о том, что хроническое воспаление, а не конкретный этиологический фактор, является движущей силой канцерогенеза желчевыводящих путей.
Связь между воспалением и TP53 также изучалась при неопухолевых патологиях. TP53 Мутации и хромосомные изменения обнаруживаются в атеросклеротических бляшках и синовиях у пациентов с ревматоидным артритом, оба состояния сильно связаны с хроническим воспалением [43]. Это наблюдение поддерживает идею о том, что нарушение регуляции p53 стимулируется в контексте повреждения тканей и воспаления, что, по-видимому, происходит во время канцерогенеза желчного пузыря.Хотя механизмы, которые связывают TP53 с хроническим воспалением и канцерогенезом, не ясны, TP53 активируется при остром повреждении ДНК, гиперпролиферативных сигналах, окислительном стрессе и истощении рибонуклеотидов. Активация TP53 делает возможным остановку клеточного цикла, позволяя клеткам восстанавливать повреждение генома до прохождения клеточного цикла и тем самым ограничивая распространение потенциально онкогенных мутаций [44]. Если репарация не выполняется, клетка может погибнуть в результате апоптоза или вступить в репликативное старение, что является наиболее важным механизмом устранения поврежденных клеток.Оба эти процесса часто управляются активацией TP53 [45]. В этом контексте было обнаружено, что предопухолевые поражения человека имеют широко распространенную активацию передачи сигналов повреждения ДНК (даже до появления мутаций р53), обеспечивая барьер против туморогенеза за счет индукции апоптоза или старения [46,47]. Следовательно, в стареющей ткани, подвергающейся в течение многих лет повреждению и хроническому воспалению, барьер, создаваемый p53 дикого типа, кажется, возможно, самым большим препятствием для преодоления, что может быть причиной того, что мутировавшие клоны так эффективно отбираются в контексте GBC.
3. Желчнокаменная болезнь, хроническое воспаление и риск рака желчного пузыря
GSD является основным фактором риска GBC, и его сложный патогенез подробно рассмотрен в другом месте [48]. Полиморфизм ABCG8-Dh29 у гетеродимерного партнера ABCG5 / G8 был первым генетическим фактором риска GSD холестерина, обнаруженным в исследовании GWAS и впоследствии воспроизведенным в различных популяциях [49]. Этот литогенный полиморфизм вызывает усиление функции белка, позволяя увеличить секрецию билиарного стерола из канальцевой мембраны гепатоцитов в желчное дерево, способствуя перенасыщению холестерина и тем самым способствуя образованию желчных камней [50].Интересно, что помимо роли фактора риска GSD, этот полиморфизм также был связан с повышенным риском развития GBC в различных этнических популяциях [51,52]. Механизм, с помощью которого усиление функции в гене ABCG5 / G8 может также увеличивать риск GBC, не выяснен, хотя он может быть связан с более высоким риском развития GSD в раннем возрасте [53] и / или способность транспортировать в желчное дерево другие субстраты, такие как растительные стерины или другие химические вещества с потенциально канцерогенными эффектами [54–57].Помимо сильного влияния этого модулирующего желчный камень полиморфизма на развитие GBC, полиморфизмы в генах, связанных с иммунной системой, воспалением и окислительным стрессом, были связаны с повышенным риском GBC, а именно PTGS2 [58], TLR2, TLR4 [59], IL1RN, IL1B [60], IL10 [61], IL8 [62], CCR5 [63], LXRβ [64] и OGG1 [65]. Таким образом, варианты генов, связанных с воспалением, могут под воздействием камней в желчном пузыре или других повреждений ускорять развитие GBC.
Исследования на моделях GSD мышиного холестерина, подвергнутых литогенной диете (содержащей большое количество холестерина и холевой кислоты), позволили получить представление о воспалительных изменениях, которые происходят в процессе образования камней в желчном пузыре. В одном исследовании у мышей с кристаллами холестерина, ранней стадией образования камней в желчном пузыре, развились локальные изменения в желчном пузыре, характеризующиеся увеличением толщины слоя слизи, интерлейкина-1 и активности миелопероксидазы в стенке желчного пузыря [66].В другом исследовании с использованием той же модели морфологические изменения, включая гиперплазию эпителия, гипертрофию мышечной ткани и увеличение толщины стенки, наблюдались уже через четыре недели после того, как мыши начали литогенную диету. Эти изменения сопровождались воспалительным инфильтратом, состоящим из эозинофилов, макрофагов, нейтрофилов и лимфоцитов в пластинке пропиа [67]. Умеренный инфильтрат гранулоцитов также наблюдался в желчном пузыре с прогрессирующим нарушением опорожнения желчного пузыря [68].Маурер и его коллеги показали, что функциональные Т-клетки имеют решающее значение в развитии GSD, поскольку мыши Rag2 — / — с дефицитом В- и Т-клеток были устойчивы к образованию холестериновых желчных камней при питании литогенной диетой в течение 8 недель [69 ]. Таким образом, по крайней мере, на мышиных моделях GSD хроническое воспаление желчного пузыря возникает на ранних стадиях как местный ответ на присутствие литогенной желчи (т.е. желчи, перенасыщенной холестерином), даже до того, как будут обнаружены макроскопические желчные камни [68]. Кроме того, было обнаружено, что ткань желчного пузыря пациентов с GSD содержит более высокие уровни инфильтрации COX-2 / iNOS-позитивных макрофагов, iNOS-позитивных гранулоцитов и тучных клеток, чем в контрольной группе без GSD.Эти уровни снижались, когда пациенты получали урсодезоксихолевую кислоту, гидрофильную желчную кислоту, которая снижает содержание холестерина в желчных путях (т.е. снижает индекс насыщения холестерина желчных путей) и улучшает сократимость мышц желчного пузыря за счет снижения содержания холестерина в плазматической мембране гладкомышечных клеток [70]. . Интересно, что межэтническое исследование, сравнивающее литогенные свойства желчи от пациентов с холестериновым GSD из Чили (латиноамериканцы) и Нидерландов (голландцы), ясно показало значительные различия между образцами желчи из этих двух стран.Желчь чилийцев показала значительно более быстрое время зародышеобразования холестерина и более высокое содержание белка (в основном IgA и, вероятно, также муцина), несмотря на более низкий индекс насыщения холестерином [71]. Несмотря на то, что гистологический анализ не проводился, это исследование предполагает, что литогенный процесс и степень воспалительной реакции желчного пузыря различаются между этническими группами с различным риском GSD GBC [71]. Следует отметить, что коренные американцы и латиноамериканцы с высоким уровнем коренного происхождения имеют тенденцию к развитию GSD в раннем возрасте и с большей вероятностью развивают симптомы или осложнения и имеют несколько желчных камней, а не одиночные камни в желчном пузыре [72].Действительно, больший или больший объем желчных камней (в случае одиночных или множественных камней, соответственно) коррелирует с более высоким риском GBC, что, скорее всего, отражает историю длительной стадии носительства желчных камней и / или более высокое литогенное состояние [3]. Наконец, хроническая воспалительная инфильтрация, наряду с другими гистологическими изменениями, почти повсеместно наблюдается в желчном пузыре у пациентов с GSD [73]. Хотя текущая парадигма утверждает, что эти гистологические изменения вызваны асептическим химическим стимулом (т.е. литогенная желчь), в эпоху взрывных знаний, связанных с кишечной микробиотой, эта парадигма могла измениться. Последние данные свидетельствуют о том, что среда желчного пузыря у пациентов с GSD не является асептической; одно недавнее исследование идентифицировало микробиоту кишечного происхождения почти повсеместно в желчи большинства пациентов с GSD [74]. Взятые вместе, данные показывают, что хронический воспалительный инфильтрат присутствует в желчном пузыре пациентов с GSD и что эти изменения могут происходить на ранних стадиях формирования GSD и, по-видимому, различаются по интенсивности между популяциями с более высоким и низким риском, что свидетельствует о генетической предрасположенности.
В желчном пузыре распознаются две модели злокачественной трансформации: метаплазия – дисплазия – карцинома и последовательность аденома – карцинома [75–80]. Однако канцерогенез желчного пузыря, связанный с желчными камнями, происходит в основном по метаплазии-дисплазии-карциноме, а не через трансформацию ранее существовавшего доброкачественного опухолевого образования [81]. Эпителиальная метаплазия определяется как трансформация дифференцированного эпителия в другой дифференцированный эпителий и связана с повреждением тканей и хроническим воспалением [32].Метаплазия — частая находка в тканях желчного пузыря, подвергшихся воздействию желчных камней, с частотой от 59,5 до 95,0% для псевдопилорической и 9,5-58,1% для кишечной метаплазии [82,83]. Метаплазия также обнаруживается в 66% желчных пузырей с инфильтрирующей карциномой [73]. Кроме того, тяжесть поражений, обнаруженных в эпителии желчного пузыря, ухудшается по мере увеличения веса, объема и размера желчных камней [84]. Учитывая высокую частоту метаплазии при хроническом холецистите вместе с доказательствами генетических и эпигенетических изменений, уже присутствующих в метаплазии [42], метаплазия считается местом инициации рака желчного пузыря, по аналогии с опухолями других анатомических участков (например.g., плоскоклеточная метаплазия легких, связанная с длительным воздействием сигаретного дыма, пищевод Барретта с кислотным рефлюксом желудочного сока, кишечная метаплазия желудка с инфекцией Helicobacter pylori и ацинарно-протоковая метаплазия с панкреатитом) [85]. Кроме того, в желудке экспрессия человеческого интерлейкина-1β (IL-1β) у трансгенных мышей приводит к спонтанному воспалению желудка в отсутствие инфекции Helicobacter . Сверхэкспрессия IL-1β приводит к хроническому гастриту, метаплазии и дисплазии / карциноме высокой степени [86], что предполагает, что передача сигналов хронического воспаления в отсутствие инсульта может быть достаточной для запуска метаплазии.
Кроме того, метапластические поражения возникают при экспрессии ключевых факторов транскрипции, которые перенаправляют эпителиальный фенотип на другой тип, а метаплазия желчного пузыря часто коррелирует с экспрессией CDX2 [87], фактора транскрипции гомеобокса, участвующего в нормальном развитии кишечника. это также часто встречается при кишечной метаплазии пищевода и желудка [85]. Нормальный эпителий желчного пузыря не экспрессирует CDX2, а окружающие лейкоциты в основном состоят из Т-клеточных лимфоцитов (CD3 +; CD4 + и CD8 +) и популяций макрофагов (CD14 +; CD68 + и CD163 +) с низким или нулевым уровнем В-клеток (CD20 +) ().Напротив, CDX2-положительный метапластический эпителий желчного пузыря часто инфильтрируется более плотными популяциями Т- и В-лимфоцитов и макрофагов (). Кроме того, наличие метапластических изменений коррелирует с увеличением средней толщины стенки желчного пузыря [88]. Диффузное утолщение стенки желчного пузыря, определяемое как увеличение> 3 мм, измеренное ультразвуком, может наблюдаться при первичных воспалительных процессах желчного пузыря, таких как острый, хронический и бескаменный холецистит [89].
Популяции лейкоцитов на неметапластическом эпителии желчного пузыря.Популяции Т-клеток (CD3, CD4 и CD8) обычно наблюдаются в неметапластическом эпителии (отрицательный по CDX2) и подслизистой оболочке. Также в подслизистой оболочке желчного пузыря может наблюдаться низкая инфильтрация В-клеток (CD20) и макрофагов (CD14, CD68 и CD163).
Субпопуляции лейкоцитов в пропии пластинки желчного пузыря с эпителиальной атипией, связанной с кишечной метаплазией. Метапластический эпителий (CDX2-положительный) часто инфильтрируется популяциями Т-клеток, В-клеток и макрофагов с более высокой плотностью, чем наблюдаемая в нормальном эпителии, что является признаком хронического воспаления.
PTGS2 (также называемый циклооксигеназой-2 ЦОГ-2) представляет собой фермент, который участвует в биосинтезе простагландинов и, таким образом, участвует в стимулировании и разрешении воспаления. PTGS2 обычно не экспрессируется в нормальном эпителии желчного пузыря, но проявляется в диспластических поражениях с повышенной экспрессией при высокой степени злокачественности по сравнению с поражениями низкой степени. Повышенная экспрессия ЦОГ-2 особенно характерна для образцов со сверхэкспрессией р53 [90,91]. Аспирин, ингибитор циклооксигеназы, был связан со снижением риска GBC [92], аналогично тому, что наблюдалось при колоректальном раке [93].Было высказано предположение, что это снижение риска GBC может быть связано с ослаблением образования желчных камней, связанным с применением нестероидных противовоспалительных препаратов (НПВП) [94–96]; однако во многих исследованиях не удалось продемонстрировать снижение риска образования камней в желчном пузыре, связанного с применением НПВП [97–103]. Фактически, популяционное исследование случай-контроль в Шанхае, Китай, которое включало более 350 случаев GBC, более 1000 пациентов с камнями желчных путей и более 1000 здоровых взрослых, выявило обратную связь между использованием аспирина и GBC [отношение шансов (OR), 0.37; 95% доверительный интервал (ДИ) 0,17–0,88 по сравнению со здоровым контролем и OR 0,44; 95% ДИ, 0,19–0,99 по сравнению с пациентами с желчными камнями], но нет связи между аспирином и желчными камнями (OR, 0,92; 95% ДИ, 0,59–1,44 по сравнению со здоровым контролем) [92]. Эти результаты показывают, что НПВП не влияют на риск образования камней в желчном пузыре, но могут помочь снизить риск GBC, даже в контексте GSD. Необходимы дополнительные исследования для оценки возможности использования НПВП в профилактике GBC.
С-реактивный белок острой фазы (СРБ) давно признан маркером воспаления и привлек внимание как прогностический маркер будущих сердечно-сосудистых событий [104]. Вложенное исследование случай-контроль в рамках когорты Европейского проспективного исследования рака и питания (EPIC) показало, что высокие уровни CRP связаны с более высоким риском развития GBC. Хотя это исследование не сообщало истории GSD, вполне вероятно, что большинство случаев GBC были связаны с GSD в этой когорте, что предполагает, что GSD может вызывать воспалительное состояние, которое можно измерить в плазме за несколько лет до начала новообразования [105].В поддержку этой гипотезы, повышение уровня CRP в желчи было связано с увеличением количества присутствующих желчных камней [106]. Кроме того, недавнее исследование случаев GBC и контроля желчных камней в Китае и Чили обнаружило сильную связь между маркерами воспаления и GBC (Koshiol, представленный). В частности, CCL20, CRP, CXCL8, CXCL10, резистин и сывороточный амилоид A были сильно связаны в обеих исследуемых популяциях с OR в диапазоне от 7,2 (95% ДИ: 2,8–18,4) для CXCL10 до 58.2 (12,4–273,0) для CXCL8 (Koshiol, представлен). Хемокины часто ассоциировались с GBC по сравнению с камнями в желчном пузыре, что позволяет предположить, что хемокиновые системы могут иметь важное значение для канцерогенеза желчного пузыря. Механистическая характеристика хемокиновых систем может помочь определить цели для лечения [107].
Печеночные X-рецепторы (LXR), ядерные рецепторы, принадлежащие к семейству лиганд-активируемых факторов транскрипции, участвуют в контроле липидного гомеостаза, метаболизма глюкозы, пролиферации и развития ЦНС и были предложены в качестве мишени для лекарств при нескольких патологических состояниях из-за его связи с воспалительными состояниями [108].Важно отметить, что генотипы LXR-β, как было обнаружено, в значительной степени связаны с женщинами-пациентами с GBC или желчными камнями, предполагая, что полиморфизм LXRβ влияет на предрасположенность к раку желчного пузыря через эстроген и желчные камни [64]. У самок мышей, у которых был инактивирован LXRβ, развивались предопухолевые поражения желчного пузыря, которые у старых животных переросли в рак. LXRβ — / — женский желчный пузырь демонстрирует тяжелое воспаление с участками дисплазии и высокой плотностью клеток, гиперхромазией, метаплазией и аденомами в возрасте 11 месяцев, а также с активацией компонентов сигнального пути TGF-β.Удаление эстрогенов у животных, подвергшихся овариэктомии, предотвратило любые признаки воспаления, дисплазии или метаплазии. Авторы пришли к выводу, что предопухолевые поражения желчного пузыря у мышей LXRβ обусловлены сложным взаимодействием между отсутствием антипролиферативного и противовоспалительного действия LXRβ и гиперактивацией передачи сигналов TGF-β и действием эстрогенов [109]. Эта модель на мышах представляет особый интерес, поскольку у этих мышей развиваются раковые поражения на фоне воспалительного процесса, но без литиаза или инфекции, что позволяет предположить, что воспаление может приводить к канцерогенезу желчного пузыря независимо от агента, который его генерирует.
4. Другие воспалительные патологии, предрасполагающие к раку желчного пузыря
4.1. Аномальное расположение панкреатобилиарного протока (AAPBD)
AAPBD — это врожденная аномалия желчных протоков, связанная с высокой частотой GBC, с относительным риском от 167,2 до 419,6 раз выше среди пациентов с AAPBD, чем в общей популяции [110]. Накопленные данные указывают на то, что канцерогенез в желчном пузыре и желчном эпителии у пациентов с AAPBD представляет собой многоступенчатый процесс, который прогрессирует через последовательность метаплазия-дисплазия-карцинома, управляемая хроническим воспалением, подобно GBC, вызванному желчными камнями.Этот процесс, по-видимому, связан со смесью желчи и панкреатического сока, которая застаивается в желчном пузыре и желчном протоке, особенно в расширенном общем желчном протоке. При этом хроническом воспалении могут активироваться ферменты поджелудочной железы, фракция желчных кислот может измениться, и могут образоваться мутагенные или иногда канцерогенные вещества, что приведет к генетическим и морфологическим изменениям [111]. В большинстве образцов желчного пузыря с AAPBD наблюдается инфильтрация мононуклеарных клеток и фиброз под столбчатым эпителием выстилки и в субсерозной фиброзной ткани, как и при хроническом холецистите, вместе с интенсивной иммунореактивностью ЦОГ-2 в эпителиальных клетках, фибробластах, эндотелиальных клетках и гладкомышечных клетках. [112].Интересно, что распространенность мутаций KRAS выше в GBC, связанных с AAPBD, чем в GBC, не связанных с AAPBD [113,114]. Эта закономерность предполагает, что возникновение мутаций KRAS у пациентов с AAPBD больше связано с этиологией рака поджелудочной железы [111, 115], где распространенность KRAS очень высока [116], по сравнению с GBC, связанным с желчными камнями, где частота из мутаций KRAS мало или отсутствует [117,118].
4.2. Аутоиммунные заболевания
Аутоиммунные заболевания связаны с повышенным риском рака [119, 120], включая GBC [121].Недавно пять аутоиммунных состояний были связаны с более высокими стандартизованными коэффициентами заболеваемости GBC: целиакия, болезнь Крона, пернициозная анемия, язвенный колит и полимиозит / дерматомиозит [122]. Однако это исследование не смогло оценить первичный склерозирующий холангит (ПСХ), который является установленным фактором риска GBC [1]. ПСХ является классическим гепатобилиарным проявлением воспалительного заболевания кишечника и других иммуноопосредованных заболеваний и характеризуется хроническим разрушением желчных протоков и прогрессированием до терминальной стадии заболевания печени.Хроническое повреждение происходит в малых, средних и крупных желчных протоках с воспалительным и облитерирующим концентрическим перидуктальным фиброзом, приводящим к стриктурам желчных протоков [123]. Метаплазия желчного пузыря, дисплазия и карцинома возникают с высокой частотой у пациентов с ПСХ. Последовательность метаплазия-дисплазия-карцинома, наблюдаемая в условиях PSC, аналогична последовательности, предложенной для спорадических GBC. При гистологическом исследовании 72 желчных пузырей, удаленных от пациентов с ПСХ, были обнаружены сильные морфологические изменения. Лимфоплазмоцитарный хронический холецистит присутствовал в 49%, псевдопилорическая метаплазия в 96%, кишечная метаплазия в 50%, дисплазия в 37% и аденокарцинома в 14% образцов.Тесная связь между неоплазией желчного пузыря и внутрипеченочной желчной неоплазией поддерживает концепцию неопластического «эффекта поля» в желчных путях пациентов с ПСХ [124]. Около половины пациентов с ПСХ имеют патологические изменения желчного пузыря, а камни желчных протоков обнаруживаются в 25% случаев [125]. В другой серии из 102 пациентов с ПСХ, перенесших холецистэктомию, у 13% было образование желчного пузыря, из них у 7 были аденокарциномы, а у других 6 — доброкачественные образования. Среди пациентов с доброкачественными новообразованиями у 33% была сопутствующая дисплазия эпителия, в то время как у пациентов с первичным GBC у 57% была сопутствующая дисплазия [126].В другом исследовании дисплазия / карцинома желчного пузыря была обнаружена в 30% оперативных образцов, а признаки воспаления и фиброза стенки желчного пузыря были обнаружены почти в половине случаев дисплазии и карциномы желчного пузыря, соответственно [127]. Как показано на примере PSC, аутоиммунные заболевания, вероятно, увеличивают риск GBC из-за обострения воспаления желчных путей.
4.3. Бактериальные инфекции
Из множества воспалительных причин предрасположенности к раку инфекция постепенно стала считаться основным фактором индуцированного воспалением туморогенеза, при этом до 20% всех случаев рака во всем мире связаны с микробной инфекцией [21].Лучшим доказательством причинного бактериального участия в вызванном воспалением раке является инфекция, вызванная H. pylori , известным фактором риска аденокарциномы желудка [128]. Несколько родов бактерий были идентифицированы путем посева или ПЦР в желчном пузыре пациентов с холециститом и холелитиазом, включая, среди прочего, Salmonella, Escherichia, Klebsiella и Helicobacter [129]. Хотя роль этих микроорганизмов в канцерогенезе желчного пузыря до сих пор неизвестна, связь между S. Typhi и GBC — одни из наиболее охарактеризованных.
Ранние доказательства связи S. Typhi с осложнениями со стороны желчного пузыря через десятилетия после первичной инфекции были представлены Ботсфордом в 1941 году [130], который описал острый брюшной тиф и холелитиаз, возникшие через 43 года после брюшного тифа, и Axelrod et al. в 1971 г. [131], который описал холецистит и GBC у 80-летней женщины, перенесшей брюшной тиф в возрасте 13 лет. В 1979 году Welton et al. показали, что хронические носители брюшного тифа умирают от гепатобилиарного рака в шесть раз чаще, чем в контрольной группе [132].Подобные выводы были позже получены в других исследованиях, в которых обнаружена эпидемиологическая связь между хроническим носительством брюшного тифа и риском гепатобилиарного рака [133–136]. Исследования, проведенные в Северной Индии, регионе высокой эндемичности как для брюшного тифа, так и для GBC, показали OR для GBC 8,5 [137], 9,2 [138], 14 [139] и 22,8 [140] среди хронических носителей брюшного тифа, что подтверждает сильная связь между этими патологиями. В других регионах, таких как Шанхай, ассоциации между S. Тиф и рак желчных путей из-за очень низкой распространенности хронических носителей в этой популяции [141]. Однако в этой же исследуемой популяции липополисахарид (ЛПС), основной компонент внешней мембраны грамотрицательных бактерий, и два белка пути ЛПС были связаны с GBC по сравнению с желчными камнями, что позволяет предположить, что бактериальные инфекции в более широком смысле могут иметь отношение к переход от желчных камней к GBC (Ван Дайк, рукопись в стадии подготовки). В районах с более высокой распространенностью S. Typhi, исторически или в настоящее время, связь с GBC удивительно постоянна (Koshiol, рукопись в стадии подготовки).
Донгол и соавторы выполнили клинический анализ микробиологического посева желчи и профилирование антисывороток, классифицировав пациентов как положительные по S. Typhi и Paratyphi (N = 48), положительные по бактериям, отличным от Salmonella (N = 226). ) или отрицательный для Salmonella (N = 1103). По сравнению с контрольной группой они обнаружили, что желчный пузырь с положительным результатом на Salmonella демонстрирует более высокую частоту вздутий, воспалений и эмпием (гной в полости желчного пузыря) и более выраженную полиморфно-ядерную инфильтрацию, чем лимфоцитарную инфильтрацию, с 13% из Salmonella-положительных желчных пузырей . образцы с массивным инфильтратом нейтрофилов возле просвета по сравнению с 4% отрицательных культур (P <0.05) и 5% положительных результатов посевов Salmonella , отличных от (P <0,05), соответственно. Кроме того, еще 15% образцов желчного пузыря с положительным результатом на Salmonella имели острый хронический холецистит (инфильтрат нейтрофилов возле просвета с лимфоцитарным инфильтратом и дисплазией слизистой оболочки) по сравнению с 5% (P <0,05) и 7% ( P <0,05) отрицательных посевов и положительных посевов Salmonella , отличных от , соответственно [142]. В инфицированном желчном пузыре наблюдается гистопатологическое повреждение, характеризующееся разрушением эпителия и массивной инфильтрацией нейтрофилов, сопровождающейся локальным увеличением провоспалительных цитокинов [143].
Эпидемиологические исследования, проведенные в эндемичных регионах, показали прочную связь между хроническим носительством брюшного тифа и желчными камнями; около 90% хронически инфицированных носителей имеют камни в желчном пузыре [144]. Salmonella , в частности S . Typhi особенно эффективен в производстве биопленок [145]. В мышиной модели 129 × 1 / SvJ у мышей, получавших литогенную диету, постоянно образовывались желчные камни, которые усиливали колонизацию и сохранение серовара Typhimurium в ткани желчного пузыря и желчи после инфекции.Присутствие этого материала желчных камней было связано со значительным количеством Salmonellae , которое со временем увеличивалось, и у этих мышей, содержащих желчные камни, наблюдалось 3-логарифмическое увеличение фекального выделения серовара Typhimurium по сравнению с инфицированным контролем без желчных камней [146]. Кроме того, гены капсулы O-антигена Salmonella индуцируются желчью и специфически необходимы для образования биопленок на холестериновых камнях в желчном пузыре [147]. Эти результаты предполагают, что биопленка Salmonella на холестериновых камнях желчного пузыря значительно облегчает колонизацию желчного пузыря во время хронической бессимптомной инфекции.
Недавно были получены молекулярные доказательства связи инфекции Salmonella с развитием GBC. Salmonella enterica индуцировала злокачественную трансформацию у предрасположенных мышей, органоидов желчного пузыря и фибробластов с мутациями TP53 и амплификацией MYC. Этот процесс зависел от активации путей MAPK и AKT для поддержания трансформации. После инфицирования, Salmonella стабильно активирует ряд генов интерфероновой реакции, которые подавляют воспалительные реакции хозяина, что свидетельствует о отпечатке нормального ответа клетки-хозяина на бактериальную инфекцию [9].Кроме того, недавние исследования показывают, что разные серовары Salmonella вызывают разные иммунные ответы. Например, капсульный полисахарид S. Typhi, по-видимому, подавляет воспаление слизистой, в то время как нетифоидные серовары Salmonella (например, S . Typhimurium, Salmonella Enteritidis) вызывают сильные воспалительные реакции [148, 149]. S. Typhi может способствовать хроническому носительству путем подавления острого воспаления, потенциально приводящего к хроническому измененному иммунному ответу.
Хотя на популяционном уровне мало что известно об истинном канцерогенном действии Salmonella в отсутствие камней в желчном пузыре, эпидемиологические данные, подтверждающие, что хроническая инфекция Salmonella является фактором риска для GBC, последовательны [8]. Мы знаем, что инфекция Salmonella особенно эффективна при наличии камней в желчном пузыре. И камни в желчном пузыре, и бактерии способны вызывать воспалительную реакцию, поэтому можно предположить, что совместное появление этих агентов повысит риск развития GBC.
5. Выводы и перспективы на будущее
Доказательства, собранные GBC, и сравнения с более изученными новообразованиями убедительно подтверждают гипотезу о том, что устойчивое хроническое воспаление способствует канцерогенезу в желчном пузыре, где литогенная желчь, желчные камни, токсины и, возможно, бактериальные инфекции вызывают воспалительный процесс. это не решено и сохраняется в течение десятилетий (). Этот сценарий открывает новые возможности для исследований. Во-первых, GBC — идеальная модель для изучения роли воспаления в канцерогенезе.Создание моделей на животных, которые воспроизводят процесс канцерогенеза желчного пузыря человека, все еще требует развития. Такие модели будут способствовать исследованиям канцерогенеза, профилактики и диагностики GBC. Во-вторых, хотя считается, что холецистэктомия способствует снижению заболеваемости Джи-би-си в западных странах [150, 151] и в настоящее время используется в качестве средства для снижения бремени Джи-би-си в Чили [152], все еще есть возможности для изучения реализации стратегий, направленных на то, чтобы уменьшить возникновение камней в желчном пузыре и / или ослабить хроническое воспаление, например, с помощью фармакологического вмешательства.Наконец, хотя GBC относительно редко встречается во всем мире и менее изучен, чем другие солидные опухоли, включая другие злокачественные опухоли печени и желчевыводящих путей, он представляет собой проблему общественного здравоохранения для нескольких стран. Существует потребность в механистических исследованиях и сложных экспериментальных моделях канцерогенеза желчного пузыря, чтобы получить знания, которые помогут улучшить профилактику и клиническое ведение групп высокого риска.
Хроническое воспаление и развитие рака желчного пузыря. Постоянное повреждение, наносимое литогенной желчью, желчными камнями и, возможно, инфекциями и аутоиммунными заболеваниями, делает возможными повторяющиеся циклы разрушения и регенерации эпителия.Изменение структуры эпителия прогрессирует от воспаленной ткани к накоплению метапластических и диспластических поражений, что в конечном итоге приводит к возникновению инвазивной карциномы. Высвобождение медиаторов воспаления вызывает набор популяций лейкоцитов (особенно лимфоцитов и макрофагов) с увеличением количества активных форм кислорода (АФК) и сверхэкспрессии ЦОГ-2. В этом контексте мутация TP53 предпочтительно выбирается на ранних стадиях, способствуя дальнейшему повреждению ДНК и прогрессированию опухоли.ROS = активные формы кислорода; СОХ-2 = циклооксигеназа 2; IM = кишечная метаплазия; и PM = псевдопилорическая метаплазия.
Выражение признательности
Этот обзор был поддержан FONDECYT Fondo Nacional de Investigación y Tecnología (JAE-3140308, CA-3140426, PG-11130515, JFM-1130303 и JCR-1130204), Финансовый центр исследований и исследований Prioritarias ACCDiS (JCR-15130011) и общие средства из Программы внутренних исследований Национального института здоровья и Национального института рака, Отдел эпидемиологии и генетики рака (DCEG).Мы благодарим Марию Хосе Апуд за ее экспертную работу в дизайне фигур.
Сокращения:
| GBC | Рак желчного пузыря | ||
| GSD | желчнокаменная болезнь | ||
| PTGS2 (COX-2) | простагландин-синтаза-синтаза-цитохлорид | ||
| AAPBD | аномальное расположение панкреатобилиарного протока | ||
| PSC | первичный склерозирующий холангит | ||
| LXRs стопа | Liver X Receptors | 9048 X-рецепторы | 9





