Диета при хроническом панкреатите: правила питания при обострении
Оглавление
Диета при таком заболевании поджелудочной железы, как панкреатит, не менее важна, чем лекарственная терапия. Именно благодаря постоянному правильному питанию пациентам удается избежать обострений патологии. Сбалансированный рацион дает возможности и для устранения целого ряда неприятных симптомов заболевания (сильная боль, тошнота и рвота, лихорадка и др.).
Факторы появления и симптомы панкреатита
Для патологии характерны воспалительные рецидивы, вследствие которых нарушаются нормальная работа поджелудочной железы и выделение ей достаточного количества ферментов и гормонов. Заболевание опасно своим прогрессированием. При развитии панкреатита ткани органа разрушаются, что приводит к необратимым последствиям для всего организма.
Важно! Воспалительные явления могут быть следствием острой стадии заболевания или самостоятельным проявлением, если больной страдал желтухой, циррозом печени, атеросклерозом, злоупотребляет алкоголем или жирной, вредной пищей.
К основным симптомам панкреатита относят:
- Тяжесть в желудке (преимущественно после еды)
- Выраженный болевой синдром с правой стороны в области пупка
- Отрыжку
- Изжогу
- Вздутие живота
- Острое ощущение голода
- Сладковатый привкус в ротовой полости
- Неприятный запах изо рта
- Тошноту
- Частый стул маслянистого и жидкого характера
- Отечность век
- Сухость губ
- Покраснение кожи
Также для заболевания характерны накопление в организме пациента токсических веществ и нарушение производства инсулина.
Особенности специального рациона
Диета при панкреатите должна содержать большое количество белка, но при этом минимальное количество жиров. Такие компоненты следует устранить из рациона во время обострений полностью или свести их к минимуму. Это позволит улучшить состояние поджелудочной железы и желчного пузыря. В некоторых случаях допускается употребление небольшого количества растительного масла. Необходимость в белке обусловлена тем, что он позволяет быстро обновить травмированные участки поджелудочной железы. Больным можно употреблять и углеводы, но при условии отсутствия предрасположенности к сахарному диабету. Если такая предрасположенность имеется, следует отказаться от продуктов, в составе которых содержится сахар.
Это позволит улучшить состояние поджелудочной железы и желчного пузыря. В некоторых случаях допускается употребление небольшого количества растительного масла. Необходимость в белке обусловлена тем, что он позволяет быстро обновить травмированные участки поджелудочной железы. Больным можно употреблять и углеводы, но при условии отсутствия предрасположенности к сахарному диабету. Если такая предрасположенность имеется, следует отказаться от продуктов, в составе которых содержится сахар.
Диета при хроническом панкреатите (при обострениях) также подразумевает и сокращение употребления соли. Снизить отечность железы позволит полное исключение соленой пищи всего на 2-3 недели. Если при сильных обострениях пациент страдает от выраженных симптомов заболевания, ему назначают только жидкую и протертую пищу. Употреблять любые блюда следует в теплом виде. Отказаться нужно от слишком горячих и холодных напитков и пищи.
Еду для больного следует готовить без приправ и специй. Важно тщательно отслеживать и свежесть используемых продуктов. Если пациент питается кашами, готовить их нужно исключительно на воде. Полезными будут овощные пюре, нежирный творог, чай (без сахара и некрепкий), пюреобразные супы.
Важно тщательно отслеживать и свежесть используемых продуктов. Если пациент питается кашами, готовить их нужно исключительно на воде. Полезными будут овощные пюре, нежирный творог, чай (без сахара и некрепкий), пюреобразные супы.
Постепенно в рацион можно вводить белки яиц, постные мясо и рыбу, слегка подсушенный хлеб, желе. Порции должны быть небольшими, но употреблять пищу нужно достаточно часто, чтобы не допускать возникновения ощущения голода, при котором многие больные жалуются на выраженный дискомфорт в области органа. Лучше всего перейти на шестиразовое питание.
Когда назначается диета при панкреатите?
Обычно питание пациентов корректируется сразу же после постановки диагноза. Особенно важно обратить внимание на рацион в период обострения. При выраженной симптоматике панкреатита специалисты советуют придерживаться принципа «холод, голод и покой». В первые 2-3 дня после приступа разрешается пить некрепкий и несладкий чай, минеральную негазированную воду и отвар шиповника. При выходе из голодания постепенно включают в рацион блюда, которые хорошо сказываются на состоянии воспаленного органа. К ним относят отвар овса и овощные бульоны.
При выходе из голодания постепенно включают в рацион блюда, которые хорошо сказываются на состоянии воспаленного органа. К ним относят отвар овса и овощные бульоны.
При обострениях специальное щадящее дробное питание рекомендовано как минимум на 6-12 месяцев. За такой срок орган может полностью восстановиться. Одновременно с этим сам пациент уже успеет привыкнуть к полезному питанию. Диета при панкреатите не станет для него слишком жесткой и требующей высокого уровня самоконтроля. При этом она будет залогом выздоровления. Благодаря ей можно избежать не только оперативного вмешательства, но и длительной и часто утомительной консервативной терапии.
Важно! Как лечение, так и диета при панкреатите поджелудочной железы у мужчин и женщин, вне зависимости от симптомов, должны назначаться исключительно врачом. Только гастроэнтеролог владеет точной информацией о состоянии поджелудочной железы, а также обладает специальными профессиональными навыками и знаниями.
Продукты, которые рекомендуются и не рекомендуются при болезни
При панкреатите следует употреблять такие продукты, как:
- Нежирное мясо: постную свинину, телятину, курицу, крольчатину, индюшатину
- Нежирную рыбу: щуку, камбалу, минтай и треску
- Крупы: овсяную, манную и рис
- Макаронные изделия из твердых сортов пшеницы
- Кисломолочную продукцию
- Овощи: картофель, кабачки, свеклу, морковь
Молоко разрешается употреблять только в составе каш, молочных супов и киселей. При улучшении состояния можно дополнить рацион неострыми и нежирными сортами сыра. При приготовлении паровых омлетов можно использовать яйца. Из фруктов лучше отдать предпочтение некислым яблокам. Их можно запекать и употреблять в виде пюре.
Категорически запрещены:
- Репчатый лук
- Щавель и шпинат
- Редис, редька, хрен и ревень
- Болгарский перец
- Приправы и острые специи
- Алкогольная продукция
- Кофе и какао
- Газированные напитки
Во время диеты при хроническом панкреатите следует постараться исключить гусиное и утиное мясо, баранину и сало.
Не рекомендуется при приготовлении блюд использовать маргарин, а также говяжий и свиной жир. Хотя бы на время обострений следует отказаться от масел в любом виде.
Преимущества лечения в МЕДСИ
- Опытные гастроэнтерологи. Наши врачи располагают необходимыми знаниями и навыками для комплексного ведения пациентов с хроническим панкреатитом (в том числе при обострении). Гастроэнтерологи могут подобрать подходящую диету, которая учитывает все особенности образа жизни больного и его текущее состояние
- Современные методы диагностики. Для обследований применяются лабораторные и инструментальные техники.
 Мы располагаем необходимым оборудованием экспертного уровня, что позволяет быстро поставить диагноз и назначить адекватную терапию в любых ситуациях (в том числе при возникших осложнениях)
Мы располагаем необходимым оборудованием экспертного уровня, что позволяет быстро поставить диагноз и назначить адекватную терапию в любых ситуациях (в том числе при возникших осложнениях) - Современные методы лечения. Мы используем как отработанные способы, так и собственные авторские наработки, позволяющие проводить терапию хронического панкреатита при обострении быстро и грамотно, с минимальным дискомфортом для пациента, с использованием эффективных и безопасных лекарственных средств. Особое внимание уделяется правильному питанию
- Подключение к работе с пациентом других специалистов. При необходимости больные могут наблюдаться не только у гастроэнтерологов, но и у диетологов, эндокринологов и др.
Если вы хотите, чтобы наш гастроэнтеролог провел необходимое лечение и подобрал оптимальный для вас рацион питания, позвоните по номеру + 7 (812) 336-33-33.
Диета при панкреатите поджелудочной железы
Время чтения: 3 мин. , 16 сек.
, 16 сек.
Панкреатит — это заболевание поджелудочной железы, связанное с развитием воспалительного процесса в органе. При этом заболевании возникает нарушение поступления ферментов, участвующих в пищеварении, из поджелудочной железы в двенадцатиперстную кишку. Пищеварительные ферменты остаются в самой железе и разрушают ее. Главной причиной данного заболевания является неправильное и несбалансированное питание. Именно поэтому в основе лечения панкреатита стоит правильно подобранная диета.
Общие правила. Длительность диеты.
Общие правила диеты:
- Необходимо избегать переедания
- Питание должно быть дробным, не менее 5-6 раз в сутки
- Еда должна быть теплой. Необходимо полностью исключить горячие и холодные блюда.

- Исключить из рациона сырые овощи и фрукты и продукты богатые клетчаткой.
- Готовить пищу нужно только рекомендуемыми способами.
Питание при панкреатите в период обострения:
В случае обострения панкреатита необходимо исключить прием любой пищи на несколько суток. Во время голодания показано пить очищенную негазированную воду. Суточный объем воды должен составлять не более 1,5-1,7 литра. После стихания болевых ощущений и симптомов в рацион можно добавить низкокалорийную пищу в небольшом объеме (жидкие каши, овощные супы, паровые котлеты из рыбы или мяса куры).
В случае не соблюдения диеты при остром течении панкреатита заболевание может быстро перейти в хроническую форму.
Заметьте! В острый период противопоказано санаторно-курортное лечение: лучше обратиться в стационар.
Питание при хроническом панкреатите:
Хроническая форма панкреатита требует педантичного подхода к питанию. Правильное питание, без нарушений, позволяет избежать обострений. Каждое обострение приводит к недостаточности железы.
Правильное питание, без нарушений, позволяет избежать обострений. Каждое обострение приводит к недостаточности железы.
При хронической форме панкреатита необходимо соблюдать диету № 5.
- Дробное питание до 6 раз в сутки
- количество соли не более 6 грамм
- отварные блюда в протертом или измельченном виде
- питание с повышенным содержанием белка
Список разрешенных продуктов:
|
Крупа (гречка, овсянка, рис, манка) |
Крупу необходимо варить на воде, с последующим добавлением молока и небольшого количества сливочного масла |
|
овощи |
Овощи можно употреблять в виде первых блюд (овощные супы, суп-пюре) или в виде измельченных отварных кусочков. Из разрешенных плодов – картофель, морковь, зеленый горошек, кабачок, тыква, свекла и цветная капуста. |
|
фрукты |
Сырые фрукты употреблять в пищу нельзя. Можно есть фруктовые варенья, пастилу, печеные яблоки, компоты, кисели. |
|
мясо |
Можно употреблять нежирные сорта мяса: говядину, телятину, крольчатину и мясо куры. Мясо готовится на пару и в виде суфле или котлет из фарша. |
|
рыба |
В еду допускается белая речная рыба, приготовленная на пару. |
|
яйцо |
Допускает приготовление парового омлета из 1 куриного яйца или 3 перепелиных яиц. |
|
Молочные продукты |
Молочные продукты должны быть минимальной жирности |
|
хлеб |
Можно есть небольшое количество пшеничного хлеба 2-3-х дневной давности |
Список полностью или частично ограниченных продуктов:
|
Финики, виноград, бананы |
Провоцируют вздутие живота |
|
Грибы, бобовые, капуста белокачанная |
Содержат грубую клетчатку |
|
Копчености, соленое, фаст фуд, продукты содержащие консерванты и красители |
Раздражают слизистую пищеварительного тракта |
|
Субпродукты (печень, язык, сердце, почки и др. |
Содержат много холестерина |
|
Любые жареные и жирные блюда |
Приводят к обострению заболевания |
|
Молочные продукты с высоким процентом жирности |
Высок риск развития обострения или осложнения заболевания |
Меню питания при панкреатите. Режим питания.
Необходимо помнить, что питание при панкреатите должно быть дробным, порции небольшого размера. Пищу надо отваривать или готовить на пару и измельчать.
Все продукты должны быть качественными без содержания консервантов и красителей.
Соблюдение режима питания и правил диеты позволит избежать осложнений и обострения заболевания.
Рецепты диетических блюд при панкреатите:
Примерное меню диеты при панкреатите:
Завтрак: гречневая каша сваренная на воде с добавлением нежирного молока. Отвар шиповника.
Второй завтрак: запеченое яблоко. Травяной чай
Обед: овощной суп с куриными фрикадельками. Паштет из телятины. Компот из сухофруктов
Полдник: творожная запеканка из нежирного творога. Кисель
Ужин: Паровая рыбная котлета с отварными овощами и рисом. Травяной чай
Перед сном: компот из шиповника.
«Правильный выбор санатория является значительным шагом на пути к сохранению и приумножению здоровья. «Горный» – это курортный комплекс, объединивший опыт и знания российской и советской курортологии. Наличие современного медицинского оборудования и инновационных установок, профессионализм персонала и любовь к своему делу послужат залогом в продлении долголетия» – главный врач санатория Караулов Александр Олегович.
их роль и функции, что делать при недостатке пищеварительных ферментов?
Многие считают, что пищеварение происходит исключительно в желудке, однако это не так. В пищеварении участвует множество органов, и этот процесс начинается в момент жевания, а заканчивается в кишечнике. На протяжении всего пути на пищевой комок воздействуют различные ферменты, благодаря которым пища расщепляется на отдельные компоненты и усваивается. Что это за вещества, откуда они берутся и почему ферменты так важны для здоровья?
Какие бывают пищеварительные ферменты и для чего они нужны?
Пищеварительные ферменты — это белковые структуры, в состав которых входят различные аминокислоты. Но если не углубляться в химический состав, пищеварительные ферменты — вещества, участвующие в переваривании пищи. Они «разбирают» любую еду на базовые элементы и помогают нам усваивать полезные вещества.
Человеческий организм вырабатывает огромное количество пищеварительных ферментов — десятки разных типов. Для чего так много? Дело в том, что каждый выполняет определенную часть работы. Одни ферменты могут расщеплять только молочный сахар — лактозу, другие отвечают за расщепление белковой пищи, третьи занимаются жирами, четвертые — исключительно желатином и так далее.
Обработка пищи начинается еще во рту, при пережевывании пищи. Слюнные железы выделяют фермент под названием альфа-амилаза. Он отвечает за расщепление крахмала и превращение его в сахар. Любой способен проследить, как работает альфа-амилаза: попробуйте пожевать две–три минуты небольшой кусочек хлеба, и вы почувствуете, как во рту появится сладковатый привкус. В хлебе содержится очень много крахмала, который под воздействием фермента распадается на легкоусвояемые сахара.
Пройдя обработку слюной, пища попадает в желудок, где за нее принимается целый ряд ферментов: пепсин, расщепляющий белки, желатиназа, которая обрабатывает коллаген (например, хрящи и соединительные ткани мяса), амилаза, которая завершает начатое во рту расщепление крахмала, липаза, с помощью которой начинается усвоение жиров.
Большинство людей думает, что в желудке все и заканчивается, но нет — здесь все только начинается. Пища, обработанная только желудочными ферментами, не может полноценно усвоиться. Поэтому она направляется в двенадцатиперстную кишку и там подвергается обработке ферментами, вырабатываемыми поджелудочной железой. Их очень много, не менее 20. Только в кишечнике компоненты пищи наконец-то начинают всасываться и усваиваться организмом.
Процесс продолжается в тонком кишечнике, там присутствуют отдельные ферменты, которые завершают «разборку» соединений, начатую в верхних отделах ЖКТ. На этой стадии всасывается большая часть полезных веществ, а окончательную обработку пища проходит в толстом кишечнике, где процесс завершают ферменты, вырабатываемые нашей кишечной микрофлорой.
Над обработкой пищи трудится огромное количество ферментов, и сбой на любом из этапов приводит к различным проблемам с пищеварением: диарее или запорам, вздутию, изжоге, отрыжке. В норме вся система работает как часы, тем не менее иногда ферменты не могут выполнять свою работу как положено.
Причины нехватки ферментов для пищеварения
Наш организм вырабатывает ограниченное количество ферментов, и иногда их не хватает для полноценного переваривания пищи.
Нехватка пищеварительных ферментов, как правило, обусловлена функциональными или органическими заболеваниями органов пищеварения. К ферментной недостаточности приводят воспалительные заболевания поджелудочной железы (в частности, панкреатит), воспаления кишечника, гастрит, патологии печени и желчевыводящих путей, патологии слизистой оболочки кишечника, характерные для некоторых аутоиммунных заболеваний.
На заметку
Ферменты и энзимы — синонимы. Однако в русскоязычной медицинской литературе чаще употребляется первый термин.
Но гораздо чаще симптомы нехватки ферментов проявляются не по причине того, что организм вырабатывает слишком мало этих веществ, а потому что количество пищи слишком велико. Да, переедание и несбалансированная диета — наиболее распространенные причины проблем с пищеварением.
В среднем объем желудка составляет около литра, а если вы съедаете больше, пищеварительной системе сложно выработать достаточно ферментов для усвоения такого количества пищи. Ситуацию может усугубить слишком жирная и острая еда, а также алкоголь.
Плохое переваривание пищи грозит не только бурлением в животе, изжогой и болью. Последствия могут быть и более тяжелыми. Непереваренные фрагменты пищи — это отличная питательная среда для патогенной микрофлоры, которая в норме не представляет опасности. Но если таких условно безопасных бактерий станет слишком много, они могут нанести вред здоровью. Например, сахар — отличное питание для грибка, вызывающего кандидоз. Не полностью расщепленная пища и сама по себе вредит внутренним органам. В частности, нерасщепленные жиры раздражают стенки кишечника и вызывают воспаление.
Сколько нужно ферментов для пищеварения и как нормализовать ферментацию?
Для того чтобы определить количество ферментов, нужно пройти врачебное обследование. Но вы и сами можете заметить признаки того, что ферментов не хватает. Недостаток этих веществ проявляется такими неприятными симптомами, как:
- изжога после еды;
- чувство тяжести в верхней части живота;
- вздутие и метеоризм;
- отрыжка;
- неприятный привкус во рту;
- тошнота, особенно после жирной пищи;
- обильный жидкий стул.
Эти симптомы неприятны сами по себе, но длительная ферментная недостаточность вызывает и более существенные неприятности. Поскольку при нехватке ферментов пища усваивается плохо, организм недополучает основные нутриенты, витамины и минералы. Такая ситуация приводит к мышечной слабости и быстрой утомляемости из-за недостатка белков, жиров и углеводов, а также из-за анемии, так как железо из пищи не поступает в кровь. Вдобавок это провоцирует нервное истощение, ухудшает состояние волос, кожи и ногтей, снижает остроту зрения, служит причиной проблем в половой сфере и множества других болезненных состояний, вызванных дефицитом витаминов.
Если вам знакомы перечисленные выше симптомы, необходимо срочно обратиться к врачу. Как мы уже говорили, нехватка ферментов для пищеварения может быть следствием серьезных болезней и патологических состояний. Если же обследование не выявит никаких заболеваний, врач порекомендует изменить диету. К счастью, у здоровых людей пересмотр меню может практически полностью снять симптомы недостатка пищеварительных ферментов и наладить работу ЖКТ. Главный принцип диетотерапии при недостатке ферментов для пищеварения — умеренное дробное питание. Есть желательно понемногу, но каждые три–четыре часа. Нелишне исключить очень жирную пищу — бекон и сало, еду, приготовленную во фритюре. Также придется отказаться от алкоголя и неумеренного потребления сладостей и выпечки. А вот фрукты и овощи, прошедшие термическую обработку, помогают пищеварению, поэтому их следует есть больше.
Для улучшения пищеварительных процессов у здоровых людей врачи могут посоветовать дополнительно принимать ферментные препараты. Они дополнят действие собственных ферментов и помогут справиться с большими объемами пищи или непривычной едой. Однако не стоит воспринимать такие средства как панацею и разрешение есть что угодно и в любых количествах. Они все же предназначены для особых ситуаций — например, обильных и продолжительных праздничных обедов. Ферментные препараты не могут заменить сбалансированную диету.
Определенно, не стоит заниматься самолечением, используя ферментные средства. Они хорошее подспорье, но назначать препараты такого типа должен врач. Не забывайте, что недостаток ферментов для пищеварения часто является проявлением патологий, требующих серьезной терапии.
что к ней относится, почему появляются боли и тошнота и что можно принять после жирной пищи?
Наверняка многим знакомы неприятные ощущения после обильного сытного обеда с большим количеством масла или жирных соусов. Жиры — вовсе не абсолютное зло, они нужны нашему организму. Однако даже небольшой переизбыток жиров в пище может привести к изжоге, боли и чувству тяжести в желудке. Почему это происходит, от каких продуктов следует отказаться и как бороться с симптомами диспепсии, диареей, метеоризмом после приема жирной пищи?
Что относится к жирной пище?
Жиры содержатся практически во всех продуктах питания: мясе, рыбе, молоке, крупах, минимально даже в некоторых овощах и фруктах. К продуктам с самым высоким содержанием жира относятся сало и бекон, сливочное и растительное масла, орехи, колбасные изделия, сыр, сливки, шоколад. Употреблять их стоит дозированно. Например, 70 граммов сала (а это всего несколько небольших ломтиков) полностью покрывают суточную потребность взрослого человека в жирах. Но, помимо этой крошечной порции сала, человек обязательно съест и другие продукты, содержащие жиры, и в результате к концу дня норма будет превышена в два–три раза.
Некоторые продукты выглядят очень полезными и диетическими, но не стоит обманываться: в них тоже очень высокое содержание жиров. Они не видны и практически неощутимы на вкус, что и создает иллюзию «легкости». К продуктам с такими «сюрпризами» относятся докторская колбаса (она состоит из жиров на треть), легкий майонез, в котором содержится до 40% жиров, а также попкорн и кукурузные хлопья, сухарики, любые замороженные полуфабрикаты в панировке, печенье, творог и йогурты, многие соусы — в частности, горчица и кетчуп.
Диетологи советуют употреблять один грамм жиров на один килограмм массы тела в сутки. В среднем около трети калорий должно поступать именно из жирных продуктов. Нехватка жиров сказывается на внешности: кожа становится сухой, а волосы и ногти — слабыми и ломкими. Страдает эндокринная система (особенно у женщин), сердце и сосуды, когнитивные функции. Но и увлекаться жирной пищей не стоит: избыток жиров еще опаснее, чем их недостаток.
Жирные кислоты: польза или вред?
Итак, мы уже сказали, что и врачи, и диетологи согласны: жиры полезны, но не все. Однако следует разобраться в этом вопросе чуть подробнее, чтобы различать разные типы жиров.
Жирные кислоты бывают насыщенными и ненасыщенными. Молекулярная структура у них отличается, и они по-разному воздействуют на организм.
Насыщенные жирные кислоты содержатся в сыре, мясе, сливочном масле и некоторых растительных маслах — пальмовом, кокосовом. При злоупотреблении этим видом жиров есть риск нажить проблемы с сосудами, воспаления, может повыситься уровень холестерина и нарушиться метаболизм.
На заметку
Утверждение, будто от «хороших» жиров не поправляются — миф. Все без исключения жиры очень калорийны, и избыток калорий, полученных из оливкового масла, откладывается на боках точно так же, как избыток калорий, полученных из бекона и колбасы.
Ненасыщенные жирные кислоты входят в состав полезных жиров, которые содержатся в рыбе и большинстве растительных масел, в орехах и бобах. Эти жиры необходимы организму: они поддерживают целостность клеточных оболочек, помогают работе эндокринной системы, улучшают прочность и эластичность сосудов, участвуют в регуляции метаболизма и кроветворении. Словом, они жизненно необходимы, но в человеческом организме ненасыщенные жирные кислоты не вырабатываются, они могут поступать только с пищей.
Тем не менее, и этот вид может принести проблемы: избыток ненасыщенных кислот повышает риск возникновения заболеваний почек и печени.
Почему тошнит и болит желудок после жирной пищи
Вы наверняка замечали, что иногда после жирного обеда возникают неприятные ощущения: боль, тошнота, изжога, отрыжка. Почему так происходит и о чем это говорит?
Первая причина боли и тошноты — собственно переедание. Объем желудка невелик — пол-литра в пустом состоянии. Оцените объем съеденного: если порция по размеру превышает маленькую бутылочку минералки, вы съели больше положенного. Но причина неприятных ощущений кроется не только в механическом растяжении желудка. Для переваривания пищи наш организм вырабатывает ферменты. Однако если вы съели слишком много, ферментов попросту не хватает, и пищеварение замедляется. В таких условиях печень вынуждена работать на пределе возможностей, чтобы выделять как можно больше желчи. Из-за этого мы ощущаем тяжесть в животе и тошноту, боль в желудке и другие расстройства пищеварения.
Впрочем, чтобы почувствовать недомогание, не обязательно объедаться. Жирная пища сама по себе — тяжелое испытание для пищеварительной системы. Жиры перевариваются очень медленно, задерживаются в желудке слишком долго и вызывают раздражение слизистой оболочки, что и приводит к изжоге. А если запивать еду алкоголем, раздражение только усилится.
И, наконец, жир оказывает определенное воздействие на работу сфинктеров пищевода. Он нарушает работу клапана, который отделяет желудок от пищевода. Из-за этого содержимое желудка забрасывается в пищевод вместе с кислотой, что вызывает ожоги, отрыжку и неприятный привкус во рту.
Все эти симптомы знакомы даже людям без установленных заболеваний ЖКТ. Но они проявляются гораздо сильнее, если человек страдает заболеваниями желудочно-кишечного тракта или болезнями печени, поджелудочной железы и желчного пузыря. Боль от жирной пищи и тошнота после еды могут быть признаками гастрита, патологий желчевыводящих путей, панкреатита, синдрома раздраженного кишечника, язвы желудка. Систематическое переедание может значительно ухудшить течение болезни и вызвать обострение.
Даже если у вас нет никаких проблем со здоровьем, жирная пища может привести к развитию множества заболеваний и патологических состояний. В первую очередь — к появлению лишнего веса, который является предпосылкой к целому ряду заболеваний, от проблем с опорно-двигательным аппаратом, сердечно-сосудистой и эндокринной системами до ферментной недостаточности.
Жирная пища не должна составлять основу диеты. Не исключайте жиры полностью, но контролируйте их количество и качество и постарайтесь по возможности исключить из рациона пищу, которая одновременно является жирной, соленой и острой: это очень неблагоприятное сочетание для желудка. Питаться желательно часто, но маленькими порциями — размер одной порции не должен превышать размер кулака. Так вы поможете ЖКТ справляться с расщеплением белков, жиров и углеводов.
|
РЕКОМЕНДУЮТСЯ |
!!! ЗАПРЕЩАЮТСЯ!!!! |
|
Хлеб и хлебобулочные изделия |
|
|
Вчерашний пшеничный хлеб, пшеничные сухари, малосладкое галетное печенье. |
Свежий хлеб, ржаной хлеб, сдобное тесто, жареные и свежие печёные пирожки, блины, вареники, пицца, песочное сладкое печенье. |
|
Крупяные и макаронные изделия |
|
|
Гречневая, геркулесовая, овсяная, манная, рисовая каши, протертые, полувязкие, сваренные на воде или пополам с молоком низкой жирности, суфле, пудинги, запеканки. |
Пшено, перловая, ячневая, кукурузная крупы, рассыпчатые каши, макаронные изделия, бобовые. |
|
МЯСО |
|
|
Нежирное нежилистое мясо: говядина, кролик, курица, телятина протёртые или рубленые; в отварном или паровом виде (котлеты, кнели, бефстроганов из отварного мяса) |
Жирные сорта мяса: баранина, свинина, гусь, утка, печень, почки, мозги; жареное, тушеное, копчёное мясо, колбасы, консервы. |
|
РЫБА |
|
|
Нежирная отварная, в виде суфле, кнелей, котлет, кусков — судак, треска, окунь, щука, серебристый хек |
Жирная, жареная, тушеная, копчёная, запеченная, солёная, консервированная; икра, морепродукты. |
|
СУПЫ |
|
|
Овощные, вегетарианские, слизистые из круп (овсяный, перловый, рисовый, манный), суп-крем из выварённого нежирного мяса, вегетарианские борщи, протёртые супы с картофелем, морковью. |
Супы на мясном и рыбном бульоне, отваре грибов, окрошка, молочные супы, щи, невегетарианский и зелёный борщ, свекольник. |
|
СОУСЫ И ПРЯНОСТИ |
|
|
Фруктово-ягодные подливки, несладкие или сладкие |
Томатные подливки и соусы, поджарки, острые соусы, пряности. |
|
ЯЙЦА |
|
|
Омлет белковый паровой из 1—2 яиц в день, ½ желтка в день в блюдах |
Крутые, жареные |
|
МОЛОКО И МОЛОЧНЫЕ ПРОДУКТЫ |
|
|
Нежирное молоко в блюдах, творог некислый свежеприготовленный, паровые пудинги; свежий кефир и цельное молоко в ограниченном количестве при хорошей переносимости, нежирный неострый сыр, нежирные йогурты |
Молочные продукты высокой жирности, кумыс, сладкие, сливки, мороженое, сметана, майонез, жирный и солёный сыр. |
|
ЖИРЫ |
|
|
Сливочное масло несоленое и растительное рафинированное масло в готовых блюдах в ограниченном количестве. |
Маргарин, куриный, гусиный, бараний, свиной жир, сало. |
|
ОВОЩИ |
|
|
Картофель, морковь, кабачки, цветная капуста в виде пюре и паровых пудингов, в отварном, протёртом или печёном виде. |
Белокочанная капуста, баклажаны, репа, редька, редис, брюква, шпинат, щавель, чеснок, лук, бобовые, перец, в т. ч. сладкий, огурцы, помидоры, грибы. |
|
ФРУКТЫ И ЯГОДЫ |
|
|
На десерт: яблоки некислых сортов, печёные, бананы, клубника, черника, чёрная смородина в ограниченном количестве, протёртые компоты, кисели, мусс, желе на ксилите или сорбите |
Цитрысовые, гранаты, кислые яблоки, виноград, финики, инжир. |
|
СЛАСТИ |
|
|
Мёд в ограниченном количестве, зефир, пастила на ксилите или сорбите. |
Кексы, кондитерские изделия, шоколад, варенье, мороженое. |
|
НАПИТКИ |
|
|
Слабый чай, малосладкий или с ксилитом и сорбитом; соки: банановый, клубничный, морковный — в небольшом количестве. Минеральные воды: Боржом, Поляна Купель, Поляна Квасова, Свалява через 1,5—2 часа после еды; Славяновская, Ессентуки № 4 и № 20, Лужанская — за 1 час до еды. Минеральные воды применяют по ¼-1/2 стакана, комнатной температуры без газа |
Алкогольные напитки, крепкий чай, кофе, соки: апельсиновый, грейпфрутовый, яблочный, виноградный, гранатовый, абрикосовый, мультивитамин. |
Лечебное питание при хроническом панкреатите
Дата публикации: .
Врач-реабилитолог отделения
медицинской реабилитации Тарапова ИН
Комплекс лечебных мероприятий, в том числе лечебное питание, способствует уменьшению воспалительного процесса не только в самой поджелудочной железе, но и в органах, анатомически и функционально связанных (двенадцатиперстной кишке, гепатобиллиарной системе и желудке).
В период ремиссии больные получают диету достаточной калорийности ( 3000 ккал), полноценную по количеству пищевых веществ. При обострении заболевания назначается несколько голодных дней или строго щадящая диета с ограничением калорийности. Рекомендуется отдавать предпочтение белкам молочного происхождения, разрешается употребление нежирного мяса и рыбы. Уменьшение количества жира диктуется нарушениями кишечного переваривания в связи с недостаточностью поступления панкреатической липазы. Жир рекомендуется в количествах, не превышающих 60 -70г. в сутки. А при тяжелом течении – 50г., предпочтение отдают растительным маслам ввиду их лучшего эмульгирования. Углеводы следует ограничивать, особенно легковсасываемых, так как они оказывают раздражающее действие на секреторную функцию поджелудочной железы. Пища при панкреатите должна приниматься небольшими порциями 5-6 раз в день. Дробное питание в строго определенное время способствует правильному режиму работы пищеварительных желез, влияя на функцию желчевыделения и секрецию других пищеварительных желез. Все холодные блюда запрещаются, так как они могут вызвать спазм привратника, дуоденоспазм, спазм сфинктера Одди. Исключаются все продукты, раздражающие слизистую оболочку желудка и двенадцатиперстной кишки и обладающие сокогонным действием (острые, соленые блюда, маринады, бульоны, продукты богатые эфирными маслами, пряности, приправы), запрещается алкоголь. Все блюда готовятся в вареном виде или на пару, протертые. Калорийность – 2100 ккал, состав: белков — 100 г., жиров — 70 г., углеводов — 250 г. Количество жидкости – 1,5- 2 литра. Поваренная соль — 8-10 грамм. Вес суточного рациона – 3 кг. Температура пищи от 57 до 62 градусов, холодных не ниже 15 градусов.
Перечень рекомендуемых блюд
Хлеб и хлебобулочные изделия: сухари из высших сортов белого хлеба, тонко нарезанные и неподжаристые.
Супы: на слабом обезжиренном мясном или рыбном бульоне с добавлением слизистых отваров, паровых или сваренных в воде мясных или рыбных кнелей, фрикаделек, яичных хлопьев, варенного и потертого мяса.
Блюда из мяса и рыбы: паровые или сваренные мясные и рыбные котлеты, кнели, фрикадельки, суфле из отварного мяса и рыбы. Мясо нежирных сортов, обезжиренное( говядина, курица, индейка без кожи, кролик). Мясной фарш пропускают через мясорубку 3-4 раза, рыба только свежая, нежирных сортов (судак, карп, щука, треска).
Гарниры: Протертые каши на воде или обезжиренном мясном бульоне (рисовая, овсяная, гречневая, манная). Исключаются все бобовые и макаронные изделия.
Блюда из яиц: яйца в ограниченном количестве — не более 1 шт в день, только в блюдах по кулинарным показаниям. При хорошей переносимости разрешаются диетические яйца всмятку в виде паровых омлетов не более 2 шт. в день.
Сладкие блюда: сахар до 40 г. в день, кисели, желе их черники, спелых груш и других ягод и фруктов, богатыми дубильными веществами.
Молочные продукты: свежий творог, натуральный или протертый, а так же в виде парового суфле.
Жиры: масло сливочное в ограниченном количестве, не жарить, добавлять в готовые блюда по 5г. на порцию.
Напитки: чай натуральный, какао на воде, отвар шиповника, черемух
Диета при остром панкреатите
Дата публикации: .
Хирургическое отделение № 1 (экстренное)
Врач-хирург Скипор Л.В.
Острый панкреатит — это острое воспаление поджелудочной железы. Поджелудочная железа играет важную роль в процессе пищеварения и обмена веществ. При пищеварении поджелудочная железа выделяет ферменты, которые поступают в двенадцатиперстную кишку и способствуют перевариванию белков, жиров и углеводов. Такой фермент, как трипсин, способствует усвоению белков, липаза — жиров, амилаза — углеводов.
Острое воспаление поджелудочной железы сопровождается от еком, некрозом, а нередко и нагноением или фиброзом, при этом замедляется выделение ферментов, нарушается нормальное пищеварение.
Развитию панкреатита способствуют переедание, длительное употребление жирной, жареной, острой, слишком горячей или слишком холодной пищи, злоупотребление алкоголем, недостаточное употребление белков. Заболевание может развиться на фоне хронического холецистита, желчнокаменной болезни, сосудистых поражений, язвенной болезни, инфекционных заболеваний, разных интоксикаций, травм поджелудочной железы.
Питание при остром панкреатите направлено на обеспечение максимального покоя поджелудочной железы, уменьшение желудочной и панкреатической секреции. В первые 6 — 7 дней назначают голодание, можно пить минеральные воды без газа (Боржоми, Ессентуки №4) в небольшом количестве, маленьким глотками.
Пищу необходимо в течение первых 2-х недель готовить с ограничением соли. Питание должно быть 5-6 раз в день небольшими порциями. Пищу принимать в теплом виде (45-60 С). Необходимо, чтобы блюда были жидкими, полужидкими по консистенции. Тушеные и жареные блюда запрещены, рекомендуется употреблять перетертую пищу.
В диету на 6-7-й день заболевания включают:
- Супы овощные; супы вегетарианские; супы слизистые из круп (овсяной, перловой, рисовой, манной), протертые с картофелем и морковью.
- Крупяные и макаронные изделия: геркулесовая, овсяная, манная, рисовая каши, протертые, полувязкие, сваренные на воде или пополам с молоком низкой жирности; суфле, пудинги, запеканки.
- Мясо: говядина, кролик, курица, телятина, индейка в протёртом или паровом виде (котлеты, кнели, бефстроганов из отварного мяса).
- Рыба: нежирная отварная, в виде суфле, кнелей, котлет (судак, треска, окунь, щука, серебристый хек).
- Яйца: омлет белковый паровой из 1 — 2 яиц в день, 1/2 желтка в день в блюдах.
- Молоко и молочные продукты: нежирное молоко в блюдах, творог некислый свежеприготовленный, паровые пудинги; свежий кефир и молоко в ограниченном количестве при хорошей переносимости, нежирный йогурт.
- Жиры: сливочное масло несолёное и растительное рафинированное масло в готовых блюдах в ограниченном количестве.
- Овощи: картофель, морковь, кабачки, цветная капуста в виде пюре и паровых пудингов, в отварном, протертом или печёном виде.
- Хлеб и хлебобулочные изделия: вчерашний пшеничный хлеб, пшеничные сухари, малосладкое галеточное печение.
- Фрукты и ягоды: яблоки некислых сортов печеные, бананы, клубника, черника, чёрная смородина в ограниченном количестве, протертые компоты, кисели, мусс, желе на ксилите или сорбите.
- Сладости: мёд в ограниченном количестве, зефир, пастила на ксилите или сорбите.
- Напитки: слабый чай малосладкий или с ксилитом либо сорбитом; соли банановый, клубничный, морковный в небольшом количестве. Минеральные воды употребляются по 1/2 — 2/3 стакана, комнатной температуры (без газа).
Далее рацион можно расширить за счет паровых пудингов из свежего сыра, белкового омлета, морковного пюре.
Исключаются на длительное время жареные блюда, копчености, соления, маринады, консервы, сало, сметана, сдобное тесто, сливки, алкогольные напитки. Больным панкреатитом необходимо придерживаться диеты около года, опасаться переедания.
CPE Monthly: Chronic Pancreatitis — Today’s Dietitian Magazine
Февраль 2016 Выпуск
CPE Monthly: Хронический панкреатит — узнайте о патофизиологии, симптомах, причинах и вариантах лечения, а также о MNT для оптимизации статуса питания пациентов
Меган Баумлер, доктор философии, RD
Сегодняшний диетолог
Т. 18 № 2 стр. 44
Предлагаемые коды обучения CDR: 3005, 3020, 5000, 5220
Предлагаемые показатели эффективности CDR: 8.1.5, 10.2.5, 10.2.5, 10.2.9
Уровень CPE: 3
Пройдите этот курс и заработайте 2 CEU в нашей учебной библиотеке непрерывного образования
Мужчина 45 лет поступил в отделение неотложной помощи с жалобами на сильную боль в животе. Это его четвертая госпитализация в отделение неотложной помощи за восемь месяцев из-за болей в животе. По результатам предыдущих госпитализаций был поставлен диагноз панкреатит, который разрешился самопроизвольно. В результате этого визита снова ставят диагноз панкреатит, и его помещают в больницу.После компьютерной томографии лечащий врач объясняет пациенту, что он видит морфологические изменения в поджелудочной железе, которые указывают на фиброз. Врач диагностирует у мужчины хронический панкреатит и назначает консультацию по питанию.
Панкреатит — наиболее распространенное заболевание, поражающее поджелудочную железу и характеризующееся воспалением органа. Панкреатит может быть острым, большинство случаев которого проходит без последствий, хотя небольшой процент случаев острого панкреатита заканчивается смертью.Для сравнения: хронический панкреатит — это продолжающееся воспаление, приводящее к повторяющимся травмам тканей и морфологическим изменениям, которые необратимо нарушают нормальную функцию поджелудочной железы.1
Заболеваемость хроническим панкреатитом оценивается у четырех из каждых 100000 человек в Соединенных Штатах.2 В 2009 году хронический панкреатит стал причиной 19 724 госпитализаций и обошелся здравоохранению в 172 миллиона долларов США.3 Хронический панкреатит критически влияет на состояние питания, поскольку центральной роли поджелудочной железы в пищеварении и гомеостазе глюкозы.
Поджелудочная железа — это орган, выполняющий как эндокринную (секреция в кровоток), так и экзокринную (секреция в протоки) функцию. Хотя островки Лангерганса, часть железы, содержащая альфа- и бета-клетки, выделяющие гормоны в кровоток, составляют от 1% до 2% органа, эндокринные функции поджелудочной железы могут быть лучше известны из-за их взаимосвязи. к диабету. 4 Альфа- и бета-клетки регулируют уровень инсулина в сыворотке крови, секретируя глюкагон и инсулин соответственно.Остальные 98% ткани поджелудочной железы содержат клетки, которые участвуют в синтезе и секреции пищеварительных ферментов, способствующих пищеварению и всасыванию пищи. Поджелудочная железа имеет самый высокий уровень синтеза белка по сравнению с любым другим органом или тканью в организме. Пищеварительные ферменты синтезируются в ацинарных клетках в неактивной форме и секретируются в желчные протоки при потреблении еды. Из желчного протока ферменты выводятся в проксимальный отдел двенадцатиперстной кишки и быстро активируются ферментом, присутствующим на микроворсинках клеток, выстилающих тонкий кишечник, известным как энтеропептидаза, для облегчения переваривания пищи, так что углеводы, аминокислоты и липиды могут всасываться.Если ферменты аномально активируются в органе, ферменты переваривают ткань поджелудочной железы, что называется самовоспламенением, и вызывает воспаление.6
Обычно поджелудочная железа защищена от самопереваривания, но определенные ситуации, такие как непроходимость желчных протоков, алкоголизм, врожденные аномалии и специфические генетические мутации, повышают риск ранней активации зимогенов (неактивных пищеварительных ферментов) до их секреции в желчный проток. Воспаление поджелудочной железы или панкреатит нарушает экзокринную, а со временем и эндокринную функции поджелудочной железы, что в конечном итоге приводит к недоеданию из-за недостаточного количества пищеварительных ферментов и диабету.7 К сожалению, нет никакого вмешательства или лечения панкреатита, кроме фармакологического лечения для контроля боли и лечения последующих осложнений, таких как ферментная недостаточность, недоедание и диабет. Кроме того, пациентам с хроническим панкреатитом обычно требуется заместительная терапия ферментами поджелудочной железы (PERT) при недостаточности пищеварительных ферментов и вмешательство при диабете. патофизиология заболевания и действующие рекомендации по МНТ.
Этот курс непрерывного образования рассматривает патофизиологию, симптомы, причины и методы лечения хронического панкреатита. Кроме того, он исследует MNT, используемый для оптимизации статуса питания у пациентов, страдающих хроническим панкреатитом.
Внутренняя защита от панкреатита
Поджелудочная железа, которая находится под желудком и рядом с двенадцатиперстной кишкой, состоит из клеток разных типов, которые равномерно распределены между головкой и хвостом органа.Альфа- и бета-островковые клетки выполняют эндокринную функцию, синтезируя метаболические гормоны глюкагон и инсулин, соответственно, которые выбрасываются в кровоток для поддержания гомеостаза сывороточной глюкозы. Ацинарные клетки собираются, как виноград, вокруг протоков, которые в конечном итоге соединяются, образуя желчный проток. Ацинарные клетки синтезируют и секретируют неактивные пищеварительные ферменты, такие как липаза, амилаза и трипсиноген, вместе с водой и бикарбонатом.9
Когда пищевые углеводы, липиды и белки попадают в тонкий кишечник, нервные и эндокринные клетки, выстилающие двенадцатиперстную кишку, стимулируются к секреции холецистокинина и ацетилхолина в кровоток, которые стимулируют ацинарные клетки поджелудочной железы.При стимуляции ацинарные клетки секретируют неактивные пищеварительные ферменты в протоки, которые в конечном итоге попадают в двенадцатиперстную кишку через желчный проток. Попадая в двенадцатиперстную кишку, неактивный трипсиноген активируется энтеропептидазой, ферментом щеточной каймы двенадцатиперстной кишки. Трипсин, активный протеолитический (переваривающий белок) фермент, активирует другие ферменты, включая липазу, амилазу и карбоксипептидазу. После активации ферменты гидролизуют пищевые углеводы, пептиды и липиды до глюкозы, аминокислот и жирных кислот, соответственно, которые абсорбируются в один слой эпителиальных клеток, отделяющих просвет желудочно-кишечного тракта от кровотока.Эти питательные вещества мигрируют через клетки и попадают в кровоток, откуда организм может использовать их по мере необходимости.
В нормальных физиологических условиях поджелудочная железа защищена от самопереваривания или самопереваривания органа активными пищеварительными ферментами с помощью трех механизмов. Во-первых, ферменты синтезируются в неактивной форме, поэтому они не могут переваривать сам орган. Во-вторых, неактивные ферменты или зимогены содержатся в отдельном клеточном компартменте внутри ацинарных клеток, называемом гранулами зимогена.Это предотвращает воздействие зимогенов на гидролазы или другие ферменты, которые могут активировать зимогены. Наконец, защитная молекула, называемая ингибитором трипсина, которая присутствует в ацинарных клетках, инактивирует небольшие количества активного трипсина, прежде чем он вызовет какое-либо повреждение.10 Обычно небольшое количество трипсиногена активируется в трипсин в ацинарных клетках. Ингибитор трипсина способен предотвращать самопереваривание, пока активный трипсин находится на нормальном низком уровне.В условиях панкреатита большее количество аберрантно активированного трипсина оказывается слишком большим для ингибитора трипсина.4
Патофизиология и этиология
Панкреатит вызывается преждевременной активацией трипсина в самой поджелудочной железе, что приводит к самоперевариванию. Самостоятельное пищеварение поджелудочной железы приводит к сильной боли в животе и, со временем, к хроническому воспалению, которое вызывает необратимые морфологические изменения и фиброз.4 Воспалительная реакция вызывает замену ацинарных и островковых клеток нефункциональными фиброзными клетками, что приводит к снижению функции поджелудочной железы.Помимо фиброза, к другим морфологическим изменениям относятся кальцификаты, которые также могут развиваться внутри органа.4 К счастью, поджелудочная железа является очень резервным органом, а это означает, что почти 90% функций может быть потеряно до того, как появятся какие-либо клинические проявления.1
Хотя этиология панкреатита влияет на скорость прогрессирования заболевания, у пациентов с хроническим панкреатитом, вызванным алкоголизмом, в среднем развивается экзокринная недостаточность примерно через пять лет после постановки диагноза.11 Прогрессирующий характер хронического панкреатита в конечном итоге приводит к неспособности вырабатывать достаточное количество пищеварительных ферментов. адекватно переваривать обычно потребляемое количество пищи.Эндокринная поджелудочная железа также поражена, и у большинства людей с хроническим панкреатитом развивается панкреатогенный диабет из-за потери островковых клеток.12 Диабет классифицируется как панкреатогенный, если он вызван заболеванием поджелудочной железы, а не аутоиммунным заболеванием, как в случае типа 1. или нарушение обмена веществ, как в случае типа 2.12 Большинство случаев панкреатогенного диабета вызвано хроническим панкреатитом.12
При хроническом панкреатите трипсин может аберрантно и непрерывно активироваться в органе рядом нарушителей, которые делятся на четыре категории: токсичные метаболиты, генетические мутации, аутоиммунное заболевание и длительная непроходимость.Также существует значительное количество необъяснимых случаев хронического панкреатита, этиология которого классифицируется как идиопатическая.
Наиболее частой причиной постоянного хронического воспаления поджелудочной железы в США является алкоголизм.13 Алкогольный хронический панкреатит чаще встречается у мужчин, и типичный возраст, в котором ставится диагноз, составляет от 40 до 50 лет4. Механизмы, лежащие в основе взаимосвязи между алкоголизмом и панкреатитом, неясны, но было показано, что хроническое воздействие на поджелудочную железу токсичных побочных продуктов метаболизма алкоголя увеличивает окислительный стресс, что приводит к некрозу (гибели тканей) и продукции цитокинов.13 Цитокины вызывают активацию звездчатых клеток и образование фиброзной ткани, которая со временем заменяет ацинарные и островковые клетки.14 Одно исследование показало, что 80 г алкоголя, или примерно восемь стандартных алкогольных напитков в день в течение шести-12 лет, являются необходимо, чтобы вызвать панкреатит.15 В то время как большинство людей с хроническим панкреатитом борются с алкоголизмом, менее 10% людей с алкоголизмом заболевают панкреатитом, что указывает на то, что есть дополнительный фактор или факторы, работающие в сочетании с алкоголизмом, которые должны присутствовать, чтобы вызвать болезнь .12,15 Воспаление, вызванное воздействием алкоголя, может повысить чувствительность поджелудочной железы к другим триггерам, таким как плохое питание, потребление никотина и генетическая предрасположенность. Тем не менее полное воздержание от алкоголя имеет первостепенное значение для замедления прогрессирования алкогольного панкреатита16
Другие этиологические факторы в категории токсичных метаболитов включают курение сигарет и диету. В прошлые десятилетия была известна связь между курением сигарет и риском хронического панкреатита, но только недавно эта связь была доказана как причинная.Североамериканское исследование панкреатита, многоцентровое исследование в Соединенных Штатах, в которое вошли 540 пациентов с хроническим панкреатитом, определило курение как независимый фактор риска панкреатита, поскольку те, кто курил дольше и больше, подвергались большему риску панкреатита, когда все другие переменные были равны.17 В другом исследовании у курильщиков хронического панкреатита было больше диагнозов кальцификации поджелудочной железы и диагнозов диабета, чем у некурящих, независимо от употребления алкоголя.18 Одно исследование после контроля потребления алкоголя показало, что у курильщиков вдвое выше риск хронического панкреатита. чем некурящие.19
Пищевые жиры и белки являются макроэлементами, которые стимулируют секрецию поджелудочной железы, но неясно, является ли сама диета независимым фактором риска хронического панкреатита. В одном из немногих исследований, в которых диета рассматривалась как возможный фактор риска хронического панкреатита, исследователи провели кросс-секционное тематическое исследование, чтобы изучить взаимосвязь между потреблением жира и возрастом диагноза хронического панкреатита и развитием осложнений20. в исследовании 24 человека придерживались диеты с высоким содержанием жиров, у них был значительно более молодой средний возраст постановки диагноза (37 лет по сравнению с 46 годами) и у них была более высокая вероятность постоянной боли в животе по сравнению с теми, кто придерживался диеты с низким содержанием жиров.Прежде чем исследователи смогут сделать какие-либо выводы, необходимы дополнительные исследования диеты как независимого фактора риска хронического панкреатита.
За последние пару десятилетий было признано, что несколько наследственных факторов предрасполагают к риску хронического панкреатита. У людей с генетическими мутациями, вызывающими панкреатит, заболевание обычно возникает рано, в возрасте до 10 лет, в отличие от более позднего начала, типичного для хронического панкреатита, связанного с алкоголизмом.21 Большинство пациентов с наследственным хроническим панкреатитом имеют мутацию в ген трипсиногена.22 Несколько мутаций в этом гене, который кодирует пищеварительный фермент трипсин, связаны с риском хронического панкреатита. Наиболее распространенная мутация в этом гене, вызывающая хронический панкреатит, затрагивает участок фермента, где он расщепляется и становится инактивированным. Этот сайт важен для инактивации, если трипсин аномально активируется в поджелудочной железе. Мутация не позволяет инактивировать фермент, который предрасполагает носителя к панкреатиту.
Любая мутация в гене ингибитора секреторного трипсина поджелудочной железы, PSTI, может быть наследственной причиной хронического панкреатита.22 PSTI подавляет трипсин, который активируется в поджелудочной железе в качестве защитного механизма против панкреатита. Когда этот защитный механизм не работает, даже небольшое количество активированного трипсина в поджелудочной железе может привести к панкреатиту, поскольку активация трипсина является самовоспроизводящейся. Некоторые мутации в гене трансмембранного регулятора проводимости муковисцидоза (CFTR) были связаны с хроническим панкреатитом даже при отсутствии диагноза муковисцидоза. Ген CFTR кодирует хлоридный канал, присутствующий в клетках поджелудочной железы и легких.Нарушение нормальной секреции хлоридов из-за мутаций в гене CFTR вызывает густые вязкие выделения, которые могут вызвать панкреатит из-за блокировки. У людей с муковисцидозом развивается недостаточность поджелудочной железы.
Аутоиммунный панкреатит (AIP) — это редкая и недавно выявленная, но все более широко признанная причина хронического панкреатита с ранним началом, хотя патология неясна. 23 Существует два типа AIP, которые трудно отличить диагностически от карциномы поджелудочной железы.Что отличает AIP от карциномы поджелудочной железы, так это повышенный уровень сывороточного иммуноглобулина G (IgG) и / или IgG4; наличие аутоантител; визуализация, которая выявляет фиброз; и увеличение и / или сужение протока.23 В остальном клиническая картина аналогична. Поэтому методы исследования сыворотки и визуализации имеют решающее значение для предотвращения ненужной резекции поджелудочной железы из-за неправильного диагноза рака поджелудочной железы, поскольку AIP можно лечить стероидами. 23 AIP — это единственный известный тип панкреатита, который имеет успешный протокол нехирургического лечения.24 Изучаются процессы, лежащие в основе заболеваний, вызываемых AIP, а также рекомендации по диагностике и лечению.
Pancreas divisum (PD) — врожденная аномалия, которая может вызывать хронический панкреатит из-за нарушения нормального оттока секрета. Обструктивный панкреатит возникает, когда секреты поджелудочной железы не могут быть выведены в двенадцатиперстную кишку. В этой среде секреция поджелудочной железы накапливается в протоке поджелудочной железы, и трипсин активируется под давлением, которое нарастает, что приводит к повреждению тканей.БП является относительно распространенным явлением, по оценкам, присутствует у 5–11% населения США.25 Во время нормального эмбрионального развития два протока поджелудочной железы сливаются, образуя главный проток поджелудочной железы. При БП отсутствие этого слияния приводит к появлению двух дренажных протоков от поджелудочной железы, оба из которых уже, чем нормальный одиночный сросшийся проток. Узкие протоки, особенно в сочетании с другим фактором риска, таким как генетическая предрасположенность, увеличивают вероятность блокирования секреции поджелудочной железы и последующего панкреатита.26 Многие люди с БП не проявляют клинических проявлений, но у подгруппы людей с БП разовьется хронический панкреатит, который можно лечить хирургическим путем резекцией и дренированием поджелудочной железы.25
Хотя выявлено несколько причин панкреатита, этиология от 10% до 30% случаев неясна и классифицируется как идиопатическая. Существуют вероятные генетические мутации и воздействия окружающей среды, которые еще предстоит идентифицировать, которые предрасполагают людей к панкреатиту. Фактически, в одном исследовании было проведено генетическое секвенирование у пациентов с идиопатическим панкреатитом у взрослых для поиска новых генетических мутаций.27 Из 67 субъектов у 44 была обнаружена мутация, но у большинства из них не было семейного анамнеза.
Об этиологии панкреатита известно много, но очевидно, что дополнительные исследования помогут более точно определить основные процессы, лежащие в основе множественных причин хронического панкреатита. В конечном итоге это приведет к более высокой вероятности успешного лечения и ведения.
Симптомы и диагностика
И острый, и хронический панкреатит вызывают сильную боль в животе, которая является основной причиной обращения пациентов за медицинской помощью.4 Острый панкреатит легко диагностируется на основании повышенного уровня амилазы и липазы в сыворотке крови, наиболее чувствительных и специфических измерений. 4 Хронический панкреатит сложнее диагностировать, особенно если заболевание находится на ранних стадиях, во время которых морфологические изменения ткани могут быть неопределяемыми. если вырабатывается достаточное количество пищеварительных ферментов и уровень пищеварительных ферментов в сыворотке нормален. Универсального золотого стандарта диагностики хронического панкреатита не существует. Биопсия поджелудочной железы, вероятно, будет наиболее показательной, но она не идеальна, потому что пораженная ткань может быть неоднородной по всему органу и, следовательно, может быть пропущена, а сама процедура биопсии может вызвать острый панкреатит.28 Более того, не существует стандартной шкалы морфологических изменений для диагностики хронического панкреатита.
Недавно Американская ассоциация поджелудочной железы опубликовала рекомендации по диагностике хронического панкреатита.29 Три уровня диагностики включают окончательные, вероятные или недостаточные доказательства, основанные на диагностическом алгоритме STEP (обследование, томография, эндоскопия и тестирование функции поджелудочной железы). Морфологические изменения, которые указывают на окончательный или вероятный диагноз, включают кальцификаты в ткани поджелудочной железы или в протоке, расширение протока и псевдокисты.Морфологические изменения могут быть идентифицированы с помощью медицинских методов визуализации, включая рентгенограммы брюшной полости, УЗИ брюшной полости, компьютерную томографию и магнитно-резонансную томографию (МРТ) / магнитно-резонансную холангиопанкреатографию (MRCP), каждый из которых имеет свои сильные и слабые стороны28. рентгенограммы и ультразвук могут выявить изменения протоков и кальцификаты, которые присутствуют при запущенном хроническом панкреатите. КТ более чувствительны для выявления изменений в ткани поджелудочной железы.28 Наиболее чувствительным методом визуализации является МРТ, поскольку с ее помощью можно уловить изменения, которые происходят на более ранней стадии заболевания, например, в боковых ветвях протока поджелудочной железы. 28 Стимуляция секретином MRCP также может быть полезна для выявления более ранних изменений при хроническом панкреатите. 30,31 Эндоскопическая ретроградная холангиопанкреатография может выявить изменения в протоке поджелудочной железы, но может вызвать острый панкреатит и поэтому не рекомендуется для диагностических целей.28 Эндоскопическое ультразвуковое исследование оказалось очень специфичным и чувствительным к морфологическим изменениям, характерным для панкреатита, но Результаты варьировались в зависимости от того, кто проводил сонографию.32
Функциональные изменения происходят при хроническом панкреатите из-за замены нормальных ацинарных клеток поджелудочной железы фиброзной тканью. Оценка функциональных изменений для диагностики хронического панкреатита включает прямое или косвенное измерение секреции пищеварительных ферментов. Непосредственное измерение ферментов полезно, потому что это с большей вероятностью позволит выявить легкую и умеренную раннюю стадию нарушения функции поджелудочной железы, в то время как косвенные измерения побочных ферментативных продуктов не так чувствительны.28 Выявление болезни на ранних стадиях дает преимущество, так как вмешательства, направленные на отсрочку или предотвращение осложнений, могут быть реализованы немедленно. Внутривенная инъекция гормона секретина для стимуляции ацинарных клеток и измерения последующей выработки бикарбоната поджелудочной железой является золотым стандартом для непосредственного тестирования внешнесекреторной функции поджелудочной железы.28 Жидкий объем панкреатического секрета собирается из двенадцатиперстной кишки, и если концентрация бикарбоната составляет менее 80 мМ / L, секреторная функция поджелудочной железы нарушена.33 Инъекции холецистокинина также могут использоваться для стимуляции поджелудочной железы и последующего измерения концентрации липазы в секрете поджелудочной железы. Уровень липазы менее 780 000 МЕ / л на литр указывает на нарушение секреторной функции поджелудочной железы. 34
Золотым стандартом диагностики стеатореи, наличия жира в стуле, который является косвенным показателем экзокринной функции поджелудочной железы, является 72-часовой анализ фекального жира. Обычно стеатореи не наблюдается до тех пор, пока хронический панкреатит не станет более развитым.Пациенты потребляют 100 г жира в день в течение трех дней, а их стул собирают и оценивают. Более 7 г фекального жира в день указывает на мальабсорбцию жира. 28 Недостатком этого теста является то, что стеаторея не является специфической для панкреатита и может быть вызвана другим состоянием, например глютеновой болезнью или избыточным бактериальным ростом тонкой кишки. Другой способ измерения мальабсорбции жира, который более удобен и специфичен для панкреатической недостаточности (ИП), — это тест на эластазу поджелудочной железы. Эластаза — это фермент поджелудочной железы, который обычно содержится в стуле, поскольку он не расщепляется при прохождении через кишечник.Если поджелудочная железа функционирует нормально, вырабатывая адекватные пищеварительные ферменты, определенное количество фекальной эластазы будет присутствовать в стуле. Уровень эластазы в фекалиях от 100 до 200 мкг / г стула указывает на умеренный ИП, тогда как менее 100 указывает на тяжелый ИП.35 Недостатком теста на эластазу кала является то, что он недостаточно чувствителен для выявления умеренного ИП.
MNT
Помимо обезболивания, цели лечения хронического панкреатита в основном связаны с питанием.Боль почти всегда лечится анальгетиками, иногда безуспешно 28. Хирургические подходы к лечению хронического панкреатита включают процедуру Пуэстоу для облегчения гипертензии протока поджелудочной железы и панкреатэктомию с аутотрансплантацией островков; хотя последнее все еще встречается довольно редко, исследования показывают успех.36 PERT также связан со снижением боли.37 Использование антиоксидантов для контроля боли показало многообещающие, но, поскольку исследования были непоследовательными, и особенно потому, что они могут увеличивать риск смертности, их не рекомендуется использовать для обезболивания.38
Три основные цели в области питания пациентов с хроническим панкреатитом — это потребление достаточного количества калорий, профилактика и / или коррекция дефицита питательных веществ и успешный PERT. Поддержание адекватного количества калорий может быть проблемой из-за сочетания снижения аппетита, увеличения потребности в калориях и мальабсорбции. Было показано, что у людей с хроническим панкреатитом потребление энергии в состоянии покоя увеличивается на 20–50%. 39,40 Рекомендации Европейского общества парентерального и энтерального питания по калорийности при хроническом панкреатите составляют 35 ккал / кг / день.41 Исторически считалось, что диета с низким содержанием жиров подходит для лечения хронического панкреатита для уменьшения стимуляции поджелудочной железы; однако данные не подтверждают, эффективны ли диеты с низким содержанием жиров, и соблюдение требований к калорийности может быть затруднено без дополнительных калорий из жира42. Рекомендации по составу макроэлементов: 30% калорий в виде жира и от 1 до 1,5 г. / кг белка в день.41 Могут быть полезны пероральные пищевые добавки для увеличения количества потребляемых калорий. Следует рассмотреть возможность энтерального питания, если пациенты не могут удовлетворить потребность в калориях через рот, и парентерального питания, только если энтеральное питание не подходит.43
Мальабсорбция жира и стеаторея обычно не обнаруживаются до тех пор, пока болезнь не перейдет на поздние стадии, когда фиброзная ткань заменила значительную часть нормальной ткани поджелудочной железы. Поскольку липаза поджелудочной железы отвечает примерно за 90% переваривания жиров, мальабсорбция жиров представляет собой более серьезную проблему, чем мальабсорбция углеводов и белков.44 Существуют ферменты из других желез, помимо поджелудочной железы, которые переваривают углеводы и белок, поэтому переваривание этих макроэлементов не так скомпрометированы, как и с жиром при хроническом панкреатите.44 Наибольшую озабоченность при мальабсорбции жиров вызывают потеря калорий и нарушение всасывания жирорастворимых витаминов. Дефицит витамина D может присутствовать более чем у 50% людей с хроническим панкреатитом, в то время как дефицит витаминов A и E оценивается как относительно низкий, 3% и 10% соответственно.45 Рекомендуется ежегодная оценка уровня витаминов в сыворотке крови, чтобы вмешательство может быть индивидуальным, и можно будет избежать ненужных добавок. Нет единого мнения относительно приема витаминов при хроническом панкреатите, но некоторые руководящие принципы предлагают следовать протоколам для пациентов с муковисцидозом (ИП и, следовательно, мальабсорбция жира и дефицит растворимых витаминов сопровождают муковисцидоз).46
Низкий уровень витамина D в сыворотке крови и заболевания костей чаще встречаются у людей с хроническим панкреатитом, чем у здоровых людей.47 Распространенность заболеваний костей у пациентов с хроническим панкреатитом оценивается от 39% до 74% из-за множества факторов риска, включая низкий сывороточный витамин D, отсутствие физической активности, курение и мальабсорбция.48,49 Недавний метаанализ 10 исследований с участием 513 субъектов показал, что 65% людей с хроническим панкреатитом страдали остеопорозом или остеопенией.50 Ежегодных тестов на плотность костной ткани, определение уровня витамина D в сыворотке крови, упражнения с отягощением и воздержание от алкоголя и курения помогут предотвратить заболевание костей у пациентов с хроническим панкреатитом, хотя формальных рекомендаций по лечению нет35. Ключом в этой ситуации является ранняя диагностика. хронического панкреатита, так что профилактические меры могут быть приняты до развития болезни костей. К сожалению, диагноз хронического панкреатита может не диагностироваться до поздних стадий.
PERT имеет решающее значение для адекватного усвоения пищевых макроэлементов людьми с хроническим панкреатитом.Ферменты свиного происхождения и покрыты кишечнорастворимой оболочкой, чтобы выдержать кислотность желудочного сока, и представлены в низких и высоких дозах. Нормальная секреция липазы поджелудочной железой составляет примерно от 3000 до 5000 единиц в минуту после еды.28 Первоначальные рекомендации PERT при явном проявлении стеатореи составляют 1000 единиц липазы / кг веса за один прием пищи, исходя из того, что требуется 2000 единиц на грамм пищевые жиры28. Индивидуальные потребности различаются, но общее практическое правило состоит в том, что на прием пищи требуется от 25 000 до 75 000 единиц липазы, а на перекус — 25 000 единиц; половину принимать во время еды, а другую — в конце еды.51 Использование эндогенных ферментов поджелудочной железы считается успешным, если оно снижает стеаторею, сводит к минимуму желудочно-кишечные расстройства и предотвращает дефицит калорий и жирорастворимых витаминов. PERT не может полностью предотвратить мальабсорбцию жира или стеаторею, но должен обеспечивать поддержание веса и повышенный комфорт желудочно-кишечного тракта.8 Потребление клетчатки может повлиять на PERT, и его следует пересмотреть в случае неэффективного PERT.28 Если первоначальный режим дозирования не дает результата. в случае удовлетворительных результатов рекомендуется увеличить дозу в два-три раза или попробовать другие ферменты.28
Диабет — это более позднее осложнение хронического панкреатита, которое возникает из-за замены секретирующих инсулин островковых клеток нефункциональной фиброзной тканью. Приблизительно у 90% людей с хроническим панкреатитом разовьется диабет.11 Диабет, вызванный хроническим панкреатитом, также называется панкреатогенным диабетом и характеризуется инсулинорезистентностью в сочетании с PI52. По оценкам, панкреатогенный диабет составляет почти одну десятую всех. случаев диабета в Соединенных Штатах, но, к сожалению, отсутствуют рекомендации по лечению этого типа диабета.52
Риск рака поджелудочной железы беспокоит людей с хроническим панкреатитом. Многоцентровое историческое когортное исследование 2015 субъектов с хроническим панкреатитом выявило 4% -ный риск рака поджелудочной железы через 20 лет после постановки диагноза хронического панкреатита.53 Совсем недавно метаанализ показал относительный риск 13,3% .54 Риск хронического панкреатита — ассоциированный рак поджелудочной железы наиболее высок у пациентов с хроническим панкреатитом с ранним началом54. Хотя скрининг на рак поджелудочной железы у всех пациентов с хроническим панкреатитом не считается экономически эффективным, важно осознавать повышенный риск.
Заключение
Мужчина 45 лет с диагнозом хронический панкреатит направлен к диетологу. Диетолог проводит оценку питания пациента и работает с междисциплинарной медицинской командой для оценки функции поджелудочной железы. Обнаружив низкий уровень витамина D в сыворотке крови, признаки стеатореи, ИП и недавнюю потерю веса, диетолог прописывает пациенту пероральную пищевую добавку и разрабатывает режим PERT. Пациент регулярно наблюдает за тем, чтобы PERT был эффективным и чтобы избежать потери веса.Диетолог также советует пациенту воздерживаться от алкоголя.
Хронический панкреатит — болезненное заболевание, имеющее серьезные последствия для питания и качества жизни. Вмешательство по питанию, в том числе консультирование по вопросам воздержания от алкоголя, если это необходимо, облегчает желудочно-кишечный дискомфорт и замедляет прогрессирование заболевания. Исследования показали, что диетическое консультирование эффективно для предотвращения недоедания у пациентов с хроническим панкреатитом55. Понимание пищевых рисков панкреатита, включая недоедание и диабет, позволяет врачам-терапевтам лучше оценивать, вмешиваться и наблюдать за людьми с хроническим панкреатитом.
— Меган Баумлер, доктор философии, доктор медицинских наук, доцент Университета Маунт Мэри в Милуоки.
Цели обучения
После завершения этого курса повышения квалификации специалисты по питанию должны уметь:
1. Обсудить нормальную физиологию поджелудочной железы, которая защищает от панкреатита.
2. Консультировать пациентов по симптомам и патофизиологии панкреатита.
3. Оцените причины панкреатита.
4. Разработайте план лечения MNT для пациентов с панкреатитом.
Ежемесячный осмотр CPE
1. Что из следующего является верным относительно физиологической защиты от панкреатита?
а. Неактивные пищеварительные ферменты поджелудочной железы размещаются в клеточных гранулах вместе с лизосомальными гидролазами.
г. Секреторный ингибитор трипсина присутствует в поджелудочной железе, чтобы при необходимости инактивировать трипсин.
г. Пищеварительные ферменты поджелудочной железы активируются энтерокиназой в ацинарных клетках.
г. Проток поджелудочной железы достаточно большой, поэтому он не блокируется и не вызывает панкреатит.
2. Какое из утверждений относительно хронического панкреатита, вызванного алкоголем, верно?
а. Воздержание может замедлить прогрессирование болезни.
г. Продолжение употребления алкоголя не повлияет на прогрессирование болезни.
г. Потребление трех алкогольных напитков в день в течение одного года обычно достаточно, чтобы вызвать панкреатит.
г. У большинства алкоголиков развивается хронический панкреатит.
3.Что из перечисленного верно относительно этиологии хронического панкреатита?
а. Курение увеличивает риск хронического панкреатита только при наличии другого фактора риска.
г. Выявлены все генетические факторы риска.
г. Мутации в гене трипсиногена являются наиболее распространенным из известных наследственных факторов риска.
г. Любая мутация в гене ингибитора секреторного трипсина поджелудочной железы защищает от панкреатита.
4. Почему хронический панкреатит диагностировать труднее, чем острый панкреатит?
а.На ранних стадиях хронического панкреатита изменения могут быть неопределяемыми, а стандарты диагностики отсутствуют.
г. Все случаи хронического панкреатита легко распознать с помощью магнитно-резонансной томографии, КТ или эндоскопического ультразвукового исследования.
г. Нет никаких процедур или протоколов для диагностики хронического панкреатита.
г. В большинстве учреждений нет оборудования, необходимого для обследования на хронический панкреатит.
5. Что из перечисленного является первым физиологическим событием хронического панкреатита, независимо от этиологии?
а.Повышение уровня амилазы и липазы в сыворотке
b. Закупорка протока поджелудочной железы
c. Преждевременная активация трипсина в ацинарных клетках
d. Отсутствие адекватных пищеварительных ферментов и последующее недоедание
6. Что из следующего является верным в отношении заместительной терапии ферментами поджелудочной железы (PERT)?
а. Он полностью устранит мальабсорбцию жира и стеаторею.
г. Он должен облегчить симптомы со стороны желудочно-кишечного тракта, помочь достичь достаточного количества калорий и снизить риск заболеваний костей.
г. Это бесполезно, потому что желудочная кислота инактивирует ферменты до того, как они заработают.
г. Рекомендуется для снятия боли.
7. Почему у большинства людей с хроническим панкреатитом развивается диабет и панкреатическая недостаточность?
а. Секреция поджелудочной железы блокируется из-за камней в желчном пузыре, поэтому инсулин и пищеварительные ферменты не могут достичь тонкой кишки.
г. Рецепторы инсулина в организме становятся устойчивыми, и пищеварительные ферменты не могут активироваться.
г.Бета- и ацинарные клетки, которые обычно секретируют инсулин и неактивные пищеварительные ферменты соответственно, заменяются нефункционирующей фиброзной тканью.
г. Причина развития инсулиновой и панкреатической недостаточности у пациентов с хроническим панкреатитом неизвестна.
8. Почему люди с хроническим панкреатитом подвержены риску недоедания?
а. Их потребности в калориях обычно ниже, чем у здорового населения.
г. Нарушение всасывания жира затрудняет получение достаточного количества калорий и усвоение жирорастворимых витаминов.
г. Генетические мутации, вызывающие хронический панкреатит, также вызывают дефицит витамина А.
г. Хронический панкреатит сильно коррелирует с протеинурией.
9. Что наиболее важно для нутритивного ухода за больным хроническим панкреатитом?
а. Подсчет углеводов при панкреатогенном диабете для достижения адекватного контроля уровня глюкозы в крови для предотвращения долгосрочных осложнений.
г. Потребление белка 1,5 г / кг для предотвращения потери мышечной массы, которая обычно возникает при хроническом панкреатите.
г. Обезболивание для достижения максимального качества жизни.
г. Достаточное количество калорий, успешный PERT и предотвращение дефицита питательных микроэлементов.
10. Почему люди с хроническим панкреатитом подвергаются повышенному риску заболевания костей?
а. У них более вероятно низкий уровень витамина D в сыворотке крови, нарушение всасывания жиров, отсутствие физической активности и курение сигарет.
г. Они не могут усваивать кальций из-за изменений в тонком кишечнике, влияющих на площадь абсорбирующей поверхности.
г.Генетическая предрасположенность к хроническому панкреатиту обычно сочетается с генетической предрасположенностью к заболеваниям костей.
г. Они избегают молочных продуктов, чтобы не допустить обострения болезни, что приводит к снижению потребления кальция.
Ссылки
1. Райна А., О’Киф, SJD. Питание при заболеваниях поджелудочной железы. В: Росс А.С., Кабальеро Б., Казинс Р.Дж., Такер К.Л., Циглер Т.Р., ред. Современное питание в условиях здоровья и болезней . 11-е изд.Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 2014.
2. Ядав Д., Тиммонс Л., Бенсон Дж. Т., Дирхизинг Р.А., Чари СТ. Заболеваемость, распространенность и выживаемость хронического панкреатита: популяционное исследование. Ам Дж. Гастроэнтерол . 2011; 106 (12): 2192-2199.
3. Пири А.Ф., Деллон Э.С., Лунд Дж. И др. Бремя желудочно-кишечных заболеваний в США: обновление 2012 г. Гастроэнтерология . 2012; 143 (5): 1179-1187.e1-3.
4.Беглер Х.Г., Уоршоу А.Л., Бухлер М.В. и др. Поджелудочная железа: единый учебник фундаментальных наук, медицины и хирургии . 2-е изд. Мальден, Массачусетс: издательство Wiley-Blackwell Publishing Limited; 2008.
5. Корпус RM. Синтез, внутриклеточный транспорт и разгрузка экспортируемых белков в ацинарных клетках поджелудочной железы и других клетках. Биол Рев Камб Филос Соц . 1978; 53 (2): 211-354.
6. Крюгер Б., Альбрехт Э., Лерх М.М. Роль внутриклеточной передачи сигналов кальция в преждевременной активации протеаз и возникновении панкреатита. Ам Дж. Патол . 2000; 157 (1): 43-50.
7. Расмуссен Х. Х., Иртун О., Олесен С. С., Древес А. М., Холст М. Питание при хроническом панкреатите. Мир Дж. Гастроэнтерол . 2013; 19 (42): 7267-7275.
8. Транг Т., Чан Дж., Грэм Д. Заместительная терапия панкреатическими ферментами при экзокринной недостаточности поджелудочной железы в 21 веке. Мир Дж. Гастроэнтерол . 2014; 20 (33): 11467-11485.
9. Келлер Дж., Лайер П. Экзокринная реакция поджелудочной железы человека на питательные вещества при здоровье и болезнях. Кишка . 2005; 54 (Приложение 6): 1-28.
10. Ван ГП, Сюй CS. Ингибитор секреторного трипсина поджелудочной железы: больше, чем ингибитор трипсина. World J Gastrointest Pathophysiol . 2010; 1 (2): 85-90.
11. Ammann RW. Естественное течение алкогольного хронического панкреатита. Intern Med . 2001; 40 (5): 368-375.
12. Эвальд Н., Хардт П.Д. Диагностика и лечение сахарного диабета при хроническом панкреатите. Мир Дж. Гастроэнтерол .2013; 19 (42): 7276-7281.
13. Клеменс Д.Л., Уэллс М.А., Шнайдер К.Дж., Сингх С. Молекулярные механизмы алкогольного панкреатита. World J Gastrointest Pathophysiol . 2014; 5 (3): 147-157.
14. Vonlaufen A, Wilson JS, Apte MV. Молекулярные механизмы панкреатита: современное мнение. J Гастроэнтерол Hepatol . 2008; 23 (9): 1339-1348.
15. Дюфур М.С., Адамсон Мэриленд. Эпидемиология алкогольного панкреатита. Поджелудочная железа . 2003; 27 (4): 286-290.
16. Nordback I, Pelli H, Lappalainen-Lehto R, Järvinen S, Räty S, Sand J. Рецидив острого алкогольного панкреатита можно уменьшить: рандомизированное контролируемое исследование. Гастроэнтерология . 2009; 136 (3): 848-855.
17. Ядав Д., Хавс Р. Х., Бренд RE и др. Употребление алкоголя, курение сигарет и риск повторного острого и хронического панкреатита. Arch Intern Med .2009; 169 (11): 1035-1045.
18. Maisonneuve P, Lowenfels AB, Müllhaupt B, et al. Курение сигарет ускоряет прогрессирование хронического алкогольного панкреатита. Кишка . 2005; 54 (4): 510-514.
19. Ло Р., Парси М., Лопес Р., Зуккаро Дж., Стивенс Т. Курение сигарет независимо связано с хроническим панкреатитом. Панкреатология . 2010; 10 (1): 54-59.
20. Кастиньейра-Альвариньо М., Линдквист Б., Луасес-Регейра М. и др.Роль жирной диеты в развитии осложнений хронического панкреатита. Clin Nutr . 2013; 32 (5): 830-836.
21. Мейер А., Коффи MJ, Оливер MR, Ooi CY. Контрасты и сравнения острого панкреатита с дебютом у детей и взрослых. Панкреатология . 2013; 13 (4): 429-435.
22. Масамунэ А. Генетика панкреатита: обновление 2014 г.. Tohoku J Exp Med . 2014; 232 (2): 69-77.
23.Камисава Т., Сатаке К. Клиническое лечение аутоиммунного панкреатита. Адв. Мед. Наук . 2007; 52: 61-65.
24. Pezzilli R, Pagano N. Патофизиология аутоиммунного панкреатита. World J Gastrointest Pathophysiol . 2014; 5 (1): 11-17.
25. Лернер А., Брански Д., Лебенталь Э. Заболевания поджелудочной железы у детей. Педиатр Clin North Am . 1996; 43 (1): 125-156.
26. Skórzewska M, Romanowicz T, Mielko J, et al.Операция Фрея при хроническом панкреатите, связанном с делением поджелудочной железы: клинический случай и обзор литературы. Прз Гастроэнтерол . 2014; 9 (3): 175-178.
27. Ballard DD, Flueckiger JR, Fogel EL, et al. Обследование взрослых с идиопатическим панкреатитом на предмет генетической предрасположенности: более высокая частота аномальных результатов при использовании полного секвенирования генов. Поджелудочная железа . 2015; 44 (1): 116-121.
28. Афгани Э., Синха А., Сингх В.К.Обзор диагностики и управления питанием при хроническом панкреатите. Нутр Клин Практик . 2014; 29 (3): 295-311.
29. Конвелл Д.Л., Ли Л.С., Ядав Д. и др. Практические рекомендации Американской ассоциации поджелудочной железы при хроническом панкреатите: научно обоснованный отчет о диагностических рекомендациях. Поджелудочная железа . 2014; 43 (8): 1143-1162.
30. Bian Y, Wang L, Chen C, et al. Количественная оценка экзокринной функции поджелудочной железы при хроническом панкреатите с использованием MRCP с повышенным секретином. Мир Дж. Гастроэнтерол . 2013; 19 (41): 7177-7182.
31. Hansen TM, Nilsson M, Gram M, Frøkjr JB. Морфофункциональная оценка хронического панкреатита с помощью магнитно-резонансной томографии. World J Гастроэнтерол . 2013; 19 (42): 7241-7246.
32. Уоллес М.Б., Хоуз Р.Х. Эндоскопическое ультразвуковое исследование в оценке и лечении хронического панкреатита. Поджелудочная железа . 2001; 23 (1): 26-35.
33. Стивенс Т, Парси Массачусетс. Обновленная информация об эндоскопическом тестировании функции поджелудочной железы. Мир Дж. Гастроэнтерол . 2011; 17 (35): 3957-3961.
34. Конвелл Д.Л., Зуккаро Дж., Морроу Дж. Б. и др. Пиковая концентрация липазы, стимулированная холецистокинином, в дренажной жидкости двенадцатиперстной кишки: новый тест функции поджелудочной железы. Ам Дж. Гастроэнтерол . 2002; 97 (6): 1392-1397.
35. Дагган С.Н., Конлон К.С. Практическое руководство по питанию при хроническом панкреатите. Прак Гастроэнтерол . 2013; 118: 24-32.
36. Сазерленд Д.Е., Радосевич Д.М., Беллин М.Д. и др. Тотальная панкреатэктомия и аутотрансплантация островков при хроническом панкреатите. J Am Coll Surg . 2012; 214 (4): 409-424.
37. Whitcomb DC, Lehman GA, Vasileva G, et al. Капсулы с замедленным высвобождением панкрелипазы (CREON) при внешнесекреторной недостаточности поджелудочной железы, вызванной хроническим панкреатитом или хирургическим вмешательством на поджелудочной железе: двойное слепое рандомизированное исследование. Ам Дж. Гастроэнтерол . 2010; 105 (10): 2276-2286.
38. Белакович Г., Николова Д., Глууд Л.Л., Симонетти Р.Г., Глууд С. Смертность в рандомизированных испытаниях антиоксидантных добавок для первичной и вторичной профилактики: систематический обзор и метаанализ. JAMA . 2007; 297 (8): 842-857.
39. Hébuterne X, Hastier P, Péroux JL, Zeboudj N, Delmont JP, Rampal P. Расход энергии в покое у пациентов с хроническим алкогольным панкреатитом. Dig Dis Sci . 1996; 41 (3): 533-539.
40. Дикерсон Р.Н., Вехе К.Л., Маллен Дж. Л., Feurer ID. Расход энергии в покое у больных панкреатитом. Crit Care Med . 1991; 19 (4): 484-490.
41. Meier R, Ockenga J, Pertkiewicz M, et al. Руководство ESPEN по энтеральному питанию: поджелудочная железа. Clin Nutr . 2006; 25 (2): 275-284.
42. Дагган С., О’Салливан М., Фихан С., Риджуэй П., Конлон К. Нутритивное лечение недостаточности и недоедания при хроническом панкреатите: обзор. Нутр Клин Практик . 2010; 25 (4): 362-370.
43. Hamvas J, Schwab R, Pap A. Jejunal кормление при хроническом панкреатите с тяжелым некрозом. СОП . 2001; 2 (3): 112-116.
44. DiMagno EP, Go VL. Внешнесекреторная недостаточность поджелудочной железы. Современные концепции патофизиологии. Постградская медицина . 1972; 52 (1): 135-140.
45. Sikkens EC, Cahen DL, Koch AD, et al. Распространенность дефицита жирорастворимых витаминов и снижение костной массы у пациентов с хроническим панкреатитом. Панкреатология . 2013; 13 (3): 238-242.
46. Роджерс CL. Питание взрослых с муковисцидозом — Часть I. Pract Gastroenterol . 2013; 113: 10-24.
47. Teichmann J, Mann ST, Stracke H, et al. Нарушения метаболизма витамина D3 у молодых женщин с хроническим панкреатитом различной степени тяжести. Eur J Med Res . 2007; 12 (8): 347-350.
48. Дуйсикова Х., Дите П, Томандл Дж., Шевчикова А, Пречечтелова М.Возникновение метаболической остеопатии у больных хроническим панкреатитом. Панкреатология . 2008; 8 (6): 583-586.
49. Дагган С.Н., О’Салливан М., Гамильтон С., Фихан С.М., Риджуэй П.Ф., Конлон К.С. Пациенты с хроническим панкреатитом подвержены повышенному риску остеопороза. Поджелудочная железа . 2012; 41 (7): 1119-1124.
50. Дагган С.Н., Смит Н.Д., Мерфи А., Макнотон Д., О’Киф С.Дж., Конлон К.С.. Высокая распространенность остеопороза у пациентов с хроническим панкреатитом: систематический обзор и метаанализ. Клин Гастроэнтерол Гепатол . 2014; 12 (2): 219-228.
51. Домингес-Муньос Дж. Э., Иглесиас-Гарсия Дж., Иглесиас-Рей М., Фигейрас А., Вилариньо-Инсуа М. Влияние схемы приема на терапевтическую эффективность пероральных добавок ферментов поджелудочной железы у пациентов с внешнесекреторной недостаточностью поджелудочной железы: рандомизированное, трехстороннее кроссоверное исследование. Алимент Фармакол Тер . 2005; 21 (8): 993-1000.
52. Cui Y, Andersen DK. Панкреатогенный диабет: особенности ведения. Панкреатология . 2011; 11 (3): 279-294.
53. Lowenfels AB, Maisonneuve P, Cavallni G, et al. Панкреатит и риск рака поджелудочной железы. Международная группа по изучению панкреатита. N Engl J Med . 1993; 328 (20): 1433-1437.
54. Раймонди С., Лоуэнфельс А.Б., Морселли-Лабате А.М., Мезоннев П., Пеззилли Р. Рак поджелудочной железы при хроническом панкреатите: этиология, заболеваемость и раннее выявление. Лучшая Практика Рес Клин Гастроэнтерол .2010; 24 (3): 349-358.
55. Сингх С., Мидха С., Сингх Н., Джоши Ю.К., Гарг П.К. Диетическое консультирование по сравнению с диетическими добавками при недостаточности питания при хроническом панкреатите: рандомизированное контролируемое исследование. Клин Гастроэнтерол Гепатол . 2008; 6 (3): 353-359.
Диетические вмешательства при панкреатите — Today’s Dietitian Magazine
Июнь / Июль 2020 Выпуск
Диетические вмешательства при панкреатите
Кэрри Деннетт, MPH, RDN, CD
Сегодняшний диетолог
Vol.22, № 6, стр. 24
Питание играет ключевую роль в спасении жизней и сохранении качества жизни.
И острый, и хронический панкреатит представляют собой серьезное бремя для здоровья и системы здравоохранения. Острый панкреатит является одной из наиболее частых желудочно-кишечных причин госпитализации в США, а хронический панкреатит значительно ухудшает качество жизни1. Как в условиях неотложной помощи, так и в амбулаторных условиях питание является ключевым фактором в лечении этих состояний.
Панкреатит — это воспаление поджелудочной железы — большой железы, которая выделяет пищеварительные соки в тонкий кишечник и высвобождает гормоны инсулин и глюкагон в кровоток — которое возникает, когда пищеварительные ферменты начинают переваривать саму поджелудочную железу. И острый, и хронический панкреатит являются серьезными заболеваниями, которые иногда могут привести к опасным для жизни осложнениям.
Острый панкреатит возникает внезапно, чаще всего проявляется болью от слабой до сильной в верхней части живота, которая может распространяться на спину, грудь или бока.Интенсивность и локализация боли не коррелируют с ее тяжестью. Также могут присутствовать жар, тошнота и рвота.2
В 40–70% случаев основной причиной являются камни в желчном пузыре, которые могут вызвать воспаление, поскольку они проходят через желчный или панкреатический проток и застревают. Сильное употребление алкоголя — более 50 г в день в течение более пяти лет — составляет от 25% до 35% случаев. Острый панкреатит также может возникать у людей с уровнем триглицеридов выше 1000 мг / дл или у людей с доброкачественными или злокачественными опухолями поджелудочной железы, причем последнее особенно важно, когда панкреатит является идиопатическим, т. Е. Не имеет идентифицируемой причины.2
В Соединенных Штатах ежегодно более 270000 госпитализаций связаны с острым панкреатитом.3,4 Случаи заболевания классифицируются как легкие, средние и тяжелые, а общая смертность колеблется от 5% до 30% в зависимости от степени тяжести3. острый панкреатит легкой степени обычно проходит в течение нескольких дней; однако от 15% до 20% случаев являются тяжелыми, для разрешения требуется больше времени и требуется более длительное пребывание в больнице2
Считается, что иммунная система играет роль в прогрессировании острого панкреатита — у некоторых пациентов высвобождение провоспалительных медиаторов, вызванное самовоспалительным перевариванием поджелудочной железы, может вызвать некротический панкреатит и нарушение барьера тонкой кишки.Это делает возможным бактериальную транслокацию, которая, в свою очередь, может привести к синдрому системной воспалительной реакции и синдрому полиорганной дисфункции.5
Рецидивирующие эпизоды острого панкреатита могут привести к хроническому панкреатиту, которым страдают от 42 до 73 из 100 000 взрослых в США, 6 что приводит к 86 000 госпитализаций в год.7 Хотя прогрессирование хронического панкреатита варьирует и может включать длительные периоды без симптомов, состояние со временем ухудшается, что приводит к необратимым повреждениям.Симптомы могут включать боль в животе, а при наличии боли она может стать постоянной и более сильной после еды. По иронии судьбы, по мере того, как состояние прогрессирует, боль может уменьшаться.7
Другие симптомы включают тошноту, рвоту, диарею, жирный и зловонный стул и потерю веса. При обострениях лечение хронического панкреатита аналогично лечению острого панкреатита.7
Постоянные боли в животе, рубцы поджелудочной железы, диабет и рак поджелудочной железы могут быть осложнениями хронического панкреатита.Также могут возникать нарушения пищеварения, недоедания и мальабсорбции, потенциально приводящие к остеопении и остеопорозу, что, в свою очередь, может привести к переломам костей8
Мужчины и чернокожие американцы подвергаются более высокому риску, как и люди, у которых в семейном или личном анамнезе были камни в желчном пузыре или семейный анамнез панкреатита. Помимо чрезмерного употребления алкоголя и высокого уровня триглицеридов, причины могут включать высокий уровень кальция в крови, генетические нарушения поджелудочной железы и прием некоторых лекарств.8 Наличие целиакии увеличивает риск хронического панкреатита, в частности подтипа, известного как аутоиммунный панкреатит, за счет примерно в три раза, а люди с воспалительным заболеванием кишечника и другими аутоиммунными заболеваниями также имеют повышенный риск.9
У людей с муковисцидозом может быть хронический панкреатит без боли из-за недостаточности поджелудочной железы. Токсины окружающей среды, такие как продолжающееся употребление алкоголя и табака, способствуют прогрессированию хронического панкреатита.7
Диагностика и лечение
Рекомендации Американского колледжа гастроэнтерологии утверждают, что диагноз острого панкреатита определяется наличием двух из этих трех критериев: боль в верхней части живота, уровень амилазы и / или липазы в сыворотке, превышающий верхний предел нормы и характерные результаты визуализации брюшной полости.Уровни липазы в сыворотке предпочтительнее уровней амилазы в сыворотке, потому что они остаются повышенными дольше после начала заболевания.
Легкие случаи определяются отсутствием органной недостаточности и / или некроза поджелудочной железы. В умеренно тяжелых случаях наблюдаются местные осложнения, включая некроз, но без стойкой органной недостаточности. В тяжелых случаях есть две отдельные фазы. Ранняя фаза, в течение первой недели, характеризуется синдромом системной воспалительной реакции и / или органной недостаточностью, тяжесть которой определяется органной недостаточностью.Вторая фаза характеризуется местными осложнениями. Поскольку у большинства пациентов с тяжелым панкреатитом на момент госпитализации нет органной недостаточности или некроза, у них может быть неточно диагностировано легкое заболевание, что откладывает необходимое лечение2
Не существует единого теста, который бы однозначно диагностировал хронический панкреатит. Обычно это подозревается, если у пациента есть боль в верхней части живота, постоянное употребление алкоголя или табака, острый панкреатит в анамнезе и семейный анамнез панкреатита, а затем подтверждается с помощью компьютерной томографии или МРТ.7,10 Тестирование функции поджелудочной железы часто используется в качестве дополнительной меры. Поскольку эндоскопическое ультразвуковое исследование является инвазивным и недостаточно специфичным, оно рекомендуется только в том случае, если поперечное сечение не может подтвердить диагноз.10
Лечение хронического панкреатита основано на обезболивании, лечении панкреатической недостаточности и лечении осложнений.11 Обезболивание с помощью медицинских или, реже, хирургических средств является одним из первых шагов в лечении хронического панкреатита, за которым следуют алкоголь и курение. прекращение, если применимо.6
Если продолжающегося лечения с помощью заместительной терапии ферментами поджелудочной железы (PERT) и питания недостаточно, могут быть назначены ингибиторы протонной помпы для предотвращения денатурирования липазы поджелудочной железы желудочной кислотой. Более чем у половины пациентов с хроническим панкреатитом развивается диабет, известный как панкреатогенный диабет или диабет типа 3c, из-за потери массы островковых клеток в поджелудочной железе, что, в свою очередь, увеличивает риск рака поджелудочной железы. Медикаментозное лечение диабета, вторичного по отношению к панкреатиту, обычно включает в себя инсулино-сенсибилизирующие препараты, такие как метформин, вместе с PERT.9
Лечение легкого острого панкреатита обычно включает кратковременное пребывание в больнице для внутривенного введения жидкостей, обезболивающих и антибиотиков, если есть инфекционные осложнения, но не профилактически.2,12 Тяжелый острый панкреатит требует более длительного пребывания в больнице.
Некоторым пациентам с острым панкреатитом или обострениями хронического панкреатита могут потребоваться хирургические вмешательства для удаления закупорки, включая камни в желчном пузыре, или лечения сужения протоков поджелудочной железы или желчных протоков.Некоторым пациентам требуется хирургическое удаление некротической ткани и, в более редких случаях, удаление желчного пузыря или поджелудочной железы.2,13 Из-за сложной этиологии и различных клинических проявлений острого панкреатита найти лекарственное лечение было непросто.5
Диетологическое лечение острого панкреатита
Что представляет собой оптимальную нутритивную поддержку при остром панкреатите, обсуждается на протяжении десятилетий. Обычным лечением было NPO (ничего не перорально), чтобы дать поджелудочной железе отдохнуть — несмотря на отсутствие клинических данных, подтверждающих это, 2,5 с большинством руководящих принципов, рекомендующих NPO до исчезновения боли и некоторой отсрочки перорального кормления до нормализации уровня ферментов поджелудочной железы или воспаления. стихает.2
Однако это способствует возникновению множества других проблем, включая недостаточность питания и катаболизм из-за ограничения потребления энергии в то время, когда потребности организма в энергии увеличиваются.5 Фактически, новые рекомендации, представленные Европейским обществом клинического питания и метаболизма ( ESPEN) Конгресс в прошлом году заявил, что все пациенты с прогнозируемым острым панкреатитом легкой и средней степени тяжести должны проходить скрининг на предмет риска, связанного с питанием, и что пациенты с прогнозируемым тяжелым острым панкреатитом всегда должны считаться находящимися в группе риска, связанного с питанием.14
Поскольку недостаточность питания вызывает особую озабоченность при тяжелом остром панкреатите, полное парентеральное питание (ПП) стало стандартной практикой для обеспечения питания без стимуляции поджелудочной железы.15 Однако это также предотвращает стимуляцию кишечника, и этот отдых кишечника связан с атрофия слизистой оболочки кишечника, которая ухудшает барьерную функцию тонкого кишечника примерно у 60% пациентов, что приводит к потенциально серьезным осложнениям.2,5 ППП не только не способствует здоровью кишечника, но и существует риск инфекций, исходящих из центрального венозного катетера.16
У пациентов, которые не переносят пероральное питание, энтеральное питание (ЭП) помогает защитить слизистую кишечника и предотвращает избыточный бактериальный рост за счет стимуляции перистальтики кишечника. 5,15 A 2010 Кокрановский обзор показал, что ЭП более вероятно, чем ПП снижение системных инфекций, полиорганной недостаточности и смерти15. Систематический обзор 11 рандомизированных контролируемых исследований в 2009 г. показал аналогичные результаты. Однако исследователи отметили, что, хотя ЭП приводило к лучшим результатам, чем ПП, когда нутритивная поддержка была начата в течение 48 часов после поступления, не было разницы между ЭП и ППП, когда питание откладывалось более чем на 48 часов.Предполагается, что это произошло из-за повсеместного воздействия отложенного питания17.
Таким образом, хотя EN может давать лучшие результаты, чем TPN, также оказывается, что лучше проводить EN раньше, чем позже. Несколько исследований показали, что начало ЭП в течение 48 часов после госпитализации по сравнению с ожиданием более 48 часов снижает частоту серьезной инфекции и, в некоторых случаях, смертность.17-20 Это соответствует рекомендациям обществ питания в США. Государства и Европа, включая Американское общество парентерального и энтерального питания, ESPEN и журнал Journal of Parenteral and Enteral Nutrition .14,21 В этих рекомендациях рекомендуется ранняя ЭП у всех пациентов с тяжелым острым панкреатитом, используя ПП только в тех случаях, когда ЭП не переносится или неосуществимо.
При введении ЭП пациентам с панкреатитом традиционно предпочтительным является назоеюнальный путь — доставка питания к тощей кишке тонкой кишки, поскольку он резко снижает стимуляцию поджелудочной железы, но при этом способствует перистальтике кишечника2,5,15. их труднее поместить в пациентов, что требует специального персонала и увеличивает расходы.22 Недавние исследования показали, что кормление через назогастральный зонд кажется безопасным, и Международная ассоциация панкреатологов и Американская панкреатическая ассоциация рекомендуют использовать любой из этих методов.3
Систематический обзор и метаанализ 2014 года показали, что назогастральное кормление было эффективным у 90% пациентов с тяжелым острым панкреатитом, обеспечивая адекватное питание без увеличения частоты таких осложнений, как диарея, вздутие живота или обострение боли. 22 A 2020 Обзор Cochrane показал, что имеющихся данных недостаточно, чтобы показать преимущества или недостатки любого из режимов зондового питания.23
А как насчет перорального кормления? Многоцентровое исследование 2014 года в Нидерландах рандомизировало пациентов с тяжелым острым панкреатитом с высоким риском осложнений, которые получали либо ЭП в течение 24 часов после поступления, либо пероральную диету через 72 часа. Пациенты, которым назначена пероральная диета, получали жидкости внутривенно в течение первых 72 часов, и, если пероральная диета не переносилась через 72 часа, ее снова предлагали через 96 часов; если все еще не переносился, предлагался ЭП. Исследователи не обнаружили разницы в частоте серьезных инфекций — некроза поджелудочной железы, пневмонии или бактерий в кровотоке — или смерти в течение шести месяцев после госпитализации.Они также не увидели различий в уровне воспалительной реакции16 — примечательно, потому что уменьшение этой реакции было предположено как преимущество раннего кормления согласно EN.19
Вопрос о том, когда начинать пероральное кормление у пациентов с острым панкреатитом легкой степени, имеет более четкий ответ. 24-26 Одно рандомизированное клиническое исследование показало, что немедленное пероральное кормление у пациентов с легким острым панкреатитом ускоряет выздоровление без неблагоприятных желудочно-кишечных эффектов26. Другое рандомизированное исследование 2007 г. Исследование показало, что твердая диета с низким содержанием жиров переносится, а также прозрачная жидкая диета у пациентов с легкими формами заболевания, но не приводит к сокращению срока пребывания в больнице, как предполагалось.24 Однако рандомизированное контролируемое исследование 2010 года показало, что пациенты, начавшие на полностью твердую диету, имели более короткий срок пребывания в больнице, чем те, кто начал на чистой жидкой диете или мягкой диете.25
Соответственно, для пациентов с прогнозируемым острым панкреатитом легкой степени новые руководящие принципы ESPEN, а также руководящие принципы Американского колледжа гастроэнтерологии рекомендуют начинать пероральное кормление с твердой диеты с низким содержанием жиров, как только они переносятся, поскольку это может ускорить выздоровление, при этом предпочтительнее EN, чем TPN. если не терпят.14,26,27
Когда EN является подходящим вмешательством, какая формулировка лучше? Полимер с неповрежденным белком, углеводами и длинноцепочечными жирными кислотами? Олигомерный — также известный как элементарный или полуэлементный — с пептидами и свободными аминокислотами, моносахаридами, среднецепочечными и свободными жирными кислотами? Специальная формула с противовоспалительными иммунонутриентами, такими как глутамин и омега-3 жирные кислоты, или формула с пребиотиками и пробиотиками?
A 2015 Кокрановский обзор обнаружил недостаточно доказательств, чтобы рекомендовать какой-либо конкретный тип рецептуры EN.В частности, доказательства эффективности и безопасности иммунонутриентов были низкого или очень низкого качества, а исследования, посвященные пробиотикам в лечении острого панкреатита, дали непоследовательные — даже противоречивые — результаты, особенно в отношении безопасности.28 Соответственно, Международная ассоциация панкреатологов этого не делает. Не рекомендую использовать пробиотики для уменьшения инфекционных осложнений, отчасти потому, что существуют значительные различия в типах и дозировках пробиотических добавок. В одном рандомизированном контролируемом исследовании использование конкретной комбинации или пробиотических штаммов не предотвратило осложнений, но увеличило смертность.3 Суть? При условии, что формула не содержит пробиотиков или иммунонутриентов, выбор между полимерными и олигомерными формулами будет в значительной степени основываться на переносимости пациентом.
Диетологическое лечение хронического панкреатита
Хронический панкреатит требует другого подхода к питанию с постоянным лечением, которое включает питание, дополнительные пищеварительные ферменты и отказ от табака и алкоголя. Недоедание часто встречается у пациентов с хроническим панкреатитом из-за множества факторов, в том числе следующих 14,27,29:
• повышенный расход энергии в сочетании с связанной с болью потерей аппетита и / или страхом перед едой;
• недостаточность ферментов поджелудочной железы;
• задержка опорожнения желудка; и
• продолжающееся злоупотребление алкоголем.
Низкий уровень липазы поджелудочной железы может снизить всасывание пищевых жиров и жирорастворимых питательных веществ (витаминов A, D, E, K), вызывая вздутие живота, диарею или жирный стул, что приводит к дальнейшему отказу от жира и препятствует адекватному потреблению энергии. Недостаточный уровень протеазы поджелудочной железы может привести как к белковой недостаточности, так и к дефициту витамина B12, а хроническое воспаление может препятствовать использованию белка организмом.30
Пациенты с хроническим панкреатитом — даже те, кто не злоупотребляет алкоголем — чаще страдают дефицитом питательных микроэлементов, чем пациенты без этого заболевания.Маркеры обновления и формирования костной ткани также ниже, 30 и сообщается о специфическом дефиците кальция, магния, цинка, тиамина и фолиевой кислоты27. PERT помогает минимизировать дефицит, но некоторым пациентам необходимо будет принимать дополнительные формы питательных микроэлементов, на которые он влияет. состояние 27,30
Давний совет ограничить потребление жиров в рационе больше не рекомендуется, в основном потому, что это снижает секрецию ферментов поджелудочной железы и может снизить эффективность дополнительных ферментов поджелудочной железы.Кроме того, ограничение пищевых жиров может маскировать начало мальабсорбции жира, которое проявляется в виде жира в стуле (стеаторея) 31 и увеличивает риск обострения потери веса и дефицита жирорастворимых витаминов.9
ESPEN рекомендует употреблять пищу с высоким содержанием белка и калорий, состоящую из пяти-шести небольших приемов пищи в день, избегая при этом диет с очень высоким содержанием клетчатки, поскольку клетчатка может поглощать или блокировать действие липазы поджелудочной железы, что приводит к снижению потребления питательных веществ. Нет необходимости ограничивать потребление жиров, если только невозможно контролировать стеаторею.14,32 Потребление белка от 1 до 1,5 г / кг обычно достаточно и хорошо переносится. В более чем 80% случаев достаточно пищи, дополненной ферментами поджелудочной железы перед каждым приемом пищи и перекуса, в то время как от 10% до 15% требуют пероральные пищевые добавки — на основе цельного белка, если переносится, и на основе пептидов, если нет, а 5% нуждаются в ЭП. Пациенты с риском непреднамеренной потери веса могут принимать добавки со среднецепочечным триглицеридом (MCT), которое всасывается непосредственно в кровоток без потребности в ферментах поджелудочной железы.Масло 27 MCT содержится в кокосовом и пальмоядровом маслах, а также в виде добавок.
Заключительные мысли
Хотя медицинские, а иногда и хирургические вмешательства важны для лечения острого и хронического панкреатита, питание также играет решающую роль в предотвращении осложнений и сохранении качества жизни.
— Кэрри Деннетт, магистр здравоохранения, RDN, CD, обозреватель по питанию для The Seattle Times , владелец Nutrition By Carrie и автор книги Healthy for Your Life: A Holistic Guide to Optimal Wellness .
Ссылки
1. Ядав Д., Ловенфельс А.Б. Эпидемиология панкреатита и рака поджелудочной железы. Гастроэнтерология . 2013; 144 (6): 1252-1261.
2. Теннер С., Бэйли Дж., ДеВитт Дж., Ведж С.С.; Американский колледж гастроэнтерологии. Рекомендации Американского колледжа гастроэнтерологии: ведение острого панкреатита. Ам Дж. Гастроэнтерол . 2013; 108 (9): 1400-1415.
3. Рекомендации Рабочей группы IAP / APA по острому панкреатиту.Рекомендации IAP / APA по лечению острого панкреатита, основанные на фактических данных. Панкреатология . 2013; 13 (4 Приложение 2): e1-e15.
4. Forsmark CE, Vege SS, Wilcox CM. Острый панкреатит. N Engl J Med . 2016; 375 (20): 1972-1981.
5. Пан Л.Л., Ли Дж., Шамун М., Бхатиа М., Сан Дж. Последние достижения в области питания при лечении острого панкреатита. Фронт Иммунол . 2017; 8: 762.
6. Сингх В.К., Ядав Д., Гарг П.К.Диагностика и лечение хронического панкреатита: обзор. JAMA . 2019; 322 (24): 2422-2434.
7. Кетвару Г.А., Фридман С.Д., Шет С.Г. Подход к пациентам с подозрением на хронический панкреатит: всесторонний обзор. Поджелудочная железа . 2015; 44 (2): 173-180.
8. Определения и факты о панкреатите. Веб-сайт Национального института диабета, болезней органов пищеварения и почек. https://www.niddk.nih.gov/health-information/digestive-diseases/pancreatitis/definition-facts.Обновлено в ноябре 2017 г.
9. Pham A, Forsmark C. Хронический панкреатит: обзор и обновление этиологии, факторов риска и лечения. F1000Res . 2018; 7: F1000 факультет Rev-607.
10. Гарднер Т.Б., Адлер Д.Г., Форсмарк CE, Зауэр Б.Г., Тейлор Дж. Р., Уиткомб, округ Колумбия. Клинические рекомендации АЧГ: хронический панкреатит. Ам Дж. Гастроэнтерол . 2020; 115 (3): 322-339.
11. Джалал М., Кэмпбелл Дж. А., Хоппер А. Д.. Практическое руководство по лечению хронического панкреатита. Фронтлайн Гастроэнтерол . 2019; 10 (3): 253-260.
12. Крокетт С.Д., Вани С., Гарднер ТБ, Фальк-Иттер Ю., Баркун А.Н.; Комитет по клиническим рекомендациям Института Американской гастроэнтерологической ассоциации. Руководство института Американской гастроэнтерологической ассоциации по начальному ведению острого панкреатита. Гастроэнтерология . 2018; 154 (4): 1096-1101.
13. Лечение панкреатита. Веб-сайт Национального института диабета, болезней органов пищеварения и почек.https://www.niddk.nih.gov/health-information/digestive-diseases/pancreatitis/treatment. Обновлено в ноябре 2017 г.
14. Безмаревич М; Европейское общество клинического питания и метаболизма. Руководство ESPEN по нутриционной поддержке при заболеваниях поджелудочной железы (острый и хронический панкреатит). http://www.espen.org/presfile/Bezmarevic_2019.pdf. Опубликовано 2019.
15. Аль-Омран М., Альбалави Ж.Х., Ташканди М.Ф., Аль-Ансари Л.А. Энтеральное и парентеральное питание при остром панкреатите. Кокрановская база данных Syst Rev . 2010; (1): CD002837.
16. Баккер О.Дж., ван Бруншот С., ван Сантворт Х.С. и др. Раннее кормление через назоэнтерический зонд в сравнении с кормлением по требованию при остром панкреатите. N Engl J Med . 2014; 371 (21): 1983–1993.
17. Петров М.С., Пилипчук Р.Д., Учугина А.Ф. Систематический обзор сроков искусственного питания при остром панкреатите. Br J Nutr . 2009; 101 (6): 787-793.
18.Ли JY, Yu T, Chen GC и др. Энтеральное питание в течение 48 часов после поступления улучшает клинические исходы острого панкреатита за счет уменьшения осложнений: метаанализ. PLoS One . 2013; 8 (6): e64926.
19. Sun JK, Mu XW, Li WQ, Tong ZH, Li J, Zheng SY. Влияние раннего энтерального питания на иммунную функцию пациентов с тяжелым острым панкреатитом. Мир Дж. Гастроэнтерол . 2013; 19 (6): 917-922.
20. Wereszczynska-Siemiatkowska U, Swidnicka-Siergiejko A, Siemiatkowski A, Dabrowski A.Раннее энтеральное питание превосходит отложенное энтеральное питание для предотвращения инфицированного некроза и смертности при остром панкреатите. Поджелудочная железа . 2013; 42 (4): 640-646.
21. Мирталло Дж. М., Форбс А., Макклейв С. А., Дженсен Г. Л., Вайцберг Д. Л., Дэвис А. Р.. Международные согласованные рекомендации по диетотерапии при панкреатите. JPEN J Parenter Enteral Nutr . 2012; 36 (3): 284-291.
22. Нэлли Д.М., Келли Э.Г., Кларк М., Риджуэй П.Назогастральное питание эффективно при тяжелом остром панкреатите: систематический обзор и метаанализ. Br J Nutr . 2014; 112 (11): 1769-1778.
23. Датта А.К., Гоэль А., Кирубакаран Р., Чако А., Тариан П. Сравнение назогастрального и назоеюнального зондового питания при тяжелом остром панкреатите. Кокрановская база данных Syst Rev . 2020; (3): CD010582.
24. Якобсон BC, Вандер Влит МБ, Хьюз М.Д., Маурер Р., Макманус К., Бэнкс, Пенсильвания. Проспективное рандомизированное исследование прозрачных жидкостей в сравнении с твердой диетой с низким содержанием жиров в качестве начального приема пищи при легком остром панкреатите. Клин Гастроэнтерол Гепатол . 2007; 5 (8): 946-951.
25. Moraes JM, Felga GE, Chebli LA, et al. Полноценная твердая диета в качестве начального приема пищи при остром панкреатите легкой степени является безопасной и сокращает продолжительность госпитализации: результаты проспективного рандомизированного контролируемого двойного слепого клинического исследования. Дж Клин Гастроэнтерол . 2010; 44 (7): 517-522.
26. Eckerwall GE, Tingstedt BB, Bergenzaun PE, Andersson RG. Немедленное пероральное кормление у пациентов с острым панкреатитом легкой степени безопасно и может ускорить выздоровление — это рандомизированное клиническое исследование. Clin Nutr . 2007; 26 (6): 758-763.
27. Meier R, Ockenga J, Pertkiewicz M, et al. Руководство ESPEN по энтеральному питанию: поджелудочная железа. Clin Nutr . 2006; 25 (2): 275-284.
28. Поропат Г., Гиляца В., Хаузер Г., Штимац Д. Составы для энтерального питания при остром панкреатите. Кокрановская база данных Syst Rev . 2015; (3): CD010605.
29. О’Брайен С.Дж., Омер Э. Хронический панкреатит и диетотерапия. Нутр Клин Практик . 2019; 34 Приложение 1: S13-S26.
30. Грир Дж. Б., Грир П., Сандху Б. С. и др. Питание и воспалительные биомаркеры у больных хроническим панкреатитом. Нутр Клин Практик . 2019; 34 (3): 387-399.
31. Домингес-Муньос Дж. Э., Филлипс М. Нутритивная терапия при хроническом панкреатите. Гастроэнтерол Clin North Am . 2018; 47 (1): 95-106.
32. Арванитакис М., Окенга Дж., Безмаревич М. и др.Руководство ESPEN по лечебному питанию при остром и хроническом панкреатите. Clin Nutr . 2020; 39 (3): 612-631.
Управление питанием при остром панкреатите: рассмотрение клинической практики
Авторские права © Автор (ы) 2020. Опубликовано Baishideng Publishing Group Inc. Все права защищены.Управление питанием при остром панкреатите: рассмотрение клинической практики
Нарисорн Лакананурак, Лия Грамлих
Нарисорн Лакананурак, Лия Грамлих, Медицинский факультет, Университет Альберты, Эдмонтон, T6G 2R3, Альберта, Канада
Нарисорн Лакананурак, Медицинский факультет, Медицинский факультет, Университет Чулалонгкорн,
10330, ТаиландВклад авторов : Все авторы в равной степени внесли свой вклад в этот документ с концепцией и дизайном исследования, обзором и анализом литературы, составлением и критическим пересмотром и редактированием, а также окончательным утверждением окончательной версии.
Заявление о конфликте интересов : Нет потенциальных конфликтов интересов. Финансовой поддержки нет.
Открытый доступ : Эта статья представляет собой статью с открытым доступом, которая была выбрана штатным редактором и полностью прорецензирована внешними рецензентами. Он распространяется в соответствии с лицензией Creative Commons Attribution NonCommercial (CC BY-NC 4.0), которая разрешает другим распространять, ремикшировать, адаптировать, использовать эту работу в некоммерческих целях и лицензировать свои производные работы на других условиях, при условии, что оригинал работа правильно процитирована и используется в некоммерческих целях.См .: http://creativecommons.org/licenses/by-nc/4.0/
Автор, ответственный за переписку : Нарисорн Лакананурак, доктор медицины, магистр наук, доктор, кафедра медицины, медицинский факультет, университет Чулалонгкорн, 254 Phayathai Road, Pathumwan , Бангкок 10330, Таиланд. [email protected]
Получено: 20 декабря 2019 г.
Началась экспертная оценка : 20 декабря 2019 г.
Первое решение : 12 января 2020 г.
Доработано: 7 марта 2020 г.
Принято: 21 апреля 2020 г.
Статья в прессе : 21 апреля 2020 г.
Опубликована онлайн: 6 мая 2020 г.
ВВЕДЕНИЕ
Острый панкреатит (ОП) — это острый воспалительный процесс поджелудочной железы с различным поражением других региональных тканей и систем удаленных органов.Диагноз основывается на двух из следующих трех критериев: (1) боль в животе, соответствующая панкреатиту; (2) уровень амилазы или липазы в сыворотке более чем в 3 раза превышает верхний предел нормы; и (3) характерные результаты визуализации брюшной полости [1]. Две наиболее распространенные этиологии АП — камни в желчном пузыре (40–70%) и алкоголь (25–35%). Другие причины включают прием лекарств, инфекционные заболевания и метаболические причины, такие как гиперкальциемия и гипертриглицеридемия [2].
Заболеваемость ОП колеблется от 4.9 и 73,4 случая на 100000 в мире [3,4]. Общая летальность колеблется от 5% до 20%, в зависимости от тяжести панкреатита. По степени тяжести это заболевание классифицируется как легкое, умеренно тяжелое или тяжелое в соответствии с пересмотренной классификацией Атланты 2012 г. [5]. В то время как уровень смертности при легком панкреатите очень низок (1%), при тяжелом панкреатите смертность резко возрастает на 30%. Кроме того, смертность может достигать 50% при обширном некрозе поджелудочной железы и до 80% при сепсисе [6].AP ассоциируется с продолжительностью пребывания в больнице около 30 дней и ежегодными расходами на здравоохранение в 2,6 миллиарда долларов в США [7,8].
Есть две отличительные фазы AP: (1) ранняя фаза (в течение 1 недели), характеризующаяся как локальным воспалением поджелудочной железы, так и синдромом системной воспалительной реакции и / или органной недостаточностью; и (2) поздняя фаза (> 1 недели), характеризующаяся местными осложнениями и / или стойкой органной недостаточностью [2]. Следовательно, профилактика и лечение синдрома системной воспалительной реакции, органной недостаточности и осложнений являются обязательными для снижения заболеваемости и смертности при этом потенциально смертельном заболевании.В настоящее время не найдено конкретных лекарств для эффективного лечения ОП, поэтому лечение сосредоточено на поддерживающих вмешательствах, таких как жидкостная реанимация и вмешательство в питание. Управление питанием продемонстрировало необходимость не только в профилактике и лечении недостаточности питания, но и в предотвращении системного воспаления, уменьшении осложнений и, следовательно, в изменении течения болезни [9,10].
Эта статья направлена на обзор последних данных и рекомендации основанного на фактических данных практического подхода к управлению питанием при ОП, который включает оценку пациентов, управление питанием при легком, умеренно тяжелом и тяжелом панкреатите и внешнесекреторной недостаточности поджелудочной железы (ПЭН) при ОП. .
ПАТОФИЗИОЛОГИЯ НЕДОСТАТОЧНОСТИ И ОБМЕН НУТРИЕНТОВ В AP
Множественные факторы могут ухудшить статус питания при AP, и одним из наиболее важных факторов является воспаление. Воспалительные цитокины (фактор некроза опухоли альфа, интерлейкины 1 и 6) и гормоны стресса (кортизол, катехоламины и глюкагон), высвобождаемые при панкреатите, вызывают нарушение метаболизма, подобное сепсису [11].
Расход энергии в покое (РЗЭ) у пациентов с панкреатитом обычно выше, чем у здоровых людей, из-за гиперметаболизма, вызванного воспалением, и / или септических осложнений.РЗЭ, измеренные с помощью непрямой калориметрии (ИК), увеличивались у 61% пациентов с ОП и у 82% при панкреатите, осложненном инфекцией. m ± SD измеренных REE составило 111% ± 15% при легком панкреатите, 126% ± 10% при тяжелом панкреатите и 120% ± 11% при панкреатическом сепсисе, по сравнению с предсказанными REE по уравнению Харриса-Бенедикта [12]. В этом случае нутритивная поддержка может помочь восстановить энергетический баланс и предотвратить недоедание.
Сильное воспаление приводит к катаболизму белков. Аминокислоты, высвобождаемые при распаде белка, служат субстратом для производства белка острой фазы.Это было обнаружено у 80% пациентов с тяжелым некротическим панкреатитом [11]. Баланс азота может быть отрицательным до 20-40 г / сут [13,14], и у пациентов с отрицательным балансом смертность в десять раз выше, чем у пациентов с нормальным балансом [15]. Мышечная масса и функция, измеряемая по силе захвата и силе дыхательных мышц, быстро снижались в течение 5 дней без нутриционной поддержки у здоровых мужчин, страдающих АП [16].
Что касается углеводного обмена, гипергликемия часто встречается у пациентов с панкреатитом.Это результат инсулинорезистентности, увеличения выработки глюкозы печенью (глюконеогенез) и нарушения секреции инсулина, вызванного повреждением бета-клеток [17]. Гипергликемия связана с некрозом поджелудочной железы и инфекционными осложнениями. В результате у всех пациентов следует контролировать и контролировать уровень глюкозы в крови [18].
Гипертриглицеридемия встречается часто и может быть причиной или следствием панкреатита. Катаболизм липидов и нарушение клиренса липидов в результате снижения секреции инсулина способствуют повышению уровня триглицеридов в сыворотке [18].При отсутствии камней в желчном пузыре и значительном употреблении алкоголя тяжелая гипертриглицеридемия (уровень триглицеридов в сыворотке> 11,3 ммоль / л) может рассматриваться как причина АД [2,19]. Следует контролировать уровень триглицеридов в сыворотке крови, особенно у тех, кто получает внутривенные липидные эмульсии (ИЛЭ).
Недоедание при ОП может возникать из-за пониженного перорального приема в результате анорексии, болей в животе, рвоты, кишечной непроходимости, пареза желудка, обструкции выходного отверстия желудка и несоответствующего голодания для отдыха поджелудочной железы [20].Кроме того, экзокринная дисфункция поджелудочной железы приводит к нарушению переваривания питательных веществ и может сохраняться до 6-18 месяцев после острого приступа [21].
Нарушения микронутриентов часто встречаются при ОП. Хроническое употребление алкоголя часто приводит к дефициту питательных микроэлементов из-за недостаточного потребления, снижения абсорбции и нарушения хранения и использования питательных веществ. У пациентов с алкоголизмом биохимические данные демонстрируют дефицит нескольких питательных микроэлементов, включая витамины B1, B2, B3, B12, C, A, фолиевую кислоту и цинк [22,23].Более того, риск дефицита увеличивается у пациентов с тяжелым осложненным панкреатитом, требующим длительного приема. Этиология многофакторна, включая снижение потребления, нарушение пищеварения и повышенную потребность в тяжелом воспалении. Гипокальциемия может возникнуть у 40-60% пациентов. Основные причины гипокальциемии могут быть связаны с омылением кальция, гипомагниемией, снижением высвобождения паратироидного гормона и повышенным уровнем кальцитонина [24,25].
КОНЦЕПЦИЯ «ПАНКРЕАТИЧЕСКОГО ОТДЫХА»
Питательные вещества, поступающие в желудочно-кишечный тракт проксимальнее средней части тощей кишки (примерно на 40 см дистальнее связки Trietz), стимулируют секрецию ферментов поджелудочной железы.Традиционно считалось, что это может привести к усилению самопереваривания поджелудочной железы и обострению панкреатита. В результате концепция «панкреатического покоя» ранее использовалась для руководства лечением ОП с 1970-х годов. Эта концепция гласит, что энтеральное питание (ЭП) следует начинать только тогда, когда боль в животе полностью исчезла и ферменты поджелудочной железы нормализовались. На основе этой концепции используются стратегии минимизации стимуляции поджелудочной железы, такие как парентеральное питание (ПП), элементарная смесь и поэтапное введение пероральной диеты, начиная с прозрачной жидкости.Однако эта концепция основана только на физиологических предположениях и не поддерживается хорошими научными данными и действительно может привести к ухудшению нутритивного статуса и плохим результатам [7,26].
Дальнейшие исследования показали, что секреция ферментов поджелудочной железы значительно снижена при АР, и секреция была обратно пропорциональна тяжести панкреатита. Более низкая секреция трипсина (в 16 раз), амилазы (в 22 раза) и липазы (в 102 раза) была обнаружена при тяжелом панкреатите [27]. Кроме того, раннее применение ЭП приводило к клинически значимому обострению симптомов только в 4% случаев [28].Эти данные предполагают, что поврежденные ацинарные клетки не могут полностью реагировать на физиологические стимулы, и могут объяснить, почему энтеральное питание безопасно и не ухудшает самопереваривание во время приступа панкреатита.
С 1990-х годов несколько рандомизированных контролируемых исследований (РКИ) и метаанализов продемонстрировали безопасность и преимущества энтеральных питательных веществ с точки зрения смертности, полиорганной недостаточности, инфекции, осложнений и хирургического вмешательства [29–32]. Эти данные подтверждают назначение ЭП для стимуляции и поддержания функции кишечника, что противоположно «отдыху поджелудочной железы», который может привести к дисфункции кишечника и ухудшению клинических исходов.Энтеральные питательные вещества помогают поддерживать целостность кишечника, лимфоидную ткань, связанную с кишечником, и состав кишечной микробиоты. Эта стратегия снижает транслокацию бактерий, эндотоксинов и ферментов поджелудочной железы, что может ослабить системное воспаление, полиорганную недостаточность, инфекцию и тяжесть заболевания при ОП [26,33-35]. На основании этих данных желудочно-кишечный тракт следует рассматривать как важный орган у пациентов с панкреатитом.
ОЦЕНКА ПАЦИЕНТА
Основная цель оценки пациента: (1) спланировать нутритивную поддержку в зависимости от тяжести панкреатита; (2) Оценить статус питания; и (3) Выявить группы риска, которым требуются особые потребности в питании [22].
Поскольку ОП имеет широкий спектр тяжести заболевания, подход к управлению питанием различается между легким, самоограничивающимся заболеванием и тяжелым, фульминантным панкреатитом. Таким образом, полезно оценить серьезность заболевания, прежде чем принимать решение о плане лечения питанием. В пересмотренной классификации Атланты 2012 (таблица 1) определены три степени тяжести: легкий, умеренно тяжелый, тяжелый панкреатит в зависимости от органной недостаточности (модифицированный балл Маршалла ≥ 2, таблица 2) и местные или системные осложнения.
Таблица 1 Пересмотренная классификация Атланты 2012 г. по степени тяжести острого панкреатита.| Степень тяжести | Критерии |
| Легкая | Отсутствие органной недостаточности |
| Отсутствие местных или системных осложнений, которые разрешаются в течение 48984 | |
| Местные или системные осложнения без стойкой органной недостаточности | |
| Тяжелая | Стойкая органная недостаточность (> 48 ч) |
| Одноорганная недостаточность | |
| Полиорганная недостаточность |
| Органная система | Оценка | ||||
| 0 | 1 | 2 | 3 | > 400 | 301-400 | 201-300 | 101-200 | ≤ 100 |
| Ренал 1 | ≤ 134 | 134-169 | 170-310 | 311-439 | > 439 |
| Cr сыворотки (мг / дл) | <1.4 | 1,4-1,8 | 1,9-3,6 | 3,6-4,9 | > 4,9 |
| Сердечно-сосудистое (САД, мм рт. Ст.) 2 | > 90 | <90, чувствительно к жидкости | <90, не реагирует на жидкость | <90, pH <7,3 | <90, pH <7,2 |
Существовавшее ранее недоедание было обнаружено в 30% случаев во время первоначального приступа. В группы риска недоедания входят хронический алкоголизм и пожилые люди [22].Недоедание связано с отрицательными исходами (осложнениями, более высокой заболеваемостью и длительным пребыванием в больнице) [13,36], и поэтому статус питания следует оценивать с помощью проверенных инструментов скрининга и оценки питания, особенно в группах высокого риска.
Пациентам с хроническим алкоголизмом требуется особое внимание для оценки клинических признаков и / или биохимических уровней питательных микроэлементов (витамин B1, B2, B3, B12, C, A, фолиевая кислота и цинк) [22]. Пациенты с ожирением могут рассматриваться и лечиться как группы риска тяжелого панкреатита.Мета-анализ продемонстрировал значительно более высокую частоту тяжелого панкреатита [отношение шансов (OR) = 2,9, 95% доверительный интервал (CI): 1,8–4,6], местных осложнений (OR = 3,8, 95% CI: 2,4–6,6), системных осложнения (OR = 2,3, 95% CI: 1,4–3,8) и смерть (OR = 2,89, 95% CI: 1,1–7,36) у пациентов с ожирением [37,38]. Патофизиология может быть связана с нерегулируемым липолизом висцерального жира вокруг поджелудочной железы, который ингибирует митохондриальный комплекс I и V, что приводит к некрозу поджелудочной железы и плохим результатам [39].
УПРАВЛЕНИЕ ПИТАНИЕМ ПРИ ЛЕГКОЙ АП
Легкая АП встречается в 75% -85% всех эпизодов АП. Это преходящее, самоограничивающееся состояние, поэтому специализированное питание (ЭП и / или ПП) обычно не требуется [7]. Пациенты могут употреблять оральную диету, когда уменьшаются боли в животе, тошнота и рвота. Можно безопасно начать полноценную твердую диету, а поэтапное введение пероральной диеты, начиная с прозрачных жидкостей, не требуется. Рандомизированные испытания, сравнивающие прозрачную жидкую диету и твердую диету при легком панкреатите, показали, что начало перорального кормления с твердой диеты было безопасным, хорошо переносимым и могло сократить продолжительность пребывания в больнице на 2 дня по сравнению с жидкой диетой [40-42] .Что касается состава рациона, даже несмотря на то, что в предыдущих исследованиях использовалась диета с низким содержанием жиров (<30% общей энергии) [40,42], эта диета не подтверждается хорошими научными данными и может привести к недостаточному потреблению энергии. Питание через зонд рекомендуется только в том случае, если оральное питание невозможно более 5 дней [13]. Примером этого являются пациенты с плохим пероральным приемом в результате постоянной тошноты, рвоты и болей в животе.
УПРАВЛЕНИЕ ПИТАНИЕМ В УМЕРЕ ТЯЖЕЛЫХ И ТЯЖЕЛЫХ УСЛОВИЯХ AP
Нутриционная поддержка хорошо документирована в своих преимуществах при умеренно тяжелом и тяжелом панкреатите.В этой группе пациентов следует учитывать следующие аспекты.
Потребность в питательных веществах
Потребность в энергии следует оценивать с помощью IC, если это возможно, или 25 ккал / кг / день можно использовать в качестве целевого значения энергии. Многие нестатические переменные влияют на расход энергии при тяжелом панкреатите, например, температура тела, объем и принимаемые лекарства. Эти переменные приводят к низкой точности прогнозных уравнений. IC является целевым стандартом для определения расхода энергии, и, таким образом, измерение IC может помочь предотвратить перекармливание или недокорм.Потребность в энергии, будь то калориметрия или прогнозное уравнение, следует пересматривать чаще, чем раз в неделю, чтобы достичь надлежащего энергетического баланса. Расчетная потребность в белке выше, чем у здоровых людей (1,2–1,5 г / кг / сут). Это может улучшить азотный баланс и связано со снижением 28-дневной смертности у пациентов в критическом состоянии [43]. Необходимо обеспечить смешанный источник энергии из углеводов, жиров и белков [20,44].
Рекомендуется суточная доза поливитаминов и микроэлементов, особенно пациентам, получающим общее ПП [44].Микронутриенты следует добавлять пациентам с подтвержденным или предполагаемым дефицитом.
Способ нутриционной поддержки
EN: Энтеральное питание следует рассматривать как предпочтительный способ нутриционной поддержки [2,13,45]. Метаанализ 5 РКИ (348 пациентов) 2018 года показал, что ЭП по сравнению с ПП ассоциировалась со значительным снижением смертности с соотношением риска (ОР) 0,36 (95% ДИ: 0,20-0,65) и полиорганной недостаточностью. с ОР 0,39 (95% ДИ: 0,21-0.73) [31]. Эти преимущества были подтверждены в недавнем метаанализе 11 исследований с участием 562 пациентов. Результаты показали, что ЭП значительно снижает уровень смертности (ОР = 0,43; 95% ДИ: 0,23-0,78), риск осложнений (ОР = 0,53; 95% ДИ: 0,39-0,71) и среднюю продолжительность пребывания в больнице (средняя разница = -2,93, 95% ДИ: от -4,52 до -1,34) [32]. Местные осложнения (некроз, свищи, асцит, псевдокиста) не являются противопоказаниями для энтерального питания [13].
EN следует начинать после адекватной реанимации и стабильного гемодинамического статуса.Многие исследования показали преимущества раннего энтерального питания при тяжелом панкреатите. Мета-анализ показал, что ранняя ЭП в течение 48 часов после госпитализации была связана со значительным снижением смертности, инфекционных осложнений, полиорганной недостаточности, хирургического вмешательства и продолжительности госпитализации [46,47]. Напротив, ранняя ЭП не может быть лучше, чем пероральная диета по требованию через 72 часа. В многоцентровом РКИ с участием 205 пациентов сравнивалась ранняя ЭП в течение 24 часов и оральная диета по требованию через 72 часа, с питанием через зонд на 4 день, если пероральная диета не переносилась.Между двумя группами не было существенной разницы в частоте серьезной инфекции или смерти, и зондовое кормление можно было предотвратить у 69% пациентов в группе по требованию [48]. Более 80% пациентов в этом исследовании были госпитализированы в медицинское отделение, и только 18% потребовалось госпитализация в отделение интенсивной терапии (ОИТ), что указывает на то, что у большинства из них на самом деле может быть панкреатит средней степени тяжести. Этот результат предполагает, что у пациентов, не получающих ОИТ, пероральную диету по требованию можно попробовать в течение 3 дней, а кормление через зонд следует начать на 4-й день, если пероральная диета не принесла успеха.Однако для того, чтобы дать рекомендацию по этой проблеме, необходимы дополнительные данные.
У пациентов, которым требуется зондовое питание, в соответствии с действующими рекомендациями рекомендуется непрерывное питание вместо болюсного [2,13]. Лучшая переносимость кормления и меньшее количество перерывов в доставке ЭП из-за повышенных остаточных количеств и рвоты были обнаружены при непрерывной инфузии по сравнению с группой болюсного введения [49,50].
Учитывая, что ферменты поджелудочной железы, стимулируемые энтеральными питательными веществами, могут приводить к самоперевариванию поджелудочной железы, роль антисекреторных агентов, включая соматостатин и его аналоги (октреотид), изучалась в нескольких исследованиях.Однако результат остается неубедительным. РКИ и недавний Кокрановский обзор не выявили положительного эффекта в группе лечения в отношении смертности, осложнений и продолжительности боли [51,52]. Это может быть связано с резким снижением секреции поджелудочной железы во время АП.
Желудочное против кормление из тонкой кишки: Традиционно считается, что кормление через тонкий кишечник было связано с меньшей стимуляцией поджелудочной железы и самоперевариваемой пищей. Тем не менее, метаанализ показал, что назогастральное кормление не уступает назоеюнальному кормлению с точки зрения обострения боли (ОР = 0.94; 95% ДИ: 0,32-2,70), аспирация (ОР = 0,46; 95% ДИ: 0,14-1,53), соблюдение энергетического баланса (ОР = 1,00; 95% ДИ: 0,92-1,09) и смертность (ОР = 0,69; 95% ДИ: 0,37–1,29) [53]. Это обусловлено отсутствием воздействия на секрецию поджелудочной железы независимо от способа кормления во время АП. Начало ЭП в желудке технически проще, дешевле и может сократить время начала ЭП, в то время как кормление тонкой кишкой обычно требует специальной техники и требует больше времени для установки зонда. По этим причинам назогастральный зонд может использоваться в качестве терапии первой линии для достижения преимуществ ранней ЭП у пациентов с тяжелым панкреатитом.
Кормление тощей кишкой следует рассматривать у пациентов, которые не переносят желудочное кормление. Это может быть необходимо пациентам с тяжелым парезом желудка или частичной обструкцией выходного отверстия желудка из-за отека поджелудочной железы или псевдокист [54]. Интраоперационная еюностомическая трубка может быть установлена для послеоперационного кормления пациентам, перенесшим операцию по другим показаниям [13].
Полимерный против элементарных / полуэлементных формул: Считается, что элементарные и полуэлементные формулы вызывают меньшую стимуляцию поджелудочной железы, требуют меньшего переваривания и легко всасываются в тонком кишечнике.Физиологическое исследование на здоровых людях показало, что секреция ферментов поджелудочной железы снизилась на 50%, когда полимерная формула была заменена на элементарную [55]. Таким образом, полуэлементные и элементарные формулы использовались во многих исследованиях AP. Несмотря на то, что несколько исследований напрямую сравнивают элементные / полуэлементные формулы и полимерные формулы, есть одно РКИ и одно ретроспективное когортное исследование, показывающие, что элементные и полуэлементные формулы не превосходят полимерные смеси с точки зрения переносимости питания, диареи и инфекционных осложнений. [56,57].Кроме того, метаанализ 10 РКИ с использованием метода косвенной корректировки показал, что использование полуэлементной или элементарной смеси не привело к значительным различиям в непереносимости кормления (ОР = 0,62; 95% ДИ: 0,10-3,97), инфекции ( ОР = 0,48; 95% ДИ: 0,06–3,76) и смерть (ОР = 0,63; 95% ДИ: 0,04–9,86) [58]. Кроме того, еженедельная стоимость полуэлементной формулы в 7 раз выше, чем полимерной формулы [7]. Следовательно, использование полимерной формулы может быть эффективным и практичным при тяжелом панкреатите.
PN: PN показан, когда пациенты не переносят EN. У некоторых пациентов кишечная недостаточность I или II типа развивается в результате системных или местных осложнений, таких как тяжелая кишечная непроходимость и дуоденальная непроходимость из-за отека поджелудочной железы или псевдокисты. Когда требуется PN, рекомендуется смешанный топливный раствор (углевод, белок и липиды). Уровень глюкозы не должен превышать максимальный уровень окисления глюкозы (4-7 мг / кг / мин или 5-6 г / кг / день), а целевой диапазон глюкозы крови рекомендуется 7,7-10 ммоль / л [59, 60].ИВС можно безопасно начинать, и рекомендуемая доза составляет 0,8–1,5 г / кг / сут [20,44]. Если концентрация триглицеридов в сыворотке превышает 4,5 ммоль / л [18,61], может потребоваться уменьшение или прекращение приема ИЛЭ. Возможно, потребуется отложить начало PN до 5-7 дней после поступления [20,59]. Поскольку начало ПП на этом этапе может быть связано с лучшими результатами, включая снижение смертности, общих осложнений и продолжительности госпитализации [62]. Необходимы дальнейшие исследования, чтобы подтвердить подходящее время и клинические преимущества ПП при ОП с кишечной недостаточностью.Рекомендуемый способ нутритивной поддержки представлен на Рисунке 1.
Рис. 1. Схема питания при остром панкреатите. ICU: отделение интенсивной терапии; NG: назогастральный зонд; Нью-Джерси: Назоеюнальная трубка.
Роль пищевых добавок
Глютамин: Глютамин считается условно незаменимой аминокислотой с антиоксидантным действием, улучшающей иммунную функцию и целостность кишечника.Его истощение было продемонстрировано у пациентов в критическом состоянии из-за повышенной потребности во время метаболического стресса [63]. Добавки глутамина могут играть роль при серьезных заболеваниях, включая тяжелый панкреатит [10].
Мета-анализ 12 РКИ продемонстрировал, что глутамин был связан с более низкими инфекционными осложнениями (ОР = 0,58; 95% ДИ: 0,39-0,87) и смертностью (ОР = 0,30; 95% ДИ: 0,15-0,60). В этом исследовании только пациенты, получавшие ПП, но не ЭП, показали статистически значимые преимущества [64].Другой метаанализ подтвердил эти данные, и, опять же, внутривенный прием глутамина имел больше преимуществ [65]. Недавнее РКИ энтерального глутамина показало улучшение показателей органной недостаточности без значительных преимуществ в отношении инфицированного некроза и смертности [66]. В целом, внутривенное введение глутамина, по-видимому, дает преимущества у пациентов с полным ПП, в то время как положительные эффекты энтерального глутамина необходимо исследовать в будущем. Рекомендуемая доза добавок глютамина составляет 0,3-0.5 г / кг / сут.
Пробиотики: Дисфункция кишечного барьера может вызывать бактериальную транслокацию и инфицированный некроз, что является основной причиной заболеваемости и смертности при тяжелом панкреатите. Пробиотики могут помочь улучшить целостность кишечника и иммунную функцию и, таким образом, предотвратить бактериальную транслокацию [67,68]. Lactobacillus plantarum снизил кишечную проницаемость, инфекционные осложнения, системное воспаление и полиорганную недостаточность, но не повысил уровень смертности в небольших РКИ [69–71].Напротив, многовидовой пробиотический препарат не уменьшал инфекцию и был связан с повышенной смертностью (ОР = 2,53; 95% ДИ: 1,22–5,25) [72]. Эти данные предполагают потенциальные преимущества пробиотика одного штамма ( Lactobacillus plantarum ) при тяжелом панкреатите; однако необходимы дальнейшие подтвержденные исследования, прежде чем можно будет подтвердить его преимущества.
Омега-3 жирные кислоты: Омега-3 жирные кислоты продемонстрировали полезные противовоспалительные эффекты и могут улучшить системное воспаление, полиорганную недостаточность и клинические исходы при тяжелом панкреатите.Мета-анализ 8 небольших РКИ продемонстрировал, что введение омега-3 жирных кислот было полезным для снижения смертности, инфекционных осложнений и продолжительности пребывания в больнице, особенно при парентеральном введении. Тем не менее, необходимы крупные и тщательно разработанные РКИ для выяснения эффективности добавок омега-3 жирных кислот при тяжелом панкреатите [73].
Антиоксиданты: Антиоксиданты (витамин A, витамин C, витамин E, селен и N-ацетилцистеин) могут уменьшить воспаление и улучшить исходы при тяжелом панкреатите.Тем не менее несколько небольших исследований с различными дозами и продолжительностью приема антиоксидантов привели к смешанным результатам [10]. Чтобы подтвердить потенциальную пользу антиоксидантов при этом заболевании, необходимы более масштабные и хорошо спланированные клинические испытания.
PEI IN AP
Хотя нет данных, подтверждающих рутинное использование ферментов поджелудочной железы в течение первых 5-10 дней AP, данные подтверждают, что некоторые пациенты испытывают экзокринную дисфункцию в течение определенного периода времени после острого приступа панкреатита [74,75] . Мета-анализ 2018 года, содержащий 32 исследования (1495 пациентов), показал, что распространенность PEI после панкреатита составляла 27.1%. Это состояние напрямую связано со степенью повреждения паренхимы поджелудочной железы и чаще встречается при алкогольном панкреатите (22,7%), тяжелом панкреатите (33,4%) и некротическом панкреатите (32%) [76]. Пациенты должны находиться под наблюдением на предмет симптомов нарушения пищеварения (диарея, стеаторея) и / или неинвазивных функциональных тестов поджелудочной железы (, например, ., Фекальный жир и фекальная эластаза) [77] в течение как минимум 6-18 месяцев после АП, особенно при алкоголизме. , тяжелый и некротический панкреатит. Добавку ферментов поджелудочной железы следует начинать, как показано [75].
CLINICAL VIGNETTE
Случай 1
Женщина 48 лет поступила с острым началом сильной боли в эпигастрии с тошнотой и рвотой. У нее не было серьезной истории болезни и она отрицала употребление алкоголя. Масса ее тела была стабильной, индекс массы тела 24 кг / м 2 2 . Первоначальные лабораторные результаты показали липазу 560 Ед / л (0-60 Ед / л). УЗИ брюшной полости выявило несколько камней в желчном пузыре с нормальным желчным протоком. При поступлении у нее не было органной недостаточности, поэтому был диагностирован острый желчнокаменный панкреатит легкой степени.Боль в животе и тошнота уменьшились после приема анальгезии и противорвотных препаратов. Какая диета является наиболее подходящей для этого пациента?
Комментарий: У больного классический острый желчнокаменный панкреатит. Учитывая, что степень тяжести ее заболевания была легкой, а боли в животе и тошнота уменьшились, следует начать твердую пероральную диету. Поэтапный подход, начиная с прозрачной жидкости, не нужен и может быть связан с более длительным пребыванием в больнице у этого пациента.
Случай 2
Мужчина 55 лет обратился с жалобой на острую сильную боль в эпигастрии, сопровождавшуюся изменением сознания, рвотой и лихорадкой. В анамнезе он хронически употреблял алкоголь 100 г / сут более 20 лет. Его масса тела была стабильной с индексом массы тела 22 кг / м 2 . Первоначальные лабораторные результаты продемонстрировали липазу 720 Ед / л (0-60 Ед / л) и креатинин 180 мкмоль / л (50-120 мкмоль / л). Ему интубировали для защиты дыхательных путей и поместили в отделение интенсивной терапии.Первоначальное лечение включало внутривенное введение раствора кристаллоидов и симптоматическое лечение. На 2-й день приема его креатинин повысился до 190 мкмоль / л. Диагностирован тяжелый острый алкогольный панкреатит. Какое диетическое лечение является наиболее подходящим для этого пациента?
Комментарий: У больного диагностирован острый алкогольный панкреатит со стойкой органной недостаточностью. Ему интубировали и поместили в реанимацию. Следовательно, раннюю ЭП следует начинать после адекватной реанимации.Назогастральный зонд можно использовать для достижения раннего ЭП. Стандартный полимерный состав можно вводить со скоростью 20 мл в час, и его следует титровать для удовлетворения потребностей в белке и энергии (1,2–1,5 г / кг / день и 25 ккал / кг / день, соответственно). Принимая во внимание хронический алкоголизм в анамнезе, можно оценить уровни микронутриентов, включая витамины B1, B2, B3, B12, C, A, фолиевую кислоту и цинк, и следует начать лечение, если есть доказательства дефицита микронутриентов.
Прогресс болезни
На 5-й день госпитализации у него все еще сохранялась температура и сильная боль в животе, требовалось круглосуточное внутривенное введение опиоидов.Физикальное обследование выявило гипотензию, отсутствие звука кишечника, выраженное вздутие живота и общую болезненность живота. Он не мог переносить энтеральное питание из-за рвоты. Компьютерная томография показала обширный некроз поджелудочной железы с газом в теле и хвосте поджелудочной железы, а также общее расширение тонкой и толстой кишки. Были назначены вазопрессоры и антибиотики, и была запланирована хирургическая обработка раны. Какое диетическое лечение является наиболее подходящим в соответствии с его клиническим статусом?
Комментарий: У больного инфицированный панкреонекроз с септическим шоком.Он не мог переносить ЭП из-за тяжелой кишечной непроходимости. В результате в данном случае был указан PN. ИВС можно назначать, если уровень триглицеридов в сыворотке был менее 4,5 ммоль / л, а доза должна составлять 0,8–1,5 г / кг / сут. Уровень глюкозы в крови следует контролировать и контролировать в пределах 7,7-10 ммоль / л. В этом случае можно рассмотреть возможность внутривенного введения глутамина в дозе 0,3-0,5 г / кг / сут.
ЗАКЛЮЧЕНИЕ
ОП — это распространенное желудочно-кишечное заболевание с различной степенью тяжести, от самоограничивающегося легкого ОП до разрушительного и смертельного тяжелого ОП.В настоящее время лечение конкретного заболевания остается неясным, а поддерживающая терапия, включая меры по питанию, имеет решающее значение. Лечебное питание не только помогает предотвратить недоедание, но и является ключом к уменьшению системного воспаления, осложнений и смерти. Оценка степени тяжести — это первый шаг к правильному питанию. При панкреатите легкой степени пациенты обычно могут перейти на твердую пероральную диету и не нуждаются в специализированном питании. При панкреатите средней тяжести или тяжелой степени кишечник следует рассматривать как важный орган, и следует назначать ЭП на ранней стадии для поддержания функции кишечника и достижения положительных клинических результатов.Питание через желудок и тощую кишку одинаково эффективно при тяжелом панкреатите. Полимерная формула безопасна и недорога по сравнению с элементной формулой. PN следует назначать только пациентам, которые не переносят EN. Некоторые пищевые добавки, такие как внутривенное введение глутамина пациентам с полным ПП, могут привести к положительным результатам. Однако в других случаях необходимы дальнейшие исследования. В таблице 3 собраны все рекомендации и области, требующие дальнейшего изучения в AP.
Таблица 3 Резюме управления питанием при тяжелом остром панкреатите и области будущих исследований.| Рекомендация | Области для будущих исследований |
| Потребность в энергии следует измерять с помощью IC, или можно использовать 25 ккал / кг / день | Роль пероральной диеты по требованию |
| Требования к белку составляют 1,2-1,5 г / кг / день | Полимерная формула против элементарной / полуэлементной формулы |
| Рекомендуется ранний EN в течение 48 часов II | |
| Приемлемо кормление через желудок или тощую кишку | Роль энтерального глутамина, пробиотиков, жирных кислот омега-3, антиоксидантов |
| Внутривенное введение глутамина может быть рассмотрено у пациентов с TPN | |
| PEI под контролем алкогольный, тяжелый и некротический панкреатит |
БЛАГОДАРНОСТИ
Авторы выражают благодарность Chanokporn Piempring, MD, за полезную и критически отредактированную рукопись.
Источник рукописи: Приглашенная рукопись
Тип специальности: Медицина, исследовательская и экспериментальная
Страна / территория происхождения: Канада
Классификация научного качества отчета экспертной оценки
Оценка A (отлично): 0
Оценка B (очень хорошо ): B
Оценка C (хорошо): C, C
Оценка D (удовлетворительная): 0
Оценка E (плохая): 0
P-рецензент: Huan C, Manenti A, Neri V S-редактор: Тан JZ L-редактор: Электронный редактор: Xing YX
Как снизить риск будущих атак панкреатита — Основы здоровья от клиники Кливленда
Вы когда-нибудь испытывали сильную острую боль в животе из-за панкреатита? Или это было больше похоже на постоянный тупой дискомфорт?
Клиника Кливленда — некоммерческий академический медицинский центр.Реклама на нашем сайте помогает поддерживать нашу миссию. Мы не поддерживаем продукты или услуги, не принадлежащие Cleveland Clinic. Политика
В любом случае вам необходимо решить эту проблему, тесно сотрудничая с врачом и внося важные изменения в образ жизни.
«Раннее и агрессивное лечение панкреатита может улучшить результаты, ускорить выздоровление и ограничить количество осложнений», — говорит специалист по поджелудочной железе Прабхлин Чахал, доктор медицины.
Что вызывает панкреатит?
Панкреатит возникает, когда воспаляется поджелудочная железа — длинный орган, расположенный за желудком и рядом с тонкой кишкой.Поджелудочная железа помогает пищеварению и помогает регулировать уровень гормонов сахара и метаболизма.
«Панкреатит бывает двух форм: острой и хронической», — говорит доктор Чахал. «Проблемы начинаются, когда поджелудочная железа слишком быстро высвобождает пищеварительные ферменты, и они атакуют саму поджелудочную железу вместо того, чтобы расщеплять пищу, которую вы едите».
Если у вас острый случай, симптомы могут варьироваться от легкого дискомфорта до опасных для жизни. Легкие приступы обычно длятся несколько дней.
Приступ панкреатита от умеренного до тяжелого может вызвать:
- Полиорганная недостаточность (почечная, легочная или сердечная).
- Кровотечение / образование тромбов в кровеносных сосудах.
- Разрушение поджелудочной железы (некроз).
- Инфекция.
- Образование воспалительного скопления жидкости (псевдокисты).
- Недоедание.
- Сепсис.
- Торможение работы желудочно-кишечного тракта.
Хронический панкреатит, однако, является результатом прогрессирующего длительного воспаления. Он может развиться после острого приступа, и со временем могут появиться следующие симптомы:
- Боль в верхней части живота и вздутие живота.
- Тошнота и рвота.
- Мальабсорбционная диарея.
- Снижение веса (из-за того, что ваше тело неправильно усваивает питательные вещества).
- Диабет.
- Дефицит жирорастворимых витаминов, таких как A, D, E и K.
Как остановить будущие приступы
Возможно купирование будущих приступов панкреатита. Чтобы начать здоровый образ жизни, важно внести некоторые изменения в свое поведение и образ жизни.
«Заболевание поджелудочной железы существенно влияет на качество вашей жизни», — говорит она.«Успешное управление потребует многопрофильной помощи, включая изменение поведения и образа жизни».
Если у вас продолжаются обострения панкреатита, это может в конечном итоге привести к рубцеванию поджелудочной железы, поэтому крайне важно внести эти необходимые изменения. Сделайте все возможное, чтобы снизить эти факторы риска:
- Желчные камни . Если у вас диагностированы камни в желчном пузыре и вы перенесли приступ панкреатита, удаление желчного пузыря может помочь предотвратить проблемы в будущем.
- Пьян .Чрезмерное употребление алкоголя вызывает до 70% случаев хронического панкреатита и почти половину случаев острого панкреатита, поэтому имеет смысл отказаться от употребления алкоголя.
- Курение . Это может ухудшить ваши результаты, ускорить прогрессирование болезни (хронического панкреатита) и повысить риск рака поджелудочной железы.
- Плохое диета . Избегайте продуктов с высоким содержанием жиров, особенно жареной пищи, которая может вызвать нагрузку на пищеварительную систему. Вместо этого сосредоточьтесь на диете с низким содержанием жиров и высоким содержанием белка, богатой витаминами и питательными веществами.Пациенты с хроническим панкреатитом часто получают пользу от включения в свой рацион масла триглицеридов со средней длиной цепи (MCT). Вы также можете рассмотреть возможность приема искусственных пищеварительных ферментов, которые помогают вашему организму расщеплять пищу и усваивать питательные вещества и витамины. Проконсультируйтесь с врачом о том, стоит ли принимать искусственные пищеварительные ферменты.
Как справиться с болью
Если панкреатит вызывает у вас слабую или умеренную боль, могут помочь безрецептурные обезболивающие, такие как ацетаминофен или ибупрофен, принятые в течение короткого периода времени.
«При постоянной и сильной боли рассмотрите возможность консультации с врачом по обезболиванию, который часто назначает лекарства, называемые нейро-модуляторами боли», — говорит д-р Чахал. «Пациентам также предлагается специализированная процедура, называемая блокадой чревного сплетения, для купирования хронической боли, связанной с хроническим панкреатитом».
Если у вас случился острый приступ, не допускайте его повторения, начав с приема лекарств и изменив поведение. В некоторых случаях необходимы дополнительные эндоскопические процедуры, такие как эндоскопическое ультразвуковое исследование (ЭРХПГ) или хирургическое вмешательство.
Если у вас есть камни в поджелудочной железе, ваш врач может использовать ударные волны, чтобы разбить камни, которые создают закупорку.
«Это может помочь при боли и повторяющихся обострениях поджелудочной железы», — говорит она. «При необходимости хирурги могут удалить пораженные или воспаленные участки поджелудочной железы или всю поджелудочную железу.
В конечном итоге, лечение этого состояния часто требует как медицинских, эндоскопических, хирургических, так и личных изменений.
Советы и предложения — Guts UK
Советы и предложения по управлению пищевыми продуктами
Прием пищи и поддержание нутритивного статуса может быть сложной задачей для людей с хроническим панкреатитом.Причины этого сложны и могут включать снижение общего потребления пищи, отказ от определенных продуктов и питательных веществ (например, жиров), плохое или полное отсутствие всасывания питательных веществ в кишечнике (мальабсорбция), боль, тошнота, рвота, вздутие живота, негативные чувства по отношению к кишечнику. определенные продукты и питание в целом, диабет, стресс, социальное давление и финансовые ограничения.
В руководстве NICE по панкреатиту отмечается, что все люди с хроническим панкреатитом подвергаются высокому риску мальабсорбции, недоедания и ухудшения качества жизни.В руководстве рекомендуется, когда это применимо, людям с хроническим панкреатитом и членам их семей или лицам, осуществляющим уход (в зависимости от обстоятельств), давать советы по питанию, включая советы о том, как принимать заместительную терапию поджелудочной железы (PERT) при экзокринной недостаточности поджелудочной железы (PEI).
В руководстве NICE также предлагается рассмотреть возможность оценки специалистом-диетологом любого, у кого диагностирован хронический панкреатит, или следования плану (протоколу) ухода, согласованному со специализированным панкреатическим центром, чтобы определить, когда необходима консультация специалиста-диетолога, включая рекомендации по питанию и добавкам. и долгосрочную заместительную терапию ферментами поджелудочной железы, и когда начинать эти вмешательства.Попросите специалиста по поджелудочной железе направить вас к диетологу, имеющему опыт лечения панкреатита и болей в поджелудочной железе. Помните, что хронический панкреатит — довольно редкое заболевание, поэтому диетолог может не иметь большого опыта лечения этого состояния.
Управление жиром в рационе
Многие продукты могут вызывать проблемы у людей с панкреатитом, но жирная пища чаще всего вызывает симптомы. Из-за этого некоторые пациенты стараются контролировать количество жиров в рационе.Медицинские работники рекомендуют избегать диет с низким содержанием жиров при хроническом панкреатите и рассмотреть возможность проведения PERT и / или дополнительных тестов. Контролировать уровень жиров в рационе сложно, потому что пациенту необходимо сбалансировать четыре основных фактора. Это:
- Употребление жиров стимулирует поджелудочную железу, поэтому диета с низким содержанием жиров может помочь справиться с симптомами, особенно с болью.
- Жир содержит калории, поэтому диета с низким содержанием жиров затрудняет поддержание калорийности и может затруднить поддержание веса, особенно если вы также изо всех сил пытаетесь съесть достаточно.
- У многих пациентов с хроническим панкреатитом также развивается мальабсорбция. Это то место, где кишечник пациента не может усвоить все съеденные питательные вещества. Некоторые витамины жирорастворимы (они могут усваиваться только в том случае, если еда содержит немного жира). Если вы придерживаетесь диеты с низким содержанием жиров, вы рискуете недоедать. Недоедание означает, что вам не хватает определенных питательных веществ, и это может быть проблемой, даже если пациент имеет «здоровый» вес.
- У пациентов может развиться экзокринная недостаточность поджелудочной железы
ncy (PEI).Именно здесь поджелудочная железа больше не вырабатывает достаточно ферментов для адекватного переваривания пищи. Лечится с помощью заместительной терапии ферментами поджелудочной железы (например, креон). Непереваренный жир в стуле вызывает стеаторею. Если у вас стеаторея, это означает, что вы не принимаете достаточное количество заместительной терапии ферментами поджелудочной железы. Обсудите это со своим врачом или диетологом.
Логический совет — есть как можно больше жира, не усугубляя симптомы. Однако это непросто решить, потому что все пациенты разные.«Опасная пища» для одного человека может быть «безопасной пищей» для другого. Другая проблема заключается в том, что пациенты могут чувствовать, что еда может быть хорошей в один день и вызвать проблемы на следующий. Единственный способ выяснить это — методом проб и ошибок и записи симптомов после еды. Ведите дневник питания и симптомов. Вы можете сделать это с помощью приложения или записной книжки. Обратитесь за помощью к диетологу.
Многие пациенты считают, что подсчет жира работает очень хорошо, потому что это означает, что они могут съесть небольшое количество еды, которая им действительно нравится (например,грамм. шоколад), не усугубляя их симптомы. Может потребоваться некоторое время, чтобы понять, сколько жира вы можете съесть за день, не делая себя более больным. Помните, что вам нужно разумно распределять жир на весь день. Если у вас 30 г жира в день и вы съедаете все 30 г жира за один прием пищи, вы можете серьезно заболеть.
Как узнать, работает ли ваш план диеты?
- Во-первых, и самое главное, ваши симптомы будут более контролируемыми.
- У вас здоровый вес, и вы не худеете.
- Вы поглощаете питательные вещества. Единственный способ проверить это — попросить вашего терапевта провести анализы крови, чтобы проверить уровни питательных веществ, особенно жирорастворимых питательных веществ.
- У вас нет стеатореи.
«Безопасные» продукты и продукты для просмотра
Важно, чтобы вы скорректировали свой рацион, чтобы справиться с симптомами недоедания. Люди с хроническим панкреатитом часто разрабатывают индивидуальные подходы к повседневному питанию и выбору продуктов питания. Они также разрабатывают стратегии преодоления обострения болезни, которые включают определение «безопасных» продуктов, которые они могут есть, когда выздоравливают после болезни.Однако иногда организм решает, что ему не нужна конкретная еда, даже «безопасная», и реагирует негативно.
Голодание во время обострения и после него может помочь кратковременно, но губительно в долгосрочной перспективе. Диетологи и медицинские работники рекомендуют как можно скорее вернуться к нормальной и сбалансированной диете, избегая пищевых ограничений. Однако ваше тело может не чувствовать себя едой в течение нескольких дней, поэтому принимайте ее медленно и доверяйте тому, что ваше тело говорит вам, что оно хочет (в пределах разумного).
Часто помогает регулярно есть четыре или пять небольших порций пищи в течение дня.Это означает, что поджелудочной железе не нужно работать так много, потому что вы распределяете пищевую нагрузку в течение дня. Старайтесь не есть поздно, чтобы ваш желудок не был полон, когда вы ложитесь спать. Сушеные продукты легче перевариваются, в то время как с некоторыми видами красного мяса могут возникнуть проблемы. Постная птица или рыба могут быть легче перевариваются. Хорошая пословица, которую стоит принять во внимание: «Если она летает или плавает, можно есть — это нормально!»
Некоторые люди обнаруживают, что в первые несколько дней после приступа поджелудочной железы они предпочитают придерживаться супов.Начните с жидких супов и постепенно увеличивайте консистенцию в течение нескольких дней, пока у вас не получатся небольшие комочки. Добавление небольшого кусочка хлеба или крекеров делает суп более сытным. Будьте осторожны со специями, пока не выясните, с чем вы можете справиться.
Если вам нужно изменить диету, начинайте медленно, чтобы все казалось менее сложным. Заменяйте продукты с высоким содержанием жиров на более безопасные, чтобы не чувствовать себя лишним. Немного проб и ошибок вы скоро узнаете, что лучше всего работает для вашего тела.Если вам нравится готовить, вам поможет приготовление с нуля из свежих ингредиентов, поскольку вы знаете, что входит в вашу пищу, и можете контролировать жиры, масла и специи.
В приведенном ниже списке содержатся предложения людей с панкреатитом в отношении «безопасных» продуктов, а также продуктов, которые они ограничивают или полностью избегают. Обратите внимание, что это их личный выбор, который может не иметь отношения к вам.
| Безопасные продукты | Продукты для наблюдения | Продукты, которых следует избегать |
Тонкие супы | Мясной фарш (содержание жира может быть слишком высоким) | Продукты с высоким содержанием жира |
Помогаем друзьям и семье разобраться в проблемах, связанных с едой и питьем
Друзьям и членам семьи иногда трудно понять и принять тот факт, что людям с панкреатитом, возможно, придется в некотором роде ограничить свой рацион.Они думают, что их друг или родственник ведет себя непросто, придирчиво или следит за своим весом. Они могут не понимать, что дело не в том, что их друг или родственник не хочет есть определенные продукты, а в том, что боль просто того не стоит.
Пациенты с панкреатитом борются с едой, потому что еда может сильно усугубить симптомы. Если кто-то страдает глютеновой болезнью, он почувствует себя намного лучше, полностью отказавшись от продуктов, содержащих глютен. К сожалению, пациентам с панкреатитом бывает сложнее справиться с ограничениями в питании.Хотя простой прием пищи может вызвать боль, пища, содержащая жир, может иметь поистине ужасные последствия. Кроме того, иногда еда может быть хорошей в один день, а на следующий день та же самая еда может вызвать у пациента ужасное самочувствие. Подумайте, каково это, когда вы выздоравливаете после неприятной болезни желудка. Идея даже положить еду в рот может вызывать отвращение. Когда вы чувствуете это, вероятно, есть только несколько продуктов, с которыми вы можете справиться.
Многим пациентам с хроническим панкреатитом необходимо подсчитывать жир (подсчитывать количество жира в еде).Это означает, что то, что они могут съесть за один прием, будет зависеть от того, что они ели раньше (например, если у них есть что-то с большим содержанием жира на завтрак, они будут есть меньше жира в остальную часть дня). Узнайте, как считать жир, и помогите в этом другу. Для этого может потребоваться довольно много работы, потому что им нужно рассчитывать количество жира во всем, что они едят.
Часто люди с панкреатитом не хотят есть, поэтому приготовление небольших блюд для них — огромная помощь. Не поддавайтесь соблазну переполнить тарелки — подойдет детская порция, они попросят еще, если она им понадобится.И, пожалуйста, не обижайтесь и не расстраивайтесь, если они не могут его съесть или допить. Если возможно, заморозьте остатки еды, чтобы их можно было съесть в другой день. Также не обижайтесь, если ваш друг или член семьи принесет свою еду. Иногда проще и безопаснее съесть то, что вы точно знаете, что в этом есть. Многим пациентам гораздо легче съесть шесть небольших приемов пищи, чем три больших приема пищи. Некоторые пациенты не едят, а вместо этого пасутся. Постарайтесь придерживаться того режима питания и графика, который лучше всего подходит вашему другу или члену семьи.И помните, что люди с хроническим панкреатитом не могут употреблять алкоголь, поэтому избегайте приготовления пищи с использованием алкоголя или предлагайте альтернативу своему другу или члену семьи.
Многие пациенты, их друзья и семьи расстраиваются из-за того, что не могут поесть в ресторанах. Есть несколько способов сделать это «безопасным»:
- Позвоните в ресторан заранее и обсудите, что можно, а что нельзя. С предварительным предупреждением, большинство ресторанов с радостью сделают для вас что-то особенное.
- Запишите подробности того, что вы можете и что нельзя есть, и передайте обслуживающему персоналу, чтобы передать шеф-повару (или предложите отправить им по электронной почте, когда вы впервые позвоните им).
- Перед тем, как съесть, точно проверьте, что содержится в пище.
Причины, методы оценки и терапевтическое лечение
Цель . В последние годы все больше внимания уделяется ранней диагностике и адекватному лечению недостаточности питания в течение хронических заболеваний (ХП). Одно из этих заболеваний — хронический панкреатит, при котором недоедание может развиться как следствие боли в животе, рвоты, диареи и злоупотребления алкоголем. Целью данной обзорной статьи является признание того, сможем ли мы улучшить состояние питания пациентов с ХП. Методы . Эта статья основана на систематическом обзоре литературы по данным PubMed. Результаты . Одна из важнейших проблем — отсутствие «золотого стандарта» в скрининге статуса питания пациентов с ХП, особенно в амбулаторных условиях. Еще одна проблема — предотвратить истощение у этих пациентов и начать лечение уже на значительных стадиях заболевания. Чтобы предотвратить недоедание, вы должны сначала распознать причины недоедания при ХП, адекватно оценить его тяжесть с помощью одного из доступных вопросников, а затем применить соответствующее терапевтическое лечение.При каждом посещении не забывайте оценивать состояние питания пациента, включая лабораторные маркеры и антропометрические измерения. Пациентам следует рекомендовать бросить курить и употреблять алкоголь и принимать адекватные ферментные добавки. Заключение . Пациенты с ХП должны находиться под руководством группы гастроэнтеролога, диабетолога и психолога и проконсультироваться у диетолога, специалиста по обезболиванию и хирурга.
1. Введение
В последние годы все больше внимания уделяется ранней диагностике и адекватному лечению недоедания в ходе хронических заболеваний.Его возникновение связано с более высокой частотой госпитализаций, повышенным риском осложнений и затратами на лечение, а также вызывает более высокую смертность [1, 2].
Хронический панкреатит (ХП) — хронический воспалительный процесс поджелудочной железы, вызванный повторяющимися воспалительными эпизодами, характеризующийся необратимыми морфологическими изменениями с замещением паренхимы поджелудочной железы волокнистой соединительной тканью. Результатом морфологических изменений является прогрессирующая экзокринная и эндокринная недостаточность поджелудочной железы.Последствиями этих явлений являются клинические симптомы: боль, неправильное питание и сахарный диабет. Недоедание часто встречается у пациентов с ХП и может развиться в результате боли в животе, рвоты, диареи и злоупотребления алкоголем [3]. Сахарный диабет может усилить это явление [4].
Одной из важнейших проблем является отсутствие «золотого стандарта» в скрининге статуса питания пациентов с ХП, особенно в амбулаторных условиях. Существует несколько шкал, используемых для скрининга пациентов в больницах: скрининг нутриционного риска (NRS-2002), инструмент скрининга недостаточности питания (MST) и краткий опросный лист для оценки нутритивного статуса (SNAQ) [5].У большинства пациентов с ХП статус питания оценивается только по массе тела и основным биохимическим показателям крови. В клинических испытаниях используется процедура CONUT, основанная на измерении альбумина, общего количества лимфоцитов и холестерина [6]. Недоедание становится большой проблемой для пациентов с ХП, что недооценивается врачами и медсестрами. Мало внимания уделяется профилактике недоедания у этих пациентов путем раннего начала лечения на значительных стадиях заболевания. Точная статистика недостаточности питания при ХП не известна, и многие врачи считают эту проблему несущественной [7].Целью данной обзорной статьи является признание того, сможем ли мы улучшить состояние питания пациентов с ХП.
2. Методы
Эта статья основана на систематическом обзоре литературы согласно PubMed.
2.1. Причины недоедания в CP
Недоедание в CP имеет несколько причин, которые могут частично совпадать. Мы можем разделить их на три основные группы в зависимости от заболевания, пациента и врача [8].
Суть болезни заключается в прогрессирующем снижении экзокринной функции поджелудочной железы, что приводит к снижению выработки ферментов поджелудочной железы и, как следствие, нарушению переваривания всех основных питательных веществ [9].
Переваривание триглицеридов особенно нарушено, что приводит к снижению всасывания жиров и жирорастворимых витаминов, таких как A, D, E и K, а также нарушение секреции протеаз может вызвать белковую недостаточность и дефицит витамина B12. В крайних случаях, если не лечить, это приводит к диарее. Одним из основных симптомов ХП является боль после еды, которая ограничивает потребление пациентом. В свою очередь, хроническое воспаление может вызвать анаболическое состояние, которое ухудшает использование белка. Диабет, который проявляется на поздних стадиях ХП, обычно нестабилен, с высокими колебаниями уровня глюкозы в крови, что приводит к нарушению аппетита [9].Причины, зависящие от пациента, — это, прежде всего, употребление стимуляторов: курение и употребление алкоголя, несмотря на диагноз заболевания. Такое действие усугубляет неполноценное питание. Влияние продолжающегося употребления алкоголя на состояние питания следует обсудить с пациентами. Кроме того, пациенты, злоупотребляющие алкоголем, не посещают регулярные осмотры, не принимают адекватных ферментных добавок и не проходят систематические лабораторные анализы. Пациенты, посещающие врача, играют важную роль в предотвращении недоедания.К сожалению, у врачей общей практики недостаточно знаний о ХП. Часто используется недостаточное количество ферментных добавок, слишком мало времени уделяется обучению пациентов (время и терпение). скрининг на недостаточность питания и диабет не проводится. Врачи не принимают адекватных добавок питательных микроэлементов и витаминов, не лечат боль должным образом и слишком поздно обращаются к хирургическому вмешательству. Также не уделяется должного внимания регулярным консультациям диетологов, а советы врачей или медсестер часто оказываются недостаточными [10].
2.2. Оценка недостаточности питания
Как я упоминал выше, не существует золотого стандарта в оценке статуса питания пациентов с ХП, особенно в амбулаторных условиях. Оценка индекса массы тела (ИМТ) недостаточна даже в сочетании с оценкой альбумина и преальбумина [11]. Однако альбумин является белком острой фазы, его пониженная концентрация также наблюдается при инфекциях, ожогах, гипергидратации, печеночной недостаточности, раке и нефротическом синдроме, поэтому он не является надежным маркером недостаточности питания.Кроме того, наблюдалось, что концентрация альбумина остается неизменной до позднего голодания (ИМТ <12 или период голодания> 6 недель) [11].
Следовательно, альбумин не может быть надежным маркером для диагностики белково-энергетической недостаточности [12]. Более надежным маркером оценки питания является преальбумин, его период полувыведения намного короче (2-3 дня), а общий запас меньше. Однако его концентрация также может снижаться при инфекциях, гипертиреозе и печеночной недостаточности и повышаться при почечной недостаточности и гипотиреозе [13].Трансферрин — еще один белок плазмы, который, как предполагается, может быть полезен при оценке недостаточности питания, но его концентрация зависит от метаболизма железа и функции почек [14]. В исследовании, проведенном с участием пациентов с разной массой тела, в том числе с истощением, корреляции между массой без жира и концентрацией трансферрина не наблюдалось [15]. Ретинол-связывающий белок (RBP) часто ниже у пациентов с ХП, чем у здоровых людей, и часто рассматривается как признак белково-калорийной недостаточности питания [16].Однако все вышеперечисленные биохимические маркеры, за исключением альбумина, обычно не определяются в клинической практике, особенно в амбулаторных условиях. В связи с недавними сообщениями, в которых подчеркивается роль воспалительного процесса в патогенезе истощения, внимание было уделено С-реактивному белку (СРБ). Хотя на его концентрацию влияют факторы, не связанные с недостаточностью питания, такие как воспалительные процессы, он помогает дифференцировать снижение концентрации общего белка из-за наличия воспаления или из-за недостаточного питания, как в случае недостаточности питания [17].
Фекальная эластаза -1 — простой инструмент для ранней диагностики экзокринной недостаточности поджелудочной железы (PEI). Других простых инструментов, подобных фекальной эластазе-1, для ранней диагностики экзокринной недостаточности поджелудочной железы (PEI) не существует. Фекальная эластаза-1 является наиболее чувствительным ранним тестом, а визуализирующие исследования — это тесты выбора для выявления хронического панкреатита. Несмотря на растущую доступность этого теста, он по-прежнему не работает в общем понимании среди врачей общей практики и не используется.Каждый пациент с впервые диагностированным ХП должен пройти скрининг на ПЭИ с фекальной эластазой-1. Это позволяет на раннем этапе принимать адекватные ферментные добавки, которые могут предотвратить недоедание [18, 19].
Оценка недостаточности питания может быть полезной при измерении антропометрических параметров, таких как индекс массы тела (ИМТ), определение трехглавой кожной складки (TSF), окружности средней части руки (MAC), определение силы захвата (HSG) и анализ биоэлектрического импеданса. На практике, кроме антропометрических измерений, другие тесты широко не используются, так как требуют использования специального оборудования, которое не является широко доступным [20].
В последнее время было опубликовано множество исследований, целью которых была оценка недостаточности питания у пациентов с ХП. Грир и др. оценили 301 пациента с ХП и 266 из контрольной группы на предмет недоедания. Обращали внимание на значительно более низкий ИМТ, чем в контрольной группе; однако до 44,5% пациентов с ХП имели избыточный вес или ожирение. Существенных различий в ИМТ у людей, страдающих ХП менее 5 лет, отмечено не было. Однако статистически значимо более низкий уровень vit.Были отмечены A и E, остеокальцин и преальбумин, ретинол-связывающий белок у пациентов с ХП, но эта разница не была показана для vit. D. В свою очередь, неожиданно статистически значимые более высокие значения вит. B12 у пациентов с ХП не наблюдалось. Авторы статьи не могут объяснить это явление, поскольку в связи с дефицитом протеазы следует ожидать более низких значений витамина B12 в сыворотке крови [9]. Исследователи подтвердили более ранние сообщения [21] о том, что уровень СРБ немного, но статистически значимо выше у пациентов с ХП, в то время как уровень TNF-альфа у большинства пациентов с ХП был ниже порога обнаружения.Важные выводы работы заключаются в том, что наличие диабета и употребления алкоголя не влияло на биомаркеры питания и воспаления, но влияло на состояние питания. В свою очередь, наблюдалось негативное влияние курения на биомаркеры питания и воспаления. Систематическое использование ферментных и витаминных добавок улучшает пищевой статус пациентов с ХП независимо от этиологии [9].
Важной проблемой, возникающей при ХП, является обострение недоедания по мере прогрессирования болезни.Hintaran et al. [22] изучали изменения в статусе питания пациентов с ХП, а также продолжительность заболевания и влияние проведения систематической оценки на статус питания голландского населения. В исследовании приняли участие 50 человек с ХП, которые были обследованы в начальной точке и через 2 года. Каждый человек заполнил анкету SF-36, которая охватывает несколько областей восприятия здоровья. Оценка питания состояла из мини-оценки питания (MNA), антропометрического измерения, определения силы захвата (HGS), анализа биоэлектрического импеданса (BIA), а также фекальных и серологических биомаркеров [22].28 пациентов прошли повторную оценку нутритивного статуса спустя прибл. 2 года. После этого периода болезни существенных различий в качестве жизни не было. Авторы подчеркивают, что при оценке статуса питания важнее оценивать состав тела, чем массу тела. Исследования обнаружили статистически значимое увеличение окружности талии, окружности бедер, площади мышц плеча, окружности мышц средней руки, жировой массы и индекса жировой массы. Оценка свободной жировой массы, которая также коррелирует со снижением мышечной силы, кажется особенно важной.Напротив, наблюдалось статистически значимое уменьшение окружности средней части руки, кожной складки трицепса, силы захвата кисти, безжировой массы и индекса безжировой массы. Кроме того, оценка силы захвата, по-видимому, полезна для оценки любой потери безжировой массы, поскольку она больше указывает на недоедание, чем на потерю веса [22].
2.3. Терапевтическое лечение
Одной из наиболее важных проблем при лечении недостаточности питания при ХП должна быть нормализация пищеварения с помощью адекватных добавок ферментов.Было показано, что он улучшает вес, снижает секрецию фекального жира, уменьшает боль в животе и улучшает качество жизни. Такое лечение не дает побочных эффектов. Минимальная доза липазы 40000–50000 Ph.U. рекомендуется с основными приемами пищи и половиной этой дозы с закусками. Наиболее эффективными являются микросферы или мини-микросферы с энтеросолюбильным покрытием размером <2 мм. Также могут быть эффективны микротаблетки или мини-таблетки размером 2,2–2,5 мм [18, 23].
Ответ на замену фермента следует оценивать не только на основании симптомов, но и на основе нормализации маркеров недостаточности питания в плазме, таких как жирорастворимые витамины, ретинол-связывающий белок, альбумин, преальбумин, минералы (железо, цинк, и магний).У пациентов с ХП не рекомендуется снижать количество диетического жира; эта процедура может привести к снижению секреции эндогенных ферментов. Если улучшения в питании нет, включите подавление соляной кислоты, исключите избыточный бактериальный рост в тонком кишечнике (SIBO), целиакию, воспалительное заболевание кишечника (IBD), непереносимость лактозы и снижение всасывания желчных кислот [23].
Одним из наиболее частых осложнений недоедания у пациентов с ХП является прогрессирующий остеопороз. Этот феномен не был хорошо изучен, поэтому было проведено многоцентровое исследование для набора пациентов из нескольких стран [24].Остеопения была обнаружена у 40% пациентов, остеопороз — у 25%, у всех этих пациентов ИМТ был ниже, чем у остальных пациентов с ХП. Риск остеопороза был выше у пожилых женщин с более низким ИМТ. У 32% пациентов был дефицит витамина К, что значительно увеличивало риск остеопороза у мужчин. Интересно, что дефицит витамина D и PEI не был связан с повышенным риском остеопатии. Важным выводом из этой работы является необходимость проведения тестов на минеральную плотность костной ткани (денситометрия), определения витаминов D и K в сыворотке крови, а в случае дефицита — одновременного их приема.Недооцененной проблемой у пациентов с ХП является саркопения. Между тем, недавние исследования подтвердили, что саркопения является независимым фактором риска осложнений, увеличения количества госпитализаций и снижения выживаемости [25]. Саркопению измеряли с помощью SMI (индекса массы скелетных мышц), HGS (силы захвата кисти) и TUG (теста с ускорением по времени) в зависимости от возраста и пола. Большинство пациентов с саркопенией имели нормальную массу тела и ИМТ или страдали ожирением. Саркопения связана с более низким качеством жизни, меньшей физической активностью, увеличением количества госпитализаций и более короткой выживаемостью.Внешнесекреторная недостаточность поджелудочной железы была независимым и значимым фактором риска саркопении [25].
Роль кишечной микробиоты в течении ХП и ее влияние на метаболические процессы, включая недостаточность питания, также является важным вопросом [26]. Пациенты с диабетом в ходе ХП имели значительно более длительную продолжительность заболевания, поэтому следует ожидать, что у них будет больше нарушений микробиоты кишечника [27].
Это наблюдение было подтверждено в публикации Саи Манаса Джандхьялы [28].Выяснилось, что больные сахарным диабетом в процессе ХП чаще страдают от недоедания. Увеличение соотношения Firmicutes : Bacteroidetes наблюдается у пациентов с сахарным диабетом и без него; наблюдается снижение количества Faecalibacterium prausnitzii (который является одним из важнейших комменсалов кишечника человека) у пациентов с ХП и отрицательная корреляция между этой бактерией и циркулирующим эндотоксином. Повышенный синтез эндотоксина был обнаружен у пациентов с ХП и ассоциированным диабетом.Уменьшение количества штамма Ruminococcus bromii у пациентов с ХП нарушает слизистый барьер и метаболизм, поскольку эта бактерия расщепляет ферментно-резистентный крахмал. Дисбактериоз зависел от продолжительности заболевания и его тяжести. Также оценивались корреляции между бактериями и выбранными клиническими параметрами. Среди прочего, была обнаружена значимая положительная корреляция численности Faecalibacterium prausnitzii с уровнями инсулина в плазме. Однако не было никакой корреляции численности Ruminococcus bromii с эндотоксином плазмы и уровнем глюкозы в крови.Исследователи наблюдали отрицательную корреляцию между Bacteroides и Escherichia с ИМТ; отрицательная корреляция Akkermansia с PEI; положительная корреляция Lactobacillus с преальбумином сыворотки; положительная корреляция Prevotella с витамином B12 в сыворотке крови; отрицательная корреляция Clostridium с сывороточным витамином B12; и положительная корреляция Shigella с уровнем эндотоксина в плазме. Изменение бактериальной микрофлоры может иметь важное значение для предотвращения или замедления развития метаболических осложнений, включая диабет, и, таким образом, предотвращения недоедания [28].В самой последней статье Zhou et al. исследовали микробиоту кишечника у пациентов с ХП по сравнению со здоровым контролем. Они наблюдали дисбактериоз кишечной микробиоты с уменьшенным разнообразием и богатством, а также изменениями в составе таксонов. Микробиом кишечника группы CP показал более низкую численность Firmicutes и Actinobacteria , чем контрольную группу, и более высокую численность Proteobacteria . Численность Escherichia, Shigella, и других родов была высокой в группе ЦП, тогда как численность Faecalibacterium была низкой.Авторы подтвердили, что пациенты с ХП имеют дисбактериоз кишечной микробиоты, на который может частично влиять экзокринная функция поджелудочной железы [29].
Важным вопросом, связанным с дисбактериозом, является взаимосвязь между избыточным бактериальным ростом в тонком кишечнике (SIBO) и PEI при хроническом панкреатите. Capurso et al. проанализировали данные из девяти публикаций, и на этом основании они пришли к выводу, что одна треть пациентов с ХП имеет СИБР с диапазоном от 14 до 92% и значительной неоднородностью. Распространенность СИБР, по-видимому, зависит от типа теста, используемого для диагностики, а также от критериев включения пациентов с ХП, с более высокими показателями положительности в исследованиях, включающих пациентов, которые ранее перенесли хирургическое вмешательство.Взаимосвязь между наличием и тяжестью симптомов и диагнозом СИБР у пациентов с ХП, по-видимому, различалась в разных исследованиях. О более высоком уровне симптомов у пациентов с СИБР сообщалось только в трех из пяти исследований. Лечение СИБР антибиотиками у пациентов с ХП может привести к уменьшению симптомов [30].
Некоторые пациенты с ХП, несмотря на соблюдение рекомендаций (отказ от курения и употребления алкоголя), прием адекватных ферментных добавок и антиболевое лечение, все еще имеют жалобы и недостаточное питание.В этом случае пациента следует немедленно направить на консультацию к хирургу для рассмотрения возможности хирургического лечения. Такое разбирательство не следует откладывать до тех пор, пока у пациента не будет наблюдаться кахексия, и тогда риск выполнения процедуры очень велик. Хирургическое лечение при ХП состоит из двух стратегий: дренирования протока поджелудочной железы и резекции целевого очага (панкреатэктомия). Первая концепция включает панкреатоеюностомию с дистальной панкреатэктомией, процедуру Пуэстоу [31] и продольную панкреатоеюностомию (процедура Партингтона) [32].Вторая концепция включает дистальную резекцию поджелудочной железы (DP), панкреатодуоденэктомию (PD) и резекцию головки поджелудочной железы с сохранением двенадцатиперстной кишки (процедура Бегера) [33]. Методика, состоящая из дренирования и резекции, называется процедурой Фрея [34]. Сато Х. недавно опубликовал статью, в которой оценивает полезность процедуры Фрея не только для уменьшения боли, но и для улучшения нутритивного статуса по сравнению с панкреатодуоденэктомией. Статус питания оценивался с использованием протокола CONUT (альбумин, общее количество лимфоцитов и холестерин).Это исследование показало, что послеоперационный нутритивный статус пациентов с ХП значительно улучшился после процедуры Фрея, тогда как после ПД изменений в питании не наблюдалось. Авторы предлагают три основных механизма, участвующих в улучшении нутритивного статуса: облегчение боли, позволяющее возобновить пероральный прием; уменьшение хронического воспаления и устранение обструкции протоков поджелудочной железы и, как следствие, улучшение внешнесекреторной функции поджелудочной железы; Процедура Фрея также сохраняет паренхиму поджелудочной железы и поддерживает потенциальный источник панкреатического сока и инсулина.Как правило, операцию не следует откладывать до тех пор, пока пациент не станет тяжелой кахектикой, а тип операции должен зависеть от локализации воспалительных поражений, анатомических условий и опыта центра [32]. В литературе нет данных о влиянии эндоскопического лечения на улучшение питания пациентов с хроническим панкреатитом.
3. Основные рекомендации
В 2018 г. были опубликованы рекомендации Объединенного европейского руководства по гастроэнтерологии по диагностике и лечению хронического панкреатита, некоторые из которых касаются профилактики, диагностики и лечения недостаточности питания.Рекомендуемый инструмент для скрининга — ОБЯЗАТЕЛЬНО (универсальные инструменты скрининга на недостаточность питания) или NRS, оказались полезными антропометрические измерения (ИМТ, окружность руки, кожная складка под трицепсом) и сила мышц кисти. Также рекомендуется оценить дефицит альбумина, жирорастворимых витаминов (K и D) и микроэлементов. Добавки Fe, Zn и Mg следует использовать только в случае дефицита. Самыми важными в лечении были адекватное ферментативное замещение и частое, малокалорийное питание без ограничения количества жиров в рационе.Также следует избегать продуктов с высоким содержанием клетчатки. Если вам трудно соблюдать правильную диету, проконсультируйтесь с диетологом. В свою очередь, энтеральное питание показано пациентам, которые не реагируют на пероральное питание, с задержкой опорожнения кишечника, с болью и тошнотой и / или рвотой. Парентеральное питание рекомендуется только пациентам с желудочно-кишечной непроходимостью, свищами или глубоким недоеданием перед плановым хирургическим вмешательством [18].
4. Резюме
Пациенты с ХП должны находиться под руководством группы гастроэнтеролога, диабетолога и психолога и проконсультироваться у диетолога, специалиста по обезболиванию и хирурга.При каждом посещении не забывайте оценивать состояние питания пациента, включая лабораторные маркеры и антропометрические измерения. Пациентам следует рекомендовать бросить курить и употреблять алкоголь и принимать адекватные ферментные добавки. Необходимо лечить боль и диабет и реагировать на ухудшение питания пациента: рассмотреть возможность энтерального или парентерального питания и даже хирургического вмешательства. Благодаря этой процедуре мы можем улучшить состояние питания пациентов с хроническим панкреатитом.
Доступность данных
Все данные, содержащиеся в рукописи, доступны в базе данных PubMed. В этой широко используемой базе данных читатель может найти все процитированные статьи.
Конфликт интересов
Автор заявляет об отсутствии конфликта интересов.
Сроки возобновления перорального кормления после острого панкреатита
Абстракция
Первоначальное лечение острого панкреатита в основном является поддерживающим и состоит из режима «ничего не перорально» вместе с внутривенной инфузией и обезболиванием.Несмотря на то, что дефицит питания является обычным явлением при остром панкреатите, длительное время считалось, что нутритивная терапия — перорально или через зонд — оказывает негативное влияние на прогрессирование заболевания. Было опубликовано несколько исследований для определения оптимального времени, режима и типа перорального питания при остром панкреатите. Они показывают, что раннее возобновление питания с твердой диеты безопасно и может сократить продолжительность пребывания в больнице. Не было обнаружено повышенного риска непереносимости возобновления питания, рецидива заболевания или других побочных эффектов, связанных с более активным протоколом возобновления питания.При легком и тяжелом остром панкреатите в Руководстве ESPEN рекомендуется активно пытаться оральное кормление после того, как будет устранена обструкция выходного отверстия желудка и будут приняты меры по контролю осложнений. В зависимости от клинического курса питание может быть изменено на легкую полноценную диету, и нет особой необходимости в поэтапном переходе к нормальной полноценной диете, согласно Немецкому обществу диетологии в сотрудничестве со швейцарским, австрийским и немецким обществами в их S3- Директива.
1.Введение
Начало острого панкреатита связано с ранней активацией пищеварительных ферментов, за которой следует системный воспалительный ответ, опосредованный цитокинами. Лечение зависит от степени тяжести (9).
Несмотря на то, что дефицит питательных веществ является обычным явлением при остром панкреатите, длительное время считалось, что нутритивная терапия — перорально или через зонд — оказывает негативное влияние на исход болезни из-за предполагаемой стимуляции экзокринной секреции поджелудочной железы и последующего ухудшения ауто-пищеварения. процессы в поджелудочной железе (17).Целью голодания как традиционной терапии острого панкреатита было «успокоить поджелудочную железу». Во многом это мнение основано на физиологических исследованиях и не подтверждено данными проспективных клинических испытаний.
Мета-анализ клинических исследований показал, что при остром панкреатите энтеральное питание превосходит парентеральное питание с точки зрения сопутствующих осложнений и стоимости. Для энтерального питания есть преимущества с точки зрения снижения риска инфекционных осложнений и смертности (5, 15, 16, 22, 24).Мета-анализ показывает, что при остром панкреатите, когда энтеральное питание было начато в течение 24 часов после госпитализации, наблюдались значительно более низкие показатели смертности по сравнению с введением между 24 и 72 часами (14), что несколько оспаривается недавно завершившимся голландским исследованием, которое не обнаружило преимущество начала возобновления кормления особенно рано (2).
При остром панкреатите легкой степени традиционное лечение по-прежнему включает голодание в течение 2 или 3 дней. С этого момента оральное питание постепенно увеличивается от прозрачных жидкостей до мягких, и выписка из больницы планируется на основе толерантности пациентов к твердой пище (25).Исследования по оптимальному времени и диете для возобновления перорального кормления при остром панкреатите все еще редки.
2. Когда начинать пероральное повторное кормление
Пациенты с острым панкреатитом легкой степени обычно не имеют повышенных потребностей в питательных веществах или энергии (17). Этим пациентам энтеральное питание не требуется, если пациент может принимать обычную пищу орально через 5-7 дней. Энтеральное питание в течение 5-7 дней не оказывает положительного влияния на течение заболевания и поэтому не рекомендуется (17).
При остром панкреатите легкой и тяжелой степени в Руководстве ESPEN по энтеральному питанию рекомендуется активно пытаться оральное кормление (обычная пища и / или пищевые добавки) после устранения обструкции выходного отверстия желудка, учитывая, что это не вызывает боли и осложнения отсутствуют. контроль. Таким образом, можно постепенно сокращать зондовое питание по мере улучшения приема внутрь (17).
В клинических исследованиях изучались различные подходы к выбору времени обычного перорального приема пищи после острого панкреатита.В проспективном исследовании Lévy et al. показали, что пациенты могут питаться перорально после короткого периода голодания, если боль прекратилась и уровни амилазы и липазы снижаются (13). Рецидив боли после перорального возобновления питания произошел у 21% пациентов в первый и второй день возобновления питания (4). Факторами риска были определены трехкратное превышение липазы, превышающей верхний предел нормы, и более высокий балл по шкале КТ Бальхазара в начале возобновления питания. рецидив боли (13, 23).
Teich et al. исследовали оптимальное время возобновления питания через рот при легком остром панкреатите (25).Они сравнили группу, выбранную самостоятельно, в которой пациентам разрешили возобновить прием пищи по своему выбору, и группу, в которой пациентам не разрешали есть, пока липаза не упадет ниже значения, в 2 раза превышающего верхний предел контрольного диапазона. . Они показали, что группа, выбранная самостоятельно, не превосходит группу с липазой, но также не создает дополнительного риска по сравнению с традиционным голоданием. Они также показали тенденцию к более короткому пребыванию в больнице в самостоятельно выбранной группе возобновления питания и отсутствию обострения боли или более высокой частоте рецидивов (25).
В исследовании Ли аналогичным образом были проанализированы две группы острого панкреатита легкой степени (14). Один начал есть, как только почувствовал голод, а другой начал есть, когда они соответствовали следующим критериям: 1) отсутствие боли в животе; 2) снижение уровня амилазы и липазы в сыворотке менее чем в 2 раза по сравнению с верхним пределом референсного диапазона; 3) нормальные кишечные шумы; 4) субъективное чувство голода. Между этими группами не было различий в рецидивах абдоминальной боли, переходном вздутии живота, активности амилазы или липазы в сыворотке крови, превышающей верхний предел нормы, или гипергликемии после перорального возобновления питания (14).Это исследование доказывает, что лучшее время для возобновления перорального кормления — это когда пациент чувствует голод, и этот подход безопасен и сокращает продолжительность пребывания в больнице. Нет необходимости откладывать возобновление питания через рот до тех пор, пока боль в животе не исчезнет или пока уровень ферментов поджелудочной железы не нормализуется.
Тот же вопрос исследовали у пациентов с умеренным и тяжелым острым панкреатитом. Умеренный или тяжелый острый панкреатит часто вызывает осложнения и приводит к высококатаболическому, гиперметаболическому и гипердинамическому стрессу с более высокой заболеваемостью и смертностью.Оптимальная нутритивная поддержка стала ключевым элементом в лечении этих пациентов. Данные о возобновлении перорального кормления при умеренном или тяжелом панкреатите в основном отсутствуют. Исследование Li et al. показали эквивалентные результаты при возобновлении питания на основании голода при панкреатите средней и тяжелой степени (14). Чжао и др. Показали, что возобновление питания на основании чувства голода пациента безопасно. Хотя это увеличивает риск гипергликемии, который можно свести к минимуму с помощью строгого протокола контроля уровня глюкозы, не было различий между двумя группами с точки зрения боли в животе, рецидива вздутия живота, органной недостаточности или возникновения местных или системных осложнений перед выпиской. из больницы (27).
Eckerwall et al. в клиническом рандомизированном исследовании продемонстрировали эффективность и осуществимость немедленного перорального кормления ad libitum по сравнению с традиционным голоданием и поэтапным повторным введением перорального приема у пациентов с легким острым панкреатитом (6). Они показали, что пациенты с немедленным пероральным кормлением раньше начинали с твердой пищи и нуждались в меньшем количестве дней внутривенного введения жидкости. Признаков обострения болезненного процесса, усиления болей в животе и ряда желудочно-кишечных симптомов в результате немедленного перорального кормления не было.Они также показали связь со значительным сокращением продолжительности пребывания в больнице с 6 до 4 дней по сравнению с группой, принимавшей голодание (6).
Lariño-Noia et al. Аналогичным образом было обнаружено, что раннее возобновление питания, как только появятся звуки кишечника, сокращает продолжительность пребывания в больнице на два дня по сравнению со стандартным протоколом возобновления питания (12).
3. Тип рецептуры перорального питания
В типичном протоколе перорального возобновления питания диета восстанавливается постепенно, начиная с небольшого количества прозрачных жидкостей в течение первых 24 часов.При переносимости диету постепенно меняют на мягкий режим с низким содержанием жиров, а затем следует твердую диету. В таком случае выписка из больницы зависит от переносимости твердой диеты с низким содержанием жиров (26).
Исследование Jacobson et al. исследовали начало перорального питания в течение 3 дней после госпитализации с прозрачной жидкой диеты (588 ккал, 2 г жира) или твердой диеты с низким содержанием жиров (1200 ккал, 35 г жира) у пациентов после легкого острого панкреатита. Они не обнаружили значительной разницы в доле пациентов, не переносящих пероральное возобновление питания, что позволяет предположить, что оба метода безопасны (10).
Стандартное возобновление питания с постепенным увеличением потребления калорий не требуется, как показано Lariño-Noia et al. (12). Было продемонстрировано, что раннее возобновление питания с использованием диеты с низким содержанием жиров 1800 ккал с первого дня, как только появились кишечные шумы, хорошо переносятся и безопасно. Жалобы со стороны желудочно-кишечного тракта были зарегистрированы без существенных отличий от группы стандартного возобновления питания (12). Аналогичные результаты были обнаружены между гипокалорийной чистой жидкой диетой, средней гипокалорийной мягкой диетой и полноценной твердой диетой у пациентов с легким острым панкреатитом.Не было различий в частоте рецидивов боли или продолжительности пребывания в больнице (18, 20).
Таким образом, Немецкое общество диетологии в сотрудничестве с Обществом клинического питания Швейцарии, Австрийским консорциумом клинического питания и Немецким обществом гастроэнтерологов рекомендуют в своих рекомендациях S3, что в зависимости от клинического курса питание может быть изменено на более легкое. полноценное питание (21). Нет особой необходимости в постепенном переходе к нормальному полноценному питанию.Признаки клинически значимой мальабсорбции во время тяжелого острого панкреатита могут привести к замещению ферментов поджелудочной железы (21). Рекомендуется пероральное возобновление питания с диетой, богатой углеводами и белками и с низким содержанием жиров (<30% от общего количества потребляемой энергии), но никакие клинические испытания не показали, что она превосходит другие составы пищи. Если диета хорошо переносится, оральное питание можно постоянно увеличивать, и в специальных продуктах нет необходимости (17).
4. Добавление ферментов при раннем пероральном кормлении
Внешнесекреторная недостаточность поджелудочной железы — актуальная проблема после острого панкреатита.Выраженность внешнесекреторной недостаточности напрямую связана с тяжестью заболевания (3, 7, 8, 19). Даже у пациентов с легким острым панкреатитом внешнесекреторная функция нарушена на раннем этапе после острого приступа, но у большинства пациентов восстанавливается (7). У некоторых из этих пациентов во время перорального возобновления питания наблюдаются абдоминальные симптомы (например, метеоризм, диарея и боль). Это может быть связано с внешнесекреторной недостаточностью поджелудочной железы в момент начала возобновления кормления (11). Эффект раннего приема ферментов поджелудочной железы в период возобновления питания после острого панкреатита был оценен Kahl et al (11).Они показали тенденцию к более быстрому выздоровлению от внешнесекреторной недостаточности поджелудочной железы при добавлении ферментов по сравнению с плацебо (14 дней против 23; p = 0,641) и никаких существенных различий в отношении безопасности и переносимости. Airey et al. также показали значительное улучшение внешнесекреторной функции поджелудочной железы после пяти дней возобновления кормления с добавлением ферментов поджелудочной железы (1).
5. Заключение
Было проведено небольшое количество исследований для определения оптимального времени, режима и типа перорального питания при остром панкреатите.Они показывают, что нормализация уровня ферментов поджелудочной железы не является предварительным условием для возобновления перорального кормления. Наиболее подходящим вариантом может быть предоставление пациенту возможности выбора, когда возобновить пероральное возобновление питания независимо от уровня ферментов в сыворотке. Кроме того, раннее возобновление питания может сократить продолжительность пребывания в больнице. До сих пор нет единого мнения относительно определения «раннего возобновления питания».
Пероральный прием, обычно начинающийся с прозрачных жидкостей, с последующим приемом твердой пищи с низким содержанием жира с повышением калорийности в течение 3-6 дней, похоже, не имеет преимуществ перед началом приема обычных легких блюд.Таким образом, раннее пероральное возобновление питания с твердой диеты может обеспечить лучшие результаты и безопасно для пациентов с острым панкреатитом легкой и средней степени тяжести. Тем не менее, лучшее рандомизированное исследование не смогло продемонстрировать преимущества раннего возобновления питания по сравнению с возобновлением питания пациентов по требованию (2), когда пациенты чувствуют себя готовыми принимать обычную пищу через рот. Ни в одном из ранее опубликованных исследований не наблюдалось повышенного риска непереносимости возобновления питания или других побочных эффектов, связанных с более активным протоколом возобновления питания.

 Мы располагаем необходимым оборудованием экспертного уровня, что позволяет быстро поставить диагноз и назначить адекватную терапию в любых ситуациях (в том числе при возникших осложнениях)
Мы располагаем необходимым оборудованием экспертного уровня, что позволяет быстро поставить диагноз и назначить адекватную терапию в любых ситуациях (в том числе при возникших осложнениях)

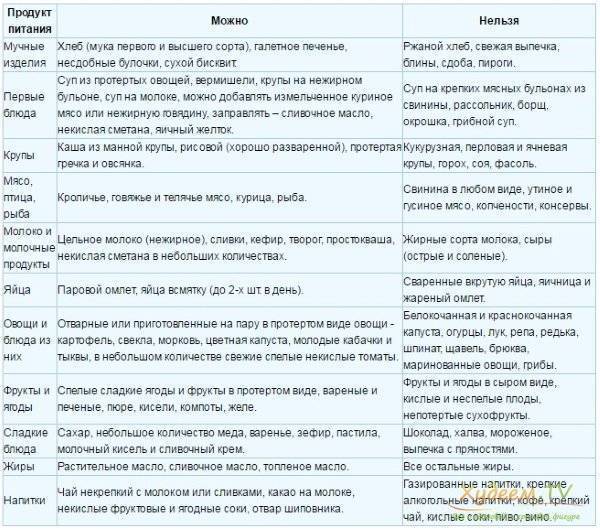 )
)