Лечение панкреатита у детей в Москве
Панкреатит – воспаление поджелудочной железы, к которому приводит повышение активности ферментов. В норме они активируются после поступления в кишечник и обеспечивают функцию переваривания пищи. При задержке секрета ферменты начинают работать еще до выхода из поджелудочной железы, что приводит к воспалению тканей, протоков, сосудов. Лечение панкреатита у детей должно быть своевременным, это крайне важно для профилактики серьезных осложнений.
Почему возникает панкреатит
Хроническая форма воспаления является следствием острого процесса. Впервые панкреатит может проявиться в силу разных причин:
-
механических: травмы, диагностические вмешательства, перенесенные операции;
-
токсико-аллергических: пищевые аллергии, инфекционные заболевания, интоксикации и отравления;
-
врожденных: анатомические особенности – дефекты строения протоков железы, желчного пузыря, двенадцатиперстной кишки.

Нередко панкреатит у ребенка возникает на фоне других заболеваний желудочно-кишечного тракта: воспаления желчного пузыря и прочие нарушения функции ЖКТ после перенесенного вирусного и простудного заболевания.
Симптомы панкреатита у ребенка
Воспаление органа приводит к поступлению ферментов и токсинов в кровь и лимфу, поэтому могут возникать симптомы общей интоксикации детского организма. Несмотря на это болезнь часто протекает в стертой, легкой форме. Даже острое воспаление у маленького ребенка может не вызывать сильных болей, обычно не сопряжено с тяжелой симптоматикой.
У детей старшего возраста возникают приступообразные боли в верхней части живота. Они носят опоясывающий, ноющий характер, могут отдавать в правое подреберье, лопатку, спину. Частым спутником панкреатита является комплекс диспепсических нарушений:
-
снижение аппетита;
-
тошнота;
-
нарушения стула;
-
рвота;
-
вздутие живота и повышенное газообразование.

К другим, менее распространенным симптомам, относят повышение температуры тела (незначительное), бледность кожи или чуть заметную желтушность, редко цианоз и мраморность кожных покровов лица, рук, ног. Могут наблюдаться сухость слизистой полости рта, белесоватый налет на языке.
В целом симптоматика зависит от того, на какой стадии заболевание, как давно оно наблюдается, насколько угнетена функция поджелудочной железы. Лечение панкреатита у ребенка 7–8 лет нередко начинается с посещения врача по поводу периодических ноющих болей в животе, обостряющихся после употребления сладкой пищи, физической нагрузки, стресса.
Приступ боли может длиться от 50–60 минут до нескольких дней. Многие дети отмечают появление изжоги, чередование запоров и диареи. По результатам плановых медицинских осмотров и наблюдениям родителей у многих маленьких пациентов с панкреатитом имеет место потеря веса, астеновегетативный синдром.
Методы диагностики
Врач диагностирует панкреатит на основании жалоб и выявленных симптомов, результатов лабораторных и аппаратных исследований. Обычно прибегают к УЗИ органов брюшной полости, клиническому и биохимическому анализу крови. Иногда требуется компьютерная томография или МРТ внутренних органов, если есть основания подозревать осложнения или другие патологии поджелудочной железы.
Особенности лечения
Лечение панкреатита у детей направлено на следующие результаты:
-
снятие неприятных симптомов;
-
устранение причин болезни;
-
нормализация функции поджелудочной железы.
Первой задачей является обеспечение функционального покоя органа. Важно быстро купировать неприятные симптомы, а также не допустить действия первопричин. При обострении прописывается лечебное голодание в течение суток, но оно должно проходить под контролем врача.
Дальнейшее медикаментозное лечение основывается на следующих лекарствах:
-
анальгетики и спазмолитики для снятия боли;
-
антисекреторные препараты;
-
ферментные препараты;
-
ингибиторы протеазы при тяжелом течении заболевания.
Важно соблюдать лечебную диету в течение всего курса лечения и некоторое время после. Под запретом – жирная, жареная, тяжелая пища, острые продукты и соусы, газировка. Специалист составит диету с учетом возрастных потребностей, общего состояния здоровья ребенка.
Профилактика панкреатита должна основываться на рациональном питании в соответствии с возрастом ребенка, предупреждении и своевременном лечении заболеваний пищеварительной системы.
Для записи к детскому врачу-гастроэнтерологу на удобное для Вас время, позвоните по телефону единого контакт-центра в Москве +7 (495) 775 75 66, заполните форму онлайн-записи или обратитесь в регистратуру клиники.
Стоимость
врач-педиатр, гастроэнтеролог, ведущий специалист клиники
врач-педиатр, гастроэнтеролог, к.м.н.
Панкреатит у детей — Into-Sana
 Это заболевание является опасным, поскольку в ряде случаев может привести к летальному исходу.
Это заболевание является опасным, поскольку в ряде случаев может привести к летальному исходу.Причины возникновения панкреатита
Причина возникновения панкреатита связана с перевариванием клеток поджелудочной железы собственными пищеварительными ферментами. Протеолитические ферменты, липаза, амилаза и эластаза способны разрушать ткани, сосуды и выводные протоки железы, что влечет за собой выраженный воспалительный процесс и выброс в кровь и лимфу токсических продуктов распада.
Детский организм острее, чем взрослый, реагирует на воспалительные и аллергические процессы. Поэтому факторов, провоцирующих воспаление поджелудочной железы, довольно много. Среди них:
- злоупотребление фастфудом и другими продуктами, провоцирующими интенсивную выработку панкреатических ферментов;
- инфекции;
- травмы живота, ушибы;
- другие заболевания пищеварительной системы;
- прием некоторых медикаментов;
- наличие в организме гельминтов;
- наследственность.

Виды панкреатита
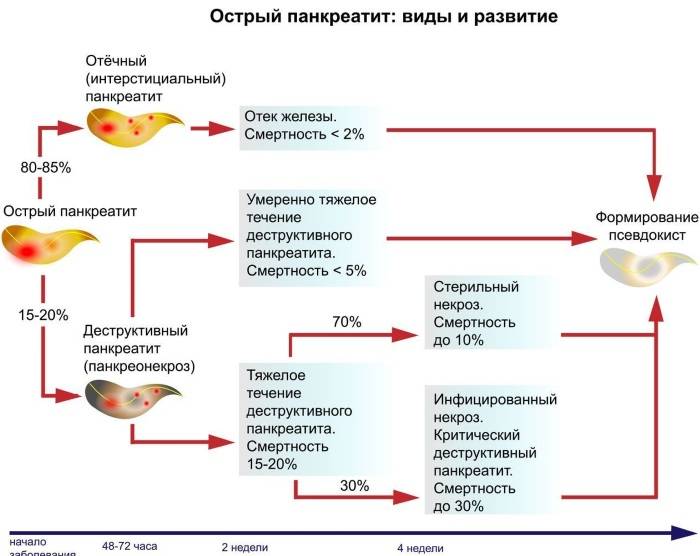
По характеру болезни различают острую и хроническую форму панкреатита. Острый панкреатит в детском возрасте встречается довольно редко и характеризуется воспалением и отеком панкреаса (поджелудочной железы). Хронический панкреатит обычно развивается на фоне других патологий: фиброза, склероза, атрофии поджелудочной железы, муковисцидоза. При этой форме заболевания у детей возникают диспепсические явления, повышенное газообразование, нарушение стула, потеря веса.
Реактивный панкреатит, как правило, бывает следствием пищевого отравления, воспалительных процессов в желудочно-кишечном тракте, острой вирусной инфекции. При должном лечении основного заболевания он проходит бесследно, однако при отсутствии терапии может трансформироваться в «истинный» панкреатит с последующим разрушением поджелудочной железы.
Деструктивный панкреатит (панкреонекроз) – наиболее тяжелая форма заболевания. По статистике, четверть случаев панкреонекроза имеют летальный исход. При этой патологии происходит стремительное отмирание ткани поджелудочной железы вследствие преждевременной активации собственных ферментов в выводящих протоках. У взрослых причиной этого заболевания чаще всего выступает чрезмерное употребление алкоголя, у детей – патология желчевыводящих путей. Данная болезнь характеризуется так называемой триадой Мондора – метеоризмом, обильной рвотой и болью в животе.
По статистике, четверть случаев панкреонекроза имеют летальный исход. При этой патологии происходит стремительное отмирание ткани поджелудочной железы вследствие преждевременной активации собственных ферментов в выводящих протоках. У взрослых причиной этого заболевания чаще всего выступает чрезмерное употребление алкоголя, у детей – патология желчевыводящих путей. Данная болезнь характеризуется так называемой триадой Мондора – метеоризмом, обильной рвотой и болью в животе.
Симптомы панкреатита
Симптомы панкреатита у детей различаются в зависимости от возраста. Однако существует ряд характерных признаков, при появлении которых нужно проявить бдительность и в обязательном порядке показать ребенка доктору:
- Острая боль в животе, при которой ребенку трудно находиться в вертикальном положении. Боль может носить постоянный или спастический характер, иметь разную локализацию (в зависимости от воспалительно-дистрофического поражения головки, тела или хвоста поджелудочной железы), обычно усиливается после приема пищи, эмоционального перенапряжения.

- Вздутие живота.
- Тошнота, рвота, не приносящая облегчения.
- Ухудшение аппетита.
- Нарушение стула.
- Повышение температуры тела.
- Учащение сердцебиения.
Поскольку симптомы панкреатита неспецифичны, т. е. свойственны не только ему, а и другим заболеваниям ЖКТ, для подтверждения или опровержения диагноза в обязательном порядке нужно обратиться к врачу.
Диагностика панкреатита
Диагностика панкреатита у детей бывает затруднена, поскольку клинические признаки болезни при хронических формах обычно неспецифичны (боль, тошнота, рвота, метеоризм). Для точной постановки диагноза педиатр или детский гастроэнтеролог после осмотра и сбора анамнеза может назначить такие лабораторные исследования:
- Общий анализ крови. Позволяет выявить наличие воспалительного процесса в организме и узнать уровень лейкоцитов.
- Биохимический анализ крови. Дает возможность обнаружить в крови повышенный уровень панкреатических ферментов: амилазы, липазы, трипсина, эластазы, а также глюкозы крови.

- Анализ на амилазу в моче.
- Копрограмма. Позволяет рассмотреть непереваренные частички пищи, свидетельствующие о недостаточной выработке энзимов поджелудочной железой.
- УЗИ органов брюшной полости. Дает возможность достоверно визуализировать размеры, структуру, контуры, форму поджелудочной железы, печени и желчевыводящих путей, увидеть нарушения в их работе, диагностировать особенности кровообращения органов.
- Гастроскопия. Требуется для уточнения или исключения сопутствующего воспаления желудка и двенадцатиперстной кишки в результате ретроградного заброса панкреатического сока в эти органы пищеварения.
- Обзорная рентгенография. Позволяет увидеть внутрипротоковые камни, кальциноз поджелудочной железы.
- КТ или МРТ. Помогают диагностировать аномалии в развитии органа, кисты, новообразования, очаги деструкции панкреаса.

- При хроническом панкреатите обязательно назначают анализ кала на фекальную эластазу, чтобы оценить внешнюю секреторную активность поджелудочной железы.
Также, проводя диагностику, врач назначит дообследование, если подозревает системное заболевание соединительной ткани, муковисцидоз, целиакию.
Методы лечения панкреатита
Лечение ребенка, больного панкреатитом, осуществляется в условиях стационара. В настоящее время “голодная” диета не приветствуется гастроэнтерологами. Назначается лечебное питание с первого дня.
Медикаментозное лечение обычно включает в себя применение обезболивающих препаратов, антисекреторных и спазмолитических средств, а также препаратов ферментов панкреаса. По строгим показаниям вводятся антибиотики, антигистаминные препараты, кортикостероиды и средства, улучшающие микроциркуляцию. В редких случаях, при прогрессировании панкреонекроза или неэффективности медикаментозной терапии, применяется хирургическое лечение.
Последствия панкреатита
Как правило, если лечение было начато вовремя, панкреатит у детей полностью излечивается. Осложнениями панкреатита могут выступать перитонит, плеврит, ложная киста, сахарный диабет.
Заболевания поджелудочной железы у детей: панкреатит или панкреатопатия?
Авторы: Ю. В. Белоусов, д. м. н., профессор, заведующий кафедрой детской гастроэнтерологии ХМАПО
Своевременная диагностика и терапия заболеваний поджелудочной железы у детей являются одной из наиболее сложных проблем клинической гастроэнтерологии. Практика показывает, что, с одной стороны, отмечается определенная тенденция к нарастанию частоты этих заболеваний, с другой, распознавание их представляет значительные трудности и вне специализированных учреждений нередко сопровождается диагностическими ошибками.
Это касается и выявления патологии pancreas как основного заболевания, и дифференциальной диагностики воспалительных (панкреатит) и функциональных ее изменений (панкреатопатия). Необходимо также учитывать возможность аномалий и пороков развития поджелудочной железы, среди которых чаще встречается врожденная гипоплазия поджелудочной железы (синдром Швахмана). Достаточно сложен также вопрос адекватной терапии болезней поджелудочной железы, которая должна быть дифференцирована в зависимости от наличия или отсутствия воспалительных изменений, периода заболевания и характера нарушения внешнесекреторной функции pancreas.
Ключевое заболевание поджелудочной железы у детей хронический панкреатит, который протекает в детском возрасте достаточно тяжело и требует дифференцированной поэтапной терапии в стационарных условиях. По современным представлениям, хронический панкреатит это прогрессирующее воспалительное заболевание, характеризующееся очаговыми или диффузными деструктивными и дегенеративными изменениями ацинарной ткани и протоковой системы с развитием различной функциональной недостаточности органа. Морфологические изменения ткани поджелудочной железы носят стойкий характер, сохраняются и прогрессируют даже после прекращения воздействия этиологических факторов и приводят к экзокринной и эндокринной недостаточности. Морфологическим субстратом хронического панкреатита являются отек, воспаление и очаговые некрозы поджелудочной железы, нарушающие отток панкреатического сока, способствующие внутрипротоковой гипертонии, прогрессированию некроза ацинарной ткани с последующими атрофией ацинусов, интралобулярным и перилобулярным фиброзом органа. В начальной стадии патологический процесс может носить ограниченный характер и локализоваться в каком-либо одном отделе поджелудочной железы, по мере развития заболевания диффузно поражается вся железа.
Морфологические изменения ткани поджелудочной железы носят стойкий характер, сохраняются и прогрессируют даже после прекращения воздействия этиологических факторов и приводят к экзокринной и эндокринной недостаточности. Морфологическим субстратом хронического панкреатита являются отек, воспаление и очаговые некрозы поджелудочной железы, нарушающие отток панкреатического сока, способствующие внутрипротоковой гипертонии, прогрессированию некроза ацинарной ткани с последующими атрофией ацинусов, интралобулярным и перилобулярным фиброзом органа. В начальной стадии патологический процесс может носить ограниченный характер и локализоваться в каком-либо одном отделе поджелудочной железы, по мере развития заболевания диффузно поражается вся железа.
Этиологические факторы хронического панкреатита
Хронический панкреатит у детей чаще вторичен и развивается на фоне заболеваний органов пищеварения, прежде всего двенадцатиперстной кишки и желчевыводящих путей. Значительно реже встречается первичный хронический панкреатит, но именно эта форма протекает наиболее тяжело и имеет выраженную клиническую симптоматику.
Этиологические факторы хронического панкреатита многочисленны, обычно на организм ребенка действует не один, а комплекс факторов, обусловливающих развитие заболевания на фоне измененной реактивности организма. Наиболее частые причины развития панкреатита у взрослых алкогольное и токсическое воздействия, у детей эксквизитны. Значительно большее влияние в детском возрасте имеет травматическое повреждение поджелудочной железы с сотрясением органа, разрушением определенного количества ацинусов и высвобождением биологически активных веществ. Причиной повышения давления в протоках поджелудочной железы может стать их аномалия или обтурация камнем, что приводит к нарушению пассажа панкреатического сока с развитием воспалительных изменений и гиперферментемии. Прямое повреждающее действие на ткань поджелудочной железы оказывают инфекционные агенты, в частности велика роль вируса эпидемического паротита; нельзя исключить и участие иерсиний, влияние других бактериальных инфекций. Важное значение в развитии хронического панкреатита имеет активация ферментов панкреатического сока вследствие регургитации в протоки содержимого двенадцатиперстной кишки, в том числе желчи. К развитию заболевания может привести длительный прием лекарственных средств, прежде всего антибиотиков тетрациклинового ряда, сульфаниламидов, диуретиков, сульфасалазина, 6-меркаптопурина. Возможно возникновение наследственного панкреатита с аутосомно-доминантным типом наследования с неполной пенетрантностью патологического гена. Эта патология проявляется обычно у детей в возрасте 10-12 лет. Наконец, заболевание может носить аутоиммунный характер с образованием аутоантител к ткани поврежденного органа. Несмотря на многообразие этиологических факторов, у 10-40% больных установить причину хронического панкреатита не удается (идиопатическая форма заболевания).
К развитию заболевания может привести длительный прием лекарственных средств, прежде всего антибиотиков тетрациклинового ряда, сульфаниламидов, диуретиков, сульфасалазина, 6-меркаптопурина. Возможно возникновение наследственного панкреатита с аутосомно-доминантным типом наследования с неполной пенетрантностью патологического гена. Эта патология проявляется обычно у детей в возрасте 10-12 лет. Наконец, заболевание может носить аутоиммунный характер с образованием аутоантител к ткани поврежденного органа. Несмотря на многообразие этиологических факторов, у 10-40% больных установить причину хронического панкреатита не удается (идиопатическая форма заболевания).
Патогенетические механизмы хронического панкреатита
Патогенетические механизмы хронического панкреатита чрезвычайно сложны и во многом остаются неясными. Одним из ведущих факторов развития заболевания является активация панкреатических ферментов в протоках и паренхиме железы, что приводит к возникновению отека, некроза и последующему фиброзу с экзокринной и эндокринной недостаточностью. Развитию гиперферментемии способствуют факторы, приводящие к нарушению оттока панкреатического сока, существенную роль при этом играют нарушения микроциркуляции, в результате которых развиваются ишемия, отек, нарушение проницаемости клеточных мембран, деструкция ацинарных клеток. В системный кровоток выходят панкреатические ферменты и другие биологически активные вещества, в частности вазоактивные амины, что нарушает микроциркуляцию вне поджелудочной железы и вызывает повреждение других органов и систем. В последние годы обсуждается проблема окислительного стресса накопления в ацинарных клетках продуктов перекисного окисления липидов, свободных радикалов, вызывающих повреждение клеток, воспаление, синтез белков острой фазы. Предполагается также роль врожденного или приобретенного дефекта синтеза литостатина, приводящего к преципитации белка и кальция и обструкции мелких протоков с последующими перидуктальным воспалением и фиброзом.
Развитию гиперферментемии способствуют факторы, приводящие к нарушению оттока панкреатического сока, существенную роль при этом играют нарушения микроциркуляции, в результате которых развиваются ишемия, отек, нарушение проницаемости клеточных мембран, деструкция ацинарных клеток. В системный кровоток выходят панкреатические ферменты и другие биологически активные вещества, в частности вазоактивные амины, что нарушает микроциркуляцию вне поджелудочной железы и вызывает повреждение других органов и систем. В последние годы обсуждается проблема окислительного стресса накопления в ацинарных клетках продуктов перекисного окисления липидов, свободных радикалов, вызывающих повреждение клеток, воспаление, синтез белков острой фазы. Предполагается также роль врожденного или приобретенного дефекта синтеза литостатина, приводящего к преципитации белка и кальция и обструкции мелких протоков с последующими перидуктальным воспалением и фиброзом.
Особенности клинического течения панкреатитов у детей
Хронический панкреатит обычно развивается постепенно и характеризуется наличием латентной (субклинической) стадии, во время которой отмечаются ухудшение самочувствия, аппетита, неинтенсивная боль в животе, признаки микроциркуляционных расстройств: акроцианоз, экхимозы, иногда геморрагическая сыпь, нарастает ферментемия. На этом фоне появляется наиболее характерный и постоянный признак хронического панкреатита боль в верхнем отделе живота (преимущественно в околопупочной области), прогрессивно нарастающая, усиливающаяся после приема пищи и физической нагрузки и ослабевающая в положении сидя при наклоне туловища вперед. У значительной части детей отмечается иррадиация боли в поясницу, нижнюю часть спины; опоясывающая боль в детском возрасте наблюдается редко. Продолжительность болевых приступов различна: от нескольких часов до нескольких суток, иногда они перемежаются достаточно длительными безболевыми периодами. Возникновение болевого синдрома при хроническом панкреатите обусловлено внутрипротоковой гипертонией за счет сохраняющейся секреции панкреатических ферментов воспаленной железой в условиях обструкции ее протоков, воспалением внутрипанкреатических нервных стволов с развитием перипанкреатического воспаления и вовлечением в процесс двенадцатиперстной кишки и ретроперитонеального пространства.
На этом фоне появляется наиболее характерный и постоянный признак хронического панкреатита боль в верхнем отделе живота (преимущественно в околопупочной области), прогрессивно нарастающая, усиливающаяся после приема пищи и физической нагрузки и ослабевающая в положении сидя при наклоне туловища вперед. У значительной части детей отмечается иррадиация боли в поясницу, нижнюю часть спины; опоясывающая боль в детском возрасте наблюдается редко. Продолжительность болевых приступов различна: от нескольких часов до нескольких суток, иногда они перемежаются достаточно длительными безболевыми периодами. Возникновение болевого синдрома при хроническом панкреатите обусловлено внутрипротоковой гипертонией за счет сохраняющейся секреции панкреатических ферментов воспаленной железой в условиях обструкции ее протоков, воспалением внутрипанкреатических нервных стволов с развитием перипанкреатического воспаления и вовлечением в процесс двенадцатиперстной кишки и ретроперитонеального пространства.
Болевой синдром при хроническом панкреатите обычно сопровождается диспептическим, наиболее характерные проявления которого тошнота, рвота, резкое снижение аппетита. Позднее присоединяются изменения со стороны кишечника, обусловленные развитием синдрома нарушенного всасывания с диареей и панкреатической стеатореей, о чем свидетельствует появление «жирного» блестящего кала, трудно смываемого со стенок унитаза. Кал, особенно в начальных стадиях и при легком течении заболевания, может оставаться оформленным, иногда отмечается склонность к запору. На фоне болевого и диспептического синдромов всегда наблюдаются признаки хронической интоксикации: общая слабость, повышенная утомляемость, головная боль, эмоциональная лабильность, реже повышение температуры тела.
Позднее присоединяются изменения со стороны кишечника, обусловленные развитием синдрома нарушенного всасывания с диареей и панкреатической стеатореей, о чем свидетельствует появление «жирного» блестящего кала, трудно смываемого со стенок унитаза. Кал, особенно в начальных стадиях и при легком течении заболевания, может оставаться оформленным, иногда отмечается склонность к запору. На фоне болевого и диспептического синдромов всегда наблюдаются признаки хронической интоксикации: общая слабость, повышенная утомляемость, головная боль, эмоциональная лабильность, реже повышение температуры тела.
У больных иногда снижается масса тела (у некоторых детей во время обострения заболевания потеря массы тела весьма значительна). Следует подчеркнуть, что клиническая картина хронического панкреатита у детей весьма вариабельна и во многом определяется периодом заболевания, тяжестью процесса, степенью гиперферментемии, наличием осложнений и сопутствующих заболеваний.
Обострение хронического панкреатита следует дифференцировать с острым панкреатитом, в основе которого лежит активация панкреатических ферментов, обусловливающая аутолиз железы с развитием реактивного воспаления и токсемии. Острый панкреатит у детей протекает по типу интерстициального, реже геморрагического, при наличии инфекции он может трансформироваться в гнойный панкреатит. Острый отек поджелудочной железы при интерстициальном панкреатите обусловливает развитие болевого синдрома, заставляющего ребенка принять вынужденное положение на левом боку или коленно-локтевое. При этом характерно несоответствие между интенсивным характером боли и результатами пальпации: живот остается мягким, доступным пальпации; характерные для заболевания болевые зоны и мышечная защита отсутствуют. В большинстве случаев процесс ограничивается воспалением без развития некроза.
Острый панкреатит у детей протекает по типу интерстициального, реже геморрагического, при наличии инфекции он может трансформироваться в гнойный панкреатит. Острый отек поджелудочной железы при интерстициальном панкреатите обусловливает развитие болевого синдрома, заставляющего ребенка принять вынужденное положение на левом боку или коленно-локтевое. При этом характерно несоответствие между интенсивным характером боли и результатами пальпации: живот остается мягким, доступным пальпации; характерные для заболевания болевые зоны и мышечная защита отсутствуют. В большинстве случаев процесс ограничивается воспалением без развития некроза.
В отличие от интерстициального, геморрагический панкреатит характеризуется не только выраженным болевым синдромом, но и типичными пальпаторными признаками: болезненность и мышечная защита в верхнем отделе живота, положительные симптомы Керте, Кача, Мейо-Робсона, прогрессирующее ухудшение состояния ребенка, нарастание болевого синдрома, резкое повышение температуры тела, развитие токсикоза с эксикозом; при гнойном процессе развивается септическое состояние с симптоматикой острого раздражения брюшины. При панкреонекрозе и гнойном процессе прибегают к хирургическому вмешательству, лечение при интерстициальном панкреатите консервативное. Цель инструментального исследования (ультразвукового, рентгенологического, томографического, а при необходимости лапароскопии) прежде всего определение показаний к операции: геморрагическая жидкость в брюшной полости, абсцедирование, очаги некроза и кисты поджелудочной железы.
При панкреонекрозе и гнойном процессе прибегают к хирургическому вмешательству, лечение при интерстициальном панкреатите консервативное. Цель инструментального исследования (ультразвукового, рентгенологического, томографического, а при необходимости лапароскопии) прежде всего определение показаний к операции: геморрагическая жидкость в брюшной полости, абсцедирование, очаги некроза и кисты поджелудочной железы.
Функциональные нарушения поджелудочной железы панкреатопатии
Значительно чаще хронический панкреатит у детей дифференцируют с функциональными нарушениями поджелудочной железы панкреатопатиями, при которых нарушается преимущественно внешнесекреторная функция органа (диспанкреатизм) со слабовыраженной клинической симптоматикой. Воспалительные изменения поджелудочной железы при этом отсутствуют, процесс развивается по типу висцеро-висцерального рефлекса и, по-видимому, ограничивается преходящим отеком. Панкреатопатия обычно сопутствует заболеваниям гастродуоденальной зоны и гепатобилиарной системы и проявляется кратковременной болью преимущественно в левом подреберье, снижением аппетита, иногда неустойчивым стулом, стеатореей, реже креатореей. Область левого реберно-позвоночного угла, куда проецируется и непосредственно прилежит забрюшинно расположенная поджелудочная железа, иногда слегка напряжена и чувствительна при пальпации. При ультразвуковом исследовании поджелудочная железа практически не отличается от нормальной и лишь динамическое наблюдение в некоторых случаях позволяет выявить незначительное ее увеличение.
Область левого реберно-позвоночного угла, куда проецируется и непосредственно прилежит забрюшинно расположенная поджелудочная железа, иногда слегка напряжена и чувствительна при пальпации. При ультразвуковом исследовании поджелудочная железа практически не отличается от нормальной и лишь динамическое наблюдение в некоторых случаях позволяет выявить незначительное ее увеличение.
Осложнения хронического панкреатита
Осложнения хронического панкреатита у детей встречаются значительно реже, чем у взрослых. На фоне обострения заболевания (и при остром панкреатите) возможно формирование ложной кисты, образующейся в результате аутолиза поджелудочной железы и реактивного воспаления брюшины. Внутренняя поверхность кисты не имеет эпителиального покрова, содержимое ее состоит из панкреатического секрета бурого цвета. Формирование ложной кисты обычно сопровождается усилением боли в области проекции тела и хвоста железы с иррадиацией в спину, температурной реакцией, периодической рвотой. При пальпации живота отмечается защитное напряжение мышц в верхнем отделе, чаще слева; при значительных размерах кисты может прощупываться плотное образование. Диагноз устанавливается с помощью ультразвукового исследования или ретроградной панкреатохолангиографии. Лечение консервативное, лишь при значительных по объему ложных кистах, а также при их осложнениях острой кишечной непроходимости, образовании свищей, нагноении, разрыве кисты проводится оперативное вмешательство. Ложная киста, в свою очередь, может служить одним из механизмов формирования стеноза дистального отдела общего желчного протока и стеноза двенадцатиперстной кишки, а при присоединении вторичной инфекции абсцесса поджелудочной железы. Однако такие случаи в детской практике исключительно редки.
При пальпации живота отмечается защитное напряжение мышц в верхнем отделе, чаще слева; при значительных размерах кисты может прощупываться плотное образование. Диагноз устанавливается с помощью ультразвукового исследования или ретроградной панкреатохолангиографии. Лечение консервативное, лишь при значительных по объему ложных кистах, а также при их осложнениях острой кишечной непроходимости, образовании свищей, нагноении, разрыве кисты проводится оперативное вмешательство. Ложная киста, в свою очередь, может служить одним из механизмов формирования стеноза дистального отдела общего желчного протока и стеноза двенадцатиперстной кишки, а при присоединении вторичной инфекции абсцесса поджелудочной железы. Однако такие случаи в детской практике исключительно редки.
Диагностика заболеваний поджелудочной железы у детей
Диагностика заболеваний поджелудочной железы основывается на данных анамнеза и характерных клинических симптомах, оценке экзокринной и эндокринной деятельности органа и результатах инструментальных исследований, способных определить наличие структурных изменений pancreas. К прямым методам исследования экзокринной (внешнесекреторной) функции поджелудочной железы относится изучение показателей секреторной деятельности органа натощак и после введения стимуляторов.
К прямым методам исследования экзокринной (внешнесекреторной) функции поджелудочной железы относится изучение показателей секреторной деятельности органа натощак и после введения стимуляторов.
Для диагностики обострения хронического панкреатита важное значение имеет определение активности панкреатических ферментов амилазы, липазы и трипсина в крови, а также амилазы и липазы в моче. Однократного определения активности фермента может быть недостаточно, поскольку показатели амилазы и липазы в крови натощак обычно повышаются в 1,5-2 раза на короткий период времени (через 2-12 часов после обострения и достигает максимума к концу первых суток с последующим быстрым падением и нормализацией в течение 2-4 дней). Активность амилазы в моче возрастает примерно на 6 часов позже сывороточной. В то же время повышение активности сывороточной амилазы в два и более раз в сочетании с увеличением липазы и трипсина (или одного из них) является достаточно достоверным тестом обострения заболевания. Однако и нормальные показатели концентрации ферментов в крови и моче не дают основания исключить диагноз хронического панкреатита. В таких случаях применяется «провокационный» тест, при котором определяется активность ферментов до и после стимуляции. Наиболее широко используют определение амилазы в крови после стимуляции панкреозимином или глюкозой, а также уровень амилазы в моче на фоне стимуляции прозерином. После введения раздражителей наблюдается феномен «уклонения ферментов» (гиперферментемия), что свидетельствует о поражении ткани поджелудочной железы или препятствии для оттока панкреатического сока. Иногда провокационные тесты могут быть отрицательными (уровень ферментов не изменяется или даже снижается), что связано с уменьшением числа ацинарных клеток, продуцирующих эти ферменты при тяжелом панкреатите.
Однако и нормальные показатели концентрации ферментов в крови и моче не дают основания исключить диагноз хронического панкреатита. В таких случаях применяется «провокационный» тест, при котором определяется активность ферментов до и после стимуляции. Наиболее широко используют определение амилазы в крови после стимуляции панкреозимином или глюкозой, а также уровень амилазы в моче на фоне стимуляции прозерином. После введения раздражителей наблюдается феномен «уклонения ферментов» (гиперферментемия), что свидетельствует о поражении ткани поджелудочной железы или препятствии для оттока панкреатического сока. Иногда провокационные тесты могут быть отрицательными (уровень ферментов не изменяется или даже снижается), что связано с уменьшением числа ацинарных клеток, продуцирующих эти ферменты при тяжелом панкреатите.
В последние годы альтернативой достаточно инвазивному секретин-панкреозиминовому тесту стало определение в кале эластазы-1. Этот фермент секретируется поджелудочной железой и не метаболизируется в кишечнике, его активность в кале объективно отражает состояние экзокринной функции органа, а органоспецифичность исключает возможность ошибки, связанной с активностью кишечных ферментов. В отличие от других тестов, определение эластазы-1 можно проводить, не отменяя препараты заместительной терапии. В норме активность эластазы-1 в кале более 200 мкг/г кала, снижение концентрации эластазы свидетельствует о панкреатической недостаточности.
В отличие от других тестов, определение эластазы-1 можно проводить, не отменяя препараты заместительной терапии. В норме активность эластазы-1 в кале более 200 мкг/г кала, снижение концентрации эластазы свидетельствует о панкреатической недостаточности.
Признаком внешнесекреторной недостаточности поджелудочной железы является полифекалия, когда кал имеет сальный вид, сероватого цвета, кашицеобразный, вязкий, с резким гнилостным запахом, плохо смывается со стенок унитаза. При микроскопическом исследовании могут обнаруживаться непереваренные мышечные волокна (креаторея) признак тяжелого течения панкреатита; наличие капель нейтрального жира (стеаторея) один из ранних симптомов панкреатической недостаточности.
Для оценки внутрисекреторной функции поджелудочной железы применяется метод определения гликемической кривой.
Из инструментальных методов диагностики хронического панкреатита наиболее доступным, но не всегда достаточно информативным, особенно в начальном периоде заболевания, является ультразвуковое исследование, позволяющее наблюдать больного в динамике. При ультразвуковом исследовании определяют размеры поджелудочной железы и степень эхогенности паренхимы. В норме толщина головки поджелудочной железы у детей колеблется от 8 до 18 мм, тела от 5 до 15 мм и хвоста от 5 до 16 мм, ширина главного протока не превышает 2 мм. В периоде обострения хронического панкреатита отмечается диффузное или локальное увеличение головки, тела или хвоста поджелудочной железы, нечеткость ее контуров, расширение протока, усиление эхогенности органа. В таких случаях необходимо провести повторные исследования, чтобы оценить динамику состояния железы. При длительном течении хронического панкреатита контуры железы становятся неровными, отмечается негомогенное усиление эхогенности, признаки фиброза, очаги обызвествления. Ультразвуковое исследование позволяет выявить калькулез в протоках железы, псевдокисты, гематому или разрыв поджелудочной железы при травме брюшной полости. Чувствительность метода (60-70%) и его специфичность (80-90%) позволяют использовать ультразвуковое исследование в качестве одного из основных диагностических методов верификации хронического панкреатита.
При ультразвуковом исследовании определяют размеры поджелудочной железы и степень эхогенности паренхимы. В норме толщина головки поджелудочной железы у детей колеблется от 8 до 18 мм, тела от 5 до 15 мм и хвоста от 5 до 16 мм, ширина главного протока не превышает 2 мм. В периоде обострения хронического панкреатита отмечается диффузное или локальное увеличение головки, тела или хвоста поджелудочной железы, нечеткость ее контуров, расширение протока, усиление эхогенности органа. В таких случаях необходимо провести повторные исследования, чтобы оценить динамику состояния железы. При длительном течении хронического панкреатита контуры железы становятся неровными, отмечается негомогенное усиление эхогенности, признаки фиброза, очаги обызвествления. Ультразвуковое исследование позволяет выявить калькулез в протоках железы, псевдокисты, гематому или разрыв поджелудочной железы при травме брюшной полости. Чувствительность метода (60-70%) и его специфичность (80-90%) позволяют использовать ультразвуковое исследование в качестве одного из основных диагностических методов верификации хронического панкреатита. Для уточнения диагноза панкреатита используют также компьютерную томографию (чувствительность ее около 90%, специфичность 85%). Метод дополняет и уточняет результаты ультразвукового исследования, позволяя выявить изменения контуров и размеров поджелудочной железы, очаги обызвествления и некроза, расширение панкреатического протока, псевдокисты и кисты, все это ставит компьютерную томографию в ряд наиболее информативных исследований при диагностике заболеваний pancreas.
Для уточнения диагноза панкреатита используют также компьютерную томографию (чувствительность ее около 90%, специфичность 85%). Метод дополняет и уточняет результаты ультразвукового исследования, позволяя выявить изменения контуров и размеров поджелудочной железы, очаги обызвествления и некроза, расширение панкреатического протока, псевдокисты и кисты, все это ставит компьютерную томографию в ряд наиболее информативных исследований при диагностике заболеваний pancreas.
Рентгенологическое исследование, включающее прицельный снимок брюшной полости в проекции поджелудочной железы, контроль пассажа бария по верхним отделам желудочно-кишечного тракта, дуоденографию в условиях гипотонии, в связи с большой лучевой нагрузкой и внедрением в практику более информативных методов диагностика хронического панкреатита в настоящее время применяется редко. Значительно более информативным методом исследования является эндоскопическая ретроградная панкреатохолангиография золотой стандарт в диагностике хронического панкреатита, позволяющая выявить стеноз протока и локализацию обструкции, обнаружить структурные изменения мелких протоков, внутрипротоковые кальцинаты и белковые пробки. На основании результатов исследования диагностируют вероятный хронический панкреатит (если изменены один-два мелких протока), легкий (более трех мелких протоков), умеренный (поражение главного протока и ответвлений) и выраженный (изменение главного протока и ответвлений, внутрипротоковые дефекты или камни, обструкция протока, стриктуры или значительная неравномерность поражения). В связи со сложностью исследования разработаны четкие показания: хронический панкреатит с выраженным болевым синдромом и повторными обострениями; вторичный панкреатит, развившийся на фоне калькулезного холецистита; рецидивирующая желтуха неясной этиологии; боль в верхних отделах брюшной полости, появившаяся после травмы живота; дуоденостаз с расширением петли двенадцатиперстной кишки на рентгенограмме.
На основании результатов исследования диагностируют вероятный хронический панкреатит (если изменены один-два мелких протока), легкий (более трех мелких протоков), умеренный (поражение главного протока и ответвлений) и выраженный (изменение главного протока и ответвлений, внутрипротоковые дефекты или камни, обструкция протока, стриктуры или значительная неравномерность поражения). В связи со сложностью исследования разработаны четкие показания: хронический панкреатит с выраженным болевым синдромом и повторными обострениями; вторичный панкреатит, развившийся на фоне калькулезного холецистита; рецидивирующая желтуха неясной этиологии; боль в верхних отделах брюшной полости, появившаяся после травмы живота; дуоденостаз с расширением петли двенадцатиперстной кишки на рентгенограмме.
Радионуклидное сканирование поджелудочной железы с метионином, меченным 75-Se обеспечивает возможность визуального контроля, определяет при хроническом панкреатите снижение накопления в поджелудочной железе радионуклида, нечеткость и размытость ее контуров, ускорение поступления меченного панкреатического содержимого в кишечник.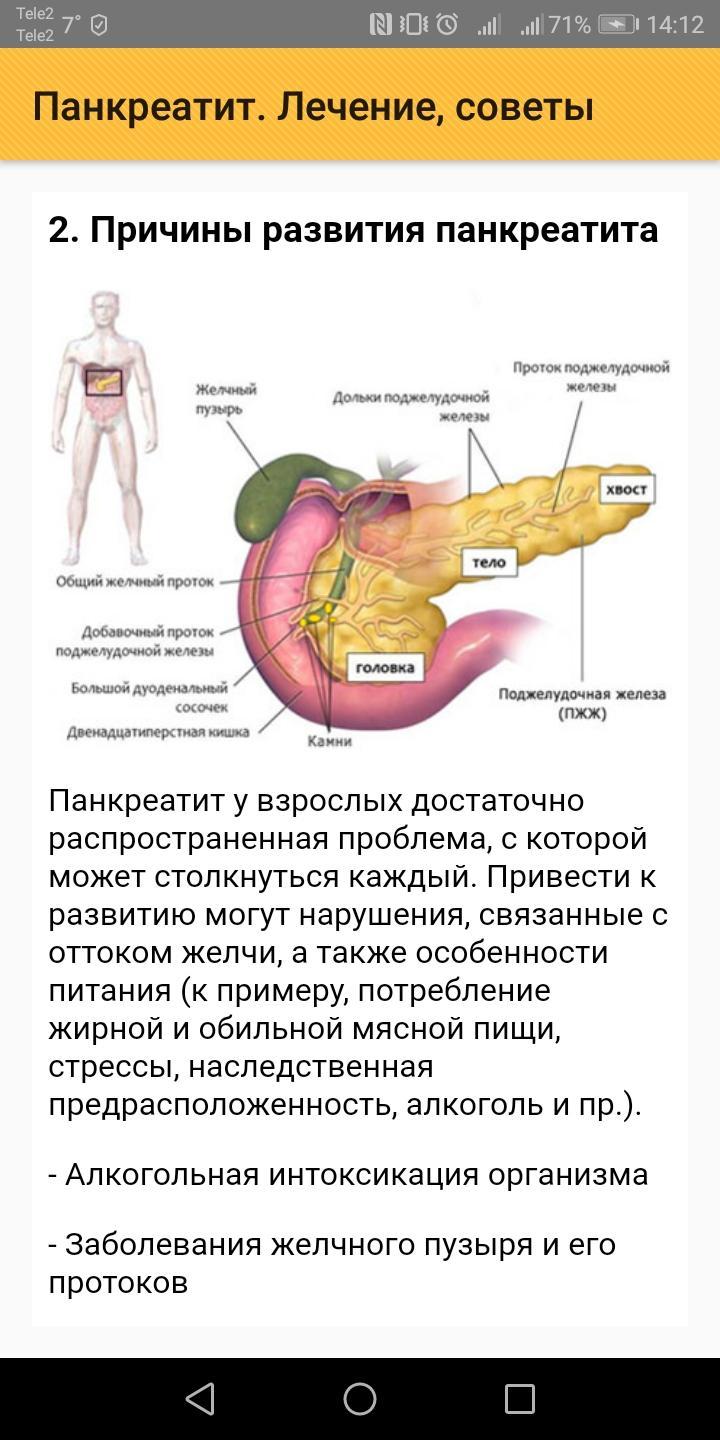 Однако из-за значительной лучевой нагрузки в педиатрической практике метод применяется редко.
Однако из-за значительной лучевой нагрузки в педиатрической практике метод применяется редко.
Термографические методы исследования (дистанционная и контактная жидкокристаллическая термография) используют на догоспитальном этапе в качестве скрининг-метода. Результаты термографического исследования с учетом клинических данных позволяют дифференцировать воспалительные и реактивные изменения железы (панкреатопатия) и наметить план исследования с использованием более сложных диагностических методов.
Лечение хронического панкреатита
Терапия при хроническом панкреатите предполагает устранение провоцирующих факторов, купирование болевого синдрома, коррекцию экзокринной и эндокринной функций поджелудочной железы, устранение сопутствующих расстройств со стороны пищеварительной системы.
В периоде обострения хронического панкреатита и при остром панкреатите больные должны находиться на стационарном лечении с ежедневным (до стихания острых явлений) контролем гемодинамических параметров (пульс, артериальное давление, центральное венозное давление), водного баланса, гематокрита, кислотно-основного состояния, содержания гемоглобина, лейкоцитов, амилазы, липазы, калия, кальция, глюкозы, мочевины в сыворотке крови.
Чрезвычайно важную роль на всех этапах лечения больного хроническим панкреатитом играет диетическое питание, которое должно обеспечивать физиологический покой поджелудочной железе, облегчать всасывание пищевых веществ и компенсировать энергетические затраты организма. При остром панкреатите и тяжело протекающем обострении хронического панкреатита в первые 2-3 дня назначается «голодная» пауза с одновременным обильным питьем (отвар шиповника, несладкий чай, щелочные минеральные воды без газа). В периоде голодания следует несколько раз в день проводить отсасывание желудочного секрета с помощью назогастрального зонда.
После стихания острых явлений ребенку назначают диету с физиологической нормой содержания белка от 80 до 120 г в сутки в виде легкоусвояемых продуктов ( молочные блюда, яйца, нежирные сорта мяса и рыбы), углеводов ( 250-300 г в сутки высокомолекулярных полисахаридов), ограничивая жиры до 55-60 г в сутки за счет уменьшения количества животных жиров и использования хорошо переносимых растительных, не вызывающих усиления панкреатической секреции. Необходимо соблюдать принцип частого питания небольшими порциями (диета №5-П). Диета должна быть максимально индивидуализирована с учетом личностных особенностей больного ребенка и соответствующей гастродуоденальной патологии. Диетическое лечение в период ремиссии предусматривает использование диеты №5-П в течение 5-6 месяцев, которая обеспечивает физиологическую потребность организма ребенка в основных пищевых ингредиентах и энергии.
Необходимо соблюдать принцип частого питания небольшими порциями (диета №5-П). Диета должна быть максимально индивидуализирована с учетом личностных особенностей больного ребенка и соответствующей гастродуоденальной патологии. Диетическое лечение в период ремиссии предусматривает использование диеты №5-П в течение 5-6 месяцев, которая обеспечивает физиологическую потребность организма ребенка в основных пищевых ингредиентах и энергии.
Важнейший принцип лечения больных с хроническим панкреатитом в периоде обострения купирование болевого синдрома.
Основная причина боли внутрипротоковая гипертония, поэтому препаратами выбора являются средства, блокирующие стимулированную панкреатическую секрецию, Соматостатин (октреотид) и даларгин.
Являясь мощным ингибитором нейроэндокринных гормонов желудочно-кишечного тракта, окреотид угнетает стимулированную секрецию поджелудочной железы путем прямого действия на экзокринную ткань и уменьшения высвобождения секретина и холецистокинина. Препарат активен также при лечении больных с псевдокистами, быстро улучшается состояние больных, уменьшается боль в животе, ликвидируется парез кишечника, нормализуется активность панкреатических ферментов. Назначают октреотид детям 25-100 мкг 3 раза в день подкожно или внутривенно в течение 5-7 дней.
Препарат активен также при лечении больных с псевдокистами, быстро улучшается состояние больных, уменьшается боль в животе, ликвидируется парез кишечника, нормализуется активность панкреатических ферментов. Назначают октреотид детям 25-100 мкг 3 раза в день подкожно или внутривенно в течение 5-7 дней.
Даларгин синтетический аналог опиоидных пептидов также антагонист панкреатической секреции, его применяют по 1 мг 2-3 раза в день внутримышечно или внутривенно капельно в 100-200 мл изотонического раствора хлорида натрия.
Эффективность использования антипротеазных препаратов как ингибиторов протеолитических ферментов, прежде всего циркулирующего в крови трипсина, в настоящее время подвергается сомнению, поскольку они не влияют на активность липолитических ферментов, обладающих выраженным деструктивным действием, и не могут купировать некротические процессы в железе даже при высоких суточных дозах введения. В то же время, при условии применения антипротеазных препаратов в первые часы обострения панкреатита, удается получить обезболивающий эффект за счет подавления трипсиновой и кининовой активности.
В остром периоде заболевания могут быть использованы панкреатические ферменты в комбинации с блокаторами Н2-рецепторов гистамина или жидкими антацидами (Маалокс, Фосфалюгель) для предупреждения инактивации экзогенных панкреатических ферментов кислотой желудочного сока. Эффективность панкреатических ферментов в остром периоде заболевания основывается на их свойстве уменьшать болевой синдром за счет включения механизма обратной связи: повышение уровня протеаз в просвете двенадцатиперстной кишки вызывает уменьшение высвобождения и синтеза холецистокинина, что приводит к снижению стимуляции экзокринной функции поджелудочной железы, уменьшению внутрипротокового и тканевого давления, поскольку холецистокинин является основным стимулятором экзогенной функции поджелудочной железы. Назначают ферментные препараты, не содержащие желчных кислот (Панкреатин, Мезим Форте, трифермент, Креон).
При неосложненном панкреатите болевой синдром обычно купируют в течение 2-3 дней. Если болевой синдром сохраняется дольше, используют аналгезирующие препараты: 50% раствор Аналгина 1-2 мл или Баралгина 3-5 мл 2-3 раза в день. При отсутствии эффекта дополнительно назначают нейролептики: 0,25% раствор дроперидола по 1-2 мл (2,5-5мг) с 0,05-0,1 мг (1-2 мл 0,005% раствора) фентанила внутримышечно или внутривенно 1-2 раза в сутки. С первых суток обострения для профилактики развития септических осложнений применяют антибиотики.
При отсутствии эффекта дополнительно назначают нейролептики: 0,25% раствор дроперидола по 1-2 мл (2,5-5мг) с 0,05-0,1 мг (1-2 мл 0,005% раствора) фентанила внутримышечно или внутривенно 1-2 раза в сутки. С первых суток обострения для профилактики развития септических осложнений применяют антибиотики.
Инфузионная терапия при обострении хронического панкреатита проводится с первых часов обострения заболевания (желательно под контролем центрального венозного давления). Внутривенно применяют 5% раствор глюкозы, изотонический раствор хлорида натрия, полиионный раствор, на основе которых вводят необходимые для интенсивной терапии при болевом синдроме препараты: октреотид, даларгин, антипротеазные препараты, аналгетики, нейролептики и другие.
При обострении заболевания минимальные исследования должны включать: определение амилазы мочи (ежедневно), биохимический нализ крови (уровни амилазы, аминотрансфераз, щелочной фосфатазы) один раз в 2 дня. В дальнейшем эти исследования проводятся не реже одного раза в неделю.
При уменьшении или ликвидации болевого синдрома и диспептических расстройств, стабилизации гемодинамических показателей, нормализации содержания в крови и моче панкреатических ферментов начинается следующий этап лечения больных с хроническим панкреатитом. Решают вопрос о необходимости коррекции внешнесекреторной функции поджелудочной железы путем компенсации ее недостаточности. Последняя проявляется в первую очередь стеатореей. Заместительная ферментативная терапия с общепринятой точки зрения необходима в тех случаях, когда ежедневное выделение жира превышает 15 г, и (или) больной теряет массу тела, и (или) имеют место диарея и диспептические симптомы. Во всех случаях, когда предполагается экзокринная недостаточность и решается вопрос о назначении панкреатических ферментов, целесообразно определение эластазы-1, это позволяет избежать необоснованного их назначения или, напротив, подтвердить необходимость. Из большого числа предлагаемых ферментных препаратов (табл.) при экзокринной недостаточности поджелудочной железы следует прежде всего предпочесть формы, не содержащие желчь и экстракты слизистой оболочки желудка. Важным условием успешной терапии является оптимальное содержание в препарате липазы, особенно учитывая ее нестабильность при транзите после приема пищи (сохраняется только около 8% липазной активности панкреатина в кишечнике). Максимальное количество липазы содержат (в порядке убывания) Панцитрат, Креон, Панзинорм и Фестал, однако последние два препарата малоприемлемы из-за наличия в них желчи. Наконец, ферментный препарат не должен инактивироваться в кислом содержимом желудка, хотя этого можно избежать дополнительным одновременным назначением жидких антацидов или блокаторов Н2-рецепторов гистамина. Большинство гастроэнтерологов отдают предпочтение при лечении больных с экзокринной недостаточностью поджелудочной железы Креону защищенному от воздействия соляной кислоты ферментному препарату.
Важным условием успешной терапии является оптимальное содержание в препарате липазы, особенно учитывая ее нестабильность при транзите после приема пищи (сохраняется только около 8% липазной активности панкреатина в кишечнике). Максимальное количество липазы содержат (в порядке убывания) Панцитрат, Креон, Панзинорм и Фестал, однако последние два препарата малоприемлемы из-за наличия в них желчи. Наконец, ферментный препарат не должен инактивироваться в кислом содержимом желудка, хотя этого можно избежать дополнительным одновременным назначением жидких антацидов или блокаторов Н2-рецепторов гистамина. Большинство гастроэнтерологов отдают предпочтение при лечении больных с экзокринной недостаточностью поджелудочной железы Креону защищенному от воздействия соляной кислоты ферментному препарату.
При затяжном течении хронического панкреатита ферментные препараты принимают длительно, дозы подбирают индивидуально и корректируют в процессе лечения с учетом диетического питания (уменьшают при строгой диете, увеличивают при ее расширении). Принимая во внимание, что при хроническом панкреатите ферментные препараты используют в различные периоды заболевания, в остром периоде следует предпочесть препараты, содержащие высокие дозы трипсина и химотрипсина, а при внешнесекреторной недостаточности высокие дозы липазы.
Принимая во внимание, что при хроническом панкреатите ферментные препараты используют в различные периоды заболевания, в остром периоде следует предпочесть препараты, содержащие высокие дозы трипсина и химотрипсина, а при внешнесекреторной недостаточности высокие дозы липазы.
Симптоматическая терапия при хроническом панкреатите чаще включает препараты, нормализующие нарушения моторики двенадцатиперстной кишки, желчного пузыря и сфинктеров большого дуоденального сосочка (холинолитики, прокинетики), гипосенсибилизирующие средства (Кларитин, Фенистил), пробиотики (бифидум- и лактобактерины, Симбитер).
В фазе ремиссии после выписки из стационара ребенка наблюдает гастроэнтеролог. Стабильное состояние больного поддерживается соблюдением диетического режима (диета №5-П в течение 6-12 месяцев, иногда и более) после обострения. Обязательным компонентом диспансеризации является противорецидивная терапия, которая на первом году наблюдения проводится 3-4 раза в год, через 2-3 года 1-2 курса в год. Продожительность курса противорецидивной терапии от 4 до 6 недель. В диспансерном периоде для профилактики широко используют лекарственные растения и сборы из них, основным показанием к назначению которых является недостаточность внешнесекреторной функции поджелудочной железы.
Продожительность курса противорецидивной терапии от 4 до 6 недель. В диспансерном периоде для профилактики широко используют лекарственные растения и сборы из них, основным показанием к назначению которых является недостаточность внешнесекреторной функции поджелудочной железы.
Благоприятные результаты в предупреждении рецидивов хронического панкреатита дает курортное лечение, которое следует проводить только в период ремиссии при нормальных показателях экзокринной и эндокринной функций поджелудочной железы.
Успех комплексной терапии хронического панкреатита состоит в тщательном соблюдении последовательности корригирующих мероприятий с учетом основных показателей функционирования поджелудочной железы в различные периоды заболевания.
СТАТТІ ЗА ТЕМОЮ
24. 10.2021
Гастроентерологія Коморбідний пацієнт із хронічним панкреатитом
10.2021
Гастроентерологія Коморбідний пацієнт із хронічним панкреатитомУ статті розглянуті патогенетичні механізми виникнення дуоденогастрального рефлюксу (ДГР), дуоденогастроезофагеального рефлюксу (ДГЕР), їх ролі у виникненні жовчного рефлюкс-гастриту, рефлюкс-езофагіту. Принциповими засадами формування жовчного рефлюксу є неспроможність сфінктерного апарату, антродуоденальна дисмоторика, ліквідація природного антирефлюксного бар’єру. Факторами ризику розвитку первинного ДГР вважають дисфункцію жовчного міхура і дуоденальну дисмоторику….
24. 10.2021
Гастроентерологія «Гастротандем 2021»: міждисциплінарний підхід до актуальних питань гастроентерології
10.2021
Гастроентерологія «Гастротандем 2021»: міждисциплінарний підхід до актуальних питань гастроентерологіїЗахворювання шлунково-кишкового тракту (ШКТ) значною мірою коморбідні та часто супроводжуються супутньою патологією. Тому в цих випадках їх діагностика та лікування повинні базуватися на міждисциплінарному підході із залученням фахівців декількох спеціальностей. Саме такий підхід був детально розглянутий під час науково-практичної конференції «Гастротандем 2021. На стику дисциплін», яка проходила з 30 червня по 2 липня 2021 року в Одесі. Захід відбувся за підтримки Міжнародної асоціації медицини та Одеського відділення Української гастроентерологічної асоціації. …
Панкреатит у ребенка.
 Симптомы, лечение, диета
Симптомы, лечение, диетаВоспаление поджелудочной железы крайне неприятная, а временами довольно опасная проблема детского здоровья. При возникновении симптомов обязательно нужен врач.
Источник: instagram @prosto_o_gkt
Что такое панкреатит
Задача поджелудочной железы – выработка специфической жидкости, которая так и называется – сок поджелудочной железы, необходимого для переваривания пищи. В этом соке содержатся активные ферменты, которые в норме начинают «работать», когда сок поджелудочной железы оказывается в двенадцатиперстной кишке, где и происходит один из этапов расщепления белков.
Если случился сбой, и ферменты активизировались в самой поджелудочной железе, возникает воспалительный процесс, который и получил название панкреатит.
Острый панкреатит у детей встречается относительно редко. Это серьезное заболевание при котом меры необходимо предпринимать как можно скорее, поскольку начинается разрушение тканей железы, в кровь попадают биологически активные ферменты, которые могут непредсказуемо повлиять на все органы, до которых доберутся с током крови.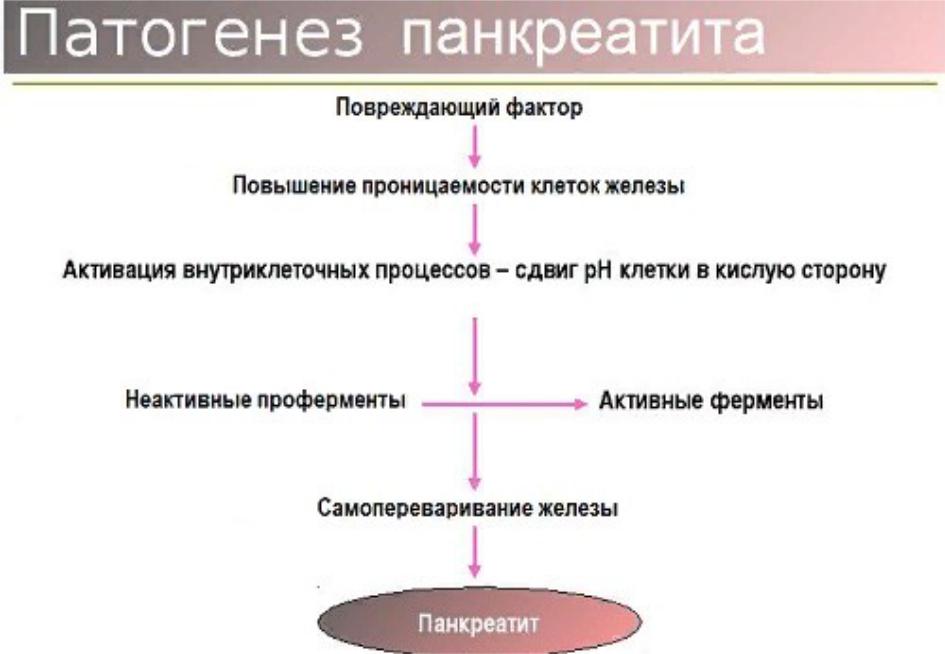
Хронический панкреатит в состоянии покоя практически никак не проявляется, однако, если нарушение существует, то периодически могут возникать обострения, при которых ребенок жалуется на боль в верхней части живота, тошноту, у него пропадает аппетит, возможна рвота и понос.
Реактивный панкреатит, считается, что этот вид панкреатита у детей встречается чаще всего и связано это с незрелостью пищеварительной системы. Воспаление поджелудочной железы могут спровоцировать: любая инфекция, вплоть до ОРЗ, резкое изменение рациона питания, даже сильный стресс.
Burda Media
Диагностика панкреатита
Во время воспалительного процесса происходит изменение состава крови, поскольку в ней обнаруживаются вещества, которых в норме быть не должно. Основной метод диагностики панкреатита – клинический анализ крови на наличие ферментов поджелудочной железы амилазы, липазы и трипсина.
При обострении хронического панкреатита анализ кала ребенка показывает остатки непереваренной пищи, следы нерасщепленного жира и другие примеси.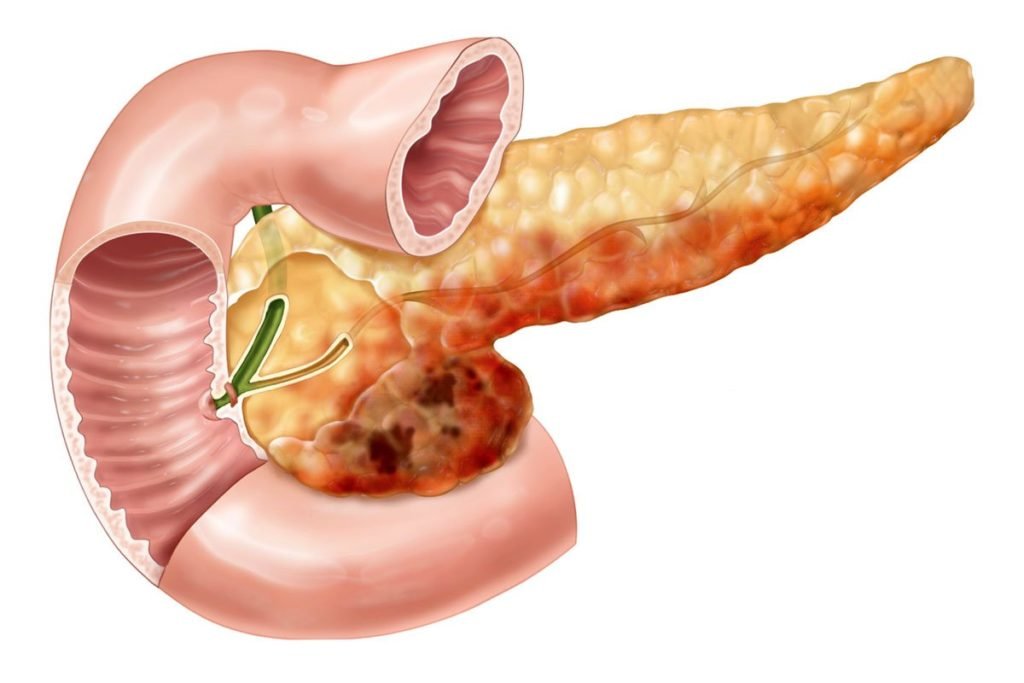
Возможно, понадобится дополнительное исследование, например УЗИ.
Burda Media
Лечение панкреатита
Любая форма панкреатита острый, реактивный или обострение хронического требует медицинской помощи и наблюдения специалиста. Возможно даже понадобится госпитализация, поскольку могут быть назначены препараты, которые необходимо вводить внутривенно в виде капельниц.
В схему лечения включают обезболивающие препараты, поскольку панкреатит может взывать нестерпимую боль.
При панкреатите одним и основных компонентов лечения является полное голодание, продолжительность которого назначает врач с учетом состояния ребенка, его возраста и степени поражения поджелудочной железы. Как правило этот период продолжается от 1 до 3 дней и в это время ребенку можно и нужно пить воду в достаточном количестве.
Burda Media
Как вести себя после приступа
- После приступа панкреатита любой разновидности и голодания возвращаться к нормальному питанию нужно постепенно.

- В день, когда разрешается прекратить голодание, предложите ребенку немного перетертой каши без масла (гречневая, овсяная), чай с сухариками.
- На следующий день можно съесть несколько ложек протертого овощного супа (исключив белокочанную капусту), а так же паровой омлет.
- Затем разрешают небольшое количество печеного яблока и немного нежирного ворога, разведенного кефиром
- После приступа нельзя есть сырые фрукты и овощи, шоколад, мясные бульоны, жирную пищу.
- Питание ребенка должно быть дробным — мелкими порциями, 5-6 раз в день.
- В дальнейшем ребенку назначают диету по Повзнеру №5 или 5п. Диеты рассчитаны таким образом, чтобы уменьшить количество жиров и грубой клетчатки при нормальном поступлении белков. В диете 5п, которая рассчитана именно на восстановление поджелудочной железы, уменьшено еще и количество углеводов, все блюда позволяется только варить или готовить на пару, в основном предлагать ребенку в перетертом виде. Кроме того, блюда не должны быть холодными либо горячими – только теплыми.

Если придерживаться правильного питания, вполне вероятно, что со временем ребенок проблему перерастет и поджелудочная железа полностью восстановится.
Мнение редакции может не совпадать с мнением автора статьи.
Использование фото: П.4 ст.21 ЗУ «Об авторских и смежных правах — «Воспроизведение с целью освещения текущих событий средствами фотографии или кинематографии, публичное сообщение или сообщение произведений, увиденных или услышанных во время таких событий, в объеме, оправданном информационной целью.»
симптомы и лечение – Medaboutme.ru
Острый панкреатит (воспаление поджелудочной железы) чаще встречается у взрослых, более того, у детей он протекает с менее выраженной симптоматикой. Но несмотря на это, у ребенка такой диагноз может стать причиной тяжелых осложнений. Как определить острый панкреатит, чем лечить малыша и как не допустить повторного воспаления, разбирался MedAboutMe.
Причины панкреатита у детей
Прежде всего, следует отличать острый панкреатит от реактивного. Первый, который врачи часто называют истинным, вызван патологиями самой поджелудочной — чрезмерный синтез ферментов наносит ущерб органу, по сути, железа сама себя отравляет. Реактивный панкреатит, который встречается у детей намного чаще, развивается на фоне интоксикации организма, вызванной пищевым отравлением или инфекционным заболеванием. Следует помнить, что частые реактивные воспаления могут перейти в острый панкреатит. Поэтому среди причин развития этой болезни часто упоминают неправильное питание с обилием жирной и сладкой пищи.
Первый, который врачи часто называют истинным, вызван патологиями самой поджелудочной — чрезмерный синтез ферментов наносит ущерб органу, по сути, железа сама себя отравляет. Реактивный панкреатит, который встречается у детей намного чаще, развивается на фоне интоксикации организма, вызванной пищевым отравлением или инфекционным заболеванием. Следует помнить, что частые реактивные воспаления могут перейти в острый панкреатит. Поэтому среди причин развития этой болезни часто упоминают неправильное питание с обилием жирной и сладкой пищи.
У 25% заболевших детей установить, почему развился панкреатит, не удается. В других же случаях врачи выделяют такие факторы риска:
- Воспаление в ЖКТ, застойные явления в кишечнике.
- Применение некоторых лекарственных средств.
- Бактериальные и вирусные инфекции — сальмонеллез, дизентерия, свинка, гепатиты, энтеровирусная инфекция, герпес, грипп, краснуха.
- Желчнокаменная болезнь, хронический холецистит.

- Переизбыток витамина D.
- Травма живота.
- Болезни, при которых повреждается панкреатический проток.
- Гельминтозы, в том числе клонорхоз и аскаридоз.
- Опухоль в поджелудочной.
Симптомы панкреатита: боль, тошнота и другое
Гастроэнтерологи выделяют две формы острой болезни — интерстициальное (отечно-серозное) и деструктивное (панкреонекроз) воспаление поджелудочной железы. У детей чаще встречается первая форма, она менее опасна и хорошо поддается лечению. Симптомы панкреатита в этом случае такие:
- Боль в животе, часто острая, приступообразная, которая усиливается после пальпации.
- Тошнота, периодическая рвота.
- Чувство тяжести в желудке.
- Плохой аппетит или его полное отсутствие.
- Метеоризм, вздутость живота.
- Диарея.
- Бледность.
- Учащенное сердцебиение.

При интерстициальном воспалении у ребенка очень редко повышается температура, а общее состояние оценивается как удовлетворительное.
При панкреонекрозе симптомы панкреатита будут следующими:
- Постоянная сильная боль в левом боку.
- Частая рвота.
- Твердый вздутый живот (сильное напряжение брюшной стенки).
- Повышение температуры до 37°С, иногда выше.
- Желтушные склеры.
- Сильное ухудшение общего состояния.
- Учащенный поверхностей пульс.
У детей деструктивный панкреатит диагностируется редко, но если такое заболевание все же развивается, оно требует неотложной помощи врачей, в некоторых случаях — реанимационных мероприятий. Ребенок может пострадать от токсического шока, смертность при таком диагнозе — 40-70%. Иногда панкреонекроз диагностируется как осложнение интерстициального воспаления. Поэтому при первых же симптомах панкреатита нужно срочно обращаться к врачу и проводить необходимое лечение.
Диагностика острого панкреатита у детей
Поскольку основным симптомом панкреатита является резкая боль в животе, прежде всего, врачи проверяют ребенка на болезни со схожей симптоматикой. Гастроэнтерологи исключают острый аппендицит, острый холецистит, обострение язвенной болезни (может встречаться у подростков), кишечную непроходимость и другое.
Диагностируют панкреатит с помощью таких аппаратных и лабораторных исследований:
- Общий анализ крови (проверяется уровень лейкоцитов, СОЭ).
- Биохимия крови (выявляется повышение количества ферментов амилазы, трипсина и липазы, а также высокий уровень глюкозы).
- Анализ кала (обнаружение непереваренных частичек пищи).
- УЗИ органов брюшной полости.
- Рентген.
Диагностика проводится в стационаре, поскольку ребенок с признаками поражения поджелудочной железы госпитализируется в обязательном порядке. Обследования помогают дифференцировать острый панкреатит от реактивного, а это крайне важно для выбора лечения и дальнейшей профилактики.
Правильное питание при панкреатите
Основой лечения панкреатита считается диета. Именно правильное питание поможет уменьшить нагрузку на поджелудочную железу. При остром воспалении в первые 24-48 часов всем пациентам вне зависимости от возраста назначается голодная диета. А это значит, что исключается любая пища, больному разрешено пить простую или минеральную щелочную воду. Совсем маленьким детям, а также ослабленным пациентам дополнительно может вводиться глюкоза.
После «пищевой паузы» рацион наполняется постепенно:
- 1-й день — жидкая протертая каша (готовится без соли), жидкое овощное пюре (только отварные овощи), компоты, кисели. Еда дается маленькими порциями, для первого дня лучше выбрать 1-2 блюда.
- 2-7-й день — добавляются овощные супы, омлет на пару (без желтков).
- 2-3-я неделя — в рацион вводятся печеные яблоки, приготовленные на пару овощи, можно предложить перетертую отварную куриную грудку.

Ограничения в питании при лечении панкреатита нужно соблюдать как минимум 2 месяца, при этом лечащий врач может порекомендовать более длительную диету. Начиная с 3-4-й недели в меню ребенка можно включить:
- Отварное нежирное мясо.
- Отварную или запеченную рыбу.
- Творожные запеканки.
- Тушеное овощное рагу.
- Макароны.
- Вареные яйца или омлеты.
Полностью исключается употребление жареной и жирной пищи, при панкреатите не рекомендованы также свежие овощи и фрукты, соки. Следует на время отказаться от крепкого чая, газированных сладких напитков, бобовых, грибов, любых полуфабрикатов, мороженого.
Лечение панкреатита: лекарства и диета
Лечение панкреатита в острой форме включает в себя и обязательную медикаментозную терапию. Одни лекарства применяются симптоматически, другие нужно будет пропить полным курсом. При приступах боли, особенно в первые дни лечения, ребенку назначаются анальгетики и спазмолитики:
Поскольку при остром панкреатите наблюдается повышенный синтез ферментов, детям назначаются антисекреторные лекарства:
Помогают улучшить состояние и антациды — лекарства, понижающие уровень соляной кислоты (альмагель, маалокс и другие). При этом важной частью терапии, когда закончена голодная диета, являются ферментативные препараты — панкреатин, креон и другие.
При этом важной частью терапии, когда закончена голодная диета, являются ферментативные препараты — панкреатин, креон и другие.
Успешное лечение панкреатита — это всегда комплексный подход. Без предварительной диагностики, а иногда и длительного стационара полное избавление от заболевания невозможно. Препараты, их дозы и продолжительность приема назначает исключительно врач. Самолечение при воспалении поджелудочной железы не просто неэффективно, но и опасно, ведь неправильно подобранные лекарства могут нанести дополнительный вред органу, а также повредить печень или почки.
«Хронические панкреатиты у детей» | Городской центр медицинской профилактики
Хронический панкреатит – прогрессирующее заболевание поджелудочной железы, характеризующееся появлением во время обострения признаков острого некротизирующего воспалительного процесса. Панкреатит составляет от 5 до 25% всей структуры заболеваний органов пищеварения у детей. В США за последние пятнадцать лет хронический панкреатит вырос с 3,6 до 13,2 случаев на 100 тысяч детского населения. В России все обстоит не так критично, хотя панкреатит не редкое заболевание у детей.
В России все обстоит не так критично, хотя панкреатит не редкое заболевание у детей.
Течение панкреатита у ребенка, в отличие от взрослого, имеет свои особенности: заболевание может вызываться широким кругом экзогенных и эндогенных факторов, протекать малосимптомно, а также маскироваться другими заболеваниями пищеварительного тракта, например, гастритом, гастродуоденитом, дисбактериозом кишечника и др. Поиск методов раннего выявления и своевременного лечения панкреатита у детей является актуальнейшей задачей педиатров и детских гастроэнтерологов.
По характеру течения панкреатит у детей может быть острым и хроническим. В зависимости от клинико-морфологических изменений поджелудочной железы выделяют острый отечный, геморрагический, гнойный панкреатит, жировой панкреонекроз.
Хронические панкреатиты у детей различаются: по происхождению -первичный и вторичный; по течению — рецидивирующий и латентный; по тяжести течения — легкая, среднетяжелая и тяжелая формы. По причинам заболевание делят на метаболический, алиментарный, идиопатический, наследственный.
Что провоцирует хронический панкреатит у детей? Чаще всего хронический панкреатит возникает по причине болезней желчевыводящей системы, из-за виру сных инфекций, аллергии, травмы поджелудочной железы, приема некоторых лекарственных средств, системных заболеваний, на фоне диабетического кетоацидоза, васкулита, болезни Крона. В группе риска находятся девушки, которые решили очень быстро и кардинально похудеть – к выпускному балу, к лету и т.д. Способствуют развитию болезни наследственные факторы, неполноценный рацион, в котором содержится слишком мало белка, нарушение обмена веществ. В 10-30% случаев этиологию заболевания установить не удается.
Симптомов хронического панкреатита у детей множество, но зачастую они бывают стерты и слабо проявлены. Для заболевания типичны такие симптомы: боли в области эпигастрия с иррадиацией в левое подреберье, поясницу, левую лопатку; боли опоясывающего характера; боли длительные и кратковременные; боли после приема жирной пищи, при нарушении режима питания. Наряду с болью возникают отвращение к жирной пище, плохой аппетит, рвота или тошнота, избыточное образование газов в кишечнике, дисфункция кишечника.
Наряду с болью возникают отвращение к жирной пище, плохой аппетит, рвота или тошнота, избыточное образование газов в кишечнике, дисфункция кишечника.
Если говорить о методах диагностики заболевания поджелудочной железы, то различают: функциональные – прямые (зондовые и беззондовые) и косвенные; морфологические. Самый доступный метод – копрограмма (лабораторное исследование на панкреатическую недостаточность). Первый выбор диагностики – УЗИ органов брюшной полости.
Что касается лечения острого панкреатита и обострения хронического, то оно должно проводиться в стационаре. Здесь назн ачают восполнение жидкости через внутривенное введение, питание через назогастральный зонд, обезболивающие средства, заместительную ферментную терапию, антибиотики назначают только при остром панкреанекрозе.
Большую роль в лечении отводят диете.
Панкреатит у детей — признаки, причины, симптомы, лечение и профилактика
Диагностика
Учитывается яркая быстронарастающая симптоматика, исследуют кровь в клинической лаборатории на трансаминазы (АЛТ, АСТ), активность ферментов – липазы, амилазы, трипсина, протеаз. Очень информативно определение эластазы в кале (менее 200 мг/г). Показано УЗИ органов ЖКТ.
Очень информативно определение эластазы в кале (менее 200 мг/г). Показано УЗИ органов ЖКТ.
Лечение
В детском гастроэнтерологическом отделении пациенту обеспечивают физический и психоэмоциональный покой. На первые 2-3 суток назначается голодная диета с жидкостным режимом из расчета 5 мл/кг массы. От степени тяжести внутривенно капельно вводятся с целью детоксикации и регидратации 5-10%-ая глюкоза, гемодез, реополиглюкин, плазма, другие белковые растворы. Выпаивают щелочной минеральной водой без газа (боржоми).
С 3-4 дня вводятся обезжиренные легкоусваиваемые продукты – каши на разведенном молоке, омлет, сок с водой, печеное яблоко. С 4-5 – цельное молоко, творог, а с 8-10 – мясной или рыбный фарш из нежирных сортов, дозировано сливочное мало, свежие фрукты. Через полтора месяца такой диеты переходят на стол №5 (паровая и нежирная пища). Придерживаются ее до 3-6 месяцев. Такая терапия бывает достаточной при реактивных панкреатитах или нетяжелом течении острого.
Необходимо также лечение сопутствующего заболевания. С деструктивной формой пациент находится в реанимационном отделении с обилием инфузионных лекарств. При гнойных осложнениях переводится в хирургическое отделение.
С деструктивной формой пациент находится в реанимационном отделении с обилием инфузионных лекарств. При гнойных осложнениях переводится в хирургическое отделение.
Профилактика
В качестве профилактических мер необходимо:
- остерегаться всех перечисленных негативных воздействий на поджелудочную железу;
- не переедать жирную и острую пищу.
- избегать травм живота (спортивная и уличная борьба у подростков), стрессов, нервных срывов;
- вовремя лечить другие проблемы ЖКТ;
- для недопущения перехода острой фазы в хроническую регулярно проходить в детской поликлинике под контролем педиатра диспансеризацию;
- проходить санаторно-курортное лечение через полгода после выписка из стационара.
Литература и источники
Видео по теме:
Клиническая Отчет Комитета по поджелудочной железе NASPGHAN
1. ПЕРВОНАЧАЛЬНАЯ ОЦЕНКА И ДИАГНОСТИКА ОСТРОГО ПЕДИАТРИЧЕСКОГО ПАНКРЕАТИТА
Недавние исследования оценивают заболеваемость острым панкреатитом (ОП) при ~ 1/10 000 детей в год (2, 7), заболеваемость приближается к взрослым. Есть нет научно обоснованных руководств по диагностике ОП у детей. ВДОХНОВЕНИЕ ( IN международный S tudy Группа компаний P медицинский P анкреатит: I n Найдите Cu RE ) определение детской AP является экспертное определение смоделировано по критериям Атланты у взрослых (8).Согласно критериям INSPPIRE, для диагностики АП требуется как минимум 2 из следующего: (1) боль в животе совместима с AP, (2) значениями сывороточной амилазы и / или липазы ≥3 раза верхние пределы нормы, (3) визуализация результаты согласуются с AP (9, 10). INSPPIRE или другие критерии не касаются этапов (ранних или поздний) АП у детей или типов (интерстициальный отечный панкреатит, некротический панкреатит, инфицированный панкреонекроз) или степень тяжести ОП (легкая, умеренная или тяжелая форма ОП при мультисистемной органной недостаточности).
Детский диагноз ОП обычно подозревается клинически с совместимым симптомом презентации, подтвержденные лабораторными и / или радиологическими исследованиями. Боль в животе и / или раздражительность являются наиболее частыми проявлениями ОП у детей, за которыми следуют эпигастральные болезненность, тошнота и рвота (11, 12). У младенцев и детей ясельного возраста симптомы могут быть незаметными; поэтому диагноз требует высокого уровня подозрений. Желчные / обструктивные факторы, лекарственные препараты и системные заболевания являются основными причинами ОП у детей (1, 4, 9, 12–23), и знание этих возможных причин поможет руководить начальными исследованиями.
Процент детей, у которых развиваются «тяжелые» острые панкреатит варьирует в опубликованных сериях (6–34), но дети с ОП в в целом имеют легкое течение (11, 24, 25). В подмножестве у пациентов АП может иметь тяжелое течение (8), но нет установленные клинические инструменты предсказывают этот результат. Балльные системы оценки степени тяжести АП у взрослых (Рэнсон, Глазго, модифицированный Глазго, Прикроватный индекс тяжести острых заболеваний). Панкреатит (BISAP) и оценка острой физиологии и хронического здоровья II (APACHE II)) не легко применимы к детям по нескольким причинам (26).Детская шкала острого панкреатита (PAPS) ДеБанто (27) была оценена у детей, но имеет низкую чувствительность. и требует 48 часов для прогнозирования рисков. Точно так же степень тяжести компьютерной томографии индекс (CTSI) или балл Бальтазара (28), опирается на радиологический внешний вид и, следовательно, нежелателен в детской возрастной группе из-за радиации экспозиция. Благодаря своей широкой доступности липаза является привлекательным маркером для выявления тяжелых случаев AP (25), но может выявить много ложных положительных из-за его низкой положительной прогностической ценности и специфичности.Коффи и др., обнаружили, что липаза сыворотки в семь раз превышает верхний предел нормы в течение 24 часов после презентация помогла предсказать тяжесть острого панкреатита (25). Тем не менее, это ретроспективное исследование с участием 211 детей и не были проверены в более крупных исследовательских группах. Suzuki и др. В Японии разработали удобная для детей система оценки степени тяжести с использованием 9 параметров (29), но это также было ретроспективным исследованием, в котором оценивались только 145 пациентов, и авторы пришли к выводу, что результаты не могут быть широко применимы к педиатрическое население.Совсем недавно Сабо и др. Сообщили, что ранняя степень тяжести прогностическая модель с использованием сывороточного альбумина, липазы и количества лейкоцитов, полученных в 24 часа продемонстрировали положительную прогностическую ценность 35% и отрицательную прогностическую ценность значение 91% (30).
Необходимы дальнейшие проспективные исследования для определения клинической применимости любой из этих инструментов. В вышеупомянутых исследованиях использовались различные определения степени тяжести. AP, что ограничивает возможности проведения сравнений между исследованиями. Недавняя публикация Комитет по поджелудочной железе NASPGHAN обратился к необходимости иметь четко определенную классификацию степени тяжести АП, предлагая определения легкой, средней и тяжелой степени АП для повысить однородность исследований (31).
Биомаркеры сыворотки
Острый панкреатит — это в первую очередь клинический диагноз, основанный на наличие как минимум двух из трех критериев, опубликованных INSPPIRE и Atlanta классификация (8, 9). Без выполнения двух из этих трех критериев трудно сделать диагностика АП. Основные биохимические маркеры, используемые для диагностики АП, включают сывороточную липазу. и сывороточная амилаза. Поскольку уровень липазы или амилазы в сыворотке не менее чем в три раза превышает верхний предел нормы считается совместимым с панкреатитом, важно знать справочные значения лаборатории для определения этого порога.И амилаза, и липаза обычно повышается на ранней стадии заболевания. Однако соотношение сыворотки уровни липазы или амилазы и тяжесть заболевания низкая (25, 32, 33). Липаза в основном секретируется поджелудочной железой, хотя другие источники липазы включают желудочные и язычные липазы. При АП липаза обычно увеличился в течение 6 часов после появления симптомов; уровень в сыворотке достигает максимума через 24–30 часов и может остаются повышенными более одной недели (34). Некоторые выступают за то, чтобы сывороточная липаза без сывороточной амилазы была достаточной для диагностики АП, поскольку липаза является более чувствительным и специфическим маркером АП (87–100% и 95–100% соответственно) (35–38).Липаза, кроме того, остается повышенным дольше, чем амилаза, что полезно в случаях отсроченного проявления (34, 39, 40). Уровни липазы также меньше изменяются этиология AP в отличие от амилазы, особенно в случае этанола (37, 41) или гиперлипидемия (42, 43). Но следует соблюдать осторожность при интерпретации уровней у детей. упражнения, поскольку было продемонстрировано, что нормальные значения липазы связаны с возрастом ребенок, растущий от новорожденного к ребенку, к взрослому (44, 45). Амилаза секретируется несколькими органами, прежде всего слюнные железы и поджелудочная железа.Большинство лабораторий измеряют общую амилазу уровни, которые содержат изоформы s-амилазы (слюна) и p-амилазы (поджелудочная железа) (46). Существуют лабораторные тесты для фракционирования p- и s-амилаза, но эта практика менее доступна. Эталонные значения амилазы отличаются в зависимости от используемого лабораторного теста, но также зависят от возраста и пола (47, 48). Сыворотка Уровни амилазы могут изменяться в зависимости от этиологии панкреатита, как указано выше. Амилаза уровни повышаются быстрее, чем уровни липазы, и часто могут нормализоваться через 24 часа после начала симптомы, ограничивающие полезность у пациентов с отсроченным обращением к врачу объект (34).Поскольку почки выводят амилазу и липазы, повышение этих ферментов не на уровне поджелудочной железы может наблюдаться у пациентов с повреждение или заболевание почек (46).
Несколько состояний, не связанных с панкреатитом, вызывают повышение уровня поджелудочной железы амилаза и / или липаза, включая декомпенсированную печеночную недостаточность, почечную недостаточность, кишечную воспаление (включая целиакию и воспалительное заболевание кишечника) брюшной полости травмы, диабетический кетоацидоз и травмы головы (49). Кроме того, некоторые люди продуцируют большие комплексы амилазы или липаза с иммуноглобулинами (так называемая макроамилаза и макролипаза), которые плохо фильтруется и выводится из-за большого размера, что приведет к повышенным значениям, если уровень фермента измеряется в крови, несмотря на то, что он не связан с воспалением поджелудочная железа (50).
Другие биомаркеры для диагностики и лечения панкреатита были предложены и изучены на животных моделях или небольших клинических испытаниях (см. обзоры в (46, 51, 52)). Однако ни один из них не получил известности, и многие еще предстоит пройти валидацию для общеклинического использования.
Несколько лабораторных тестов помогают контролировать течение АП (53). В целом электролиты сыворотки крови, мочевина крови азот (BUN) и креатинин, а также общий анализ крови (CBC) важны для мониторинга состояние жидкости / гидратации и почечная функция.Панель печеночных ферментов показана для поиска желчнокаменной или желчнокаменной этиологии, а также для оценки поражения органов. Кальций и Уровни триглицеридов следует рассматривать как исходные исследования (9). Мониторинг респираторного статуса может предупредить врача о том, что прогрессирование от легкой до среднетяжелой или тяжелой АД.
Этиология
Как упоминалось ранее, анатомическая, обструктивная (в том числе желчная), инфекционные, травматические, токсические, метаболические, системные заболевания, врожденные нарушения обмена веществ, генетическая предрасположенность и идиопатия были описаны как потенциальные этиологии при детском ОП, остром рецидивирующем панкреатите (АРП) и хроническом панкреатите (ХП) (3, 4, 54).Обзор Lowe et al суммировал 6 лучших общие этиологические категории в опубликованных обзорах как идиопатические / другие в 24%, травмы у 17%, системные заболевания у 15%, структурные аномалии в 14%, лекарства в 10% и инфекции в 8%. (3) Учитывая более частую этиологию, а также те, которые для которых существует направленная терапия, в рукописи 2012 года Morinville et al. опрос детских гастроэнтерологов, оказывающих панкреатологическую помощь, и предложили после обследования в первых случаях панкреатита: сывороточные ферменты печени, триглицериды и уровень кальция и УЗИ брюшной полости.Они предложили отложить тестирование на генетические причины / предрасположенности (которые в то время включали CFTR (муковисцидоз) регулятор трансмембранной проводимости), SPINK1 (ингибитор сериновой протеазы Kazal типа 1) и PRSS1 (катионный трипсиноген)), хлорид пота и более подробные изображения для случаев ARP, CP или первых экземпляров AP с повышенным риском рецидив, основанный на представлении, прошлой истории болезни или семейном анамнезе (9). При необходимости, поиск может быть проведен для конкретных факторы токсико-метаболического риска (55).Недавний публикация Gariepy et al, посвященная причинно-следственной оценке ARP и CP у детей, который имеет тенденцию быть более обширным из-за повторяющегося / хронического характера презентации (56) Аутоиммунный панкреатит (АИП) типов 1 и 2 редко диагностируются, но представляют разные типы панкреатита со специфическими гистологические данные в контексте суггестивных симптомов, визуализации, лабораторных исследований. результаты и ответ на терапию. Если AIP подозревается как этиология AP, в дальнейшем необходима поддерживающая оценка.Заинтересованные читатели будут перенаправлены на недавний публикация Scheers et al по педиатрической AIP (57).
Визуализация
Визуализация на ранней стадии ОП обычно не требуется, если в анамнезе / при предъявлении симптомы и биохимические маркеры сыворотки присутствуют для постановки диагноза. Визуализация становится актуально для документирования некроза поджелудочной железы, осложнений панкреатита, включая жидкость скопления и этиология панкреатита, например, камни в желчном пузыре / желчевыводящие пути или анатомические аномалии.
Золотым стандартом диагностической визуализации остается КЭКТ и несколько оценок. системы разработаны (58).Тем не мение, несмотря на то, что CETC является золотым стандартом визуализации, он часто не указывается и необходим для диагностики или лечения педиатрического AP. В неоднозначных случаях для диагностики ОП, например, при отсроченном проявлении, когда сывороточные маркеры могут быть низкими, компьютерная томография с контрастным усилением (CECT) может потребоваться для подтверждения AP. IV контраст является ключом к различению некротических участков поджелудочной железы (59). Поскольку ранняя визуализация может недооценивать степень заболевания и поскольку осложнения развиваются со временем, и результаты могут отсутствовать на ранних этапах фазе заболевания, в идеале CETC следует отложить как минимум на 96 часов после начала симптомы (8, 60).В легких случаях КЭКТ может показать усиление гомогенного органа, воспалительное изменения перипанкреатического жира или жидкости, окружающей поджелудочную железу (59) В тяжелых случаях КЭКТ может показать неоднородный орган усиление, некроз в поджелудочной железе или в окружающей перипанкреатической ткани. Кроме того, CECT может также идентифицировать скопления перипанкреатической жидкости или псевдокисты. КЭКТ следует пересмотреть при ухудшении клинического состояния пациента. или постоянно тяжелый (8). Lautz et al. нашел что индекс тяжести компьютерной томографии (шкала CTSI или Balthazar) в педиатрической пациенты дали чувствительность, специфичность, положительную прогностическую ценность и отрицательную прогностическая ценность 81%, 76%, 62% и 90%, соответственно, по степени тяжести в ретроспективном исследовании 64 детей (61).
Ультразвук широко используется в случаях, когда есть высокие подозрения на билиарный панкреатит, при котором полезно заранее определить необходимость терапевтического вмешательство (33, 58). Ультразвук имеет отличный профиль безопасности, неинвазивен и не использовать радиацию. Тем не менее, использование ультразвука может быть ограничено в оценке состояния. поджелудочной железы из-за мешающих структур, таких как кишечные газы в кишечнике и ожирение и имеет более низкую чувствительность при визуализации поджелудочной железы по сравнению с КЭКТ.
Магнитно-резонансная томография (МРТ) обычно не используется в качестве первичной визуализации техника при АП, но может быть полезна при поздних осложнениях (59). Это может быть особенно полезно для молодых или беременных. пациентам (с намерением ограничить облучение), и может разрешить использование альтернативных методов внутривенного контраста в пациенты с нарушением функции почек или аллергией на йодсодержащий контраст (60). МРТ также может быть более чувствительным при оценке некротическая ткань по сравнению с КЭКТ (59, 61). МР-холангиопанкреатография (MRCP) при AP наиболее часто используется для обнаружения камней в дистальных отделах общего желчного протока и диагностики желчных путей АП.МРТ / MRCP с использованием секретина помогает исследовать систему протоков в поджелудочной железы, а также общие аномалии желчных протоков, включая стриктуры или камни (62, 63). К оптимизировать обнаружение патологий протоков, MRCP может выполняться после атаки AP исчез, поскольку острый отек может затруднять визуализацию протоков. Использование MRCP, усиленный секретином, при заболевании поджелудочной железы у детей полностью не установлен (64) и доступ к секретину неодинаков через учреждения и страны.Lin et al подробно описывают использование МРТ и MRCP у детей. требуется визуализация поджелудочной железы, а также общие аспекты визуализации при AP (65).
Резюме и рекомендации
Рекомендация 1a: Диагностика острых заболеваний у детей панкреатит должен соответствовать ранее опубликованным критериям INSPPIRE.
Для диагностики ОП у педиатрических пациентов необходимы как минимум 2 из следующего: (1) боль в животе, совместимая с AP, (2) уровни амилазы и / или липазы в сыворотке ≥3 раза верхние пределы нормы, (3) результаты визуализации в соответствии с AP.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1b: Возможно выполнение первичной визуализации. с помощью трансабдоминального ультразвукового исследования, с другими методами визуализации (КТ, МРТ), зарезервированными для большего сложные случаи +/– с учетом подозреваемой этиологии.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 4; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1c: Основана на наиболее частой этиологии и те, для которых существуют варианты лечения, первый приступ острого панкреатита тестирование должно включать ферменты печени (АЛТ, АСТ, ГГТ, ЩФ, билирубин), триглицериды уровень и уровень кальция.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2. СООБРАЖЕНИЯ ВЕДЕНИЯ ПРИ ОСТРЫХ ПЕДИАТРИЧЕСКИХ ПАНКРЕАТИТАХ
2a.Инфузионная терапия при остром панкреатите
Внутривенная инфузионная терапия является основой лечения во время эпизода AP. Жидкая реанимация поддерживает адекватный жидкостный статус и диурез, но в последнее время внимание было сосредоточено на использовании внутривенных жидкостей для предотвращения потенциальных осложнений при ОП, такие как некроз и органная недостаточность. Патогенез ОП и прогрессирование до тяжелой степени. считается вторичным по отношению к нарушению микроциркуляции поджелудочной железы событиями, включая гиповолемию, повышенную проницаемость капилляров и образование микротромбы.Считается, что жидкостная реанимация не только устраняет гиповолемию, но и помогает сохранить микроциркуляцию поджелудочной железы, обеспечивая адекватную перфузию и предотвращая возможное образование микротромбов и, таким образом, предотвращение осложнений и прогрессирования тяжелое заболевание (66).
Тип жидкости
Отсутствует консенсус относительно идеального количества и типа жидкости для использования во время эпизода ОП во взрослой практике, и существует еще меньше данных, относящихся к жидкости в педиатрической популяции. Кристаллоид был наиболее рекомендуемым типом жидкость в руководствах для взрослых (33, 67–70).А Основное преимущество кристаллоидов в том, что они легко и быстро доступны. Обычный физиологический раствор (NS) долгое время был предпочтительным кристаллоидом для начальной жидкостной реанимации в в целом, но в некоторой литературе для взрослых предполагается, что лактатные звонаги (LR) являются более оптимальными для AP. В небольшом рандомизированном контрольном исследовании (РКИ) с участием 40 взрослых с AP Wu et al. что LR снижает частоту синдрома системного воспалительного ответа (SIRS) и уровни С-реактивного белка через 24 часа по сравнению с NS (71). Напротив, ретроспективный обзор 103 пациентов не смогли показать какой-либо существенной разницы между LR и NS в качестве начального реанимационная жидкость у взрослых с панкреатитом различной степени тяжести (72).LR был рекомендован по сравнению с NS в Международном Рекомендации Ассоциации панкреатологов / Американской панкреатической ассоциации (IAP / APA), но в рекомендациях Американской гастроэнтерологической ассоциации (AGA) только говорится, что LR может быть лучший выбор, но не был сильной рекомендацией (68, 70). В педиатрии это было показали, что агрессивное введение жидкости в течение первых 24 часов с помощью физиологического раствора с 5% декстрозой является безопасным и хорошо переносимым вариантом (73), но его не сравнивали с другими типами жидкостей для внутривенного вливания. (например, LR).
Коллоиды (например, альбумин, свежезамороженная плазма или упакованные эритроциты) не рекомендованы в качестве начальной реанимационной жидкости при АП. Коллоидные компоненты оставаться во внутрисосудистом пространстве из-за большего размера и может втягивать жидкость в кровообращение из интерстиция вторично по отношению к осмотическому эффекту. Руководящие принципы AGA рекомендует коллоид в определенных ситуациях, когда гематокрит < 25% альбумина составляет <2 г / дл (68), при этом другая публикация рекомендует соотношение кристаллоидов и кристаллоидов 3: 1. коллоид (74).
Скорость введения жидкости
Агрессивность жидкостной реанимации при АП также обсуждалась. В время вмешательства агрессивной жидкостной терапии может быть ключевым. Учеба взрослых в пользу ранних и агрессивных жидкостей в AP включают несколько ретроспективных исследований, которые использовали разные стратегии, такие как предоставление> против <33% от общего количества жидкости в течение первых 24 часов, а другой обеспечивает 3,5 л по сравнению с 2,4 л внутривенно в течение первых 24 часов (75). В основном, те, кто получает более агрессивные объемы жидкости внутривенно в течение первых 24 часов, как правило, улучшили результаты, включая смертность, но даже в рамках различных исследований результаты противоречивы в отношении того, снижает ли более высокое раннее введение жидкости некроз, синдром системного воспалительного ответа (SIRS) и продолжительность пребывания в стационаре (76).Напротив, Mao et al. Сообщили о РКИ 76 пациентам с тяжелым АП назначена медленная гемодилюция (5–10 мл / кг / ч) или быстрая гемодилюция (10–15 мл / кг / ч), демонстрирующая, что быстрая агрессивная ранняя жидкость введение привело к более высоким показателям сепсиса и смертности (77). de-Madaria et al провели проспективное исследование 247 человек. пациенты делятся на пациентов в зависимости от количества жидкости, введенной в первые 24 периода. часы. Группа, получавшая наибольший объем,> 4,1 л, имела повышенный уровень стойкая органная недостаточность (78).Weitz и др., рассмотрели 391 случай АП и обнаружили, что использование агрессивных жидкостей (примерно 5 л) было неэффективным. связаны с обострением заболевания и местными осложнениями (79). Опасения по поводу этой последней группы исследований заключаются в том, что в основном они касались более больных пациентов, и жидкостные режимы не ограничивались первые 24 часа реанимации.
Несколько экспертов и групп с тех пор дали рекомендации по скорости жидкостная реанимация в первые 24–48 часов у взрослых с ОП.МАП / АПА руководящие принципы рекомендуют пациентам получать 5–10 мл / кг / час до реанимации. цели достигаются в отношении улучшения частоты сердечных сокращений, диуреза, среднего артериальное давление и / или гематокрит (70). В Американский колледж гастроэнтерологии (ACG) рекомендует начальную скорость 250–500 мл / час, в дополнение к болюсу жидкости, если гипотензия или тахикардия присутствуют и используют BUN для направления терапии (33). Подобные рекомендации сделаны в обзоре Whitcomb et al (80). Aggarwal et al. советует 3–4 л жидкости в первые 24 часа (не более 4 л) с начальным болюсом 1 л и последующие 3 мл / кг / час в течение первых 24–48 часов (81).Наср и др. первоначально рекомендуют болюсы 1–2 л и 150–300 мл / час (82). Впоследствии они рекомендуют 2 мл / кг / час, если пациент отвечает на первоначальную реанимацию, но в противном случае использовать 3 мл / кг / час (82).
Только в одном педиатрическом исследовании оценивались разные нормы поддерживающей жидкости. администрации с участием 201 пациента с ОП [69]. Это исследование показало, что сочетание ранних энтеральное питание (<48 часов) и агрессивные жидкости (> 1,5–2x техническое обслуживание в первые 24 часа) уменьшилась продолжительность пребывания и возникновение тяжелое заболевание по сравнению с более традиционным историческим лечением.Агрессивные внутривенные жидкости не повлияли отрицательно на исходы (в первую очередь, легочные осложнения или повторная госпитализация). ставки). Никакие исследования не указывают идеальную норму поддерживающих жидкостей в AP после начальная реанимация (> 24–48 часов), хотя Сабо и др. что 1,5–2-кратное поддержание было безопасным для их популяции пациентов (73). Нет педиатрических исследований, сравнивающих первоначальную реанимацию тома.
Резюме: В начальной фазе реанимации острого панкреатит, теоретические и потенциальные клинические преимущества в пользу LR выше NS на основе данные о взрослых, но отсутствуют педиатрические данные.
Рекомендация 2ai: Дети с острым панкреатит необходимо первоначально реанимировать кристаллоидами, либо с LR, либо с NS в острой постановке. На основании оценки статуса гидратации / гемодинамического статуса, если при наличии гемодинамических нарушений рекомендуется болюсное введение 10–20 мл / кг.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Резюме: Педиатрическая литература жидкостная реанимация и скорость введения жидкости при остром панкреатите.Взрослый литература предлагает болюсы 250–1000 мл на начальном этапе и до 3–4 л. жидкости в течение первых 24 часов.
Рекомендация 2aii: Дети с диагнозом острой панкреатит следует назначать 1,5–2-кратное поддерживающее внутривенное введение жидкостей с мониторингом диуреза в течение следующих 24–48 часов.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 12; согласен = 10; нейтральный = 2; не согласен = 0; категорически не согласен = 0.
2b. Мониторинг детей с диагнозом ОП / внепанкреатические проявления острый панкреатит
Хотя это еще не изучено у педиатрических пациентов, полиорганная болезнь у взрослых пациенты с ОП связаны с худшими клиническими исходами с более чем половиной случаев, связанных с ОП. смерть в течение 1 недели от начала полиорганной дисфункции (83).Поражение сердца, легких и почек является ключевым фактором. компоненты систем оценки взрослых, используемых для прогнозирования тяжести эпизода ОП, включая модифицированная атлантская классификация, критерии Рэнсона, степень серьезности по Японии Оценка, оценка по Глазго, BISAP и APACHE II (8, 84–87). Педиатрические модели, прогнозирующие тяжесть ОП, также придают большое значение вовлечению нескольких органов, но оказались менее надежными (88) или еще не прошли проспективную валидацию (29). Повышенный эндотелиальный барьер проницаемость и глубокий выброс цитокинов, связанные с ССВО в сочетании с агрессивным гидратация теоретически увеличивает риск пациента для жидкости третьего промежутка и развитие внепанкреатических проявлений АП.Надлежащий мониторинг жизненно важен для сбалансировать соответствующую жидкостную реанимацию, пытаясь предотвратить сердечную, легочную и почечные осложнения (89).
Сердечно-сосудистый мониторинг
Гиповолемия при поступлении является надежным предиктором заболеваемости и смертности среди взрослых с AP и, по-видимому, коррелирует с величиной SIRS (89). Тахикардия использовалась как при системы оценки взрослых и детей для прогнозирования тяжести ОП и ее улучшение использовались для подтверждения адекватной реанимации жидкости в дополнение к мониторингу мочи объем и тургор кожи (71, 81).Регулярный кардиологический мониторинг взрослых у пациентов, не получающих ОИТ включает регулярные измерения жизненно важных функций каждые 8 часов для получения информации о состоянии сердечно-сосудистой системы (71). Дополнительно редкие случаи тампонады сердца и предсердий. Сообщалось о фибрилляции при АП, и ее следует учитывать при стандартном кардиологическом исследовании. обследование начато у пациентов с необъяснимой гипотонией, одышкой и / или боль в груди (90–93).
Мониторинг легких
Исследования на взрослых и животных модели показывают острый респираторный дистресс синдром (ОРДС), пневмония и отек / выпот легких как ранние осложнения ОП, обычно в течение первых 48 часов (15, 94).Поскольку ОРДС является наиболее распространенным критическим осложнение тяжелого АП, связанного с полиорганной дисфункцией у взрослых (95), аномальное P a O 2 или аномальные изображения легких являются компонентами всех обычно используемых систем оценки для предсказать тяжесть приступа ОП (8, 29, 84–87). Регулярный мониторинг насыщение кислородом во время агрессивной гидратации обычно осуществляется, с некоторыми койки пациентов должны быть подняты на угол 30 градусов, чтобы снизить вероятность легочная секвестрация (71).Стандарт следует рассмотреть возможность обследования легких и ухода за пациентами с необъяснимыми одышка, ухудшение кашля и / или затрудненное дыхание (94).
Мониторинг почек
Острое повреждение почек (ОПП) через синдром брюшной полости (83, 96) или вызванное воспалением повреждение проксимального извитого канальца (97), отмеченное повышением уровня азота мочевины и креатинина, а также снижение диуреза, это известное раннее осложнение АП у детей и факторы занимает важное место в оценочных системах AP для прогнозирования тяжести заболевания (8, 15, 29, 84–87).В некоторых исследованиях на взрослых было показано, что только мочевины быть столь же эффективным в прогнозировании тяжести заболевания, как и более продвинутые системы оценки (98) и AKI был связан с В 10 раз повышен риск смерти при тяжелом ОП (99). Таким образом, BUN и креатинин считаются важными маркерами для следить за проведением инфузии и контролировать ОПП у взрослых во время первого 48 часов и при агрессивном увлажнении (71, 81, 98). Хотя нет никаких руководств, документирующих частоту мониторинга этих параметров, 8–12 часов использовались в одном исследовании для определения реакции на управление жидкостями (71).Рекомендации ACG подчеркивают важность снижения АМК и поддержания нормального уровня креатинина в первые 24 часа, поэтому очень важен ранний мониторинг (33). В редких случаях требуется непрерывная вено-венозная гемофильтрация (CVVH). для предотвращения дальнейшего повреждения почек, предотвращения синдрома брюшной полости и / или removae воспалительных цитокинов, но его использование не изучалось у педиатрических пациентов с AP (100). Может понадобиться установить мочевой катетер для точного документирования диуреза, особенно при седативном ребенок в условиях отделения интенсивной терапии.
Резюме и рекомендации
Наблюдение за пациентами с острым панкреатитом может дать индикаторы возникающие осложнения, включая ССВО и органную дисфункцию / недостаточность. Сердечный, следует особенно внимательно следить за респираторным и почечным статусом в течение первого Через 48 часов после обращения, так как большинство осложнений начинается в течение этого периода. период времени. Диурез — важный маркер адекватной жидкостной реанимации, при этом литература для взрослых, предлагающая стремиться к достижению> 0.5–1 куб. См / кг / час (Руководство IAP / APA).
Рекомендация 2bii: Пациентам, поступившим в в стационарном отделении необходимо измерять жизненно важные показатели не реже, чем каждые 4 часа в течение первых 48 дней. часы приема и в периоды агрессивной гидратации для контроля кислорода сатурация, артериальное давление и частота дыхания. Частота регулируется в зависимости от клинический статус. Нарушения жизненно важных функций должны требовать обследования у специалиста.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2biii: АМК, креатинин и моча производительность следует регулярно контролировать в течение первых 48 часов как маркер соответствующее ведение жидкости и скрининг на острое повреждение почек. Аномалии должен вызвать нефрологическое обследование.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 4; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
2с. Обезболивание при остром панкреатите
Боль в животе является наиболее частым симптомом ОП.В педиатрической АП исследования, от 80% до 95% пациентов жаловались на боль в животе. Пациенты присутствует с болью в эпигастрии у 62-89% и диффузно у 12% до 20%. «Классическое» проявление иррадиации боли в эпигастрии. к спине встречается только у 1,6–5,6% педиатрических пациентов (15, 16).
Патофизиология ОП характеризуется потерей внутриклеточных и внеклеточная компартментализация, которая может быть результатом различных механизмов: обструкция секреторного транспорта поджелудочной железы; активация ферментов; или неспособность остановить каскад активации.АП встречается у генетически предрасположенных лиц, у которых воспалительная реакция вызывает панкреатит. Это, в свою очередь, стимулирует внутреннюю панкреатические и соматические болевые рецепторы брюшины (101). Другие постулируемые механизмы, вызывающие боль в переднем отделе позвоночника, включают высокое давление. внутри железы или протока поджелудочной железы с последующей ишемией железы. Боль в AP тоже бывает вероятно, связано с высвобождением тахикинина, вещества P и кальцитонина, связанного с геном. пептид. Факторы, которые стимулируют первичные сенсорные нейроны, включают ионы водорода, тепло, лейкотриены, метаболиты арахидоновой кислоты, брадикинины и протеазы, такие как трипсин, выпущен во время AP (102).
Обезболивание — важная терапевтическая цель при лечении ОП и обычно включает использование анальгетиков периферического и центрального действия. Нет данных опубликованы по оптимальному обезболиванию в педиатрической AP, а исследования у взрослых не определили одно лучшее лекарство (67).
Опиоидные анальгетики
Потому что классические анальгетики периферического действия (такие как ацетаминофен) часто недостаточны при тяжелом панкреатите, часто требуются опиаты для контроля боль.Морфин или родственные ему опиоиды употребляли 94% респондентов для вести детей с ОП в соответствии с анкетой для врачей INSPPIRE 2012 года (103). Сообщалось, что морфин вызывает дисфункция сфинктера Одди после системного введения (104). Однако нет четких доказательств, подтверждающих эту теорию, и морфин можно безопасно применять у пациентов с ОП (105). Меперидин применялся у взрослых с АП, но его недостатки включают: короткий период полураспада и потенциал нейротоксичности за счет накопления токсичных веществ. нейрометаболиты, которые могут приводить к судорогам, миоклонусу и тремору (106).Обзор наркотиков и функции сфинктера Одди. Thomson et al, документально подтверждают, что на сегодняшний день нет исследований, напрямую сравнивающих эффекты меперидин и морфин на сфинктере манометрии Одди и никаких сравнительных исследований существуют у пациентов с АП. Кроме того, не существует исследований или доказательств, указывающих на то, что морфин противопоказан к применению при ОП (107). Кокрановский обзор 2013 года включает 5 исследований, в общей сложности 227 Субъекты для оценки эффективности и безопасности нескольких опиоидов. Включенные лекарства были бупренорфин, петидин, пентазоцин, фентанил и морфин.Общий вывод состоит в том, что опиоиды могут быть подходящим выбором при лечении боли. связанных с AP, и они могут уменьшить потребность в дополнительной анальгезии. Кроме того, риск осложнений, связанных с панкреатитом, или клинически серьезных побочные эффекты не отличаются от опиоидов и других анальгетиков (108).
Опиоидсберегающие анальгетики
Предполагается, что НПВП являются потенциальными участниками развитие AP, но также показали преимущества при лечении боли в AP.Профилактическое Было показано, что НПВП, включая индометацин и диклофенак, полезны при нескольких исследования по профилактике панкреатита после ЭРХПГ (109, 110). Что касается боли После постановки диагноза АР индометацин превосходит плацебо и не показали повышенного риска желудочно-кишечного кровотечения в небольшом исследовании (111). По сравнению с морфином метамизол показал улучшение снятие боли через 24 часа, но разница не достигла статистической значимости (105).
Системное введение местных анестетиков, в основном новокаина, было выступает в качестве основного обезболивающего при АП.Предлагается внутривенное введение новокаина для уменьшения боли. и / или необходимость вспомогательных обезболивающих и, возможно, улучшения клиническое течение АП. В одном контролируемом исследовании системное введение новокаина в улучшение панкреатита и ускоренное послеоперационное восстановление после обширного абдоминального хирургическое вмешательство, включая уменьшение боли, улучшение когнитивных функций и сокращение длительность кишечной непроходимости, а также общая госпитализация (112). Но доказательства ограничены, а плацебо-контролируемые исследования отсутствуют. данные.
Эпидуральная анестезия (ЭА) широко используется для индукции обезболивания в в периоперационный период, а также для уменьшения боли у пациентов с ОП. В принцип действия был приписан блокаде симпатического нерва, который перераспределяет внутренний кровоток к неперфузируемым областям поджелудочной железы. В исследовании с участием 35 пациентов с прогнозируемым тяжелым ОП, ЭА значительно уменьшала болевые ощущения, улучшала перфузия поджелудочной железы на основе радиологических исследований перфузии и улучшения клинических исходы (снижение потребности в некрэктомии) (113).Проспективное исследование 121 пациента продемонстрировало хорошую эффективность. и безопасность EA у взрослых AP (114).
Резюме: Нет данных, обеспечивающих оптимальную боль управление в педиатрической АП. Исследования на взрослых не выявили ни одного превосходящего медикамент. Нет доказательств, подтверждающих утверждение, что морфин вызывает неблагоприятные события на сфинктере Одди.
Рекомендации 2ci: Внутривенный морфин или другой препарат опиоид следует использовать при острой боли при панкреатите, не реагирующей на ацетаминофен или НПВП.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 2cii: Услуги специалиста по острой боли в идеале следует проконсультироваться в случаях более сильной боли, чтобы уменьшить боль управление.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2d. Энтеральное и парентеральное питание при остром панкреатите у детей
Пероральное и энтеральное питание
Традиционно пациенты с ОП лечились, не вводя перорально (115) и давая парентеральное питание (PN) (116).Было высказано предположение, что отдыхая кишечник, поджелудочной железе дали «отдохнуть» и, таким образом, зажить быстрее. В Обоснованием этой теории было то, что наличие пищи в кишечнике стимулируют высвобождение холецистокинина (ХЦК), что, в свою очередь, стимулирует поджелудочную железу. секреция ферментов, что может привести к дальнейшей активации протеолитических ферментов и преувеличивают процесс самопереваривания и усугубляют травму (117, 118)
У взрослых проводится ряд контролируемых исследований, обзоров и метаанализов. лечебному питанию как при тяжелом, так и при легком ОП, включая обзор голландских Группа по изучению панкреатита и согласованные рекомендации, опубликованные Международный комитет по руководящим принципам консенсуса (119).Lodewijkx et al., Считают, что энтеральное питание превосходит парентеральное питание, а стратегия кормления по требованию в прогнозируемой тяжелый АП (120). Мирталло и др. Рассмотрели 8 социальные отчеты с целью разработки международных согласованных руководящих принципов по питанию терапия в АП (119). Они пришли к выводу, что в АП у взрослых, энтеральное питание (ЭП) было предпочтительнее, чем ПП, и его следует использовать в первую очередь даже при наличие свищей, асцита и псевдокист.
Рекомендуется начинать EN как можно раньше, тем более, что одна из целей энтеропатии — предотвратить бактериальную транслокацию и тем самым предотвратить развитие ССВО.Ранняя нутритивная терапия также предназначена для снизить цитокиновый ответ и частоту пареза желудка и кишечной непроходимости. В то время как некоторые исследования (121) не показывают разницы в исходы, когда ЭП была начата до или после 72 часов презентации, 2008 г. метаанализ, изучавший одиннадцать РКИ, показал, что ЭП началась в течение 48 часов после презентация значительно снизила показатели смертности, инфекций и полиорганной отказ по сравнению с PN (122). Эти эффекты были уменьшены, когда ЭП была начата через 48 часов.В обзоре питания за 2011 г. поддержка взрослых AP, был сделан вывод, что ранняя нутритивная поддержка, особенно ЭП, но также и ПП, уменьшали количество осложнений и улучшали выживаемость (123). В этом обзоре говорилось, что для его эффективности нутритивная поддержка должна была начаться в течение 72 часов. Было заявлено, что EN следует считается « активным терапевтическим вмешательством, улучшающим исход больных панкреатитом »(124).
Клинические исследования, сравнивающие результаты PN и EN у пациентов с AP сообщить, что использование EN при тяжелом остром панкреатите (SAP) или прогнозируемые результаты SAP значительно снижает частоту осложнений (125–133).Недавний метаанализ продемонстрировал превосходство ЭП по сравнению с ПП с меньшей частотой инфекции и полиорганной недостаточности, что приводит к снижению показателей смертности и сокращению пребывание в больнице (134). Однако, поскольку полный EN не всегда возможно во время AP из-за усиления боли или непереносимости кормления, некоторые отстаивают роль комбинации EN и PN. В одном исследовании рандомизировали 100 пациентов для получения только ПП по сравнению с ПП в комбинации только с ЭП или ЭП, сепсис, внутрибрюшная инфекция и продолжительность госпитализации снизились, когда ЭП была входит в состав руководства (135).
Описанные пути ЭП включали желудочный и тощей кишки. Два маленьких исследования не обнаружили разницы в результатах между назогастральным (НГ) и назоеюнальным (НД) сытые группы (136, 137). Мета-анализ 10 РКИ не показал различий в исходы между группами, получавшими (полу) элементарные и полимерные формулы. (138)
Никаких руководств по нутриционной поддержке дети с АП. Недавнее исследование Abu-El-Haija et al. продемонстрировал выполнимость установления энтерального питания в педиатрической АП, не усложняя курс или влияя на оценку боли AP (139).Из того же центра ретроспективное исследование показало, что сочетание раннего энтерального кормления плюс более чем 1,5-кратное поддерживающее внутривенное введение жидкости были связаны с более коротким продолжительность пребывания и более легкое заболевание по сравнению с теми, кто оставался НКО в течение 48 часов и имели более низкую частоту ЭКО, чем поддерживающую терапию (73). Сообщается о двух детях с тяжелым ОП, которые успешно вылечились. с назоеюнальным кормлением в отделении интенсивной терапии интенсивной терапии и переключением на пероральное кормление при выписке в общая палата (140).
Парентеральное питание
Родительское питание обеспечивает организм необходимыми калориями и питательными веществами. компенсировать катаболическое состояние.Обеспокоенность, что ПП может стимулировать поджелудочную железу. и приводить к преувеличению процесса самопищеварения не было подтверждено литература (141, 142). Данные показывают, что настой протеина не стимулируют секрецию поджелудочной железы (143). Когда при сравнении различных форм ПП, сообщалось, что ПП, усиленный глутамином, снизить общую частоту осложнений, а также сократить продолжительность пребывания в стационаре (144–148). Введение глюкозы внутривенно также не стимулирует секреция поджелудочной железы (149, 150).Инфузия глюкозы тяжелобольным пациентам может быть полезно для обеспечения легкодоступного источника энергии во время катаболического состояния и противодействуют глюконеогенезу из-за распада белка. Но настой глюкозы обязательно под наблюдением, так как это может предрасполагать к гипергликемии (151), поскольку воспаленная поджелудочная железа может не подавать соответствующий инсулин отклик.
Гипертриглицеридемия связана с тяжелым ОП (152–155), но механизм, ведущий к SAP, не ясен (156). Недостаточно данных, чтобы рекомендовать или препятствовать использованию парентеральные липиды при АП.
Что касается времени PN в AP, где измеренный результат был смертности, данные свидетельствуют о том, что раннее ПП значительно более полезно, чем покой кишечника. при тяжелом ОП у взрослых (122). Во всех случаях, когда ЭП невозможна в течение длительного времени, например, при кишечной непроходимости, сложных свищах и т. Д. синдром брюшного отдела, PN. Напротив, недавнее исследование выступал за отсрочку начала ПП до 7 дней у тяжелобольных детей из-за повышенный риск инфицирования и повышенная частота осложнений после начала ПП в течение первых 24 часов после пребывания в отделении интенсивной терапии.Раннее энтеральное питание было разрешено в обоих группы. Однако присутствие или процент пациентов с ОП конкретно не было указано в этом отчете (157).
Резюме: Литература для взрослых поддерживает раннее энтеральное питание, чтобы уменьшить осложнения AP и улучшить выживаемость. Педиатрическая литература поддерживает раннее энтеральное питание в легких случаях ОП и небольшое сообщение в тяжелых случаях AP.
Рекомендация 2di: За исключением наличия прямого противопоказания к употреблению кишечника, детям с острым панкреатитом легкой степени может помочь от раннего (в течение 48–72 часов после обращения) орального / энтерального питания до уменьшения продолжительность пребывания и снижение риска органной дисфункции.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2dii: Парентеральное питание (ПП) должно следует рассматривать в тех случаях, когда ЭП невозможна в течение длительного периода времени (дольше более 5-7 дней), например, в кишечной непроходимости, сложных свищах, брюшной полости синдром, снижающий катаболическое состояние организма. Следует начать энтеральное питание. как можно скорее, причем комбинация EN и PN превосходит одиночную PN.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15 согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2diii: В случае панкреатической разрыв, перелом или разрыв протока, неясно, является ли пероральное / энтеральное питание может быть вредным в острой фазе. Это требует дальнейшего изучения.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 13; согласен = 8; нейтральный = 2; не согласен = 0; категорически не согласен = 0; нет голоса = 1.
2д. Использование антибиотиков при остром панкреатите у детей
Обоснование использования антибиотиков при лечении ОП связано к беспокойству по поводу бактериальной инфекции из-за перемещенной кишечной микробиоты. Антибиотики не рекомендуются для взрослых с легким ОП (70).
При лечении тяжелого ОП у взрослых изучались антибиотики для предотвращения и управлять инфекциями. Имипенем и / или цефалоспорины третьего поколения были наиболее исторически часто использовались в попытке снизить заболеваемость и смертность.Этот Профилактический подход является спорным: предыдущие исследования предполагали пользу (158–160), в то время как другие исследования не продемонстрировали пользы от рутинного использования (161) в отсутствие документально подтвержденной инфекции. Профилактические антибиотики использовались в условиях стерильной некротической болезни. панкреатит для предотвращения инфицированного некротического панкреатита (162, 163), особенно имипенем (163). Однако систематические обзоры не поддерживает преимущества в отношении смертности от инфекций, не затрагивающих поджелудочную железу, или для сокращения хирургических вмешательств у взрослых (162).Более поздние метаанализы подтверждают использование антибиотиков для инфицированы некротическим панкреатитом, но не для стерильный некроз (164–166). Текущий взрослый AP рекомендации — использовать антибиотики только при инфицированном некрозе или у пациентов с некротический панкреатит, госпитализированные и без клинического улучшения использование антибиотиков (70). Зараженный некроз должен быть подозревается, если клиническое состояние пациента ухудшается из-за лихорадки или наличие газа в коллекциях на снимках.В определенных ситуациях стремление жидкость под контролем эндоскопии или с помощью интервенционной радиологии и для руководства лечением может потребоваться создание соответствующего дренажа (8). При некротическом панкреатите известные антибиотики: проникают в некротические ткани, такие как карбапенемы, хинолоны и метронидазол, поскольку использование антибиотика в этих условиях, как было показано, задерживает хирургическое вмешательство. вмешательства и снизить заболеваемость и смертность (33).
Документированные инфекции, происходящие за пределами поджелудочной железы, следует рассматривать как указано.
Не было опубликовано исследований по использованию антибиотиков для лечения АП у детей.
Резюме: Антибиотики нельзя использовать в лечение ОП, за исключением случаев документально подтвержденного инфицированного некроза или у пациентов с некротическим панкреатитом, которые госпитализированы и клинически не улучшаются без использование антибиотиков. Антибиотики, о которых известно, что они проникают в некротические ткани, следует использовать при лечение инфицированного панкреонекроза, поскольку это может отсрочить хирургическое вмешательство и снизить заболеваемость и смертность.
Рекомендации 2ei: Профилактические антибиотики не эмпирически рекомендуется при тяжелом остром панкреатите.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
Рекомендация 2eii: показано только использование антибиотиков. в случаях документально подтвержденного инфицированного некроза при остром панкреатите.
16/24 = 67% согласны с рекомендацией. Рекомендация не поддерживается.Это было определено как область особых разногласий, требующих дальнейшего учиться.
Результаты голосования: Полностью согласен = 10; согласен = 6; нейтральный = 2; не согласен = 4; категорически не согласен = 0; нет голоса = 2.
2f. Использование ингибиторов протеазы при остром панкреатите у детей
Поскольку AP предположительно является некровоспалительным процессом, начавшимся через острая и несоответствующая активация трипсина протеазы и зимогенов поджелудочной железы внутри паренхимы, исследователи были очень заинтересованы в блокировании этого воспалительный процесс, чтобы ограничить степень травмы.
Два основных соединения, описанных в литературе для ингибирования этого фермента активация включает ингибитор сериновой протеазы габексат мезилат и трипсин ингибитор апротинин. В 1993 году Pederzoli et al. сообщил результаты рандомизированного, двойное слепое многоцентровое клиническое исследование использования габексата мезилата по сравнению с апротинином в АП-терапия. В этом исследовании мезилат габексата оказался более предпочтительным по сравнению с апротинином в отношении период 24–72 часа, но, что важно, отсутствует контрольная группа плацебо (167).Сроки лечения и способ родоразрешения кажутся быть ключевыми факторами эффективности (167, 168). Ино и др. изучили эффективность непрерывного инфузия регионарной артерии CRAI с габексатом мезилатом и антибиотиками при тяжелом ОП через небольшое проспективное исследование с участием 9 пациентов, получавших CRAI в течение 3-5 дней и 9 пациентов. другие получают терапию системными ингибиторами протеазы и антибиотики. Боль в животе и SIRS исчезал быстрее, LOS был значительно короче в группе CRAI (168). CRAI антипротеаз и антибиотиков имеет Сообщалось о снижении показателей CRP и APACHE II при применении в течение 72 часов после начала болезни (169), подход, описанный в педиатрических больных (170).
Обзор 2007 года, проведенный Китагавой и Хаякавой, не нашел доказательств, оправдывающих рутинное использование антипротеаз при AP, и хотя использование непрерывного внутривенного ингибиторы протеазы и антибиотики в высоких дозах могут быть эффективными для предотвращения обострения тяжелого ОП, необходимы исследования экономической эффективности. Важно, эти соединения не одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США. Штаты (171–173).
Резюме: Некоторые исследования взрослых подтверждают использование антипротеаз в лечении тяжелого АП, но никаких конкретных рекомендаций никогда не было были сделаны для их использования.Исследования не были рандомизированы с контрольными группами плацебо, и только несколько случаи описаны в педиатрических больных.
Рекомендации 2f: Антипротеазы не могут быть рекомендуется при лечении острого панкреатита у детей в это время.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 7; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2г. Использование антиоксидантов при остром панкреатите у детей
Окислительный стресс способствует повреждению ОП из-за образования кислорода свободные радикалы, вызывающие повреждение липидной мембраны клетки поджелудочной железы, деполяризацию митохондриальной мембраны и индукции фрагментации ДНК (174).Это способствует отеку, возникновению боли и может также быть вовлеченными в процесс некроза. Таким образом, была выдвинута гипотеза об антиоксидантах. иметь потенциальную пользу в качестве дополнительного лечения при АП, предотвращая образование свободные радикалы или улавливание существующих свободных радикалов кислорода.
Наиболее изученными агентами были витамины-антиоксиданты (аскорбиновая кислота, α-токоферол, β-каротин), неорганические антиоксиданты (селен) и глютамин. В двух частично совпадающих метаанализах, опубликованных в 2015 г., используются разные методологии оценки пользы антиоксидантов при остром панкреатите, один обзор 11 и другие 12 рандомизированных контролируемых исследований на взрослых [169, 170].Pederzoli et al. Обнаружили, что антиоксиданты снижают количество осложнений, связанных с ОП, и укороченный LOS с глутамином, снижающим частоту осложнений и смертность [169]. Ино и др. Сообщили, что антиоксидант терапия сокращает LOS и снижает уровень СРБ в сыворотке, но только через 10 дней [170].
Существенным ограничением опубликованных данных об антиоксидантах у взрослых AP является эти испытания включали весь спектр легкого и тяжелого АД. Кроме того, различные комбинации антиоксидантов и время доставки были использованы в испытания.В крупных рандомизированных исследованиях также отсутствует стандартизация конкретных антиоксидантов. как сроки и продолжительность лечения.
Нет данных об использовании антиоксидантов при AP в педиатрической популяции.
Резюме: педиатрические данные об использовании не хватает антиоксидантов в АП. Публикации для взрослых демонстрируют значительную неоднородность относительно состава, времени и продолжительности терапии. Несмотря на потенциальные преимущества описанных в сериях для взрослых, доказательств недостаточно, чтобы поддержать их использование в педиатрия в это время.
Рекомендация 2g: Антиоксиданты не следует считается стандартной терапией при лечении острого панкреатита у детей.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
2ч. Роль пробиотиков в лечении острого панкреатита у детей
Примерно у трети взрослых пациентов может развиться тяжелая форма АП, характеризующаяся ССВО, органная недостаточность и повышенный риск инфицирования (175).У пациентов с инфицированным перипанкреатическим и панкреонекрозом риск летального исхода значительно увеличивается. Снижение проницаемости кишечника и Предполагается, что избыточный бактериальный рост во время AP снижает риск инфицирования некроз поджелудочной железы и тем самым снизить риск смерти (176, 177).
Всемирная организация здравоохранения определяет пробиотики как «живые микробы. которые при введении в адекватных количествах приносят пользу их здоровью. хозяин». Доказано, что пробиотики играют роль в поддержании микрофлоры кишечника. баланс, подавляя рост вредных бактерий и усиливая иммунную функцию (178).Важно, что опубликованные исследования использовали различные составы и режимы дозирования пробиотических бактерий.
Muftuoglu et al. продемонстрировали, что lactobacillus acidophilus и bifidobacterium lactis уменьшают тяжесть гистологического повреждения в экспериментальной модели панкреатита (178). Ранние небольшие клинические испытания для взрослых показали положительную роль пробиотиков в управление АП. Olah et al. рандомизировали 45 пациентов для приема 10 9 живые или убитые теплом lactobacillus plantarum два раза в день вместе с энтеральное питание (179).Они обнаружили статистически значительно более низкий риск инфицированного панкреонекроза в исследуемой группе по сравнению с контрольные группы.
Однако впоследствии исследование PROPATRIA, двойное слепое, плацебо-контролируемое рандомизированное многоцентровое исследование роли пробиотиков в профилактике инфекционные осложнения при ОП) в составе 298 взрослых пациентов с прогнозируемой тяжелой AP продемонстрировал значительно более высокий риск смерти у многовидовых пробиотиков. группа (180, 181). Два небольших рандомизированных испытания с момента завершения не продемонстрировали увеличение смертности (182, 183), но влияние неблагоприятных результатов исследования PROPATRIA Исследование привело к общей осторожности при использовании пробиотиков у взрослых с ОП.
Ни одно педиатрическое исследование не изучало роль пробиотиков у детей с AP.
Резюме: После серии небольших дел, предполагающих потенциальная польза пробиотиков при ОП у взрослых, большое рандомизированное исследование продемонстрировало повышенная смертность в группе пробиотиков. Педиатрических исследований не опубликовано.
Рекомендации 2 часа: Нельзя рекомендовать пробиотики в лечении острого панкреатита у детей в настоящее время. Высшее качество опубликованные данные для взрослых показывают, что они могут не только не принести пользы, но и увеличивать смертность.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 14; согласен = 9; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2i. Роль эндоскопии в лечении острого панкреатита у детей
Различные причины воспаления слизистой оболочки двенадцатиперстной кишки связаны с увеличением риск AP. Проявления, связанные с глютеновой болезнью поджелудочной железы, включают эндокринные и внешнесекреторная недостаточность, острый и хронический панкреатит, нарушение питания, папиллярный стеноз вторичный по отношению к дуодениту или иммунологическим нарушениям, и все предположили, что быть вовлеченными механистически (184–186).Желчнокаменная болезнь была обнаружена до 34% пациентов с болезнью Крона и может проявляться как АП (187). Аутоиммунный панкреатит (АИП) и первичный склерозирование холангит (188) также может быть обнаружен у пациентов с воспалительным заболеванием кишечника, проявляющимся AP (189–191). Повышение уровня IgG4 наблюдается у взрослых пациентов с AIP типа I, педиатрические пациенты с AIP обычно без повышения уровня IgG4, при биопсии двенадцатиперстной или желудочно-дуоденальной воспалительной поражения могут быть полезны в диагностике (192, 193).Были случаи острого и хронического панкреатита. редко регистрируется как проявление или ассоциация инфекции H. pylori (194, 195). Чрезвычайно редко возможными причинами панкреатита у детей являются опухоли, связанные с ампула или периампулярная область двенадцатиперстной кишки. Такие поражения могут быть первыми идентифицируется рентгенологическим исследованием, но также может быть обнаружено во время эндоскопического исследования. оценка. Судя по имеющимся историям болезни, механизм развития у этих пациентов рецидивирующий панкреатит до конца не изучен, но, вероятно, связан с опухолью непроходимость на уровне ампулы (196, 197).Но в целом роль эзофагогастродуоденоскопия при ОП ограничена.
Нет исследований, оценивающих показания или преимущества эзофагогастродуоденоскопии в педиатрический AP.
Резюме: Роль эндоскопии в неотложной помощи дети с AP неясно. Возможность первичных внепанкреатических заболеваний В результате разработка AP требует вдумчивого рассмотрения.
Рекомендации 2i: Эзофагогастродуоденоскопия не в настоящее время считается стандартным диагностическим инструментом при остром панкреатите у детей.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2j. Роль ЭРХПГ при остром панкреатите у детей
Роль ЭРХПГ при ОП эволюционировала с технологическими улучшениями в диагностические возможности МРТ / MRCP и с увеличением педиатрического опыта с эндоскопическое ультразвуковое исследование (ЭУЗИ). Благодаря наличию этих последних диагностических инструментов для при заболеваниях поджелудочной железы, ERCP все чаще используется в первую очередь для лечения вмешательства или для неясных диагнозов после MRCP или EUS.ЭРХПГ безопасна для детей при этом наиболее частым осложнением является легкий панкреатит после ЭРХПГ. аналогичны таковым у взрослых (~ 3–10%), когда выполняются опытные эндоскописты (198–206). Обструкция желчевыводящих путей и хронический панкреатит являются наиболее частыми показаниями к ЭРХПГ у детей. В педиатрической AP ERCP имеет ограниченная роль, выполняется почти исключительно при билиарном панкреатите, вторичном по отношению к холедохолитиаз или отстой. ЭРХПГ при холедохолитиазе без панкреатита безопасна и эффективны (207, 208), но в педиатрии нет конкретных рекомендаций по сроки проведения ЭРХПГ при холедохолитиазе или остром билиарном панкреатите.У взрослых большой метаанализ и научно обоснованные рекомендации IAP по ведению острых билиарный панкреатит рекомендовал ЭРХПГ в течение 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. В противном случае можно провести ЭРХПГ. планово при неосложненном холедохолитиазе и в других случаях желчевыводящих путей. панкреатит независимо от степени тяжести (209, 210).
Менее распространенными показаниями для ЭРХПГ при ОП являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы (211).Камни и стриктуры протоков поджелудочной железы обычно признаки острого рецидивирующего или хронического панкреатита, поэтому встречаются относительно редко показания к ЭРХПГ при АП. В редких случаях, когда непроходимость протока предотвращает разрешение панкреатита, может быть проведена терапевтическая ЭРХПГ. Псевдокисты поджелудочной железы в у детей может развиться острый или хронический панкреатит, но чаще всего возникает после тупая травма. Псевдокисты поджелудочной железы представляют собой однородное скопление панкреатической жидкости. окружены фиброзной или грануляционной тканью, но не имеют эпителиальной выстилки (15, 212), и может развиться из скоплений жидкости, сохраняющихся более 4 недель (213).ERCP может использоваться для оценки коммуникации псевдокиста с протоком поджелудочной железы, куда можно установить транспапиллярный стент для дренаж. В противном случае — эндоскопическая цистагастростомия (214–216) и под контролем EUS. дренаж (217) — безопасные и эффективные способы дренировать псевдокисты поджелудочной железы у детей и может быть рассмотрено в зависимости от расположения псевдокиста. Повреждение протока поджелудочной железы и утечка также могут возникнуть в результате травмы. Рано эндоскопическое или хирургическое вмешательство может помочь свести к минимуму продолжающуюся заболеваемость протоковым утечка, поскольку ERCP обеспечивает быстрый и более точный метод определения местоположения и степень повреждения, чем MRCP или CT, а также дает возможность терапевтического стента размещение поперек травмы (218, 219).
Резюме: Роль ЭРХПГ при остром панкреатите. в первую очередь относится к терапевтическому лечению билиарного панкреатита, вторичного по отношению к холедохолитиаз или отстой. Литература для взрослых предполагает эффективность ERCP в пределах 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. Менее распространенными показаниями к ЭРХПГ при остром панкреатите являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы или разрывы протока.
Рекомендации 2ji и 2jii: (2ji) Роль ERCP ограничен при остром панкреатите и зависит от местных знаний.(2jii) ERCP — это показан при лечении острого панкреатита, связанного с холедохолитиазом, вызывающим билиарный панкреатит и патологии протоков поджелудочной железы, такие как протоковые камни или протоки протока.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 21; согласен = 3; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2к. Роль EUS при остром панкреатите у детей
Эндоскопическое ультразвуковое исследование (EUS) использовалось для определения этиология АП.EUS не только всесторонне оценивает паренхиму поджелудочной железы и протока, но также и гепато-билиарной анатомии. Заболевания желчевыводящих путей, такие как холедохолитиаз можно оценить с помощью EUS, особенно когда трансабдоминальное УЗИ не позволяет визуализировать дистальный общий желчный проток. EUS также может определить наличие микролитиаза у желчный пузырь, который часто не визуализируется при трансабдоминальном УЗИ или КТ сканировать. Микролитиаз может привести к ОП и лечится холецистэктомией (220). Хотя у детей это случается крайне редко, опухоли поджелудочной железы, которые могут быть вызваны новообразованием поджелудочной железы или AIP, могут проявляться с AP и пройти дальнейшее обследование с помощью EUS с возможностью взятия пробы ткани поджелудочной железы. (221, 222).
Терапевтическая роль EUS при AP в основном ограничена для лечения осложнения АП, а именно скопление жидкости поджелудочной железы или некроз стенок. EUS имеет было показано, что он полезен при лечении скоплений жидкости поджелудочной железы / некроза вторичный по отношению к тяжелому AP. Считается, что спонтанное рассасывание псевдокист происходит чаще. чаще у детей, чем у взрослых, особенно если размер <5 см (мнение эксперта). Таким образом, с большинством коллекций любого типа можно обращаться консервативно и терапевтически. вмешательство не требуется в остром состоянии, за исключением случаев наличия инфекции (223).Однако, если происходит созревание (обычно через 4–6 недель) саморегулирование менее вероятно, и пациент может нужен эндоскопический дренаж. Другие показания к вмешательству EUS и дренированию включают: большой размер при возникновении клинических симптомов, подозрении на заражение скоплений или стойких симптомы от псевдокисты. Дренаж под контролем EUS и создание цистгастростомы было продемонстрировано, что он столь же эффективен и безопасен, как хирургическая цистгастростомия, и имеет было показано, что он эффективен даже у детей (224).
Резюме: на основании литературы для взрослых, EUS может быть полезным для определения этиологии острого панкреатита, которая может включать диагностику дистального камни общего желчного протока, новообразования поджелудочной железы или аутоиммунный панкреатит. Его роль для терапия в основном ограничена лечением осложнений острого панкреатита, а именно скопления жидкости поджелудочной железы или некроз стенок, вторичный по отношению к тяжелому АД.
Рекомендация 2k: EUS не считается стандартом диагностический инструмент при остром панкреатите у детей в настоящее время.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2L Роль хирургии / хирургической консультации при остром панкреатите у детей
Хирургические вмешательства не являются частью алгоритма ведения больного. Типичный эпизод АП. Публикации относятся к взрослому опыту. Раннее указание на хирургия включает лечение синдрома брюшной полости.Однако управление некроз поджелудочной железы с ранней некрэктомией в течение первых 72 часов, как было показано, приводит к повышенная заболеваемость и смертность по сравнению с отсроченными сроками не менее чем на 12 дней (225). Руководящие принципы Международного Ассоциация панкреатологов с 2002 г. предлагает отложить операцию некрэктомии для по крайней мере, через 3-4 недели после начала заболевания снижает заболеваемость и смертность (210). Руководящие принципы ACG 2013 года по управлению взрослый AP прокомментировал возможность хирургического вмешательства в связи с желчнокаменной болезнью. панкреатит, санация некроза (инфицированные vs.стерильный), и малоинвазивный лечение некроза поджелудочной железы (33). Рекомендации включали раннюю холецистэктомию во время той же госпитализации по поводу легкий приступ желчнокаменного панкреатита и обсуждение между гастроэнтерологами и хирургия для выбора времени холецистэктомии по сравнению с другими терапевтическими вариантами в случаях тяжелый АД, особенно с некрозом. Для пациентов с сохраняющейся клинической нестабильностью и ухудшение состояния на фоне некроза поджелудочной железы, дренирование может потребоваться для улучшить статус пациентов и снизить заболеваемость и смертность.Руководящие принципы АЧГ предлагают что санацию некроза следует отложить, когда это возможно, в идеале более четырех недель с момента обращения, чтобы лучше организовать воспалительные реакции. Даже в необходимость некрэктомии, менее инвазивных методов, включая чрескожную радиологию, или следует рассмотреть возможность эндоскопического дренирования / хирургической обработки раны наряду с лапароскопическим хирургическим вмешательством. предпочтение отдается лечению перед открытым хирургическим вмешательством (33).
Исследование PONCHO 2015 г. с участием 266 стационарных пациентов, рандомизированных по интервалу холецистэктомия или холецистэктомия с тем же госпитализацией также поддерживали ту же госпитализацию. холецистэктомия снизила частоту повторных осложнений, связанных с желчнокаменной болезнью, у взрослых пациенты с желчнокаменным панкреатитом легкой степени с очень низким риском холецистэктомии осложнения (226).
В случае тяжелой травмы живота, требующей неотложной лапаротомии (в том числе дорожно-транспортных происшествий) следует искать повреждения поджелудочной железы, в том числе вовлекающий проток поджелудочной железы. Тяжесть травмы поджелудочной железы может быть оценена в соответствии с Американской ассоциации хирургии травм поджелудочной железы по шкале, в которой 5 могут быть присвоены степени травмы (227). Выше травмы поджелудочной железы в результате травмы, как правило, также включают ассоциированную дуоденальную травмы. Пациентам с более легкими тупыми травмами I и II степени можно лечить в нерабочем состоянии.В случае травмы поджелудочной железы мультидисциплинарный подход, включающий: показаны бригады врачей / гастроэнтерологов и хирургов.
В педиатрической литературе о показаниях к операции гораздо больше ограничено. Что касается билиарного панкреатита, ретроспективная серия случаев из 19 детей, госпитализированных с билиарным панкреатитом, зарегистрировано 9 детей, перенесших ранний холецистэктомия без побочных эффектов и 4 из 10 детей, перенесших отсроченную операцию возникновение нежелательных клинических явлений (включая рецидив панкреатита) (228).
Резюме: Показания к острому хирургическому вмешательству. к показаниям АП относятся травмы живота, при которых у пациента нестабильность и / или поиск происходит сопутствующее повреждение других органов. В контексте билиарного панкреатита было показано, что холецистэктомия не только безопасна, но и предотвращает рецидивы, если они происходят. в рамках индекса госпитализации. Литература для взрослых предполагает, что раннее вмешательство в некроз поджелудочной железы приводит к увеличению заболеваемости и смертности, и, следовательно, к санации раны желательно отсрочить некроз поджелудочной железы, вызывающий нестабильность у пациента, по крайней мере, на 4 часа. недель с момента обращения, в идеале — эндоскопическим или чрескожным способом.
Рекомендация 2li: холецистэктомия безопасно может и следует выполнять перед выпиской в случаях легкой неосложненной острой желчной болезни. панкреатит.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2lii: В ведении острых некротических скоплений, вмешательств следует избегать и откладывать, даже для инфицированных некроз, поскольку результаты лучше при отсроченном (> 4 недель) подходе.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 6; нейтральный = 2; не согласен = 1; категорически не согласен = 0.
Рекомендация 2liii: Когда требуется дренирование или некрэктомия. необходимые нехирургические доступы, включая эндоскопические (EUS и ERCP) или чрескожные методы предпочтительнее открытой некрэктомии или открытой псевдокисты дренаж.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 9; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
3. ИСХОДЫ ОСТРОГО ПАНКРЕАТИТА ПЕДИАТРИИ
Общие исходы ОП у детей благоприятны по сравнению со взрослыми. В средняя продолжительность госпитализации детей с ОП составляет в среднем от 2,8 до 8 дней, хотя младенцы / малыши, как правило, поступают на более длительный период времени (в среднем 19,5 дней) (15, 73, 229–231). Раннее начало энтерального питания и агрессивная жидкостная реанимация был связан с более коротким пребыванием в больнице, меньшим количеством госпитализаций в отделения интенсивной терапии и снижение показателей тяжелого АП по сравнению с пациентами, находящимися в НКО (73).Эти результаты в целом совпадают с выводами большинства взрослых. исследований (232), но, возможно, не применялись к педиатрические пациенты до недавнего времени. Более высокая смертность при ПД у детей связана с системное заболевание, но в целом низкий и составляет менее 5% в большинстве когорт, даже в том числе в реанимации (15, 30, 233, 234).
Осложнения с ранним началом при ОП включают полиорганную дисфункцию или шок (15). Острые скопления перипанкреатической жидкости наблюдаются в острая фаза панкреатита и имеет тенденцию к спонтанному разрешению.Частота образование псевдокист колеблется от 8% до 41% у детей с панкреатитом, и более высокие показатели наблюдаются у пациентов с панкреатитом, связанным с абдоминальной травма (15, 212, 235). Псевдокисты часто бессимптомный и может лечиться консервативно или стать больше и вызвать боль в животе, рвота или лихорадка. Они также могут заразиться в 10–15% случаев. (236). Еще одно осложнение с поздним началом связано с до некроза поджелудочной железы. Некроз может проявляться в первую очередь в виде острого некротического скопления. (ANC), а затем созревают до некроза без стенок (WON) (8).Варианты лечения при дренировании псевдокист и некротических стенок коллекции включают эндоскопический (транспапиллярный или трансмуральный) дренаж, чрескожный катетерный дренаж или открытая / лапароскопическая операция. Выбранная модальность зависит от размера, расположение, анатомия и риски / преимущества процедуры, хотя чрескожная и Трансгастроинтестинальный дренаж под контролем эндоскопического ультразвука (ЭУЗИ) в настоящее время становится все более популярным. широко распространено (237).
Примерно 15–35% детей с острым у панкреатита будет еще один приступ панкреатита.Острый рецидивирующий заболевание у детей панкреатит связан с панкреатико-билиарными аномалиями, аутоиммунным панкреатитом, нарушения обмена веществ и наследственный панкреатит (15).
Резюме: За детьми необходимо следить во время их курс АП при местных и системных осложнениях, которые могут включать дисфункцию органов, острые скопления жидкости и впоследствии некроз или псевдокисты. Общий педиатрические пациенты с острым панкреатитом имеют хороший прогноз с очень низким уровнем смертность, но сообщается о частоте рецидивов до 15–35%.
Рекомендация 3: Дети с острым панкреатитом должны получить тщательное наблюдение со стороны поставщика медицинских услуг для выявления раннего или позднего осложнения или рецидивы.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
A Clinical Отчет Комитета по поджелудочной железе NASPGHAN
1. ПЕРВОНАЧАЛЬНАЯ ОЦЕНКА И ДИАГНОСТИКА ОСТРОГО ПЕДИАТРИЧЕСКОГО ПАНКРЕАТИТА
Недавние исследования оценивают заболеваемость острым панкреатитом (ОП) при ~ 1/10 000 детей в год (2, 7), заболеваемость приближается к взрослым.Есть нет научно обоснованных руководств по диагностике ОП у детей. ВДОХНОВЕНИЕ ( IN международный S tudy Группа компаний P медицинский P анкреатит: I n Найдите Cu RE ) определение детской AP является экспертное определение смоделировано по критериям Атланты у взрослых (8). Согласно критериям INSPPIRE, для диагностики АП требуется как минимум 2 из следующего: (1) боль в животе совместима с AP, (2) значениями сывороточной амилазы и / или липазы ≥3 раза верхние пределы нормы, (3) визуализация результаты согласуются с AP (9, 10).INSPPIRE или другие критерии не касаются этапов (ранних или поздний) АП у детей или типов (интерстициальный отечный панкреатит, некротический панкреатит, инфицированный панкреонекроз) или степень тяжести ОП (легкая, умеренная или тяжелая форма ОП при мультисистемной органной недостаточности).
Детский диагноз ОП обычно подозревается клинически с совместимым симптомом презентации, подтвержденные лабораторными и / или радиологическими исследованиями. Боль в животе и / или раздражительность являются наиболее частыми проявлениями ОП у детей, за которыми следуют эпигастральные болезненность, тошнота и рвота (11, 12).У младенцев и детей ясельного возраста симптомы могут быть незаметными; поэтому диагноз требует высокого уровня подозрений. Желчные / обструктивные факторы, лекарственные препараты и системные заболевания являются основными причинами ОП у детей (1, 4, 9, 12–23), и знание этих возможных причин поможет руководить начальными исследованиями.
Процент детей, у которых развиваются «тяжелые» острые панкреатит варьирует в опубликованных сериях (6–34), но дети с ОП в в целом имеют легкое течение (11, 24, 25). В подмножестве у пациентов АП может иметь тяжелое течение (8), но нет установленные клинические инструменты предсказывают этот результат.Балльные системы оценки степени тяжести АП у взрослых (Рэнсон, Глазго, модифицированный Глазго, Прикроватный индекс тяжести острых заболеваний). Панкреатит (BISAP) и оценка острой физиологии и хронического здоровья II (APACHE II)) не легко применимы к детям по нескольким причинам (26). Детская шкала острого панкреатита (PAPS) ДеБанто (27) была оценена у детей, но имеет низкую чувствительность. и требует 48 часов для прогнозирования рисков. Точно так же степень тяжести компьютерной томографии индекс (CTSI) или балл Бальтазара (28), опирается на радиологический внешний вид и, следовательно, нежелателен в детской возрастной группе из-за радиации экспозиция.Благодаря своей широкой доступности липаза является привлекательным маркером для выявления тяжелых случаев AP (25), но может выявить много ложных положительных из-за его низкой положительной прогностической ценности и специфичности. Коффи и др., обнаружили, что липаза сыворотки в семь раз превышает верхний предел нормы в течение 24 часов после презентация помогла предсказать тяжесть острого панкреатита (25). Тем не менее, это ретроспективное исследование с участием 211 детей и не были проверены в более крупных исследовательских группах. Suzuki и др. В Японии разработали удобная для детей система оценки степени тяжести с использованием 9 параметров (29), но это также было ретроспективным исследованием, в котором оценивались только 145 пациентов, и авторы пришли к выводу, что результаты не могут быть широко применимы к педиатрическое население.Совсем недавно Сабо и др. Сообщили, что ранняя степень тяжести прогностическая модель с использованием сывороточного альбумина, липазы и количества лейкоцитов, полученных в 24 часа продемонстрировали положительную прогностическую ценность 35% и отрицательную прогностическую ценность значение 91% (30).
Необходимы дальнейшие проспективные исследования для определения клинической применимости любой из этих инструментов. В вышеупомянутых исследованиях использовались различные определения степени тяжести. AP, что ограничивает возможности проведения сравнений между исследованиями. Недавняя публикация Комитет по поджелудочной железе NASPGHAN обратился к необходимости иметь четко определенную классификацию степени тяжести АП, предлагая определения легкой, средней и тяжелой степени АП для повысить однородность исследований (31).
Биомаркеры сыворотки
Острый панкреатит — это в первую очередь клинический диагноз, основанный на наличие как минимум двух из трех критериев, опубликованных INSPPIRE и Atlanta классификация (8, 9). Без выполнения двух из этих трех критериев трудно сделать диагностика АП. Основные биохимические маркеры, используемые для диагностики АП, включают сывороточную липазу. и сывороточная амилаза. Поскольку уровень липазы или амилазы в сыворотке не менее чем в три раза превышает верхний предел нормы считается совместимым с панкреатитом, важно знать справочные значения лаборатории для определения этого порога.И амилаза, и липаза обычно повышается на ранней стадии заболевания. Однако соотношение сыворотки уровни липазы или амилазы и тяжесть заболевания низкая (25, 32, 33). Липаза в основном секретируется поджелудочной железой, хотя другие источники липазы включают желудочные и язычные липазы. При АП липаза обычно увеличился в течение 6 часов после появления симптомов; уровень в сыворотке достигает максимума через 24–30 часов и может остаются повышенными более одной недели (34). Некоторые выступают за то, чтобы сывороточная липаза без сывороточной амилазы была достаточной для диагностики АП, поскольку липаза является более чувствительным и специфическим маркером АП (87–100% и 95–100% соответственно) (35–38).Липаза, кроме того, остается повышенным дольше, чем амилаза, что полезно в случаях отсроченного проявления (34, 39, 40). Уровни липазы также меньше изменяются этиология AP в отличие от амилазы, особенно в случае этанола (37, 41) или гиперлипидемия (42, 43). Но следует соблюдать осторожность при интерпретации уровней у детей. упражнения, поскольку было продемонстрировано, что нормальные значения липазы связаны с возрастом ребенок, растущий от новорожденного к ребенку, к взрослому (44, 45). Амилаза секретируется несколькими органами, прежде всего слюнные железы и поджелудочная железа.Большинство лабораторий измеряют общую амилазу уровни, которые содержат изоформы s-амилазы (слюна) и p-амилазы (поджелудочная железа) (46). Существуют лабораторные тесты для фракционирования p- и s-амилаза, но эта практика менее доступна. Эталонные значения амилазы отличаются в зависимости от используемого лабораторного теста, но также зависят от возраста и пола (47, 48). Сыворотка Уровни амилазы могут изменяться в зависимости от этиологии панкреатита, как указано выше. Амилаза уровни повышаются быстрее, чем уровни липазы, и часто могут нормализоваться через 24 часа после начала симптомы, ограничивающие полезность у пациентов с отсроченным обращением к врачу объект (34).Поскольку почки выводят амилазу и липазы, повышение этих ферментов не на уровне поджелудочной железы может наблюдаться у пациентов с повреждение или заболевание почек (46).
Несколько состояний, не связанных с панкреатитом, вызывают повышение уровня поджелудочной железы амилаза и / или липаза, включая декомпенсированную печеночную недостаточность, почечную недостаточность, кишечную воспаление (включая целиакию и воспалительное заболевание кишечника) брюшной полости травмы, диабетический кетоацидоз и травмы головы (49). Кроме того, некоторые люди продуцируют большие комплексы амилазы или липаза с иммуноглобулинами (так называемая макроамилаза и макролипаза), которые плохо фильтруется и выводится из-за большого размера, что приведет к повышенным значениям, если уровень фермента измеряется в крови, несмотря на то, что он не связан с воспалением поджелудочная железа (50).
Другие биомаркеры для диагностики и лечения панкреатита были предложены и изучены на животных моделях или небольших клинических испытаниях (см. обзоры в (46, 51, 52)). Однако ни один из них не получил известности, и многие еще предстоит пройти валидацию для общеклинического использования.
Несколько лабораторных тестов помогают контролировать течение АП (53). В целом электролиты сыворотки крови, мочевина крови азот (BUN) и креатинин, а также общий анализ крови (CBC) важны для мониторинга состояние жидкости / гидратации и почечная функция.Панель печеночных ферментов показана для поиска желчнокаменной или желчнокаменной этиологии, а также для оценки поражения органов. Кальций и Уровни триглицеридов следует рассматривать как исходные исследования (9). Мониторинг респираторного статуса может предупредить врача о том, что прогрессирование от легкой до среднетяжелой или тяжелой АД.
Этиология
Как упоминалось ранее, анатомическая, обструктивная (в том числе желчная), инфекционные, травматические, токсические, метаболические, системные заболевания, врожденные нарушения обмена веществ, генетическая предрасположенность и идиопатия были описаны как потенциальные этиологии при детском ОП, остром рецидивирующем панкреатите (АРП) и хроническом панкреатите (ХП) (3, 4, 54).Обзор Lowe et al суммировал 6 лучших общие этиологические категории в опубликованных обзорах как идиопатические / другие в 24%, травмы у 17%, системные заболевания у 15%, структурные аномалии в 14%, лекарства в 10% и инфекции в 8%. (3) Учитывая более частую этиологию, а также те, которые для которых существует направленная терапия, в рукописи 2012 года Morinville et al. опрос детских гастроэнтерологов, оказывающих панкреатологическую помощь, и предложили после обследования в первых случаях панкреатита: сывороточные ферменты печени, триглицериды и уровень кальция и УЗИ брюшной полости.Они предложили отложить тестирование на генетические причины / предрасположенности (которые в то время включали CFTR (муковисцидоз) регулятор трансмембранной проводимости), SPINK1 (ингибитор сериновой протеазы Kazal типа 1) и PRSS1 (катионный трипсиноген)), хлорид пота и более подробные изображения для случаев ARP, CP или первых экземпляров AP с повышенным риском рецидив, основанный на представлении, прошлой истории болезни или семейном анамнезе (9). При необходимости, поиск может быть проведен для конкретных факторы токсико-метаболического риска (55).Недавний публикация Gariepy et al, посвященная причинно-следственной оценке ARP и CP у детей, который имеет тенденцию быть более обширным из-за повторяющегося / хронического характера презентации (56) Аутоиммунный панкреатит (АИП) типов 1 и 2 редко диагностируются, но представляют разные типы панкреатита со специфическими гистологические данные в контексте суггестивных симптомов, визуализации, лабораторных исследований. результаты и ответ на терапию. Если AIP подозревается как этиология AP, в дальнейшем необходима поддерживающая оценка.Заинтересованные читатели будут перенаправлены на недавний публикация Scheers et al по педиатрической AIP (57).
Визуализация
Визуализация на ранней стадии ОП обычно не требуется, если в анамнезе / при предъявлении симптомы и биохимические маркеры сыворотки присутствуют для постановки диагноза. Визуализация становится актуально для документирования некроза поджелудочной железы, осложнений панкреатита, включая жидкость скопления и этиология панкреатита, например, камни в желчном пузыре / желчевыводящие пути или анатомические аномалии.
Золотым стандартом диагностической визуализации остается КЭКТ и несколько оценок. системы разработаны (58).Тем не мение, несмотря на то, что CETC является золотым стандартом визуализации, он часто не указывается и необходим для диагностики или лечения педиатрического AP. В неоднозначных случаях для диагностики ОП, например, при отсроченном проявлении, когда сывороточные маркеры могут быть низкими, компьютерная томография с контрастным усилением (CECT) может потребоваться для подтверждения AP. IV контраст является ключом к различению некротических участков поджелудочной железы (59). Поскольку ранняя визуализация может недооценивать степень заболевания и поскольку осложнения развиваются со временем, и результаты могут отсутствовать на ранних этапах фазе заболевания, в идеале CETC следует отложить как минимум на 96 часов после начала симптомы (8, 60).В легких случаях КЭКТ может показать усиление гомогенного органа, воспалительное изменения перипанкреатического жира или жидкости, окружающей поджелудочную железу (59) В тяжелых случаях КЭКТ может показать неоднородный орган усиление, некроз в поджелудочной железе или в окружающей перипанкреатической ткани. Кроме того, CECT может также идентифицировать скопления перипанкреатической жидкости или псевдокисты. КЭКТ следует пересмотреть при ухудшении клинического состояния пациента. или постоянно тяжелый (8). Lautz et al. нашел что индекс тяжести компьютерной томографии (шкала CTSI или Balthazar) в педиатрической пациенты дали чувствительность, специфичность, положительную прогностическую ценность и отрицательную прогностическая ценность 81%, 76%, 62% и 90%, соответственно, по степени тяжести в ретроспективном исследовании 64 детей (61).
Ультразвук широко используется в случаях, когда есть высокие подозрения на билиарный панкреатит, при котором полезно заранее определить необходимость терапевтического вмешательство (33, 58). Ультразвук имеет отличный профиль безопасности, неинвазивен и не использовать радиацию. Тем не менее, использование ультразвука может быть ограничено в оценке состояния. поджелудочной железы из-за мешающих структур, таких как кишечные газы в кишечнике и ожирение и имеет более низкую чувствительность при визуализации поджелудочной железы по сравнению с КЭКТ.
Магнитно-резонансная томография (МРТ) обычно не используется в качестве первичной визуализации техника при АП, но может быть полезна при поздних осложнениях (59). Это может быть особенно полезно для молодых или беременных. пациентам (с намерением ограничить облучение), и может разрешить использование альтернативных методов внутривенного контраста в пациенты с нарушением функции почек или аллергией на йодсодержащий контраст (60). МРТ также может быть более чувствительным при оценке некротическая ткань по сравнению с КЭКТ (59, 61). МР-холангиопанкреатография (MRCP) при AP наиболее часто используется для обнаружения камней в дистальных отделах общего желчного протока и диагностики желчных путей АП.МРТ / MRCP с использованием секретина помогает исследовать систему протоков в поджелудочной железы, а также общие аномалии желчных протоков, включая стриктуры или камни (62, 63). К оптимизировать обнаружение патологий протоков, MRCP может выполняться после атаки AP исчез, поскольку острый отек может затруднять визуализацию протоков. Использование MRCP, усиленный секретином, при заболевании поджелудочной железы у детей полностью не установлен (64) и доступ к секретину неодинаков через учреждения и страны.Lin et al подробно описывают использование МРТ и MRCP у детей. требуется визуализация поджелудочной железы, а также общие аспекты визуализации при AP (65).
Резюме и рекомендации
Рекомендация 1a: Диагностика острых заболеваний у детей панкреатит должен соответствовать ранее опубликованным критериям INSPPIRE.
Для диагностики ОП у педиатрических пациентов необходимы как минимум 2 из следующего: (1) боль в животе, совместимая с AP, (2) уровни амилазы и / или липазы в сыворотке ≥3 раза верхние пределы нормы, (3) результаты визуализации в соответствии с AP.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1b: Возможно выполнение первичной визуализации. с помощью трансабдоминального ультразвукового исследования, с другими методами визуализации (КТ, МРТ), зарезервированными для большего сложные случаи +/– с учетом подозреваемой этиологии.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 4; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1c: Основана на наиболее частой этиологии и те, для которых существуют варианты лечения, первый приступ острого панкреатита тестирование должно включать ферменты печени (АЛТ, АСТ, ГГТ, ЩФ, билирубин), триглицериды уровень и уровень кальция.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2. СООБРАЖЕНИЯ ВЕДЕНИЯ ПРИ ОСТРЫХ ПЕДИАТРИЧЕСКИХ ПАНКРЕАТИТАХ
2a.Инфузионная терапия при остром панкреатите
Внутривенная инфузионная терапия является основой лечения во время эпизода AP. Жидкая реанимация поддерживает адекватный жидкостный статус и диурез, но в последнее время внимание было сосредоточено на использовании внутривенных жидкостей для предотвращения потенциальных осложнений при ОП, такие как некроз и органная недостаточность. Патогенез ОП и прогрессирование до тяжелой степени. считается вторичным по отношению к нарушению микроциркуляции поджелудочной железы событиями, включая гиповолемию, повышенную проницаемость капилляров и образование микротромбы.Считается, что жидкостная реанимация не только устраняет гиповолемию, но и помогает сохранить микроциркуляцию поджелудочной железы, обеспечивая адекватную перфузию и предотвращая возможное образование микротромбов и, таким образом, предотвращение осложнений и прогрессирования тяжелое заболевание (66).
Тип жидкости
Отсутствует консенсус относительно идеального количества и типа жидкости для использования во время эпизода ОП во взрослой практике, и существует еще меньше данных, относящихся к жидкости в педиатрической популяции. Кристаллоид был наиболее рекомендуемым типом жидкость в руководствах для взрослых (33, 67–70).А Основное преимущество кристаллоидов в том, что они легко и быстро доступны. Обычный физиологический раствор (NS) долгое время был предпочтительным кристаллоидом для начальной жидкостной реанимации в в целом, но в некоторой литературе для взрослых предполагается, что лактатные звонаги (LR) являются более оптимальными для AP. В небольшом рандомизированном контрольном исследовании (РКИ) с участием 40 взрослых с AP Wu et al. что LR снижает частоту синдрома системного воспалительного ответа (SIRS) и уровни С-реактивного белка через 24 часа по сравнению с NS (71). Напротив, ретроспективный обзор 103 пациентов не смогли показать какой-либо существенной разницы между LR и NS в качестве начального реанимационная жидкость у взрослых с панкреатитом различной степени тяжести (72).LR был рекомендован по сравнению с NS в Международном Рекомендации Ассоциации панкреатологов / Американской панкреатической ассоциации (IAP / APA), но в рекомендациях Американской гастроэнтерологической ассоциации (AGA) только говорится, что LR может быть лучший выбор, но не был сильной рекомендацией (68, 70). В педиатрии это было показали, что агрессивное введение жидкости в течение первых 24 часов с помощью физиологического раствора с 5% декстрозой является безопасным и хорошо переносимым вариантом (73), но его не сравнивали с другими типами жидкостей для внутривенного вливания. (например, LR).
Коллоиды (например, альбумин, свежезамороженная плазма или упакованные эритроциты) не рекомендованы в качестве начальной реанимационной жидкости при АП. Коллоидные компоненты оставаться во внутрисосудистом пространстве из-за большего размера и может втягивать жидкость в кровообращение из интерстиция вторично по отношению к осмотическому эффекту. Руководящие принципы AGA рекомендует коллоид в определенных ситуациях, когда гематокрит < 25% альбумина составляет <2 г / дл (68), при этом другая публикация рекомендует соотношение кристаллоидов и кристаллоидов 3: 1. коллоид (74).
Скорость введения жидкости
Агрессивность жидкостной реанимации при АП также обсуждалась. В время вмешательства агрессивной жидкостной терапии может быть ключевым. Учеба взрослых в пользу ранних и агрессивных жидкостей в AP включают несколько ретроспективных исследований, которые использовали разные стратегии, такие как предоставление> против <33% от общего количества жидкости в течение первых 24 часов, а другой обеспечивает 3,5 л по сравнению с 2,4 л внутривенно в течение первых 24 часов (75). В основном, те, кто получает более агрессивные объемы жидкости внутривенно в течение первых 24 часов, как правило, улучшили результаты, включая смертность, но даже в рамках различных исследований результаты противоречивы в отношении того, снижает ли более высокое раннее введение жидкости некроз, синдром системного воспалительного ответа (SIRS) и продолжительность пребывания в стационаре (76).Напротив, Mao et al. Сообщили о РКИ 76 пациентам с тяжелым АП назначена медленная гемодилюция (5–10 мл / кг / ч) или быстрая гемодилюция (10–15 мл / кг / ч), демонстрирующая, что быстрая агрессивная ранняя жидкость введение привело к более высоким показателям сепсиса и смертности (77). de-Madaria et al провели проспективное исследование 247 человек. пациенты делятся на пациентов в зависимости от количества жидкости, введенной в первые 24 периода. часы. Группа, получавшая наибольший объем,> 4,1 л, имела повышенный уровень стойкая органная недостаточность (78).Weitz и др., рассмотрели 391 случай АП и обнаружили, что использование агрессивных жидкостей (примерно 5 л) было неэффективным. связаны с обострением заболевания и местными осложнениями (79). Опасения по поводу этой последней группы исследований заключаются в том, что в основном они касались более больных пациентов, и жидкостные режимы не ограничивались первые 24 часа реанимации.
Несколько экспертов и групп с тех пор дали рекомендации по скорости жидкостная реанимация в первые 24–48 часов у взрослых с ОП.МАП / АПА руководящие принципы рекомендуют пациентам получать 5–10 мл / кг / час до реанимации. цели достигаются в отношении улучшения частоты сердечных сокращений, диуреза, среднего артериальное давление и / или гематокрит (70). В Американский колледж гастроэнтерологии (ACG) рекомендует начальную скорость 250–500 мл / час, в дополнение к болюсу жидкости, если гипотензия или тахикардия присутствуют и используют BUN для направления терапии (33). Подобные рекомендации сделаны в обзоре Whitcomb et al (80). Aggarwal et al. советует 3–4 л жидкости в первые 24 часа (не более 4 л) с начальным болюсом 1 л и последующие 3 мл / кг / час в течение первых 24–48 часов (81).Наср и др. первоначально рекомендуют болюсы 1–2 л и 150–300 мл / час (82). Впоследствии они рекомендуют 2 мл / кг / час, если пациент отвечает на первоначальную реанимацию, но в противном случае использовать 3 мл / кг / час (82).
Только в одном педиатрическом исследовании оценивались разные нормы поддерживающей жидкости. администрации с участием 201 пациента с ОП [69]. Это исследование показало, что сочетание ранних энтеральное питание (<48 часов) и агрессивные жидкости (> 1,5–2x техническое обслуживание в первые 24 часа) уменьшилась продолжительность пребывания и возникновение тяжелое заболевание по сравнению с более традиционным историческим лечением.Агрессивные внутривенные жидкости не повлияли отрицательно на исходы (в первую очередь, легочные осложнения или повторная госпитализация). ставки). Никакие исследования не указывают идеальную норму поддерживающих жидкостей в AP после начальная реанимация (> 24–48 часов), хотя Сабо и др. что 1,5–2-кратное поддержание было безопасным для их популяции пациентов (73). Нет педиатрических исследований, сравнивающих первоначальную реанимацию тома.
Резюме: В начальной фазе реанимации острого панкреатит, теоретические и потенциальные клинические преимущества в пользу LR выше NS на основе данные о взрослых, но отсутствуют педиатрические данные.
Рекомендация 2ai: Дети с острым панкреатит необходимо первоначально реанимировать кристаллоидами, либо с LR, либо с NS в острой постановке. На основании оценки статуса гидратации / гемодинамического статуса, если при наличии гемодинамических нарушений рекомендуется болюсное введение 10–20 мл / кг.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Резюме: Педиатрическая литература жидкостная реанимация и скорость введения жидкости при остром панкреатите.Взрослый литература предлагает болюсы 250–1000 мл на начальном этапе и до 3–4 л. жидкости в течение первых 24 часов.
Рекомендация 2aii: Дети с диагнозом острой панкреатит следует назначать 1,5–2-кратное поддерживающее внутривенное введение жидкостей с мониторингом диуреза в течение следующих 24–48 часов.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 12; согласен = 10; нейтральный = 2; не согласен = 0; категорически не согласен = 0.
2b. Мониторинг детей с диагнозом ОП / внепанкреатические проявления острый панкреатит
Хотя это еще не изучено у педиатрических пациентов, полиорганная болезнь у взрослых пациенты с ОП связаны с худшими клиническими исходами с более чем половиной случаев, связанных с ОП. смерть в течение 1 недели от начала полиорганной дисфункции (83).Поражение сердца, легких и почек является ключевым фактором. компоненты систем оценки взрослых, используемых для прогнозирования тяжести эпизода ОП, включая модифицированная атлантская классификация, критерии Рэнсона, степень серьезности по Японии Оценка, оценка по Глазго, BISAP и APACHE II (8, 84–87). Педиатрические модели, прогнозирующие тяжесть ОП, также придают большое значение вовлечению нескольких органов, но оказались менее надежными (88) или еще не прошли проспективную валидацию (29). Повышенный эндотелиальный барьер проницаемость и глубокий выброс цитокинов, связанные с ССВО в сочетании с агрессивным гидратация теоретически увеличивает риск пациента для жидкости третьего промежутка и развитие внепанкреатических проявлений АП.Надлежащий мониторинг жизненно важен для сбалансировать соответствующую жидкостную реанимацию, пытаясь предотвратить сердечную, легочную и почечные осложнения (89).
Сердечно-сосудистый мониторинг
Гиповолемия при поступлении является надежным предиктором заболеваемости и смертности среди взрослых с AP и, по-видимому, коррелирует с величиной SIRS (89). Тахикардия использовалась как при системы оценки взрослых и детей для прогнозирования тяжести ОП и ее улучшение использовались для подтверждения адекватной реанимации жидкости в дополнение к мониторингу мочи объем и тургор кожи (71, 81).Регулярный кардиологический мониторинг взрослых у пациентов, не получающих ОИТ включает регулярные измерения жизненно важных функций каждые 8 часов для получения информации о состоянии сердечно-сосудистой системы (71). Дополнительно редкие случаи тампонады сердца и предсердий. Сообщалось о фибрилляции при АП, и ее следует учитывать при стандартном кардиологическом исследовании. обследование начато у пациентов с необъяснимой гипотонией, одышкой и / или боль в груди (90–93).
Мониторинг легких
Исследования на взрослых и животных модели показывают острый респираторный дистресс синдром (ОРДС), пневмония и отек / выпот легких как ранние осложнения ОП, обычно в течение первых 48 часов (15, 94).Поскольку ОРДС является наиболее распространенным критическим осложнение тяжелого АП, связанного с полиорганной дисфункцией у взрослых (95), аномальное P a O 2 или аномальные изображения легких являются компонентами всех обычно используемых систем оценки для предсказать тяжесть приступа ОП (8, 29, 84–87). Регулярный мониторинг насыщение кислородом во время агрессивной гидратации обычно осуществляется, с некоторыми койки пациентов должны быть подняты на угол 30 градусов, чтобы снизить вероятность легочная секвестрация (71).Стандарт следует рассмотреть возможность обследования легких и ухода за пациентами с необъяснимыми одышка, ухудшение кашля и / или затрудненное дыхание (94).
Мониторинг почек
Острое повреждение почек (ОПП) через синдром брюшной полости (83, 96) или вызванное воспалением повреждение проксимального извитого канальца (97), отмеченное повышением уровня азота мочевины и креатинина, а также снижение диуреза, это известное раннее осложнение АП у детей и факторы занимает важное место в оценочных системах AP для прогнозирования тяжести заболевания (8, 15, 29, 84–87).В некоторых исследованиях на взрослых было показано, что только мочевины быть столь же эффективным в прогнозировании тяжести заболевания, как и более продвинутые системы оценки (98) и AKI был связан с В 10 раз повышен риск смерти при тяжелом ОП (99). Таким образом, BUN и креатинин считаются важными маркерами для следить за проведением инфузии и контролировать ОПП у взрослых во время первого 48 часов и при агрессивном увлажнении (71, 81, 98). Хотя нет никаких руководств, документирующих частоту мониторинга этих параметров, 8–12 часов использовались в одном исследовании для определения реакции на управление жидкостями (71).Рекомендации ACG подчеркивают важность снижения АМК и поддержания нормального уровня креатинина в первые 24 часа, поэтому очень важен ранний мониторинг (33). В редких случаях требуется непрерывная вено-венозная гемофильтрация (CVVH). для предотвращения дальнейшего повреждения почек, предотвращения синдрома брюшной полости и / или removae воспалительных цитокинов, но его использование не изучалось у педиатрических пациентов с AP (100). Может понадобиться установить мочевой катетер для точного документирования диуреза, особенно при седативном ребенок в условиях отделения интенсивной терапии.
Резюме и рекомендации
Наблюдение за пациентами с острым панкреатитом может дать индикаторы возникающие осложнения, включая ССВО и органную дисфункцию / недостаточность. Сердечный, следует особенно внимательно следить за респираторным и почечным статусом в течение первого Через 48 часов после обращения, так как большинство осложнений начинается в течение этого периода. период времени. Диурез — важный маркер адекватной жидкостной реанимации, при этом литература для взрослых, предлагающая стремиться к достижению> 0.5–1 куб. См / кг / час (Руководство IAP / APA).
Рекомендация 2bii: Пациентам, поступившим в в стационарном отделении необходимо измерять жизненно важные показатели не реже, чем каждые 4 часа в течение первых 48 дней. часы приема и в периоды агрессивной гидратации для контроля кислорода сатурация, артериальное давление и частота дыхания. Частота регулируется в зависимости от клинический статус. Нарушения жизненно важных функций должны требовать обследования у специалиста.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2biii: АМК, креатинин и моча производительность следует регулярно контролировать в течение первых 48 часов как маркер соответствующее ведение жидкости и скрининг на острое повреждение почек. Аномалии должен вызвать нефрологическое обследование.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 4; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
2с. Обезболивание при остром панкреатите
Боль в животе является наиболее частым симптомом ОП.В педиатрической АП исследования, от 80% до 95% пациентов жаловались на боль в животе. Пациенты присутствует с болью в эпигастрии у 62-89% и диффузно у 12% до 20%. «Классическое» проявление иррадиации боли в эпигастрии. к спине встречается только у 1,6–5,6% педиатрических пациентов (15, 16).
Патофизиология ОП характеризуется потерей внутриклеточных и внеклеточная компартментализация, которая может быть результатом различных механизмов: обструкция секреторного транспорта поджелудочной железы; активация ферментов; или неспособность остановить каскад активации.АП встречается у генетически предрасположенных лиц, у которых воспалительная реакция вызывает панкреатит. Это, в свою очередь, стимулирует внутреннюю панкреатические и соматические болевые рецепторы брюшины (101). Другие постулируемые механизмы, вызывающие боль в переднем отделе позвоночника, включают высокое давление. внутри железы или протока поджелудочной железы с последующей ишемией железы. Боль в AP тоже бывает вероятно, связано с высвобождением тахикинина, вещества P и кальцитонина, связанного с геном. пептид. Факторы, которые стимулируют первичные сенсорные нейроны, включают ионы водорода, тепло, лейкотриены, метаболиты арахидоновой кислоты, брадикинины и протеазы, такие как трипсин, выпущен во время AP (102).
Обезболивание — важная терапевтическая цель при лечении ОП и обычно включает использование анальгетиков периферического и центрального действия. Нет данных опубликованы по оптимальному обезболиванию в педиатрической AP, а исследования у взрослых не определили одно лучшее лекарство (67).
Опиоидные анальгетики
Потому что классические анальгетики периферического действия (такие как ацетаминофен) часто недостаточны при тяжелом панкреатите, часто требуются опиаты для контроля боль.Морфин или родственные ему опиоиды употребляли 94% респондентов для вести детей с ОП в соответствии с анкетой для врачей INSPPIRE 2012 года (103). Сообщалось, что морфин вызывает дисфункция сфинктера Одди после системного введения (104). Однако нет четких доказательств, подтверждающих эту теорию, и морфин можно безопасно применять у пациентов с ОП (105). Меперидин применялся у взрослых с АП, но его недостатки включают: короткий период полураспада и потенциал нейротоксичности за счет накопления токсичных веществ. нейрометаболиты, которые могут приводить к судорогам, миоклонусу и тремору (106).Обзор наркотиков и функции сфинктера Одди. Thomson et al, документально подтверждают, что на сегодняшний день нет исследований, напрямую сравнивающих эффекты меперидин и морфин на сфинктере манометрии Одди и никаких сравнительных исследований существуют у пациентов с АП. Кроме того, не существует исследований или доказательств, указывающих на то, что морфин противопоказан к применению при ОП (107). Кокрановский обзор 2013 года включает 5 исследований, в общей сложности 227 Субъекты для оценки эффективности и безопасности нескольких опиоидов. Включенные лекарства были бупренорфин, петидин, пентазоцин, фентанил и морфин.Общий вывод состоит в том, что опиоиды могут быть подходящим выбором при лечении боли. связанных с AP, и они могут уменьшить потребность в дополнительной анальгезии. Кроме того, риск осложнений, связанных с панкреатитом, или клинически серьезных побочные эффекты не отличаются от опиоидов и других анальгетиков (108).
Опиоидсберегающие анальгетики
Предполагается, что НПВП являются потенциальными участниками развитие AP, но также показали преимущества при лечении боли в AP.Профилактическое Было показано, что НПВП, включая индометацин и диклофенак, полезны при нескольких исследования по профилактике панкреатита после ЭРХПГ (109, 110). Что касается боли После постановки диагноза АР индометацин превосходит плацебо и не показали повышенного риска желудочно-кишечного кровотечения в небольшом исследовании (111). По сравнению с морфином метамизол показал улучшение снятие боли через 24 часа, но разница не достигла статистической значимости (105).
Системное введение местных анестетиков, в основном новокаина, было выступает в качестве основного обезболивающего при АП.Предлагается внутривенное введение новокаина для уменьшения боли. и / или необходимость вспомогательных обезболивающих и, возможно, улучшения клиническое течение АП. В одном контролируемом исследовании системное введение новокаина в улучшение панкреатита и ускоренное послеоперационное восстановление после обширного абдоминального хирургическое вмешательство, включая уменьшение боли, улучшение когнитивных функций и сокращение длительность кишечной непроходимости, а также общая госпитализация (112). Но доказательства ограничены, а плацебо-контролируемые исследования отсутствуют. данные.
Эпидуральная анестезия (ЭА) широко используется для индукции обезболивания в в периоперационный период, а также для уменьшения боли у пациентов с ОП. В принцип действия был приписан блокаде симпатического нерва, который перераспределяет внутренний кровоток к неперфузируемым областям поджелудочной железы. В исследовании с участием 35 пациентов с прогнозируемым тяжелым ОП, ЭА значительно уменьшала болевые ощущения, улучшала перфузия поджелудочной железы на основе радиологических исследований перфузии и улучшения клинических исходы (снижение потребности в некрэктомии) (113).Проспективное исследование 121 пациента продемонстрировало хорошую эффективность. и безопасность EA у взрослых AP (114).
Резюме: Нет данных, обеспечивающих оптимальную боль управление в педиатрической АП. Исследования на взрослых не выявили ни одного превосходящего медикамент. Нет доказательств, подтверждающих утверждение, что морфин вызывает неблагоприятные события на сфинктере Одди.
Рекомендации 2ci: Внутривенный морфин или другой препарат опиоид следует использовать при острой боли при панкреатите, не реагирующей на ацетаминофен или НПВП.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 2cii: Услуги специалиста по острой боли в идеале следует проконсультироваться в случаях более сильной боли, чтобы уменьшить боль управление.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2d. Энтеральное и парентеральное питание при остром панкреатите у детей
Пероральное и энтеральное питание
Традиционно пациенты с ОП лечились, не вводя перорально (115) и давая парентеральное питание (PN) (116).Было высказано предположение, что отдыхая кишечник, поджелудочной железе дали «отдохнуть» и, таким образом, зажить быстрее. В Обоснованием этой теории было то, что наличие пищи в кишечнике стимулируют высвобождение холецистокинина (ХЦК), что, в свою очередь, стимулирует поджелудочную железу. секреция ферментов, что может привести к дальнейшей активации протеолитических ферментов и преувеличивают процесс самопереваривания и усугубляют травму (117, 118)
У взрослых проводится ряд контролируемых исследований, обзоров и метаанализов. лечебному питанию как при тяжелом, так и при легком ОП, включая обзор голландских Группа по изучению панкреатита и согласованные рекомендации, опубликованные Международный комитет по руководящим принципам консенсуса (119).Lodewijkx et al., Считают, что энтеральное питание превосходит парентеральное питание, а стратегия кормления по требованию в прогнозируемой тяжелый АП (120). Мирталло и др. Рассмотрели 8 социальные отчеты с целью разработки международных согласованных руководящих принципов по питанию терапия в АП (119). Они пришли к выводу, что в АП у взрослых, энтеральное питание (ЭП) было предпочтительнее, чем ПП, и его следует использовать в первую очередь даже при наличие свищей, асцита и псевдокист.
Рекомендуется начинать EN как можно раньше, тем более, что одна из целей энтеропатии — предотвратить бактериальную транслокацию и тем самым предотвратить развитие ССВО.Ранняя нутритивная терапия также предназначена для снизить цитокиновый ответ и частоту пареза желудка и кишечной непроходимости. В то время как некоторые исследования (121) не показывают разницы в исходы, когда ЭП была начата до или после 72 часов презентации, 2008 г. метаанализ, изучавший одиннадцать РКИ, показал, что ЭП началась в течение 48 часов после презентация значительно снизила показатели смертности, инфекций и полиорганной отказ по сравнению с PN (122). Эти эффекты были уменьшены, когда ЭП была начата через 48 часов.В обзоре питания за 2011 г. поддержка взрослых AP, был сделан вывод, что ранняя нутритивная поддержка, особенно ЭП, но также и ПП, уменьшали количество осложнений и улучшали выживаемость (123). В этом обзоре говорилось, что для его эффективности нутритивная поддержка должна была начаться в течение 72 часов. Было заявлено, что EN следует считается « активным терапевтическим вмешательством, улучшающим исход больных панкреатитом »(124).
Клинические исследования, сравнивающие результаты PN и EN у пациентов с AP сообщить, что использование EN при тяжелом остром панкреатите (SAP) или прогнозируемые результаты SAP значительно снижает частоту осложнений (125–133).Недавний метаанализ продемонстрировал превосходство ЭП по сравнению с ПП с меньшей частотой инфекции и полиорганной недостаточности, что приводит к снижению показателей смертности и сокращению пребывание в больнице (134). Однако, поскольку полный EN не всегда возможно во время AP из-за усиления боли или непереносимости кормления, некоторые отстаивают роль комбинации EN и PN. В одном исследовании рандомизировали 100 пациентов для получения только ПП по сравнению с ПП в комбинации только с ЭП или ЭП, сепсис, внутрибрюшная инфекция и продолжительность госпитализации снизились, когда ЭП была входит в состав руководства (135).
Описанные пути ЭП включали желудочный и тощей кишки. Два маленьких исследования не обнаружили разницы в результатах между назогастральным (НГ) и назоеюнальным (НД) сытые группы (136, 137). Мета-анализ 10 РКИ не показал различий в исходы между группами, получавшими (полу) элементарные и полимерные формулы. (138)
Никаких руководств по нутриционной поддержке дети с АП. Недавнее исследование Abu-El-Haija et al. продемонстрировал выполнимость установления энтерального питания в педиатрической АП, не усложняя курс или влияя на оценку боли AP (139).Из того же центра ретроспективное исследование показало, что сочетание раннего энтерального кормления плюс более чем 1,5-кратное поддерживающее внутривенное введение жидкости были связаны с более коротким продолжительность пребывания и более легкое заболевание по сравнению с теми, кто оставался НКО в течение 48 часов и имели более низкую частоту ЭКО, чем поддерживающую терапию (73). Сообщается о двух детях с тяжелым ОП, которые успешно вылечились. с назоеюнальным кормлением в отделении интенсивной терапии интенсивной терапии и переключением на пероральное кормление при выписке в общая палата (140).
Парентеральное питание
Родительское питание обеспечивает организм необходимыми калориями и питательными веществами. компенсировать катаболическое состояние.Обеспокоенность, что ПП может стимулировать поджелудочную железу. и приводить к преувеличению процесса самопищеварения не было подтверждено литература (141, 142). Данные показывают, что настой протеина не стимулируют секрецию поджелудочной железы (143). Когда при сравнении различных форм ПП, сообщалось, что ПП, усиленный глутамином, снизить общую частоту осложнений, а также сократить продолжительность пребывания в стационаре (144–148). Введение глюкозы внутривенно также не стимулирует секреция поджелудочной железы (149, 150).Инфузия глюкозы тяжелобольным пациентам может быть полезно для обеспечения легкодоступного источника энергии во время катаболического состояния и противодействуют глюконеогенезу из-за распада белка. Но настой глюкозы обязательно под наблюдением, так как это может предрасполагать к гипергликемии (151), поскольку воспаленная поджелудочная железа может не подавать соответствующий инсулин отклик.
Гипертриглицеридемия связана с тяжелым ОП (152–155), но механизм, ведущий к SAP, не ясен (156). Недостаточно данных, чтобы рекомендовать или препятствовать использованию парентеральные липиды при АП.
Что касается времени PN в AP, где измеренный результат был смертности, данные свидетельствуют о том, что раннее ПП значительно более полезно, чем покой кишечника. при тяжелом ОП у взрослых (122). Во всех случаях, когда ЭП невозможна в течение длительного времени, например, при кишечной непроходимости, сложных свищах и т. Д. синдром брюшного отдела, PN. Напротив, недавнее исследование выступал за отсрочку начала ПП до 7 дней у тяжелобольных детей из-за повышенный риск инфицирования и повышенная частота осложнений после начала ПП в течение первых 24 часов после пребывания в отделении интенсивной терапии.Раннее энтеральное питание было разрешено в обоих группы. Однако присутствие или процент пациентов с ОП конкретно не было указано в этом отчете (157).
Резюме: Литература для взрослых поддерживает раннее энтеральное питание, чтобы уменьшить осложнения AP и улучшить выживаемость. Педиатрическая литература поддерживает раннее энтеральное питание в легких случаях ОП и небольшое сообщение в тяжелых случаях AP.
Рекомендация 2di: За исключением наличия прямого противопоказания к употреблению кишечника, детям с острым панкреатитом легкой степени может помочь от раннего (в течение 48–72 часов после обращения) орального / энтерального питания до уменьшения продолжительность пребывания и снижение риска органной дисфункции.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2dii: Парентеральное питание (ПП) должно следует рассматривать в тех случаях, когда ЭП невозможна в течение длительного периода времени (дольше более 5-7 дней), например, в кишечной непроходимости, сложных свищах, брюшной полости синдром, снижающий катаболическое состояние организма. Следует начать энтеральное питание. как можно скорее, причем комбинация EN и PN превосходит одиночную PN.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15 согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2diii: В случае панкреатической разрыв, перелом или разрыв протока, неясно, является ли пероральное / энтеральное питание может быть вредным в острой фазе. Это требует дальнейшего изучения.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 13; согласен = 8; нейтральный = 2; не согласен = 0; категорически не согласен = 0; нет голоса = 1.
2д. Использование антибиотиков при остром панкреатите у детей
Обоснование использования антибиотиков при лечении ОП связано к беспокойству по поводу бактериальной инфекции из-за перемещенной кишечной микробиоты. Антибиотики не рекомендуются для взрослых с легким ОП (70).
При лечении тяжелого ОП у взрослых изучались антибиотики для предотвращения и управлять инфекциями. Имипенем и / или цефалоспорины третьего поколения были наиболее исторически часто использовались в попытке снизить заболеваемость и смертность.Этот Профилактический подход является спорным: предыдущие исследования предполагали пользу (158–160), в то время как другие исследования не продемонстрировали пользы от рутинного использования (161) в отсутствие документально подтвержденной инфекции. Профилактические антибиотики использовались в условиях стерильной некротической болезни. панкреатит для предотвращения инфицированного некротического панкреатита (162, 163), особенно имипенем (163). Однако систематические обзоры не поддерживает преимущества в отношении смертности от инфекций, не затрагивающих поджелудочную железу, или для сокращения хирургических вмешательств у взрослых (162).Более поздние метаанализы подтверждают использование антибиотиков для инфицированы некротическим панкреатитом, но не для стерильный некроз (164–166). Текущий взрослый AP рекомендации — использовать антибиотики только при инфицированном некрозе или у пациентов с некротический панкреатит, госпитализированные и без клинического улучшения использование антибиотиков (70). Зараженный некроз должен быть подозревается, если клиническое состояние пациента ухудшается из-за лихорадки или наличие газа в коллекциях на снимках.В определенных ситуациях стремление жидкость под контролем эндоскопии или с помощью интервенционной радиологии и для руководства лечением может потребоваться создание соответствующего дренажа (8). При некротическом панкреатите известные антибиотики: проникают в некротические ткани, такие как карбапенемы, хинолоны и метронидазол, поскольку использование антибиотика в этих условиях, как было показано, задерживает хирургическое вмешательство. вмешательства и снизить заболеваемость и смертность (33).
Документированные инфекции, происходящие за пределами поджелудочной железы, следует рассматривать как указано.
Не было опубликовано исследований по использованию антибиотиков для лечения АП у детей.
Резюме: Антибиотики нельзя использовать в лечение ОП, за исключением случаев документально подтвержденного инфицированного некроза или у пациентов с некротическим панкреатитом, которые госпитализированы и клинически не улучшаются без использование антибиотиков. Антибиотики, о которых известно, что они проникают в некротические ткани, следует использовать при лечение инфицированного панкреонекроза, поскольку это может отсрочить хирургическое вмешательство и снизить заболеваемость и смертность.
Рекомендации 2ei: Профилактические антибиотики не эмпирически рекомендуется при тяжелом остром панкреатите.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
Рекомендация 2eii: показано только использование антибиотиков. в случаях документально подтвержденного инфицированного некроза при остром панкреатите.
16/24 = 67% согласны с рекомендацией. Рекомендация не поддерживается.Это было определено как область особых разногласий, требующих дальнейшего учиться.
Результаты голосования: Полностью согласен = 10; согласен = 6; нейтральный = 2; не согласен = 4; категорически не согласен = 0; нет голоса = 2.
2f. Использование ингибиторов протеазы при остром панкреатите у детей
Поскольку AP предположительно является некровоспалительным процессом, начавшимся через острая и несоответствующая активация трипсина протеазы и зимогенов поджелудочной железы внутри паренхимы, исследователи были очень заинтересованы в блокировании этого воспалительный процесс, чтобы ограничить степень травмы.
Два основных соединения, описанных в литературе для ингибирования этого фермента активация включает ингибитор сериновой протеазы габексат мезилат и трипсин ингибитор апротинин. В 1993 году Pederzoli et al. сообщил результаты рандомизированного, двойное слепое многоцентровое клиническое исследование использования габексата мезилата по сравнению с апротинином в АП-терапия. В этом исследовании мезилат габексата оказался более предпочтительным по сравнению с апротинином в отношении период 24–72 часа, но, что важно, отсутствует контрольная группа плацебо (167).Сроки лечения и способ родоразрешения кажутся быть ключевыми факторами эффективности (167, 168). Ино и др. изучили эффективность непрерывного инфузия регионарной артерии CRAI с габексатом мезилатом и антибиотиками при тяжелом ОП через небольшое проспективное исследование с участием 9 пациентов, получавших CRAI в течение 3-5 дней и 9 пациентов. другие получают терапию системными ингибиторами протеазы и антибиотики. Боль в животе и SIRS исчезал быстрее, LOS был значительно короче в группе CRAI (168). CRAI антипротеаз и антибиотиков имеет Сообщалось о снижении показателей CRP и APACHE II при применении в течение 72 часов после начала болезни (169), подход, описанный в педиатрических больных (170).
Обзор 2007 года, проведенный Китагавой и Хаякавой, не нашел доказательств, оправдывающих рутинное использование антипротеаз при AP, и хотя использование непрерывного внутривенного ингибиторы протеазы и антибиотики в высоких дозах могут быть эффективными для предотвращения обострения тяжелого ОП, необходимы исследования экономической эффективности. Важно, эти соединения не одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США. Штаты (171–173).
Резюме: Некоторые исследования взрослых подтверждают использование антипротеаз в лечении тяжелого АП, но никаких конкретных рекомендаций никогда не было были сделаны для их использования.Исследования не были рандомизированы с контрольными группами плацебо, и только несколько случаи описаны в педиатрических больных.
Рекомендации 2f: Антипротеазы не могут быть рекомендуется при лечении острого панкреатита у детей в это время.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 7; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2г. Использование антиоксидантов при остром панкреатите у детей
Окислительный стресс способствует повреждению ОП из-за образования кислорода свободные радикалы, вызывающие повреждение липидной мембраны клетки поджелудочной железы, деполяризацию митохондриальной мембраны и индукции фрагментации ДНК (174).Это способствует отеку, возникновению боли и может также быть вовлеченными в процесс некроза. Таким образом, была выдвинута гипотеза об антиоксидантах. иметь потенциальную пользу в качестве дополнительного лечения при АП, предотвращая образование свободные радикалы или улавливание существующих свободных радикалов кислорода.
Наиболее изученными агентами были витамины-антиоксиданты (аскорбиновая кислота, α-токоферол, β-каротин), неорганические антиоксиданты (селен) и глютамин. В двух частично совпадающих метаанализах, опубликованных в 2015 г., используются разные методологии оценки пользы антиоксидантов при остром панкреатите, один обзор 11 и другие 12 рандомизированных контролируемых исследований на взрослых [169, 170].Pederzoli et al. Обнаружили, что антиоксиданты снижают количество осложнений, связанных с ОП, и укороченный LOS с глутамином, снижающим частоту осложнений и смертность [169]. Ино и др. Сообщили, что антиоксидант терапия сокращает LOS и снижает уровень СРБ в сыворотке, но только через 10 дней [170].
Существенным ограничением опубликованных данных об антиоксидантах у взрослых AP является эти испытания включали весь спектр легкого и тяжелого АД. Кроме того, различные комбинации антиоксидантов и время доставки были использованы в испытания.В крупных рандомизированных исследованиях также отсутствует стандартизация конкретных антиоксидантов. как сроки и продолжительность лечения.
Нет данных об использовании антиоксидантов при AP в педиатрической популяции.
Резюме: педиатрические данные об использовании не хватает антиоксидантов в АП. Публикации для взрослых демонстрируют значительную неоднородность относительно состава, времени и продолжительности терапии. Несмотря на потенциальные преимущества описанных в сериях для взрослых, доказательств недостаточно, чтобы поддержать их использование в педиатрия в это время.
Рекомендация 2g: Антиоксиданты не следует считается стандартной терапией при лечении острого панкреатита у детей.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
2ч. Роль пробиотиков в лечении острого панкреатита у детей
Примерно у трети взрослых пациентов может развиться тяжелая форма АП, характеризующаяся ССВО, органная недостаточность и повышенный риск инфицирования (175).У пациентов с инфицированным перипанкреатическим и панкреонекрозом риск летального исхода значительно увеличивается. Снижение проницаемости кишечника и Предполагается, что избыточный бактериальный рост во время AP снижает риск инфицирования некроз поджелудочной железы и тем самым снизить риск смерти (176, 177).
Всемирная организация здравоохранения определяет пробиотики как «живые микробы. которые при введении в адекватных количествах приносят пользу их здоровью. хозяин». Доказано, что пробиотики играют роль в поддержании микрофлоры кишечника. баланс, подавляя рост вредных бактерий и усиливая иммунную функцию (178).Важно, что опубликованные исследования использовали различные составы и режимы дозирования пробиотических бактерий.
Muftuoglu et al. продемонстрировали, что lactobacillus acidophilus и bifidobacterium lactis уменьшают тяжесть гистологического повреждения в экспериментальной модели панкреатита (178). Ранние небольшие клинические испытания для взрослых показали положительную роль пробиотиков в управление АП. Olah et al. рандомизировали 45 пациентов для приема 10 9 живые или убитые теплом lactobacillus plantarum два раза в день вместе с энтеральное питание (179).Они обнаружили статистически значительно более низкий риск инфицированного панкреонекроза в исследуемой группе по сравнению с контрольные группы.
Однако впоследствии исследование PROPATRIA, двойное слепое, плацебо-контролируемое рандомизированное многоцентровое исследование роли пробиотиков в профилактике инфекционные осложнения при ОП) в составе 298 взрослых пациентов с прогнозируемой тяжелой AP продемонстрировал значительно более высокий риск смерти у многовидовых пробиотиков. группа (180, 181). Два небольших рандомизированных испытания с момента завершения не продемонстрировали увеличение смертности (182, 183), но влияние неблагоприятных результатов исследования PROPATRIA Исследование привело к общей осторожности при использовании пробиотиков у взрослых с ОП.
Ни одно педиатрическое исследование не изучало роль пробиотиков у детей с AP.
Резюме: После серии небольших дел, предполагающих потенциальная польза пробиотиков при ОП у взрослых, большое рандомизированное исследование продемонстрировало повышенная смертность в группе пробиотиков. Педиатрических исследований не опубликовано.
Рекомендации 2 часа: Нельзя рекомендовать пробиотики в лечении острого панкреатита у детей в настоящее время. Высшее качество опубликованные данные для взрослых показывают, что они могут не только не принести пользы, но и увеличивать смертность.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 14; согласен = 9; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2i. Роль эндоскопии в лечении острого панкреатита у детей
Различные причины воспаления слизистой оболочки двенадцатиперстной кишки связаны с увеличением риск AP. Проявления, связанные с глютеновой болезнью поджелудочной железы, включают эндокринные и внешнесекреторная недостаточность, острый и хронический панкреатит, нарушение питания, папиллярный стеноз вторичный по отношению к дуодениту или иммунологическим нарушениям, и все предположили, что быть вовлеченными механистически (184–186).Желчнокаменная болезнь была обнаружена до 34% пациентов с болезнью Крона и может проявляться как АП (187). Аутоиммунный панкреатит (АИП) и первичный склерозирование холангит (188) также может быть обнаружен у пациентов с воспалительным заболеванием кишечника, проявляющимся AP (189–191). Повышение уровня IgG4 наблюдается у взрослых пациентов с AIP типа I, педиатрические пациенты с AIP обычно без повышения уровня IgG4, при биопсии двенадцатиперстной или желудочно-дуоденальной воспалительной поражения могут быть полезны в диагностике (192, 193).Были случаи острого и хронического панкреатита. редко регистрируется как проявление или ассоциация инфекции H. pylori (194, 195). Чрезвычайно редко возможными причинами панкреатита у детей являются опухоли, связанные с ампула или периампулярная область двенадцатиперстной кишки. Такие поражения могут быть первыми идентифицируется рентгенологическим исследованием, но также может быть обнаружено во время эндоскопического исследования. оценка. Судя по имеющимся историям болезни, механизм развития у этих пациентов рецидивирующий панкреатит до конца не изучен, но, вероятно, связан с опухолью непроходимость на уровне ампулы (196, 197).Но в целом роль эзофагогастродуоденоскопия при ОП ограничена.
Нет исследований, оценивающих показания или преимущества эзофагогастродуоденоскопии в педиатрический AP.
Резюме: Роль эндоскопии в неотложной помощи дети с AP неясно. Возможность первичных внепанкреатических заболеваний В результате разработка AP требует вдумчивого рассмотрения.
Рекомендации 2i: Эзофагогастродуоденоскопия не в настоящее время считается стандартным диагностическим инструментом при остром панкреатите у детей.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2j. Роль ЭРХПГ при остром панкреатите у детей
Роль ЭРХПГ при ОП эволюционировала с технологическими улучшениями в диагностические возможности МРТ / MRCP и с увеличением педиатрического опыта с эндоскопическое ультразвуковое исследование (ЭУЗИ). Благодаря наличию этих последних диагностических инструментов для при заболеваниях поджелудочной железы, ERCP все чаще используется в первую очередь для лечения вмешательства или для неясных диагнозов после MRCP или EUS.ЭРХПГ безопасна для детей при этом наиболее частым осложнением является легкий панкреатит после ЭРХПГ. аналогичны таковым у взрослых (~ 3–10%), когда выполняются опытные эндоскописты (198–206). Обструкция желчевыводящих путей и хронический панкреатит являются наиболее частыми показаниями к ЭРХПГ у детей. В педиатрической AP ERCP имеет ограниченная роль, выполняется почти исключительно при билиарном панкреатите, вторичном по отношению к холедохолитиаз или отстой. ЭРХПГ при холедохолитиазе без панкреатита безопасна и эффективны (207, 208), но в педиатрии нет конкретных рекомендаций по сроки проведения ЭРХПГ при холедохолитиазе или остром билиарном панкреатите.У взрослых большой метаанализ и научно обоснованные рекомендации IAP по ведению острых билиарный панкреатит рекомендовал ЭРХПГ в течение 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. В противном случае можно провести ЭРХПГ. планово при неосложненном холедохолитиазе и в других случаях желчевыводящих путей. панкреатит независимо от степени тяжести (209, 210).
Менее распространенными показаниями для ЭРХПГ при ОП являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы (211).Камни и стриктуры протоков поджелудочной железы обычно признаки острого рецидивирующего или хронического панкреатита, поэтому встречаются относительно редко показания к ЭРХПГ при АП. В редких случаях, когда непроходимость протока предотвращает разрешение панкреатита, может быть проведена терапевтическая ЭРХПГ. Псевдокисты поджелудочной железы в у детей может развиться острый или хронический панкреатит, но чаще всего возникает после тупая травма. Псевдокисты поджелудочной железы представляют собой однородное скопление панкреатической жидкости. окружены фиброзной или грануляционной тканью, но не имеют эпителиальной выстилки (15, 212), и может развиться из скоплений жидкости, сохраняющихся более 4 недель (213).ERCP может использоваться для оценки коммуникации псевдокиста с протоком поджелудочной железы, куда можно установить транспапиллярный стент для дренаж. В противном случае — эндоскопическая цистагастростомия (214–216) и под контролем EUS. дренаж (217) — безопасные и эффективные способы дренировать псевдокисты поджелудочной железы у детей и может быть рассмотрено в зависимости от расположения псевдокиста. Повреждение протока поджелудочной железы и утечка также могут возникнуть в результате травмы. Рано эндоскопическое или хирургическое вмешательство может помочь свести к минимуму продолжающуюся заболеваемость протоковым утечка, поскольку ERCP обеспечивает быстрый и более точный метод определения местоположения и степень повреждения, чем MRCP или CT, а также дает возможность терапевтического стента размещение поперек травмы (218, 219).
Резюме: Роль ЭРХПГ при остром панкреатите. в первую очередь относится к терапевтическому лечению билиарного панкреатита, вторичного по отношению к холедохолитиаз или отстой. Литература для взрослых предполагает эффективность ERCP в пределах 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. Менее распространенными показаниями к ЭРХПГ при остром панкреатите являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы или разрывы протока.
Рекомендации 2ji и 2jii: (2ji) Роль ERCP ограничен при остром панкреатите и зависит от местных знаний.(2jii) ERCP — это показан при лечении острого панкреатита, связанного с холедохолитиазом, вызывающим билиарный панкреатит и патологии протоков поджелудочной железы, такие как протоковые камни или протоки протока.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 21; согласен = 3; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2к. Роль EUS при остром панкреатите у детей
Эндоскопическое ультразвуковое исследование (EUS) использовалось для определения этиология АП.EUS не только всесторонне оценивает паренхиму поджелудочной железы и протока, но также и гепато-билиарной анатомии. Заболевания желчевыводящих путей, такие как холедохолитиаз можно оценить с помощью EUS, особенно когда трансабдоминальное УЗИ не позволяет визуализировать дистальный общий желчный проток. EUS также может определить наличие микролитиаза у желчный пузырь, который часто не визуализируется при трансабдоминальном УЗИ или КТ сканировать. Микролитиаз может привести к ОП и лечится холецистэктомией (220). Хотя у детей это случается крайне редко, опухоли поджелудочной железы, которые могут быть вызваны новообразованием поджелудочной железы или AIP, могут проявляться с AP и пройти дальнейшее обследование с помощью EUS с возможностью взятия пробы ткани поджелудочной железы. (221, 222).
Терапевтическая роль EUS при AP в основном ограничена для лечения осложнения АП, а именно скопление жидкости поджелудочной железы или некроз стенок. EUS имеет было показано, что он полезен при лечении скоплений жидкости поджелудочной железы / некроза вторичный по отношению к тяжелому AP. Считается, что спонтанное рассасывание псевдокист происходит чаще. чаще у детей, чем у взрослых, особенно если размер <5 см (мнение эксперта). Таким образом, с большинством коллекций любого типа можно обращаться консервативно и терапевтически. вмешательство не требуется в остром состоянии, за исключением случаев наличия инфекции (223).Однако, если происходит созревание (обычно через 4–6 недель) саморегулирование менее вероятно, и пациент может нужен эндоскопический дренаж. Другие показания к вмешательству EUS и дренированию включают: большой размер при возникновении клинических симптомов, подозрении на заражение скоплений или стойких симптомы от псевдокисты. Дренаж под контролем EUS и создание цистгастростомы было продемонстрировано, что он столь же эффективен и безопасен, как хирургическая цистгастростомия, и имеет было показано, что он эффективен даже у детей (224).
Резюме: на основании литературы для взрослых, EUS может быть полезным для определения этиологии острого панкреатита, которая может включать диагностику дистального камни общего желчного протока, новообразования поджелудочной железы или аутоиммунный панкреатит. Его роль для терапия в основном ограничена лечением осложнений острого панкреатита, а именно скопления жидкости поджелудочной железы или некроз стенок, вторичный по отношению к тяжелому АД.
Рекомендация 2k: EUS не считается стандартом диагностический инструмент при остром панкреатите у детей в настоящее время.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2L Роль хирургии / хирургической консультации при остром панкреатите у детей
Хирургические вмешательства не являются частью алгоритма ведения больного. Типичный эпизод АП. Публикации относятся к взрослому опыту. Раннее указание на хирургия включает лечение синдрома брюшной полости.Однако управление некроз поджелудочной железы с ранней некрэктомией в течение первых 72 часов, как было показано, приводит к повышенная заболеваемость и смертность по сравнению с отсроченными сроками не менее чем на 12 дней (225). Руководящие принципы Международного Ассоциация панкреатологов с 2002 г. предлагает отложить операцию некрэктомии для по крайней мере, через 3-4 недели после начала заболевания снижает заболеваемость и смертность (210). Руководящие принципы ACG 2013 года по управлению взрослый AP прокомментировал возможность хирургического вмешательства в связи с желчнокаменной болезнью. панкреатит, санация некроза (инфицированные vs.стерильный), и малоинвазивный лечение некроза поджелудочной железы (33). Рекомендации включали раннюю холецистэктомию во время той же госпитализации по поводу легкий приступ желчнокаменного панкреатита и обсуждение между гастроэнтерологами и хирургия для выбора времени холецистэктомии по сравнению с другими терапевтическими вариантами в случаях тяжелый АД, особенно с некрозом. Для пациентов с сохраняющейся клинической нестабильностью и ухудшение состояния на фоне некроза поджелудочной железы, дренирование может потребоваться для улучшить статус пациентов и снизить заболеваемость и смертность.Руководящие принципы АЧГ предлагают что санацию некроза следует отложить, когда это возможно, в идеале более четырех недель с момента обращения, чтобы лучше организовать воспалительные реакции. Даже в необходимость некрэктомии, менее инвазивных методов, включая чрескожную радиологию, или следует рассмотреть возможность эндоскопического дренирования / хирургической обработки раны наряду с лапароскопическим хирургическим вмешательством. предпочтение отдается лечению перед открытым хирургическим вмешательством (33).
Исследование PONCHO 2015 г. с участием 266 стационарных пациентов, рандомизированных по интервалу холецистэктомия или холецистэктомия с тем же госпитализацией также поддерживали ту же госпитализацию. холецистэктомия снизила частоту повторных осложнений, связанных с желчнокаменной болезнью, у взрослых пациенты с желчнокаменным панкреатитом легкой степени с очень низким риском холецистэктомии осложнения (226).
В случае тяжелой травмы живота, требующей неотложной лапаротомии (в том числе дорожно-транспортных происшествий) следует искать повреждения поджелудочной железы, в том числе вовлекающий проток поджелудочной железы. Тяжесть травмы поджелудочной железы может быть оценена в соответствии с Американской ассоциации хирургии травм поджелудочной железы по шкале, в которой 5 могут быть присвоены степени травмы (227). Выше травмы поджелудочной железы в результате травмы, как правило, также включают ассоциированную дуоденальную травмы. Пациентам с более легкими тупыми травмами I и II степени можно лечить в нерабочем состоянии.В случае травмы поджелудочной железы мультидисциплинарный подход, включающий: показаны бригады врачей / гастроэнтерологов и хирургов.
В педиатрической литературе о показаниях к операции гораздо больше ограничено. Что касается билиарного панкреатита, ретроспективная серия случаев из 19 детей, госпитализированных с билиарным панкреатитом, зарегистрировано 9 детей, перенесших ранний холецистэктомия без побочных эффектов и 4 из 10 детей, перенесших отсроченную операцию возникновение нежелательных клинических явлений (включая рецидив панкреатита) (228).
Резюме: Показания к острому хирургическому вмешательству. к показаниям АП относятся травмы живота, при которых у пациента нестабильность и / или поиск происходит сопутствующее повреждение других органов. В контексте билиарного панкреатита было показано, что холецистэктомия не только безопасна, но и предотвращает рецидивы, если они происходят. в рамках индекса госпитализации. Литература для взрослых предполагает, что раннее вмешательство в некроз поджелудочной железы приводит к увеличению заболеваемости и смертности, и, следовательно, к санации раны желательно отсрочить некроз поджелудочной железы, вызывающий нестабильность у пациента, по крайней мере, на 4 часа. недель с момента обращения, в идеале — эндоскопическим или чрескожным способом.
Рекомендация 2li: холецистэктомия безопасно может и следует выполнять перед выпиской в случаях легкой неосложненной острой желчной болезни. панкреатит.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2lii: В ведении острых некротических скоплений, вмешательств следует избегать и откладывать, даже для инфицированных некроз, поскольку результаты лучше при отсроченном (> 4 недель) подходе.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 6; нейтральный = 2; не согласен = 1; категорически не согласен = 0.
Рекомендация 2liii: Когда требуется дренирование или некрэктомия. необходимые нехирургические доступы, включая эндоскопические (EUS и ERCP) или чрескожные методы предпочтительнее открытой некрэктомии или открытой псевдокисты дренаж.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 9; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
3. ИСХОДЫ ОСТРОГО ПАНКРЕАТИТА ПЕДИАТРИИ
Общие исходы ОП у детей благоприятны по сравнению со взрослыми. В средняя продолжительность госпитализации детей с ОП составляет в среднем от 2,8 до 8 дней, хотя младенцы / малыши, как правило, поступают на более длительный период времени (в среднем 19,5 дней) (15, 73, 229–231). Раннее начало энтерального питания и агрессивная жидкостная реанимация был связан с более коротким пребыванием в больнице, меньшим количеством госпитализаций в отделения интенсивной терапии и снижение показателей тяжелого АП по сравнению с пациентами, находящимися в НКО (73).Эти результаты в целом совпадают с выводами большинства взрослых. исследований (232), но, возможно, не применялись к педиатрические пациенты до недавнего времени. Более высокая смертность при ПД у детей связана с системное заболевание, но в целом низкий и составляет менее 5% в большинстве когорт, даже в том числе в реанимации (15, 30, 233, 234).
Осложнения с ранним началом при ОП включают полиорганную дисфункцию или шок (15). Острые скопления перипанкреатической жидкости наблюдаются в острая фаза панкреатита и имеет тенденцию к спонтанному разрешению.Частота образование псевдокист колеблется от 8% до 41% у детей с панкреатитом, и более высокие показатели наблюдаются у пациентов с панкреатитом, связанным с абдоминальной травма (15, 212, 235). Псевдокисты часто бессимптомный и может лечиться консервативно или стать больше и вызвать боль в животе, рвота или лихорадка. Они также могут заразиться в 10–15% случаев. (236). Еще одно осложнение с поздним началом связано с до некроза поджелудочной железы. Некроз может проявляться в первую очередь в виде острого некротического скопления. (ANC), а затем созревают до некроза без стенок (WON) (8).Варианты лечения при дренировании псевдокист и некротических стенок коллекции включают эндоскопический (транспапиллярный или трансмуральный) дренаж, чрескожный катетерный дренаж или открытая / лапароскопическая операция. Выбранная модальность зависит от размера, расположение, анатомия и риски / преимущества процедуры, хотя чрескожная и Трансгастроинтестинальный дренаж под контролем эндоскопического ультразвука (ЭУЗИ) в настоящее время становится все более популярным. широко распространено (237).
Примерно 15–35% детей с острым у панкреатита будет еще один приступ панкреатита.Острый рецидивирующий заболевание у детей панкреатит связан с панкреатико-билиарными аномалиями, аутоиммунным панкреатитом, нарушения обмена веществ и наследственный панкреатит (15).
Резюме: За детьми необходимо следить во время их курс АП при местных и системных осложнениях, которые могут включать дисфункцию органов, острые скопления жидкости и впоследствии некроз или псевдокисты. Общий педиатрические пациенты с острым панкреатитом имеют хороший прогноз с очень низким уровнем смертность, но сообщается о частоте рецидивов до 15–35%.
Рекомендация 3: Дети с острым панкреатитом должны получить тщательное наблюдение со стороны поставщика медицинских услуг для выявления раннего или позднего осложнения или рецидивы.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
A Clinical Отчет Комитета по поджелудочной железе NASPGHAN
1. ПЕРВОНАЧАЛЬНАЯ ОЦЕНКА И ДИАГНОСТИКА ОСТРОГО ПЕДИАТРИЧЕСКОГО ПАНКРЕАТИТА
Недавние исследования оценивают заболеваемость острым панкреатитом (ОП) при ~ 1/10 000 детей в год (2, 7), заболеваемость приближается к взрослым.Есть нет научно обоснованных руководств по диагностике ОП у детей. ВДОХНОВЕНИЕ ( IN международный S tudy Группа компаний P медицинский P анкреатит: I n Найдите Cu RE ) определение детской AP является экспертное определение смоделировано по критериям Атланты у взрослых (8). Согласно критериям INSPPIRE, для диагностики АП требуется как минимум 2 из следующего: (1) боль в животе совместима с AP, (2) значениями сывороточной амилазы и / или липазы ≥3 раза верхние пределы нормы, (3) визуализация результаты согласуются с AP (9, 10).INSPPIRE или другие критерии не касаются этапов (ранних или поздний) АП у детей или типов (интерстициальный отечный панкреатит, некротический панкреатит, инфицированный панкреонекроз) или степень тяжести ОП (легкая, умеренная или тяжелая форма ОП при мультисистемной органной недостаточности).
Детский диагноз ОП обычно подозревается клинически с совместимым симптомом презентации, подтвержденные лабораторными и / или радиологическими исследованиями. Боль в животе и / или раздражительность являются наиболее частыми проявлениями ОП у детей, за которыми следуют эпигастральные болезненность, тошнота и рвота (11, 12).У младенцев и детей ясельного возраста симптомы могут быть незаметными; поэтому диагноз требует высокого уровня подозрений. Желчные / обструктивные факторы, лекарственные препараты и системные заболевания являются основными причинами ОП у детей (1, 4, 9, 12–23), и знание этих возможных причин поможет руководить начальными исследованиями.
Процент детей, у которых развиваются «тяжелые» острые панкреатит варьирует в опубликованных сериях (6–34), но дети с ОП в в целом имеют легкое течение (11, 24, 25). В подмножестве у пациентов АП может иметь тяжелое течение (8), но нет установленные клинические инструменты предсказывают этот результат.Балльные системы оценки степени тяжести АП у взрослых (Рэнсон, Глазго, модифицированный Глазго, Прикроватный индекс тяжести острых заболеваний). Панкреатит (BISAP) и оценка острой физиологии и хронического здоровья II (APACHE II)) не легко применимы к детям по нескольким причинам (26). Детская шкала острого панкреатита (PAPS) ДеБанто (27) была оценена у детей, но имеет низкую чувствительность. и требует 48 часов для прогнозирования рисков. Точно так же степень тяжести компьютерной томографии индекс (CTSI) или балл Бальтазара (28), опирается на радиологический внешний вид и, следовательно, нежелателен в детской возрастной группе из-за радиации экспозиция.Благодаря своей широкой доступности липаза является привлекательным маркером для выявления тяжелых случаев AP (25), но может выявить много ложных положительных из-за его низкой положительной прогностической ценности и специфичности. Коффи и др., обнаружили, что липаза сыворотки в семь раз превышает верхний предел нормы в течение 24 часов после презентация помогла предсказать тяжесть острого панкреатита (25). Тем не менее, это ретроспективное исследование с участием 211 детей и не были проверены в более крупных исследовательских группах. Suzuki и др. В Японии разработали удобная для детей система оценки степени тяжести с использованием 9 параметров (29), но это также было ретроспективным исследованием, в котором оценивались только 145 пациентов, и авторы пришли к выводу, что результаты не могут быть широко применимы к педиатрическое население.Совсем недавно Сабо и др. Сообщили, что ранняя степень тяжести прогностическая модель с использованием сывороточного альбумина, липазы и количества лейкоцитов, полученных в 24 часа продемонстрировали положительную прогностическую ценность 35% и отрицательную прогностическую ценность значение 91% (30).
Необходимы дальнейшие проспективные исследования для определения клинической применимости любой из этих инструментов. В вышеупомянутых исследованиях использовались различные определения степени тяжести. AP, что ограничивает возможности проведения сравнений между исследованиями. Недавняя публикация Комитет по поджелудочной железе NASPGHAN обратился к необходимости иметь четко определенную классификацию степени тяжести АП, предлагая определения легкой, средней и тяжелой степени АП для повысить однородность исследований (31).
Биомаркеры сыворотки
Острый панкреатит — это в первую очередь клинический диагноз, основанный на наличие как минимум двух из трех критериев, опубликованных INSPPIRE и Atlanta классификация (8, 9). Без выполнения двух из этих трех критериев трудно сделать диагностика АП. Основные биохимические маркеры, используемые для диагностики АП, включают сывороточную липазу. и сывороточная амилаза. Поскольку уровень липазы или амилазы в сыворотке не менее чем в три раза превышает верхний предел нормы считается совместимым с панкреатитом, важно знать справочные значения лаборатории для определения этого порога.И амилаза, и липаза обычно повышается на ранней стадии заболевания. Однако соотношение сыворотки уровни липазы или амилазы и тяжесть заболевания низкая (25, 32, 33). Липаза в основном секретируется поджелудочной железой, хотя другие источники липазы включают желудочные и язычные липазы. При АП липаза обычно увеличился в течение 6 часов после появления симптомов; уровень в сыворотке достигает максимума через 24–30 часов и может остаются повышенными более одной недели (34). Некоторые выступают за то, чтобы сывороточная липаза без сывороточной амилазы была достаточной для диагностики АП, поскольку липаза является более чувствительным и специфическим маркером АП (87–100% и 95–100% соответственно) (35–38).Липаза, кроме того, остается повышенным дольше, чем амилаза, что полезно в случаях отсроченного проявления (34, 39, 40). Уровни липазы также меньше изменяются этиология AP в отличие от амилазы, особенно в случае этанола (37, 41) или гиперлипидемия (42, 43). Но следует соблюдать осторожность при интерпретации уровней у детей. упражнения, поскольку было продемонстрировано, что нормальные значения липазы связаны с возрастом ребенок, растущий от новорожденного к ребенку, к взрослому (44, 45). Амилаза секретируется несколькими органами, прежде всего слюнные железы и поджелудочная железа.Большинство лабораторий измеряют общую амилазу уровни, которые содержат изоформы s-амилазы (слюна) и p-амилазы (поджелудочная железа) (46). Существуют лабораторные тесты для фракционирования p- и s-амилаза, но эта практика менее доступна. Эталонные значения амилазы отличаются в зависимости от используемого лабораторного теста, но также зависят от возраста и пола (47, 48). Сыворотка Уровни амилазы могут изменяться в зависимости от этиологии панкреатита, как указано выше. Амилаза уровни повышаются быстрее, чем уровни липазы, и часто могут нормализоваться через 24 часа после начала симптомы, ограничивающие полезность у пациентов с отсроченным обращением к врачу объект (34).Поскольку почки выводят амилазу и липазы, повышение этих ферментов не на уровне поджелудочной железы может наблюдаться у пациентов с повреждение или заболевание почек (46).
Несколько состояний, не связанных с панкреатитом, вызывают повышение уровня поджелудочной железы амилаза и / или липаза, включая декомпенсированную печеночную недостаточность, почечную недостаточность, кишечную воспаление (включая целиакию и воспалительное заболевание кишечника) брюшной полости травмы, диабетический кетоацидоз и травмы головы (49). Кроме того, некоторые люди продуцируют большие комплексы амилазы или липаза с иммуноглобулинами (так называемая макроамилаза и макролипаза), которые плохо фильтруется и выводится из-за большого размера, что приведет к повышенным значениям, если уровень фермента измеряется в крови, несмотря на то, что он не связан с воспалением поджелудочная железа (50).
Другие биомаркеры для диагностики и лечения панкреатита были предложены и изучены на животных моделях или небольших клинических испытаниях (см. обзоры в (46, 51, 52)). Однако ни один из них не получил известности, и многие еще предстоит пройти валидацию для общеклинического использования.
Несколько лабораторных тестов помогают контролировать течение АП (53). В целом электролиты сыворотки крови, мочевина крови азот (BUN) и креатинин, а также общий анализ крови (CBC) важны для мониторинга состояние жидкости / гидратации и почечная функция.Панель печеночных ферментов показана для поиска желчнокаменной или желчнокаменной этиологии, а также для оценки поражения органов. Кальций и Уровни триглицеридов следует рассматривать как исходные исследования (9). Мониторинг респираторного статуса может предупредить врача о том, что прогрессирование от легкой до среднетяжелой или тяжелой АД.
Этиология
Как упоминалось ранее, анатомическая, обструктивная (в том числе желчная), инфекционные, травматические, токсические, метаболические, системные заболевания, врожденные нарушения обмена веществ, генетическая предрасположенность и идиопатия были описаны как потенциальные этиологии при детском ОП, остром рецидивирующем панкреатите (АРП) и хроническом панкреатите (ХП) (3, 4, 54).Обзор Lowe et al суммировал 6 лучших общие этиологические категории в опубликованных обзорах как идиопатические / другие в 24%, травмы у 17%, системные заболевания у 15%, структурные аномалии в 14%, лекарства в 10% и инфекции в 8%. (3) Учитывая более частую этиологию, а также те, которые для которых существует направленная терапия, в рукописи 2012 года Morinville et al. опрос детских гастроэнтерологов, оказывающих панкреатологическую помощь, и предложили после обследования в первых случаях панкреатита: сывороточные ферменты печени, триглицериды и уровень кальция и УЗИ брюшной полости.Они предложили отложить тестирование на генетические причины / предрасположенности (которые в то время включали CFTR (муковисцидоз) регулятор трансмембранной проводимости), SPINK1 (ингибитор сериновой протеазы Kazal типа 1) и PRSS1 (катионный трипсиноген)), хлорид пота и более подробные изображения для случаев ARP, CP или первых экземпляров AP с повышенным риском рецидив, основанный на представлении, прошлой истории болезни или семейном анамнезе (9). При необходимости, поиск может быть проведен для конкретных факторы токсико-метаболического риска (55).Недавний публикация Gariepy et al, посвященная причинно-следственной оценке ARP и CP у детей, который имеет тенденцию быть более обширным из-за повторяющегося / хронического характера презентации (56) Аутоиммунный панкреатит (АИП) типов 1 и 2 редко диагностируются, но представляют разные типы панкреатита со специфическими гистологические данные в контексте суггестивных симптомов, визуализации, лабораторных исследований. результаты и ответ на терапию. Если AIP подозревается как этиология AP, в дальнейшем необходима поддерживающая оценка.Заинтересованные читатели будут перенаправлены на недавний публикация Scheers et al по педиатрической AIP (57).
Визуализация
Визуализация на ранней стадии ОП обычно не требуется, если в анамнезе / при предъявлении симптомы и биохимические маркеры сыворотки присутствуют для постановки диагноза. Визуализация становится актуально для документирования некроза поджелудочной железы, осложнений панкреатита, включая жидкость скопления и этиология панкреатита, например, камни в желчном пузыре / желчевыводящие пути или анатомические аномалии.
Золотым стандартом диагностической визуализации остается КЭКТ и несколько оценок. системы разработаны (58).Тем не мение, несмотря на то, что CETC является золотым стандартом визуализации, он часто не указывается и необходим для диагностики или лечения педиатрического AP. В неоднозначных случаях для диагностики ОП, например, при отсроченном проявлении, когда сывороточные маркеры могут быть низкими, компьютерная томография с контрастным усилением (CECT) может потребоваться для подтверждения AP. IV контраст является ключом к различению некротических участков поджелудочной железы (59). Поскольку ранняя визуализация может недооценивать степень заболевания и поскольку осложнения развиваются со временем, и результаты могут отсутствовать на ранних этапах фазе заболевания, в идеале CETC следует отложить как минимум на 96 часов после начала симптомы (8, 60).В легких случаях КЭКТ может показать усиление гомогенного органа, воспалительное изменения перипанкреатического жира или жидкости, окружающей поджелудочную железу (59) В тяжелых случаях КЭКТ может показать неоднородный орган усиление, некроз в поджелудочной железе или в окружающей перипанкреатической ткани. Кроме того, CECT может также идентифицировать скопления перипанкреатической жидкости или псевдокисты. КЭКТ следует пересмотреть при ухудшении клинического состояния пациента. или постоянно тяжелый (8). Lautz et al. нашел что индекс тяжести компьютерной томографии (шкала CTSI или Balthazar) в педиатрической пациенты дали чувствительность, специфичность, положительную прогностическую ценность и отрицательную прогностическая ценность 81%, 76%, 62% и 90%, соответственно, по степени тяжести в ретроспективном исследовании 64 детей (61).
Ультразвук широко используется в случаях, когда есть высокие подозрения на билиарный панкреатит, при котором полезно заранее определить необходимость терапевтического вмешательство (33, 58). Ультразвук имеет отличный профиль безопасности, неинвазивен и не использовать радиацию. Тем не менее, использование ультразвука может быть ограничено в оценке состояния. поджелудочной железы из-за мешающих структур, таких как кишечные газы в кишечнике и ожирение и имеет более низкую чувствительность при визуализации поджелудочной железы по сравнению с КЭКТ.
Магнитно-резонансная томография (МРТ) обычно не используется в качестве первичной визуализации техника при АП, но может быть полезна при поздних осложнениях (59). Это может быть особенно полезно для молодых или беременных. пациентам (с намерением ограничить облучение), и может разрешить использование альтернативных методов внутривенного контраста в пациенты с нарушением функции почек или аллергией на йодсодержащий контраст (60). МРТ также может быть более чувствительным при оценке некротическая ткань по сравнению с КЭКТ (59, 61). МР-холангиопанкреатография (MRCP) при AP наиболее часто используется для обнаружения камней в дистальных отделах общего желчного протока и диагностики желчных путей АП.МРТ / MRCP с использованием секретина помогает исследовать систему протоков в поджелудочной железы, а также общие аномалии желчных протоков, включая стриктуры или камни (62, 63). К оптимизировать обнаружение патологий протоков, MRCP может выполняться после атаки AP исчез, поскольку острый отек может затруднять визуализацию протоков. Использование MRCP, усиленный секретином, при заболевании поджелудочной железы у детей полностью не установлен (64) и доступ к секретину неодинаков через учреждения и страны.Lin et al подробно описывают использование МРТ и MRCP у детей. требуется визуализация поджелудочной железы, а также общие аспекты визуализации при AP (65).
Резюме и рекомендации
Рекомендация 1a: Диагностика острых заболеваний у детей панкреатит должен соответствовать ранее опубликованным критериям INSPPIRE.
Для диагностики ОП у педиатрических пациентов необходимы как минимум 2 из следующего: (1) боль в животе, совместимая с AP, (2) уровни амилазы и / или липазы в сыворотке ≥3 раза верхние пределы нормы, (3) результаты визуализации в соответствии с AP.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1b: Возможно выполнение первичной визуализации. с помощью трансабдоминального ультразвукового исследования, с другими методами визуализации (КТ, МРТ), зарезервированными для большего сложные случаи +/– с учетом подозреваемой этиологии.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 4; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1c: Основана на наиболее частой этиологии и те, для которых существуют варианты лечения, первый приступ острого панкреатита тестирование должно включать ферменты печени (АЛТ, АСТ, ГГТ, ЩФ, билирубин), триглицериды уровень и уровень кальция.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2. СООБРАЖЕНИЯ ВЕДЕНИЯ ПРИ ОСТРЫХ ПЕДИАТРИЧЕСКИХ ПАНКРЕАТИТАХ
2a.Инфузионная терапия при остром панкреатите
Внутривенная инфузионная терапия является основой лечения во время эпизода AP. Жидкая реанимация поддерживает адекватный жидкостный статус и диурез, но в последнее время внимание было сосредоточено на использовании внутривенных жидкостей для предотвращения потенциальных осложнений при ОП, такие как некроз и органная недостаточность. Патогенез ОП и прогрессирование до тяжелой степени. считается вторичным по отношению к нарушению микроциркуляции поджелудочной железы событиями, включая гиповолемию, повышенную проницаемость капилляров и образование микротромбы.Считается, что жидкостная реанимация не только устраняет гиповолемию, но и помогает сохранить микроциркуляцию поджелудочной железы, обеспечивая адекватную перфузию и предотвращая возможное образование микротромбов и, таким образом, предотвращение осложнений и прогрессирования тяжелое заболевание (66).
Тип жидкости
Отсутствует консенсус относительно идеального количества и типа жидкости для использования во время эпизода ОП во взрослой практике, и существует еще меньше данных, относящихся к жидкости в педиатрической популяции. Кристаллоид был наиболее рекомендуемым типом жидкость в руководствах для взрослых (33, 67–70).А Основное преимущество кристаллоидов в том, что они легко и быстро доступны. Обычный физиологический раствор (NS) долгое время был предпочтительным кристаллоидом для начальной жидкостной реанимации в в целом, но в некоторой литературе для взрослых предполагается, что лактатные звонаги (LR) являются более оптимальными для AP. В небольшом рандомизированном контрольном исследовании (РКИ) с участием 40 взрослых с AP Wu et al. что LR снижает частоту синдрома системного воспалительного ответа (SIRS) и уровни С-реактивного белка через 24 часа по сравнению с NS (71). Напротив, ретроспективный обзор 103 пациентов не смогли показать какой-либо существенной разницы между LR и NS в качестве начального реанимационная жидкость у взрослых с панкреатитом различной степени тяжести (72).LR был рекомендован по сравнению с NS в Международном Рекомендации Ассоциации панкреатологов / Американской панкреатической ассоциации (IAP / APA), но в рекомендациях Американской гастроэнтерологической ассоциации (AGA) только говорится, что LR может быть лучший выбор, но не был сильной рекомендацией (68, 70). В педиатрии это было показали, что агрессивное введение жидкости в течение первых 24 часов с помощью физиологического раствора с 5% декстрозой является безопасным и хорошо переносимым вариантом (73), но его не сравнивали с другими типами жидкостей для внутривенного вливания. (например, LR).
Коллоиды (например, альбумин, свежезамороженная плазма или упакованные эритроциты) не рекомендованы в качестве начальной реанимационной жидкости при АП. Коллоидные компоненты оставаться во внутрисосудистом пространстве из-за большего размера и может втягивать жидкость в кровообращение из интерстиция вторично по отношению к осмотическому эффекту. Руководящие принципы AGA рекомендует коллоид в определенных ситуациях, когда гематокрит < 25% альбумина составляет <2 г / дл (68), при этом другая публикация рекомендует соотношение кристаллоидов и кристаллоидов 3: 1. коллоид (74).
Скорость введения жидкости
Агрессивность жидкостной реанимации при АП также обсуждалась. В время вмешательства агрессивной жидкостной терапии может быть ключевым. Учеба взрослых в пользу ранних и агрессивных жидкостей в AP включают несколько ретроспективных исследований, которые использовали разные стратегии, такие как предоставление> против <33% от общего количества жидкости в течение первых 24 часов, а другой обеспечивает 3,5 л по сравнению с 2,4 л внутривенно в течение первых 24 часов (75). В основном, те, кто получает более агрессивные объемы жидкости внутривенно в течение первых 24 часов, как правило, улучшили результаты, включая смертность, но даже в рамках различных исследований результаты противоречивы в отношении того, снижает ли более высокое раннее введение жидкости некроз, синдром системного воспалительного ответа (SIRS) и продолжительность пребывания в стационаре (76).Напротив, Mao et al. Сообщили о РКИ 76 пациентам с тяжелым АП назначена медленная гемодилюция (5–10 мл / кг / ч) или быстрая гемодилюция (10–15 мл / кг / ч), демонстрирующая, что быстрая агрессивная ранняя жидкость введение привело к более высоким показателям сепсиса и смертности (77). de-Madaria et al провели проспективное исследование 247 человек. пациенты делятся на пациентов в зависимости от количества жидкости, введенной в первые 24 периода. часы. Группа, получавшая наибольший объем,> 4,1 л, имела повышенный уровень стойкая органная недостаточность (78).Weitz и др., рассмотрели 391 случай АП и обнаружили, что использование агрессивных жидкостей (примерно 5 л) было неэффективным. связаны с обострением заболевания и местными осложнениями (79). Опасения по поводу этой последней группы исследований заключаются в том, что в основном они касались более больных пациентов, и жидкостные режимы не ограничивались первые 24 часа реанимации.
Несколько экспертов и групп с тех пор дали рекомендации по скорости жидкостная реанимация в первые 24–48 часов у взрослых с ОП.МАП / АПА руководящие принципы рекомендуют пациентам получать 5–10 мл / кг / час до реанимации. цели достигаются в отношении улучшения частоты сердечных сокращений, диуреза, среднего артериальное давление и / или гематокрит (70). В Американский колледж гастроэнтерологии (ACG) рекомендует начальную скорость 250–500 мл / час, в дополнение к болюсу жидкости, если гипотензия или тахикардия присутствуют и используют BUN для направления терапии (33). Подобные рекомендации сделаны в обзоре Whitcomb et al (80). Aggarwal et al. советует 3–4 л жидкости в первые 24 часа (не более 4 л) с начальным болюсом 1 л и последующие 3 мл / кг / час в течение первых 24–48 часов (81).Наср и др. первоначально рекомендуют болюсы 1–2 л и 150–300 мл / час (82). Впоследствии они рекомендуют 2 мл / кг / час, если пациент отвечает на первоначальную реанимацию, но в противном случае использовать 3 мл / кг / час (82).
Только в одном педиатрическом исследовании оценивались разные нормы поддерживающей жидкости. администрации с участием 201 пациента с ОП [69]. Это исследование показало, что сочетание ранних энтеральное питание (<48 часов) и агрессивные жидкости (> 1,5–2x техническое обслуживание в первые 24 часа) уменьшилась продолжительность пребывания и возникновение тяжелое заболевание по сравнению с более традиционным историческим лечением.Агрессивные внутривенные жидкости не повлияли отрицательно на исходы (в первую очередь, легочные осложнения или повторная госпитализация). ставки). Никакие исследования не указывают идеальную норму поддерживающих жидкостей в AP после начальная реанимация (> 24–48 часов), хотя Сабо и др. что 1,5–2-кратное поддержание было безопасным для их популяции пациентов (73). Нет педиатрических исследований, сравнивающих первоначальную реанимацию тома.
Резюме: В начальной фазе реанимации острого панкреатит, теоретические и потенциальные клинические преимущества в пользу LR выше NS на основе данные о взрослых, но отсутствуют педиатрические данные.
Рекомендация 2ai: Дети с острым панкреатит необходимо первоначально реанимировать кристаллоидами, либо с LR, либо с NS в острой постановке. На основании оценки статуса гидратации / гемодинамического статуса, если при наличии гемодинамических нарушений рекомендуется болюсное введение 10–20 мл / кг.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Резюме: Педиатрическая литература жидкостная реанимация и скорость введения жидкости при остром панкреатите.Взрослый литература предлагает болюсы 250–1000 мл на начальном этапе и до 3–4 л. жидкости в течение первых 24 часов.
Рекомендация 2aii: Дети с диагнозом острой панкреатит следует назначать 1,5–2-кратное поддерживающее внутривенное введение жидкостей с мониторингом диуреза в течение следующих 24–48 часов.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 12; согласен = 10; нейтральный = 2; не согласен = 0; категорически не согласен = 0.
2b. Мониторинг детей с диагнозом ОП / внепанкреатические проявления острый панкреатит
Хотя это еще не изучено у педиатрических пациентов, полиорганная болезнь у взрослых пациенты с ОП связаны с худшими клиническими исходами с более чем половиной случаев, связанных с ОП. смерть в течение 1 недели от начала полиорганной дисфункции (83).Поражение сердца, легких и почек является ключевым фактором. компоненты систем оценки взрослых, используемых для прогнозирования тяжести эпизода ОП, включая модифицированная атлантская классификация, критерии Рэнсона, степень серьезности по Японии Оценка, оценка по Глазго, BISAP и APACHE II (8, 84–87). Педиатрические модели, прогнозирующие тяжесть ОП, также придают большое значение вовлечению нескольких органов, но оказались менее надежными (88) или еще не прошли проспективную валидацию (29). Повышенный эндотелиальный барьер проницаемость и глубокий выброс цитокинов, связанные с ССВО в сочетании с агрессивным гидратация теоретически увеличивает риск пациента для жидкости третьего промежутка и развитие внепанкреатических проявлений АП.Надлежащий мониторинг жизненно важен для сбалансировать соответствующую жидкостную реанимацию, пытаясь предотвратить сердечную, легочную и почечные осложнения (89).
Сердечно-сосудистый мониторинг
Гиповолемия при поступлении является надежным предиктором заболеваемости и смертности среди взрослых с AP и, по-видимому, коррелирует с величиной SIRS (89). Тахикардия использовалась как при системы оценки взрослых и детей для прогнозирования тяжести ОП и ее улучшение использовались для подтверждения адекватной реанимации жидкости в дополнение к мониторингу мочи объем и тургор кожи (71, 81).Регулярный кардиологический мониторинг взрослых у пациентов, не получающих ОИТ включает регулярные измерения жизненно важных функций каждые 8 часов для получения информации о состоянии сердечно-сосудистой системы (71). Дополнительно редкие случаи тампонады сердца и предсердий. Сообщалось о фибрилляции при АП, и ее следует учитывать при стандартном кардиологическом исследовании. обследование начато у пациентов с необъяснимой гипотонией, одышкой и / или боль в груди (90–93).
Мониторинг легких
Исследования на взрослых и животных модели показывают острый респираторный дистресс синдром (ОРДС), пневмония и отек / выпот легких как ранние осложнения ОП, обычно в течение первых 48 часов (15, 94).Поскольку ОРДС является наиболее распространенным критическим осложнение тяжелого АП, связанного с полиорганной дисфункцией у взрослых (95), аномальное P a O 2 или аномальные изображения легких являются компонентами всех обычно используемых систем оценки для предсказать тяжесть приступа ОП (8, 29, 84–87). Регулярный мониторинг насыщение кислородом во время агрессивной гидратации обычно осуществляется, с некоторыми койки пациентов должны быть подняты на угол 30 градусов, чтобы снизить вероятность легочная секвестрация (71).Стандарт следует рассмотреть возможность обследования легких и ухода за пациентами с необъяснимыми одышка, ухудшение кашля и / или затрудненное дыхание (94).
Мониторинг почек
Острое повреждение почек (ОПП) через синдром брюшной полости (83, 96) или вызванное воспалением повреждение проксимального извитого канальца (97), отмеченное повышением уровня азота мочевины и креатинина, а также снижение диуреза, это известное раннее осложнение АП у детей и факторы занимает важное место в оценочных системах AP для прогнозирования тяжести заболевания (8, 15, 29, 84–87).В некоторых исследованиях на взрослых было показано, что только мочевины быть столь же эффективным в прогнозировании тяжести заболевания, как и более продвинутые системы оценки (98) и AKI был связан с В 10 раз повышен риск смерти при тяжелом ОП (99). Таким образом, BUN и креатинин считаются важными маркерами для следить за проведением инфузии и контролировать ОПП у взрослых во время первого 48 часов и при агрессивном увлажнении (71, 81, 98). Хотя нет никаких руководств, документирующих частоту мониторинга этих параметров, 8–12 часов использовались в одном исследовании для определения реакции на управление жидкостями (71).Рекомендации ACG подчеркивают важность снижения АМК и поддержания нормального уровня креатинина в первые 24 часа, поэтому очень важен ранний мониторинг (33). В редких случаях требуется непрерывная вено-венозная гемофильтрация (CVVH). для предотвращения дальнейшего повреждения почек, предотвращения синдрома брюшной полости и / или removae воспалительных цитокинов, но его использование не изучалось у педиатрических пациентов с AP (100). Может понадобиться установить мочевой катетер для точного документирования диуреза, особенно при седативном ребенок в условиях отделения интенсивной терапии.
Резюме и рекомендации
Наблюдение за пациентами с острым панкреатитом может дать индикаторы возникающие осложнения, включая ССВО и органную дисфункцию / недостаточность. Сердечный, следует особенно внимательно следить за респираторным и почечным статусом в течение первого Через 48 часов после обращения, так как большинство осложнений начинается в течение этого периода. период времени. Диурез — важный маркер адекватной жидкостной реанимации, при этом литература для взрослых, предлагающая стремиться к достижению> 0.5–1 куб. См / кг / час (Руководство IAP / APA).
Рекомендация 2bii: Пациентам, поступившим в в стационарном отделении необходимо измерять жизненно важные показатели не реже, чем каждые 4 часа в течение первых 48 дней. часы приема и в периоды агрессивной гидратации для контроля кислорода сатурация, артериальное давление и частота дыхания. Частота регулируется в зависимости от клинический статус. Нарушения жизненно важных функций должны требовать обследования у специалиста.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2biii: АМК, креатинин и моча производительность следует регулярно контролировать в течение первых 48 часов как маркер соответствующее ведение жидкости и скрининг на острое повреждение почек. Аномалии должен вызвать нефрологическое обследование.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 4; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
2с. Обезболивание при остром панкреатите
Боль в животе является наиболее частым симптомом ОП.В педиатрической АП исследования, от 80% до 95% пациентов жаловались на боль в животе. Пациенты присутствует с болью в эпигастрии у 62-89% и диффузно у 12% до 20%. «Классическое» проявление иррадиации боли в эпигастрии. к спине встречается только у 1,6–5,6% педиатрических пациентов (15, 16).
Патофизиология ОП характеризуется потерей внутриклеточных и внеклеточная компартментализация, которая может быть результатом различных механизмов: обструкция секреторного транспорта поджелудочной железы; активация ферментов; или неспособность остановить каскад активации.АП встречается у генетически предрасположенных лиц, у которых воспалительная реакция вызывает панкреатит. Это, в свою очередь, стимулирует внутреннюю панкреатические и соматические болевые рецепторы брюшины (101). Другие постулируемые механизмы, вызывающие боль в переднем отделе позвоночника, включают высокое давление. внутри железы или протока поджелудочной железы с последующей ишемией железы. Боль в AP тоже бывает вероятно, связано с высвобождением тахикинина, вещества P и кальцитонина, связанного с геном. пептид. Факторы, которые стимулируют первичные сенсорные нейроны, включают ионы водорода, тепло, лейкотриены, метаболиты арахидоновой кислоты, брадикинины и протеазы, такие как трипсин, выпущен во время AP (102).
Обезболивание — важная терапевтическая цель при лечении ОП и обычно включает использование анальгетиков периферического и центрального действия. Нет данных опубликованы по оптимальному обезболиванию в педиатрической AP, а исследования у взрослых не определили одно лучшее лекарство (67).
Опиоидные анальгетики
Потому что классические анальгетики периферического действия (такие как ацетаминофен) часто недостаточны при тяжелом панкреатите, часто требуются опиаты для контроля боль.Морфин или родственные ему опиоиды употребляли 94% респондентов для вести детей с ОП в соответствии с анкетой для врачей INSPPIRE 2012 года (103). Сообщалось, что морфин вызывает дисфункция сфинктера Одди после системного введения (104). Однако нет четких доказательств, подтверждающих эту теорию, и морфин можно безопасно применять у пациентов с ОП (105). Меперидин применялся у взрослых с АП, но его недостатки включают: короткий период полураспада и потенциал нейротоксичности за счет накопления токсичных веществ. нейрометаболиты, которые могут приводить к судорогам, миоклонусу и тремору (106).Обзор наркотиков и функции сфинктера Одди. Thomson et al, документально подтверждают, что на сегодняшний день нет исследований, напрямую сравнивающих эффекты меперидин и морфин на сфинктере манометрии Одди и никаких сравнительных исследований существуют у пациентов с АП. Кроме того, не существует исследований или доказательств, указывающих на то, что морфин противопоказан к применению при ОП (107). Кокрановский обзор 2013 года включает 5 исследований, в общей сложности 227 Субъекты для оценки эффективности и безопасности нескольких опиоидов. Включенные лекарства были бупренорфин, петидин, пентазоцин, фентанил и морфин.Общий вывод состоит в том, что опиоиды могут быть подходящим выбором при лечении боли. связанных с AP, и они могут уменьшить потребность в дополнительной анальгезии. Кроме того, риск осложнений, связанных с панкреатитом, или клинически серьезных побочные эффекты не отличаются от опиоидов и других анальгетиков (108).
Опиоидсберегающие анальгетики
Предполагается, что НПВП являются потенциальными участниками развитие AP, но также показали преимущества при лечении боли в AP.Профилактическое Было показано, что НПВП, включая индометацин и диклофенак, полезны при нескольких исследования по профилактике панкреатита после ЭРХПГ (109, 110). Что касается боли После постановки диагноза АР индометацин превосходит плацебо и не показали повышенного риска желудочно-кишечного кровотечения в небольшом исследовании (111). По сравнению с морфином метамизол показал улучшение снятие боли через 24 часа, но разница не достигла статистической значимости (105).
Системное введение местных анестетиков, в основном новокаина, было выступает в качестве основного обезболивающего при АП.Предлагается внутривенное введение новокаина для уменьшения боли. и / или необходимость вспомогательных обезболивающих и, возможно, улучшения клиническое течение АП. В одном контролируемом исследовании системное введение новокаина в улучшение панкреатита и ускоренное послеоперационное восстановление после обширного абдоминального хирургическое вмешательство, включая уменьшение боли, улучшение когнитивных функций и сокращение длительность кишечной непроходимости, а также общая госпитализация (112). Но доказательства ограничены, а плацебо-контролируемые исследования отсутствуют. данные.
Эпидуральная анестезия (ЭА) широко используется для индукции обезболивания в в периоперационный период, а также для уменьшения боли у пациентов с ОП. В принцип действия был приписан блокаде симпатического нерва, который перераспределяет внутренний кровоток к неперфузируемым областям поджелудочной железы. В исследовании с участием 35 пациентов с прогнозируемым тяжелым ОП, ЭА значительно уменьшала болевые ощущения, улучшала перфузия поджелудочной железы на основе радиологических исследований перфузии и улучшения клинических исходы (снижение потребности в некрэктомии) (113).Проспективное исследование 121 пациента продемонстрировало хорошую эффективность. и безопасность EA у взрослых AP (114).
Резюме: Нет данных, обеспечивающих оптимальную боль управление в педиатрической АП. Исследования на взрослых не выявили ни одного превосходящего медикамент. Нет доказательств, подтверждающих утверждение, что морфин вызывает неблагоприятные события на сфинктере Одди.
Рекомендации 2ci: Внутривенный морфин или другой препарат опиоид следует использовать при острой боли при панкреатите, не реагирующей на ацетаминофен или НПВП.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 2cii: Услуги специалиста по острой боли в идеале следует проконсультироваться в случаях более сильной боли, чтобы уменьшить боль управление.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2d. Энтеральное и парентеральное питание при остром панкреатите у детей
Пероральное и энтеральное питание
Традиционно пациенты с ОП лечились, не вводя перорально (115) и давая парентеральное питание (PN) (116).Было высказано предположение, что отдыхая кишечник, поджелудочной железе дали «отдохнуть» и, таким образом, зажить быстрее. В Обоснованием этой теории было то, что наличие пищи в кишечнике стимулируют высвобождение холецистокинина (ХЦК), что, в свою очередь, стимулирует поджелудочную железу. секреция ферментов, что может привести к дальнейшей активации протеолитических ферментов и преувеличивают процесс самопереваривания и усугубляют травму (117, 118)
У взрослых проводится ряд контролируемых исследований, обзоров и метаанализов. лечебному питанию как при тяжелом, так и при легком ОП, включая обзор голландских Группа по изучению панкреатита и согласованные рекомендации, опубликованные Международный комитет по руководящим принципам консенсуса (119).Lodewijkx et al., Считают, что энтеральное питание превосходит парентеральное питание, а стратегия кормления по требованию в прогнозируемой тяжелый АП (120). Мирталло и др. Рассмотрели 8 социальные отчеты с целью разработки международных согласованных руководящих принципов по питанию терапия в АП (119). Они пришли к выводу, что в АП у взрослых, энтеральное питание (ЭП) было предпочтительнее, чем ПП, и его следует использовать в первую очередь даже при наличие свищей, асцита и псевдокист.
Рекомендуется начинать EN как можно раньше, тем более, что одна из целей энтеропатии — предотвратить бактериальную транслокацию и тем самым предотвратить развитие ССВО.Ранняя нутритивная терапия также предназначена для снизить цитокиновый ответ и частоту пареза желудка и кишечной непроходимости. В то время как некоторые исследования (121) не показывают разницы в исходы, когда ЭП была начата до или после 72 часов презентации, 2008 г. метаанализ, изучавший одиннадцать РКИ, показал, что ЭП началась в течение 48 часов после презентация значительно снизила показатели смертности, инфекций и полиорганной отказ по сравнению с PN (122). Эти эффекты были уменьшены, когда ЭП была начата через 48 часов.В обзоре питания за 2011 г. поддержка взрослых AP, был сделан вывод, что ранняя нутритивная поддержка, особенно ЭП, но также и ПП, уменьшали количество осложнений и улучшали выживаемость (123). В этом обзоре говорилось, что для его эффективности нутритивная поддержка должна была начаться в течение 72 часов. Было заявлено, что EN следует считается « активным терапевтическим вмешательством, улучшающим исход больных панкреатитом »(124).
Клинические исследования, сравнивающие результаты PN и EN у пациентов с AP сообщить, что использование EN при тяжелом остром панкреатите (SAP) или прогнозируемые результаты SAP значительно снижает частоту осложнений (125–133).Недавний метаанализ продемонстрировал превосходство ЭП по сравнению с ПП с меньшей частотой инфекции и полиорганной недостаточности, что приводит к снижению показателей смертности и сокращению пребывание в больнице (134). Однако, поскольку полный EN не всегда возможно во время AP из-за усиления боли или непереносимости кормления, некоторые отстаивают роль комбинации EN и PN. В одном исследовании рандомизировали 100 пациентов для получения только ПП по сравнению с ПП в комбинации только с ЭП или ЭП, сепсис, внутрибрюшная инфекция и продолжительность госпитализации снизились, когда ЭП была входит в состав руководства (135).
Описанные пути ЭП включали желудочный и тощей кишки. Два маленьких исследования не обнаружили разницы в результатах между назогастральным (НГ) и назоеюнальным (НД) сытые группы (136, 137). Мета-анализ 10 РКИ не показал различий в исходы между группами, получавшими (полу) элементарные и полимерные формулы. (138)
Никаких руководств по нутриционной поддержке дети с АП. Недавнее исследование Abu-El-Haija et al. продемонстрировал выполнимость установления энтерального питания в педиатрической АП, не усложняя курс или влияя на оценку боли AP (139).Из того же центра ретроспективное исследование показало, что сочетание раннего энтерального кормления плюс более чем 1,5-кратное поддерживающее внутривенное введение жидкости были связаны с более коротким продолжительность пребывания и более легкое заболевание по сравнению с теми, кто оставался НКО в течение 48 часов и имели более низкую частоту ЭКО, чем поддерживающую терапию (73). Сообщается о двух детях с тяжелым ОП, которые успешно вылечились. с назоеюнальным кормлением в отделении интенсивной терапии интенсивной терапии и переключением на пероральное кормление при выписке в общая палата (140).
Парентеральное питание
Родительское питание обеспечивает организм необходимыми калориями и питательными веществами. компенсировать катаболическое состояние.Обеспокоенность, что ПП может стимулировать поджелудочную железу. и приводить к преувеличению процесса самопищеварения не было подтверждено литература (141, 142). Данные показывают, что настой протеина не стимулируют секрецию поджелудочной железы (143). Когда при сравнении различных форм ПП, сообщалось, что ПП, усиленный глутамином, снизить общую частоту осложнений, а также сократить продолжительность пребывания в стационаре (144–148). Введение глюкозы внутривенно также не стимулирует секреция поджелудочной железы (149, 150).Инфузия глюкозы тяжелобольным пациентам может быть полезно для обеспечения легкодоступного источника энергии во время катаболического состояния и противодействуют глюконеогенезу из-за распада белка. Но настой глюкозы обязательно под наблюдением, так как это может предрасполагать к гипергликемии (151), поскольку воспаленная поджелудочная железа может не подавать соответствующий инсулин отклик.
Гипертриглицеридемия связана с тяжелым ОП (152–155), но механизм, ведущий к SAP, не ясен (156). Недостаточно данных, чтобы рекомендовать или препятствовать использованию парентеральные липиды при АП.
Что касается времени PN в AP, где измеренный результат был смертности, данные свидетельствуют о том, что раннее ПП значительно более полезно, чем покой кишечника. при тяжелом ОП у взрослых (122). Во всех случаях, когда ЭП невозможна в течение длительного времени, например, при кишечной непроходимости, сложных свищах и т. Д. синдром брюшного отдела, PN. Напротив, недавнее исследование выступал за отсрочку начала ПП до 7 дней у тяжелобольных детей из-за повышенный риск инфицирования и повышенная частота осложнений после начала ПП в течение первых 24 часов после пребывания в отделении интенсивной терапии.Раннее энтеральное питание было разрешено в обоих группы. Однако присутствие или процент пациентов с ОП конкретно не было указано в этом отчете (157).
Резюме: Литература для взрослых поддерживает раннее энтеральное питание, чтобы уменьшить осложнения AP и улучшить выживаемость. Педиатрическая литература поддерживает раннее энтеральное питание в легких случаях ОП и небольшое сообщение в тяжелых случаях AP.
Рекомендация 2di: За исключением наличия прямого противопоказания к употреблению кишечника, детям с острым панкреатитом легкой степени может помочь от раннего (в течение 48–72 часов после обращения) орального / энтерального питания до уменьшения продолжительность пребывания и снижение риска органной дисфункции.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2dii: Парентеральное питание (ПП) должно следует рассматривать в тех случаях, когда ЭП невозможна в течение длительного периода времени (дольше более 5-7 дней), например, в кишечной непроходимости, сложных свищах, брюшной полости синдром, снижающий катаболическое состояние организма. Следует начать энтеральное питание. как можно скорее, причем комбинация EN и PN превосходит одиночную PN.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15 согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2diii: В случае панкреатической разрыв, перелом или разрыв протока, неясно, является ли пероральное / энтеральное питание может быть вредным в острой фазе. Это требует дальнейшего изучения.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 13; согласен = 8; нейтральный = 2; не согласен = 0; категорически не согласен = 0; нет голоса = 1.
2д. Использование антибиотиков при остром панкреатите у детей
Обоснование использования антибиотиков при лечении ОП связано к беспокойству по поводу бактериальной инфекции из-за перемещенной кишечной микробиоты. Антибиотики не рекомендуются для взрослых с легким ОП (70).
При лечении тяжелого ОП у взрослых изучались антибиотики для предотвращения и управлять инфекциями. Имипенем и / или цефалоспорины третьего поколения были наиболее исторически часто использовались в попытке снизить заболеваемость и смертность.Этот Профилактический подход является спорным: предыдущие исследования предполагали пользу (158–160), в то время как другие исследования не продемонстрировали пользы от рутинного использования (161) в отсутствие документально подтвержденной инфекции. Профилактические антибиотики использовались в условиях стерильной некротической болезни. панкреатит для предотвращения инфицированного некротического панкреатита (162, 163), особенно имипенем (163). Однако систематические обзоры не поддерживает преимущества в отношении смертности от инфекций, не затрагивающих поджелудочную железу, или для сокращения хирургических вмешательств у взрослых (162).Более поздние метаанализы подтверждают использование антибиотиков для инфицированы некротическим панкреатитом, но не для стерильный некроз (164–166). Текущий взрослый AP рекомендации — использовать антибиотики только при инфицированном некрозе или у пациентов с некротический панкреатит, госпитализированные и без клинического улучшения использование антибиотиков (70). Зараженный некроз должен быть подозревается, если клиническое состояние пациента ухудшается из-за лихорадки или наличие газа в коллекциях на снимках.В определенных ситуациях стремление жидкость под контролем эндоскопии или с помощью интервенционной радиологии и для руководства лечением может потребоваться создание соответствующего дренажа (8). При некротическом панкреатите известные антибиотики: проникают в некротические ткани, такие как карбапенемы, хинолоны и метронидазол, поскольку использование антибиотика в этих условиях, как было показано, задерживает хирургическое вмешательство. вмешательства и снизить заболеваемость и смертность (33).
Документированные инфекции, происходящие за пределами поджелудочной железы, следует рассматривать как указано.
Не было опубликовано исследований по использованию антибиотиков для лечения АП у детей.
Резюме: Антибиотики нельзя использовать в лечение ОП, за исключением случаев документально подтвержденного инфицированного некроза или у пациентов с некротическим панкреатитом, которые госпитализированы и клинически не улучшаются без использование антибиотиков. Антибиотики, о которых известно, что они проникают в некротические ткани, следует использовать при лечение инфицированного панкреонекроза, поскольку это может отсрочить хирургическое вмешательство и снизить заболеваемость и смертность.
Рекомендации 2ei: Профилактические антибиотики не эмпирически рекомендуется при тяжелом остром панкреатите.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
Рекомендация 2eii: показано только использование антибиотиков. в случаях документально подтвержденного инфицированного некроза при остром панкреатите.
16/24 = 67% согласны с рекомендацией. Рекомендация не поддерживается.Это было определено как область особых разногласий, требующих дальнейшего учиться.
Результаты голосования: Полностью согласен = 10; согласен = 6; нейтральный = 2; не согласен = 4; категорически не согласен = 0; нет голоса = 2.
2f. Использование ингибиторов протеазы при остром панкреатите у детей
Поскольку AP предположительно является некровоспалительным процессом, начавшимся через острая и несоответствующая активация трипсина протеазы и зимогенов поджелудочной железы внутри паренхимы, исследователи были очень заинтересованы в блокировании этого воспалительный процесс, чтобы ограничить степень травмы.
Два основных соединения, описанных в литературе для ингибирования этого фермента активация включает ингибитор сериновой протеазы габексат мезилат и трипсин ингибитор апротинин. В 1993 году Pederzoli et al. сообщил результаты рандомизированного, двойное слепое многоцентровое клиническое исследование использования габексата мезилата по сравнению с апротинином в АП-терапия. В этом исследовании мезилат габексата оказался более предпочтительным по сравнению с апротинином в отношении период 24–72 часа, но, что важно, отсутствует контрольная группа плацебо (167).Сроки лечения и способ родоразрешения кажутся быть ключевыми факторами эффективности (167, 168). Ино и др. изучили эффективность непрерывного инфузия регионарной артерии CRAI с габексатом мезилатом и антибиотиками при тяжелом ОП через небольшое проспективное исследование с участием 9 пациентов, получавших CRAI в течение 3-5 дней и 9 пациентов. другие получают терапию системными ингибиторами протеазы и антибиотики. Боль в животе и SIRS исчезал быстрее, LOS был значительно короче в группе CRAI (168). CRAI антипротеаз и антибиотиков имеет Сообщалось о снижении показателей CRP и APACHE II при применении в течение 72 часов после начала болезни (169), подход, описанный в педиатрических больных (170).
Обзор 2007 года, проведенный Китагавой и Хаякавой, не нашел доказательств, оправдывающих рутинное использование антипротеаз при AP, и хотя использование непрерывного внутривенного ингибиторы протеазы и антибиотики в высоких дозах могут быть эффективными для предотвращения обострения тяжелого ОП, необходимы исследования экономической эффективности. Важно, эти соединения не одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США. Штаты (171–173).
Резюме: Некоторые исследования взрослых подтверждают использование антипротеаз в лечении тяжелого АП, но никаких конкретных рекомендаций никогда не было были сделаны для их использования.Исследования не были рандомизированы с контрольными группами плацебо, и только несколько случаи описаны в педиатрических больных.
Рекомендации 2f: Антипротеазы не могут быть рекомендуется при лечении острого панкреатита у детей в это время.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 7; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2г. Использование антиоксидантов при остром панкреатите у детей
Окислительный стресс способствует повреждению ОП из-за образования кислорода свободные радикалы, вызывающие повреждение липидной мембраны клетки поджелудочной железы, деполяризацию митохондриальной мембраны и индукции фрагментации ДНК (174).Это способствует отеку, возникновению боли и может также быть вовлеченными в процесс некроза. Таким образом, была выдвинута гипотеза об антиоксидантах. иметь потенциальную пользу в качестве дополнительного лечения при АП, предотвращая образование свободные радикалы или улавливание существующих свободных радикалов кислорода.
Наиболее изученными агентами были витамины-антиоксиданты (аскорбиновая кислота, α-токоферол, β-каротин), неорганические антиоксиданты (селен) и глютамин. В двух частично совпадающих метаанализах, опубликованных в 2015 г., используются разные методологии оценки пользы антиоксидантов при остром панкреатите, один обзор 11 и другие 12 рандомизированных контролируемых исследований на взрослых [169, 170].Pederzoli et al. Обнаружили, что антиоксиданты снижают количество осложнений, связанных с ОП, и укороченный LOS с глутамином, снижающим частоту осложнений и смертность [169]. Ино и др. Сообщили, что антиоксидант терапия сокращает LOS и снижает уровень СРБ в сыворотке, но только через 10 дней [170].
Существенным ограничением опубликованных данных об антиоксидантах у взрослых AP является эти испытания включали весь спектр легкого и тяжелого АД. Кроме того, различные комбинации антиоксидантов и время доставки были использованы в испытания.В крупных рандомизированных исследованиях также отсутствует стандартизация конкретных антиоксидантов. как сроки и продолжительность лечения.
Нет данных об использовании антиоксидантов при AP в педиатрической популяции.
Резюме: педиатрические данные об использовании не хватает антиоксидантов в АП. Публикации для взрослых демонстрируют значительную неоднородность относительно состава, времени и продолжительности терапии. Несмотря на потенциальные преимущества описанных в сериях для взрослых, доказательств недостаточно, чтобы поддержать их использование в педиатрия в это время.
Рекомендация 2g: Антиоксиданты не следует считается стандартной терапией при лечении острого панкреатита у детей.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
2ч. Роль пробиотиков в лечении острого панкреатита у детей
Примерно у трети взрослых пациентов может развиться тяжелая форма АП, характеризующаяся ССВО, органная недостаточность и повышенный риск инфицирования (175).У пациентов с инфицированным перипанкреатическим и панкреонекрозом риск летального исхода значительно увеличивается. Снижение проницаемости кишечника и Предполагается, что избыточный бактериальный рост во время AP снижает риск инфицирования некроз поджелудочной железы и тем самым снизить риск смерти (176, 177).
Всемирная организация здравоохранения определяет пробиотики как «живые микробы. которые при введении в адекватных количествах приносят пользу их здоровью. хозяин». Доказано, что пробиотики играют роль в поддержании микрофлоры кишечника. баланс, подавляя рост вредных бактерий и усиливая иммунную функцию (178).Важно, что опубликованные исследования использовали различные составы и режимы дозирования пробиотических бактерий.
Muftuoglu et al. продемонстрировали, что lactobacillus acidophilus и bifidobacterium lactis уменьшают тяжесть гистологического повреждения в экспериментальной модели панкреатита (178). Ранние небольшие клинические испытания для взрослых показали положительную роль пробиотиков в управление АП. Olah et al. рандомизировали 45 пациентов для приема 10 9 живые или убитые теплом lactobacillus plantarum два раза в день вместе с энтеральное питание (179).Они обнаружили статистически значительно более низкий риск инфицированного панкреонекроза в исследуемой группе по сравнению с контрольные группы.
Однако впоследствии исследование PROPATRIA, двойное слепое, плацебо-контролируемое рандомизированное многоцентровое исследование роли пробиотиков в профилактике инфекционные осложнения при ОП) в составе 298 взрослых пациентов с прогнозируемой тяжелой AP продемонстрировал значительно более высокий риск смерти у многовидовых пробиотиков. группа (180, 181). Два небольших рандомизированных испытания с момента завершения не продемонстрировали увеличение смертности (182, 183), но влияние неблагоприятных результатов исследования PROPATRIA Исследование привело к общей осторожности при использовании пробиотиков у взрослых с ОП.
Ни одно педиатрическое исследование не изучало роль пробиотиков у детей с AP.
Резюме: После серии небольших дел, предполагающих потенциальная польза пробиотиков при ОП у взрослых, большое рандомизированное исследование продемонстрировало повышенная смертность в группе пробиотиков. Педиатрических исследований не опубликовано.
Рекомендации 2 часа: Нельзя рекомендовать пробиотики в лечении острого панкреатита у детей в настоящее время. Высшее качество опубликованные данные для взрослых показывают, что они могут не только не принести пользы, но и увеличивать смертность.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 14; согласен = 9; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2i. Роль эндоскопии в лечении острого панкреатита у детей
Различные причины воспаления слизистой оболочки двенадцатиперстной кишки связаны с увеличением риск AP. Проявления, связанные с глютеновой болезнью поджелудочной железы, включают эндокринные и внешнесекреторная недостаточность, острый и хронический панкреатит, нарушение питания, папиллярный стеноз вторичный по отношению к дуодениту или иммунологическим нарушениям, и все предположили, что быть вовлеченными механистически (184–186).Желчнокаменная болезнь была обнаружена до 34% пациентов с болезнью Крона и может проявляться как АП (187). Аутоиммунный панкреатит (АИП) и первичный склерозирование холангит (188) также может быть обнаружен у пациентов с воспалительным заболеванием кишечника, проявляющимся AP (189–191). Повышение уровня IgG4 наблюдается у взрослых пациентов с AIP типа I, педиатрические пациенты с AIP обычно без повышения уровня IgG4, при биопсии двенадцатиперстной или желудочно-дуоденальной воспалительной поражения могут быть полезны в диагностике (192, 193).Были случаи острого и хронического панкреатита. редко регистрируется как проявление или ассоциация инфекции H. pylori (194, 195). Чрезвычайно редко возможными причинами панкреатита у детей являются опухоли, связанные с ампула или периампулярная область двенадцатиперстной кишки. Такие поражения могут быть первыми идентифицируется рентгенологическим исследованием, но также может быть обнаружено во время эндоскопического исследования. оценка. Судя по имеющимся историям болезни, механизм развития у этих пациентов рецидивирующий панкреатит до конца не изучен, но, вероятно, связан с опухолью непроходимость на уровне ампулы (196, 197).Но в целом роль эзофагогастродуоденоскопия при ОП ограничена.
Нет исследований, оценивающих показания или преимущества эзофагогастродуоденоскопии в педиатрический AP.
Резюме: Роль эндоскопии в неотложной помощи дети с AP неясно. Возможность первичных внепанкреатических заболеваний В результате разработка AP требует вдумчивого рассмотрения.
Рекомендации 2i: Эзофагогастродуоденоскопия не в настоящее время считается стандартным диагностическим инструментом при остром панкреатите у детей.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2j. Роль ЭРХПГ при остром панкреатите у детей
Роль ЭРХПГ при ОП эволюционировала с технологическими улучшениями в диагностические возможности МРТ / MRCP и с увеличением педиатрического опыта с эндоскопическое ультразвуковое исследование (ЭУЗИ). Благодаря наличию этих последних диагностических инструментов для при заболеваниях поджелудочной железы, ERCP все чаще используется в первую очередь для лечения вмешательства или для неясных диагнозов после MRCP или EUS.ЭРХПГ безопасна для детей при этом наиболее частым осложнением является легкий панкреатит после ЭРХПГ. аналогичны таковым у взрослых (~ 3–10%), когда выполняются опытные эндоскописты (198–206). Обструкция желчевыводящих путей и хронический панкреатит являются наиболее частыми показаниями к ЭРХПГ у детей. В педиатрической AP ERCP имеет ограниченная роль, выполняется почти исключительно при билиарном панкреатите, вторичном по отношению к холедохолитиаз или отстой. ЭРХПГ при холедохолитиазе без панкреатита безопасна и эффективны (207, 208), но в педиатрии нет конкретных рекомендаций по сроки проведения ЭРХПГ при холедохолитиазе или остром билиарном панкреатите.У взрослых большой метаанализ и научно обоснованные рекомендации IAP по ведению острых билиарный панкреатит рекомендовал ЭРХПГ в течение 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. В противном случае можно провести ЭРХПГ. планово при неосложненном холедохолитиазе и в других случаях желчевыводящих путей. панкреатит независимо от степени тяжести (209, 210).
Менее распространенными показаниями для ЭРХПГ при ОП являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы (211).Камни и стриктуры протоков поджелудочной железы обычно признаки острого рецидивирующего или хронического панкреатита, поэтому встречаются относительно редко показания к ЭРХПГ при АП. В редких случаях, когда непроходимость протока предотвращает разрешение панкреатита, может быть проведена терапевтическая ЭРХПГ. Псевдокисты поджелудочной железы в у детей может развиться острый или хронический панкреатит, но чаще всего возникает после тупая травма. Псевдокисты поджелудочной железы представляют собой однородное скопление панкреатической жидкости. окружены фиброзной или грануляционной тканью, но не имеют эпителиальной выстилки (15, 212), и может развиться из скоплений жидкости, сохраняющихся более 4 недель (213).ERCP может использоваться для оценки коммуникации псевдокиста с протоком поджелудочной железы, куда можно установить транспапиллярный стент для дренаж. В противном случае — эндоскопическая цистагастростомия (214–216) и под контролем EUS. дренаж (217) — безопасные и эффективные способы дренировать псевдокисты поджелудочной железы у детей и может быть рассмотрено в зависимости от расположения псевдокиста. Повреждение протока поджелудочной железы и утечка также могут возникнуть в результате травмы. Рано эндоскопическое или хирургическое вмешательство может помочь свести к минимуму продолжающуюся заболеваемость протоковым утечка, поскольку ERCP обеспечивает быстрый и более точный метод определения местоположения и степень повреждения, чем MRCP или CT, а также дает возможность терапевтического стента размещение поперек травмы (218, 219).
Резюме: Роль ЭРХПГ при остром панкреатите. в первую очередь относится к терапевтическому лечению билиарного панкреатита, вторичного по отношению к холедохолитиаз или отстой. Литература для взрослых предполагает эффективность ERCP в пределах 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. Менее распространенными показаниями к ЭРХПГ при остром панкреатите являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы или разрывы протока.
Рекомендации 2ji и 2jii: (2ji) Роль ERCP ограничен при остром панкреатите и зависит от местных знаний.(2jii) ERCP — это показан при лечении острого панкреатита, связанного с холедохолитиазом, вызывающим билиарный панкреатит и патологии протоков поджелудочной железы, такие как протоковые камни или протоки протока.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 21; согласен = 3; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2к. Роль EUS при остром панкреатите у детей
Эндоскопическое ультразвуковое исследование (EUS) использовалось для определения этиология АП.EUS не только всесторонне оценивает паренхиму поджелудочной железы и протока, но также и гепато-билиарной анатомии. Заболевания желчевыводящих путей, такие как холедохолитиаз можно оценить с помощью EUS, особенно когда трансабдоминальное УЗИ не позволяет визуализировать дистальный общий желчный проток. EUS также может определить наличие микролитиаза у желчный пузырь, который часто не визуализируется при трансабдоминальном УЗИ или КТ сканировать. Микролитиаз может привести к ОП и лечится холецистэктомией (220). Хотя у детей это случается крайне редко, опухоли поджелудочной железы, которые могут быть вызваны новообразованием поджелудочной железы или AIP, могут проявляться с AP и пройти дальнейшее обследование с помощью EUS с возможностью взятия пробы ткани поджелудочной железы. (221, 222).
Терапевтическая роль EUS при AP в основном ограничена для лечения осложнения АП, а именно скопление жидкости поджелудочной железы или некроз стенок. EUS имеет было показано, что он полезен при лечении скоплений жидкости поджелудочной железы / некроза вторичный по отношению к тяжелому AP. Считается, что спонтанное рассасывание псевдокист происходит чаще. чаще у детей, чем у взрослых, особенно если размер <5 см (мнение эксперта). Таким образом, с большинством коллекций любого типа можно обращаться консервативно и терапевтически. вмешательство не требуется в остром состоянии, за исключением случаев наличия инфекции (223).Однако, если происходит созревание (обычно через 4–6 недель) саморегулирование менее вероятно, и пациент может нужен эндоскопический дренаж. Другие показания к вмешательству EUS и дренированию включают: большой размер при возникновении клинических симптомов, подозрении на заражение скоплений или стойких симптомы от псевдокисты. Дренаж под контролем EUS и создание цистгастростомы было продемонстрировано, что он столь же эффективен и безопасен, как хирургическая цистгастростомия, и имеет было показано, что он эффективен даже у детей (224).
Резюме: на основании литературы для взрослых, EUS может быть полезным для определения этиологии острого панкреатита, которая может включать диагностику дистального камни общего желчного протока, новообразования поджелудочной железы или аутоиммунный панкреатит. Его роль для терапия в основном ограничена лечением осложнений острого панкреатита, а именно скопления жидкости поджелудочной железы или некроз стенок, вторичный по отношению к тяжелому АД.
Рекомендация 2k: EUS не считается стандартом диагностический инструмент при остром панкреатите у детей в настоящее время.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2L Роль хирургии / хирургической консультации при остром панкреатите у детей
Хирургические вмешательства не являются частью алгоритма ведения больного. Типичный эпизод АП. Публикации относятся к взрослому опыту. Раннее указание на хирургия включает лечение синдрома брюшной полости.Однако управление некроз поджелудочной железы с ранней некрэктомией в течение первых 72 часов, как было показано, приводит к повышенная заболеваемость и смертность по сравнению с отсроченными сроками не менее чем на 12 дней (225). Руководящие принципы Международного Ассоциация панкреатологов с 2002 г. предлагает отложить операцию некрэктомии для по крайней мере, через 3-4 недели после начала заболевания снижает заболеваемость и смертность (210). Руководящие принципы ACG 2013 года по управлению взрослый AP прокомментировал возможность хирургического вмешательства в связи с желчнокаменной болезнью. панкреатит, санация некроза (инфицированные vs.стерильный), и малоинвазивный лечение некроза поджелудочной железы (33). Рекомендации включали раннюю холецистэктомию во время той же госпитализации по поводу легкий приступ желчнокаменного панкреатита и обсуждение между гастроэнтерологами и хирургия для выбора времени холецистэктомии по сравнению с другими терапевтическими вариантами в случаях тяжелый АД, особенно с некрозом. Для пациентов с сохраняющейся клинической нестабильностью и ухудшение состояния на фоне некроза поджелудочной железы, дренирование может потребоваться для улучшить статус пациентов и снизить заболеваемость и смертность.Руководящие принципы АЧГ предлагают что санацию некроза следует отложить, когда это возможно, в идеале более четырех недель с момента обращения, чтобы лучше организовать воспалительные реакции. Даже в необходимость некрэктомии, менее инвазивных методов, включая чрескожную радиологию, или следует рассмотреть возможность эндоскопического дренирования / хирургической обработки раны наряду с лапароскопическим хирургическим вмешательством. предпочтение отдается лечению перед открытым хирургическим вмешательством (33).
Исследование PONCHO 2015 г. с участием 266 стационарных пациентов, рандомизированных по интервалу холецистэктомия или холецистэктомия с тем же госпитализацией также поддерживали ту же госпитализацию. холецистэктомия снизила частоту повторных осложнений, связанных с желчнокаменной болезнью, у взрослых пациенты с желчнокаменным панкреатитом легкой степени с очень низким риском холецистэктомии осложнения (226).
В случае тяжелой травмы живота, требующей неотложной лапаротомии (в том числе дорожно-транспортных происшествий) следует искать повреждения поджелудочной железы, в том числе вовлекающий проток поджелудочной железы. Тяжесть травмы поджелудочной железы может быть оценена в соответствии с Американской ассоциации хирургии травм поджелудочной железы по шкале, в которой 5 могут быть присвоены степени травмы (227). Выше травмы поджелудочной железы в результате травмы, как правило, также включают ассоциированную дуоденальную травмы. Пациентам с более легкими тупыми травмами I и II степени можно лечить в нерабочем состоянии.В случае травмы поджелудочной железы мультидисциплинарный подход, включающий: показаны бригады врачей / гастроэнтерологов и хирургов.
В педиатрической литературе о показаниях к операции гораздо больше ограничено. Что касается билиарного панкреатита, ретроспективная серия случаев из 19 детей, госпитализированных с билиарным панкреатитом, зарегистрировано 9 детей, перенесших ранний холецистэктомия без побочных эффектов и 4 из 10 детей, перенесших отсроченную операцию возникновение нежелательных клинических явлений (включая рецидив панкреатита) (228).
Резюме: Показания к острому хирургическому вмешательству. к показаниям АП относятся травмы живота, при которых у пациента нестабильность и / или поиск происходит сопутствующее повреждение других органов. В контексте билиарного панкреатита было показано, что холецистэктомия не только безопасна, но и предотвращает рецидивы, если они происходят. в рамках индекса госпитализации. Литература для взрослых предполагает, что раннее вмешательство в некроз поджелудочной железы приводит к увеличению заболеваемости и смертности, и, следовательно, к санации раны желательно отсрочить некроз поджелудочной железы, вызывающий нестабильность у пациента, по крайней мере, на 4 часа. недель с момента обращения, в идеале — эндоскопическим или чрескожным способом.
Рекомендация 2li: холецистэктомия безопасно может и следует выполнять перед выпиской в случаях легкой неосложненной острой желчной болезни. панкреатит.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2lii: В ведении острых некротических скоплений, вмешательств следует избегать и откладывать, даже для инфицированных некроз, поскольку результаты лучше при отсроченном (> 4 недель) подходе.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 6; нейтральный = 2; не согласен = 1; категорически не согласен = 0.
Рекомендация 2liii: Когда требуется дренирование или некрэктомия. необходимые нехирургические доступы, включая эндоскопические (EUS и ERCP) или чрескожные методы предпочтительнее открытой некрэктомии или открытой псевдокисты дренаж.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 9; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
3. ИСХОДЫ ОСТРОГО ПАНКРЕАТИТА ПЕДИАТРИИ
Общие исходы ОП у детей благоприятны по сравнению со взрослыми. В средняя продолжительность госпитализации детей с ОП составляет в среднем от 2,8 до 8 дней, хотя младенцы / малыши, как правило, поступают на более длительный период времени (в среднем 19,5 дней) (15, 73, 229–231). Раннее начало энтерального питания и агрессивная жидкостная реанимация был связан с более коротким пребыванием в больнице, меньшим количеством госпитализаций в отделения интенсивной терапии и снижение показателей тяжелого АП по сравнению с пациентами, находящимися в НКО (73).Эти результаты в целом совпадают с выводами большинства взрослых. исследований (232), но, возможно, не применялись к педиатрические пациенты до недавнего времени. Более высокая смертность при ПД у детей связана с системное заболевание, но в целом низкий и составляет менее 5% в большинстве когорт, даже в том числе в реанимации (15, 30, 233, 234).
Осложнения с ранним началом при ОП включают полиорганную дисфункцию или шок (15). Острые скопления перипанкреатической жидкости наблюдаются в острая фаза панкреатита и имеет тенденцию к спонтанному разрешению.Частота образование псевдокист колеблется от 8% до 41% у детей с панкреатитом, и более высокие показатели наблюдаются у пациентов с панкреатитом, связанным с абдоминальной травма (15, 212, 235). Псевдокисты часто бессимптомный и может лечиться консервативно или стать больше и вызвать боль в животе, рвота или лихорадка. Они также могут заразиться в 10–15% случаев. (236). Еще одно осложнение с поздним началом связано с до некроза поджелудочной железы. Некроз может проявляться в первую очередь в виде острого некротического скопления. (ANC), а затем созревают до некроза без стенок (WON) (8).Варианты лечения при дренировании псевдокист и некротических стенок коллекции включают эндоскопический (транспапиллярный или трансмуральный) дренаж, чрескожный катетерный дренаж или открытая / лапароскопическая операция. Выбранная модальность зависит от размера, расположение, анатомия и риски / преимущества процедуры, хотя чрескожная и Трансгастроинтестинальный дренаж под контролем эндоскопического ультразвука (ЭУЗИ) в настоящее время становится все более популярным. широко распространено (237).
Примерно 15–35% детей с острым у панкреатита будет еще один приступ панкреатита.Острый рецидивирующий заболевание у детей панкреатит связан с панкреатико-билиарными аномалиями, аутоиммунным панкреатитом, нарушения обмена веществ и наследственный панкреатит (15).
Резюме: За детьми необходимо следить во время их курс АП при местных и системных осложнениях, которые могут включать дисфункцию органов, острые скопления жидкости и впоследствии некроз или псевдокисты. Общий педиатрические пациенты с острым панкреатитом имеют хороший прогноз с очень низким уровнем смертность, но сообщается о частоте рецидивов до 15–35%.
Рекомендация 3: Дети с острым панкреатитом должны получить тщательное наблюдение со стороны поставщика медицинских услуг для выявления раннего или позднего осложнения или рецидивы.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
A Clinical Отчет Комитета по поджелудочной железе NASPGHAN
1. ПЕРВОНАЧАЛЬНАЯ ОЦЕНКА И ДИАГНОСТИКА ОСТРОГО ПЕДИАТРИЧЕСКОГО ПАНКРЕАТИТА
Недавние исследования оценивают заболеваемость острым панкреатитом (ОП) при ~ 1/10 000 детей в год (2, 7), заболеваемость приближается к взрослым.Есть нет научно обоснованных руководств по диагностике ОП у детей. ВДОХНОВЕНИЕ ( IN международный S tudy Группа компаний P медицинский P анкреатит: I n Найдите Cu RE ) определение детской AP является экспертное определение смоделировано по критериям Атланты у взрослых (8). Согласно критериям INSPPIRE, для диагностики АП требуется как минимум 2 из следующего: (1) боль в животе совместима с AP, (2) значениями сывороточной амилазы и / или липазы ≥3 раза верхние пределы нормы, (3) визуализация результаты согласуются с AP (9, 10).INSPPIRE или другие критерии не касаются этапов (ранних или поздний) АП у детей или типов (интерстициальный отечный панкреатит, некротический панкреатит, инфицированный панкреонекроз) или степень тяжести ОП (легкая, умеренная или тяжелая форма ОП при мультисистемной органной недостаточности).
Детский диагноз ОП обычно подозревается клинически с совместимым симптомом презентации, подтвержденные лабораторными и / или радиологическими исследованиями. Боль в животе и / или раздражительность являются наиболее частыми проявлениями ОП у детей, за которыми следуют эпигастральные болезненность, тошнота и рвота (11, 12).У младенцев и детей ясельного возраста симптомы могут быть незаметными; поэтому диагноз требует высокого уровня подозрений. Желчные / обструктивные факторы, лекарственные препараты и системные заболевания являются основными причинами ОП у детей (1, 4, 9, 12–23), и знание этих возможных причин поможет руководить начальными исследованиями.
Процент детей, у которых развиваются «тяжелые» острые панкреатит варьирует в опубликованных сериях (6–34), но дети с ОП в в целом имеют легкое течение (11, 24, 25). В подмножестве у пациентов АП может иметь тяжелое течение (8), но нет установленные клинические инструменты предсказывают этот результат.Балльные системы оценки степени тяжести АП у взрослых (Рэнсон, Глазго, модифицированный Глазго, Прикроватный индекс тяжести острых заболеваний). Панкреатит (BISAP) и оценка острой физиологии и хронического здоровья II (APACHE II)) не легко применимы к детям по нескольким причинам (26). Детская шкала острого панкреатита (PAPS) ДеБанто (27) была оценена у детей, но имеет низкую чувствительность. и требует 48 часов для прогнозирования рисков. Точно так же степень тяжести компьютерной томографии индекс (CTSI) или балл Бальтазара (28), опирается на радиологический внешний вид и, следовательно, нежелателен в детской возрастной группе из-за радиации экспозиция.Благодаря своей широкой доступности липаза является привлекательным маркером для выявления тяжелых случаев AP (25), но может выявить много ложных положительных из-за его низкой положительной прогностической ценности и специфичности. Коффи и др., обнаружили, что липаза сыворотки в семь раз превышает верхний предел нормы в течение 24 часов после презентация помогла предсказать тяжесть острого панкреатита (25). Тем не менее, это ретроспективное исследование с участием 211 детей и не были проверены в более крупных исследовательских группах. Suzuki и др. В Японии разработали удобная для детей система оценки степени тяжести с использованием 9 параметров (29), но это также было ретроспективным исследованием, в котором оценивались только 145 пациентов, и авторы пришли к выводу, что результаты не могут быть широко применимы к педиатрическое население.Совсем недавно Сабо и др. Сообщили, что ранняя степень тяжести прогностическая модель с использованием сывороточного альбумина, липазы и количества лейкоцитов, полученных в 24 часа продемонстрировали положительную прогностическую ценность 35% и отрицательную прогностическую ценность значение 91% (30).
Необходимы дальнейшие проспективные исследования для определения клинической применимости любой из этих инструментов. В вышеупомянутых исследованиях использовались различные определения степени тяжести. AP, что ограничивает возможности проведения сравнений между исследованиями. Недавняя публикация Комитет по поджелудочной железе NASPGHAN обратился к необходимости иметь четко определенную классификацию степени тяжести АП, предлагая определения легкой, средней и тяжелой степени АП для повысить однородность исследований (31).
Биомаркеры сыворотки
Острый панкреатит — это в первую очередь клинический диагноз, основанный на наличие как минимум двух из трех критериев, опубликованных INSPPIRE и Atlanta классификация (8, 9). Без выполнения двух из этих трех критериев трудно сделать диагностика АП. Основные биохимические маркеры, используемые для диагностики АП, включают сывороточную липазу. и сывороточная амилаза. Поскольку уровень липазы или амилазы в сыворотке не менее чем в три раза превышает верхний предел нормы считается совместимым с панкреатитом, важно знать справочные значения лаборатории для определения этого порога.И амилаза, и липаза обычно повышается на ранней стадии заболевания. Однако соотношение сыворотки уровни липазы или амилазы и тяжесть заболевания низкая (25, 32, 33). Липаза в основном секретируется поджелудочной железой, хотя другие источники липазы включают желудочные и язычные липазы. При АП липаза обычно увеличился в течение 6 часов после появления симптомов; уровень в сыворотке достигает максимума через 24–30 часов и может остаются повышенными более одной недели (34). Некоторые выступают за то, чтобы сывороточная липаза без сывороточной амилазы была достаточной для диагностики АП, поскольку липаза является более чувствительным и специфическим маркером АП (87–100% и 95–100% соответственно) (35–38).Липаза, кроме того, остается повышенным дольше, чем амилаза, что полезно в случаях отсроченного проявления (34, 39, 40). Уровни липазы также меньше изменяются этиология AP в отличие от амилазы, особенно в случае этанола (37, 41) или гиперлипидемия (42, 43). Но следует соблюдать осторожность при интерпретации уровней у детей. упражнения, поскольку было продемонстрировано, что нормальные значения липазы связаны с возрастом ребенок, растущий от новорожденного к ребенку, к взрослому (44, 45). Амилаза секретируется несколькими органами, прежде всего слюнные железы и поджелудочная железа.Большинство лабораторий измеряют общую амилазу уровни, которые содержат изоформы s-амилазы (слюна) и p-амилазы (поджелудочная железа) (46). Существуют лабораторные тесты для фракционирования p- и s-амилаза, но эта практика менее доступна. Эталонные значения амилазы отличаются в зависимости от используемого лабораторного теста, но также зависят от возраста и пола (47, 48). Сыворотка Уровни амилазы могут изменяться в зависимости от этиологии панкреатита, как указано выше. Амилаза уровни повышаются быстрее, чем уровни липазы, и часто могут нормализоваться через 24 часа после начала симптомы, ограничивающие полезность у пациентов с отсроченным обращением к врачу объект (34).Поскольку почки выводят амилазу и липазы, повышение этих ферментов не на уровне поджелудочной железы может наблюдаться у пациентов с повреждение или заболевание почек (46).
Несколько состояний, не связанных с панкреатитом, вызывают повышение уровня поджелудочной железы амилаза и / или липаза, включая декомпенсированную печеночную недостаточность, почечную недостаточность, кишечную воспаление (включая целиакию и воспалительное заболевание кишечника) брюшной полости травмы, диабетический кетоацидоз и травмы головы (49). Кроме того, некоторые люди продуцируют большие комплексы амилазы или липаза с иммуноглобулинами (так называемая макроамилаза и макролипаза), которые плохо фильтруется и выводится из-за большого размера, что приведет к повышенным значениям, если уровень фермента измеряется в крови, несмотря на то, что он не связан с воспалением поджелудочная железа (50).
Другие биомаркеры для диагностики и лечения панкреатита были предложены и изучены на животных моделях или небольших клинических испытаниях (см. обзоры в (46, 51, 52)). Однако ни один из них не получил известности, и многие еще предстоит пройти валидацию для общеклинического использования.
Несколько лабораторных тестов помогают контролировать течение АП (53). В целом электролиты сыворотки крови, мочевина крови азот (BUN) и креатинин, а также общий анализ крови (CBC) важны для мониторинга состояние жидкости / гидратации и почечная функция.Панель печеночных ферментов показана для поиска желчнокаменной или желчнокаменной этиологии, а также для оценки поражения органов. Кальций и Уровни триглицеридов следует рассматривать как исходные исследования (9). Мониторинг респираторного статуса может предупредить врача о том, что прогрессирование от легкой до среднетяжелой или тяжелой АД.
Этиология
Как упоминалось ранее, анатомическая, обструктивная (в том числе желчная), инфекционные, травматические, токсические, метаболические, системные заболевания, врожденные нарушения обмена веществ, генетическая предрасположенность и идиопатия были описаны как потенциальные этиологии при детском ОП, остром рецидивирующем панкреатите (АРП) и хроническом панкреатите (ХП) (3, 4, 54).Обзор Lowe et al суммировал 6 лучших общие этиологические категории в опубликованных обзорах как идиопатические / другие в 24%, травмы у 17%, системные заболевания у 15%, структурные аномалии в 14%, лекарства в 10% и инфекции в 8%. (3) Учитывая более частую этиологию, а также те, которые для которых существует направленная терапия, в рукописи 2012 года Morinville et al. опрос детских гастроэнтерологов, оказывающих панкреатологическую помощь, и предложили после обследования в первых случаях панкреатита: сывороточные ферменты печени, триглицериды и уровень кальция и УЗИ брюшной полости.Они предложили отложить тестирование на генетические причины / предрасположенности (которые в то время включали CFTR (муковисцидоз) регулятор трансмембранной проводимости), SPINK1 (ингибитор сериновой протеазы Kazal типа 1) и PRSS1 (катионный трипсиноген)), хлорид пота и более подробные изображения для случаев ARP, CP или первых экземпляров AP с повышенным риском рецидив, основанный на представлении, прошлой истории болезни или семейном анамнезе (9). При необходимости, поиск может быть проведен для конкретных факторы токсико-метаболического риска (55).Недавний публикация Gariepy et al, посвященная причинно-следственной оценке ARP и CP у детей, который имеет тенденцию быть более обширным из-за повторяющегося / хронического характера презентации (56) Аутоиммунный панкреатит (АИП) типов 1 и 2 редко диагностируются, но представляют разные типы панкреатита со специфическими гистологические данные в контексте суггестивных симптомов, визуализации, лабораторных исследований. результаты и ответ на терапию. Если AIP подозревается как этиология AP, в дальнейшем необходима поддерживающая оценка.Заинтересованные читатели будут перенаправлены на недавний публикация Scheers et al по педиатрической AIP (57).
Визуализация
Визуализация на ранней стадии ОП обычно не требуется, если в анамнезе / при предъявлении симптомы и биохимические маркеры сыворотки присутствуют для постановки диагноза. Визуализация становится актуально для документирования некроза поджелудочной железы, осложнений панкреатита, включая жидкость скопления и этиология панкреатита, например, камни в желчном пузыре / желчевыводящие пути или анатомические аномалии.
Золотым стандартом диагностической визуализации остается КЭКТ и несколько оценок. системы разработаны (58).Тем не мение, несмотря на то, что CETC является золотым стандартом визуализации, он часто не указывается и необходим для диагностики или лечения педиатрического AP. В неоднозначных случаях для диагностики ОП, например, при отсроченном проявлении, когда сывороточные маркеры могут быть низкими, компьютерная томография с контрастным усилением (CECT) может потребоваться для подтверждения AP. IV контраст является ключом к различению некротических участков поджелудочной железы (59). Поскольку ранняя визуализация может недооценивать степень заболевания и поскольку осложнения развиваются со временем, и результаты могут отсутствовать на ранних этапах фазе заболевания, в идеале CETC следует отложить как минимум на 96 часов после начала симптомы (8, 60).В легких случаях КЭКТ может показать усиление гомогенного органа, воспалительное изменения перипанкреатического жира или жидкости, окружающей поджелудочную железу (59) В тяжелых случаях КЭКТ может показать неоднородный орган усиление, некроз в поджелудочной железе или в окружающей перипанкреатической ткани. Кроме того, CECT может также идентифицировать скопления перипанкреатической жидкости или псевдокисты. КЭКТ следует пересмотреть при ухудшении клинического состояния пациента. или постоянно тяжелый (8). Lautz et al. нашел что индекс тяжести компьютерной томографии (шкала CTSI или Balthazar) в педиатрической пациенты дали чувствительность, специфичность, положительную прогностическую ценность и отрицательную прогностическая ценность 81%, 76%, 62% и 90%, соответственно, по степени тяжести в ретроспективном исследовании 64 детей (61).
Ультразвук широко используется в случаях, когда есть высокие подозрения на билиарный панкреатит, при котором полезно заранее определить необходимость терапевтического вмешательство (33, 58). Ультразвук имеет отличный профиль безопасности, неинвазивен и не использовать радиацию. Тем не менее, использование ультразвука может быть ограничено в оценке состояния. поджелудочной железы из-за мешающих структур, таких как кишечные газы в кишечнике и ожирение и имеет более низкую чувствительность при визуализации поджелудочной железы по сравнению с КЭКТ.
Магнитно-резонансная томография (МРТ) обычно не используется в качестве первичной визуализации техника при АП, но может быть полезна при поздних осложнениях (59). Это может быть особенно полезно для молодых или беременных. пациентам (с намерением ограничить облучение), и может разрешить использование альтернативных методов внутривенного контраста в пациенты с нарушением функции почек или аллергией на йодсодержащий контраст (60). МРТ также может быть более чувствительным при оценке некротическая ткань по сравнению с КЭКТ (59, 61). МР-холангиопанкреатография (MRCP) при AP наиболее часто используется для обнаружения камней в дистальных отделах общего желчного протока и диагностики желчных путей АП.МРТ / MRCP с использованием секретина помогает исследовать систему протоков в поджелудочной железы, а также общие аномалии желчных протоков, включая стриктуры или камни (62, 63). К оптимизировать обнаружение патологий протоков, MRCP может выполняться после атаки AP исчез, поскольку острый отек может затруднять визуализацию протоков. Использование MRCP, усиленный секретином, при заболевании поджелудочной железы у детей полностью не установлен (64) и доступ к секретину неодинаков через учреждения и страны.Lin et al подробно описывают использование МРТ и MRCP у детей. требуется визуализация поджелудочной железы, а также общие аспекты визуализации при AP (65).
Резюме и рекомендации
Рекомендация 1a: Диагностика острых заболеваний у детей панкреатит должен соответствовать ранее опубликованным критериям INSPPIRE.
Для диагностики ОП у педиатрических пациентов необходимы как минимум 2 из следующего: (1) боль в животе, совместимая с AP, (2) уровни амилазы и / или липазы в сыворотке ≥3 раза верхние пределы нормы, (3) результаты визуализации в соответствии с AP.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1b: Возможно выполнение первичной визуализации. с помощью трансабдоминального ультразвукового исследования, с другими методами визуализации (КТ, МРТ), зарезервированными для большего сложные случаи +/– с учетом подозреваемой этиологии.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 4; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1c: Основана на наиболее частой этиологии и те, для которых существуют варианты лечения, первый приступ острого панкреатита тестирование должно включать ферменты печени (АЛТ, АСТ, ГГТ, ЩФ, билирубин), триглицериды уровень и уровень кальция.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2. СООБРАЖЕНИЯ ВЕДЕНИЯ ПРИ ОСТРЫХ ПЕДИАТРИЧЕСКИХ ПАНКРЕАТИТАХ
2a.Инфузионная терапия при остром панкреатите
Внутривенная инфузионная терапия является основой лечения во время эпизода AP. Жидкая реанимация поддерживает адекватный жидкостный статус и диурез, но в последнее время внимание было сосредоточено на использовании внутривенных жидкостей для предотвращения потенциальных осложнений при ОП, такие как некроз и органная недостаточность. Патогенез ОП и прогрессирование до тяжелой степени. считается вторичным по отношению к нарушению микроциркуляции поджелудочной железы событиями, включая гиповолемию, повышенную проницаемость капилляров и образование микротромбы.Считается, что жидкостная реанимация не только устраняет гиповолемию, но и помогает сохранить микроциркуляцию поджелудочной железы, обеспечивая адекватную перфузию и предотвращая возможное образование микротромбов и, таким образом, предотвращение осложнений и прогрессирования тяжелое заболевание (66).
Тип жидкости
Отсутствует консенсус относительно идеального количества и типа жидкости для использования во время эпизода ОП во взрослой практике, и существует еще меньше данных, относящихся к жидкости в педиатрической популяции. Кристаллоид был наиболее рекомендуемым типом жидкость в руководствах для взрослых (33, 67–70).А Основное преимущество кристаллоидов в том, что они легко и быстро доступны. Обычный физиологический раствор (NS) долгое время был предпочтительным кристаллоидом для начальной жидкостной реанимации в в целом, но в некоторой литературе для взрослых предполагается, что лактатные звонаги (LR) являются более оптимальными для AP. В небольшом рандомизированном контрольном исследовании (РКИ) с участием 40 взрослых с AP Wu et al. что LR снижает частоту синдрома системного воспалительного ответа (SIRS) и уровни С-реактивного белка через 24 часа по сравнению с NS (71). Напротив, ретроспективный обзор 103 пациентов не смогли показать какой-либо существенной разницы между LR и NS в качестве начального реанимационная жидкость у взрослых с панкреатитом различной степени тяжести (72).LR был рекомендован по сравнению с NS в Международном Рекомендации Ассоциации панкреатологов / Американской панкреатической ассоциации (IAP / APA), но в рекомендациях Американской гастроэнтерологической ассоциации (AGA) только говорится, что LR может быть лучший выбор, но не был сильной рекомендацией (68, 70). В педиатрии это было показали, что агрессивное введение жидкости в течение первых 24 часов с помощью физиологического раствора с 5% декстрозой является безопасным и хорошо переносимым вариантом (73), но его не сравнивали с другими типами жидкостей для внутривенного вливания. (например, LR).
Коллоиды (например, альбумин, свежезамороженная плазма или упакованные эритроциты) не рекомендованы в качестве начальной реанимационной жидкости при АП. Коллоидные компоненты оставаться во внутрисосудистом пространстве из-за большего размера и может втягивать жидкость в кровообращение из интерстиция вторично по отношению к осмотическому эффекту. Руководящие принципы AGA рекомендует коллоид в определенных ситуациях, когда гематокрит < 25% альбумина составляет <2 г / дл (68), при этом другая публикация рекомендует соотношение кристаллоидов и кристаллоидов 3: 1. коллоид (74).
Скорость введения жидкости
Агрессивность жидкостной реанимации при АП также обсуждалась. В время вмешательства агрессивной жидкостной терапии может быть ключевым. Учеба взрослых в пользу ранних и агрессивных жидкостей в AP включают несколько ретроспективных исследований, которые использовали разные стратегии, такие как предоставление> против <33% от общего количества жидкости в течение первых 24 часов, а другой обеспечивает 3,5 л по сравнению с 2,4 л внутривенно в течение первых 24 часов (75). В основном, те, кто получает более агрессивные объемы жидкости внутривенно в течение первых 24 часов, как правило, улучшили результаты, включая смертность, но даже в рамках различных исследований результаты противоречивы в отношении того, снижает ли более высокое раннее введение жидкости некроз, синдром системного воспалительного ответа (SIRS) и продолжительность пребывания в стационаре (76).Напротив, Mao et al. Сообщили о РКИ 76 пациентам с тяжелым АП назначена медленная гемодилюция (5–10 мл / кг / ч) или быстрая гемодилюция (10–15 мл / кг / ч), демонстрирующая, что быстрая агрессивная ранняя жидкость введение привело к более высоким показателям сепсиса и смертности (77). de-Madaria et al провели проспективное исследование 247 человек. пациенты делятся на пациентов в зависимости от количества жидкости, введенной в первые 24 периода. часы. Группа, получавшая наибольший объем,> 4,1 л, имела повышенный уровень стойкая органная недостаточность (78).Weitz и др., рассмотрели 391 случай АП и обнаружили, что использование агрессивных жидкостей (примерно 5 л) было неэффективным. связаны с обострением заболевания и местными осложнениями (79). Опасения по поводу этой последней группы исследований заключаются в том, что в основном они касались более больных пациентов, и жидкостные режимы не ограничивались первые 24 часа реанимации.
Несколько экспертов и групп с тех пор дали рекомендации по скорости жидкостная реанимация в первые 24–48 часов у взрослых с ОП.МАП / АПА руководящие принципы рекомендуют пациентам получать 5–10 мл / кг / час до реанимации. цели достигаются в отношении улучшения частоты сердечных сокращений, диуреза, среднего артериальное давление и / или гематокрит (70). В Американский колледж гастроэнтерологии (ACG) рекомендует начальную скорость 250–500 мл / час, в дополнение к болюсу жидкости, если гипотензия или тахикардия присутствуют и используют BUN для направления терапии (33). Подобные рекомендации сделаны в обзоре Whitcomb et al (80). Aggarwal et al. советует 3–4 л жидкости в первые 24 часа (не более 4 л) с начальным болюсом 1 л и последующие 3 мл / кг / час в течение первых 24–48 часов (81).Наср и др. первоначально рекомендуют болюсы 1–2 л и 150–300 мл / час (82). Впоследствии они рекомендуют 2 мл / кг / час, если пациент отвечает на первоначальную реанимацию, но в противном случае использовать 3 мл / кг / час (82).
Только в одном педиатрическом исследовании оценивались разные нормы поддерживающей жидкости. администрации с участием 201 пациента с ОП [69]. Это исследование показало, что сочетание ранних энтеральное питание (<48 часов) и агрессивные жидкости (> 1,5–2x техническое обслуживание в первые 24 часа) уменьшилась продолжительность пребывания и возникновение тяжелое заболевание по сравнению с более традиционным историческим лечением.Агрессивные внутривенные жидкости не повлияли отрицательно на исходы (в первую очередь, легочные осложнения или повторная госпитализация). ставки). Никакие исследования не указывают идеальную норму поддерживающих жидкостей в AP после начальная реанимация (> 24–48 часов), хотя Сабо и др. что 1,5–2-кратное поддержание было безопасным для их популяции пациентов (73). Нет педиатрических исследований, сравнивающих первоначальную реанимацию тома.
Резюме: В начальной фазе реанимации острого панкреатит, теоретические и потенциальные клинические преимущества в пользу LR выше NS на основе данные о взрослых, но отсутствуют педиатрические данные.
Рекомендация 2ai: Дети с острым панкреатит необходимо первоначально реанимировать кристаллоидами, либо с LR, либо с NS в острой постановке. На основании оценки статуса гидратации / гемодинамического статуса, если при наличии гемодинамических нарушений рекомендуется болюсное введение 10–20 мл / кг.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Резюме: Педиатрическая литература жидкостная реанимация и скорость введения жидкости при остром панкреатите.Взрослый литература предлагает болюсы 250–1000 мл на начальном этапе и до 3–4 л. жидкости в течение первых 24 часов.
Рекомендация 2aii: Дети с диагнозом острой панкреатит следует назначать 1,5–2-кратное поддерживающее внутривенное введение жидкостей с мониторингом диуреза в течение следующих 24–48 часов.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 12; согласен = 10; нейтральный = 2; не согласен = 0; категорически не согласен = 0.
2b. Мониторинг детей с диагнозом ОП / внепанкреатические проявления острый панкреатит
Хотя это еще не изучено у педиатрических пациентов, полиорганная болезнь у взрослых пациенты с ОП связаны с худшими клиническими исходами с более чем половиной случаев, связанных с ОП. смерть в течение 1 недели от начала полиорганной дисфункции (83).Поражение сердца, легких и почек является ключевым фактором. компоненты систем оценки взрослых, используемых для прогнозирования тяжести эпизода ОП, включая модифицированная атлантская классификация, критерии Рэнсона, степень серьезности по Японии Оценка, оценка по Глазго, BISAP и APACHE II (8, 84–87). Педиатрические модели, прогнозирующие тяжесть ОП, также придают большое значение вовлечению нескольких органов, но оказались менее надежными (88) или еще не прошли проспективную валидацию (29). Повышенный эндотелиальный барьер проницаемость и глубокий выброс цитокинов, связанные с ССВО в сочетании с агрессивным гидратация теоретически увеличивает риск пациента для жидкости третьего промежутка и развитие внепанкреатических проявлений АП.Надлежащий мониторинг жизненно важен для сбалансировать соответствующую жидкостную реанимацию, пытаясь предотвратить сердечную, легочную и почечные осложнения (89).
Сердечно-сосудистый мониторинг
Гиповолемия при поступлении является надежным предиктором заболеваемости и смертности среди взрослых с AP и, по-видимому, коррелирует с величиной SIRS (89). Тахикардия использовалась как при системы оценки взрослых и детей для прогнозирования тяжести ОП и ее улучшение использовались для подтверждения адекватной реанимации жидкости в дополнение к мониторингу мочи объем и тургор кожи (71, 81).Регулярный кардиологический мониторинг взрослых у пациентов, не получающих ОИТ включает регулярные измерения жизненно важных функций каждые 8 часов для получения информации о состоянии сердечно-сосудистой системы (71). Дополнительно редкие случаи тампонады сердца и предсердий. Сообщалось о фибрилляции при АП, и ее следует учитывать при стандартном кардиологическом исследовании. обследование начато у пациентов с необъяснимой гипотонией, одышкой и / или боль в груди (90–93).
Мониторинг легких
Исследования на взрослых и животных модели показывают острый респираторный дистресс синдром (ОРДС), пневмония и отек / выпот легких как ранние осложнения ОП, обычно в течение первых 48 часов (15, 94).Поскольку ОРДС является наиболее распространенным критическим осложнение тяжелого АП, связанного с полиорганной дисфункцией у взрослых (95), аномальное P a O 2 или аномальные изображения легких являются компонентами всех обычно используемых систем оценки для предсказать тяжесть приступа ОП (8, 29, 84–87). Регулярный мониторинг насыщение кислородом во время агрессивной гидратации обычно осуществляется, с некоторыми койки пациентов должны быть подняты на угол 30 градусов, чтобы снизить вероятность легочная секвестрация (71).Стандарт следует рассмотреть возможность обследования легких и ухода за пациентами с необъяснимыми одышка, ухудшение кашля и / или затрудненное дыхание (94).
Мониторинг почек
Острое повреждение почек (ОПП) через синдром брюшной полости (83, 96) или вызванное воспалением повреждение проксимального извитого канальца (97), отмеченное повышением уровня азота мочевины и креатинина, а также снижение диуреза, это известное раннее осложнение АП у детей и факторы занимает важное место в оценочных системах AP для прогнозирования тяжести заболевания (8, 15, 29, 84–87).В некоторых исследованиях на взрослых было показано, что только мочевины быть столь же эффективным в прогнозировании тяжести заболевания, как и более продвинутые системы оценки (98) и AKI был связан с В 10 раз повышен риск смерти при тяжелом ОП (99). Таким образом, BUN и креатинин считаются важными маркерами для следить за проведением инфузии и контролировать ОПП у взрослых во время первого 48 часов и при агрессивном увлажнении (71, 81, 98). Хотя нет никаких руководств, документирующих частоту мониторинга этих параметров, 8–12 часов использовались в одном исследовании для определения реакции на управление жидкостями (71).Рекомендации ACG подчеркивают важность снижения АМК и поддержания нормального уровня креатинина в первые 24 часа, поэтому очень важен ранний мониторинг (33). В редких случаях требуется непрерывная вено-венозная гемофильтрация (CVVH). для предотвращения дальнейшего повреждения почек, предотвращения синдрома брюшной полости и / или removae воспалительных цитокинов, но его использование не изучалось у педиатрических пациентов с AP (100). Может понадобиться установить мочевой катетер для точного документирования диуреза, особенно при седативном ребенок в условиях отделения интенсивной терапии.
Резюме и рекомендации
Наблюдение за пациентами с острым панкреатитом может дать индикаторы возникающие осложнения, включая ССВО и органную дисфункцию / недостаточность. Сердечный, следует особенно внимательно следить за респираторным и почечным статусом в течение первого Через 48 часов после обращения, так как большинство осложнений начинается в течение этого периода. период времени. Диурез — важный маркер адекватной жидкостной реанимации, при этом литература для взрослых, предлагающая стремиться к достижению> 0.5–1 куб. См / кг / час (Руководство IAP / APA).
Рекомендация 2bii: Пациентам, поступившим в в стационарном отделении необходимо измерять жизненно важные показатели не реже, чем каждые 4 часа в течение первых 48 дней. часы приема и в периоды агрессивной гидратации для контроля кислорода сатурация, артериальное давление и частота дыхания. Частота регулируется в зависимости от клинический статус. Нарушения жизненно важных функций должны требовать обследования у специалиста.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2biii: АМК, креатинин и моча производительность следует регулярно контролировать в течение первых 48 часов как маркер соответствующее ведение жидкости и скрининг на острое повреждение почек. Аномалии должен вызвать нефрологическое обследование.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 4; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
2с. Обезболивание при остром панкреатите
Боль в животе является наиболее частым симптомом ОП.В педиатрической АП исследования, от 80% до 95% пациентов жаловались на боль в животе. Пациенты присутствует с болью в эпигастрии у 62-89% и диффузно у 12% до 20%. «Классическое» проявление иррадиации боли в эпигастрии. к спине встречается только у 1,6–5,6% педиатрических пациентов (15, 16).
Патофизиология ОП характеризуется потерей внутриклеточных и внеклеточная компартментализация, которая может быть результатом различных механизмов: обструкция секреторного транспорта поджелудочной железы; активация ферментов; или неспособность остановить каскад активации.АП встречается у генетически предрасположенных лиц, у которых воспалительная реакция вызывает панкреатит. Это, в свою очередь, стимулирует внутреннюю панкреатические и соматические болевые рецепторы брюшины (101). Другие постулируемые механизмы, вызывающие боль в переднем отделе позвоночника, включают высокое давление. внутри железы или протока поджелудочной железы с последующей ишемией железы. Боль в AP тоже бывает вероятно, связано с высвобождением тахикинина, вещества P и кальцитонина, связанного с геном. пептид. Факторы, которые стимулируют первичные сенсорные нейроны, включают ионы водорода, тепло, лейкотриены, метаболиты арахидоновой кислоты, брадикинины и протеазы, такие как трипсин, выпущен во время AP (102).
Обезболивание — важная терапевтическая цель при лечении ОП и обычно включает использование анальгетиков периферического и центрального действия. Нет данных опубликованы по оптимальному обезболиванию в педиатрической AP, а исследования у взрослых не определили одно лучшее лекарство (67).
Опиоидные анальгетики
Потому что классические анальгетики периферического действия (такие как ацетаминофен) часто недостаточны при тяжелом панкреатите, часто требуются опиаты для контроля боль.Морфин или родственные ему опиоиды употребляли 94% респондентов для вести детей с ОП в соответствии с анкетой для врачей INSPPIRE 2012 года (103). Сообщалось, что морфин вызывает дисфункция сфинктера Одди после системного введения (104). Однако нет четких доказательств, подтверждающих эту теорию, и морфин можно безопасно применять у пациентов с ОП (105). Меперидин применялся у взрослых с АП, но его недостатки включают: короткий период полураспада и потенциал нейротоксичности за счет накопления токсичных веществ. нейрометаболиты, которые могут приводить к судорогам, миоклонусу и тремору (106).Обзор наркотиков и функции сфинктера Одди. Thomson et al, документально подтверждают, что на сегодняшний день нет исследований, напрямую сравнивающих эффекты меперидин и морфин на сфинктере манометрии Одди и никаких сравнительных исследований существуют у пациентов с АП. Кроме того, не существует исследований или доказательств, указывающих на то, что морфин противопоказан к применению при ОП (107). Кокрановский обзор 2013 года включает 5 исследований, в общей сложности 227 Субъекты для оценки эффективности и безопасности нескольких опиоидов. Включенные лекарства были бупренорфин, петидин, пентазоцин, фентанил и морфин.Общий вывод состоит в том, что опиоиды могут быть подходящим выбором при лечении боли. связанных с AP, и они могут уменьшить потребность в дополнительной анальгезии. Кроме того, риск осложнений, связанных с панкреатитом, или клинически серьезных побочные эффекты не отличаются от опиоидов и других анальгетиков (108).
Опиоидсберегающие анальгетики
Предполагается, что НПВП являются потенциальными участниками развитие AP, но также показали преимущества при лечении боли в AP.Профилактическое Было показано, что НПВП, включая индометацин и диклофенак, полезны при нескольких исследования по профилактике панкреатита после ЭРХПГ (109, 110). Что касается боли После постановки диагноза АР индометацин превосходит плацебо и не показали повышенного риска желудочно-кишечного кровотечения в небольшом исследовании (111). По сравнению с морфином метамизол показал улучшение снятие боли через 24 часа, но разница не достигла статистической значимости (105).
Системное введение местных анестетиков, в основном новокаина, было выступает в качестве основного обезболивающего при АП.Предлагается внутривенное введение новокаина для уменьшения боли. и / или необходимость вспомогательных обезболивающих и, возможно, улучшения клиническое течение АП. В одном контролируемом исследовании системное введение новокаина в улучшение панкреатита и ускоренное послеоперационное восстановление после обширного абдоминального хирургическое вмешательство, включая уменьшение боли, улучшение когнитивных функций и сокращение длительность кишечной непроходимости, а также общая госпитализация (112). Но доказательства ограничены, а плацебо-контролируемые исследования отсутствуют. данные.
Эпидуральная анестезия (ЭА) широко используется для индукции обезболивания в в периоперационный период, а также для уменьшения боли у пациентов с ОП. В принцип действия был приписан блокаде симпатического нерва, который перераспределяет внутренний кровоток к неперфузируемым областям поджелудочной железы. В исследовании с участием 35 пациентов с прогнозируемым тяжелым ОП, ЭА значительно уменьшала болевые ощущения, улучшала перфузия поджелудочной железы на основе радиологических исследований перфузии и улучшения клинических исходы (снижение потребности в некрэктомии) (113).Проспективное исследование 121 пациента продемонстрировало хорошую эффективность. и безопасность EA у взрослых AP (114).
Резюме: Нет данных, обеспечивающих оптимальную боль управление в педиатрической АП. Исследования на взрослых не выявили ни одного превосходящего медикамент. Нет доказательств, подтверждающих утверждение, что морфин вызывает неблагоприятные события на сфинктере Одди.
Рекомендации 2ci: Внутривенный морфин или другой препарат опиоид следует использовать при острой боли при панкреатите, не реагирующей на ацетаминофен или НПВП.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 2cii: Услуги специалиста по острой боли в идеале следует проконсультироваться в случаях более сильной боли, чтобы уменьшить боль управление.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2d. Энтеральное и парентеральное питание при остром панкреатите у детей
Пероральное и энтеральное питание
Традиционно пациенты с ОП лечились, не вводя перорально (115) и давая парентеральное питание (PN) (116).Было высказано предположение, что отдыхая кишечник, поджелудочной железе дали «отдохнуть» и, таким образом, зажить быстрее. В Обоснованием этой теории было то, что наличие пищи в кишечнике стимулируют высвобождение холецистокинина (ХЦК), что, в свою очередь, стимулирует поджелудочную железу. секреция ферментов, что может привести к дальнейшей активации протеолитических ферментов и преувеличивают процесс самопереваривания и усугубляют травму (117, 118)
У взрослых проводится ряд контролируемых исследований, обзоров и метаанализов. лечебному питанию как при тяжелом, так и при легком ОП, включая обзор голландских Группа по изучению панкреатита и согласованные рекомендации, опубликованные Международный комитет по руководящим принципам консенсуса (119).Lodewijkx et al., Считают, что энтеральное питание превосходит парентеральное питание, а стратегия кормления по требованию в прогнозируемой тяжелый АП (120). Мирталло и др. Рассмотрели 8 социальные отчеты с целью разработки международных согласованных руководящих принципов по питанию терапия в АП (119). Они пришли к выводу, что в АП у взрослых, энтеральное питание (ЭП) было предпочтительнее, чем ПП, и его следует использовать в первую очередь даже при наличие свищей, асцита и псевдокист.
Рекомендуется начинать EN как можно раньше, тем более, что одна из целей энтеропатии — предотвратить бактериальную транслокацию и тем самым предотвратить развитие ССВО.Ранняя нутритивная терапия также предназначена для снизить цитокиновый ответ и частоту пареза желудка и кишечной непроходимости. В то время как некоторые исследования (121) не показывают разницы в исходы, когда ЭП была начата до или после 72 часов презентации, 2008 г. метаанализ, изучавший одиннадцать РКИ, показал, что ЭП началась в течение 48 часов после презентация значительно снизила показатели смертности, инфекций и полиорганной отказ по сравнению с PN (122). Эти эффекты были уменьшены, когда ЭП была начата через 48 часов.В обзоре питания за 2011 г. поддержка взрослых AP, был сделан вывод, что ранняя нутритивная поддержка, особенно ЭП, но также и ПП, уменьшали количество осложнений и улучшали выживаемость (123). В этом обзоре говорилось, что для его эффективности нутритивная поддержка должна была начаться в течение 72 часов. Было заявлено, что EN следует считается « активным терапевтическим вмешательством, улучшающим исход больных панкреатитом »(124).
Клинические исследования, сравнивающие результаты PN и EN у пациентов с AP сообщить, что использование EN при тяжелом остром панкреатите (SAP) или прогнозируемые результаты SAP значительно снижает частоту осложнений (125–133).Недавний метаанализ продемонстрировал превосходство ЭП по сравнению с ПП с меньшей частотой инфекции и полиорганной недостаточности, что приводит к снижению показателей смертности и сокращению пребывание в больнице (134). Однако, поскольку полный EN не всегда возможно во время AP из-за усиления боли или непереносимости кормления, некоторые отстаивают роль комбинации EN и PN. В одном исследовании рандомизировали 100 пациентов для получения только ПП по сравнению с ПП в комбинации только с ЭП или ЭП, сепсис, внутрибрюшная инфекция и продолжительность госпитализации снизились, когда ЭП была входит в состав руководства (135).
Описанные пути ЭП включали желудочный и тощей кишки. Два маленьких исследования не обнаружили разницы в результатах между назогастральным (НГ) и назоеюнальным (НД) сытые группы (136, 137). Мета-анализ 10 РКИ не показал различий в исходы между группами, получавшими (полу) элементарные и полимерные формулы. (138)
Никаких руководств по нутриционной поддержке дети с АП. Недавнее исследование Abu-El-Haija et al. продемонстрировал выполнимость установления энтерального питания в педиатрической АП, не усложняя курс или влияя на оценку боли AP (139).Из того же центра ретроспективное исследование показало, что сочетание раннего энтерального кормления плюс более чем 1,5-кратное поддерживающее внутривенное введение жидкости были связаны с более коротким продолжительность пребывания и более легкое заболевание по сравнению с теми, кто оставался НКО в течение 48 часов и имели более низкую частоту ЭКО, чем поддерживающую терапию (73). Сообщается о двух детях с тяжелым ОП, которые успешно вылечились. с назоеюнальным кормлением в отделении интенсивной терапии интенсивной терапии и переключением на пероральное кормление при выписке в общая палата (140).
Парентеральное питание
Родительское питание обеспечивает организм необходимыми калориями и питательными веществами. компенсировать катаболическое состояние.Обеспокоенность, что ПП может стимулировать поджелудочную железу. и приводить к преувеличению процесса самопищеварения не было подтверждено литература (141, 142). Данные показывают, что настой протеина не стимулируют секрецию поджелудочной железы (143). Когда при сравнении различных форм ПП, сообщалось, что ПП, усиленный глутамином, снизить общую частоту осложнений, а также сократить продолжительность пребывания в стационаре (144–148). Введение глюкозы внутривенно также не стимулирует секреция поджелудочной железы (149, 150).Инфузия глюкозы тяжелобольным пациентам может быть полезно для обеспечения легкодоступного источника энергии во время катаболического состояния и противодействуют глюконеогенезу из-за распада белка. Но настой глюкозы обязательно под наблюдением, так как это может предрасполагать к гипергликемии (151), поскольку воспаленная поджелудочная железа может не подавать соответствующий инсулин отклик.
Гипертриглицеридемия связана с тяжелым ОП (152–155), но механизм, ведущий к SAP, не ясен (156). Недостаточно данных, чтобы рекомендовать или препятствовать использованию парентеральные липиды при АП.
Что касается времени PN в AP, где измеренный результат был смертности, данные свидетельствуют о том, что раннее ПП значительно более полезно, чем покой кишечника. при тяжелом ОП у взрослых (122). Во всех случаях, когда ЭП невозможна в течение длительного времени, например, при кишечной непроходимости, сложных свищах и т. Д. синдром брюшного отдела, PN. Напротив, недавнее исследование выступал за отсрочку начала ПП до 7 дней у тяжелобольных детей из-за повышенный риск инфицирования и повышенная частота осложнений после начала ПП в течение первых 24 часов после пребывания в отделении интенсивной терапии.Раннее энтеральное питание было разрешено в обоих группы. Однако присутствие или процент пациентов с ОП конкретно не было указано в этом отчете (157).
Резюме: Литература для взрослых поддерживает раннее энтеральное питание, чтобы уменьшить осложнения AP и улучшить выживаемость. Педиатрическая литература поддерживает раннее энтеральное питание в легких случаях ОП и небольшое сообщение в тяжелых случаях AP.
Рекомендация 2di: За исключением наличия прямого противопоказания к употреблению кишечника, детям с острым панкреатитом легкой степени может помочь от раннего (в течение 48–72 часов после обращения) орального / энтерального питания до уменьшения продолжительность пребывания и снижение риска органной дисфункции.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2dii: Парентеральное питание (ПП) должно следует рассматривать в тех случаях, когда ЭП невозможна в течение длительного периода времени (дольше более 5-7 дней), например, в кишечной непроходимости, сложных свищах, брюшной полости синдром, снижающий катаболическое состояние организма. Следует начать энтеральное питание. как можно скорее, причем комбинация EN и PN превосходит одиночную PN.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15 согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2diii: В случае панкреатической разрыв, перелом или разрыв протока, неясно, является ли пероральное / энтеральное питание может быть вредным в острой фазе. Это требует дальнейшего изучения.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 13; согласен = 8; нейтральный = 2; не согласен = 0; категорически не согласен = 0; нет голоса = 1.
2д. Использование антибиотиков при остром панкреатите у детей
Обоснование использования антибиотиков при лечении ОП связано к беспокойству по поводу бактериальной инфекции из-за перемещенной кишечной микробиоты. Антибиотики не рекомендуются для взрослых с легким ОП (70).
При лечении тяжелого ОП у взрослых изучались антибиотики для предотвращения и управлять инфекциями. Имипенем и / или цефалоспорины третьего поколения были наиболее исторически часто использовались в попытке снизить заболеваемость и смертность.Этот Профилактический подход является спорным: предыдущие исследования предполагали пользу (158–160), в то время как другие исследования не продемонстрировали пользы от рутинного использования (161) в отсутствие документально подтвержденной инфекции. Профилактические антибиотики использовались в условиях стерильной некротической болезни. панкреатит для предотвращения инфицированного некротического панкреатита (162, 163), особенно имипенем (163). Однако систематические обзоры не поддерживает преимущества в отношении смертности от инфекций, не затрагивающих поджелудочную железу, или для сокращения хирургических вмешательств у взрослых (162).Более поздние метаанализы подтверждают использование антибиотиков для инфицированы некротическим панкреатитом, но не для стерильный некроз (164–166). Текущий взрослый AP рекомендации — использовать антибиотики только при инфицированном некрозе или у пациентов с некротический панкреатит, госпитализированные и без клинического улучшения использование антибиотиков (70). Зараженный некроз должен быть подозревается, если клиническое состояние пациента ухудшается из-за лихорадки или наличие газа в коллекциях на снимках.В определенных ситуациях стремление жидкость под контролем эндоскопии или с помощью интервенционной радиологии и для руководства лечением может потребоваться создание соответствующего дренажа (8). При некротическом панкреатите известные антибиотики: проникают в некротические ткани, такие как карбапенемы, хинолоны и метронидазол, поскольку использование антибиотика в этих условиях, как было показано, задерживает хирургическое вмешательство. вмешательства и снизить заболеваемость и смертность (33).
Документированные инфекции, происходящие за пределами поджелудочной железы, следует рассматривать как указано.
Не было опубликовано исследований по использованию антибиотиков для лечения АП у детей.
Резюме: Антибиотики нельзя использовать в лечение ОП, за исключением случаев документально подтвержденного инфицированного некроза или у пациентов с некротическим панкреатитом, которые госпитализированы и клинически не улучшаются без использование антибиотиков. Антибиотики, о которых известно, что они проникают в некротические ткани, следует использовать при лечение инфицированного панкреонекроза, поскольку это может отсрочить хирургическое вмешательство и снизить заболеваемость и смертность.
Рекомендации 2ei: Профилактические антибиотики не эмпирически рекомендуется при тяжелом остром панкреатите.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
Рекомендация 2eii: показано только использование антибиотиков. в случаях документально подтвержденного инфицированного некроза при остром панкреатите.
16/24 = 67% согласны с рекомендацией. Рекомендация не поддерживается.Это было определено как область особых разногласий, требующих дальнейшего учиться.
Результаты голосования: Полностью согласен = 10; согласен = 6; нейтральный = 2; не согласен = 4; категорически не согласен = 0; нет голоса = 2.
2f. Использование ингибиторов протеазы при остром панкреатите у детей
Поскольку AP предположительно является некровоспалительным процессом, начавшимся через острая и несоответствующая активация трипсина протеазы и зимогенов поджелудочной железы внутри паренхимы, исследователи были очень заинтересованы в блокировании этого воспалительный процесс, чтобы ограничить степень травмы.
Два основных соединения, описанных в литературе для ингибирования этого фермента активация включает ингибитор сериновой протеазы габексат мезилат и трипсин ингибитор апротинин. В 1993 году Pederzoli et al. сообщил результаты рандомизированного, двойное слепое многоцентровое клиническое исследование использования габексата мезилата по сравнению с апротинином в АП-терапия. В этом исследовании мезилат габексата оказался более предпочтительным по сравнению с апротинином в отношении период 24–72 часа, но, что важно, отсутствует контрольная группа плацебо (167).Сроки лечения и способ родоразрешения кажутся быть ключевыми факторами эффективности (167, 168). Ино и др. изучили эффективность непрерывного инфузия регионарной артерии CRAI с габексатом мезилатом и антибиотиками при тяжелом ОП через небольшое проспективное исследование с участием 9 пациентов, получавших CRAI в течение 3-5 дней и 9 пациентов. другие получают терапию системными ингибиторами протеазы и антибиотики. Боль в животе и SIRS исчезал быстрее, LOS был значительно короче в группе CRAI (168). CRAI антипротеаз и антибиотиков имеет Сообщалось о снижении показателей CRP и APACHE II при применении в течение 72 часов после начала болезни (169), подход, описанный в педиатрических больных (170).
Обзор 2007 года, проведенный Китагавой и Хаякавой, не нашел доказательств, оправдывающих рутинное использование антипротеаз при AP, и хотя использование непрерывного внутривенного ингибиторы протеазы и антибиотики в высоких дозах могут быть эффективными для предотвращения обострения тяжелого ОП, необходимы исследования экономической эффективности. Важно, эти соединения не одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США. Штаты (171–173).
Резюме: Некоторые исследования взрослых подтверждают использование антипротеаз в лечении тяжелого АП, но никаких конкретных рекомендаций никогда не было были сделаны для их использования.Исследования не были рандомизированы с контрольными группами плацебо, и только несколько случаи описаны в педиатрических больных.
Рекомендации 2f: Антипротеазы не могут быть рекомендуется при лечении острого панкреатита у детей в это время.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 7; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2г. Использование антиоксидантов при остром панкреатите у детей
Окислительный стресс способствует повреждению ОП из-за образования кислорода свободные радикалы, вызывающие повреждение липидной мембраны клетки поджелудочной железы, деполяризацию митохондриальной мембраны и индукции фрагментации ДНК (174).Это способствует отеку, возникновению боли и может также быть вовлеченными в процесс некроза. Таким образом, была выдвинута гипотеза об антиоксидантах. иметь потенциальную пользу в качестве дополнительного лечения при АП, предотвращая образование свободные радикалы или улавливание существующих свободных радикалов кислорода.
Наиболее изученными агентами были витамины-антиоксиданты (аскорбиновая кислота, α-токоферол, β-каротин), неорганические антиоксиданты (селен) и глютамин. В двух частично совпадающих метаанализах, опубликованных в 2015 г., используются разные методологии оценки пользы антиоксидантов при остром панкреатите, один обзор 11 и другие 12 рандомизированных контролируемых исследований на взрослых [169, 170].Pederzoli et al. Обнаружили, что антиоксиданты снижают количество осложнений, связанных с ОП, и укороченный LOS с глутамином, снижающим частоту осложнений и смертность [169]. Ино и др. Сообщили, что антиоксидант терапия сокращает LOS и снижает уровень СРБ в сыворотке, но только через 10 дней [170].
Существенным ограничением опубликованных данных об антиоксидантах у взрослых AP является эти испытания включали весь спектр легкого и тяжелого АД. Кроме того, различные комбинации антиоксидантов и время доставки были использованы в испытания.В крупных рандомизированных исследованиях также отсутствует стандартизация конкретных антиоксидантов. как сроки и продолжительность лечения.
Нет данных об использовании антиоксидантов при AP в педиатрической популяции.
Резюме: педиатрические данные об использовании не хватает антиоксидантов в АП. Публикации для взрослых демонстрируют значительную неоднородность относительно состава, времени и продолжительности терапии. Несмотря на потенциальные преимущества описанных в сериях для взрослых, доказательств недостаточно, чтобы поддержать их использование в педиатрия в это время.
Рекомендация 2g: Антиоксиданты не следует считается стандартной терапией при лечении острого панкреатита у детей.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
2ч. Роль пробиотиков в лечении острого панкреатита у детей
Примерно у трети взрослых пациентов может развиться тяжелая форма АП, характеризующаяся ССВО, органная недостаточность и повышенный риск инфицирования (175).У пациентов с инфицированным перипанкреатическим и панкреонекрозом риск летального исхода значительно увеличивается. Снижение проницаемости кишечника и Предполагается, что избыточный бактериальный рост во время AP снижает риск инфицирования некроз поджелудочной железы и тем самым снизить риск смерти (176, 177).
Всемирная организация здравоохранения определяет пробиотики как «живые микробы. которые при введении в адекватных количествах приносят пользу их здоровью. хозяин». Доказано, что пробиотики играют роль в поддержании микрофлоры кишечника. баланс, подавляя рост вредных бактерий и усиливая иммунную функцию (178).Важно, что опубликованные исследования использовали различные составы и режимы дозирования пробиотических бактерий.
Muftuoglu et al. продемонстрировали, что lactobacillus acidophilus и bifidobacterium lactis уменьшают тяжесть гистологического повреждения в экспериментальной модели панкреатита (178). Ранние небольшие клинические испытания для взрослых показали положительную роль пробиотиков в управление АП. Olah et al. рандомизировали 45 пациентов для приема 10 9 живые или убитые теплом lactobacillus plantarum два раза в день вместе с энтеральное питание (179).Они обнаружили статистически значительно более низкий риск инфицированного панкреонекроза в исследуемой группе по сравнению с контрольные группы.
Однако впоследствии исследование PROPATRIA, двойное слепое, плацебо-контролируемое рандомизированное многоцентровое исследование роли пробиотиков в профилактике инфекционные осложнения при ОП) в составе 298 взрослых пациентов с прогнозируемой тяжелой AP продемонстрировал значительно более высокий риск смерти у многовидовых пробиотиков. группа (180, 181). Два небольших рандомизированных испытания с момента завершения не продемонстрировали увеличение смертности (182, 183), но влияние неблагоприятных результатов исследования PROPATRIA Исследование привело к общей осторожности при использовании пробиотиков у взрослых с ОП.
Ни одно педиатрическое исследование не изучало роль пробиотиков у детей с AP.
Резюме: После серии небольших дел, предполагающих потенциальная польза пробиотиков при ОП у взрослых, большое рандомизированное исследование продемонстрировало повышенная смертность в группе пробиотиков. Педиатрических исследований не опубликовано.
Рекомендации 2 часа: Нельзя рекомендовать пробиотики в лечении острого панкреатита у детей в настоящее время. Высшее качество опубликованные данные для взрослых показывают, что они могут не только не принести пользы, но и увеличивать смертность.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 14; согласен = 9; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2i. Роль эндоскопии в лечении острого панкреатита у детей
Различные причины воспаления слизистой оболочки двенадцатиперстной кишки связаны с увеличением риск AP. Проявления, связанные с глютеновой болезнью поджелудочной железы, включают эндокринные и внешнесекреторная недостаточность, острый и хронический панкреатит, нарушение питания, папиллярный стеноз вторичный по отношению к дуодениту или иммунологическим нарушениям, и все предположили, что быть вовлеченными механистически (184–186).Желчнокаменная болезнь была обнаружена до 34% пациентов с болезнью Крона и может проявляться как АП (187). Аутоиммунный панкреатит (АИП) и первичный склерозирование холангит (188) также может быть обнаружен у пациентов с воспалительным заболеванием кишечника, проявляющимся AP (189–191). Повышение уровня IgG4 наблюдается у взрослых пациентов с AIP типа I, педиатрические пациенты с AIP обычно без повышения уровня IgG4, при биопсии двенадцатиперстной или желудочно-дуоденальной воспалительной поражения могут быть полезны в диагностике (192, 193).Были случаи острого и хронического панкреатита. редко регистрируется как проявление или ассоциация инфекции H. pylori (194, 195). Чрезвычайно редко возможными причинами панкреатита у детей являются опухоли, связанные с ампула или периампулярная область двенадцатиперстной кишки. Такие поражения могут быть первыми идентифицируется рентгенологическим исследованием, но также может быть обнаружено во время эндоскопического исследования. оценка. Судя по имеющимся историям болезни, механизм развития у этих пациентов рецидивирующий панкреатит до конца не изучен, но, вероятно, связан с опухолью непроходимость на уровне ампулы (196, 197).Но в целом роль эзофагогастродуоденоскопия при ОП ограничена.
Нет исследований, оценивающих показания или преимущества эзофагогастродуоденоскопии в педиатрический AP.
Резюме: Роль эндоскопии в неотложной помощи дети с AP неясно. Возможность первичных внепанкреатических заболеваний В результате разработка AP требует вдумчивого рассмотрения.
Рекомендации 2i: Эзофагогастродуоденоскопия не в настоящее время считается стандартным диагностическим инструментом при остром панкреатите у детей.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2j. Роль ЭРХПГ при остром панкреатите у детей
Роль ЭРХПГ при ОП эволюционировала с технологическими улучшениями в диагностические возможности МРТ / MRCP и с увеличением педиатрического опыта с эндоскопическое ультразвуковое исследование (ЭУЗИ). Благодаря наличию этих последних диагностических инструментов для при заболеваниях поджелудочной железы, ERCP все чаще используется в первую очередь для лечения вмешательства или для неясных диагнозов после MRCP или EUS.ЭРХПГ безопасна для детей при этом наиболее частым осложнением является легкий панкреатит после ЭРХПГ. аналогичны таковым у взрослых (~ 3–10%), когда выполняются опытные эндоскописты (198–206). Обструкция желчевыводящих путей и хронический панкреатит являются наиболее частыми показаниями к ЭРХПГ у детей. В педиатрической AP ERCP имеет ограниченная роль, выполняется почти исключительно при билиарном панкреатите, вторичном по отношению к холедохолитиаз или отстой. ЭРХПГ при холедохолитиазе без панкреатита безопасна и эффективны (207, 208), но в педиатрии нет конкретных рекомендаций по сроки проведения ЭРХПГ при холедохолитиазе или остром билиарном панкреатите.У взрослых большой метаанализ и научно обоснованные рекомендации IAP по ведению острых билиарный панкреатит рекомендовал ЭРХПГ в течение 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. В противном случае можно провести ЭРХПГ. планово при неосложненном холедохолитиазе и в других случаях желчевыводящих путей. панкреатит независимо от степени тяжести (209, 210).
Менее распространенными показаниями для ЭРХПГ при ОП являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы (211).Камни и стриктуры протоков поджелудочной железы обычно признаки острого рецидивирующего или хронического панкреатита, поэтому встречаются относительно редко показания к ЭРХПГ при АП. В редких случаях, когда непроходимость протока предотвращает разрешение панкреатита, может быть проведена терапевтическая ЭРХПГ. Псевдокисты поджелудочной железы в у детей может развиться острый или хронический панкреатит, но чаще всего возникает после тупая травма. Псевдокисты поджелудочной железы представляют собой однородное скопление панкреатической жидкости. окружены фиброзной или грануляционной тканью, но не имеют эпителиальной выстилки (15, 212), и может развиться из скоплений жидкости, сохраняющихся более 4 недель (213).ERCP может использоваться для оценки коммуникации псевдокиста с протоком поджелудочной железы, куда можно установить транспапиллярный стент для дренаж. В противном случае — эндоскопическая цистагастростомия (214–216) и под контролем EUS. дренаж (217) — безопасные и эффективные способы дренировать псевдокисты поджелудочной железы у детей и может быть рассмотрено в зависимости от расположения псевдокиста. Повреждение протока поджелудочной железы и утечка также могут возникнуть в результате травмы. Рано эндоскопическое или хирургическое вмешательство может помочь свести к минимуму продолжающуюся заболеваемость протоковым утечка, поскольку ERCP обеспечивает быстрый и более точный метод определения местоположения и степень повреждения, чем MRCP или CT, а также дает возможность терапевтического стента размещение поперек травмы (218, 219).
Резюме: Роль ЭРХПГ при остром панкреатите. в первую очередь относится к терапевтическому лечению билиарного панкреатита, вторичного по отношению к холедохолитиаз или отстой. Литература для взрослых предполагает эффективность ERCP в пределах 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. Менее распространенными показаниями к ЭРХПГ при остром панкреатите являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы или разрывы протока.
Рекомендации 2ji и 2jii: (2ji) Роль ERCP ограничен при остром панкреатите и зависит от местных знаний.(2jii) ERCP — это показан при лечении острого панкреатита, связанного с холедохолитиазом, вызывающим билиарный панкреатит и патологии протоков поджелудочной железы, такие как протоковые камни или протоки протока.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 21; согласен = 3; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2к. Роль EUS при остром панкреатите у детей
Эндоскопическое ультразвуковое исследование (EUS) использовалось для определения этиология АП.EUS не только всесторонне оценивает паренхиму поджелудочной железы и протока, но также и гепато-билиарной анатомии. Заболевания желчевыводящих путей, такие как холедохолитиаз можно оценить с помощью EUS, особенно когда трансабдоминальное УЗИ не позволяет визуализировать дистальный общий желчный проток. EUS также может определить наличие микролитиаза у желчный пузырь, который часто не визуализируется при трансабдоминальном УЗИ или КТ сканировать. Микролитиаз может привести к ОП и лечится холецистэктомией (220). Хотя у детей это случается крайне редко, опухоли поджелудочной железы, которые могут быть вызваны новообразованием поджелудочной железы или AIP, могут проявляться с AP и пройти дальнейшее обследование с помощью EUS с возможностью взятия пробы ткани поджелудочной железы. (221, 222).
Терапевтическая роль EUS при AP в основном ограничена для лечения осложнения АП, а именно скопление жидкости поджелудочной железы или некроз стенок. EUS имеет было показано, что он полезен при лечении скоплений жидкости поджелудочной железы / некроза вторичный по отношению к тяжелому AP. Считается, что спонтанное рассасывание псевдокист происходит чаще. чаще у детей, чем у взрослых, особенно если размер <5 см (мнение эксперта). Таким образом, с большинством коллекций любого типа можно обращаться консервативно и терапевтически. вмешательство не требуется в остром состоянии, за исключением случаев наличия инфекции (223).Однако, если происходит созревание (обычно через 4–6 недель) саморегулирование менее вероятно, и пациент может нужен эндоскопический дренаж. Другие показания к вмешательству EUS и дренированию включают: большой размер при возникновении клинических симптомов, подозрении на заражение скоплений или стойких симптомы от псевдокисты. Дренаж под контролем EUS и создание цистгастростомы было продемонстрировано, что он столь же эффективен и безопасен, как хирургическая цистгастростомия, и имеет было показано, что он эффективен даже у детей (224).
Резюме: на основании литературы для взрослых, EUS может быть полезным для определения этиологии острого панкреатита, которая может включать диагностику дистального камни общего желчного протока, новообразования поджелудочной железы или аутоиммунный панкреатит. Его роль для терапия в основном ограничена лечением осложнений острого панкреатита, а именно скопления жидкости поджелудочной железы или некроз стенок, вторичный по отношению к тяжелому АД.
Рекомендация 2k: EUS не считается стандартом диагностический инструмент при остром панкреатите у детей в настоящее время.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2L Роль хирургии / хирургической консультации при остром панкреатите у детей
Хирургические вмешательства не являются частью алгоритма ведения больного. Типичный эпизод АП. Публикации относятся к взрослому опыту. Раннее указание на хирургия включает лечение синдрома брюшной полости.Однако управление некроз поджелудочной железы с ранней некрэктомией в течение первых 72 часов, как было показано, приводит к повышенная заболеваемость и смертность по сравнению с отсроченными сроками не менее чем на 12 дней (225). Руководящие принципы Международного Ассоциация панкреатологов с 2002 г. предлагает отложить операцию некрэктомии для по крайней мере, через 3-4 недели после начала заболевания снижает заболеваемость и смертность (210). Руководящие принципы ACG 2013 года по управлению взрослый AP прокомментировал возможность хирургического вмешательства в связи с желчнокаменной болезнью. панкреатит, санация некроза (инфицированные vs.стерильный), и малоинвазивный лечение некроза поджелудочной железы (33). Рекомендации включали раннюю холецистэктомию во время той же госпитализации по поводу легкий приступ желчнокаменного панкреатита и обсуждение между гастроэнтерологами и хирургия для выбора времени холецистэктомии по сравнению с другими терапевтическими вариантами в случаях тяжелый АД, особенно с некрозом. Для пациентов с сохраняющейся клинической нестабильностью и ухудшение состояния на фоне некроза поджелудочной железы, дренирование может потребоваться для улучшить статус пациентов и снизить заболеваемость и смертность.Руководящие принципы АЧГ предлагают что санацию некроза следует отложить, когда это возможно, в идеале более четырех недель с момента обращения, чтобы лучше организовать воспалительные реакции. Даже в необходимость некрэктомии, менее инвазивных методов, включая чрескожную радиологию, или следует рассмотреть возможность эндоскопического дренирования / хирургической обработки раны наряду с лапароскопическим хирургическим вмешательством. предпочтение отдается лечению перед открытым хирургическим вмешательством (33).
Исследование PONCHO 2015 г. с участием 266 стационарных пациентов, рандомизированных по интервалу холецистэктомия или холецистэктомия с тем же госпитализацией также поддерживали ту же госпитализацию. холецистэктомия снизила частоту повторных осложнений, связанных с желчнокаменной болезнью, у взрослых пациенты с желчнокаменным панкреатитом легкой степени с очень низким риском холецистэктомии осложнения (226).
В случае тяжелой травмы живота, требующей неотложной лапаротомии (в том числе дорожно-транспортных происшествий) следует искать повреждения поджелудочной железы, в том числе вовлекающий проток поджелудочной железы. Тяжесть травмы поджелудочной железы может быть оценена в соответствии с Американской ассоциации хирургии травм поджелудочной железы по шкале, в которой 5 могут быть присвоены степени травмы (227). Выше травмы поджелудочной железы в результате травмы, как правило, также включают ассоциированную дуоденальную травмы. Пациентам с более легкими тупыми травмами I и II степени можно лечить в нерабочем состоянии.В случае травмы поджелудочной железы мультидисциплинарный подход, включающий: показаны бригады врачей / гастроэнтерологов и хирургов.
В педиатрической литературе о показаниях к операции гораздо больше ограничено. Что касается билиарного панкреатита, ретроспективная серия случаев из 19 детей, госпитализированных с билиарным панкреатитом, зарегистрировано 9 детей, перенесших ранний холецистэктомия без побочных эффектов и 4 из 10 детей, перенесших отсроченную операцию возникновение нежелательных клинических явлений (включая рецидив панкреатита) (228).
Резюме: Показания к острому хирургическому вмешательству. к показаниям АП относятся травмы живота, при которых у пациента нестабильность и / или поиск происходит сопутствующее повреждение других органов. В контексте билиарного панкреатита было показано, что холецистэктомия не только безопасна, но и предотвращает рецидивы, если они происходят. в рамках индекса госпитализации. Литература для взрослых предполагает, что раннее вмешательство в некроз поджелудочной железы приводит к увеличению заболеваемости и смертности, и, следовательно, к санации раны желательно отсрочить некроз поджелудочной железы, вызывающий нестабильность у пациента, по крайней мере, на 4 часа. недель с момента обращения, в идеале — эндоскопическим или чрескожным способом.
Рекомендация 2li: холецистэктомия безопасно может и следует выполнять перед выпиской в случаях легкой неосложненной острой желчной болезни. панкреатит.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2lii: В ведении острых некротических скоплений, вмешательств следует избегать и откладывать, даже для инфицированных некроз, поскольку результаты лучше при отсроченном (> 4 недель) подходе.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 6; нейтральный = 2; не согласен = 1; категорически не согласен = 0.
Рекомендация 2liii: Когда требуется дренирование или некрэктомия. необходимые нехирургические доступы, включая эндоскопические (EUS и ERCP) или чрескожные методы предпочтительнее открытой некрэктомии или открытой псевдокисты дренаж.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 9; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
3. ИСХОДЫ ОСТРОГО ПАНКРЕАТИТА ПЕДИАТРИИ
Общие исходы ОП у детей благоприятны по сравнению со взрослыми. В средняя продолжительность госпитализации детей с ОП составляет в среднем от 2,8 до 8 дней, хотя младенцы / малыши, как правило, поступают на более длительный период времени (в среднем 19,5 дней) (15, 73, 229–231). Раннее начало энтерального питания и агрессивная жидкостная реанимация был связан с более коротким пребыванием в больнице, меньшим количеством госпитализаций в отделения интенсивной терапии и снижение показателей тяжелого АП по сравнению с пациентами, находящимися в НКО (73).Эти результаты в целом совпадают с выводами большинства взрослых. исследований (232), но, возможно, не применялись к педиатрические пациенты до недавнего времени. Более высокая смертность при ПД у детей связана с системное заболевание, но в целом низкий и составляет менее 5% в большинстве когорт, даже в том числе в реанимации (15, 30, 233, 234).
Осложнения с ранним началом при ОП включают полиорганную дисфункцию или шок (15). Острые скопления перипанкреатической жидкости наблюдаются в острая фаза панкреатита и имеет тенденцию к спонтанному разрешению.Частота образование псевдокист колеблется от 8% до 41% у детей с панкреатитом, и более высокие показатели наблюдаются у пациентов с панкреатитом, связанным с абдоминальной травма (15, 212, 235). Псевдокисты часто бессимптомный и может лечиться консервативно или стать больше и вызвать боль в животе, рвота или лихорадка. Они также могут заразиться в 10–15% случаев. (236). Еще одно осложнение с поздним началом связано с до некроза поджелудочной железы. Некроз может проявляться в первую очередь в виде острого некротического скопления. (ANC), а затем созревают до некроза без стенок (WON) (8).Варианты лечения при дренировании псевдокист и некротических стенок коллекции включают эндоскопический (транспапиллярный или трансмуральный) дренаж, чрескожный катетерный дренаж или открытая / лапароскопическая операция. Выбранная модальность зависит от размера, расположение, анатомия и риски / преимущества процедуры, хотя чрескожная и Трансгастроинтестинальный дренаж под контролем эндоскопического ультразвука (ЭУЗИ) в настоящее время становится все более популярным. широко распространено (237).
Примерно 15–35% детей с острым у панкреатита будет еще один приступ панкреатита.Острый рецидивирующий заболевание у детей панкреатит связан с панкреатико-билиарными аномалиями, аутоиммунным панкреатитом, нарушения обмена веществ и наследственный панкреатит (15).
Резюме: За детьми необходимо следить во время их курс АП при местных и системных осложнениях, которые могут включать дисфункцию органов, острые скопления жидкости и впоследствии некроз или псевдокисты. Общий педиатрические пациенты с острым панкреатитом имеют хороший прогноз с очень низким уровнем смертность, но сообщается о частоте рецидивов до 15–35%.
Рекомендация 3: Дети с острым панкреатитом должны получить тщательное наблюдение со стороны поставщика медицинских услуг для выявления раннего или позднего осложнения или рецидивы.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
A Clinical Отчет Комитета по поджелудочной железе NASPGHAN
1. ПЕРВОНАЧАЛЬНАЯ ОЦЕНКА И ДИАГНОСТИКА ОСТРОГО ПЕДИАТРИЧЕСКОГО ПАНКРЕАТИТА
Недавние исследования оценивают заболеваемость острым панкреатитом (ОП) при ~ 1/10 000 детей в год (2, 7), заболеваемость приближается к взрослым.Есть нет научно обоснованных руководств по диагностике ОП у детей. ВДОХНОВЕНИЕ ( IN международный S tudy Группа компаний P медицинский P анкреатит: I n Найдите Cu RE ) определение детской AP является экспертное определение смоделировано по критериям Атланты у взрослых (8). Согласно критериям INSPPIRE, для диагностики АП требуется как минимум 2 из следующего: (1) боль в животе совместима с AP, (2) значениями сывороточной амилазы и / или липазы ≥3 раза верхние пределы нормы, (3) визуализация результаты согласуются с AP (9, 10).INSPPIRE или другие критерии не касаются этапов (ранних или поздний) АП у детей или типов (интерстициальный отечный панкреатит, некротический панкреатит, инфицированный панкреонекроз) или степень тяжести ОП (легкая, умеренная или тяжелая форма ОП при мультисистемной органной недостаточности).
Детский диагноз ОП обычно подозревается клинически с совместимым симптомом презентации, подтвержденные лабораторными и / или радиологическими исследованиями. Боль в животе и / или раздражительность являются наиболее частыми проявлениями ОП у детей, за которыми следуют эпигастральные болезненность, тошнота и рвота (11, 12).У младенцев и детей ясельного возраста симптомы могут быть незаметными; поэтому диагноз требует высокого уровня подозрений. Желчные / обструктивные факторы, лекарственные препараты и системные заболевания являются основными причинами ОП у детей (1, 4, 9, 12–23), и знание этих возможных причин поможет руководить начальными исследованиями.
Процент детей, у которых развиваются «тяжелые» острые панкреатит варьирует в опубликованных сериях (6–34), но дети с ОП в в целом имеют легкое течение (11, 24, 25). В подмножестве у пациентов АП может иметь тяжелое течение (8), но нет установленные клинические инструменты предсказывают этот результат.Балльные системы оценки степени тяжести АП у взрослых (Рэнсон, Глазго, модифицированный Глазго, Прикроватный индекс тяжести острых заболеваний). Панкреатит (BISAP) и оценка острой физиологии и хронического здоровья II (APACHE II)) не легко применимы к детям по нескольким причинам (26). Детская шкала острого панкреатита (PAPS) ДеБанто (27) была оценена у детей, но имеет низкую чувствительность. и требует 48 часов для прогнозирования рисков. Точно так же степень тяжести компьютерной томографии индекс (CTSI) или балл Бальтазара (28), опирается на радиологический внешний вид и, следовательно, нежелателен в детской возрастной группе из-за радиации экспозиция.Благодаря своей широкой доступности липаза является привлекательным маркером для выявления тяжелых случаев AP (25), но может выявить много ложных положительных из-за его низкой положительной прогностической ценности и специфичности. Коффи и др., обнаружили, что липаза сыворотки в семь раз превышает верхний предел нормы в течение 24 часов после презентация помогла предсказать тяжесть острого панкреатита (25). Тем не менее, это ретроспективное исследование с участием 211 детей и не были проверены в более крупных исследовательских группах. Suzuki и др. В Японии разработали удобная для детей система оценки степени тяжести с использованием 9 параметров (29), но это также было ретроспективным исследованием, в котором оценивались только 145 пациентов, и авторы пришли к выводу, что результаты не могут быть широко применимы к педиатрическое население.Совсем недавно Сабо и др. Сообщили, что ранняя степень тяжести прогностическая модель с использованием сывороточного альбумина, липазы и количества лейкоцитов, полученных в 24 часа продемонстрировали положительную прогностическую ценность 35% и отрицательную прогностическую ценность значение 91% (30).
Необходимы дальнейшие проспективные исследования для определения клинической применимости любой из этих инструментов. В вышеупомянутых исследованиях использовались различные определения степени тяжести. AP, что ограничивает возможности проведения сравнений между исследованиями. Недавняя публикация Комитет по поджелудочной железе NASPGHAN обратился к необходимости иметь четко определенную классификацию степени тяжести АП, предлагая определения легкой, средней и тяжелой степени АП для повысить однородность исследований (31).
Биомаркеры сыворотки
Острый панкреатит — это в первую очередь клинический диагноз, основанный на наличие как минимум двух из трех критериев, опубликованных INSPPIRE и Atlanta классификация (8, 9). Без выполнения двух из этих трех критериев трудно сделать диагностика АП. Основные биохимические маркеры, используемые для диагностики АП, включают сывороточную липазу. и сывороточная амилаза. Поскольку уровень липазы или амилазы в сыворотке не менее чем в три раза превышает верхний предел нормы считается совместимым с панкреатитом, важно знать справочные значения лаборатории для определения этого порога.И амилаза, и липаза обычно повышается на ранней стадии заболевания. Однако соотношение сыворотки уровни липазы или амилазы и тяжесть заболевания низкая (25, 32, 33). Липаза в основном секретируется поджелудочной железой, хотя другие источники липазы включают желудочные и язычные липазы. При АП липаза обычно увеличился в течение 6 часов после появления симптомов; уровень в сыворотке достигает максимума через 24–30 часов и может остаются повышенными более одной недели (34). Некоторые выступают за то, чтобы сывороточная липаза без сывороточной амилазы была достаточной для диагностики АП, поскольку липаза является более чувствительным и специфическим маркером АП (87–100% и 95–100% соответственно) (35–38).Липаза, кроме того, остается повышенным дольше, чем амилаза, что полезно в случаях отсроченного проявления (34, 39, 40). Уровни липазы также меньше изменяются этиология AP в отличие от амилазы, особенно в случае этанола (37, 41) или гиперлипидемия (42, 43). Но следует соблюдать осторожность при интерпретации уровней у детей. упражнения, поскольку было продемонстрировано, что нормальные значения липазы связаны с возрастом ребенок, растущий от новорожденного к ребенку, к взрослому (44, 45). Амилаза секретируется несколькими органами, прежде всего слюнные железы и поджелудочная железа.Большинство лабораторий измеряют общую амилазу уровни, которые содержат изоформы s-амилазы (слюна) и p-амилазы (поджелудочная железа) (46). Существуют лабораторные тесты для фракционирования p- и s-амилаза, но эта практика менее доступна. Эталонные значения амилазы отличаются в зависимости от используемого лабораторного теста, но также зависят от возраста и пола (47, 48). Сыворотка Уровни амилазы могут изменяться в зависимости от этиологии панкреатита, как указано выше. Амилаза уровни повышаются быстрее, чем уровни липазы, и часто могут нормализоваться через 24 часа после начала симптомы, ограничивающие полезность у пациентов с отсроченным обращением к врачу объект (34).Поскольку почки выводят амилазу и липазы, повышение этих ферментов не на уровне поджелудочной железы может наблюдаться у пациентов с повреждение или заболевание почек (46).
Несколько состояний, не связанных с панкреатитом, вызывают повышение уровня поджелудочной железы амилаза и / или липаза, включая декомпенсированную печеночную недостаточность, почечную недостаточность, кишечную воспаление (включая целиакию и воспалительное заболевание кишечника) брюшной полости травмы, диабетический кетоацидоз и травмы головы (49). Кроме того, некоторые люди продуцируют большие комплексы амилазы или липаза с иммуноглобулинами (так называемая макроамилаза и макролипаза), которые плохо фильтруется и выводится из-за большого размера, что приведет к повышенным значениям, если уровень фермента измеряется в крови, несмотря на то, что он не связан с воспалением поджелудочная железа (50).
Другие биомаркеры для диагностики и лечения панкреатита были предложены и изучены на животных моделях или небольших клинических испытаниях (см. обзоры в (46, 51, 52)). Однако ни один из них не получил известности, и многие еще предстоит пройти валидацию для общеклинического использования.
Несколько лабораторных тестов помогают контролировать течение АП (53). В целом электролиты сыворотки крови, мочевина крови азот (BUN) и креатинин, а также общий анализ крови (CBC) важны для мониторинга состояние жидкости / гидратации и почечная функция.Панель печеночных ферментов показана для поиска желчнокаменной или желчнокаменной этиологии, а также для оценки поражения органов. Кальций и Уровни триглицеридов следует рассматривать как исходные исследования (9). Мониторинг респираторного статуса может предупредить врача о том, что прогрессирование от легкой до среднетяжелой или тяжелой АД.
Этиология
Как упоминалось ранее, анатомическая, обструктивная (в том числе желчная), инфекционные, травматические, токсические, метаболические, системные заболевания, врожденные нарушения обмена веществ, генетическая предрасположенность и идиопатия были описаны как потенциальные этиологии при детском ОП, остром рецидивирующем панкреатите (АРП) и хроническом панкреатите (ХП) (3, 4, 54).Обзор Lowe et al суммировал 6 лучших общие этиологические категории в опубликованных обзорах как идиопатические / другие в 24%, травмы у 17%, системные заболевания у 15%, структурные аномалии в 14%, лекарства в 10% и инфекции в 8%. (3) Учитывая более частую этиологию, а также те, которые для которых существует направленная терапия, в рукописи 2012 года Morinville et al. опрос детских гастроэнтерологов, оказывающих панкреатологическую помощь, и предложили после обследования в первых случаях панкреатита: сывороточные ферменты печени, триглицериды и уровень кальция и УЗИ брюшной полости.Они предложили отложить тестирование на генетические причины / предрасположенности (которые в то время включали CFTR (муковисцидоз) регулятор трансмембранной проводимости), SPINK1 (ингибитор сериновой протеазы Kazal типа 1) и PRSS1 (катионный трипсиноген)), хлорид пота и более подробные изображения для случаев ARP, CP или первых экземпляров AP с повышенным риском рецидив, основанный на представлении, прошлой истории болезни или семейном анамнезе (9). При необходимости, поиск может быть проведен для конкретных факторы токсико-метаболического риска (55).Недавний публикация Gariepy et al, посвященная причинно-следственной оценке ARP и CP у детей, который имеет тенденцию быть более обширным из-за повторяющегося / хронического характера презентации (56) Аутоиммунный панкреатит (АИП) типов 1 и 2 редко диагностируются, но представляют разные типы панкреатита со специфическими гистологические данные в контексте суггестивных симптомов, визуализации, лабораторных исследований. результаты и ответ на терапию. Если AIP подозревается как этиология AP, в дальнейшем необходима поддерживающая оценка.Заинтересованные читатели будут перенаправлены на недавний публикация Scheers et al по педиатрической AIP (57).
Визуализация
Визуализация на ранней стадии ОП обычно не требуется, если в анамнезе / при предъявлении симптомы и биохимические маркеры сыворотки присутствуют для постановки диагноза. Визуализация становится актуально для документирования некроза поджелудочной железы, осложнений панкреатита, включая жидкость скопления и этиология панкреатита, например, камни в желчном пузыре / желчевыводящие пути или анатомические аномалии.
Золотым стандартом диагностической визуализации остается КЭКТ и несколько оценок. системы разработаны (58).Тем не мение, несмотря на то, что CETC является золотым стандартом визуализации, он часто не указывается и необходим для диагностики или лечения педиатрического AP. В неоднозначных случаях для диагностики ОП, например, при отсроченном проявлении, когда сывороточные маркеры могут быть низкими, компьютерная томография с контрастным усилением (CECT) может потребоваться для подтверждения AP. IV контраст является ключом к различению некротических участков поджелудочной железы (59). Поскольку ранняя визуализация может недооценивать степень заболевания и поскольку осложнения развиваются со временем, и результаты могут отсутствовать на ранних этапах фазе заболевания, в идеале CETC следует отложить как минимум на 96 часов после начала симптомы (8, 60).В легких случаях КЭКТ может показать усиление гомогенного органа, воспалительное изменения перипанкреатического жира или жидкости, окружающей поджелудочную железу (59) В тяжелых случаях КЭКТ может показать неоднородный орган усиление, некроз в поджелудочной железе или в окружающей перипанкреатической ткани. Кроме того, CECT может также идентифицировать скопления перипанкреатической жидкости или псевдокисты. КЭКТ следует пересмотреть при ухудшении клинического состояния пациента. или постоянно тяжелый (8). Lautz et al. нашел что индекс тяжести компьютерной томографии (шкала CTSI или Balthazar) в педиатрической пациенты дали чувствительность, специфичность, положительную прогностическую ценность и отрицательную прогностическая ценность 81%, 76%, 62% и 90%, соответственно, по степени тяжести в ретроспективном исследовании 64 детей (61).
Ультразвук широко используется в случаях, когда есть высокие подозрения на билиарный панкреатит, при котором полезно заранее определить необходимость терапевтического вмешательство (33, 58). Ультразвук имеет отличный профиль безопасности, неинвазивен и не использовать радиацию. Тем не менее, использование ультразвука может быть ограничено в оценке состояния. поджелудочной железы из-за мешающих структур, таких как кишечные газы в кишечнике и ожирение и имеет более низкую чувствительность при визуализации поджелудочной железы по сравнению с КЭКТ.
Магнитно-резонансная томография (МРТ) обычно не используется в качестве первичной визуализации техника при АП, но может быть полезна при поздних осложнениях (59). Это может быть особенно полезно для молодых или беременных. пациентам (с намерением ограничить облучение), и может разрешить использование альтернативных методов внутривенного контраста в пациенты с нарушением функции почек или аллергией на йодсодержащий контраст (60). МРТ также может быть более чувствительным при оценке некротическая ткань по сравнению с КЭКТ (59, 61). МР-холангиопанкреатография (MRCP) при AP наиболее часто используется для обнаружения камней в дистальных отделах общего желчного протока и диагностики желчных путей АП.МРТ / MRCP с использованием секретина помогает исследовать систему протоков в поджелудочной железы, а также общие аномалии желчных протоков, включая стриктуры или камни (62, 63). К оптимизировать обнаружение патологий протоков, MRCP может выполняться после атаки AP исчез, поскольку острый отек может затруднять визуализацию протоков. Использование MRCP, усиленный секретином, при заболевании поджелудочной железы у детей полностью не установлен (64) и доступ к секретину неодинаков через учреждения и страны.Lin et al подробно описывают использование МРТ и MRCP у детей. требуется визуализация поджелудочной железы, а также общие аспекты визуализации при AP (65).
Резюме и рекомендации
Рекомендация 1a: Диагностика острых заболеваний у детей панкреатит должен соответствовать ранее опубликованным критериям INSPPIRE.
Для диагностики ОП у педиатрических пациентов необходимы как минимум 2 из следующего: (1) боль в животе, совместимая с AP, (2) уровни амилазы и / или липазы в сыворотке ≥3 раза верхние пределы нормы, (3) результаты визуализации в соответствии с AP.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1b: Возможно выполнение первичной визуализации. с помощью трансабдоминального ультразвукового исследования, с другими методами визуализации (КТ, МРТ), зарезервированными для большего сложные случаи +/– с учетом подозреваемой этиологии.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 4; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 1c: Основана на наиболее частой этиологии и те, для которых существуют варианты лечения, первый приступ острого панкреатита тестирование должно включать ферменты печени (АЛТ, АСТ, ГГТ, ЩФ, билирубин), триглицериды уровень и уровень кальция.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2. СООБРАЖЕНИЯ ВЕДЕНИЯ ПРИ ОСТРЫХ ПЕДИАТРИЧЕСКИХ ПАНКРЕАТИТАХ
2a.Инфузионная терапия при остром панкреатите
Внутривенная инфузионная терапия является основой лечения во время эпизода AP. Жидкая реанимация поддерживает адекватный жидкостный статус и диурез, но в последнее время внимание было сосредоточено на использовании внутривенных жидкостей для предотвращения потенциальных осложнений при ОП, такие как некроз и органная недостаточность. Патогенез ОП и прогрессирование до тяжелой степени. считается вторичным по отношению к нарушению микроциркуляции поджелудочной железы событиями, включая гиповолемию, повышенную проницаемость капилляров и образование микротромбы.Считается, что жидкостная реанимация не только устраняет гиповолемию, но и помогает сохранить микроциркуляцию поджелудочной железы, обеспечивая адекватную перфузию и предотвращая возможное образование микротромбов и, таким образом, предотвращение осложнений и прогрессирования тяжелое заболевание (66).
Тип жидкости
Отсутствует консенсус относительно идеального количества и типа жидкости для использования во время эпизода ОП во взрослой практике, и существует еще меньше данных, относящихся к жидкости в педиатрической популяции. Кристаллоид был наиболее рекомендуемым типом жидкость в руководствах для взрослых (33, 67–70).А Основное преимущество кристаллоидов в том, что они легко и быстро доступны. Обычный физиологический раствор (NS) долгое время был предпочтительным кристаллоидом для начальной жидкостной реанимации в в целом, но в некоторой литературе для взрослых предполагается, что лактатные звонаги (LR) являются более оптимальными для AP. В небольшом рандомизированном контрольном исследовании (РКИ) с участием 40 взрослых с AP Wu et al. что LR снижает частоту синдрома системного воспалительного ответа (SIRS) и уровни С-реактивного белка через 24 часа по сравнению с NS (71). Напротив, ретроспективный обзор 103 пациентов не смогли показать какой-либо существенной разницы между LR и NS в качестве начального реанимационная жидкость у взрослых с панкреатитом различной степени тяжести (72).LR был рекомендован по сравнению с NS в Международном Рекомендации Ассоциации панкреатологов / Американской панкреатической ассоциации (IAP / APA), но в рекомендациях Американской гастроэнтерологической ассоциации (AGA) только говорится, что LR может быть лучший выбор, но не был сильной рекомендацией (68, 70). В педиатрии это было показали, что агрессивное введение жидкости в течение первых 24 часов с помощью физиологического раствора с 5% декстрозой является безопасным и хорошо переносимым вариантом (73), но его не сравнивали с другими типами жидкостей для внутривенного вливания. (например, LR).
Коллоиды (например, альбумин, свежезамороженная плазма или упакованные эритроциты) не рекомендованы в качестве начальной реанимационной жидкости при АП. Коллоидные компоненты оставаться во внутрисосудистом пространстве из-за большего размера и может втягивать жидкость в кровообращение из интерстиция вторично по отношению к осмотическому эффекту. Руководящие принципы AGA рекомендует коллоид в определенных ситуациях, когда гематокрит < 25% альбумина составляет <2 г / дл (68), при этом другая публикация рекомендует соотношение кристаллоидов и кристаллоидов 3: 1. коллоид (74).
Скорость введения жидкости
Агрессивность жидкостной реанимации при АП также обсуждалась. В время вмешательства агрессивной жидкостной терапии может быть ключевым. Учеба взрослых в пользу ранних и агрессивных жидкостей в AP включают несколько ретроспективных исследований, которые использовали разные стратегии, такие как предоставление> против <33% от общего количества жидкости в течение первых 24 часов, а другой обеспечивает 3,5 л по сравнению с 2,4 л внутривенно в течение первых 24 часов (75). В основном, те, кто получает более агрессивные объемы жидкости внутривенно в течение первых 24 часов, как правило, улучшили результаты, включая смертность, но даже в рамках различных исследований результаты противоречивы в отношении того, снижает ли более высокое раннее введение жидкости некроз, синдром системного воспалительного ответа (SIRS) и продолжительность пребывания в стационаре (76).Напротив, Mao et al. Сообщили о РКИ 76 пациентам с тяжелым АП назначена медленная гемодилюция (5–10 мл / кг / ч) или быстрая гемодилюция (10–15 мл / кг / ч), демонстрирующая, что быстрая агрессивная ранняя жидкость введение привело к более высоким показателям сепсиса и смертности (77). de-Madaria et al провели проспективное исследование 247 человек. пациенты делятся на пациентов в зависимости от количества жидкости, введенной в первые 24 периода. часы. Группа, получавшая наибольший объем,> 4,1 л, имела повышенный уровень стойкая органная недостаточность (78).Weitz и др., рассмотрели 391 случай АП и обнаружили, что использование агрессивных жидкостей (примерно 5 л) было неэффективным. связаны с обострением заболевания и местными осложнениями (79). Опасения по поводу этой последней группы исследований заключаются в том, что в основном они касались более больных пациентов, и жидкостные режимы не ограничивались первые 24 часа реанимации.
Несколько экспертов и групп с тех пор дали рекомендации по скорости жидкостная реанимация в первые 24–48 часов у взрослых с ОП.МАП / АПА руководящие принципы рекомендуют пациентам получать 5–10 мл / кг / час до реанимации. цели достигаются в отношении улучшения частоты сердечных сокращений, диуреза, среднего артериальное давление и / или гематокрит (70). В Американский колледж гастроэнтерологии (ACG) рекомендует начальную скорость 250–500 мл / час, в дополнение к болюсу жидкости, если гипотензия или тахикардия присутствуют и используют BUN для направления терапии (33). Подобные рекомендации сделаны в обзоре Whitcomb et al (80). Aggarwal et al. советует 3–4 л жидкости в первые 24 часа (не более 4 л) с начальным болюсом 1 л и последующие 3 мл / кг / час в течение первых 24–48 часов (81).Наср и др. первоначально рекомендуют болюсы 1–2 л и 150–300 мл / час (82). Впоследствии они рекомендуют 2 мл / кг / час, если пациент отвечает на первоначальную реанимацию, но в противном случае использовать 3 мл / кг / час (82).
Только в одном педиатрическом исследовании оценивались разные нормы поддерживающей жидкости. администрации с участием 201 пациента с ОП [69]. Это исследование показало, что сочетание ранних энтеральное питание (<48 часов) и агрессивные жидкости (> 1,5–2x техническое обслуживание в первые 24 часа) уменьшилась продолжительность пребывания и возникновение тяжелое заболевание по сравнению с более традиционным историческим лечением.Агрессивные внутривенные жидкости не повлияли отрицательно на исходы (в первую очередь, легочные осложнения или повторная госпитализация). ставки). Никакие исследования не указывают идеальную норму поддерживающих жидкостей в AP после начальная реанимация (> 24–48 часов), хотя Сабо и др. что 1,5–2-кратное поддержание было безопасным для их популяции пациентов (73). Нет педиатрических исследований, сравнивающих первоначальную реанимацию тома.
Резюме: В начальной фазе реанимации острого панкреатит, теоретические и потенциальные клинические преимущества в пользу LR выше NS на основе данные о взрослых, но отсутствуют педиатрические данные.
Рекомендация 2ai: Дети с острым панкреатит необходимо первоначально реанимировать кристаллоидами, либо с LR, либо с NS в острой постановке. На основании оценки статуса гидратации / гемодинамического статуса, если при наличии гемодинамических нарушений рекомендуется болюсное введение 10–20 мл / кг.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 22; согласен = 2; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Резюме: Педиатрическая литература жидкостная реанимация и скорость введения жидкости при остром панкреатите.Взрослый литература предлагает болюсы 250–1000 мл на начальном этапе и до 3–4 л. жидкости в течение первых 24 часов.
Рекомендация 2aii: Дети с диагнозом острой панкреатит следует назначать 1,5–2-кратное поддерживающее внутривенное введение жидкостей с мониторингом диуреза в течение следующих 24–48 часов.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 12; согласен = 10; нейтральный = 2; не согласен = 0; категорически не согласен = 0.
2b. Мониторинг детей с диагнозом ОП / внепанкреатические проявления острый панкреатит
Хотя это еще не изучено у педиатрических пациентов, полиорганная болезнь у взрослых пациенты с ОП связаны с худшими клиническими исходами с более чем половиной случаев, связанных с ОП. смерть в течение 1 недели от начала полиорганной дисфункции (83).Поражение сердца, легких и почек является ключевым фактором. компоненты систем оценки взрослых, используемых для прогнозирования тяжести эпизода ОП, включая модифицированная атлантская классификация, критерии Рэнсона, степень серьезности по Японии Оценка, оценка по Глазго, BISAP и APACHE II (8, 84–87). Педиатрические модели, прогнозирующие тяжесть ОП, также придают большое значение вовлечению нескольких органов, но оказались менее надежными (88) или еще не прошли проспективную валидацию (29). Повышенный эндотелиальный барьер проницаемость и глубокий выброс цитокинов, связанные с ССВО в сочетании с агрессивным гидратация теоретически увеличивает риск пациента для жидкости третьего промежутка и развитие внепанкреатических проявлений АП.Надлежащий мониторинг жизненно важен для сбалансировать соответствующую жидкостную реанимацию, пытаясь предотвратить сердечную, легочную и почечные осложнения (89).
Сердечно-сосудистый мониторинг
Гиповолемия при поступлении является надежным предиктором заболеваемости и смертности среди взрослых с AP и, по-видимому, коррелирует с величиной SIRS (89). Тахикардия использовалась как при системы оценки взрослых и детей для прогнозирования тяжести ОП и ее улучшение использовались для подтверждения адекватной реанимации жидкости в дополнение к мониторингу мочи объем и тургор кожи (71, 81).Регулярный кардиологический мониторинг взрослых у пациентов, не получающих ОИТ включает регулярные измерения жизненно важных функций каждые 8 часов для получения информации о состоянии сердечно-сосудистой системы (71). Дополнительно редкие случаи тампонады сердца и предсердий. Сообщалось о фибрилляции при АП, и ее следует учитывать при стандартном кардиологическом исследовании. обследование начато у пациентов с необъяснимой гипотонией, одышкой и / или боль в груди (90–93).
Мониторинг легких
Исследования на взрослых и животных модели показывают острый респираторный дистресс синдром (ОРДС), пневмония и отек / выпот легких как ранние осложнения ОП, обычно в течение первых 48 часов (15, 94).Поскольку ОРДС является наиболее распространенным критическим осложнение тяжелого АП, связанного с полиорганной дисфункцией у взрослых (95), аномальное P a O 2 или аномальные изображения легких являются компонентами всех обычно используемых систем оценки для предсказать тяжесть приступа ОП (8, 29, 84–87). Регулярный мониторинг насыщение кислородом во время агрессивной гидратации обычно осуществляется, с некоторыми койки пациентов должны быть подняты на угол 30 градусов, чтобы снизить вероятность легочная секвестрация (71).Стандарт следует рассмотреть возможность обследования легких и ухода за пациентами с необъяснимыми одышка, ухудшение кашля и / или затрудненное дыхание (94).
Мониторинг почек
Острое повреждение почек (ОПП) через синдром брюшной полости (83, 96) или вызванное воспалением повреждение проксимального извитого канальца (97), отмеченное повышением уровня азота мочевины и креатинина, а также снижение диуреза, это известное раннее осложнение АП у детей и факторы занимает важное место в оценочных системах AP для прогнозирования тяжести заболевания (8, 15, 29, 84–87).В некоторых исследованиях на взрослых было показано, что только мочевины быть столь же эффективным в прогнозировании тяжести заболевания, как и более продвинутые системы оценки (98) и AKI был связан с В 10 раз повышен риск смерти при тяжелом ОП (99). Таким образом, BUN и креатинин считаются важными маркерами для следить за проведением инфузии и контролировать ОПП у взрослых во время первого 48 часов и при агрессивном увлажнении (71, 81, 98). Хотя нет никаких руководств, документирующих частоту мониторинга этих параметров, 8–12 часов использовались в одном исследовании для определения реакции на управление жидкостями (71).Рекомендации ACG подчеркивают важность снижения АМК и поддержания нормального уровня креатинина в первые 24 часа, поэтому очень важен ранний мониторинг (33). В редких случаях требуется непрерывная вено-венозная гемофильтрация (CVVH). для предотвращения дальнейшего повреждения почек, предотвращения синдрома брюшной полости и / или removae воспалительных цитокинов, но его использование не изучалось у педиатрических пациентов с AP (100). Может понадобиться установить мочевой катетер для точного документирования диуреза, особенно при седативном ребенок в условиях отделения интенсивной терапии.
Резюме и рекомендации
Наблюдение за пациентами с острым панкреатитом может дать индикаторы возникающие осложнения, включая ССВО и органную дисфункцию / недостаточность. Сердечный, следует особенно внимательно следить за респираторным и почечным статусом в течение первого Через 48 часов после обращения, так как большинство осложнений начинается в течение этого периода. период времени. Диурез — важный маркер адекватной жидкостной реанимации, при этом литература для взрослых, предлагающая стремиться к достижению> 0.5–1 куб. См / кг / час (Руководство IAP / APA).
Рекомендация 2bii: Пациентам, поступившим в в стационарном отделении необходимо измерять жизненно важные показатели не реже, чем каждые 4 часа в течение первых 48 дней. часы приема и в периоды агрессивной гидратации для контроля кислорода сатурация, артериальное давление и частота дыхания. Частота регулируется в зависимости от клинический статус. Нарушения жизненно важных функций должны требовать обследования у специалиста.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2biii: АМК, креатинин и моча производительность следует регулярно контролировать в течение первых 48 часов как маркер соответствующее ведение жидкости и скрининг на острое повреждение почек. Аномалии должен вызвать нефрологическое обследование.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 4; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
2с. Обезболивание при остром панкреатите
Боль в животе является наиболее частым симптомом ОП.В педиатрической АП исследования, от 80% до 95% пациентов жаловались на боль в животе. Пациенты присутствует с болью в эпигастрии у 62-89% и диффузно у 12% до 20%. «Классическое» проявление иррадиации боли в эпигастрии. к спине встречается только у 1,6–5,6% педиатрических пациентов (15, 16).
Патофизиология ОП характеризуется потерей внутриклеточных и внеклеточная компартментализация, которая может быть результатом различных механизмов: обструкция секреторного транспорта поджелудочной железы; активация ферментов; или неспособность остановить каскад активации.АП встречается у генетически предрасположенных лиц, у которых воспалительная реакция вызывает панкреатит. Это, в свою очередь, стимулирует внутреннюю панкреатические и соматические болевые рецепторы брюшины (101). Другие постулируемые механизмы, вызывающие боль в переднем отделе позвоночника, включают высокое давление. внутри железы или протока поджелудочной железы с последующей ишемией железы. Боль в AP тоже бывает вероятно, связано с высвобождением тахикинина, вещества P и кальцитонина, связанного с геном. пептид. Факторы, которые стимулируют первичные сенсорные нейроны, включают ионы водорода, тепло, лейкотриены, метаболиты арахидоновой кислоты, брадикинины и протеазы, такие как трипсин, выпущен во время AP (102).
Обезболивание — важная терапевтическая цель при лечении ОП и обычно включает использование анальгетиков периферического и центрального действия. Нет данных опубликованы по оптимальному обезболиванию в педиатрической AP, а исследования у взрослых не определили одно лучшее лекарство (67).
Опиоидные анальгетики
Потому что классические анальгетики периферического действия (такие как ацетаминофен) часто недостаточны при тяжелом панкреатите, часто требуются опиаты для контроля боль.Морфин или родственные ему опиоиды употребляли 94% респондентов для вести детей с ОП в соответствии с анкетой для врачей INSPPIRE 2012 года (103). Сообщалось, что морфин вызывает дисфункция сфинктера Одди после системного введения (104). Однако нет четких доказательств, подтверждающих эту теорию, и морфин можно безопасно применять у пациентов с ОП (105). Меперидин применялся у взрослых с АП, но его недостатки включают: короткий период полураспада и потенциал нейротоксичности за счет накопления токсичных веществ. нейрометаболиты, которые могут приводить к судорогам, миоклонусу и тремору (106).Обзор наркотиков и функции сфинктера Одди. Thomson et al, документально подтверждают, что на сегодняшний день нет исследований, напрямую сравнивающих эффекты меперидин и морфин на сфинктере манометрии Одди и никаких сравнительных исследований существуют у пациентов с АП. Кроме того, не существует исследований или доказательств, указывающих на то, что морфин противопоказан к применению при ОП (107). Кокрановский обзор 2013 года включает 5 исследований, в общей сложности 227 Субъекты для оценки эффективности и безопасности нескольких опиоидов. Включенные лекарства были бупренорфин, петидин, пентазоцин, фентанил и морфин.Общий вывод состоит в том, что опиоиды могут быть подходящим выбором при лечении боли. связанных с AP, и они могут уменьшить потребность в дополнительной анальгезии. Кроме того, риск осложнений, связанных с панкреатитом, или клинически серьезных побочные эффекты не отличаются от опиоидов и других анальгетиков (108).
Опиоидсберегающие анальгетики
Предполагается, что НПВП являются потенциальными участниками развитие AP, но также показали преимущества при лечении боли в AP.Профилактическое Было показано, что НПВП, включая индометацин и диклофенак, полезны при нескольких исследования по профилактике панкреатита после ЭРХПГ (109, 110). Что касается боли После постановки диагноза АР индометацин превосходит плацебо и не показали повышенного риска желудочно-кишечного кровотечения в небольшом исследовании (111). По сравнению с морфином метамизол показал улучшение снятие боли через 24 часа, но разница не достигла статистической значимости (105).
Системное введение местных анестетиков, в основном новокаина, было выступает в качестве основного обезболивающего при АП.Предлагается внутривенное введение новокаина для уменьшения боли. и / или необходимость вспомогательных обезболивающих и, возможно, улучшения клиническое течение АП. В одном контролируемом исследовании системное введение новокаина в улучшение панкреатита и ускоренное послеоперационное восстановление после обширного абдоминального хирургическое вмешательство, включая уменьшение боли, улучшение когнитивных функций и сокращение длительность кишечной непроходимости, а также общая госпитализация (112). Но доказательства ограничены, а плацебо-контролируемые исследования отсутствуют. данные.
Эпидуральная анестезия (ЭА) широко используется для индукции обезболивания в в периоперационный период, а также для уменьшения боли у пациентов с ОП. В принцип действия был приписан блокаде симпатического нерва, который перераспределяет внутренний кровоток к неперфузируемым областям поджелудочной железы. В исследовании с участием 35 пациентов с прогнозируемым тяжелым ОП, ЭА значительно уменьшала болевые ощущения, улучшала перфузия поджелудочной железы на основе радиологических исследований перфузии и улучшения клинических исходы (снижение потребности в некрэктомии) (113).Проспективное исследование 121 пациента продемонстрировало хорошую эффективность. и безопасность EA у взрослых AP (114).
Резюме: Нет данных, обеспечивающих оптимальную боль управление в педиатрической АП. Исследования на взрослых не выявили ни одного превосходящего медикамент. Нет доказательств, подтверждающих утверждение, что морфин вызывает неблагоприятные события на сфинктере Одди.
Рекомендации 2ci: Внутривенный морфин или другой препарат опиоид следует использовать при острой боли при панкреатите, не реагирующей на ацетаминофен или НПВП.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Рекомендация 2cii: Услуги специалиста по острой боли в идеале следует проконсультироваться в случаях более сильной боли, чтобы уменьшить боль управление.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2d. Энтеральное и парентеральное питание при остром панкреатите у детей
Пероральное и энтеральное питание
Традиционно пациенты с ОП лечились, не вводя перорально (115) и давая парентеральное питание (PN) (116).Было высказано предположение, что отдыхая кишечник, поджелудочной железе дали «отдохнуть» и, таким образом, зажить быстрее. В Обоснованием этой теории было то, что наличие пищи в кишечнике стимулируют высвобождение холецистокинина (ХЦК), что, в свою очередь, стимулирует поджелудочную железу. секреция ферментов, что может привести к дальнейшей активации протеолитических ферментов и преувеличивают процесс самопереваривания и усугубляют травму (117, 118)
У взрослых проводится ряд контролируемых исследований, обзоров и метаанализов. лечебному питанию как при тяжелом, так и при легком ОП, включая обзор голландских Группа по изучению панкреатита и согласованные рекомендации, опубликованные Международный комитет по руководящим принципам консенсуса (119).Lodewijkx et al., Считают, что энтеральное питание превосходит парентеральное питание, а стратегия кормления по требованию в прогнозируемой тяжелый АП (120). Мирталло и др. Рассмотрели 8 социальные отчеты с целью разработки международных согласованных руководящих принципов по питанию терапия в АП (119). Они пришли к выводу, что в АП у взрослых, энтеральное питание (ЭП) было предпочтительнее, чем ПП, и его следует использовать в первую очередь даже при наличие свищей, асцита и псевдокист.
Рекомендуется начинать EN как можно раньше, тем более, что одна из целей энтеропатии — предотвратить бактериальную транслокацию и тем самым предотвратить развитие ССВО.Ранняя нутритивная терапия также предназначена для снизить цитокиновый ответ и частоту пареза желудка и кишечной непроходимости. В то время как некоторые исследования (121) не показывают разницы в исходы, когда ЭП была начата до или после 72 часов презентации, 2008 г. метаанализ, изучавший одиннадцать РКИ, показал, что ЭП началась в течение 48 часов после презентация значительно снизила показатели смертности, инфекций и полиорганной отказ по сравнению с PN (122). Эти эффекты были уменьшены, когда ЭП была начата через 48 часов.В обзоре питания за 2011 г. поддержка взрослых AP, был сделан вывод, что ранняя нутритивная поддержка, особенно ЭП, но также и ПП, уменьшали количество осложнений и улучшали выживаемость (123). В этом обзоре говорилось, что для его эффективности нутритивная поддержка должна была начаться в течение 72 часов. Было заявлено, что EN следует считается « активным терапевтическим вмешательством, улучшающим исход больных панкреатитом »(124).
Клинические исследования, сравнивающие результаты PN и EN у пациентов с AP сообщить, что использование EN при тяжелом остром панкреатите (SAP) или прогнозируемые результаты SAP значительно снижает частоту осложнений (125–133).Недавний метаанализ продемонстрировал превосходство ЭП по сравнению с ПП с меньшей частотой инфекции и полиорганной недостаточности, что приводит к снижению показателей смертности и сокращению пребывание в больнице (134). Однако, поскольку полный EN не всегда возможно во время AP из-за усиления боли или непереносимости кормления, некоторые отстаивают роль комбинации EN и PN. В одном исследовании рандомизировали 100 пациентов для получения только ПП по сравнению с ПП в комбинации только с ЭП или ЭП, сепсис, внутрибрюшная инфекция и продолжительность госпитализации снизились, когда ЭП была входит в состав руководства (135).
Описанные пути ЭП включали желудочный и тощей кишки. Два маленьких исследования не обнаружили разницы в результатах между назогастральным (НГ) и назоеюнальным (НД) сытые группы (136, 137). Мета-анализ 10 РКИ не показал различий в исходы между группами, получавшими (полу) элементарные и полимерные формулы. (138)
Никаких руководств по нутриционной поддержке дети с АП. Недавнее исследование Abu-El-Haija et al. продемонстрировал выполнимость установления энтерального питания в педиатрической АП, не усложняя курс или влияя на оценку боли AP (139).Из того же центра ретроспективное исследование показало, что сочетание раннего энтерального кормления плюс более чем 1,5-кратное поддерживающее внутривенное введение жидкости были связаны с более коротким продолжительность пребывания и более легкое заболевание по сравнению с теми, кто оставался НКО в течение 48 часов и имели более низкую частоту ЭКО, чем поддерживающую терапию (73). Сообщается о двух детях с тяжелым ОП, которые успешно вылечились. с назоеюнальным кормлением в отделении интенсивной терапии интенсивной терапии и переключением на пероральное кормление при выписке в общая палата (140).
Парентеральное питание
Родительское питание обеспечивает организм необходимыми калориями и питательными веществами. компенсировать катаболическое состояние.Обеспокоенность, что ПП может стимулировать поджелудочную железу. и приводить к преувеличению процесса самопищеварения не было подтверждено литература (141, 142). Данные показывают, что настой протеина не стимулируют секрецию поджелудочной железы (143). Когда при сравнении различных форм ПП, сообщалось, что ПП, усиленный глутамином, снизить общую частоту осложнений, а также сократить продолжительность пребывания в стационаре (144–148). Введение глюкозы внутривенно также не стимулирует секреция поджелудочной железы (149, 150).Инфузия глюкозы тяжелобольным пациентам может быть полезно для обеспечения легкодоступного источника энергии во время катаболического состояния и противодействуют глюконеогенезу из-за распада белка. Но настой глюкозы обязательно под наблюдением, так как это может предрасполагать к гипергликемии (151), поскольку воспаленная поджелудочная железа может не подавать соответствующий инсулин отклик.
Гипертриглицеридемия связана с тяжелым ОП (152–155), но механизм, ведущий к SAP, не ясен (156). Недостаточно данных, чтобы рекомендовать или препятствовать использованию парентеральные липиды при АП.
Что касается времени PN в AP, где измеренный результат был смертности, данные свидетельствуют о том, что раннее ПП значительно более полезно, чем покой кишечника. при тяжелом ОП у взрослых (122). Во всех случаях, когда ЭП невозможна в течение длительного времени, например, при кишечной непроходимости, сложных свищах и т. Д. синдром брюшного отдела, PN. Напротив, недавнее исследование выступал за отсрочку начала ПП до 7 дней у тяжелобольных детей из-за повышенный риск инфицирования и повышенная частота осложнений после начала ПП в течение первых 24 часов после пребывания в отделении интенсивной терапии.Раннее энтеральное питание было разрешено в обоих группы. Однако присутствие или процент пациентов с ОП конкретно не было указано в этом отчете (157).
Резюме: Литература для взрослых поддерживает раннее энтеральное питание, чтобы уменьшить осложнения AP и улучшить выживаемость. Педиатрическая литература поддерживает раннее энтеральное питание в легких случаях ОП и небольшое сообщение в тяжелых случаях AP.
Рекомендация 2di: За исключением наличия прямого противопоказания к употреблению кишечника, детям с острым панкреатитом легкой степени может помочь от раннего (в течение 48–72 часов после обращения) орального / энтерального питания до уменьшения продолжительность пребывания и снижение риска органной дисфункции.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 5; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2dii: Парентеральное питание (ПП) должно следует рассматривать в тех случаях, когда ЭП невозможна в течение длительного периода времени (дольше более 5-7 дней), например, в кишечной непроходимости, сложных свищах, брюшной полости синдром, снижающий катаболическое состояние организма. Следует начать энтеральное питание. как можно скорее, причем комбинация EN и PN превосходит одиночную PN.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15 согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
Рекомендация 2diii: В случае панкреатической разрыв, перелом или разрыв протока, неясно, является ли пероральное / энтеральное питание может быть вредным в острой фазе. Это требует дальнейшего изучения.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 13; согласен = 8; нейтральный = 2; не согласен = 0; категорически не согласен = 0; нет голоса = 1.
2д. Использование антибиотиков при остром панкреатите у детей
Обоснование использования антибиотиков при лечении ОП связано к беспокойству по поводу бактериальной инфекции из-за перемещенной кишечной микробиоты. Антибиотики не рекомендуются для взрослых с легким ОП (70).
При лечении тяжелого ОП у взрослых изучались антибиотики для предотвращения и управлять инфекциями. Имипенем и / или цефалоспорины третьего поколения были наиболее исторически часто использовались в попытке снизить заболеваемость и смертность.Этот Профилактический подход является спорным: предыдущие исследования предполагали пользу (158–160), в то время как другие исследования не продемонстрировали пользы от рутинного использования (161) в отсутствие документально подтвержденной инфекции. Профилактические антибиотики использовались в условиях стерильной некротической болезни. панкреатит для предотвращения инфицированного некротического панкреатита (162, 163), особенно имипенем (163). Однако систематические обзоры не поддерживает преимущества в отношении смертности от инфекций, не затрагивающих поджелудочную железу, или для сокращения хирургических вмешательств у взрослых (162).Более поздние метаанализы подтверждают использование антибиотиков для инфицированы некротическим панкреатитом, но не для стерильный некроз (164–166). Текущий взрослый AP рекомендации — использовать антибиотики только при инфицированном некрозе или у пациентов с некротический панкреатит, госпитализированные и без клинического улучшения использование антибиотиков (70). Зараженный некроз должен быть подозревается, если клиническое состояние пациента ухудшается из-за лихорадки или наличие газа в коллекциях на снимках.В определенных ситуациях стремление жидкость под контролем эндоскопии или с помощью интервенционной радиологии и для руководства лечением может потребоваться создание соответствующего дренажа (8). При некротическом панкреатите известные антибиотики: проникают в некротические ткани, такие как карбапенемы, хинолоны и метронидазол, поскольку использование антибиотика в этих условиях, как было показано, задерживает хирургическое вмешательство. вмешательства и снизить заболеваемость и смертность (33).
Документированные инфекции, происходящие за пределами поджелудочной железы, следует рассматривать как указано.
Не было опубликовано исследований по использованию антибиотиков для лечения АП у детей.
Резюме: Антибиотики нельзя использовать в лечение ОП, за исключением случаев документально подтвержденного инфицированного некроза или у пациентов с некротическим панкреатитом, которые госпитализированы и клинически не улучшаются без использование антибиотиков. Антибиотики, о которых известно, что они проникают в некротические ткани, следует использовать при лечение инфицированного панкреонекроза, поскольку это может отсрочить хирургическое вмешательство и снизить заболеваемость и смертность.
Рекомендации 2ei: Профилактические антибиотики не эмпирически рекомендуется при тяжелом остром панкреатите.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 20; согласен = 3; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
Рекомендация 2eii: показано только использование антибиотиков. в случаях документально подтвержденного инфицированного некроза при остром панкреатите.
16/24 = 67% согласны с рекомендацией. Рекомендация не поддерживается.Это было определено как область особых разногласий, требующих дальнейшего учиться.
Результаты голосования: Полностью согласен = 10; согласен = 6; нейтральный = 2; не согласен = 4; категорически не согласен = 0; нет голоса = 2.
2f. Использование ингибиторов протеазы при остром панкреатите у детей
Поскольку AP предположительно является некровоспалительным процессом, начавшимся через острая и несоответствующая активация трипсина протеазы и зимогенов поджелудочной железы внутри паренхимы, исследователи были очень заинтересованы в блокировании этого воспалительный процесс, чтобы ограничить степень травмы.
Два основных соединения, описанных в литературе для ингибирования этого фермента активация включает ингибитор сериновой протеазы габексат мезилат и трипсин ингибитор апротинин. В 1993 году Pederzoli et al. сообщил результаты рандомизированного, двойное слепое многоцентровое клиническое исследование использования габексата мезилата по сравнению с апротинином в АП-терапия. В этом исследовании мезилат габексата оказался более предпочтительным по сравнению с апротинином в отношении период 24–72 часа, но, что важно, отсутствует контрольная группа плацебо (167).Сроки лечения и способ родоразрешения кажутся быть ключевыми факторами эффективности (167, 168). Ино и др. изучили эффективность непрерывного инфузия регионарной артерии CRAI с габексатом мезилатом и антибиотиками при тяжелом ОП через небольшое проспективное исследование с участием 9 пациентов, получавших CRAI в течение 3-5 дней и 9 пациентов. другие получают терапию системными ингибиторами протеазы и антибиотики. Боль в животе и SIRS исчезал быстрее, LOS был значительно короче в группе CRAI (168). CRAI антипротеаз и антибиотиков имеет Сообщалось о снижении показателей CRP и APACHE II при применении в течение 72 часов после начала болезни (169), подход, описанный в педиатрических больных (170).
Обзор 2007 года, проведенный Китагавой и Хаякавой, не нашел доказательств, оправдывающих рутинное использование антипротеаз при AP, и хотя использование непрерывного внутривенного ингибиторы протеазы и антибиотики в высоких дозах могут быть эффективными для предотвращения обострения тяжелого ОП, необходимы исследования экономической эффективности. Важно, эти соединения не одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США. Штаты (171–173).
Резюме: Некоторые исследования взрослых подтверждают использование антипротеаз в лечении тяжелого АП, но никаких конкретных рекомендаций никогда не было были сделаны для их использования.Исследования не были рандомизированы с контрольными группами плацебо, и только несколько случаи описаны в педиатрических больных.
Рекомендации 2f: Антипротеазы не могут быть рекомендуется при лечении острого панкреатита у детей в это время.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 17; согласен = 7; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2г. Использование антиоксидантов при остром панкреатите у детей
Окислительный стресс способствует повреждению ОП из-за образования кислорода свободные радикалы, вызывающие повреждение липидной мембраны клетки поджелудочной железы, деполяризацию митохондриальной мембраны и индукции фрагментации ДНК (174).Это способствует отеку, возникновению боли и может также быть вовлеченными в процесс некроза. Таким образом, была выдвинута гипотеза об антиоксидантах. иметь потенциальную пользу в качестве дополнительного лечения при АП, предотвращая образование свободные радикалы или улавливание существующих свободных радикалов кислорода.
Наиболее изученными агентами были витамины-антиоксиданты (аскорбиновая кислота, α-токоферол, β-каротин), неорганические антиоксиданты (селен) и глютамин. В двух частично совпадающих метаанализах, опубликованных в 2015 г., используются разные методологии оценки пользы антиоксидантов при остром панкреатите, один обзор 11 и другие 12 рандомизированных контролируемых исследований на взрослых [169, 170].Pederzoli et al. Обнаружили, что антиоксиданты снижают количество осложнений, связанных с ОП, и укороченный LOS с глутамином, снижающим частоту осложнений и смертность [169]. Ино и др. Сообщили, что антиоксидант терапия сокращает LOS и снижает уровень СРБ в сыворотке, но только через 10 дней [170].
Существенным ограничением опубликованных данных об антиоксидантах у взрослых AP является эти испытания включали весь спектр легкого и тяжелого АД. Кроме того, различные комбинации антиоксидантов и время доставки были использованы в испытания.В крупных рандомизированных исследованиях также отсутствует стандартизация конкретных антиоксидантов. как сроки и продолжительность лечения.
Нет данных об использовании антиоксидантов при AP в педиатрической популяции.
Резюме: педиатрические данные об использовании не хватает антиоксидантов в АП. Публикации для взрослых демонстрируют значительную неоднородность относительно состава, времени и продолжительности терапии. Несмотря на потенциальные преимущества описанных в сериях для взрослых, доказательств недостаточно, чтобы поддержать их использование в педиатрия в это время.
Рекомендация 2g: Антиоксиданты не следует считается стандартной терапией при лечении острого панкреатита у детей.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 7; нейтральный = 1; не согласен = 0; категорически не согласен = 1.
2ч. Роль пробиотиков в лечении острого панкреатита у детей
Примерно у трети взрослых пациентов может развиться тяжелая форма АП, характеризующаяся ССВО, органная недостаточность и повышенный риск инфицирования (175).У пациентов с инфицированным перипанкреатическим и панкреонекрозом риск летального исхода значительно увеличивается. Снижение проницаемости кишечника и Предполагается, что избыточный бактериальный рост во время AP снижает риск инфицирования некроз поджелудочной железы и тем самым снизить риск смерти (176, 177).
Всемирная организация здравоохранения определяет пробиотики как «живые микробы. которые при введении в адекватных количествах приносят пользу их здоровью. хозяин». Доказано, что пробиотики играют роль в поддержании микрофлоры кишечника. баланс, подавляя рост вредных бактерий и усиливая иммунную функцию (178).Важно, что опубликованные исследования использовали различные составы и режимы дозирования пробиотических бактерий.
Muftuoglu et al. продемонстрировали, что lactobacillus acidophilus и bifidobacterium lactis уменьшают тяжесть гистологического повреждения в экспериментальной модели панкреатита (178). Ранние небольшие клинические испытания для взрослых показали положительную роль пробиотиков в управление АП. Olah et al. рандомизировали 45 пациентов для приема 10 9 живые или убитые теплом lactobacillus plantarum два раза в день вместе с энтеральное питание (179).Они обнаружили статистически значительно более низкий риск инфицированного панкреонекроза в исследуемой группе по сравнению с контрольные группы.
Однако впоследствии исследование PROPATRIA, двойное слепое, плацебо-контролируемое рандомизированное многоцентровое исследование роли пробиотиков в профилактике инфекционные осложнения при ОП) в составе 298 взрослых пациентов с прогнозируемой тяжелой AP продемонстрировал значительно более высокий риск смерти у многовидовых пробиотиков. группа (180, 181). Два небольших рандомизированных испытания с момента завершения не продемонстрировали увеличение смертности (182, 183), но влияние неблагоприятных результатов исследования PROPATRIA Исследование привело к общей осторожности при использовании пробиотиков у взрослых с ОП.
Ни одно педиатрическое исследование не изучало роль пробиотиков у детей с AP.
Резюме: После серии небольших дел, предполагающих потенциальная польза пробиотиков при ОП у взрослых, большое рандомизированное исследование продемонстрировало повышенная смертность в группе пробиотиков. Педиатрических исследований не опубликовано.
Рекомендации 2 часа: Нельзя рекомендовать пробиотики в лечении острого панкреатита у детей в настоящее время. Высшее качество опубликованные данные для взрослых показывают, что они могут не только не принести пользы, но и увеличивать смертность.
23/24 = 96% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 14; согласен = 9; нейтральный = 1; не согласен = 0; категорически не согласен = 0.
2i. Роль эндоскопии в лечении острого панкреатита у детей
Различные причины воспаления слизистой оболочки двенадцатиперстной кишки связаны с увеличением риск AP. Проявления, связанные с глютеновой болезнью поджелудочной железы, включают эндокринные и внешнесекреторная недостаточность, острый и хронический панкреатит, нарушение питания, папиллярный стеноз вторичный по отношению к дуодениту или иммунологическим нарушениям, и все предположили, что быть вовлеченными механистически (184–186).Желчнокаменная болезнь была обнаружена до 34% пациентов с болезнью Крона и может проявляться как АП (187). Аутоиммунный панкреатит (АИП) и первичный склерозирование холангит (188) также может быть обнаружен у пациентов с воспалительным заболеванием кишечника, проявляющимся AP (189–191). Повышение уровня IgG4 наблюдается у взрослых пациентов с AIP типа I, педиатрические пациенты с AIP обычно без повышения уровня IgG4, при биопсии двенадцатиперстной или желудочно-дуоденальной воспалительной поражения могут быть полезны в диагностике (192, 193).Были случаи острого и хронического панкреатита. редко регистрируется как проявление или ассоциация инфекции H. pylori (194, 195). Чрезвычайно редко возможными причинами панкреатита у детей являются опухоли, связанные с ампула или периампулярная область двенадцатиперстной кишки. Такие поражения могут быть первыми идентифицируется рентгенологическим исследованием, но также может быть обнаружено во время эндоскопического исследования. оценка. Судя по имеющимся историям болезни, механизм развития у этих пациентов рецидивирующий панкреатит до конца не изучен, но, вероятно, связан с опухолью непроходимость на уровне ампулы (196, 197).Но в целом роль эзофагогастродуоденоскопия при ОП ограничена.
Нет исследований, оценивающих показания или преимущества эзофагогастродуоденоскопии в педиатрический AP.
Резюме: Роль эндоскопии в неотложной помощи дети с AP неясно. Возможность первичных внепанкреатических заболеваний В результате разработка AP требует вдумчивого рассмотрения.
Рекомендации 2i: Эзофагогастродуоденоскопия не в настоящее время считается стандартным диагностическим инструментом при остром панкреатите у детей.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2j. Роль ЭРХПГ при остром панкреатите у детей
Роль ЭРХПГ при ОП эволюционировала с технологическими улучшениями в диагностические возможности МРТ / MRCP и с увеличением педиатрического опыта с эндоскопическое ультразвуковое исследование (ЭУЗИ). Благодаря наличию этих последних диагностических инструментов для при заболеваниях поджелудочной железы, ERCP все чаще используется в первую очередь для лечения вмешательства или для неясных диагнозов после MRCP или EUS.ЭРХПГ безопасна для детей при этом наиболее частым осложнением является легкий панкреатит после ЭРХПГ. аналогичны таковым у взрослых (~ 3–10%), когда выполняются опытные эндоскописты (198–206). Обструкция желчевыводящих путей и хронический панкреатит являются наиболее частыми показаниями к ЭРХПГ у детей. В педиатрической AP ERCP имеет ограниченная роль, выполняется почти исключительно при билиарном панкреатите, вторичном по отношению к холедохолитиаз или отстой. ЭРХПГ при холедохолитиазе без панкреатита безопасна и эффективны (207, 208), но в педиатрии нет конкретных рекомендаций по сроки проведения ЭРХПГ при холедохолитиазе или остром билиарном панкреатите.У взрослых большой метаанализ и научно обоснованные рекомендации IAP по ведению острых билиарный панкреатит рекомендовал ЭРХПГ в течение 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. В противном случае можно провести ЭРХПГ. планово при неосложненном холедохолитиазе и в других случаях желчевыводящих путей. панкреатит независимо от степени тяжести (209, 210).
Менее распространенными показаниями для ЭРХПГ при ОП являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы (211).Камни и стриктуры протоков поджелудочной железы обычно признаки острого рецидивирующего или хронического панкреатита, поэтому встречаются относительно редко показания к ЭРХПГ при АП. В редких случаях, когда непроходимость протока предотвращает разрешение панкреатита, может быть проведена терапевтическая ЭРХПГ. Псевдокисты поджелудочной железы в у детей может развиться острый или хронический панкреатит, но чаще всего возникает после тупая травма. Псевдокисты поджелудочной железы представляют собой однородное скопление панкреатической жидкости. окружены фиброзной или грануляционной тканью, но не имеют эпителиальной выстилки (15, 212), и может развиться из скоплений жидкости, сохраняющихся более 4 недель (213).ERCP может использоваться для оценки коммуникации псевдокиста с протоком поджелудочной железы, куда можно установить транспапиллярный стент для дренаж. В противном случае — эндоскопическая цистагастростомия (214–216) и под контролем EUS. дренаж (217) — безопасные и эффективные способы дренировать псевдокисты поджелудочной железы у детей и может быть рассмотрено в зависимости от расположения псевдокиста. Повреждение протока поджелудочной железы и утечка также могут возникнуть в результате травмы. Рано эндоскопическое или хирургическое вмешательство может помочь свести к минимуму продолжающуюся заболеваемость протоковым утечка, поскольку ERCP обеспечивает быстрый и более точный метод определения местоположения и степень повреждения, чем MRCP или CT, а также дает возможность терапевтического стента размещение поперек травмы (218, 219).
Резюме: Роль ЭРХПГ при остром панкреатите. в первую очередь относится к терапевтическому лечению билиарного панкреатита, вторичного по отношению к холедохолитиаз или отстой. Литература для взрослых предполагает эффективность ERCP в пределах 48 часов с момента появления симптомов, если у пациента механическая желтуха и / или холангит. Менее распространенными показаниями к ЭРХПГ при остром панкреатите являются протоковые камни поджелудочной железы, стриктуры, дренаж псевдокисты и протечки протока поджелудочной железы или разрывы протока.
Рекомендации 2ji и 2jii: (2ji) Роль ERCP ограничен при остром панкреатите и зависит от местных знаний.(2jii) ERCP — это показан при лечении острого панкреатита, связанного с холедохолитиазом, вызывающим билиарный панкреатит и патологии протоков поджелудочной железы, такие как протоковые камни или протоки протока.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 21; согласен = 3; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2к. Роль EUS при остром панкреатите у детей
Эндоскопическое ультразвуковое исследование (EUS) использовалось для определения этиология АП.EUS не только всесторонне оценивает паренхиму поджелудочной железы и протока, но также и гепато-билиарной анатомии. Заболевания желчевыводящих путей, такие как холедохолитиаз можно оценить с помощью EUS, особенно когда трансабдоминальное УЗИ не позволяет визуализировать дистальный общий желчный проток. EUS также может определить наличие микролитиаза у желчный пузырь, который часто не визуализируется при трансабдоминальном УЗИ или КТ сканировать. Микролитиаз может привести к ОП и лечится холецистэктомией (220). Хотя у детей это случается крайне редко, опухоли поджелудочной железы, которые могут быть вызваны новообразованием поджелудочной железы или AIP, могут проявляться с AP и пройти дальнейшее обследование с помощью EUS с возможностью взятия пробы ткани поджелудочной железы. (221, 222).
Терапевтическая роль EUS при AP в основном ограничена для лечения осложнения АП, а именно скопление жидкости поджелудочной железы или некроз стенок. EUS имеет было показано, что он полезен при лечении скоплений жидкости поджелудочной железы / некроза вторичный по отношению к тяжелому AP. Считается, что спонтанное рассасывание псевдокист происходит чаще. чаще у детей, чем у взрослых, особенно если размер <5 см (мнение эксперта). Таким образом, с большинством коллекций любого типа можно обращаться консервативно и терапевтически. вмешательство не требуется в остром состоянии, за исключением случаев наличия инфекции (223).Однако, если происходит созревание (обычно через 4–6 недель) саморегулирование менее вероятно, и пациент может нужен эндоскопический дренаж. Другие показания к вмешательству EUS и дренированию включают: большой размер при возникновении клинических симптомов, подозрении на заражение скоплений или стойких симптомы от псевдокисты. Дренаж под контролем EUS и создание цистгастростомы было продемонстрировано, что он столь же эффективен и безопасен, как хирургическая цистгастростомия, и имеет было показано, что он эффективен даже у детей (224).
Резюме: на основании литературы для взрослых, EUS может быть полезным для определения этиологии острого панкреатита, которая может включать диагностику дистального камни общего желчного протока, новообразования поджелудочной железы или аутоиммунный панкреатит. Его роль для терапия в основном ограничена лечением осложнений острого панкреатита, а именно скопления жидкости поджелудочной железы или некроз стенок, вторичный по отношению к тяжелому АД.
Рекомендация 2k: EUS не считается стандартом диагностический инструмент при остром панкреатите у детей в настоящее время.Показания к его применению следует определять в индивидуальном порядке.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
2L Роль хирургии / хирургической консультации при остром панкреатите у детей
Хирургические вмешательства не являются частью алгоритма ведения больного. Типичный эпизод АП. Публикации относятся к взрослому опыту. Раннее указание на хирургия включает лечение синдрома брюшной полости.Однако управление некроз поджелудочной железы с ранней некрэктомией в течение первых 72 часов, как было показано, приводит к повышенная заболеваемость и смертность по сравнению с отсроченными сроками не менее чем на 12 дней (225). Руководящие принципы Международного Ассоциация панкреатологов с 2002 г. предлагает отложить операцию некрэктомии для по крайней мере, через 3-4 недели после начала заболевания снижает заболеваемость и смертность (210). Руководящие принципы ACG 2013 года по управлению взрослый AP прокомментировал возможность хирургического вмешательства в связи с желчнокаменной болезнью. панкреатит, санация некроза (инфицированные vs.стерильный), и малоинвазивный лечение некроза поджелудочной железы (33). Рекомендации включали раннюю холецистэктомию во время той же госпитализации по поводу легкий приступ желчнокаменного панкреатита и обсуждение между гастроэнтерологами и хирургия для выбора времени холецистэктомии по сравнению с другими терапевтическими вариантами в случаях тяжелый АД, особенно с некрозом. Для пациентов с сохраняющейся клинической нестабильностью и ухудшение состояния на фоне некроза поджелудочной железы, дренирование может потребоваться для улучшить статус пациентов и снизить заболеваемость и смертность.Руководящие принципы АЧГ предлагают что санацию некроза следует отложить, когда это возможно, в идеале более четырех недель с момента обращения, чтобы лучше организовать воспалительные реакции. Даже в необходимость некрэктомии, менее инвазивных методов, включая чрескожную радиологию, или следует рассмотреть возможность эндоскопического дренирования / хирургической обработки раны наряду с лапароскопическим хирургическим вмешательством. предпочтение отдается лечению перед открытым хирургическим вмешательством (33).
Исследование PONCHO 2015 г. с участием 266 стационарных пациентов, рандомизированных по интервалу холецистэктомия или холецистэктомия с тем же госпитализацией также поддерживали ту же госпитализацию. холецистэктомия снизила частоту повторных осложнений, связанных с желчнокаменной болезнью, у взрослых пациенты с желчнокаменным панкреатитом легкой степени с очень низким риском холецистэктомии осложнения (226).
В случае тяжелой травмы живота, требующей неотложной лапаротомии (в том числе дорожно-транспортных происшествий) следует искать повреждения поджелудочной железы, в том числе вовлекающий проток поджелудочной железы. Тяжесть травмы поджелудочной железы может быть оценена в соответствии с Американской ассоциации хирургии травм поджелудочной железы по шкале, в которой 5 могут быть присвоены степени травмы (227). Выше травмы поджелудочной железы в результате травмы, как правило, также включают ассоциированную дуоденальную травмы. Пациентам с более легкими тупыми травмами I и II степени можно лечить в нерабочем состоянии.В случае травмы поджелудочной железы мультидисциплинарный подход, включающий: показаны бригады врачей / гастроэнтерологов и хирургов.
В педиатрической литературе о показаниях к операции гораздо больше ограничено. Что касается билиарного панкреатита, ретроспективная серия случаев из 19 детей, госпитализированных с билиарным панкреатитом, зарегистрировано 9 детей, перенесших ранний холецистэктомия без побочных эффектов и 4 из 10 детей, перенесших отсроченную операцию возникновение нежелательных клинических явлений (включая рецидив панкреатита) (228).
Резюме: Показания к острому хирургическому вмешательству. к показаниям АП относятся травмы живота, при которых у пациента нестабильность и / или поиск происходит сопутствующее повреждение других органов. В контексте билиарного панкреатита было показано, что холецистэктомия не только безопасна, но и предотвращает рецидивы, если они происходят. в рамках индекса госпитализации. Литература для взрослых предполагает, что раннее вмешательство в некроз поджелудочной железы приводит к увеличению заболеваемости и смертности, и, следовательно, к санации раны желательно отсрочить некроз поджелудочной железы, вызывающий нестабильность у пациента, по крайней мере, на 4 часа. недель с момента обращения, в идеале — эндоскопическим или чрескожным способом.
Рекомендация 2li: холецистэктомия безопасно может и следует выполнять перед выпиской в случаях легкой неосложненной острой желчной болезни. панкреатит.
22/24 = 92% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 16; согласен = 6; нейтральный = 1; не согласен = 1; категорически не согласен = 0.
Рекомендация 2lii: В ведении острых некротических скоплений, вмешательств следует избегать и откладывать, даже для инфицированных некроз, поскольку результаты лучше при отсроченном (> 4 недель) подходе.
21/24 = 88% согласны с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 6; нейтральный = 2; не согласен = 1; категорически не согласен = 0.
Рекомендация 2liii: Когда требуется дренирование или некрэктомия. необходимые нехирургические доступы, включая эндоскопические (EUS и ERCP) или чрескожные методы предпочтительнее открытой некрэктомии или открытой псевдокисты дренаж.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 15; согласен = 9; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
3. ИСХОДЫ ОСТРОГО ПАНКРЕАТИТА ПЕДИАТРИИ
Общие исходы ОП у детей благоприятны по сравнению со взрослыми. В средняя продолжительность госпитализации детей с ОП составляет в среднем от 2,8 до 8 дней, хотя младенцы / малыши, как правило, поступают на более длительный период времени (в среднем 19,5 дней) (15, 73, 229–231). Раннее начало энтерального питания и агрессивная жидкостная реанимация был связан с более коротким пребыванием в больнице, меньшим количеством госпитализаций в отделения интенсивной терапии и снижение показателей тяжелого АП по сравнению с пациентами, находящимися в НКО (73).Эти результаты в целом совпадают с выводами большинства взрослых. исследований (232), но, возможно, не применялись к педиатрические пациенты до недавнего времени. Более высокая смертность при ПД у детей связана с системное заболевание, но в целом низкий и составляет менее 5% в большинстве когорт, даже в том числе в реанимации (15, 30, 233, 234).
Осложнения с ранним началом при ОП включают полиорганную дисфункцию или шок (15). Острые скопления перипанкреатической жидкости наблюдаются в острая фаза панкреатита и имеет тенденцию к спонтанному разрешению.Частота образование псевдокист колеблется от 8% до 41% у детей с панкреатитом, и более высокие показатели наблюдаются у пациентов с панкреатитом, связанным с абдоминальной травма (15, 212, 235). Псевдокисты часто бессимптомный и может лечиться консервативно или стать больше и вызвать боль в животе, рвота или лихорадка. Они также могут заразиться в 10–15% случаев. (236). Еще одно осложнение с поздним началом связано с до некроза поджелудочной железы. Некроз может проявляться в первую очередь в виде острого некротического скопления. (ANC), а затем созревают до некроза без стенок (WON) (8).Варианты лечения при дренировании псевдокист и некротических стенок коллекции включают эндоскопический (транспапиллярный или трансмуральный) дренаж, чрескожный катетерный дренаж или открытая / лапароскопическая операция. Выбранная модальность зависит от размера, расположение, анатомия и риски / преимущества процедуры, хотя чрескожная и Трансгастроинтестинальный дренаж под контролем эндоскопического ультразвука (ЭУЗИ) в настоящее время становится все более популярным. широко распространено (237).
Примерно 15–35% детей с острым у панкреатита будет еще один приступ панкреатита.Острый рецидивирующий заболевание у детей панкреатит связан с панкреатико-билиарными аномалиями, аутоиммунным панкреатитом, нарушения обмена веществ и наследственный панкреатит (15).
Резюме: За детьми необходимо следить во время их курс АП при местных и системных осложнениях, которые могут включать дисфункцию органов, острые скопления жидкости и впоследствии некроз или псевдокисты. Общий педиатрические пациенты с острым панкреатитом имеют хороший прогноз с очень низким уровнем смертность, но сообщается о частоте рецидивов до 15–35%.
Рекомендация 3: Дети с острым панкреатитом должны получить тщательное наблюдение со стороны поставщика медицинских услуг для выявления раннего или позднего осложнения или рецидивы.
24/24 = 100% согласие с рекомендацией.
Результаты голосования: Полностью согласен = 18; согласен = 6; нейтральный = 0; не согласен = 0; категорически не согласен = 0.
Что нужно знать
Что такое панкреатит?
Узнайте, как выглядит панкреатит у детей и как он влияет на них. Вы также узнаете разницу между острым и хроническим панкреатитом.
Панкреатит — это заболевание, вызывающее воспаление поджелудочной железы. Поджелудочная железа — это большой орган в верхнем левом углу живота (область живота) за желудком. Поджелудочная железа вырабатывает гормоны и ферменты, которые помогают контролировать уровень сахара в крови и переваривать жиры, белки и углеводы. Существует два типа панкреатита: острый панкреатит (внезапный и излечимый) и хронический панкреатит (длительный и не всегда излечимый).
Острый панкреатит возникает внезапно.Воспаление обычно длится всего несколько дней или недель. Иногда острый панкреатит проходит самостоятельно без лечения.
Хронический панкреатит — хроническая (длительная) форма панкреатита. Со временем длительное воспаление может повредить поджелудочную железу. Во многих случаях хронический панкреатит вызван множественными прошлыми случаями острого панкреатита ( рецидивирующих острых панкреатитов ).
Причины панкреатита у детей
У детей часто развивается острый панкреатит, когда камни в желчном пузыре блокируют желчный проток, проходящий через поджелудочную железу.Хронический панкреатит может развиться в результате рецидивирующего (повторного) острого панкреатита.
Каковы общие причины панкреатита?
Самая частая причина панкреатита — желчнокаменная болезнь . Камни в желчном пузыре — это небольшие затвердевшие кусочки желчи (пищеварительная жидкость, вырабатываемая печенью), холестерина (воскообразное вещество в крови) и кальция в желчном пузыре (небольшой мешочек под печенью). Панкреатит может развиться, когда желчные камни блокируют желчный проток (трубку, по которой желчь из печени и желчного пузыря проходит через поджелудочную железу в двенадцатиперстную кишку или первую часть тонкой кишки).
Каковы факторы риска панкреатита?
Хотя причина панкреатита может быть неясной, существуют определенные факторы, которые могут повысить риск развития этого состояния у вашего ребенка. Эти факторы риска включают:
- Семейный или личный анамнез панкреатита
- Предыдущая травма (травма) живота (область живота)
- Абдоминальная хирургия
- Определенные метаболические состояния или аномалии органов пищеварения
- Высокий уровень жира или очень высокий уровень кальция в крови
- Муковисцидоз (генетическое заболевание)
- Некоторые лекарства
- Сильное или длительное употребление алкоголя
Симптомы и диагностика панкреатита
Симптомы острого и хронического панкреатита могут быть схожими.Ниже вы узнаете симптомы каждого типа панкреатита.
Признаки и симптомы острого панкреатита включают:
- Боль в верхней части живота (область живота), продолжающаяся часами или днями
- Боль в животе, усиливающаяся после еды
- Боль в животе, которая распространяется на спину или грудь
- Болезненность в животе
- Тошнота и / или рвота
- Лихорадка
- Учащенное сердцебиение
- Низкое артериальное давление
- Пожелтение кожи или глаз
Признаки и симптомы хронического панкреатита включают:
- Хроническая потеря веса (даже если ребенок ест нормально)
- Диарея
- Стул маслянистый, бледный и меловой
- Проблемы или неспособность переваривать пищу
- Диабет
Как врачи проверяют панкреатит?
Обследование на панкреатит может включать:
- Анализы крови
- Диагностические методы визуализации, такие как рентген, компьютерная томография, магнитно-резонансная томография или ультразвук
- Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ), визуализирующий тест, в котором используется эндоскоп (небольшая тонкая гибкая трубка с камерой на конце), чтобы заглянуть внутрь тела и проверить поджелудочную железу
- Эндоскопическое УЗИ (визуализация поджелудочной железы с помощью УЗИ и эндоскопа)
Варианты лечения
Панкреатит часто лечат с помощью лекарств, голодания или жидкости через капельницу.Ниже вы узнаете, как врачи лечат острый и хронический панкреатит.
Лечение обычно направлено на купирование боли и уменьшение воспаления. Процедуры могут включать:
- Пост для восстановления поджелудочной железы и уменьшения воспаления
- Обезболивающее для уменьшения боли
- Лекарство с ферментами поджелудочной железы для улучшения пищеварения
- Витамины A, E, D и K
- Вводит жидкость через капельницу, чтобы организм вашего ребенка оставался гидратированным, пока он лечит поджелудочную железу
- Лечение состояний , вызвавших панкреатит у вашего ребенка (например, желчнокаменная болезнь)
- В некоторых случаях панкреатита: Операция по очистке или дренированию закупоренного желчного протока
Хирургия хронического панкреатита
Когда панкреатит необходимо лечить хирургическим путем, врач обычно выполняет операцию на поджелудочной железе или операцию на желчном пузыре .Они также могут устранить закупорку желчного протока. Ниже вы узнаете о различных типах хирургических вмешательств, которые могут помочь при панкреатите.
Хирургия лучше всего подходит для детей с определенными нарушениями обмена веществ или аномалиями органов пищеварения. Бригада по уходу может поговорить с вами о том, является ли операция хорошим вариантом лечения для вашего ребенка.
К наиболее распространенным видам операций при панкреатите относятся:
- Хирургия поджелудочной железы для отвода жидкости из поджелудочной железы или удаления пораженных тканей.
- Панкреатекомия с аутотрансплантатом островковых клеток. Это когда врачи перемещают островковые клетки (группы клеток поджелудочной железы, которые слишком рано вырабатывают гормоны) в печень.
- Операция на желчном пузыре по удалению желчного пузыря. Это может помочь предотвратить образование большего количества желчных камней.
- Устранение непроходимости желчного протока.
- Эндоскопия (визуализирующий тест с использованием эндоскопа , — тонкой гибкой трубки с камерой на конце, чтобы заглянуть внутрь тела и проверить поджелудочную железу).
Оперативное лечение хронического панкреатита у детей | Гастроэнтерология | JAMA Surgery
Гипотеза Хронический панкреатит в детстве — редкое, но потенциально изнурительное заболевание, и часто бывает неэффективность консервативной терапии с использованием хронических обезболивающих. Мы предполагаем, что агрессивная хирургическая терапия обещает долгосрочную ремиссию.
Дизайн Ретроспективный анализ данных, собранных проспективно за 12 лет.
Настройка Детский стационар третичного уровня.
Пациенты Восемнадцать детей (3-13 лет, 11 девочек) подверглись хирургическому лечению хронического панкреатита после 1-6 лет применения различных лекарственных препаратов (парентеральное питание, соматостатин или обезболивающие). Этим пациентам потребовалось в среднем ± стандартное отклонение 6 ± 0 госпитализаций до операции. Панкреатит был семейным у 9 пациентов, идиопатическим — у 5, и вторичным из-за травмы и приема лекарств — у 2 пациентов.Предоперационная эндоскопическая ретроградная холангиопанкреатография показала дилатацию протока поджелудочной железы у 7, стриктуры в 5, протоковые камни у 4 и нормальные результаты у 2 детей. Оперативное лечение включало продольную панкреатикоеюностомию у 2 детей (у обоих детей панкреатикоеюностомия не удалась, но улучшение после перенесенной панкреатэктомии) и дистальной панкреатэктомии. с панкреатикоеюноанастомозом по Ру у 16 детей.
Показатели результата Выживаемость, необходимость в госпитализации или повторной операции, а также потребность в приеме хронических обезболивающих.
Результаты Все пациенты выжили. Срок наблюдения составил от 1 года до 15 лет. Тринадцать (72%) из 18 пациентов не нуждались ни в госпитализации, ни в приеме лекарств. Двум пациентам потребовалась вторая операция для преобразования продольной панкреатикоеюностомии в дистальную панкреатэктомию, а 3 пациентам потребовалось от 2 до 5 дополнительных госпитализаций по поводу рецидивирующего панкреатита. Эндоскопическая ретроградная холангиопанкреатография у 5 пациентов через 2–4 года после операции показала открытую дистальную панкреатикоеюностомию.
Выводы Эта серия исследований предполагает, что дистальная панкреатэктомия и панкреатикоеюностомия являются эффективными методами лечения этой сложной группы пациентов, в то время как продольная панкреатикоеюностомия оказалась неэффективной. Обычные результаты после этой процедуры — долгосрочное облегчение боли и снижение потребности в повторной госпитализации.
ХОТЯ хронический панкреатит редко встречается у детей, тем не менее, он может быть таким же изнурительным и неумолимым, как и у взрослых.Причины панкреатита у детей, как правило, больше связаны с наследственностью, приемом лекарств, травмой или идиопатическим происхождением, а не с выбором образа жизни (например, злоупотреблением алкоголем) у взрослых. Хронический панкреатит у детей прогрессирует и в большинстве случаев плохо поддается лечению, часто наблюдается зависимость от обезболивающих, чрезмерное количество пропущенных школьных дней и ограничение активности (например, занятий спортом). 1 В нескольких сообщениях об оперативном лечении панкреатита у детей подчеркивается коррекция анатомических дефектов (поджелудочная железа) или представлены небольшие серии декомпрессии расширенного протока поджелудочной железы, но имеется мало сообщений об относительно большой группе детей, у которых есть был пролечен с помощью агрессивной резекции и диверсии.В этом отчете подробно описывается ведение 18 детей с хроническим панкреатитом, ослабляющим здоровье, в течение 12 лет.
Восемнадцать детей прошли хирургическое лечение хронического панкреатита в детской больнице Кардинала Гленнона, Центр медицинских наук Университета Сент-Луиса, Сент-Луис, Миссури, с января 1986 года по декабрь 1998 года. Их возраст на момент операции составлял от 3 до 13 лет (средний 8 лет), 11 (61%) пациентов — девушки. Эта группа пациентов представляет собой группу из более чем 100 детей, обследованных в тот же период с острым или острым рецидивирующим панкреатитом, которые не были склонны к постоянной боли при хроническом панкреатите или у которых панкреатит полностью разрешился без оперативного лечения.Кроме того, в данную серию не были включены дети с псевдокистой поджелудочной железы.
Девять (50%) из 18 пациентов имели семейный анамнез панкреатита (не связанный со злоупотреблением алкоголем, камнями в желчном пузыре или другими причинами). У пяти из них были родители (4 матери и 1 отец), у которых был диагностирован панкреатит в детстве, у 2 были тетя или дядя с аналогичным панкреатитом в анамнезе, а у 2 других были бабушка и дедушка с таким анамнезом. В этой серии не было случаев панкреатита у братьев и сестер.У пяти пациентов был идиопатический панкреатит, хотя у 2 из них при эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ) была обнаружена перегородка поджелудочной железы. Однако, как объяснялось в данном документе, анатомия поджелудочной железы не считалась основной причиной эпизодов панкреатита у этих пациентов. У двух пациентов развился хронический панкреатит от 6 месяцев до 2 лет после тупой травмы брюшной полости поджелудочной железы (оба были травмами руля велосипеда), а у последних 2 пациентов был хронический панкреатит, связанный с приемом лекарств (длительное применение кортикостероидов при красной волчанке и кортикостероиды и аспарагиназа, применяемая для лечения лимфомы).
Все пациенты в этой серии почти ежедневно страдали хронической болью в животе, которая существенно мешала их деятельности. Только у 2 из 18 детей были безболезненные периоды продолжительностью более 4 недель, у остальных по существу ежедневные эпизоды боли в верхней части живота, которые часто передавались в спину. Также были распространены тошнота и анорексия, и 12 (67%) из 18 потеряли вес. У большинства детей исходная хроническая боль усиливалась во время еды.
Эпизоды острого «обострения» панкреатита, потребовавшего госпитализации, были обычным явлением в этой группе пациентов, так же как и множественные менее тяжелые эпизоды, лечившиеся вне больницы.Количество госпитализаций по поводу обострений панкреатита у этих детей варьировалось от 4 до 13 (в среднем 6), что было подтверждено физическим осмотром, гиперамилаземией, повышением липазы в сыворотке крови или радиологическими исследованиями (ультразвуковое исследование и компьютерная томография).
Различные методы лечения, которые использовались для этих пациентов до направления на хирургическое лечение, включали диеты с низким содержанием жиров (18 пациентов), пероральные ферменты поджелудочной железы (16 пациентов), парентеральное питание в больнице (14 пациентов) и дома (5 пациентов), соматостатин внутривенно во время госпитализации (13 пациентов) и в течение 1-3 месяцев дома (3 пациента), а также внутривенное и пероральное обезболивающее (18 пациентов).Восемь из 18 пациентов зависели от употребления наркотиков для поддержания повседневной активности.
Пациенты были обследованы с помощью УЗИ поджелудочной железы и желчного дерева (18 пациентов), компьютерной томографии (13 пациентов) и ERCP (18 пациентов). Эндоскопическая ретроградная холангиопанкреатография у детей младшего возраста (<14 лет) проводилась под общим наркозом, в то время как дети старшего возраста переносили ЭРХПГ с седацией в сознании. Эндоскопическая сфинктеротомия была выполнена 10 детям во время ЭРХПГ, в том числе 2 детям с поджелудочной железой, и во всех случаях безуспешно.
Все дети были направлены на хирургическое лечение, когда медикаментозное лечение оказалось неэффективным, когда нельзя было отменить наркотические препараты или когда эпизоды панкреатита и хроническая боль мешали повседневной деятельности, такой как школа, спорт и социальные контакты. Пять пациентов прошли консультацию у психиатра до направления к специалистам, трое прошли курс реабилитации от наркозависимости и один выразил суицидальные мысли.
Оперативный доступ несколько продиктован результатами компьютерной томографии и ERCP.Двум пациентам с сильно расширенным протоком поджелудочной железы, обнаруженным на ЭРХПГ (рис. 1), первоначально была проведена продольная панкреатикоеюностомия (процедура Пуэстоу), 2 , но продолжающиеся эпизоды панкреатита потребовали повторной операции и перехода на дистальную (дистальнее верхних брыжеечных сосудов, 50% — 60%) панкреатэктомия через 6 месяцев и 2 года после первичной операции. Двум другим пациентам с делением поджелудочной железы была выполнена первичная дуоденотомия и инъекция контрастного вещества в оба сосочка, что показало нормальную анатомию.Оба эти пациента ранее перенесли эндоскопическую сфинктеротомию. Затем им была выполнена дистальная панкреатэктомия с панкреатикоеюностомией по Ру. Остальным 14 пациентам, многие из которых имели диффузное заболевание, наблюдаемое на ERCP (рис. 2), была выполнена дистальная (50–90%) панкреатэктомия с панкреатикоеюностомией Roux-en-Y (процедура Дюваля). 3 Спленэктомия не потребовалась ни одному из этих пациентов. Тщательное рассечение поджелудочной железы от сосудов селезенки с сохранением селезенки было возможно у каждого пациента.Этим пациентам не требовалось сопутствующих операций на желчевыводящих путях.
Пациенты наблюдались гастроэнтерологическими и хирургическими службами и оценивались на выживаемость, периодические боли, необходимость повторных госпитализаций при эпизодах панкреатита или корректировку обезболивающих, а также качество жизни, включая изменение социальной или спортивной активности. Метадон использовался по мере необходимости, чтобы помочь отлучить от наркотических средств, а консультация психиатра была полезна в послеоперационной реабилитации для нескольких пациентов.
Все дети выжили с последующим наблюдением от 1 до 15 лет (в среднем 7,5 лет). Операционных осложнений не было, пациенты были выписаны через 5-11 дней после операции.
Гистологическое исследование резецированных образцов показало сочетание интенсивного фиброза, уплотненных и слоистых внутрипротоковых конкрементов (рис. 3) и гипертрофии островковых клеток возле протоков (рис. 4). Кроме того, были замечены множественные нервные стволы, захваченные в зонах фиброза и воспаления (Рисунок 5).
Тринадцать (72%) из 18 пациентов не нуждались в дальнейшей госпитализации по поводу эпизодов панкреатита. Кроме того, эти пациенты были успешно отлучены от всех обезболивающих, могут выдерживать обычную диету без потребления жиров или других ограничений и участвовать в обычной повседневной деятельности. В эту подгруппу входят 2 пациента, которым потребовалось преобразовать процедуру Пуэстоу в дистальную резекцию поджелудочной железы. Также включены 2 пациента с панкреатитом, связанным с приемом лекарств.Пациент с волчанкой продолжает периодически принимать кортикостероиды без повторяющихся болей, а ребенок с панкреатитом, связанным с химиотерапией лимфомы, не получает химиотерапию в течение 5 лет. Наконец, у 2 пациентов с посттравматическими стриктурами больше не было эпизодов боли.
У трех пациентов были рецидивирующие эпизоды документально подтвержденного панкреатита (боль в животе и гиперамилаземия) через 2–6 лет после операции. 2 -8 Все эти пациенты имеют документацию ERCP о патентной панкреатикоеюностомии (рис. 6), и их эпизоды панкреатита легко купируются с помощью низкожировой диеты, пероральных панкреатических ферментов, краткосрочных внутривенных обезболивающих и соматостатина.Ни один из 3 пациентов не принимает длительно обезболивающие. У двух последних пациентов периодически возникали боли в животе, сопровождающиеся тошнотой. Однако эти эпизоды непродолжительны, не требуют госпитализации и не задокументированы как эпизоды панкреатита. Оба эти пациента также испытывали трудности с прекращением приема пероральных наркотических средств, несмотря на попытки реабилитации от наркозависимости. У всех 5 пациентов с повторяющимися эпизодами боли изначально был диагностирован наследственный панкреатит.
Ни у одного пациента не развилась эндокринная или внешнесекреторная недостаточность поджелудочной железы в результате резекции поджелудочной железы. Однако 5 пациентов с подозреваемым или задокументированным рецидивирующим панкреатитом продолжают получать пероральные ферменты поджелудочной железы в попытке подавить секрецию поджелудочной железы для предотвращения панкреатита, и поэтому точный статус их внешнесекреторной функции поджелудочной железы остается неизвестным. Последующие исследования на предмет наличия диабета (уровни инсулина и тесты на толерантность к глюкозе) обычно не проводились.
Хронический панкреатит редко встречается у детей и гораздо чаще встречается у взрослых, у которых он обычно связан со злоупотреблением алкоголем. Большинство случаев острого панкреатита у детей (вторичных по отношению к травмам, приемам лекарств и камням в желчных путях) непродолжительны и редко переходят в хроническое состояние. Однако хронический панкреатит у детей может быть таким же изнурительным, как и у взрослых 1 , и может привести к изменению образа жизни, пропуску школы, ограничению питания и зависимости от обезболивающих.
Хронический панкреатит у детей можно в общих чертах классифицировать по наличию или отсутствию наследственных факторов, 4 аномалий анатомии протоков, 5 и наличию связанных метаболических нарушений, таких как муковисцидоз, гиперпаратиреоз, гиперлипидемия и недоедание. 6 Независимо от причины хронический панкреатит у детей обычно имеет неумолимое прогрессирование, которое, как известно, трудно поддается медикаментозному лечению.Хронический панкреатит у детей, как и у взрослых, отличается от острого рецидивирующего панкреатита, при котором между эпизодами обострения возникают периоды без боли или других симптомов. Периоды между эпизодами могут составлять от 1 до 2 лет, и, как правило, острый рецидивирующий панкреатит не приводит к серьезной инвалидности, изменению образа жизни или хроническому использованию лекарств. У многих пациентов приступы обычно прекращаются. 7 Кроме того, большинство случаев острого панкреатита у детей, обычно связанного с травмой, инфекцией или приемом лекарств, проходят самостоятельно и редко прогрессируют до хронического панкреатита, если не развивается конкретный анатомический дефект, такой как стриктура протока поджелудочной железы, которая присутствовал у 2 наших пациентов после травмы.
Наследственный или семейный панкреатит — аутосомно-доминантное заболевание с 80% пенетрантностью. Было идентифицировано несколько родств, и «пропуск» поколений не является чем-то необычным. 8 Тщательный семейный анамнез необходимо собрать для каждого пациента с панкреатитом, который не может быть объяснен никакими другими причинами. Наследственный панкреатит может быть связан с расширением протока поджелудочной железы, который поддается дренированию. Недавно сообщалось, что мутация в катионном гене трипсиногена является причиной наследственного панкреатита. 9 Предполагается, что этот дефект приводит к неспособности инактивировать трипсин, что делает возможным самопереваривание поджелудочной железы у этих пациентов.
Различные патологии протоков, которые, как сообщалось, являются причинами хронического панкреатита у детей, включают травматическую стриктуру, 10 деления поджелудочной железы, 5 врожденный сфинктер Одди, 11 киста холедоха, 12 дуоденальная дупликация , и кольцевидная поджелудочная железа.Очевидно, поражения, которые закупоривают проток поджелудочной железы или ампулу Фатера, могут вызывать эпизоды острого панкреатита, но обычно поражения обнаруживаются и восстанавливаются до того, как разовьется более хроническое состояние. В этом отношении может быть полезна ранняя ЭРХПГ. Аналогичным образом, сопутствующие метаболические нарушения, которые приводят к панкреатиту, обычно выявляются и лечатся, хотя эпизоды острого и хронического панкреатита могут продолжаться во время лечения основного заболевания.
Среди различных патологий протоков, о которых сообщалось у детей, наибольшее внимание уделялось поджелудочной железе.Pancreas divisum обнаруживается у 10% населения в целом и, как полагают, возникает в результате несращения дорсального и вентрального зачатков поджелудочной железы плода. Считается, что панкреатит возникает из-за стеноза дорсального протока поджелудочной железы (протока Санторини), дренирующего через малый сосочек. Эндоскопическая ретроградная холангиопанкреатография со сфинктеротомией сосочков была предложена в качестве первичной терапии, 5 , хотя эта процедура не всегда была успешной.В нашу серию входят 2 пациента с этим анатомическим вариантом, которым не удалось улучшить результаты при сфинктеротомии ERCP, но которые в конечном итоге значительно улучшились после дистальной панкреатэктомии и панкреатикоеюностомии.
Несмотря на некоторые противоречия, агрессивное оперативное лечение хронического панкреатита у взрослых показало свою эффективность у многих пациентов, у которых неоперативное лечение оказалось неэффективным, 13 , но его применение у детей было ограничено. Выбор операции при хроническом панкреатите у ребенка, как и у взрослого, неоднозначен.Попытки сохранить ткань поджелудочной железы одним только отводом протока без резекции дали неоднозначные результаты. 4 , 7 , 14 Поскольку хронический панкреатит имеет тенденцию быть диффузным заболеванием желез и поскольку источник хронической боли, вероятно, больше связан с нейропатией, а не с давлением протоков, 15 неудивительно, что простая протоковая декомпрессия может не принести значительного долговременного облегчения. 16 В нашу серию вошли 2 ребенка, которым не удалось выполнить простую продольную панкреатикоеюноанастомию, но впоследствии улучшилось состояние после дистальной панкреатэктомии, что в некоторой степени подтверждает это наблюдение.Точно так же простая резекция дистального отдела поджелудочной железы без отведения протока также не может облегчить боль. 17
По этим причинам мы выбрали резекцию дистального отдела поджелудочной железы, которая была областью с наиболее интенсивным фиброзом у большинства пациентов в данной серии, в сочетании с дренированием по Roux-en-Y дистального конца оставшейся поджелудочной железы (процедура Дюваля). ). 3 По нашему опыту, это обеспечило долгосрочное облегчение боли, а последующая ЭРХПГ продемонстрировала проходимость анастомоза даже несколько лет спустя (рис. 6).В этом случае успешно использовалась альтернативная процедура, дистальная панкреатэктомия в сочетании с продольной панкреатикоеюностомией (модифицированная процедура Пуэстоу), 2 , 14 .
Неудивительно, что некоторые пациенты продолжают испытывать приступы боли после операции, и это также подчеркивалось в других опубликованных сериях. 4 , 14 Хотя некоторые исследования предполагают, что успешный дренаж протока может обратить вспять прогрессирование заболевания, 18 другие авторы сообщают о более безжалостном течении, несмотря на успешное дренирование. 19 Мы считаем, что эти процедуры обеспечивают значительное облегчение боли, но мы не исследовали их влияние на долгосрочную эндокринную и внешнесекреторную функцию поджелудочной железы у этих пациентов. Однако ни у одного пациента из нашей серии не было признаков диабета, стеатореи или других проявлений недостаточности поджелудочной железы.
Оперативное лечение хронического панкреатита у детей останется спорным, несмотря на в целом хорошие результаты в этой и других опубликованных сериях.Попытки сохранить ткань поджелудочной железы путем выполнения панкреатикоеюностомии без дистальной резекции могут облегчить боль, но хирург должен быть готов к более агрессивному подходу в случае неудачной консервативной операции. Мы обнаружили, что сочетание дистальной резекции с дренажом протока может обеспечить долгосрочное облегчение боли и позволит этой группе детей вернуться к более нормальному образу жизни и развитию.
Представлено на 108-й научной сессии Западной хирургической ассоциации, Дана-Пойнт, Калифорния, 15 ноября 2000 г.
Автор, ответственный за переписку: Томас Р. Вебер, доктор медицины, отделение детской хирургии, отделение хирургии, Детская больница кардинала Гленнона, 1465 S Grand Boulevard, St Louis, MO 63104 (электронная почта: [email protected]).
1. маленький JMTait Н. Ричардсон ADubois R Хронический панкреатит, начинающийся в детском и подростковом возрасте. Arch Surg. 1992; 12790-92Google ScholarCrossref 2.Puestow CBGillesby WJ Ретроградный хирургический дренаж поджелудочной железы при хроническом рецидивирующем панкреатите. Arch Surg. 1958; 76898-907Google ScholarCrossref 3.Duval MC Каудальная панкреатикоеюностомия при хроническом панкреатите. Ann Surg. 1954; 140775-785Google ScholarCrossref 4.Moir CRKonzen KMPerrault J Хирургическая терапия и долгосрочное наблюдение при детском наследственном панкреатите. J Pediatr Surg. 1992; 27282–287Google ScholarCrossref 5.Neblett WWO’Neill J Хирургическое лечение рецидивирующего панкреатита у детей с делением поджелудочной железы. Ann Surg. 2000; 231899-908Google ScholarCrossref 6. Гешан FKGreene HLAvant GO’Neill JNeblett W Хронический рецидивирующий панкреатит в детском возрасте. J Pediatr. 1983; 102514-518Google ScholarCrossref 7. Скотт HWNeblett WWO’Neill JSawyers JLAvant GStarnes V Продольная панкреатикоеюностомия при хроническом рецидивирующем панкреатите с дебютом в детском возрасте. Ann Surg. 1984; 199610-622Google ScholarCrossref 9.Вон Димри CKelleher JDrumm B Стентирование протока поджелудочной железы как лечение наследственного панкреатита. Педиатрия. 1999; 1041129-1133Google ScholarCrossref 10.Fonkalsrud EWHennoy RPRiemonschneider TABarker WF Управление панкреатитом у младенцев и детей. Am J Surg. 1968; 116198-203Google ScholarCrossref 11.Hendren WHGreep JMPatton JS Панкреатит в детстве: опыт 15 случаев. Arch Dis Child. 1965; 40132-1388Google ScholarCrossref 12. Гибсон ЛЕХаллер JA. Острый панкреатит, связанный с врожденной кистой общего желчного протока. J Pediatr. 1959; 48486-489Google ScholarCrossref 13.Morel PRohner Хирургия хронического панкреатита. Хирургия. 1987; 101130-135Google Scholar14.Crombleholme TdeLorimier Прочь LWAdzick NSLongaker MTHarrison MR Модифицированная процедура Puestow при хроническом рецидивирующем панкреатите у детей. J Pediatr Surg. 1990; 25749-754Google ScholarCrossref 15.Bockman DEBuchler М.М.альфертхаймер PBeger HG Анализ нервов при хроническом панкреатите. Гастроэнтерология. 1988; 941459–1469. Google Scholar, 16. Марковиц. JSRattner DWarshaw А.Л. Отсутствие симптоматического облегчения после панкреатоеюнальной декомпрессии при хроническом панкреатите. Arch Surg. 1994; 129374-380Google ScholarCrossref 17.Rattner ДФернандес-дель-Кастильо CWarshaw А.Л. Подводные камни дистальной панкреатэктомии для облегчения боли при хроническом панкреатите. Am J Surg. 1996; 171142-146Google ScholarCrossref 18.Нилан WHTownsend CThompson JC. Оперативное дренирование протока поджелудочной железы задерживает функциональные нарушения у пациентов с хроническим панкреатитом. Ann Surg. 1988; 208321-327Google ScholarCrossref 19.Berney Трудисухли TOberholzer Дж. Колфилд AMorel P Отдаленные результаты метаболизма после резекции поджелудочной железы по поводу тяжелого хронического панкреатита. Arch Surg. 2000; 1351106-11111Google ScholarCrossrefКарен В. Уэст, доктор медицины, Индианаполис, штат Индиана: [Прочитано Фабрицио Микеласси, доктор медицины, в отсутствие доктора Уэста.] Этот отчет касается очень сложной группы детей с хроническим панкреатитом и дает представление о долгосрочных проблемах. встречается у послеоперационного больного. У половины этих пациентов был семейный панкреатит. Авторы отмечают, что симптомы присутствовали от 1 до 6 лет до хирургического вмешательства.Девять из 18 пациентов к моменту операции испытывали наркотическую зависимость или психологические проблемы. Примечательно, что послеоперационных осложнений не было, независимо от типа использованных процедур. Доктор Вебер напоминает нам, что пациенты с семейным панкреатитом имеют самые плохие отдаленные результаты: 5 из 9 испытывают гораздо более легкие, но продолжающиеся эпизоды боли после хирургического вмешательства. Мои вопросы: (1) Десяти пациентам была выполнена эндоскопическая сфинктеротомия без улучшения.Каковы были показания (проксимальные камни, стриктуры, повышенное давление), и вы рекомендуете продолжить эту процедуру в свете этих результатов? Встречались ли какие-либо осложнения после сфинктеротомии после ЭРХПГ?
(2) Удалось ли вам сопоставить продолжительность симптомов до операции с проблемами с повторяющейся болью или с необходимостью перехода от процедуры Puestow к процедуре Дюваля? Как вы думаете, может ли более раннее вмешательство до развития фиброза и нейропатии сыграть роль в последующем течении пациентов с семейным панкреатитом? Насколько обширна ваша дистальная панкреатэктомия? Как долго длился продольный анастомоз панкреатикоеюноанастомоза? Нам не нужно было преобразовывать какие-либо из наших процедур Puestow, хотя у 2 были эпизоды ограниченной боли и преходящей гиперамилаземии при долгосрочном наблюдении.Процедура Puestow может успешно применяться у этих сложных педиатрических пациентов.
(3) Вы указали, что ни у одного из пациентов не было симптомов экзокринной / эндокринной дисфункции. Наблюдаются ли за этими детьми в многопрофильной среде, чтобы иметь возможность решать долгосрочные проблемы, включая наркотическую зависимость?
Стивен Джолли, доктор медицины, Анкоридж, Аляска: Как указывает доктор Вест, это очень сложная группа пациентов.У меня 2 вопроса к доктору Веберу. Во-первых, удалось ли вам сохранить селезенку во всех этих резекциях поджелудочной железы? Во-вторых, если я правильно понял вашу презентацию, вы прооперировали 2 пациентов с нормальными ERCP. Почему это было сделано и какие операции были сделаны, и каковы были последующие наблюдения у этих пациентов?
Ричард К. Тирлби, доктор медицины, Сиэтл, Вашингтон: Доктор Вебер, результаты в семейной группе были не такими хорошими; 4 из 9, или 44%, не имели боли. Были ли у этих пациентов расширенные протоки, и, если нет, может ли им лучше подойти к резекции головы, сохраняющей поджелудочную железу Уипплу, которая, как я думаю, была предпочтительнее у взрослого населения с хроническим панкреатитом малых протоков?
Dr Weber: Что касается первого вопроса доктора Веста, то показания к сфинктеротомии были определены гастроэнтерологами.Все сфинктеротомии были выполнены во время ERCP, и это было сделано до направления пациентов. У нас не было особых осложнений после сфинктеротомии, о которых я знаю, за исключением нескольких случаев легкого панкреатита.
Не было корреляции между характером, тяжестью или продолжительностью боли и выбором операции. Двое детей прошли процедуру Пуэстоу, у обоих был наследственный панкреатит, но ни у одного из этих пациентов не произошло значительного улучшения.При контрольной ЭРХПГ оба анастомоза Пуэстоу были закрыты. 2 Пуэстоу были выполнены почти до головки поджелудочной железы, и поэтому я считаю, что они были довольно обширными.
Панкреатэктомии обычно выполнялись до верхних брыжеечных сосудов. Мы были несколько удивлены, обнаружив, что можно обнаружить признаки тяжелого поражения дистальных отделов поджелудочной железы и что головка и шейка поджелудочной железы не вовлечены серьезно. Мы склонны выбирать место для удаления поджелудочной железы на основе наших интраоперационных наблюдений.
За всеми этими пациентами наблюдают гастроэнтерологи и хирурги, но, как я уже упоминал, психиатры очень помогли, особенно в прекращении приема наркотических средств.
Доктор Джолли, мы выполнили все операции поджелудочной железы без спленэктомии. Интересны двое детей с нормальной ЭРХПГ. У них обоих был наследственный панкреатит, и они были относительно маленькими детьми. Их направили довольно рано, и я считаю, что их нормальная ЭРХПГ была связана с тем, что у них просто не было много лет повторяющихся эпизодов тяжелого панкреатита, чтобы их ЭРХПГ стала ненормальной.Однако очевидно, что у этих двух детей был хронический панкреатит, и им была сделана резекция поджелудочной железы.
Доктор Тирлби, группа наследственного панкреатита представляет собой проблему как в наших сериях, так и в литературе. У этих детей трудно достичь полной ремиссии боли, и то, что мы смогли сделать с большинством из них, — это уменьшить или устранить их зависимость от наркотиков. Я не сомневаюсь, что мне или одному из моих взрослых коллег-хирургов придется повторно оперировать некоторых из этих детей и завершить их резекцию поджелудочной железы, возможно, даже с помощью процедуры типа Уиппла.