Публикации в СМИ
Химические ожоги пищевода вызывают концентрированные щёлочи и кислоты.
Причины. Случайный или преднамеренный (с суицидальной целью) приём внутрь концентрированных кислот (уксусная эссенция, аккумуляторный электролит) или щёлочей (нашатырный спирт, каустическая сода).
Патогенез • Местное действие •• Кислоты вызывают коагуляционный некроз с образованием плотного струпа, препятствующего проникновению вещества вглубь и уменьшающего проникновение его в кровь •• Щёлочи вызывают колликвационный некроз, способствующий переносу и распространению щёлочи на подлежащие первично неповреждённые ткани • Общетоксическое действие с развитием полиорганной недостаточности (прежде всего печёночно-почечной).
Патологическая анатомия • Ожоги щёлочами характеризуются более глубоким и распространённым поражением стенки пищевода • Наиболее выраженные изменения возникают в местах физиологических сужений • Стадии ожога •• I — гиперемия и отёк слизистой оболочки •• II — некроз и изъязвление слизистой оболочки •• III — образование грануляционной ткани •• IV — рубцевание • К концу первой недели некротизированные участки отторгаются образуя изъязвления.
Клиническая картина • I стадия (острая) — 5–10 сут •• Боль в области рта, глотки, за грудиной, в эпигастральной области •• Гиперсаливация •• Дисфагия •• Шок в ближайшие часы после травмы •• Ожоговая токсемия, симптомы которой начинают превалировать через несколько часов • II стадия (мнимого благополучия) — 7–30 сут. В результате отторжения некротизированных тканей глотание становится несколько более свободным. Осложнения: •• пищеводные кровотечения •• перфорации стенки пищевода •• сепсис • III стадия (образование стриктуры) — от 2 до 6 мес, иногда годами. На стенке пищевода образуются различной протяжённости участки с вялым течением процессов заживления, раневые поверхности покрыты струпом, легко кровоточат. Дисфагия до степени полной непроходимости пищевода; ларингоспазм, кашель, удушье, обусловленные попаданием пищи в дыхательные пути.
ЛЕЧЕНИЕ
Диета.
Консервативное лечение • Наркотические анальгетики — тримеперидин, омнопон • Промывание полости рта и желудка р-рами антидотов в первые часы после попадания химического вещества в пищевод • Обильное питьё (вода, молоко) с последующим вызыванием рвоты в качестве первой помощи на месте происшествия • Обязательное раннее (в первые часы) промывание желудка (объём жидкости от 1 до 5 л в зависимости от возраста) • Интенсивная противошоковая терапия • Антигистаминные препараты с выраженным седативным действием (прометазин, хлоропирамин) • Дезинтоксикационная терапия • При развитии ОПН — экстракорпоральное очищение крови • Инфузионная терапия с форсированным диурезом, антибиотикотерапия • ГК • Рыбий жир, растительное масло внутрь • Раннее начало (2 мес после ожога) бужирования пищевода в течение 1–1,5 мес в сочетании с ГК и лидазой • В стадии образования стриктуры бужирование — основной метод лечения •• Слепое •• Полыми рентгеноконтрастными бужами по металлическому проводнику •• Под контролем эзофагоскопа •• По принципу бужирование без конца (бужирование с последовательным увеличением диаметра бужей в течение одной процедуры с использованием гастростомы — бужи проводят через ротовую полость, пищевод и гастростому) •• Ретроградное (через гастростому).
Хирургическое лечение • При сегментарных стриктурах — частичная пластика пищевода • При обширных стриктурах — тотальная пластика пищевода с предгрудинным или внутригрудинным расположением трансплантата из тонкой или толстой кишки.
Осложнения • Рубцовое сужение пищевода • Внутрисосудистый гемолиз при ожогах уксусной эссенцией • Аспирационная пневмония • Психоз • Сепсис.
МКБ-10 • T28.6 Химический ожог пищевода
| № п/п | Название МНН | | Кратность | Способ введения | Продолжительность лечения | Примечание | УД |
| Анальгетики | |||||||
| 1 | Тримеперидин или | 2% — 1 мл | через каждые 4-6 часов | в/м | 1-2 дня | наркотический анальгетик – для обезболивания в послеоперационном периоде | А |
| 2 | Трамадол или | 100 мг – 2 мл | 2-3 раза | в течение 2-3 дней | анальгетик смешанного типа действия — в послеоперационном периоде | А | |
| 3 | метомизол натрия или | 1-2 ml 50% или 2,0-5,0 мл-25% | 2-3 раза | в/в, в/м внутрь, | по мере купирования боли | ненаркотический анальгетик – для обезболивания | С |
| 4 | кетопрофен | 150 мг, 100 мг; 100–200 мг | 2-3 раза | В/м, в/в, внутрь | в течение 2-3 дней | ненаркотический анальгетик – для обезболивания | А |
| Антибиотики и антибактериальные средства | |||||||
| 5 | Цефтазидим или | 0,5–2,0 | 2-3 раза в сутки | в\м, в/в | 7-14 дней | цефалоспорины 3-го поколения | А |
| 6 | Цефтриаксон или | 0,5–1,0 каждые 12 ч. | 1-2 раза | в\м, в/в | 7-14 (зависит от течения заболевания) | цефалоспорины 3-го поколения | А |
| 7 | цефепим | 0,5–1,0 | 2-3 раза | в\м, в/в | 7–10 дней и более | цефалоспорины 4-го поколения | А |
| 8 | имипенем | 0,5-1,0 | 3-4 раза в сутки | в\м, в\в | 7-10 дней | антибиотики — карбапенемы | А |
| 9 | азитромицин | 500 мг | 1 раз в сутки | внутрь | 3 дня | антибиотики — макролиды | |
| Глюкокортикостероиды | |||||||
| 10 | преднизолон | 5-10мг | 3-6 раза в сутки | в/в , в/м | длительность и кратность устанавливается индивидуально | глюкокортикостероидный препарат поддерживающая доза | А |
| Растворы для инфузий | |||||||
| 11 | декстроза | 5%, 10% — 400- 500 мл; 40% -5-10 мл | 1 раз | в/в капельно | в зависимости от показания | раствор для инфузий, при гипогликемии, гиповолемии, интоксикации, дегидратации | А |
| Гипогликемические средства | |||||||
| 12 | инсулин | 4-8 ЕД | по показаниям | п\к | в зависимости от введения декстрозы | гормоны поджелудочной железы | А |
| Плазмозамещающие средства | |||||||
| 13 | декстран | 400-1200 мл | 1 раз | в/в капельно | по показаниям | заменители плазмы | В |
| Адреномиметики | |||||||
| 14 | эпинефрин | 200 мкг-1 мг | при неотложных состояниях | п/к, реже в/в, в/м | однократно | адреномиметик | А |
| средства для коррекции КЩС | |||||||
| 15 | гидрокарбонат натрия | 0,5–1 г | 1-2 раза | в/в | по показаниям в зависимости от КОС крови | средства для коррекции КЩС | В |
| Мочегонные средства | |||||||
| 16 | фуросемид | 20- 80 мг | 1-2 раза в сутки | в/в, внутрь | по показаниям | диуретик | А |
| Антисекреторные средства | |||||||
| 17 | Фамотидин или | 20-40 мг | 2 раз в сутки или на ночь | Внутрь | 4–8 нед | антисекреторный препарат – блокатор гистаминовых рецепторов | А |
| 18 | Ранитидин или | По 0,15 | 2 раза в день | внутрь | в течение 7-30 дней | антисекреторный препарат – блокатор гистаминовых рецепторов | А |
| 19 | омепразол | 20мг | 1 раз в день | внутрь | в течение 7-30 дней | антисекреторный препарат — ингибитор протонной помпы | А |
| Гемостатики | |||||||
| 20 | этамзилат | 2–4 мл -12,5% | 1-4 раза в сутки | в/в в/м | по показаниям | коагулянты, гемостатики | В |
| Витаминные препараты | |||||||
| 21 | тиамина хлорид | 1мл- 5% раствора | 1 раз в день | в/м | 10-30 инъекций | водорастворимые витамины | С |
| 22 | токоферола ацетат | 50-100 мг | 1 раз в день | внутрь и в/в | в течение 1 месяца | водорастворимые витамины | С |
| 23 | аскорбиновая кислота | 1,0- 10 % | 3-5 раза в день | в/в в/м | 2-3 нед.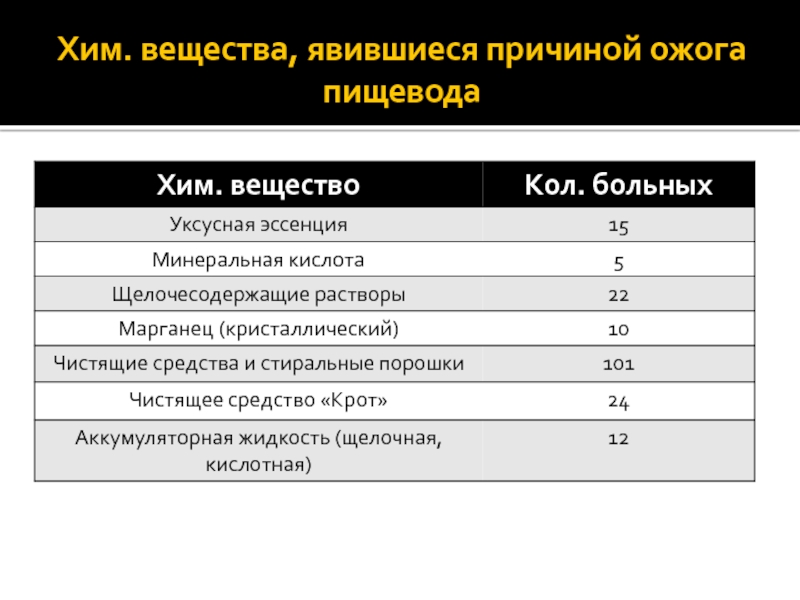 | водорастворимые витамины | С |
| 24 | пиридоксин | 50-150 мг | 1-2 раза в день | в/в в/м | 1-2 мес. | водорастворимые витамины | С |
| 25 | цианкобаламин | 100-300мкг | 2-3 раза в нед. | П\к, в/в и в/м | 10-20 инъекций | водорастворимые витамины | С |
| Гепатопротекторы | |||||||
| 26 | адеметионин | 400-800 мг | 1 раз в день | в/м в/в, внутрь | 2-4 нед. | гепатопротектор | С |
| Антигипоксанты, антиоксиданты | |||||||
| 27 | солкосерил | 1-2 амп. | 1 раз | в/в и в/м | 4-8 нед. | антигипоксанты, антиоксиданты | С |
| Антидоты | |||||||
| 28 | тетацин-кальций | 20,0-10%— | 1-2 раза | в/в | 3-4 дня | дезинтоксикационные, комплексообразующие средства | В |
| Средства для парентерального питания | |||||||
| 29 | альбумин | 10%-200 мл, 20%-100,0 мл. | Доза и концентрация зависит от уровня альбумина в крови. | в/в капельно | по показаниям | Средства для парентерального питания — для коррекции гипопротеинемии | В |
| Препараты компонентов крови | |||||||
| 30 | эритроцитная взвесь лейкофильтрованная, 350 мл | По показаниям | 1-2 раза | в/в капельно | по показаниям | Препараты компонентов крови — для коррекции анемии | А |
| 31 | свежезамороженная плазма | 220 мл | 1-2 раза | в/в капельно | по показаниям | Препараты компонентов крови-для коррекции коагулопатии | А |
T20-T32 Термические и химические ожоги
T20 Термические и химические ожоги головы и шеи
- T20.
 0 Термический ожог головы и шеи неуточненной степени
0 Термический ожог головы и шеи неуточненной степени - T20.1 Термический ожог головы и шеи первой степени
- T20.2 Термический ожог головы и шеи второй степени
- T20.3 Термический ожог головы и шеи третьей степени
- T20.4 Химический ожог головы и шеи неуточненной степени
- T20.5 Химический ожог головы и шеи первой степени
- T20.6 Химический ожог головы и шеи второй степени
- T20.7 Химический ожог головы и шеи третьей степени
T21 Термические и химические ожоги туловища
- T21.0 Термический ожог туловища неуточненной степени
- T21.1 Термический ожог туловища первой степени
- T21.2 Термический ожог туловища второй степени
- T21.3 Термический ожог туловища третьей степени
- T21.4 Химический ожог туловища неуточненной степени
- T21.
 5 Химический ожог туловища первой степени
5 Химический ожог туловища первой степени - T21.6 Химический ожог туловища второй степени
- T21.7 Химический ожог туловища третьей степени
T22 Термические и химические ожоги области плечевого пояса и верхней конечности, исключая запястье и кисть
- T22.0 Термический ожог области плечевого пояса и верхней конечности, исключая запястье и кисть, неуточненной степени
- T22.1 Термический ожог области плечевого пояса и верхней конечности, исключая запястье и кисть, первой степени
- T22.2 Термический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, второй степени
- T22.3 Термический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, третьей степени
- T22.4 Химический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, неуточненной степени
- T22.
 5 Химический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, первой степени
5 Химический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, первой степени - T22.6 Химический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, второй степени
- T22.7 Химический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, третьей степени
T23 Термические и химические ожоги запястья и кисти
- T23.0 Термический ожог запястья и кисти неуточненной степени
- T23.1 Термический ожог запястья и кисти первой степени
- T23.2 Термический ожог запястья и кисти второй степени
- T23.3 Термический ожог запястья и кисти третьей степени
- T23.4 Химический ожог запястья и кисти неуточненной степени
- T23.5 Химический ожог запястья и кисти первой степени
- T23.6 Химический ожог запястья и кисти второй степени
- T23.
 7 Химический ожог запястья и кисти третьей степени
7 Химический ожог запястья и кисти третьей степени
T24 Термические и химические ожоги тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, неуточненной степени
- T24.0 Термический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, неуточненной степени
- T24.1 Термический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, первой степени
- T24.2 Термический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, второй степени
- T24.3 Термический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, третьей степени
- T24.4 Химический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, неуточненной степени
- T24.5 Химический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, первой степени
- T24.
 6 Химический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, второй степени
6 Химический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, второй степени - T24.7 Химический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, третьей степени
T25 Термические и химические ожоги области голеностопного сустава и стопы
- T25.0 Термический ожог области голеностопного сустава и стопы неуточненной степени
- T25.1 Термический ожог области голеностопного сустава и стопы первой степени
- T25.2 Термический ожог области голеностопного сустава и стопы второй степени
- T25.3 Термический ожог области голеностопного сустава и стопы третьей степени
- T25.4 Химический ожог области голеностопного сустава и стопы неуточненной степени
- T25.5 Химический ожог области голеностопного сустава и стопы первой степени
- T25.6 Химический ожог области голеностопного сустава и стопы второй степени
- T25.
 7 Химический ожог области голеностопного сустава и стопы третьей степени
7 Химический ожог области голеностопного сустава и стопы третьей степени
T26 Термические и химические ожоги, ограниченные областью глаза и его придаточного аппарата
- T26.0 Термический ожог века и окологлазничной области
- T26.1 Термический ожог роговицы и конъюктивального мешка
- T26.2 Термический ожог, ведущий к разрыву и разрушению глазного яблока
- T26.3 Термический ожог других частей глаза и его придаточного аппарата
- T26.4 Термический ожог глаза и его придаточного аппарата неуточненной локализации
- T26.5 Химический ожог века и окологлазничной области
- T26.6 Химический ожог роговицы и конъюктивального мешка
- T26.7 Химический ожог, ведущий к разрыву и разрушению глазного яблока
- T26.8 Химический ожог других частей глаза и его придаточного аппарата
- T26.9 Химический ожог глаза и его придаточного аппарата неуточненной локализации
T27 Термические и химические ожоги дыхательных путей
- T27.
 0 Термический ожог гортани и трахеи
0 Термический ожог гортани и трахеи - T27.1 Термический ожог гортани, трахеи и легкого
- T27.2 Термический ожог других отделов дыхательных путей
- T27.3 Термический ожог дыхательных путей неуточненной локализации
- T27.4 Химический ожог гортани и трахеи
- T27.5 Химический ожог гортани, трахеи и легкого
- T27.6 Химический ожог других отделов дыхательных путей
- T27.7 Химический ожог дыхательных путей неуточненной локализации
T28 Термические и химические ожоги других внутренних органов
- T28.0 Термический ожог рта и глотки
- T28.1 Термический ожог пищевода
- T28.2 Термический ожог других отделов пищеварительного тракта
- T28.3 Термический ожог внутренних мочеполовых органов
- T28.4 Термический ожог других и неуточненных внутренних органов
- T28.
 5 Химический ожог рта и глотки
5 Химический ожог рта и глотки - T28.6 Химический ожог пищевода
- T28.7 Химический ожог других отделов пищеварительного тракта
- T28.8 Химический ожог внутренних мочеполовых органов
- T28.9 Химический ожог других и неуточненных внутренних органов
T29 Термические и химические ожоги нескольких областей тела
- T29.0 Термические ожоги нескольких областей тела неуточненной степени
- T29.1 Термические ожоги нескольких областей тела с указанием на не более чем первую степень ожогов
- T29.2 Термические ожоги нескольких областей тела с указанием на не более чем на вторую степень ожогов
- T29.3 Термические ожоги нескольких областей тела с указанием хотя бы на один ожог третьей степени
- T29.4 Химические ожоги нескольких областей тела неуточненной степени
- T29.5 Химические ожоги нескольких областей тела с указанием на не более чем первую степень химических ожогов
- T29.
 6 Химические ожоги нескольких областей тела с указанием на не более чем вторую степень химических ожогов
6 Химические ожоги нескольких областей тела с указанием на не более чем вторую степень химических ожогов - T29.7 Химические ожоги нескольких областей тела с указанием хотя бы на один химический ожог третьей степени
T30 Термические и химические ожоги неуточненной локализации
- T30.0 Термический ожог неуточненной степени неуточненной локализации
- T30.1 Термический ожог первой степени неуточненной локализации
- T30.2 Термический ожог второй степени неуточненной локализации
- T30.3 Термический ожог третьей степени неуточненной локализации
- T30.4 Химический ожог неуточненной степени неуточненной локализации
- T30.5 Химический ожог первой степени неуточненной локализации
- T30.6 Химический ожог второй степени неуточненной локализации
- T30.7 Химический ожог третьей степени неуточненной локализации
T31 Термические ожоги, классифицированные в зависимости от площади пораженной поверхности тела
- T31.
 0 Термический ожог менее 10% поверхности тела
0 Термический ожог менее 10% поверхности тела - T31.1 Термический ожог 10-19% поверхности тела
- T31.2 Термический ожог 20-29% поверхности тела
- T31.3 Термический ожог 30-39% поверхности тела
- T31.4 Термический ожог 40-49% поверхности тела
- T31.5 Термический ожог 50-59% поверхности тела
- T31.6 Термический ожог 60-69% поверхности тела
- T31.7 Термический ожог 70-79% поверхности тела
- T31.8 Термический ожог 80-89% поверхности тела
- T31.9 Термический ожог 90% поверхности тела или более
T32 Химические ожоги, классифицированные в зависимости от площади пораженной поверхности тела
- T32.0 Химический ожог менее 10% поверхности тела
- T32.1 Химический ожог 10-19% поверхности тела
- T32.2 Химический ожог 20-29% поверхности тела
- T32.
 3 Химический ожог 30-39% поверхности тела
3 Химический ожог 30-39% поверхности тела - T32.4 Химический ожог 40-49% поверхности тела
- T32.5 Химический ожог 50-59% поверхности тела
- T32.6 Химический ожог 60-69% поверхности тела
- T32.7 Химический ожог 70-79% поверхности тела
- T32.8 Химический ожог 80-89% поверхности тела
- T32.9 Химический ожог 90% поверхности тела и более
Первая помощь при химических ожогах
Обзор темы
Примечание : Если было проглочено химическое вещество , которое может быть ядом или вызвать жжение в горле и пищеводе, позвоните в местный центр по борьбе с отравлениями или на горячую линию по национальным отравлениям (1-800-222-1222 ) сразу за информацией по обращению. Когда вы звоните в Центр по борьбе с отравлениями, возьмите с собой контейнер с химическим веществом, чтобы вы могли прочитать этикетку с содержимым сотруднику по борьбе с отравлениями. Центр борьбы с отравлениями может помочь определить, что делать дальше.
Центр борьбы с отравлениями может помочь определить, что делать дальше.
Большинство химических ожогов кожи сначала лечат смыванием химического вещества с тела большим количеством воды комнатной температуры, но не все химические вещества обрабатываются таким образом. Важно правильно лечить ожог, чтобы избежать дальнейших осложнений.
Химические ожоги промыть водой
- Промыть место не менее 20 минут.
- Не используйте сильную струю воды, так как это может повредить место ожога.
- Попросите человека с ожогом удалить химическое вещество, если он или она может.
- Наденьте перчатки, чтобы защитить себя от химического вещества, если вам нужно его удалить.
- Во время промывки зоны снимите всю одежду или украшения, на которых есть это химическое вещество.
- Если по прошествии 20 минут ощущение жжения не исчезнет, снова промойте пораженный участок проточной водой в течение 10–15 минут.
Плавиковая кислота промывается большим количеством воды и обрабатывается глюконатом кальция. Вам нужна немедленная медицинская помощь.
Вам нужна немедленная медицинская помощь.
Химические ожоги без промывки водой
Некоторые химические ожоги усугубляются, если промыть (промыть) водой.
- Карболовая кислота или фенол не смешивается с водой, поэтому сначала используйте изопропиловый (медицинский) спирт, чтобы смыть химическое вещество с кожи, а затем промойте водой. Если спирт недоступен, промойте большим количеством воды. Не промывайте глаза спиртом.
- Серная кислота промывают мягким мыльным раствором, если ожоги не тяжелые.При добавлении воды к кислоте серная кислота становится горячей, но лучше промыть пораженный участок и не оставлять кислоту на коже.
- Сухие порошки , такие как сухая известь, сначала удаляются щеткой, потому что добавление воды может привести к образованию горящей жидкости. Смахнув порошок, смойте его водой в течение 20 минут.
- Металлические соединения покрыты минеральным маслом.
Самая важная первая помощь при попадании химического вещества в глаза — это немедленно промыть вещество большим количеством воды, чтобы снизить вероятность серьезного повреждения глаз.Информацию о химическом ожоге глаз см. В разделе «Ожоги глаза».
Если необходимо обследование у врача, возьмите с собой контейнер с химическим веществом.
Кредиты
Текущий по состоянию на: 26 февраля 2020 г.
Автор: Healthwise Staff
Медицинский обзор:
Уильям Х. Блахд-младший, доктор медицины, FACEP — неотложная медицина
Адам Хусни, доктор медицины, семейная медицина
Кэтлин Ромито, доктор медицины — семейная медицина
H.Майкл О’Коннор, врач неотложной помощи
Мартин Дж. Габика, доктор медицины, семейная медицина
По состоянию на 26 февраля 2020 г.
Автор: Здоровый персонал
Медицинский обзор: Уильям Х. Блахд младший, доктор медицины, FACEP — неотложная медицина и Адам Хусни, доктор медицины — семейная медицина, и Кэтлин Ромито, доктор медицины — семейная медицина, и доктор Х. Майкл О’Коннор — неотложная медицина и Мартин Дж. Габика, доктор медицины — семья Медицина
Особые роли в патофизиологических условиях
% PDF-1.4 % 1 0 объект > эндобдж 5 0 объект > поток Acrobat Distiller 10.0.0 (Windows) doi: 10.1124 / pr.120.019331application / pdf
Раков | Бесплатный полнотекстовый | Роль TRAIL / DR в модуляции иммунных клеток и ответов
2.1.1. Нейтрофилы
Нейтрофилы крови человека конститутивно экспрессируют мРНК TRAIL [11,12,13]. Однако то, сколько TRAIL может быть обнаружено на поверхности клетки, если оно вообще есть, по-видимому, зависит от донора [11,12,13]. Было высказано предположение, что TRAIL скорее предварительно хранится внутриклеточно в гранулах [14,15,16] и что часть этого предварительно сохраненного TRAIL находится в расщепленной растворимой форме, которая может способствовать секреции [14,16].Действительно, после активации нейтрофилы человека активируют TRAIL и секретируют функциональный растворимый TRAIL. Это наиболее эффективно наблюдалось с IFNα и IFNβ [14,15,17,18], но также, в меньшей степени [13], с IFNγ [11,13,15]. Несколько других провоспалительных стимулов, таких как fMLP, IL-8, Hsp96 [15]; Ил-17 [19]; CD184-лиганд SDF1 [20]; и TLR2-лиганд Pam3C [14]; было показано, что они усиливают высвобождение TRAIL нейтрофилами человека. Напротив, не сообщалось о влиянии на экспрессию TRAIL нейтрофилов человека для IL-1, G-CSF, GM-CSF, TGFβ и TLR3-лиганда Poly I: C [11,13,14,17].Противоречивые данные были получены для TNF и TLR4-лиганда LPS, при этом в некоторых сообщениях было обнаружено усиление TRAIL на нейтрофилы [14,15,18], отсутствие эффекта [13,17] или даже подавление TRAIL [11]. ]. У мышей TRAIL не экспрессируется нейтрофилами [21,22], но может усиливаться после стимуляции IFNβ [23]. Интересно, что стимуляция нейтрофилов мыши с помощью IL-6 и G-CSF индуцировала опухолевый фенотип N2, характеризующийся подавлением TRAIL [24,25], но экспрессию TRAIL можно было восстановить с помощью IFNγ или TNF [26].В большинстве исследований сообщается об экспрессии DR5 [11,12,17,20] и DcR1 [11,12,20,27,28,29] на нейтрофилах человека, и только два отчета показывают экспрессию DR4 и DcR2 [20,29]. Важно отметить, что экспрессия DR4 / DR5 на нейтрофилах имеет тенденцию быть ниже, чем экспрессия рецепторов-ловушек DcR1 / DcR2 [11,12,17,28,29]. Активация нейтрофилов человека TNF или SDF1 [11,20] или нейтрофилов мыши IFNβ [23] увеличивала экспрессию DR4 / DR5. Напротив, стимуляция TNF [11] или стресс ER [30] подавляет DcR1 / DcR2 на нейтрофилах человека.У мышей экспрессия DR5 наблюдалась на нейтрофилах [28,31,32,33], но DcR1 и DcR2 не были обнаружены в одном исследовании, в котором проверялась их экспрессия [34]. В соответствии с экспрессией рецепторов смерти, большинство [20,23,28,29], но не все [17] исследования показали, что свежевыделенные нейтрофилы не чувствительны к TRAIL-индуцированному апоптозу. Однако нейтрофилы стали чувствительными после активации [11,20,23,29] или после старения [12,20]. Интересно, что при таком старении стареющие нейтрофилы активировали CD184 / CXCR4 [35] и становились восприимчивыми к SDF1, что увеличивало чувствительность к TRAIL, посредством активации DR4 и DR5 [20].Это способствовало миграции стареющих нейтрофилов в костный мозг для удаления апоптоза на модели мышей [20]. Функционально большинство сообщений соответствует интерпретации, согласно которой активность TRAIL / DR участвует в апоптотическом удалении активированных, подвергнутых стрессу, или старые нейтрофилы in vivo. Поскольку нейтрофилы являются основными движущими силами воспаления [36,37,38], их устранение обычно ограничивает воспаление и связанное с ним повреждение тканей и способствует разрешению воспаления. Таким образом, мыши с дефицитом TRAIL демонстрировали сниженный апоптоз нейтрофилов, что приводило к увеличению числа нейтрофилов и воспалению.Это было отмечено при сепсисе, индуцированном TLR-лигандами [39], в модели фиброза легких с блеомицином [21] и после инфицирования ЦНС Streptococcus pneumoniae [31]. Следовательно, введение растворимых TRAIL или агонистических αDR5-антител увеличивало апоптоз нейтрофилов, что приводило к уменьшению воспаления после инфекции Streptococcus pneumoniae [31] и во время сепсиса, вызванного бактериями [32,34] или TLR-лигандами [39]. В других системах также наблюдалось, что блокирование апоптоза нейтрофилов усиливает воспаление и повреждение тканей [40].Однако TRAIL-чувствительность активированных нейтрофилов не наблюдалась на всех моделях, поскольку, например, после инфицирования S. pneumoniae апоптоза нейтрофилов в легких отсутствие TRAIL не влияло [41]. Сами нейтрофилы человека могут опосредовать цитотоксичность TRAIL-чувствительных опухолей [13,14,17,42,43]. Однако полученные из крови нейтрофилы человека некоторых пациентов с опухолями (плоскоклеточная карцинома [44]; B-клеточный хронический лимфоцитарный лейкоз [45]) экспрессировали меньше TRAIL, чем здоровые доноры, и IFNα-терапия in vivo усиливала экспрессию TRAIL на нейтрофилах хронического миелоидного лейкоза ( ХМЛ) [18].Помимо цитотоксичности опухоли, TRAIL, полученный из нейтрофилов, также участвует в разрешении воспалений, воздействуя на макрофаги. TRAIL, полученный из нейтрофилов, может вызывать апоптоз альвеолярных и легочных макрофагов у мышей, инфицированных S. pneumoniae [41]. Этот апоптоз макрофагов, инфицированных S. pneumoniae, поддерживал бактериальный клиренс в дыхательных путях и ограничивал воспаление и последующее повреждение тканей [41].2.1.2. Моноциты и макрофаги
Свежеочищенные моноциты крови человека имеют базальный уровень внутриклеточной экспрессии TRAIL [11,46].Были получены противоречивые данные о поверхностной экспрессии TRAIL на моноцитах крови человека; с двумя исследованиями, сообщающими об отсутствии TRAIL-экспрессии [46,47] и двумя исследованиями, показывающими экспрессию [11,48]. Созданные in vitro макрофаги, происходящие из моноцитов человека, экспрессируют высокие уровни TRAIL внутриклеточно, но низкие уровни на поверхности [48]. Экспрессия TRAIL может быть быстро индуцирована в моноцитах человека с помощью IFNα [47,49,50,51,52] и IFNβ [53]. Кроме того, сообщалось о секреции растворимого TRAIL после стимуляции IFNα моноцитами человека [17].Кроме того, введение IFNα-индуктора БЦЖ в мочевой пузырь больных раком мочевого пузыря приводило к увеличению экспрессии TRAIL на опухолевых макрофагах [54]. При обработке моноцитов крови человека ЛПС повышенная поверхностная экспрессия TRAIL была обнаружена после 24 ч инкубации [48], но не через 12 ч [47]. Кроме того, PEDF, антиангиогенный и противовоспалительный агент, широко используемый в клинических испытаниях для лечения рака [55], индуцирует продукцию TRAIL макрофагами, происходящими из моноцитов человека [56].Напротив, воздействие на человеческие моноциты CD14 + С-реактивного белка (CRP) привело к подавлению TRAIL [57]. У мышей ок. 25% перитонеальных макрофагов экспрессируют TRAIL [58]. TLR2 (липотейхоевая кислота), TLR3 (поли I: C) и TLR4 (LPS) лиганды, но не лиганд TLR9 (CpG), индуцировали экспрессию TRAIL в макрофагах мыши [59]. Более того, макрофаги, происходящие из костного мозга мышей (BMDM), обработанные PEDF in vitro, или макрофаги, инфильтрирующие опухоль от мышей, обработанных PEDF, повышали экспрессию TRAIL [56].Химически индуцированный стресс ER также привел к усилению регуляции растворимого TRAIL в линии моноцитарных клеток мыши и в первичных перитонеальных макрофагах мыши [60]. Периферические моноциты человека и полученные из моноцитов макрофаги экспрессируют функциональные DR4 и DR5, причем DR5 обычно экспрессируется выше, чем DR4 [60]. 28,47]. Напротив, резидентные в ткани макрофаги имеют очень низкую экспрессию DR5 [28]. Хотя одно исследование продемонстрировало поверхностную экспрессию DcR1 в периферических моноцитах человека [47], в других исследованиях сообщалось, что рецепторы-ловушки практически не экспрессируются моноцитами [28,52].Макрофаги, как правило, экспрессируют более высокий уровень DcR1 по сравнению с моноцитами [28]. Однако макрофаги неоднородны, и несколько субпопуляций проявляют разную функциональную активность. Макрофаги могут дифференцироваться на два основных типа в присутствии определенных факторов поляризации при рекрутировании в периферические ткани [61]. Провоспалительные сигналы, такие как лечение LPS и IFNγ, поляризуют макрофаги в направлении M1 или классически активированных макрофагов, которые являются цитотоксическими, провоспалительными и эффективными в борьбе с опухолями и патогенами.Напротив, противовоспалительные цитокины, такие как IL-4, IL-10 и IL-13, индуцируют M2 или, альтернативно, активированные макрофаги, которые играют роль в подавлении иммунитета, стимулировании опухоли, ангиогенезе и ремоделировании тканей [61]. Рецепторы смерти по-разному экспрессируются на макрофагах типа M1 и M2. M2-подобные опухоль-ассоциированные макрофаги (TAM) и M2-поляризованные макрофаги THP-1 экспрессируют больше DR5, чем макрофаги M1 [28,62,63]. Соответственно, агенты, которые поддерживают поляризацию M2, усиливают экспрессию DR4 и DR5 на человеческих моноцитах и макрофагах, происходящих из моноцитов [28].Кроме того, медиаторы воспаления, такие как IFNγ [47] и IFNα [52], могут подавлять поверхностную экспрессию DR5 на моноцитах крови человека. Напротив, в одном исследовании сообщается, что LPS увеличивает экспрессию DR4 на моноцитах человека [64]. Более того, макрофаги M1 в синовиальной оболочке пациентов с ревматоидным артритом экспрессируют более высокие уровни DR5, чем макрофаги M2 [65]. У мышей моноциты и макрофаги экспрессируют DR5 конститутивно [28,62,65,66,67,68], и его экспрессия может быть усилена ДНК-связывающим трабектином [62].Периферические моноциты человека чувствительны к TRAIL-индуцированному апоптозу с 50% снижением их выживаемости через 72 часа после обработки TRAIL in vitro [28]. Кроме того, предварительное лечение противовоспалительными цитокинами IL-4 или IL-10, по-видимому, повышало чувствительность моноцитов к TRAIL-опосредованной гибели клеток [28,69]. TRAIL также индуцировал апоптоз в клеточной линии макрофагов человека U937 [70] и в перитонеальных макрофагах мыши [71]. Макрофаги M2 более чувствительны к TRAIL-индуцированному апоптозу, чем макрофаги M1 из-за их более высокой поверхностной экспрессии DR5 [28] и из-за повышенного O-гликозилирования DR5, которое усиливает олигомеризацию рецепторов [63].О чувствительности моноцитов и макрофагов к TRAIL-опосредованному апоптозу также сообщалось на моделях болезней. На модели опухоли мышей было показано, что обработка TRAIL in vivo подавляет рост опухоли за счет устранения моноцитов и M2-подобных ТАМ в опухоли [28,62]. В модели атеросклероза на мышах ApoE — / — обработка TRAIL in vivo избирательно индуцировала апоптоз в инфильтрирующих сосуды воспалительных макрофагах [66,67]. Это может быть связано с активацией DR5 в сосудистых макрофагах за счет ER стресса на поздних стадиях атерогенеза [72].В целом активированные макрофаги чувствительны к TRAIL-индуцированному апоптозу, и это имеет решающее значение для регуляции гомеостаза [58,71]. Помимо индукции апоптоза, TRAIL-опосредованные сигналы могут сделать моноциты и макрофаги также противоопухолевыми [17,47,50,52,53,73]. Помимо апоптотических эффектов, взаимодействие TRAIL / DR может также воздействовать на моноциты и макрофаги другими способами. Например, обработка TRAIL может усиливать созревание моноцитов первичных гематопоэтических стволовых клеток человека CD34 + , не вызывая какой-либо цитотоксичности [74].Более того, TRAIL-опосредованный запуск DR4 может индуцировать миграцию моноцитов THP-1 и LPS-активируемых первичных моноцитов человека [64]. Более того, обработка растворимым TRAIL индуцировала экспрессию провоспалительных цитокинов в макрофагах, происходящих из моноцитов человека, и в перитонеальных макрофагах мыши [75]. Аналогичным образом, у голых мышей, зараженных опухолью, которым вводили растворимый TRAIL, сообщалось, что ТАМ демонстрируют повышенную экспрессию провоспалительных цитокинов [75]. В отличие от этих провоспалительных эффектов TRAIL, одно исследование показало противовоспалительную роль.На модели мышей с колоректальным раком, ассоциированным с колитом (CAC), раннее лечение TRAIL in vivo защищало мышей за счет уменьшения воспаления, вероятно, за счет снижения уровней инфильтрирующих макрофагов и провоспалительных цитокинов и увеличения процента макрофагов M2 [76 ]. Кроме того, после стимуляции LPS и TRAIL in vitro линия макрофагов мыши RAW264.7 показала снижение экспрессии iNOS, IL-6 и TNF по сравнению с одним LPS [76].2.1.3. Дендритные клетки
Дендритные клетки (ДК) человека, выделенные из крови или полученные из моноцитов, не экспрессировали поверхностный TRAIL в большинстве [47,49,77,78,79,80], но не во всех [46,81] исследованиях.Однако TRAIL может быть обнаружен внутриклеточно [46,77,78,79,80] и в супернатанте культуры [79]. Подобно нейтрофилам, активация DC с помощью IFNα [49,77,82,83,84,85,86,87,88] или IFNβ [77,81,85] увеличивает уровни мембраносвязанного и растворимого TRAIL. Известные индукторы IFNα / IFNβ, такие как TLR-лиганды [77,84,88,89,90] и вирусные частицы [85,88,91,92,93], также индуцируют экспрессию / секрецию TRAIL человеческими DC. Противоречивые результаты, полученные с LPS, могут быть связаны со сроками, поскольку индукция TRAIL наблюдалась не через 12 часов [49,81], а через 1-2 дня [82,90] инкубации.Также существуют разногласия относительно влияния IFNγ на экспрессию TRAIL на человеческих DC [49,85]. Интересно, что было высказано предположение, что лигирование CD40 [77] или действие регуляторных Т-клеток (Tregs) [94] может ингибировать повышающую регуляцию TRAIL на стимулированных DC человека. Как и у людей, у мышей было обнаружено, что TRAIL активируется на DC мыши с помощью IFNα и IFNβ прямо [86] или опосредованно [94,95,96]. Кроме того, было высказано предположение, что IL-15 является индуктором экспрессии TRAIL на ДК мыши [97,98]. За исключением одного сообщения, показывающего слабое окрашивание на поверхностный DR5 [90], в большинстве исследований не обнаружено поверхностной экспрессии DR4 / DR5 [46,90,99,100] или DcR1 / DcR2 [90,100] на DC человека.Однако DR4 и DR5 могут быть обнаружены с помощью мРНК [82,99] и внутриклеточного окрашивания [46]. Поверхностная экспрессия DR4 и DR5 повышалась после 2 дней стимуляции LPS in vitro [82]. Однако в другом исследовании инкубация с LPS в течение 20 часов привела к другому результату: DR4 не изменился, а DR5 подавлялся [90]. В мышиной системе сообщалось о поверхностной экспрессии DR5 для происходящих из костного мозга DCs [101]. Удивительно, но мало что известно о чувствительности DC к TRAIL-индуцированному апоптозу.Два исследования, одно на человеческих ДК из моноцитов [90] и одно на ДК из костного мозга мыши [101], предполагают, что стимулированные ДК менее чувствительны к TRAIL-индуцированному апоптозу, чем незрелые ДК. Напротив, многие исследования продемонстрировали, что человеческие DC могут проявлять TRAIL-зависимую цитотоксическую активность против различных опухолевых клеток. Об этом сообщалось для нестимулированных ДК [46,102], для ДК, полученных из моноцитов, стимулированных IFNα / β [49,77,81,82,83,87,92,103,104], для пДК [78,79] и для ДК, стимулированных TLR- лиганды [77,84,88] или вирусные частицы [85,88,91,93,105].Подобные наблюдения были сделаны в системе мышей [86,95,96,98]. Интересно, что два исследования подтверждают, что взаимодействие TRAIL / DR также может оказывать прямое влияние на TRAIL + DCs независимым от апоптоза образом, хотя они конфликтуют по своему значению. Для ДК, происходящих из моноцитов человека, стимулированных ЛПС, TRAIL действовал как костимуляторная молекула, поскольку блокирование TRAIL снижало повышающую регуляцию маркеров активации и продукцию цитокинов ДК [90]. Напротив, в исследовании на мышах вовлечение DR5 в ДК мыши нарушало антигенпредставляющие функции ДК, что приводило к снижению праймирования Т-клеток CD4 + и CD8 + [106].Химические повреждения пищевода: этиопатологические проблемы в Нигерии | Journal of Cardiothoracic Surgery
Химические повреждения пищевода вызваны проглатыванием коррозионных веществ, таких как кислоты, щелочи и некоторые нейтральные вещества. Другие причины эзофагита включают аутоиммунные заболевания, инфекции, радиацию и гастроэзофагеальную рефлюксную болезнь (ГЭРБ) [1–13].
Проглатывание разъедающих веществ вызывает травмы ротоглотки и желудочно-пищеводного тракта, от легких ожогов до тяжелого некроза, в зависимости от агента, количества проглоченного вещества, концентрации и продолжительности воздействия.Это может привести к коррозионным стриктурам пищевода [2].
Различные аспекты коррозионных стриктур пищевода были изучены во всем мире. В отчете Ajao, OG и Solanke, TF [3] из Ибадана, на юго-западе Нигерии, сделан вывод о том, что наиболее частой причиной доброкачественной стриктуры пищевода является прием внутрь разъедающих веществ.
Кислоты имеют тенденцию обжигать ротовую полость, глотку или гортань в верхнем конце, а привратник часто повреждается при обильном приеме кислот. Попытка выплюнуть кислоту может привести к появлению контрольных признаков на коже груди.
Щелочи имеют свойство поражать тело пищевода, особенно в местах естественных сужений. Порошкообразные вещества, такие как карбид кальция, с трудом скользят по пищеводу, поэтому они, как правило, вызывают локальные повреждения, которые часто приводят к перфорации.
Патология повреждений пищевода широко изучалась на животных и людях. Для описания патология делится на острую и хроническую фазы.
Острая фаза
Важно отметить, что даже несмотря на то, что острая воспалительная реакция обнаруживается в острой фазе, независимо от возбудителя [6].В моделях на животных большинство авторов соглашаются с присутствием внутриэпителиальных сегментированных лейкоцитов, субэпителиальных лейкоцитов, гиперплазии базальных клеток и язв в зависимости от глубины поражения стенок. В тяжелых случаях перфорация стенки может привести к медиастиниту.
Эта гистологическая картина является основой для принятия классификации повреждений тощей кишки Дэмерона и Вангенстина [6] для оценки повреждений пищевода, как показано ниже.
Оценка 1 для некроза, ограниченного слизистой оболочкой.Вовлечение подслизистых оболочек оценивается в 2 балла; вовлечение собственной мышечной мышцы, адвентиции или прямой перфорации оценивается в 3, 4 и 5 баллов соответственно.
Система балльной оценки пептического повреждения пищевода существенно отличается. Классификация гастроэзофагеальной рефлюксной болезни (ГЭРБ) следующая:
Степень I: неспецифический эзофагит. Помимо нейтрофильной инфильтрации, биопсия показывает гиперплазию базальных слоев.
Степень II: разрушение слизистой оболочки и явное изъязвление.
Степень III: Степень II плюс попытки заживления (отложение грануляционной ткани).
Степень IV: стриктура пищевода, вызванная рефлюксом.
Степень IV также может быть связана с миграцией чешуйчато-столбчатого сочленения в головку или предшествовать ей, при этом диагностируется состояние пищевода Барретта.Это предзлокачественное поражение.
Поздняя фаза
Это фаза установленной стриктуры. Он развивается, когда острая фаза не лечится должным образом [6].
Происходит прогрессирующее рубцевание пораженного сегмента пищевода, приводящее к образованию стриктуры. У живого человека контрастная эзофагограмма и эзофагоскопия покажут количество, длину и калибр стриктуры (ов).
В 14-летнем обзоре, проведенном Osinowo O и Alonge T [4] в Ибадане, Юго-Западная Нигерия, коррозионные стриктуры составили 17.4% показаний к замене пищевода среди 47 обследованных пациентов.
Для хирургических целей стриктуры целесообразно классифицировать как расширяемые и нерасширяемые. Дилатируемые стриктуры представляют собой одиночные короткие сегментные стриктуры (<2,5 см) с остаточным просветом, через который можно пройти через расширители бужей.
Нерасширяющиеся стриктуры — это стриктуры нескольких или длинных сегментов.
Полная потеря просвета попадает в эту категорию независимо от длины.

 0 Термический ожог головы и шеи неуточненной степени
0 Термический ожог головы и шеи неуточненной степени 5 Химический ожог туловища первой степени
5 Химический ожог туловища первой степени 5 Химический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, первой степени
5 Химический ожог области плечевого пояса и верхней конечности, за исключением запястья и кисти, первой степени 7 Химический ожог запястья и кисти третьей степени
7 Химический ожог запястья и кисти третьей степени 6 Химический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, второй степени
6 Химический ожог тазобедренного сустава и нижней конечности, исключая голеностопный сустав и стопу, второй степени 7 Химический ожог области голеностопного сустава и стопы третьей степени
7 Химический ожог области голеностопного сустава и стопы третьей степени 0 Термический ожог гортани и трахеи
0 Термический ожог гортани и трахеи 5 Химический ожог рта и глотки
5 Химический ожог рта и глотки 6 Химические ожоги нескольких областей тела с указанием на не более чем вторую степень химических ожогов
6 Химические ожоги нескольких областей тела с указанием на не более чем вторую степень химических ожогов 0 Термический ожог менее 10% поверхности тела
0 Термический ожог менее 10% поверхности тела 3 Химический ожог 30-39% поверхности тела
3 Химический ожог 30-39% поверхности тела