Диета при панкреатите ᐈ Меню на каждый день при панкреатите
02 декабря 2020
При лечении панкреатита особое внимание уделяется правильному режиму питания. Больному нужно подготовиться к исключению из рациона вредной пищи и обязательному употреблению некоторых видов продуктов, необходимых для поддержания работы ЖКТ и других жизненно важных органов. Программа здорового питания при панкреатите составляется индивидуально с учетом формы и характера протекания заболевания.
При воспалении поджелудочной железы пациенту назначается диета «Стол №5». Программа здорового питания складывается из трех этапов:
- 1. При остром панкреатите и обострении хронической формы назначается голодание на протяжении 2-4 дней. Больного переводят на парентеральное питание.
- 2. Переход на щадящее питание.
- 3. Постепенное добавление в рацион новых продуктов с увеличением калорийности и объема блюд.

Существует два варианта программы питания: первый (острая форма) и второй (хроническая фаза).
Диета при остром панкреатите или обострении хронической формы направлена на устранение болевого синдрома. Она назначается после голодания. В ежедневное меню обязательно входят продукты, содержащие следующие вещества:
- Белки: 90 г;
- Углеводы: 300-350 г.
Второй вариант назначается при хронической форме. Пациент должен употреблять больше белка (130-140 г), содержание углеводов в продуктах остается прежним, разрешается включить в рацион жиры — не более 80 г. Энергетическая ценность рациона составляет 2440-2680 ккал в сутки.
Диета при хроническом панкреатите корректируется при плохом переваривании еды с содержанием белков. В этом случае концентрацию белковой пищи можно сократить и заместить углеводами. Дневная норма потребления соли составляет не более 8 грамм. Абсолютно противопоказаны экстрактивные вещества и грубая клетчатка.
Ниже предлагаем Вашему вниманию список продуктов, которые запрещены и разрешены при соблюдении диеты.
| Виды продуктов | Запрещенные | |
| Напитки |
Соки: тыквенные, шиповниковые, абрикосовые, морковные. |
Соки: апельсиновые, виноградные. Другие напитки: алкоголь (в т.ч. безалкогольное пиво), кофе, газированная вода |
| Фрукты | Сладкие груши, сладкие сорта яблок, некоторые сухофрукты | Все виды ягод, апельсины, бананы, кислые яблоки, финики, изюм, орехи |
| Овощи | Огурцы, помидоры (в небольшом количестве), брокколи, цветная капуста, кабачки, тыква, картофель | Закрутки, баклажаны, болгарский перец, белокочанная капуста, редька, редис, хрен, горох, грибы, болгарский перец, щавель |
| Рыба |
Все нежирные сорта: минтай, щука, камбала, хек и др. |
Лососевая икра, копченая и все жирные сорта рыбы |
| Мясо | Говядина, кролик, грудка индейки, курица | Копченое и жирное мясо, сало, колбасы, гусь, утка |
| Молочная продукция | Простокваша с небольшой жирностью, кефир, 1% творог | Сливки, сметана и молоко повышенной жирности |
| Масла и жиры | Сливочное и растительное масло | Жиры животного происхождения |
| Сыры | Неострые сорта | Острые сорта сыров |
| Яйца | Куриные яйца | - |
| Хлебобулочная продукция | Пшеничный и хлеб, выпеченный днем ранее | Свежевыпеченный и ржаной хлеб, сдоба |
| Кондитерка |
Желе, зефир, мед. Несдобное печенье, мармелад, варенье, пастила Несдобное печенье, мармелад, варенье, пастила
|
Шоколад, мороженое, песочное тесто |
| Рис, овсяная, манная и гречневая каша | Фасоль, горох, пшенная, ячменная и кукурузная каша | |
| Соусы и пряности | - | Кетчуп, горчица, майонез, приправы и пряности |
При воспалении поджелудочной железы диета предполагает 5-разовое дробное питание. Ежедневное меню можно составлять на основе следующих блюд:
- Завтрак: овсяная или рисовая каша на воде, чай (можно с медом), несоленый сыр или творог с вареньем;
- Второй завтрак:
- Обед: овощной или куриный бульон, молочный суп с мясным пюре, суп с овощами и крупой, фруктовый кисель, рулет из говядины;
- Полдник: омлет из белка, некрепкий чай, фруктовый кисель, компот из сухофруктов, несдобное и галетное печенье, творожный пудинг;
- Ужин: овощной салат, овощное пюре, тушеный кролик, котлеты из судака, филе индейки, цветная капуста на пару, чай или компот из сухофруктов.

Непосредственно перед сном можно выпить стакан кефира или простокваши.
Врач-гастроэнтеролог расписывает индивидуальное меню при панкреатите с учетом характера протекания болезни, противопоказаний и вкусовых предпочтений пациента.
При воспалении поджелудочной железы нужно соблюдать следующие правила питания:
- Продукты должны быть только запеченными или отварными (рыбу можно готовить на пару), жареные блюда запрещены больным панкреатитом;
- Блюда имеют комнатную температуру — слишком холодная и горячая пища противопоказана при заболеваниях ЖКТ;
- Каши готовятся только на воде, супы — на овощных отварах;
- Допускается употребление только черствого хлеба, чтобы не вызвать вздутие кишечника из-за содержания дрожжей в продукте.
Для консультации и составления диеты для лечения или профилактики заболеваний поджелудочной железы, обращайтесь за помощью в клинику «Консилиум Медикал».
Страница не найдена — Confetissimo — женский блог
С чем носить
Модной вещью сезона стал кожаный пиджак. Он выглядит стильно и весьма необычно, подходит как
Обувь
Качественная, модная, стильная обувь в женском образе – это неотъемлемая и важная составляющая, которая
Как собрать стильный образ? Существует много способов. Во-первых, с помощью аксессуаров. Во-вторых, использовав в
Во-первых, с помощью аксессуаров. Во-вторых, использовав в
Стиль в одежде
Винтажный стиль — это современная одежда, основанная на предметах, которые были модные несколько десятилетий
Стиль в одежде
Для каждой женщины очень важно выглядеть привлекательно в любой ситуации не только для себя,
Типы женской фигуры
Формируя деловой образ, мы следуем определенным правилам и традициям. На протяжении многих сезонов в
На протяжении многих сезонов в
Можно ли при панкреатите? Диета при обострении воспаления желчного пузыря
Рассказываем, из-за чего может воспалиться желчный пузырь и что можно есть и пить при таком заболевании.
— Мне 30, поставили диагноз «панкреатит». Подскажите, чем питаться? Что можно, а что нельзя?
Причиной панкреатита (воспаления поджелудочной железы) в большинстве случаев является злоупотребление алкоголем. Кроме того, спровоцировать заболевание может длительный приём большого количества лекарств, неправильное питание и частые стрессы. Вторичный (реактивный) панкреатит возникает на фоне неблагополучия в желудочно-кишечном тракте (ЖКТ), часто заболевание провоцирует желчекаменная болезнь и состояние после удаления желчного пузыря.
Как отмечают в клинике «Наедине» при хроническом течении заболевания человек чувствует постоянную тупую боль в животе, из-за нехватки ферментов для переваривания пищи может возникать понос, вздутие в животе, неустойчивый стул. Острая форма или обострение характеризуется очень сильной болью в животе. Терпеть её невозможно, поэтому пациенту сразу вызывают скорую и везут в больницу. Иногда в таких случаях требуется хирургическое вмешательство.
Острая форма или обострение характеризуется очень сильной болью в животе. Терпеть её невозможно, поэтому пациенту сразу вызывают скорую и везут в больницу. Иногда в таких случаях требуется хирургическое вмешательство.
Можно ли полностью вылечить панкреатит?
По словам гастроэнтеролога клиники «Наедине» Татьяны Кузьминых, острая форма может закончиться только одним приступом, хроническую вылечить невозможно, но можно добиться ремиссии. Для этого необходимо вовремя принимать лекарства, сдавать анализы (кровь на ферменты, кал на копрограмму, узи брюшной полости, КТ и МРТ), заниматься профилактикой и следить за питанием.
Диета при панкреатите
Людям с хронической формой воспаления всю жизнь приходится соблюдать диету. В противном случае вы рискуете спровоцировать обострение. Диета заключается в отказе от продуктов, которые раздражают слизистую оболочку ЖКТ и обладают сокогонным действием. Также стоит исключить холодные напитки и блюда.
Еду можно запекать или готовить на пару, также разрешена протёртая пища. Питаться лучше часто: по пять или шесть раз в день. Пожилым людям с хроническим панкреатитом и сопутствующими сердечно-сосудистыми заболеваниями ко всему прочему необходимо исключить соль. В списке запрещённых продуктов и блюд — бобовые, пшено, соленья, виноград, клюква, вишня, кислые соки, холодные, газированные напитки, шоколад, наваристые супы на мясных и рыбных бульонах. Ниже мы более подробно расскажем о напитках и еде, которые вызывают больше всего вопросов.
Питаться лучше часто: по пять или шесть раз в день. Пожилым людям с хроническим панкреатитом и сопутствующими сердечно-сосудистыми заболеваниями ко всему прочему необходимо исключить соль. В списке запрещённых продуктов и блюд — бобовые, пшено, соленья, виноград, клюква, вишня, кислые соки, холодные, газированные напитки, шоколад, наваристые супы на мясных и рыбных бульонах. Ниже мы более подробно расскажем о напитках и еде, которые вызывают больше всего вопросов.
Можно ли пить алкоголь?
Длительное и регулярное употребление алкоголя недопустимо. По праздникам можно позволить себе немного выпить, но стоит исключить холодные и газированные напитки: они особенно вредны. Острое воспаление может вызвать даже немного шампанского в Новый год, подчеркнула Татьяна Кузьминых.
Можно ли масло?
Запрещены тугоплавкие жиры — маргарин, бараний или говяжий жир. В ограниченных количествах можно несолёное сливочное масло (30 грамм в день), оливковое или рафинированное подсолнечное (10-15 грамм в день).
Можно ли яйца?
Гастроэнтеролог советует съедать не больше одного яйца в день. Например, можно сделать омлет. Жареные и сваренные вкрутую яйца стоит ограничить.
Какие овощи разрешены и как их готовить?
Все овощи нужно варить или запекать, сырые под строгим запретом. Нужно отказаться от белокочанной капусты, репы, редиса, бобовых, лука, чеснока, сладкого перца, особенно в сыром виде. Можно есть морковь, свёклу, кабачки, тыкву, стручковую фасоль, цветную капусту, картошку, зелёный горошек. Квашенная капуста, солёные помидоры и огурцы запрещены также.
Можно ли хлеб?
Нельзя употреблять ржаной хлеб, сдобную выпечку, слоёное тесто. Пшеничный хлеб можно, но только вчерашний и II сорта, разрешено несладкое сухое печенье.
Можно ли молоко и молочные продукты?
Нужно отказаться от мороженого, сладких сливок, сметаны. Разрешается нежирный и некислый творог, молоко и некислый кефир, ряженка, простокваша.
Можно ли мясо?
Необходимо отказаться от жирной свинины, баранины и колбасы. Также нельзя печёнку, почки, мозги, куриную шкурку. Врачи рекомендуют есть филе курицы, говядину, индейку и кролика.
Также нельзя печёнку, почки, мозги, куриную шкурку. Врачи рекомендуют есть филе курицы, говядину, индейку и кролика.
Можно ли кофе?
Кофе, как и какао, нужно пить с осторожностью. Лучше ограничить количество выпитых в день чашек до одной, кофе можно только с молоком.
Можно ли заниматься спортом при панкреатите?
При тяжёлой стадии панкреатита спорт противопоказан. При хроническом истинном панкреатите запрещены тяжёлые физические нагрузки. В остальных случаях заниматься можно.
Коротко о главном:
1. Чтобы избежать обострений при хроническом панкреатите, нужно тщательно следить за своим питанием. Нужно есть по пять или шесть раз в день, при этом порции не должны быть большими.
2. Полностью из рациона необходимо исключить продукты, которые механически раздражают слизистую оболочку желудочно-кишечного тракта и обладают сокогонным действием. Запрещены холодные блюда, а также холодные, газированные и алкогольные напитки.
3. Всю пищу нужно готовить на пару, также еду можно запекать в духовке.
4. Если вам поставили диагноз «хронический панкреатит», придерживаться диеты придётся всю жизнь.
Если у вас есть вопросы, на которые вы не можете найти ответ, задайте их нам, и мы постараемся на них ответить.
Фото: Сергей Зыков
0
Диета При Панкреатите Поджелудочной Железы При Обострении – Telegraph
>>> ПОДРОБНЕЕ ЖМИТЕ ЗДЕСЬ <<<
Диета При Панкреатите Поджелудочной Железы При Обострении
Диета при хроническом панкреатите отличается от строго течения болезни. Итак, давайте рассмотрим, какая должна быть диета при остром панкреатите? В основе заболевания лежит воспалительный процесс, который нарушает работу ПЖ.
Необходимо отметить, что при остром течении болезни, железа начинает сама себя «поедать». Поэтому диета при остром панкреатите достаточно строгая. Если не придерживаться всех правил по питанию и лечению, то это может привести к сильному некрозу.
Если не придерживаться всех правил по питанию и лечению, то это может привести к сильному некрозу.
Диета при остром панкреатите – один из способов устранить симптомы данного заболевания, тем самым улучшить работу поджелудочной железы. Основное лечение проходит под наблюдением терапевта, часто контролирует лечение и врач-хирург.
Главный гастроэнтеролог РФ: «ПАНКРЕАТИТ не проходит?! Простой способ лечения уже исцелил сотни пациентов в домашних условиях! Чтобы навсегда вылечить поджелудочную нужно…» Читать далее »
В первый день при панкреатите поджелудочной железы после приступа, врачи назначают на протяжении 3-х дней. Отметим, что голодание может длиться и на протяжении 6-ти дней. В этот период времени, больному разрешается пить только воду.
Необходимо отметить, что срок голодания зависит именно от степени тяжести самого приступа.
Важно! При приступе панкреатита врачи назначают голод, и проводят все необходимые медикаментозные мероприятия по устранению приступа.
Наряду с голоданием, врачи назначают лекарственные препараты, которые помогают устранить все неприятные симптомы заболевания. При правильно подобранной терапии, можно за короткий промежуток времени восстановить работу ПЖ, а также поддержать местный иммунитет.
При правильно подобранной терапии, можно за короткий промежуток времени восстановить работу ПЖ, а также поддержать местный иммунитет.
Для того чтобы контролировать ферменты воспаленной ПЖ, назначают общий анализ мочи и крови.
Как только в результатах лабораторного обследования будет выявлено снижение ферментов, то можно будут расширить лечебную диету.
Примерно на 2 или 3 день, можно постепенно вводить и иные продукты. Несмотря на то, что питание при панкреатите строгое, больному разрешается употреблять тефтели, но только их необходимо готовить на пару. После приступа острого панкреатита ввести в рацион питания говядину, курицу и кремообразные супы из овощей.
Также читайте: Кисель при панкреатите поджелудочной железы
Питание при обострении панкреатита должно осуществляться небольшими порциями, кушать примерно 4-6 раз в день. Если кушать большими порциями, то это создаст дополнительную нагрузку на воспаленную железу, а также можно спровоцировать повторный приступ заболевания.
Список запрещенных продуктов достаточно обширный. Под запретом:
Дополнительно запрещается кушать свежий хлеб и разнообразные выпечки. Мы привели не весь список, более детальную информацию можно узнать у лечащего врача. Помните, что диетическое питание будет зависеть от степени тяжести болезни, а также от сопутствующих болезней.
Диета при панкреатите в период обострения помогает набрать силы и пополнить организм питательными компонентами. Назначается лечебное питание под номером 5. Данное меню включает в себя много зелени, фруктов и овощей. При этом из рациона питания необходимо ограничить употребление сахара и соли.
Диета при обострении гастрита и панкреатита, что можно кушать:
Дополнительно необходимо обогатить свое питание мясной продукцией. Например: приготовить курицу, ягненка или кролика.
Диетическое питание под номером 5 назначается при остром или же хроническом течении болезни. Такая диетотерапия назначается и при болезнях 12-перстной кишки, при поражении кишечника. Очень часто диетический стол №5 назначают и при заболеваниях печени.
Очень часто диетический стол №5 назначают и при заболеваниях печени.
Диета помогает снизить нагрузку на воспаленную поджелудочную железу. В этот момент главное не передать, поэтому необходимо кушать дробно. В сутки больному нужно выпивать не менее чем 1.5-3 литра воды без газа.
Также читайте: Яблоки при панкреатите
Как вы видите, что диета при обострении панкреатита очень строгая.
Диета после приступа панкреатита назначается в стационаре. Больному даже после выписки необходимо на протяжении определенного времени придерживаться диетического питания. В этот момент необходимо обогатить свой рацион питания полезными белками, которые помогут восстановить весь организм в целом.
Диета после обострения панкреатита, основные правила:
Необходимо отметить, что обострение панкреатита и несоблюдение диеты, может привести к серьезным осложнениям. Поэтому не стоит пренебрегать правилами лечащего врача.
Обратите внимание, что у женщин чаще всего развивается билиарный острый панкреатит, поэтому врачи настоятельно рекомендуют включить в рацион питания как можно больше кисломолочной обезжиренной продукции.
Если панкреатит возникает в сочетании с сахарным диабетом, то необходимо исключить из рациона: рис, макароны, сахар, картофель и сладкие фрукты.
Диета при остром холецистите и панкреатите одинаковая. Рассмотрим, что можно есть.
Взрослым на завтрак разрешается выпить стакан чая, можно скушать также овсяное печенье или приготовить смузи из свежей малины и нежирной сметаны.
В обед приготовить овсяную кашу, при необходимости можно добавить немного изюма или сухих яблок, бананов или иных фруктов. Включить на обед: хлебцы и выпить стакан свежевыжатого морковного сока.
На полдник разрешается приготовить овощную запеканку. Выпить на полдник стакан березового сока или некрепкого чай. При желании можно скушать яблоко или иной фрукт.
Питание на ужин: приготовить крем суп из овощей (например, использовать для приготовления морковь, цветную капусту).
Также читайте: Диета при панкреатите поджелудочной железы
На второй ужин разрешается скушать имбирное печенье, один банан или яблоко, а также выпить стакан обезжиренного молока.
Рекомендации от Еленой Малышевой в спецвыпуске «Жить здорово!», как побороть пакреатит при помощи исцеляющих воздействии природных средств.
При обострении хронического панкреатита диета более разнообразная, но тем не менее имеет много ограничений. Для тех, кто не знает, как правильно приготовить блюда, рекомендуем ознакомиться с информацией ниже.
Рассмотрим несколько самых распространённых рецептов, которые врачи рекомендует готовить при остром панкреатите.
Если обострился панкреатит, то можно приготовить мятный чай. Для его приготовления вам понадобится:
Приготовление: в кружке кипятка запарить мяту или высыпать все остальные ингредиенты. Настаивать 5 минут, пить в теплом виде.
Для приготовления этого рецепта вам понадобится:
Приготовление: рыбу натереть зеленью и смазать сметаной. После чего поставить в духовую печь на 20 минут, затем посыпать сыром и поставить еще на 10-15 минут.
Запекать рыбу можно в фольге, рядом выложить овощи, например: перец, морковь, капусту, кабачок, картофель.
Для приготовления рецепта вам необходимо купить свежий говяжий фарш, также понадобится 1 яйцо, немного сыра, можно купить с копченостями.
Приготовление: в тару положить фарш, затем добавить яйцо, тертый сыр и все хорошо перемешать. Сформировать небольшие кружочки и готовить блюда на пару в течение 15-20 минут. Готовое блюдо можно подавать с гречневой кашей.
Отварить и растолочь картофель, затем в него добавить перемолотое мясо и мелко нарезанный лук. Все перемешать и вбить яйцо. Сформировать форму и запекать в духовой печи на протяжении 30 минут.
Важно! В момент приготовления запеканки следите, чтобы не образовывалась корочка. Картофельную запеканку можно подавать с мясными блюдами.
Теперь вы знаете, какое питание должно быть. Помните, при пренебрежении правилами диетического питания, могут возникнуть серьезные осложнения со здоровьем.
Понравилась статья? Поделиться с друзьями:
При воспалении поджелудочной железы диетическое питание нестрогое, однако имеется определенный список запрещенных продуктов. Похожие
Похожие
Можно ли бананы при панкреатите? Такой продукт любят не только дети, но и взрослые.
Хронический панкреатит поджелудочной железы — болезнь, требующая внимательного отношения больного к своему питанию. Правильным
Диетическое питание при воспаленной поджелудочной железе достаточно разнообразное. Овощи при панкреатите можно кушать, но
Панкреатит – достаточно распространенное заболевание, которое при несвоевременном лечении приводит к тяжелым осложнениям. При
Можно ли пить кефир при панкреатите? Именно на этот вопрос мы сегодня ответим. Сразу
Диета при остром панкреатите имеет свои особенности, отличающие ее от других диет. О том, что характерно для диеты при остром панкреатите, об особенностях питания при заболеваниях поджелудочной железы расскажет этот пост.
Острый панкреатит – воспаление поджелудочной железы, протекающее в острой форме, вызванное активацией пищеварительных ферментов.
Причин возникновения острого панкреатита много, но чаще всего острый панкреатит возникает у лиц злоупотребляющих алкоголем и лиц с заболеваниями желчевыводящей системы – хронический холецистит, желчнокаменная болезнь.
Приступ острого панкреатита возникает, как правило, внезапно и проявляется нестерпимыми болями и другими характерными для данного заболевания симптомами.
Заболевание поджелудочной железы воспалительного характера называется панкреатит. Железа выполняет секреторные функции: вырабатывает инсулин, липокаин и глюкагон, а участие в пищеварении заключается в секреции панкреатического сока. Причины поражения ее многообразны: токсическое отравление, травмы, обструкция панкреатического протока, сосудистые нарушения, заболевания желчного пузыря и протоков, воздействие лекарственных средств, инфекционные и паразитарные заболевания.
Различают острый и хронический панкреатит. Острый панкреатит связан с ферментным самоперевариванием (аутолизом) поджелудочной железы и в тяжелых случаях наблюдается некроз тканей железы и близлежащих органов. Часто развивается при приеме лекарственных препаратов (метилдопа, Азатиоприн, 5-аминосалицилаты, тетрациклины, Фуросемид, Циметидин, Метронидазол). В половине случаев причиной его развития является ЖКБ, а часть — связана со злоупотреблением алкоголем.
Для больных диагноз «панкреатит» – настоящая трагедия, так как это заболевание – до конца жизни. Если человек привык есть, что придется, не задумываться о принципах ЗОЖ, то острые боли заставят организовать пожизненную диетотерапию. Воспаленная поджелудочная железа требует внимательного отношения к принципам питания. Медициной разработана специальная диета № 5, которая включает в себя щадящие рецепты при панкреатите. Диета ограничивает привычные для здоровых людей продукты питания, но продумана так, чтобы организм больного получал сбалансированную пищу.
Поэтому надо продумать рацион для разных этапов болезни при помощи лечащего врача. Если пациент серьезно настроен избегать обострения заболеваний, то изучить и соблюдать правила питания не составит для него туда.
Панкреатит – серьезное заболевание поджелудочной железы, при котором воспаляются ткани органа секреции. Поджелудочная железа участвует в процессах пищеварения, вырабатывая панкреатический сок. Он нейтрализует кислую среды желудочного сока, способствует расщеплению пищи и процессам всасывания питательных веществ. При нарушении оттока панкреатического сока из органа или обратном забросе из двенадцатиперстной кишки, ферменты начинают переваривать окружающие ткани, вызывая воспаление протоков и самой поджелудочной железы.
При нарушении оттока панкреатического сока из органа или обратном забросе из двенадцатиперстной кишки, ферменты начинают переваривать окружающие ткани, вызывая воспаление протоков и самой поджелудочной железы.
Причины болезни самые различные, но в основном они связаны с нарушением питания: голодания, диеты, жирная и острая пища, отравления, употребление алкоголя, иные воспалительные заболевания – например, гастрит, цирроз печени. Иногда панкреатиту способствуют гормональные нарушения, инфекции, наследственность. Чаще всего заболевание возникает в среднем и пожилом возрасте, поэтому нужно особенно тщательно следить за своим питанием в это время и избежать болезни.
Люди в группе риска по данному заболеванию, а также заболевшие, вынуждены соблюдать целый ряд ограничений в питании. В противном случае неполноценно работающая, воспаленная железа не справляется с нагрузкой, происходит сужение протоков и застой сока, орган начинает переваривать сам себя.
Панкреатит — это целая группа заболеваний, связанных с воспалением поджелудочной железы. Болезнь может проявиться неожиданно — одним из ее проявлений является болевой синдром. Чтобы снять боль и предотвратить повторные приступы, важен правильный рацион. Панкреатит делится на хронический и острый, в зависимости от характера болезни нужно выбирать необходимое питание.
Болезнь может проявиться неожиданно — одним из ее проявлений является болевой синдром. Чтобы снять боль и предотвратить повторные приступы, важен правильный рацион. Панкреатит делится на хронический и острый, в зависимости от характера болезни нужно выбирать необходимое питание.
При обострении панкреатита возникает необходимость в хирургическом вмешательстве (вскрытии оболочки поджелудочной железы) в случае малого эффекта от медикаментозного лечения, голодания, удаления из желудка остатков пищи. Хронический панкреатит обостряется под влиянием переедания, алкоголизма, длительного применения глюкокортикоидных гормонов, эстрогенов, наркотических препаратов, Индометацина, Фуросемида, на фоне больной печени (при которой необходимо соблюдать специальную диету) и желчного пузыря, которые довольно часто встречаются у взрослых людей. При повышении давления внутри живота у женщин в конце беременности возможно развитие панкреатита.
Диета при остром панкреатите – это комплекс строгих правил, которые необходимо соблюдать. Давайте детальнее рассмотрим особенности питания при заболевании поджелудочной железы.
Давайте детальнее рассмотрим особенности питания при заболевании поджелудочной железы.
В основе панкреатита лежат нарушения в работе поджелудочной железы. Острый панкреатит отличается тем, что поджелудочная железа начинает сама себя «поедать», отсюда и идет некроз поджелудочной. Причин множество. Больной должен понимать, что если не соблюдать правила питания, последствия болезни могут быть плачевны.
Диета при остром панкреатите соблюдается строго, она направлена на восстановление функции поджелудочной железы. Поджелудочная железа играет огромную роль в организме человека. Она вырабатывает ферменты, которые помогаю организму усваивать белки, жиры и углеводы. При панкреатите нарушается выработка инсулина, что грозит риском развития такого заболевания как сахарный диабет.
Этот сайт использует Akismet для борьбы со спамом. Узнайте как обрабатываются ваши данные комментариев.
Час назад пришла печальная весть из СИЗО о Ефремове
В Москве из канализации вытащили огромного крокодила!
Удав напал на ягуарунди. То, что произошло дальше, поразило всех
То, что произошло дальше, поразило всех
Этот сайт использует cookie для хранения данных. Продолжая использовать сайт, Вы даете свое согласие на работу с этими файлами. OK
Диета при остром панкреатите , при обострении у взрослых…
Диета при панкреатите поджелудочной железы
Лечение панкреатита в домашних условиях народными…
Диета при панкреатите: примерное меню на неделю, рецепты
Диета при остром панкреатите поджелудочной железы: что…
Похудение Без Диет
Сладкая Диета
Диета При Панкреатите И Холецистите Меню
Диета На Каждый День
Диета Поджелудочной Железы Примерное
Диета при панкреатите: меню на каждый день
Диета: PixabayДиета при панкреатите оказывает благотворное влияние на организм человека. Проблемы, которые возникают из-за заболевания поджелудочной железы, выражаются острыми болезненными ощущениями в теле. Такие симптомы мешают вести привычный образ жизни. Давайте разбираться, как исправить ситуацию, что можно добавить в рацион, а от чего стоит отказаться при панкреатите.
Питание при панкреатите: принципы и рекомендации
Панкреатит — это воспаление поджелудочной железы, рассказывает WebMD. С этим заболеванием сталкивается не каждый. Оно возникает при долгом употреблении в пищу вредных продуктов, повреждениях брюшной области, интоксикациях и проблемах с функционированием печени. Обычно, как пишут авторы авторитетного издания British Medical Journal Джо Хайнс и Стивен Дж. Пандол, недуг развивается медленно в результате регулярного поступления в желудок жирного и жареного, в особенности фастфуда. Не менее ощутимый вред организму наносят пагубные зависимости.
Читайте также
Зеленые помидоры на зиму: подборка рецептов
Как обычному человеку выяснить, что у него формируется панкреатит? Симптомы обычно не радуют. Как правило, больные замечают:
- тошноту;
- резкие боли в животе;
- диарею;
- снижение массы.
Дополнительно дискомфорт может распространяться на всё тело. В этой ситуации достаточно тяжело понять, где именно локализуется боль. При первых симптомах панкреатита немедленно запишитесь на прием к медицинскому сотруднику. Таким образом вы сможете обезопасить себя и не дать заболеванию перерасти в хроническую стадию.
При первых симптомах панкреатита немедленно запишитесь на прием к медицинскому сотруднику. Таким образом вы сможете обезопасить себя и не дать заболеванию перерасти в хроническую стадию.
Более детально ознакомиться с диетическим питанием и рекомендациями при диагностировании панкреатита можно в научной статье Новоселя Н.В., Кокуевой О.В., Абрамяна В.В. из РГБУ Кубанского медицинского института.
В повседневной практике пациенты часто обращаются ко мне и моим коллегам за помощью при панкреатите. Научные исследования и анализы показывают нарушения, которые происходят в теле больного. В работе медики используют именно эту информацию для составления терапии и особого рациона питания.
Читайте также
Брокколи на зиму: рецепты заготовок
Если поджелудочная железа, диета для восстановления которой подбирается специалистом, хоть раз воспалилась, то придется соблюдать указания врача по меню на протяжении всей жизни. Употребление здоровой пищи позволяет организму расслабиться и помогает устранить существующий недуг.
Употребление здоровой пищи позволяет организму расслабиться и помогает устранить существующий недуг.
Медицинские рекомендации диетического питания, когда болит поджелудочная:
- Частое дробное питание 5–6 раз в день.
- Протертая через сито или измельченная в блендере еда, не вызывающая раздражение на слизистой.
- Все блюда употребляют в вареном и запеченном виде, а также готовят на пару.
- Для стабилизации и укрепления организма увеличивают количество белков, поступающих вовнутрь. Врачи рекомендуют употреблять нежирное мясо птицы или кролика, рыбу по типу щуки или трески, а также кисломолочные продукты.
- Снижение потребления жиров и углеводов. Диетологи разрешают есть пшеничные, овсяные и гречневые каши, а также мелкую вермишель.
- Употребление большого количества очищенной воды на протяжении всего дня. За сутки врачи советуют выпивать 2 л воды.

Читайте также
Как солить капусту на зиму кусочками: простые рецепты
Если начал проявляться панкреатит, обязательно обратитесь к доктору. Он расскажет, что лечение должно включать в себя не только ПП, но и борьбу с пагубными пристрастиями.
Мои коллеги из Университета Магдебурга тоже разбирались в корректировке питания для людей с нарушением пищеварения в своей научной статье.
Диета при хроническом панкреатите полностью запрещает есть мясные бульоны и блюда на их основе. Чтобы поджелудочная железа не вызывала боли в области живота, я рекомендую убрать из меню:
- копчености;
- жареные блюда;
- снизить количество используемой соли;
- ограничить употребление сладостей.
Мои коллеги также рекомендуют отказаться от приема капусты, щавеля и редиса. Сладкие напитки, газировка и алкоголь полностью исключаются из меню лиц, страдающих от проблем с поджелудочной железой.
Читайте также
Как хранить яблоки на зиму в домашних условиях
youtube.com/embed/G5h00ASBCTY» frameborder=»0″ loading=»lazy»/>
Что можно есть при панкреатите: меню
После перечня ограничений многих людей интересует вопрос: что можно есть больному в таком случае? Диета при панкреатите стол №5 предполагает отказ от неправильной пищи, ведь она направлена на стабилизацию всего организма и снятие воспалительных очагов. Нужно понимать, что панкреатит хронического характера неизлечим, но избавиться от его проявлений вполне реально.
Больше информации можно узнать из научной статьи моего коллеги Кучерявого Ю.А. «Хронический панкреатит взглядом терапевта: от международных рекомендаций к практическому здравоохранению».
Мой практический опыт подтверждает приведенное выше утверждение, однако ни для одного из моих пациентов жизнь на этом не закончилась. Они придерживаются утвержденной терапии и живут полноценно. Достоверно известно, что специальная медицинская диета помогает бороться с различными проявлениями заболевания, и я являлась свидетелем ее эффективности.
Читайте также
Как хранить тыкву зимой правильно
Леонович С.И., Кондратенко Г.Г., Протасевич А.А., Неверов П.С.: Острый панкреатит. — М.: Медицина, 2009.Ниже расписано меню для людей с диагнозом «панкреатит». Диета разработана по дням недели, которые можно менять местами и дополнять по своему вкусу полезными продуктами без опасений для здоровья. Однако, если сомневаетесь, обязательно обсудите меню с лечащим доктором, чтобы не навредить здоровью.
Понедельник:
- На завтрак готовим перетертую смесь из отварного картофеля с говядиной. В качестве напитка делаем черный или зеленый чай без добавления сахара.
- На перекус возьмем куриную котлету, приготовленную на паровой бане или в пароварке, зернистый творог и запеченное яблоко со специями. Помните, что список разрешенных специй невелик. Лучше заранее обсудите этот вопрос с врачом.
- На обед делаем легкий суп из лапши и запиваем все чайным напитком.
- На второй перекус съедаем немного творога или йогурта без наполнителей и сахара.
 Постоянно пьем воду.
Постоянно пьем воду. - На ужин запекаем мясной рулет, а на десерт съедаем пудинг из творога. Пьем чай.
Читайте также
Как солить грузди на зиму холодным и горячим способом
Вторник:
- Утром съедаем гречневую кашу, приготовленную на воде без соли и сахара, выпиваем компот из фруктов.
- На второй завтрак берем суфле из кабачков и паровую котлету из птицы. Разрешается подсушить небольшой кусочек хлеба. Запиваем всё некрепким чаем.
- На обед подойдет суп с мелкой лапшой, отварное измельченное мясо, пюре из картофеля и компот.
- На полдник съедаем запеченный фрукт (яблоко или грушу), горсть сухого печенья и натуральный йогурт.
- Ужин у нас будет состоять из овсяной каши, биточков, сделанных на пару, ломтика хлеба и крепкого чая.
Среда:
- Для завтрака готовим молочную рисовую кашу, пьем компот.
- На перекус съедаем тарелку низкокалорийного творога и запеченную или свежую мягкую грушу, пьем негазированную воду.

- В обед готовим морковный суп и отвариваем говядину.
- Во время перекуса насыщаем организм овощным рагу, несколькими кусочками твердого сыра и чайным напитком.
- На ужин готовим картофельное пюре, делаем бутерброд с сыром, пьем чай с молоком.
Четверг:
- На первый завтрак делаем омлет. При панкреатите рекомендуется использовать только белки. Выпиваем чай на основе ромашки.
- Второй раз завтракаем творогом в сыром или запеченном виде и пьем теплый черный чай.
- На обед делаем легкий суп из брокколи, варим рыбу, съедаем половину банана. В этот раз чай следует заменить свежим отваром из шиповника.
- На перекус готовим десерт: запекаем в духовке грушу или яблоко с измельченными орехами.
- Вечером отвариваем рыбу с морковью и готовим чай.
Пятница:
- С утра делаем питательные мясные шарики, рис без специй и соусов, пьем минеральную воду.

- В полдень съедаем тарелку творога и немного отварной курицы или говядины.
- В обед готовим манку на молоке, мясные биточки (обязательно на пару) и запиваем блюда ароматным ягодным киселем.
- На перекус берем ягодное желе или натуральный йогурт.
- Вечером варим немного овсянки, две паровые котлеты и пьем кисель.
Суббота:
- Утром готовим пюре и рыбу, в качестве напитка берем фруктовый компот. Можно добавить немного свежего зеленого салата. Помним, что помидоры лучше исключить из рациона.
- В качестве передобеденного перекуса употребляем пудинг из творога, омлет с большим количеством белка, запиваем компотом.
- Обедаем супом-пюре из овощей, кусочком куриной грудки и хлебом, запиваем блюдо очищенной водой.
- После полудня съедаем запеченные фрукты, пьем чаем.
- На ужин сделаем гречневую кашу на воде, съедим один небольшой банан и выпьем стакан кефира.
Воскресенье:
- Утром делаем пудинг из творога, гречневую кашу и слабый чай.

- На первый перекус съедаем питательный мясной рулет, пьем йогурт и напиток из шиповника.
- В обед делаем овсяный суп, котлеты из нежирного мяса на пару, пюре. Запиваем все минеральной водой.
- На перекус съедаем фруктовое желе, творожную запеканку и выпиваем 200 мл кефира.
- Заканчиваем день тарелкой мелкой вермишели, запеченной рыбой, чаем.
Мои пациенты одобряют представленный рацион питания. Я лично прорабатывала представленное меню, чтобы организм получал достаточное количество витаминов и полезных микроэлементов. Диетическое меню, составленное экспертом, поможет предотвратить возникновение боли и дискомфорта в брюшной полости.
Здоровое питание способствует налаживанию процессов пищеварения и возвращает организм пациента в первоначальное состояние, которые было до возникновения панкреатита.
Изменяйте составляющие вышеописанного меню, выбирая наиболее подходящие для вас продукты, однако не забывайте согласовывать рацион с лечащим врачом. Помните, что лучше каждый день контролировать то, что попадает к нам в желудок, чем потом заниматься лечением и мучиться от боли.
Помните, что лучше каждый день контролировать то, что попадает к нам в желудок, чем потом заниматься лечением и мучиться от боли.
Внимание! Материал носит лишь ознакомительный характер. Не следует прибегать к описанным в нем методам лечения без предварительной консультации с врачом.
Источники:
- Гётц Т. и др. Нутриционная поддержка при остром панкреатите // Международный опыт. — 2009. — №2. —170–177.
- Кучерявый Ю.А. Хронический панкреатит взглядом терапевта: от международных рекомендаций к практическому здравоохранению // Медицинский совет. — 2012. —№9. — 45–50.
- Новоселя Н.В. и др. Особенности диеты и нутриционной поддержки при хроническом панкреатите // Экспериментальная и клиническая гастроэнтерология. — 2014. —№4. — С. 15–17.
- Minesh Khatri. What is pancreatitis? // WebMD. — 2019. — 12 October.
- O Joe Hines, Stephen J Pandol. Management of severe acute pancreatitis // BMJ.
Автор: кандидат медицинских наук Анна Ивановна Тихомирова
Рецензент: кандидат медицинских наук, профессор Иван Георгиевич Максаков
youtube.com/embed/VLirgnT4dGQ» frameborder=»0″ loading=»lazy»/>
Оригинал статьи: https://www.nur.kz/food/healthy-eating/1774953-dieta-pri-pankreatite-menu-na-kazdyj-den/
Основы диеты при панкреатите — МК
+ A —
Если панкреатит имеет хроническое течение, тогда периоды активации процесса сменяются периодами затухания, когда изменения внутри железы минимальны
Панкреатит – это воспалительный процесс в зоне тканей поджелудочной железы, одного из важнейших органов пищеварения. При остром процессе резко нарушается состояние, пациент чувствует себя крайне плохо и воспаление грозит серьезными осложнениями, вплоть до летальных исходов. Однако, стоит помнить, что малейшие патогенные влияния способны привести к обострению процесса, что требует госпитализации и активного лечения. С целью предотвращения обострений или снижения их частоты применяется особая диета при панкреатите.
С целью предотвращения обострений или снижения их частоты применяется особая диета при панкреатите.
Хронический панкреатит
Обычно хронический процесс формируется после острых воспалений, если лечение было проведено не в полном объеме, и по мере улучшения состояния пациент перестал выполнять все предписания врача. Это не самая благоприятная ситуация, так как наличие постоянного очага вяло текущего воспаления грозит и нарушением функций органа, и его дистрофическими изменениями, а также при провоцирующих факторах – снова и снова будут обострения. Кроме того, хронический панкреатит может формироваться вторично, на фоне имеющихся различных пищеварительных проблем – патологий желудка и тонкой кишки, глистных инвазий, камнеобразования в желчном пузыре. Наличие проблем с работой поджелудочной железы осложняет течение этих патологий и требует более основательного и длительного лечения. Немалую роль в терапии будут играть и диетические рекомендации, соблюдение которых может существенно помочь в снятии воспалительного процесса, нормализации обменных процессов и улучшении общего состояния. Диета при панкреатите
Диета при панкреатите
Естественно, что только одна диета при панкреатите не сможет полностью вылечить пациента, но она может существенно снизить риски обострения и разгрузит пищеварение, дав ему возможность работать с меньшим напряжением. Соблюдение принципов питания поможет существенно снизить частоту обострений, снижает риск осложнений и улучшает процессы переваривания пищи и усвоение питательных веществ.
Для лечения панкреатитов существует особая диета, стол №5. Ее стоит придерживаться на протяжении длительного времени, в идеале – всю жизнь при наличии хронического панкреатита, при котором функции железы полностью уже не восстанавливаются. В зависимости от того, обострение это процесса или стадия его ремиссии, имеются особенности питания. Если это острое воспаление (на фоне провоцирующих факторов), показано голодание на протяжении нескольких суток, что разгрузит железу и даст ей отдых. По мере того, как постепенно сходит отек железы, и она может хотя бы частично выполнять свои функции, расширяют диету до щелочных напитков, не раздражающих ткани железы и протертой парой и отварной пищи. Это могут быть овсяный отвар, кисель или желе, подсушенный в сухарики хлеб, пюре из картофеля на воде и без масла, протертые овощные супы и каши, галетное печенье.Что стоит исключать в обострение
Это могут быть овсяный отвар, кисель или желе, подсушенный в сухарики хлеб, пюре из картофеля на воде и без масла, протертые овощные супы и каши, галетное печенье.Что стоит исключать в обострение
При обострении панкреатита, особенно в первое время, в питании категорически запрещены острые и жирные блюда, специи, наваристые супы и бульоны, масла и избыток белка. В первые дни исключают мясо и рыбу, яйца, молочные блюда и бобовые, сыры и избыток свежих овощей и фруктов.
По мере улучшения диета при панкреатите немного расширяется за счет творога и паровых омлетов, нежирных кисломолочных продуктов, отварных и приготовленных на пару овощей, перетертых в пюре, легких супов, также протертых, фруктовых пюре и каш на воде.
По мере того, как пациент приходит в себя, из питания на последующее время исключают алкоголь и раздражающие блюда, острое и жирное, слишком кислые продукты и много специй. Основу рациона должны составлять сложные углеводы, белок и совсем немного жиров.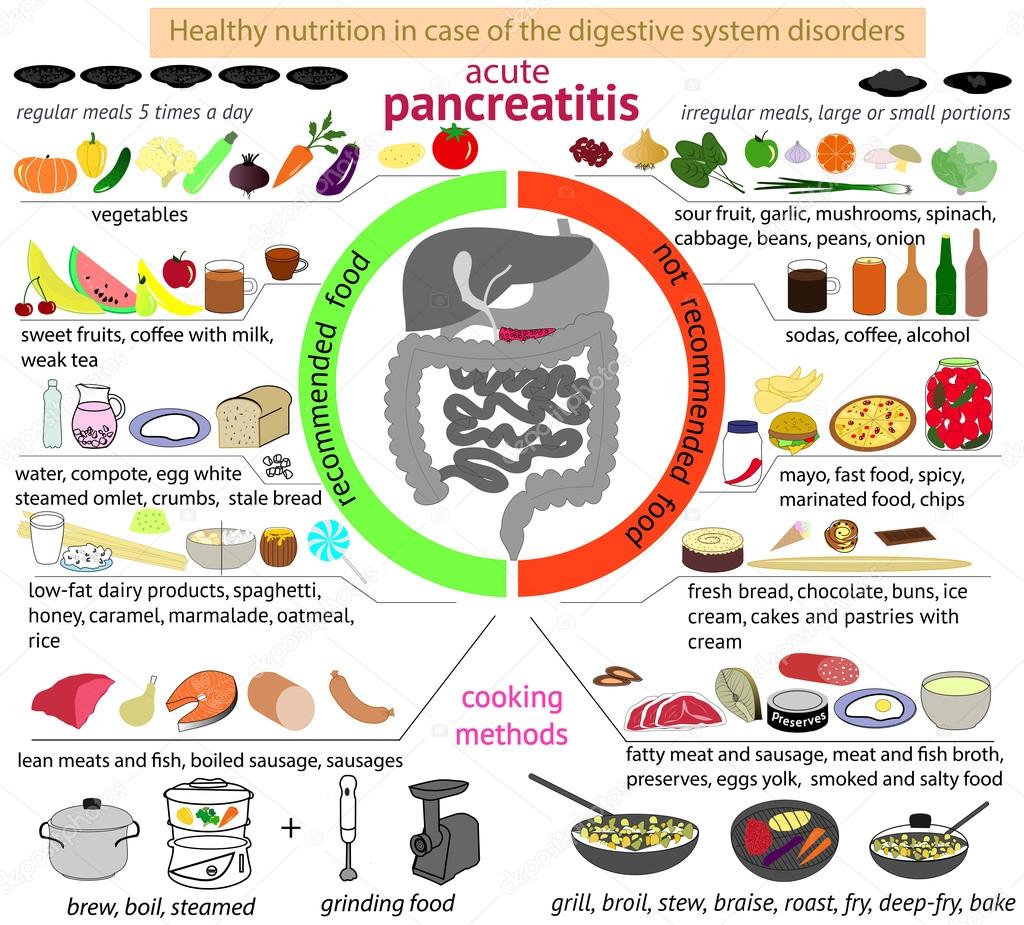 Блюда готовят отварными, паровыми, запеченными без масла и жира.
Блюда готовят отварными, паровыми, запеченными без масла и жира.
Всё о панкреатите Вы можете прочитать на сайте MedAboutMe — https://medaboutme.ru/zdorove/spravochnik/slovar-medicinskih-terminov/pankreatit/
18+
На правах рекламы
остром и хроническом; стол 5
Принципы и цели диеты при панкреатите
Панкреатит — это воспалительное повреждение поджелудочной железы. Поджелудочная железа выполняет важные функции: вырабатывает пищеварительные ферменты (пищеварительные соки), а также гормоны углеводного обмена — инсулин и глюкагон.
Пищеварительные соки расщепляют еду до простых соединений, которые затем всасываются в тонкой кишке. Таким образом, снабжение организма питательными веществами напрямую зависит от функционирования поджелудочной железы.
Независимо от формы панкреатита (острый, хронический, реактивный), заболевание имеет общий механизм развития — затруднение оттока поджелудочного секрета в двенадцатиперстную кишку и, как следствие, накопление и активация ферментов в самой железе, что вызывает воспаление и даже самопереваривание ткани железы.
Поэтому, основной принцип лечения панкреатита — подавить секрецию поджелудочной железы. Соответственно, принцип питания при панкреатите — максимально снизить раздражение поджелудочной железы и нагрузку на нее, чтобы железе не требовалось вырабатывать пищеварительный секрет. Поскольку это очень важно и сравнительно легко достижимо, правильная диета на 50% определяет успех лечения панкреатита и на 80% — профилактику обострений заболевания. Диету при панкреатите назначает врач — диетолог или гастроэнтеролог.
При остром панкреатите диету соблюдают 6-9 месяцев. При хроническом — всю жизнь. Врачи разработали специальные лечебные диеты (столы) при заболеваниях пищеварительной системы, в частности при стол №5п при панкреатите. Он показан пациентам с любой формой панкреатита. Основное правило — пища должна содержать максимум белков и минимум жиров и углеводов. Вот оптимальное соотношение ключевых составляющих стола №5п:
- белки — 150 г. (75% животного, 25% растительного происхождения)
- жиры — 90 г.

- углеводы до 150 г.
- соль до 5-7 г.
- жидкость — 2 литра в день;
Общая дневная калорийность рациона — 2300-2600 ккал.
Что важно знать, приготавливая и потребляя стол номер 5:
- пищу нужно измельчать или перетирать до мелких кусочков;
- еду нельзя жарить и коптить; только варить, запекать или готовить на пару;
- горячую и холодную еду есть нельзя. Оптимальная температура пищи — 25-40 градусов.
- передать нельзя. Нужно вставать из-за стола с легким чувством голода.
- показано частое дробное питание — 5-6 раз в день.
- употреблять алкоголь и курить нельзя.
Вот продукты, облегчающие работу поджелудочной железы и, соответственно, разрешенные при панкреатите:
- хлеб 3-х дневной свежести, белые сухари;
- протертые овощные супы;
- филе курицы, индейки;
- нежирная рыба;
- гречневая каша, овсянка;
- молочные продукты до 2% жирности;
- некрепкий чай, негазированная вода.

А это есть нельзя:
- первые блюда на основе бульонов из животных жиров;
- хлебобулочные изделия;
- жирное мясо, колбасы;
- жирную рыбу;
- копчености, консервы;
- жирные молочные продукты;
- каши из перловки, пшена, кукурузы;
- яйца;
- свежие овощи;
- сладости;
- специи, соусы, пряности;
- кофе, газировку, соки.
При выраженном болевом синдроме следует на 3 дня полностью отказаться от еды и минимизировать питье до 750 мл. в сутки. Чтобы не было сомнений, повторим: первые трое суток нужно голодать и только пить воду. На 4 день начинают употреблять некрепкий чай и жидкую кашу (кашу варят от 40 мин), нежирный творог. Через неделю меню расширяют до белкового омлета, протертой гречневой и овсяной каши. Первые 3 недели еда должна быть полужидкой. Чтобы избежать повторных обострений болезни (хронического панкреатита), строгой диеты придерживаются 6-9 месяцев. Вот пример однодневной диеты:
Вот пример однодневной диеты:
Завтрак:
- овсяная каша 200 г.
- чай
Дневной перекус:
- творог — 100 г.
Обед:
- картофельное пюре — 200 г.
- индюшиные паровые котлеты — 150 г.
Полдник:
- паровой омлет — 100 г.
Ужин:
- рыба, приготовленная на пару — 200 г.
- протертые кабачки — 100 г.
- чай
Если к вечеру возникает сильное чувство голода, можно выпить стакан простокваши.
Хронический панкреатит характеризуется чередованием стадий обострения и ремиссии. Цель лечебного питания — избежать обострений. Хронический панкреатит опасен тем, что без соблюдения диеты возникают частые обострения и, как следствие, развивается сахарный диабет. Поэтому диету соблюдают всю жизнь.
Диета при хроническом панкреатите почти не отличается от таковой при остром панкреатите. Но она чуть менее строгая — можно не голодать в течение первых трех суток, ограничившись сутками или двумя. За основу также берут лечебный стол номер 5п. Пользуйтесь списком разрешенных продуктов и чередуйте блюда по вашему усмотрению. Подходы к диете при хроническом панкреатите и реактивном панкреатите одинаковы. Питание отличается особенностями основного заболевания, спровоцировавшего реактивный панкреатит.
Но она чуть менее строгая — можно не голодать в течение первых трех суток, ограничившись сутками или двумя. За основу также берут лечебный стол номер 5п. Пользуйтесь списком разрешенных продуктов и чередуйте блюда по вашему усмотрению. Подходы к диете при хроническом панкреатите и реактивном панкреатите одинаковы. Питание отличается особенностями основного заболевания, спровоцировавшего реактивный панкреатит.
Пример однодневной диеты при хроническом панкреатите:
Завтрак:
- рисовая каша 200 г.
- чай
Дневной перекус:
- печеные овощи — 150 г.
Обед:
- протертый овощной суп — 200 г.
- овощи, приготовленные на пару — 120 г.
- компот
Полдник:
- запеканка — 150 г.
Ужин:
- картофельное пюре — 200 г.
- рыба, приготовленная на пару — 100 г.
- чай
К какому врачу обратиться
Чтобы правильно питаться при панкреатите, проконсультируйтесь у диетолога и гастроэнтеролога. Обратитесь к врачам сервиса врачебных видеоконсультаций Botkin.pro. Посмотрите, как наши врачи отвечают на вопросы пациентов. Задайте вопрос врачам сервиса бесплатно, не покидая данной страницы, или здесь. Проконсультируйтесь у понравившегося врача.
Обратитесь к врачам сервиса врачебных видеоконсультаций Botkin.pro. Посмотрите, как наши врачи отвечают на вопросы пациентов. Задайте вопрос врачам сервиса бесплатно, не покидая данной страницы, или здесь. Проконсультируйтесь у понравившегося врача.
-
Панкреатит — чем питаться?
Перенес острый панкреатит. промучился 3 недели, пока не стихли боли и не прошел понос. Первые 2 дня вообще есть не давали. Выписался из стационара, а диету не расписали. Написали: «стол 5». Что это за стол?
Ваш рацион должен включать дробное питание маленькими порциями 5-6 раз в день. Пища состоит из вареных, тушенных и приготовленных на пару продуктов. Исключается алкоголь, газированные напитки, кофе, фреши, жирная, жареная, острая и копченная пища, орехи, грибы, редис, лук, чеснок, томаты, баклажаны, свежий хлеб, выпечка, вареники, блины, оладьи, кетчуп и другие соусы. В рационе преобладают каши, овощные и творожные суфле, запеканки, пюрированные супы на овощной основе, отварная курица, телятина, индейка, белая рыба.
 Мясо лучше в виде тефтель и паровых котлет. Осторожно с фруктами и овощами — можно отварную морковь, брокколи, банан, печенное яблоко. Строгую диету нужно соблюдать несколько месяцев и осторожно расширять в дальнейшем при условии удовлетворительного самочувствия.
Мясо лучше в виде тефтель и паровых котлет. Осторожно с фруктами и овощами — можно отварную морковь, брокколи, банан, печенное яблоко. Строгую диету нужно соблюдать несколько месяцев и осторожно расширять в дальнейшем при условии удовлетворительного самочувствия.
Рекомендации WSES по ведению тяжелого острого панкреатита 2019 | Всемирный журнал неотложной хирургии
Диагностика
Вопросы:
- 1.
Каковы критерии для постановки диагноза тяжелого острого панкреатита?
- 2.
Какое визуализационное обследование необходимо при подозрении на тяжелый острый панкреатит? Какова роль магнитно-резонансной томографии (МРТ), компьютерной томографии (КТ), УЗИ (УЗИ), эндоскопического УЗИ (ЭУЗИ) и других дополнительных тестов?
- 3.
Какие лабораторные параметры следует учитывать в процессе диагностики?
- 4.
Как различная этиология влияет на диагностику?
- 5.
Какие баллы указаны для оценки риска?
- 6.
Каковы сроки и подходящий тест для ранней последующей визуализации?
Заявления (оценка серьезности)
- 1.
Тяжелый острый панкреатит связан со стойкой органной недостаточностью (сердечно-сосудистой, дыхательной и / или почечной) и высокой смертностью.Обе новые системы классификации, пересмотренная атлантская классификация и основанная на детерминантах классификация острого панкреатита, схожи в установлении диагноза и степени тяжести острого панкреатита (1С).
- 2.
Пациенты со стойкой органной недостаточностью с инфицированным некрозом имеют самый высокий риск смерти (1С).
- 3.
Пациенты с недостаточностью органов по возможности должны быть госпитализированы в отделение интенсивной терапии (1С).
Обсуждение
Острый панкреатит (ОП) представляет собой заболевание, характеризующееся острым воспалением поджелудочной железы и гистологическим разрушением ацинарных клеток [6]. Диагноз AP требует наличия как минимум двух из трех следующих критериев: (i) боль в животе, соответствующая заболеванию, (ii) биохимические признаки панкреатита (уровень амилазы и / или липазы в сыворотке более чем в три раза превышает верхний предел нормы). ), и (iii) характерные результаты визуализации брюшной полости [2].
У большинства пациентов (80–85%) разовьется легкое течение болезни (самоограничение, смертность <1–3%), но около 20% будут иметь умеренный или тяжелый эпизод АП с уровнем смертности от 13 до 35 % [7, 8]. Таким образом, важно диагностировать (или лучше предсказать) эпизод тяжелого острого панкреатита (SAP) и выявить пациентов с высоким риском развития осложнений.
В течение почти 20 лет использовалась Атлантская классификация 1992 г., но некоторые определения и классификации вводили в заблуждение [9].В редакции 447 статей Bollen et al. обнаружили, что альтернативные определения Атлантской классификации 1992 г. использовались более чем в половине исследований, и что определения часто используются ошибочно [9].
Важные идеи по ведению ОП, лучшее понимание патофизиологии органной недостаточности и некротического панкреатита, улучшенная диагностическая визуализация, минимально инвазивные методы и исследования, показывающие, что пациенты в тяжелой группе классификации Атланты 1992 г. составляют подгруппы с очень разными исходами. были указанием на то, что необходима более точная классификация.
В обзоре 2004 г. Johnson et al. сообщили, что стойкая органная недостаточность (ПОЯ) более 48 часов в течение первой недели тесно связана с риском смерти или местных осложнений [10]. Они использовали предыдущую базу данных о 290 пациентах с прогнозируемым SAP, набранных из 78 больниц через 18 центров в Великобритании, а также указали, что разрешение органной недостаточности в течение 48 часов предполагает хороший прогноз.
Ретроспективное исследование 759 пациентов с АП, проведенное Эдинбургским университетом, показало, что 25.4% пациентов с синдромом стойкого системного воспалительного ответа (ССВО) умерли, по сравнению с 8% с преходящим ССВО и 0,7% без ССВО [11].
Эти и другие исследования показали, что органная недостаточность занимает центральное место в определении SAP. Если органная недостаточность сохраняется более 48 часов, пациент подвергается высокому риску смерти (один из трех), и может быть установлена «тяжелая» категория. Также важно напомнить, что период заболевания с выраженной воспалительной реакцией (ССВО) предшествовал органной недостаточности, и если ССВО присутствует, у пациента есть риск прогрессирования до органной недостаточности, и необходимо предпринимать все попытки для восстановления. нормализация как можно скорее [12].
Практически одновременно в 2012 г. были опубликованы две новые системы классификации ОП: Классификация тяжести острого панкреатита на основе детерминантов (DBC) и Пересмотренная классификация Атланты 2012 г. (RAC) [2, 13]. Новый DBC был основан на глобальном интернет-опросе и специализированном международном симпозиуме с участниками из разных дисциплин: приглашения по электронной почте были доставлены 528 панкреатологам из 55 стран, и 240 панкреатологов из 49 стран приняли участие в опросе.Во время Всемирного конгресса Международной ассоциации панкреатологов 2011 г. (Кочи, Индия) около 100 участников обсудили предложенную классификацию и попытались согласовать определения [13].
RAC был создан в ходе итеративного процесса онлайн-консультаций, включающего ответы членов 11 национальных и международных обществ поджелудочной железы. В ответ на комментарии были внесены поправки, и онлайн-консультация повторилась три раза.Был пересмотрен окончательный консенсус, и были сохранены только утверждения, основанные на опубликованных доказательствах [2]. RAC представляет собой более широкий обзор, чем DBC: помимо классификации степени тяжести, он дает четкое определение диагностики AP, выделяет начало боли как важный ориентир и определяет отдельные местные осложнения, а также интерстициальный и некротический панкреатит [2, 14]. RAC делится на три категории: легкая, умеренно тяжелая и тяжелая, в зависимости от органной недостаточности и местных или системных осложнений.DBC добавил четвертую категорию: критическую, основанную на двух основных детерминантах смертности: (пери) панкреонекрозе и органной недостаточности (таблица 2).
Таблица 2 Определение степени тяжести острого панкреатитаВпоследствии Bansal et al. в когорте из 248 пациентов было обнаружено, что RAC и DBC схожи при поступлении в ОИТ, необходимости чрескожного дренирования, хирургии и внутрибольничной смертности. Критическая категория в DBC определила самое тяжелое заболевание [15]. Nawaz et al.проспективно набрали 256 пациентов и назначили категорию тяжести для всех трех классификаций: RAC, DBC и Atlanta 1992. Они обнаружили, что категории тяжести RAC и DBC точно отражают клинические исходы и превосходят Атланту 1992 г. (оценка смертности, госпитализация, длительность ICU пребывания) [16].
Два года спустя ретроспективное исследование 395 пациентов в Китае с общей госпитальной летальностью 8,9% дало аналогичные результаты. Авторы обнаружили, что все три системы классификации (RAC, BDC и Atlanta 1992) точно классифицируют степень тяжести AP.Однако RAC и DBC работали лучше, чем Atlanta 1992, и они были сопоставимы в прогнозировании долгосрочного клинического прогноза, серьезных осложнений и клинических вмешательств [17].
Choi et al. изучение 553 пациентов с ОП, госпитализированных в один центр в течение 7-летнего периода, подтвердило, что RAC хорошо коррелирует с клиническим исходом, несмотря на то, что не учитывается инфицированный некроз. Однако пациентов в тяжелой группе и с инфицированным некрозом (классифицируемым как критический в DBC) следует рассматривать отдельно от пациентов без него (уровень смертности увеличился в четыре раза: до 32%) [18].Другое исследование проанализировало 543 эпизода ОП у 459 пациентов в проспективной когорте пациентов. Они обнаружили, что разные категории тяжести для каждой системы классификации были связаны со статистически значимыми и клинически значимыми различиями в продолжительности пребывания в больнице, необходимости госпитализации в отделение интенсивной терапии, нутритивной поддержке, инвазивном лечении и внутрибольничной смертности. Кроме того, прямое сравнение категорий обеих классификаций (после объединения тяжелой и критической категории DBC) не дало существенных различий [19].
Как правило, пациенты с органной недостаточностью (точно определенные с использованием одного из установленных критериев или систем оценки) нуждаются в срочном переводе в отделение интенсивной терапии. Соответственно, может быть ненужным переводить пациентов с преходящей органной недостаточностью ни в специализированный медицинский центр, ни в отделение интенсивной терапии. Тем не менее, чтобы подтвердить стойкую органную недостаточность, ее необходимо задокументировать в течение более 48 часов.
Выписки (визуализация)
- 1.
При поступлении необходимо провести ультразвуковое исследование (УЗИ) для определения этиологии острого панкреатита (билиарного) (1С).
- 2.
Если есть сомнения, компьютерная томография (КТ) дает хорошее доказательство наличия или отсутствия панкреатита (1С).
- 3.
Все пациенты с тяжелым острым панкреатитом должны быть обследованы с помощью компьютерной томографии с контрастным усилением (КЭ-КТ) или магнитно-резонансной томографии (МРТ). Оптимальное время для первой оценки CE-CT — 72–96 ч после появления симптомов (1C).
- 4.
Магнитно-резонансная холангиопанкреатография (MRCP) или эндоскопическое ультразвуковое исследование следует рассматривать для скрининга скрытых камней общего желчного протока у пациентов с неизвестной этиологией (1C).
Обсуждение
При поступлении следует определить этиологию ОП, чтобы спрогнозировать необходимость окончательного лечения (например, желчнокаменная болезнь) и избежать рецидива (например, прием алкоголя, гипертриглицеридемия) [20]. Лечение и последующее наблюдение зависят от этиологии ОП. При поступлении следует провести трансабдоминальное УЗИ (для выполнения холецистэктомии по поводу билиарного панкреатита, если это необходимо).Практически все мировые руководящие принципы AP (основанные на пересмотрах и мета-анализах) рекомендуют выполнять УЗИ при поступлении или в первые 48 часов [7, 8, 20, 21, 22, 23].
Большинству пациентов с ОП КТ не требуется [24]. Распространение (пери) панкреонекроза может быть обнаружено с помощью КТ с контрастным усилением (КЭКТ) через 72 часа от начала ОП [20]. Высказывались опасения по поводу постконтрастного острого повреждения почек (ОПП). Недавний метаанализ с участием 28 обсервационных исследований и более 100 000 участников не нашел доказательств, подтверждающих связь контраста с ОПП, заместительной почечной терапией или смертностью [25].Однако сравнительных исследований у пациентов с тяжелым острым панкреатитом или сепсисом нет, поэтому следует соблюдать осторожность.
Ранняя компьютерная томография не покажет некротические / ишемические области и не изменит клиническое лечение в течение первой недели болезни. Однако, если диагноз не определен, следует рассмотреть возможность проведения КТ, особенно для исключения вторичного перфорационного перитонита или мезентериальной ишемии. Также показаны активные кровоизлияния и тромбозы, связанные с панкреатитом [21, 22].
Было показано, чтоCECT дает общий уровень раннего обнаружения 90% с чувствительностью, близкой к 100%, через 4 дня для некроза поджелудочной железы [26]. Balthazar et al. установили индекс тяжести КТ (таблица 3), который классифицировал панкреатит в зависимости от степени воспаления, наличия скоплений жидкости и степени некроза: более высокий балл связан с повышенной заболеваемостью и смертностью [26,27,28].
Таблица 3 Индекс серьезности КТ (Изменено из: Balthazar EJ, Robinson DL, Megibow AJ, Ranson JH.Острый панкреатит: значение КТ для установления прогноза. Радиология. 1990; 174: 331–6 [27])CECT является методом выбора для диагностики, определения стадии и выявления осложнений острого панкреатита и играет важную роль в оценке пациентов с известным или предполагаемым ОП: (i) диагноз, (ii) определение степени тяжести и (iii) выявление осложнений, в частности идентификация и количественная оценка (пери) панкреонекроза [20, 24, 26]. Однако частые повторные компьютерные томографии увеличивают общую дозу облучения и имеют ограниченный эффект при последующем принятии решений [29].
МРТ предпочтительнее КЭКТ у пациентов с аллергией на йодированный контраст, у пациентов с почечной недостаточностью / недостаточностью (неусиленная МРТ), у молодых или беременных пациентов, чтобы свести к минимуму радиационное облучение с целью выявления несжиженного материала (например, мусора или некротической ткани). но менее чувствителен, чем КТ для обнаружения газа в коллекциях флюидов [24, 26]. КТ без контраста является альтернативой для первых двух групп пациентов, если МРТ недоступна.
Когда УЗИ не выявляет камни в желчном пузыре, ил или обструкцию желчевыводящих путей и при отсутствии холангита и / или аномальных функциональных тестов печени, предполагающих обструкцию желчевыводящих путей, вместо диагностической эндоскопической ретроградной холангиопанкреатографии используют магнитно-резонансную холангиопанкреатографию (MRCP) или эндоскопическое ультразвуковое исследование (EUS) (ERCP) следует использовать для скрининга скрытого холедохолитиаза, если нельзя установить другую этиологию [20, 24].В ретроспективной когорте, изучающей 221 пациента, MRCP имеет чувствительность 97,98% и специфичность 84,4% для холедохолитиаза, что позволяет избежать необходимости инвазивной визуализации у большинства пациентов с подозрением на холедохолитиаз [30].
Выписки (диагностические лабораторные параметры)
- 1.
Пороговое значение сывороточной амилазы и липазы обычно определяется как трехкратное превышение верхнего предела.
- 2.
Уровень С-реактивного белка ≥ 150 мг / л на третий день может использоваться в качестве прогностического фактора для тяжелого острого панкреатита (2A).
- 3.
Гематокрит> 44% представляет собой независимый фактор риска некроза поджелудочной железы (1B).
- 4.
Мочевина> 20 мг / дл выступает в качестве независимого предиктора смертности (2B).
- 5.
Прокальцитонин — наиболее чувствительный лабораторный тест для выявления инфекции поджелудочной железы, и низкие значения в сыворотке крови, по-видимому, являются сильными отрицательными предикторами инфицированного некроза (2A).
- 6.
При отсутствии камней в желчном пузыре или значительном употреблении алкоголя в анамнезе следует измерить уровни триглицеридов и кальция в сыворотке крови. Уровни триглицеридов в сыворотке выше 11,3 ммоль / л (1000 мг / дл) указывают на это как на этиологию (2C).
Обсуждение
Измерение ферментов поджелудочной железы в сыворотке крови является «золотым стандартом» для диагностики ОП [31].В эпизоде АП амилаза, липаза, эластаза и трипсин попадают в кровоток одновременно, но клиренс варьируется в зависимости от времени забора крови. Амилаза — это фермент, секретируемый поджелудочной железой, а также слюнными железами, тонкой кишкой, яичниками, жировой тканью и скелетными мышцами. Существуют две основные изоформы амилазы: панкреатическая и слюнная, и ведущей функцией является переваривание крахмала, гликогена и родственных поли- и олигосахаридов путем гидролиза [32].При АП уровни амилазы в сыворотке обычно повышаются в течение 6–24 часов, достигают максимума через 48 часов и снижаются до нормальных или близких к нормальным уровням в течение следующих 3–7 дней [23, 32, 33].
Липаза — еще один фермент, секретируемый поджелудочной железой. AP является основной причиной увеличения липазы, и многие исследователи подчеркивают, что липаза более специфична, но может быть обнаружена повышенным также при заболеваниях, не связанных с поджелудочной железой, таких как почечная недостаточность, аппендицит, острый холецистит, хронический панкреатит, непроходимость кишечника и т. Д.[23]. При AP липаза сыворотки остается повышенной в течение более длительного периода, чем сывороточная амилаза. Он повышается в течение 4-8 часов, достигает пика через 24 часа и снижается до нормального или близкого к нормальному уровню в течение следующих 8-14 дней [32, 33].
Трипсиноген — это зимоген трипсина фермента поджелудочной железы. При АП концентрация трипсиногена в сыворотке и моче обычно повышается до высоких уровней в течение нескольких часов и снижается через 3 дня [32, 33].
В совокупности липаза сыворотки считается более надежным диагностическим маркером AP, чем сывороточная амилаза.Ни один тест не показывает оптимальную диагностическую точность, но большинство текущих руководств и рекомендаций указывают, что липаза должна быть предпочтительнее общей и p-амилазы [32]. Основные причины поддержки липазы по сравнению с обоими типами амилазы для диагностики острого панкреатита включают более высокую чувствительность и большее диагностическое окно [32]. Кокрановский пересмотр с целью сравнения диагностической точности различных ферментов поджелудочной железы при диагностике ОП показал чувствительность и специфичность 72% и 93% для сывороточной амилазы и 79% и 89% для сывороточной липазы, соответственно [33].
Chang et al. В метаанализе, включающем 13 исследований, было обнаружено, что тест-полоска на трипсиноген-2 является быстрым и неинвазивным прикроватным тестом с чувствительностью 82% и специфичностью 94% для АР [34].
Многочисленные биомаркеры были изучены как потенциальные ранние предикторы тяжести ОП, так что лечение может быть оптимально адаптировано для предотвращения осложнений [34, 35]. На данный момент практически нет лабораторных тестов для прогнозирования степени тяжести ОП [23].
При отсутствии камней в желчном пузыре или значительном употреблении алкоголя в анамнезе следует измерить уровень триглицеридов в сыворотке и принять во внимание этиологию, если значение> 11,3 ммоль / л (> 1000 мг / дл) [23].
Во многих учебниках С-реактивный белок (СРБ) рассматривается как золотой стандарт оценки тяжести заболевания [36]. Используя пороговое значение от 110 до 150 мг / л, чувствительность и специфичность варьировались от 38 до 61% и от 89 до 90%, соответственно, на момент госпитализации [36].Основным недостатком CRP является то, что пиковые уровни достигаются только через 48-72 часа.
В проспективном исследовании 175 пациентов, разделенных на легкий и нелегкий острый панкреатит в соответствии с классификацией Атланты, комбинация CRP и IL-6 продемонстрировала хорошую различительную способность с площадью под кривой 0,803 [37].
Резистин — это недавно идентифицированный пептидный гормон, специфически секретируемый адипоцитами, который может вызывать ожирение и гипертриглицеридемию из-за его связи с инсулинорезистентностью.Исследования показали, что резистин также является важным цитокином при воспалительных реакциях и в регуляции других цитокинов [38]. В проспективном обсервационном исследовании уровни резистина были лучше для прогнозирования SAP, чем уровни CRP или WBC на 3 день, и лучше, чем уровни CRP для прогнозирования развития некроза [38]. Ретроспективное когортное исследование данных 90 пациентов показало, что резистин имеет аналогичную точность с оценкой Acute Physiology and Chronic Health Evaluation II (APACHE II) при прогнозировании POF, а лептин имеет слабую корреляцию с POF [39].
Другими лабораторными данными, используемыми для характеристики эпизода SAP, являются BUN> 20 мг / дл (> 7,14 ммоль / л) или повышение BUN, гематокрит (HCT)> 44% или повышение HCT, лактатдегидрогеназа (LDH) и прокальцитонин для прогнозирования инфицированный некроз у пациентов с подтвержденным панкреонекрозом [36, 40, 41, 42, 43]. Уровень прокальцитонина 3,8 нг / мл или выше в течение 96 часов после появления симптомов указывает на некроз поджелудочной железы с чувствительностью и специфичностью 93% и 79% [36, 42].Уровень лактата в сыворотке крови при поступлении позволяет прогнозировать тяжелую АП, смерть и поступление в ОИТ, но его следует рассматривать как субоптимальный как единственный маркер [44].
Заявления (диагностика при идиопатическом панкреатите)
- 1.
При идиопатическом панкреатите билиарную этиологию следует исключить с помощью двух ультразвуковых исследований и, при необходимости, MRCP и / или эндоскопического ультразвукового EUS, чтобы предотвратить рецидив панкреатита (2B).
Обсуждение
Идиопатический ОП определяется как панкреатит, этиология которого не установлена после первоначальных лабораторных и визуализирующих исследований. У пациентов с идиопатическим АП необходимо провести как минимум два УЗИ, чтобы исключить билиарную этиологию [31]. После этого КЭ-КТ и ЭУЗИ после окончания острой фазы являются следующими шагами для оценки микролитиаза, новообразования или хронического панкреатита.Если EUS отрицательный, необходимо выполнить МРТ для выявления морфологических аномалий [31]. Лапароскопическая холецистэктомия, по-видимому, предотвращает рецидивирующий идиопатический острый панкреатит; однако в настоящее время нет достаточных доказательств для повседневной поддержки этого подхода [45].
Заявление (оценка риска)
- 1.
Не существует «золотого стандарта» прогностической шкалы для прогнозирования тяжелого острого панкреатита.Вероятно, оценка прикроватного индекса тяжести острого панкреатита (BISAP) является одним из наиболее точных и применимых в повседневной клинической практике из-за простоты и возможности прогнозирования тяжести, смерти и органной недостаточности, а также APACHE-II (очень комплекс) и другие баллы (1B).
Обсуждение
Было разработано несколько систем оценки для прогнозирования SAP, но данные об их прогностической эффективности разнятся [46, 47].В настоящее время ни один систематический обзор не включал исследования, оценивающие точность различных систем клинической оценки, используемых для прогнозирования тяжести и смертности людей с острым панкреатитом. Кокрановская база данных систематических обзоров разрабатывает протокол для обобщения исследований, оценивающих прогностическую точность систем клинической оценки (измеряемой при поступлении и до 48 часов после госпитализации) [46].
Большинство оценок прогнозов в AP фокусировались на смерти как исходе.Поскольку общая смертность снижается за последние десятилетия, следует рассмотреть вопрос о том, должна ли смерть оставаться основным исходом для прогнозирования панкреатита [48].
Другой аспект заключается в том, что более или менее для всех оценок степени тяжести требуется более 24 часов для стратификации пациентов, и, вероятно, это означает потерю времени у некоторых пациентов в критическом состоянии [48]. Ретроспективное когортное исследование, проведенное в Великобритании в 159 отделениях интенсивной терапии с участием 2,462 пациентов, поступивших в отделение интенсивной терапии с SAP, показало, что 75% пациентов, которым требовалась интенсивная терапия, были переведены в отделение интенсивной терапии в течение первых 72 часов после поступления в больницу, со средним временем до -перенос через 24 ч после приема [49].
С течением времени большинство баллов основывалось на демографических характеристиках пациента, клинических характеристиках, лабораторных параметрах или методах визуализации и оценивалось при поступлении или в течение 48 часов: критерии Рэнсона (1974), оценка Глазго-Имри (1978), острая физиология и хронические заболевания. Оценка здоровья II (APACHE II), упрощенная оценка острой физиологии (SAPS II) (1984), оценка последовательной органной недостаточности (SOFA), индекс тяжести КТ (CTSI), оценка прикроватного индекса тяжести острого панкреатита (BISAP) (2008), Оценка серьезности по японскому языку [46].
Предикторы (или потенциальные предикторы), присутствующие почти во всех упомянутых выше системах оценки, включают возраст, органную недостаточность или иммунодефицит, предыдущую историю хронических заболеваний, температуру, артериальное давление, частоту пульса, частоту дыхания, индекс массы тела, уровень сознания, наличие перитонита, наличие острой почечной недостаточности, количество лейкоцитов в крови, гематокрит крови, количество тромбоцитов, глюкоза крови, азот мочевины крови, креатинин сыворотки, аспартаттрансаминаза сыворотки, лактатдегидрогеназа сыворотки, кальций сыворотки, электролиты сыворотки, билирубин сыворотки, плазма альбумин, насыщение кислородом, pH и дефицит оснований, а также различные методы визуализации, в основном КТ.
Оценка Apache II оценивает показатель хронического состояния здоровья и 12 физиологических показателей, но не специфичен для AP и не предназначен для повседневной оценки любого пациента. Преимущества этой партитуры заключаются в том, что это широко проверенный инструмент, и его можно сделать в любое время, но у него есть недостатки; т.е. громоздкие и не все параметры обычно собираются [48]. В исследовании 81 последовательного пациента с АП Thandassery et al. обнаружили, что независимыми предикторами возникновения инфицированного некроза были гипотония и оценка по шкале APACHE II через 24 часа после госпитализации [50].
В исследовании с участием 161 пациента оценивалась и сравнивалась ранняя предсказуемость различных параметров, наиболее широко используемых при ОП. Они обнаружили, что значимые пороговые значения для прогнозирования тяжелого AP были Ranson ≥ 3, BISAP ≥ 2, APACHE-II ≥ 8, CTSI ≥ 3 и CRP через 24 часа ≥ 21 мг / дл (> 210 мг / л). Они пришли к выводу, что разные системы оценки показали одинаковую точность прогнозирования тяжести ОП, но APACHE-II продемонстрировал наивысшую точность для прогнозирования SAP [51].
PPV по шкале Рэнсона колеблется от 28,6 до 49% (чувствительность 75–87%, специфичность 68–77,5%), для шкалы Глазго от 59 до 66% (чувствительность 61–71%, специфичность 88–89%), по шкале APACHE II — 55,6% через 48 часов (чувствительность 83,3%, специфичность 91%), а по шкале APACHE-O — 54–80% (чувствительность 69–74%, специфичность 86–90%). Все эти баллы можно оценить только через 48 часов и, таким образом, не позволяют стратифицировать риск при поступлении. Несмотря на свои недостатки, эти баллы по-прежнему полезны для подтверждения или исключения тяжелого заболевания [31].
BISAP, недавно разработанная прогностическая балльная система, была предложена в качестве простого метода прогнозирования тяжелого АД по сравнению с традиционными балльными системами. BISAP представляет собой аббревиатуру параметров, оцениваемых в баллах (Таблица 3) [48].
Оценка BISAP была получена с использованием данных, полученных для 17 992 пациентов, и подтверждена на 18 256 пациентах в США [52]. Он имеет такую же точность, что и оценка APACHE-II для прогнозирования смерти, и представляет собой очень упрощенную систему оценки, которую можно легко применить на самых ранних этапах.Одним из ключевых моментов этого исследования является то, что оно позволило идентифицировать пациентов с повышенным риском смертности до начала органной недостаточности [52]. Ретроспективный анализ 303 пациентов показал, что BISAP предсказывает тяжесть, смерть и особенно органную недостаточность (OF) при AP так же, как APACHE-II, и лучше, чем критерии Ranson, индекс тяжести CT, CRP, гематокрит и ИМТ. Оценка BISAP, равная двум, была статистически значимым пороговым значением для диагностики тяжелого острого панкреатита, органной недостаточности и смертности [53] (таблица 4).
Таблица 4 Оценка прикроватного индекса тяжести острого панкреатита (BISAP) [48]Многочисленные исследования указывают на то, что ИМТ, ожирение и / или избыточный вес являются независимыми факторами риска развития тяжелого ОП, местных осложнений или смерти [54, 55]. Исследование, проведенное в двух больницах из Нанкина, Китай, с использованием когорты из 1073 пациентов для разработки новой шкалы и 326 пациентов для ее проверки, подтвердило, что изменения внутрибрюшного давления (ВБД) и ИМТ в значительной степени связаны с тяжестью ОП. [46].Кроме того, они обнаружили, что новое моделирование с использованием ИМТ и изменений ВБД имеет лучшую чувствительность и специфичность (77,6% и 82,6%), чем APACHE-II (73,1% и 81,7%), BISAP (68,7% и 76,2%), CTSI ( 70,6% и 78,5%) и оценка Рэнсона (68,5% и 75,9%) соответственно [55].
Выписки (контрольные изображения)
- 1.
При тяжелом остром панкреатите (индекс тяжести компьютерной томографии ≥ 3) повторное сканирование КЭКТ показано через 7–10 дней после первоначального сканирования КТ (1С).
- 2.
Дополнительные сеансы CE-CT рекомендуются только в том случае, если клинический статус ухудшается или не показывает дальнейшего улучшения, или когда рассматривается инвазивное вмешательство (1C).
Обсуждение
Пациентам с легким ОП в большинстве случаев не требуется КТ.Этим пациентам потребуется дополнительная компьютерная томография только в том случае, если есть изменение клинического статуса пациента, которое предполагает новое осложнение [20].
Плановая контрольная КТ (например, еженедельно или каждые 10 дней) рекомендуется в нескольких руководствах, но отсутствуют доказательства, оправдывающие эту практику. Подавляющее большинство осложнений у пациента с AP / SAP можно заподозрить при клинической или лабораторной оценке [20]. Следовательно, при SAP рекомендуется дополнительное последующее сканирование только в том случае, если клиническое состояние пациента ухудшается или не показывает дальнейшего улучшения [21, 31].
Разрешение КТ-проявлений (пери) воспаления поджелудочной железы практически всегда отстает от улучшения клинического статуса пациента. Таким образом, если у пациента улучшается клинический статус, дополнительные контрольные обследования во время госпитализации рекомендуются только в том случае, если клинический статус пациента ухудшается или не показывает дальнейшего улучшения.
Лечение антибиотиками
Вопросы
- 1.
Каковы показания к антимикробной терапии при тяжелом остром панкреатите?
- 2.
Эффективна ли антибиотикопрофилактика при тяжелом стерильном остром панкреатите?
- 3.
Какое правильное время для начала антимикробной терапии?
- 4.
Какой режим антимикробных препаратов следует использовать?
- 5.
Какова правильная продолжительность антимикробной терапии?
Заявление (антибиотики профилактические)
- 1.
Последние данные показали, что профилактическое назначение антибиотиков пациентам с острым панкреатитом не приводит к значительному снижению смертности или заболеваемости. Таким образом, обычные профилактические антибиотики больше не рекомендуются для всех пациентов с острым панкреатитом (1A).
Обсуждение
Использование и эффективность профилактической антибиотикотерапии при остром панкреатите долгое время были предметом споров.Профилактика относится к назначению антибиотиков пациентам при отсутствии клинической инфекции с целью предотвращения инфекции поджелудочной железы. Хотя ранние испытания предполагали, что назначение антибиотиков может предотвратить инфекционные осложнения у пациентов со стерильным некрозом [56], последующие, лучше спланированные испытания неизменно не подтверждали преимущества. Последние данные показали, что профилактическое назначение антибиотиков пациентам с острым панкреатитом не связано со значительным снижением смертности или заболеваемости [57,58,59,60,61].Таким образом, профилактическое назначение антибиотиков всем пациентам с острым панкреатитом больше не рекомендуется.
Заявление(инфицированный некроз и антибиотики)
- 1.
Антибиотики всегда рекомендуются для лечения инфицированного тяжелого острого панкреатита. Однако диагноз затруднен из-за клинической картины, которую нельзя отличить от других инфекционных осложнений или от воспалительного статуса, вызванного острым панкреатитом (2A).
- 2.
Измерение прокальцитонина (ПКТ) в сыворотке может быть полезным для прогнозирования риска развития инфицированного панкреонекроза (1B).
- 3.
Тонкоигольная аспирация (FNA) под контролем КТ для окрашивания по Граму и посева может подтвердить инфицированный тяжелый острый панкреатит и вызвать терапию антибиотиками, но больше не используется в повседневной практике (1B).
Обсуждение
Антибиотики всегда рекомендуются для лечения инфицированного острого панкреатита. Однако диагностика инфицированного панкреатита является сложной задачей из-за клинической картины, которую нельзя отличить от других инфекционных осложнений или от воспалительного статуса, вызванного острым панкреатитом. Сроки инфицирования при панкреонекрозе изменчивы и непредсказуемы и достигают пика на второй-четвертой неделе после начала панкреатита.Клинические признаки могут быть очень чувствительными, но недостаточно специфичными [62, 63].
В ограниченном количестве небольших исследований оценивали С-реактивный белок (СРБ). Напротив, ПКТ был исследован как эффективный предиктор тяжести острого панкреатита и риска развития инфицированного панкреатита. PCT представляет собой неактивный пропептид из 116 аминокислот биологически активного гормона кальцитонина, который, как было впервые описано, имеет значительно повышенные концентрации у пациентов с бактериальными и грибковыми инфекциями [64].
Несколько исследований продемонстрировали, что измерение ПКТ в сыворотке может быть полезным для прогнозирования риска развития инфицированного панкреонекроза [65,66,67,68].
Предпочтительным диагностическим инструментом остается FNA поджелудочной железы под контролем некроза под контролем КТ. FNA под контролем КТ для окрашивания по Граму и посева может помочь клиницистам выбрать подходящую индивидуальную схему лечения антибиотиками [69, 70]. Однако из-за большого количества ложноотрицательных результатов некоторые центры отказались от рутинного использования FNA.
Наличие газа в забрюшинной области считается признаком инфицированного панкреатита в контексте тяжелого острого панкреатита, но он присутствует только у ограниченного числа пациентов [62].
Заявление (вид антибиотиков)
- 1.
У пациентов с инфицированным некрозом следует применять антибиотики, проникающие через панкреонекроз (1B).
- 2.
У пациентов с инфицированным некрозом спектр эмпирической схемы антибиотикотерапии должен включать как аэробные, так и анаэробные грамотрицательные и грамположительные микроорганизмы. Обычное профилактическое введение противогрибковых средств не рекомендуется пациентам с инфицированным острым панкреатитом, хотя Candida spp. часто встречаются у пациентов с инфицированным панкреонекрозом и указывают на пациентов с более высоким риском смерти (1B).
Обсуждение
Аминогликозидные антибиотики (например, гентамицин и тобрамицин) в стандартных внутривенных дозах не проникают в поджелудочную железу в тканевых концентрациях, достаточных для покрытия минимальной ингибирующей концентрации (МПК) бактерий, которые обычно встречаются при вторичных инфекциях поджелудочной железы [71].
Ацилуреидопенициллины и цефалоспорины третьего поколения имеют промежуточное проникновение в ткань поджелудочной железы, эффективны против грамотрицательных микроорганизмов и могут перекрывать МИК для большинства грамотрицательных микроорганизмов, обнаруживаемых при инфекциях поджелудочной железы [72].Среди этих антибиотиков только пиперациллин / тазобактам эффективен против грамположительных бактерий и анаэробов.
Хинолоны (ципрофлоксацин и моксифлоксацин) и карбапенемы демонстрируют хорошее проникновение в ткани поджелудочной железы, а также превосходное анаэробное покрытие [73,74,75,76]. Однако из-за высокого уровня устойчивости к хинолонам во всем мире не рекомендуется применять хинолоны и применять их только у пациентов с аллергией на бета-лактамные агенты. Карбапенемы из-за распространения резистентного к карбапенему Klebsiella pneumoniae следует всегда оптимизировать и применять только у очень тяжелых пациентов.
Метронидазол с его бактерицидным спектром, направленным почти исключительно против анаэробов, также хорошо проникает в поджелудочную железу.
Патогенез вторичной бактериальной инфекции поджелудочной железы все еще обсуждается. Патогены могут достигать поджелудочной железы гематогенным путем, через билиарную систему, восходящую из двенадцатиперстной кишки через главный проток поджелудочной железы или через трансмуральную миграцию через толстую кишку через транслокацию бактерий толстой кишки [77].
Большинство возбудителей инфекции поджелудочной железы — это грамотрицательные бактерии желудочно-кишечного тракта ( Escherichia coli , Proteus , Klebsiella pneumonia ), которые возникают в результате нарушения кишечной флоры и повреждения слизистой оболочки кишечника. Нарушение защитных сил организма предрасполагает к транслокации желудочно-кишечных организмов и токсинов с последующей вторичной инфекцией поджелудочной железы. Однако также были обнаружены грамположительные бактерии ( Staphylococcus aureus , Streptococcus faecalis , Enterococcus ), анаэробы и, иногда, грибы [78].
Грибковая инфекция — серьезное осложнение острого панкреатита, сопровождающееся увеличением заболеваемости и смертности [79]. Candida albicans — наиболее часто встречающийся организм, за ним следуют Candida tropicalis и Candida krusei. Хотя грибковые инфекции, осложняющие острый панкреатит, обычно возникают пропорционально степени некроза поджелудочной железы, недостаточно данных для поддержки профилактики грибковых инфекций, и поэтому не рекомендуется.
Отделение интенсивной терапии
Вопросы:
- 1.
Каковы показания для поступления в отделение интенсивной терапии (ОИТ)?
- 2.
Когда показана жидкостная реанимация и какую жидкость следует использовать? Какова оптимальная скорость инфузии жидкости и измерение ответа для начальной реанимации? Какой фармакологический подход к стойкому шоку является предпочтительным?
- 3.
Каков правильный подход к обезболиванию?
- 4.
Какие показания к ИВЛ?
- 5.
Каков медицинский подход к синдрому абдоминального компартмента? Какова роль таких лекарств, как габексат мезилат и аналоги соматостатина?
- 6.
Энтеральное питание: по каким показаниям, какой тип питания следует использовать и как лучше всего проводить энтеральное питание?
Выписка (мониторинг)
- 1.
Постоянный мониторинг жизненно важных функций в отделении интенсивной терапии необходим при нарушении функции органов.Стойкая органная дисфункция или возникновение органной недостаточности, несмотря на адекватную жидкостную реанимацию, является показанием для госпитализации в ОИТ (1С).
Обсуждение
Мировая неоднородность отделений интенсивной и промежуточной терапии затрудняет определение универсальных путей. Не существует единого маркера, позволяющего определить степень тяжести заболевания. Для оценки степени тяжести в разных фазах, местах и пациентах следует использовать несколько систем баллов.
Обширное введение жидкости, адекватное обезболивание с помощью потенциально вредных стратегий и оценка функций органов во время начального лечения — вот причина, по которой постоянный мониторинг жизненно важных функций имеет решающее значение, независимо от условий. Стойкая органная дисфункция, несмотря на адекватную жидкостную реанимацию, требующую специальной поддержки органов, обычно осуществляется только в отделениях интенсивной терапии [11, 80].
Заявление(жидкостная реанимация)
- 1.
Ранняя жидкостная реанимация показана для оптимизации целевых показателей тканевой перфузии, не дожидаясь ухудшения гемодинамики. При приеме жидкости следует руководствоваться частой переоценкой гемодинамического статуса, поскольку известно, что перегрузка жидкостью имеет пагубные последствия. Изотонические кристаллоиды являются предпочтительной жидкостью (1B).
Обсуждение
Снижение смертности, наблюдаемое за последнее десятилетие, может быть связано с профилактикой панкреонекроза путем поддержания микроциркуляции за счет более обширной инфузионной реанимации.Данные о количестве жидкости, необходимой для предотвращения некроза или улучшения исхода, противоречивы, и объем должен быть скорректирован с учетом возраста, веса пациента и ранее существовавших почечных и / или сердечных заболеваний [81].
Гематокрит, азот мочевины крови, креатинин и лактат являются лабораторными маркерами волемии и адекватной тканевой перфузии, и их следует контролировать. Лактат Рингера может быть связан с противовоспалительным действием, но доказательства превосходства лактата Рингера надфизиологический раствор, основанный на рандомизированных исследованиях, является слабым [82,83,84]. Было бы лучше скорректировать уровень калия. Значение ранней целенаправленной терапии у пациентов с острым панкреатитом остается неизвестным [81, 85].
Заявление (обезболивание)
- 1.
Нет данных или рекомендаций об ограничении приема обезболивающих. При остром повреждении почек (ОПП) следует избегать приема нестероидных противовоспалительных препаратов (НПВП).Эпидуральная анальгезия должна быть альтернативой или агонистом внутривенной анальгезии при мультимодальном подходе. Обезболивание, контролируемое пациентом (PCA), должно быть интегрировано в каждую описанную стратегию. (1C) Дилаудид предпочтительнее морфина или фентанила у неинтубированных пациентов.
Обсуждение
Боль является основным симптомом острого панкреатита, и ее облегчение является приоритетной клинической задачей.Все пациенты с острым панкреатитом должны получить какую-либо форму анальгезии в первые 24 часа госпитализации, чтобы не ухудшить качество жизни пациента. В большинстве учреждений дилаудид предпочтительнее морфина или фентанила у неинтубированных пациентов. Эпидуральная анальгезия может быть рассмотрена для тех пациентов с тяжелым и острым критическим панкреатитом, которым требуются высокие дозы опиоидов в течение длительного периода [63].
Несмотря на некоторые данные РКИ, остается неопределенность в отношении предпочтительного анальгетика и наилучшего метода введения.Вот почему лучшая текущая рекомендация — придерживаться самых последних руководств по лечению острой боли в периоперационных условиях [63].
Заявление(ИВЛ)
- 1.
Необходимо ввести механическую вентиляцию легких, если подача кислорода, даже при высоком потоке кислорода через нос или постоянное положительное давление в дыхательных путях, перестала быть эффективной для коррекции тахипноэ и одышки.Могут использоваться как неинвазивные, так и инвазивные методы, но инвазивная вентиляция является обязательной, когда очистка бронхиального секрета становится неэффективной и / или пациент устает от прогнозируемой усталости. При необходимости инвазивной вентиляции легких следует использовать стратегии защиты легких (1С).
Обсуждение
Нет вопросов по лечению дыхательной недостаточности, специфичных для этой темы.Подача кислорода, даже с помощью устройств с высоким потоком или постоянным положительным давлением, может оказаться недостаточной для поддержания дыхательной недостаточности. Различные уровни тахипноэ и одышки лишь частично оправдываются гипоксией. Боль, возможная внутрибрюшная гипертензия и плевральный выпот могут вызывать эти симптомы, несмотря на адекватную оксигенацию артерий. Повышенная системная проницаемость может вызвать отек легких после жидкостной реанимации [86, 87].
Заявление (повышенное внутрибрюшное давление)
- 1.
Предлагается ограничение седативного действия, жидкости и вазоактивных препаратов для достижения реанимационных целей при более низких пределах нормы. Для ограничения внутрибрюшной гипертензии может потребоваться глубокая седация и паралич, если все другие неоперационные методы лечения, включая чрескожный дренаж внутрибрюшинной жидкости, являются недостаточными, перед выполнением хирургической абдоминальной декомпрессии (1B)
Обсуждение
Повышенная системная проницаемость, вызванная системным воспалением и терапевтическими попытками, такими как жидкостная реанимация и вазоактивные препараты, связана с кишечной недостаточностью и ухудшением внутрибрюшного давления.Чрезмерная седация может еще больше усугубить дисфункцию кишечника с последующим повышением внутрибрюшного давления. Ограничение «обычных лекарств в ОИТ», когда побочные эффекты превосходят преимущества, имеет решающее значение [88].
Заявление (фармакологическое лечение)
- 1.
Не следует назначать какое-либо специфическое фармакологическое лечение, кроме поддержки органов и питания (1B).
Обсуждение
Несмотря на многочисленные исследования, эффективного фармакологического лечения не найдено [89].
Постановление (энтеральное питание)
- 1.
Энтеральное питание рекомендуется для профилактики кишечной недостаточности и инфекционных осложнений. Следует избегать полного парентерального питания (ПП), но следует рассмотреть возможность частичной интеграции парентерального питания для удовлетворения потребностей в калориях и белках, если энтеральный путь не переносится полностью. Можно безопасно проводить кормление как желудком, так и тощей кишкой (1A).
Обсуждение
Энтеральное питание поддерживает барьер слизистой оболочки кишечника, предотвращает его нарушение и предотвращает транслокацию бактерий, вызывающих некроз поджелудочной железы. В большинстве учреждений непрерывная инфузия предпочтительнее циклического или болюсного введения. Энтеральное питание по сравнению с полным парентеральным питанием снижает инфекционные осложнения, органную недостаточность и смертность [90].В многоцентровом рандомизированном исследовании, сравнивающем раннее назоэнтериальное зондовое питание в течение 24 часов после рандомизации с пероральной диетой, начатой через 72 часа после обращения в отделение неотложной помощи с некротическим панкреатитом, раннее назоэнтеральное кормление не снизило частоту инфицирования или смерти. В группе пероральной диеты 69% пациентов переносили пероральную диету и не нуждались в питании через зонд [91].
Хирургическое и оперативное управление
Вопросы:
- 1.
Каковы показания для неотложной ЭРХПГ при тяжелом остром панкреатите?
- 2.
Какая оперативная / хирургическая тактика является правильной при тяжелом остром панкреатите?
- 3.
Какие показания к чрескожному / эндоскопическому дренированию панкреатических скоплений (т.е., стерильный некроз, инфицированный некроз и др.)?
- 4.
Каковы показания к хирургическому вмешательству?
- 5.
Каковы сроки проведения операции и какова подходящая хирургическая стратегия (т.е., лапароскопия или лапаротомия, внутрибрюшинная или внебрюшинная, ранняя или отсроченная)?
- 6.
Когда рекомендуется холецистэктомия и каковы правильные сроки?
Выписки (показания для неотложной ERCP)
- 1.
Рутинная ЭРХПГ при остром желчнокаменном панкреатите не показана (степень 1А).
- 2.
ЭРХПГ показана пациентам с острым желчнокаменным панкреатитом и холангитом (степень 1B).
- 3.Показана
ERCP при остром желчнокаменном панкреатите с обструкцией общего желчного протока (степень 2B).
- 4.
ERCP у пациентов с прогнозируемым тяжелым острым желчнокаменным панкреатитом без холангита или обструкции общего желчного протока в настоящее время не может быть рекомендован (степень 2B).
Обсуждение
Систематический обзор семи рандомизированных контролируемых исследований (РКИ) с участием 757 человек не выявил доказательств в пользу рутинной ЭРХПГ для всех пациентов с острым желчнокаменным панкреатитом (AGP) [92].Не было никаких доказательств того, что результаты зависели от прогнозируемой тяжести AGP. Однако были высказаны опасения по поводу ограничений дизайна исследования, отсутствия объединенных выборок с прогнозируемым тяжелым AGP, а также сроков и техники ERCP. В том же метаанализе среди испытаний, в которых участвовали пациенты с холангитом, ранняя рутинная ЭРХПГ значительно снизила смертность, а также местные и системные осложнения.
У пациентов с обструкцией желчевыводящих путей ранняя рутинная ЭРХПГ была связана со значительным сокращением местных осложнений и незначительной тенденцией к снижению системных осложнений.В случае прогнозируемого тяжелого АГП рекомендации противоречивы [93]. В этом систематическом обзоре были изучены восемь метаанализов и 12 руководств и сделан вывод об отсутствии консенсуса в отношении рутинной ЭРХПГ с прогнозируемой тяжелой формой АГП. Текущее рандомизированное контролируемое исследование, исследование APEC, призвано ответить на этот вопрос [94]. Набор закончился, но результаты еще не опубликованы.
Заявление (показания к чрескожному / эндоскопическому дренированию панкреатических сборов)
- 1.
Клиническое ухудшение с признаками или сильным подозрением на инфицированный некротический панкреатит является показанием к вмешательству (чрескожное / эндоскопическое дренирование)
Через 4 недели после начала заболевания:
Продолжающаяся органная недостаточность без признаков инфицированного некроза
Продолжающаяся непроходимость выходного отверстия желудка, желчных путей или кишечника из-за большого некротического скопления, отделенного стенками
Синдром отсоединенного протока
Симптоматическая или растущая псевдокиста
Через 8 недель от начала заболевания:
(степень 1С)
Обсуждение
Доказательства показаний основаны на понимании естественного течения болезни, обосновании механизмов и нерандомизированных исследованиях.Вмешательства при некротическом панкреатите предпочтительно проводить, когда некроз перестал быть стенкой, обычно через 4 недели после начала заболевания [2].
Признаки или сильное подозрение на инфицированный некроз у пациента с симптомами требует вмешательства, хотя было показано, что небольшое количество пациентов выздоравливает только с помощью антибиотиков [1]. При ухудшении состояния пациента показан поэтапный подход, начинающийся с чрескожного или эндоскопического дренирования [20, 95, 96, 97].
Большинство пациентов со стерильным некротическим панкреатитом можно лечить без вмешательства [1]. Однако следует отметить, что почти половина пациентов, прооперированных из-за продолжающейся органной недостаточности без признаков инфицированного некроза, имеют положительную бактериальную культуру в оперативном препарате [98]. Следовательно, вмешательство следует рассматривать, если дисфункция органов сохраняется более 4 недель.
Огражденные стеной некротические скопления или псевдокисты могут вызывать симптомы и / или механическую непроходимость, и если они не исчезают после прекращения воспаления, рекомендуется повышенный подход.Симптоматическое отключение протока поджелудочной железы приводит к перипанкреатическому скоплению и является показанием для вмешательства [99, 100].
Показания (показания к оперативному вмешательству)
Показания к оперативному вмешательству являются:
Как продолжение в поэтапном подходе после чрескожной / эндоскопической процедуры с теми же показаниями
Синдром брюшной полости
Острое продолжающееся кровотечение при неудачном эндоваскулярном доступе
Ишемия кишечника или острый некротический холецистит при остром панкреатите
Кишечный свищ, переходящий в перипанкреатический сбор
(марка 1С)
Обсуждение
Доказательства показаний основаны на понимании естественного течения болезни, обосновании механизмов и нерандомизированных исследованиях.Если чрескожные или эндоскопические методы не улучшают состояние пациента, следует рассмотреть возможность дальнейших хирургических вмешательств. Синдром брюшного отдела сначала следует лечить консервативными методами [101]. Если консервативные методы недостаточны, следует рассмотреть возможность хирургической декомпрессии с помощью лапаростомии [102].
Кровотечение при остром тяжелом панкреатите может потребовать хирургического вмешательства, если эндоваскулярный доступ оказался безуспешным. Осложнения кишечника и другие экстрапанкреатические осложнения относительно редки, но могут потребовать хирургического вмешательства.
Выписка (сроки операции)
- 1.
Откладывание хирургических вмешательств более чем на 4 недели после начала заболевания снижает смертность (2B).
Обсуждение
Раннее хирургическое вмешательство сравнивалось с поздним хирургическим вмешательством в недавнем систематическом обзоре и метаанализе Восточной ассоциации хирургии травм [103].Исследование состояло из девяти исследований, одно из которых было рандомизированным контролируемым. Сроки оперативных вмешательств сравнивали в трех разных точках отсчета (72 часа, 12 дней и 30 дней). Во всех случаях поздняя операция привела к явному увеличению выживаемости. При отсроченной операции происходит отделение некроза от жизненно важных тканей, что приводит к меньшему повреждению жизненно важных тканей. Следовательно, на поздних сроках операции кровотечение меньше, а некрэктомия более эффективна.
Неизвестно, на какой срок можно отложить операцию, сможет ли пациент ее перенести, и приведет ли более длительная отсрочка к большему количеству осложнений, таких как учащение кишечных свищей или кишечная непроходимость.Если экстренное хирургическое вмешательство необходимо раньше по другим показаниям, таким как синдром брюшной полости или некроз кишечника, дренирование или некрэктомия обычно не рекомендуются [20, 97].
Выписки (хирургическая тактика)
- 1.
При инфицированном панкреонекрозе чрескожный дренаж в качестве первой линии лечения (поэтапный подход) откладывает хирургическое лечение до более благоприятного времени или даже приводит к полному разрешению инфекции у 25–60% пациентов и рекомендуется в качестве первая линия лечения (1А).
- 2.
Минимально инвазивные хирургические стратегии, такие как трансгастральная эндоскопическая некрэктомия или видеоассистированная ретроперитонеальная обработка (VARD), приводят к меньшему количеству случаев послеоперационной впервые возникшей органной недостаточности, но требуют большего количества вмешательств (1B).
- 3.
Что касается смертности, недостаточно доказательств в поддержку открытого хирургического, миниинвазивного или эндоскопического доступа (1B).
- 4.
В отдельных случаях с некрозом без стенок и у пациентов с отсоединением протока поджелудочной железы возможна одномоментная хирургическая трансжелудочная некрэктомия (2C).
- 5.
Многопрофильная группа экспертов должна индивидуализировать хирургическое лечение с учетом местной экспертизы (2C)
Обсуждение
Систематический обзор чрескожного катетерного дренажа как основного лечения некротического панкреатита включал 11 исследований и 384 пациентов [97].Инфицированный некроз был доказан у 71%, и 56% пациентов не потребовали хирургического вмешательства после чрескожного дренирования. Кроме того, чрескожный дренаж позволяет отложить возможное позднее хирургическое вмешательство на более благоприятное время.
Важный вопрос — какая стратегия предпочтительнее, если чрескожный дренаж не приводит к разрешению инфекции. Варианты лечения включают открытую хирургию, мини-инвазивную хирургию, эндоскопическую хирургию и их комбинацию.Принято считать, что открытая операция вызывает более тяжелую воспалительную реакцию. Существуют различные РКИ и обзор, в котором сравниваются разные стратегии [104, 105, 106]. Таким образом, минимально инвазивные стратегии (например, минимально инвазивный пошаговый подход, санация забрюшинного пространства с помощью видео, VARD или эндоскопия) приводят к меньшему количеству впервые возникших органной недостаточности, но требуют большего количества вмешательств. Однако никаких различий в смертности обнаружено не было. Эти выводы подтверждаются систематическим обзором [107].При интерпретации результатов следует отметить значительную неоднородность пациентов, недостаточность органов и размер, а также локализацию некроза. К тому же хирургическая техника и показания к вмешательству неоднородны.
В серии из 178 отобранных случаев некроза со стенками 96% пациентов перенесли одномоментную хирургическую трансгастральную некрэктомию с послеоперационной летальностью и заболеваемостью 2% и 38% соответственно [108].Это также хороший вариант для пациентов с синдромом отсоединенного протока.
При рассмотрении смертности важно отметить, что смертность, связанная с панкреатитом, в основном не вызвана инфицированным некрозом. Следовательно, в будущих исследованиях следует рассмотреть другие критерии оценки исходов. Эти показатели результатов должны позволять определять полное исчезновение симптомов, качество жизни, время для возвращения к нормальной повседневной деятельности или работе и необходимость дальнейших вмешательств.Следует учитывать местную экспертизу различных хирургических подходов, так как только небольшой процент пациентов требует хирургического вмешательства, и даже в крупных центрах количество операций остается небольшим. Мы рекомендуем, чтобы местная многопрофильная группа экспертов разработала индивидуальную хирургическую стратегию.
Заявления (сроки холецистэктомии)
- 1.
Лапароскопическая холецистэктомия во время первичной госпитализации рекомендуется при легком остром желчнокаменном панкреатите (1A).
- 2.
При выполнении ЭРХПГ и сфинктеротомии во время первичной госпитализации риск рецидива панкреатита снижается, но холецистэктомия при госпитализации все еще рекомендуется, поскольку существует повышенный риск других желчных осложнений (1B).
- 3.
При остром желчнокаменном панкреатите с скоплением перипанкреатической жидкости холецистэктомию следует отложить до разрешения или стабилизации скопления жидкости и прекращения острого воспаления (2C).
Обсуждение
В двух различных систематических обзорах утверждается, что индексная холецистэктомия при приеме у пациентов с умеренным AGP безопасна [109, 110]. Чтобы сократить продолжительность пребывания в стационаре и общие затраты, холецистэктомию можно выполнять уже на второй день госпитализации, если состояние пациента улучшается [111, 112].Рутинная интраоперационная холангиография, по-видимому, не нужна пациентам с легким желчнокаменным панкреатитом и нормализацией уровня билирубина [113]. Если ЭРХПГ выполнялась во время первичной госпитализации, риск рецидивов желчевыводящих путей, особенно рецидивов АГП, был снижен, но все еще выше, чем при холецистэктомии при том же госпитализации. Многоцентровое рандомизированное контролируемое исследование с участием 266 пациентов показало, что интервальная холецистэктомия приводит к увеличению числа осложнений, связанных с желчнокаменной болезнью, особенно рецидивирующего панкреатита и колик, без увеличения количества осложнений, связанных с холецистэктомией [114].Существует единственное ретроспективное исследование сроков холецистэктомии у пациентов с АГП средней и тяжелой степени с накоплением перипанкреатической жидкости [115]. В этом исследовании сообщалось о большем количестве осложнений после ранней холецистэктомии.
Открытый живот
Вопросы
- 1.
Какие показания к открытию живота при тяжелом остром панкреатите?
- 2.
Какая система временного закрытия живота лучше всего подходит для открытого живота?
- 3.
Каковы правильные сроки для смены повязки?
- 4.
Какое правильное время для закрытия живота?
Выписки (открытый живот)
- 1.
У пациентов с тяжелым острым панкреатитом, не поддающимся консервативному лечению ИАГ / ОКС, хирургическая декомпрессия и использование открытого живота эффективны при лечении синдрома брюшной полости (2C).
- 2.
Мы предлагаем клиницистам проявлять осторожность, чтобы не реанимировать пациентов с ранним SAP и регулярно измерять внутрибрюшное давление (1C).
- 3.
Мы предлагаем избегать открытого живота (ОА), если другие стратегии могут быть использованы для смягчения или лечения тяжелой внутрибрюшной гипертензии при SAP (1C).
- 4.
Мы рекомендуем не использовать ОА после некрэктомии для SAP (если только тяжелая ВБГ не требует выполнения ОА в качестве обязательной процедуры) (1С).
- 5.
Мы рекомендуем не проводить санацию или раннюю некрэктомию, если вынуждены провести ранний ОА из-за синдрома брюшной полости или висцеральной ишемии (1A).
Обсуждение
Потенциальное обоснование для потенциального использования лечения ОА у пациентов с тяжелым острым панкреатитом (SAP) исторически состояло в том, чтобы потенциально уменьшить IAH / ACS, улучшить дренаж воспалительного асцита, разрешить возможный лаваж поджелудочной железы и потенциально облегчить релапаротомию с повторной некрэктомией [ 116,117,118].
Однако в SAP отсутствуют доказательства уровня 1 относительно эффективности открытого живота для SAP, без рандомизированных контролируемых исследований (РКИ) и метаанализов. Был опубликован протокол такого исследования [119], но составители обзора не смогли найти доказательств того, что это исследование когда-либо проводилось.
В качестве следующего лучшего уровня доказательств существуют согласованные рекомендации Всемирного общества экстренной хирургии [120] и Международной ассоциации панкреатологов / Американской ассоциации поджелудочной железы [20], которые рекомендуют как медикаментозное, так и минимально инвазивное лечение тяжелых внутриклеточных заболеваний. -абдоминальная гипертензия (ИАГ), приводящая к синдрому абдоминального компартмента (ОКС) согласно алгоритмам управления синдромом абдоминального компартмента [101].Однако, осознавая, что выявленный явный ОКС всегда фатален при отсутствии лечения, потребуется открытая декомпрессивная лапаротомия (ДКЛ), которая рекомендуется, если менее инвазивные меры не эффективны. При проведении ДКЛ забрюшинную полость и малый сальниковый мешок следует оставить нетронутыми, чтобы снизить риск инфицирования перипанкреатического и панкреонекроза [20, 121].
В связи с этой основной рекомендацией есть дополнительные утверждения, которые относятся к основным принципам, согласно которым чрезмерная инфузионная реанимация, по-видимому, тесно связана с возникновением ВБГ / ОКС при тяжелом шоке и что ранняя некрэктомия не оправдана при SAP.Теперь уже классическое исследование показало, что ранняя (<72 ч) по сравнению с поздней (> 12 дней) некрэктомия имела 56% при ранних вмешательствах и 27% при поздних операциях, а интраоперационная кровопотеря была существенно снижена за счет отсроченного подхода, результаты, которые только продолжала улучшаться благодаря постоянным усовершенствованиям в хирургии и реанимации [122, 123, 124].
Выписки (ведение открытой брюшной полости и временное закрытие живота)
- 1.
Мы рекомендуем использовать перитонеальную терапию отрицательным давлением для лечения ОА (1B).
- 2.
Мы предлагаем добавить фасциальную тракцию к методам NPWT (2B).
- 3.
Мы предлагаем провести дальнейшие контролируемые исследования внутрибрюшинной осмотической терапии при SAP (нет рекомендаций)
Обсуждение
Не было РКИ или метаанализов, которые бы прямо представляли сравнительные данные о методах ОА при SAP, поэтому все доказательства будут косвенными, связанными с изучением ОА в других связанных условиях, таких как внутрибрюшинный сепсис [125, 126] или смешанные группы травматологов [127,128,129,130] с методологическими проблемами.
Исследование Pliakos примечательно тем, что рандомизированное включение фасциальных тракционных швов в дополнение к перитонеальной вакуумной терапии было значительно связано с продемонстрированным превосходством в отношении более короткой продолжительности открытого живота, меньшего количества смен повязок, снижения частоты повторных обследований, более успешного закрытия брюшной полости. частота и уменьшение энтероатмосферных свищей [125]. РКИ, в котором сравнивали активную перитонеальную терапию отрицательным давлением с более пассивным давлением, продемонстрировало улучшение смертности при повышенном перитонеальном давлении [129], подтверждая нерандомизированные результаты [130], но биологический механизм не был очевиден.Было проведено несколько метаанализов, включая данные нерандомизированных исследований, без явного превосходства какого-либо одного метода [131, 132]. Самый современный из них заключил: «Хотя наилучшие результаты с точки зрения достижения отсроченного закрытия фасции и риска энтероатмосферной фистулы были показаны для NPWT с непрерывной фасциальной тракцией, общее качество имеющихся доказательств было низким, и единообразных рекомендаций дать нельзя». [131].
Последней терапией, которую следует тщательно рассмотреть при лечении ОА, является прямая перитонеальная реанимация (DPR), внутрибрюшинная инстилляция диализирующего раствора, эффективность которой у пациентов с травмами [133].В рандомизированном контролируемом исследовании, проведенном Смитом и коллегами, интраабдоминальные осложнения (8% против 18%), частота абсцессов (3% против 14%) и 30-дневная смертность были ниже, несмотря на схожие оценки тяжести травм (13% против 28%). %; р = 0,06) (20). Поскольку нет прямых доказательств у пациентов с SAP, не было сделано никаких рекомендаций относительно DPR.
Выписка (сроки смены повязки)
- 1.
Повторное обследование открытого живота следует проводить не позднее, чем через 24–48 ч после индексации и любой последующей операции, при этом продолжительность предыдущей операции сокращается с увеличением степени неулучшения пациента и нестабильности гемодинамики (1С).
Обсуждение
Нет РКИ или метаанализов относительно сроков, когда пациента с открытой брюшной полостью следует вернуть в операционную, в частности, когда показанием ОА было SAP, или каких-либо других показаний на самом деле. Другие руководящие принципы признанных обществ также не содержат доказательств того, когда следует проводить повторную операцию с ОА [101, 131, 134, 135]. Однако в одном обзоре повторное обследование, проведенное более чем через 48 часов после первоначальной операции, привело к значительно более высокому уровню смертности; самый низкий уровень смертности (9%) был достигнут у пациентов, перенесших повторную операцию в течение 48 часов [136].
Современные данные показывают, что существует линейная корреляция между днями остеоартрита и серьезными осложнениями, такими как развитие кожно-кишечного свища [137]. Другая проспективная серия исследований отметила, что, в частности, каждый час задержки возвращения в операционную через 24 часа после начальной лапаротомии, а также снижение первичного фасциального закрытия на 1,1% и тенденция к увеличению внутрибрюшных осложнений через 48 часов [138].
В отсутствие каких-либо новых данных рецензенты SAP OA предлагают принять предыдущее современное заявление о руководящих принципах WSES OA, чтобы поддерживать согласованность между санкционированными WSES рекомендациями до тех пор, пока новые данные не потребуют возможного пересмотра [120].Поскольку общие результаты заметно улучшаются за счет отказа от ранних и ненужных вмешательств на поджелудочной железе [124], хирурги должны сопротивляться любым искушениям «вмешаться в дела поджелудочной железы», которые могут возникнуть в ходе повторной операции по поводу остеоартроза, недоступной при менее сложные случаи SAP.
Выписки (сроки закрытия живота)
- 1.
Раннее фасциальное и / или абдоминальное окончательное закрытие должно быть стратегией ведения открытой брюшной полости после того, как исчезнут любые потребности в продолжающейся реанимации, окончательно достигнут контроль источника, не останется никаких опасений относительно жизнеспособности кишечника, больше не будет повторного хирургического вмешательства. необходимо исследование, и нет никаких опасений по поводу синдрома брюшной полости (1B).
Обсуждение
Рискуя быть рассмотренным в шутку, команда авторов подчеркивает важность попытки оптимизировать превентивные стратегии ВБГ посредством тщательной и усердной реанимации, раннего внедрения медицинских и минимально инвазивных методов лечения ВБГ [101, 139, 140], чтобы попытаться чтобы избежать перехода в ACS с требованием DCL.
Отсроченное закрытие фасции определяется как формальная фасция, полученная через семь или более дней после индексной процедуры ОА [141].Стало очевидно, что количество осложнений намного выше, а первичное закрытие фасции намного ниже у тех, кто подвергается позднему закрытию по сравнению с ранним, хотя это также может быть связано с факторами пациента в неконтролируемых нерандомизированных исследованиях. Однако метаанализ показал, что по сравнению с отсроченным закрытием брюшной полости раннее ПФК было связано со снижением смертности и частоты осложнений [142]. Таким образом, бывшее Всемирное общество по синдрому абдоминального отдела рекомендовало, чтобы среди пациентов ОИТ с ОА были предприняты сознательные и / или протоколированные усилия для получения раннего или, по крайней мере, на момент госпитализации абдоминального фасциального закрытия [101].
Как и в предыдущем вопросе, до тех пор, пока не появятся новые данные об окончательном закрытии OA в SAP или любых других условиях, рецензенты предлагают принять предыдущее современное заявление руководящих принципов WSES, чтобы поддерживать согласованность между санкционированными рекомендациями WSES до тех пор, пока новые данные не потребуют возможного пересмотра [120] .
Изменения в лечении острого панкреатита
Сара Гланц, MS, RD, LD, CNSC
Если вы работаете в отделении неотложной помощи, лечение пациентов с острым панкреатитом, вероятно, уже давно устарело.НПО, чистая жидкая диета, вы знаете упражнение. Или ты? Новые рекомендации бросают вызов традиционным методам лечения и дадут вам что-то новое, о чем можно поговорить с вашей междисциплинарной командой.
Первые дела в первую очередь
Острый панкреатит — это состояние, которое может варьироваться от очень легкого (пациент сообщает о легкой боли в животе) до довольно тяжелого (возьмите тележку для аварийной остановки). Таким образом, наши рекомендации по питанию могут сильно различаться в зависимости от тяжести состояния.
Теперь мы знаем, что если пациент может терпеть это, раннее пероральное или энтеральное питание в течение первых 24 часов лучше всего как для легких, так и для тяжелых случаев.И будьте готовы к этому: не нужно начинать с прозрачных жидкостей!
Исследования не показывают разницы в переносимости пациентами жидких, твердых, мягких, обезжиренных или обычных жиров. Оказывается, питание кишечника может помочь уменьшить прогрессирование и тяжесть острого панкреатита, в первую очередь за счет сохранения целостности кишечника и предотвращения локализации бактерий. Итак, сначала выясните, может ли ваш пациент есть через рот. Если нет, начните кормление через зонд. (Правильно, я не сказал TPN. Читайте дальше…)
EN, кроме PN
Традиционное лечение панкреатита включало отдых поджелудочной железы.Он воспаленный и злой — не беспокойтесь. В результате нутритивная терапия свелась к NPO или парентеральному питанию, единственным двум вариантам, которые не обеспечивают питание кишечника и не стимулируют высвобождение ферментов поджелудочной железы. Как оказалось, энтеральное питание — это вариант , а на самом деле — лучший вариант .
Возможно, это не новость для вас. Зондирование тонкой кишки через тощую кишку рекомендовано в течение многих лет как способ воспользоваться преимуществами питания кишечника без стимуляции поджелудочной железы.Но многие учреждения испытывают трудности с безопасным и успешным размещением назоеюнальных трубок. В результате кормление через тонкий кишечник было просто невозможно. Подождите, пока не заказывайте TPN; есть больше.
Недавно исследователи изучали назогастральное кормление пациентов с острым панкреатитом. (Готовы ли вы к этому?) Они обнаружили, что нет значительной разницы между кормлением из желудка и тонкой кишки, когда речь идет о таких осложнениях, как диарея, вздутие живота, обострение боли или необходимость прибегать к ППП. И обычно было доставлено от 75 до 80 процентов предписанного количества энтерального питания. Иными словами, зондовое питание NG безопасно, хорошо переносится и подходит для пациентов с острым панкреатитом.
Теперь все зависит от вас
Верно! Теперь, когда вы знаете, что лучше всего подходит для пациентов с острым панкреатитом, пора действовать. Поделитесь хорошими новостями со своими врачами и медсестрами. И в следующий раз, когда ваш пациент с панкреатитом будет работать на девятом дне НКО, найдите трубку NG и сотворите волшебство.
Хотите узнать больше о выборе смеси для зондового питания, добавках для энтерального питания и лечении хронического панкреатита? Щелкните здесь, чтобы перейти к нашему вебинару «Рекомендации при остром и хроническом панкреатите».
Сара Гланц, MS, RD, LD, CNSC в течение двух лет работала путешествующим диетологом в Dietitians On Demand, прежде чем присоединиться к команде в качестве корпоративного диетолога. В этой роли она отстаивала программу непрерывного образования, чтобы дать диетологам повсюду возможности для достижения своих профессиональных целей.
Dietitians On Demand — это общенациональная компания по подбору персонала и найму зарегистрированных диетологов, специализирующаяся на краткосрочных, временных и постоянных должностях в отделениях неотложной помощи, долгосрочной помощи и в сфере общественного питания. Мы нацелены на диетологов и помогаем им улучшить свою практику и добиться успеха на рабочем месте. Ознакомьтесь с нашими вакансиями, запросите страховое покрытие или посетите наш магазин сегодня!
Ссылки:
Яо Х, Хе Ц, Дэн Л., Ляо Г.Энтеральное и парентеральное питание у тяжелобольных пациентов с тяжелым панкреатитом: метаанализ.
Европейский журнал клинического питания. 2018; 72: 66-68.Wu P, Li L, Sun W. Сравнение эффективности энтерального питания и парентерального питания у пациентов с тяжелым острым панкреатитом: метаанализ рандомизированных контролируемых исследований.
Bioscience Reports. https://doi.org/10.1042/BSR20181515Налли Д.М., Келли Э.Г., Кларк М., Риджуэй П.Назогастральное питание эффективно при тяжелом остром панкреатите: систематический обзор и метаанализ.
Британский журнал питания. 2014; 112: 1769-78.Теннер С, Бэйли Дж, ДеВитт Дж, Веге СС. Рекомендации Американского колледжа гастроэнтерологии: ведение острого панкреатита.
Американский журнал гастроэнтерологии. 2013: 1-16.Crockett S, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN. Руководство Института Американской гастроэнтерологической ассоциации по начальному ведению острого панкреатита.2018; 154: 1096-1101.
% PDF-1.2 % 333 0 obj> эндобдж xref 333 109 0000000016 00000 н. 0000003091 00000 н. 0000003226 00000 н. 0000003364 00000 н. 0000002476 00000 н. 0000003416 00000 н. 0000003442 00000 н. 0000003473 00000 н. 0000003719 00000 н. 0000003777 00000 н. 0000003884 00000 н. 0000003991 00000 н. 0000004098 00000 н. 0000004205 00000 н. 0000004312 00000 н. 0000004391 00000 п. 0000004470 00000 н. 0000004550 00000 н. 0000004629 00000 н. 0000004708 00000 н. 0000004786 00000 н. 0000004865 00000 н. 0000004943 00000 н. 0000005022 00000 н. 0000005100 00000 н. 0000005179 00000 н. 0000005257 00000 н. 0000005336 00000 н. 0000005414 00000 н. 0000005493 00000 п. 0000005571 00000 н. 0000005650 00000 н. 0000005728 00000 н. 0000005806 00000 н. 0000005883 00000 н. 0000005960 00000 н. 0000006036 00000 н. 0000006115 00000 п. 0000006320 00000 н. 0000006533 00000 н. 0000006598 00000 н. 0000006987 00000 н. 0000007472 00000 н. 0000008051 00000 н. 0000008216 00000 н. 0000008738 00000 н. 0000009244 00000 н. 0000026607 00000 п. 0000026956 00000 п. 0000027979 00000 п. 0000028894 00000 п. 0000029190 00000 п. 0000029472 00000 п. 0000029612 00000 п. 0000035756 00000 п. 0000036792 00000 п. 0000036982 00000 п. 0000037565 00000 п. 0000038718 00000 п. 0000039039 00000 п. 0000039204 00000 п. 0000039530 00000 п. 0000049796 00000 п. 0000050928 00000 п. 0000051998 00000 п. 0000052619 00000 п. 0000052827 00000 п. 0000053985 00000 п. 0000055130 00000 п. 0000055341 00000 п. 0000055726 00000 п. 0000056461 00000 п. 0000056695 00000 п. 0000057348 00000 п. 0000060961 00000 п. 0000061350 00000 п. 0000062146 00000 п. 0000062511 00000 п. 0000062707 00000 п. 0000062759 00000 п. 0000063046 00000 п. 0000063392 00000 п. 0000063598 00000 п. 0000064080 00000 п. 0000064640 00000 п. 0000065858 00000 п. 0000065917 00000 п. 0000065976 00000 п. 0000066035 00000 п. 0000066094 00000 п. 0000066153 00000 п. 0000066223 00000 п. 0000066303 00000 п. 0000066380 00000 п. 0000066486 00000 п. 0000066535 00000 п. 0000066640 00000 п. 0000066689 00000 п. 0000066790 00000 н. 0000066839 00000 п. 0000066943 00000 п. 0000066992 00000 п. 0000067093 00000 п. 0000067142 00000 п. 0000067268 00000 п. 0000067317 00000 п. 0000067487 00000 п. 0000067536 00000 п. 0000067584 00000 п. трейлер ] >> startxref 0 %% EOF 337 0 obj> поток ؆ а \ JgAQBAƞ˃br: i7 k! y! Iqax ± v% @ $ pigr ڐ dp> ҺKȗa% F + & ‘J8Yc> F AQMdJt70 \ lHcOqe — 㹲 s_? OU 辮 = {~ 4 Ջ MΉ $;) =) E {+ t | O «6DjIiỿ {, d? :: QJƈD-N]> KGfw [\ m * n (bu.: r \ VZP܀ Vr1ƸK ~ 3 «FN & ~ _W00Rha_ \ 3: 7JZ8X- ~ t!] 9iH 蟯 OWMkm; WGLWGs: Ez = 13J k конечный поток эндобдж 334 0 obj fz * e5x6G +) / P 65524 / U (: ѫi «GrXuTPßp) / V 1 >> эндобдж 335 0 объект> эндобдж 336 0 obj> эндобдж 338 0 obj [339 0 R] эндобдж 339 0 объектов> эндобдж 340 0 obj> эндобдж 341 0 obj [342 0 R 343 0 R 344 0 R 345 0 R 346 0 R] эндобдж 342 0 объект> эндобдж 343 0 объект> эндобдж 344 0 объект> эндобдж 345 0 объект> эндобдж 346 0 obj> эндобдж 347 0 объект> эндобдж 348 0 объектов> эндобдж 349 0 объектов> эндобдж 350 0 obj> эндобдж 351 0 объект> эндобдж 352 0 объект> эндобдж 353 0 obj> эндобдж 354 0 obj> эндобдж 355 0 obj> эндобдж 356 0 obj> эндобдж 357 0 obj> эндобдж 358 0 obj> эндобдж 359 0 obj> эндобдж 360 0 obj> эндобдж 361 0 объект> эндобдж 362 0 объект> эндобдж 363 0 obj> эндобдж 364 0 obj> эндобдж 365 0 obj> эндобдж 366 0 obj> эндобдж 367 0 obj> эндобдж 368 0 obj> эндобдж 369 0 объектов> эндобдж 370 0 объект> / XObject> / ProcSet [/ PDF / Text / ImageB] / ExtGState >>> эндобдж 371 0 объект ~ SJn
Научно обоснованные клинические рекомендации по лечению хронического панкреатита, 2015 г.
Симосегава Т., Катаока К., Камисава Т. и др. Пересмотренные японские клинические диагностические критерии хронического панкреатита. J Gastroenterol. 2010; 45: 584–91.
Артикул PubMed Google ученый
Schünemann HJ, Oxman AD, Brozek J, et al. УРОВЕНЬ: оценка качества доказательств для диагностических рекомендаций. Evid Based Med. 2008; 13: 162–3.
Артикул PubMed Google ученый
Schünemann HJ, Oxman AD, Brozek J, et al. Оценка качества доказательств и силы рекомендаций по диагностическим тестам и стратегиям. BMJ. 2008; 336: 1106–10.
PubMed Central Статья PubMed Google ученый
Guyatt GH, Oxman AD, Vist GE, et al. ОЦЕНКА: формирующийся консенсус по оценке качества доказательств и силы рекомендаций. BMJ. 2008; 336: 924–6.
PubMed Central Статья PubMed Google ученый
Pezzilli R, Talamini G, Gullo L. Поведение сывороточных ферментов поджелудочной железы при хроническом панкреатите. Dig Liver Dis. 2000. 32: 233–7.
Артикул CAS PubMed Google ученый
Вентруччи М., Гулло Л., Даниэле С. и др. Сравнительное исследование сывороточной изоамилазы, липазы и трипсиноподобной иммунореактивности поджелудочной железы при заболевании поджелудочной железы. Пищеварение. 1983; 28: 114–21.
Артикул CAS PubMed Google ученый
Амманн Р.В., Мюнч Р., Отто Р. и др. Эволюция и регресс кальцификации поджелудочной железы при хроническом панкреатите: проспективное долгосрочное исследование 107 пациентов. Гастроэнтерология. 1988; 95: 1018–28.
CAS PubMed Google ученый
Бускейл Л., Эскурру Дж., Моро Дж. И др. Эндоскопическая ультрасонография при хроническом панкреатите: сравнительное проспективное исследование с 8 стандартными ультразвуковыми исследованиями, компьютерной томографией и ERCP.Поджелудочная железа. 1995; 10: 251–7.
Артикул CAS PubMed Google ученый
Рош Т., Шусдзиарра В., Борн П. и др. Современные методы визуализации в сравнении с клинической оценкой при оценке стационарных пациентов с подозрением на заболевание поджелудочной железы. Am J Gastroenterol. 2000; 95: 2261–70.
Артикул CAS PubMed Google ученый
Бозкурт Т., Браун У., Леферинк С. и др.Сравнение морфологии поджелудочной железы и внешнесекреторных функциональных нарушений у пациентов с хроническим панкреатитом. Кишечник. 1994; 35: 1132–6.
PubMed Central Статья CAS PubMed Google ученый
Саньял Р., Стивенс Т., Новак Э. и др. MRCP с усилением секретина: обзор техники и применения с предложением количественной оценки экзокринной функции. AJR Am J Roentgenol. 2012; 198: 124–32.
Артикул PubMed Google ученый
Catalano MF, Lahoti S, Geenen JE и др. Проспективная оценка эндоскопической ультрасонографии, эндоскопической ретроградной панкреатографии и секретинового теста в диагностике хронического панкреатита. Gastrointest Endosc. 1998. 48: 11–7.
Артикул CAS PubMed Google ученый
Wiersema MJ, Hawes RH, Lehman GA, et al. Проспективная оценка результатов эндоскопической ультрасонографии и эндоскопической ретроградной холангиопанкреатографии у пациентов с хронической болью в животе с подозрением на панкреатическое происхождение.Эндоскопия. 1993. 25: 555–64.
Артикул CAS PubMed Google ученый
Бускейл Л., Эскурру Дж., Моро Дж. И др. Эндоскопическое ультразвуковое исследование при хроническом панкреатите: сравнительное проспективное исследование с обычным ультразвуковым исследованием, компьютерной томографией и ERCP. Поджелудочная железа. 1995; 10: 251–7.
Артикул CAS PubMed Google ученый
Миката Р., Исихара Т., Тада М. и др.Клиническая полезность повторной цитологии сока поджелудочной железы с помощью эндоскопической назо-панкреатической дренажной трубки у пациентов с раком поджелудочной железы. J Gastroenterol. 2013; 48: 866–73.
Артикул PubMed Google ученый
Катаока К., Ямане Ю., Като М. и др. Диагностика хронического панкреатита с использованием неинвазивных тестов внешнесекреторной функции поджелудочной железы: сравнение с тестами дуоденальной интубации. Поджелудочная железа. 1997; 15: 409–15.
Артикул CAS PubMed Google ученый
Stasi MD, Lencioni R, Solmi L, et al. Тонкоигольная биопсия новообразований поджелудочной железы под ультразвуковым контролем: результаты многоцентрового исследования. Am J Gastroenterol. 1998. 93: 1329–33.
Артикул PubMed Google ученый
Танно С., Накано Ю., Коидзуми К. и др. Аденокарциномы протоков поджелудочной железы в отдаленном периоде наблюдения у пациентов с внутрипротоковыми папиллярными муцинозными новообразованиями ветвей протока. Поджелудочная железа. 2010; 39: 36–40.
Артикул PubMed Google ученый
Ellis I, Lerch MM, Whitcomb DC. Генетическое тестирование на наследственный панкреатит: руководство по показаниям, консультированию, согласию и вопросам конфиденциальности. Панкреатология. 2001; 1: 405–15.
Артикул CAS PubMed Google ученый
Тейч Н., Мосснер Дж. Наследственный хронический панкреатит. Лучшие Практики Рес Клин Гастроэнтерол. 2008; 22: 115–30.
Артикул CAS PubMed Google ученый
Ammann RW. Клинически обоснованная система классификации хронического алкогольного панкреатита: резюме международного семинара по хроническому панкреатиту. Поджелудочная железа. 1997. 14: 215–21.
Артикул CAS PubMed Google ученый
Рамеш Х. Предложение по новой системе классификации хронического панкреатита. J Clin Gastroenterol. 2002; 35: 67–70.
Артикул CAS PubMed Google ученый
Вентруччи М., Гулло Л., Даниэле С. и др. Сравнительное исследование сывороточной изоамилазы, липазы и трипсиноподобной иммунореактивности поджелудочной железы при заболевании поджелудочной железы. Пищеварение. 1983; 28: 114–21.
Артикул CAS PubMed Google ученый
Камисава Т., Мацукава М., Йошиике М. и др. Хронический панкреатит, прогрессирующий из сегментарных поражений. Гепатогастроэнтерология. 2005; 52: 1255–8.
PubMed Google ученый
Оцуки М. Хронический панкреатит: проблемы диагностических критериев. Панкреатология. 2004; 4: 28–41.
Артикул PubMed Google ученый
Каталано М.Ф., Сахай А., Леви М. и др. Критерии диагностики хронического панкреатита на основе EUS: классификация Rosemont. Gastrointest Endosc. 2009; 69: 1251–61.
Артикул PubMed Google ученый
Китагава М., Нарусэ С., Исигуро Х. и др. Оценка тестов внешнесекреторной функции для диагностики хронического панкреатита. Поджелудочная железа. 1997; 15: 402–8.
Артикул CAS PubMed Google ученый
Катаока К., Ямане И., Като М. и др. Диагностика хронического панкреатита с использованием неинвазивных тестов внешнесекреторной функции поджелудочной железы: сравнение с тестами дуоденальной интубации. Поджелудочная железа. 1997; 15: 409–15.
Артикул CAS PubMed Google ученый
Хаякава Т., Кондо Т., Шибата Т. Взаимосвязь между внешнесекреторной функцией поджелудочной железы и гистологическими изменениями при хроническом панкреатите. Am J Gastroenterol. 1992; 87: 1170–4.
CAS PubMed Google ученый
Коидзуми М., Йошида Ю., Абэ Н. и др. Сахарный диабет в Японии. Поджелудочная железа. 1998. 16: 385–91.
Артикул CAS PubMed Google ученый
Чари СТ, Певица М.В. Проблема классификации и стадирования хронического панкреатита. Сканд Дж Гастроэнтерол. 1994; 29: 949–60.
Артикул CAS PubMed Google ученый
Шнайдер А., Лер Дж. М., Зингер М. В.. Классификация хронического панкреатита M-ANNHEIM: введение единой системы классификации, основанной на обзоре предыдущих классификаций болезни. J Gastroenterol. 2007; 42: 101–19.
Артикул PubMed Google ученый
Etemad B, Уиткомб, округ Колумбия. Хронический панкреатит: диагностика, классификация и новые генетические разработки. Гастроэнтерология. 2001; 120: 682–707.
Артикул CAS PubMed Google ученый
Axon AT, Classen M, Cotton PB, et al. Панкреатография при хроническом панкреатите: международные определения. Кишечник. 1984; 25: 1107–12.
PubMed Central Статья CAS PubMed Google ученый
Ammann RW. Диагностика и лечение хронического панкреатита: современные знания. Swiss Med Wkly. 2006; 136: 166–74.
PubMed Google ученый
Накамура Т., Такеучи Т., Тандо Ю. Дисфункция поджелудочной железы и варианты лечения. Поджелудочная железа. 1998. 16: 329–36.
Артикул CAS PubMed Google ученый
Маротта Ф., О’Киф С.Дж., Маркс И.Н. и др.Заместительная терапия ферментами поджелудочной железы: важность секреции кислоты желудочного сока, антагонисты h3 и энтеросолюбильное покрытие. Dig Dis Sci. 1989; 34: 456–61.
Артикул CAS PubMed Google ученый
Ланкиш П.Г. Ферментное лечение внешнесекреторной недостаточности поджелудочной железы при хроническом панкреатите. Пищеварение. 1993; 54 (Дополнение 2): 21–9.
Артикул PubMed Google ученый
Layer P, Keller J, Lankisch PG. Заместительная терапия панкреатическими ферментами. Curr Gastroenterol Rep. 2001; 3: 101–8.
Артикул CAS PubMed Google ученый
Накамура Т., Араи Ю., Тандо И. и др. Влияние омепразола на изменение уровня pH желудка и верхнего отдела тонкой кишки у пациентов с хроническим панкреатитом. Clin Ther. 1995; 17: 448–59.
Артикул CAS PubMed Google ученый
Lankisch PG. Острый и хронический панкреатит: новая информация о лечении. Наркотики. 1984. 28: 554–64.
Артикул CAS PubMed Google ученый
Scolapio JS, Malhi-Chowla N, Ukleja A. Пищевые добавки у пациентов с острым и хроническим панкреатитом. Гастроэнтерол Clin North Am. 1999; 28: 695–707.
Артикул CAS PubMed Google ученый
Perry RS, Gallagher J. Управление нарушением пищеварения, связанным с недостаточностью поджелудочной железы. Clin Pharm. 1985; 4: 161–9.
CAS PubMed Google ученый
Кавабе К., Ито Т., Игараси Х. и др. Текущие методы лечения диабета поджелудочной железы в Японии. Clin J Gastroenterol. 2009; 2: 1–8.
Артикул PubMed Google ученый
Ито Т., Оцуки М., Игараси Х. и др.Эпидемиологическое исследование диабета поджелудочной железы в Японии в 2005 г .: общенациональное исследование. Поджелудочная железа. 2010; 39: 829–35.
Артикул PubMed Google ученый
Daniel JD, Michael AN. Инкретиновая система: агонисты рецепторов глюкагоноподобного пептида-1 и ингибиторы дипептидилпептидазы-4 при диабете 2 типа. Ланцет. 2006; 368: 1969–75.
Google ученый
Елашов М., Матвеенко А.В., Гиер Б. и др.Панкреатит, рак поджелудочной железы и щитовидной железы с терапией на основе глюкагоноподобного пептида-1. Гастроэнтерология. 2011; 141: 150–6.
PubMed Central Статья CAS PubMed Google ученый
Butler PC, Elashoff M, Elahoff R, et al. Критический анализ клинического использования препаратов на основе инкретина: безопасны ли методы лечения GLP-1? Уход за диабетом. 2013; 36: 2118–25.
PubMed Central Статья PubMed Google ученый
Доре Д.Д., Хусейн М., Хоффман С. и др. Объединенный анализ использования эксенатида и риска острого панкреатита. Curr Med Res Opin. 2013; 29: 1577–86.
Артикул CAS PubMed Google ученый
Наук М.А. Критический анализ клинического использования препаратов на основе инкретина: преимущества намного перевешивают потенциальные риски. Уход за диабетом. 2013; 36: 2126–32.
PubMed Central Статья PubMed Google ученый
Бэнкс ПА, Боллен Т.Л., Дервенис С. и др. Классификация острого панкреатита – 2012: пересмотр классификации и определений Атланты на основе международного консенсуса. Кишечник. 2013; 62: 102–11.
Артикул PubMed Google ученый
Varadarajulu S, Bang JY, Sutton BS, et al. Равная эффективность эндоскопической и хирургической цистогастростомии для дренирования псевдокисты поджелудочной железы в рандомизированном исследовании. Гастроэнтерология. 2013; 145: 583–90.
Артикул PubMed Google ученый
Nealon WH, Walser E. Одного проточного дренажа достаточно для оперативного лечения псевдокисты поджелудочной железы у пациентов с хроническим панкреатитом. Ann Surg. 2003; 237: 614–20.
PubMed Central PubMed Google ученый
Schlosser W, Siech M, Beger HG. Лечение псевдокисты при хроническом панкреатите: хирургическое лечение основного заболевания увеличивает долгосрочный успех.Dig Surg. 2005; 22: 340–5.
Артикул PubMed Google ученый
Olakowski M, Mieczkowska-Palacz H, Olakowska E, et al. Хирургическое лечение панкреатикоплевральных свищей. Acta Chir Belg. 2009; 109: 735–40.
CAS PubMed Google ученый
Таджима Ю., Цуцуми Р., Куроки Т. и др. Оценка и лечение торакопанкреатической фистулы. Операция.2006; 140: 773–8.
Артикул PubMed Google ученый
Ohge H, Yokoyama T, Kodama T, et al. Хирургические доступы при асците поджелудочной железы: отчет о трех случаях. Хирург сегодня. 1999; 29: 458–61.
Артикул CAS PubMed Google ученый
Dumonceau JM, Tringali A, Blero D, et al. Стентирование желчевыводящих путей: показания, выбор стентов и результаты: клинические рекомендации Европейского общества гастроинтестинальной эндоскопии (ESGE).Эндоскопия. 2012; 44: 277–89.
Артикул PubMed Google ученый
Lermite E, Regenet N, Tuech JJ, et al. Диагностика и лечение поджелудочной железы: развитие эндоваскулярной терапии. Поджелудочная железа. 2007. 34: 229–32.
Артикул PubMed Google ученый
Инуи К., Тадзума С., Ямагути Т. и др. Лечение камней поджелудочной железы методом экстракорпоральной ударно-волновой литотрипсии.Поджелудочная железа. 2005; 30: 26–30.
PubMed Google ученый
Охара Х., Хосино М., Хаякава Т. и др. Однократная экстракорпоральная ударно-волновая литотрипсия — лучший выбор для пациентов с камнями протока поджелудочной железы. Am J Gastroenterol. 1996; 91: 1388–94.
CAS PubMed Google ученый
Зауэрбрух Т., Холл Дж., Паумгартнер Г. Экстракорпоральная литотрипсия камней поджелудочной железы у пациентов с хроническим панкреатитом и болью: проспективное последующее исследование.Кишечник. 1992; 33: 969–72.
PubMed Central Статья CAS PubMed Google ученый
Хаякава Т., Кондо Т., Шибата Т. и др. Хронический алкоголизм, эволюция боли и прогноз при хроническом панкреатите. Пищеварение. 1993; 54: 148–55.
Артикул Google ученый
Lankisch PG, Lohr-Happe A, Otto J, et al. Естественное течение при хроническом панкреатите.Пищеварение. 1993; 54: 148–55.
Артикул CAS PubMed Google ученый
Мияке Х., Харада Х., Куничика К. и др. Клиническое течение и прогноз хронического панкреатита. Поджелудочная железа. 1987; 2: 378–85.
Артикул CAS PubMed Google ученый
Андриулли А., Боттери Э., Алмасио П.Л. и др. Курение как кофактор хронического панкреатита: метаанализ.Поджелудочная железа. 2010; 39: 1205–10.
Артикул PubMed Google ученый
Каваллини Дж., Таламини Дж., Ваона Б. и др. Влияние алкоголя и курения на литогенез поджелудочной железы при хроническом панкреатите. Поджелудочная железа. 1994; 9: 42–6.
Артикул CAS PubMed Google ученый
Imoto M, DiMagno EP. Курение сигарет увеличивает риск кальцификации поджелудочной железы при позднем, но не раннем идиопатическом хроническом панкреатите.Поджелудочная железа. 2000; 21: 115–9.
Артикул CAS PubMed Google ученый
Канох М., Ибата Х., Миягава М. и др. Клинические эффекты камостата при хроническом панкреатите. Biomed Res. 1989; 10 (Дополнение 1): 145–50.
Google ученый
Cahen DL, Gouma DJ, Laramée P, et al. Отдаленные результаты эндоскопического и хирургического дренирования протока поджелудочной железы у пациентов с хроническим панкреатитом.Гастроэнтерология. 2011; 141: 1690–5.
Артикул PubMed Google ученый
Dumonceau JM, Delhaye M, Tringali A, et al. Эндоскопическое лечение хронического панкреатита: Клинические рекомендации Европейского общества гастроинтестинальной эндоскопии (ESGE). Эндоскопия. 2012; 44: 784–800.
Артикул PubMed Google ученый
Катаока К., Сакагами Дж., Хирота М. и др.Эффекты перорального приема элементарной диеты у пациентов с болезненным хроническим панкреатитом в реальных условиях в Японии. Поджелудочная железа. 2014; 43: 451–7.
Артикул CAS PubMed Google ученый
Lowenfels AB, Maisonneuve P, Cavallini G, et al. Панкреатит и риск рака поджелудочной железы: Международная исследовательская группа по панкреатиту. N Engl J Med. 1993; 328: 1433–147.
Артикул CAS PubMed Google ученый
Камисава Т., Ту И, Эгава Н. и др. Заболеваемость раком поджелудочной железы и экстрапанкреатическим раком у японских пациентов с хроническим панкреатитом. Гепатогастроэнтерология. 2007. 54: 1579–81.
PubMed Google ученый
Capurso G, Falconi M, Panzuto F, et al. Факторы риска спорадических эндокринных опухолей поджелудочной железы: исследование случай-контроль проспективно оцениваемых пациентов. Am J Gastroenterol. 2009. 104: 3034–304.
Артикул CAS PubMed Google ученый
Lankisch MR, Imoto M, Layer P и др. Влияние небольшого количества алкоголя на клиническое течение хронического панкреатита. Mayo Clin Proc. 2001; 76: 242–51.
Артикул CAS PubMed Google ученый
Arvanitakis M, Van Laethem JL, Parma J, et al. Факторы прогнозирования рака поджелудочной железы у пациентов с хроническим панкреатитом в связи с мутацией гена K-ras. Эндоскопия. 2004; 36: 535–42.
Артикул CAS PubMed Google ученый
Лер М., Мюллер П., Мора Дж. И др. Мутации p53 и K-ras в образцах сока поджелудочной железы пациентов с хроническим панкреатитом. Gastrointest Endosc. 2001; 53: 734–43.
Артикул PubMed Google ученый
Нойгаард С., Бендтсен Ф., Беккер У. и др. У датских пациентов с хроническим панкреатитом уровень смертности в четыре раза выше, чем у датского населения. Clin Gastroenterol Hepatol. 2010; 8: 384–90.
Артикул PubMed Google ученый
Lankisch PG, Löhr-Happe A, Otto J, et al. Естественное течение при хроническом панкреатите: боль, внешнесекреторная и эндокринная недостаточность поджелудочной железы и прогноз заболевания. Пищеварение. 1993; 54: 148–55.
Артикул CAS PubMed Google ученый
Кноп Ф.К., Вилсболл Т., Ларсен С. и др. Отсутствие гипогликемии после подкожного введения глюкагоноподобного пептида-1 у худых пациентов с диабетом 2 типа и у пациентов с диабетом, вторичным по отношению к хроническому панкреатиту.Уход за диабетом. 2003. 26: 2581–7.
Артикул CAS PubMed Google ученый
Энтеральное питание и острый панкреатит: обзор
Введение . Пациентам с острым панкреатитом (ОП) необходима нутритивная поддержка, если нормальная пища не переносится в течение нескольких дней. Энтеральное питание предпочтительнее парентерального. Мы рассмотрели литературу по энтеральному питанию при АП. Методы .Поиск в MEDLINE англоязычной литературы между 1999–2009 гг. Результатов . Кормление через назогастральный зонд, по-видимому, безопасно и хорошо переносится большинством пациентов с тяжелым ОП, что делает концепцию покоя поджелудочной железы менее вероятной. Энтеральное питание благотворно влияет на исход АП и, вероятно, должно быть начато как можно раньше (в течение 48 часов). Прием энтеральных смесей с глутамином или пребиотиками и пробиотиками не может быть рекомендован в обычном порядке. Выводы . Нутритивная терапия у пациентов с ОП превратилась из поддерживающей дополнительной терапии в превентивное первичное вмешательство. Необходимы крупные многоцентровые исследования, чтобы подтвердить безопасность и эффективность назогастрального кормления и изучить роль поддержки в раннем питании.
1. Введение
Острый панкреатит (ОП) варьируется от легкого и самоизлечивающегося заболевания (80%), которое обычно проходит спонтанно в течение нескольких дней, до быстро прогрессирующего молниеносного заболевания со значительной заболеваемостью и смертностью [1, 2].Двумя наиболее частыми этиологическими факторами, составляющими более 80% случаев, являются камни в желчном пузыре и злоупотребление алкоголем [1, 3].
Клиническое течение приступа ОП варьируется от короткого периода госпитализации с поддерживающей терапией до длительной госпитализации и помещения в отделение интенсивной терапии (ОИТ) из-за развития синдрома системного воспалительного ответа (ССВР), полиорганной недостаточности (ПОН). ) и септические осложнения. В целом, примерно у 15-20% пациентов АП прогрессирует до тяжелого заболевания с продолжительным течением болезни.У этих тяжело больных пациентов может развиться органная недостаточность и / или местные осложнения, такие как некроз поджелудочной железы. У пациентов с некротическим панкреатитом смертность близка к 17%, смертность составляет 12% в случае стерильного некроза и до 30% в случае инфицированного некроза [1].
Обычно начальное лечение АП состоит из режима без перорального введения (NPO) и введения анальгетиков и большого количества внутривенных жидкостей [1, 2, 4]. Обоснованием периода без приема пищи является предположение, что стимуляция поджелудочной железы энтеральным кормлением может усугубить воспаление поджелудочной железы.Обоснованность этой концепции «панкреатического покоя» активно обсуждается [5–7]. Более того, многие пациенты страдают анорексией и могут испытывать усиление болевых ощущений во время еды, а также тошноту и рвоту, связанные с кишечной непроходимостью. Возобновление перорального кормления зависит от уменьшения боли в животе, отсутствия тошноты и рвоты и восстановления аппетита. Нутритивная поддержка требуется тем пациентам, которые не могут переносить нормальную пищу в течение нескольких дней [1, 4, 8, 9].
На сегодняшний день имеются серьезные научные доказательства того, что энтеральное питание превосходит полное парентеральное питание (ПП) [5, 6, 10–15].Благоприятное влияние энтерального питания на целостность слизистой оболочки и предотвращение избыточного бактериального роста вполне может объяснить превосходство энтерального питания над парным парентеральным питанием [16, 17]. Энтеральное питание значительно снижает риск инфекций, снижает потребность в хирургических вмешательствах и сокращает продолжительность пребывания в больнице [5, 6, 10–12, 15, 18]. Недавно Петров и его коллеги пришли к выводу в своем метаанализе, что смертность значительно снижается, когда пациенты с прогнозируемым тяжелым АД получают энтеральное питание [14].Важно отметить, что это снижение смертности у пациентов с тяжелым ОП также может быть связано со сроком начала питания, в пределах 48 часов после госпитализации [13]. Каждый раз, когда начинается энтеральное питание, следует учитывать такие вопросы, как идеальный состав, время и способ доставки, поскольку все они могут повлиять на исход АП. Пациенты, которые не переносят энтеральное питание, должны получать парентеральное питание до тех пор, пока они не смогут переносить энтеральное питание [9]. В этом обзоре дается обновленная информация о некоторых аспектах энтерального питания при легком и тяжелом ОП.
2. Покой поджелудочной железы и секреция поджелудочной железы
Попыткам не отставать от повышенных энергетических потребностей в случае АП мешает пословица о покое поджелудочной железы и избегании стимуляции поджелудочной железы посредством питания просвета кишечника. Как упоминалось во введении, эта пословица заслуживает пересмотра. Концепция «покоя поджелудочной железы» предполагает, что покой поджелудочной железы способствует заживлению, уменьшает боль и снижает секрецию и утечку сока поджелудочной железы в паренхиму поджелудочной железы и перипанкреатическую ткань [19].Концепция панкреатического покоя восходит к классической работе Ragins et al. на основе модели собаки [20]. Они продемонстрировали, что питание тощей кишкой не стимулировало секрецию поджелудочной железы в отличие от внутрижелудочного или интрадуоденального кормления. Однако эта концепция «остановки поджелудочной железы» игнорирует постоянство базальной экзокринной секреции поджелудочной железы. Из трех компонентов секреции поджелудочной железы (белковые ферменты, объем жидкости и бикарбонат) продукция белковых ферментов отвечает за самопереваривание железы и продолжение воспалительного процесса [19].Следовательно, подавление выработки белковых ферментов при продолжении выработки объема бикарбоната и жидкости может быть достаточным для того, чтобы успокоить поджелудочную железу.
2.1. Физиология секреции поджелудочной железы
Базальная секреция ферментов составляет 20% от максимальной секреции ферментов и регулируется холинергическими и холоцистокинин-опосредованными механизмами. Кормление через рот увеличивает секрецию поджелудочной железы за счет трех уровней стимуляции через три взаимосвязанные фазы: головную, желудочную и кишечную [21, 22].Головная фаза опосредуется прямой холинергической стимуляцией блуждающим нервом на ацинарных клетках поджелудочной железы. Блуждающий нерв также действует косвенно, стимулируя высвобождение гастрина из антрального отдела и высвобождение вазоактивного кишечного пептида (VIP) из тонкой кишки. Желудочная фаза панкреатической секреции полностью не выяснена. Гастрин влияет на секрецию поджелудочной железы посредством двух механизмов: секреция желудочного сока, приводящая к секреции секретина, когда низкий pH достигает двенадцатиперстной кишки, и прямое воздействие гастрина на ацинарные клетки с образованием секреции, богатой ферментами.Кишечная фаза отвечает за большую часть постпрандиального экзокринного секреторного выброса поджелудочной железы и управляется множеством медиаторов: блуждающим нервом, CCK и VIP, секретиноподобным гормоном и холинергическими энтеропанкреатическими рефлексами.
Выход ферментов поджелудочной железы человека достигает максимальных значений после смешанного приема пищи 20 ккал / кг массы тела [23, 24]. Продолжительность ответа увеличивается с увеличением калорийной нагрузки. На реакцию поджелудочной железы также влияют физические свойства еды: смешанная твердо-жидкая еда вызывает более высокую реакцию, чем жидкая или гомогенизированная еда с аналогичным содержанием энергии.В обоих случаях скорость опорожнения желудка и, следовательно, доставка питательных веществ через двенадцатиперстную кишку являются ключевыми факторами, определяющими продолжительность панкреатической секреции. Соотношение содержания жиров, углеводов и белков в пище также влияет на продолжительность и ферментный состав ответа поджелудочной железы у людей.
2.2. Секреция поджелудочной железы при общем энтеральном питании
Недавние исследования на людях показали, что все распространенные формы энтерального питания в некоторой степени стимулируют поджелудочную железу, и только парентеральное питание позволяет избежать стимуляции поджелудочной железы [25, 26].Существуют значительные доказательства того, что степень стимуляции поджелудочной железы энтеральным питанием (ЭП) определяется участком желудочно-кишечного тракта, в котором происходит инфузия пищи. Питание, введенное в тощую кишку за связкой Treitz, может обойти головную, желудочную и кишечную фазы стимуляции секреции поджелудочной железы, с меньшей вероятностью будет стимулировать CCK и секретин и может стимулировать ингибирующие полипептиды [27–29]. В исследованиях на людях во время кормления тощей кишкой было продемонстрировано, что выработка фермента поджелудочной железы значительно увеличилась по сравнению с базальным уровнем, когда он был доставлен в связку Treitz, тогда как не было значительного увеличения при более дистальном кормлении тощей кишкой, на 60 см от связки Treitz [ 30].Более недавнее исследование на здоровых добровольцах показало, что ЭП можно давать без стимуляции секреции трипсина поджелудочной железы при условии, что он доставляется в средне-дистальный отдел тощей кишки [31]. Кормление с 20 до 120 см за связку Трейца не имело стимулирующего эффекта.
Также важен состав настоянных кормов. Существует множество доказательств, подтверждающих дополнительное преимущество элементных формул для остановки поджелудочной железы по сравнению со стандартными смесями с интактным белком или смешанными диетами [19].Элементарные диеты вызывают меньшую стимуляцию, чем стандартные смеси, из-за их низкого содержания жира, наличия свободных аминокислот вместо интактных белков, которые связываются со свободным трипсином в кишечнике, вызывая падение уровня трипсина и меньшее производство кислоты в желудке.
2.3. Результаты панкреатического покоя
Вопрос о том, играет ли панкреатический отдых роль у пациентов с тяжелым ОП, все еще остается неясным, поскольку для ответа на этот конкретный вопрос не проводились надежные рандомизированные проспективные исследования [6].Необходимость панкреатического покоя вообще ставится под сомнение по результатам нескольких исследований, сравнивающих назогастральное и назоеюнальное кормление при тяжелом ОП, поскольку назогастральное кормление, по-видимому, безопасно и хорошо переносится [32, 33].
Приведение поджелудочной железы в покой основано на предположении, что воспаленная и / или некротизированная поджелудочная железа все еще является секретором активированных ферментов после стимуляции. Исследования на животных показали, что экзокринная секреция поджелудочной железы в экспериментальном AP в ответ на стимуляцию CCK подавляется [34].Небольшое проспективное исследование показало, что внешнесекреторная недостаточность поджелудочной железы часто встречается у пациентов, выздоравливающих после тяжелого АП; его тяжесть коррелировала со степенью некроза поджелудочной железы [35]. Другое исследование продемонстрировало, что секреция трипсина у пациентов с ОП, особенно с некротизирующим АП, значительно подавлена по сравнению со здоровыми людьми. Однако, несмотря на такую низкую скорость секреции просвета, скорость появления вновь синтезированного трипсина не изменилась [36]. Таким образом, более вероятным альтернативным объяснением отсутствия обострения заболевания во время ЭП является то, что поджелудочная железа становится менее восприимчивой к стимуляции ЭП во время атаки АП и что секреторный ответ на ЭП подавляется с базовой скоростью [34, 37].Тем не менее, все еще есть некоторые сомнения в том, полностью ли подавлена секреция поджелудочной железы. В целом концепция панкреатического покоя кажется менее вероятной.
3. Результаты нутриционной поддержки
Нутриционная терапия в прошлом руководствовалась принципом, согласно которому кишечник должен находиться в покое, избегая любой стимуляции экзокринной секреции поджелудочной железы. Эти концепции теперь следует заменить принципом, согласно которому стимуляция поджелудочной железы должна быть снижена до базовых, но при этом целостность кишечника должна быть сохранена, а стрессовая реакция должна сдерживаться, чтобы снизить вероятность полиорганной недостаточности, внутрибольничных инфекций и смертности [38]. .
Остается вопрос, является ли нутритивная поддержка благоприятной для исхода ОП. Пауэлл и др. опубликовали единственное рандомизированное контролируемое исследование, сравнивающее ЭП с отсутствием нутритивной поддержки, и изучили влияние ранней ЭП на маркеры воспалительного ответа при тяжелом ОП [39]. Диетотерапия, проводимая энтеральным путем, не оказала более благоприятного влияния на исход лечения пациента, чем стандартная терапия, поскольку не было обнаружено различий между двумя группами в отношении общих осложнений, продолжительности пребывания в больнице или времени для возобновления пероральной диеты.Сывороточные маркеры воспаления оказались ниже в группе, получавшей ЭП, по сравнению с группами, рандомизированными для стандартной терапии, но ни одно из различий не было статистически значимым. Результаты этого исследования показывают, что низкокалорийная ЭП не влияет на воспалительную реакцию при тяжелом ОП, но следует указать ограничения в дизайне исследования: только 21% потребностей в калориях вводили в группу ЭН, продолжительность исследования было всего 4 дня, и было набрано небольшое количество пациентов.
Как уже упоминалось, поджелудочная железа находится в состоянии невосприимчивости во время атаки AP, а секреция панкреатического сока и трипсина снижается во время AP [34, 37]. Eckerwall et al. исследовали роль немедленного перорального кормления по сравнению с голоданием у 60 пациентов с ОП [40]. Все пациенты получали начальную агрессивную жидкостную реанимацию для поддержания объема внутрисосудистого кровообращения, микроциркуляции и функции почек, тем самым сводя к минимуму степень ишемии и реперфузионного повреждения.По сравнению с пациентами, принимавшими пищу натощак, у группы, получавшей пероральное питание, был значительно более короткий период внутривенного введения жидкости, меньшее количество дней голодания и введение твердой пищи на 2 дня раньше без различий в химическом составе крови, желудочно-кишечных симптомах, осложнениях и вмешательствах. В группе, получавшей пероральное питание, продолжительность пребывания в больнице была значительно короче на 2 дня без различий в повторяющихся приступах панкреатита при последующем наблюдении в течение 3 месяцев.
4. Модификации энтерального питания
4.1. Стандартный состав: элементные, полуэлементные или полимерные формулы
На сегодняшний день существует немного исследований, сравнивающих результаты кормления элементарными, полуэлементными и полимерными диетами пациентов с ОП [7, 15]. Формула Elemental полностью предварительно переварена и состоит из аминокислот, простых сахаров и достаточного количества жиров, чтобы предотвратить дефицит незаменимых жирных кислот. Полуэлементные смеси требуют меньшего переваривания, чем полимерные пищевые продукты, и содержат пептиды с различной длиной цепи, простые сахара, полимеры глюкозы или крахмал и жир, главным образом в виде триглицеридов со средней длиной цепи.Полимерные корма содержат негидролизованные белки, сложные углеводы и длинноцепочечные триглицериды. Основываясь на предположении, что элементарные и полуэлементные формулы вызывают меньшую стимуляцию поджелудочной железы, чем стандартные формулы, в большинстве исследований EN использовались элементарные или полуэлементные формулы. Казалось бы, расположение энтеральной трубки так же важно, как и тип энтеральных формул для стимуляции секреции поджелудочной железы. Существует немного данных об использовании стандартной энтеральной смеси у таких пациентов.Оба Виндзор и др. и Pupelis et al. показали, что полимерная смесь может безопасно вводиться через трубку тощей кишки пациентам с ОП [17, 41]. В продольном исследовании, проведенном Makola et al., 126 пациентов получали стандартную смесь через тощую кишку, которая вводилась через чрескожную эндоскопическую гастростомию (PEG-J) [42]. Стандартная энтеральная формула привела как к значительному снижению среднего индекса тяжести КТ, так и к увеличению сывороточного альбумина по сравнению с исходным уровнем до момента удаления трубки. Несколько исследований определили преимущества полуэлементных формул по сравнению с полимерными при тяжелом ОП.В 1989 году Краво и др. обнаружили аналогичную переносимость у 102 пациентов с АП, получавших полуэлементные и полимерные формулы [43]. Tiengou et al. сравнивали в рандомизированном исследовании полуэлементные и полимерные формулы у 30 пациентов с ОП [44]. Обе формулы хорошо переносились и хорошо усваивались, но полуэлементная группа имела меньшую потерю веса и более короткую продолжительность пребывания в больнице по сравнению с полимерной группой. Недавно Петров и соавт. На основании скорректированного метаанализа пришли к выводу, что использование полимера по сравнению с (полу) элементным составом не приводит к значительно более высокому риску непереносимости кормления, инфекционных осложнений или смерти у пациентов с ОП [45].Следует помнить, что (полу) элементарные корма в семь раз дороже полимерных кормов. Таким образом, доказательная база для простого использования (полу) элементарных формул становится менее очевидной.
4.2. Использование добавок в энтеральном питании
Хотя использование добавок глутамина, иммунного питания, пребиотиков и / или пробиотиков является концептуально обоснованным и привлекательным, их использование не подтверждается крупномасштабными исследованиями [15, 46, 47].
Два исследования оценивали использование иммуностимулирующих формул, содержащих глутамин, аргинин и волокна или глутамин, аргинин, -3-жирные кислоты, витамины и микроэлементы [48, 49].Hallay et al. сравнили влияние энтеральной смеси, богатой глутамином, и энтеральной смеси, не богатой глютамином, на иммунологические параметры у 16 пациентов с ОП [48]. Восстановление иммунологических параметров было лучше, а время выздоровления было короче в группе, получавшей глутамин. Пирс и др. в рандомизированном контролируемом исследовании добавлен аргинин, глутамин, -3 жирные кислоты и антиоксиданты у 31 пациента с тяжелым ОП [49]. Удивительно, но увеличение CRP было обнаружено в исследуемой группе по сравнению с контрольной группой.Существенной разницы в продолжительности пребывания в стационаре не наблюдалось. Хотя в группе, получавшей иммунное питание, наблюдалась более низкая частота пневмонии и MOF, а также более короткая продолжительность пребывания в отделении интенсивной терапии и стационара, ни одно из этих различий не достигло статистической значимости.
Lasztity et al. случайным образом вводили -3 жирных кислоты энтерально 28 пациентам с АП средней степени тяжести [50]. Добавки значительно сократили продолжительность пребывания в больнице и продолжительность нутритивной терапии без значительного снижения общей частоты осложнений.
Каракан и др. выполнили единственное исследование, чтобы изучить возможную роль пребиотиков в ослаблении тяжести ОП [51]. Они обнаружили значительное сокращение продолжительности пребывания в больнице и продолжительности острой фазы ответа у пациентов, получавших пребиотики, по сравнению с контрольной группой. В исследовании участвовало всего 30 пациентов, и оно нуждается в подтверждении на более крупных сериях.
Пробиотики могут предотвращать инфекционные осложнения за счет уменьшения избыточного бактериального роста в тонкой кишке, восстановления барьерной функции желудочно-кишечного тракта и модуляции иммунной системы [52–54].Oláh et al. продемонстрировали, что Lactobacillus plantarum (пробиотик) в сочетании с овсяной клетчаткой (пребиотик) был успешным в снижении септических осложнений (4,5%) по сравнению с контролем (30%) у пациентов с ОП, предполагая, что терапия пробиотиками усиливает эффект ЭП в снижении инфекционная заболеваемость, однако, без разницы в продолжительности пребывания в больнице [55]. Oláh et al. также изучили четыре различных пребиотика и пробиотика, содержащиеся в Synbiotic 2000, и обнаружили снижение воспалительной реакции и полиорганной недостаточности при наличии тяжелого ОП [56].Besselink et al. провели единственное крупномасштабное многоцентровое рандомизированное исследование, в котором 298 пациентов с прогнозируемым тяжелым ОП были случайным образом распределены для приема пробиотических препаратов многовидовых (Lactobacilli и Bifidobacterium) или плацебо, вводимых энтерально [57]. Не было разницы в частоте инфекционных осложнений; однако в группе пробиотиков частота MOF и смертность (16% против 6%) были значительно выше [58]. У девяти пациентов в группе пробиотиков развилась ишемия кишечника, но ни у одного в группе плацебо.Патофизиологический механизм, объясняющий, почему ишемия кишечника развивалась у пациентов, получавших пробиотики, неясен, но на основании этих неожиданных результатов исследования использование пробиотической профилактики у пациентов с прогнозируемым тяжелым ОП крайне не рекомендуется. Петров и др. В своем систематическом обзоре пришли к выводу, что добавление к ЭП иммунного питания или пробиотиков не приводит к значительному улучшению клинических исходов и их использование не рекомендуется [45]. Состав, обогащенный клетчаткой, можно вводить безопасно, но требуется проведение РКИ с достаточной мощностью.
В заключение, определенные добавки, добавленные к ЭП, такие как аргинин, глутамин, -3 полиненасыщенные жирные кислоты и пребиотики, могут быть связаны с положительным влиянием на исход, но исследований слишком мало и недостаточно для того, чтобы дать четкие рекомендации по лечению [15, 47 ]. Пробиотики не следует назначать в плановом порядке пациентам с прогнозируемым тяжелым ОП.
5. Сроки энтеральной поддержки
Точные сроки начала энтеральной поддержки не рассматривались конкретно у пациентов с панкреатитом, но в значительной степени изучались у пациентов в критических состояниях.
Введение ЭП тяжелобольным пациентам на ранних этапах поступления в отделение интенсивной терапии изменяет физиологию таким образом, что снижает регуляцию системного иммунитета, снижает общий окислительный стресс и улучшает исход болезни [59]. Ранняя ЭП, начатая до 48 часов с момента поступления, у пациентов в критическом состоянии ассоциируется со значительным снижением инфекционных осложнений на 24% и снижением смертности на 32% по сравнению с отсроченным кормлением, начатым после этого момента времени [59, 60].
Марик и Залога в своем метаанализе обнаружили, что «ранняя» ЭП (в течение 36 часов) по сравнению с отсроченной ЭП (после 36 часов) задерживает инфекционные осложнения и сокращает продолжительность пребывания в больнице при травмах головы, травмах, ожогах, послеоперационных и медицинских Пациенты интенсивной терапии [61].Однако следует проявлять осторожность, делая выводы о пациентах с панкреатитом на основе информации, полученной от пациентов в критическом состоянии.
Недавно Петров и др. провели систематический обзор рандомизированных контролируемых исследований по влиянию ЭП по сравнению с ППП у пациентов с легким и тяжелым АД в отношении времени нутритивной поддержки [13]. ЭП, начатая в течение 48 часов после поступления, привела к значительному снижению полиорганной недостаточности, инфекционных осложнений поджелудочной железы и смертности.Эти значительные различия между ЭП и ПП исчезли, когда нутритивная поддержка началась через 48 часов после приема. Таким образом, ЭП, начатая в течение 48 часов после госпитализации, может быть полезным, и рандомизированное контролируемое исследование, которое было начато, может дать более определенный ответ.
6. Способ поддержки энтерального питания и толерантность к энтеральному питанию
Пероральному приему питательных веществ часто мешают боли в животе с отвращением к пище, тошнота, рвота, атония желудка и паралитическая кишечная непроходимость или частичная дуоденальная непроходимость из-за увеличения поджелудочной железы. [19].Применение ранней ЭП может быть ограничено тяжестью приступа панкреатита и возникновением кишечной непроходимости.
Традиционно лечение ОП включало голодание пациента до исчезновения симптомов. Недавние исследования показали, что ЭП через тощую кишку безопасна и может повышать антиоксидантную активность и уменьшать острофазовый ответ и величину воспалительного ответа [17].
Большинство питающих трубок размещаются как назоеюнальные трубки с помощью эндоскопической или радиологической процедуры.В качестве альтернативы, особенно если ожидаемый период кормления составляет 4–6 недель или более, можно установить лапароскопические или радиологические питательные зонды тощей кишки. Толерантность определяется обеспечением адекватного кормления без вредных последствий. Переносимость в первую очередь определяется балансом между питанием в желудочно-кишечном тракте, который может находиться в состоянии частичной кишечной непроходимости, и обеспечением энтеральных питательных веществ, вызывая лишь минимальную стимуляцию экзокринной секреции поджелудочной железы. Таким образом, пациенты с назоинтестинальными трубками, помещенными на уровне или ниже связки Treitz, должны находиться под очень тщательным наблюдением на предмет признаков миграции трубки, а также признаков непереносимости, таких как высокий остаточный объем, тошнота и рвота, диарея или аспирация смеси для кормления.Широкий диапазон толерантности к EN существует независимо от известных факторов, таких как режим (непрерывный или болюсный) и уровень инфузии в желудочно-кишечном тракте (желудочный или постпилорический ) . У пациентов, оперированных по поводу осложнений АП, непрерывная инфузия оказалась более безопасной и уменьшала стимуляцию поджелудочной железы лучше, чем болюсная инфузия [62]. Однако недостаточные данные не позволяют определить, лучше ли инфузия — непрерывная или болюсная.
После технико-экономического обоснования Eatock et al.выполнили рандомизированное контролируемое исследование раннего назогастрального кормления по сравнению с назоеюнальным кормлением при тяжелом ОП [63, 64]. Они обнаружили удивительную толерантность к назогастральному кормлению и рекомендовали рассматривать назогастральное кормление в качестве терапевтического варианта из-за его простоты, устраняя необходимость в эндоскопических, радиологических процедурах. Однако у исследования Итока было несколько ограничений, одно из которых — отсутствие рентгеноскопического подтверждения правильного расположения назоеюнальных трубок в тощей кишке.Нет никаких указаний на то, были ли назоеюнальные трубки размещены достаточно дистально (не менее 60 см от связки Трейца), чтобы избежать стимуляции желудка и поджелудочной железы. Неспособность найти разницу могла быть связана с продолжающейся стимуляцией желудка и двенадцатиперстной кишки, происходящей в обеих группах пациентов. Аналогичные результаты рандомизированных исследований были получены Kumar et al. (назогастральный по сравнению с назоеюнальным) и Eckerwall et al. (назогастральный по сравнению с ППН) [65, 66].
Jiang et al. включили в метаанализ 3 РКИ с участием 131 пациента [32].Первичным результатом эффективности была общая смертность, вторичными результатами эффективности было пребывание в больнице, осложнения и их лечение. Конечным показателем безопасности было появление боли при возобновлении кормления и побочных эффектов, связанных с назогастральной ЭП. Компараторное вмешательство представляло собой раннюю ЭП через назогастральный зонд, контрольным вмешательством был один из общепринятых маршрутов нутритивной поддержки в режиме покоя поджелудочной железы — тотальное парентеральное или интраджунальное кормление. Метаанализ не показал значительных различий в уровне смертности между назогастральным и традиционным способами (назоеюнальное и парентеральное питание).Кроме того, не различались и другие исходы, такие как продолжительность пребывания в больнице, инфекционные осложнения, полиорганная недостаточность, частота госпитализаций в отделение интенсивной терапии или переход на операцию. Кроме того, повторяемость боли при возобновлении кормления и побочные эффекты, связанные с питанием, были аналогичными.
Петров и др. выполнили расширенный систематический обзор, который включал 3 РКИ, включенные в метаанализ Jiang и исследование Eatock [33]. Они также пришли к выводу, что назогастральное кормление оказалось безопасным и хорошо переносимым большинством (79%) пациентов.Сводные данные двух РКИ, сравнивающих назогастральное и назоеюнальное кормление, не показали статистически значимой разницы в смертности и переносимости. Оба метаанализа заключают, что хорошо обоснованное рандомизированное исследование назогастрального кормления по сравнению с назоеюнальным кормлением показано для получения более твердых и убедительных доказательств для рекомендации назогастрального кормления в качестве рутинной клинической практики у пациентов с острым панкреатитом.
7. Время и нутриентный состав пероральной поддержки
Данные о том, когда возобновлять пероральное питание у пациентов с острым панкреатитом или выбрать оптимальный состав питательных веществ, пугают [40, 67, 68].Обычными критериями для начала перорального кормления являются отсутствие боли в животе, отсутствие тошноты и рвоты, возвращение аппетита и отсутствие осложнений. Возможно, что повторение боли во время возобновления пероральной диеты связано с приемом больших объемов, а не с продолжающимся или возобновляемым интрапанкреатическим высвобождением ферментов [64]. Обычно пациенты часто получают небольшое количество пищи в течение дня, и общее количество ежедневных калорий постепенно увеличивается в течение трех-шести дней [69].Поэтому кормление часто начинают с прозрачной жидкости, диеты первые 24 часа. При переносимости диета переводится на мягкую диету с низким содержанием жиров в течение следующих 24 часов, а затем на твердую диету с низким содержанием жиров. Нет доступных клинических испытаний, оценивающих эти процедуры. При возобновлении перорального приема пациентам, выздоравливающим после АП, рекомендуется диета с низким содержанием жиров. Это основано на наблюдении, что интрадуоденальные липиды увеличивают объем, выход бикарбоната, трипсина и амилазы у добровольцев [70]. Помимо предполагаемой стимуляции экзокринной секреции поджелудочной железы жиром, может быть еще одна причина отложить прием жиров.Липаза поджелудочной железы менее устойчива, чем другие ферменты поджелудочной железы, против кислотной денатурации и разрушения пепсином и протеазами поджелудочной железы, в частности химотрипсином, присутствующим в химотрипсине. Это может сделать липидное переваривание более уязвимым при патологических состояниях [71, 72]. Трипсин инактивируется не кислотой, а только пепсином.
Толерантность к переходу на оральную диету была оценена у 274 пациентов в момент, когда боль в животе исчезла и кишечная непроходимость исчезла [73]. Шестьдесят пациентов (21.9%) испытали рецидив боли, и у 47 из этих 60 пациентов боль возобновилась в течение 48 часов после начала перорального кормления. У пациентов, рандомизированных на питание через трубку тощей кишки, у которых не было рецидивов боли или боли, начавшейся в среднем через 7 дней после появления симптомов [74]. Однако у 4 из 15 пациентов (27%), рандомизированных на пероральное болюсное кормление, спустя в среднем 5 дней после появления симптомов, боль при возобновлении питания была связана с более длительной начальной болью и более высоким индексом тяжести на КТ. Леви и др.пришли к такому же выводу на большом количестве 116 пациентов [69]. Согласно шкале Рэнсона 3, 35% имели тяжелый АП, а согласно шкале Бальтазара CT — D, это имело место у 42% пациентов. У 21% пациентов возник рецидив боли. Риск рецидива боли увеличивался, если уровень липазы в сыворотке крови превышал норму в три раза за день до начала кормления, и был выше у пациентов с более длительной продолжительностью боли (11 дней по сравнению с 6 днями) и у пациентов с более тяжелой КТ. оценка (оценка Бальтазара больше D).Обострение симптомов привело к увеличению продолжительности пребывания в стационаре вдвое (с 18 до 33 дней). Chebli et al. обнаружили аналогичное количество дней боли в животе до возобновления перорального кормления у тех, у кого был и не был рецидив [75]. Рецидив боли прогнозировали по сбору перипанкреатической жидкости, уровню СРБ в сыворотке на 4-й день и липазе сыворотки в день перорального кормления.
Jacobson et al. предположили, что пациенты, выздоравливающие после легкого ОП, будут выписаны из больницы раньше, если они возобновят пероральное питание с твердой диеты с низким содержанием жиров, по сравнению с чистой жидкой диетой [67].Пациенты с легким панкреатитом были рандомизированы на чистую жидкую диету или твердую диету с низким содержанием жиров, когда они были готовы возобновить пероральное питание. Ежедневно наблюдали за пациентами на предмет рецидива боли, необходимости прекратить кормление, продолжительности пребывания в больнице после возобновления питания (первичная конечная точка) и в течение 28 дней после возобновления кормления для определения показателей повторной госпитализации. 1335 пациентов были оценены на соответствие критериям, 66 из которых были назначены на чистую жидкую диету (588 ккал, 2 г жиров) и 55 на твердую диету с низким содержанием жиров (1200 ккал, 35 г жиров). Из-за большого количества исключенных пациентов, возможно, произошла систематическая ошибка отбора.Число пациентов, которым требовалось прекратить кормление из-за боли или тошноты, было одинаковым (6% и 11%, соответственно), средняя продолжительность пребывания после возобновления кормления была аналогичной, и не было различий в 28-дневных показателях повторной госпитализации. Пациенты, соблюдающие диету с низким содержанием жиров, потребляли значительно больше калорий и граммов жира во время первого приема пищи и в первый день исследования (301 ккал и 2 г жира по сравнению с 622 ккал и 13 г жира). Начало перорального питания после легкого панкреатита с твердой диеты с низким содержанием жиров оказалось безопасным и обеспечило больше калорий, чем чистая жидкая диета, но не привело к сокращению продолжительности госпитализации.Оценка боли в животе в день возобновления кормления была связана с неэффективным пероральным приемом пищи, при этом у тех, кто испытывал более сильную боль, была более высокая вероятность того, что они не получили ни одного приема пищи. К сожалению, авторам не удалось решить важный вопрос, какой должна быть оптимальная диета у пациентов, выздоравливающих после легкого панкреатита. Sathiaraj et al. провели рандомизированное исследование для определения продолжительности пребывания в больнице и толерантности к пероральному возобновлению питания у пациентов с легким ОП и острым хроническим панкреатитом при переходе на мягкую диету (1040 ккал и 20 г жира) по сравнению с чистой жидкой диетой (458 ккал). и 11 г жира) [68].Продолжительность пребывания в больнице (после повторного кормления и общая) значительно сократилась при использовании мягкой диеты. Они не наблюдали значительной разницы в необходимости прекращения кормления из-за боли или тошноты. Пациенты, соблюдающие мягкую диету, потребляли значительно больше калорий и граммов жира во время первого приема пищи и в первый день исследования (921 ккал и 15 г жира по сравнению с 370 ккал и 8 г жира). Они пришли к выводу, что оральное возобновление питания с мягкой диетой было безопасным и привело к сокращению продолжительности пребывания в больнице. Однако в обоих неслепых исследованиях не было дано определения того, когда выписывать пациентов.Решение о выписке из больницы было принято медицинской бригадой без участия исследовательской группы.
8. Рекомендации по энтеральному питанию при остром панкреатите
Недавно было опубликовано несколько общих практических рекомендаций по АР [1, 4, 8, 76–78]. Они комментируют управление питанием при легком и тяжелом АП. Европейское общество парентерального и энтерального питания (ESPEN) в 2006 г. опубликовало пересмотренное и всеобъемлющее руководство по ЭП при АП [8]. Несколько руководств содержат в основном одни и те же рекомендации.На сегодняшний день некоторые рекомендации требуют обновления в соответствии с наилучшими имеющимися доказательствами, о которых говорилось выше. Как правило, при легком ОП рекомендуется начинать ЭП, если пациенты не могут употреблять обычную пищу через 5–7 дней. При тяжелом АП нутритивная поддержка показана, когда становится очевидным, что пациент не сможет переносить пероральный прием в течение длительного периода времени, например, по крайней мере, в течение 7 дней. Эта оценка обычно может быть произведена в течение первых 3-4 дней после поступления. При необходимости ЭП следует дополнить парентеральным питанием.Кроме того, при тяжелом панкреатите с такими осложнениями, как свищи поджелудочной железы, асцит и псевдокисты, зондовое питание можно проводить без осложнений. Если желудочное кормление не переносится, следует попробовать тощую кишку и использовать непрерывное кормление вместо болюсного кормления. При обструкции выходного отверстия желудка следует попробовать кормление вне преграды с наконечником зонда дистальнее преграды. Если это невозможно, следует назначить парентеральное питание. В случае операции по поводу осложнений АП возможна интраоперационная еюностомия для послеоперационного кормления.
Полуэлементные формулы на основе пептидов можно использовать безопасно, и можно попробовать стандартные формулы, если они допускаются.
9. Краткое изложение последних достижений
Большинство пациентов с ОП имеют легкую форму заболевания и не нуждаются в дополнительной нутритивной поддержке во время госпитализации. Согласно руководствам, нутритивная поддержка показана, если пациенты не могут употреблять обычную пищу через 5–7 дней или когда становится очевидным, что пациент не сможет переносить пероральный прием в течение длительного периода времени (7 дней и более).Когда показано искусственное питание, ЭП предпочтительнее ПП, потому что это снижает количество осложнений и смертность при АР по сравнению с ПП. ППП следует применять только пациентам, не переносящим ЭП. Вполне вероятно, что ЭП оказывает благотворное влияние на течение заболевания и ее следует начинать как можно раньше (в течение 48 часов после госпитализации). С некоторой осторожностью можно сказать, что кормление через назогастральный зонд при тяжелом ОП возможно, что делает концепцию панкреатического покоя менее вероятной. Однако необходимы более крупные многоцентровые исследования, чтобы подтвердить безопасность и эффективность назогастрального кормления по сравнению с назоеюнальным кормлением и изучить роль раннего (в течение 48 часов) по сравнению с поздним питанием.Были начаты рандомизированные контролируемые маршруты, которые, надеюсь, дадут более определенный ответ. Клинические доказательства использования только (полу) элементарных формул слабы. Прием добавок к энтеральным смесям с глутамином и пребиотиками, а также использование иммуностимулирующих составов не рекомендуется в обычном порядке. Пробиотики не следует назначать в плановом порядке пациентам с прогнозируемым тяжелым ОП. На сегодняшний день некоторые рекомендации, изложенные в последних руководящих принципах, требуют обновления в соответствии с наилучшими имеющимися доказательствами.
Сокращения
| AP: | Острый панкреатит | |
| NPO: | Nil per os | |
| EN: | Энтеральное питание | |
| : | Синдром системного воспалительного ответа | |
| MOF: | Многоорганная недостаточность | |
| ОИТ: | Отделение интенсивной терапии | |
| РКИ: | Рандомизированное контролируемое исследование72 | |
| VIP: | Вазоактивный кишечный пептид. |
Благодарность
B. W. M. Spanier спонсируется неограниченной грандиозной компанией Axcan Pharma Incorporate, Канада.
Конкурирующий интерес
Автор заявил об отсутствии конкурирующего интереса.
Панкреатит | Американская академия педиатрии
- Thanh Huong L. Nguyen, MD *
- Karla Au Yeung, MD †
- Brian Pugmire, MD ‡
- Roberto Gugig, MD †
- * Программа детской резиденции Valley ,
- † Отделение детской гастроэнтерологии и питания, и
- ‡ Отделение радиологии, Детский госпиталь Вэлли, Мадера, Калифорния
AUTHOR NODSUY Юнг, Пагмайр и Гугиг не раскрыли никаких финансовых отношений, имеющих отношение к этой статье.Этот комментарий не содержит обсуждения несанкционированного / исследовательского использования коммерческого продукта / устройства.
- AIP:
- аутоиммунный панкреатит
- AP:
- острый панкреатит
- ARP:
- острый рецидивирующий панкреатит
- CP151583
- хронический панкреатит хронический эндопротезный панкреат. EUS:
- эндоскопическое УЗИ
- IL:
- интерлейкин
- LR:
- раствор Рингера с лактатом
- MRCP:
- магнитно-резонансная холангиопанкреатография
- SIRS
- общий воспалительный синдром питание
- TUS:
- трансабдоминальное УЗИ
Пробелы в образовании
Инфузионная терапия при остром панкреатите развивается и включает раствор Рингера с лактатом, хотя необходимы дополнительные педиатрические исследования.
Раннее энтеральное питание в течение 24 часов рекомендуется во избежание длительного отсутствия перорального введения и связанных с этим заболеваемости.
Профилактические антибиотики не рекомендуются.
Цели
Прочитав эту статью, читатели должны уметь:
Знать классификацию детского панкреатита.
Изучите этиологию, факторы риска, клинические проявления, подход к диагностике и лечению панкреатита у детей.
Признать текущие согласованные рекомендации по раннему энтеральному питанию и агрессивному ведению жидкости.
Знать осложнения панкреатита у детей и их соответствующие диагностические и терапевтические стратегии.
Введение
Панкреатит — это воспалительный процесс поджелудочной железы, представляющий собой спектр клинических заболеваний. Острый панкреатит (ОП) — обратимый процесс, но он может прогрессировать до острого рецидивирующего панкреатита (АРП).Это увеличивает риск развития хронического панкреатита (ХП), который несет более высокую заболеваемость из-за необратимых стриктур протоков поджелудочной железы, внешнесекреторной недостаточности поджелудочной железы, инсулинозависимого сахарного диабета и хронической боли. Панкреатит все чаще встречается у детей, что вызывает беспокойство, учитывая недостаточное количество исследований у педиатрических пациентов. Исторически рекомендации по лечению детского панкреатита разрабатывались на основе консенсусных конференций и исследований среди взрослого населения.В 2018 г. были опубликованы согласованные рекомендации по ведению AP как для педиатрии (1) (2) (3), так и для медицины взрослых. (4)
Классификация детского панкреатита
Согласно INSPPIRE (Международная исследовательская группа детского панкреатита: в поисках cuRE), панкреатит трех категорий: AP, ARP и CP.
AP у педиатрических пациентов требует, по крайней мере, 2 из следующих 3 критериев: 1) боль в животе, указывающая на AP, например, острое начало и…
(PDF) Рекомендации по питанию для профилактики острого панкреатита: обзор текущего мнения
Питание и диетические добавки 2012: 4
39.Андерсон Ф., Томсон С.Р., Кларк Д.Л., Букчимацца И. Клиническая оценка панкреатита с дислипидемией
и анализ тяжести заболевания и исходов
. Панкреатология. 2009. 9: 252–257.
40. Бугдачи М.С., Сокмен М., Зухур С.С., Алтунтас Ю. Изменения липидного профиля
и важность фракции альфа-липопротеинов с низкой сывороткой (липопротеин высокой плотности
) в случаях острого панкреатита. Поджелудочная железа. 2011; 40:
1241–1244.
41.Лай С.В., Муо СН, Ляо К.Ф., Сун ФК, Чен ПК. Риск острого пан-
креатита при диабете 2 типа и снижение риска на антидиабетических препаратах:
популяционное когортное исследование на Тайване. Am J Gastroenterol.
2011; 106: 1697–1704.
42. Girman CJ, Kou TD, Cai B, et al. Пациенты с сахарным диабетом 2 типа
имеют более высокий риск острого панкреатита по сравнению с пациентами без диабета
. Диабет ожирения Metab. 2010; 12: 766–771.
43. Гонсалес-Перес А., Шлингер Р.Г., Родригес Л.А. Острый панкреатит
в сочетании с сахарным диабетом 2 типа и противодиабетическими препаратами: популяционное когортное исследование на основе
. Уход за диабетом. 2010. 33: 2580–2585.
44. Ноэль Р.А., Браун Д.К., Паттерсон Р.Э., Блумгрен Г.Л. Повышенный риск
острого панкреатита и заболевания желчевыводящих путей, наблюдаемый у пациентов с
диабетом 2 типа: ретроспективное когортное исследование. Уход за диабетом. 2009; 32:
834–838.
45. Келлер Дж., Лайер П. Экзокринная реакция поджелудочной железы человека на питательные вещества в
здоровье и болезни. Кишечник. 2005; 54 Приложение 6: vi1 – vi28.
46. Roncal-Jimenez CA, Lanaspa MA, Rivard CJ, et al. Сахароза вызывает
ожирения печени и воспаления поджелудочной железы у самцов крыс-производителей независимо от избыточного потребления энергии. Обмен веществ. 2011; 60: 1259–1270.
47. Аль-Аззави Х.Х., Уэйд Т.Э., Шварц-Базиль Д.А., Ван С., Питт Х.А.,
Зиромски, штат Нью-Джерси.Острый панкреатит при ожирении: адипокины и диетический
рыбий жир. Dig Dis Sci. 2011; 56: 2318–2325.
48. Gastaminza G, Bernaola G, Camino ME. Острый панкреатит, вызванный
аллергией на киви. Аллергия. 1998. 53: 1104–1105.
49. Маттео А., Сарлес Х. Является ли пищевая аллергия причиной острого панкреатита?
Поджелудочная железа. 1990; 5: 234–237.
50. Судзуки С., Хомма Т., Курокава М. и др. Эозинофильный гастроэнтерит
, вызванный аллергией на коровье молоко, проявляющейся острым панкреатитом.Int Arch
Allergy Immunol. 2012; 158 Прил. 1: 75–82.
51. Пател Р.С., Джолин ФК мл., Мюррей Дж. А. Целиакия и рецидивирующий панкреатит
. Gastrointest Endosc. 1999; 50: 823–827.
52. Ли К.Т., Шин П.К. Изучение лизосомных изменений поджелудочной железы крыс после приема
L-глутамата натрия. Поджелудочная железа. 1994; 9: 304–308.
53. Лещенко И.В., Шевчук В.Х., Фалалиева Т.М., Берегова Т.В.
Влияние длительного приема глутамата натрия на структуру
поджелудочной железы крыс.Физиол Ж. 2012; 58: 59–65. Украинец.
54. Burton F, Alkaade S, Collins D, et al. Использование и предполагаемая эффективность —
неанальгетических медицинских методов лечения хронического панкреатита в
Соединенных Штатах. Алимент Pharmacol Ther. 2011; 33: 149–159.
55. Шафик Н., Рана С., Бхасин Д. и др. Ферменты поджелудочной железы при хроническом панкреатите
. Кокрановская база данных Syst Rev.2009; 4: CD006302.
56. Delhaye M, Meuris S, Gohimont AC, Buedts K, Cremer M.
Сравнительная оценка препарата фермента поджелудочной железы с высоким содержанием липазы
и стандартной панкреатической добавки для лечения экзокринной недостаточности поджелудочной железы
при хроническом панкреатите. Eur J Gastroenterol Hepatol.
1996; 8: 699–703.
57. Домингес-Муньос Дж., Иглесиас-Гарсия Дж., Иглесиас-Рей М., Фигейрас A,
Виларино-Инсуа М. Влияние схемы приема на терапевтическую эффективность пероральных добавок ферментов поджелудочной железы у пациентов с экзокринной
недостаточность поджелудочной железы: рандомизированное трехфакторное перекрестное исследование.
Алимент Pharmacol Ther. 2005; 21: 993–1000.
58. Halgreen H, Pederson NT, Worning H. Симптоматический эффект терапии ферментами поджелудочной железы
у пациентов с хроническим панкреатитом.
Сканд Дж Гастроэнтерол. 1986; 21: 104–108.
59. Isaksson G, Ihse I. Уменьшение боли пероральным препаратом панкреатического фермента
при хроническом панкреатите. Dig Dis Sci. 1983; 28: 97–102.
60. Lankisch PG, Lembcke B, Goke B, Creutzfeldt W.Терапия поджелудочной железы
атогенной стеатореи: дает ли кислотная защита ферментов поджелудочной железы
какие-либо преимущества? З. Гастроэнтерол. 1986; 24: 753–757.
61. Ларвин М., МакМахон М.Дж., Томас ВЕГ, Пунтис MCA. Creon (энтеросолюбильные
, покрытые панкреатином микросферы) для лечения боли при хроническом панкреатите
: двойное слепое рандомизированное плацебо-контролируемое перекрестное исследование
. Гастроэнтерология. 1991; 100: A283.
62. Malesci A, Gaia E, Fioretta A, et al.Отсутствие эффекта от длительного лечения
экстрактом поджелудочной железы на повторяющиеся боли в животе у пациентов с
хроническим панкреатитом. Сканд Дж Гастроэнтерол. 1995. 30: 392–398.
63. Мосснер Дж., Секнус Р., Майер Дж., Нидо С., Адлер Г. Лечение боли
экстрактами поджелудочной железы при хроническом панкреатите: результаты проспективного многоцентрового плацебо-контролируемого исследования
. Пищеварение. 1992; 53: 54–66.
64. О’Киф С.Дж., Карием А.К., Леви М.Обострение эндокринной дисфункции поджелудочной железы
сильнодействующими экзокринными добавками поджелудочной железы
у пациентов с хроническим панкреатитом. J Clin Gastroenterol. 2001; 32:
319–323.
65. Сафди М., Бекал П.К., Мартин С., Саид З.А., Бертон Ф., Тоскес П.П. Эффекты
пероральных ферментов поджелудочной железы (капсула Creon 10) на стеаторею:
многоцентровое плацебо-контролируемое исследование в параллельных группах с участием субъектов с
хроническим панкреатитом.Поджелудочная железа. 2006. 33: 156–162.
66. Григсби Б., Родригес-Рило Х., Хан К. Антиоксиданты и хронический панкреатит
: теория окислительного стресса и испытания антиоксидантной терапии.
Dig Dis Sci. 2012; 57: 835–841.
67. Braganza JM, Дорманди, TL. Микронутриентная терапия хронического панкреатита
: обоснование и влияние. JOP. 2010; 11: 99–112.
68. Салим А.С. Роль акцепторов свободных радикалов, полученных из кислорода, в лечении повторяющейся боли, вызванной хроническим панкреатитом: новый подход.
Arch Surg. 1991; 126: 1109–1114.
69. Бэнкс П.А., Хьюз М., Ферранте М., Нордхук ЕС, Рамагопал В.,
Сливка А. Уменьшает ли аллопуринол боль при хроническом панкреатите? Int J
Панкреатол. 1997. 22: 171–176.
70. Дургапрасад С., Пай К.Г., Васанткумар, Алврес Дж. Ф., Намита С. Пилотное исследование
антиоксидантного действия куркумина при тропическом панкреатите.
Indian J Med Res. 2005. 122: 315–318.
71.Кирк Г.Р., Уайт Дж.С., Маккай Л. и др. Комбинированная антиоксидантная терапия
уменьшает боль и улучшает качество жизни при хроническом панкреатите.
J Gastrointest Surg. 2006; 10: 499–503.
72. Бхардвадж П., Гарг П.К., Маулик С.К., Сарая А., Тандон Р.К., Ачарья С.К.
Рандомизированное контролируемое исследование добавок антиоксидантов для
обезболивающих у пациентов с хроническим панкреатитом. Гастроэнтерология.
2009; 136: 149–159.
73. Сиривардена А. К., Мейсон Дж. М., Шин А. Дж., Макин А. Дж., Шах Н. С.. Антиоксидантная терапия
не уменьшает боль у пациентов с хроническим панкреатитом: исследование
ANTICIPATE. Гастроэнтерология. 2012; 143: 655–663.
74. Зейбек Н., Горгулу С., Ягчи Г. и др. Эффекты экстракта гинкго билоба
(EGb 761) при экспериментальном остром панкреатите. J Surg Res. 2003; 115:
286–293.
75. Карвалью К.М., Мораис Т.С., де Мело Т.С. и др.Природный флавоноид
кверцетин облегчает вызванный церулеином острый панкреатит у мышей. Биол
Pharm Bull. 2010; 33: 1534–1539.
76. Дас Д., Мукерджи С., Дас А.С., Мукерджи М., Митра С. Водный экстракт
черного чая (камелия китайская) предотвращает панкреатит, вызванный этанолом + холецистокинином-
, на модели крыс. Life Sci. 2006; 78: 2194–2203.
77. Бабу Б.И., Маллео Г., Дженовезе Т. и др. Полифенолы зеленого чая amelio-
оценивают повреждение поджелудочной железы при индуцированном церулеином остром панкреатите у мышей.
Поджелудочная железа. 2009. 38: 954–967.
78. Сидху С., Панди П., Малхотра С., Вайфей К., Кхандуджа К.Л. Благоприятные эффекты
эмблики официальной при L-аргинине-индуцированном остром панкреатите
у крыс. J Med Food. 2011; 14: 147–155.
79. Насири-Асл М., Хоссейнзаде Х. Обзор фармакологических эффектов
vitis vinifera (виноград) и его биоактивных соединений. Phytother Res.




 Постоянно пьем воду.
Постоянно пьем воду.

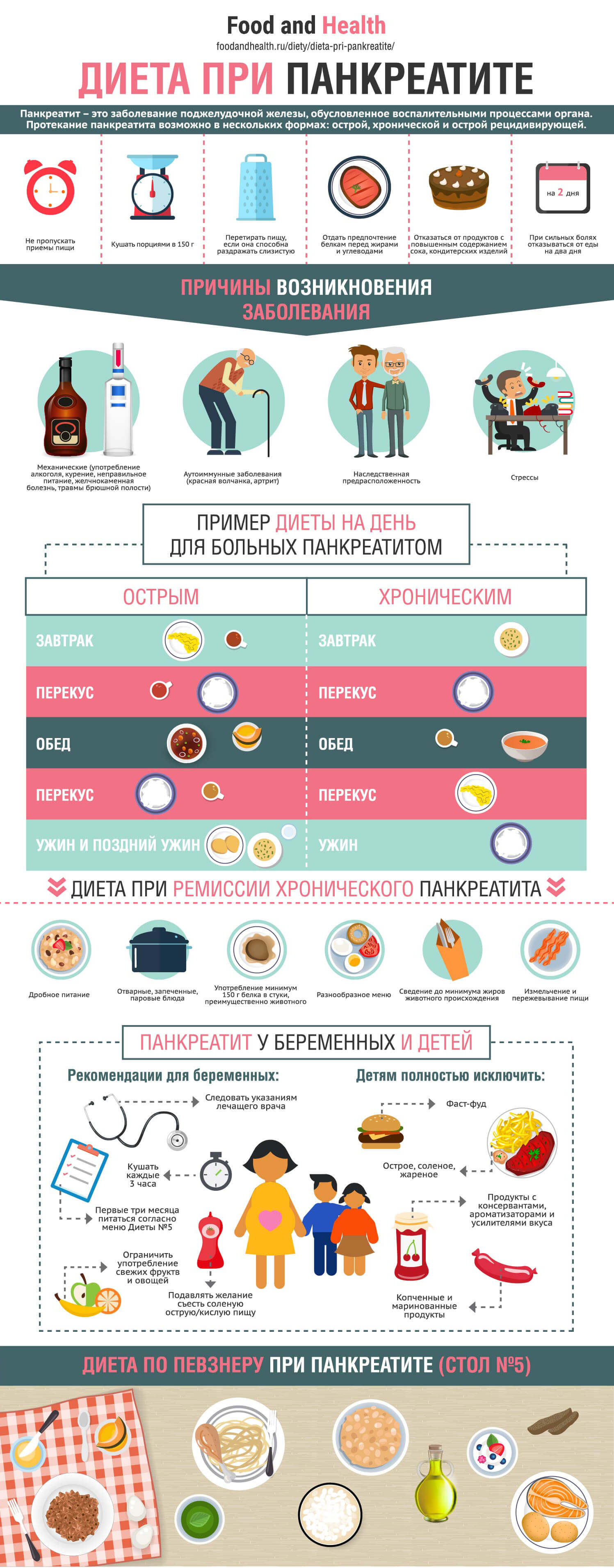

 Мясо лучше в виде тефтель и паровых котлет. Осторожно с фруктами и овощами — можно отварную морковь, брокколи, банан, печенное яблоко. Строгую диету нужно соблюдать несколько месяцев и осторожно расширять в дальнейшем при условии удовлетворительного самочувствия.
Мясо лучше в виде тефтель и паровых котлет. Осторожно с фруктами и овощами — можно отварную морковь, брокколи, банан, печенное яблоко. Строгую диету нужно соблюдать несколько месяцев и осторожно расширять в дальнейшем при условии удовлетворительного самочувствия.