Терапия кандидоза | #12/02 | «Лечащий врач» – профессиональное медицинское издание для врачей. Научные статьи.
Кандидоз — инфекционное заболевание, обусловленное дрожжеподобными грибами рода Candida. Клинические проявления микоза широко варьируют от поверхностных, слабовыраженных поражений кожи и слизистых оболочек до тяжелых, угрожающих жизни инвазивных висцеральных форм. Диагностика и терапия кандидоза непроста и часто требует привлечения специалистов различного профиля [1, 4, 8].
Число больных поверхностными и глубокими формами кандидоза в последние десятилетия значительно возросло во всех странах мира. Этот факт связывают со снижением естественной иммунной реактивности организма значительной части населения из-за поражения СПИДом, ятрогенных иммунодефицитов, возникающих при химиотерапии онкологических больных, трансплантации органов, вследствие применения глюкокортикоидов, цитостатиков, антиметаболитов, антибиотиков широкого спектра действия, в том числе в отделениях реанимации и интенсивной терапии [4, 8].
Главным возбудителем кандидоза является Candida albicans, которая, как и другие виды грибов Candida, обнаруживается в норме на слизистых и кожных покровах большинства обследованных, но поражает лишь ослабленный организм. Именно в этом кроется сложность проблемы кандидоза.
Природа возбудителя, его взаимоотношения с макроорганизмом, многие аспекты защиты организма от кандидозной инфекции, генетические механизмы резистентности различных видов Candida spp. к основным антимикотикам, применяющимся в лечении кандидоза, подробно изучена. Установлено, что подавляющее большинство штаммов 
Известно, что грибы рода Candida сапрофитируют на коже и слизистых оболочках, не вызывая заболевания и лишь при повреждении наружных покровов, снижении местного иммунитета они могут проникнуть внутрь, пройдя стадии адгезии, колонизации и инвазии.
Адгезия грибов Candida обусловлена их способностью расщеплять секреторный иммуноглобулин А и α-антитрипсин и прикреплять жизнеспособный гриб к протеинам слизистых оболочек за счет гликопротеинадгезина клеточной мембраны гриба. Адгезия гриба к эпителию является основой его инвазии в организм, что происходит уже в первые минуты его взаимодействия со слизистой. Степень адгезии определяет уровень колонизации C. albicans, а степень инвазии — его вирулентность. Грибки продуцируют эндотоксины, гемолизины, дермотоксины, пирогены, протеолитические ферменты, облегчающие адгезию грибковых клеток к ороговевшему эпителию и слизистым оболочкам. Установлено, что у разных штаммов 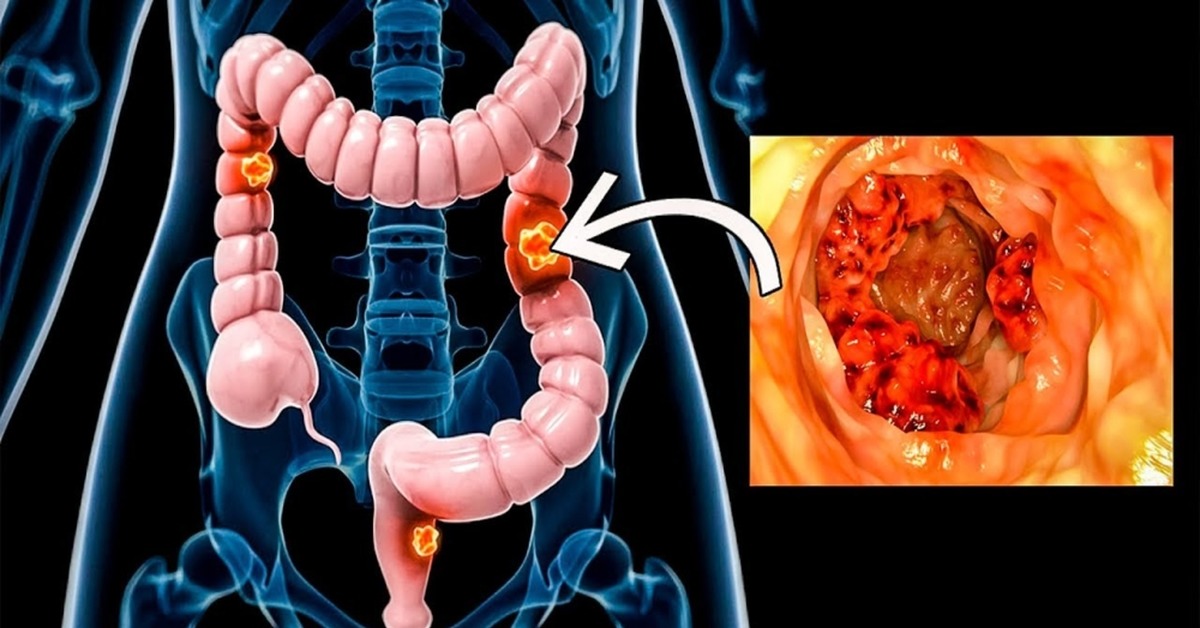 В «Проекте рекомендаций по лечению кандидоза» указано на важность определения вида возбудителей и их чувствительности к противогрибковым препаратам, даются рекомендации по лечению различных форм инвазивного кандидоза, кандидемии и острого диссеминированного кандидоза — тяжелейших форм кандида-инфекции с высокой летальностью, перечисляются показания к проведению адекватного лечения амфотерицином В и флуконазолом [4]. Замена первого дорогостоящим липосомальным препаратом амбизомом позволяет избежать высокой нефротоксичности амфотерицина В и проводить лечение больных кандидозом с почечной недостаточностью, резистентной к антибиотикам фебрильной нейтропенией, при высоком риске развития острого диссеминированного кандидоза у больных без нейтропении, его органных форм (поражения сердца, сосудов, мочевыводящих путей, желудочно-кишечного тракта). В работе также приводятся рекомендации по лечению кандидоза кожи, ее придатков, хронического кандидоза кожи и слизистых оболочек, профилактике кандидоза у реципиентов трансплантатов органов.
В «Проекте рекомендаций по лечению кандидоза» указано на важность определения вида возбудителей и их чувствительности к противогрибковым препаратам, даются рекомендации по лечению различных форм инвазивного кандидоза, кандидемии и острого диссеминированного кандидоза — тяжелейших форм кандида-инфекции с высокой летальностью, перечисляются показания к проведению адекватного лечения амфотерицином В и флуконазолом [4]. Замена первого дорогостоящим липосомальным препаратом амбизомом позволяет избежать высокой нефротоксичности амфотерицина В и проводить лечение больных кандидозом с почечной недостаточностью, резистентной к антибиотикам фебрильной нейтропенией, при высоком риске развития острого диссеминированного кандидоза у больных без нейтропении, его органных форм (поражения сердца, сосудов, мочевыводящих путей, желудочно-кишечного тракта). В работе также приводятся рекомендации по лечению кандидоза кожи, ее придатков, хронического кандидоза кожи и слизистых оболочек, профилактике кандидоза у реципиентов трансплантатов органов.
Наиболее полное, систематизированное изложение проблемы кандидоза дано в вышедшей в 2000 году монографии «Кандидоз» [8].
Этиотропная терапия любого инфекционного заболевания, в том числе и кандидоза, ставит своей целью удаление (эрадикацию) возбудителя. Однако особенностью кандидоза является то, что грибы рода Candida входят в состав постоянной биоты — нормобиоты, бактериобиоты человека, и легко колонизируют слизистые оболочки, то есть сама эрадикация этого гриба почти никогда не бывает абсолютной и окончательной. Учитывая оппортунистическую природу кандида-инфекции, саму эрадикацию возбудителя связывают с патогенетическими факторами, определяющими клиническую форму и тяжесть инфекции. Это иммунодефициты, нейтропения и другие. Вот что определяет выбор антимикотика, его дозу и длительность терапии.
Лечение может быть направлено на предупреждение гиперколонизации организма грибами рода Candida (при назначении антимикотиков широкого спектра действия и иммуносупрессантов). Местные оральные антимикотики — полиены (нистатин, леворин, микогептин) нерастворимы и почти не всасываются из желудочно-кишечного тракта, поэтому редко могут обеспечить элиминацию Candida. Здесь необходимы пероральные препараты системного действия (флуконазол, итраконазол) или препараты для инъекций, такие как флюцитозин, амфотерицин В, амбизом. Если амфотерицин В вследствие его чрезвычайной нефротоксичности назначается при кандидозе в суточной дозе 0,5 мг/кг массы тела, амбизом в 10 раз и более превышает эту дозу и не имеет противопоказаний к назначению [1, 2, 3, 4, 9, 10]. При лечении кандидозов кожи и слизистых оболочек часто используются антимикотики для наружного применения: полиены (леворин, нистатин, натамицин), производные имидазола (кетоконазол, оксиконазол, эконазол, тиоконазол, клотримазол, миконазол, изоконазол, бифоназол, амиказол), триазолы (терконазол), аллиламины (нафтифин, тербинафин), морфолины (аморолфин), прочие препараты (производные унденциленовой кислоты, анилиновые красители и др.
Местные оральные антимикотики — полиены (нистатин, леворин, микогептин) нерастворимы и почти не всасываются из желудочно-кишечного тракта, поэтому редко могут обеспечить элиминацию Candida. Здесь необходимы пероральные препараты системного действия (флуконазол, итраконазол) или препараты для инъекций, такие как флюцитозин, амфотерицин В, амбизом. Если амфотерицин В вследствие его чрезвычайной нефротоксичности назначается при кандидозе в суточной дозе 0,5 мг/кг массы тела, амбизом в 10 раз и более превышает эту дозу и не имеет противопоказаний к назначению [1, 2, 3, 4, 9, 10]. При лечении кандидозов кожи и слизистых оболочек часто используются антимикотики для наружного применения: полиены (леворин, нистатин, натамицин), производные имидазола (кетоконазол, оксиконазол, эконазол, тиоконазол, клотримазол, миконазол, изоконазол, бифоназол, амиказол), триазолы (терконазол), аллиламины (нафтифин, тербинафин), морфолины (аморолфин), прочие препараты (производные унденциленовой кислоты, анилиновые красители и др.
Одно только перечисление антикандидозных препаратов уже свидетельствует об их множестве и разной степени эффективности, связанной с химической структурой и особенностями фармакокинетики. В частности, наружные средства не всегда создают достаточную концентрацию в подслизистом слое половых путей, глубоких слоях кожи и ее придатках.
В последние годы в России и за рубежом в системной терапии кандидоза с успехом применяется медофлюкон (флуконазол) [2, 3].
Флуконазол (медофлюкон) — противогрибковый препарат из группы триазолов, эффективный при системных и локальных микозах. Флуконазол избирательно подавляет синтез эргостерина клеточной мембраны грибков на уровне образования диметил-эргостатриенола из ланостерина путем ингибирования зависимой от цитохрома Р-450 реакции С14-альфа-демитиляции. Этот путь биосинтеза стеролов характерен только для грибов. За счет более высокого сродства к ферментам, катализирующим синтез эргостерина у грибов, чем к ферментам, катализирующим образование холестерина у человека, селективность действия флуконазола на грибы рода Candida, дерматофиты и возбудители глубоких микозов в 10 000 раз выше, чем на клетки макроорганизма.
Спектр фунгистатического действия флуконазола: Candida albicans, некоторые штаммы Candida nonalbicans (C. guilliermondii, C. pseudotropicalis, C. torulopsis, C. kefyr, C. stellatoidea), Cryptococcus neoformans, Microsporum spp., Trichophyton spp., Blastomyces dermatitidis, Coccidioides immitis, Histoplasma capsulatum.
При пероральном и внутривенном применении фармакокинетика флуконазола сходная. При приеме внутрь биодоступность около 90%. Прием пищи не влияет на абсорбцию препарата. Максимальная концентрация достигается через 0,5 — 1,5 ч. После приема 150 мг она составляет 2,44 — 3,58 мкг/мл. Концентрация в крови прямо пропорциональна принятой дозе. Равновесная концентрация устанавливается к 4 — 5-му дню при приеме 1 раз в сутки. При использовании в первый день двойной дозы она достигается ко второму дню. Связь с белками плазмы 11 — 12%. Объем распределения приближается к общему объему воды в организме. Концентрации флуконазола в слюне, мокроте, суставной и перитонеальной жидкостях, вагинальном секрете, грудном молоке аналогичны таковым в плазме крови.
Медофлюкон применяется внутрь 1 раз в сутки (утром).
Дозы для взрослых:
- При кандидемии, диссеминированном кандидозе — 400 мг в первые сутки и 200 — 400 мг — в последующие дни.
 Продолжительность лечения 7 — 14 дней и более.
Продолжительность лечения 7 — 14 дней и более. - При кандидозе кожи — 50 — 100 мг 1 раз в сутки или 150 мг 1 раз в неделю в течение 2 — 6 недель.
- При орофарингеальном кандидозе — 50 мг в сутки в течение 7 — 14 дней.
- При кандидозе другой локализации (кандидурии, кандидозном эзофагите и неинвазивном бронхолегочном кандидозе) — 50 — 150 мг в сутки в течение 14 — 30 дней.
- При онихомикозе — 50 мг 1 раз в сутки или 150 мг 1 раз в неделю в течение 3 — 6 месяцев при поражении ногтей пальцев рук и 6 — 12 месяцев — при поражении ногтей пальцев ног (до замещения инфицированного ногтя).
- При кандидозном баланопостите или вагинальном кандидозе — 150 мг однократно, при кандидозном вульвовагините — 50 мг в сутки в течение 7 дней или 150 мг двукратно, при хроническом рецидивирующем (3 — 4 раза в год или чаще) кандидозном вульвовагините 150 мг 3 — 4 раза в сутки с 3 — 7-дневными интервалами, иногда до 12 раз с месячными интервалами.

- При глубоких эндемических микозах — 200 — 400 мг в сутки ежедневно до 2 лет: 11 — 24 мес. при кокцидиомикозе, 2 — 17 мес — при паракокцидиомикозе, 1 — 16 мес. — при споротрихозе, 3 — 17 мес — при гистоплазмозе.
- При криптококковом менингите, криптококковых инфекциях другой локализации — 400 мг в первые сутки и 200 — 400 мг в последующие дни. Продолжительность лечения 7 — 14 дней, при криптококковом менингите — до 6 — 8 недель.
- Для профилактики грибковых инфекций — 50 — 400 мг в сутки на протяжении всего периода антибактериальной, глюкокортикоидной, цитостатической или лучевой терапии.
Специального подбора доз для пациентов пожилого возраста не требуется, если не угнетена функция почек (клиренс креатинина менее 40 — 50 мл/мин).
У больных с нарушениями функции почек доза должна быть снижена в соответствии со степенью почечной недостаточности.
Пациентам, находящимся на гемодиализе: однократно после каждого сеанса гемодиализа.
Российские авторы [3] приводят собственные данные о применении медофлюкона при различных поражениях, в том числе при висцеральных микозах, обусловленных грибами рода Candida. В частности, опубликованы данные об успешном лечении медофлюконом 9 больных кандидозом кишечника, 11 — полости рта, 3 — пищевода, 18 — вагинальным кандидозом при суточной дозе 50 — 200 мг и длительности курса 14 дней. Отечественные исследователи, оценив эффективность и безопасность препарата, уже в 1996 году назвали медофлюкон безусловным достижением в лечении кандидоза и рекомендовали его для лечения поверхностных и висцеральных форм микоза не только в стационаре, но и в амбулаторных условиях.
К такому же выводу пришли и авторы, проводившие исследования медофлюкона в Московском центре глубоких микозов [2]. По их данным, из 79 больных кандидозным бронхитом, получавших в течение 2 недель 100 — 400 мг медофлюкона в сутки, излечено 74,7%, улучшение наступило у 22,8%, при кандидозной пневмонии выздоровело 66,75%, улучшение отмечено у 33,3%, эрадикация возбудителя — в 97,5 — 100%.
В дерматовенерологии медофлюкон наиболее часто применяется при лечении урогенитальных кандидозов, кандидоза слизистой оболочки полости рта, онихомикозах [4, 6, 7, 8].
Данные, приведенные из литературы, и наш опыт применения медофлюкона при кандидозном вульвовагините и онихомикозе свидетельствуют о его высокой эффективности, хорошей переносимости и безопасности, что делает флуконазол препаратом выбора при лечении различных форм кандидоза слизистых оболочек, кожных покровов и внутренних органов.
В. М. Лещенко, доктор медицинских наук, профессор
Городской микологический центр, Москва
Литература
- Бурова С. А. Проблемы грибковых заболеваний человека//Российский журнал кожных и венерических болезней. 1999. № 1. С. 39 — 41.
- Воинова Г. В., Бурова С. А. Опыт лечения пневмомикозов медофлюконом//Пульмонология. 2001. № 1. С. 35 — 36.
- Ивлева А. Я., Поплавко Р. М.
 , Лешкова В. М. и др. Медофлюкон (флуконазол) — последнее достижение в лечении микозов//Медико-фармацевтический вестник. 1996. № 9 — 10. С. 23 — 27.
, Лешкова В. М. и др. Медофлюкон (флуконазол) — последнее достижение в лечении микозов//Медико-фармацевтический вестник. 1996. № 9 — 10. С. 23 — 27. - Климко Н. Н., Васильева Н. В., Антонов В. Б. и др. Проект рекомендаций по лечению кандидоза//Проблемы медицинской микологии. 2001. Т. 3. № 3. С. 12 — 25.
- Климко Н. Н., Васильева Н. В., Елинов Н. П. и др. Перечень основных методов и критериев диагностики микозов. СПб., 2001. 24 с.
- Лещенко В. М., Лещенко Г. М. Флюкостат — отечественный системный антимикотик//Новые лекарственные препараты в практике дерматовенетолога. М., 2001. С. 68 — 69.
- Лещенко В. М., Богуш П. Г., Важбин Л. Б. и др. Лечение микозов флюкостатом // Вестник последипломного образования. 2002. № 1. С. 51.
- Сергеев А. Ю., Сергеев Ю. В. Кандидоз. М., 2001. 472 с.
- Henderson J. R. Fluconazol — a significant advance in the management of human fungal disease//A. Framtung (Ed.) Discovery, Development and Evaluation of Antifungal Agents.
 1987. P. 77 — 79.
1987. P. 77 — 79. - De Wit S., Weerts D., Gossens H. Comparison of fluconazole and ketokonazole for orofaringeal candidosis in AIDS //Lancet. 1989. P. 746 — 749.
Грибы рода Сandida в кишечнике: клинические аспекты
Слизистые оболочки являются «открытыми системами» макроорганизма,
непрерывно контактирующими с окружающей средой. Контакт слизистых оболочек
человека и грибов рода Candida объясняет значительную распространенность
транзиторного кандидоносительства в человеческой популяции. Клиническое значение
обнаружения грибов рода Candida в кале пациента неоднозначно, поскольку может
свидетельствовать как о норме, так и о патологии. Спектр болезней, вызываемых
Candida spp., достаточно широк и варьирует от поверхностных поражений слизистых
оболочек до висцеральных микотических поражений. Поражение слизистых оболочек
органов пищеварения, вызываемое Candida spp. , является частой инфекцией,
особенно у пациентов с иммунодефицитными состояниями.
, является частой инфекцией,
особенно у пациентов с иммунодефицитными состояниями.
Во врачебной практике среди различных форм кандидозного поражения слизистых
оболочек пищеварительного тракта кандидозный дисбиоз кишечника встречается
достаточно часто. Полагают также, что при системном кандидозе кишечник может
служить источником инфекции, где Candida spp. часто обнаруживают в составе
кишечной микробиоты, и поражение желудочно-кишечного тракта часто предшествует
инвазивному системному кандидозу. Например, при аутопсии онкологических
пациентов с системным кандидозом показано, что у 20% таких больных обнаружены
кандидозные поражения тонкой и толстой кишки. Спонтанная перфорация слепой кишки
ассоциируется с системным кандидозом у недоношенных детей – другой популяционной
группы риска.
Кандидозный дисбиоз можно представить как увеличение представительства грибов
рода Candida в составе микробиоты желудочно-кишечного тракта на фоне устойчивого
дефицита нормальной бактериобиоты. Развитию кандидозного дисбиоза кишечника как
варианта кандидоза слизистых оболочек способствовала широко распространенная
практика применения антибактериальной терапии, создающая условия для уничтожения
естественных конкурентов грибов – бактерий, а также увеличение числа пациентов с
иммунодефицитными состояниями различного генеза.
Развитию кандидозного дисбиоза кишечника как
варианта кандидоза слизистых оболочек способствовала широко распространенная
практика применения антибактериальной терапии, создающая условия для уничтожения
естественных конкурентов грибов – бактерий, а также увеличение числа пациентов с
иммунодефицитными состояниями различного генеза.
Сложность рассматриваемой проблемы лишний раз подчеркивает тот факт, что до сих
пор нет единства в вопросе нозологической терминологии, касающейся кандидоза
кишечника. Так, нам удалось обнаружить в литературе несколько терминов,
применяемых для обозначения состояний, ассоциированных с обнаружением грибов в
кишечнике: избыточный интестинальный рост Candida (intestinal Candida overgrowth),
кандидоассоциированная диарея (Candidaassociated diarrhea),
кандидоассоциированный синдром (Candidaassociated syndrom), синдром кандидозной
гиперчувствительности (сandidiasis hypersensitivity syndrome), кандидозный
энтерит (в МКБ-10), просветный предынвазивный кандидоз или кандидаколонопатия,
дисбиоз кишечника с повышенной (или избыточной) пролиферацией Candida spp.
Патогенез кандидоза слизистых оболочек пищеварительного тракта характеризуется
последовательным прохождением всех следующих этапов – адгезии, инвазии,
кандидемии, висцеральных поражений. На первом этапе микромицеты адгезируются к
эпителиоцитам какого-либо участка слизистой оболочки. Исследования, проведенные
на экспериментальной модели (мышах, получавших антибиотики), показали, что C.
albicans соединяется со слизистой оболочкой толстого кишечника по меньшей мере
посредством пяти различных механизмов. Данные механизмы включают: адгезию к
кишечному эпителию, адгезию к слизи, коадгезию к адгезированным грибам,
коадгезию к адгезированным бактериям, встраивание в структуры слизистого геля,
лежащие выше эпителия (M.J. Kennedy et al., 1987).
В дальнейшем дефекты в системе резистентности позволяют микромицетам через
трансформацию в псевдомицелий внедряться (инвазироваться) в слизистую оболочку и
подлежащие ткани. Цитопения – решающий фактор, который позволяет инвазирующимся
грибам достигать стенки сосуда, затем происходит транслокация возбудителя в
мезентеральные лимфатические узлы, а затем по системе портальной вены в
системный кровоток и внутренние органы.
Способность к пенетрации долгое время считалась основным фактором вирулентности
Candida spp., так как будучи комменсальным микроорганизмом слизистых оболочек и
непосредственно кишечной клетки Candida могут служить источником инвазивной
инфекции. Однако способность Candida заселять поверхности и образовывать
биопленки в настоящее время считается не менее значимым признаком вирулентности
гриба.
Три механизма помогают объяснить феномен транслокации: нарушение кишечной
барьерной функции, избыточный рост оппортунистической микробиоты кишечника,
нарушение защитных механизмов макроорганизма. Уникальность сосудистой анатомии
кишечника, предрасположенность к ишемии и гипоксии слизистой оболочки, нарушение
моторно-эвакуаторной функции усугубляет процесс транслокации в условиях
увеличения продукции токсинов и, соответственно, их резорбции. Массивная
транслокация грибов из кишечника в условиях нарушенного интестинального
кровотока приводит к развитию кандидемии. В отсутствие адекватной терапии
кандидемия приводит к образованию очагов инвазивного кандидоза в висцеральных
органах: легких, эндокарде, печени, центральной нервной системе.
В отсутствие адекватной терапии
кандидемия приводит к образованию очагов инвазивного кандидоза в висцеральных
органах: легких, эндокарде, печени, центральной нервной системе.
Микромицеты Candida spp. как типичные возбудители оппортунистической инфекции
проявляют свой патогенный потенциал при условии нарушений в системе
антимикробной резистентности хозяина. При оптимальной реакции механизмов
антифунгальной резистентности хозяина клетки микромицетов будут уничтожены или
после короткого присутствия отторгнуты с выделением во внешнюю среду (спонтанная
элиминация или транзиторное кандиданосительство соответственно). При
относительно легких поломах в системе антифунгальной резистентности
макроорганизма (в основе которых чаще лежит дисбиоз) грибы могут колонизировать
обширные площади «открытых систем» с формированием так называемого
персистирующего кандидоносительства, или колонизации. Клиническое значение этого
феномена еще предстоит уточнить, однако уже сейчас ясно, что принципиально
возможно возникновение клинически значимой микогенной сенсибилизации в
результате персистирующего контакта антигенных структур гриба с
иммунокомпетентными клетками слизистой оболочки человека. При выраженных
нарушениях в системе антифунгальной резистентности организма (иммунодефицитных
состояниях) возможна трансформация микромицетов в нитевидную форму
(псевдомицелий) и внедрение грибов в ткани микроорганизма, что собственно и
определяет развитие кандидоза. Таким образом, микогенная сенсибилизация и
аллергия к Candida spp. могут сформироваться как при кандидозе, так и при
колонизации слизистых оболочек макроорганизма.
При выраженных
нарушениях в системе антифунгальной резистентности организма (иммунодефицитных
состояниях) возможна трансформация микромицетов в нитевидную форму
(псевдомицелий) и внедрение грибов в ткани микроорганизма, что собственно и
определяет развитие кандидоза. Таким образом, микогенная сенсибилизация и
аллергия к Candida spp. могут сформироваться как при кандидозе, так и при
колонизации слизистых оболочек макроорганизма.
Антигены Candida spp. обладают различными аллергенными свойствами.
Протеинсодержащие компоненты клетки микромицетов (цитоплазматические белки,
алкогольдегидрогеназа, кислый Р2 протеин) индуцируют преимущественно развитие
немедленного (I) и замедленного (IV) типов аллергических реакций, гликопротеины
клеточной стенки в большей степени стимулируют синтез нереагиновых антител и
могут вызывать иммунокомплексный (III) тип реакции.
Умеренная сенсибилизация к аллергенам Candida spp. – довольно распространенное
явление. В то же время повышенный уровень специфических реагиновых антител к
Candida spp. у больных, страдающих различными аллергозами, также отмечают часто.
Например, у больных бронхиальной астмой сенсибилизацию к антигенам
дрожжеподобных грибов обнаруживают в 10-55% случаев.
В то же время повышенный уровень специфических реагиновых антител к
Candida spp. у больных, страдающих различными аллергозами, также отмечают часто.
Например, у больных бронхиальной астмой сенсибилизацию к антигенам
дрожжеподобных грибов обнаруживают в 10-55% случаев.
Инвазивный кандидоз кишечника, связанный с трансформацией грибов в псевдомицелий
и внедрением последнего в ткани кишечника, развивается у больных с глубокими
иммунодефицитными состояниями. В группе риска по инвазивному кандидозу находятся
больные СПИДом, а также пациенты, длительно получающие терапию системными
глюкокортикостероидами и иммунодепрессантами, лица с генетически
детерминированными иммунодефицитами. Клиническая картина при инвазивном
кандидозе кишечника характеризуется тяжелым состоянием больного, выраженной
интоксикацией, абдоминальным болевым синдромом, диареей (но не всегда!),
лихорадкой. При эндоскопическом исследовании выявляют выраженный
эрозивно-фибринозный колит. Характерно, что кандидозный колит «включен» в
картину кандидасепсиса, то есть одновременно выявляют специфические поражения
легких, кожи, полости рта и пищевода, гепатоспленарный кандидоз. При
морфологическом исследовании слизистых оболочек обнаруживают нитевидные формы
Candida spp. Инвазивный кандидоз кишечника у иммунокомпетентных субъектов
маловероятен (W.R. Jarvis,1995).
Характерно, что кандидозный колит «включен» в
картину кандидасепсиса, то есть одновременно выявляют специфические поражения
легких, кожи, полости рта и пищевода, гепатоспленарный кандидоз. При
морфологическом исследовании слизистых оболочек обнаруживают нитевидные формы
Candida spp. Инвазивный кандидоз кишечника у иммунокомпетентных субъектов
маловероятен (W.R. Jarvis,1995).
Течение язвенной болезни двенадцатиперстной кишки или язвенного колита также
может осложниться кандидозом. При этом инвазия псевдомицелия Candida spp.
происходит исключительно в участках кишечника, деэпителизированных вследствие
основного заболевания. Такие формы поражения называют инвазивными фокальными.
Однако в практике терапевта чаще встречается неинвазивное поражение – дисбиоз
кишечника с избыточным ростом Candida spp. Этот вариант заболевания не связан с
трансформацией грибов в нити псевдомицелия и внедрением в слизистую оболочку
кишечника. В его основе лежит действие метаболитов грибов, резорбируемых в
кишечнике при массивном росте последних в просвете кишки. Около 36% всех
дисбиозов кишечника протекают с избыточным интестинальным ростом Candida spp.
При кандидозном дисбиозе кишечника состояние больных, как правило,
удовлетворительное. Симптомы заболевания: флатуленция, умеренный абдоминальный
дискомфорт, изменения в консистенции кала и частоте стула (обычно кал
кашицеобразный, чаще 2-3 раз в сутки), признаки умеренной интоксикации и
тенденция к обострению аллергических и псевдоаллергических заболеваний.
В его основе лежит действие метаболитов грибов, резорбируемых в
кишечнике при массивном росте последних в просвете кишки. Около 36% всех
дисбиозов кишечника протекают с избыточным интестинальным ростом Candida spp.
При кандидозном дисбиозе кишечника состояние больных, как правило,
удовлетворительное. Симптомы заболевания: флатуленция, умеренный абдоминальный
дискомфорт, изменения в консистенции кала и частоте стула (обычно кал
кашицеобразный, чаще 2-3 раз в сутки), признаки умеренной интоксикации и
тенденция к обострению аллергических и псевдоаллергических заболеваний.
Важно отметить, что кандидоз слизистых оболочек часто протекает как
микст-инфекция. Это происходит из-за того, что дисбиоз (т.е. дефицит облигатных
бифидумбактерий и лактобацилл) создает условия для адгезии на слизистой оболочке
кишечника не только дрожжеподобных грибов, но и условно-патогенной бактериобиоты.
Так, частота микст-инфекции при дисбиозе кишечника с повышенной пролиферацией
грибов рода Candida составляет 63%. При этом чаще обнаруживают ассоциацию со
значительным количеством бактерий с так называемым протеолитическим основным
путем метаболизма (условно-патогенными): Esherichia coli, Ristella spp.,
Clostridium perfringens, Klebsiella spp., Morganella spp., Bacteroides spp.,
Staphilococcus aureus, Pseudomonas aeruginosa.
При этом чаще обнаруживают ассоциацию со
значительным количеством бактерий с так называемым протеолитическим основным
путем метаболизма (условно-патогенными): Esherichia coli, Ristella spp.,
Clostridium perfringens, Klebsiella spp., Morganella spp., Bacteroides spp.,
Staphilococcus aureus, Pseudomonas aeruginosa.
Заподозрить кандидозное поражение кишечника позволяет наличие характерных
факторов риска. К факторам риска кандидоза пищеварительного тракта относят:
детский возраст (недоношенные дети, дети со сниженной массой тела), старческий
возраст, лечение антибактериальными препаратами и глюкокортикостероидами,
интенсивную цитостатическую полихимиотерапию, лучевую терапию, сахарный диабет и
другие заболевания эндокринной системы, СПИД, гемодиализ, тяжелые и хронические
истощающие заболевания, нарушения трофологического статуса, генетически
детерминированные иммунодефициты. Сочетание особых факторов, таких как массивная
колонизация кишечника Candida spp. при лечении широкоспектральными антибиотиками
с анаэробной активностью, применение третьей генерации цефалоспоринов, а также
антибиотиков, интенсивно концентрирующихся в собственной пластинке кишечника,
первичное повреждение кишечника, гипохлоргидрия желудка, снижение кишечной
перистальтики, цитотоксическая химиотерапия, длительное парентеральное питание
могут привести к развитию кандидемии.
при лечении широкоспектральными антибиотиками
с анаэробной активностью, применение третьей генерации цефалоспоринов, а также
антибиотиков, интенсивно концентрирующихся в собственной пластинке кишечника,
первичное повреждение кишечника, гипохлоргидрия желудка, снижение кишечной
перистальтики, цитотоксическая химиотерапия, длительное парентеральное питание
могут привести к развитию кандидемии.
Клинические варианты течения кишечного дисбиоза и связь их с факторами риска
представлены в таблице.
Дифференциальный диагноз кандидоза и кандиданосительства в кишечнике может
представлять трудности. Довольно частая ошибка – постановка диагноза «кандидоз»
только на основании выявления факта роста дрожжеподобных грибов в фекалиях.
Между тем этот факт может отражать транзиторное кандидоносительство. Для
диагностики кандидоза, впрочем, равно как и для любой другой оппортунистической
инфекции, важно не только продемонстрировать возбудитель, но и доказать его
участие в патологическом процессе. Один из принципиальных критериев диагноза
оппортунистической инфекции – наличие поломок в системе антимикробной
резистентности, а для рассматриваемой нами формы поражения – это дефицит
облигатной бактериобиоты – естественных конкурентов микромицетов. Таким образом,
диагноз дисбиоза кишечника с избыточным ростом Candida spp. устанавливают при
наличии следующих критериев:
Один из принципиальных критериев диагноза
оппортунистической инфекции – наличие поломок в системе антимикробной
резистентности, а для рассматриваемой нами формы поражения – это дефицит
облигатной бактериобиоты – естественных конкурентов микромицетов. Таким образом,
диагноз дисбиоза кишечника с избыточным ростом Candida spp. устанавливают при
наличии следующих критериев:
– синдром кишечной диспепсии;
– лабораторно подтвержденный дисбиоз кишечника;
– рост Candida spp. свыше 1000 КОЕ/г при посеве кала.
Эндоскопические исследования с цитологическим изучением препаратов
малоинформативны, так как чаще всего патологических изменений не выявляют.
Дифференциальный диагноз кандидоза кишечника проводят также с хроническими
инфекционными колитами, ферментопатиями (лактазной, глютеновой), опухолями,
синдромом раздраженной толстой кишки.
Часть пациентов с кандидозом кишечника отмечают явления перианального кандидоза.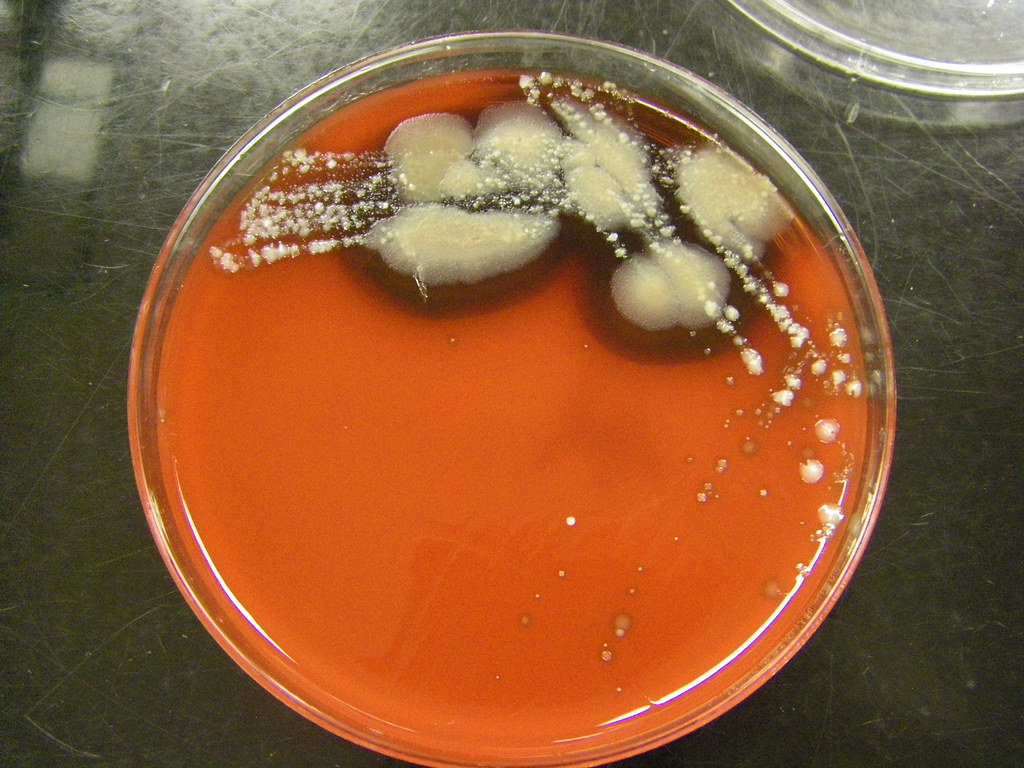 Это заболевание появляется упорно рецидивирующим анальным зудом и жжением. При
осмотре врач выявляет гиперемию и мацерацию перианальной области, резко
ограниченные от окружающей кожи, а также шелушение, поверхностные трещины и
эрозии. Диагноз перианального кандидоза подтверждают обнаружением псевдомицелия
Candida spp. при микроскопии кожных чешуек перианальной области.
Это заболевание появляется упорно рецидивирующим анальным зудом и жжением. При
осмотре врач выявляет гиперемию и мацерацию перианальной области, резко
ограниченные от окружающей кожи, а также шелушение, поверхностные трещины и
эрозии. Диагноз перианального кандидоза подтверждают обнаружением псевдомицелия
Candida spp. при микроскопии кожных чешуек перианальной области.
Диагностика кандидоза кишечника у человека иногда представляет значительные
проблемы, связанные с недостаточной осведомленностью врачей в области
клинической микологии, и трудности дифференциального диагноза между кандидозом
слизистых оболочек и кандидоносительством. Между тем этот факт может отражать
только транзиторное кандидоносительство, часто встречающееся в популяции.
Лечение же кандидоза связано не только с проблемой решения рационального выбора
противогрибкового препарата, но и с необходимостью оценивать влияние на течение
микотического поражения основного заболевания и ряда иммунопатологических
факторов.
При кандидозе органов пищеварения для постановки диагноза требуется комплексное
клинико-лабораторное обследование. Такой диагностический комплекс включает
выявление предрасполагающих факторов, объективных клинических и эндоскопических
признаков кандидоза, обнаружение Candida spp. в серии биосубстратов и в
биопсийных материалах (с подтверждением их участия в данном инфекционном
процессе).
План обследования пациента с подозрением на кандидоз кишечника и микогенную
аллергию должен дополнительно включать исследование кала на дисбиоз, копрограмму,
определение уровня специфических противокандидозных IgE антител и общего IgE, а
также кожные пробы с аллергеном Candida (в период ремиссии аллергологической
патологии). Особо следует подчеркнуть значение тщательного сбора анамнеза и
выявление характерных черт заболевания, в частности связь обострения
аллергозависимой патологии с применением антибактериальной терапии или
обострением кишечной симптоматики.
В плане лечения пациента с кандидозом кишечника необходимо предусмотреть
следующие терапевтические направления:
· лечение основного заболевания согласно принятым стандартам;
· селективная деконтаминация кишечника, направленная на устранение причины
заболевания – грибов рода Candida;
· назначение про- и пребиотиков – препаратов, способствующих восстановлению
естественной антимикробной резистентности слизистой оболочки кишечника с целью
предотвращения рецидивов дисбиоза;
· симптоматическая терапия и модификация диеты.
Во время лечения больным рекомендован пищевой рацион с ограничением простых
углеводов (сахара, сладких фруктов и ягод, кондитерских изделий, меда, молока,
яблок, винограда, белокочанной капусты, бобовых, кваса, пива). По показаниям
допускается применение ферментных препаратов, энтеросорбентов, спазмолитиков,
антибактериальных энтеросептиков.
Терапия кандидозного колита, связанного, как было указано выше, с инвазией гриба
в ткани кишечника, требует назначения резорбируемых антифунгальных средств
(например, азоловых) или внутривенного введения амфотерицина В.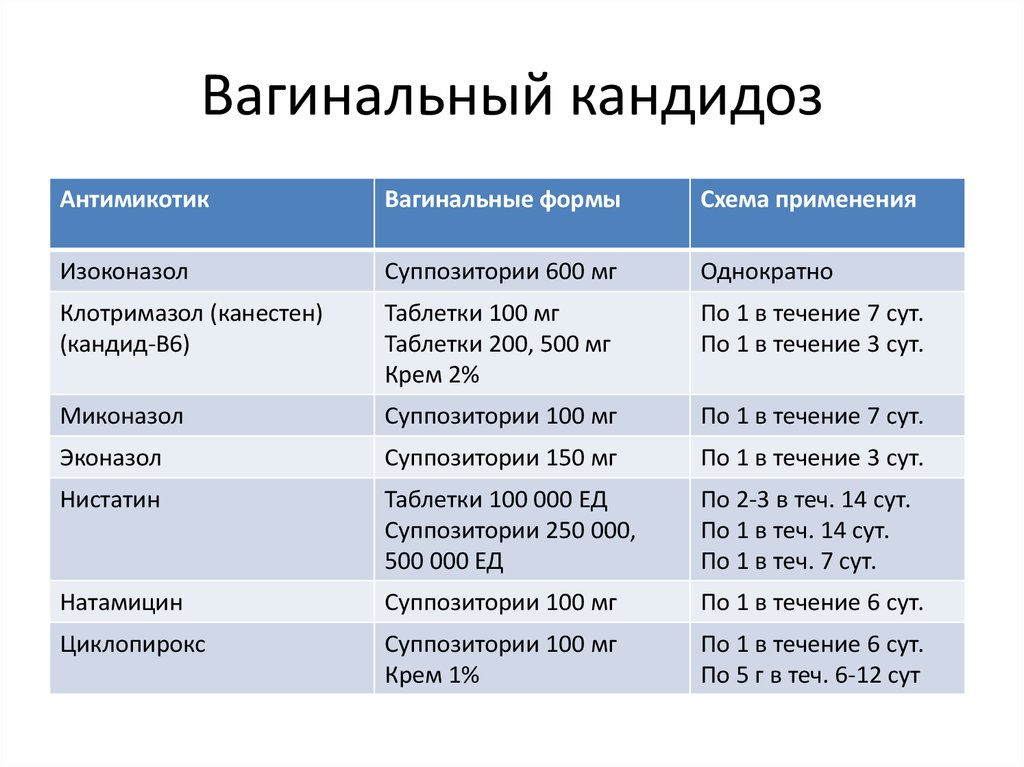 Лечение
кандидозного дисбиоза кишечника не требует назначения резорбируемых азоловых
антимикотиков. Показано, что лечение, например, флуконазолом, может угнетать
рост Candida spp. в кишечнике: до 1/3 пациентов полностью санируются, а у
остальных происходит снижение степени контаминации фекалий более чем в 6 раз. В
то же время у 2/3 пациентов полной деконтаминации кишечника от дрожжеподобных
грибов не происходит. Вероятно, это связано с тем, что около 80% активных
метаболитов флуконазола выводятся из макроорганизма с мочой, а в просвете
кишечника данный антифунгальный препарат накапливается мало.
Лечение
кандидозного дисбиоза кишечника не требует назначения резорбируемых азоловых
антимикотиков. Показано, что лечение, например, флуконазолом, может угнетать
рост Candida spp. в кишечнике: до 1/3 пациентов полностью санируются, а у
остальных происходит снижение степени контаминации фекалий более чем в 6 раз. В
то же время у 2/3 пациентов полной деконтаминации кишечника от дрожжеподобных
грибов не происходит. Вероятно, это связано с тем, что около 80% активных
метаболитов флуконазола выводятся из макроорганизма с мочой, а в просвете
кишечника данный антифунгальный препарат накапливается мало.
Чаще всего для селективной деконтаминации кишечника от микромицетов рода Candida
назначают нистатин и натамицин (Пимафуцин). В отличие от имидазоловых
антимикотиков нистатин и натамицин (Пимафуцин) практически не резорбируются в
кишечнике. Это свойство, с одной стороны, делает лечение относительно
безопасным. С другой, отсутствие резорбции обусловливает стабильно высокую
концентрацию нистатина и натамицина (Пимафуцина) именно в просвете кишечника,
что является залогом успешного лечения дисбиоза кишечника с избыточным ростом
Candida spp. Самым частым нежелательным эффектом при назначении этих средств
является раздражение слизистых оболочек и обусловленная этим тошнота и диарея.
Необходимо отметить, что у Пимафуцина эти явления выражены в меньшей степени,
чем у нистатина. В отличие от нистатина натамицин (Пимафуцин) разрешен для
применения у беременных, кормящих, новорожденных, а также при язвенной болезни и
панкреатите. Натамицин (Пимафуцин) назначают в таблетках взрослым по 100 мг
четыре раза в день, а детям по 100 мг 2 раза в день. Курсы лечения этим
средством длительностью 5-10 дней обычно приводят к элиминации дрожжеподобных
грибов из кишечника, однако при сохранении факторов, снижающих эффективность
местных антифунгальных барьеров, возможна реинфекция.
Самым частым нежелательным эффектом при назначении этих средств
является раздражение слизистых оболочек и обусловленная этим тошнота и диарея.
Необходимо отметить, что у Пимафуцина эти явления выражены в меньшей степени,
чем у нистатина. В отличие от нистатина натамицин (Пимафуцин) разрешен для
применения у беременных, кормящих, новорожденных, а также при язвенной болезни и
панкреатите. Натамицин (Пимафуцин) назначают в таблетках взрослым по 100 мг
четыре раза в день, а детям по 100 мг 2 раза в день. Курсы лечения этим
средством длительностью 5-10 дней обычно приводят к элиминации дрожжеподобных
грибов из кишечника, однако при сохранении факторов, снижающих эффективность
местных антифунгальных барьеров, возможна реинфекция.
Успешное решение первой задачи – селективной деконтаминации – позволяет
рассчитывать на успех в деле восстановления и консолидации эубиоза, т.е.
стойкого устранения дефицита нормобиоты кишечника. С этой целью традиционно
используют про- и пребиотики. Выбор пребиотиков, т.е. стимуляторов
интестинального роста резидентной нормобиоты, не содержащих живые культуры
нормобиоты, сегодня достаточно широк. Действующим началом таких средств может
являться лактулоза, пектин, некоторые биологически активные продукты обмена
облигатных бактерий и другие.
Выбор пребиотиков, т.е. стимуляторов
интестинального роста резидентной нормобиоты, не содержащих живые культуры
нормобиоты, сегодня достаточно широк. Действующим началом таких средств может
являться лактулоза, пектин, некоторые биологически активные продукты обмена
облигатных бактерий и другие.
Для лечения перианального кандидоза местно применяют мази и кремы, содержащие
антифунгальные средства, например натамицин или другие. Однако одна только
местная терапия не предотвращает рецидивов дерматита, поскольку не может
осуществить селективную деконтаминацию основного резервуара кандидозной инфекции
– кишечника. Поэтому при перианальном кандидозе необходимо одновременно
проводить терапию кандидоза кишечника согласно принципам, изложенным выше.
Список литературы находится в редакции.
Статья напечатана в сокращении.
«Проблемы медицинской микологии»,
№ 4, т. 9, 2007 г.
СТАТТІ ЗА ТЕМОЮ
09. 06.2021
Акушерство/гінекологія «Три кити» здорової вагітності: фолієва кислота, йод та омега‑3-кислоти
06.2021
Акушерство/гінекологія «Три кити» здорової вагітності: фолієва кислота, йод та омега‑3-кислотиПреконцепційна підготовка, вагітність та лактація – це надзвичайно важливі періоди для жінки, оскільки саме у цей час закладається фундамент здоров’я її майбутньої дитини. Забезпечення жінки найбільш необхідними нутрієнтами дозволяє збільшити вірогідність настання вагітності, її нормального фізіологічного перебігу та народження здорового потомства. У статті наведено міжнародні й вітчизняні рекомендації щодо підтримки нутритивного статусу жінки під час преконцепційної підготовки, вагітності та лактації, а також представлено сучасні дослідження впливу фолієвої кислоти, йоду та омега-3-кислот на здоров’я матері та дитини….
08. 06.2021
Акушерство/гінекологія Гіпертонічна хвороба у вагітних: питання та відповіді
06.2021
Акушерство/гінекологія Гіпертонічна хвороба у вагітних: питання та відповідіАртеріальна гіпертензія (АГ) у вагітних – актуальна проблема сьогодення. Одним із поширених гіпертензивних станів під час вагітності є гіпертонічна хвороба (ГХ). Виношування вагітності у жінок із цією патологією дуже часто супроводжується тяжкими ускладненнями для матері, значними порушеннями стану плода й новонародженого та втратою дитини. Найбільш характерним, частим і вкрай несприятливим ускладненням у цієї категорії хворих є поєднана прееклампсія. Саме поєднана прееклампсія, особливо така, що розвивається рано і має тяжкій перебіг, передусім визначає негативне закінчення вагітності для матері та дитини за наявності ГХ.
У результаті проведених у ДУ «Інститут педіатрії, акушерства і гінекології ім. акад. О. М. Лук’янової НАМН України» численних наукових досліджень із вивчення особливостей патогенезу ускладнень у вагітних із ГХ і розроблених на їх основі лікувально-профілактичних заходів стало можливим покращення закінчення вагітності для матері й дитини у цієї категорії хворих.
…
акад. О. М. Лук’янової НАМН України» численних наукових досліджень із вивчення особливостей патогенезу ускладнень у вагітних із ГХ і розроблених на їх основі лікувально-профілактичних заходів стало можливим покращення закінчення вагітності для матері й дитини у цієї категорії хворих.
…
Нестача заліза є найбільш поширеним харчовим дефіцитним станом у світі й однією з основних причин анемії у вагітних жінок. Залізодефіцит негативно впливає не лише на здоров’я вагітної, але й може стати причиною тяжких ускладнень у плода. Своєчасна профілактика нестачі заліза у групах ризику дозволяє покращити прогнози вагітності. У статті висвітлено проблему залізодефіциту під час гестації з визначенням основних груп ризику нестачі заліза. Представлено сучасні надійні методи діагностики та лікування цього стану на основі міжнародних і вітчизняних клінічних настанов.
…
Залізодефіцит негативно впливає не лише на здоров’я вагітної, але й може стати причиною тяжких ускладнень у плода. Своєчасна профілактика нестачі заліза у групах ризику дозволяє покращити прогнози вагітності. У статті висвітлено проблему залізодефіциту під час гестації з визначенням основних груп ризику нестачі заліза. Представлено сучасні надійні методи діагностики та лікування цього стану на основі міжнародних і вітчизняних клінічних настанов.
…
Туроктоког альфа (препарат НовоЕйт, фармацевтична компанія Novo Nordisk, Данія) – це рекомбінантний людський фактор коагуляції VIII (FVIII) з усіченим В-доменом без будь-яких інших модифікацій у послідовності амінокислот. Засіб є очищеним білком, який складається з 1445 амінокислот і має молекулярну масу близько 166 кДа. Його виготовляють за допомогою технології рекомбінантної ДНК у клітинах яєчників китайського хом’яка й отримують без додавання будь-яких білків людського чи тваринного походження в процесі культивування клітин, очищення або виробництва готового препарату….
Засіб є очищеним білком, який складається з 1445 амінокислот і має молекулярну масу близько 166 кДа. Його виготовляють за допомогою технології рекомбінантної ДНК у клітинах яєчників китайського хом’яка й отримують без додавання будь-яких білків людського чи тваринного походження в процесі культивування клітин, очищення або виробництва готового препарату….
Candida spp. являются составляющей нормальной микрофлоры кишечника человека. В ротовой полости у 25% людей, которые не имеют никаких признаков заболевания молочницей, определяются грибки. Этот грибок может располагаться абсолютно везде, в различном виде инфекции. Грибковая инфекция может сопровождаться поражением гладкой мускулатуры, полых и паренхиматозных органов, а также может быть поверхностным и глубоким. В нормальных условиях в кишечнике человека происходит регуляция роста и развития грибков за счет иммунитета, а главная роль в этой регуляции отводится фагоцитам и полиморфноядерным лейкоцитам. Также в этом процессе принимают участие кишечные симбионты, которые вырабатывают вещества, имеющие антибактериальные свойства. За счет этих веществ предотвращается появление патогенной микрофлоры и ее рост, а также блокируется рост флоры, которая имеет условную патогенность. Самыми выраженными свойствами антагонизма обладают эшерихии, бифидобактерии и энтерококки. Кандидозная инфекция это патологический процесс, при котором происходит чрезмерный рост грибков в пищеварительном канале в первую очередь, что при развитии процесса может проявится и в других органах, таких как гениталии, паренхиматозные органы, также грибок может поражать кожу. Грибы Candida проявляют адгезивность к клеткам эпителия, их прикрепление к слизистому слою это обязательное условие для дальнейшего развития. Candida очень быстро образует нити псевдомицелия, а вирулентность грибка может видоизменяться в зависимости от генотипа. Факторы рискаОбщие факторы, которые могут быть причиной и способствуют развитию грибков рода Candida, иными словами поражению организма дрожжеподобными грибами, представляют собой состояния, при которых происходит снижение защитных свойств организма:
К факторам риска относятся все состояния, при которых страдает кровообращение в кишечнике, что дает предпосылки для транслокации грибка в другие органы и ткани. При нарушении процессов пищеварения и усвоения пищи развивается избыточный рост микроорганизмов в кишечнике. Кандидоз кишечника встречается у 4% пациентов, половина из которых получала химиотерапию в связи с онкологическим процессом. ПатогенезСуществует два разных механизма развития дрожжеподобных грибков в организме человека, и органов пищеварения в частности. Инвазивный кандидоз развивается за счет внедрения в кишечник человека нитчатой формы грибка. В первую очередь происходит адгезия к клеткам эпителия, после грибок проникает в эпителий, за пределы базальной мембраны. В случае прогрессирования процесса развивается лимфогенная диссеминация грибка, что приводит к развитию системного кандидоза, при котором поражаются слизистые оболочки разных органов. Также может развиться генерализованный, которые еще называется висцеральным формой, при котором поражаются висцеральные органы. При развитии диссеминированной формы кандидоза обнаруживают гигантские клетки с несколькими ядрами в лимфатических узлах. Эти клетки содержат грибы, и, скорее всего, именно это представляет собой проявление незавершенного процесса фагоцитоза. Чаще всего инвазивный кандидоз развивается в тех органах, которые имеют плоский многослойный эпителий ротовая полость, пищевод. Несколько реже он встречается в органах с цилиндрическим эпителием желудок, кишечник. Неинвазивный кандидоз развивается без превращения грибков в нитчатую форму. Избыточный рост дрожжеподобных грибков происходит в просвете кишечника. Патогенетическим фактором в таком случае является нарушение процессов пищеварения, а также проникновение в кровяное русло продуктов метаболизма микробов, что способствует развитию реакции иммунного воспаления. Кандидоз слизистых оболочек органов, расположенных вне пищеварительного канала, а также грибковое поражение паренхиматозных органов при генерализованном кандидозе является проявлением миграции грибков из кишечника, где в норме должны располагаться эти грибки. Внекишечный кандидоз (генитальный, полости рта) является одним из проявлений развития системного кандидоза, который начинает развиваться в просвете кишечника. Классификация
КлиникаОсобенности клинической картины кишечного кандидоза мало изучены и недостаточно хорошо знакомы подавляющему большинству докторов. Данное заболевание проявляется достаточно скудными проявления, особенно со стороны органов пищеварения, а эндоскопическая картина часто расценивается ошибочно. Частой ошибкой в диагностике патологии является отсутствие морфологического исследования, направленного на подтверждение кандидоза. Симптомы патологии отличаются в зависимости от уровня, на котором локализуется грибковый процесс.
Очень часто кандидозу кишечника сопутствует гипертермическая реакция. Осложнения кандидоза кишечника достаточно численные. Ими являются перфорация кишечника, развитие язвенных дефектов кишечника и пенетрация развившихся язв в смежные органы, кровотечение, генерализация дрожжевых грибов, при котором поражаются паренхиматозные органы, а также грибковый сепсис. В случае поражения паренхиматозных органов может развиваться нейтропения, которая также может появляться в четвертой стадии СПИДа. При инвазивном кандидозе летальный исход встречается в 40%. Диагностика кандидозаДиагностические мероприятия проводятся с оглядкой на назначение противогрибковой терапии. Для обнаружения кандидоза информативным является исследование ликвора или других стерильных жидкостей организма, а также обнаружение их в тканях. С целью улучшения чувствительности методов обнаружения грибков рекомендовано использование как минимум трех биоптатов слизистой оболочки. Микроскопия проводится в окрашенных и нативных препаратах. Применяются такие методы микроскопии:
После выявления грибов проводится исследование на чувствительность к противогрибковым препаратам. Если известно, к каким препаратам Candida чувствительна, назначение лечения и прогноз значительно улучшаются, что может позволить забыть пациенту о грибах. Генерализованный кандидоз можно установить только в том случае, если грибы обнаружены в крови и клиническая картина соответствует процессу. Огромное значение имеют серологические методы, которые помогают выявить больных с вероятным развитием инвазивного микоза. Возможны ложноположительные результаты, которые могут появляться в случае носительства, сенсибилизации. Также могут быть и ложноотрицательные результаты, которые чаще всего развиваются при различных иммунодефицитах. Диагноз устанавливается с учетом локализации процесса, вида колоний грибка, а также с учетом фоновых заболеваний. Диагноз «Кандидоз» является не совсем корректным, поскольку не указывает осложнений процесса и не дает понимания другим докторам о том, как лечить такое заболевание, а также заставляет терять время на повторное обследование пациента. Дифференциальная диагностика кандидоза кишечника должна проводится с различными воспалительными заболеваниями органов пищеварения, склонных к хронизации процесса. Инвазивный кандидоз следует дифференцировать с такими заболеваниями, как диарея, ассоциированная с приемом антибиотиков, злокачественные новообразования, ишемический колит. Дифференциальный диагноз неинвазивной формы кандидоза проводится с колитами и энтеритами различных этиологических причин, а также проктитом, геморроем и другими заболеваниями. Симптомом, который может косвенно подтверждать развитие кандидоза кишечника является проявление грибкового поражения вне кишечника. Лечение кандидозаОбнаружение дрожжеподобных грибков в анализе кала не является показанием для лечения противогрибковыми препаратами. Для лечения кандидоза кишечника используют те препараты, которые не адсорбируются в кишечнике. На сегодняшний день существует внушительное разнообразие антигрибковых препаратов. Флуконазол и кетоконазол имеют системное действие. К препаратам, которые практически не всасываются относятся нистатин и леворин. Причем нистатин в последнее время вновь обрел популярность, поскольку из-за низкого его применения чувствительность грибков к нему восстановилась. Также как и флуконазол и кетоконазол, нистатин имеет большое количество побочных эффектов. При применении пероральных противогрибковых препаратов на начальных этапах лечение возможно появление диспептических расстройств, которые не являются показанием для отмены препаратов, поскольку диспепсия самостоятельно разрешается в течение нескольких дней. Тактика лечения местного кандидоза препаратами, обладающими местным действием не является правильной, поскольку источником развития грибкового поражения различных органов является кишечник. Следовательно, лечение должно быть направлено на борьбу с патологическим ростом грибка в кишечнике, тогда эффект от лечения будет носить длительный эффект, а также будет снижена возможность развития рецидивов заболевания. Распознавание и адекватное своевременно назначенное лечение являются особо важными для профилактических мероприятий развития генерализованного или системного кандидоза. К группам риска развития этих форм заболевания следует отнести пациентов, получающих химиотерапию или иммуносупрессивную терапию. Исчезновения клинических проявлений заболевания и установление нормального уровня количества грибка в морфологическом исследовании считаются критериями эффективности лечения кандидоза. В некоторых случаях следует проводить несколько курсов лечения для достижения эффекта. Профилактика кандидозаОбщими принципами профилактических мероприятий данного заболевания являются:
|
Лечение кандидоза кишечника — БИОФОН
- У Вас устойчивая форма кандидоза?
- Лечение кандидоза кишечника не приводит к позитивным результатам?
- Врачи после длительных курсов антибиотикотерапии разводят руками, а народные методы не помогают?
Кандидоз кишечника – это болезнь, которая протекает в кишечнике при появлении в нем патогенных грибков Candida. Они поражают слизистую оболочку вызывая первые симптомы. Эти грибки по сути всегда находятся в нашем кишечнике, но при появлении определенных условий они превращаются в патогенные. В большинстве случаев кандиды транзитно живут в нашем организме не проявляя никаких признаков поражения. Для грибка кишечник является привычным и естественным местом обитания. Когда создаются условия, которые непригодны для протекания жизни нормальных микроорганизмов кишечника и иммунитет организма не сопротивляется, начинает массово размножаться грибок, что в последствии и нарушает состояние микрофлоры. Далее в области ЖКТ появляются типичные для прохождения болезни кандидоза симптомы.
Врачи разделяют кандидоз по степени поражения на локализованные, единичные и в сочетании первого и второго. Неправильное питание, иммунодефициты, вирусы иммунодефицита, чрезмерная антибиотикотерапия, а также онкологические патологии – это основные факторы, которые способствуют развитию болезни.
Типичные симптомы кандидоза кишечника
Врачами различаются четыре формы кандидоза – это инвазивный, неинвазивный, фокальный и диффузный.
- Инвазивная форма в большинстве случаев проявляется у людей с сильными нарушениями иммунитета организма.
- Неинвазивный кандидоз проявляется в виде частого проноса с белыми примесями в виде хлопьев, чрезмерного метеоризма, а также постоянной боли в нижней части живота.
- Инвазивный кандидоз в фокальных формах отличается тем, что при протекании болезни поражаются участки кишечника с последующим появлением язвенной патологии.
- Диффузная форма характеризуется примесями слизи и крови в массах кала.
Кишечный кандидоз лечение
Лечение кандидоза желудочно кишечного тракта включает в себя назначение неабсорбирующих из просвета кишечника препаратов. В список таких лекарств входят кетаконазол, флуконазол, итраконазол, а также амфотерицин В. Эти антимикотические препараты имеют системное действие и вводятся в организм внутривенно или перорально. Очень часто лечение кишечного кандидоза такими лекарствами не приводят к нужным результатам. Все дело в том, что они почти полностью абсорбируются в верхних отделах желудочно-кишечного тракта не доходя до подвздошной кишки. Эта нижняя часть кишечника имеет наибольшую популяцию кандиды. Помимо этого, применение таких препаратов грозит в себе некие факторы риска, то есть побочный эффект в виде токсического гепатита.
Народные средства лечения кандидоза кишечника
В народе лечение кандидоза желудочно кишечного тракта производят с помощью отвара корня лопуха, корня кровохлебки и коры дуба, а также курильского чая. Корень кровохлебки, кору дуба и корень лопуха варят в воде до получения крепкого отвара. Его следует принимать по 3-4 столовых ложки перед едой. Курильский чай принимают в пищу как обычный в течении 2-3 недель. Конечно, кишечный кандидоз лечение такими методами проводить нецелесообразно, ведь применение трав способно только снизить признаки симптоматики.
Сложности лечения кандидоза кишечника
Применение противогрибковых препаратов может привести к появлению осложнений при протекании болезни, так как такая терапия не полностью убивает грибок понижая при этом иммунитет организма пациента. А народное самолечение только скроет признаки болезни, что может усугубить ситуацию.
Хотите избавиться от кандидоза?
Используйте в лечении аппарат «Уро-Биофон».
«Уро-Биофон» – это физиотерапевтический аппарат инфракрасной терапии нетепловой интенсивности, действует на клеточную оболочку микроба, повреждая её. В микробной клетке нарушаются обменные процессы, она инактивируется и теряет способность защищаться. Клетки иммунной системы (фагоциты) захватывают беззащитный патоген и лизируют (растворяют) его.
Достоинства «Уро-Биофона»:
- Эффективность лечения аппаратами серии «Биофон» по результатам клинических испытаний составляет от 64 до 100%.
- Прост в обращении.
- Им можно лечиться как одному, так и всей семьёй.
- Не вызывает побочных эффектов, так как действует только на патогенные микробы и их токсины.
- «Уро-Биофоном» можно пользоваться любым возрастным группам, а так же лицам, страдающим хроническими заболеваниями ЖКТ, печени, почек.
Посмотрите сами на результаты использования
«Уро-Биофона»:«Сейчас ПЦР анализы в норме
Купили Уро-Биофон полгода назад. До этого прошла 5 курсов антибиотиковой терапии от хламидиоза, микоплазмоза, герпеса и прилагающимся к ним молочнице, кольпиту, аднекситу и прочей гадости. Бесплодием страдаю уже 5 лет.
Выбрала самый «убойный» режим лечения. Параллельно лечилась антибиотиками и местно лечила шейку матки. В прошлые разы лечение не помогало вообще. Сейчас ПЦР анализы в норме. У мужа тоже.
Я, честно говоря, скептик. Но прошло уже 2,5 месяца. До сих пор не верю. Скоро попытаемся забеременеть.
Самое главное: самочувствие у меня отличное, болей внизу живота, выделений, менструальных болей, воспалений не стало!!! Кайф! Милые читатели, если у вас есть возможность, купите аппарат, а нет – закажите в складчину. Не мучайтесь!!!»
Без подписи.
«Ни хламидий, ни кандид
До лечения сдал анализы. Выявили кандиды и хламидии. После начала лечения аппаратом Уро-Биофон согласно указанному режиму лечения для молочницы, где-то через 3 недели начал замечать у себя положительные изменения в состоянии здоровья. Через 51 день после начала лечения пошел на полное обследование своего организма методом биорезонансной терапии. Ни хламидий, ни кандид, и вообще никаких намеков на какие-либо венерические инфекции»
Руслан Хазеев, г. Уфа, [email protected]
12 сентября 2008
Со всеми отзывами по аппаратам серии «Биофон» вы можете ознакомиться на странице Отзывы пациентов.
«Уро-Биофон» — это безопасная и эффективная альтернатива антибиотикам.
— Считаете информацию полезной? Поделитесь!Кандидозный дисбиоз кишечника у детей Текст научной статьи по специальности «Клиническая медицина»
Клшыш лекци
УДК 616.34-008.87:582.28]-053.2 БЕЛОУСОВА О.Ю.
Харьковская медицинская академия последипломного образования
КАНДИДОЗНЫЙ ДИСБИОЗ КИШЕЧНИКА У ДЕТЕЙ
Резюме. Обсуждаются роль грибов рода Candida в этиологии кишечного дисбиоза у детей, клинические формы заболевания, подходы к диагностике и лечению. Ключевые слова: кандидозный дисбиоз, кишечник, дети.
Одним из наиболее широко обсуждаемых вопросов не только педиатрической гастроэнтерологии, но педиатрии в целом является вопрос кишечного дисбиоза. При этом мнения, высказываемые авторами, порой диаметрально противоположны: от полного неприятия не только термина, но понятия в целом [17] до разработки новых лечебных препаратов для лечения дисбиоза кишечника [4].
Подходы зарубежных ученых к понятию «дисбиоз» более определенны. Всеми признается возможность существования дисбиоза тонкой кишки, именуемого во всем мире синдромом избыточного роста бактерий, избыточного размножения бактерий или избыточного микробного обсеменения (bacterial overgrowth syndrome) [18, 21]. Этот термин общепринят, расшифрован, изучены причины его возникновения и механизмы развития.
Что же касается толстокишечного дисбиоза, то в Международной классификации болезней 10-го пересмотра рубрика «дисбактериоз кишечника» отсутствует и клинические проявления, связываемые в нашем представлении с дисбиозом кишечника (периодические схваткообразные боли по ходу толстой кишки, метеоризм, расстройства стула со склонностью к поносу, запору или их чередование), расцениваются как проявления синдрома раздраженного кишечника (СРК). Тем не менее термин «дисбакте-риоз (дисбиоз) кишечника» широко используется в отечественной литературе и фактически является общепринятым [1, 8]. При этом целесообразно уточнить локализацию процесса — толстокишечный дисбиоз или дисбиоз толстой кишки.
Термин «дисбиоз» предпочтительнее термина «дисбактериоз». Дисбиоз — это состояние экосистемы (эубиоза), при котором имеет место нарушение функций всех ее компонентов: макроорганизма, его резидентной микрофлоры (причем не только бактерий, но и грибов рода Candida), среды их обитания, а также механизмов взаимодействия [6]. Поэтому в клиниче-
ской практике целесообразно использовать термины «дисбиоз толстой кишки» и «дисбиоз тонкой кишки». Эти изменения в большинстве случаев вторичны; может быть и по этой причине ни один из терминов не отражен в МКБ-10.
Дисбиоз кишечника на начальных этапах может не иметь четких кишечных проявлений, однако даже легкие степени кишечного дисбиоза, часто не имеющие клинического эквивалента, негативно сказываются на состоянии макроорганизма, снижая его общую резистентность и сопровождаясь метаболическими и пищеварительными дисфункциями [9, 10].
Кроме различных вариантов микробного толстокишечного дисбиоза, в последние годы все большее внимание привлекает к себе кандидозный дисбиоз [14, 20].
Кандидозный дисбиоз характеризуется увеличением представительства грибов рода Candida в составе микрофлоры кишечника на фоне устойчивого дефицита нормальной бактериальной флоры. Развитию кандидозного дисбиоза кишечника как варианта кандидоза слизистых оболочек способствуют широко распространенная практика применения антибактериальной терапии, создающая условия для уничтожения естественных конкурентов грибов — бактерий, а также увеличение числа пациентов с иммунодефи-цитными состояниями различного происхождения [12, 13].
Род Candida представляет собой дрожжевые грибы, родственные Ascomycetes, и включает разнообразные виды (Candida spp.), среди которых основное значение как возбудители кандидоза имеют: Candida albicans, Candida tropicalis, Candidaparapsilosis, Candida glabrata, Candida dubliniensis, Candida lusitaniae, Candida krusei. Candida spp. представляют собой компонент микрофлоры, симбионтной для человека. У 10—25 % населения, не имеющих клинических признаков грибкового поражения, Candida spp. непостоянно выявляются в полости рта, у 65—80 % — в содержимом кишечника [13].
КлЫчН лекцИ
6(41) • 2012
Термин «кандидоз» подразумевает патологический процесс, основу которого составляет избыточный рост Candida первично в желудочно-кишечном тракте и вторично — в других областях — на слизистой оболочке гениталий, бронхов, в паренхиматозных органах [5].
Одним из важнейших факторов риска развития кандидоза кишечника у детей является антибиотико-терапия, особенно длительное применение препаратов широкого спектра действия. Это может приводить к нарушению равновесия в микробном биоценозе кишечника, вследствие чего возможно избыточное развитие кандидозной популяции. Существенную роль играет и несбалансированное нерациональное питание, особенно детей первого года жизни (дефицит в рационе белков, витаминов). В эксперименте на животных показано, что недостаточное поступление белка в организм сопровождается снижением фагоцитарной и бактерицидной активности макрофагаль-ного звена, незавершенным фагоцитозом и повышением проницаемости кишечного барьера для Candida albicans [5, 16].
По современным представлениям, можно выделить два принципиально различных механизма патогенеза кандидоза органов пищеварения: инвазивный и неинвазивный кандидоз [11, 13].
Инвазивный кандидоз кишечника, связанный с трансформацией грибов в псевдомицелий и внедрением последнего в ткани кишечника, развивается у больных с глубокими иммунодефицитными состояниями вследствие основного заболевания.
Однако в практике педиатра чаще встречается неинвазивное поражение — дисбиоз кишечника с избыточным ростом Candida spp. В его основе лежит действие метаболитов грибов, резорбируемых в кишечнике при массивном росте последних в просвете кишки. Около 36 % всех дисбиозов кишечника протекает с избыточным интестинальным ростом Candida spp. [11, 12]. При кандидозном дисбиозе кишечника состояние больных, как правило, удовлетворительное. Симптомы заболевания характеризуются флатуленцией, умеренным абдоминальным дискомфортом, изменением консистенции кала и частоты стула (обычно кал кашицеобразный, чаще 2—3 раза в сутки), отмечаются признаки умеренной интоксикации и тенденция к обострению аллергических процессов.
Важно отметить, что кандидоз слизистых оболочек кишечника часто протекает как микст-инфекция. Это происходит из-за того, что дисбиоз (т.е. дефицит облигатных бифидобактерий и лактобацилл) создает условия для адгезии на слизистой оболочке кишечника не только дрожжеподобных грибов, но и условно-патогенной бактериобиоты. Так, частота микст-инфекции при дисбиозе кишечника с повышенной пролиферацией грибов рода Candida составляет 63 %. При этом чаще обнаруживают ассоциацию со значительным количеством бактерий с так называемым протеолитическим основным путем метаболизма (условно-патогенными): Esherichia coli, Ristella spp.,
Clostridium pefringens, Klebsiella spp., Morganella spp., Bacteroidesspp., Staphilococcus aureus, Pseudomonas [12].
Клинические варианты проявления роста микро-мицетов Candida spp. в кишечнике могут быть представлены следующим образом.
Кандидоносительство. Характеризуется транзитор-ностью, охватывает 60—80 % общей популяции.
Дисбактериоз кишечника с избыточным ростом Candida spp. Избыточное прогрессирование роста микро-мицетов в просвете кишечника на фоне дефицита нормобиоты. Факторы риска: терапия антибиотиками, острые кишечные инфекции, ферментные энте-ропатии.
Кандидозный колит. Трансформация гриба в псевдомицелий и инвазия тканей кишечника на фоне цитопенического синдрома с развитием воспалительных изменений кишечной стенки разной степени тяжести. Факторы риска: СПИД, ВИЧ-инфекция, высокодозная полихимиотерапия, генетически де-терминированые иммунодефициты, инсулинозави-симый сахарный диабет, гемодиализ, трансплантация органов, неспецифический язвенный колит, коло-ректальный рак.
Определенная роль кандидозного дисбиоза в патологии детского возраста подтверждена исследованиями, проведенными совместно кафедрой педиатрической гастроэнтерологии и нутрициологии Харьковской медицинской академии последипломного образования (проф. О.Ю. Белоусова) и бактериологической лабораторией (проф. Е.М. Савинова) Института вакцин и сывороток им. И. И. Мечникова НАМН Украины. Изучено состояние кишечного биоценоза у 134 больных с хроническим неспецифическим неязвенным колитом (ХННК). Диагноз заболевания устанавливался на основании ректоромано-скопического исследования, выявившего у всех детей явления катарального или катарально-фолликулярно-го проктосигмоидита. У значительной части больных (86 %) диагноз ХННК подтверждался также результатами морфологического исследования — кафедра патологической анатомии ХМАПО (проф. Садчиков).
Исследования микробного пейзажа кишечника показали, что у всех 134 детей с ХННК имеют место те или иные нарушения кишечного биоценоза, которые носили преимущественно однонаправленный характер. Изменения кишечной микрофлоры при ХННК у детей представлены в табл. 1.
При анализе полученных данных прежде всего обращают на себя внимание количественные нарушения, характеризующиеся умеренным снижением количества бифидо- и лактобактерий. Несмотря на относительно незначительное уменьшение облигат-ной микрофлоры, значение этого показателя нельзя недооценивать, т.к. снижение ферментативной активности бифидо- и лактобактерий, а также сдвиг рН кишечника в щелочную сторону обусловливают торможение процессов утилизации организмом ребенка биологически активных веществ, усиление бродильных и гнилостных процессов. Нарушение колонизационной резистентности вызывает адгезию и колони-
6(41) • 2012
Клтт’чт лекцН
Таблица 1. Характер изменений кишечной микрофлоры при ХННК у детей
Количественные изменения: %
— снижение бифидобактерий < 108 91,1
— снижение лактобактерий < 107 73
Качественные изменения:
— кишечная палочка со сниженной ферментативной активностью > 107 20,9
Атипичные формы кишечной палочки:
— лактозонегативная 35,8
— гемолизирующая 8,9
Грибы рода Candida spp. 18 ± 4
Из них грибы рода Candida albicans в концентрации > 104-107 КОЕ/г фекалий 90,60 ± 3,17
Грибы рода Candida cruzei в концентрации > 104-105 9,40 ± 3,17
Золотистый и гемолизирующий стафилококк 8,2
Протей 11,9
зацию на слизистой оболочке кишечника патогенных и условно-патогенных бактерий и обусловливает поступление токсинов в кровь.
Кроме количественных, выявляются нарушения качественного состава микрофлоры. Прежде всего это касается изменения качественных свойств кишечной палочки: появление форм со сниженной ферментативной активностью и атипичных форм — лактозоне-гативной, гемолизирующей. Если принять во внимание, что штаммы Exoli содержат достаточно широкий набор факторов патогенности — эндо-, экзо- и цито-токсинов, факторы адгезии и тому подобные, то недооценивать ее роль в развитии патологического процесса невозможно [2, 3].
Качественные изменения микрофлоры при ХННК у детей заключались также в появлении условно-патогенной микрофлоры (золотистый и гемолизирующий стафилококк, грибы рода Candida, протей), что свидетельствует об ослаблении защитных возможностей индигенной анаэробной микрофлоры. При этом не может не обращать на себя внимание значительное содержание грибов рода Candida в высокой концентрации.
Таким образом, выявленные изменения биоценоза кишечника свидетельствуют о значительных дисбио-тических сдвигах у всех больных ХННК, причем нарушения носят не столько количественный, сколько качественный характер. Количественные изменения состоят в незначительном снижении индигенной микрофлоры, качественные — в снижении ее защитных свойств, росте кишечной палочки с измененными свойствами и условно-патогенной микрофлоры (прежде всего грибов рода Candida). Полученные данные дают основание полагать, что дисбиотические нарушения являются одним из важнейших звеньев формирования патологического процесса при ХННК у детей наряду с нарушениями нервной регуляции пищева-
рения и иммунологическими расстройствами, причем в ряде случаев именно дисбиоз кишечника может послужить пусковым механизмом патологического процесса, который можно представить следующим образом: дисбиоз ^ нарушение слизеобразования ^ изменение градиента пролиферации и дифференциации клеток ^ изменение местного иммунитета ^ развитие транзиторного иммунодефицита ^ развитие воспалительного процесса, факторами риска которого являются: длительное течение заболевания, обильный рост условно-патогенных бактерий на фоне дефицита физиологической флоры, снижение местной защиты СО кишечника, угнетение системы местного иммунитета с активацией процесса перекисного окисления липидов. Несмотря на то, что в наших наблюдениях наличие грибов рода Candida не свидетельствует об их безусловной роли в развитии воспалительного процесса (ХННК) в кишечнике, тем не менее и отрицать эту роль не представляется возможным. По-видимому, в развитии воспаления принимает участие смешанная (бактериальная и грибковая) флора, но наличие кан-дидозного дисбиоза при ХННК тем не менее можно считать доказанным.
Вышеизложенное не только пополняет представления о механизмах формирования ХННК у детей, но и определяет необходимость комплексной терапии дис-биоза с учетом его особенностей в каждом конкретном случае заболевания. При диагностике неинвазивного кишечного кандидоза к биопсионному материалу для микологического исследования не прибегают, в качестве стандарта диагностики используют следующие критерии: рост свыше 1000 КОЕ/г Candida spp. при посеве кишечного содержимого, взятого в стерильных условиях, в сочетании с явлениями кишечной диспепсии и положительной клинико-лабораторной динамикой при лечении антимикотическими препаратами [5]. К сожалению, правильный забор кишечного содержимого для культурального исследования технически сложен; широко распространенная в нашей стране методика посева кала на дисбактериоз не может служить опорой в оценке реального состава микрофлоры кишечника [13].
В диагностике любой формы кандидоза органов пищеварения важно учитывать наличие у пациента предрасполагающих факторов риска. «Случайное» выявление кандидоза должно послужить стимулом к поиску такого фонового фактора. Важно помнить, что кандидоз может выступать в качестве ранней манифестации общих заболеваний, сопровождающихся развитием иммунодефицита [13]. В большинстве случаев диагнозу «дисбиоз кишечника» должен предшествовать диагноз основного «фонового» заболевания.
Неинвазивную форму кандидоза следует дифференцировать с широким спектром энтеритов и колитов другой этиологии. Косвенным свидетельством в пользу наличия кандидоза кишечника могут выступать внекишечные системные проявления кандидоза.
Обнаружение грибов рода Candida в большом количестве при бактериологическом анализе испражнений в сочетании с симптомом кишечной диспепсии,
КлЫчН лекцН
6(41) • 2012
особенно при безуспешности антибактериальной терапии, может служить показанием для назначения пациенту антимикотических средств в сочетаниии с про- и пребиотиками, способствующими восстановлению естественной антимикробной резистентности слизистой оболочки кишечника с целью предотвращения рецидивов дисбиоза [7, 12].
Во время лечения больным рекомендован пищевой рацион с ограничением простых углеводов (сахара, сладких фруктов и ягод, кондитерских изделий, меда, молока, яблок, винограда, белокочанной капусты, бобовых, сладких напитков). По показаниям допускается применение ферментных препаратов, энтеросорбентов, спазмолитиков, энтеросептиков. Назначаются антимикотические препараты, неадсор-бирующиеся из просвета кишечника [5].
Лечение кандидозного дисбиоза кишечника не требует назначения резорбируемых имидоазоловых антимикотиков (флуконазол). Чаще всего для селективной деконтаминации кишечника от микромице-тов рода Candida назначают нистатин и натамицин (пимафуцин) [5]. В отличие от имидазоловых антимикотиков, нистатин и натамицин (пимафуцин) практически не резорбируются в кишечнике, что обусловливает стабильно высокую их концентрацию именно в просвете кишечника. Самым частым нежелательным эффектом при назначении этих средств является раздражение слизистых оболочек и обусловленные этим тошнота и диарея. Необходимо отметить, что у пима-фуцина эти явления выражены в меньшей степени, чем у нистатина. В отличие от нистатина натамицин (пимафуцин) разрешен для применения у беременных, кормящих, новорожденных, назначают препарат в таблетках взрослым по 100 мг четыре раза в день, а детям по 100 мг 2 раза в день. Курсы лечения этим средством длительностью 5—10 дней обычно приводят к элиминации дрожжеподобных грибов из кишечника, однако при сохранении факторов, снижающих эффективность местных антифунгальных барьеров, возможна реинфекция. Поэтому на фоне лечения кандидозного дисбиоза и после его окончания широко используются пре- и пробиотики [19].
Следует помнить, что своевременное выявление и эффективная терапия кандидозного дисбиоза позволит предупредить развитие более тяжелой формы дисбиозного колита, лечение которого потребует значительно большего времени и использования более широкого спектра препаратов.
Список литературы
1. Баранов А.А. Научные и организационные приоритеты в детской гастроэнтерологии //Педиатрия. — 2002. — № 3. — С. 12-18.
2. Белоусова О.Ю. Хронический неспецифический неязвенный колит у детей. — X.: Оберк, 2009. — 184с.
3. Белоусова О.Ю. Дисбиоз кишечника как фактор риска развития хронических заболеваний кишечника у детей // Здоровье ребенка. — 2011. — № 1. — С. 73-75.
4. Бережной В.В. Микроэкологические нарушения у детей и современные возможности повышения эффективности их коррекции /Бережной В.В, Крамарев С.А., Мартынюк В.Ю. // Здоровье женщины. — 2002. — № 4. — С. 79-91.
5. ЗлаткинаА..Р, ИсаковВА., ИваниковИ.О. Кандидозкишеч-ника как новая проблема гастроэнтерологии // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. — 2001. — № 6. — С. 33-38.
6. Каширская Н.Ю. Значение пробиотиков и пребиотиков в регуляции кишечной микрофлоры // Рус. мед. журн. — 2000. — № 13— 14. — С. 3-612.
7. Сергеев А..Ю, Сергеев Ю.В. Кандидоз. Природа инфекции, механизмы агрессии и защиты, лабораторная диагностика, клиника и лечение. — М., 2001. — 472с.
8. Урсова Н.И. Проблемы функциональных расстройств би-лиарного тракта у детей и их коррекция // Русский медицинский журнал. — 2003. — № 3. — С. 138-142.
9. Хмельницкий О.К. О кандидозе слизистых оболочек//Архив патологии. — 2000. — Т. 62, № 6. — С. 3-10.
10. Циммерман Я.С. Гастроэнтерология. — М.: ГЭОТАР-Ме-диа, 2012. — С. 220-266.
11. Шевяков М.А., Авалуева Е.Б., Барышникова Н.В. Кишечный кандидоз //Здоровье Украины. — 2009. — 6(1). — С. 48-49.
12. Шевяков М.А. Диагностика и лечение кандидоза кишечника //Терапевтический архив. — 2003. — Т. 75, № 11. — С. 77-79.
13. Шульпекова Ю.О. Кандидоз кишечника// Русский медицинский журнал. — 2002. — Т. 4, № 1. — С. 25-28.
14. Forbes D., Ee L., Camer-Pesci P., Ward P.B. Faecal Candida and diarrhea //Arch. Dis. Child. — 2001. — Vol. 84. —P. 328-331.
15. Gores G.J. Mechanisms ofcellinjury and death sn cholestasis and hepatoprotectson by ursodeocsy choli acid // J. Hepatology. — 2000. — Vol. 32. — P. 11-13.
16. Danna P.L., Urban C, Bellin E, Rahal J.J. Role of Candida in pathogenesis of antibiotic-associated diarrhoea in elderly patients // Lancet. — 1991. — Vol. 337. — P. 511-514.
17. Hyams J.S. Inflammatory bowel disease/Hyams J.S. // Pediatr. Rew. — 2000. — № 21(9). — P. 291-295.
18. Levis L.G Gastroentestinal infection in children / Levis L.J. // Pediatr. — 1994. — V. 5. — P. 573-579.
19. Pancheva-Dimitrova R.Z., Georgieva-Shakola M., Tzaneva V. Probiotics and antibiotic-associated diarrhea in children //Abstracts of12 UEGW, Gut. — 2004. — 53 (Suppl. VI). — A137.
20. Segal E. Candida, still number one — what do we know and where are we goingfrom there// Mikol. Lek. — 2004. — 11(2). — Р. 133138.
21. Ott S.J. Reduction in diversity of the colonic mucosa associated bacterial microflora in patients with active inflammatory bowel diseas / S.J. Ott, M. Vusfeld, D.F. Wenderoth et al.//Gut. — 2004. — №53. — P. 685-693.
Получено 21.05.12 □
Белоусова О.Ю.
Харювська мелична академя пюлядипломно! освпи КАНДИДОЗНИЙ ДИСБЮЗ КИШЕЧНИКА У Д|ТЕЙ
Резюме.рвбёши
Мик. Кандидозы. (CANDIDOSIS).+ | Портал радиологов
КАНДИДОЗЫ (CANDIDOSIS)
Типичная для кандидозов обложенность языка белым налетом
Кандидозы (синонимы: кандидамикозы, кандидиаз) — болезни, вызываемые дрожжеподобными грибами рода Candida. Помимо относительно благоприятно протекающих кандидозов слизистых оболочек и кожи, возможны тяжелые висцеральные формы микоза, чаще с преимущественным поражением желудочно-кишечного тракта и органов дыхания. Эти формы особенно часто развиваются у ВИЧ-инфицированных лиц.
Этиология. Возбудителями чаще являются следующие виды: Candida albicans, С. tropicalis, С. parapsilosis, С. guillierinondii, С. krusei. Они относятся к дрожжеподобным грибам и отличаются от истинных дрожжей способностью образовывать мицелий и отсутствием полового способа воспроизведения, т. е. относятся к неспорообразующим дрожжам. Могут расти на агаровых питательных средах. Антигены возбудителей обладают аллергизирующими и антигенными свойствами, но титры антител высокими бывают лишь при висцеральных кандидозах. Грибы рода кандида нередко выявляются как сапрофиты в микрофлоре полости рта, кишечника, вагины.
Эпидемиология. Дрожжеподобные грибы рода Candida обитают на коже и слизистых оболочках респираторного и желудочно-кишечного тракта, входят в состав нормальной микрофлоры. Они широко распространены также в природе (на фруктах, овощах, в молочных продуктах и т. д.). Заболевание возникает обычно в результате эндогенной инфекции. Чаще всего это бывает обусловлено Candida albicans.
Патогенез. Кандидозы развиваются вследствие внедрения в ткани грибов, являющихся нормальными обитателями слизистых оболочек. Переходу Candida в паразитическое состояние может способствовать дисбактериоз, возникающий при назначении антибиотиков широкого спектра действия, снижение защитных сил организма при длительном назначении некоторых препаратов (кортикостероидов, иммунодепрессантов), наличие тяжелых заболеваний (рак, болезни крови, диабет и др.). Особенно часто кандидоз развивается у ВИЧ-инфицированных лиц. Аспергиллез и кандидоз являются наиболее частыми оппортунистическими инфекциями микозной природы у больных СПИДом. Проникновению кандид в ткани может способствовать повреждение кожи и слизистых оболочек, например, повреждение желудочно-кишечного тракта при перфорациях, травмах, хирургических операциях, введении катетеров в сосуды, при перитонеальном диализе, внутривенном введении лекарств и т. д. При висцеральных формах кандидоза отмечаются очаги некроза, нейтрофильной воспалительной инфильтрации. При висцеральных формах наиболее часто поражаются почки, мозг, сердце, печень, селезенка.
Симптомы и течение. Кандидоз слизистой оболочки полости рта (молочница) проявляется в виде белых налетов (сплошных или в виде изолированных участков) на слизистой оболочке щек, задней стенки глотки, на языке. Пораженные места обычно безболезненны, но при уплотнении налета, образовании трещин может быть нерезко выраженная болезненность в полости рта. При кожном кандидозе отмечаются краснота, мацерация кожи, могут быть баланиты, зуд в области заднего прохода, паронихии. При локализации на коже промежности или на мошонке могут наблюдаться отдельные пустулезные элементы. При хроническом кожно-слизистом кандидозе могут развиваться поражения в виде гиперкератоза, поражения ногтей, гнездного облысения в сочетании с длительными изменениями слизистых оболочек. Более глубокие поражения слизистых оболочек (что нередко отмечается при диссеминированых формах) проявляются в обширных изменениях, при которых налеты распространяются на слизистые оболочки пищевода, желудка, трахеи, бронхов. Это сопровождается нарушением глотания и загрудинными болями. Может развиться массивное кандидозное поражение слизистой оболочки после катетеризации мочевого пузыря.
Гематогенно диссеминированные формы кандидоза (кандидозный сепсис) характеризуются тяжелым течением, высокой лихорадкой и выраженными симптомами общей интоксикации. Лихорадка неправильного типа с повторными ознобами, перемежающимися с обильным потоотделением. Сопровождается поражением различных органов (легких, желудочно-кишечного тракта, мозга, почек и др.). Характерно наличие нескольких очагов поражений. Часто развиваются поражения сетчатки (один или несколько очагов), процесс распространяется на стекловидное тело. Отмечается боль в глазу, нарушение зрения. Гематогенное поражение легких характеризуется развитием инфильтратов. Больных беспокоит сильный кашель, вначале сухой, затем с небольшим количеством вязкой слизисто-гнойной мокроты, иногда с прожилками крови. При рентгенологическом исследовании выявляются инфильтраты, чаще в нижних долях, склонные к слиянию; нередко наблюдается распад с образованием полостей. В процесс может быть вовлечена плевра; прикорневые лимфатические узлы увеличены и уплотнены. При вторичном кандидозе легких (на фоне пневмонии, туберкулеза) необходимо учитывать изменение клинической симптоматики (ухудшение общего состояния, появление гектической лихорадки и др.). При кандидозе кишечника отмечаются боли в животе, вздутие кишечника, понос, испражнения часто содержат примесь крови, могут быть боль в области прямой кишки и зуд в области заднего прохода. Кандидоз органов пищеварения обычно сопровождается сплошным поражением слизистых оболочек полости рта, пищевода, желудка. Кандиды могут обусловить развитие гнойного менингита и абсцесса мозга. При гематогенной диссеминации может развиться абсцесс почек с последующей азотемией. Поражение опорно-двигательного аппарата проявляется в виде артритов, остеомиелитов, миозитов.
Кандидоз у ВИЧ-инфицированных. Кандидоз является одним из самых частых оппортунистических микозов при ВИЧ-инфекции, поэтому появление и прогрессирование симптомов кандидоза может указывать на необходимость обследования больного на ВИЧ-инфекцию. Начинается кандидоз с поражения слизистых оболочек полости рта, задней стенки глотки, пищевода, у ВИЧ-инфицированных женщин очень часто развивается хронический вагинальный кандидоз. В дальнейшем развивается гематогенно диссеминированный кандидоз, протекающий очень тяжело, который может привести к гибели больного.
Диагноз и дифференциальный диагноз. Выделение культуры из мокроты, слизи зева, испражнений, мазков и соскобов с пораженных слизистых оболочек, кожи, ногтей не может служить доказательством диссеминированного (висцерального) кандидоза. Диагностическое значение имеет выделение культуры из крови, спинномозговой жидкости, внутрисуставной жидкости или в биопсированных тканях. При поражении кожи и слизистых оболочек диагностическое значение имеет обнаружение (при микроскопии) большого количества кандид в мокроте, испражнениях, в слизи зева, а также выявление достаточно высоких титров антител в РСК и реакции агглютинации со специфическим антигеном. Положительными считаются высокие титры (1:160-1:1600) или нарастание титров антител в ходе болезни. У ВИЧ-инфицированных серологические реакции остаются отрицательными.
Кандидоз легких дифференцируют от бактериальных пневмоний, туберкулеза и от других глубоких микозов (актиномикоз, аспергиллез, нокардиоз, гистоплазмоз). Для кандидоза характерно относительно быстрое исчезновение инфильтратов и даже каверн под влиянием антимикозной терапии. Имеет значение и то, что перед развитием висцерального кандидоза отмечается появление и прогрессирование кандидозного поражения слизистых оболочек.
Лечение. Устранение факторов, способствующих возникновению кандидоза. Витамины группы В и аскорбиновая кислота. При поражении кожи используют мази с противомикозными препаратами, лечение проводят открытым способом. При поражениях слизистых оболочек (оральный, вагинальный кандидоз) используют местно суспензию, содержащую нистатин. При поражении слизистой оболочки пищевода применяют кетоконазол (Ketoconazole) по 200-400 мг в день (эффективность около 50%), если симптомы поражения пищевода не исчезают в течение 5-10 дней, то следует использовать Diflucan(fluconazole). Его назначают внутрь по 100 мг в день в течение двух дней (эффективность около 90%). В этих случаях можно также внутривенное введение амфотерицина В по 0,3 мг/кг. При кандидозном поражении мочевого пузыря в течение 5 дней проводят инстиляции раствора амфотерицина В по50 мкг/мл. При диссеминированном (системном, висцеральном) кандидозе используют амфотерицин В, его назначают внутривенно в 5% растворе в виде капельных вливаний из расчета 250 ЕД/кг массы тела (0,3 мг/кг), курс лечения может занять несколько недель. Эффективным препаратом для лечения системного кандидоза является Diflucan, который назначают внутрь по 200 мг в день в течение двух дней. Побочные реакции отмечаются относительно редко(2-4%) в виде тошноты, диареи, головной боли.
Прогноз. При кандидозе слизистых оболочек и кожи прогноз благоприятный, при гематогенно диссеминированном — серьезный.
KDL. Кандидоз. Анализы и цены
Алергология. ImmunoCAP. Индивидуальные аллергены, IgE
Аллергокомпоненты ImmunoCAP
Аллергокомпоненты деревьев
Аллергокомпоненты животных и птиц
Аллергокомпоненты плесени
Аллергокомпоненты трав
Пищевые аллергокомпоненты
Аллергология. ImmunoCAP. Комплексные исследования IgE (результат по каждому аллергену)
Аллергология. ImmunoCAP. Панели аллергенов IgE, скрининг (результат СУММАРНЫЙ)
Аллергология. ImmunoCAP. Фадиатоп
Аллергология. Immulite. Индивидуальные аллергены
Аллергены гельминтов, IgE
Аллергены грибов (кандида и плесневых), IgE
Аллергены деревьев, IgE
Аллергены животных и птиц, IgE
Аллергены клещей домашней пыли, IgE
Аллергены лекарств и химических веществ, IgE
Аллергены насекомых, IgE
Аллергены пыли, IgE
Аллергены ткани, IgE
Аллергены трав, IgE
Бактериальные аллегены (стафилококк), IgE
Пищевые аллергены, IgE
Пищевые аллергены, IgG
Аллергология. Immulite. Комплексы аллергенов, IgE (результат по каждому аллргену)
Аллергология. Immulite. Панели аллергенов, скрининг (результат СУММАРНЫЙ)
Аллергены деревьев, IgE (панель)
Аллергены животных и птиц, IgE (панель)
Аллергены трав, IgE (панель)
Ингаляционные аллергены, IgE (панель)
Пищевые аллергены, IgE (панель)
Аллергология. Immulite. Панели пищевых аллергенов IgG (результат СУММАРНЫЙ)
Аллергология. ImmunoCAP. Индивидуальные аллергены, IgE
Аллергены деревьев, IgE
Аллергены животных и птиц, IgE
Аллергены пыли, IgE
Аллергены трав, IgE
Пищевые аллергены, IgE
Аллергология. RIDA. Комплексы аллергенов, IgE
Аллергология. RIDA. Комплексы аллергенов, IgE (результат по каждому аллргену)
Аллергология. Местные анестетики, IgE
Биохимические исследования крови
Диагностика анемий
Липидный обмен
Обмен белков
Обмен пигментов
Обмен углеводов
Специфические белки
Ферменты
Электролиты и микроэлементы
Биохимические исследования мочи
Разовая порция мочи
Суточная порция мочи
Витамины, аминокислоты, жирные кислоты
Гематология
Гемостаз (коагулограмма)
Генетические исследования
HLA-типирование
Исследование генетических полиморфизмов методом пиросеквенирования
Исследование генетических полиморфизмов методом ПЦР
Молекулярно-генетический анализ мужского бесплодия
Гистологические исследования
Гистологические исследования лаборатории UNIM
Гормоны биологических жидкостей
Гормоны гипофиза и гипофизарно-адреналовой системы
Гормоны крови
Гормоны гипофиза и гипофизарно-адреналовой системы
Маркеры остеопороза
Пренатальная диагностика
Ренин-альдостероновая система
Тесты репродукции
Функция органов пищеварения
Функция щитовидной железы
Гормоны мочи
Диагностика методом ПЦР
COVID-19
Андрофлор, иследование биоценоза (муж)
Вирус герпеса VI типа
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус простого герпеса I, II типа
Вирус Эпштейна-Барр
Вирусы группы герпеса
Возбудитель туберкулеза
ВПЧ (вирус папилломы человека)
Грибы рода кандида
Листерии
Парвовирус
Респираторные инфекции
Стрептококки (вкл. S.agalactie)
Токсоплазма
Урогенитальные инфекции, ИППП
Урогенитальные инфекции, комплексные исследования
Урогенитальные инфекции, условные патогены
Фемофлор, исследование биоценоза (жен)
Флороценоз, иследование биоценоза (жен)
Цитомегаловирус
Диагностика методом ПЦР, кал
Кишечные инфекции
Диагностика методом ПЦР, клещ
Клещевые инфекции
Диагностика методом ПЦР, кровь.
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус простого герпеса I, II типа
Вирус Эпштейна-Барр
ВИЧ
Возбудитель туберкулеза
Гепатит D
Гепатит G
Гепатит А
Гепатит В
Гепатит С
Листерии
Парвовирус
Токсоплазма
Цитомегаловирус
Жидкостная цитология
Изосерология
Иммуногистохимические исследования
Иммунологические исследования
Иммунограмма (клеточный иммунитет)
Интерфероновый статус, базовое исследование
Интерфероновый статус, чувствительность к препаратам
Оценка гуморального иммунитета
Специальные иммунологические исследования
Исследование абортуса
Исследование мочевого камня
Исследование парапротеинов. Скрининг и иммунофиксация
Исследования слюны
Исследования слюны
Комплексные исследования
Лекарственный мониторинг
Маркеры аутоиммунных заболеваний
Антифосфолипидный синдром (АФС)
Аутоиммунные заболевания легких и сердца
Аутоиммунные неврологические заболевания
Аутоиммунные поражения ЖКТ и целиакия
Аутоиммунные поражения печени
Аутоиммунные поражения почек и васкулиты
Аутоиммунные эндокринопатии и бесплодие
Диагностика артритов
Пузырные дерматозы
Системные ревматические заболевания
Эли-тесты
Микробиологические исследования (посевы)
Посев крови на стерильность
Посев на гемофильную палочку
Посев на грибы (Candida)
Посев на грибы (возбудители микозов кожи и ногтей)
Посев на дифтерию
Посев на микоплазмы и уреаплазмы
Посев на пиогенный стрептококк
Посев на стафилококк
Посевы кала
Посевы мочи
Посевы на микрофлору (конъюнктива)
Посевы на микрофлору (отделяемое)
Посевы на микрофлору (урогенитальный тракт женщины)
Посевы на микрофлору (урогенитальный тракт мужчины)
Посевы на микрофлору ЛОР-органы)
Ускоренные посевы с расширенной антибиотикограммой
Неинвазивная диагностика болезней печени
Программы неинвазивной диагностики болезней печени
Неинвазивный пренатальный ДНК-тест (НИПТ)
Неинвазивный пренатальный тест (пол/резус плода)
Общеклинические исследования
Исследование назального секрета
Исследование секрета простаты
Исследования кала
Исследования мочи
Исследования эякулята
Микроскопическое исследование биологических жидкостей
Микроскопия на наличие патогенных грибов и паразитов
Микроскопия отделяемого урогенитального тракта
Онкогематология
Иммунофенотипирование при лимфопролиферативных заболеваниях
Миелограмма
Молекулярная диагностика миелопролиферативных заболеваний
Цитохимические исследования клеток крови и костного мозга
Онкогенетика
Онкомаркеры
Пищевая непереносимость, IgG4
Полногеномные исследования и панели наследственных заболеваний
Пренатальный скрининг
Серологические маркеры инфекций
Аденовирус
Бруцеллез
Вирус HTLV
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус Коксаки
Вирус кори
Вирус краснухи
Вирус эпидемического паротита
Вирус Эпштейна-Барр
Вирусы простого герпеса I и II типа
ВИЧ
Гепатит D
Гепатит А
Гепатит В
Гепатит Е
Гепатит С
Грибковые инфекции
Дифтерия
Кишечные инфекции
Клещевые инфекции
Коклюш и паракоклюш
Коронавирус
Менингококк
Паразитарные инвазии
Парвовирус
Респираторные инфекции
Сифилис
Столбняк
Токсоплазма
Туберкулез
Урогенитальные инфекции
Хеликобактер
Цитомегаловирус
Специализированные лабораторные исследования.
Дыхательный тест
Микробиоценоз по Осипову
Тяжелые металлы и микроэлементы
Тяжелые металлы и микроэлементы в волосах
Тяжелые металлы и микроэлементы в крови
Тяжелые металлы и микроэлементы в моче
Услуги
Выезд на дом
ЭКГ
Установление родства
Химико-токсикологические исследования
Хромосомный микроматричный анализ
Цитогенетические исследования
Цитологические исследования
Чекап
NORD (Национальная организация по редким заболеваниям)
Поскольку предполагается, что Candida Albicans присутствует у здоровых людей, лечение требуется очень редко. Американская академия аллергии и иммунологии заявила, что концепция аллергии на дрожжи или гиперчувствительности кандидоза является спекулятивной и бездоказательной. Здоровая пища и витамины не являются эффективным лечением.
Если пациент принимает антибиотик широкого спектра действия, полезно прекратить лечение, чтобы восстановить обычную бактериальную флору слизистых оболочек.По возможности также следует прекратить лечение кортикостероидами и иммунодепрессантами. Пациентам, которые особенно предрасположены к инфекциям кандидозом (например, диабетикам), следует особенно стараться избегать приема лекарств, способствующих росту грибка.
Лечение кандидоза кожи или влагалища с помощью местного применения нистатина, клотримазола или миконазола во многих случаях может быть эффективным. Для одновременного лечения воспаления и зуда можно использовать одновременно противогрибковые и кортикостероидные кремы.
Для профилактики и лечения кандидоза полости рта необходима тщательная гигиена полости рта, особенно при использовании зубных протезов. Для лечения острого пульпно-альвеолярного целлюлита (инфекция соединительной ткани, выстилающей корневой канал) может оказаться полезным удаление разложившихся и инородных тел со слизистых поверхностей, полоскание теплой соленой водой или раствором пищевой соды. Лекарства, вводимые через корневой канал, также доказали свою эффективность в некоторых случаях.
Вагинальный кандидоз — лечение выделений из влагалища и зуда при этом типе инфекции заключается в применении определенных противогрибковых препаратов.Правильные гигиенические привычки и контроль диабета, когда это применимо, могут помочь избежать повторных инфекций у женщин, которые особенно предрасположены к этой инфекции.
Чтобы предотвратить распространение инфекции Candida влагалища или полового члена, когда инфицирован один половой партнер, нистатин может быть прописан обоим партнерам.
При кандидозной сыпи от подгузников кожа должна быть сухой, часто меняя подгузники. Следует избегать использования вазелина и талька. В тяжелых случаях нельзя использовать пластиковые штаны и одноразовые пластиковые покрывала для подгузников.Некоторые кремы и мази могут быть прописаны врачом.
Для лечения хронического кожно-слизистого кандидоза полезны амфотерицин B, нистатин, клотримазол, миконизол или 5-фторцитозин. В лечении также используются противогрибковые и стимулирующие иммунную систему вещества (такие как молекула, которая может передавать иммунитет от сенсибилизированного к несенсибилизированному человеку), называемые фактором переноса, тимозином, трансплантацией эпителиальных клеток тимуса и левамизолом. (Для получения дополнительной информации об этих заболеваниях выберите «иммунодефицит» в качестве поискового запроса в базе данных редких заболеваний.)
Новое лекарство для лечения кандидоза, криптококкового менингита и других людей с ослабленной иммунной системой, таких как пациенты со СПИДом, недавно было одобрено FDA. Препарат дифлюкан (флуконазол) оказался эффективным против этих типов инфекций у людей с ослабленной иммунной системой.
Липидный комплекс амфотерицина B (Abelcet) получил статус орфанного препарата для лечения кандидоза. Необходимы дополнительные исследования для определения долгосрочной безопасности и эффективности этого препарата для лечения кандидоза.Для получения дополнительной информации обращайтесь:
The Liposome Company, Inc.
One Research Way
Princeton. N. 08540
Грибковая инфекция толстой кишки
Clin Exp Gastroenterol. 2014; 7: 415–426.
Сурат Праниенарарат
Отделение гастроэнтерологии, Медицинский факультет, Университет принца Сонгкла, Сонгкхла, Таиланд
Отделение гастроэнтерологии, Медицинский факультет, Университет Принца Сонгкла, Сонгкхла, Таиланд
Переписка: Сурат Праненарарат, Отделение гастроэнтерологии, Кафедра медицины, Университет Принца Сонгкла, 15 Kanjanavanich Road, Hat-Yai, Songkhla, Thailand,, Tel +66 80 441 0174, Email moc.Авторские права © 2014 Praneenararat. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения Dove Medical Press Limited при условии правильной атрибуции работы. Эта статья цитируется в других статьях PMC.Abstract
Грибы — патогены, которые обычно поражают пациентов с ослабленным иммунитетом и могут поражать любые органы тела, включая толстую кишку.Однако в литературе содержится ограниченное количество подробностей об инфекциях толстой кишки, вызванных грибками. Эта статья представляет собой подробный обзор доступной информации о грибах, которые могут вызывать инфекции толстой кишки. В нем используется сравнительный стиль, поэтому его выводы могут быть доступны для клинического применения.
Ключевые слова: грибок, колит, толстая кишка, толстая кишка
Введение
Грибы являются патогенами, которые обычно инфицируют пациентов с ослабленным иммунитетом. В настоящее время частота этих патогенов в причинах заболевания постепенно увеличивается в результате более широкого использования иммунодепрессантов, химиотерапии и трансплантации, а также инфекций, вызванных вирусом иммунодефицита человека.Грибковые инфекции могут поражать любой орган, в том числе толстую кишку.1–3 Тем не менее, в литературе доступны лишь ограниченные сведения об инфекции толстой кишки, вызванной грибами.4,5 Эта статья представляет собой интенсивный обзор исследований грибковой инфекции толстой кишки. в кратком сравнительном стиле для удобного клинического применения.
Методы
Автор инициировал обзор с исследования грибков, которые могут вызывать инфекцию толстой кишки, в MEDLINE, в основных учебниках и существующей исследовательской литературе, в которой рассматриваются грибковые инфекции толстой кишки.4–7 В MEDLINE автор использовал ключевые слова из двух групп. Первая группа состояла из названий грибов или инфекций, связанных с грибами, включая «аспергиллез», « Aspergillus », « Blastomyces », «бластомикоз», « Candida », «кандидоз», «хромобластомикоз». , « Cladophialophora », « Coccidioides », «кокцидиоидомикоз», «криптококкоз», « Cryptococcus », «дерматофит», «дерматофитоз», « Epidermophyton », «eumycetoma», «eumycetoma», , «Фузариоз», « Fusarium », « Histoplasma », «гистоплазмоз», « Madurella », « Microsporum », «мукормикоз», « Paracoccidioides », «паракокцидиоидомикоз». , « Penicillium », «феогифомикоз», « Pneumocystis », «пневмоцистоз», «скедоспориоз», « Scedosporium », « Sporothrix », «споротрихоз», « Trichophyton », « Trichophyton » »,« трихоспороноз », « Zygomycetes » и «зигомикоз».Вторая группа ключевых слов состояла из слов, связанных с локализацией заболевания, которое мы рассматривали, включая «колит», «толстая кишка», «толстая кишка», «энтероколит», «толстая кишка», «толстая кишка» и «толстая кишка». . Наконец, было установлено, что инфекции толстой кишки, которые, как сообщалось, были вызваны грибами, были аспергиллезом, кандидозом, криптококкозом, гистоплазмозом, паракокцидиоидомикозом, пенициллиозом, пневмоцистозом, скедоспориозом и зигомикозом. Подробная информация о каждом грибке была дополнительно рассмотрена из статей, найденных в MEDLINE, с использованием ключевых слов, как описано выше, цитат из этих статей и ссылок в основных учебниках.В MEDLINE были включены все типы статей, включая обзоры, серии случаев, истории болезни, редакционные статьи и письма до 30 июня 2014 г. Первоначально было найдено 124 статьи. Были отобраны только статьи, которые были на английском языке или имели аннотацию на английском языке с необходимыми подробностями, которые имели определенный диагноз грибковой инфекции толстой кишки, включая прямую визуализацию типичного грибка или положительную культуру грибка в образцах толстой кишки. Случаи кандидоза, который считается нормальным комменсалом желудочно-кишечного тракта человека, также должны соответствовать одному из следующих критериев в соответствии с принятыми отчетами о случаях и пересмотренной совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Национальным институтом. критериев группы исследования аллергии и инфекционных микозов: проникновение в глубокие ткани толстой кишки или положительный результат на Candida spp.в поверхностной слизистой оболочке с положительным посевом крови или положительным Candida spp. в поверхностной слизистой оболочке с очевидностью ответа на лечение8–14 Candida spp. только на поверхностной слизистой оболочке без положительного посева крови или свидетельств ответа на лечение были исключены. Распространение было определено как поражение двух или более несмежных органов15–19
В настоящее время уже рассмотрены гистоплазмоз, 20,21 кандидоз 13 и зигомикоз22–25. В случаях других грибковых инфекций, включая криптококкоз, пенициллиоз 26–35, аспергиллез 36–38, 9,39–44 и паракокцидиоидомикоз 45–50, автор обобщил отчеты о случаях, как показано в -.Был опубликован только один отчет о каждом случае пневмоцистоза51 и скедоспориоза.52
Таблица 1
Сводные данные о зарегистрированных случаях криптококкоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распространение в толстой кишке | Эндоскопическое исследование | Лечение и исход | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Zelman et al. | ХМЛ, химиотерапия | Не упоминается | Не упоминается | Да | Не упоминается | Язва | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Унат и др., 27 1960 | 16 / мужчина | Турция | Турция | Диарея, боли в животе, LGIB | 8 лет | Нет | Спуститься ободочной кишки | Масса | Хирургия и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hutto et al, 28 1988 | 29 / женщина | США | Синдром Джобса | Абсцесс прямой кишки | 1 год | 1 год | восходящая ободочная кишка | Стриктура восходящей ободочной кишки и периректальный абсцесс | Операция и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van Calck et al, 29 1988 | 47 / мужской | Бельгия | СПИД | Hematochezia | Hematochezia, лихорадка | , лихорадка не упоминаетсяДа | Периректум | Периректальный абсцесс | Хирургия, амфотерицин B и флуцитозин → улучшенное состояние | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Daly et al, 30 1990 | 63 / мужской | USA | Хортностерэктомия, корнеэктомия , недомогание | 7 дней | Есть | Поперечная ободочная кишка | Масса | Амфот эрицин B и флуцитозин → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bonacini et al, 31 1990 | 31 / мужчина | США | AIDS | Hemiplegia, эпилепсия | Не упоминается | Да | Не упоминается | B и флуцитозин → умер||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 38 / мужчина | США | СПИД | Эпигастральная боль, одинофагия | 3 месяца | Да | Противогрибковая терапия | 3 → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 24 / мужчина | США | Болезнь Ходжкина | Не упоминается | Не упоминается | Да | Не упоминается | Не упоминается | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 31 / женщина | США | СПИД | Не упоминается d | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 51 / мужчина | США | Кортикостероиды | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умерло | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Мелато и Горджи, 33 1998 | 84 / женщина | Италия | Нет | Ректальное кровотечение Нет | Острое | Острое толстая кишка | Полип | Полипэктомия → улучшенная | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Law et al, 34 2007 | 40 / мужчина | Канада | AIDS | Боль в животе, диарея, дисфагия, лихорадка | 6 недель Слева | 6 недель толстая кишка | Множественные эритематозные, выпуклые, пятнистые поражения | Амфотерицин B и флуцитозин → улучшенный | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сонг и др., 35 2008 | 27 / женщина | Корея | Нет | Мелена | Не упоминается | Нет | Проксимальный отдел восходящей ободочной кишки | Масса | Амфотерицин В и флуконазин B → | 9018 с улучшенным эффектом Таблица 4
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность | Продолжительность | Распространение | Распределение по толстой кишке | Эндоскопическое исследование | Лечение и результат | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Penna, 45 1979 | 8 / женщина | Бразилия | Нет | Диарея, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность | 4 года | Нет | Вся толстая кишка | Стриктура, язва | Ко-тримоксазол → улучшение | |||||||||||||||||||||||
| Chojniak et al, 46 2000 | 57 / не упоминается | Бразилия | Нет | Боль в животе, диарея, потеря веса 3 | 2 года | Слепая кишка | Масса | Кетоконазол → не упоминается | ||||||||||||||||||||||||
| Коста Виейра и др., 47 2001 | 60 / мужской | Бразилия | Нет | Лихорадка, перианальные узелки, дисфония, кашель13 лет | Да | Поперечная и нисходящая толстая кишка | Язва | Сульфадиазин → улучшение | ||||||||||||||||||||||||
| Браво и др., 48 2010 | 39 / женщина | Перу | Нет | диарея | 2 месяца | Да | Вся толстая кишка | Язва | Амфотерицин B → умер | |||||||||||||||||||||||
| Леон и др., 49 2 010 | 34 / мужчина | Перу | Нет | Диарея, язвы во рту, одинофагия, похудание, кашель | 18 месяцев | Да | Вся толстая кишка | Язва | Амфтозол | Амфтозол | Леон и др., 49 2010 | 40 / женщина | Перу | Нет | Диарея, похудание, гепатомегалия | 1 год | Да | Не упоминается | Не упоминается | Amphoteric | Benard et al, 50 2013 | 56 / женщина | Бразилия | Нет | Нет (колоноскопия для проверки) | Неизвестно | Нет | Поперечная ободочная кишка | Полип | Итраконазол | 58 / женщина | Бразилия | Нет | Диарея, потеря веса, лихорадка | 6 месяцев 9 0134 | Нет | Вся толстая кишка | Язва | Итраконазол → улучшенный |
Эпидемиология
Candida spp.являются нормальными комменсалами желудочно-кишечного тракта, 53,54, тогда как Aspergillus spp. и Pneumocystis spp. распространены повсеместно55–58 и являются причиной грибковых инфекций во всем мире. Cryptococcus spp. и Scedosporium spp. являются эндемическими микозами, которые также имеют распространение по всему миру. Cryptococcus spp. были изолированы из помета голубей 59, а Scedosporium spp. были обнаружены в приливных отмелях, болотах, прудах, навозе и почве.60,61 Aspergillus spp. и Cryptococcus spp. также могут быть обнаружены как компонент микобиоты толстой кишки человека.62
Zygomycetes можно разделить на два отряда: Mucorales и Entomophthorales. Mucorales — эндемичные грибы, встречающиеся во всем мире в органических субстратах, включая хлеб, фрукты, растительные вещества, почву, компост и экскременты животных.63 Histoplasma spp., Entomophthorales, Paracoccidioides spp. И Penicillium spp. эндемичные микозы, выделенные из почвы в ряде регионов мира.63–71 Histoplasma spp. обнаружены в почве, обогащенной пометом летучих мышей, кур и дроздов.64,65 Entomophthorales можно разделить на Conidiobolus spp. и Basidiobolus spp. и находятся в почве некоторых тропических регионов, особенно Африки, Южной Америки, Центральной Америки и Азии63. Paracoccidioides spp. ограничены почвой в странах Центральной и Южной Америки между 23 ° северной широты (юг Мексики) и 34,5 ° северной широты (Аргентина и Уругвай).Эти районы обладают уникальными экологическими особенностями, так как представляют собой тропические и субтропические леса с умеренными температурами и высокой влажностью.66,67 Penicillium spp. также изолированы от почвы в определенных областях, включая Юго-Восточную Азию, южный Китай (Гуанси), Гонконг и Индию.68–71 Эпидемиологические данные суммированы в.
Таблица 5
Эпидемиология грибков, которые могут вызывать инфекцию толстой кишки
| Грибки | Эпидемиология |
|---|---|
| Aspergillus spp., 55,56 Candida spp., 53,54 Криптококк видов, 59 Histoplasma spp., 64,65 Mucorales, 63 Pneumocystis виды, 57,58 Scedosporium spp.60,61 | Во всем мире |
| Entomophthorales63 | Тропические зоны в Африке, Южной Америке, Центральной Америке и Азии |
| Paracoccidioides spp.66,67 | странах Южной и Центральной Америки , особенно в Бразилии, Колумбии, Венесуэле и Аргентине|
| Penicillium spp.68–71 | Юго-Восточная Азия, южный Китай (Гуанси), Гонконг и Индия |
Распространенность поражения толстой кишки
Степень поражения толстой кишки грибковыми инфекциями варьируется в зависимости от типа грибка, как подробно описано в. Паракокцидиоидомикоз и гистоплазмоз являются наиболее распространенными инфекциями толстой кишки, вызываемыми грибами, с распространенностью 29% 72 и 28% 20 соответственно. Напротив, пенициллиоз, зигомикоз, пневмоцистоз и скедоспориоз редко инфильтрируют толстую кишку, при этом пенициллиоз и зигомикоз встречаются в 1.9% 68 и 0,85% инфекций толстой кишки 25 соответственно. И пневмоцистоз, и скедоспориоз известны только из одного сообщения о клиническом случае.51,52 За исключением ротоглоточного кандидоза, толстая кишка является третьим наиболее частым желудочно-кишечным органом, вовлеченным в кандидоз после пищевода и желудка. Ободочная кишка участвует в 20% случаев кандидоза желудочно-кишечного тракта.73 Криптококкоз толстой кишки является наиболее частым желудочно-кишечным проявлением диссеминированного или легочного криптококкоза с распространенностью около 17%.32
Таблица 6
Распространенность поражения толстой кишки при каждой грибковой инфекции
| Грибковые инфекции | Распространенность поражения толстой кишки | Комментарии | ||
|---|---|---|---|---|
| Паракокцидиоидомикоз3 | ||||
| Гистоплазмоз20 | 28% | |||
| Кандидоз73 | 20% желудочно-кишечного кандидоза (исключая орофарингеальный кандидоз) или легочный криптококкоз | |||
| Аспергиллез74 | 9.2% | |||
| Пенициллиоз68 | 1,9% | Всего четыре случая | ||
| Зигомикоз25 | 0,85% | |||
| 902 Нет данных | Только один случай |
Факторы риска
Криптококкоз толстой кишки и зигомикоз часто возникают у хозяев с ослабленным иммунитетом, встречаясь в 77% 26–35 и 67% 22 инфекциях соответственно, в то время как кандидоз толстой кишки, 13 пенициллиоз, 36– 38 и аспергиллез9,39–44 встречаются исключительно у хозяев с ослабленным иммунитетом.Факторами риска этих инфекций являются злокачественные новообразования, прием иммунодепрессантов, химиотерапия, нейтропения, СПИД, почечная недостаточность, спленэктомия, синдром Джоба, цирроз печени, недоедание и сахарный диабет; тем не менее, большинство пациентов с пенициллиозом толстой кишки обычно болеют СПИДом.37,38 Также были сообщения о случаях пневмоцистоза и скедоспориоза толстой кишки у пациентов с ослабленным иммунитетом, больных СПИДом и после трансплантации печени, соответственно.51,52 При паракокцидиоидомикозе толстой кишки и гистоплазмозе нет необходимости факторы риска присутствуют.20,21,45–50 Как показано на фиг.4, мужчины преобладают почти во всех грибковых инфекциях, за исключением кандидоза толстой кишки, аспергиллеза и паракокцидиоидомикоза. Более высокая частота грибковых инфекций у мужчин может быть объяснена их более интенсивным воздействием на места обитания эндемичных грибов во время работы67. При кандидозе толстой кишки предпочтения по признаку пола нет, поскольку Candida spp. нормальные комменсалы кишечника человека.13,53,54 Aspergillus spp. распространены повсеместно, поэтому секс также не является фактором риска заражения.9,39–44,55,56 Хотя паракокцидиоидомикоз обычно встречается у мужчин, среди паракокцидиоидомикоза толстой кишки преобладают 67 женщин. 45–50 Автор предполагает, что это может быть вызвано предвзятостью в сообщениях.
Таблица 7
Факторы риска грибковых инфекций толстой кишки
| Грибковые инфекции | Иммунокомпетентные | С ослабленным иммунитетом | Факторы риска | Мужчины | Комментарии | 50 | Мужской | Комментарии | 0% | — | 29% |
|---|---|---|---|---|---|---|---|---|
| Гистоплазмоз20,21 | 81% | 19% | Злокачественные новообразования, иммунодепрессанты, СПИД, синдром Джоба3 – СД | % | ||||
| Кандидоз 13 | 0% | 100% | Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, ESRD | 43% | ||||
| СПИД, иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз печени | 64% | |||||||
| Аспергиллез9,39–44 | 0% | 100% злокачественные новообразования | DM, ожог33% | |||||
| Пенициллиоз 36–38 | 0% | 100% | СПИД (75%), иммунодепрессанты | 100% | ,24 | |||
| 67% | Иммунодепрессанты, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования | 65% | Пневмоцистоз51 | 0% | 100% | СПИД | 100% | Только один случай |
| Scedosporiosis52 | 0% | 100% | 100 | 100% | трансплантация печени | Только один случай |
Иммунитет и инфекция толстой кишки, вызванная грибами
Иммунный ответ хозяина на грибы может играть важную роль в патогенезе инфекции толстой кишки, вызванной грибами, особенно организмами, которые являются частью микробиоты.75,76 Обычно клетки врожденного иммунитета имеют мембраносвязанные и растворимые рецепторы для уничтожения грибов. Связанные с мембраной рецепторы, такие как лектин, толл-подобный поглотитель и рецепторы комплемента, могут обнаруживать грибы или грибковые продукты, а затем активировать фагоцитоз и респираторный взрыв. Факторы транскрипции, которые могут индуцировать провоспалительные цитокины и хемокины, также активируются мембраносвязанными рецепторами. Растворимые рецепторы могут дополнительно активировать комплементы и опсонизировать грибы до рецепторов комплемента. Наконец, T-хелперы (Th) 1 и 17 запускаются и продуцируют другие цитокины, включая интерлейкин (IL) -17A, IL-17F и IL-22 для адаптивного иммунитета.Как врожденная, так и адаптивная иммунные системы защищают хозяина от грибов.76
Есть некоторые свидетельства того, что ослабленный иммунитет может усиливать инфекцию толстой кишки. Было продемонстрировано, что IL-22, который продуцируется врожденными клетками и регулируется IL-23, активирует воспалительные клетки и, таким образом, контролирует начальный рост грибков.75 Дефектные пути IL-23 и IL-22 увеличивают грибковую нагрузку в желудочно-кишечном тракте; тем не менее, клетки Th2 предотвращают распространение грибов. Клетки Th27 играют важную роль в адаптивных иммунных ответах, хотя их нарушение приводит к снижению устойчивости к поздней грибковой инфекции.Дефицит рецептора А IL-17 снижает активацию Th2, тем самым снижая устойчивость к грибам. 75 Таким образом, иммуносупрессивный статус является одним из основных факторов, предрасполагающих к инфекции толстой кишки, вызываемой грибами.
Клинические проявления
Инфекции толстой кишки, вызываемые грибами, имеют различные клинические проявления, как подробно описано в. За исключением зигомикоза и аспергиллеза, более половины пациентов с грибковыми инфекциями толстой кишки имеют диссеминированное заболевание. Боль в животе — наиболее частое проявление зигомикоза и аспергиллеза толстой кишки.9,22,24,39–44 Поражение глубоких тканей и ангиоинвазия, которые являются частыми патологическими проявлениями как при аспергиллезе, так и при зигомикозе, могут объяснить эти проявления.22,25,74 Диарея — симптом, который часто встречается при паракокцидиоидомикозе и кандидозе.13 , 45–50 Случаи гистоплазмоза толстой кишки и пенициллиоза включают диарею и боль в животе в качестве преобладающих симптомов.20,21,36–38 Периректальный абсцесс — специфическая особенность, которая обнаруживается только при криптококкозе толстой кишки. 28,29 Лихорадка — обычное явление при грибковых заболеваниях. инфекция толстой кишки, особенно у пациентов с пенициллиозом толстой кишки, у всех из которых наблюдается лихорадка.36–38 Например, случай пневмоцистоза толстой кишки проявился лихорадкой и диареей 51, тогда как случай скедоспориоза толстой кишки представил диарею и боль в животе.52
Таблица 8
Клинические проявления инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Распространение | Диарея | Боль в животе | LGIB | Ректальный абсцесс | Лихорадка | Комментарии | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| — | 50% | Бессимптомно у 12.5% | ||||||||||||
| Гистоплазмоз20,21 | 83% | 83% | 67% | 32% | — | 77% | — | |||||||
| 57 29% | 29% | — | 71% | — | ||||||||||
| Криптококкоз 26–35 | 71% (все пациенты с ослабленным иммунитетом) | 20% | 30% | 9013 40% 90% 30% | Бессимптомно у 20% | |||||||||
| Аспергиллез9,39–44 | 33% | 22% | 56% | 33% | — | 67% | —34 Peniciosis | 50% | 75% | 75% | 25% | — | 100% | — |
| Зигомикоз22,24 | 38% | 18% | % | – | 55% | — | ||||||||
| Пневмоцистоз51 | 100% | 100% | — | — | — | 100% | Только один случай | |||||||
| 100% | — | — | — | Только один случай |
Патологические данные и распределение
Язва толстой кишки является наиболее частой патологической находкой у пациентов с грибковой инфекцией толстой кишки, как показано на рис.Во всех случаях аспергиллеза толстой кишки и пенициллиоза есть язвы.36–38,74 Язва также обычно обнаруживается при гистоплазмозе толстой кишки, паракокцидиоидомикозе и кандидозе.21,45–50,73 Скедоспориоз толстой кишки также проявляется язвой52. криптококкоз толстой кишки представляет собой образование или полип как наиболее частую патологическую находку, в то время как криптококкоз толстой кишки может также проявляться атипичными патологическими проявлениями, включая абсцесс или стриктуру прямой кишки26–35. Другой инфекцией толстой кишки, которая может проявляться массой или полипом, является гистоплазмоз.21 В одном случае пневмоцистоза толстой кишки у пациента был отек кишечника.51
Таблица 9
Патологические данные об инфекциях толстого кишечника, вызванных грибами
| Грибковые инфекции | Язва | Воспаление слизистой оболочки / эрозия | Псевдемия | Масса / полип | Абсцесс прямой кишки | Стриктура | Комментарий | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз45–50 | 63% | — | — | Гистоплазмоз21 | 79% | 14% | — | 7% | — | — | |||||||||||
| Кандидоз73 | 64% | 14% | 14% | Из серии вскрытий | |||||||||||||||||
| Криптококкоз 26–35 | 11% | 11% | — | 44% | 22% | 11% | |||||||||||||||
| Аспергиллез74 | 100% (с некрозом 55.6%) | — | — | — | — | — | По результатам вскрытия | ||||||||||||||
| Пенициллиоз36–38 | 100% | — | — | — | |||||||||||||||||
| Зигомикоз22,25 | — | — | — | — | — | — | Язва, некроз, образовавшаяся масса, но количество пациентов не указано | 100% | — | — | — | — | Только один случай | ||||||||
| Сцедоспориоз52 | 100% | — | — | — | — |
Распространение инфекции толстой кишки, вызванной грибами, различается в зависимости от типа грибка, как показано в.Гистоплазмоз толстой кишки, зигомикоз и пенициллиоз, как правило, возникают в правой части толстой кишки.20,23,36–38 Область прямой кишки обычно поражается в случаях гистоплазмоза, кандидоза и зигомикоза.13,20,23 Криптококкоз толстой кишки — это заболевание. единственный грибок, который поражает периректальную область.28,29 Диффузное поражение толстой кишки обычно встречается при паракокцидиоидомикозе толстой кишки.45-50 Случаи как пневмоцистоза толстой кишки, так и скедоспориоза также представлены диффузными поражениями.51,52
Таблица 10
Распределения инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Слепая кишка или восходящая ободочная кишка или аппендикс | Поперечная ободочная кишка | Нисходящая или сигмовидная кишка | Прямая кишка | Надпочечная кишка | Вся толстая кишка Паракокцидиоидомикоз 45–50 | 13% | 25% | 13% | — | — | На 50% 20% | — | 20% | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Криптококкоз 27–30,32–35 | 30% | 10% | 40% | — | 20% | Аспергиллез9,39–44 | 33% | 22% | 22% | — | — | 22% | |||||
| Пенициллиоз36–38 | 503 | 9013% —— | — | ||||||||||||||
| Зигомикоз23 | 50% | — | 18% | 7% | — | 25% | 12334 | 9010— | — | — | — | — | 100% | Только один случай | |||
| Scedosporiosis52 | — | — | — | — | Только один случай
Ответ на лечение
Амфотерицин B является наиболее часто используемым препаратом для лечения почти всех грибковых инфекций толстой кишки, за исключением кандидоза и пневмоцистоза.Кандидоз толстой кишки реагирует на флуконазол или каспофунгин и имеет лучший прогноз, если противогрибковая терапия начата со 100% соблюдением режима.13 Хороший ответ был также достигнут при пневмоцистозе толстой кишки и скедоспориозе.51,52 Случай пневмоцистоза толстой кишки лечили пентамидином внутривенно из-за сульфаметоксазола -Триметоприм аллергия.51 Комбинированная противогрибковая терапия и хирургическое вмешательство использовались для лечения желудочно-кишечного зигомикоза и аспергиллеза, вызванного ангиоинвазией и инфарктом. Тем не менее прогноз в этих случаях все еще плохой, летальность составляет 50%.25,39,41,43,44 Выбор антибиотиков и ответ на лечение грибковых инфекций обобщены в.
Таблица 11
Ответ на лечение грибковых инфекций толстой кишки
| Грибковые инфекции | Лечение | Ответ на лечение | Комментарии | |||||
|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз4, 90 -13–50 амфотерицин В или итраконазол | 71% | |||||||
| Гистоплазмоз21 | Амфотерицин В | 77% | ||||||
| Кандидоз4 | Кандидоз4 | Амфотерицин В + флуцитозин ± хирургическое вмешательство | 67% | Ответ на лечение у иммунокомпетентных пациентов составил 100% | ||||
| Аспергиллез 39,41,43,44 | Амфотерицин В или каспофунгин 9013 | 90% хирургическое вмешательство | Пенициллиоз 36–38 | Амфот эрицин B | 75% | |||
| Зигомикоз25 | Амфотерицин B + хирургическое вмешательство | 50% | Комбинированное хирургическое вмешательство улучшило ответ на лечение | |||||
| Один пневмоцистоз3124 | Scedosporiosis52 | Амфотерицин B | 100% | Только один случай |
Заключение
Это первое исследование, в котором проводился интенсивный обзор литературы по грибковым инфекциям толстой кишки.Все содержание кратко изложено в. Он предоставляет основную информацию о причинах, проявлениях и лечении и может легко применяться в клинической практике. Врачи должны знать об этом грибковом образовании, когда у пациентов наблюдаются симптомы со стороны толстой кишки, особенно в случаях с ослабленным иммунитетом. Хотя сообщалось, что многие грибковые инфекции вызывают заболевания толстой кишки, включая аспергиллез, кандидоз, криптококкоз, гистоплазмоз, паракокцидиоидомикоз, пенициллиоз, пневмоцистоз, скедоспориоз и зигомикоз, знание эпидемиологических различий, факторов риска, клинических проявлений и патологических данных поможет врачам. для лучшей диагностики и лечения этих инфекций.Соответствующее лечение противогрибковыми препаратами определенно улучшает результаты; тем не менее, смертность от зигомикоза и аспергиллеза по-прежнему высока.
Таблица 12
Краткое описание инфекции толстой кишки, вызванной грибами
| Грибковые инфекции | Распространенность поражения толстой кишки | Факторы риска | Клинические проявления | Распространение | Распространение | Начальное лечение | |||
|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз 45–50,72 | 29% | • Эндемичная территория (Южная Америка) • Любой хозяин | Диарея, боль в животе, лихорадка | 50% язвы | Вся толстая кишка | Ко-тримоксазол, сульфадиазин, амфотерицин B или итраконазол | 71% | ||
| Гистоплазмоз20,21 | 28% | • Любой хозяин | лихорадка в животе, потеря веса в животе | 83% | Язва, отек слизистой оболочки | Вся толстая кишка, но преимущественно правая сторона e толстой и прямой кишки | Амфотерицин B | 77% | |
| Кандидоз13,73 | 20% кишечного кандидоза при вскрытии | • Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, пациенты с ESR | , боль в животе, лихорадка71% | Язва, зубной налет, эрозия | Вся толстая кишка | Флуконазол или каспофунгин | 100% | ||
| Криптококкоз26–35 | Криптококкоз иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз • Иммунокомпетентные пациенты (23%) | • Симптомы: LGIB, лихорадка, абдоминальная боль, диарея, ректальный абсцесс • 20% пациентов с бессимптомным иммунодефицитом | 71% (все пациенты) | Масса, периректальный абсцесс, язва толстой кишки, очаговые поражения, стриктура, полип | Вся толстая кишка | Амфо терицин B + флуцитозин ± хирургия | 60% | ||
| Аспергиллез9,39–44,74 | 9.2% | • Злокачественные новообразования, химиотерапия, нейтропения, иммунодепрессанты, сахарный диабет, ожог • Пациенты без иммунодефицита | Лихорадка, боль в животе, LGIB, диарея | 86% | Язва, некроз | 9013 Вся толстая кишка каспофунгин ± хирургия | 50% | ||
| Пенициллиоз36–38,68 | 1,9% | • Эндемичная территория (Юго-Восточная Азия, южный Китай, Гонконг и Индия) • В основном СПИД (75%) • Отсутствие иммунокомпетентности пациенты | Лихорадка, диарея, боль в животе, LGIB | 50% | Язва | Преимущественно в правой части ободочной и прямой кишки | Амфотерицин B | 75% | |
| Зигомикоз.85% | • Иммунодепрессивное средство, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования • Пациенты I мм с некомпетентностью (33,3%) | Боль в животе, вздутие живота, лихорадка, LGIB, диарея | 38% | Язва | Вся ободочная кишка, но преимущественно в правой части ободочной кишки | Операция с применением амфотерицина В + | 50% | ||
| Пневмоцистоз51 | Только один случай | • СПИД | Лихорадка, диарея% 13133 | Вся толстая кишка | Пентамидин | 100% | |||
| Скедоспориоз52 | Только один случай | • После трансплантации печени, иммунодепрессанты | Диарея, толстая кишка | 9013 | % Амфотерицин В100% |
Таблица 2
Сводные данные о зарегистрированных случаях пенициллиоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распределение по толстой кишке | Эндоскопические данные | Лечение и исход | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Цанг и др., 36 1988 | 58 / мужчина | Гонконг | Кортикостероиды 3 | гепаталиния | Гепаталий | Гепаталий | Гепаталия | Да | Нисходящая ободочная кишка | Язва | Амфотерицин B → умер | |
| Leung et al, 37 1996 | 32 / мужской | Гонконг | СПИД | Лихорадка, понос 9013, ночь Острая | Нет | Слепая кишка, поперечная и нисходящая ободочная кишка | Язва 90 134 | Амфотерицин В и итраконазол → улучшение | ||||
| Ко и др., 38 1999 | 52 / мужчина | Тайвань | СПИД | Лихорадка, диарея, анемия, боли в животе | 3 недели | Язва | Амфотерицин В и итраконазол → улучшение | |||||
| Ко и др., 38 1999 | 30 / мужчина | Тайвань | СПИД | Диспепсия, диарея, лихорадка, боль в животе3 9013, потеря веса 3 90 месяцев, LGIB4 | № | Слепая кишка, восходящая и поперечная ободочная кишка | Язва | Амфотерицин В и итраконазол → улучшенные |
Таблица 3
Сводные данные по зарегистрированным случаям аспергиллеза толстой кишки7
Сноски
Раскрытие информации
Автор сообщает об отсутствии конфликта интересов в этой работе.
Ссылки
1. Анаисси Э.Дж., Макгиннис М.Р., Пфаллер М.А., редакторы. Клиническая микология. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 2003. [Google Scholar] 2. Отклоняет редакторов WE, Pappas PG, Sobel JD. Клиническая микология. Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 2003. [Google Scholar] 3. Хоспенталь Д.Р., Ринальди М.Г., редакторы. Диагностика и лечение микозов человека. Тотова, Нью-Джерси: Humana Press; 2008. [Google Scholar] 5. Шмитт С.Л., Векснер С.Д. Бактериальный, грибковый, паразитарный и вирусный колит. Surg Clin North Am.1993. 73 (5): 1055–1062. [PubMed] [Google Scholar] 6. Lima AAM, Guerrant RL. Воспалительные энтериты. В: Манделл Г.Л., Беннетт Дж. Э., Долин Р., редакторы. Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета. 7-е изд. Филадельфия, Пенсильвания: Черчилль Ливингстон Эльзевьер; 2009. С. 1389–1398. [Google Scholar] 7. Wilcox CM. Желудочно-кишечные последствия заражения вирусом иммунодефицита человека. В: Фельдман М., Фридман Л.С., Брандт Л.Дж., редакторы. Заболевания желудочно-кишечного тракта и печени Слейзенгера и Фордтрана.9 изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2010. С. 523–535. [Google Scholar] 8. Стилианос С., Форд К.А., Бенвенисти Эл, Харди М.А. Кровоизлияние в нижнюю часть желудочно-кишечного тракта у реципиентов почечного трансплантата. Arch Surg. 1988. 123: 739–744. [PubMed] [Google Scholar] 10. Jayagopal S, Cervia JS. Колит, вызванный Candida albicans, у больного СПИДом. Clin Infect Dis. 1992; 15: 555. [PubMed] [Google Scholar] 11. Куклакис Г., Докас С., Моливас Е., Вакианис П., Эфтимиу А. Кандидозный колит у мужчины среднего возраста, получающего постоянный гемодиализ.Eur J Gastroenterol Hepatol. 2001; 13: 735–736. [PubMed] [Google Scholar] 12. Китагава KH, Kalb RE. Лечение эфализумабом при кандидозном колите. J Am Acad Dermatol. 2008; 59 (приложение 5): S120 – S121. [PubMed] [Google Scholar] 13. Praneenararat S. Первый зарегистрированный случай инфекции толстой кишки, вызванной Candida tropicalis, и обзор литературы. Случай Реп Гастроэнтерол. 2014; 8: 199–205. [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Де Пау Б., Уолш Т.Дж., Доннелли Дж. П. и др. Пересмотренные определения инвазивного грибкового заболевания, разработанные Совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Консенсусной группы Национального института аллергии и инфекционных заболеваний по изучению микозов (EORTC / MSG).Clin Infect Dis. 2008; 46: 1813–1821. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Ascioglu S, Rex JH, de Pauw B, et al. Совместная группа по инвазивным грибковым инфекциям Европейской организации по исследованию и лечению рака. Группа по изучению микозов Национального института аллергии и инфекционных заболеваний. Определение оппортунистических инвазивных грибковых инфекций у пациентов с ослабленным иммунитетом, перенесших онкологические заболевания и трансплантацию гемопоэтических стволовых клеток: международный консенсус. Clin Infect Dis. 2002; 34: 7–14.[PubMed] [Google Scholar] 16. Сафдар А., Сингхал С., Мехта Дж. Клиническое значение выделения из крови не Candida грибков у пациентов, перенесших трансплантацию аллогенных гемопоэтических стволовых клеток высокого риска (1993–2001) Рак. 2004. 100: 2456–2461. [PubMed] [Google Scholar] 17. Контойяннис Д.П., Бодей Г.П., Ханна Х и др. Детерминанты исхода фузариоза в онкологическом центре третичного уровня: влияние восстановления нейтрофилов. Лимфома лейка. 2004. 45: 139–141. [PubMed] [Google Scholar] 18. Лионакис М.С., Бодей Г.П., Тарранд Дж.Дж., Раад II, Контойяннис Д.П.Значение положительных культур крови для появления сапрофитных плесневых грибов у онкологических больных. Clin Microbiol Infect. 2004; 10: 922–925. [PubMed] [Google Scholar] 19. Сафдар А., Родригес Дж., Ролстон К.В. и др. Комбинированная противогрибковая терапия высокими дозами каспофунгина у пациентов с гематологическими злокачественными новообразованиями и трансплантацией гемопоэтических стволовых клеток. Пересадка костного мозга. 2007. 39 (3): 157–164. [PubMed] [Google Scholar] 20. Каппелл М.С., Манделл В., Граймс М.М., Нью-ХК. Гистоплазмоз желудочно-кишечного тракта. Dig Dis Sci.1988. 33: 353–360. [PubMed] [Google Scholar] 21. Асси М., Маккинси Д.С., Дрикс М.Р. и др. Гистоплазмоз желудочно-кишечного тракта при синдроме приобретенного иммунодефицита: отчет о 18 случаях и обзор литературы. Диагностика Microbiol Infect Dis. 2006; 55: 195–201. [PubMed] [Google Scholar] 22. Lyon DT, Schubert TT, Mantia AG, Kaplan MH. Фикомикоз желудочно-кишечного тракта. Am J Gastroenterol. 1979. 72 (4): 379–394. [PubMed] [Google Scholar] 23. Ага Ф. П., Ли Х. Х., Боланд Ч. Р., Брэдли С.Ф. Мукормикома толстой кишки: ранняя диагностика и успешное лечение.AJR Am J Roentgenol. 1985; 145: 739–741. [PubMed] [Google Scholar] 24. Роден М.М., Заутис Т.Э., Бьюкенен В.Л. и др. Эпидемиология и исходы зигомикоза: обзор 929 зарегистрированных случаев. Clin Infect Dis. 2005; 41: 634–653. [PubMed] [Google Scholar] 25. Альмирудис Н.Г., Саттон Д.А., Линден П., Ринальди М.Г., Фунг Дж., Кусне С. Зигомикоз у реципиентов солидных трансплантатов в центре третичной трансплантации и обзор литературы. Am J Transplant. 2006; 6: 2365–2374. [PubMed] [Google Scholar] 26. Зельман С., О’Нил Р.Х., Плаут А.Диссеминированный висцеральный торулез без поражения нервной системы с клиническими проявлениями гранулоцитарного лейкоза. Am J Med. 1951; 11: 658–664. [PubMed] [Google Scholar] 28. Хатто Дж.О., Брайан С.С., Грин Флорида, Уайт СиДжей, Галлин Джи. Криптококкоз толстой кишки, напоминающий болезнь Крона, у пациента с синдромом рецидивирующей инфекции гипериммуноглобулинемии E. Гастроэнтерология. 1988. 94: 808–812. [PubMed] [Google Scholar] 29. Ван Калк М., Мотт С., Рикаерт Ф., Серрюйс Э., Адлер М., Вибран Дж. Криптококковая анальная язва у пациента со СПИДом.Am J Gastroenterol. 1988. 83: 1306–1308. [PubMed] [Google Scholar] 30. Дэйли Дж. С., Портер К. А., Чонг Ф. К., Робиллард Р. Дж.. Распространенная неменингеальная желудочно-кишечная криптококковая инфекция у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1990; 85: 1421–1424. [PubMed] [Google Scholar] 31. Bonacini M, Nussbaum J, Ahluwalia C. Поражение желудочно-кишечного тракта, печени и поджелудочной железы с Cryptococcus neoformans при СПИДе. J Clin Gastroenterol. 1990; 12: 295–297. [PubMed] [Google Scholar] 32. Вашингтон К., Готфрид М.Р., Уилсон М.Л.Желудочно-кишечный криптококкоз. Мод Pathol. 1991; 4: 707–711. [PubMed] [Google Scholar] 33. Мелато М., Горжи Н. Первичный кишечный криптококкоз, имитирующий аденоматозный полип у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1998; 93: 1592–1593. [PubMed] [Google Scholar] 34. Ло Дж. К., Амар Дж. Н., Кирби С. Д., Зетлер П. Дж., Эннс РА. Криптококковая инфекция толстой кишки. Gastrointest Endosc. 2007. 65: 525–526. [PubMed] [Google Scholar] 35. Сонг Дж. К., Ким С. К., Ким Е. С. и др. Случай криптококкоза толстой кишки. Корейский J Gastroenterol.2008. 52: 255–260. Корейский. [PubMed] [Google Scholar] 36. Цанг Д.Н., Чан Дж.К., Лау Ю.Т., Лим В., Цзе СН, Чан Н.К. Инфекция Penicillium marneffei: недиагностируемая болезнь? Гистопатология. 1988; 13: 311–318. [PubMed] [Google Scholar] 37. Леунг Р., Сунг Дж.Й., Чоу Дж., Лай С.К. Необычная причина лихорадки и диареи у больного СПИДом. Penicillium marneffei инфекция. Dig Dis Sci. 1996; 41: 1212–1215. [PubMed] [Google Scholar] 38. Ко CI, Hung CC, Chen MY, Hsueh PR, Hsiao CH, Wong JM. Эндоскопическая диагностика кишечного пенициллиоза marneffei: отчет о трех случаях и обзор литературы.Gastrointest Endosc. 1999. 50 (1): 111–114. [PubMed] [Google Scholar] 39. Kinder RB, Jourdan MH. Диссеминированный аспергиллез и кровоточащие язвы толстой кишки у пациента с трансплантатом почки. JR Soc Med. 1985. 78 (4): 338–339. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Соуза А.Б., Феррейра Г., Вейга Дж., Карвалью А. Клиническая картина: инфаркт кишечника из-за аспергиллеза. Ланцет. 2002; 359 (9302): 210. [PubMed] [Google Scholar] 41. Финн С., Бонд Дж., Маккарти Д., Шихан К., Куинн С. Ангиоинвазивный аспергиллез, проявляющийся как нейтропенический колит.Гистопатология. 2006. 49 (4): 440–441. [PubMed] [Google Scholar] 42. Андрес Л.А., Форд Р.Д., Уилкокс Р.М. Некротический колит, вызванный системным аспергиллезом у ожогового больного. J Burn Care Res. 2007. 28 (6): 918–921. [PubMed] [Google Scholar] 43. Мохайт У., Келл Дж., Хадж М.А. и др. Инвазивный аспергиллез, локализованный в толстой кишке, проявляется в виде токсичного мегаколона. Eur J Haematol. 2007. 78: 270–273. [PubMed] [Google Scholar] 44. Чхве С.Х., Чунг Дж. В., Чо СИ, Ким Би Джей, Квон Дж. Случай изолированного инвазивного аспергиллезного колита с гематохезией у пациента с раком толстой кишки, не страдающего нейтропенией.Кишечная печень. 2010. 4 (2): 274–277. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Chojniak R, Costa Vieira RA, Lopes A, et al. Кишечный паракокцидиоидомикоз, имитирующий рак толстой кишки. Rev Soc Bras Med Trop. 2000. 33: 309–312. [PubMed] [Google Scholar] 47. Коста Виейра РА, Лопес А, Оливейра Х.В. и др. Анальный паракокцидиоидомикоз: необычное проявление диссеминированного заболевания. Rev Soc Med Trop. 2001; 34: 583–586. [PubMed] [Google Scholar] 48. Браво Э.А., Зегарра А.Дж., Пискоя А. и др. Хроническая диарея и панколит, вызванные паракокцидиоидомикозом: клинический случай.История болезни Med. 2010; 2010: 140505. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Леон М., Алаве Дж., Бустаманте Б., Кок Дж., Готуццо Е., Сис С. Т-лимфотропный вирус 1 человека и паракокцидиоидомикоз: вероятная ассоциация в Латинской Америке. Clin Infect Dis. 2010. 51 (2): 250–251. [PubMed] [Google Scholar] 50. Бенард Г., Коста А.Н., Леоперсио А.П., Висентини А.П., Коно А., Шиканаи-Ясуда М.А. Хронический паракокцидиоидомикоз кишечника как поражение одного органа указывает на альтернативный патогенез микоза.Микопатология. 2013. 176 (5–6): 353–357. [PubMed] [Google Scholar] 51. Белломо А.Р., Перлман Д.К., Камински Д.Л., Бреттхольц Е.М., Сарлин Дж. Пневмоцистный колит у больного с синдромом приобретенного иммунодефицита. Am J Gastroenterol. 1992. 87 (6): 759–761. [PubMed] [Google Scholar] 52. Лин Д., Камили К., Лай С., Мушер Д.М., Хэмилл Р. Церебральная инфекция Scedosporium apiospermum, проявляющаяся кишечными проявлениями. Инфекционное заболевание. 2013. 41 (3): 723–726. [PubMed] [Google Scholar] 53. Горбач С.Л., Нахас Л., Лернер П.И., Вайнштейн Л.Исследования микрофлоры кишечника. I. Влияние диеты, возраста и периодического отбора проб на количество фекальных микроорганизмов у человека. Гастроэнтерология. 1967; 53: 845–855. [PubMed] [Google Scholar] 54. Коэн Р., Рот Ф.Дж., Дельгадо Э., Ахерн Д.Г., Калсер М.Х. Грибковая флора нормального тонкого и толстого кишечника человека. N Engl J Med. 1969; 280: 638–641. [PubMed] [Google Scholar] 55. Деннинг DW. Инвазивный аспергиллез. Clin Infect Dis. 1998; 26: 781–803. [PubMed] [Google Scholar] 56. Марр К.А., Паттерсон Т., Деннинг Д. Аспергиллез.Патогенез, клинические проявления и терапия. Заражение Dis Clin North Am. 2002; 16: 875–894. vi. [PubMed] [Google Scholar] 57. Смулиан А.Г., Кили С.П., Сункин С.М., Стрингер-младший. Генетическая и антигенная изменчивость организмов Pneumocystis carinii: инструменты для изучения эпидемиологии и патогенеза инфекции. J Lab Clin Med. 1997. 130 (5): 461–468. [PubMed] [Google Scholar] 58. Дейли К.Р., Кох Дж., Левин Л., Уолцер П.Д. Иммуноферментный анализ и серологические ответы на Pneumocystis jiroveci. Emerg Infect Dis.2004. 10 (5): 848–854. [Бесплатная статья PMC] [PubMed] [Google Scholar] 59. Chayakulkeeree M, Perfect JR. Криптококкоз. Заражение Dis Clin North Am. 2006; 20: 507–544. [PubMed] [Google Scholar] 61. Саммербелл Р.К., Крайден С., Кейн Дж. Горшечные растения в больницах как резервуары патогенных грибов. Микопатология. 1989; 106: 13–22. [PubMed] [Google Scholar] 62. Хоффманн С., Доллив С., Грюнберг С. и др. Археи и грибы микробиома кишечника человека: корреляция с диетой и бактериальными жителями. PLoS One. 2013; 8 (6): e66019.[Бесплатная статья PMC] [PubMed] [Google Scholar] 63. Контояннис Д.П., Льюис Р.Э. Инвазивный зигомикоз: обновленная информация о патогенезе, клинических проявлениях и лечении. Заражение Dis Clin North Am. 2006; 20: 581–607. [PubMed] [Google Scholar] 64. Гудвин Р.А., младший, Шапиро Дж. Л., Турман Г. Х., Турман СС, Дес През Р. М.. Диссеминированный гистоплазмоз: клинико-патологические корреляции. Медицина (Балтимор) 1980; 59: 1–33. [PubMed] [Google Scholar] 65. Пшеница LJ, Slama TG, Eitzen HE, Kohler RB, French ML, Biesecker JL. Крупная городская вспышка гистоплазмоза: клинические особенности.Ann Intern Med. 1981; 94: 331–337. [PubMed] [Google Scholar] 66. Negroni R. Paracoccidioidomycosis (южноамериканский бластомикоз, микоз Лутца) Int J Dermatol. 1993; 32: 847–859. [PubMed] [Google Scholar] 67. Blotta MH, Mamoni RL, Oliveira SJ, et al. Эндемичные регионы паракокцидиоидомикоза в Бразилии: клиническое и эпидемиологическое исследование 584 случаев в юго-восточном регионе. Am J Trop Med Hyg. 1999. 61: 390–394. [PubMed] [Google Scholar] 68. Суппаратпиньо К., Кхамван С., Баосунг В., Нельсон К.Э., Сирисантана Т.Распространенная инфекция Penicillium marneffei в Юго-Восточной Азии. Ланцет. 1994; 344: 110–113. [PubMed] [Google Scholar] 69. Вонг К.Х., Ли С.С., Ло Ю.С. и др. Профиль оппортунистических инфекций среди людей, инфицированных ВИЧ-1, в Гонконге. Чжунхуа И Сюэ За Чжи (Тайбэй) 1995; 55: 127–136. [PubMed] [Google Scholar] 70. Duong TA. Инфекция, вызванная Penicillium marneffei, новым патогеном: обзор 155 зарегистрированных случаев. Clin Infect Dis. 1996; 23: 125–130. [PubMed] [Google Scholar] 71. Вонг К.Х., Ли СС. Сравнение первой и второй сотни случаев СПИДа в Гонконге.Singapore Med J. 1998; 39: 236–240. [PubMed] [Google Scholar] 72. Peña CE. Глубокие грибковые инфекции в Колумбии. Клинико-патологическое исследование 162 случаев. Am J Clin Pathol. 1967. 47 (4): 505–520. [PubMed] [Google Scholar] 73. Эрас П., Гольдштейн М.Дж., Шерлок П. Кандидозная инфекция желудочно-кишечного тракта. Медицина (Балтимор) 1972; 51: 367–379. [PubMed] [Google Scholar] 74. Молодой Р.С., Беннетт Дж. Э., Фогель С. Л., Карбон П. П., ДеВита В. Т.. Аспергиллез. Спектр заболевания у 98 больных. Медицина (Балтимор) 1970; 49: 147–173.[PubMed] [Google Scholar] 75. Де Лука А., Зеланте Т., Д’Анджело С. и др. IL-22 определяет новый иммунный путь устойчивости к противогрибковым препаратам. Mucosal Immunol. 2010. 3 (4): 361–373. [PubMed] [Google Scholar] 76. Андерхилл Д.М., Илиев И.Д. Микобиота: взаимодействие между комменсальными грибами и иммунной системой хозяина. Nat Rev Immunol. 2014. 14 (6): 405–416. [Бесплатная статья PMC] [PubMed] [Google Scholar]Грибковая инфекция толстой кишки
Clin Exp Gastroenterol. 2014; 7: 415–426.
Сурат Праниенарарат
Отделение гастроэнтерологии, Медицинский факультет, Университет принца Сонгкла, Сонгкхла, Таиланд
Отделение гастроэнтерологии, Медицинский факультет, Университет Принца Сонгкла, Сонгкхла, Таиланд
Переписка: Сурат Праненарарат, Отделение гастроэнтерологии, Кафедра медицины, Университет Принца Сонгкла, 15 Kanjanavanich Road, Hat-Yai, Songkhla, Thailand,, Tel +66 80 441 0174, Email moc.Авторские права © 2014 Praneenararat. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения Dove Medical Press Limited при условии правильной атрибуции работы. Эта статья цитируется в других статьях PMC.Abstract
Грибы — патогены, которые обычно поражают пациентов с ослабленным иммунитетом и могут поражать любые органы тела, включая толстую кишку.Однако в литературе содержится ограниченное количество подробностей об инфекциях толстой кишки, вызванных грибками. Эта статья представляет собой подробный обзор доступной информации о грибах, которые могут вызывать инфекции толстой кишки. В нем используется сравнительный стиль, поэтому его выводы могут быть доступны для клинического применения.
Ключевые слова: грибок, колит, толстая кишка, толстая кишка
Введение
Грибы являются патогенами, которые обычно инфицируют пациентов с ослабленным иммунитетом. В настоящее время частота этих патогенов в причинах заболевания постепенно увеличивается в результате более широкого использования иммунодепрессантов, химиотерапии и трансплантации, а также инфекций, вызванных вирусом иммунодефицита человека.Грибковые инфекции могут поражать любой орган, в том числе толстую кишку.1–3 Тем не менее, в литературе доступны лишь ограниченные сведения об инфекции толстой кишки, вызванной грибами.4,5 Эта статья представляет собой интенсивный обзор исследований грибковой инфекции толстой кишки. в кратком сравнительном стиле для удобного клинического применения.
Методы
Автор инициировал обзор с исследования грибков, которые могут вызывать инфекцию толстой кишки, в MEDLINE, в основных учебниках и существующей исследовательской литературе, в которой рассматриваются грибковые инфекции толстой кишки.4–7 В MEDLINE автор использовал ключевые слова из двух групп. Первая группа состояла из названий грибов или инфекций, связанных с грибами, включая «аспергиллез», « Aspergillus », « Blastomyces », «бластомикоз», « Candida », «кандидоз», «хромобластомикоз». , « Cladophialophora », « Coccidioides », «кокцидиоидомикоз», «криптококкоз», « Cryptococcus », «дерматофит», «дерматофитоз», « Epidermophyton », «eumycetoma», «eumycetoma», , «Фузариоз», « Fusarium », « Histoplasma », «гистоплазмоз», « Madurella », « Microsporum », «мукормикоз», « Paracoccidioides », «паракокцидиоидомикоз». , « Penicillium », «феогифомикоз», « Pneumocystis », «пневмоцистоз», «скедоспориоз», « Scedosporium », « Sporothrix », «споротрихоз», « Trichophyton », « Trichophyton » »,« трихоспороноз », « Zygomycetes » и «зигомикоз».Вторая группа ключевых слов состояла из слов, связанных с локализацией заболевания, которое мы рассматривали, включая «колит», «толстая кишка», «толстая кишка», «энтероколит», «толстая кишка», «толстая кишка» и «толстая кишка». . Наконец, было установлено, что инфекции толстой кишки, которые, как сообщалось, были вызваны грибами, были аспергиллезом, кандидозом, криптококкозом, гистоплазмозом, паракокцидиоидомикозом, пенициллиозом, пневмоцистозом, скедоспориозом и зигомикозом. Подробная информация о каждом грибке была дополнительно рассмотрена из статей, найденных в MEDLINE, с использованием ключевых слов, как описано выше, цитат из этих статей и ссылок в основных учебниках.В MEDLINE были включены все типы статей, включая обзоры, серии случаев, истории болезни, редакционные статьи и письма до 30 июня 2014 г. Первоначально было найдено 124 статьи. Были отобраны только статьи, которые были на английском языке или имели аннотацию на английском языке с необходимыми подробностями, которые имели определенный диагноз грибковой инфекции толстой кишки, включая прямую визуализацию типичного грибка или положительную культуру грибка в образцах толстой кишки. Случаи кандидоза, который считается нормальным комменсалом желудочно-кишечного тракта человека, также должны соответствовать одному из следующих критериев в соответствии с принятыми отчетами о случаях и пересмотренной совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Национальным институтом. критериев группы исследования аллергии и инфекционных микозов: проникновение в глубокие ткани толстой кишки или положительный результат на Candida spp.в поверхностной слизистой оболочке с положительным посевом крови или положительным Candida spp. в поверхностной слизистой оболочке с очевидностью ответа на лечение8–14 Candida spp. только на поверхностной слизистой оболочке без положительного посева крови или свидетельств ответа на лечение были исключены. Распространение было определено как поражение двух или более несмежных органов15–19
В настоящее время уже рассмотрены гистоплазмоз, 20,21 кандидоз 13 и зигомикоз22–25. В случаях других грибковых инфекций, включая криптококкоз, пенициллиоз 26–35, аспергиллез 36–38, 9,39–44 и паракокцидиоидомикоз 45–50, автор обобщил отчеты о случаях, как показано в -.Был опубликован только один отчет о каждом случае пневмоцистоза51 и скедоспориоза.52
Таблица 1
Сводные данные о зарегистрированных случаях криптококкоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распространение в толстой кишке | Эндоскопическое исследование | Лечение и исход | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Zelman et al. | ХМЛ, химиотерапия | Не упоминается | Не упоминается | Да | Не упоминается | Язва | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Унат и др., 27 1960 | 16 / мужчина | Турция | Турция | Диарея, боли в животе, LGIB | 8 лет | Нет | Спуститься ободочной кишки | Масса | Хирургия и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hutto et al, 28 1988 | 29 / женщина | США | Синдром Джобса | Абсцесс прямой кишки | 1 год | 1 год | восходящая ободочная кишка | Стриктура восходящей ободочной кишки и периректальный абсцесс | Операция и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van Calck et al, 29 1988 | 47 / мужской | Бельгия | СПИД | Hematochezia | Hematochezia, лихорадка | , лихорадка не упоминаетсяДа | Периректум | Периректальный абсцесс | Хирургия, амфотерицин B и флуцитозин → улучшенное состояние | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Daly et al, 30 1990 | 63 / мужской | USA | Хортностерэктомия, корнеэктомия , недомогание | 7 дней | Есть | Поперечная ободочная кишка | Масса | Амфот эрицин B и флуцитозин → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bonacini et al, 31 1990 | 31 / мужчина | США | AIDS | Hemiplegia, эпилепсия | Не упоминается | Да | Не упоминается | B и флуцитозин → умер||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 38 / мужчина | США | СПИД | Эпигастральная боль, одинофагия | 3 месяца | Да | Противогрибковая терапия | 3 → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 24 / мужчина | США | Болезнь Ходжкина | Не упоминается | Не упоминается | Да | Не упоминается | Не упоминается | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 31 / женщина | США | СПИД | Не упоминается d | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 51 / мужчина | США | Кортикостероиды | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умерло | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Мелато и Горджи, 33 1998 | 84 / женщина | Италия | Нет | Ректальное кровотечение Нет | Острое | Острое толстая кишка | Полип | Полипэктомия → улучшенная | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Law et al, 34 2007 | 40 / мужчина | Канада | AIDS | Боль в животе, диарея, дисфагия, лихорадка | 6 недель Слева | 6 недель толстая кишка | Множественные эритематозные, выпуклые, пятнистые поражения | Амфотерицин B и флуцитозин → улучшенный | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сонг и др., 35 2008 | 27 / женщина | Корея | Нет | Мелена | Не упоминается | Нет | Проксимальный отдел восходящей ободочной кишки | Масса | Амфотерицин В и флуконазин B → | 9018 с улучшенным эффектом Таблица 4
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность | Продолжительность | Распространение | Распределение по толстой кишке | Эндоскопическое исследование | Лечение и результат | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Penna, 45 1979 | 8 / женщина | Бразилия | Нет | Диарея, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность | 4 года | Нет | Вся толстая кишка | Стриктура, язва | Ко-тримоксазол → улучшение | |||||||||||||||||||||||
| Chojniak et al, 46 2000 | 57 / не упоминается | Бразилия | Нет | Боль в животе, диарея, потеря веса 3 | 2 года | Слепая кишка | Масса | Кетоконазол → не упоминается | ||||||||||||||||||||||||
| Коста Виейра и др., 47 2001 | 60 / мужской | Бразилия | Нет | Лихорадка, перианальные узелки, дисфония, кашель13 лет | Да | Поперечная и нисходящая толстая кишка | Язва | Сульфадиазин → улучшение | ||||||||||||||||||||||||
| Браво и др., 48 2010 | 39 / женщина | Перу | Нет | диарея | 2 месяца | Да | Вся толстая кишка | Язва | Амфотерицин B → умер | |||||||||||||||||||||||
| Леон и др., 49 2 010 | 34 / мужчина | Перу | Нет | Диарея, язвы во рту, одинофагия, похудание, кашель | 18 месяцев | Да | Вся толстая кишка | Язва | Амфтозол | Амфтозол | Леон и др., 49 2010 | 40 / женщина | Перу | Нет | Диарея, похудание, гепатомегалия | 1 год | Да | Не упоминается | Не упоминается | Amphoteric | Benard et al, 50 2013 | 56 / женщина | Бразилия | Нет | Нет (колоноскопия для проверки) | Неизвестно | Нет | Поперечная ободочная кишка | Полип | Итраконазол | 58 / женщина | Бразилия | Нет | Диарея, потеря веса, лихорадка | 6 месяцев 9 0134 | Нет | Вся толстая кишка | Язва | Итраконазол → улучшенный |
Эпидемиология
Candida spp.являются нормальными комменсалами желудочно-кишечного тракта, 53,54, тогда как Aspergillus spp. и Pneumocystis spp. распространены повсеместно55–58 и являются причиной грибковых инфекций во всем мире. Cryptococcus spp. и Scedosporium spp. являются эндемическими микозами, которые также имеют распространение по всему миру. Cryptococcus spp. были изолированы из помета голубей 59, а Scedosporium spp. были обнаружены в приливных отмелях, болотах, прудах, навозе и почве.60,61 Aspergillus spp. и Cryptococcus spp. также могут быть обнаружены как компонент микобиоты толстой кишки человека.62
Zygomycetes можно разделить на два отряда: Mucorales и Entomophthorales. Mucorales — эндемичные грибы, встречающиеся во всем мире в органических субстратах, включая хлеб, фрукты, растительные вещества, почву, компост и экскременты животных.63 Histoplasma spp., Entomophthorales, Paracoccidioides spp. И Penicillium spp. эндемичные микозы, выделенные из почвы в ряде регионов мира.63–71 Histoplasma spp. обнаружены в почве, обогащенной пометом летучих мышей, кур и дроздов.64,65 Entomophthorales можно разделить на Conidiobolus spp. и Basidiobolus spp. и находятся в почве некоторых тропических регионов, особенно Африки, Южной Америки, Центральной Америки и Азии63. Paracoccidioides spp. ограничены почвой в странах Центральной и Южной Америки между 23 ° северной широты (юг Мексики) и 34,5 ° северной широты (Аргентина и Уругвай).Эти районы обладают уникальными экологическими особенностями, так как представляют собой тропические и субтропические леса с умеренными температурами и высокой влажностью.66,67 Penicillium spp. также изолированы от почвы в определенных областях, включая Юго-Восточную Азию, южный Китай (Гуанси), Гонконг и Индию.68–71 Эпидемиологические данные суммированы в.
Таблица 5
Эпидемиология грибков, которые могут вызывать инфекцию толстой кишки
| Грибки | Эпидемиология |
|---|---|
| Aspergillus spp., 55,56 Candida spp., 53,54 Криптококк видов, 59 Histoplasma spp., 64,65 Mucorales, 63 Pneumocystis виды, 57,58 Scedosporium spp.60,61 | Во всем мире |
| Entomophthorales63 | Тропические зоны в Африке, Южной Америке, Центральной Америке и Азии |
| Paracoccidioides spp.66,67 | странах Южной и Центральной Америки , особенно в Бразилии, Колумбии, Венесуэле и Аргентине|
| Penicillium spp.68–71 | Юго-Восточная Азия, южный Китай (Гуанси), Гонконг и Индия |
Распространенность поражения толстой кишки
Степень поражения толстой кишки грибковыми инфекциями варьируется в зависимости от типа грибка, как подробно описано в. Паракокцидиоидомикоз и гистоплазмоз являются наиболее распространенными инфекциями толстой кишки, вызываемыми грибами, с распространенностью 29% 72 и 28% 20 соответственно. Напротив, пенициллиоз, зигомикоз, пневмоцистоз и скедоспориоз редко инфильтрируют толстую кишку, при этом пенициллиоз и зигомикоз встречаются в 1.9% 68 и 0,85% инфекций толстой кишки 25 соответственно. И пневмоцистоз, и скедоспориоз известны только из одного сообщения о клиническом случае.51,52 За исключением ротоглоточного кандидоза, толстая кишка является третьим наиболее частым желудочно-кишечным органом, вовлеченным в кандидоз после пищевода и желудка. Ободочная кишка участвует в 20% случаев кандидоза желудочно-кишечного тракта.73 Криптококкоз толстой кишки является наиболее частым желудочно-кишечным проявлением диссеминированного или легочного криптококкоза с распространенностью около 17%.32
Таблица 6
Распространенность поражения толстой кишки при каждой грибковой инфекции
| Грибковые инфекции | Распространенность поражения толстой кишки | Комментарии | ||
|---|---|---|---|---|
| Паракокцидиоидомикоз3 | ||||
| Гистоплазмоз20 | 28% | |||
| Кандидоз73 | 20% желудочно-кишечного кандидоза (исключая орофарингеальный кандидоз) или легочный криптококкоз | |||
| Аспергиллез74 | 9.2% | |||
| Пенициллиоз68 | 1,9% | Всего четыре случая | ||
| Зигомикоз25 | 0,85% | |||
| 902 Нет данных | Только один случай |
Факторы риска
Криптококкоз толстой кишки и зигомикоз часто возникают у хозяев с ослабленным иммунитетом, встречаясь в 77% 26–35 и 67% 22 инфекциях соответственно, в то время как кандидоз толстой кишки, 13 пенициллиоз, 36– 38 и аспергиллез9,39–44 встречаются исключительно у хозяев с ослабленным иммунитетом.Факторами риска этих инфекций являются злокачественные новообразования, прием иммунодепрессантов, химиотерапия, нейтропения, СПИД, почечная недостаточность, спленэктомия, синдром Джоба, цирроз печени, недоедание и сахарный диабет; тем не менее, большинство пациентов с пенициллиозом толстой кишки обычно болеют СПИДом.37,38 Также были сообщения о случаях пневмоцистоза и скедоспориоза толстой кишки у пациентов с ослабленным иммунитетом, больных СПИДом и после трансплантации печени, соответственно.51,52 При паракокцидиоидомикозе толстой кишки и гистоплазмозе нет необходимости факторы риска присутствуют.20,21,45–50 Как показано на фиг.4, мужчины преобладают почти во всех грибковых инфекциях, за исключением кандидоза толстой кишки, аспергиллеза и паракокцидиоидомикоза. Более высокая частота грибковых инфекций у мужчин может быть объяснена их более интенсивным воздействием на места обитания эндемичных грибов во время работы67. При кандидозе толстой кишки предпочтения по признаку пола нет, поскольку Candida spp. нормальные комменсалы кишечника человека.13,53,54 Aspergillus spp. распространены повсеместно, поэтому секс также не является фактором риска заражения.9,39–44,55,56 Хотя паракокцидиоидомикоз обычно встречается у мужчин, среди паракокцидиоидомикоза толстой кишки преобладают 67 женщин. 45–50 Автор предполагает, что это может быть вызвано предвзятостью в сообщениях.
Таблица 7
Факторы риска грибковых инфекций толстой кишки
| Грибковые инфекции | Иммунокомпетентные | С ослабленным иммунитетом | Факторы риска | Мужчины | Комментарии | 50 | Мужской | Комментарии | 0% | — | 29% |
|---|---|---|---|---|---|---|---|---|
| Гистоплазмоз20,21 | 81% | 19% | Злокачественные новообразования, иммунодепрессанты, СПИД, синдром Джоба3 – СД | % | ||||
| Кандидоз 13 | 0% | 100% | Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, ESRD | 43% | ||||
| СПИД, иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз печени | 64% | |||||||
| Аспергиллез9,39–44 | 0% | 100% злокачественные новообразования | DM, ожог33% | |||||
| Пенициллиоз 36–38 | 0% | 100% | СПИД (75%), иммунодепрессанты | 100% | ,24 | |||
| 67% | Иммунодепрессанты, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования | 65% | Пневмоцистоз51 | 0% | 100% | СПИД | 100% | Только один случай |
| Scedosporiosis52 | 0% | 100% | 100 | 100% | трансплантация печени | Только один случай |
Иммунитет и инфекция толстой кишки, вызванная грибами
Иммунный ответ хозяина на грибы может играть важную роль в патогенезе инфекции толстой кишки, вызванной грибами, особенно организмами, которые являются частью микробиоты.75,76 Обычно клетки врожденного иммунитета имеют мембраносвязанные и растворимые рецепторы для уничтожения грибов. Связанные с мембраной рецепторы, такие как лектин, толл-подобный поглотитель и рецепторы комплемента, могут обнаруживать грибы или грибковые продукты, а затем активировать фагоцитоз и респираторный взрыв. Факторы транскрипции, которые могут индуцировать провоспалительные цитокины и хемокины, также активируются мембраносвязанными рецепторами. Растворимые рецепторы могут дополнительно активировать комплементы и опсонизировать грибы до рецепторов комплемента. Наконец, T-хелперы (Th) 1 и 17 запускаются и продуцируют другие цитокины, включая интерлейкин (IL) -17A, IL-17F и IL-22 для адаптивного иммунитета.Как врожденная, так и адаптивная иммунные системы защищают хозяина от грибов.76
Есть некоторые свидетельства того, что ослабленный иммунитет может усиливать инфекцию толстой кишки. Было продемонстрировано, что IL-22, который продуцируется врожденными клетками и регулируется IL-23, активирует воспалительные клетки и, таким образом, контролирует начальный рост грибков.75 Дефектные пути IL-23 и IL-22 увеличивают грибковую нагрузку в желудочно-кишечном тракте; тем не менее, клетки Th2 предотвращают распространение грибов. Клетки Th27 играют важную роль в адаптивных иммунных ответах, хотя их нарушение приводит к снижению устойчивости к поздней грибковой инфекции.Дефицит рецептора А IL-17 снижает активацию Th2, тем самым снижая устойчивость к грибам. 75 Таким образом, иммуносупрессивный статус является одним из основных факторов, предрасполагающих к инфекции толстой кишки, вызываемой грибами.
Клинические проявления
Инфекции толстой кишки, вызываемые грибами, имеют различные клинические проявления, как подробно описано в. За исключением зигомикоза и аспергиллеза, более половины пациентов с грибковыми инфекциями толстой кишки имеют диссеминированное заболевание. Боль в животе — наиболее частое проявление зигомикоза и аспергиллеза толстой кишки.9,22,24,39–44 Поражение глубоких тканей и ангиоинвазия, которые являются частыми патологическими проявлениями как при аспергиллезе, так и при зигомикозе, могут объяснить эти проявления.22,25,74 Диарея — симптом, который часто встречается при паракокцидиоидомикозе и кандидозе.13 , 45–50 Случаи гистоплазмоза толстой кишки и пенициллиоза включают диарею и боль в животе в качестве преобладающих симптомов.20,21,36–38 Периректальный абсцесс — специфическая особенность, которая обнаруживается только при криптококкозе толстой кишки. 28,29 Лихорадка — обычное явление при грибковых заболеваниях. инфекция толстой кишки, особенно у пациентов с пенициллиозом толстой кишки, у всех из которых наблюдается лихорадка.36–38 Например, случай пневмоцистоза толстой кишки проявился лихорадкой и диареей 51, тогда как случай скедоспориоза толстой кишки представил диарею и боль в животе.52
Таблица 8
Клинические проявления инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Распространение | Диарея | Боль в животе | LGIB | Ректальный абсцесс | Лихорадка | Комментарии | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| — | 50% | Бессимптомно у 12.5% | ||||||||||||
| Гистоплазмоз20,21 | 83% | 83% | 67% | 32% | — | 77% | — | |||||||
| 57 29% | 29% | — | 71% | — | ||||||||||
| Криптококкоз 26–35 | 71% (все пациенты с ослабленным иммунитетом) | 20% | 30% | 9013 40% 90% 30% | Бессимптомно у 20% | |||||||||
| Аспергиллез9,39–44 | 33% | 22% | 56% | 33% | — | 67% | —34 Peniciosis | 50% | 75% | 75% | 25% | — | 100% | — |
| Зигомикоз22,24 | 38% | 18% | % | – | 55% | — | ||||||||
| Пневмоцистоз51 | 100% | 100% | — | — | — | 100% | Только один случай | |||||||
| 100% | — | — | — | Только один случай |
Патологические данные и распределение
Язва толстой кишки является наиболее частой патологической находкой у пациентов с грибковой инфекцией толстой кишки, как показано на рис.Во всех случаях аспергиллеза толстой кишки и пенициллиоза есть язвы.36–38,74 Язва также обычно обнаруживается при гистоплазмозе толстой кишки, паракокцидиоидомикозе и кандидозе.21,45–50,73 Скедоспориоз толстой кишки также проявляется язвой52. криптококкоз толстой кишки представляет собой образование или полип как наиболее частую патологическую находку, в то время как криптококкоз толстой кишки может также проявляться атипичными патологическими проявлениями, включая абсцесс или стриктуру прямой кишки26–35. Другой инфекцией толстой кишки, которая может проявляться массой или полипом, является гистоплазмоз.21 В одном случае пневмоцистоза толстой кишки у пациента был отек кишечника.51
Таблица 9
Патологические данные об инфекциях толстого кишечника, вызванных грибами
| Грибковые инфекции | Язва | Воспаление слизистой оболочки / эрозия | Псевдемия | Масса / полип | Абсцесс прямой кишки | Стриктура | Комментарий | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз45–50 | 63% | — | — | Гистоплазмоз21 | 79% | 14% | — | 7% | — | — | |||||||||||
| Кандидоз73 | 64% | 14% | 14% | Из серии вскрытий | |||||||||||||||||
| Криптококкоз 26–35 | 11% | 11% | — | 44% | 22% | 11% | |||||||||||||||
| Аспергиллез74 | 100% (с некрозом 55.6%) | — | — | — | — | — | По результатам вскрытия | ||||||||||||||
| Пенициллиоз36–38 | 100% | — | — | — | |||||||||||||||||
| Зигомикоз22,25 | — | — | — | — | — | — | Язва, некроз, образовавшаяся масса, но количество пациентов не указано | 100% | — | — | — | — | Только один случай | ||||||||
| Сцедоспориоз52 | 100% | — | — | — | — |
Распространение инфекции толстой кишки, вызванной грибами, различается в зависимости от типа грибка, как показано в.Гистоплазмоз толстой кишки, зигомикоз и пенициллиоз, как правило, возникают в правой части толстой кишки.20,23,36–38 Область прямой кишки обычно поражается в случаях гистоплазмоза, кандидоза и зигомикоза.13,20,23 Криптококкоз толстой кишки — это заболевание. единственный грибок, который поражает периректальную область.28,29 Диффузное поражение толстой кишки обычно встречается при паракокцидиоидомикозе толстой кишки.45-50 Случаи как пневмоцистоза толстой кишки, так и скедоспориоза также представлены диффузными поражениями.51,52
Таблица 10
Распределения инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Слепая кишка или восходящая ободочная кишка или аппендикс | Поперечная ободочная кишка | Нисходящая или сигмовидная кишка | Прямая кишка | Надпочечная кишка | Вся толстая кишка Паракокцидиоидомикоз 45–50 | 13% | 25% | 13% | — | — | На 50% 20% | — | 20% | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Криптококкоз 27–30,32–35 | 30% | 10% | 40% | — | 20% | Аспергиллез9,39–44 | 33% | 22% | 22% | — | — | 22% | |||||
| Пенициллиоз36–38 | 503 | 9013% —— | — | ||||||||||||||
| Зигомикоз23 | 50% | — | 18% | 7% | — | 25% | 12334 | 9010— | — | — | — | — | 100% | Только один случай | |||
| Scedosporiosis52 | — | — | — | — | Только один случай
Ответ на лечение
Амфотерицин B является наиболее часто используемым препаратом для лечения почти всех грибковых инфекций толстой кишки, за исключением кандидоза и пневмоцистоза.Кандидоз толстой кишки реагирует на флуконазол или каспофунгин и имеет лучший прогноз, если противогрибковая терапия начата со 100% соблюдением режима.13 Хороший ответ был также достигнут при пневмоцистозе толстой кишки и скедоспориозе.51,52 Случай пневмоцистоза толстой кишки лечили пентамидином внутривенно из-за сульфаметоксазола -Триметоприм аллергия.51 Комбинированная противогрибковая терапия и хирургическое вмешательство использовались для лечения желудочно-кишечного зигомикоза и аспергиллеза, вызванного ангиоинвазией и инфарктом. Тем не менее прогноз в этих случаях все еще плохой, летальность составляет 50%.25,39,41,43,44 Выбор антибиотиков и ответ на лечение грибковых инфекций обобщены в.
Таблица 11
Ответ на лечение грибковых инфекций толстой кишки
| Грибковые инфекции | Лечение | Ответ на лечение | Комментарии | |||||
|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз4, 90 -13–50 амфотерицин В или итраконазол | 71% | |||||||
| Гистоплазмоз21 | Амфотерицин В | 77% | ||||||
| Кандидоз4 | Кандидоз4 | Амфотерицин В + флуцитозин ± хирургическое вмешательство | 67% | Ответ на лечение у иммунокомпетентных пациентов составил 100% | ||||
| Аспергиллез 39,41,43,44 | Амфотерицин В или каспофунгин 9013 | 90% хирургическое вмешательство | Пенициллиоз 36–38 | Амфот эрицин B | 75% | |||
| Зигомикоз25 | Амфотерицин B + хирургическое вмешательство | 50% | Комбинированное хирургическое вмешательство улучшило ответ на лечение | |||||
| Один пневмоцистоз3124 | Scedosporiosis52 | Амфотерицин B | 100% | Только один случай |
Заключение
Это первое исследование, в котором проводился интенсивный обзор литературы по грибковым инфекциям толстой кишки.Все содержание кратко изложено в. Он предоставляет основную информацию о причинах, проявлениях и лечении и может легко применяться в клинической практике. Врачи должны знать об этом грибковом образовании, когда у пациентов наблюдаются симптомы со стороны толстой кишки, особенно в случаях с ослабленным иммунитетом. Хотя сообщалось, что многие грибковые инфекции вызывают заболевания толстой кишки, включая аспергиллез, кандидоз, криптококкоз, гистоплазмоз, паракокцидиоидомикоз, пенициллиоз, пневмоцистоз, скедоспориоз и зигомикоз, знание эпидемиологических различий, факторов риска, клинических проявлений и патологических данных поможет врачам. для лучшей диагностики и лечения этих инфекций.Соответствующее лечение противогрибковыми препаратами определенно улучшает результаты; тем не менее, смертность от зигомикоза и аспергиллеза по-прежнему высока.
Таблица 12
Краткое описание инфекции толстой кишки, вызванной грибами
| Грибковые инфекции | Распространенность поражения толстой кишки | Факторы риска | Клинические проявления | Распространение | Распространение | Начальное лечение | |||
|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз 45–50,72 | 29% | • Эндемичная территория (Южная Америка) • Любой хозяин | Диарея, боль в животе, лихорадка | 50% язвы | Вся толстая кишка | Ко-тримоксазол, сульфадиазин, амфотерицин B или итраконазол | 71% | ||
| Гистоплазмоз20,21 | 28% | • Любой хозяин | лихорадка в животе, потеря веса в животе | 83% | Язва, отек слизистой оболочки | Вся толстая кишка, но преимущественно правая сторона e толстой и прямой кишки | Амфотерицин B | 77% | |
| Кандидоз13,73 | 20% кишечного кандидоза при вскрытии | • Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, пациенты с ESR | , боль в животе, лихорадка71% | Язва, зубной налет, эрозия | Вся толстая кишка | Флуконазол или каспофунгин | 100% | ||
| Криптококкоз26–35 | Криптококкоз иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз • Иммунокомпетентные пациенты (23%) | • Симптомы: LGIB, лихорадка, абдоминальная боль, диарея, ректальный абсцесс • 20% пациентов с бессимптомным иммунодефицитом | 71% (все пациенты) | Масса, периректальный абсцесс, язва толстой кишки, очаговые поражения, стриктура, полип | Вся толстая кишка | Амфо терицин B + флуцитозин ± хирургия | 60% | ||
| Аспергиллез9,39–44,74 | 9.2% | • Злокачественные новообразования, химиотерапия, нейтропения, иммунодепрессанты, сахарный диабет, ожог • Пациенты без иммунодефицита | Лихорадка, боль в животе, LGIB, диарея | 86% | Язва, некроз | 9013 Вся толстая кишка каспофунгин ± хирургия | 50% | ||
| Пенициллиоз36–38,68 | 1,9% | • Эндемичная территория (Юго-Восточная Азия, южный Китай, Гонконг и Индия) • В основном СПИД (75%) • Отсутствие иммунокомпетентности пациенты | Лихорадка, диарея, боль в животе, LGIB | 50% | Язва | Преимущественно в правой части ободочной и прямой кишки | Амфотерицин B | 75% | |
| Зигомикоз.85% | • Иммунодепрессивное средство, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования • Пациенты I мм с некомпетентностью (33,3%) | Боль в животе, вздутие живота, лихорадка, LGIB, диарея | 38% | Язва | Вся ободочная кишка, но преимущественно в правой части ободочной кишки | Операция с применением амфотерицина В + | 50% | ||
| Пневмоцистоз51 | Только один случай | • СПИД | Лихорадка, диарея% 13133 | Вся толстая кишка | Пентамидин | 100% | |||
| Скедоспориоз52 | Только один случай | • После трансплантации печени, иммунодепрессанты | Диарея, толстая кишка | 9013 | % Амфотерицин В100% |
Таблица 2
Сводные данные о зарегистрированных случаях пенициллиоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распределение по толстой кишке | Эндоскопические данные | Лечение и исход | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Цанг и др., 36 1988 | 58 / мужчина | Гонконг | Кортикостероиды 3 | гепаталиния | Гепаталий | Гепаталий | Гепаталия | Да | Нисходящая ободочная кишка | Язва | Амфотерицин B → умер | |
| Leung et al, 37 1996 | 32 / мужской | Гонконг | СПИД | Лихорадка, понос 9013, ночь Острая | Нет | Слепая кишка, поперечная и нисходящая ободочная кишка | Язва 90 134 | Амфотерицин В и итраконазол → улучшение | ||||
| Ко и др., 38 1999 | 52 / мужчина | Тайвань | СПИД | Лихорадка, диарея, анемия, боли в животе | 3 недели | Язва | Амфотерицин В и итраконазол → улучшение | |||||
| Ко и др., 38 1999 | 30 / мужчина | Тайвань | СПИД | Диспепсия, диарея, лихорадка, боль в животе3 9013, потеря веса 3 90 месяцев, LGIB4 | № | Слепая кишка, восходящая и поперечная ободочная кишка | Язва | Амфотерицин В и итраконазол → улучшенные |
Таблица 3
Сводные данные по зарегистрированным случаям аспергиллеза толстой кишки7
Сноски
Раскрытие информации
Автор сообщает об отсутствии конфликта интересов в этой работе.
Ссылки
1. Анаисси Э.Дж., Макгиннис М.Р., Пфаллер М.А., редакторы. Клиническая микология. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 2003. [Google Scholar] 2. Отклоняет редакторов WE, Pappas PG, Sobel JD. Клиническая микология. Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 2003. [Google Scholar] 3. Хоспенталь Д.Р., Ринальди М.Г., редакторы. Диагностика и лечение микозов человека. Тотова, Нью-Джерси: Humana Press; 2008. [Google Scholar] 5. Шмитт С.Л., Векснер С.Д. Бактериальный, грибковый, паразитарный и вирусный колит. Surg Clin North Am.1993. 73 (5): 1055–1062. [PubMed] [Google Scholar] 6. Lima AAM, Guerrant RL. Воспалительные энтериты. В: Манделл Г.Л., Беннетт Дж. Э., Долин Р., редакторы. Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета. 7-е изд. Филадельфия, Пенсильвания: Черчилль Ливингстон Эльзевьер; 2009. С. 1389–1398. [Google Scholar] 7. Wilcox CM. Желудочно-кишечные последствия заражения вирусом иммунодефицита человека. В: Фельдман М., Фридман Л.С., Брандт Л.Дж., редакторы. Заболевания желудочно-кишечного тракта и печени Слейзенгера и Фордтрана.9 изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2010. С. 523–535. [Google Scholar] 8. Стилианос С., Форд К.А., Бенвенисти Эл, Харди М.А. Кровоизлияние в нижнюю часть желудочно-кишечного тракта у реципиентов почечного трансплантата. Arch Surg. 1988. 123: 739–744. [PubMed] [Google Scholar] 10. Jayagopal S, Cervia JS. Колит, вызванный Candida albicans, у больного СПИДом. Clin Infect Dis. 1992; 15: 555. [PubMed] [Google Scholar] 11. Куклакис Г., Докас С., Моливас Е., Вакианис П., Эфтимиу А. Кандидозный колит у мужчины среднего возраста, получающего постоянный гемодиализ.Eur J Gastroenterol Hepatol. 2001; 13: 735–736. [PubMed] [Google Scholar] 12. Китагава KH, Kalb RE. Лечение эфализумабом при кандидозном колите. J Am Acad Dermatol. 2008; 59 (приложение 5): S120 – S121. [PubMed] [Google Scholar] 13. Praneenararat S. Первый зарегистрированный случай инфекции толстой кишки, вызванной Candida tropicalis, и обзор литературы. Случай Реп Гастроэнтерол. 2014; 8: 199–205. [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Де Пау Б., Уолш Т.Дж., Доннелли Дж. П. и др. Пересмотренные определения инвазивного грибкового заболевания, разработанные Совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Консенсусной группы Национального института аллергии и инфекционных заболеваний по изучению микозов (EORTC / MSG).Clin Infect Dis. 2008; 46: 1813–1821. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Ascioglu S, Rex JH, de Pauw B, et al. Совместная группа по инвазивным грибковым инфекциям Европейской организации по исследованию и лечению рака. Группа по изучению микозов Национального института аллергии и инфекционных заболеваний. Определение оппортунистических инвазивных грибковых инфекций у пациентов с ослабленным иммунитетом, перенесших онкологические заболевания и трансплантацию гемопоэтических стволовых клеток: международный консенсус. Clin Infect Dis. 2002; 34: 7–14.[PubMed] [Google Scholar] 16. Сафдар А., Сингхал С., Мехта Дж. Клиническое значение выделения из крови не Candida грибков у пациентов, перенесших трансплантацию аллогенных гемопоэтических стволовых клеток высокого риска (1993–2001) Рак. 2004. 100: 2456–2461. [PubMed] [Google Scholar] 17. Контойяннис Д.П., Бодей Г.П., Ханна Х и др. Детерминанты исхода фузариоза в онкологическом центре третичного уровня: влияние восстановления нейтрофилов. Лимфома лейка. 2004. 45: 139–141. [PubMed] [Google Scholar] 18. Лионакис М.С., Бодей Г.П., Тарранд Дж.Дж., Раад II, Контойяннис Д.П.Значение положительных культур крови для появления сапрофитных плесневых грибов у онкологических больных. Clin Microbiol Infect. 2004; 10: 922–925. [PubMed] [Google Scholar] 19. Сафдар А., Родригес Дж., Ролстон К.В. и др. Комбинированная противогрибковая терапия высокими дозами каспофунгина у пациентов с гематологическими злокачественными новообразованиями и трансплантацией гемопоэтических стволовых клеток. Пересадка костного мозга. 2007. 39 (3): 157–164. [PubMed] [Google Scholar] 20. Каппелл М.С., Манделл В., Граймс М.М., Нью-ХК. Гистоплазмоз желудочно-кишечного тракта. Dig Dis Sci.1988. 33: 353–360. [PubMed] [Google Scholar] 21. Асси М., Маккинси Д.С., Дрикс М.Р. и др. Гистоплазмоз желудочно-кишечного тракта при синдроме приобретенного иммунодефицита: отчет о 18 случаях и обзор литературы. Диагностика Microbiol Infect Dis. 2006; 55: 195–201. [PubMed] [Google Scholar] 22. Lyon DT, Schubert TT, Mantia AG, Kaplan MH. Фикомикоз желудочно-кишечного тракта. Am J Gastroenterol. 1979. 72 (4): 379–394. [PubMed] [Google Scholar] 23. Ага Ф. П., Ли Х. Х., Боланд Ч. Р., Брэдли С.Ф. Мукормикома толстой кишки: ранняя диагностика и успешное лечение.AJR Am J Roentgenol. 1985; 145: 739–741. [PubMed] [Google Scholar] 24. Роден М.М., Заутис Т.Э., Бьюкенен В.Л. и др. Эпидемиология и исходы зигомикоза: обзор 929 зарегистрированных случаев. Clin Infect Dis. 2005; 41: 634–653. [PubMed] [Google Scholar] 25. Альмирудис Н.Г., Саттон Д.А., Линден П., Ринальди М.Г., Фунг Дж., Кусне С. Зигомикоз у реципиентов солидных трансплантатов в центре третичной трансплантации и обзор литературы. Am J Transplant. 2006; 6: 2365–2374. [PubMed] [Google Scholar] 26. Зельман С., О’Нил Р.Х., Плаут А.Диссеминированный висцеральный торулез без поражения нервной системы с клиническими проявлениями гранулоцитарного лейкоза. Am J Med. 1951; 11: 658–664. [PubMed] [Google Scholar] 28. Хатто Дж.О., Брайан С.С., Грин Флорида, Уайт СиДжей, Галлин Джи. Криптококкоз толстой кишки, напоминающий болезнь Крона, у пациента с синдромом рецидивирующей инфекции гипериммуноглобулинемии E. Гастроэнтерология. 1988. 94: 808–812. [PubMed] [Google Scholar] 29. Ван Калк М., Мотт С., Рикаерт Ф., Серрюйс Э., Адлер М., Вибран Дж. Криптококковая анальная язва у пациента со СПИДом.Am J Gastroenterol. 1988. 83: 1306–1308. [PubMed] [Google Scholar] 30. Дэйли Дж. С., Портер К. А., Чонг Ф. К., Робиллард Р. Дж.. Распространенная неменингеальная желудочно-кишечная криптококковая инфекция у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1990; 85: 1421–1424. [PubMed] [Google Scholar] 31. Bonacini M, Nussbaum J, Ahluwalia C. Поражение желудочно-кишечного тракта, печени и поджелудочной железы с Cryptococcus neoformans при СПИДе. J Clin Gastroenterol. 1990; 12: 295–297. [PubMed] [Google Scholar] 32. Вашингтон К., Готфрид М.Р., Уилсон М.Л.Желудочно-кишечный криптококкоз. Мод Pathol. 1991; 4: 707–711. [PubMed] [Google Scholar] 33. Мелато М., Горжи Н. Первичный кишечный криптококкоз, имитирующий аденоматозный полип у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1998; 93: 1592–1593. [PubMed] [Google Scholar] 34. Ло Дж. К., Амар Дж. Н., Кирби С. Д., Зетлер П. Дж., Эннс РА. Криптококковая инфекция толстой кишки. Gastrointest Endosc. 2007. 65: 525–526. [PubMed] [Google Scholar] 35. Сонг Дж. К., Ким С. К., Ким Е. С. и др. Случай криптококкоза толстой кишки. Корейский J Gastroenterol.2008. 52: 255–260. Корейский. [PubMed] [Google Scholar] 36. Цанг Д.Н., Чан Дж.К., Лау Ю.Т., Лим В., Цзе СН, Чан Н.К. Инфекция Penicillium marneffei: недиагностируемая болезнь? Гистопатология. 1988; 13: 311–318. [PubMed] [Google Scholar] 37. Леунг Р., Сунг Дж.Й., Чоу Дж., Лай С.К. Необычная причина лихорадки и диареи у больного СПИДом. Penicillium marneffei инфекция. Dig Dis Sci. 1996; 41: 1212–1215. [PubMed] [Google Scholar] 38. Ко CI, Hung CC, Chen MY, Hsueh PR, Hsiao CH, Wong JM. Эндоскопическая диагностика кишечного пенициллиоза marneffei: отчет о трех случаях и обзор литературы.Gastrointest Endosc. 1999. 50 (1): 111–114. [PubMed] [Google Scholar] 39. Kinder RB, Jourdan MH. Диссеминированный аспергиллез и кровоточащие язвы толстой кишки у пациента с трансплантатом почки. JR Soc Med. 1985. 78 (4): 338–339. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Соуза А.Б., Феррейра Г., Вейга Дж., Карвалью А. Клиническая картина: инфаркт кишечника из-за аспергиллеза. Ланцет. 2002; 359 (9302): 210. [PubMed] [Google Scholar] 41. Финн С., Бонд Дж., Маккарти Д., Шихан К., Куинн С. Ангиоинвазивный аспергиллез, проявляющийся как нейтропенический колит.Гистопатология. 2006. 49 (4): 440–441. [PubMed] [Google Scholar] 42. Андрес Л.А., Форд Р.Д., Уилкокс Р.М. Некротический колит, вызванный системным аспергиллезом у ожогового больного. J Burn Care Res. 2007. 28 (6): 918–921. [PubMed] [Google Scholar] 43. Мохайт У., Келл Дж., Хадж М.А. и др. Инвазивный аспергиллез, локализованный в толстой кишке, проявляется в виде токсичного мегаколона. Eur J Haematol. 2007. 78: 270–273. [PubMed] [Google Scholar] 44. Чхве С.Х., Чунг Дж. В., Чо СИ, Ким Би Джей, Квон Дж. Случай изолированного инвазивного аспергиллезного колита с гематохезией у пациента с раком толстой кишки, не страдающего нейтропенией.Кишечная печень. 2010. 4 (2): 274–277. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Chojniak R, Costa Vieira RA, Lopes A, et al. Кишечный паракокцидиоидомикоз, имитирующий рак толстой кишки. Rev Soc Bras Med Trop. 2000. 33: 309–312. [PubMed] [Google Scholar] 47. Коста Виейра РА, Лопес А, Оливейра Х.В. и др. Анальный паракокцидиоидомикоз: необычное проявление диссеминированного заболевания. Rev Soc Med Trop. 2001; 34: 583–586. [PubMed] [Google Scholar] 48. Браво Э.А., Зегарра А.Дж., Пискоя А. и др. Хроническая диарея и панколит, вызванные паракокцидиоидомикозом: клинический случай.История болезни Med. 2010; 2010: 140505. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Леон М., Алаве Дж., Бустаманте Б., Кок Дж., Готуццо Е., Сис С. Т-лимфотропный вирус 1 человека и паракокцидиоидомикоз: вероятная ассоциация в Латинской Америке. Clin Infect Dis. 2010. 51 (2): 250–251. [PubMed] [Google Scholar] 50. Бенард Г., Коста А.Н., Леоперсио А.П., Висентини А.П., Коно А., Шиканаи-Ясуда М.А. Хронический паракокцидиоидомикоз кишечника как поражение одного органа указывает на альтернативный патогенез микоза.Микопатология. 2013. 176 (5–6): 353–357. [PubMed] [Google Scholar] 51. Белломо А.Р., Перлман Д.К., Камински Д.Л., Бреттхольц Е.М., Сарлин Дж. Пневмоцистный колит у больного с синдромом приобретенного иммунодефицита. Am J Gastroenterol. 1992. 87 (6): 759–761. [PubMed] [Google Scholar] 52. Лин Д., Камили К., Лай С., Мушер Д.М., Хэмилл Р. Церебральная инфекция Scedosporium apiospermum, проявляющаяся кишечными проявлениями. Инфекционное заболевание. 2013. 41 (3): 723–726. [PubMed] [Google Scholar] 53. Горбач С.Л., Нахас Л., Лернер П.И., Вайнштейн Л.Исследования микрофлоры кишечника. I. Влияние диеты, возраста и периодического отбора проб на количество фекальных микроорганизмов у человека. Гастроэнтерология. 1967; 53: 845–855. [PubMed] [Google Scholar] 54. Коэн Р., Рот Ф.Дж., Дельгадо Э., Ахерн Д.Г., Калсер М.Х. Грибковая флора нормального тонкого и толстого кишечника человека. N Engl J Med. 1969; 280: 638–641. [PubMed] [Google Scholar] 55. Деннинг DW. Инвазивный аспергиллез. Clin Infect Dis. 1998; 26: 781–803. [PubMed] [Google Scholar] 56. Марр К.А., Паттерсон Т., Деннинг Д. Аспергиллез.Патогенез, клинические проявления и терапия. Заражение Dis Clin North Am. 2002; 16: 875–894. vi. [PubMed] [Google Scholar] 57. Смулиан А.Г., Кили С.П., Сункин С.М., Стрингер-младший. Генетическая и антигенная изменчивость организмов Pneumocystis carinii: инструменты для изучения эпидемиологии и патогенеза инфекции. J Lab Clin Med. 1997. 130 (5): 461–468. [PubMed] [Google Scholar] 58. Дейли К.Р., Кох Дж., Левин Л., Уолцер П.Д. Иммуноферментный анализ и серологические ответы на Pneumocystis jiroveci. Emerg Infect Dis.2004. 10 (5): 848–854. [Бесплатная статья PMC] [PubMed] [Google Scholar] 59. Chayakulkeeree M, Perfect JR. Криптококкоз. Заражение Dis Clin North Am. 2006; 20: 507–544. [PubMed] [Google Scholar] 61. Саммербелл Р.К., Крайден С., Кейн Дж. Горшечные растения в больницах как резервуары патогенных грибов. Микопатология. 1989; 106: 13–22. [PubMed] [Google Scholar] 62. Хоффманн С., Доллив С., Грюнберг С. и др. Археи и грибы микробиома кишечника человека: корреляция с диетой и бактериальными жителями. PLoS One. 2013; 8 (6): e66019.[Бесплатная статья PMC] [PubMed] [Google Scholar] 63. Контояннис Д.П., Льюис Р.Э. Инвазивный зигомикоз: обновленная информация о патогенезе, клинических проявлениях и лечении. Заражение Dis Clin North Am. 2006; 20: 581–607. [PubMed] [Google Scholar] 64. Гудвин Р.А., младший, Шапиро Дж. Л., Турман Г. Х., Турман СС, Дес През Р. М.. Диссеминированный гистоплазмоз: клинико-патологические корреляции. Медицина (Балтимор) 1980; 59: 1–33. [PubMed] [Google Scholar] 65. Пшеница LJ, Slama TG, Eitzen HE, Kohler RB, French ML, Biesecker JL. Крупная городская вспышка гистоплазмоза: клинические особенности.Ann Intern Med. 1981; 94: 331–337. [PubMed] [Google Scholar] 66. Negroni R. Paracoccidioidomycosis (южноамериканский бластомикоз, микоз Лутца) Int J Dermatol. 1993; 32: 847–859. [PubMed] [Google Scholar] 67. Blotta MH, Mamoni RL, Oliveira SJ, et al. Эндемичные регионы паракокцидиоидомикоза в Бразилии: клиническое и эпидемиологическое исследование 584 случаев в юго-восточном регионе. Am J Trop Med Hyg. 1999. 61: 390–394. [PubMed] [Google Scholar] 68. Суппаратпиньо К., Кхамван С., Баосунг В., Нельсон К.Э., Сирисантана Т.Распространенная инфекция Penicillium marneffei в Юго-Восточной Азии. Ланцет. 1994; 344: 110–113. [PubMed] [Google Scholar] 69. Вонг К.Х., Ли С.С., Ло Ю.С. и др. Профиль оппортунистических инфекций среди людей, инфицированных ВИЧ-1, в Гонконге. Чжунхуа И Сюэ За Чжи (Тайбэй) 1995; 55: 127–136. [PubMed] [Google Scholar] 70. Duong TA. Инфекция, вызванная Penicillium marneffei, новым патогеном: обзор 155 зарегистрированных случаев. Clin Infect Dis. 1996; 23: 125–130. [PubMed] [Google Scholar] 71. Вонг К.Х., Ли СС. Сравнение первой и второй сотни случаев СПИДа в Гонконге.Singapore Med J. 1998; 39: 236–240. [PubMed] [Google Scholar] 72. Peña CE. Глубокие грибковые инфекции в Колумбии. Клинико-патологическое исследование 162 случаев. Am J Clin Pathol. 1967. 47 (4): 505–520. [PubMed] [Google Scholar] 73. Эрас П., Гольдштейн М.Дж., Шерлок П. Кандидозная инфекция желудочно-кишечного тракта. Медицина (Балтимор) 1972; 51: 367–379. [PubMed] [Google Scholar] 74. Молодой Р.С., Беннетт Дж. Э., Фогель С. Л., Карбон П. П., ДеВита В. Т.. Аспергиллез. Спектр заболевания у 98 больных. Медицина (Балтимор) 1970; 49: 147–173.[PubMed] [Google Scholar] 75. Де Лука А., Зеланте Т., Д’Анджело С. и др. IL-22 определяет новый иммунный путь устойчивости к противогрибковым препаратам. Mucosal Immunol. 2010. 3 (4): 361–373. [PubMed] [Google Scholar] 76. Андерхилл Д.М., Илиев И.Д. Микобиота: взаимодействие между комменсальными грибами и иммунной системой хозяина. Nat Rev Immunol. 2014. 14 (6): 405–416. [Бесплатная статья PMC] [PubMed] [Google Scholar]Грибковая инфекция толстой кишки
Clin Exp Gastroenterol. 2014; 7: 415–426.
Сурат Праниенарарат
Отделение гастроэнтерологии, Медицинский факультет, Университет принца Сонгкла, Сонгкхла, Таиланд
Отделение гастроэнтерологии, Медицинский факультет, Университет Принца Сонгкла, Сонгкхла, Таиланд
Переписка: Сурат Праненарарат, Отделение гастроэнтерологии, Кафедра медицины, Университет Принца Сонгкла, 15 Kanjanavanich Road, Hat-Yai, Songkhla, Thailand,, Tel +66 80 441 0174, Email moc.Авторские права © 2014 Praneenararat. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения Dove Medical Press Limited при условии правильной атрибуции работы. Эта статья цитируется в других статьях PMC.Abstract
Грибы — патогены, которые обычно поражают пациентов с ослабленным иммунитетом и могут поражать любые органы тела, включая толстую кишку.Однако в литературе содержится ограниченное количество подробностей об инфекциях толстой кишки, вызванных грибками. Эта статья представляет собой подробный обзор доступной информации о грибах, которые могут вызывать инфекции толстой кишки. В нем используется сравнительный стиль, поэтому его выводы могут быть доступны для клинического применения.
Ключевые слова: грибок, колит, толстая кишка, толстая кишка
Введение
Грибы являются патогенами, которые обычно инфицируют пациентов с ослабленным иммунитетом. В настоящее время частота этих патогенов в причинах заболевания постепенно увеличивается в результате более широкого использования иммунодепрессантов, химиотерапии и трансплантации, а также инфекций, вызванных вирусом иммунодефицита человека.Грибковые инфекции могут поражать любой орган, в том числе толстую кишку.1–3 Тем не менее, в литературе доступны лишь ограниченные сведения об инфекции толстой кишки, вызванной грибами.4,5 Эта статья представляет собой интенсивный обзор исследований грибковой инфекции толстой кишки. в кратком сравнительном стиле для удобного клинического применения.
Методы
Автор инициировал обзор с исследования грибков, которые могут вызывать инфекцию толстой кишки, в MEDLINE, в основных учебниках и существующей исследовательской литературе, в которой рассматриваются грибковые инфекции толстой кишки.4–7 В MEDLINE автор использовал ключевые слова из двух групп. Первая группа состояла из названий грибов или инфекций, связанных с грибами, включая «аспергиллез», « Aspergillus », « Blastomyces », «бластомикоз», « Candida », «кандидоз», «хромобластомикоз». , « Cladophialophora », « Coccidioides », «кокцидиоидомикоз», «криптококкоз», « Cryptococcus », «дерматофит», «дерматофитоз», « Epidermophyton », «eumycetoma», «eumycetoma», , «Фузариоз», « Fusarium », « Histoplasma », «гистоплазмоз», « Madurella », « Microsporum », «мукормикоз», « Paracoccidioides », «паракокцидиоидомикоз». , « Penicillium », «феогифомикоз», « Pneumocystis », «пневмоцистоз», «скедоспориоз», « Scedosporium », « Sporothrix », «споротрихоз», « Trichophyton », « Trichophyton » »,« трихоспороноз », « Zygomycetes » и «зигомикоз».Вторая группа ключевых слов состояла из слов, связанных с локализацией заболевания, которое мы рассматривали, включая «колит», «толстая кишка», «толстая кишка», «энтероколит», «толстая кишка», «толстая кишка» и «толстая кишка». . Наконец, было установлено, что инфекции толстой кишки, которые, как сообщалось, были вызваны грибами, были аспергиллезом, кандидозом, криптококкозом, гистоплазмозом, паракокцидиоидомикозом, пенициллиозом, пневмоцистозом, скедоспориозом и зигомикозом. Подробная информация о каждом грибке была дополнительно рассмотрена из статей, найденных в MEDLINE, с использованием ключевых слов, как описано выше, цитат из этих статей и ссылок в основных учебниках.В MEDLINE были включены все типы статей, включая обзоры, серии случаев, истории болезни, редакционные статьи и письма до 30 июня 2014 г. Первоначально было найдено 124 статьи. Были отобраны только статьи, которые были на английском языке или имели аннотацию на английском языке с необходимыми подробностями, которые имели определенный диагноз грибковой инфекции толстой кишки, включая прямую визуализацию типичного грибка или положительную культуру грибка в образцах толстой кишки. Случаи кандидоза, который считается нормальным комменсалом желудочно-кишечного тракта человека, также должны соответствовать одному из следующих критериев в соответствии с принятыми отчетами о случаях и пересмотренной совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Национальным институтом. критериев группы исследования аллергии и инфекционных микозов: проникновение в глубокие ткани толстой кишки или положительный результат на Candida spp.в поверхностной слизистой оболочке с положительным посевом крови или положительным Candida spp. в поверхностной слизистой оболочке с очевидностью ответа на лечение8–14 Candida spp. только на поверхностной слизистой оболочке без положительного посева крови или свидетельств ответа на лечение были исключены. Распространение было определено как поражение двух или более несмежных органов15–19
В настоящее время уже рассмотрены гистоплазмоз, 20,21 кандидоз 13 и зигомикоз22–25. В случаях других грибковых инфекций, включая криптококкоз, пенициллиоз 26–35, аспергиллез 36–38, 9,39–44 и паракокцидиоидомикоз 45–50, автор обобщил отчеты о случаях, как показано в -.Был опубликован только один отчет о каждом случае пневмоцистоза51 и скедоспориоза.52
Таблица 1
Сводные данные о зарегистрированных случаях криптококкоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распространение в толстой кишке | Эндоскопическое исследование | Лечение и исход | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Zelman et al. | ХМЛ, химиотерапия | Не упоминается | Не упоминается | Да | Не упоминается | Язва | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Унат и др., 27 1960 | 16 / мужчина | Турция | Турция | Диарея, боли в животе, LGIB | 8 лет | Нет | Спуститься ободочной кишки | Масса | Хирургия и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hutto et al, 28 1988 | 29 / женщина | США | Синдром Джобса | Абсцесс прямой кишки | 1 год | 1 год | восходящая ободочная кишка | Стриктура восходящей ободочной кишки и периректальный абсцесс | Операция и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van Calck et al, 29 1988 | 47 / мужской | Бельгия | СПИД | Hematochezia | Hematochezia, лихорадка | , лихорадка не упоминаетсяДа | Периректум | Периректальный абсцесс | Хирургия, амфотерицин B и флуцитозин → улучшенное состояние | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Daly et al, 30 1990 | 63 / мужской | USA | Хортностерэктомия, корнеэктомия , недомогание | 7 дней | Есть | Поперечная ободочная кишка | Масса | Амфот эрицин B и флуцитозин → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bonacini et al, 31 1990 | 31 / мужчина | США | AIDS | Hemiplegia, эпилепсия | Не упоминается | Да | Не упоминается | B и флуцитозин → умер||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 38 / мужчина | США | СПИД | Эпигастральная боль, одинофагия | 3 месяца | Да | Противогрибковая терапия | 3 → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 24 / мужчина | США | Болезнь Ходжкина | Не упоминается | Не упоминается | Да | Не упоминается | Не упоминается | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 31 / женщина | США | СПИД | Не упоминается d | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 51 / мужчина | США | Кортикостероиды | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умерло | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Мелато и Горджи, 33 1998 | 84 / женщина | Италия | Нет | Ректальное кровотечение Нет | Острое | Острое толстая кишка | Полип | Полипэктомия → улучшенная | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Law et al, 34 2007 | 40 / мужчина | Канада | AIDS | Боль в животе, диарея, дисфагия, лихорадка | 6 недель Слева | 6 недель толстая кишка | Множественные эритематозные, выпуклые, пятнистые поражения | Амфотерицин B и флуцитозин → улучшенный | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сонг и др., 35 2008 | 27 / женщина | Корея | Нет | Мелена | Не упоминается | Нет | Проксимальный отдел восходящей ободочной кишки | Масса | Амфотерицин В и флуконазин B → | 9018 с улучшенным эффектом Таблица 4
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность | Продолжительность | Распространение | Распределение по толстой кишке | Эндоскопическое исследование | Лечение и результат | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Penna, 45 1979 | 8 / женщина | Бразилия | Нет | Диарея, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность | 4 года | Нет | Вся толстая кишка | Стриктура, язва | Ко-тримоксазол → улучшение | |||||||||||||||||||||||
| Chojniak et al, 46 2000 | 57 / не упоминается | Бразилия | Нет | Боль в животе, диарея, потеря веса 3 | 2 года | Слепая кишка | Масса | Кетоконазол → не упоминается | ||||||||||||||||||||||||
| Коста Виейра и др., 47 2001 | 60 / мужской | Бразилия | Нет | Лихорадка, перианальные узелки, дисфония, кашель13 лет | Да | Поперечная и нисходящая толстая кишка | Язва | Сульфадиазин → улучшение | ||||||||||||||||||||||||
| Браво и др., 48 2010 | 39 / женщина | Перу | Нет | диарея | 2 месяца | Да | Вся толстая кишка | Язва | Амфотерицин B → умер | |||||||||||||||||||||||
| Леон и др., 49 2 010 | 34 / мужчина | Перу | Нет | Диарея, язвы во рту, одинофагия, похудание, кашель | 18 месяцев | Да | Вся толстая кишка | Язва | Амфтозол | Амфтозол | Леон и др., 49 2010 | 40 / женщина | Перу | Нет | Диарея, похудание, гепатомегалия | 1 год | Да | Не упоминается | Не упоминается | Amphoteric | Benard et al, 50 2013 | 56 / женщина | Бразилия | Нет | Нет (колоноскопия для проверки) | Неизвестно | Нет | Поперечная ободочная кишка | Полип | Итраконазол | 58 / женщина | Бразилия | Нет | Диарея, потеря веса, лихорадка | 6 месяцев 9 0134 | Нет | Вся толстая кишка | Язва | Итраконазол → улучшенный |
Эпидемиология
Candida spp.являются нормальными комменсалами желудочно-кишечного тракта, 53,54, тогда как Aspergillus spp. и Pneumocystis spp. распространены повсеместно55–58 и являются причиной грибковых инфекций во всем мире. Cryptococcus spp. и Scedosporium spp. являются эндемическими микозами, которые также имеют распространение по всему миру. Cryptococcus spp. были изолированы из помета голубей 59, а Scedosporium spp. были обнаружены в приливных отмелях, болотах, прудах, навозе и почве.60,61 Aspergillus spp. и Cryptococcus spp. также могут быть обнаружены как компонент микобиоты толстой кишки человека.62
Zygomycetes можно разделить на два отряда: Mucorales и Entomophthorales. Mucorales — эндемичные грибы, встречающиеся во всем мире в органических субстратах, включая хлеб, фрукты, растительные вещества, почву, компост и экскременты животных.63 Histoplasma spp., Entomophthorales, Paracoccidioides spp. И Penicillium spp. эндемичные микозы, выделенные из почвы в ряде регионов мира.63–71 Histoplasma spp. обнаружены в почве, обогащенной пометом летучих мышей, кур и дроздов.64,65 Entomophthorales можно разделить на Conidiobolus spp. и Basidiobolus spp. и находятся в почве некоторых тропических регионов, особенно Африки, Южной Америки, Центральной Америки и Азии63. Paracoccidioides spp. ограничены почвой в странах Центральной и Южной Америки между 23 ° северной широты (юг Мексики) и 34,5 ° северной широты (Аргентина и Уругвай).Эти районы обладают уникальными экологическими особенностями, так как представляют собой тропические и субтропические леса с умеренными температурами и высокой влажностью.66,67 Penicillium spp. также изолированы от почвы в определенных областях, включая Юго-Восточную Азию, южный Китай (Гуанси), Гонконг и Индию.68–71 Эпидемиологические данные суммированы в.
Таблица 5
Эпидемиология грибков, которые могут вызывать инфекцию толстой кишки
| Грибки | Эпидемиология |
|---|---|
| Aspergillus spp., 55,56 Candida spp., 53,54 Криптококк видов, 59 Histoplasma spp., 64,65 Mucorales, 63 Pneumocystis виды, 57,58 Scedosporium spp.60,61 | Во всем мире |
| Entomophthorales63 | Тропические зоны в Африке, Южной Америке, Центральной Америке и Азии |
| Paracoccidioides spp.66,67 | странах Южной и Центральной Америки , особенно в Бразилии, Колумбии, Венесуэле и Аргентине|
| Penicillium spp.68–71 | Юго-Восточная Азия, южный Китай (Гуанси), Гонконг и Индия |
Распространенность поражения толстой кишки
Степень поражения толстой кишки грибковыми инфекциями варьируется в зависимости от типа грибка, как подробно описано в. Паракокцидиоидомикоз и гистоплазмоз являются наиболее распространенными инфекциями толстой кишки, вызываемыми грибами, с распространенностью 29% 72 и 28% 20 соответственно. Напротив, пенициллиоз, зигомикоз, пневмоцистоз и скедоспориоз редко инфильтрируют толстую кишку, при этом пенициллиоз и зигомикоз встречаются в 1.9% 68 и 0,85% инфекций толстой кишки 25 соответственно. И пневмоцистоз, и скедоспориоз известны только из одного сообщения о клиническом случае.51,52 За исключением ротоглоточного кандидоза, толстая кишка является третьим наиболее частым желудочно-кишечным органом, вовлеченным в кандидоз после пищевода и желудка. Ободочная кишка участвует в 20% случаев кандидоза желудочно-кишечного тракта.73 Криптококкоз толстой кишки является наиболее частым желудочно-кишечным проявлением диссеминированного или легочного криптококкоза с распространенностью около 17%.32
Таблица 6
Распространенность поражения толстой кишки при каждой грибковой инфекции
| Грибковые инфекции | Распространенность поражения толстой кишки | Комментарии | ||
|---|---|---|---|---|
| Паракокцидиоидомикоз3 | ||||
| Гистоплазмоз20 | 28% | |||
| Кандидоз73 | 20% желудочно-кишечного кандидоза (исключая орофарингеальный кандидоз) или легочный криптококкоз | |||
| Аспергиллез74 | 9.2% | |||
| Пенициллиоз68 | 1,9% | Всего четыре случая | ||
| Зигомикоз25 | 0,85% | |||
| 902 Нет данных | Только один случай |
Факторы риска
Криптококкоз толстой кишки и зигомикоз часто возникают у хозяев с ослабленным иммунитетом, встречаясь в 77% 26–35 и 67% 22 инфекциях соответственно, в то время как кандидоз толстой кишки, 13 пенициллиоз, 36– 38 и аспергиллез9,39–44 встречаются исключительно у хозяев с ослабленным иммунитетом.Факторами риска этих инфекций являются злокачественные новообразования, прием иммунодепрессантов, химиотерапия, нейтропения, СПИД, почечная недостаточность, спленэктомия, синдром Джоба, цирроз печени, недоедание и сахарный диабет; тем не менее, большинство пациентов с пенициллиозом толстой кишки обычно болеют СПИДом.37,38 Также были сообщения о случаях пневмоцистоза и скедоспориоза толстой кишки у пациентов с ослабленным иммунитетом, больных СПИДом и после трансплантации печени, соответственно.51,52 При паракокцидиоидомикозе толстой кишки и гистоплазмозе нет необходимости факторы риска присутствуют.20,21,45–50 Как показано на фиг.4, мужчины преобладают почти во всех грибковых инфекциях, за исключением кандидоза толстой кишки, аспергиллеза и паракокцидиоидомикоза. Более высокая частота грибковых инфекций у мужчин может быть объяснена их более интенсивным воздействием на места обитания эндемичных грибов во время работы67. При кандидозе толстой кишки предпочтения по признаку пола нет, поскольку Candida spp. нормальные комменсалы кишечника человека.13,53,54 Aspergillus spp. распространены повсеместно, поэтому секс также не является фактором риска заражения.9,39–44,55,56 Хотя паракокцидиоидомикоз обычно встречается у мужчин, среди паракокцидиоидомикоза толстой кишки преобладают 67 женщин. 45–50 Автор предполагает, что это может быть вызвано предвзятостью в сообщениях.
Таблица 7
Факторы риска грибковых инфекций толстой кишки
| Грибковые инфекции | Иммунокомпетентные | С ослабленным иммунитетом | Факторы риска | Мужчины | Комментарии | 50 | Мужской | Комментарии | 0% | — | 29% |
|---|---|---|---|---|---|---|---|---|
| Гистоплазмоз20,21 | 81% | 19% | Злокачественные новообразования, иммунодепрессанты, СПИД, синдром Джоба3 – СД | % | ||||
| Кандидоз 13 | 0% | 100% | Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, ESRD | 43% | ||||
| СПИД, иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз печени | 64% | |||||||
| Аспергиллез9,39–44 | 0% | 100% злокачественные новообразования | DM, ожог33% | |||||
| Пенициллиоз 36–38 | 0% | 100% | СПИД (75%), иммунодепрессанты | 100% | ,24 | |||
| 67% | Иммунодепрессанты, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования | 65% | Пневмоцистоз51 | 0% | 100% | СПИД | 100% | Только один случай |
| Scedosporiosis52 | 0% | 100% | 100 | 100% | трансплантация печени | Только один случай |
Иммунитет и инфекция толстой кишки, вызванная грибами
Иммунный ответ хозяина на грибы может играть важную роль в патогенезе инфекции толстой кишки, вызванной грибами, особенно организмами, которые являются частью микробиоты.75,76 Обычно клетки врожденного иммунитета имеют мембраносвязанные и растворимые рецепторы для уничтожения грибов. Связанные с мембраной рецепторы, такие как лектин, толл-подобный поглотитель и рецепторы комплемента, могут обнаруживать грибы или грибковые продукты, а затем активировать фагоцитоз и респираторный взрыв. Факторы транскрипции, которые могут индуцировать провоспалительные цитокины и хемокины, также активируются мембраносвязанными рецепторами. Растворимые рецепторы могут дополнительно активировать комплементы и опсонизировать грибы до рецепторов комплемента. Наконец, T-хелперы (Th) 1 и 17 запускаются и продуцируют другие цитокины, включая интерлейкин (IL) -17A, IL-17F и IL-22 для адаптивного иммунитета.Как врожденная, так и адаптивная иммунные системы защищают хозяина от грибов.76
Есть некоторые свидетельства того, что ослабленный иммунитет может усиливать инфекцию толстой кишки. Было продемонстрировано, что IL-22, который продуцируется врожденными клетками и регулируется IL-23, активирует воспалительные клетки и, таким образом, контролирует начальный рост грибков.75 Дефектные пути IL-23 и IL-22 увеличивают грибковую нагрузку в желудочно-кишечном тракте; тем не менее, клетки Th2 предотвращают распространение грибов. Клетки Th27 играют важную роль в адаптивных иммунных ответах, хотя их нарушение приводит к снижению устойчивости к поздней грибковой инфекции.Дефицит рецептора А IL-17 снижает активацию Th2, тем самым снижая устойчивость к грибам. 75 Таким образом, иммуносупрессивный статус является одним из основных факторов, предрасполагающих к инфекции толстой кишки, вызываемой грибами.
Клинические проявления
Инфекции толстой кишки, вызываемые грибами, имеют различные клинические проявления, как подробно описано в. За исключением зигомикоза и аспергиллеза, более половины пациентов с грибковыми инфекциями толстой кишки имеют диссеминированное заболевание. Боль в животе — наиболее частое проявление зигомикоза и аспергиллеза толстой кишки.9,22,24,39–44 Поражение глубоких тканей и ангиоинвазия, которые являются частыми патологическими проявлениями как при аспергиллезе, так и при зигомикозе, могут объяснить эти проявления.22,25,74 Диарея — симптом, который часто встречается при паракокцидиоидомикозе и кандидозе.13 , 45–50 Случаи гистоплазмоза толстой кишки и пенициллиоза включают диарею и боль в животе в качестве преобладающих симптомов.20,21,36–38 Периректальный абсцесс — специфическая особенность, которая обнаруживается только при криптококкозе толстой кишки. 28,29 Лихорадка — обычное явление при грибковых заболеваниях. инфекция толстой кишки, особенно у пациентов с пенициллиозом толстой кишки, у всех из которых наблюдается лихорадка.36–38 Например, случай пневмоцистоза толстой кишки проявился лихорадкой и диареей 51, тогда как случай скедоспориоза толстой кишки представил диарею и боль в животе.52
Таблица 8
Клинические проявления инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Распространение | Диарея | Боль в животе | LGIB | Ректальный абсцесс | Лихорадка | Комментарии | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| — | 50% | Бессимптомно у 12.5% | ||||||||||||
| Гистоплазмоз20,21 | 83% | 83% | 67% | 32% | — | 77% | — | |||||||
| 57 29% | 29% | — | 71% | — | ||||||||||
| Криптококкоз 26–35 | 71% (все пациенты с ослабленным иммунитетом) | 20% | 30% | 9013 40% 90% 30% | Бессимптомно у 20% | |||||||||
| Аспергиллез9,39–44 | 33% | 22% | 56% | 33% | — | 67% | —34 Peniciosis | 50% | 75% | 75% | 25% | — | 100% | — |
| Зигомикоз22,24 | 38% | 18% | % | – | 55% | — | ||||||||
| Пневмоцистоз51 | 100% | 100% | — | — | — | 100% | Только один случай | |||||||
| 100% | — | — | — | Только один случай |
Патологические данные и распределение
Язва толстой кишки является наиболее частой патологической находкой у пациентов с грибковой инфекцией толстой кишки, как показано на рис.Во всех случаях аспергиллеза толстой кишки и пенициллиоза есть язвы.36–38,74 Язва также обычно обнаруживается при гистоплазмозе толстой кишки, паракокцидиоидомикозе и кандидозе.21,45–50,73 Скедоспориоз толстой кишки также проявляется язвой52. криптококкоз толстой кишки представляет собой образование или полип как наиболее частую патологическую находку, в то время как криптококкоз толстой кишки может также проявляться атипичными патологическими проявлениями, включая абсцесс или стриктуру прямой кишки26–35. Другой инфекцией толстой кишки, которая может проявляться массой или полипом, является гистоплазмоз.21 В одном случае пневмоцистоза толстой кишки у пациента был отек кишечника.51
Таблица 9
Патологические данные об инфекциях толстого кишечника, вызванных грибами
| Грибковые инфекции | Язва | Воспаление слизистой оболочки / эрозия | Псевдемия | Масса / полип | Абсцесс прямой кишки | Стриктура | Комментарий | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз45–50 | 63% | — | — | Гистоплазмоз21 | 79% | 14% | — | 7% | — | — | |||||||||||
| Кандидоз73 | 64% | 14% | 14% | Из серии вскрытий | |||||||||||||||||
| Криптококкоз 26–35 | 11% | 11% | — | 44% | 22% | 11% | |||||||||||||||
| Аспергиллез74 | 100% (с некрозом 55.6%) | — | — | — | — | — | По результатам вскрытия | ||||||||||||||
| Пенициллиоз36–38 | 100% | — | — | — | |||||||||||||||||
| Зигомикоз22,25 | — | — | — | — | — | — | Язва, некроз, образовавшаяся масса, но количество пациентов не указано | 100% | — | — | — | — | Только один случай | ||||||||
| Сцедоспориоз52 | 100% | — | — | — | — |
Распространение инфекции толстой кишки, вызванной грибами, различается в зависимости от типа грибка, как показано в.Гистоплазмоз толстой кишки, зигомикоз и пенициллиоз, как правило, возникают в правой части толстой кишки.20,23,36–38 Область прямой кишки обычно поражается в случаях гистоплазмоза, кандидоза и зигомикоза.13,20,23 Криптококкоз толстой кишки — это заболевание. единственный грибок, который поражает периректальную область.28,29 Диффузное поражение толстой кишки обычно встречается при паракокцидиоидомикозе толстой кишки.45-50 Случаи как пневмоцистоза толстой кишки, так и скедоспориоза также представлены диффузными поражениями.51,52
Таблица 10
Распределения инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Слепая кишка или восходящая ободочная кишка или аппендикс | Поперечная ободочная кишка | Нисходящая или сигмовидная кишка | Прямая кишка | Надпочечная кишка | Вся толстая кишка Паракокцидиоидомикоз 45–50 | 13% | 25% | 13% | — | — | На 50% 20% | — | 20% | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Криптококкоз 27–30,32–35 | 30% | 10% | 40% | — | 20% | Аспергиллез9,39–44 | 33% | 22% | 22% | — | — | 22% | |||||
| Пенициллиоз36–38 | 503 | 9013% —— | — | ||||||||||||||
| Зигомикоз23 | 50% | — | 18% | 7% | — | 25% | 12334 | 9010— | — | — | — | — | 100% | Только один случай | |||
| Scedosporiosis52 | — | — | — | — | Только один случай
Ответ на лечение
Амфотерицин B является наиболее часто используемым препаратом для лечения почти всех грибковых инфекций толстой кишки, за исключением кандидоза и пневмоцистоза.Кандидоз толстой кишки реагирует на флуконазол или каспофунгин и имеет лучший прогноз, если противогрибковая терапия начата со 100% соблюдением режима.13 Хороший ответ был также достигнут при пневмоцистозе толстой кишки и скедоспориозе.51,52 Случай пневмоцистоза толстой кишки лечили пентамидином внутривенно из-за сульфаметоксазола -Триметоприм аллергия.51 Комбинированная противогрибковая терапия и хирургическое вмешательство использовались для лечения желудочно-кишечного зигомикоза и аспергиллеза, вызванного ангиоинвазией и инфарктом. Тем не менее прогноз в этих случаях все еще плохой, летальность составляет 50%.25,39,41,43,44 Выбор антибиотиков и ответ на лечение грибковых инфекций обобщены в.
Таблица 11
Ответ на лечение грибковых инфекций толстой кишки
| Грибковые инфекции | Лечение | Ответ на лечение | Комментарии | |||||
|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз4, 90 -13–50 амфотерицин В или итраконазол | 71% | |||||||
| Гистоплазмоз21 | Амфотерицин В | 77% | ||||||
| Кандидоз4 | Кандидоз4 | Амфотерицин В + флуцитозин ± хирургическое вмешательство | 67% | Ответ на лечение у иммунокомпетентных пациентов составил 100% | ||||
| Аспергиллез 39,41,43,44 | Амфотерицин В или каспофунгин 9013 | 90% хирургическое вмешательство | Пенициллиоз 36–38 | Амфот эрицин B | 75% | |||
| Зигомикоз25 | Амфотерицин B + хирургическое вмешательство | 50% | Комбинированное хирургическое вмешательство улучшило ответ на лечение | |||||
| Один пневмоцистоз3124 | Scedosporiosis52 | Амфотерицин B | 100% | Только один случай |
Заключение
Это первое исследование, в котором проводился интенсивный обзор литературы по грибковым инфекциям толстой кишки.Все содержание кратко изложено в. Он предоставляет основную информацию о причинах, проявлениях и лечении и может легко применяться в клинической практике. Врачи должны знать об этом грибковом образовании, когда у пациентов наблюдаются симптомы со стороны толстой кишки, особенно в случаях с ослабленным иммунитетом. Хотя сообщалось, что многие грибковые инфекции вызывают заболевания толстой кишки, включая аспергиллез, кандидоз, криптококкоз, гистоплазмоз, паракокцидиоидомикоз, пенициллиоз, пневмоцистоз, скедоспориоз и зигомикоз, знание эпидемиологических различий, факторов риска, клинических проявлений и патологических данных поможет врачам. для лучшей диагностики и лечения этих инфекций.Соответствующее лечение противогрибковыми препаратами определенно улучшает результаты; тем не менее, смертность от зигомикоза и аспергиллеза по-прежнему высока.
Таблица 12
Краткое описание инфекции толстой кишки, вызванной грибами
| Грибковые инфекции | Распространенность поражения толстой кишки | Факторы риска | Клинические проявления | Распространение | Распространение | Начальное лечение | |||
|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз 45–50,72 | 29% | • Эндемичная территория (Южная Америка) • Любой хозяин | Диарея, боль в животе, лихорадка | 50% язвы | Вся толстая кишка | Ко-тримоксазол, сульфадиазин, амфотерицин B или итраконазол | 71% | ||
| Гистоплазмоз20,21 | 28% | • Любой хозяин | лихорадка в животе, потеря веса в животе | 83% | Язва, отек слизистой оболочки | Вся толстая кишка, но преимущественно правая сторона e толстой и прямой кишки | Амфотерицин B | 77% | |
| Кандидоз13,73 | 20% кишечного кандидоза при вскрытии | • Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, пациенты с ESR | , боль в животе, лихорадка71% | Язва, зубной налет, эрозия | Вся толстая кишка | Флуконазол или каспофунгин | 100% | ||
| Криптококкоз26–35 | Криптококкоз иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз • Иммунокомпетентные пациенты (23%) | • Симптомы: LGIB, лихорадка, абдоминальная боль, диарея, ректальный абсцесс • 20% пациентов с бессимптомным иммунодефицитом | 71% (все пациенты) | Масса, периректальный абсцесс, язва толстой кишки, очаговые поражения, стриктура, полип | Вся толстая кишка | Амфо терицин B + флуцитозин ± хирургия | 60% | ||
| Аспергиллез9,39–44,74 | 9.2% | • Злокачественные новообразования, химиотерапия, нейтропения, иммунодепрессанты, сахарный диабет, ожог • Пациенты без иммунодефицита | Лихорадка, боль в животе, LGIB, диарея | 86% | Язва, некроз | 9013 Вся толстая кишка каспофунгин ± хирургия | 50% | ||
| Пенициллиоз36–38,68 | 1,9% | • Эндемичная территория (Юго-Восточная Азия, южный Китай, Гонконг и Индия) • В основном СПИД (75%) • Отсутствие иммунокомпетентности пациенты | Лихорадка, диарея, боль в животе, LGIB | 50% | Язва | Преимущественно в правой части ободочной и прямой кишки | Амфотерицин B | 75% | |
| Зигомикоз.85% | • Иммунодепрессивное средство, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования • Пациенты I мм с некомпетентностью (33,3%) | Боль в животе, вздутие живота, лихорадка, LGIB, диарея | 38% | Язва | Вся ободочная кишка, но преимущественно в правой части ободочной кишки | Операция с применением амфотерицина В + | 50% | ||
| Пневмоцистоз51 | Только один случай | • СПИД | Лихорадка, диарея% 13133 | Вся толстая кишка | Пентамидин | 100% | |||
| Скедоспориоз52 | Только один случай | • После трансплантации печени, иммунодепрессанты | Диарея, толстая кишка | 9013 | % Амфотерицин В100% |
Таблица 2
Сводные данные о зарегистрированных случаях пенициллиоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распределение по толстой кишке | Эндоскопические данные | Лечение и исход | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Цанг и др., 36 1988 | 58 / мужчина | Гонконг | Кортикостероиды 3 | гепаталиния | Гепаталий | Гепаталий | Гепаталия | Да | Нисходящая ободочная кишка | Язва | Амфотерицин B → умер | |
| Leung et al, 37 1996 | 32 / мужской | Гонконг | СПИД | Лихорадка, понос 9013, ночь Острая | Нет | Слепая кишка, поперечная и нисходящая ободочная кишка | Язва 90 134 | Амфотерицин В и итраконазол → улучшение | ||||
| Ко и др., 38 1999 | 52 / мужчина | Тайвань | СПИД | Лихорадка, диарея, анемия, боли в животе | 3 недели | Язва | Амфотерицин В и итраконазол → улучшение | |||||
| Ко и др., 38 1999 | 30 / мужчина | Тайвань | СПИД | Диспепсия, диарея, лихорадка, боль в животе3 9013, потеря веса 3 90 месяцев, LGIB4 | № | Слепая кишка, восходящая и поперечная ободочная кишка | Язва | Амфотерицин В и итраконазол → улучшенные |
Таблица 3
Сводные данные по зарегистрированным случаям аспергиллеза толстой кишки7
Сноски
Раскрытие информации
Автор сообщает об отсутствии конфликта интересов в этой работе.
Ссылки
1. Анаисси Э.Дж., Макгиннис М.Р., Пфаллер М.А., редакторы. Клиническая микология. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 2003. [Google Scholar] 2. Отклоняет редакторов WE, Pappas PG, Sobel JD. Клиническая микология. Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 2003. [Google Scholar] 3. Хоспенталь Д.Р., Ринальди М.Г., редакторы. Диагностика и лечение микозов человека. Тотова, Нью-Джерси: Humana Press; 2008. [Google Scholar] 5. Шмитт С.Л., Векснер С.Д. Бактериальный, грибковый, паразитарный и вирусный колит. Surg Clin North Am.1993. 73 (5): 1055–1062. [PubMed] [Google Scholar] 6. Lima AAM, Guerrant RL. Воспалительные энтериты. В: Манделл Г.Л., Беннетт Дж. Э., Долин Р., редакторы. Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета. 7-е изд. Филадельфия, Пенсильвания: Черчилль Ливингстон Эльзевьер; 2009. С. 1389–1398. [Google Scholar] 7. Wilcox CM. Желудочно-кишечные последствия заражения вирусом иммунодефицита человека. В: Фельдман М., Фридман Л.С., Брандт Л.Дж., редакторы. Заболевания желудочно-кишечного тракта и печени Слейзенгера и Фордтрана.9 изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2010. С. 523–535. [Google Scholar] 8. Стилианос С., Форд К.А., Бенвенисти Эл, Харди М.А. Кровоизлияние в нижнюю часть желудочно-кишечного тракта у реципиентов почечного трансплантата. Arch Surg. 1988. 123: 739–744. [PubMed] [Google Scholar] 10. Jayagopal S, Cervia JS. Колит, вызванный Candida albicans, у больного СПИДом. Clin Infect Dis. 1992; 15: 555. [PubMed] [Google Scholar] 11. Куклакис Г., Докас С., Моливас Е., Вакианис П., Эфтимиу А. Кандидозный колит у мужчины среднего возраста, получающего постоянный гемодиализ.Eur J Gastroenterol Hepatol. 2001; 13: 735–736. [PubMed] [Google Scholar] 12. Китагава KH, Kalb RE. Лечение эфализумабом при кандидозном колите. J Am Acad Dermatol. 2008; 59 (приложение 5): S120 – S121. [PubMed] [Google Scholar] 13. Praneenararat S. Первый зарегистрированный случай инфекции толстой кишки, вызванной Candida tropicalis, и обзор литературы. Случай Реп Гастроэнтерол. 2014; 8: 199–205. [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Де Пау Б., Уолш Т.Дж., Доннелли Дж. П. и др. Пересмотренные определения инвазивного грибкового заболевания, разработанные Совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Консенсусной группы Национального института аллергии и инфекционных заболеваний по изучению микозов (EORTC / MSG).Clin Infect Dis. 2008; 46: 1813–1821. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Ascioglu S, Rex JH, de Pauw B, et al. Совместная группа по инвазивным грибковым инфекциям Европейской организации по исследованию и лечению рака. Группа по изучению микозов Национального института аллергии и инфекционных заболеваний. Определение оппортунистических инвазивных грибковых инфекций у пациентов с ослабленным иммунитетом, перенесших онкологические заболевания и трансплантацию гемопоэтических стволовых клеток: международный консенсус. Clin Infect Dis. 2002; 34: 7–14.[PubMed] [Google Scholar] 16. Сафдар А., Сингхал С., Мехта Дж. Клиническое значение выделения из крови не Candida грибков у пациентов, перенесших трансплантацию аллогенных гемопоэтических стволовых клеток высокого риска (1993–2001) Рак. 2004. 100: 2456–2461. [PubMed] [Google Scholar] 17. Контойяннис Д.П., Бодей Г.П., Ханна Х и др. Детерминанты исхода фузариоза в онкологическом центре третичного уровня: влияние восстановления нейтрофилов. Лимфома лейка. 2004. 45: 139–141. [PubMed] [Google Scholar] 18. Лионакис М.С., Бодей Г.П., Тарранд Дж.Дж., Раад II, Контойяннис Д.П.Значение положительных культур крови для появления сапрофитных плесневых грибов у онкологических больных. Clin Microbiol Infect. 2004; 10: 922–925. [PubMed] [Google Scholar] 19. Сафдар А., Родригес Дж., Ролстон К.В. и др. Комбинированная противогрибковая терапия высокими дозами каспофунгина у пациентов с гематологическими злокачественными новообразованиями и трансплантацией гемопоэтических стволовых клеток. Пересадка костного мозга. 2007. 39 (3): 157–164. [PubMed] [Google Scholar] 20. Каппелл М.С., Манделл В., Граймс М.М., Нью-ХК. Гистоплазмоз желудочно-кишечного тракта. Dig Dis Sci.1988. 33: 353–360. [PubMed] [Google Scholar] 21. Асси М., Маккинси Д.С., Дрикс М.Р. и др. Гистоплазмоз желудочно-кишечного тракта при синдроме приобретенного иммунодефицита: отчет о 18 случаях и обзор литературы. Диагностика Microbiol Infect Dis. 2006; 55: 195–201. [PubMed] [Google Scholar] 22. Lyon DT, Schubert TT, Mantia AG, Kaplan MH. Фикомикоз желудочно-кишечного тракта. Am J Gastroenterol. 1979. 72 (4): 379–394. [PubMed] [Google Scholar] 23. Ага Ф. П., Ли Х. Х., Боланд Ч. Р., Брэдли С.Ф. Мукормикома толстой кишки: ранняя диагностика и успешное лечение.AJR Am J Roentgenol. 1985; 145: 739–741. [PubMed] [Google Scholar] 24. Роден М.М., Заутис Т.Э., Бьюкенен В.Л. и др. Эпидемиология и исходы зигомикоза: обзор 929 зарегистрированных случаев. Clin Infect Dis. 2005; 41: 634–653. [PubMed] [Google Scholar] 25. Альмирудис Н.Г., Саттон Д.А., Линден П., Ринальди М.Г., Фунг Дж., Кусне С. Зигомикоз у реципиентов солидных трансплантатов в центре третичной трансплантации и обзор литературы. Am J Transplant. 2006; 6: 2365–2374. [PubMed] [Google Scholar] 26. Зельман С., О’Нил Р.Х., Плаут А.Диссеминированный висцеральный торулез без поражения нервной системы с клиническими проявлениями гранулоцитарного лейкоза. Am J Med. 1951; 11: 658–664. [PubMed] [Google Scholar] 28. Хатто Дж.О., Брайан С.С., Грин Флорида, Уайт СиДжей, Галлин Джи. Криптококкоз толстой кишки, напоминающий болезнь Крона, у пациента с синдромом рецидивирующей инфекции гипериммуноглобулинемии E. Гастроэнтерология. 1988. 94: 808–812. [PubMed] [Google Scholar] 29. Ван Калк М., Мотт С., Рикаерт Ф., Серрюйс Э., Адлер М., Вибран Дж. Криптококковая анальная язва у пациента со СПИДом.Am J Gastroenterol. 1988. 83: 1306–1308. [PubMed] [Google Scholar] 30. Дэйли Дж. С., Портер К. А., Чонг Ф. К., Робиллард Р. Дж.. Распространенная неменингеальная желудочно-кишечная криптококковая инфекция у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1990; 85: 1421–1424. [PubMed] [Google Scholar] 31. Bonacini M, Nussbaum J, Ahluwalia C. Поражение желудочно-кишечного тракта, печени и поджелудочной железы с Cryptococcus neoformans при СПИДе. J Clin Gastroenterol. 1990; 12: 295–297. [PubMed] [Google Scholar] 32. Вашингтон К., Готфрид М.Р., Уилсон М.Л.Желудочно-кишечный криптококкоз. Мод Pathol. 1991; 4: 707–711. [PubMed] [Google Scholar] 33. Мелато М., Горжи Н. Первичный кишечный криптококкоз, имитирующий аденоматозный полип у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1998; 93: 1592–1593. [PubMed] [Google Scholar] 34. Ло Дж. К., Амар Дж. Н., Кирби С. Д., Зетлер П. Дж., Эннс РА. Криптококковая инфекция толстой кишки. Gastrointest Endosc. 2007. 65: 525–526. [PubMed] [Google Scholar] 35. Сонг Дж. К., Ким С. К., Ким Е. С. и др. Случай криптококкоза толстой кишки. Корейский J Gastroenterol.2008. 52: 255–260. Корейский. [PubMed] [Google Scholar] 36. Цанг Д.Н., Чан Дж.К., Лау Ю.Т., Лим В., Цзе СН, Чан Н.К. Инфекция Penicillium marneffei: недиагностируемая болезнь? Гистопатология. 1988; 13: 311–318. [PubMed] [Google Scholar] 37. Леунг Р., Сунг Дж.Й., Чоу Дж., Лай С.К. Необычная причина лихорадки и диареи у больного СПИДом. Penicillium marneffei инфекция. Dig Dis Sci. 1996; 41: 1212–1215. [PubMed] [Google Scholar] 38. Ко CI, Hung CC, Chen MY, Hsueh PR, Hsiao CH, Wong JM. Эндоскопическая диагностика кишечного пенициллиоза marneffei: отчет о трех случаях и обзор литературы.Gastrointest Endosc. 1999. 50 (1): 111–114. [PubMed] [Google Scholar] 39. Kinder RB, Jourdan MH. Диссеминированный аспергиллез и кровоточащие язвы толстой кишки у пациента с трансплантатом почки. JR Soc Med. 1985. 78 (4): 338–339. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Соуза А.Б., Феррейра Г., Вейга Дж., Карвалью А. Клиническая картина: инфаркт кишечника из-за аспергиллеза. Ланцет. 2002; 359 (9302): 210. [PubMed] [Google Scholar] 41. Финн С., Бонд Дж., Маккарти Д., Шихан К., Куинн С. Ангиоинвазивный аспергиллез, проявляющийся как нейтропенический колит.Гистопатология. 2006. 49 (4): 440–441. [PubMed] [Google Scholar] 42. Андрес Л.А., Форд Р.Д., Уилкокс Р.М. Некротический колит, вызванный системным аспергиллезом у ожогового больного. J Burn Care Res. 2007. 28 (6): 918–921. [PubMed] [Google Scholar] 43. Мохайт У., Келл Дж., Хадж М.А. и др. Инвазивный аспергиллез, локализованный в толстой кишке, проявляется в виде токсичного мегаколона. Eur J Haematol. 2007. 78: 270–273. [PubMed] [Google Scholar] 44. Чхве С.Х., Чунг Дж. В., Чо СИ, Ким Би Джей, Квон Дж. Случай изолированного инвазивного аспергиллезного колита с гематохезией у пациента с раком толстой кишки, не страдающего нейтропенией.Кишечная печень. 2010. 4 (2): 274–277. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Chojniak R, Costa Vieira RA, Lopes A, et al. Кишечный паракокцидиоидомикоз, имитирующий рак толстой кишки. Rev Soc Bras Med Trop. 2000. 33: 309–312. [PubMed] [Google Scholar] 47. Коста Виейра РА, Лопес А, Оливейра Х.В. и др. Анальный паракокцидиоидомикоз: необычное проявление диссеминированного заболевания. Rev Soc Med Trop. 2001; 34: 583–586. [PubMed] [Google Scholar] 48. Браво Э.А., Зегарра А.Дж., Пискоя А. и др. Хроническая диарея и панколит, вызванные паракокцидиоидомикозом: клинический случай.История болезни Med. 2010; 2010: 140505. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Леон М., Алаве Дж., Бустаманте Б., Кок Дж., Готуццо Е., Сис С. Т-лимфотропный вирус 1 человека и паракокцидиоидомикоз: вероятная ассоциация в Латинской Америке. Clin Infect Dis. 2010. 51 (2): 250–251. [PubMed] [Google Scholar] 50. Бенард Г., Коста А.Н., Леоперсио А.П., Висентини А.П., Коно А., Шиканаи-Ясуда М.А. Хронический паракокцидиоидомикоз кишечника как поражение одного органа указывает на альтернативный патогенез микоза.Микопатология. 2013. 176 (5–6): 353–357. [PubMed] [Google Scholar] 51. Белломо А.Р., Перлман Д.К., Камински Д.Л., Бреттхольц Е.М., Сарлин Дж. Пневмоцистный колит у больного с синдромом приобретенного иммунодефицита. Am J Gastroenterol. 1992. 87 (6): 759–761. [PubMed] [Google Scholar] 52. Лин Д., Камили К., Лай С., Мушер Д.М., Хэмилл Р. Церебральная инфекция Scedosporium apiospermum, проявляющаяся кишечными проявлениями. Инфекционное заболевание. 2013. 41 (3): 723–726. [PubMed] [Google Scholar] 53. Горбач С.Л., Нахас Л., Лернер П.И., Вайнштейн Л.Исследования микрофлоры кишечника. I. Влияние диеты, возраста и периодического отбора проб на количество фекальных микроорганизмов у человека. Гастроэнтерология. 1967; 53: 845–855. [PubMed] [Google Scholar] 54. Коэн Р., Рот Ф.Дж., Дельгадо Э., Ахерн Д.Г., Калсер М.Х. Грибковая флора нормального тонкого и толстого кишечника человека. N Engl J Med. 1969; 280: 638–641. [PubMed] [Google Scholar] 55. Деннинг DW. Инвазивный аспергиллез. Clin Infect Dis. 1998; 26: 781–803. [PubMed] [Google Scholar] 56. Марр К.А., Паттерсон Т., Деннинг Д. Аспергиллез.Патогенез, клинические проявления и терапия. Заражение Dis Clin North Am. 2002; 16: 875–894. vi. [PubMed] [Google Scholar] 57. Смулиан А.Г., Кили С.П., Сункин С.М., Стрингер-младший. Генетическая и антигенная изменчивость организмов Pneumocystis carinii: инструменты для изучения эпидемиологии и патогенеза инфекции. J Lab Clin Med. 1997. 130 (5): 461–468. [PubMed] [Google Scholar] 58. Дейли К.Р., Кох Дж., Левин Л., Уолцер П.Д. Иммуноферментный анализ и серологические ответы на Pneumocystis jiroveci. Emerg Infect Dis.2004. 10 (5): 848–854. [Бесплатная статья PMC] [PubMed] [Google Scholar] 59. Chayakulkeeree M, Perfect JR. Криптококкоз. Заражение Dis Clin North Am. 2006; 20: 507–544. [PubMed] [Google Scholar] 61. Саммербелл Р.К., Крайден С., Кейн Дж. Горшечные растения в больницах как резервуары патогенных грибов. Микопатология. 1989; 106: 13–22. [PubMed] [Google Scholar] 62. Хоффманн С., Доллив С., Грюнберг С. и др. Археи и грибы микробиома кишечника человека: корреляция с диетой и бактериальными жителями. PLoS One. 2013; 8 (6): e66019.[Бесплатная статья PMC] [PubMed] [Google Scholar] 63. Контояннис Д.П., Льюис Р.Э. Инвазивный зигомикоз: обновленная информация о патогенезе, клинических проявлениях и лечении. Заражение Dis Clin North Am. 2006; 20: 581–607. [PubMed] [Google Scholar] 64. Гудвин Р.А., младший, Шапиро Дж. Л., Турман Г. Х., Турман СС, Дес През Р. М.. Диссеминированный гистоплазмоз: клинико-патологические корреляции. Медицина (Балтимор) 1980; 59: 1–33. [PubMed] [Google Scholar] 65. Пшеница LJ, Slama TG, Eitzen HE, Kohler RB, French ML, Biesecker JL. Крупная городская вспышка гистоплазмоза: клинические особенности.Ann Intern Med. 1981; 94: 331–337. [PubMed] [Google Scholar] 66. Negroni R. Paracoccidioidomycosis (южноамериканский бластомикоз, микоз Лутца) Int J Dermatol. 1993; 32: 847–859. [PubMed] [Google Scholar] 67. Blotta MH, Mamoni RL, Oliveira SJ, et al. Эндемичные регионы паракокцидиоидомикоза в Бразилии: клиническое и эпидемиологическое исследование 584 случаев в юго-восточном регионе. Am J Trop Med Hyg. 1999. 61: 390–394. [PubMed] [Google Scholar] 68. Суппаратпиньо К., Кхамван С., Баосунг В., Нельсон К.Э., Сирисантана Т.Распространенная инфекция Penicillium marneffei в Юго-Восточной Азии. Ланцет. 1994; 344: 110–113. [PubMed] [Google Scholar] 69. Вонг К.Х., Ли С.С., Ло Ю.С. и др. Профиль оппортунистических инфекций среди людей, инфицированных ВИЧ-1, в Гонконге. Чжунхуа И Сюэ За Чжи (Тайбэй) 1995; 55: 127–136. [PubMed] [Google Scholar] 70. Duong TA. Инфекция, вызванная Penicillium marneffei, новым патогеном: обзор 155 зарегистрированных случаев. Clin Infect Dis. 1996; 23: 125–130. [PubMed] [Google Scholar] 71. Вонг К.Х., Ли СС. Сравнение первой и второй сотни случаев СПИДа в Гонконге.Singapore Med J. 1998; 39: 236–240. [PubMed] [Google Scholar] 72. Peña CE. Глубокие грибковые инфекции в Колумбии. Клинико-патологическое исследование 162 случаев. Am J Clin Pathol. 1967. 47 (4): 505–520. [PubMed] [Google Scholar] 73. Эрас П., Гольдштейн М.Дж., Шерлок П. Кандидозная инфекция желудочно-кишечного тракта. Медицина (Балтимор) 1972; 51: 367–379. [PubMed] [Google Scholar] 74. Молодой Р.С., Беннетт Дж. Э., Фогель С. Л., Карбон П. П., ДеВита В. Т.. Аспергиллез. Спектр заболевания у 98 больных. Медицина (Балтимор) 1970; 49: 147–173.[PubMed] [Google Scholar] 75. Де Лука А., Зеланте Т., Д’Анджело С. и др. IL-22 определяет новый иммунный путь устойчивости к противогрибковым препаратам. Mucosal Immunol. 2010. 3 (4): 361–373. [PubMed] [Google Scholar] 76. Андерхилл Д.М., Илиев И.Д. Микобиота: взаимодействие между комменсальными грибами и иммунной системой хозяина. Nat Rev Immunol. 2014. 14 (6): 405–416. [Бесплатная статья PMC] [PubMed] [Google Scholar]Грибковая инфекция толстой кишки
Clin Exp Gastroenterol. 2014; 7: 415–426.
Сурат Праниенарарат
Отделение гастроэнтерологии, Медицинский факультет, Университет принца Сонгкла, Сонгкхла, Таиланд
Отделение гастроэнтерологии, Медицинский факультет, Университет Принца Сонгкла, Сонгкхла, Таиланд
Переписка: Сурат Праненарарат, Отделение гастроэнтерологии, Кафедра медицины, Университет Принца Сонгкла, 15 Kanjanavanich Road, Hat-Yai, Songkhla, Thailand,, Tel +66 80 441 0174, Email moc.Авторские права © 2014 Praneenararat. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения Dove Medical Press Limited при условии правильной атрибуции работы. Эта статья цитируется в других статьях PMC.Abstract
Грибы — патогены, которые обычно поражают пациентов с ослабленным иммунитетом и могут поражать любые органы тела, включая толстую кишку.Однако в литературе содержится ограниченное количество подробностей об инфекциях толстой кишки, вызванных грибками. Эта статья представляет собой подробный обзор доступной информации о грибах, которые могут вызывать инфекции толстой кишки. В нем используется сравнительный стиль, поэтому его выводы могут быть доступны для клинического применения.
Ключевые слова: грибок, колит, толстая кишка, толстая кишка
Введение
Грибы являются патогенами, которые обычно инфицируют пациентов с ослабленным иммунитетом. В настоящее время частота этих патогенов в причинах заболевания постепенно увеличивается в результате более широкого использования иммунодепрессантов, химиотерапии и трансплантации, а также инфекций, вызванных вирусом иммунодефицита человека.Грибковые инфекции могут поражать любой орган, в том числе толстую кишку.1–3 Тем не менее, в литературе доступны лишь ограниченные сведения об инфекции толстой кишки, вызванной грибами.4,5 Эта статья представляет собой интенсивный обзор исследований грибковой инфекции толстой кишки. в кратком сравнительном стиле для удобного клинического применения.
Методы
Автор инициировал обзор с исследования грибков, которые могут вызывать инфекцию толстой кишки, в MEDLINE, в основных учебниках и существующей исследовательской литературе, в которой рассматриваются грибковые инфекции толстой кишки.4–7 В MEDLINE автор использовал ключевые слова из двух групп. Первая группа состояла из названий грибов или инфекций, связанных с грибами, включая «аспергиллез», « Aspergillus », « Blastomyces », «бластомикоз», « Candida », «кандидоз», «хромобластомикоз». , « Cladophialophora », « Coccidioides », «кокцидиоидомикоз», «криптококкоз», « Cryptococcus », «дерматофит», «дерматофитоз», « Epidermophyton », «eumycetoma», «eumycetoma», , «Фузариоз», « Fusarium », « Histoplasma », «гистоплазмоз», « Madurella », « Microsporum », «мукормикоз», « Paracoccidioides », «паракокцидиоидомикоз». , « Penicillium », «феогифомикоз», « Pneumocystis », «пневмоцистоз», «скедоспориоз», « Scedosporium », « Sporothrix », «споротрихоз», « Trichophyton », « Trichophyton » »,« трихоспороноз », « Zygomycetes » и «зигомикоз».Вторая группа ключевых слов состояла из слов, связанных с локализацией заболевания, которое мы рассматривали, включая «колит», «толстая кишка», «толстая кишка», «энтероколит», «толстая кишка», «толстая кишка» и «толстая кишка». . Наконец, было установлено, что инфекции толстой кишки, которые, как сообщалось, были вызваны грибами, были аспергиллезом, кандидозом, криптококкозом, гистоплазмозом, паракокцидиоидомикозом, пенициллиозом, пневмоцистозом, скедоспориозом и зигомикозом. Подробная информация о каждом грибке была дополнительно рассмотрена из статей, найденных в MEDLINE, с использованием ключевых слов, как описано выше, цитат из этих статей и ссылок в основных учебниках.В MEDLINE были включены все типы статей, включая обзоры, серии случаев, истории болезни, редакционные статьи и письма до 30 июня 2014 г. Первоначально было найдено 124 статьи. Были отобраны только статьи, которые были на английском языке или имели аннотацию на английском языке с необходимыми подробностями, которые имели определенный диагноз грибковой инфекции толстой кишки, включая прямую визуализацию типичного грибка или положительную культуру грибка в образцах толстой кишки. Случаи кандидоза, который считается нормальным комменсалом желудочно-кишечного тракта человека, также должны соответствовать одному из следующих критериев в соответствии с принятыми отчетами о случаях и пересмотренной совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Национальным институтом. критериев группы исследования аллергии и инфекционных микозов: проникновение в глубокие ткани толстой кишки или положительный результат на Candida spp.в поверхностной слизистой оболочке с положительным посевом крови или положительным Candida spp. в поверхностной слизистой оболочке с очевидностью ответа на лечение8–14 Candida spp. только на поверхностной слизистой оболочке без положительного посева крови или свидетельств ответа на лечение были исключены. Распространение было определено как поражение двух или более несмежных органов15–19
В настоящее время уже рассмотрены гистоплазмоз, 20,21 кандидоз 13 и зигомикоз22–25. В случаях других грибковых инфекций, включая криптококкоз, пенициллиоз 26–35, аспергиллез 36–38, 9,39–44 и паракокцидиоидомикоз 45–50, автор обобщил отчеты о случаях, как показано в -.Был опубликован только один отчет о каждом случае пневмоцистоза51 и скедоспориоза.52
Таблица 1
Сводные данные о зарегистрированных случаях криптококкоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распространение в толстой кишке | Эндоскопическое исследование | Лечение и исход | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Zelman et al. | ХМЛ, химиотерапия | Не упоминается | Не упоминается | Да | Не упоминается | Язва | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Унат и др., 27 1960 | 16 / мужчина | Турция | Турция | Диарея, боли в животе, LGIB | 8 лет | Нет | Спуститься ободочной кишки | Масса | Хирургия и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hutto et al, 28 1988 | 29 / женщина | США | Синдром Джобса | Абсцесс прямой кишки | 1 год | 1 год | восходящая ободочная кишка | Стриктура восходящей ободочной кишки и периректальный абсцесс | Операция и амфотерицин B → улучшение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van Calck et al, 29 1988 | 47 / мужской | Бельгия | СПИД | Hematochezia | Hematochezia, лихорадка | , лихорадка не упоминаетсяДа | Периректум | Периректальный абсцесс | Хирургия, амфотерицин B и флуцитозин → улучшенное состояние | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Daly et al, 30 1990 | 63 / мужской | USA | Хортностерэктомия, корнеэктомия , недомогание | 7 дней | Есть | Поперечная ободочная кишка | Масса | Амфот эрицин B и флуцитозин → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bonacini et al, 31 1990 | 31 / мужчина | США | AIDS | Hemiplegia, эпилепсия | Не упоминается | Да | Не упоминается | B и флуцитозин → умер||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 38 / мужчина | США | СПИД | Эпигастральная боль, одинофагия | 3 месяца | Да | Противогрибковая терапия | 3 → умер | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 24 / мужчина | США | Болезнь Ходжкина | Не упоминается | Не упоминается | Да | Не упоминается | Не упоминается | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 31 / женщина | США | СПИД | Не упоминается d | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умер | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Вашингтон и др., 32 1991 | 51 / мужчина | США | Кортикостероиды | Не упоминается | Да | Не упоминается | Не упоминается | Нет → умерло | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Мелато и Горджи, 33 1998 | 84 / женщина | Италия | Нет | Ректальное кровотечение Нет | Острое | Острое толстая кишка | Полип | Полипэктомия → улучшенная | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Law et al, 34 2007 | 40 / мужчина | Канада | AIDS | Боль в животе, диарея, дисфагия, лихорадка | 6 недель Слева | 6 недель толстая кишка | Множественные эритематозные, выпуклые, пятнистые поражения | Амфотерицин B и флуцитозин → улучшенный | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Сонг и др., 35 2008 | 27 / женщина | Корея | Нет | Мелена | Не упоминается | Нет | Проксимальный отдел восходящей ободочной кишки | Масса | Амфотерицин В и флуконазин B → | 9018 с улучшенным эффектом Таблица 4
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность | Продолжительность | Распространение | Распределение по толстой кишке | Эндоскопическое исследование | Лечение и результат | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Penna, 45 1979 | 8 / женщина | Бразилия | Нет | Диарея, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность, абдоминальная недостаточность | 4 года | Нет | Вся толстая кишка | Стриктура, язва | Ко-тримоксазол → улучшение | |||||||||||||||||||||||
| Chojniak et al, 46 2000 | 57 / не упоминается | Бразилия | Нет | Боль в животе, диарея, потеря веса 3 | 2 года | Слепая кишка | Масса | Кетоконазол → не упоминается | ||||||||||||||||||||||||
| Коста Виейра и др., 47 2001 | 60 / мужской | Бразилия | Нет | Лихорадка, перианальные узелки, дисфония, кашель13 лет | Да | Поперечная и нисходящая толстая кишка | Язва | Сульфадиазин → улучшение | ||||||||||||||||||||||||
| Браво и др., 48 2010 | 39 / женщина | Перу | Нет | диарея | 2 месяца | Да | Вся толстая кишка | Язва | Амфотерицин B → умер | |||||||||||||||||||||||
| Леон и др., 49 2 010 | 34 / мужчина | Перу | Нет | Диарея, язвы во рту, одинофагия, похудание, кашель | 18 месяцев | Да | Вся толстая кишка | Язва | Амфтозол | Амфтозол | Леон и др., 49 2010 | 40 / женщина | Перу | Нет | Диарея, похудание, гепатомегалия | 1 год | Да | Не упоминается | Не упоминается | Amphoteric | Benard et al, 50 2013 | 56 / женщина | Бразилия | Нет | Нет (колоноскопия для проверки) | Неизвестно | Нет | Поперечная ободочная кишка | Полип | Итраконазол | 58 / женщина | Бразилия | Нет | Диарея, потеря веса, лихорадка | 6 месяцев 9 0134 | Нет | Вся толстая кишка | Язва | Итраконазол → улучшенный |
Эпидемиология
Candida spp.являются нормальными комменсалами желудочно-кишечного тракта, 53,54, тогда как Aspergillus spp. и Pneumocystis spp. распространены повсеместно55–58 и являются причиной грибковых инфекций во всем мире. Cryptococcus spp. и Scedosporium spp. являются эндемическими микозами, которые также имеют распространение по всему миру. Cryptococcus spp. были изолированы из помета голубей 59, а Scedosporium spp. были обнаружены в приливных отмелях, болотах, прудах, навозе и почве.60,61 Aspergillus spp. и Cryptococcus spp. также могут быть обнаружены как компонент микобиоты толстой кишки человека.62
Zygomycetes можно разделить на два отряда: Mucorales и Entomophthorales. Mucorales — эндемичные грибы, встречающиеся во всем мире в органических субстратах, включая хлеб, фрукты, растительные вещества, почву, компост и экскременты животных.63 Histoplasma spp., Entomophthorales, Paracoccidioides spp. И Penicillium spp. эндемичные микозы, выделенные из почвы в ряде регионов мира.63–71 Histoplasma spp. обнаружены в почве, обогащенной пометом летучих мышей, кур и дроздов.64,65 Entomophthorales можно разделить на Conidiobolus spp. и Basidiobolus spp. и находятся в почве некоторых тропических регионов, особенно Африки, Южной Америки, Центральной Америки и Азии63. Paracoccidioides spp. ограничены почвой в странах Центральной и Южной Америки между 23 ° северной широты (юг Мексики) и 34,5 ° северной широты (Аргентина и Уругвай).Эти районы обладают уникальными экологическими особенностями, так как представляют собой тропические и субтропические леса с умеренными температурами и высокой влажностью.66,67 Penicillium spp. также изолированы от почвы в определенных областях, включая Юго-Восточную Азию, южный Китай (Гуанси), Гонконг и Индию.68–71 Эпидемиологические данные суммированы в.
Таблица 5
Эпидемиология грибков, которые могут вызывать инфекцию толстой кишки
| Грибки | Эпидемиология |
|---|---|
| Aspergillus spp., 55,56 Candida spp., 53,54 Криптококк видов, 59 Histoplasma spp., 64,65 Mucorales, 63 Pneumocystis виды, 57,58 Scedosporium spp.60,61 | Во всем мире |
| Entomophthorales63 | Тропические зоны в Африке, Южной Америке, Центральной Америке и Азии |
| Paracoccidioides spp.66,67 | странах Южной и Центральной Америки , особенно в Бразилии, Колумбии, Венесуэле и Аргентине|
| Penicillium spp.68–71 | Юго-Восточная Азия, южный Китай (Гуанси), Гонконг и Индия |
Распространенность поражения толстой кишки
Степень поражения толстой кишки грибковыми инфекциями варьируется в зависимости от типа грибка, как подробно описано в. Паракокцидиоидомикоз и гистоплазмоз являются наиболее распространенными инфекциями толстой кишки, вызываемыми грибами, с распространенностью 29% 72 и 28% 20 соответственно. Напротив, пенициллиоз, зигомикоз, пневмоцистоз и скедоспориоз редко инфильтрируют толстую кишку, при этом пенициллиоз и зигомикоз встречаются в 1.9% 68 и 0,85% инфекций толстой кишки 25 соответственно. И пневмоцистоз, и скедоспориоз известны только из одного сообщения о клиническом случае.51,52 За исключением ротоглоточного кандидоза, толстая кишка является третьим наиболее частым желудочно-кишечным органом, вовлеченным в кандидоз после пищевода и желудка. Ободочная кишка участвует в 20% случаев кандидоза желудочно-кишечного тракта.73 Криптококкоз толстой кишки является наиболее частым желудочно-кишечным проявлением диссеминированного или легочного криптококкоза с распространенностью около 17%.32
Таблица 6
Распространенность поражения толстой кишки при каждой грибковой инфекции
| Грибковые инфекции | Распространенность поражения толстой кишки | Комментарии | ||
|---|---|---|---|---|
| Паракокцидиоидомикоз3 | ||||
| Гистоплазмоз20 | 28% | |||
| Кандидоз73 | 20% желудочно-кишечного кандидоза (исключая орофарингеальный кандидоз) или легочный криптококкоз | |||
| Аспергиллез74 | 9.2% | |||
| Пенициллиоз68 | 1,9% | Всего четыре случая | ||
| Зигомикоз25 | 0,85% | |||
| 902 Нет данных | Только один случай |
Факторы риска
Криптококкоз толстой кишки и зигомикоз часто возникают у хозяев с ослабленным иммунитетом, встречаясь в 77% 26–35 и 67% 22 инфекциях соответственно, в то время как кандидоз толстой кишки, 13 пенициллиоз, 36– 38 и аспергиллез9,39–44 встречаются исключительно у хозяев с ослабленным иммунитетом.Факторами риска этих инфекций являются злокачественные новообразования, прием иммунодепрессантов, химиотерапия, нейтропения, СПИД, почечная недостаточность, спленэктомия, синдром Джоба, цирроз печени, недоедание и сахарный диабет; тем не менее, большинство пациентов с пенициллиозом толстой кишки обычно болеют СПИДом.37,38 Также были сообщения о случаях пневмоцистоза и скедоспориоза толстой кишки у пациентов с ослабленным иммунитетом, больных СПИДом и после трансплантации печени, соответственно.51,52 При паракокцидиоидомикозе толстой кишки и гистоплазмозе нет необходимости факторы риска присутствуют.20,21,45–50 Как показано на фиг.4, мужчины преобладают почти во всех грибковых инфекциях, за исключением кандидоза толстой кишки, аспергиллеза и паракокцидиоидомикоза. Более высокая частота грибковых инфекций у мужчин может быть объяснена их более интенсивным воздействием на места обитания эндемичных грибов во время работы67. При кандидозе толстой кишки предпочтения по признаку пола нет, поскольку Candida spp. нормальные комменсалы кишечника человека.13,53,54 Aspergillus spp. распространены повсеместно, поэтому секс также не является фактором риска заражения.9,39–44,55,56 Хотя паракокцидиоидомикоз обычно встречается у мужчин, среди паракокцидиоидомикоза толстой кишки преобладают 67 женщин. 45–50 Автор предполагает, что это может быть вызвано предвзятостью в сообщениях.
Таблица 7
Факторы риска грибковых инфекций толстой кишки
| Грибковые инфекции | Иммунокомпетентные | С ослабленным иммунитетом | Факторы риска | Мужчины | Комментарии | 50 | Мужской | Комментарии | 0% | — | 29% |
|---|---|---|---|---|---|---|---|---|
| Гистоплазмоз20,21 | 81% | 19% | Злокачественные новообразования, иммунодепрессанты, СПИД, синдром Джоба3 – СД | % | ||||
| Кандидоз 13 | 0% | 100% | Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, ESRD | 43% | ||||
| СПИД, иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз печени | 64% | |||||||
| Аспергиллез9,39–44 | 0% | 100% злокачественные новообразования | DM, ожог33% | |||||
| Пенициллиоз 36–38 | 0% | 100% | СПИД (75%), иммунодепрессанты | 100% | ,24 | |||
| 67% | Иммунодепрессанты, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования | 65% | Пневмоцистоз51 | 0% | 100% | СПИД | 100% | Только один случай |
| Scedosporiosis52 | 0% | 100% | 100 | 100% | трансплантация печени | Только один случай |
Иммунитет и инфекция толстой кишки, вызванная грибами
Иммунный ответ хозяина на грибы может играть важную роль в патогенезе инфекции толстой кишки, вызванной грибами, особенно организмами, которые являются частью микробиоты.75,76 Обычно клетки врожденного иммунитета имеют мембраносвязанные и растворимые рецепторы для уничтожения грибов. Связанные с мембраной рецепторы, такие как лектин, толл-подобный поглотитель и рецепторы комплемента, могут обнаруживать грибы или грибковые продукты, а затем активировать фагоцитоз и респираторный взрыв. Факторы транскрипции, которые могут индуцировать провоспалительные цитокины и хемокины, также активируются мембраносвязанными рецепторами. Растворимые рецепторы могут дополнительно активировать комплементы и опсонизировать грибы до рецепторов комплемента. Наконец, T-хелперы (Th) 1 и 17 запускаются и продуцируют другие цитокины, включая интерлейкин (IL) -17A, IL-17F и IL-22 для адаптивного иммунитета.Как врожденная, так и адаптивная иммунные системы защищают хозяина от грибов.76
Есть некоторые свидетельства того, что ослабленный иммунитет может усиливать инфекцию толстой кишки. Было продемонстрировано, что IL-22, который продуцируется врожденными клетками и регулируется IL-23, активирует воспалительные клетки и, таким образом, контролирует начальный рост грибков.75 Дефектные пути IL-23 и IL-22 увеличивают грибковую нагрузку в желудочно-кишечном тракте; тем не менее, клетки Th2 предотвращают распространение грибов. Клетки Th27 играют важную роль в адаптивных иммунных ответах, хотя их нарушение приводит к снижению устойчивости к поздней грибковой инфекции.Дефицит рецептора А IL-17 снижает активацию Th2, тем самым снижая устойчивость к грибам. 75 Таким образом, иммуносупрессивный статус является одним из основных факторов, предрасполагающих к инфекции толстой кишки, вызываемой грибами.
Клинические проявления
Инфекции толстой кишки, вызываемые грибами, имеют различные клинические проявления, как подробно описано в. За исключением зигомикоза и аспергиллеза, более половины пациентов с грибковыми инфекциями толстой кишки имеют диссеминированное заболевание. Боль в животе — наиболее частое проявление зигомикоза и аспергиллеза толстой кишки.9,22,24,39–44 Поражение глубоких тканей и ангиоинвазия, которые являются частыми патологическими проявлениями как при аспергиллезе, так и при зигомикозе, могут объяснить эти проявления.22,25,74 Диарея — симптом, который часто встречается при паракокцидиоидомикозе и кандидозе.13 , 45–50 Случаи гистоплазмоза толстой кишки и пенициллиоза включают диарею и боль в животе в качестве преобладающих симптомов.20,21,36–38 Периректальный абсцесс — специфическая особенность, которая обнаруживается только при криптококкозе толстой кишки. 28,29 Лихорадка — обычное явление при грибковых заболеваниях. инфекция толстой кишки, особенно у пациентов с пенициллиозом толстой кишки, у всех из которых наблюдается лихорадка.36–38 Например, случай пневмоцистоза толстой кишки проявился лихорадкой и диареей 51, тогда как случай скедоспориоза толстой кишки представил диарею и боль в животе.52
Таблица 8
Клинические проявления инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Распространение | Диарея | Боль в животе | LGIB | Ректальный абсцесс | Лихорадка | Комментарии | |||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| — | 50% | Бессимптомно у 12.5% | ||||||||||||
| Гистоплазмоз20,21 | 83% | 83% | 67% | 32% | — | 77% | — | |||||||
| 57 29% | 29% | — | 71% | — | ||||||||||
| Криптококкоз 26–35 | 71% (все пациенты с ослабленным иммунитетом) | 20% | 30% | 9013 40% 90% 30% | Бессимптомно у 20% | |||||||||
| Аспергиллез9,39–44 | 33% | 22% | 56% | 33% | — | 67% | —34 Peniciosis | 50% | 75% | 75% | 25% | — | 100% | — |
| Зигомикоз22,24 | 38% | 18% | % | – | 55% | — | ||||||||
| Пневмоцистоз51 | 100% | 100% | — | — | — | 100% | Только один случай | |||||||
| 100% | — | — | — | Только один случай |
Патологические данные и распределение
Язва толстой кишки является наиболее частой патологической находкой у пациентов с грибковой инфекцией толстой кишки, как показано на рис.Во всех случаях аспергиллеза толстой кишки и пенициллиоза есть язвы.36–38,74 Язва также обычно обнаруживается при гистоплазмозе толстой кишки, паракокцидиоидомикозе и кандидозе.21,45–50,73 Скедоспориоз толстой кишки также проявляется язвой52. криптококкоз толстой кишки представляет собой образование или полип как наиболее частую патологическую находку, в то время как криптококкоз толстой кишки может также проявляться атипичными патологическими проявлениями, включая абсцесс или стриктуру прямой кишки26–35. Другой инфекцией толстой кишки, которая может проявляться массой или полипом, является гистоплазмоз.21 В одном случае пневмоцистоза толстой кишки у пациента был отек кишечника.51
Таблица 9
Патологические данные об инфекциях толстого кишечника, вызванных грибами
| Грибковые инфекции | Язва | Воспаление слизистой оболочки / эрозия | Псевдемия | Масса / полип | Абсцесс прямой кишки | Стриктура | Комментарий | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз45–50 | 63% | — | — | Гистоплазмоз21 | 79% | 14% | — | 7% | — | — | |||||||||||
| Кандидоз73 | 64% | 14% | 14% | Из серии вскрытий | |||||||||||||||||
| Криптококкоз 26–35 | 11% | 11% | — | 44% | 22% | 11% | |||||||||||||||
| Аспергиллез74 | 100% (с некрозом 55.6%) | — | — | — | — | — | По результатам вскрытия | ||||||||||||||
| Пенициллиоз36–38 | 100% | — | — | — | |||||||||||||||||
| Зигомикоз22,25 | — | — | — | — | — | — | Язва, некроз, образовавшаяся масса, но количество пациентов не указано | 100% | — | — | — | — | Только один случай | ||||||||
| Сцедоспориоз52 | 100% | — | — | — | — |
Распространение инфекции толстой кишки, вызванной грибами, различается в зависимости от типа грибка, как показано в.Гистоплазмоз толстой кишки, зигомикоз и пенициллиоз, как правило, возникают в правой части толстой кишки.20,23,36–38 Область прямой кишки обычно поражается в случаях гистоплазмоза, кандидоза и зигомикоза.13,20,23 Криптококкоз толстой кишки — это заболевание. единственный грибок, который поражает периректальную область.28,29 Диффузное поражение толстой кишки обычно встречается при паракокцидиоидомикозе толстой кишки.45-50 Случаи как пневмоцистоза толстой кишки, так и скедоспориоза также представлены диффузными поражениями.51,52
Таблица 10
Распределения инфекций толстой кишки, вызванных грибами
| Грибковые инфекции | Слепая кишка или восходящая ободочная кишка или аппендикс | Поперечная ободочная кишка | Нисходящая или сигмовидная кишка | Прямая кишка | Надпочечная кишка | Вся толстая кишка Паракокцидиоидомикоз 45–50 | 13% | 25% | 13% | — | — | На 50% 20% | — | 20% | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Криптококкоз 27–30,32–35 | 30% | 10% | 40% | — | 20% | Аспергиллез9,39–44 | 33% | 22% | 22% | — | — | 22% | |||||
| Пенициллиоз36–38 | 503 | 9013% —— | — | ||||||||||||||
| Зигомикоз23 | 50% | — | 18% | 7% | — | 25% | 12334 | 9010— | — | — | — | — | 100% | Только один случай | |||
| Scedosporiosis52 | — | — | — | — | Только один случай
Ответ на лечение
Амфотерицин B является наиболее часто используемым препаратом для лечения почти всех грибковых инфекций толстой кишки, за исключением кандидоза и пневмоцистоза.Кандидоз толстой кишки реагирует на флуконазол или каспофунгин и имеет лучший прогноз, если противогрибковая терапия начата со 100% соблюдением режима.13 Хороший ответ был также достигнут при пневмоцистозе толстой кишки и скедоспориозе.51,52 Случай пневмоцистоза толстой кишки лечили пентамидином внутривенно из-за сульфаметоксазола -Триметоприм аллергия.51 Комбинированная противогрибковая терапия и хирургическое вмешательство использовались для лечения желудочно-кишечного зигомикоза и аспергиллеза, вызванного ангиоинвазией и инфарктом. Тем не менее прогноз в этих случаях все еще плохой, летальность составляет 50%.25,39,41,43,44 Выбор антибиотиков и ответ на лечение грибковых инфекций обобщены в.
Таблица 11
Ответ на лечение грибковых инфекций толстой кишки
| Грибковые инфекции | Лечение | Ответ на лечение | Комментарии | |||||
|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз4, 90 -13–50 амфотерицин В или итраконазол | 71% | |||||||
| Гистоплазмоз21 | Амфотерицин В | 77% | ||||||
| Кандидоз4 | Кандидоз4 | Амфотерицин В + флуцитозин ± хирургическое вмешательство | 67% | Ответ на лечение у иммунокомпетентных пациентов составил 100% | ||||
| Аспергиллез 39,41,43,44 | Амфотерицин В или каспофунгин 9013 | 90% хирургическое вмешательство | Пенициллиоз 36–38 | Амфот эрицин B | 75% | |||
| Зигомикоз25 | Амфотерицин B + хирургическое вмешательство | 50% | Комбинированное хирургическое вмешательство улучшило ответ на лечение | |||||
| Один пневмоцистоз3124 | Scedosporiosis52 | Амфотерицин B | 100% | Только один случай |
Заключение
Это первое исследование, в котором проводился интенсивный обзор литературы по грибковым инфекциям толстой кишки.Все содержание кратко изложено в. Он предоставляет основную информацию о причинах, проявлениях и лечении и может легко применяться в клинической практике. Врачи должны знать об этом грибковом образовании, когда у пациентов наблюдаются симптомы со стороны толстой кишки, особенно в случаях с ослабленным иммунитетом. Хотя сообщалось, что многие грибковые инфекции вызывают заболевания толстой кишки, включая аспергиллез, кандидоз, криптококкоз, гистоплазмоз, паракокцидиоидомикоз, пенициллиоз, пневмоцистоз, скедоспориоз и зигомикоз, знание эпидемиологических различий, факторов риска, клинических проявлений и патологических данных поможет врачам. для лучшей диагностики и лечения этих инфекций.Соответствующее лечение противогрибковыми препаратами определенно улучшает результаты; тем не менее, смертность от зигомикоза и аспергиллеза по-прежнему высока.
Таблица 12
Краткое описание инфекции толстой кишки, вызванной грибами
| Грибковые инфекции | Распространенность поражения толстой кишки | Факторы риска | Клинические проявления | Распространение | Распространение | Начальное лечение | |||
|---|---|---|---|---|---|---|---|---|---|
| Паракокцидиоидомикоз 45–50,72 | 29% | • Эндемичная территория (Южная Америка) • Любой хозяин | Диарея, боль в животе, лихорадка | 50% язвы | Вся толстая кишка | Ко-тримоксазол, сульфадиазин, амфотерицин B или итраконазол | 71% | ||
| Гистоплазмоз20,21 | 28% | • Любой хозяин | лихорадка в животе, потеря веса в животе | 83% | Язва, отек слизистой оболочки | Вся толстая кишка, но преимущественно правая сторона e толстой и прямой кишки | Амфотерицин B | 77% | |
| Кандидоз13,73 | 20% кишечного кандидоза при вскрытии | • Злокачественные новообразования, иммунодепрессанты, нейтропения, СПИД, пациенты с ESR | , боль в животе, лихорадка71% | Язва, зубной налет, эрозия | Вся толстая кишка | Флуконазол или каспофунгин | 100% | ||
| Криптококкоз26–35 | Криптококкоз иммунодепрессанты, гематологические злокачественные новообразования, спленэктомия, синдром Джоба, цирроз • Иммунокомпетентные пациенты (23%) | • Симптомы: LGIB, лихорадка, абдоминальная боль, диарея, ректальный абсцесс • 20% пациентов с бессимптомным иммунодефицитом | 71% (все пациенты) | Масса, периректальный абсцесс, язва толстой кишки, очаговые поражения, стриктура, полип | Вся толстая кишка | Амфо терицин B + флуцитозин ± хирургия | 60% | ||
| Аспергиллез9,39–44,74 | 9.2% | • Злокачественные новообразования, химиотерапия, нейтропения, иммунодепрессанты, сахарный диабет, ожог • Пациенты без иммунодефицита | Лихорадка, боль в животе, LGIB, диарея | 86% | Язва, некроз | 9013 Вся толстая кишка каспофунгин ± хирургия | 50% | ||
| Пенициллиоз36–38,68 | 1,9% | • Эндемичная территория (Юго-Восточная Азия, южный Китай, Гонконг и Индия) • В основном СПИД (75%) • Отсутствие иммунокомпетентности пациенты | Лихорадка, диарея, боль в животе, LGIB | 50% | Язва | Преимущественно в правой части ободочной и прямой кишки | Амфотерицин B | 75% | |
| Зигомикоз.85% | • Иммунодепрессивное средство, недостаточность питания, почечная недостаточность, СД, гематологические злокачественные новообразования • Пациенты I мм с некомпетентностью (33,3%) | Боль в животе, вздутие живота, лихорадка, LGIB, диарея | 38% | Язва | Вся ободочная кишка, но преимущественно в правой части ободочной кишки | Операция с применением амфотерицина В + | 50% | ||
| Пневмоцистоз51 | Только один случай | • СПИД | Лихорадка, диарея% 13133 | Вся толстая кишка | Пентамидин | 100% | |||
| Скедоспориоз52 | Только один случай | • После трансплантации печени, иммунодепрессанты | Диарея, толстая кишка | 9013 | % Амфотерицин В100% |
Таблица 2
Сводные данные о зарегистрированных случаях пенициллиоза толстой кишки
| Источник, год | Возраст (лет) / пол | Источник отчета | Основное заболевание / лекарство | Клинические проявления | Продолжительность начала | Распространение | Распределение по толстой кишке | Эндоскопические данные | Лечение и исход | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Цанг и др., 36 1988 | 58 / мужчина | Гонконг | Кортикостероиды 3 | гепаталиния | Гепаталий | Гепаталий | Гепаталия | Да | Нисходящая ободочная кишка | Язва | Амфотерицин B → умер | |
| Leung et al, 37 1996 | 32 / мужской | Гонконг | СПИД | Лихорадка, понос 9013, ночь Острая | Нет | Слепая кишка, поперечная и нисходящая ободочная кишка | Язва 90 134 | Амфотерицин В и итраконазол → улучшение | ||||
| Ко и др., 38 1999 | 52 / мужчина | Тайвань | СПИД | Лихорадка, диарея, анемия, боли в животе | 3 недели | Язва | Амфотерицин В и итраконазол → улучшение | |||||
| Ко и др., 38 1999 | 30 / мужчина | Тайвань | СПИД | Диспепсия, диарея, лихорадка, боль в животе3 9013, потеря веса 3 90 месяцев, LGIB4 | № | Слепая кишка, восходящая и поперечная ободочная кишка | Язва | Амфотерицин В и итраконазол → улучшенные |
Таблица 3
Сводные данные по зарегистрированным случаям аспергиллеза толстой кишки7
Сноски
Раскрытие информации
Автор сообщает об отсутствии конфликта интересов в этой работе.
Ссылки
1. Анаисси Э.Дж., Макгиннис М.Р., Пфаллер М.А., редакторы. Клиническая микология. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 2003. [Google Scholar] 2. Отклоняет редакторов WE, Pappas PG, Sobel JD. Клиническая микология. Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 2003. [Google Scholar] 3. Хоспенталь Д.Р., Ринальди М.Г., редакторы. Диагностика и лечение микозов человека. Тотова, Нью-Джерси: Humana Press; 2008. [Google Scholar] 5. Шмитт С.Л., Векснер С.Д. Бактериальный, грибковый, паразитарный и вирусный колит. Surg Clin North Am.1993. 73 (5): 1055–1062. [PubMed] [Google Scholar] 6. Lima AAM, Guerrant RL. Воспалительные энтериты. В: Манделл Г.Л., Беннетт Дж. Э., Долин Р., редакторы. Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета. 7-е изд. Филадельфия, Пенсильвания: Черчилль Ливингстон Эльзевьер; 2009. С. 1389–1398. [Google Scholar] 7. Wilcox CM. Желудочно-кишечные последствия заражения вирусом иммунодефицита человека. В: Фельдман М., Фридман Л.С., Брандт Л.Дж., редакторы. Заболевания желудочно-кишечного тракта и печени Слейзенгера и Фордтрана.9 изд. Филадельфия, Пенсильвания: Сондерс Эльзевьер; 2010. С. 523–535. [Google Scholar] 8. Стилианос С., Форд К.А., Бенвенисти Эл, Харди М.А. Кровоизлияние в нижнюю часть желудочно-кишечного тракта у реципиентов почечного трансплантата. Arch Surg. 1988. 123: 739–744. [PubMed] [Google Scholar] 10. Jayagopal S, Cervia JS. Колит, вызванный Candida albicans, у больного СПИДом. Clin Infect Dis. 1992; 15: 555. [PubMed] [Google Scholar] 11. Куклакис Г., Докас С., Моливас Е., Вакианис П., Эфтимиу А. Кандидозный колит у мужчины среднего возраста, получающего постоянный гемодиализ.Eur J Gastroenterol Hepatol. 2001; 13: 735–736. [PubMed] [Google Scholar] 12. Китагава KH, Kalb RE. Лечение эфализумабом при кандидозном колите. J Am Acad Dermatol. 2008; 59 (приложение 5): S120 – S121. [PubMed] [Google Scholar] 13. Praneenararat S. Первый зарегистрированный случай инфекции толстой кишки, вызванной Candida tropicalis, и обзор литературы. Случай Реп Гастроэнтерол. 2014; 8: 199–205. [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Де Пау Б., Уолш Т.Дж., Доннелли Дж. П. и др. Пересмотренные определения инвазивного грибкового заболевания, разработанные Совместной группой Европейской организации по исследованию и лечению рака / инвазивных грибковых инфекций и Консенсусной группы Национального института аллергии и инфекционных заболеваний по изучению микозов (EORTC / MSG).Clin Infect Dis. 2008; 46: 1813–1821. [Бесплатная статья PMC] [PubMed] [Google Scholar] 15. Ascioglu S, Rex JH, de Pauw B, et al. Совместная группа по инвазивным грибковым инфекциям Европейской организации по исследованию и лечению рака. Группа по изучению микозов Национального института аллергии и инфекционных заболеваний. Определение оппортунистических инвазивных грибковых инфекций у пациентов с ослабленным иммунитетом, перенесших онкологические заболевания и трансплантацию гемопоэтических стволовых клеток: международный консенсус. Clin Infect Dis. 2002; 34: 7–14.[PubMed] [Google Scholar] 16. Сафдар А., Сингхал С., Мехта Дж. Клиническое значение выделения из крови не Candida грибков у пациентов, перенесших трансплантацию аллогенных гемопоэтических стволовых клеток высокого риска (1993–2001) Рак. 2004. 100: 2456–2461. [PubMed] [Google Scholar] 17. Контойяннис Д.П., Бодей Г.П., Ханна Х и др. Детерминанты исхода фузариоза в онкологическом центре третичного уровня: влияние восстановления нейтрофилов. Лимфома лейка. 2004. 45: 139–141. [PubMed] [Google Scholar] 18. Лионакис М.С., Бодей Г.П., Тарранд Дж.Дж., Раад II, Контойяннис Д.П.Значение положительных культур крови для появления сапрофитных плесневых грибов у онкологических больных. Clin Microbiol Infect. 2004; 10: 922–925. [PubMed] [Google Scholar] 19. Сафдар А., Родригес Дж., Ролстон К.В. и др. Комбинированная противогрибковая терапия высокими дозами каспофунгина у пациентов с гематологическими злокачественными новообразованиями и трансплантацией гемопоэтических стволовых клеток. Пересадка костного мозга. 2007. 39 (3): 157–164. [PubMed] [Google Scholar] 20. Каппелл М.С., Манделл В., Граймс М.М., Нью-ХК. Гистоплазмоз желудочно-кишечного тракта. Dig Dis Sci.1988. 33: 353–360. [PubMed] [Google Scholar] 21. Асси М., Маккинси Д.С., Дрикс М.Р. и др. Гистоплазмоз желудочно-кишечного тракта при синдроме приобретенного иммунодефицита: отчет о 18 случаях и обзор литературы. Диагностика Microbiol Infect Dis. 2006; 55: 195–201. [PubMed] [Google Scholar] 22. Lyon DT, Schubert TT, Mantia AG, Kaplan MH. Фикомикоз желудочно-кишечного тракта. Am J Gastroenterol. 1979. 72 (4): 379–394. [PubMed] [Google Scholar] 23. Ага Ф. П., Ли Х. Х., Боланд Ч. Р., Брэдли С.Ф. Мукормикома толстой кишки: ранняя диагностика и успешное лечение.AJR Am J Roentgenol. 1985; 145: 739–741. [PubMed] [Google Scholar] 24. Роден М.М., Заутис Т.Э., Бьюкенен В.Л. и др. Эпидемиология и исходы зигомикоза: обзор 929 зарегистрированных случаев. Clin Infect Dis. 2005; 41: 634–653. [PubMed] [Google Scholar] 25. Альмирудис Н.Г., Саттон Д.А., Линден П., Ринальди М.Г., Фунг Дж., Кусне С. Зигомикоз у реципиентов солидных трансплантатов в центре третичной трансплантации и обзор литературы. Am J Transplant. 2006; 6: 2365–2374. [PubMed] [Google Scholar] 26. Зельман С., О’Нил Р.Х., Плаут А.Диссеминированный висцеральный торулез без поражения нервной системы с клиническими проявлениями гранулоцитарного лейкоза. Am J Med. 1951; 11: 658–664. [PubMed] [Google Scholar] 28. Хатто Дж.О., Брайан С.С., Грин Флорида, Уайт СиДжей, Галлин Джи. Криптококкоз толстой кишки, напоминающий болезнь Крона, у пациента с синдромом рецидивирующей инфекции гипериммуноглобулинемии E. Гастроэнтерология. 1988. 94: 808–812. [PubMed] [Google Scholar] 29. Ван Калк М., Мотт С., Рикаерт Ф., Серрюйс Э., Адлер М., Вибран Дж. Криптококковая анальная язва у пациента со СПИДом.Am J Gastroenterol. 1988. 83: 1306–1308. [PubMed] [Google Scholar] 30. Дэйли Дж. С., Портер К. А., Чонг Ф. К., Робиллард Р. Дж.. Распространенная неменингеальная желудочно-кишечная криптококковая инфекция у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1990; 85: 1421–1424. [PubMed] [Google Scholar] 31. Bonacini M, Nussbaum J, Ahluwalia C. Поражение желудочно-кишечного тракта, печени и поджелудочной железы с Cryptococcus neoformans при СПИДе. J Clin Gastroenterol. 1990; 12: 295–297. [PubMed] [Google Scholar] 32. Вашингтон К., Готфрид М.Р., Уилсон М.Л.Желудочно-кишечный криптококкоз. Мод Pathol. 1991; 4: 707–711. [PubMed] [Google Scholar] 33. Мелато М., Горжи Н. Первичный кишечный криптококкоз, имитирующий аденоматозный полип у ВИЧ-отрицательного пациента. Am J Gastroenterol. 1998; 93: 1592–1593. [PubMed] [Google Scholar] 34. Ло Дж. К., Амар Дж. Н., Кирби С. Д., Зетлер П. Дж., Эннс РА. Криптококковая инфекция толстой кишки. Gastrointest Endosc. 2007. 65: 525–526. [PubMed] [Google Scholar] 35. Сонг Дж. К., Ким С. К., Ким Е. С. и др. Случай криптококкоза толстой кишки. Корейский J Gastroenterol.2008. 52: 255–260. Корейский. [PubMed] [Google Scholar] 36. Цанг Д.Н., Чан Дж.К., Лау Ю.Т., Лим В., Цзе СН, Чан Н.К. Инфекция Penicillium marneffei: недиагностируемая болезнь? Гистопатология. 1988; 13: 311–318. [PubMed] [Google Scholar] 37. Леунг Р., Сунг Дж.Й., Чоу Дж., Лай С.К. Необычная причина лихорадки и диареи у больного СПИДом. Penicillium marneffei инфекция. Dig Dis Sci. 1996; 41: 1212–1215. [PubMed] [Google Scholar] 38. Ко CI, Hung CC, Chen MY, Hsueh PR, Hsiao CH, Wong JM. Эндоскопическая диагностика кишечного пенициллиоза marneffei: отчет о трех случаях и обзор литературы.Gastrointest Endosc. 1999. 50 (1): 111–114. [PubMed] [Google Scholar] 39. Kinder RB, Jourdan MH. Диссеминированный аспергиллез и кровоточащие язвы толстой кишки у пациента с трансплантатом почки. JR Soc Med. 1985. 78 (4): 338–339. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Соуза А.Б., Феррейра Г., Вейга Дж., Карвалью А. Клиническая картина: инфаркт кишечника из-за аспергиллеза. Ланцет. 2002; 359 (9302): 210. [PubMed] [Google Scholar] 41. Финн С., Бонд Дж., Маккарти Д., Шихан К., Куинн С. Ангиоинвазивный аспергиллез, проявляющийся как нейтропенический колит.Гистопатология. 2006. 49 (4): 440–441. [PubMed] [Google Scholar] 42. Андрес Л.А., Форд Р.Д., Уилкокс Р.М. Некротический колит, вызванный системным аспергиллезом у ожогового больного. J Burn Care Res. 2007. 28 (6): 918–921. [PubMed] [Google Scholar] 43. Мохайт У., Келл Дж., Хадж М.А. и др. Инвазивный аспергиллез, локализованный в толстой кишке, проявляется в виде токсичного мегаколона. Eur J Haematol. 2007. 78: 270–273. [PubMed] [Google Scholar] 44. Чхве С.Х., Чунг Дж. В., Чо СИ, Ким Би Джей, Квон Дж. Случай изолированного инвазивного аспергиллезного колита с гематохезией у пациента с раком толстой кишки, не страдающего нейтропенией.Кишечная печень. 2010. 4 (2): 274–277. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Chojniak R, Costa Vieira RA, Lopes A, et al. Кишечный паракокцидиоидомикоз, имитирующий рак толстой кишки. Rev Soc Bras Med Trop. 2000. 33: 309–312. [PubMed] [Google Scholar] 47. Коста Виейра РА, Лопес А, Оливейра Х.В. и др. Анальный паракокцидиоидомикоз: необычное проявление диссеминированного заболевания. Rev Soc Med Trop. 2001; 34: 583–586. [PubMed] [Google Scholar] 48. Браво Э.А., Зегарра А.Дж., Пискоя А. и др. Хроническая диарея и панколит, вызванные паракокцидиоидомикозом: клинический случай.История болезни Med. 2010; 2010: 140505. [Бесплатная статья PMC] [PubMed] [Google Scholar] 49. Леон М., Алаве Дж., Бустаманте Б., Кок Дж., Готуццо Е., Сис С. Т-лимфотропный вирус 1 человека и паракокцидиоидомикоз: вероятная ассоциация в Латинской Америке. Clin Infect Dis. 2010. 51 (2): 250–251. [PubMed] [Google Scholar] 50. Бенард Г., Коста А.Н., Леоперсио А.П., Висентини А.П., Коно А., Шиканаи-Ясуда М.А. Хронический паракокцидиоидомикоз кишечника как поражение одного органа указывает на альтернативный патогенез микоза.Микопатология. 2013. 176 (5–6): 353–357. [PubMed] [Google Scholar] 51. Белломо А.Р., Перлман Д.К., Камински Д.Л., Бреттхольц Е.М., Сарлин Дж. Пневмоцистный колит у больного с синдромом приобретенного иммунодефицита. Am J Gastroenterol. 1992. 87 (6): 759–761. [PubMed] [Google Scholar] 52. Лин Д., Камили К., Лай С., Мушер Д.М., Хэмилл Р. Церебральная инфекция Scedosporium apiospermum, проявляющаяся кишечными проявлениями. Инфекционное заболевание. 2013. 41 (3): 723–726. [PubMed] [Google Scholar] 53. Горбач С.Л., Нахас Л., Лернер П.И., Вайнштейн Л.Исследования микрофлоры кишечника. I. Влияние диеты, возраста и периодического отбора проб на количество фекальных микроорганизмов у человека. Гастроэнтерология. 1967; 53: 845–855. [PubMed] [Google Scholar] 54. Коэн Р., Рот Ф.Дж., Дельгадо Э., Ахерн Д.Г., Калсер М.Х. Грибковая флора нормального тонкого и толстого кишечника человека. N Engl J Med. 1969; 280: 638–641. [PubMed] [Google Scholar] 55. Деннинг DW. Инвазивный аспергиллез. Clin Infect Dis. 1998; 26: 781–803. [PubMed] [Google Scholar] 56. Марр К.А., Паттерсон Т., Деннинг Д. Аспергиллез.Патогенез, клинические проявления и терапия. Заражение Dis Clin North Am. 2002; 16: 875–894. vi. [PubMed] [Google Scholar] 57. Смулиан А.Г., Кили С.П., Сункин С.М., Стрингер-младший. Генетическая и антигенная изменчивость организмов Pneumocystis carinii: инструменты для изучения эпидемиологии и патогенеза инфекции. J Lab Clin Med. 1997. 130 (5): 461–468. [PubMed] [Google Scholar] 58. Дейли К.Р., Кох Дж., Левин Л., Уолцер П.Д. Иммуноферментный анализ и серологические ответы на Pneumocystis jiroveci. Emerg Infect Dis.2004. 10 (5): 848–854. [Бесплатная статья PMC] [PubMed] [Google Scholar] 59. Chayakulkeeree M, Perfect JR. Криптококкоз. Заражение Dis Clin North Am. 2006; 20: 507–544. [PubMed] [Google Scholar] 61. Саммербелл Р.К., Крайден С., Кейн Дж. Горшечные растения в больницах как резервуары патогенных грибов. Микопатология. 1989; 106: 13–22. [PubMed] [Google Scholar] 62. Хоффманн С., Доллив С., Грюнберг С. и др. Археи и грибы микробиома кишечника человека: корреляция с диетой и бактериальными жителями. PLoS One. 2013; 8 (6): e66019.[Бесплатная статья PMC] [PubMed] [Google Scholar] 63. Контояннис Д.П., Льюис Р.Э. Инвазивный зигомикоз: обновленная информация о патогенезе, клинических проявлениях и лечении. Заражение Dis Clin North Am. 2006; 20: 581–607. [PubMed] [Google Scholar] 64. Гудвин Р.А., младший, Шапиро Дж. Л., Турман Г. Х., Турман СС, Дес През Р. М.. Диссеминированный гистоплазмоз: клинико-патологические корреляции. Медицина (Балтимор) 1980; 59: 1–33. [PubMed] [Google Scholar] 65. Пшеница LJ, Slama TG, Eitzen HE, Kohler RB, French ML, Biesecker JL. Крупная городская вспышка гистоплазмоза: клинические особенности.Ann Intern Med. 1981; 94: 331–337. [PubMed] [Google Scholar] 66. Negroni R. Paracoccidioidomycosis (южноамериканский бластомикоз, микоз Лутца) Int J Dermatol. 1993; 32: 847–859. [PubMed] [Google Scholar] 67. Blotta MH, Mamoni RL, Oliveira SJ, et al. Эндемичные регионы паракокцидиоидомикоза в Бразилии: клиническое и эпидемиологическое исследование 584 случаев в юго-восточном регионе. Am J Trop Med Hyg. 1999. 61: 390–394. [PubMed] [Google Scholar] 68. Суппаратпиньо К., Кхамван С., Баосунг В., Нельсон К.Э., Сирисантана Т.Распространенная инфекция Penicillium marneffei в Юго-Восточной Азии. Ланцет. 1994; 344: 110–113. [PubMed] [Google Scholar] 69. Вонг К.Х., Ли С.С., Ло Ю.С. и др. Профиль оппортунистических инфекций среди людей, инфицированных ВИЧ-1, в Гонконге. Чжунхуа И Сюэ За Чжи (Тайбэй) 1995; 55: 127–136. [PubMed] [Google Scholar] 70. Duong TA. Инфекция, вызванная Penicillium marneffei, новым патогеном: обзор 155 зарегистрированных случаев. Clin Infect Dis. 1996; 23: 125–130. [PubMed] [Google Scholar] 71. Вонг К.Х., Ли СС. Сравнение первой и второй сотни случаев СПИДа в Гонконге.Singapore Med J. 1998; 39: 236–240. [PubMed] [Google Scholar] 72. Peña CE. Глубокие грибковые инфекции в Колумбии. Клинико-патологическое исследование 162 случаев. Am J Clin Pathol. 1967. 47 (4): 505–520. [PubMed] [Google Scholar] 73. Эрас П., Гольдштейн М.Дж., Шерлок П. Кандидозная инфекция желудочно-кишечного тракта. Медицина (Балтимор) 1972; 51: 367–379. [PubMed] [Google Scholar] 74. Молодой Р.С., Беннетт Дж. Э., Фогель С. Л., Карбон П. П., ДеВита В. Т.. Аспергиллез. Спектр заболевания у 98 больных. Медицина (Балтимор) 1970; 49: 147–173.[PubMed] [Google Scholar] 75. Де Лука А., Зеланте Т., Д’Анджело С. и др. IL-22 определяет новый иммунный путь устойчивости к противогрибковым препаратам. Mucosal Immunol. 2010. 3 (4): 361–373. [PubMed] [Google Scholar] 76. Андерхилл Д.М., Илиев И.Д. Микобиота: взаимодействие между комменсальными грибами и иммунной системой хозяина. Nat Rev Immunol. 2014. 14 (6): 405–416. [Бесплатная статья PMC] [PubMed] [Google Scholar]Внутрибрюшной кандидоз: рекомендации — забытый некандидемический инвазивный кандидоз
Pappas PG, Kauffman CA, Andes D, Benjamin DK Jr, Calandra TF, Edwards JE Jr, Filler SG, Fisher JF, Kullberg BJ, Ostrosky-Zeichner L, Reboli AC, Rex JH, Walsh TJ, Sobel JD (2009) Рекомендации по клинической практике для лечения кандидоза: обновление 2009 года Американского общества инфекционных болезней.Clin Infect Dis 48: 503–535. DOI: 10.1086 / 5
PubMed Статья CAS Google Scholar
Корнели О.А., Бассетти М., Каландра Т., Гарбино Дж., Куллберг Б.Дж., Лортолари О., Меерсеман В., Акова М., Арендруп М.С., Арикан-Акдагли С., Билле Дж., Кастаньола Е., Куэнка-Эстрелла М., Доннелли JP, Groll AH, Herbrecht R, Hope WW, Jensen HE, Lass-Florl C, Petrikkos G, Richardson MD, Roilides E, Verweij PE, Viscoli C, Ullmann AJ (2012) Руководство ESCMID * по диагностике и лечению Candida заболеваний 2012: взрослые пациенты без нейтропении.Clin Microbiol Infect 18 [Дополнение 7]: 19–37. DOI: 10.1111 / 1469-0691.12039
PubMed Статья CAS Google Scholar
Calandra T, Bille J, Schneider R, Mosimann F, Francioli P (1989) Клиническое значение Candida , выделенного из брюшины у хирургических пациентов. Ланцет 2: 1437–1440
PubMed Статья CAS Google Scholar
Dupont H, Paugam-Burtz C, Muller-Serieys C, Fierobe L, Chosidow D, Marmuse JP, Mantz J, Desmonts JM (2002) Прогностические факторы смертности из-за полимикробного перитонита с выделением Candida в перитонеальной жидкости у критически больных пациенты. Arch Surg 137: 1341–1346 обсуждение 1347
PubMed Статья Google Scholar
Montravers P, Dupont H, Gauzit R, Veber B, Auboyer C, Blin P, Hennequin C, Martin C (2006) Candida как фактор риска смертности при перитоните.Crit Care Med 34: 646–652. DOI: 10.1097 / 01.ccm.0000201889.39443.d2
PubMed Статья Google Scholar
Бассетти М., Маркетти М., Чакрабарти А. и др. (2013) Программа исследований по лечению внутрибрюшного кандидоза: результаты консенсуса международных экспертов. Intensive Care Med. DOI: 10.1007 / s00134-013-3109-3
PubMed Google Scholar
Leroy O, Gangneux JP, Montravers P, Mira JP, Gouin F, Sollet JP, Carlet J, Reynes J, Rosenheim M, Regnier B, Lortholary O (2009) Эпидемиология, лечение и факторы риска смерти от инвазивной Candida инфекции в отделениях интенсивной терапии: многоцентровое проспективное обсервационное исследование, проведенное во Франции (2005–2006 гг.). Crit Care Med 37: 1612–1618. DOI: 10.1097 / CCM.0b013e31819efac0
PubMed Статья Google Scholar
Pittet D, Monod M, Suter PM, Frenk E, Auckenthaler R (1994) Колонизация Candida и последующие инфекции у тяжелобольных хирургических пациентов. Ann Surg 220: 751–758
PubMed Статья CAS Google Scholar
Соломкин JS, Mazuski JE, Брэдли JS, Родволд К.А., Голдштейн EJ, Барон EJ, О’Нил П.Дж., Чоу А.В., Деллинджер Е.П., Eachempati SR, Горбач С., Хилфикер М., Мэй А.К., Натенс А.Б., Sawyer RG, Bartlett JG (2010) Диагностика и лечение осложненной внутрибрюшной инфекции у взрослых и детей: рекомендации Общества хирургических инфекций и Общества инфекционных болезней Америки.Clin Infect Dis 50: 133–164. DOI: 10.1086 / 649554
PubMed Статья Google Scholar
Dupont H, Bourichon A, Paugam-Burtz C, Mantz J, Desmonts JM (2003) Можно ли предсказать выделение дрожжей в перитонеальной жидкости у пациентов отделения интенсивной терапии с перитонитом? Crit Care Med 31: 752–757. DOI: 10.1097 / 01.CCM.0000053525.49267.77
PubMed Статья Google Scholar
Eggimann P, Francioli P, Bille J, Schneider R, Wu MM, Chapuis G, Chiolero R, Pannatier A, Schilling J, Geroulanos S, Glauser MP, Calandra T (1999) Профилактика флуконазолом предотвращает внутрибрюшной кандидоз в группе высокого риска хирургические пациенты. Crit Care Med 27: 1066–1072
PubMed Статья CAS Google Scholar
Сенн Л., Эггиманн П., Ксонтини Р., Паскуаль А., Демартинес Н., Билле Дж, Каландра Т., Маркетти О. (2009) Каспофунгин для профилактики внутрибрюшного кандидоза у хирургических пациентов с высоким риском.Intensive Care Med 35: 903–908. DOI: 10.1007 / s00134-009-1405-8
PubMed Статья Google Scholar
Montravers P, Mira JP, Gangneux JP, Leroy O, Lortholary O (2011) Многоцентровое исследование противогрибковых стратегий и результатов Candida spp. перитонит в реанимации. Clin Microbiol Infect 17: 1061–1067. DOI: 10.1111 / j.1469-0691.2010.03360.x
PubMed Статья CAS Google Scholar
Eggimann P, Ostrosky-Zeichner L (2010) Стратегии раннего противогрибкового вмешательства у пациентов в отделении интенсивной терапии. Curr Opin Crit Care 16: 465–469. DOI: 10.1097 / MCC.0b013e32833e0487
PubMed Статья Google Scholar
Леон С., Руис-Сантана С., Сааведра П., Кастро С., Убеда А., Лоза А., Мартин-Мазуэлос Е., Бланко А., Херес В., Баллус Дж., Альварес-Роча Л., Утанде-Васкес А., Farinas O (2012) Значение бета-d-глюкана и антитела к зародышевой трубке Candida albicans для различения колонизации Candida и инвазивного кандидоза у пациентов с тяжелыми абдоминальными состояниями.Intensive Care Med 38: 1315–1325. DOI: 10.1007 / s00134-012-2616-y
PubMed Статья CAS Google Scholar
Леон С., Руис-Сантана С., Сааведра П., Гальван Б., Бланко А., Кастро С., Баласини С., Утанде-Васкес А., Гонсалес де Молина Ф. Дж., Бласко-Навальпрото М. А., Лопес М. Дж., Чарльз П. Е., Martin E, Hernandez-Viera MA (2009). Полезность « баллов Candida » для различения колонизации Candida и инвазивного кандидоза у критически больных пациентов без нейтропении: проспективное многоцентровое исследование.Crit Care Med 37: 1624–1633. DOI: 10.1097 / CCM.0b013e31819daa14
PubMed Статья Google Scholar
Posteraro B, De Pascale G, Tumbarello M, Torelli R, Pennisi MA, Bello G, Maviglia R, Fadda G, Sanguinetti M, Antonelli M (2011) Ранняя диагностика кандидемии у пациентов отделения интенсивной терапии с сепсисом : проспективное сравнение (1 → 3) -бета-d-глюкана, оценка Candida и индекс колонизации.Crit Care 15: R249. DOI: 10.1186 / cc10507
PubMed Статья Google Scholar
Tissot F, Lamoth F, Hauser PM, Orasch C, Fluckiger U, Siegemund M, Zimmerli S, Calandra T, Bille J, Eggimann P, Marchetti O (2013) Бета-глюкановая антигенемия предполагает диагностику посева крови -отрицательный внутрибрюшной кандидоз. Am J Respir Crit Care Med. DOI: 10.1164 / rccm.201211-2069OC
PubMed Google Scholar
Семейный кандидоз: MedlinePlus Genetics
Семейный кандидоз — это наследственная тенденция к развитию инфекций, вызываемых грибком Candida .У больных обычно есть инфекции кожи, ногтей и влажной оболочки полостей тела (слизистых оболочек). Эти инфекции являются повторяющимися и постоянными, а это означает, что они возвращаются повторно и могут длиться долгое время. Этот тип инфекции называется хроническим кандидозом слизистых оболочек кожи.
Кандида обычно присутствует на коже и слизистых оболочках и у большинства людей обычно не вызывает проблем со здоровьем. Однако некоторые лекарства (например, антибиотики и кортикостероиды) и другие факторы могут приводить к случайному чрезмерному росту Candida (кандидоз) во рту (где он известен как молочница) или во влагалище.Эти эпизоды, обычно называемые дрожжевыми инфекциями, обычно длятся недолго, прежде чем будут устранены здоровой иммунной системой.
Большинство людей с семейным кандидозом страдают хроническими или рецидивирующими дрожжевыми инфекциями, которые начинаются в раннем детстве. Кожные инфекции приводят к появлению сыпи с твердыми утолщенными пятнами; Когда эти пятна появляются на коже головы, они могут вызвать потерю волос в пораженной области (рубцовая алопеция). Кандидоз ногтей может привести к образованию толстых, потрескавшихся и обесцвеченных ногтей, а также к опуханию и покраснению окружающей кожи.Молочница и желудочно-кишечные симптомы, такие как вздутие живота, запор или диарея, часто встречаются у больных. У женщин с семейным кандидозом могут часто развиваться вагинальные дрожжевые инфекции, а у младенцев могут быть грибковые инфекции на коже, которые вызывают стойкую опрелость.
В зависимости от генетического изменения, связанного с этим состоянием, некоторые пораженные люди подвержены риску развития системного кандидоза, более тяжелого состояния, при котором инфекция распространяется через кровоток к различным органам, включая головной мозг и мозговые оболочки, которые представляют собой покрывающие мембраны головной и спинной мозг.Системный кандидоз может быть опасным для жизни.
Хронические или рецидивирующие дрожжевые инфекции могут возникать у людей без семейного кандидоза. У некоторых людей рецидивирующий кандидоз является частью общей предрасположенности к инфекциям, потому что их иммунная система ослаблена таким заболеванием, как синдром приобретенного иммунодефицита (СПИД) или тяжелый комбинированный иммунодефицит (SCID), лекарствами или другими факторами.

 Продолжительность лечения 7 — 14 дней и более.
Продолжительность лечения 7 — 14 дней и более.
 , Лешкова В. М. и др. Медофлюкон (флуконазол) — последнее достижение в лечении микозов//Медико-фармацевтический вестник. 1996. № 9 — 10. С. 23 — 27.
, Лешкова В. М. и др. Медофлюкон (флуконазол) — последнее достижение в лечении микозов//Медико-фармацевтический вестник. 1996. № 9 — 10. С. 23 — 27. 1987. P. 77 — 79.
1987. P. 77 — 79.
 муцин гликопротеин стенки эпителиальной клетки преставляет собой защитный барьер для прикрепления грибов к слизистой оболочке. Однако муцин расчепляется под воздействием факторов агрессии кандид.
муцин гликопротеин стенки эпителиальной клетки преставляет собой защитный барьер для прикрепления грибов к слизистой оболочке. Однако муцин расчепляется под воздействием факторов агрессии кандид. Нарушается микрофлора в кишечнике, что способствует развитию кандидоза;
Нарушается микрофлора в кишечнике, что способствует развитию кандидоза; К ним относят инвазивный и неинвазивный.
К ним относят инвазивный и неинвазивный.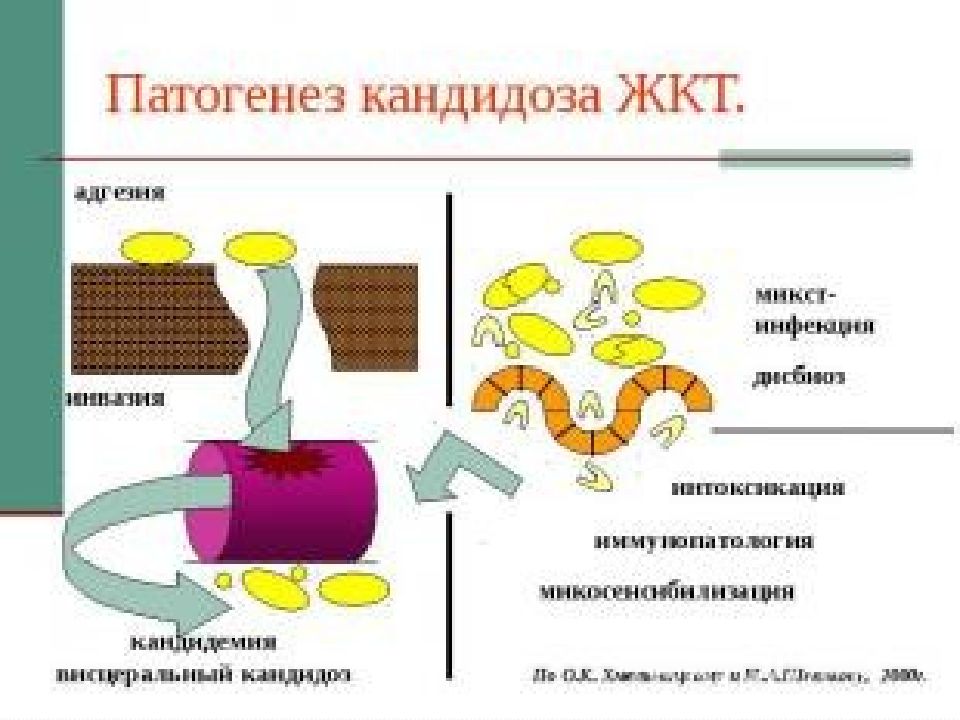 Это связано с местным иммунитетом органов.
Это связано с местным иммунитетом органов. Также возможна клиника неспецифического язвенного колита;
Также возможна клиника неспецифического язвенного колита; Данные манипуляции могут позволить избежать такого явления, как хронический кандидоз. Некоторые из штаммов кандид проявляют высокую устойчивость к противогрибковым препаратам, таким как амфотерицин или флуконазол.
Данные манипуляции могут позволить избежать такого явления, как хронический кандидоз. Некоторые из штаммов кандид проявляют высокую устойчивость к противогрибковым препаратам, таким как амфотерицин или флуконазол.