где находится в организме, ее функции и строение, профилактика заболеваний печени
Печень человека – один из самых важных органов, выполняющих чрезвычайно ответственные функции. Люди, не имеющие отношения к медицине, не слишком хорошо осведомлены о том, какую именно роль играет печень и к чему могут привести сбои в ее работе. В нашей статье мы выясним, за что отвечает печень в организме, что для нее вредно, и чем ей можно помочь в случае возникновения патологий.
Строение и расположение печени у человека
Печень человека располагается под диафрагмой и занимает большую часть верхнего правого отдела брюшной полости. Именно поэтому симптомом практически всех заболеваний печени является выраженная боль или дискомфорт в области правого подреберья. Сама печень не имеет болевых рецепторов, и все эти неприятные ощущения в «правом боку» вызывает увеличение размера органа и растяжение его капсулы, спровоцированного различными поражениями. Основной единицей печени является так называемая печеночная долька, у человека в среднем может насчитываться до 100 000 таких долек, каждая из которых состоит из особых клеток – гепатоцитов.
Свои особенности имеет кровоснабжение печени. В нем участвует не только артерия, по которой в печень поступает насыщенная кислородом кровь, и вены, транспортирующие кровь от печени, но и особая воротная вена, несущая к печени кровь из желудка, кишечника, желчного пузыря и селезенки.
Кстати, желчный пузырь – это особый орган в форме небольшого мешочка, который находится на нижней правой части нижней доли печени и в котором хранится неизрасходованная часть желчи. Одна из функций печени, пищеварительная, тесно связана с работой этого органа.
Функции органа
- Защита организма от токсинов, бактерий и инфекций. По сути, печень играет роль некоего «очистительного сооружения». Вместе с почками она очищает кровь и нейтрализует и удаляет все токсины, которые попадают в организм через кишечник, например, с приемом алкоголя или медикаментов или образуются в ходе реакций распада.
 А пропуская через себя всю кровь человека, она обезвреживает большинство попавших извне бактерий.
А пропуская через себя всю кровь человека, она обезвреживает большинство попавших извне бактерий. - Участие в пищеварении. Печень вырабатывает желчь, без которой пищеварение практически невозможно, поскольку именно желчь отвечает за расщепление жиров в кишечнике, а также стимулирует его двигательную функцию.
- Накопление питательных веществ. Печень способна депонировать витамины и минералы и при необходимости высвобождать их, поддерживая организм. Кроме того, некоторые вещества она преобразует в витамины самостоятельно, например, получаемый с пищей каротин в печени преобразуется в витамин А.

- Участие в обменных процессах. Печень участвует в метаболизме жиров, белков и углеводов. Она также способна сама вырабатывать некоторые жизненно необходимые организму белки, например, альбумин, благодаря которому кровь не покидает кровяного русла, некоторые белки, которые отвечают за перенос гормонов к местам из назначения и отдельные факторы свертываемости крови
Это интересно!
Печень человека – весьма крупный орган. Его вес может доходить до 1/40 части массы тела у взрослого и 1\20 части у новорожденного младенца.
Основные заболевания
Самыми распространенными заболевания печени специалисты сегодня считают гепатит (воспаление печени), гепатоз и цирроз.
Термин «гепатит» объединяет некоторые хронические и острые воспалительные заболевания органа, имеющие различную этиологию. Основной причиной гепатита является вирусная инфекция, медицине известны несколько типов вирусного гепатита, но наиболее распространенными являются три типа — А, В и С, последний из которых является самым опасным – у 20 % больных развиваются цирроз или рак печени.
Гепатоз вызывается скоплением жира в печени, чаще всего она поражает людей 40 – 56 лет. Нередко гепатоз развивается при наличии у человека сахарного диабета и ожирения. В группу риска входят и те, кто имеет даже небольшой лишний вес и не придерживаются принципов здорового питания, предпочитая жирную и жареную пищу, а также люди, злоупотребляющие алкоголем
Цирроз печени –

На заметку
По статистике у людей с лишним весом в 5% случаев развивается цирроз, а в 65% — жировая дистрофия печени.
Причины патологических процессов
Причинить вред печени и в целом здоровью человека могут различные факторы. Поговорим о самых распространенных из них.
Алкоголь и токсины
Алкогольные и токсические поражения печени, по статистике, являются причиной 40-50 % всех патологий. Печень способна расщеплять алкоголь, но в случае злоупотребления она просто не способна справиться с его объемом, к тому же для гепатоцитов этиловый спирт является настоящим ядом, поскольку способствует росту соединительной ткани, ведущему к фиброзу. В большинстве случаев алкоголь вызывает жировое поражении печени, алкогольный гепатит и фиброз. Без надлежащего лечения и отказа от употребления спиртного эти заболевания могут постепенно трансформироваться в цирроз.
Кстати, в быту существует немало мифов об алкоголе и его влиянии на состояние печени. Например, некоторые «специалисты» утверждают, что от небольшой дозы спиртного вреда не будет, что нужно пить только качественные напитки и после приема алкоголя обязательно проводить реабилитацию народными средствами, включая и стопку водки. Все это опасные заблуждения. Печень и алкоголь — понятия практически несовместимые, безопасной дозы для органа просто не существует. Условно безопасная дневная доза, рассчитанная ВОЗ, составляет приблизительно 20 г этилового спирта в сутки – это соответствует небольшой рюмке коньяка или водки, бокалу вина или бутылочке пива. При этом берется в расчет, что алкоголь имеет самое высокое качество,
Например, некоторые «специалисты» утверждают, что от небольшой дозы спиртного вреда не будет, что нужно пить только качественные напитки и после приема алкоголя обязательно проводить реабилитацию народными средствами, включая и стопку водки. Все это опасные заблуждения. Печень и алкоголь — понятия практически несовместимые, безопасной дозы для органа просто не существует. Условно безопасная дневная доза, рассчитанная ВОЗ, составляет приблизительно 20 г этилового спирта в сутки – это соответствует небольшой рюмке коньяка или водки, бокалу вина или бутылочке пива. При этом берется в расчет, что алкоголь имеет самое высокое качество,
все органы человека, включая и печень, абсолютно здоровы, а сам он как минимум два дня в неделю вообще не употребляет спиртные напитки. Для женщин «условно безопасная доза» еще меньше.
При этом термин «условно безопасная» отнюдь не значит полезная или рекомендуемая. Для печени даже самое минимальное количество алкоголя – это тяжелая работа и несомненный вред, а при употреблении ее хозяином нескольких рюмок она начинает работать в режиме перегрузок, теряя собственные клетки.
Инфекции
Как уже было сказано, инфекции, такие как вирусный гепатит, являются причиной опасных вирусных заболеваний органа. Гепатитом А можно заразиться через грязную воду или продукты питания, но этот тип болезни относительно легко поддается терапии и к тому же не вызывает в печени необратимых изменений. Два других типа — В и С распространяются по организму с кровью и прочими жидкостями, часто переходят в хроническую форму и вызывают цирроз.
Неправильное питание
Столь любимый многими, особенно молодежью, фастфуд, жареная и жирная пища, однообразный рацион без овощей и фруктов легко приводят к набору лишнего веса и недостатку в организме необходимых для правильного функционирования печени набору витаминов групп В, С, D и А. При этом нужно помнить, что вред может нанести не только лишний вес, но и резкое похудение. На потерю веса в короткий срок организм реагирует как на сигнал тревоги и срочно начинает копить жиры и углеводы, а значит на печень ложится дополнительная нагрузка.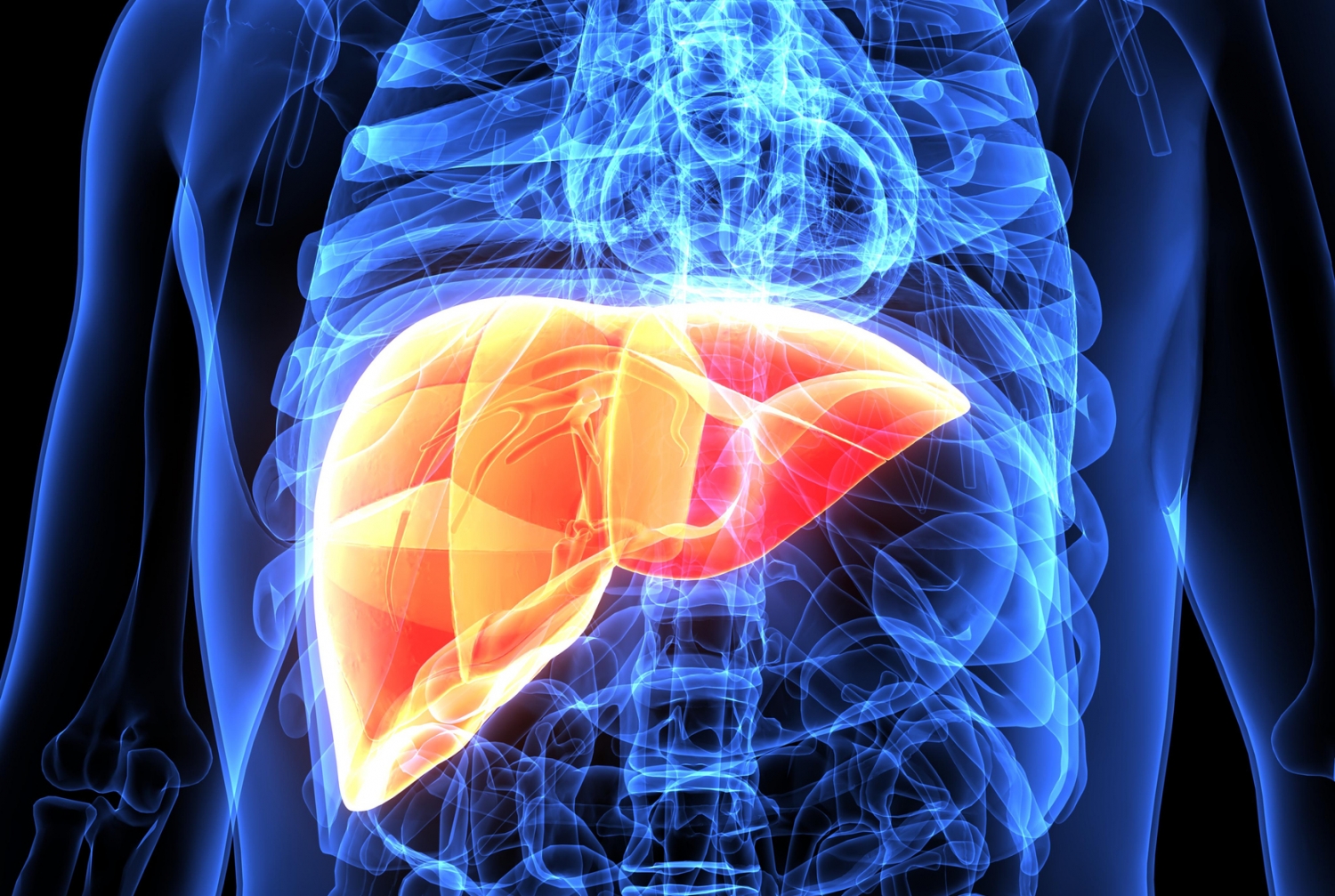
Сахарный диабет
Сахарный диабет практически всегда сопровождается печеночной недостаточностью и жировым гепатозом. Это вызвано тем, что заболевание провоцирует выход из-под контроля процесса расщепления жиров, что ведет к накопление их в клетках самой печени.
Признаки больной печени
Диагностировать заболевание печени может и должен только врач и только по итогам проведенных исследований и анализов. Но и сам больной должен проявить бдительность и обратиться к специалисту в случае появления некоторых симптомов.
Астения. Человек начинает быстро утомляться, постоянно испытывает слабость, сонливость. Это первые признаки сбоев в работе печени из-за нарушения вывода их организма продуктов азотистого обмена.
Боль. Как мы уже говорили, печень не имеет нервных окончаний, и сама она не болит. Но в результате некоторых поражений орган увеличиваете в размерах и начинает давить на капсулу, в которой находится. Именно в этой капсуле и находятся болевые рецепторы, которые создают ощущение боли. Сначала это может быть только чувство тяжести в правом подреберье, затем оно переходит в ноющую боль, усиливающуюся после еды. Если боль нарастает ежедневно, то это может говорить о наличии кисты или опухоли. Острая, невыносимая боль, иногда охватывающая всю брюшную полость, является симптомом желчнокаменной болезни, во время которой желчные протоки перекрываются камнями.
Именно в этой капсуле и находятся болевые рецепторы, которые создают ощущение боли. Сначала это может быть только чувство тяжести в правом подреберье, затем оно переходит в ноющую боль, усиливающуюся после еды. Если боль нарастает ежедневно, то это может говорить о наличии кисты или опухоли. Острая, невыносимая боль, иногда охватывающая всю брюшную полость, является симптомом желчнокаменной болезни, во время которой желчные протоки перекрываются камнями.
Проблемы с пищеварением. Из-за неправильного функционирование печени возникают и сложности с перевариванием пищи. Нередко больные жалуются на тошноту, метеоризм, диарею, горький или кислый привкус во рту.
Желтуха. Желтый цвет белков глаз и кожи человека всегда свидетельствует о заболеваниях печени. Такой симптом связан с нарушением обмена билирубина или транспорта желчи.
Состояние кожных покровов. Поскольку больная печень не способна полноценно защищать организм от проникновения бактерий и токсинов, их отрицательное воздействие может отражаться на коже в виде сыпи и прыщей. Еще одни признак болезней печени — сосудистые звездочки, которые появляются из-за нарушения свёртываемости крови и увеличивающейся хрупкости кровеносных сосудов.
Еще одни признак болезней печени — сосудистые звездочки, которые появляются из-за нарушения свёртываемости крови и увеличивающейся хрупкости кровеносных сосудов.
Профилактика болезней печени
Как можно защитить печень от отрицательных воздействий и помочь ей качественно выполнять работу по защите организма?
Во-первых, необходимо полностью пересмотреть, а при необходимости и изменить, режим питания. Откажитесь от продуктов, оказывающих негативное влияние на орган. В это список входят жирные и жареные блюда, трансжиры, уксус, специи, белый хлеб и сладкая выпечка, жирные молочные продукты, грибы, алкоголь. В рацион рекомендуется включить больше овощей и фруктов, макароны, крупы, нежирное мясо и рыба в отварном или запеченном виде, зерновой хлеб. Кстати, японцы, которые в основном едят рис, овощи и морепродукты, гораздо менее подвержены заболеваниям печени, чем американцы и европейцы.
Во-вторых, стоит позаботиться о своем весе. Лишний вес или ожирение для печени очень вредны, но и в этом вопросе не стоит действовать слишком агрессивно. Помним, что резкое похудение также очень негативно влияет на работу печени.
Помним, что резкое похудение также очень негативно влияет на работу печени.
В-третьих, нельзя принимать медикаменты без назначения врача. Никогда и никакие. Это особенно актуально для россиян, поскольку все мы очень любим заниматься самолечением, а некоторые таблетки дают очень серьезную нагрузку на печень, особенно антибиотики.
В-четвертых, необходимо по возможности защитится от воздействия токсинов. Их источниками могут быть самые простые вещи – отделочные и ремонтные материалы, бытовая химия, пластиковая посуда, синтетические ткани.
Тем не менее, избежать всех факторов риска, конечно, невозможно. Но можно помочь печени справляться с ними, принимая специальные препараты – гепатопротекторы. Они позволяют укрепить ее органа и минимизировать тот вред, который человек ежедневно наносит своему организму.
Профилактические препараты
Гепатопротекторы используются не для лечения заболеваний, а для их профилактики и улучшения функционирования печени. На рынке сегодня присутствует очень много различных видов гепатопротекторов, но особенно популярны те, в составе которых содержатся эссенциальные фосфолипиды. Это вещества растительного происхождения, сходные с теми фосфолипидами, которые в человеческом теле являются основой для строительства клеточных мембран.
На рынке сегодня присутствует очень много различных видов гепатопротекторов, но особенно популярны те, в составе которых содержатся эссенциальные фосфолипиды. Это вещества растительного происхождения, сходные с теми фосфолипидами, которые в человеческом теле являются основой для строительства клеточных мембран.
Препараты с фосфолипидами восстанавливают поврежденные клетки печени и помогают в их регенерации. Но сами по себе фосфолипиды не способны справиться с воспалением, являющимся причиной повреждения печени. Поэтому особенно эффективна комбинация веществ, которая останавливает воспалительный процесс и одновременно занижает гепатоциты от разрушения. Одним из эффективных сочетаний является сочетание фосфолипидов и глицирризиновой кислоты, в природе она встречается в корне солодки. Эта кислота не только способна устранять вопленице (кстати, это свойство солодки отмечено давно и широко используется в медицине), но оказывает хорошее антифибротическое и антиоксидантное воздействие на ткани и органы. Эффективность сочетания эссенциальных фосфолипидов и глицирризиновой кислоты доказана в ходе ряда клинических исследований и во врачебной практике. Комбинация на основе этих двух веществ включена в российский перечень жизненно необходимых и важнейших лекарственных средств в раздел «Препараты для лечения заболеваний печени».
Эффективность сочетания эссенциальных фосфолипидов и глицирризиновой кислоты доказана в ходе ряда клинических исследований и во врачебной практике. Комбинация на основе этих двух веществ включена в российский перечень жизненно необходимых и важнейших лекарственных средств в раздел «Препараты для лечения заболеваний печени».
Вся информация, касающаяся здоровья и медицины, представлена исключительно в ознакомительных целях и не является поводом для самодиагностики или самолечения.
Что такое печень и зачем она нужна?
Что такое печень и зачем она нужна?
Печень уникальный орган, функции которого не дублируются организмом.
Важнейшие функции печени:
- обезвреживание токсических веществ;
- регуляция поступления в организм аминокислот, белков, углеводов, жиров и витаминов из пищи;
- участие в выработке желчи, необходимой для расщепления жиров;
- продуцирование различных элементов и ферментов крови;
-
непосредственная регуляция кровяного тока.

Значительное угнетение даже одной из основных функций печени ведёт к гибели всего организма.
Большинство случаев гепатита вызывается вирусами, но нередко к нему приводят другие инфекции, а также воздействие токсинов, например, алкоголя, наркотиков, некоторых химикатов и лекарственных препаратов, способных вызывать воспаление печени.
Развитию рака печени в высокой степени способствует хронический вирусный гепатит В, паразитарные заболевания печени, воздействие на организм ядов химической промышленности, образ жизни и вредные привычки — именно алкоголизм.
Гепатит – это воспалительное заболевание, разрушающее клетки печени и нарушающее ее функционирование.
Как гепатит влияет на печень?
Хронические гепатиты В и С могут переходить в тяжёлое заболевание – цирроз печени, а также быть причиной первичного рака печени.
Из общего числа случаев рака печени возникновение более половины случаев связано с инфицированием вирусом гепатита В, четверть – с инфицированием вирусом гепатита С и 22% по другой причине.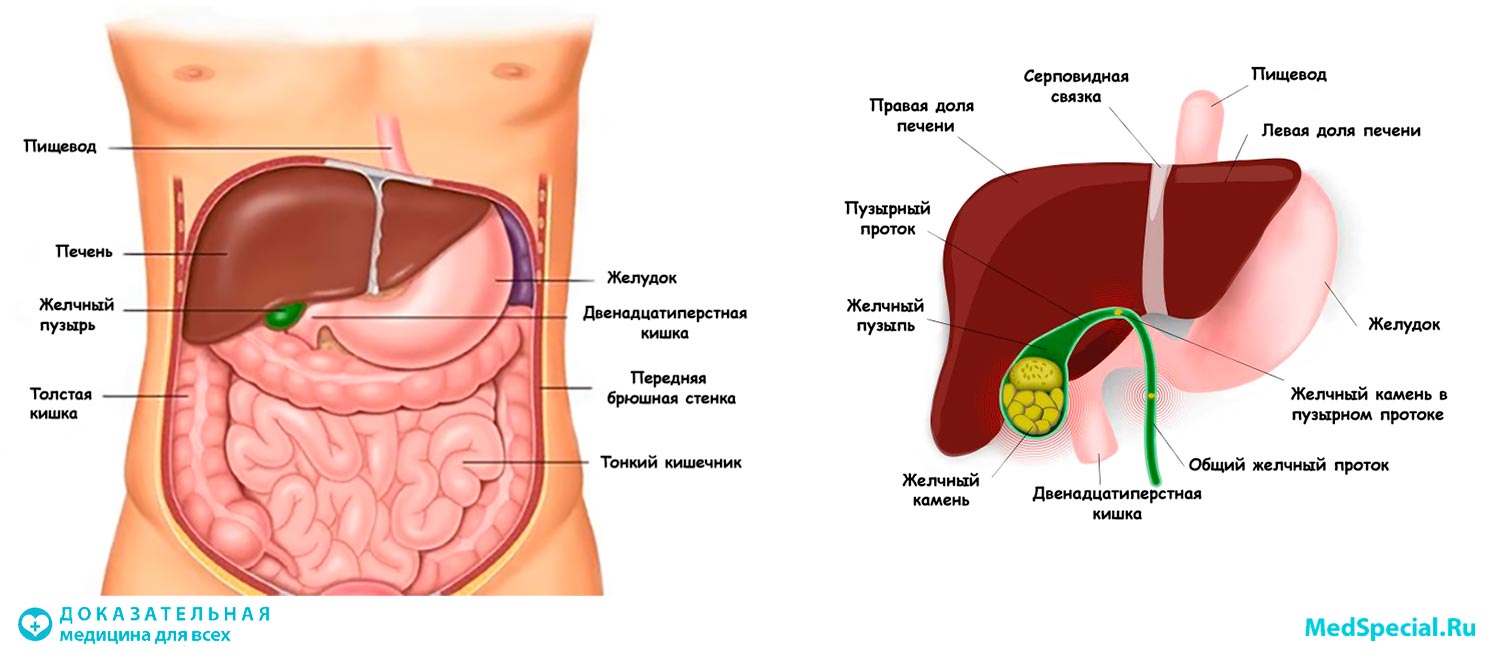
С этими вирусами ассоциированы гепатоцеллюлярные карциномы, которые составляют 4,5% всех опухолей, при этом риск развития карцином у мужчин в 100 раз выше, чем у женщин.
Гепатоцеллюлярные карциномы с высокой частотой (38%) ассоциированы с циррозом, возникшим в результате хронической инфекции вирус гепатита В. 5-10% карцином возникает при алкогольном циррозе печени.
У пациентов, инфицированных вирусом гепатита С, клинические и биохимические признаки острого гепатита могут и не развиваться, но они становятся вирусоносителями.
Рак печени, как и любое злокачественное образование в организме человека, вызывает общую слабость, гиподинамию, снижение аппетита, анемию, тошноту и рвоту и, как следствие, потерю веса.
При появлении даже незначительных симптомов, необходимо обязательно обращаться к врачу.
По материалам: «Вирусы, онкогенные для человека.» Гурцевич В.Э , профессор , ГУ «Российский онкологический научный центр» им. Н.Н. Блохина РАМН. Информационный бюллетень «Первичная профилактика рака», №1(3), 2006.
Н.Н. Блохина РАМН. Информационный бюллетень «Первичная профилактика рака», №1(3), 2006.
Печень и ее функции в организме человека
Название «печень» происходит от слова «печь», т.к. печень обладает самой высокой температурой из всех органов живого тела. С чем это связано? Скорее всего с тем, что в печени на единицу массы происходит самое высокое количество образования энергии. До 20% массы всей клетки печени занимают митохондрии, «силовые станции клетки», которые непрерывно образуют АТФ, распределяющуюся по всему организму.
Вся ткань печени состоит из долек. Долька — это структурная и функциональная единица печени. Пространство между печеночными клетками представляют собой желчные ходы. В центре дольки проходит вена, в междольковой ткани проходят сосуды и нервы.
Печень как орган состоит из двух неравных больших долей: правой и левой. Правая доля печени намного больше левой, поэтому она так легко прощупывается в правом подреберье. Правая и левая доли печени сверху разделяются серповидной связкой, на которой как бы «подвешена» печень, а внизу правая и левая доли разделены глубокой поперечной бороздой. В этой глубокой поперечной борозде находятся так называемые ворота печени, в этом месте в печень входят сосуды и нервы, выходят отводящие желчь печеночные протоки. Малые печеночные протоки постепенно объединяются в один общий. Общий желчный проток, включает в себя проток желчного пузыря — специального резервуара, в котором накапливается желчь. Общий желчный проток впадает в 12-ти перстную кишку, почти в том же самом месте, где впадает в нее проток поджелудочной железы.
Правая и левая доли печени сверху разделяются серповидной связкой, на которой как бы «подвешена» печень, а внизу правая и левая доли разделены глубокой поперечной бороздой. В этой глубокой поперечной борозде находятся так называемые ворота печени, в этом месте в печень входят сосуды и нервы, выходят отводящие желчь печеночные протоки. Малые печеночные протоки постепенно объединяются в один общий. Общий желчный проток, включает в себя проток желчного пузыря — специального резервуара, в котором накапливается желчь. Общий желчный проток впадает в 12-ти перстную кишку, почти в том же самом месте, где впадает в нее проток поджелудочной железы.
Кровообращение печени не похоже на кровообращение других внутренних органов. Как все органы, печень снабжается артериальной кровью, насыщенной кислородом из печеночной артерии. Через нее оттекает венозная кровь, бедная кислородом и богатая углекислым газом, и впадает в воротную вену. Однако помимо этого, обычного для всех органов кровообращения, печень получает большое количество крови, оттекающей от всего желудочно-кишечного тракта. Все, что всасывается в желудке, 12-ти перстной кишке, тонком и толстом кишечнике, собирается в большую воротную вену и впадает в печень.
Все, что всасывается в желудке, 12-ти перстной кишке, тонком и толстом кишечнике, собирается в большую воротную вену и впадает в печень.
Цель воротной вены не в том, чтобы снабдить печень кислородом и избавить от углекислого газа, а в том, чтобы пропустить через печень все питательные (и не питательные) вещества, которые всосались на протяжении всего желудочно-кишечного тракта. Сначала через воротную вену они проходят через печень, а потом уже в печени, претерпев определенные изменения, всасываются в общий кровоток. На долю воротной вены приходится 80% крови, получаемой печенью. Кровь воротной вены имеет смешанный характер. Она содержит как артериальную, так и венозную кровь, оттекающую от желудочно-кишечного тракта. Таким образом в печени имеются 2 капиллярные системы: обычная, между артериями и венами и капиллярная сеть воротной вены, которую иногда называют «чудесной сетью». Обычная и капиллярная чудесная сеть соединяются между собой.
Симпатическая иннервация
Иннервируется печень из солнечного сплетения и ветвями блуждающего нерва (парасимпатическая импульсация).
Через симпатические волокна стимулируется образование мочевины по парасимпатическим нервам передаются импульсы, усиливающие желчеотделение, способствующие накопление гликогена.
Печень иногда называют самой крупной эндокринной железой организма, но это не совсем верно. Печень выполняет и эндокринные выделительные функции, а также принимает участие в пищеварении.
Продукты расщепления всех питательных веществ образуют в известной степени, общий резервуар обмена веществ, который весь проходит через печень. Из этого резервуара организм по мере необходимости синтезирует необходимые вещества и расщепляет ненужные.
Углеводный обмен
Глюкоза и другие моносахариды, поступающие в печень, превращаются ею в гликоген. Гликоген откладывается в печени как «сахарный резерв». В гликоген помимо моносахаридов превращается и молочная кислота, продукты расщепления белков (аминокислоты), жиров (триглицериды и жирные кислоты). Все эти вещества начинают превращаться в гликоген в том случае, если углеводов в пище не хватает.
По мере необходимости, при расходовании глюкозы гликоген здесь же в печени превращается в глюкозу и поступает в кровь. Содержание гликогена в печени независимо от приема пищи подвержено определенному ритмическому колебанию в течение суток. Наибольшее количество гликогена содержится в печени ночью, наименьшее — в течении дня. Это связано с активным расходом энергии днем и образованием глюкозы. Синтез гликогена из других углеводов и расщепление до глюкозы имеет место как в печени, так и в мышцах. Однако образование гликогена из белка и жира возможно только в печени, в мышцах этот процесс не протекает.
Пировиноградная кислота и молочная, жирные кислоты и кетоновые тела — то, что называют токсинами усталости — утилизируются в основном в печени и преобразуются в глюкозу. В организме высоктренированного спортсмена более 50% всей молочной кислоты преобразуется в печени в глюкозу.
Только в печени происходит «цикл трикарбоновых кислот», которые иначе называют «циклом Кребса» по имени английского биохимика Кребса, который, кстати говоря, жив до сих пор. Ему принадлежат классические труды по биохимии, в т.ч. и современный учебник.
Ему принадлежат классические труды по биохимии, в т.ч. и современный учебник.
Сахарный галлостаз необходим для нормальной деятельности всех систем и органом. В норме количество углеводов в крови составляет 80-120 мг% (т.е. мг на 100 мл крови), и их колебания не должны превышать 20-30 мг%. Значительное понижение содержания углеводов в крови (гипогликемия), а также стойкое повышение их содержания (гипергликемия) могут привести к тяжелым для организма последствиям.
Во время всасывания сахара из кишечника, содержание глюкозы в крови воротной вены может достигать 400 мг%. Содержание сахара в крови печеночной вены и в периферической крови повышается при этом лишь незначительно и редко достигает 200 мг%. Повышение содержания сахара в крови сразу включает «регуляторы», встроенные в печень. Глюкоза превращается, с одной стороны, в гликоген, который ускоряется, с другой стороны, она используется для получения энергии, а если и после этого остается избыток глюкозы, то она превращается в жир.
В последнее время появились данные о способности образования из глюкозы заменителя аминокислот, однако процесс носит в организме органический характер и развивается только в организме высококвалифицированных спортсменов. При понижении уровня глюкозы (длительное голодание, большой объем физических нагрузок) в печени происходит расщепление глюкогена, а если этого недостаточно, то превращаются в сахар аминокислоты и жиры, которые затем превращаются в гликоген.
Глюкозорегулитарная функция печени поддерживается механизмами нейрогуморальной регуляции (регуляция с помощью нервной и эндокринной системы). Содержание сахара в крови повышается адреналином, глюкозеном, тироксином, глюкокортикоидами и диабетогенными факторами гипофиза. При определенных условиях стабилизующим влиянием на сахарный обмен обладают половые гормоны.
Уровень сахара в крови понижается инсулином, который через систему воротной вены сначала попадает в печень и только оттуда в общее кровообращение. В норме антагонистические эндокринные факторы находятся в состоянии равновесия. При гипергликемии усиливается секреция инсулина, при гипогликемии — адреналина. Свойством повышать содержание сахара в крови обладает глюкагон — гормон, секретирующий а-клетками отростков поджелудочной железы.
При гипергликемии усиливается секреция инсулина, при гипогликемии — адреналина. Свойством повышать содержание сахара в крови обладает глюкагон — гормон, секретирующий а-клетками отростков поджелудочной железы.
Глюкозостатическая функция печени может подвергаться и прямому нервному воздействию. Центральная нервная система может вызвать гипергликемию как гуморальным путем, так и рефлекторно. Некоторые опыты свидетельствуют о том, что в печени существует так же система автономной регуляции уровня сахара в крови.
Белковый обмен
Роль печени в белковом обмене заключается в расщеплении и «перестройке» аминокислот, образовании химически нейтральной мочевины из токсичного для организма аммиака, а также в синтезе белковых молекул. Аминокислоты, которые всасываются в кишечнике и образуются при расщеплении тканевого белка, составляют «резервуар аминокислот» организма, который может служить как источником энергии, так и строительным материалом для синтеза белков. Изотопными методами было установлено, что в организме человека в стуки расщепляется и вновь синтезируется 80-100 г белка. Приблизительно половина этого белка трансформируется в печени. Об интенсивности белковых превращений в печени можно судить по тому, что белки печени обновляются примерно за 7 (!) дней. В других органах этот процесс происходит как минимум за 17 дней. В печени содержится так называемый «резервный белок», который идет на нужды организма в том случае, если не хватает белка с пищей. При двухдневном голодании печень теряет примерно 20% своего белка, в то время, как общая потеря белка всех других органов составляет только около 4%.
Приблизительно половина этого белка трансформируется в печени. Об интенсивности белковых превращений в печени можно судить по тому, что белки печени обновляются примерно за 7 (!) дней. В других органах этот процесс происходит как минимум за 17 дней. В печени содержится так называемый «резервный белок», который идет на нужды организма в том случае, если не хватает белка с пищей. При двухдневном голодании печень теряет примерно 20% своего белка, в то время, как общая потеря белка всех других органов составляет только около 4%.
Трансформация и синтез недостающих аминокислот могут происходить только в печени; даже если печень удалить на 80%, такой процесс, как дезаминирование, сохраняется. Образование заменимых аминокислот в печени идет через образование глютаминовой и аспарагиновой кислоты, которые служат как бы промежуточным звеном.
Избыточное количество той или иной аминокислоты подвергается снижению сначала до пировиноградной кислоты, а потом в цикле Кребса до воды и углекислого газа с образованием энергии, запасаемой в виде АТФ.
В процессе деземинирования аминокислот — отщепления от них аминогрупп, образуется большое количество токсичного аммиака. Печень преобразует аммиак в нетоксичную мочевину (карбамид), который затем почками выводится из организма. Синтез мочевины происходит только в печени и нигде больше.
Синтез белков плазмы крови — альбуминов и глобулинов происходит в печени. Если произошла кровопотеря, то при здоровой печени содержание белков плазмы крови очень быстро восстанавливается при больной печени такое восстановление значительно замедляется.
Жировой обмен
Печень может депонировать жира намного больше, чем гликогена. Так называемый «структурный липоид» — структурные липиды печени фосфолипиды и холестерин составляют 10-16% сухого вещества печени. Это количество довольно постоянно. Помимо структурных липидов печень имеет включения нейтрального жира, сходного по своему составу с жиром подкожной клетчатки. Содержание нейтрального жира в печени подвержено значительным колебаниям. В целом же, можно сказать, что печень имеет определенный жировой запас, который при дефиците нейтрального жира в организме может расходоваться на энергетические нужды. Жирные кислоты при дефиците энергии могут хорошо окисляться в печени с образованием энергии, запасаемой в виде АТФ. В принципе, жирные кислоты могут окисляться и в любых других внутренних органах, однако процентное соотношение будет таким: 60% печень и 40% все остальные органы.
В целом же, можно сказать, что печень имеет определенный жировой запас, который при дефиците нейтрального жира в организме может расходоваться на энергетические нужды. Жирные кислоты при дефиците энергии могут хорошо окисляться в печени с образованием энергии, запасаемой в виде АТФ. В принципе, жирные кислоты могут окисляться и в любых других внутренних органах, однако процентное соотношение будет таким: 60% печень и 40% все остальные органы.
Желчь, выделяемая печенью в кишечник, эмульгирует жиры, и только лишь в составе такой эмульсии жиры могут впоследствии всасываться в кишечнике.
Половина имеющегося в организме холестерина синтезируется в печени и лишь другая половина имеет пищевое происхождение.
Механизм окисления печенью жирных кислот был выяснен в начале нашего века. Он сводится к так называемому b-окислению. Окисление жирных кислот происходит до 2-го углеродного атома (b-атома). Получается более короткая жирная кислота и уксусная кислота, которая потом превращается в ацетоуксусную. Ацетоуксусная кислота превращается в ацетон, а новая b-окисленная кислота подвергается окислению с большим трудом. И ацетон и b-окисленная кислота объединяют под одним названием «кетоновые тела».
Ацетоуксусная кислота превращается в ацетон, а новая b-окисленная кислота подвергается окислению с большим трудом. И ацетон и b-окисленная кислота объединяют под одним названием «кетоновые тела».
Для расщепления кетоновых тел нужно достаточно большое количество энергии и при дефиците глюкозы в организме (голодание, диабет, длительные аэробные нагрузки) у человека изо рта может появиться запах ацетона. У биохимиков даже есть такое выражение: «жиры сгорают в огне углеводов». Для полного сгорания, полной утилизации жиров до воды и углекислого газа с образованием большого количества АТФ необходимо хотя бы небольшое количество глюкозы. Иначе процесс застопорится на стадии образования кетоновых тел, которые сдвигают рН крови в кислую сторону, вместе с молочной кислотой принимая участие в формировании усталости. Не зря их поэтому и называют «токсинами усталости».
На жировой обмен в печени влияют такие гормоны, как инсулин, АКТГ, диабетогенный фактор гипофиза, глюкокортикоиды. Действие инсулина способствует накоплению жира в печени. Действие АКТГ, диабетогенного фактора, глюкокортикоидов прямо противоположно. Одна из важнейших функций печени в жировом обмене — это образование жира и сахара. Углеводы — непосредственный источник энергии, а жиры — важнейшие запасы энергии в организме. Поэтому при избытке углеводов и, в меньшей степени белков, преобладает синтез жира, а при недостатке углеводов доминирует глюконеогенез (образование глюкозы) из белка и жира.
Действие АКТГ, диабетогенного фактора, глюкокортикоидов прямо противоположно. Одна из важнейших функций печени в жировом обмене — это образование жира и сахара. Углеводы — непосредственный источник энергии, а жиры — важнейшие запасы энергии в организме. Поэтому при избытке углеводов и, в меньшей степени белков, преобладает синтез жира, а при недостатке углеводов доминирует глюконеогенез (образование глюкозы) из белка и жира.
Холестериновый обмен
Холестериновые молекулы составляют структурный каркас всех без исключения клеточных мембран. Деление клеток без достаточного количества холестерина попросту невозможно. Из холестерина образуются желчные кислоты, т.е. по сути сама желчь. Из холестерина образуются все стероидные гормоны: глюкокортикоиды, минералокортикоиды, все половые гормоны.
Синтез холестерина, поэтому, генетически детерминирован. Холестерин может синтезироваться во многих органах, но, наиболее интенсивно синтезируется он в печени. К слову сказать, в печени, так же, происходит и расщепление холестерина. Часть холестерина выделяется с желчью в неизменном виде в просвет кишечника, но большая часть холестерина — 75% превращается в желчные кислоты. Образование желчных кислот — основной путь катаболизма холестерина в печени. Для сравнения скажем, что на все стероидные гормоны вместе взятые расходуется лишь 3% холестерина. С желчными кислотами у человека в сутки выделяется 1-1,5 г холестерина. 1/5 этого количества выделяется из кишечника наружу, а остальное вновь всасывается в кишечник и попадает в печень.
Часть холестерина выделяется с желчью в неизменном виде в просвет кишечника, но большая часть холестерина — 75% превращается в желчные кислоты. Образование желчных кислот — основной путь катаболизма холестерина в печени. Для сравнения скажем, что на все стероидные гормоны вместе взятые расходуется лишь 3% холестерина. С желчными кислотами у человека в сутки выделяется 1-1,5 г холестерина. 1/5 этого количества выделяется из кишечника наружу, а остальное вновь всасывается в кишечник и попадает в печень.
Витамины
Все жирорастворимые витамины (А, Д, Е, К и др.) всасываются в стенки кишечника только в присутствии желчных кислот, выделяемых печенью. Некоторые витамины (А, В1, Р, Е, К, РР и др.) депонируются печенью. Многие из них участвуют в химических реакция, происходящих в печени (В1, В2, В5, В12, С, К и др.). Часть витаминов активизируется в печени, подвергаясь в ней фосфорицированию (В1, В2, В6, холин и др.). Без фосфорных остатков эти витамины совершенно неактивны и часто нормальный витаминный баланс в организме больше зависит от нормального состояния печени, чем от достаточного поступления того или иного витамина в организм.
Как видим, в печени могут депонировать как жирорастворимые, так и водорастворимые витамины, только время депонирования жирорастворимых витаминов, конечно, несоизмеримо больше, нежели водорастворимых.
Обмен гормонов
Роль печени на метаболизм стероидных гормонов не ограничивается тем, что она синтезирует холестерины — основу, из которой затем образуются все стероидные гормоны. В печени все стероидные гормоны подвергаются инактивации, хотя образуются они и не в печени.
Распад стероидных гормонов в печени является ферментативным процессом. Большая часть стероидных гормонов инактивируется, соединяясь в печени с глюкуроновой жирной кислотой. При нарушении функции печени в организме в первую очередь повышается содержание гормонов коры надпочечников, которые не подвергаются полному расщеплению. Отсюда возникает очень много различных заболеваний. Больше всего накапливается в организме альдостерона — минералокортикоидного гормона, избыток которого приводит к задержке натрия и воды в организме. В результате возникают отеки, подъем артериального давления и т. д.
В результате возникают отеки, подъем артериального давления и т. д.
В печени в значительной степени происходит инактивация гормонов щитовидной железы, антидиуретического гормона, инсулина, половых гормонов. При некоторых заболеваниях печени мужские половые гормоны не разрушаются, а превращаются в женские. Особенно часто такое расстройство возникает после отравления метиловым спиртом. Сам по себе избыток андрогенов, вызванный введением большого количества их извне, может привести к усилению синтеза женских половых гормонов. Существует, очевидно, некий порог содержания андрогенов в организме, превышение которого приводит к превращению андрогенов в женские половые гормоны. Хотя, в последнее время появились публикации о том, что некоторые лекарственные препараты способны предотвратить превращение в печени андрогенов в эстрогены. Такие препараты называют блокаторами.
Помимо вышеперечисленных гормонов печень инактивирует нейромедиаторы (катехоламины, серотонин, гистамин и многие другие вещества). В некоторых случаях даже развитие психических заболеваний вызвано неспособностью печени инактивировать те или иные нейромедиаторы.
В некоторых случаях даже развитие психических заболеваний вызвано неспособностью печени инактивировать те или иные нейромедиаторы.
Микроэлементы
Обмен практически всех микроэлементов напрямую зависит от работы печени. Печень, например, оказывает влияние на всасывание железа из кишечника, она депонирует железо и обеспечивает постоянство его концентрации в крови. Печень — депо меди и цинка. Она принимает участие в обмене марганца, молибдена кобальта и других микроэлементов.
Желчеобразование
Желчь, вырабатываемая печенью, как мы уже говорили, принимает активное участие в переваривании жиров. Однако дело не ограничивается всего лишь их эмульгированием. Желчь активизирует жирорасщепляющий фермент липозу панкреатического и кишечного сока. Желчь также ускоряет всасывание в кишечнике жирных кислот, каротина, витаминов Р, Е, К, холестерина, аминокислот, солей кальция. Желчь стимулирует перистальтику кишечника.
За сутки печень вырабатывает не менее 1 л желчи. Желчь представляет собой зеленовато-желтую жидкость слабощелочной реакции. Главные компоненты желчи: соли желчных кислот, желчные пигменты, холестерин, лецитин, жиры, неорганические соли. Печеночная желчь содержит до 98% воды. По своему осмотическому давлению, желчь равна плазме крови. Из печени желчь по внутрипеченочным желчным ходам поступает в печеночный проток, оттуда ее непосредственно выделяется через пузырный проток попадает в желчный пузырь. Здесь происходит концентрация желчи вследствие всасывания воды. Плотность пузырной желчи 1,026-1,095.
Желчь представляет собой зеленовато-желтую жидкость слабощелочной реакции. Главные компоненты желчи: соли желчных кислот, желчные пигменты, холестерин, лецитин, жиры, неорганические соли. Печеночная желчь содержит до 98% воды. По своему осмотическому давлению, желчь равна плазме крови. Из печени желчь по внутрипеченочным желчным ходам поступает в печеночный проток, оттуда ее непосредственно выделяется через пузырный проток попадает в желчный пузырь. Здесь происходит концентрация желчи вследствие всасывания воды. Плотность пузырной желчи 1,026-1,095.
Часть веществ, входящих в состав желчи синтезируется непосредственно в печени. Другая часть образуется вне печени и после ряда метаболических изменений выводится с желчью в кишечник. Таким образом, желчь образуется двумя путями. Одни ее компоненты фильтруются из плазмы крови (вода, глюкоза, креатинин, калий, натрий, хлор), другие образуются в печени: желчные кислоты, глюкурониды, парные кислоты и т. д.
Важнейшие желчные кислоты холевая и дезоксихолевая в соединении с аминокислотами глицином и таурином образуют парные желчные кислоты — гликохолевую и таурохолевую.
Печень человека вырабатывает в сутки 10-20 г желчных кислот. Попадая с желчью в кишечник, желчные кислоты расщепляются с помощью ферментов кишечных бактерий, хотя большая их часть подвергается обратному всасыванию кишечными стенками и вновь оказывается в печени.
С калом выделяется лишь 2-3 г желчных кислот, которые в результате разлагающего действия кишечных бактерий меняют зеленый цвет на коричневый и изменяют запах.
Таким образом, существует как бы печеночно-кишечный кругооборот желчных кислот. Если необходимо увеличить выведение желчных кислот из организма (например, с целью выведения из организма больших количеств холестерина), то принимаются вещества, необратимо связывающие желчные кислоты, которые не позволяют желчным кислотам всасываться в кишечнике и выводят их из организма вместе с калом. Самыми эффективными в этом плане являются специальные ионообменные смолы (например, холестирамин), которые будучи принятыми внутрь, способны связать в кишечнике очень большое количество желчи и, соответственно, желчных кислот.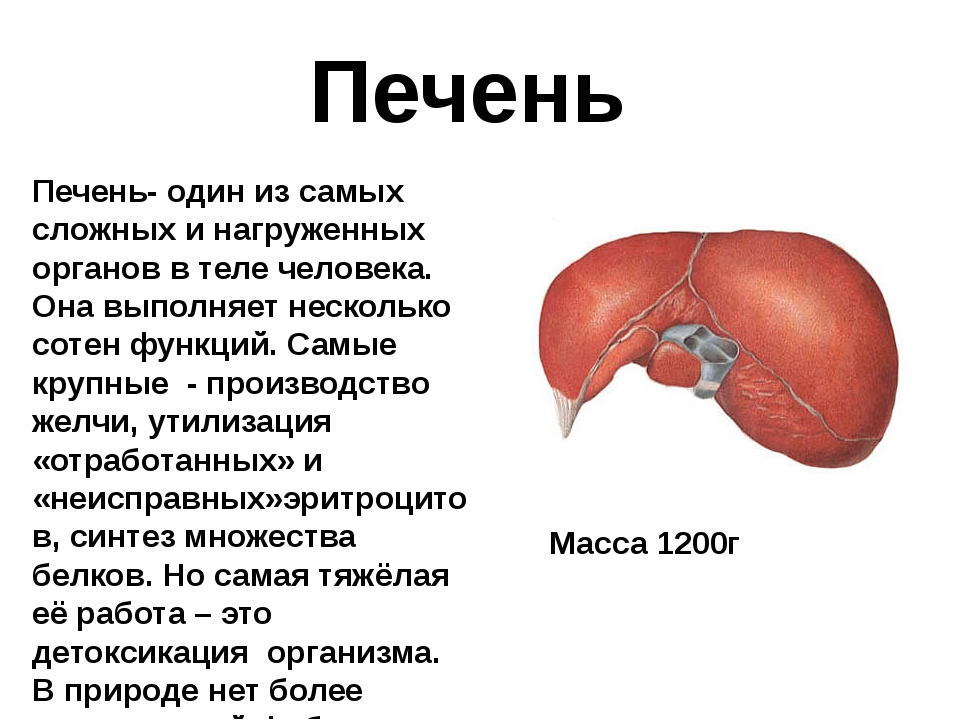 Ранее с этой целью использовали активированный уголь.
Ранее с этой целью использовали активированный уголь.
Используют, впрочем и теперь. Свойством абсорбировать желчные кислоты и выводить их из организма обладает клетчатка овощей и фруктов, но в еще большей степени пектиновые вещества. Наибольшее количество пектиновых веществ содержится в ягодах и фруктах, из которых можно приготовить желе без применения желатина. В первую очередь, это красная смородина, затем, по желеобразующей способности за ней следуют черная смородина, крыжовник, яблоки. Примечательно, что в печеных яблоках пектинов содержится в несколько раз больше, нежели в свежих. В свежем яблоке содержатся протопектины, которые при печении яблок превращаются в пектины. Печеные яблоки — непременный атрибут всех диет, когда нужно удалить из организма большое количество желчи (атеросклероз, заболевания печени, некоторые отравления и т. д.).
Желчные кислоты помимо всего прочего могут образовываться из холестерина. При употреблении мясной пищи, количество желчных кислот увеличивается, при голодании — уменьшается. Благодаря желчным кислотам и их солям, желчь выполняет свои функции в процессе пищеварения и всасывания.
Благодаря желчным кислотам и их солям, желчь выполняет свои функции в процессе пищеварения и всасывания.
Желчные пигменты (основной из них билирубин) не принимают участие в пищеварении. Их выделение печенью — чисто экскреторный выделительный процесс.
Билирубин образуется из гемоглобина разрушенных эритроцитов в селезенке и особых клетках печени (купферовские клетки). Не зря селезенку называют кладбищем эритроцитов. В отношении билирубина главной задачей печени является его выделение, а не образование, хотя немалая часть его образуется именно в печени. Интересно то, что распад гемоглобина до билирубина осуществляется при участии витамина С. Между гемоглобином и билирубином имеется множество промежуточных продуктов, способных ко взаимному превращению друг в друга. Часть их выделяется с мочой, а часть с калом.
Образование желчи регулируется центральной нервной системой путем разнообразных рефлекторных влияний. Желчеотделение происходит непрерывно, усиливаясь во время еды. Раздражение чревного нерва приводит к уменьшению образования желчи, а раздражение блуждающего нерва и гистамины увеличивают образование желчи.
Раздражение чревного нерва приводит к уменьшению образования желчи, а раздражение блуждающего нерва и гистамины увеличивают образование желчи.
Желчевыделение, т.е. поступление желчи в кишечник происходит периодически в результате сокращения желчного пузыря в зависимости от приема пищи и ее состава.
Выделительная (экскреторная) функция
Выделительная функция печени очень тесно связана с желчеобразованием, поскольку экскретируемые печенью вещества экскретируются через желчь и хотя бы уже поэтому они автоматически становятся составной частью желчи. К таким веществам относятся уже вышеописанные гормоны щитовидной железы, стероидные соединения, холестерин, медь и другие микроэлементы, витамины, порфириновые соединеиия (пигменты) и т. д.
Вещества, выделяемые практически только с желчью подразделяются на две группы:
- Вещества, связанные в плазме крови с белками (например, гормоны).
- Вещества, нерастворимые в воде (холестерин, стероидные соединения).

Одна из особенностей выделительной функции желчи заключается в том, что она способна вводить из организма такие вещества, которые никаким другим образом из организма выведены быть не могут. В крови мало свободных соединений. Большинство тех же гормонов прочно соединены с транспортными белками крови и будучи прочно соединенными с белками не могут преодолеть почечный фильтр. Такие вещества выделяются из организма вместе с желчью. Другой большой группой веществ, которые не могут быть выведены с мочой являются вещества, нерастворимые в воде.
Роль печени в данном случае сводится к тому, что она соединяет эти вещества с глюкуроновой кислотой и переводит, таким образом, в водорастворимое состояние, после чего они свободно выделяются через почки.
Есть и другие механизмы, которые позволяют печени выделить из организма нерастворимые в воде соединения.
Обезвреживающая функция
Печень выполняет защитную роль не только за счет обезвреживания и выведения токсичных соединений, но, даже за счет попавших в нее микробов, которых она уничтожает. Специальные клетки печени (купферовские клетки) подобно амебам захватывают чужеродные бактерии и переваривают их.
Специальные клетки печени (купферовские клетки) подобно амебам захватывают чужеродные бактерии и переваривают их.
В процессе эволюции печень превратилась в идеальный орган обезвреживания токсических веществ. Если она не может превратить токсичное вещество в полностью нетоксичное, она делает его менее токсичным. Мы уже знаем, что токсичный аммиак превращается в печени в нетоксичную мочевину (карбамид). Чаще всего печень обезвреживает токсичные соединения за счет образования с ними парных соединений с глюкурановой и серной кислотой, глицином, таурином, цистеином и др. так обезвреживаются высокотоксичные фенолы, нейтрализуются стероиды и другие вещества. Большую роль в обезвреживании играют окислительные и восстановительные процессы, ацетилирование, метилирование (поэтому для печени так полезны витамины, содержащие свободные метильные радикалы-СН3), гидролиз и др. Для выполнения печенью своей дезинтоксикационной функции, необходимо достаточное энергетическое обеспечение, а для этого, в свою очередь, необходимо достаточное содержание в ней гликогена и присутствие достаточного количества АТФ.
Свертывание крови
В печени синтезируются вещества, необходимые для свертывания крови, компоненты протромбинового комплекса (факторы II, VII, IX, X) для синтеза которых необходим витамин К. В печени образуются также фибраноген (белок, необходимый для свертывания крови), факторы V, XI, XII, XIII. Как это ни странно может показаться на первый взгляд, в печени же происходит синтез элементов противосвертывающей системы — гепарина (вещество, препятствующее свертыванию крови), антитромбина (вещество, препятствующее образованию тромбов), антиплазмина. У эмбрионов (зародышей) печень также служит кроветворным органом, где формируются эритроциты. С рождением человека эти функции берет на себя костный мозг.
Перераспределение крови в организме
Печень, помимо всех своих прочих функций неплохо выполняет функцию депо крови в организме. В связи с этим она может влиять на кровообращение всего организма. Все внутрипеченочные артерии и вены имеют сфинктеры, которые в очень широких пределах могут изменять кровоток в печени. В среднем кровоток в печени составляют 23 мл/кс/мин. В норме почти 75 мелких сосудов печени выключено сфинктерами из общей циркуляции. При повышении общего кровяного давления происходит расширение сосудов печени и печеночный кровоток в несколько раз возрастает. Наоборот, падение кровяного давления приводит к сужению сосудов в печени и печеночный кровоток уменьшается.
В среднем кровоток в печени составляют 23 мл/кс/мин. В норме почти 75 мелких сосудов печени выключено сфинктерами из общей циркуляции. При повышении общего кровяного давления происходит расширение сосудов печени и печеночный кровоток в несколько раз возрастает. Наоборот, падение кровяного давления приводит к сужению сосудов в печени и печеночный кровоток уменьшается.
Изменение положения тела также сопровождается изменениями печеночного кровотока. Так, например, в положении стоя кровоток печени на 40% ниже, чем в положении лежа.
Норадреналин и симпатические повышают сопротивление сосудов печени, что уменьшает количество крови, протекающей через печень. Блуждающий нерв, наоборот, уменьшает сопротивление сосудов печени, что увеличивает количество крови, протекающей через печень.
Печень весьма чувствительна к недостатку кислорода. В условиях гипоксии (недостатка кислорода в тканях) в печени образуются сосудорасширяющие вещества, снижающие чувствительность капилляров к адреналину и увеличивающие печеночный кровоток.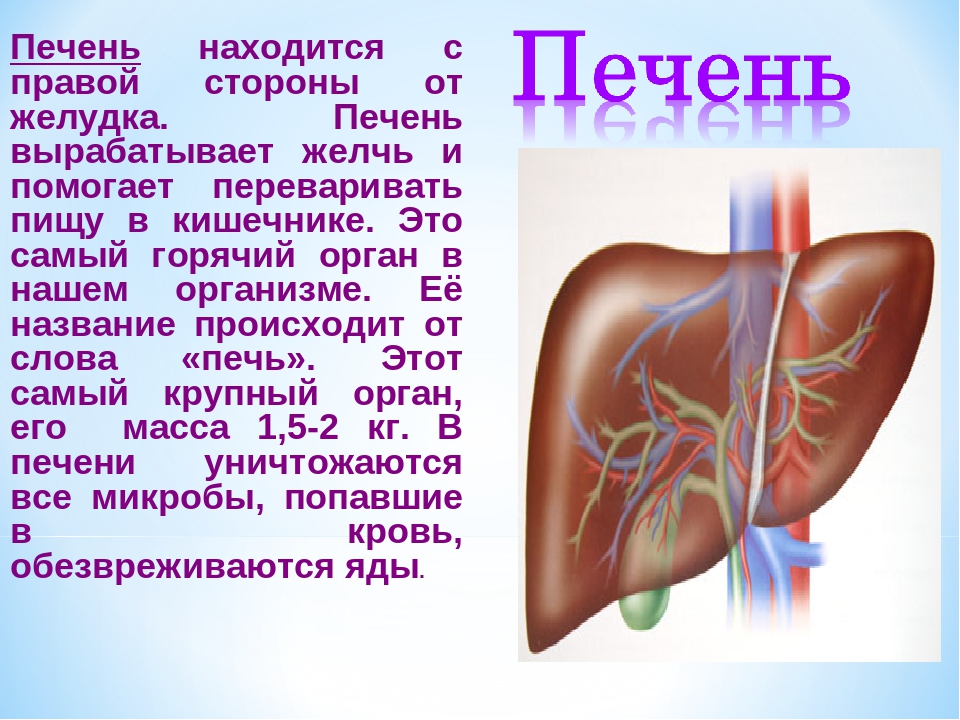 При длительной аэробной работе ( бег , плавание, гребля и т. д.) увеличение печеночного кровотока может достигнуть такой степени, что печень сильно увеличивается в объеме и начинает давить на свою наружную капсулу, богато снабженную нервными окончаниями. В результате появляется боль в печени, знакомая каждому бегуну, да и вообще всем тем, кто занимается аэробными видами спорта.
При длительной аэробной работе ( бег , плавание, гребля и т. д.) увеличение печеночного кровотока может достигнуть такой степени, что печень сильно увеличивается в объеме и начинает давить на свою наружную капсулу, богато снабженную нервными окончаниями. В результате появляется боль в печени, знакомая каждому бегуну, да и вообще всем тем, кто занимается аэробными видами спорта.
Возрастные изменения
Функциональные возможности печени человека наиболее высоки в раннем детском возрасте и очень медленно умньшаются в возрастом.
Масса печени новорожденного ребенка в среднем составляет 130-135 г. Максимума своего масса печени достигает в возрасте между 30-40 годами, а затем постепенно снижается, особенно между 70-80 годами, причем, у мужчин масса печени падает сильнее, чем у женщин. Регенерационные способности печени к старости несколько снижаются. В молодом возрасте после удаления печени на 70% (ранения, травмы и т. д.), печень восстанавливает через несколько недель утраченную ткань на 113% (с избытком). Такая высокая способность к регенерации не присуща ни одному другому органу и даже используется для лечения тяжелых хронических заболеваний печени. Так, например, некоторым больным циррозом печени, ее частично удаляют и она снова отрастает, но вырастает уже новая, здоровая ткань. С возрастом печень уже не восстанавливается полностью. У старых лиц она отрастает лишь на 91% (что, в принципе, тоже немало).
Такая высокая способность к регенерации не присуща ни одному другому органу и даже используется для лечения тяжелых хронических заболеваний печени. Так, например, некоторым больным циррозом печени, ее частично удаляют и она снова отрастает, но вырастает уже новая, здоровая ткань. С возрастом печень уже не восстанавливается полностью. У старых лиц она отрастает лишь на 91% (что, в принципе, тоже немало).
Синтез альбуминов и глобулинов падает в пожилом возрасте. Преимущественно падает синтез альбуминов. Однако, это не приводит к каким-либо нарушениями в питании тканей и падению онкотичесокого давления крови, т.к. к старости уменьшается интенсивность распада и потребления белков в плазме другими тканями. Таким образом, печень даже в старости обеспечивает потребности организма в синтезе белков плазмы. Способность печени к депонированию гликогена тоже различна в различные возрастные периоды. Гликогенная емкость достигает максимума к трехмесячному возрасту, сохраняется на всю жизнь и лишь слегка снижается к старости. Жировой обмен в печени достигает своего обычного уровня также в очень раннем возрасте и лишь незначительно снижается к старости.
Жировой обмен в печени достигает своего обычного уровня также в очень раннем возрасте и лишь незначительно снижается к старости.
На разных этапах развития организма печень вырабатывает разные количества желчи, но всегда покрывает потребности организма. Состав желчи на протяжении жизни несколько меняется. Так, если у новорожденного ребенка в печеночной желчи содержится желчных кислот около 11 мг-экв/л, то к четырехлетнему возрасту это количество снижается почти в 3 раза, а к 12 годам вновь повышается и достигает приблизительно 8 мг-экв/л.
Скорость опорожнения желчного пузыря, по некоторым данным наименьшая у молодых людей, а у детей и стариков она значительно выше.
Вообще, по всем своим показателям, печень — малостареющий орган. Она исправно служит человеку на протяжении всей его жизни.
Автор: Буланов Ю.Б.
Ученые придумали, как ускорить восстановление печени — Российская газета
У каждого ученого есть мечта — получить Нобелевскую премию. А на втором месте — публикация в самом знаменитом и престижном научном журнале Nature (у него самый высокий в мире импакт-фактор — свыше 30). Эта перспектива стала реальностью для группы ученых из шотландского Центра регенеративной медицины в Эдинбурге, Массачусетского технологического института и Сколковского института науки и технологий. Их работа признана прорывом в борьбе с заболеваниями печени.
А на втором месте — публикация в самом знаменитом и престижном научном журнале Nature (у него самый высокий в мире импакт-фактор — свыше 30). Эта перспектива стала реальностью для группы ученых из шотландского Центра регенеративной медицины в Эдинбурге, Массачусетского технологического института и Сколковского института науки и технологий. Их работа признана прорывом в борьбе с заболеваниями печени.
Этот важнейший орган, по сути, первая и главная линия обороны от ядов, токсинов, любых чужаков, пытающих проникнуть в организм. Кроме того, печень обеспечивает нас необходимыми веществами и витаминами, выполняет множество других функций. Кстати, в произведениях Гомера именно печень олицетворяла средоточие жизни в человеческом организме.
Но стоя на страже организма, она с годами основательно изнашивается. Особенно у тех, кто ведет неправильный образ жизни, злоупотребляет в еде и питие. Увы, часто понимание этого приходит слишком поздно, когда износ зашел слишком далеко. В ведущих лабораториях мира ищут способы помочь печени. Сегодня единственным радикальным методом лечения больных с необратимым, прогрессирующим поражением считается трансплантация органа от донора. Ежегодно в мире выполняется около 12 тысяч таких сложнейших операций, но потребность минимум вдвое больше.
Сегодня единственным радикальным методом лечения больных с необратимым, прогрессирующим поражением считается трансплантация органа от донора. Ежегодно в мире выполняется около 12 тысяч таких сложнейших операций, но потребность минимум вдвое больше.
Цена, прямо скажем, заоблачная, почти 300 тысяч долларов.
— Есть другой вариант — регенерация или восстановление клеток печени, — сказал корреспонденту «РГ» профессор Сколтеха, один из авторов статьи в Nature Юрий Котелевцев. — Дело в том, что в отличие практически от всех других органов печень может восстанавливаться, даже если сохранилось всего 25 процентов здоровой ткани. Но делает это не так быстро, как ящерица отращивает новый хвост. Увы, во много раз медленней. Мы пытались понять, можно ли ускорить этот процесс. Если да, то как это сделать.
Известно, что ремонтом печени занимается основной вид ее клеток — гепатоциты. Точнее, те из них, которые еще не повреждены болезнью. Говоря образно, размножаясь, они делятся с органом своим здоровьем.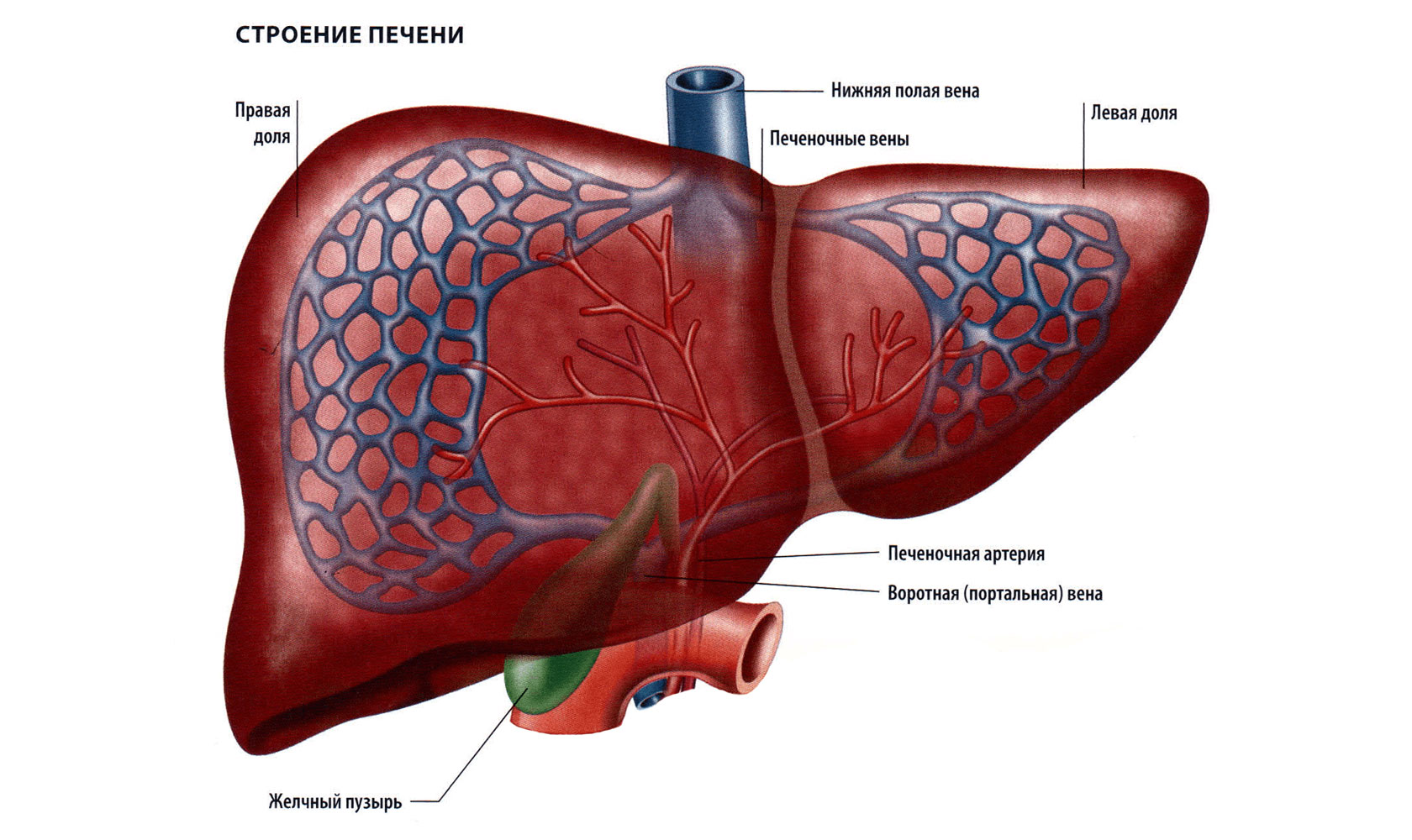 Но, к сожалению, чаще всего в больной печени способных к размножению гепатоцитов остается мало, и болезнь прогрессирует намного быстрей, чем идет восстановление. Поэтому ученые ищут в организме других «ремонтников». Было предположение, что это могут быть клетки желчных протоков — холангиоциты. Но от версии до доказательства — огромная дистанция.
Но, к сожалению, чаще всего в больной печени способных к размножению гепатоцитов остается мало, и болезнь прогрессирует намного быстрей, чем идет восстановление. Поэтому ученые ищут в организме других «ремонтников». Было предположение, что это могут быть клетки желчных протоков — холангиоциты. Но от версии до доказательства — огромная дистанция.
— Сегодня для изучения многих процессов в организме используется так называемый нокаут генов, — говорит Юрий Котелевцев. — Речь идет о выключении генов, ответственных за различные процессы. Нокаутируя ген, по сути, прекращая процесс, ученые оценивают его роль в работе органа.
Но такой вариант подходит далеко не всегда, так как сложен, требует дополнительных манипуляций с геномом. Поэтому мы применили другой вариант, не нокаут гена, а нокдаун. Ген отключается лишь на время, а главное не нужно ничего менять в геноме. Эта технология появилась около 20 лет назад, а в 2006 году ее авторы были удостоены Нобелевской премии.
В данном случае, применив нокдаун, ученым удалось отключить ген, который управляет делением и миграцией гепатоцитов.:max_bytes(150000):strip_icc()/anatomy-of-liver--antero-visceral-view--188057933-5a3424a29802070037cd9f86.jpg) В результате они прекратили делиться и перемещаться по печени, а в зоне, где произошла регенерация, она продолжалась за счет холангиоцитов. Так было доказано, что есть другие варианты ремонта печени.
В результате они прекратили делиться и перемещаться по печени, а в зоне, где произошла регенерация, она продолжалась за счет холангиоцитов. Так было доказано, что есть другие варианты ремонта печени.
Наряду с гепатоцитами это могут быть холангиоциты. Более того, они лучше размножаются, так как ближе к эмбриональным клеткам. Можно сказать, что они помнят многое из эмбриональной программы.
— В Сколтехе под руководством профессора Виктора Котелянского внедрена технология нокдауна генов печени, — говорит Юрий Котелевцев. — Она хорошо известна уже около 7 лет, однако применение ее на живом организме требует высокого экспериментального уровня и пока доступна в немногих лабораториях. Контакты с зарубежными учеными, работающие над подобными проблемами, позволили значительно продвинуть эти исследования.
Данная работа может стать прорывом в борьбе с болезнями печени. Надо брать у пациента клетки холангиоцитов, размножать, а затем вводить в организм.
Ученые изучили новый механизм регенерации клеток печени
Ученые из Центра регенеративной медицины в Эдинбурге (Шотландия), Массачусетского технологического института (США) и Сколковского института науки и технологий впервые продемонстрировали роль холеангиоцитов — клеток внутрипеченочных желчных протоков в регенерации тканей печени. Полученные результаты полезны для регенеративной медицины и борьбы с заболеваниями печени. Результаты исследования опубликованы в журнале Nature.
Полученные результаты полезны для регенеративной медицины и борьбы с заболеваниями печени. Результаты исследования опубликованы в журнале Nature.
Печень один из немногих органов в организме человека, способных к регенерации. В случае повреждении печени в результате травмы или хронического заболевания главные клетки печени — гепатоциты (именно они ответственны за все основные функции печени) способны регенерировать за счет деления неповрежденных гепатоцитов. Стимуляции регенерации печени — проблема остро стоящая перед медициной, однако подробности данного механизма и то участвуют ли другие типы печеночных клеток в процессе образования новых гепатоцитов до сих пор были не ясны.
Международная группа ученых использовали мышей в качестве модельного объекта, на них удалось сымитировать повреждения печени характерные для человека. Эксперимент проводился на двух независимых моделях, где специально была снижена способность гепатоцитов к делению, чтобы оценить вклад других клеток печени в регенерацию. В результате данной работы было показано, что эпителиальные клетки желчных протоков — холеангиоциты участвуют в регенерации гепатоцитов. Также ученые предполагают, что потенциал к регенерации у гепатоцитов, полученных из холангиоцитов, может быть выше, чем у обычных гепатоцитов.
В результате данной работы было показано, что эпителиальные клетки желчных протоков — холеангиоциты участвуют в регенерации гепатоцитов. Также ученые предполагают, что потенциал к регенерации у гепатоцитов, полученных из холангиоцитов, может быть выше, чем у обычных гепатоцитов.
Юрий Котелевцев, профессор Сколтеха, замдиректора Центра Трансляционной Биомедицины (бывший Центр Функциомальной геномики) Сколтеха: «Чуть больше года назад я встречался с моими коллегами по Эдинбургскому университету с целью создания совместных научных проектов. Рассказывал о том, как нам в Сколтехе, в центре Функциональной геномики под руководством профессора Виктора Котелянского удалось наладить технологию нокдауна генов печени. Эта технология хорошо известна уже около 7 лет, однако применение ее, in vivo, требует высокого экспериментального уровня и пока доступна в немногих академических лабораториях. Оказалось, что лаборатория профессора Стюарта Форбса работает над проблемой, в решении которой именно нокдаун может быстро и однозначно подтвердить гипотез ключевой роли холеангиоцитов в регенерации печени.
Вклад Сколтеха совместно с MIT заключается в том, что мы создали и предоставили для эксперимета липидные наночастицы с siRNA к бета 1 интегрину, которые заблокировали экспрессию этого гена в гепатоцитах у мышей, а последующие наблюдения, над фенотипом полученной модели позволили идентифицировать холеангиоциты, как клетки, участвующие в регенерации печени. В настоящее время в Шотландском центре регенеративной медицины под руководством порфессора С. Форбса начинаются работы направленные на выделение и трансплантацию аутологичных холеангиоцитов пациентам с циррозом печени. Мы сейчас продолжаем коллаборацию с лаб. проф Форбса и занимаемся проверкой новых генов мишеней, блокирование которых может предотвращать или стабилизировать процессы связанные с фиброзом и последующим циррозом печени.»
В Боткинской больнице спасли молодую девушку, печень которой почти полностью состояла из кист с паразитами
Хирурги московской Боткинской больницы
спасли молодую девушку, печень которой на две трети была
поражена эхинококком, то есть состояла из огромных кист, содержащих
паразитов. Врачам пришлось удалить всю правую долю печени, а левую
предварительно «вырастить», чтобы после удаления она могла работать
за весь орган. Такое сложное лечение стало возможным,
благодаря современныммедицинским технологиям и мастерству хирургов
больницы.
Врачам пришлось удалить всю правую долю печени, а левую
предварительно «вырастить», чтобы после удаления она могла работать
за весь орган. Такое сложное лечение стало возможным,
благодаря современныммедицинским технологиям и мастерству хирургов
больницы.
Молодая девушка, студентка третьего курсапоступила в больницу имени Боткина Департамента здравоохранения Москвы для уточнения характера кист в печени и селезенке. Из симптомов ее беспокоило только нарастание слабости, однако ее родители все списывали на учебу. Однако на всякий случай решили провести минимальное обследование, в том числе УЗИ брюшной полости. Оно и выявило множество кист в печени и в селезенке.
Уже в
Боткинской больнице пациентке выполнили диагностическое КТ и МРТ, а
также взяли кровь на антитела
к эхинококку – так хирурги подтвердили свои
подозрения, кисты в печени и селезенке – эхинококковые. Они занимали
всю правую долю печени и составляли 6-10 см в
диаметре, здоровой ткани в правой
части органа практически не осталось.
При таком поражении печени необходимо было удалять большую часть печени – из 8 сегментов у пациентки осталось бы лишь три. Но этого не хватило бы для жизни, что подтвердило функциональное исследование органа. В таких случаях в Боткинской больнице применяют новую технологию – фактически «выращивают» здоровую часть печени, в данном случае – не пораженную эхинококком. Для этого за месяц до планируемой большой операции девушке провели эмболизациюправой ветви воротной вены. Суть процедуры состоит в том, что хирурги под УЗИ-контролем прокалывают воротную вену и перекрывают кровоток в правую долю, чтобы вся кровь шла в левую, сохранную, долю печени.
Через месяц было проведено повторное исследование функционального состояния печени, которое показало, что левая доля печени выросла, и теперьможно проводить основную операцию по удалению эхинококковых кист.
Дополнительная
сложность была в том, что у молодой пациентки была огромная киста в
селезенке. Но благодаря мастерству хирургов этот важный для молодой
девушки орган удалось сохранить, убрав только нижний ее полюс с кистой. Правая
доля печени была удалена полностью вместе с кистами. Операция прошла без
осложнений, без развития печеночной недостаточности. Практически с первых суток
пациентка стала чувствовать себя нормально.
Но благодаря мастерству хирургов этот важный для молодой
девушки орган удалось сохранить, убрав только нижний ее полюс с кистой. Правая
доля печени была удалена полностью вместе с кистами. Операция прошла без
осложнений, без развития печеночной недостаточности. Практически с первых суток
пациентка стала чувствовать себя нормально.
Операция по удалению кист эхинококка – довольно сложная технически и требует высокой квалификации и опыта хирурга, так как нельзя оставить даже минимальные доли оболочек паразита, в которой он обитает. Кисты крайне важно удалить без их разрыва.
Хотя для европейской части России это по-прежнему относительно редкое заболевание, в Боткинской больнице за последний год прооперировали примерно в 5 раз больше таких пациентов, чем за пять последних лет.
Эхинококк – это
паразит, ленточный червь. Он обустраивается в организме человека,
попадая в него через кишечник, то есть это болезнь «грязных рук». Человек
взаимодействует с домашними животными, убирает за ними, а потом, недостаточно
вымыв руки, ест. Переносят эхинококк животные, а в зоне
риска –работники ферм и контактные зоопарки.
Человек
взаимодействует с домашними животными, убирает за ними, а потом, недостаточно
вымыв руки, ест. Переносят эхинококк животные, а в зоне
риска –работники ферм и контактные зоопарки.
В подавляющем большинстве случаев человек узнает о существующей проблеме случайно во время планового обследования и УЗИ органов брюшной полости. Пациента чаще всего ничего не беспокоит, он может годами жить с проблемой и не подозревать о ней. Специалист УЗИ обнаруживает кисту в селезенке или печени – реже в легких или мозге – а затем направляет больного к специалисту, чтобы уточнить природу этой кисты.
Городская клиническая
больница имени С.П. Боткина Департамента здравоохранения города
Москвы – одна из крупнейших многопрофильных клиникстолицы, где
можно получить все виды лечения. Ежегодно здесь проходят лечение около 100
тысяч человек. Пациентов принимают более 70 отделений. Стационар
располагает коечным фондов в 1800 мест. Хирургическая служба Боткинской
включает в себя клиники хирургии, урологии, гинекологии, сердечно-сосудистой
хирургии, травматологии и ортопедии, нейрохирургии, офтальмологии,
оториноларингологии и челюстно-лицевой хирургии, хирургии печени и
поджелудочной железы.
Хирургическая служба Боткинской
включает в себя клиники хирургии, урологии, гинекологии, сердечно-сосудистой
хирургии, травматологии и ортопедии, нейрохирургии, офтальмологии,
оториноларингологии и челюстно-лицевой хирургии, хирургии печени и
поджелудочной железы.
Печень растет на крови | Наука и жизнь
Давление крови на стенки печеночных сосудов заставляет клетки печени активнее делиться.
Чтобы из горстки зародышевых клеток получились полноценная печень, почки, легкие и т. д., эти клетки должны постоянно получать разнообразные сигналы, управляющие их ростом и делением: иногда рост нужно тормозить, иногда – подстегивать. То же самое происходит, когда орган уже вырос и его нужно время от времени подновлять – например, восстанавливать после травмы или заменять отмершие клетки на новые.
В случае печени молекулярные сигналы, управляющие ростом органов, идут от так называемых синусоидальных эндотелиальных клеток, которые выстилают печеночные кровеносные сосуды. Но тут возникает другой вопрос: как эти сосудистые клетки понимают, что нужно выбросить очередную порцию ростовых факторов – белков, стимулирующих деление клеток печени?
Но тут возникает другой вопрос: как эти сосудистые клетки понимают, что нужно выбросить очередную порцию ростовых факторов – белков, стимулирующих деление клеток печени?
В статье в Nature сотрудники Дюссельдорфского университета им. Генриха Гейне вместе с коллегами из других научных центров Германии и Финляндии пишут, что ростовые сигналы и рост печени зависят от того, сколько крови прокачивается по ее двум большим сосудам – печеночной артерии и воротной вене. Кровь периодически растягивает их стенки, кроме того, поток крови вызывает касательное напряжения в клетках, которые он омывает.
Чем больше крови идет по сосуду, тем сильнее действуют механическое растяжение и касательное напряжение. Именно механическая сила служит сигналом для синусоидальных эндотелиальных клеток, которые понимают, что нужно расширять как сосуды, так и всю печень, и начинают производить соответствующие регуляторные белки, стимулирующие клеточное деление.
Исследователи попытались выяснить подробности того, что при этом происходит. Эксперименты ставили с мышиными эмбрионами, которых извлекали из беременных самок и дальше уже выращивали в лабораторных условиях. Печень эмбрионов росла в соответствии с тем, как менялся поток крови через нее, и активнее всего клетки делились как раз в тех местах, где поток был интенсивнее. У регуляторных клеток удалось определить два белка, которые отвечали за их механическую чувствительность – это были интегрин β1 и рецептор к эндотелиальному фактору роста.
Белки интегрины прошивают наружную клеточную мембрану, улавливая сигналы из внешней среды. От интегринов зависит многое, от формы самой клетки до деления. Рецептор же, как понятно по его названию, ловит белок под названием эндотелиальный фактор роста (который, в свою очередь, стимулирует развитие сосудов). Однако рецептор, как оказалось, реагирует также и на механические силы, подобно интегрину. Оба вместе они понуждают регуляторные клетки выделять сигналы, понуждающие клетки печени к делению.
Эксперименты ставили не только с эмбрионами, но и с печенью взрослых мышей: в ней усиливали кровоток, либо разбавляя кровь специальным раствором, либо удаляя часть печени, чтобы на оставшуюся часть пришлось больше крови. Результат был тот же: синусоидальные эндотелиальные клетки чувствовали большее механическое напряжение (что, кстати, было видно даже по их меняющейся форме), в них активировались оба вышеупомянутых белка (интегрин и рецептор), после чего клетки начинали активно синтезировать сигналы к делению.
Более того, когда то же самое попытались проделать с человеческими клетками – а в нашей печени тоже есть клетки, которые управляют ее ростом – то снова получалось то же самое: растягивая их, исследователи добивались того, что человеческие клетки начинали активно выделять все те же стимуляторы роста для всей печени. Наконец, последнее: авторы работы оценили размер печени у здоровых людей, и заметили, что у тех, у кого кровяное давление в среднем выше, у тех и печень больше.
Очевидно, действуя на то или иное звено этого молекулярно-клеточного механизма, можно при медицинской необходимости усилить регенерацию печени. Однако пока тут остаются несколько вопросов, которые нужно решить, прежде чем думать о каких-то лечебных методах.
Во-первых, не ясно, как именно должна действовать механическая сила: в каком-то одном направлении, и если да, то в каком; или же клетка прислушивается к равнодействующей всех сил, что на нее действуют.
Во-вторых, нужно все-таки разобраться, почему тот рецептор активируют механические силы – до сих пор считалось, что он включается по иному механизму. Наконец, если мы хотим восстанавливать печень, испорченную по болезни, то нужно понять, не мешают ли такой механической стимуляции разные неприятные вещи вроде воспаления и других иммунных реакций, которые часто сопутствуют травмам и заболеваниям.
По материалам Nature
Сегменты печени человека: роль скрытых долей печени и физиология сосудов в развитии печеночных вен и лево-правой асимметрии
Couinaud, C. (Masson, Paris, 1957).
Ганс, Х. Введение в хирургию печени . (Эльзевир, 1955).
Голдсмит Н. А. и Вудберн Р. Т. Хирургическая анатомия, относящаяся к резекции печени. Хирургический гинекологический акушер 105 , 310–318 (1957).
CAS PubMed Google ученый
Хили, Дж. Э. Мл. И Шрой, П. С. Анатомия желчных протоков в печени человека; анализ преобладающего типа разветвлений и основных вариаций желчных протоков. AMA Arch Surg 66 , 599–616 (1953).
Артикул PubMed Google ученый
Hjortsjö, C.H. Топография систем внутрипеченочных протоков. Акта Анат 11 , 599–615 (1951).
Артикул PubMed Google ученый
Комитет терминологии IHPBA и терминология Брисбена 2000 по анатомии и резекциям печени. Сургут 2 , 333–339 (2000).
Кантли, Дж.О новом расположении правой и левой долей печени. Труды Анатомического общества Великобритании и Ирландии 32 , 4–9 (1897).
Google ученый
Когуре, К., Кувано, Х., Фудзимаки, Н., Исикава, Х. и Такада, К. Репродукция сегментарной анатомии Хьортджо на переднем сегменте печени человека. Arch Surg 137 , 1118–1124 (2002).
Артикул PubMed Google ученый
Висмут Х. Хирургическая анатомия и анатомическая хирургия печени. Мир J Surg 6 , 3–9 (1982).
CAS Статья PubMed Google ученый
Висмут, Х. Возвращаясь к анатомии печени и терминологии гепатэктомий. Энн Сург 257 , 383–386, https: // doi.org / 10.1097 / SLA.0b013e31827f171f (2013 г.).
Артикул PubMed Google ученый
Фазель, Дж. Х. и др. . Сегментарная анатомия печени: плохая корреляция с КТ. Радиология 206 , 151–156, https://doi.org/10.1148/radiology.206.1.9423665 (1998).
CAS Статья PubMed Google ученый
Platzer, W. & Maurer, H. Zur segmenteinteilung der leber. Акта Анат 63 , 8–31 (1966).
CAS Статья PubMed Google ученый
van Leeuwen, M. S. et al. . Портальная венозная и сегментарная анатомия правого полушария: наблюдения на основе трехмерной спиральной компьютерной томографии. Am J Рентгенол 163 , 1395–1404, https: // doi.org / 10.2214 / ajr.163.6.7992736 (1994).
Артикул Google ученый
Фазель, Дж. Х. и Шенк, А. Концепции классификации сегментов печени: ни старые, ни новые, но всеобъемлющая. J Clin Imaging Sci 3 , 48, https://doi.org/10.4103/2156-7514.120803 (2013).
Артикул PubMed PubMed Central Google ученый
Фазель, Дж. Х. Портальные венозные территории в печени человека: анатомическая переоценка. Anat Rec 291 , 636–642, https://doi.org/10.1002/ar.20658 (2008).
Артикул Google ученый
Страсберг, С. М. Терминология анатомии печени и резекций печени: вступая в борьбу с печеночным Бабелем. J Am Coll Surgeons 184 , 413–434 (1997).
CAS Google ученый
Такасаки, К. Метод пересечения ножки глиссонеана для резекции печени: новая концепция сегментации печени. J Гепато-желчный поддон 5 , 286–291 (1998).
CAS Статья Google ученый
Чо, А. и др. . Предложение о реклассификации анатомии печени по разветвлениям портала. Am J Surg 189 , 195–199, https://doi.org/10.1016/j.amjsurg.2004.04.014 (2005).
Артикул PubMed Google ученый
Soler, L., Mutter, D., Pessaux, P. & Marescaux, J. Анатомия пациента: новая область анатомии, основанная на информатике, проиллюстрированная на печени. J Vis Surg 1 , 1–12 (2015).
Google ученый
Bismuth, H. Новый взгляд на анатомию печени: потребности и средства выхода за рамки схемы Куино. Дж Гепатол 60 , 480–481, https://doi.org/10.1016/j.jhep.2013.12.010 (2014).
Артикул PubMed Google ученый
Майно, П. и др. . Анатомия печени: схема с тремя уровнями сложности — еще один шаг к индивидуальной территориальной резекции печени. Дж Гепатол 60 , 654–662, https://doi.org/10.1016/j.jhep.2013.10.026 (2014).
Артикул PubMed Google ученый
Элиас, Х. и Петти, Д. Общая анатомия кровеносных сосудов и протоков в печени человека. Am J Anat 90 , 59–111, https://doi.org/10.1002/aja.1000
4 (1952).CAS Статья PubMed Google ученый
Лассау, Дж. П. и Бастиан, Д. Органогенез венозных структур печени человека: гемодинамическая теория. анатомическая клиника 5 , 97–102 (1983).
Артикул Google ученый
Nettelblad, S. C. Die lobierung und innere topographie der saugerleber. Акта Анат 21 (приложение 20), 7–246 (1954).
Google ученый
Хикспурс, Дж. П. Дж. М. и др. . Судьба желточной и пупочной вен в процессе развития печени человека. J Anat , н / д-н / д, https://doi.org/10.1111/joa.12671 (2017).
Бенко Т. и др. . Портальное снабжение и венозный отток хвостатой доли в печени здорового человека: объемное исследование виртуальной трехмерной компьютерной томографии. Мир J Surg 41 , 817–824, https: // doi.org / 10.1007 / s00268-016-3791-8 (2017).
CAS Статья PubMed Google ученый
Thompson, P. Развитие квадратной доли печени с особым упором на необычную аномалию этой доли у взрослых. J Anat Physiol 48 , 222–237 (1914).
CAS PubMed PubMed Central Google ученый
Фанг, К. Х. и др. . Анатомические вариации печеночных вен: трехмерные компьютерные томографии 200 человек. Мир J Surg 36 , 120–124, https://doi.org/10.1007/s00268-011-1297-y (2012).
Артикул PubMed Google ученый
Lhuaire, M. et al. . Анатомия развития печени на основе компьютерных трехмерных реконструкций четырех человеческих эмбрионов (от 14 до 23 стадии Карнеги). Анн Анат 200 , 105–113, https://doi.org/10.1016/j.aanat.2015.02.012 (2015).
Артикул PubMed Google ученый
Замир М. Распределительные и доставочные сосуды человеческого сердца. J Gen Physiol 91 , 725–735 (1988).
CAS Статья PubMed Google ученый
Текин, Э., Хант, Д., Ньюберри, М. Г. и Сэвидж, В. М. Разветвляются ли сосудистые сети оптимальным или случайным образом в пространственных масштабах? PLoS Comput Biol 12 , e1005223, https://doi.org/10.1371/journal.pcbi.1005223 (2016).
ADS Статья PubMed PubMed Central Google ученый
Брюммер А. Б., Сэвидж В. М. и Энквист Б. Дж. Общая модель метаболического масштабирования в самоподобных асимметричных сетях. PLoS Comput Biol 13 , e1005394, https://doi.org/10.1371/journal.pcbi.1005394 (2017).
ADS Статья PubMed PubMed Central Google ученый
Кесслер, Дж., Расмуссен, С., Годфри, К., Хэнсон, М. и Кисеруд, Т. Венозный кровоток в печени и регуляция роста плода человека: данные макросомных плодов. Am J Obstet Gynecol 204 (429), e421–427, https: // doi.org / 10.1016 / j.ajog.2010.12.038 (2011).
Google ученый
Germain, T. et al. . Сегментация печени: практические советы. Диагностика интервальной визуализации 95 , 1003–1016, https://doi.org/10.1016/j.diii.2013.11.004 (2014).
CAS Статья PubMed Google ученый
Shindoh, J. et al. .Сосудистая архитектура аномальной правой круглой связки: трехмерный анализ у 35 пациентов. HPB (Оксфорд) 14 , 32–41, https://doi.org/10.1111/j.1477-2574.2011.00398.x (2012).
Артикул Google ученый
Когуре, К., Кувано, Х., Фудзимаки, Н. и Макуучи, М. Связь между портальной сегментацией, собственно печеночной веной и внешней выемкой хвостатой доли в печени человека. Энн Сург 231 , 223–228 (2000).
CAS Статья PubMed PubMed Central Google ученый
Бартч, Ф., Акерманн, М., Ланг, Х. и Генрих, С. Незамороженные сегменты печени: клинический случай неизвестного фенотипа синдрома Конради-Хунерманна-Хаппла. J Gastrointestin Liver Dis 25 , 547–549, https: // doi.org / 10.15403 / jgld.2014.1121.254.sch (2016).
PubMed Google ученый
Oishi, Y. et al. . Анатомическая оценка сосудистой системы печени у здоровых гончих с помощью рентгеноконтрастной компьютерной томографии. J Vet Med Sci 77 , 925–929, https://doi.org/10.1292/jvms.14-0469 (2015).
CAS Статья PubMed PubMed Central Google ученый
Couinaud, C. Анатомия печени: портальная (и надпеченочная) или сегментация желчных протоков. Dig Surg 16 , 459–467 (1999).
CAS Статья PubMed Google ученый
Когуре, К., Ишизаки, М., Немото, М., Кувано, Х. и Макуучи, М. Сравнительное исследование анатомии печени крысы и человека. J Хирургия гепатобилиарной поджелудочной железы 6 , 171–175 (1999).
CAS Статья PubMed Google ученый
Gouysse, G. et al. . Взаимосвязь между развитием сосудов и дифференцировкой сосудов во время органогенеза печени у человека. Дж Гепатол 37 , 730–740 (2002).
CAS Статья PubMed Google ученый
Наканума, Ю., Хосо, М., Санзен, Т. и Сасаки, М. Микроструктура и развитие нормальных и патологических желчных путей у людей, включая кровоснабжение. Microsc Res Tech 38 , 552–570, https://doi.org/10.1002/(SICI) 1097-0029 (19970915) 38: 6 <552 :: AID-JEMT2> 3.0.CO; 2-H (1997).
Роскамс Т. и Десмет В. Эмбриология внепеченочных и внутрипеченочных желчных протоков, протоковая пластинка. Анат Рек (Хобокен) 291 , 628–635, https: // doi.org / 10.1002 / ar.20710 (2008).
CAS Статья Google ученый
Коста А. М., Пегадо С. С. и Порто Л. С. Количественная оценка внутрипеченочного желчного дерева во время внутриутробного развития плода человека. Anat Rec 251 , 297–302 (1998).
CAS Статья PubMed Google ученый
Тани, К. и др. .Карта венозного оттока печени при сложных гепатобилиарных операциях и трансплантации печени. HPB (Оксфорд) 18 , 1031–1038, https://doi.org/10.1016/j.hpb.2016.08.007 (2016).
Артикул Google ученый
Lee, J. H., Jin, G. Y., Jin, Z. W., Yu, H. C. & Cho, B.H. Разветвление периферических ветвей оболочки Глиссона и клинические последствия в эпоху местной абляционной терапии. Рентген хирургический Анат 32 , 911–917, https://doi.org/10.1007/s00276-010-0643-3 (2010).
Артикул PubMed Google ученый
О’Рахилли Р. и Мюллер Ф. Стадии развития человеческих эмбрионов: пересмотренные и новые измерения. Клетки тканей органов 192 , 73–84, https://doi.org/10.1159/000289817 (2010).
Артикул PubMed Google ученый
Байер, С. А. и Альтман, Дж. Человеческий мозг в начале первого триместра . (CRC Press, 2007).
Софферс, Дж. Х., Хикспурс, Дж. П., Меконен, Х. К., Кёлер, С. Э. и Ламерс, У. Х. Характер роста кишечника человека и его брыжейки. BMC Dev Biol 15 , 31, https://doi.org/10.1186/s12861-015-0081-x (2015).
Артикул PubMed PubMed Central Google ученый
Хикспурс, Дж. П. и др. . Развитие надпеченочной нижней полой и непарнокопытной венозной системы человека. Дж Анат 226 , 113–125, https://doi.org/10.1111/joa.12266 (2015).
Артикул PubMed Google ученый
Регенерация печени — Центр регенеративной медицины
Регенерация печени
Хирурги-трансплантологи, гепатологи и другие исследователи разрабатывают регенеративную терапию на основе клеток печени для пациентов, которым в противном случае потребовалась бы трансплантация всей печени.
Печень обладает наибольшей регенеративной способностью из всех органов тела. Восстановление печени было признано на протяжении многих лет, начиная с Прометея в древнегреческой мифологии.
Когда печень повреждена сверх ее способности к самовосстановлению, трансплантация печени является методом выбора. Трансплантаты используются для лечения широкого спектра заболеваний печени, включая рак печени, цирротическое заболевание печени, острую печеночную недостаточность и генетические нарушения печени.
Но, как и в случае с большинством донорских органов, печени не хватает — количество людей, ожидающих новой печени, намного превышает количество доступной донорской печени.
Основные направления
Хирурги-трансплантологи Mayo Clinic, гепатологи и другие исследователи из Центра регенеративной медицины разрабатывают и совершенствуют ряд методов регенеративной терапии печени для пациентов, которым сегодня приходится ждать трансплантации цельной печени.
- Терапия на основе внеклеточных везикул. Исследователи клиники Майо показали, что биологические наночастицы, называемые внеклеточными везикулами, секретируемые стволовыми клетками, могут уменьшить повреждение тканей в печени и могут улучшить восстановление и регенерацию. Исследователи Центра регенеративной медицины в настоящее время проектируют и разрабатывают масштабируемые производственные процессы для использования везикул, полученных из стволовых клеток, в клинических условиях в качестве нового терапевтического подхода к лечению повреждений печени.
Трансплантаты от живых доноров. Рак печени и запущенные случаи цирроза печени могут потребовать пересадки печени.Учитывая нехватку цельной печени для трансплантации, кампусы клиники Мэйо в Миннесоте и Аризоне уже более десяти лет проводят трансплантации печени от живых доноров — вместе они представляют собой одну из крупнейших подобных программ в стране.
При трансплантации от живого донора часть донорской печени удаляется и используется для замены больной печени пациента. После операции печень донора восстанавливается до нормальных размеров, а новая печень пациента также увеличивается до нормальных размеров.
Поскольку безопасность живых доноров имеет первостепенное значение для успеха этой программы, исследователи клиники Мэйо провели долгосрочную оценку результатов донорства, таких как регенерация печени, а также психическое и физическое благополучие. Результаты исследования были очень обнадеживающими, поскольку они показали, что у живых доноров печени Майо все хорошо после донорства.
Вспомогательные устройства для печени. В последние годы было разработано несколько типов биоискусственной печени — устройств, выполняющих функции печени для пациентов с печеночной недостаточностью.Эти устройства поддерживают пациентов, когда их печень восстанавливается после болезни или когда они ждут трансплантации печени.
Исследователи Центра регенеративной медициныработают над созданием собственной версии биоискусственной печени, известной как биоискусственная печень с резервуаром сфероидов. Это устройство содержит сфероиды клеток печени свиней (гепатоцитов), которые заменяют функцию печени пациента. Исследования использования гепатоцитов человека в устройстве продолжаются.
Трансплантация клеток печени пациентам. Существующие процедуры трансплантации клеток печени, используемые для лечения генетических заболеваний печени, не используют специфические для пациента клетки и требуют иммуносупрессии. Исследователи Центра регенеративной медицины разрабатывают индивидуальный подход к трансплантации клеток печени, в котором используются собственные клетки пациента.
При таком подходе у пациента будут собираться клетки и использоваться генная терапия для исправления генетического дефекта, ответственного за болезнь пациента. Скорректированные здоровые клетки затем будут трансплантированы обратно в печень пациента.Поскольку скорректированные гепатоциты изначально были получены из собственных клеток пациента, иммунодепрессанты не потребовались.
Доказательные исследования на первой генно-инженерной модели метаболического заболевания печени на крупных животных уже доказали свою эффективность. Исследователи клиники Мэйо теперь планируют перенести эту регенеративную терапию в клинические условия.
.
Регенерация печени человека после обширной резекции печени.Исследование нормальной печени и печени при хроническом гепатите и циррозе
Регенеративный процесс оценивался с точки зрения размера, функции и гистологии печени у 28 взрослых, перенесших обширную резекцию печени: гепатоцеллюлярная карцинома (ГЦК) у 21, вторичный рак печени из толстой кишки у четырех, карцинома желчного пузыря у одного, опухоль Клацкина у один, и болезнь Кароли — в одном. Было 22 мужчины и шесть женщин. Возраст составлял от 17 до 74 лет, средний возраст — 56 лет.7. Все пациенты с ГЦК имели основное заболевание печени: цирроз печени у 14 и хронический гепатит у семи. Расширенная правая лобэктомия была выполнена 10 пациентам, правая лобэктомия — 16 пациентам и левая лобэктомия — двум пациентам. Остаточный размер печени был серийно оценен с помощью компьютерной томографии (КТ) у 15 пациентов: шесть с нормальной печенью, пять с хроническим гепатитом и четыре с циррозом. Полное восстановление остаточного размера печени было обнаружено в течение 3 месяцев через 3 и 6 месяцев соответственно у двух пациентов с нормальной печенью.Печень увеличивалась у всех пациентов с паренхиматозными заболеваниями, но, очевидно, медленнее по сравнению с нормальной печенью. Функции печени восстанавливались в норме в течение 2-3 недель у пациентов с нормальной печенью, но гипербилирубинемия сохранялась дольше у пациентов с хроническим гепатитом и циррозом. Постоянное повышение уровня билирубина было зловещим признаком печеночной недостаточности и последующей смерти, которая произошла у пяти пациентов с циррозом печени. Уровень альфа-фетопротеина в сыворотке крови не повышался в соответствии с регенерацией.Гистологически признаки активной регенерации с повышенной митотической активностью были обнаружены через 10 и 35 дней у пациентов с нормальной печенью. В образце, взятом через 7 дней, митоз не наблюдался. Увеличенные кубовидные гепатоциты и клетки с базофильной цитоплазмой или двумя ядрами наблюдались более или менее во всех образцах. Печень с циррозом или гепатитом также показала гистологические доказательства регенерации в течение первых 2 месяцев, но значительно меньше по сравнению с нормальной печенью, что было хорошо подтверждено объемным исследованием остатков печени с помощью КТ.
Новое понимание морфологии печени человека: исследование трупов
Предпосылки . Ежедневные достижения в таких областях радиологии, как сонография и КТ, должны возродить интерес к изучению морфологических особенностей печени на трупах, поскольку добавочные трещины являются потенциальным источником диагностических ошибок. Добавочные трещины варьируются от единичных до множественных на разных участках печени. Цель . В настоящем исследовании морфологические особенности образцов печени человека были оценены с помощью макроскопического исследования и морфометрического анализа. Методы . Исследование проводилось на 58 образцах, полученных из трупов, которые использовались для обычного вскрытия у студентов-медиков с 2004 по 2012 год на кафедре анатомии Медицинского колледжа MIMS. Результаты . В настоящем исследовании печень, описанная в анатомической литературе с нормальными поверхностями, трещинами и границами, считалась нормальной. Из 58 образцов 24 были нормальными, без каких-либо дополнительных трещин или долей и с нормальными контурами.Два образца были с гипоплазией левых долей. Язычный отросток левой доли обнаружен только у одного экземпляра. Выводы . Знание различных дополнительных трещин печени предотвращает неправильный диагноз кистозных поражений или любых патологических поражений печени.
1. Введение
Печень является самым массивным из внутренних органов, занимает значительную часть брюшной полости, то есть правое подреберье и эпигастрий, и простирается в левое подреберье до левой боковой линии [1].Это клиновидный орган с узким концом, направленным влево. Он выпуклый спереди, справа, сверху и сзади и несколько вогнутый снизу, где он принимает форму соседних внутренностей [2]. Несмотря на то, что поверхность гладкая, анатомы обычно делят печень на большую правую и гораздо меньшую левую долю по линии прикрепления серповидной связки спереди и щели для круглой связки и венозной связки на нижней поверхности.В дополнение к правой и левой долям, есть две дополнительные доли, квадратная доля спереди и хвостатая доля сзади, отделенные друг от друга воротами печени (рис. 1).
Квадратная доля, видимая на нижней поверхности, выглядит несколько прямоугольной и ограничена спереди нижней границей, слева — трещиной круглой связки, сзади — воротами печени и справа — ямкой желчного пузыря. (Рисунок 1).
Хвостатая доля видна на задней поверхности, ограничена слева бороздой для венозной связки, внизу — воротами печени, а справа — бороздой для нижней полой вены.Выше он продолжается до верхней поверхности. Внизу и справа у него узкий хвостатый отросток. Снизу и слева он имеет небольшой круглый сосочковый отросток (рис. 1).
Грубые аномалии печени, несмотря на комплексное развитие, встречаются редко. Наиболее частыми грубыми отклонениями являются неправильная форма, количество долек и наличие кист. Менее распространенной аномалией является появление одной или нескольких добавочных печеночных или долей [3].
2. Материалы и методы
58 образцов печени, имеющихся в анатомическом отделении Института медицинских наук Махараджи, составили материал для исследования.Образцы печени были взяты из трупов взрослых людей во время обычного вскрытия для студентов-медиков с 2004 по 2012 год, а затем сохранены в 10% формалине.
Каждая доля печени, то есть правая доля, левая доля, хвостатая доля и квадратная доля была детально изучена на предмет размера, формы, дополнительных трещин и дополнительных долей. Морфометрические данные включали вес, максимальную высоту по вертикали и максимальную ширину.
3. Результаты
3.1. Морфометрические данные
Вес печени колебался от 900 граммов до 2 кг.Максимальная высота колебалась от 9 см до 24 см. Максимальная ширина колебалась от 11,8 см до 20 см.
3.2. Морфологические аспекты
В настоящем исследовании печень с нормальными поверхностями, трещинами и границами считалась нормальной. Из 58 образцов 24 (41,37%) были нормальными без каких-либо дополнительных трещин или долей и с нормальным контуром (рис. 1). Из оставшихся 34 экземпляров 31 (53,44%) образец, хотя они и выглядят нормальными, имел добавочные трещины на левой доле, правой доле, хвостатой доле и квадратной доле, что привело к образованию вспомогательных долей.Гипоплазия левой доли отмечена в 2 (3,44%) экземплярах. Язычный отросток левой доли присутствовал только в 1 (1,72%) экземпляре (табл. 1).
| |||||||||||||
3.2.1. Правая доля
У 8 образцов добавочные трещины наблюдались в различных областях правой доли (таблица 2). Из этих 8 образцов, 6 образцов показали дополнительные трещины между хвостатым отростком и двенадцатиперстной кишкой (рис. 2). Эти трещины различались по размеру и глубине. В 1 образце 2 небольшие дополнительные трещины привели к появлению 2 небольших дополнительных долей у основания желчного пузыря рядом с его нижней границей (рис. 3).Один образец с диафрагмальными отпечатками, то есть печень Неттера типа 7 [4], также был отмечен в настоящем исследовании (рис. 4).
3.2.2. Левая доляВ 6 образцах были отмечены дополнительные трещины на различных участках левой доли печени (Рисунки 5 и 6) (Таблица 2). Два образца были с гипоплазией левых долей (рис. 7). В 1 образце выявлен язычный отросток левой доли, то есть тип Неттера 5 [4], (рис. 8). 3.2.3. Хвостовая доляИз 31 образца у 8 были обнаружены добавочные щели и добавочные доли в хвостатой доле (Таблица 2) (Рисунок 9).В 1 образце трещина оказалась между хвостатым отростком и сосочковым отростком (рис. 10). 3.2.4. Квадратная доляИз 9 образцов с дополнительными трещинами в квадратной доле 1 образец показывает полную поперечную трещину, разделяющуюся на верхнюю и нижнюю доли (рис. 11). Квадратная доля варьируется по форме от треугольной (Рисунок 12) до неправильной (Рисунок 13), а также варьируется по размеру от очень узкой (Рисунок 14) до плохо очерченной, а также непрерывной с левой долей из-за наличия неполной трещины связки. teres (рисунок 15). В 1 образце дополнительные трещины присутствуют над правой, левой, хвостатой и квадратной долями (рис. 16). В одном экземпляре добавочные доли присутствуют как в хвостатой, так и в квадратной долях (рис. 17). 4. ОбсуждениеИз всех органов пищеварения печень начинает свой органогенез рано, на 3-й неделе внутриутробной жизни и развивается наиболее быстро [5].Грубые аномалии печени, несмотря на комплексное развитие, встречаются редко. Более частыми грубыми отклонениями являются неправильные формы, а менее распространенными отклонениями являются появление одной или нескольких добавочных долей печени или долей [3]. Брэдли [6] много сделал для выяснения развития печени. Единая печень у некоторых низших животных, таких как свинья и собака, имеет отчетливые дольки, разделенные тяжами соединительной ткани, и иногда печень человека показывает это изменение путем реверсии [3]. Вариации анатомии печени человека классифицируются как врожденные и приобретенные [7].Врожденные аномалии печени можно разделить на аномалии из-за дефекта развития и аномалии из-за чрезмерного развития. Неправильное развитие левой доли печени может привести к завороту желудка, тогда как неправильное развитие правой доли может оставаться латентным или прогрессировать до портальной гипертензии [8]. Чрезмерное развитие печени приводит к образованию добавочных долей печени, которые могут нести риск перекрута [8]. Приобретенные изменения морфологии печени представлены следующими характерными признаками: (1) язычковые доли, (2) реберный орган с очень маленькой левой долей, (3) глубокие почечные вдавления и сужение по типу «корсет» и локальное воспаление органа или желчный пузырь [9].Дополнительные трещины печени являются потенциальными источниками диагностических ошибок как при сонографии, так и при КТ (Y.H. Auh et al. [10]). Сонографически множественные дополнительные трещины также могут быть ошибочно приняты за макронодулярную печень, поэтому дополнительная компьютерная томография часто бывает полезной для дальнейшей оценки [10]. Множественные печеночные трещины и доли чаще встречались на нижней поверхности печени, напротив квадратной доли, и в левой доле [11]. В настоящем исследовании 53,44% печени имеют дополнительные трещины на различных частях, особенно на нижней поверхности, согласно Каллену [11].В настоящем исследовании 9 образцов имеют добавочные трещины только в квадратной доле, тогда как в 1 образце добавочные трещины присутствуют как в хвостатой, так и в квадратной долях (Рисунок 16), а в другой печени — во всех долях, то есть правой, левой, хвостатой, и квадратные доли имеют дополнительные бороздки на нижней поверхности. Так, всего 11 из 31 экземпляра (35,48%) имеют добавочные трещины в квадратной доле. 5. ЗаключениеВ устоявшейся анатомической литературе очень редко упоминается частота добавочных трещин в различных долях печени.Это исследование, безусловно, пролило бы свет на важность таких вариантов появления. Знание дополнительных трещин над различными частями печени важно для рентгенологов, что предотвращает ошибочный диагноз кистозных поражений или любых макроскопических патологических поражений печени. Ученые выращивают простую человеческую печень в чашке Петри: выстрелыВ чашках Петри растут «печеночные почки». Зачатки имеют ширину около 5 мм, что составляет половину высоты классического блока Lego. Предоставлено Таканори Такебе / Высшая школа медицины городского университета Иокогамы скрыть подпись переключить подпись Предоставлено Таканори Такебе / Высшая школа медицины городского университета Иокогамы«Почки печени» выращивают в чашках Петри.Зачатки имеют ширину около 5 мм, что составляет половину высоты классического блока Lego. Предоставлено Таканори Такебе / Высшая школа медицины городского университета ИокогамыЯпонские ученые открыли новую причудливую главу в эпоху научно-фантастического взаимодействия со стволовыми клетками. Группа из Иокогамы сообщила, что вырастила примитивную печень в чашке Петри, используя клетки кожи человека. Орган неполный. Не хватает нескольких частей.И пройдут годы, а может быть, десятилетия, прежде чем техника попадет в клиники. Тем не менее, эта рудиментарная печень — первый сложный функционирующий орган, который будет выращен в лаборатории из стволовых клеток кожи человека. Когда ученые трансплантировали этот орган мыши, она работала как обычная человеческая печень. «Это огромный шаг вперед», — говорит Джордж Дейли из Гарвардского института стволовых клеток Робу Штайну из NPR. «Были группы, которые пытались генерировать клетки печени, и это было многообещающим», — говорит Дейли, который не участвовал в текущем исследовании.«Это первая попытка регенерировать орган путем смешивания клеток, которые являются критическими компонентами этого органа». Несколько лабораторий по всему миру пытались выращивать органы на пластиковых каркасах, которые предлагают трехмерную поверхность, на которой могут прилипать клетки. Этот подход был использован для создания трахеи из собственных клеток человека. И врачи даже пересадили эти синтетические органы нескольким пациентам. Но более сложные органы — почки, поджелудочная железа и печень — были неуловимы.Итак, Таканори Такебе и команда из городского университета Йокогамы попробовали более непринужденную стратегию: они позволили клеткам построить свои собственные леса. Команда взяла несколько клеток печени (сделанных из индуцированных человеком плюрипотентных стволовых клеток), а затем смешала их с двумя другими типами клеток: одним из которых формируются кровеносные сосуды, а другим — соединительной тканью, которая скрепляет орган. Пять дней спустя Такебе был «совершенно потрясен» тем, что он увидел в чашке Петри, сказал он репортерам во вторник с помощью переводчика. Смеси клеток собрались в крошечные трехмерные структуры, которые выглядели и действовали как миниатюрные печень или «печеночные почки», как их называет Такебе. Прото-органы были всего около 5 миллиметров в высоту, или половину высоты кубика Лего.Но у ливретов были построены собственные кровеносные сосуды, что позволило Такебе и его команде протестировать их на мышах. Они вырвали почки печени из чашки Петри и затем соединили их с кровеносными сосудами мыши. Примерно через 10 дней бутоны заработали. Они расщепляли человеческие лекарства и производили белки крови, как и обычная печень. Один протоорган даже спас мышь от печеночной недостаточности, сообщают Такебе и его коллеги в журнале Nature . Результаты «чрезвычайно обнадеживают», — говорит Стюарт Форбс из Эдинбургского университета, занимающийся стволовыми клетками.«Но [требуется] значительное количество дополнительных исследований, прежде чем мы сможем перевести это в клиническую терапию для пациента», — говорит он Стейну. Во-первых, органы слишком малы, чтобы быть полезными. Врачам понадобятся тысячи из них, чтобы помочь человеку с повреждением печени. И маленькие бутоны не образуют полноценную печень. У них отсутствуют желчные протоки или трубки, по которым выводятся токсины. Plus, по словам Forbes, все еще остается под большим вопросом о безопасности. Стволовые клетки склонны к образованию опухолей.И текущее исследование не рассматривает долгосрочный эффект трансплантированной печени. «Чтобы сделать это на людях, мы хотели бы провести много испытаний на безопасность», — говорит Форбс. Применение органоидов печени человека в качестве первичной модели для пациентов с инфекцией HBV и родственной гепатоцеллюлярной карциномой
Действительно, как отмечают обозреватели, мы наблюдали значительные различия в показаниях разных доноров.Как предлагают составители обзора, чтобы лучше охарактеризовать, является ли источник вариабельности ДНК HBV, как внутриклеточной, так и кскДНК, обусловленной вариабельностью донора, вариацией от партии к партии или вариациями в методе обнаружения, мы количественно исследовали вирусные нуклеиновые кислоты после ex vivo HBV. инфицирование органоидов, полученных от четырех независимых доноров. Органоиды от четырех доноров были инфицированы одновременно одной и той же партией вируса, и внутриклеточная ДНК HBV была количественно определена и обнаружена параллельно, чтобы исключить вклад вариаций в методе обнаружения в наблюдаемую изменчивость (линии 135-137 и рисунок 1, приложение к рисунку 3c из переработанная рукопись).Чтобы оценить влияние вариации от партии к партии на наблюдаемую вариабельность уровней инфекции, мы также заразили независимых доноров на двух разных пассажах культур одной и той же партией HBV, и мы наблюдали сопоставимые уровни внутриклеточной ДНК HBV в органоидах, полученных из один и тот же донор в разных отрывках (строки 135–137 и рис. 1, приложение к рис. 3d отредактированной рукописи). Таким образом, наши данные демонстрируют, что вариации от партии к партии не вносят значительного вклада в наблюдаемую изменчивость.Тем не менее, мы наблюдали значительные различия во внутриклеточных уровнях ДНК HBV между разными донорами органоидов, которые были инфицированы в одно и то же время одной и той же партией вируса и обрабатывались одновременно (строки 136 и рисунок 1, приложение к рисунку 3c пересмотренной рукописи), демонстрируя, что Наблюдаемая нами вариабельность эффективности инфекции — это действительно вариабельность от донора к донору. Наши данные также согласуются с вариабельностью эффективности инфицирования от донора к донору, наблюдаемой для первичных гепатоцитов человека (Shlomai et.al, PNAS 2014). Теперь мы обсудим эти результаты в строках 135–137 исправленной рукописи.
Как отмечают составители обзора, присутствие либо кскДНК, либо коровой ДНК HBV было продемонстрировано с помощью саузерн-блоттинга сыворотки от пациентов, инфицированных HBV, на клеточных линиях, содержащих стабильно интегрированный геном HBV (например,грамм. HepG2.2.15), клеточные линии, трансфицированные геномом HBV, содержащим плазмиду, или NTCP, сверхэкспрессирующие клетки HepG2, и полученные из ИПСК гепатоподобные клетки, инфицированные HBV, которые можно вносить в крупномасштабную культуру, а также эффективно выделять коровые частицы HBV. [например Zhou et al., Antiviral Res. 2006; 72: 116-124; Cai et al., Methods Mol Biol. 2013; 1030: 151–161; Сантантонио и др., Rec Clin Lab 1990; 20 (1): 29-35; Бонино и др., Hepatology 1981; 1 (5): 386-391; Guo et al., Scientific Rep., 2016; 6: 2552; Cui et al., J. Virology 2013; 87 (21): 11494-11503; Ли и др., Virus Genes 2003; 27 (3): 227-235; Кониг и др., J. Hepatology, 2019; 71 (2): 289-300; Сакураи и др., Научный представитель 2017; 7: 45698]. Расширение органоидов печени в крупномасштабных трехмерных культурах, их дифференциация и заражение ex vivo, помимо того, что они требуют много времени и дороговизны, создают серьезные проблемы для получения больших количеств внутриклеточной ядерной ДНК HBV. Действительно, недавняя статья, в которой описывалась трехмерная hiPSC органоидная система печени в качестве модели для изучения инфекции HBV, продемонстрировала присутствие внутриклеточной ядерной ДНК HBV с помощью ПЦР, а не блоттинга по Саузерну (Nie et al., EBioMedicine 2018; 35: 114–123). Мы приложили значительные усилия для организации эксперимента по Саузерн-блоттингу для модели органоида, инфицированного вирусом гепатита B ex vivo, который мы подробно рассмотрим ниже. 10 4 копий внутриклеточной ядерной ДНК HBV.Это означает, что для получения надежного сигнала в нашем эксперименте с блоттингом нам потребуется от 100 (минимум) до 10000 (оптимум) лунок инфицированных органоидов для одного отдельного состояния (с обработкой Nuc или без нее). Предел обнаружения генома HBV с помощью саузерн-блоттинга.A. Последовательное разведение клонированного генома HBV (верхний ряд) и плазмиды, отличной от HBV (нижний ряд), наносили на мембрану Hybond-XL и детектировали с помощью ПЦР-генерированного биотинилированного зонда HBV почти полной длины.Сигнал регистрировали с использованием стрептавидина IRDye 800CW на инфракрасном тепловизоре Li-COR Odyssey. Б. Такое же серийное разведение клонированного генома HBV анализировали с помощью кПЦР. Значения Cq, полученные из выделений ДНК, соответствующих одной лунке 24-луночного планшета от шести независимых инфекций различных донорских органоидов, обозначены цветом + . Обычно для производства вируса HBV мы собираем 500 мл супернатанта, который после концентрирования используется для заражения до 50 лунок (из 24-луночного планшета), содержащих органоиды печени.Следовательно, чтобы заразить количество органоидов, необходимое для эксперимента по Саузерн-блоттингу, нам нужно было бы собрать и сконцентрировать до 50 литров супернатанта. Важно отметить, что во время процедуры экстракции тотальной ДНК выделяется клеточная гДНК (~ 1 мкг), а также внутриклеточная коровая ДНК HBV. Поэтому мы применили существующий протокол выделения нуклеокапсида HBV, обычно используемый для клеточных линий и сывороток [например, Guo et al., J Virol 2005; 79 (5): 2729-42] к органоидам печени и обнаружили, что это привело к потере ~ 50% внутриклеточной ядерной ДНК HBV по сравнению с протоколом экстракции тотальной ДНК, пока она все еще содержит высокий фон геномной ДНК (100 нг геномной ДНК / 0.10 6 копий очищенной ДНК HBV Мы также загружаем ~ 100 мкг геномной ДНК, что превышает связывающую способность мембраны HybondXL (42 мкг для лунки диаметром 3 мм). Однако, чтобы усилить вирусологию HBV, представленную в рукописи, и дополнительно охарактеризовать инфекцию HBV ex vivo органоидов печени, мы провели дополнительные эксперименты с использованием расщепления, опосредованного экзонуклеазой T5, более надежного метода на основе ПЦР для обнаружения внутриклеточной кзкДНК в четырех дополнительные линии донорских органоидов.Используя этот метод, мы подтверждаем, что органоиды печени действительно инфицированы HBV и продуцируют кзкДНК (рис. 1f исправленной рукописи). Эти данные вместе с обширной иммунофлуоресцентной характеристикой экспрессии белков HBV HBx и ядра HBV, а также характеристикой внутриклеточной РНК, ДНК HBV, а также супернатантов органоидной культуры, содержащих инфекционные частицы HBV, обеспечивают однозначные данные, которые демонстрируют успешное инфицирование вирусом. органоиды печени.
Действительно ли наблюдаемая iP-сигнатура соответствует инфекции HBV или является следствием цирроза, это очень важный вопрос, который, следуя комментариям рецензентов, мы приложили значительные усилия для решения, включив в нашу РНК дополнительных доноров и полученные от пациентов линии органоидов. seq анализ (рисунок 6).В частности, в дополнение к здоровому инфицированному донору, представленному в первой версии рукописи, мы теперь включаем двух дополнительных доноров, которые ранее были инфицированы, но избавились от HBV-инфекции (iDonors). Важно отметить, что у этих доноров была печень без цирроза, которую использовали для трансплантации реципиентам, инфицированным HBV (чья циррозная печень была эксплантирована). Мы также включаем двух доноров с фенотипом цирроза печени, перенесших эксплантацию из-за неалкогольного стеатогепатита (НАСГ), но не инфицированных HBV (CN).Мы также включили шестую линию здоровых доноров (hD22) (строки 309–311 и рис. 6a-d отредактированной рукописи). Линии органоидов были засеяны из биоптатов печени или эксплантатов от этих доноров / пациентов и использовались в анализе последовательности РНК. При применении iP-сигнатуры, которую мы сгенерировали при сравнении пяти линий органоидов здоровых доноров (hD) с пятью линиями органоидов, полученных от пациентов с циррозом печени, инфицированных HBV, iDonors, а также iP-CN сгруппированы вдали от здоровых доноров ( Рисунок 6a-d). Интересно, что в то время как iDonors тесно сгруппированы вместе с iPs (Рисунок 6a), образцы CN сгруппированы вдали от iPs (Рисунок 6c).Эти результаты демонстрируют, что полученная нами iP-сигнатура является индикатором инфекции HBV, а не цирротического состояния как такового: инфицированные HBV органоиды iDonors, объединяясь вместе с инфицированными HBV iPs, не были получены из цирроза печени, и, следовательно, подпись не может быть цирротической подписью. Эти результаты теперь обсуждаются в строках 295–318 исправленной рукописи.
Следуя предложению рецензентов, чтобы подтвердить, что наблюдаемые нами различия транскриптомов согласуются с образцами печени до образования органоидов, мы исследовали экспрессию генов-кандидатов, идентифицированных в нашей генной сигнатуре, в первичных гепатоцитах, полученных из тканей здоровых или инфицированных HBV. доноры.Мы действительно наблюдали повышенную регуляцию экспрессии мРНК ADAMTS1, CORO1A, PTHLH, STMN2 и STY5 в первичных гепатоцитах iP по сравнению с гепатоцитами hD (рис. 5c). Кроме того, мы исследовали экспрессию выбранных кандидатных генов сигнатуры с повышенной регуляцией в независимых линиях органоидов hD, инфицированных ex vivo HBV или инактивированным нагреванием вирусом. В ответ на инфицирование органоидов HBV сигнатурные гены были умеренно активированы, хотя и незначительно, учитывая низкий процент инфекции, а также изменчивость донора к донору, присущую системе (рис. 5, приложение 1а).Мы обсуждаем эти результаты в строках 282–289 исправленной рукописи.
Здоровый донор, полученный от пациентов и трансдуцированный лентивирусом NTCP, сверхэкспрессированные органоиды печени проявляли печеночные свойства после семи дней культивирования в среде для дифференцировки (DM).Маркеры дифференцированных гепатоцитов, которые указывают на свойства клеток печени, остаются стабильно экспрессируемыми в органоидах DM в течение всего периода культивирования, которые, как мы показали на Рисунке 1 — рисунке в приложении 2, могут сохраняться более одного месяца (27 дней после заражения). (строка 132-134). В отсутствие спиновой инфекции ex vivo дифференцированные культуры органоидов можно поддерживать до двух месяцев с периодическим культивированием в среде для размножения (данные не показаны). Теперь мы предоставляем эту информацию в разделе методов (строки 588–590).
Как отмечают обозреватели, мы не смогли найти каких-либо количественных признаков репликации HBV в органоидах, полученных от пациентов. Супернатанты культуры iP-органоидов не содержали ДНК HBV ни в среде для размножения, ни в среде дифференцировки. Нам также не удалось обнаружить внутриклеточную РНК HBV или ДНК из органоидов iP.Органоиды печени образуются из взрослых стволовых клеток, присутствующих в печени. Хотя эти ASC могут не поддерживать активную репликацию вируса, они все же могут содержать части интегрированной ДНК HBV с еще не охарактеризованной функцией. Предыдущие полногеномные анализы тканей пациентов с ГЦК выявили области генома HBV, которые должны быть интегрированы как в ткань, не инфицированную HBV, так и в HCC, полученную у этих пациентов (Sung et al., 2012; Zhao et al., 2016). Поэтому, чтобы лучше учесть комментарии рецензентов, мы провели ПЦР-анализ геномной ДНК, полученной из инфицированных органоидов, полученных от пациентов, чтобы проверить, интегрирован ли HBV в геном этих iP-линий.Интересно, что в пяти из шести проанализированных линий органоидов iP мы обнаружили интегрированные части генома HBV, соответствующие части кодирующей области HBx (Рисунок 4 — рисунок в приложении 1). Интересно, что у здорового донора, который ранее был инфицирован HBV, но после того, как инфекция исчезла (iDonor1), также наблюдалась интеграция HBV, соответствующая области HBx (рисунок 4 — приложение к рисунку 1). Это открытие указывает на то, что, хотя у человека, возможно, исчезла активная репликация HBV, части генома остаются интегрированными в ДНК хозяина, функциональные последствия для которых еще предстоит охарактеризовать.Эти новые данные теперь представлены на Рисунке 4 — добавлении к рисунку 1 и обсуждаются в строках 243–250 и строках 406–417 исправленной рукописи. [Примечание редакции: до принятия были предложены дальнейшие исправления, как описано ниже.]
Благодарим рецензентов за это предложение. На рисунках 6C и 6D пересмотренной рукописи мы теперь включаем доноров, которые избавились от инфекции (iDonors 1-4), вместе с донорами, у которых был цирроз печени из-за НАСГ (CN1-4), в тот же иерархический кластерный анализ и график MDS. Мы приложили значительные усилия для усиления нашего анализа и выводов, включив, как указано выше, еще одного инфицированного донора, избавившегося от HBV (iDonor 4), и двух дополнительных доноров, у которых был цирротический фенотип из-за НАСГ (CN3-4).Применяя iP-сигнатуру, управляемую HBV, которую мы сгенерировали при сравнении пяти линий органоидов здоровых доноров (hD) с пятью HBV-инфицированными линиями органоидов (iPs) пациентов с циррозом печени, мы заметили, что iDonors тесно группируются с iPs и вдали от HD, хотя они фенотипически напоминают HD (рис. 6A-B). Важно отметить, что включение iDonors в анализ не изменило кластеризацию образцов CN отдельно от iPs (рис. 6 C-D). Эти данные, полученные от дополнительных доноров, согласуются с нашими предыдущими данными и подтверждают представление о том, что сгенерированная нами iP-сигнатура является управляемой HBV, а не общей цирротической сигнатурой (строки 313, 320, Таблица -1).
Основываясь на рекомендациях составителей обзора, чтобы подтвердить NTCP-зависимость HBV-инфекции органоидов печени, мы провели эксперименты с HBV-инфекцией in vitro с (предварительной) обработкой органоидов печени мирклюдексом-B, ингибитором проникновения HBV, который функции путем блокировки NTCP.Действительно, блокирование NTCP приводит к снижению инфицирования HBV, что измеряется посредством количественного определения внутриклеточной РНК HBV, а также ДНК HBV и HBeAg в супернатанте инфицированных органоидов (представленных на рис. 3 C, D и E исправленной рукописи (строки 190 -197)). Мы также измерили, как было предложено составителями обзора, присутствие HBeAg в культуральных супернатантах инфицированных органоидов печени в качестве дополнительного маркера активной репликации HBV (подтверждая наши данные, демонстрирующие внутриклеточные РНК и ДНК HBV, ДНК HBV и поверхностный Ag, продуцируемые и обнаруживаемые в супернатант культуры и вирусные белки HBV, обнаруженные с помощью иммунофлуоресцентной микроскопии).Данные, демонстрирующие опосредованную инфекцией HBV продукцию HBeAg в инфицированных органоидах печени, представлены на Рисунке 1G исправленной рукописи (строки 122-123). https://doi.org/10.7554/eLife.60747.sa2границ | Стволовые клетки печени человека: мезенхимальные стромальные клетки, полученные из печени, с прорегенеративными свойствамиВведениеПо оценкам, в настоящее время 1,5 миллиарда человек страдают хроническими заболеваниями печени, которые в конечном итоге переходят в фиброз и цирроз (Moon et al., 2020). Трансплантация печени в настоящее время является единственным эффективным методом лечения, радикально улучшающим исход печеночной недостаточности. Несмотря на усилия по расширению пула доноров органов за счет расширения критериев отбора и трансплантации органов от родственных живых доноров, нехватка доноров по-прежнему остается главной проблемой, которую необходимо решить (Adam et al., 2018). Хотя трансплантация гепатоцитов, полученных из печени взрослых или новорожденных, считается альтернативой трансплантации органов и представляет собой потенциальный вариант лечения также у пациентов с острой печеночной недостаточностью (Dhawan et al., 2010), основным ограничением является доступность органов для выделения гепатоцитов, а также сложность их увеличения in vitro (Squires et al., 2017). В этом состязании использование стволовых клеток в качестве возможного источника клеток для восстановления печени стало новым потенциальным терапевтическим подходом. Стволовые клетки печени человека (HLSC) были впервые выделены в 2006 году с использованием уникального метода, основанного на строгих условиях культивирования, при котором зрелые гепатоциты претерпевают клеточную гибель, оставляя клоны HLSC, которые легко расширяются и обладают множественной способностью к дифференцировке (Herrera et al. al., 2006). Это открытие было признано инновационным и привело к получению в 2006 г. патента на новый источник стволовых клеток печени (WO2006126219A1, клетки-предшественники печени). Цель этого обзора — описать HLSC и их биопродукты, а также их потенциальные эффекты в различных терапевтических областях, таких как регенеративная медицина, онкология и генетические заболевания печени. Выделение и характеристика HLSCHLSC были выделены как из первичных культур, так и из криоконсервированных гепатоцитов человека, культивированных в строгих условиях (Herrera et al., 2006). Они достигли слияния в течение 3 недель после культивирования, и их можно было субкультивировать и размножать до больших количеств в течение примерно 6 месяцев, не подвергаясь старению (Herrera et al., 2006). Напр., HLSCs, поддерживаемые в недифференцированных условиях культивирования в течение приблизительно 2–3 месяцев с продолжительностью жизни 200–250 удвоений, сохраняют замечательную стабильность, демонстрируемую сохранением длины теломер во время экспансии (Bruno et al., 2019b). HLSC отрицательны в отношении гемопоэтических маркеров (CD34, CD45, CD117 и CD133), а также лейкоцитарного антигена человека (HLA) класса II и костимулирующих молекул, таких как CD40, CD80 и CD86 (Bruno et al., 2016). Кроме того, они экспрессируют некоторые маркеры мезенхимальных стромальных клеток (MSC) (CD29, CD73, CD44 и CD90) вместе с альбумином, α-фетопротеином, цитокератином (CK) -8 и CK-18, что указывает на мезенхимальное происхождение с частичной детерминацией. к печеночной линии. Они также экспрессируют обычные маркеры стволовых клеток, такие как виментин и нестин, и маркеры эмбриональных стволовых клеток, такие как Oct3 / 4, Nanog, SSEA4, Sox2 и Musashi1 (рис. 1), которые связаны с самообновляющейся способностью и мультипотентностью. Однако, в отличие от хорошо известной популяции печеночных клеток-предшественников, известной как овальные клетки у грызунов, HLSC не экспрессируют CK-7, CK-19, c-kit, CD133 и альфа-актин гладких мышц (α-SMA) (Gaudio et al. al., 2009). Овальные клетки были впервые описаны в 1950-х годах Фарбером и его коллегами и имеют овальное ядро и скудную цитоплазму. В своих экспериментах Фабер и его коллеги наблюдали митоз в мелких желчных протоках и гиперплазию овальных клеток после этиониновой диеты (Farber, 1956). Последующие исследования показали, что активность этих клеток-предшественников в основном присутствовала в канале Геринга и участвовала в бипотентной активности, замещая как поврежденные гепатоциты, так и холангиоциты (Wei et al., 2020). Хотя существуют различия в фенотипических маркерах между HLSC и овальными клетками, мы можем только предполагать, что HLSC представляют собой отдельную нишу стволовых клеток в печени, поскольку это не было подтверждено in vivo . Рисунок 1. Фенотипическая характеристика и дифференцировочная способность HLSC. Белковые маркеры, экспрессируемые и не экспрессируемые HLSC, перечислены в двух верхних панелях. При культивировании в соответствующих условиях HLSC могут дифференцироваться в гепатоцитоподобные клетки, эндотелиальные клетки, остеоциты и клетки поджелудочной железы.Экспрессия тканеспецифических маркеров, полученных с помощью дифференцированных HLSC, представлена на нижних четырех панелях. Было показано, что печень взрослого и плода содержит другие популяции стволовых клеток, которые экспрессируют некоторые маркеры, подобные HLSC (Таблица 1). Например, Najimi et al. Описали в 2007 году взрослые стволовые клетки печени человека (ADHLSC), которые экспрессируют как печеночные, так и мезенхимальные маркеры, такие как альбумин и виментин. Однако их положительность в отношении α-SMA и CD13, а не CD105 (Najimi et al., 2007), предположили, что ADHLSC отличаются от HLSC. Альтернативный подход, описанный Lee et al., Который включал культивирование непаренхимальной фракции нормальной взрослой печени человека (Lee et al., 2012), привел к выделению HLSC, экспрессирующих маркеры MSC (CD29, CD73, CD44, CD90, CD105 и CD166, виментин), нестин и печеночные маркеры (CD26, CK-8 и CK-18) (Lee et al., 2012). Более того, Пан и его коллеги описали присутствие МСК-подобной популяции печени (L-МСК), положительной по CD90, CD105 и CD166 (Pan et al., 2011) в консервирующей жидкости трансплантата печени. Стромальные клетки печени (LSC), описанные Kellner et al. была еще одна популяция клеток, выделенная и размноженная из биопсии печени человека, которая экспрессировала CD105, CD90 и CD73 (Kellner et al., 2015). Помимо ткани печени взрослого человека, стволовые клетки также были выделены из ткани печени плода. Например, стволовые клетки печени с характеристиками МСК и маркерами (CD29, CD73, CD44, CD90, CD105, CD166 и виментин) были получены из печени плода в первом и втором триместре (LHMSC).Эти клетки были положительными по CD26, альбумину, СК-8 и СК-18, что указывает на частичную приверженность к дифференцировке печени (Campagnoli et al., 2001; In‘t Anker et al., 2003). Кроме того, Dan et al. идентифицировали другую популяцию клеток из печени плода, известную как мультипотентные клетки-предшественники фетальной печени человека (hFLMPCs). Эти клетки коэкспрессируют MSC (CD44, CD90 и виментин), гематопоэтические (CD34, c-kit) и холангиоцитарные (CK-19) маркеры, а также EPCAM, c-met, SSEA4 и гепатоциты (CK-18). ) (Дэн и др., 2006). Таким образом, эти исследования указывают на несколько популяций клеток-предшественников / стволовых клеток, происходящих из печени человека, которые имеют сходства и различия и проявляют регенеративные свойства, тем не менее, остаются ли эти клетки локализованными в печени или развиваются в условиях культивирования ex vivo , еще предстоит выяснить (таблица 1). Таблица 1. Происхождение, маркеры и возможности дифференциации МСК-подобных популяций печени. Подобно МСК, HLSC проявляют иммуномодулирующие свойства, подавляя активацию иммунных клеток.В частности, поскольку HLSC конститутивно экспрессировали циклооксигеназу 1 и индоламин-2,3-диоксигеназу, они были способны снижать пролиферацию стимулированных митогеном Т-лимфоцитов дозозависимым образом. HLSC также предотвращали способность естественных клеток-киллеров (NK) к дегрануляции, и эксперименты с блокировкой антител против HLA-G показали, что ингибирующее действие HLSC на активность NK опосредовано высвобождением растворимого HLA-G. Более того, HLSC подавляли дифференцировку и созревание дендритных клеток (ДК), а ингибирование простагландина E2 значительно снижало негативный эффект HLSC на дифференцировку ДК (Bruno et al., 2016). Кроме того, ADHLS (Lombard et al., 2019), LSC и LHMSC также проявляли иммуномодулирующие эффекты (In‘t Anker et al., 2003; Kellner et al., 2015). Недавние исследования показали, что можно получить и расширить HLSC в рамках надлежащей производственной практики (GMP). Основной банк клеток (MCB) HLSC был создан в 2011 году утвержденным центром GMP (Areta International, Геренцано, Италия), начиная с фрагмента печени донора от 10 до 15 мм, в соответствии со стандартными критериями, установленными Centro Nazionale Trapianti. и требованиям Директивы 2001/20 / EC (Bruno et al., 2019b; Spada et al., 2020). Все реагенты в процессе производства MCB были пригодны для клинического использования, проверены на соответствие спецификациям, чтобы гарантировать, что они получены от квалифицированного поставщика в соответствии с европейскими и итальянскими стандартами GMP. Качество продукта было проверено на безопасность и эффективность в соответствии с утвержденными методами (Spada et al., 2020). Кроме того, HLSC, полученные в этих условиях, экспрессировали маркеры MSC (CD29, CD73, CD90 и т. Д.), Маркер-предшественник гепатоцитов (α-фетопротеин), белок зрелого гепатоцита (альбумин), маркеры стволовых клеток (виментин и нестин) и эмбриональные стволовые клетки. маркеры (Oct3 / 4, Nanog, SSEA4, Sox2 и Musashi1).Кроме того, они были отрицательными в отношении маркера печеночных овальных клеток CK-19 и α-SMA (маркера активированных звездчатых клеток) (Bruno et al., 2019b; Spada et al., 2020). Более того, профилирование генов HLSC с MSC, полученными из костного мозга, с использованием специфического массива MSC PCR выявило HLSC, которые демонстрируют профиль экспрессии генов, аналогичный MSC. Только 13 из 84 генов дифференциально экспрессировались в HLSC по сравнению с MSC. Профиль экспрессии генов также подтвердил присутствие специфических печеночных маркеров, таких как фактор роста гепатоцитов (HGF) и CK-18 в HLSC (Bruno et al., 2019б). Способность к дифференцировке HLSCin vitroУспех в создании «новой печени» представляет собой одну из наиболее важных экспериментальных стратегий, которая может решить проблему нехватки доноров для трансплантации печени (Saito et al., 2020). О способности HLSC дифференцироваться в функциональные гепатоцитоподобные клетки сообщалось с использованием различных систем in vitro или ex vivo (рис. 1). Для получения дифференцировки в гепатоциты HLSC культивировали как в условиях адгезии, так и в условиях микрогравитации в средах, дополненных факторами роста.В частности, HLSC, поддерживаемые в течение 15 дней в присутствии HGF и фактора роста фибробластов (FGF) 4, изменили свою морфологию с удлиненных на кубовидные клетки. Экспрессия AFP была снижена, а экспрессия CK-8 и CK-18 увеличена. При культивировании в ротационной системе культивирования клеток (RCCS) в присутствии HGF и FGF-4 HLSC дифференцировались в функциональные гепатоцитоподобные клетки, которые экспрессировали цитохром P450 (CYP450) и были способны продуцировать мочевину (Herrera et al., 2006; Fonsato et al., 2010). В отличие от этого открытия, альбумин был синтезирован и высвобожден HLSC, культивированными как в условиях адгезии, так и в условиях микрогравитации (Herrera et al., 2006). Эти данные показали, что вращающаяся система способствует созреванию HLSC в функциональные гепатоцитоподобные клетки, поскольку та же самая комбинация факторов роста не позволяет дифференцироваться в функциональные гепатоциты HLSC в 2D-культурах. Кроме того, при культивировании в биоискусственной печени, состоящей из фильтра из упакованных полых волокон, соединенных с перфузионной системой роторного биореактора, HLSC утратили свои маркеры стволовых клеток и приобрели некоторые свойства, такие как зрелые гепатоциты, такие как секреция альбумина, мочевины и HGF и повышенная экспрессия изоферментов CYP450 по сравнению с HLSC, поддерживаемыми в условиях адгезионного культивирования.Более того, во вращающейся системе HLSC приобрели специфические функции зрелых гепатоцитов, такие как потребление глюкозы, ферментативная активность CYP450, синтез гликогена и включение / высвобождение индоцианинового зеленого (Fonsato et al., 2010). Напротив, ADHLCS уже проявляли ферментативную активность CyP3A4 в базовых условиях (Najimi et al., 2007) и эффективно дифференцировались в метаболически активные гепатоцитоподобные клетки в условиях адгезии, покрытых коллагеном I in vitro после последовательной инкубации со специфическими факторами роста и цитокинами. (Хуу и др., 2011). Для создания функционального органа печени важно воссоздать компоненты нативных клеток (гепатоциты, эндотелиальные и эпителиальные клетки) вместе со специфическим микросредой печени (компоненты внеклеточного матрикса), способные обеспечить структурную и функциональную поддержку новому органу. Один из наиболее инновационных экспериментальных подходов представлен технологиями ксенотрансплантации и тканевой инженерии, которые пытаются децеллюляризировать и рецеллюляризовать остаточный каркас с клетками-реципиентами (Rossi et al., 2019). Используя бесклеточные каркасы печени крысы (RLAS) в качестве биологической поддержки, HLSC смогли дифференцироваться в гепатоцитоподобные клетки (Navarro-Tableros et al., 2015; Рисунок 1). Они приобрели экспрессию зрелых печеночных маркеров, таких как лактатдегидрогеназа (ЛДГ) и три подтипа CYP450 с параллельным повышением экспрессии альбумина. Кроме того, гепатоцитоподобные клетки, полученные с использованием RLAS, оказались метаболически активными, о чем свидетельствует присутствие азота мочевины в кондиционированной среде.Кроме того, рецеллюляризованный HLSC RLAS содержит подгруппы клеток, расположенных поблизости или должным образом прикрепленных к трубчатым структурам матрикса остатков. Эти клетки экспрессировали маркер холангиоцитов СК-19, эндотелиальный маркер CD31 и мезенхимальный маркер виментин. Все эти наблюдения подтверждают способность HLSC не только дифференцироваться в зрелые гепатоцитоподобные клетки, но также в эпителиально-подобные и эндотелиально-подобные клетки при посеве в естественные каркасы печени (Navarro-Tableros et al., 2015). Следовательно, взаимодействие с матричным дифференциальным пространственным распределением может управлять специфической дифференцировкой HLSC, воспроизводящей, по крайней мере частично, структуру печени. Дифференцировка HLSC в эндотелиальные клетки также была получена путем поддержания HLSC в присутствии фактора роста эндотелия сосудов (VEGF) в течение до 2 недель (рис. 1). В этом состоянии HLSC больше не экспрессировали маркеры стволовых клеток и начали экспрессировать специфические эндотелиальные маркеры, такие как CD31, CD144, фактор фон Виллебранда и рецептор 2 VEGF (Herrera et al., 2006). Поскольку печень и поджелудочная железа имеют общее эмбриональное происхождение (Jennings et al., 2015), мы исследовали, обладают ли HLSCs способность дифференцироваться в клетки поджелудочной железы (Рисунок 1). После длительного культивирования в присутствии высокого содержания глюкозы и никотинамида HLSC изменили свою морфологию и начали формировать небольшие скопления сфероидных клеток поверх монослоя сливающихся клеток. Эти трехмерные кластеры клеток положительно окрашиваются на человеческий инсулин и переносчик глюкозы Glut-2, что указывает на способность HLSC дифференцироваться в островковые структуры (HLSC-ILS) (Herrera et al., 2006). Совсем недавно было продемонстрировано, что HLSC могут быстро дифференцироваться в производящие инсулин трехмерные сфероидальные клеточные агрегаты с помощью одноэтапного протокола, основанного на зарядозависимой агрегации, индуцированной протамином. Полученные HLSC-ILS представляли собой трехмерные органоиды сфероидальных клеток, состоящие из различных клеточных субпопуляций, экспрессирующих инсулин, глюкагон, соматостатин, полипептид поджелудочной железы и грелин, как и α-, β-, δ- и ε-клетки. В базовых условиях HLSC-ILS синтезировали и секретировали базальные уровни инсулина и С-пептида человека, проявляющих незрелый фенотип (Navarro-Tableros et al., 2019). Однако в присутствии высоких концентраций глюкозы и калия HLSC-ILS были способны повышать уровни секретируемого C-пептида (Navarro-Tableros et al., 2019; Gomez et al., 2020). В установке in vivo при имплантации под капсулу почек мышей со стрептозотоциновым диабетом с иммунодефицитом HLSC-ILS значительно снижали гипергликемию. Примечательно, что дальнейшее фенотипическое созревание произошло, когда HLSC-ILS были имплантированы диабетическим мышам, что продемонстрировано активацией специфических транскриптов дифференцировки бета-клеток, таких как PDX1 и NGN3 (Navarro-Tableros et al., 2019). Подобно МСК, HLSC также могут дифференцироваться в направлении остеогенного происхождения (Рис. 1). После 3 недель культивирования в среде для остеогенной дифференцировки образование минерализованной культуры с отложениями кальция с положительным ализарином красным указывает на остеогенную дифференцировку HLSC. Эти остеогенно дифференцированные HLSC утратили экспрессию альбумина, альфа-фетопротеина и CK-18 и приобрели экспрессию костно-специфических белков, таких как остеокальцин и остеопонтин. В отличие от МСК, у HLSC не наблюдалось способности к адипогенной дифференцировке (Herrera et al., 2006). Взятые вместе, эти результаты указывают на плюрипотентность HLSC. Регенеративные способности HLSCin vivoПервое доказательство того, что HLSCs могут вносить вклад в регенерацию печени, было получено на мышиных моделях острого повреждения печени (ALI) (Herrera et al., 2006, 2013). Человеческие клетки были обнаружены в тканях печени мышей через 30 дней после инъекции 2 × 10 5 мышам с иммунодефицитом с повреждением, вызванным N-ацетил-п-аминофеном, что указывает на то, что HLSC могут интегрироваться в регенерирующую печень (Herrera et al., 2006). Это было дополнительно подтверждено на мышиной модели молниеносной печеночной недостаточности (FLF), вызванной лечением мышей внутрибрюшинными инъекциями D-галактозамина и липополисахарида. Инокуляция HLSC (2 × 10 6 ) значительно увеличивала выживаемость мышей и улучшала регенерацию печени, уменьшая апоптоз и увеличивая пролиферацию печеночных клеток, которые пережили травму. На мышиной модели FLF локализацию клеток печени оценивали с помощью IVIS. После внутривенной инъекции HLSC преимущественно накапливались в печени мышей с FLF, но не в печени здоровых мышей.Более того, человеческие клетки были обнаружены в паренхиме печени мышей с иммунодефицитом уже через 7 дней после инъекции. Кроме того, эти клетки совместно экспрессировали CK-8 и CK-18, что указывает на дифференцировку HLSC в гепатоциты. Кроме того, недифференцированная популяция HLSC все еще сохранялась в ткани печени мышей через 21 день после инокуляции. Общий эффект, наблюдаемый после лечения HLSC, включал улучшение функции печени, что оценивалось по снижению уровней аланина и аспартатаминотрансфераз (АЛТ и АСТ) и уровня аммония в плазме.Интересно, что инъекционная кондиционированная среда HLSC (HLSC-CM) имела те же положительные эффекты, что и клетки, что указывает на то, что паракринные факторы, продуцируемые HLSC, могут играть роль в наблюдаемом прорегенеративном эффекте в ограничении острого повреждения. HLSC-CM содержит несколько факторов роста, которые потенциально могут участвовать в регенерации печени, такие как интерлейкин (IL) 8 и 6, VEGF и HGF. В частности, обработка мышей нейтрализующими антителами против HGF человека отменяла защитный эффект HLSC-CM, что свидетельствует не только о важной роли HGF в отношении гепатопротекторных эффектов HLSC-CM, но и о паракринном механизме действия HLSC ( Herrera et al., 2013). Сходные результаты были также получены Khuu et al., Согласно которым ADHLSC были способны ускорять регенерацию печени и приживать in vivo после ALI (Khuu et al., 2013; Herrero et al., 2017). Терапевтический эффект HLSC также оценивался при хроническом заболевании печени (ХЗП), например, на мышиной модели неалкогольного стеатогепатита (НАСГ), вызванного диетой, лишенной метионина и холина (Bruno et al., 2019b). Инъекция 1,5 × 10 6 HLSC в разные моменты времени развития ХЗП не только вызывала улучшение функции и морфологии печени, но также уменьшала воспаление и фиброз, что демонстрировалось снижением экспрессии специфических транскриптов, таких как коллаген I, α -SMA, трансформирующий фактор роста (TGF) -бета и IL-бета-1.Подобно острым моделям повреждения печени, мы также наблюдали присутствие человеческих клеток у мышей с НАСГ через 21 день после инъекции HLSC, что подтверждено гистологическими и молекулярными анализами. Интересно, что в модели НАСГ большинство человеческих клеток, обнаруженных в паренхиме печени, не экспрессировало специфических маркеров печеночной приверженности, предполагая, что дифференцировка HLSC в зрелые гепатоциты не была необходимой для уменьшения фиброза и воспаления печени. В другой экспериментальной модели хронического заболевания печени, вызванного четыреххлористым углеродом, ADHLSC также проявляли антифиброзную активность (Najimi et al., 2017). Кроме того, этот эффект был подтвержден in vitro на звездчатых клетках печени, в результате чего ADHLSC и их CM ингибировали их активацию (Najimi et al., 2017). Помимо повреждения печени, HLSC также способны вызывать регенерацию тканей в различных моделях острого повреждения почек (AKI). Например, в модели мышей AKI, индуцированной внутримышечной инъекцией глицерина, HLSC (3,5 × 10 5 ) были способны вызывать функциональное и морфологическое восстановление повреждения почек.Функциональные параметры, такие как азот мочевины в крови (АМК) и уровни креатинина в плазме, были восстановлены до почти нормальных уровней, и после лечения HLSC наблюдалось уменьшение некроза почечных канальцев и увеличение пролиферации канальцевых клеток. Кроме того, аналогично летальной модели печеночной недостаточности, лечение HLSC-CM также способно индуцировать защиту почек и регенерацию при ОПП, что указывает на то, что паракринные факторы, продуцируемые HLSC, также проявляют прорегенеративные эффекты на почечную ткань (Herrera Sanchez et al. al., 2014). Островковые органоиды, полученные изHLSC, при имплантации под почечную капсулу значительно снижали гипергликемию до нормогликемии и восстанавливали диабетический профиль у мышей SCID с диабетом, индуцированным стрептозотоцином (Navarro-Tableros et al., 2019). Кроме того, у этих мышей обнаруживались уровни человеческого С-пептида, указывающие на то, что наблюдаемое обращение диабета могло быть связано с трансплантацией островковых органоидов. Кроме того, при сравнении генного профиля органоидов, полученных из HLSC, трансплантированных in vivo с in vitro , последний показал профиль незрелой экспрессии гена по сравнению с первым, который претерпел дальнейшую дифференцировку β-клеток и стал способен обращать вспять гипергликемию у диабетиков. Мыши SCID. ЭМ, полученные на основе HLSC: характеристикаСреди различных паракринных факторов, выделяемых стволовыми клетками, их мембранные везикулы выступают в качестве важного медиатора их биологической активности (Ratajczak et al., 2006). Возможное применение внеклеточных везикул (EV), полученных из стволовых клеток, в регенеративной медицине исследовалось в последние годы как новаторский подход. EV описываются как гетерогенная популяция ограниченных мембранами частиц, выделяемых всеми типами клеток и присутствующих в различных биологических жидкостях (Bruno et al., 2019а). Было показано, что электромобили обладают функцией связи между ячейками, которая может изменять поведение целевых ячеек. Этот эффект актуален как в физиологических, так и в патологических состояниях и опосредуется различными механизмами, такими как прямая передача сигналов через взаимодействие рецепторов или перенос их груза, который включает: несколько видов РНК (мРНК, миРНК, длинные некодирующие РНК, тРНК , рРНК, кольцевые РНК и пиРНК), белки и биоактивные липиды (Derkus et al., 2017). ЭВ, полученные из стволовых клеток, также могут вызывать эпигенетические изменения в поврежденных реципиентных клетках с активацией регенеративных программ (Camussi et al., 2010). В течение последних нескольких лет было приложено много усилий для характеристики содержания HLSC-EV, чтобы выяснить роль различных компонентов, ответственных за наблюдаемые эффекты in vitro и in vivo . HLSC-EV демонстрируют типичную форму и размер EV, а также экспрессию типичных экзосомальных маркеров, таких как CD9, CD81 и CD63. Более того, на HLSC-EV наблюдались те же поверхностные маркеры, что и у исходной клетки. В частности, они экспрессировали высокие уровни CD29, CD44, CD105 и CD49e, тогда как CD142, CD146, SSEA4 и MCPS экспрессировались на среднем / низком уровне.Гематопоэтические (CD3, CD4, CD8, CD19), эндотелиальные и эпителиальные маркеры не были обнаружены на HLSC-EV (Bruno et al., 2020). Omic анализ показал, что HLSC-EV содержат РНК-связывающие белки, такие как AGO2 и Alix (ответственные за доставку miRNA), Staufen1 и 2 (участвующие в транспорте и стабильности мРНК), Т-клеточный внутриклеточный антиген-1 (TIA), Связанный с TIA-1 (TIAR) белок, связывающий элементы с высоким содержанием AU, а также многофункциональные белки, экспрессируемые в ядрах и стрессовых гранулах. Однако, в отличие от стрессовых гранул, ЭВ не содержали человеческий рибосомный белок S29 (Collino et al., 2010; Iavello et al., 2016). Белки, участвующие в формировании эндосомного сортировочного комплекса, необходимого для транспорта (ESCRT), также были описаны в HLSC EV (Iavello et al., 2016), в частности Tsg101, CHMP4a, CHMP4b и CHMP4c, которые были обнаружены с помощью вестерн-блоттинга. Скрининг белкового массива продемонстрировал присутствие многих цитокинов и факторов транскрипции, участвующих в регуляции воспаления, путей p53 и PI3K, поддерживающих противовоспалительный эффект in vivo (Bruno et al., 2020). Помимо белков, различные виды РНК также могут доставляться с помощью электромобилей к клеткам-мишеням (Villarroya-Beltri et al., 2014). Анализ микроматрицы продемонстрировал, что HLSC-EV перемещаются по определенному подмножеству мРНК, участвующему в контроле транскрипции и метаболизма. В частности, некоторые обнаруженные транскрипты генов участвуют в пролиферации клеток, такие как MATK, MRE11A, CHECK2, MYh21, VASP и CDK2, что позволяет предположить, что HLSC-EV могут оказывать свой прорегенеративный эффект посредством переноса этих транскриптов (Herrera et al., 2010). Среди видов РНК, обогащенных EV, miRNA привлекают большой интерес из-за их роли в регуляции трансляции генов (Bartel, 2004; Quesenberry et al., 2015). Было показано, что HLSC-EV обогащены более чем сотней миРНК, общих с клеткой происхождения, которые, как было показано, потенциально регулируют клеточный цикл, процессы, связанные с программой пролиферации и гибели клеток. Среди этих микроРНК некоторые специфически перемещаются ЭВ, и их мишени вносят вклад в регуляцию транскрипционных и биосинтетических функций, таких как биосинтез макромолекул (Collino et al., 2010). Кроме того, HLSC-EVs переносят miRNA, которые могут эпигенетически модифицировать клетки-мишени, вызывая прорегенеративную и антифиброзную программу (Kholia et al., 2018; Grange et al., 2019). HLSC-EV:in vivo и ex vivo Про-регенеративные способности ЭВ, происходящие изHLSC, имитируют прорегенеративные эффекты исходных клеток (рис. 2). Например, HLSC-EV смогли ускорить морфологическое и функциональное восстановление печени в экспериментальной модели in vivo ALI, состоящей из частичной гепатэктомии (70% гепатэктомии у крыс) (Herrera et al., 2010). Этот эффект был связан с увеличением пролиферации гепатоцитов в сочетании со снижением апоптоза гепатоцитов, оба из которых были подтверждены in vitro. Интересно, что этот прорегенеративный эффект исчез после предварительной обработки EV РНКазами, что указывает на РНК-зависимый эффект через горизонтальный перенос РНК. Таким образом, эти данные предполагают, что HLSC-EV могут активировать пролиферативную программу в остаточных гепатоцитах после гепатэктомии путем горизонтального переноса РНК.Совсем недавно было сообщено, что HLSC-EV могут способствовать улучшению функции и морфологии печени в модели ХЗЛ на мышах с НАСГ. Введение HLSC-EV значительно улучшило функцию печени, а также уменьшило фиброз и воспаление на гистологическом уровне. Кроме того, большинство связанных с фиброзом генов, активируемых при НАСГ, возвращались обратно после лечения HLSC-EV. Примечательно, что эксперименты по биораспределению продемонстрировали, что HLSC-EV могут преимущественно накапливаться в фиброзной печени (Bruno et al., 2020). Рисунок 2. Терапевтические эффекты HLSC и HLSC-EV. При повреждении почек и печени HLSC и HLSC-EV действуют как модуляторы регенерации тканей, воспаления и фиброза, как in vitro , так и in vivo . Они также обладают способностью подавлять опухоль при различных типах рака (гепатома, лимфобластома, глиома, рак почек и груди). HLSC и их EV могут также восстанавливать надлежащую ферментативную активность при генетических заболеваниях печени (цитруллинемия типа I и синдром Криглера-Наджара типа I).Этот факт, вместе с демонстрацией того, что введение HLSC безопасно у младенцев с наследственной гипераммонемией, открывает путь для возможного использования HLSC и HLSC-EV в лечении генетического заболевания печени. Подобно своим клеточным аналогам, HLSC-EV также улучшали функцию почек и улучшали морфологические повреждения в различных моделях острых и хронических повреждений почек на мышах. Например, HLSC-EV были способны накапливать in vivo в поврежденных почечных канальцах мыши и стимулировать пролиферацию канальцевых клеток, вызывая ускоренное восстановление повреждений канальцев.Пролиферативные эффекты HLSC-EV были подтверждены также in vitro на эпителиальные клетки канальцев мышей (Herrera Sanchez et al., 2014). HLSC-EV были также протестированы на различных моделях хронической болезни почек (ХБП) на мышах. Неиммунокомпетентные мыши, получавшие многократные инъекции HLSC-EV, показали значительное снижение гистопатологических признаков ХЗП и улучшение функции почек. Прогрессирование почечного фиброза, развившегося при диабетической нефропатии (DN) и нефропатии аристолоховой кислоты (AAN), значительно подавлялось после лечения HLSC-EV.Уровни экспрессии профиброзных генов, таких как коллаген I, α-SMA и TGF-бета, значительно подавлялись у мышей, получавших HLSC-EV (Kholia et al., 2018; Grange et al., 2019). Анализ мышиного miRnome почек мышей AAN, получавших или не получавших HLSC-EV, позволил идентифицировать miRNA, которые были обратно коррелированы между двумя группами лечения. Биоинформатический анализ выявил более 7000 генов, которые регулируются miRNA, подавляемыми HLSC-EV, которые связаны примерно со 140 путями.Среди них сигнальный путь WNT и другие воспалительные цитокины и пути хемокинов, такие как TGF-бета, фактор роста тромбоцитов (PDGF) и пути FGF, были связаны с развитием фиброза (Kholia et al., 2018). Кроме того, HLSC-EV перемещались по определенному подмножеству miRNA, и биоинформатический анализ показал, что они могут действовать на профиброзные пути, такие как TGF-бета, фактор роста инсулина-1 (IGF-1), рецептор эпидермального фактора роста (EGF). и рецептор PDGF, что согласуется с их терапевтическим действием на ХБП (Grange et al., 2019). Некоторые из miRNA, обогащенных HLSC-EV, включают miRNA-29a, семейство let-7, miRNA-30a, miRNA-24 и miRNA-21, которые, как известно, напрямую нацелены на профибротические гены, такие как Collagen I (Schug et al. , 2013; Balakrishnan et al., 2014), Snail57 и лиганд FAS (Sayed et al., 2010). Следовательно, подавление профиброзных генов, модуляция miRNAs, которые регулируют фиброзные пути, и перемещение определенных подмножеств miRNA могут быть механизмами, посредством которых HLSC-EVs проявляют свои антифиброзные эффекты при CKD. Для выяснения антифиброзного механизма HLSC-EV была принята модель in vitro CKD, которая включала совместное культивирование мТЭК, поврежденных аристолоховой кислотой, с кортикальными фибробластами почек мыши (mkCF) (Kholia et al., 2018). Обработка HLSC-EV ингибировала активацию профиброзных генов, таких как коллаген I, α-SMA и TGF-бета, как это наблюдалось in vivo . Дальнейший анализ показал, что обработка HLSC-EV подавляла регуляцию пяти miRNA в поврежденных mkCF, которые также были связаны с CKD.В частности, было показано, что miR-377-3p активируется при диабетической нефропатии и усиливает продукцию фибронектина (Wang et al., 2008). Предварительное кондиционирование печени с помощью HLSC-EV может быть интересным вариантом для ограничения повреждения тканей из-за ишемического реперфузионного повреждения (IRI). Фактически, нынешний метод сохранения органов в статическом холодильном хранилище не может полностью защитить неоптимальную печень от IRI. Нормотермическая машинная перфузия (NMP) появляется как метод консервации, потенциально способный улучшить результаты трансплантации печени с использованием трансплантатов с расширенными критериями (Butler et al., 2002; Имбер и др., 2002; Brockmann et al., 2009). Физиологическая температура вместе с активным метаболизмом в печени при NMP позволила фармакологическому вмешательству улучшить качество печени перед трансплантацией (Goldaracena et al., 2017). Добавление HLSC-EV во время NMP способствовало снижению гистологического повреждения, апоптоза и молекулярной сверхэкспрессии как фактора, индуцируемого гипоксией 1-α, так и TGF-бета 1, что указывает на то, что лечение HLSC-EV во время NMP снижает повреждение печени (Rigo и другие., 2018). Совсем недавно было продемонстрировано, что HLSC-EV уменьшают повреждение печени на мышиной модели IRI, полученной путем селективного пережатия внутрипеченочных ножек в течение 90 минут с последующими 6 часами реперфузии. Внутривенное введение HLSC-EV ослабляет печеночный IRI за счет значительного уменьшения некроза, высвобождения трансаминаз и ЛДГ, а также экспрессии провоспалительных цитокинов TNF-α, хемокина (мотив CC) лиганда 2 (CCL-2) и хемокина. (Мотив CXC) лиганд 10 (CXCL-10) (Calleri et al., 2020). HLSC и HLSC-EV: противоопухолевая активностьПаракринные факторы, выделяемые эмбриональными стволовыми клетками (ЭСК), могут ингибировать рост опухоли (Postovit et al., 2008; Giuffrida et al., 2009). Точно так же было описано, что биопродукты, высвобождаемые HLSC, способны подавлять рост опухоли in vitro и in vivo (фигура 2). В условиях in vivo внутриопухолевое введение HLSC-CM ингибировало рост клеток гепатомы HepG2, имплантированных подкожно мышам SCID, а в условиях in vitro HLSC-CM не только подавляло рост, но и способствовало апоптозу. клеток HepG2 (Cavallari et al., 2013). HLSC высвобождают Lefty A, ингибитор передачи сигналов Nodal, который является одним из медиаторов противоопухолевого эффекта, проявляемого ESC (Topczewska et al., 2006). HLSC-CM, полученные из HLSC с молчанием Lefty A, неспособны ингибировать рост опухоли. Этот результат показал, что Lefty A, высвобождаемый HLSC, может объяснять, по крайней мере частично, опухолевую супрессивную активность HLSC-CM, как описано для ESC. Сообщалось также, чтоHLSC-EV проявляют противоопухолевую активность in vitro и in vivo .Внутриопухолевая инъекция очищенных HLSC-EV ингибировала рост клеток HepG2 in vivo , и miRNA, перемещаемые HLSC-EV, могли участвовать в их противоопухолевой активности. Среди них miR451, miR223 и miR31, как было показано, действуют как супрессоры опухолей при переносе в HepG2 и клетки первичной гепатокарциномы с помощью HLSC-EV (Fonsato et al., 2012). Участие этих микроРНК в прогрессировании опухоли широко задокументировано при различных типах неопластических патологий (Nan et al., 2018; Bai and Wu, 2019; Dou et al., 2019; Джеффрис и др., 2019; Мамури и др., 2019). Противоопухолевый эффект HLSC-EV неспецифичен для клеток гепатомы, поскольку этот феномен также был описан на опухолевых клетках, происходящих от других видов рака, таких как лимфобластома и глиома (Fonsato et al., 2012). Интересно, что способность HLSC-EV подавлять опухоль была продемонстрирована на раковых стволовых клетках (CSC), которые, как известно, поддерживают инициирование, поддержание и рецидив опухолей. Кроме того, лечение HLSC-EV может вызывать апоптоз как в почечных, так и в молочных железах (Fonsato et al., 2018). Механизм, лежащий в основе противоопухолевой активности, оказываемой на CSC HLSC-EV, отдельно или в комбинации с несколькими ингибиторами тирозинкиназ (TKI), можно приписать модуляции путей PI3K и Erk. Участие пути PI3k / Akt / mTOR в ингибировании роста рака хорошо задокументировано (Lv et al., 2018; Nan et al., 2018; Slattery et al., 2018). В частности, ингибирование путей Akt и mTOR и PTEN с последующим ингибированием пролиферации опухолевых клеток и индукции апоптоза было результатом синергизма HLSC-EV с TKI.Этот синергизм был очевиден при использовании HLSC-EV и низких доз TKI и мог увеличивать ответ на TKI на CSC, таким образом обеспечивая доказательство концепции комбинированного использования этих продуктов при лечении карциномы почек. Противоопухолевый эффект HLSC-EV был также продемонстрирован in vivo на модели почечной карциномы, полученной путем подкожной инъекции почечных CSC. В этой модели внутривенное введение HLSC-EV влияло на развитие и рост опухоли и улучшало выживаемость легких без опухолей (Brossa et al., 2020). Противоопухолевая активность HLSC-EV наблюдалась in vitro, за счет уменьшения инвазии и организации CSC в сферы, характеристики, связанной со стеблем, а также in vivo за счет ингибирования роста опухоли, а также ангиогенеза опухоли. Было показано, что перенос miR-145 и индукция транскрипции miR-200b и miR-200c играют ключевую роль в нарушении функций почечных CSC (Brossa et al., 2020). HLSC-EV также продемонстрировали антиангиогенный потенциал за счет повреждения эндотелиальных клеток опухоли с образованием капилляроподобных структур in vitro и сосудов опухоли in vivo. Кроме того, было обнаружено, что антиангиогенный эффект HLSC-EV опосредован переносом специфических антиангиогенных miRNA (Lopatina et al., 2019). Все эти недавние открытия предполагают возможное использование HLSC-EV в качестве возможной альтернативы в лечении рака для повышения эффективности существующих методов лечения. HLSC и HLSC-EV: инструменты для лечения генетических заболеванийВведение HLSC может быть очень многообещающим подходом к коррекции функции печени при моногенных заболеваниях печени (рис. 2).Фактически, эффективность HLSC была протестирована на мышиной модели моногенного заболевания синдрома Криглера-Наджара I типа, вызванного дефицитом уридин-дифосфат-глюкуронозилтрансферазы (UGT1A1), фермента, ответственного за конъюгацию билирубина в печени. После внутрипаренхимальной инъекции HLSC показали региональное и гетерогенное приживление в инъецированной доле. Кроме того, экспрессия UGT1A1 в печени мышей, которым инъецировали HLSC, увеличивалась, демонстрируя, что HLSC способны частично корректировать дефицит активности этого фермента (Famulari et al., 2020). Трансплантация печени использовалась для лечения врожденных нарушений метаболизма с 95% -ным успехом детей, достигших долгосрочной выживаемости. Однако трансплантация печени новорожденным не может проводиться в обычном порядке, особенно из-за высокой периоперационной смертности в этом возрасте. Несколько исследований указали на возможное использование трансплантации клеток печени в качестве промежуточной терапии для коррекции унаследованного дефицита ферментов с переходной метаболической эффективностью (Lee et al., 2018). Однако несколько технических ограничений, а также доступность клеток печени привели к повышенному интересу к потенциальному использованию стволовых клеток, способных дифференцироваться в печени.Потенциальная дифференцировка HLSC в зрелые гепатоциты является кандидатом на эти клетки для лечения наследственной недостаточности ферментов. В частности, возможность использования HLSC в качестве альтернативной клеточной терапии генетических / метаболических заболеваний была недавно продемонстрирована в клиническом исследовании фазы I у младенцев (Spada et al., 2020). HLSC, полученные Европейским медицинским агентством (EMA) в 2012 году, признаны орфанными препаратами для лечения редких заболеваний (дефицит карбамоилфосфат-синтазы-1 EU / 3/12/971; дефицит орнитин-транскарбамилазы EU / 3/11/904) .Регулирующее агентство AIFA (Agenzia Italiana del Farmaco) санкционировало клиническое исследование I фазы с участием человека (HLSC 01–11, EudraCT-№ 2012–002120-33) в качестве открытого проспективного неконтролируемого моноцентрического исследования. для лечения группы редких генетических нарушений у педиатрических пациентов с неонатальной наследственной гипераммониемией из-за нарушений метаболизма, известных как нарушения цикла мочевины (UCD). Исследование проводилось в Центре трансплантации печени Университетской больницы города здравоохранения и науки (Azienda Ospedaliero-Universitaria Città della Salute e della Scienza di Torino) в Турине, Италия.Это клиническое испытание, начавшееся в январе 2014 г. и завершившееся в декабре 2016 г., показало, что чрескожное внутрипеченочное введение HLSC безопасно и хорошо переносится новорожденными с наследственной гипераммониемией. В фазу 1 клинического исследования были включены 3 новорожденных без введения каких-либо иммунодепрессантов, чтобы определить безопасность клеток in vivo и оценить печеночные и внепеченочные осложнения после интрапаренхимальной инъекции HLSC в печень. Новорожденные получали размороженные HLSC, полученные из замороженных пакетов.Размороженные клетки промывали, чтобы снизить концентрацию диметилсульфоксида, и дозы корректировали в зависимости от массы тела новорожденного. Во время и после введения HLSC пациенты постоянно контролировались на предмет температуры, частоты сердечных сокращений и дыхания, артериального давления и сатурации кислорода, а паренхима печени контролировалась с помощью эхографии. В конце периода наблюдения ни у одного из пациентов не было признаков инфекций, декомпенсации гипераммониемии, внутрипеченочных или внепеченочных осложнений или других нежелательных явлений.Более того, несмотря на увеличение (~ 30%) потребления белка, все леченные пациенты были метаболически стабильными. После эксплантации в нативной печени двух пациентов, перенесших трансплантацию (через 19 и 11 месяцев соответственно), гистологических изменений не было. Эти данные подтвердили основной результат исследования — безопасность HLSC (рис. 2). ADHLSC также были одобрены для клинических испытаний фазы I / II при метаболических нарушениях печени у детей (F. Smets et al., 2019). Результаты этого исследования показали переносимость введения стволовых клеток через воротную вену. Побочные эффекты, наблюдаемые в этом исследовании, соответствовали ожиданиям в отношении размещения катетера, инфузии клеток, сопутствующих лекарств, возраста и основных заболеваний (J. Häberle et al., 2012). В таблице 2 перечислены одобренные клинические испытания стволовых клеток печени при заболеваниях печени. Таблица 2. Резюме клинических испытаний стволовых клеток печени при заболеваниях печени. HLSC-EV были исследованы как возможный терапевтический подход к коррекции генетических заболеваний печени (рис. 2). Поскольку цикл мочевины происходит в основном в печени, а HLSC имеют печеночное происхождение, возможное применение HLSC-EV для коррекции UCD было специально изучено при цитруллинемии I типа, вызванной дефицитом аргиносукцинатсинтазы-1 (ASS-1). ), один из ферментов, участвующих в цикле мочевины. Было продемонстрировано, что HLSC-EV несут и переносят версию ASS-1 дикого типа в HLSC-1 с мутацией ASS-1 in vitro , тем самым восстанавливая ферментативную активность и продукцию мочевины в HLSC, полученном от пациента с наследственной недостаточностью аргиносукцинатсинтаза-1.ASS-1-мутированные HLSC были получены из небольшой биопсии выброшенной печени от трансплантированного пациента с цитруллинемией типа I. Мутированные HLSC были охарактеризованы цитофлуориметрическим анализом для подтверждения типичных маркеров HLSC. Секвенирование мутировавших HLSC с помощью SNaPshot показало, что ASS-1 несет две мутации кодона с заменой оснований C и G на T и A (g.55277 C> T и g.59839 G> A), что влияет на функциональный аспект фермента. . Кроме того, обмен белка ASS-1 дикого типа был способен восстанавливать ферментативную активность ASS-1 до базальных уровней в гепатоцитах, полученных из дифференцированных HLSC с мутацией ASS-1, обработанных очищенными EV из HLSC дикого типа (Herrera Sanchez и другие., 2017). Для дальнейшего изучения вклада HLSC-EV, обогащенного мРНК ASS-1, HLSC временно трансфицировали ASS-1-shRNA. EV, выделенные и очищенные из трансфицированных клеток, анализировали с помощью ферментативного анализа in vitro ASS-1 для подтверждения отсутствия белка ASS-1 внутри EV. В отличие от нормальных HLSC-EV, EV из HLSC с молчанием ASS-1 были неспособны восстанавливать продукцию мочевины в гепатоцитах, дифференцированных от мутантных ASS-1-HLSC, что позволяет предположить, что механизм восстановления может зависеть от переноса не только белка, но и интактной функциональной мРНК ASS-1 (Herrera Sanchez et al., 2017). Прямая доставка чистой мРНК также оказалась эффективной для лечения дефицита цикла мочевины. Например, группа, изучающая дефицит орнитин-транскарбамилазы (OTC), успешно нормализовала уровень аммиака в крови и улучшила выживаемость мышей с дефицитом OTC после прямого введения мРНК OTC человека (Prieve et al., 2018). Хотя такая прямая доставка мРНК имеет некоторые преимущества (Soria et al., 2019; Trepotec et al., 2019), одним из основных ограничений является нестабильность и относительно короткий период полужизни мРНК in vivo (Soria et al., 2019; Trepotec et al., 2019). Это ограничение не применимо к электромобилям, поскольку они являются мембраносвязанными частицами, и обогащенный в них груз, включая мРНК и белки, не только очень хорошо защищен от разложения, но также проявляет пролонгированную биологическую активность in vivo , поэтому они являются подходящими кандидатами для терапии генетических нарушений (Bruno et al., 2019a; Meng et al., 2020). ЗаключениеКлеточная терапия — это альтернативная форма лечения заболеваний печени, которая включает амплификацию in vitro с последующей трансплантацией здоровых стволовых клеток / клеток-предшественников пациентам, в идеале с помощью минимально инвазивной процедуры (Wei et al., 2020). В настоящее время проведены или продолжаются многие клинические испытания методов лечения заболеваний печени на основе стволовых клеток, включая МСК, гемопоэтические стволовые клетки и другие клетки, полученные из костного мозга (Wei et al., 2020). Тем не менее, для достижения этой цели необходимо принять во внимание несколько вопросов: во-первых, важно, чтобы клетки оставались генетически стабильными и неканцерогенными по мере их пролиферации; во-вторых, требуется достаточное количество здоровых клеток и, в-третьих, клетки должны сохранять свои свойства в условиях хранения. Другие источники стволовых клеток также обладают терапевтическими свойствами, но также обладают негативными аспектами, препятствующими их потенциальному использованию в терапии. Например, эмбриональные стволовые клетки обладают способностью к устойчивой пролиферации, а также способностью дифференцироваться в функционирующие печеночные клетки-предшественники: однако этические вопросы, связанные с их источником происхождения, вместе с их туморогенностью, остаются препятствием (Rao, 2007). В последнее время стало известно о дифференцировке индуцибельных плюрипотентных стволовых клеток человека в гепатоцитоподобные клетки, хотя получение полнофункциональных гепатоцитов с помощью этого метода оказалось трудным, поскольку весь процесс дифференцировки включает несколько этапов, которые влияют на формирование гепатоцитов в организме. отрицательный путь и требует дальнейшей доработки (Cai et al., 2007). Эффективность МСК при остром и хроническом повреждении печени была продемонстрирована на многих экспериментальных моделях на животных. Однако были выявлены некоторые потенциальные риски и побочные эффекты при применении МСК для лечения заболеваний печени. Напр., МСК обладают потенциалом дифференцироваться в звездчатые клетки печени и миофибробласты, тем самым способствуя фиброзу печени (Yang et al., 2012). Кроме того, существует возможность злокачественной трансформации МСК после трансплантации (Wu and Chen, 2006). Мы рассмотрели свойства HLSC на основе исследований, проводимых в нашей лаборатории более десяти лет. Тем не менее, необходимы дальнейшие исследования, чтобы понять механизмы их действия. HLSC обладают разносторонней клеточной пластичностью, что отражается в их способности множественной дифференцировки in vitro , что делает их подходящим источником для клеточной терапии. Кроме того, эксперименты по биораспределению на различных моделях in vivo показали способность HLSC достигать поврежденной печени.Попав в орган-мишень, HLSC смогли прижиться, как показано при острых и хронических повреждениях печени, при этом они были обнаружены как клетки человеческого происхождения через 21 день после их инъекции (Herrera et al., 2006, 2013; Bruno et al., 2019b). Более того, также было обнаружено, что они дифференцировались в гепатоциты, экспрессирующие CK8 и CK18, даже если недифференцированная популяция человеческих клеток сохранялась в мышиной модели острого повреждения печени (Herrera et al., 2013). Кроме того, на модели хронического повреждения печени НАСГ мы продемонстрировали присутствие клеток человека, которые не экспрессировали маркеры дифференцировки гепатоцитов (Bruno et al., 2019б). Эти данные показали, что положительные эффекты, наблюдаемые in vivo , не зависели от дифференцировки HLSC, что позволяет предположить, что биопродукт HLSC может опосредовать положительные эффекты клеток. Эксперименты, в которых вводили кондиционированную среду HLSC, подтвердили, что паракринные факторы участвуют в прорегенеративных и противоопухолевых свойствах клеток (Cavallari et al., 2013; Herrera et al., 2013). Среди паракринных эффекторов, присутствующих в кондиционированной среде, ЭВ были тщательно исследованы.Мы продемонстрировали на множестве острых и хронических моделей повреждений печени и почек, что HLSC-EV проявляют прорегенеративные и тканезащитные эффекты (Herrera et al., 2010; Herrera Sanchez et al., 2014; Kholia et al. , 2018; Grange et al., 2019; Bruno et al., 2020). Эти эксперименты подтверждают идею о том, что бесклеточная терапия может быть альтернативным подходом к лечению различных острых и хронических заболеваний. По сравнению с клеточной терапией лечение электромобилями имеет ряд преимуществ.EV демонстрируют превосходный профиль эффективности, поскольку они преодолевают биологические барьеры и действуют как переносчики различных молекул (РНК, белков и липидов). Существенным преимуществом электромобилей по сравнению с клеточной терапией является возможность избежать потенциальной онкогенности. In vitro и in vivo Эксперименты показали, что HLSC-EV могут не только подавлять рост опухоли, но и синергетически повышать эффективность противоопухолевых препаратов (Fonsato et al., 2012, 2018; Brossa et al., 2020).Несмотря на усилия по изучению ЭМ и их взаимодействия с микросредой с помощью нескольких доклинических моделей, необходимо рассмотреть несколько аспектов, прежде чем применять их в клинических условиях. К ним относятся, среди прочего, высококлассное производство в формате GMP, характеристика, фармакокинетика, фармакодинамика, токсичность и иммунная реакция хозяина. Более того, ЭВ из различных источников стволовых клеток (эмбриональных, взрослых, костного мозга, пуповины) были протестированы на различных моделях in vitro и in vivo .Прямое сравнение HLSC-EV с EV, полученными из других источников стволовых клеток в моделях заболеваний печени, все еще отсутствует. Среди различных источников МСК пуповины человека могут быть одним из лучших клеточных источников, поскольку они доступны и не вызывают возражений этического характера (Ifrah et al., 2020). Несмотря на многочисленные исследования, описывающие возможную роль стволовых клеток печени и ЭВ в регенерации печени, их вклад в гемостаз печени все еще обсуждается (Groeneveld et al., 2019; Михалопулос и Бхушан, 2021). Недавно Groeneveld et al. идентифицировали новый механизм, согласно которому зависящее от коагуляции отложение фибрина (огена) в печени приводит к накоплению тромбоцитов и, следовательно, активирует регенерацию печени после частичной гепатэктомии. Насколько нам известно, вклад стволовых клеток и их ЭВ в этот новый механизм не выяснен, поэтому необходимы дальнейшие исследования. В заключение, было показано, что HLSC представляют собой особую клеточную сущность, которая взаимодействует с другими клетками локально и системно, обеспечивая клеточные ответы с несколькими терапевтическими свойствами.Еще многое предстоит сделать с точки зрения научных знаний и клинической пользы, поскольку комплексная биология и терапевтический потенциал HLSC постоянно развиваются. Авторские взносыSB, MH, GCh, VF, VN-T, CP и MT провели исследование соответствующей литературы, разработали и составили рукопись. GCa отредактировал и отредактировал рукопись. Все авторы внесли свой вклад в статью и одобрили представленную версию. ФинансированиеРабота поддержана грантом Unicyte AG (Обердорф, Северо-Запад, Швейцария). Конфликт интересовGCa входил в состав научно-консультативного совета Unicyte AG. SB, MH, VF, VN-T и GCa были названы изобретателями в соответствующих патентах. Остальные авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов. СокращенияAAN, нефропатия аристолохиевой кислоты; ADHLSC, стволовые клетки печени человека взрослого происхождения; ОПП — острое повреждение почек; ALI — острое повреждение печени; АЛТ, аланинаминотрансфераза; AST, аспартатаминотрансфераза; AIFA, Agenzia Italiana del Farmaco; ASS-1, аргининосукцинатсинтаза-1; АМК — азот мочевины крови; CYP450, цитохром P450; СК, цитокератин; CCL-2, хемокиновый (мотив C-C) лиганд 2; CXCL-10, хемокиновый (мотив C-X-C) лиганд 10; РСК — раковые стволовые клетки; ХБП — хроническая болезнь почек; ДН — диабетическая нефропатия; ХЗБ — хроническое заболевание печени; ДК, дендритные клетки; ЭСК, эмбриональные стволовые клетки; EVs, внеклеточные везикулы; EMA, Европейское медицинское агентство; EGF, фактор роста эпидермиса; ESCRT, эндосомальный сортировочный комплекс, необходимый для транспортировки; FGF, фактор роста фибробластов; FLF, фульминантная печеночная недостаточность; GMP, надлежащая производственная практика; HGF, фактор роста гепатоцитов; HLSC, стволовые клетки печени человека; HLSC-ILS, HLSC-островковые структуры; hFLMPCs, мультипотентные клетки-предшественники фетальной печени человека; HLA, лейкоцитарный антиген человека; HLSC-CM, кондиционированная среда HLSC; ИЛ, Интерлейкин; IGF-1, фактор роста инсулина-1; IRI — ишемия-реперфузионное повреждение; L-MSC — МСК-подобная популяция печени; LHMSC, МСК печени человека; ЛДГ, лактатдегидрогеназа; MCB, основной банк клеток; МСК, мезенхимальные стромальные клетки; NKs, естественные клетки-киллеры; НАСГ, неалкогольный стеатогепатит; НМП, нормотермическая машинная перфузия; OTC, орнитин-транскарбамилаза; PDGF, фактор роста тромбоцитов; RCCS, ротационная система культивирования клеток; RLAS — бесклеточные каркасы печени крысы; TGF, трансформирующий фактор роста; mkCF, кортикальный фибробласт почек мыши; TIA-1, внутренний антиген 1 Т-клеток; TIAR, связанные с TIA-1; UGT1A1, уридин-дифосфат-глюкуронозилтрансфераза; UCD, нарушения цикла мочевины; VEGF, фактор роста эндотелия сосудов; α-SMA, альфа-актин гладких мышц. Список литературыAdam, R., Karam, V., Cailliez, V., O Grady, J. G., Mirza, D., Cherqui, D., et al. (2018). Годовой отчет Европейского реестра трансплантатов печени (ELTR) за 2018 год — 50-летняя эволюция трансплантации печени. Транспл. Int. 31, 1293–1317. DOI: 10.1111 / tri.13358 PubMed Аннотация | CrossRef Полный текст | Google Scholar Балакришнан И., Янг X., Браун Дж., Рамакришнан А., Торок-Сторб Б., Кабос П. и др. (2014). Полногеномный анализ взаимодействий miRNA-mRNA в стромальных клетках костного мозга. Стволовые клетки 32, 662–673. DOI: 10.1002 / стержень.1531 PubMed Аннотация | CrossRef Полный текст | Google Scholar Бартель, Д. П. (2004). МикроРНК: геномика, биогенез, механизм и функции. Cell 116, 281–297. DOI: 10.1016 / S0092-8674 (04) 00045-5 CrossRef Полный текст | Google Scholar Brockmann, J., Reddy, S., Coussios, C., Pigott, D., Guirriero, D., Hughes, D., et al. (2009). Нормотермическая перфузия: новая парадигма сохранения органов. Ann. Surg. 250, 1–6. DOI: 10.1097 / SLA.0b013e3181a63c10 PubMed Аннотация | CrossRef Полный текст | Google Scholar Бросса, А., Фонсато, В., Грейндж, К., Тритта, С., Таппаро, М., Кальветти, Р. и др. (2020). Внеклеточные везикулы из стволовых клеток печени человека подавляют рост опухоли, происходящей из стволовых клеток рака почки, in vitro и in vivo. Внутр. J. Cancer 147, 1694–1706. DOI: 10.1002 / ijc.32925 PubMed Аннотация | CrossRef Полный текст | Google Scholar Бруно, С., Чиаботто, Дж., Фаваро, Э., Дерегибус, М. К., и Камусси, Дж. (2019a). Роль внеклеточных везикул в биологии стволовых клеток. г. J. Physiol. Cell Physiol. 317, C303 – C313. DOI: 10.1152 / ajpcell.00129.2019 PubMed Аннотация | CrossRef Полный текст | Google Scholar Бруно, С., Гранж, К., Таппаро, М., Паскуино, К., Романьоли, Р., Даметто, Э. и др. (2016). Стволовые клетки печени человека подавляют пролиферацию Т-клеток, активность NK и дифференцировку дендритных клеток. Stem Cells Int. 2016: 8468549. DOI: 10.1155 / 2016/8468549 PubMed Аннотация | CrossRef Полный текст | Google Scholar Бруно С., Эррера Санчес М. Б., Паскуино К., Таппаро М., Седрино М., Тетта К. и др. (2019b). Стволовые клетки, полученные из печени человека, улучшают фиброз и воспаление, связанные с неалкогольным стеатогепатитом. Stem Cells Int. 2019: 6351091. DOI: 10.1155 / 2019/6351091 PubMed Аннотация | CrossRef Полный текст | Google Scholar Бруно, С., Паскуино, К., Эррера Санчес, М. Б., Таппаро, М., Фиглиолини, Ф., Грандж, К. и др. (2020). Внеклеточные везикулы, происходящие из HLSC, ослабляют фиброз и воспаление печени на мышиной модели неалкогольного стеатогепатита. Мол. Ther. 28, 479–489. DOI: 10.1016 / j.ymthe.2019.10.016 PubMed Аннотация | CrossRef Полный текст | Google Scholar Батлер, А. Дж., Рис, М. А., Уайт, Д. Г. Д., Кейси, Н. Д., Александер, Г., Уайт, Д. Дж. Г. и др. (2002). Успешная экстракорпоральная перфузия свиной печени в течение 72 часов. Трансплантация 73, 1212–1218. DOI: 10.1097 / 00007890-200204270-00005 PubMed Аннотация | CrossRef Полный текст | Google Scholar Цай, Дж., Чжао, Ю., Лю, Ю., Е, Ф., Сун, З., Цинь, Х. и др. (2007). Направленная дифференцировка эмбриональных стволовых клеток человека в функциональные клетки печени. Гепатология 45, 1229–1239. DOI: 10.1002 / hep.21582 PubMed Аннотация | CrossRef Полный текст | Google Scholar Calleri, A., Roggio, D., Navarro-Tableros, V., Де Стефано, Н., Паскуино, К., Дэвид, Э. и др. (2020). Защитные эффекты внеклеточных везикул, полученных из стволовых клеток печени человека, на мышиной модели ишемического реперфузионного повреждения печени. Stem Cell Rev. Rep. 17, 459–470. DOI: 10.1007 / s12015-020-10078-7 PubMed Аннотация | CrossRef Полный текст | Google Scholar Кампаньоли К., Робертс И. А., Кумар С., Беннетт П. Р., Беллантуоно И. и Фиск Н. М. (2001). Идентификация мезенхимальных стволовых / предшественников в крови плода, печени и костном мозге человека в первом триместре. Кровь 98, 2396–2402. DOI: 10.1182 / blood.v98.8.2396 PubMed Аннотация | CrossRef Полный текст | Google Scholar Камусси, Г., Дерегибус, М. К., Бруно, С., Канталуппи, В., и Бьянконе, Л. (2010). Экзосомы / микровезикулы как механизм межклеточной коммуникации. Kidney Int. 78, 838–848. DOI: 10.1038 / ki.2010.278 PubMed Аннотация | CrossRef Полный текст | Google Scholar Каваллари, К., Фонсато, В., Эррера, М. Б., Бруно, С., Тетта, К., Камусси, Г. (2013). Роль Левши в противоопухолевой активности стволовых клеток печени взрослого человека. Онкоген 32, 819–826. DOI: 10.1038 / onc.2012.114 PubMed Аннотация | CrossRef Полный текст | Google Scholar Collino, F., Deregibus, M.C., Bruno, S., Sterpone, L., Aghemo, G., Viltono, L., et al. (2010). Микровезикулы, полученные из костного мозга взрослого человека, и тканеспецифические мезенхимальные стволовые клетки перемещают выбранный образец miRNA. PLoS One 5: e11803.DOI: 10.1371 / journal.pone.0011803 PubMed Аннотация | CrossRef Полный текст | Google Scholar Дэн, Ю. Ю., Риле, К. Дж., Лазаро, К., Теох, Н., Хак, Дж., Кэмпбелл, Дж. С. и др. (2006). Выделение мультипотентных клеток-предшественников из печени плода человека, способных дифференцироваться в печеночные и мезенхимальные клоны. Proc. Natl. Акад. Sci. США 103, 9912–9917. DOI: 10.1073 / pnas.0603824103 PubMed Аннотация | CrossRef Полный текст | Google Scholar Деркус, Б., Эмрегул, К. К., Эмрегул, Э. (2017). Новый подход в исследовании стволовых клеток — экзосомы: их механизм действия через клеточные пути. Cell Biol. Int. 41, 466–475. DOI: 10.1002 / cbin.10742 PubMed Аннотация | CrossRef Полный текст | Google Scholar Дхаван А., Пуппи Дж., Хьюз Р. Д. и Митри Р. Р. (2010). Трансплантация гепатоцитов человека: текущий опыт и будущие задачи. Нац. Преподобный Гастроэнтерол. Гепатол. 7, 288–298. DOI: 10.1038 / nrgastro.2010,44 PubMed Аннотация | CrossRef Полный текст | Google Scholar Доу, Л., Хань, К., Сяо, М., и Львов, Ф. (2019). miR-223-5p подавляет рост опухоли и метастазирование при немелкоклеточном раке легкого, воздействуя на E2F8. Онкол. Res. 27, 261–268. DOI: 10.3727 / 096504018X15219188894056 PubMed Аннотация | CrossRef Полный текст | Google Scholar Famulari, E. S., Navarro-Tableros, V., Herrera Sanchez, M. B., Bortolussi, G., Gai, M., Conti, L., et al.(2020). Стволовые клетки печени человека экспрессируют UGT1A1 и улучшают фенотип мышей с ослабленным иммунитетом с синдромом Криглера-Наджара типа I. Sci. Реп. 10: 887. DOI: 10.1038 / s41598-020-57820-2 PubMed Аннотация | CrossRef Полный текст | Google Scholar Фарбер, Э. (1956). Сходство последовательности ранних гистологических изменений, индуцированных в печени крысы этионином, 2-ацетиламинофлуореном и 3’-метил-4-диметиламиноазобензолом. Cancer Res. 16, 142–148. Google Scholar Фонсато, В., Коллино, Ф., Эррера, М. Б., Каваллари, К., Дерегибус, М. К., Цистерна, Б., и др. (2012). Микровезикулы, полученные из стволовых клеток печени человека, подавляют рост гепатомы у мышей SCID, доставляя противоопухолевые микроРНК. Стволовые клетки 30, 1985–1998. DOI: 10.1002 / стержень.1161 PubMed Аннотация | CrossRef Полный текст | Google Scholar Фонсато В., Де Лена М., Тритта С., Бросса А., Кальветти Р., Тетта К. и др. (2018).Внеклеточные везикулы, полученные из стволовых клеток печени человека, повышают чувствительность раковых стволовых клеток к ингибиторам тирозинкиназы за счет комбинированной модуляции Akt / mTOR / PTEN. Oncotarget 9, 36151–36165. DOI: 10.18632 / oncotarget.26319 PubMed Аннотация | CrossRef Полный текст | Google Scholar Фонсато В., Эррера М. Б., Буттильери С., Гатти С., Камусси Г. и Тетта К. (2010). Использование ротационной биоискусственной печени в дифференцировке стволовых клеток печени человека. Tissue Eng.Часть C Методы 16, 123–132. DOI: 10.1089 / ten.TEC.2008.0634 PubMed Аннотация | CrossRef Полный текст | Google Scholar Гаудио, Э., Карпино, Г., Кардинале, В., Франчитто, А., Онори, П., и Альваро, Д. (2009). Новое понимание стволовых клеток печени. Dig. Liver Dis. 41, 455–462. DOI: 10.1016 / j.dld.2009.03.009 PubMed Аннотация | CrossRef Полный текст | Google Scholar Джуффрида, Д., Роджерс, И. М., Надь, А., Калоджеро, А. Э., Браун, Т. Дж.и Каспер Р.Ф. (2009). Эмбриональные стволовые клетки человека выделяют растворимые факторы, подавляющие рост раковых клеток. Cell Prolif. 42, 788–798. DOI: 10.1111 / j.1365-2184.2009.00640.x PubMed Аннотация | CrossRef Полный текст | Google Scholar Goldaracena, N., Spetzler, V. N., Echeverri, J., Kaths, J.M., Cherepanov, V., Persson, R., et al. (2017). Индуцирование устойчивости к вирусу гепатита С после трансплантации печени свиньи — доказательство концепции модификации трансплантата печени с использованием теплой перфузии ex vivo. г. J. Transplant. 17, 970–978. DOI: 10.1111 / ajt.14100 PubMed Аннотация | CrossRef Полный текст | Google Scholar Гомес, Ю., Наварро-Таблерос, В., Тетта, К., Камусси, Г., и Бриззи, М. Ф. (2020). Универсальная модель микрофлюидной системы перифузии для оценки профилей секреции с-пептида: сравнение островков поджелудочной железы человека и островковых структур, полученных из HLSC. Биомедицина 8:26. DOI: 10.3390 / biomedicines8020026 PubMed Аннотация | CrossRef Полный текст | Google Scholar Grange, C., Tritta, S., Tapparo, M., Cedrino, M., Tetta, C., Camussi, G., et al. (2019). Внеклеточные везикулы, происходящие из стволовых клеток, подавляют и обращают вспять прогрессирование фиброза на мышиной модели диабетической нефропатии. Sci. Реп. 9: 4468. DOI: 10.1038 / s41598-019-41100-9 PubMed Аннотация | CrossRef Полный текст | Google Scholar Groeneveld, D., Pereyra, D., Veldhuis, Z., Adelmeijer, J., Ottens, P., Kopec, A. K., et al. (2019). Отложение внутрипеченочного фибрина (огена) стимулирует регенерацию печени после частичной гепатэктомии у мышей и людей. Кровь 133, 1245–1256. DOI: 10.1182 / кровь-2018-08-869057 PubMed Аннотация | CrossRef Полный текст | Google Scholar Häberle, J., Boddaert, N., Burlina, A., Chakrapani, A., Dixon, M., Huemer, M., et al. (2012). Предлагаемые руководящие принципы диагностики и лечения нарушений цикла мочевины. Orphanet J. Rare Dis. 2012: 32. DOI: 10.1186 / 1750-1172-7-32 PubMed Аннотация | CrossRef Полный текст | Google Scholar Эррера, М. Б., Бруно, С., Buttiglieri, S., Tetta, C., Gatti, S., Deregibus, M. C., et al. (2006). Выделение и характеристика популяции стволовых клеток из печени взрослого человека. Стволовые клетки 24, 2840–2850. DOI: 10.1634 / стволовые клетки.2006-0114 PubMed Аннотация | CrossRef Полный текст | Google Scholar Эррера, М. Б., Фонсато, В., Бруно, С., Гранж, К., Гильбо, Н., Романьоли, Р. и др. (2013). Стволовые клетки печени человека улучшают повреждение печени на модели молниеносной печеночной недостаточности. Гепатология 57, 311–319.DOI: 10.1002 / hep.25986 PubMed Аннотация | CrossRef Полный текст | Google Scholar Эррера, М. Б., Фонсато, В., Гатти, С., Дерегибус, М. К., Сорди, А., Кантарелла, Д. и др. (2010). Микровезикулы, полученные из стволовых клеток печени человека, ускоряют регенерацию печени у гепатэктомированных крыс. J. Cell. Мол. Med. 14, 1605–1618. DOI: 10.1111 / j.1582-4934.2009.00860.x PubMed Аннотация | CrossRef Полный текст | Google Scholar Эррера Санчес, М. Б., Бруно, С., Grange, C., Tapparo, M., Cantaluppi, V., Tetta, C., et al. (2014). Стволовые клетки печени человека и производные внеклеточные везикулы улучшают выздоровление на мышиной модели острого повреждения почек. Stem Cell Res. Ther. 5: 124. DOI: 10.1186 / scrt514 PubMed Аннотация | CrossRef Полный текст | Google Scholar Эррера Санчес, М. Б., Превиди, С., Бруно, С., Фонсато, В., Дерегибус, М. К., Холия, С., и др. (2017). Внеклеточные везикулы стволовых клеток печени человека восстанавливают дефицит аргининосукцинатсинтазы. Stem Cell Res. Ther. 8: 176. DOI: 10.1186 / s13287-017-0628-9 PubMed Аннотация | CrossRef Полный текст | Google Scholar Herrero, A., Prigent, J., Lombard, C., Rosseels, V., Daujat-Chavanieu, M., Breckpot, K., et al. (2017). Стволовые клетки печени человека / клетки-предшественники, полученные от взрослых людей, инфузированные в течение 3 дней после операции, улучшают регенерацию печени на мышиной модели расширенной гепатэктомии. Пересадка клеток. 26, 351–364. DOI: 10.3727 / 096368916X692960 PubMed Аннотация | CrossRef Полный текст | Google Scholar Иавелло, А., Фрех, В. С. Л., Гай, К., Дерегибус, М. К., Кузенберри, П. Дж., И Камусси, Г. (2016). Роль Alix в упаковке miRNA во время биогенеза внеклеточных везикул. Внутр. J. Mol. Med. 37, 958–966. DOI: 10.3892 / ijmm.2016.2488 PubMed Аннотация | CrossRef Полный текст | Google Scholar Ифрах А., Усман А. и Зишан С. (2020). Лечебный потенциал стволовых клеток пуповины для регенерации печени. Curr. Stem Cell Res. Ther. 15, 219–232. DOI: 10.2174/1568026620666200220122536 PubMed Аннотация | CrossRef Полный текст | Google Scholar Имбер, К. Дж., Сент-Питер, С. Д., Лопес де Сенаррузабейтиа, И., Пиготт, Д., Джеймс, Т., Тейлор, Р. и др. (2002). Преимущества нормотермической перфузии перед холодным хранением в сохранении печени. Трансплантация 73, 701–709. DOI: 10.1097 / 00007890-200203150-00008 PubMed Аннотация | CrossRef Полный текст | Google Scholar In‘t Anker, P. S., Noort, W. A., Scherjon, S.A., Kleijburg-van der Keur, C., Kruisselbrink, A. B., van Bezooijen, R. L., et al. (2003). Мезенхимальные стволовые клетки в костном мозге, печени, легких и селезенке человека во втором триместре обладают сходным иммунофенотипом, но обладают гетерогенным потенциалом многолинейной дифференцировки. Haematologica 88, 845–852. Google Scholar Дженнингс, Р. Э., Берри, А. А., Стратт, Дж. П., Джеррард, Д. Т., и Хэнли, Н. А. (2015). Развитие поджелудочной железы человека. Девелопмент 142, 3126–3137.DOI: 10.1242 / dev.120063 PubMed Аннотация | CrossRef Полный текст | Google Scholar Келлнер, Дж., Шиваджоти, С., и Макнейс, И. (2015). Дифференциальные свойства стромальных клеток человека из костного мозга, жировой ткани, печени и сердечной ткани. Цитотерапия 7, 1514–1523. DOI: 10.1016 / j.jcyt.2015.07.009 PubMed Аннотация | CrossRef Полный текст | Google Scholar Холия, С., Эррера Санчес, М. Б., Седрино, М., Пападимитриу, Э., Таппаро, М., Дерегибус, М.C., et al. (2018). Внеклеточные везикулы, полученные из стволовых клеток печени человека, предотвращают индуцированный аристолоховой кислотой фиброз почек. Фронт. Иммунол. 9: 1639. DOI: 10.3389 / fimmu.2018.01639 PubMed Аннотация | CrossRef Полный текст | Google Scholar Хуу, Д. Н., Ньяби, О., Меркс, К., Сокал, Э., и Надзими, М. (2013). Мезенхимальные стволовые клетки / клетки-предшественники печени взрослого человека участвуют в регенерации печени мыши после гепатэктомии. Пересадка клеток. 22, 1369–1380.DOI: 10.3727 / 096368912X659853 PubMed Аннотация | CrossRef Полный текст | Google Scholar Хуу Д. Н., Шеерс И., Энерт С., Джазули Н., Ньяби О., Бук-Кальдерон П. и др. (2011). Дифференцированные in vitro клетки-предшественники печени взрослого человека демонстрируют зрелые метаболические функции печени: потенциальный инструмент для фармакотоксикологического тестирования in vitro. Пересадка клеток. 20, 287–302. DOI: 10.3727 / 096368910X516655 PubMed Аннотация | CrossRef Полный текст | Google Scholar Ли, К.А., Синха, С., Фицпатрик, Э., и Дхаван, А. (2018). Трансплантация гепатоцитов и достижения в области альтернативных источников клеток для регенеративной медицины на основе печени. J. Mol. 96, 469–481. Google Scholar Ли, Дж .-Х., Пак, Х.-Дж., Ким, Й.-А., Ли, Д.-Х., Но, Дж .-К., Квон, К. Х. Д. и др. (2012). Фенотипические характеристики стволовых клеток печени, полученных из донорской печени человека. Пересадка. Proc. 44, 1110–1112. DOI: 10.1016 / j.transproceed.2012.02.020 PubMed Аннотация | CrossRef Полный текст | Google Scholar Ломбард, К. А., Сана, Г., Лемо, Дж., Наджар, М., Равау, Дж., Андре, Ф. и др. (2019). Гепатоциты человека и дифференцированные взрослые стволовые клетки / клетки-предшественники печени человека проявляют in vitro иммуносупрессивные свойства, опосредованные, по крайней мере частично, неклассической молекулой HLA класса I HLA-G. J. Immunol. Res. 12, 8250584. doi: 10.1155 / 2019/8250584 PubMed Аннотация | CrossRef Полный текст | Google Scholar Лопатина, Т., Grange, C., Fonsato, V., Tapparo, M., Brossa, A., Fallo, S., et al. (2019). Внеклеточные везикулы стволовых клеток печени человека подавляют ангиогенез опухоли. Внутр. J. Cancer 144, 322–333. DOI: 10.1002 / ijc.31796 PubMed Аннотация | CrossRef Полный текст | Google Scholar Lv, X., Li, C.-Y., Han, P., and Xu, X.-Y. (2018). MicroRNA-520a-3p подавляет рост клеток и метастазирование немелкоклеточного рака легкого через сигнальный путь PI3K / AKT / mTOR. евро. Rev. Med.Pharmacol. Sci. 22, 2321–2327. DOI: 10.26355 / eurrev_201804_14822 CrossRef Полный текст | Google Scholar Мамури, А., Вахаб, Р., Видер, Дж., Гопалан, В., и Лам, А. К.-Й. (2019). Эффекты подавления опухоли и регуляция раковых стволовых клеток с помощью фактора ингибирования миграции макрофагов нацелены на miR-451 при раке толстой кишки. Gene 697, 165–174. DOI: 10.1016 / j.gene.2019.02.046 PubMed Аннотация | CrossRef Полный текст | Google Scholar Мэн, В., Хэ, К., Хао, Ю., Ван, Л., Ли, Л. и Чжу, Г. (2020). Перспективы и проблемы системы доставки лекарств на основе внеклеточных везикул: с учетом клеточного источника. Достав. Лекарств. 27, 585–598. DOI: 10.1080 / 10717544.2020.1748758 PubMed Аннотация | CrossRef Полный текст | Google Scholar Михалопулос, Г. К., и Бхушан, Б. (2021 г.). Регенерация печени: биологические и патологические механизмы и последствия. Нац. Преподобный Гастроэнтерол. Гепатол. 18, 40–55. DOI: 10.1038 / s41575-020-0342-4 PubMed Аннотация | CrossRef Полный текст | Google Scholar Мун, А. М., Сингал, А. Г., Таппер, Э. Б. (2020). Современная эпидемиология хронических заболеваний печени и цирроза. Clin. Гастроэнтерол. Гепатол. 18, 2650–2666. DOI: 10.1016 / j.cgh.2019.07.060 PubMed Аннотация | CrossRef Полный текст | Google Scholar Надзими, М., Берардис, С., Эль-Кехди, Х., Росселс, В., Эвраертс, Дж., Ломбард, К., и др. (2017). Мезенхимальные стволовые клетки / клетки-предшественники печени человека подавляют активацию звездчатых клеток печени: оценка in vitro и in vivo. Stem Cell Res. Ther. 8: 131. DOI: 10.1186 / s13287-017-0575-5 PubMed Аннотация | CrossRef Полный текст | Google Scholar Надзими М., Хуу Д. Н., Лизи П. А., Джазули Н., Абарка Дж., Семпу К. и др. (2007). Мезенхимоподобные клетки печени взрослого человека как потенциальный резервуар гепатоцитов-предшественников? Пересадка клеток. 6, 717–728. DOI: 10.3727 / 000000007783465154 PubMed Аннотация | CrossRef Полный текст | Google Scholar Нан, Ю., Guo, H., Guo, L., Wang, L., Ren, B., Yu, K., et al. (2018). MiRNA-451 подавляет пролиферацию и инвазию клеток глиомы через сигнальный путь mTOR / HIF-1α / VEGF, воздействуя на CAB39. Hum. Gene Ther. Clin. Dev. 29, 156–166. DOI: 10.1089 / humc.2018.133 PubMed Аннотация | CrossRef Полный текст | Google Scholar Navarro-Tableros, V., Gai, C., Gomez, Y., Giunti, S., Pasquino, C., Deregibus, M.C., et al. (2019). Островковидные структуры, полученные in vitro из стволовых клеток печени взрослого человека, обращают гипергликемию у мышей SCID с диабетом. Stem Cell Rev. Rep. 15, 93–111. DOI: 10.1007 / s12015-018-9845-6 PubMed Аннотация | CrossRef Полный текст | Google Scholar Наварро-Таблерос, В., Эррера Санчес, М. Б., Фиглиолини, Ф., Романьоли, Р., Тетта, К., и Камусси, Г. (2015). Рекеллюляризация каркасов печени крыс стволовыми клетками печени человека. Tissue Eng. Часть A 21, 1929–1939. DOI: 10.1089 / ten.TEA.2014.0573 PubMed Аннотация | CrossRef Полный текст | Google Scholar Пан, К., Фурашен, С. М., Кайя, Ф. С., Верстеген, М. М., Пескатори, М., Стаббс, А. П. и др. (2011). Мобилизация мезенхимальных стволовых клеток печени из трансплантатов печени человека. Транспл. Печени. 17, 596–609. DOI: 10.1002 / lt.22260 PubMed Аннотация | CrossRef Полный текст | Google Scholar Постовит Л.-М., Маргарян Н.В., Сефтор Э.А., Киршманн Д.А., Липавский А., Уитон В.В. и др. (2008). Микроокружение эмбриональных стволовых клеток человека подавляет онкогенный фенотип агрессивных раковых клеток. Proc. Natl. Акад. Sci. США 105, 4329–4334. DOI: 10.1073 / pnas.0800467105 PubMed Аннотация | CrossRef Полный текст | Google Scholar Приве, М. Г., Харви, П., Монахан, С. Д., Рой, Д., Ли, А. Г., Блевинс, Т. Л. и др. (2018). Таргетная терапия мРНК при дефиците орнитин-транскарбамилазы. Мол. Ther. 26, 801–813. DOI: 10.1016 / j.ymthe.2017.12.024 PubMed Аннотация | CrossRef Полный текст | Google Scholar Quesenberry, P.Дж., Алиотта, Дж., Дерегибус, М. К., и Камусси, Г. (2015). Роль внеклеточных везикул, несущих РНК, в дифференцировке и репрограммировании клеток. Stem Cell Res. Ther. 6, 153. DOI: 10.1186 / s13287-015-0150-x PubMed Аннотация | CrossRef Полный текст | Google Scholar Ратайчак, Дж., Миекус, К., Кусия, М., Чжан, Дж., Река, Р., Дворжак, П., и др. (2006). Микровезикулы, полученные из эмбриональных стволовых клеток, репрограммируют гематопоэтических предшественников: доказательства горизонтального переноса мРНК и доставки белка. Лейкемия 20, 847–856. DOI: 10.1038 / sj.leu2404132 CrossRef Полный текст | Google Scholar Rigo, F., De Stefano, N., Navarro-Tableros, V., David, E., Rizza, G., Catalano, G., et al. (2018). Внеклеточные везикулы из стволовых клеток печени человека уменьшают повреждение в модели перфузии печени крыс с нормотермической гипоксией ex vivo. Трансплантация 102, e205 – e210. DOI: 10.1097 / TP.0000000000002123 PubMed Аннотация | CrossRef Полный текст | Google Scholar Росси, Э.А., Кинтанилья, Л. Ф., Нонака, К. К. В., Соуза, Б. С., и де, Ф. (2019). Достижения в области биоинженерии ткани печени с децеллюляризованным биокаффолдом печени. Stem Cells Int. 2019, 2693189. DOI: 10.1155 / 2019/2693189 PubMed Аннотация | CrossRef Полный текст | Google Scholar Сайто Ю., Икемото Т., Морин Ю. и Шимада М. (2020). Текущее состояние гепатоцитоподобной клеточной терапии стволовыми клетками. Surg. Сегодня 51, 340–349. DOI: 10.1007 / s00595-020-02092-6 PubMed Аннотация | CrossRef Полный текст | Google Scholar Сайед Д., Хе, М., Хун, К., Гао, С., Рэйн, С., Ян, З. и др. (2010). МикроРНК-21 является последующим эффектором AKT, который опосредует его антиапоптотические эффекты посредством подавления лиганда Fas. J. Biol. Chem. 285, 20281–20290. DOI: 10.1074 / jbc.M110.109207 PubMed Аннотация | CrossRef Полный текст | Google Scholar Schug, J., McKenna, L. B., Walton, G., Hand, N., Mukherjee, S., Essuman, K., et al. (2013). Динамическое привлечение микроРНК к их мРНК-мишеням в регенерирующей печени. BMC Genomics 14: 264. DOI: 10.1186 / 1471-2164-14-264 PubMed Аннотация | CrossRef Полный текст | Google Scholar Слэттери, М. Л., Маллани, Л. Е., Сакода, Л. К., Вольф, Р. К., Стивенс, Дж. Р., Самовиц, В. С. и др. (2018). Путь передачи сигналов PI3K / AKT: ассоциации miRNA с дисрегулируемой экспрессией генов при колоректальном раке. Мол. Канцерогенный. 57, 243–261. DOI: 10.1002 / mc.22752 PubMed Аннотация | CrossRef Полный текст | Google Scholar Смец, Ф., Dobbelaere, D., McKiernan, P., Dionisi-Vici, C., Broué, P., Jacquemin, E., et al. (2019). Испытание фазы I / II мезенхимальных стволовых клеток печени при метаболических нарушениях печени у детей: проспективное открытое, многоцентровое, частично рандомизированное исследование безопасности одного цикла гетерологичных взрослых клеток-предшественников, полученных из печени человека (HepaStem), в мочевине нарушения цикла и пациенты с синдромом криглера-наджара. Трансплантация 103, 1903–1915. DOI: 10.1097 / TP.0000000000002605 PubMed Аннотация | CrossRef Полный текст | Google Scholar Сориа, Л.Р., Ах Мью, Н., Брунетти-Пьерри, Н. (2019). Прогресс и проблемы в разработке новых методов лечения нарушений цикла мочевины. Hum. Мол. Genet. 28, R42 – R48. DOI: 10.1093 / hmg / ddz140 PubMed Аннотация | CrossRef Полный текст | Google Scholar Спада, М., Порта, Ф., Риги, Д., Газзера, К., Тандой, Ф., Ферреро, И., и др. (2020). Внутрипеченочное введение стволовых клеток печени человека младенцам с наследственной неонатальной гипераммониемией: исследование фазы I. Stem Cell Rev.Rep. 16, 186–197. DOI: 10.1007 / s12015-019-09925-z PubMed Аннотация | CrossRef Полный текст | Google Scholar Сквайрс, Дж. Э., Солтис, К. А., Маккирнан, П., Сквайрс, Р. Х., Стром, С. К., Фокс, И. Дж. И др. (2017). Клиническая трансплантация гепатоцитов: что дальше? Curr. Пересадка. Rep. 4, 280–289. DOI: 10.1007 / s40472-017-0165-6 PubMed Аннотация | CrossRef Полный текст | Google Scholar Topczewska, J.M., Postovit, L.-M., Margaryan, N.В., Сэм, А., Гесс, А. Р., Уитон, В. В. и др. (2006). Эмбриональные и канцерогенные пути сходятся посредством передачи сигналов Nodal: роль в агрессивности меланомы. Нац. Med. 12, 925–932. DOI: 10,1038 / нм1448 PubMed Аннотация | CrossRef Полный текст | Google Scholar Trepotec, Z., Lichtenegger, E., Plank, C., Aneja, M.K., and Rudolph, C. (2019). Доставка терапевтических мРНК для лечения заболеваний печени. Мол. Ther. 27, 794–802. DOI: 10.1016 / j.ymthe.2018.12.012 PubMed Аннотация | CrossRef Полный текст | Google Scholar Вильярроя-Бельтри, К., Байшаули, Ф., Гутьеррес-Васкес, К., Санчес-Мадрид, Ф., и Миттельбрун, М. (2014). Разборка: регуляция загрузки экзосом. Семин. Cancer Biol. 28, 3–13. DOI: 10.1016 / j.semcancer.2014.04.009 PubMed Аннотация | CrossRef Полный текст | Google Scholar Wang, Q., Wang, Y., Minto, A. W., Wang, J., Shi, Q., Li, X., et al. (2008). Уровень микроРНК-377 активируется и может приводить к увеличению продукции фибронектина при диабетической нефропатии. FASEB J. 22, 4126–4135. DOI: 10.1096 / fj.08-112326 PubMed Аннотация | CrossRef Полный текст | Google Scholar Вэй, С., Тан, Дж., И Цай, X. (2020). Клетки-основатели гепатоцитов при регенерации печени: от идентификации до применения. Ячейка. Мол. Life Sci. CMLS 77, 2887–2898. DOI: 10.1007 / s00018-020-03457-3 PubMed Аннотация | CrossRef Полный текст | Google Scholar Ян, Л., Чанг, Н., Лю, Х., Хань, З., Чжу, Т., Ли, К., и другие. (2012). Мезенхимальные стволовые клетки костного мозга дифференцируются в миофибробласты печени путем трансформации фактора роста-β1 через ось сфингозинкиназа / сфингозин-1-фосфат (S1P) / рецептор S1P. г. J. pathol. 181, 85–97. DOI: 10.1016 / j.ajpath.2012.03.014 PubMed Аннотация | CrossRef Полный текст | Google Scholar . Leave a Reply
| |||||||||||||||||

 А пропуская через себя всю кровь человека, она обезвреживает большинство попавших извне бактерий.
А пропуская через себя всю кровь человека, она обезвреживает большинство попавших извне бактерий.


 Вклад Сколтеха совместно с MIT заключается в том, что мы создали и предоставили для эксперимета липидные наночастицы с siRNA к бета 1 интегрину, которые заблокировали экспрессию этого гена в гепатоцитах у мышей, а последующие наблюдения, над фенотипом полученной модели позволили идентифицировать холеангиоциты, как клетки, участвующие в регенерации печени. В настоящее время в Шотландском центре регенеративной медицины под руководством порфессора С. Форбса начинаются работы направленные на выделение и трансплантацию аутологичных холеангиоцитов пациентам с циррозом печени. Мы сейчас продолжаем коллаборацию с лаб. проф Форбса и занимаемся проверкой новых генов мишеней, блокирование которых может предотвращать или стабилизировать процессы связанные с фиброзом и последующим циррозом печени.»
Вклад Сколтеха совместно с MIT заключается в том, что мы создали и предоставили для эксперимета липидные наночастицы с siRNA к бета 1 интегрину, которые заблокировали экспрессию этого гена в гепатоцитах у мышей, а последующие наблюдения, над фенотипом полученной модели позволили идентифицировать холеангиоциты, как клетки, участвующие в регенерации печени. В настоящее время в Шотландском центре регенеративной медицины под руководством порфессора С. Форбса начинаются работы направленные на выделение и трансплантацию аутологичных холеангиоцитов пациентам с циррозом печени. Мы сейчас продолжаем коллаборацию с лаб. проф Форбса и занимаемся проверкой новых генов мишеней, блокирование которых может предотвращать или стабилизировать процессы связанные с фиброзом и последующим циррозом печени.»