Антральный гастрит — причины, симптомы, диагностика и лечение
Антральный гастрит – это хроническое воспалительное заболевание желудка, поражающее слизистую в выходном отделе (антруме). Относится к хроническому гастриту типа В – бактериально обусловленному. Проявляется болями в эпигастрии (голодными или через пару часов после еды), тошнотой, отрыжкой кислотой, диспепсическими явлениями при сохраненном аппетите. Основным методом диагностики является фиброгастродуоденоскопия, исследование на предмет наличия хеликобактерий. В лечение обязательно включаются антихеликобактерные антибиотики, антациды, регенерирующие и обезболивающие препараты.
Общие сведения
Антральный гастрит – хроническое воспаление слизистой желудка, локализующееся в пилорическом отделе. Данный отдел желудка выполняет функцию ощелачивания пищевого химуса перед переходом в кишечник. Воспаление в антруме вызывает блокировку выработки бикарбонатов, кислотность желудочного сока повышается, а в двенадцатиперстную кишку попадает кислое содержимое, провоцируя образование язв. Антральный гастрит обычно рассматривается как ранняя стадия хронического гастрита, при этой форме воспаления хеликобактерии выявляются в очень большом количестве. При распространении инфекции на другие отделы количество бактерии уменьшается. Антральный гастрит имеет симптоматику, весьма сходную с язвенной болезнью желудка. 85% всех заболеваний желудка приходится на эту патологию, тем не менее, обращаются к гастроэнтерологу лишь 10-15% всех больных хроническим гастритом.
Антральный гастрит обычно рассматривается как ранняя стадия хронического гастрита, при этой форме воспаления хеликобактерии выявляются в очень большом количестве. При распространении инфекции на другие отделы количество бактерии уменьшается. Антральный гастрит имеет симптоматику, весьма сходную с язвенной болезнью желудка. 85% всех заболеваний желудка приходится на эту патологию, тем не менее, обращаются к гастроэнтерологу лишь 10-15% всех больных хроническим гастритом.
Антральный гастрит
Причины
По наблюдениям специалистов в сфере клинической гастроэнтерологии, около 95% всех случаев хронического антрального гастрита связаны с обнаружением в слизистой желудка бактерии под названием Helicobacter pylori. Этот возбудитель может комфортно обитать в желудочной слизи при рН от 4 до 6, хотя и в более кислой среде сохраняет свою активность. Губительной для хеликобактерий является гипохлоргидрия (пониженная кислотность желудочного сока). В неблагоприятных условиях бактерия может принимать специальную форму покоя, а при попадании в комфортную среду – снова становится активной.
Способствуют хеликобактерной инвазии дуодено-гастральный рефлюкс (заброс содержимого кишечника в желудок из-за слабости пилоруса), прием некоторых препаратов (салицилаты, НПВС, противотуберкулезные средства), пищевая аллергия, неправильное питание, употребление спиртного, курение. Также предрасполагают к развитию этой патологии некоторые внутренние факторы: очаги хронической инфекции, эндокринная патология, недостаток железа, сердечная и дыхательная недостаточность, хроническая почечная недостаточность.
Патогенез
Особенностью хеликобактерий является выработка ими ряда ферментов, которые способствую изменению среды вокруг них. Так, уреаза расщепляет находящуюся в желудке мочевину до аммиака, защелачивая среду вокруг микроорганизма. Муциназа способствует снижению вязкости желудочной слизи. В таких условиях подвижные бактерии легко проникают сквозь слой защитной слизи к антральному эпителию желудка, где и начинают активно размножаться, вызывая повреждение слизистой и нарушение работы желудочных желез. Пилорический отдел перестает вырабатывать бикарбонаты (ощелачивающая среда), в связи с чем кислотность желудочного сока постепенно повышается, дополнительно повреждая эпителий желудка и в других отделах.
Пилорический отдел перестает вырабатывать бикарбонаты (ощелачивающая среда), в связи с чем кислотность желудочного сока постепенно повышается, дополнительно повреждая эпителий желудка и в других отделах.
Симптомы антрального гастрита
Обычно воспаление антральной части желудка проходит на начальных стадиях как неатрофический процесс без недостаточности секреции желудочного сока. Клиника этой патологии язвенноподобна: боли в эпигастральной области, голодные или через несколько часов после еды; изжога, отрыжка кислым и воздухом, склонность к запорам. Аппетит при этом не страдает. При осмотре язык чистый, влажный. При пальпации живота болезненность локализуется в эпигастрии справа (пилородуоденальная зона). Потеря веса бывает только при тяжелом течении заболевания.
Диагностика
При гастрографии с контрастированием у больных антральным гастритом отмечается утолщение рельефных складок в пилорическом отделе, спазм пилоруса, сегментирующая перистальтика, беспорядочная эвакуация желудочного содержимого. При ФЭГДС видна пятнистая гиперемия слизистой, отек тканей в антральном отделе, могут обнаруживаться кровоизлияния и эрозии. Отмечается повышенная экссудация, застой содержимого в желудке из-за спазма пилоруса. Во время эндоскопического исследования обязательно производится биопсия ткани для гистологического исследования и выделения возбудителя. При этом гистологически определяется выраженное воспаление, большое количество хеликобактерий на поверхности эпителия.
При ФЭГДС видна пятнистая гиперемия слизистой, отек тканей в антральном отделе, могут обнаруживаться кровоизлияния и эрозии. Отмечается повышенная экссудация, застой содержимого в желудке из-за спазма пилоруса. Во время эндоскопического исследования обязательно производится биопсия ткани для гистологического исследования и выделения возбудителя. При этом гистологически определяется выраженное воспаление, большое количество хеликобактерий на поверхности эпителия.
Уреазный тест на определение хеликобактерий проводится с помощью специальных экспресс-наборов во время гастроскопии. Для этого биоптат слизистой помещают в специальную среду, которая меняет свою окраску в зависимости от концентрации микроорганизмов на малиновую – от часа до суток. Если окраска не изменилась в течение суток – тест отрицательный. Также существует С-уреазный дыхательный тест. Для его проведения в желудок вводят меченную С13 мочевину, а затем в выдыхаемом воздухе определяют концентрацию С13. Если в желудке есть хеликобактерии, они разрушат мочевину, и концентрация С13 будет выше 1% (3,5% — легкая степень инвазии, 9,5% — крайне тяжелая).
С биоптатов слизистой обязательно делают посевы, инкубация которых происходит при крайне низкой концентрации кислорода (менее 5%) на кровяных средах. Результат посева с чувствительностью к антибиотикам будет получен уже через 3-5 суток. Достаточно чувствительным является ИФА метод выявления антител к хеликобактериям в крови, слюне и желудочном соке. Антитела появляются в крови в течение месяца после инфицирования, сохраняют свою активность также в течение месяца после полного излечения. Для определения кислотности желудочного сока используют внутрижелудочную рН-метрию, фракционное исследование желудочного сока с применением стимуляторов секреции. Заболеване дифференцируют с функциональными расстройствами, язвенной болезнью желудка.
Лечение антрального гастрита
Лечением данной патологии занимаются врачи-гастроэнтерологи, терапевты, эндоскописты; при обострениях больной находится в отделении гастроэнтерологии или терапии. Начинается лечение антрального гастрита с назначения специальной лечебной диеты: в период обострения стол 1б с постепенным расширением до первого стола в течение нескольких недель или месяцев.
Обязательно назначаются антихеликобактерные препараты. Этиотропная терапия H.pylori достаточно сложна, так как это микроорганизм быстро приспосабливается к популярным антибиотикам. Чаще всего назначают двойную или тройную схему лечения, в которую включают метронидазол, кларитромицин, ампициллин или тетрациклин. В схему рекомендуется добавлять ингибиторы протонной помпы, которые угнетают хеликобактерии, а антибактериальными препаратами проводят их полную эрадикацию.
Противовоспалительная терапия может проводиться как аптечными препаратами, так и травами по рецептам народной медицины. Так, в период обострения рекомендуется употреблять настои ромашки, мяты, зверобоя, семян льна. При появлении эрозий на слизистой антрального отдела желудка, повышенной кислотности желудочного сока назначают антисекреторные средства. При спазме пилоруса успешно применяются миотропные спазмолитики: дротаверин, папаверин. Для нормализации перистальтики и устранения дуоденогастрального рефлюкса используется метоклопрамид.
Условием полного выздоровления является назначение репаративных средств. Это могут быть препараты, стимулирующие синтез белка (инозин, анаболические стероиды), карнитин, масло облепихи. Важное место занимает и физиотерапия: гальванизация желудка с электрофорезом лекарственных средств (при спазме пилорического отдела), УВЧ-терапия, лечение ультразвуком (с обезболивающей целью), диадинамическими токами Бернара, синусоидальными модулированными токами (для устранения боли и диспепсии). После купирования обострения рекомендуют проведение грязе- и парафинотерапии, лечение минеральными водами.
Прогноз и профилактика
Прогноз при антральном гастрите благоприятный только при своевременном начале лечения, соблюдении всех рекомендаций, режима дня и питания. Если вовремя не обратиться к гастроэнтерологу, гастрит переходит в диффузную форму, которая может закончиться образованием язв (при гиперфункции слизистой) или опухолей желудка (при атрофии слизистой).
Антральный гастрит (Тип в) — признаки, причины, симптомы, лечение и профилактика
Лечение
Терапия в первую очередь сконцентрирована на уничтожении патогенной микрофлоры Helicobacter pylori. Проводится она с помощью антибиотиков, в основном это метронидазол, ампициллин, тетрациклин.
Назначается лечебный диетический стол. Пищу нужно принимать часто и маленькими порциями, приготовленную на пару. Необходимо уменьшить нагрузку на пораженный орган, исключаются тяжелые продукты, алкоголь, жареное, копченое, кофе, свежие фрукты и овощи, шоколад.
Симптоматическая терапия – это спазмолитики (но-шпа), препараты, нормализирующие кислотный фон (омепразол), ферменты (панкреатин, мезим), медикаменты, при помощи которых восстанавливается слизистая — солкосерил, актовегин.
Длительность и эффективность лечения зависит от соблюдения всех назначенных врачом рекомендаций, в основном затягивается до нескольких месяцев.
Прогноз благоприятный при своевременном лечении, в противном же случае болезнь может осложниться язвой или онкологией.
Профилактика
Чтобы обезопасить себя от заболевания, следует вести здоровый образ жизни, не злоупотреблять вредной едой, спиртным и сигаретами. Периодически проходить профилактические медосмотры.
При наличии хронического гастрита важно соблюдать диету. Полезные продукты: нежирное мясо, сухое печенье, хлеб, крупы (рисовая, гречневая, манная), легкие супы, сладкие фрукты и ягоды в печеном виде.
Народные средства борьбы с недомоганием очень разнообразны.
Натощак утром рекомендуют выпивать стакан свежевыжатого картофельного сока. Это снизит болевые ощущения, травяные чаи со зверобоем, ромашкой, шиповником. Семена льна при варке образуют слизь, данный настой обволакивает слизистую оболочку, чем предохраняет ее от пагубного действия кислоты. Показана умеренная физическая нагрузка, минимум нервных стрессов.
Показана умеренная физическая нагрузка, минимум нервных стрессов.
Литература и источники
Видео по теме:
Пепсиноген II
Общая информация об исследовании
Пепсиноген – неактивный предшественник фермента пепсина. Доказано, что концентрация пепсиногена в крови отражает функциональные и морфологические изменения слизистой оболочки желудка, такие как воспаление, атрофия, мета- и неоплазия. Пепсиноген существует в двух вариантах – пепсиноген I и II. Секреция пепсиногена I осуществляется только в клетках желез тела желудка, пепсиноген II секретируется в клетках желез тела, кардиального и пилорического отделов желудка, а также в бруннеровых железах двенадцатиперстной кишки.
Концентрация пепсиногена II повышена при всех заболеваниях, связанных с инфекцией H. pylori. Эта бактерия – единственный известный микроорганизм, способный заселять слизистую оболочку желудка. Н. pylori занимает только эпителий желудочного типа, поэтому не может колонизировать нормальный эпителий двенадцатиперстной кишки и пищевода. Около 50 % населения всей Земли инфицировано Н. pylori
 Как правило, Н. pylori инфицируются в детстве, инфицирование не сопровождается какими-либо симптомами и остается незамеченным. Без лечения
Как правило, Н. pylori инфицируются в детстве, инфицирование не сопровождается какими-либо симптомами и остается незамеченным. Без лечения Повреждающее действие Н. pylori осуществляется на поверхности слизистой желудка – бактерия проникает сквозь слой слизи и прикрепляется к эпителию (но не попадает при этом внутрь клеток). Н. pylori обладает множеством факторов болезнетворности, основные из которых: уреаза, цитотоксин-ассоциированые гены (в особенности cagA), цитотоксин VacA и адгезин BabA. Они поддерживают длительное воспаление слизистой оболочки желудка, что проявляется как 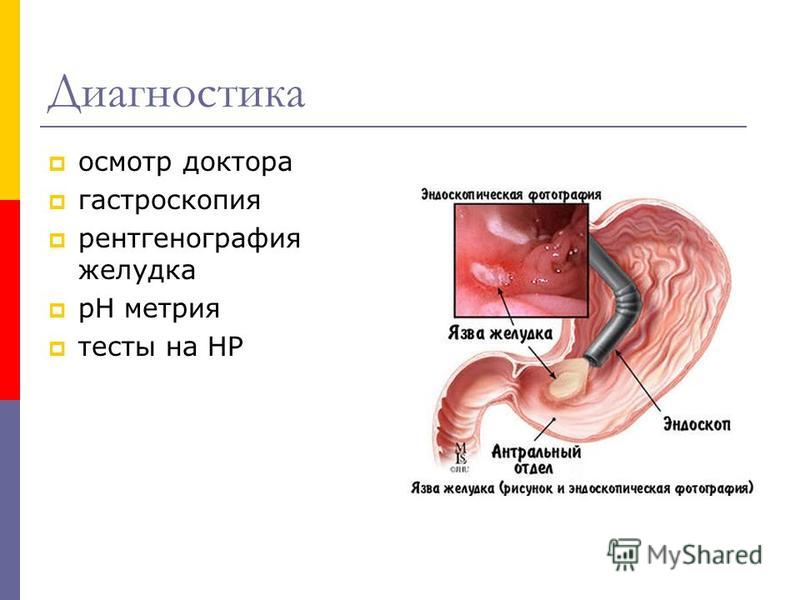 В зависимости от степени выраженности воспалительной реакции различают H. pylori-ассоциированный гастрит с преимущественным поражением антрального отдела желудка, с поражением тела желудка или пангастрит. Почему у одних людей гастрит развивается в основном в антральном отделе при относительной сохранности слизистой оболочки тела желудка и наоборот, остается не до конца ясным. Доказано, что различные части слизистой оболочки желудка характеризуются разной степенью устойчивости к
В зависимости от степени выраженности воспалительной реакции различают H. pylori-ассоциированный гастрит с преимущественным поражением антрального отдела желудка, с поражением тела желудка или пангастрит. Почему у одних людей гастрит развивается в основном в антральном отделе при относительной сохранности слизистой оболочки тела желудка и наоборот, остается не до конца ясным. Доказано, что различные части слизистой оболочки желудка характеризуются разной степенью устойчивости к 
При антральном H. pylori-ассоциированном гастрите нарушается нормальный ритм секреции гастрина и возникает гипергастринемия. Она приводит к повышению активности главных и обкладочных клеток желудка, что сопровождается усилением секреции пепсиногена I и II и соляной кислоты. В норме синтез гастрина провоцируется приемом пищи, а избыток пепсиногена I, II и соляной кислоты расходуется в процессе переваривания белков. При
Под воздействием хронического избытка соляной кислоты на фоне длительной гипергастринемии эпителий двенадцатиперстной кишки подвергается желудочной метаплазии.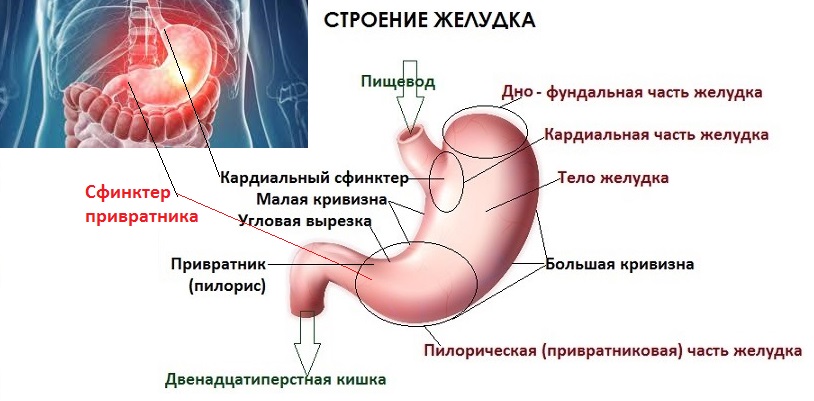 Несмотря на то что H. pylori не способна колонизировать нормальную слизистую оболочку двенадцатиперстной кишки, она может заселять метаплазированный эпителий. Хроническая инфекция H.
Несмотря на то что H. pylori не способна колонизировать нормальную слизистую оболочку двенадцатиперстной кишки, она может заселять метаплазированный эпителий. Хроническая инфекция H. 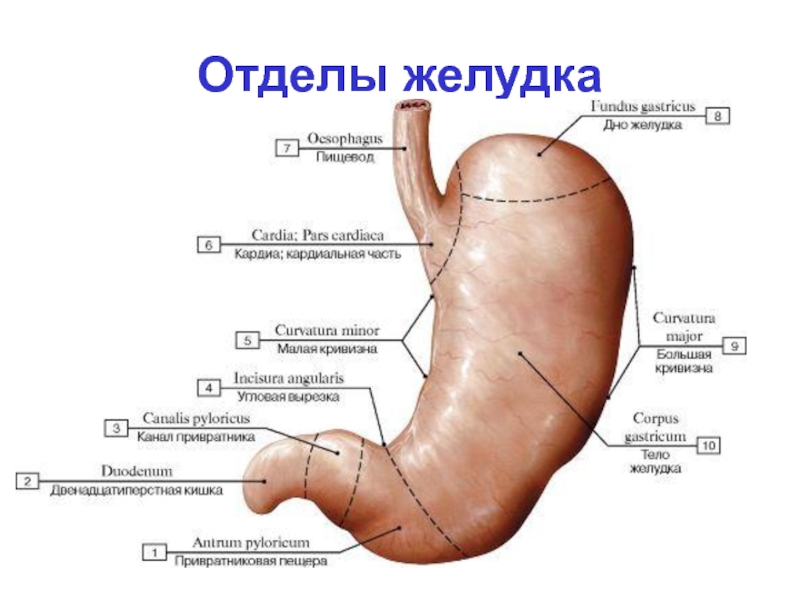 pylori.
pylori.
У меньшей части пациентов развивается H. pylori-ассоциированный гастрит с преимущественным поражением тела желудка. Воспалительная реакция сопровождается угнетением и постепенной потерей главных и обкладочных клеток слизистой оболочки, что проявляется атрофическим гастритом. Атрофия слизистой тела желудка сопровождается снижением концентрации пепсиногена I и соляной кислоты. В отсутствие отрицательной обратной связи со стороны соляной кислоты гастрин вырабатывается в больших количествах. В отличие от Н. pylori—ассоциированного антрального гастрита, гипергастринемия при атрофическом гастрите является не причиной болезни, а ответом на нее. Избыток гастрина стимулирует выработку пепсиногена II клетками кардиального и пилорического отделов желудка, поэтому его концентрация, в отличие от пепсиногена I, не снижается, а, наоборот, нарастает в результате гипергастринемии. Изменения концентраций пепсиногена I и II являются диагностическим маркером атрофического гастрита.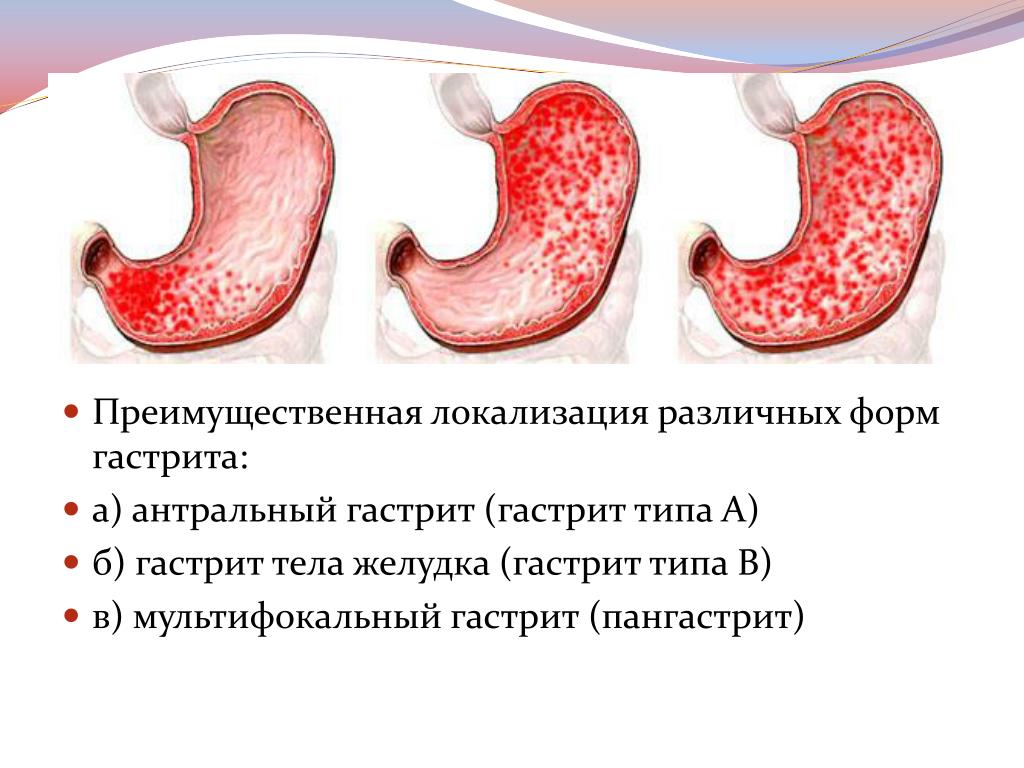
Также для раннего выявления такого гастрита и его осложнений используют индекс PGI/PGII – соотношение концентраций пепсиногена I и II, он снижен при атрофическом гастрите тела желудка и пангастрите, причем степень снижения пропорциональна тяжести процесса. Измерение концентраций пепсиногенов I и II и расчет индекса PGI/PGII – оптимальный скрининговый метод оценки слизистой оболочки тела желудка, его преимущества заключаются в безопасности, специфичности и чувствительности. Измерение концентрации пепсиногенов I и II с измерением гастрина 17 и теста на H. pylori позволяет оценить состояние слизистой оболочки всех отделов желудка. Такой подход не уступает стандартному эндоскопическому исследованию и поэтому называется «серологической биопсией». При атрофическом гастрите нарушаются механизмы всасывания витамина B
Атрофический гастрит – значимая причина аденокарциномы желудка. Вероятность рака увеличивается при воздействии дополнительных факторов, таких как курение, злоупотребление алкоголем, некоторыми лекарственными средствами. Для раннего выявления аденокарциномы у пациентов с факторами риска необходимо контролировать уровни пепсиногена I и II и индекс PGI/PGII. H. pylori удается обнаружить в 70 % случаев язвенной болезни желудка. В подавляющем большинстве случаев язва желудка локализована на малой кривизне желудка в области «переходной зоны» – участка слизистой оболочки, где происходит смена эпителия тела желудка на эпителий антрального отдела. Переходная зона интенсивно колонизирована H. pylori и характеризуется максимально выраженным воспалительным ответом, который приводит к язве. Следует отметить, что язва желудка, в отличие от язвы двенадцатиперстной кишки, возникает на фоне нормального или пониженного уровня секреции соляной кислоты при отсутствии гипергастринемии. Считается, что в образовании язвы желудка большее значение имеет непосредственное повреждение H. pylori слизистой переходной зоны, а не гормонональный дисбаланс. Другой особенностью язвы желудка является ее способность перерождаться в аденокарциному (в 3 % случаев). Язва желудка характеризуется болями сразу после приема пищи и сопровождается потерей веса. Уровень пепсиногена II значительно повышен у пациентов с H. pylori-ассоциированной язвой желудка и может быть использован для диагностики этого заболевания.
pylori слизистой переходной зоны, а не гормонональный дисбаланс. Другой особенностью язвы желудка является ее способность перерождаться в аденокарциному (в 3 % случаев). Язва желудка характеризуется болями сразу после приема пищи и сопровождается потерей веса. Уровень пепсиногена II значительно повышен у пациентов с H. pylori-ассоциированной язвой желудка и может быть использован для диагностики этого заболевания.
При лечении H. pylori-ассоциированных заболеваний концентрация пепсиногена II возвращается к норме или значительно уменьшается, что отражает улучшение состояния слизистой оболочки желудка или двенадцатиперстной кишки. Поэтому повторное измерение концентрации пепсиногена II может быть использовано на этапе контроля лечения с целью оценить его результат и восстановление слизистой оболочки. В онкологической практике тест на пепсиноген II применяют для диагностики опухолей. При гастриноме, гормонально-активной опухоли, избыток гастрина стимулирует секрецию солянойкислоты обкладочными клетками желудка и провоцирует образование язвы, данное состояние известно как синдром Золлингера – Эллисона. Гастринома чаще локализуется в ткани поджелудочной железы, однако может находиться в любом другом органе. В 60 % случаев она является злокачественным образованием. Язвы, возникающие при синдроме Золлингера – Эллисона, характеризуются упорным рецидивирующим течением, не поддаются медикаментозному лечению, множественные, с атипичной локализацией в дистальном отделе двенадцатиперстной кишки. Они образуются в результате прямого повреждающего действия избытка соляной кислоты и не связаны с H. pylori.
Гастринома чаще локализуется в ткани поджелудочной железы, однако может находиться в любом другом органе. В 60 % случаев она является злокачественным образованием. Язвы, возникающие при синдроме Золлингера – Эллисона, характеризуются упорным рецидивирующим течением, не поддаются медикаментозному лечению, множественные, с атипичной локализацией в дистальном отделе двенадцатиперстной кишки. Они образуются в результате прямого повреждающего действия избытка соляной кислоты и не связаны с H. pylori.
Уровень пепсиногена II при гастриноме значительно повышен.
Для многих злокачественных новообразований характерна секреция проферментов, гормонов и белков-онкомаркеров, в норме несвойственных ткани, из которой происходит опухолевый клон. Например, около 50 % аденокарцином молочной железы производят пепсиноген II, хотя нормальной ткани молочной железы синтез этого профермента несвойственен. Активная секреция пепсиногена II характерна для высокодифференцированных (медленно растущих) аденокарцином, а также для аденокарцином, экспрессирующих эстрогеновые рецепторы. Поэтому интенсивный синтез этого профермента опухолью считается благоприятным прогностическим признаком и, наоборот, низкий уровень секреции пепсиногена II аденокарциномой связан с более частыми рецидивами.
Для чего используется исследование?
- Для диагностики Н. pylori-ассоциированного антрального гастрита, атрофического гастрита и пангастрита.
- Для диагностики язвы желудка и двенадцатиперстной кишки.
- Для раннего выявления аденокарциномы желудка.
- Для контроля за лечением H. pylori-ассоциированного гастрита, язвы желудка и двенадцатиперстной кишки.
- Для диагностики гастриномы.
- Для того чтобы дать прогноз аденокарциномы молочной железы.
Когда назначается исследование?
- При симптомах гиперацидного (антрального) гастрита: дискомфорте в эпигастральной области через 1,5-2 часа после приема пищи и натощак, изжоге, ночном кашле.
- При симптомах атрофического гастрита: дискомфорте в эпигастральной области, чувстве быстрого насыщения, тошноте.
- При симптомах дефицита витамина B12: головокружении, сердцебиении, нарушении периферической чувствительности, парезе, диарее.
- При симптомах язвы двенадцатиперстной кишки: боли в эпигастральной области через 1,5-2 часа после еды, натощак и в ночное время суток, изжоге, ночном кашле, диарее.
- При симптомах язвы желудка: боли в эпигастральной области сразу после приема пищи, чувстве быстрого насыщения, потере веса.
- При имеющихся факторах риска аденокарциномы желудка: атрофическом гастрите, употреблении копченой пищи и большого количества алкоголя, курении, наследственной предрасположенности, предраковых состояниях.
- При симптомах гастриномы: интенсивных болях в эпигастральной или поясничной области, выраженной изжоге, упорной диарее.
- При оценке лечения от H. pylori и восстановления слизистой оболочки желудка или двенадцатиперстной кишки.
- При планировании тактики лечения аденокарциномы молочной железы, а также при оценке риска рецидива аденокарциномы.
Атрофический гастрит хронический, слизистая желудка гиперемирована
Здравствуйте уважаемые доктора. Мне 33 года. Пошла на ФГДС, просто провериться, тк в принципе ничего не беспокоило, но у меня плохая наслед., потому решила. Результат меня шокировал( ФГДС: слизистая желудка — розовая во всех отделах, гиперемирована и истончена очагово умеренно и незначительно в антральном отделе желудка, отечна незначительно, без эрозивных изменений. Заключение: эриматозная очаговая гастропатия. Эндоскопические признаки гипотрофического очагового антрального хеликобактерного гастрита (был сразу выполнен тест на Хелик +) Биопсия: 1.Гастрит хронический антральный атрофический незначительный, угла желудка без атрофии. Активность и лимфоидная инфильтрация незначительная. Внутрислизистые геморрагии. Хелик+, 2. Гастрит хронический тела и свода желудка без атрофии. Активность умеренная, лимфоидная инфильрация выраженная. Хелик++ Лечение: пептипак 7 дн.+ линекс. Вопрос: можно ли регинирировать какими-либо препаратами слизистую и возможно ли избавится от атрофии, может еще какой-то препарат надо подключить? Достаточно ли на хелик лечения 7 дн…везде пишут 10-14? К слову не пью и не курю. Спасибо
Алина, женщина, 1988 лет, 13 ноября 2019
Здравствуйте.
Самым опасным и коварным гастритом принято считать именно атрофический гастрит.
Именно атрофический гастрит считается непосредственным предшественником онкологии желудка. Здесь Ваши опасения не беспочвенны и Ваше волнение вполне обоснованно.
Поэтому очень важной задачей является пожизненное наблюдение у врача. Это позволит своевременно назначить лечение и улучшить состояние слизистой желудка. Атрофированные клетки вернуть в первоначальное состояние на данном этапе развития медицины не возможно.
Но у Вас пока атрофии и нет. Это очень хорошо.
Думаю, Вам стоит лично показаться гастроэнтерологу лично и учитывая серьезность заболевания еще раз все обсудить . Не забудьте результаты ваших исследований.
Здоровья Вам.
GastroPanel® | Лабораторія Др. Рьодгера
Лабораторная диагностика
GastroPanel®: диагностика атрофического гастрита — in vitro
Каждый, кто неоднократно или постоянно имел такие симптомы, как боль в желудке, тошнота или проблемы с пищеварением, должен быть обследован как можно раньше. Если у вас присутствует кровь в кале или в рвотных массах, следует немедленно обратиться к врачу. Тщательный анамнез и физическое обследование (например, ультразвуковое исследование) иногда могут предоставить достаточно доказательств гастрита. Однако, надежный диагноз возможен только при помощи гастроскопии.Для пациентов, которые хотят избежать неудобств во время проведения гастроскопии, или для которых такое вмешательство может быть затруднительным в силу их возраста, неинвазивная диагностика является предпочтительной альтернативой гастроскопии.
Это также касается пациентов, которым гастроскопия не может быть проведена в силу анатомических особенностей. GastroPanel®- доступный анализ крови, с помощью которого можно проверить предположительный диагноз атрофического гастрита и определить возможную локализацию воспаления слизистой желудка.Преимущество анализа крови заключается в том, что он не является стрессовым, а значит, может быть использован и для профилактического медицинского осмотра у пожилых людей. GastroPanel® был подтвержден в нескольких крупных исследованиях, основанных на гастроскопии, подтвержденных биопсией.13-17Все исследования были включены в соответствующий мета-анализ.18В рамках анализа крови GastroPanel® для оценки структуры и функции слизистой желудка определяют концентрацию четырех различных параметров в плазме крови с помощью количественного иммуноферментного теста (ИФА):
■H. Pylori IgG (анти-Hp антитела)
Наличие или отсутствие H. pylori
■Пепсиноген I и II
Состояние слизистой тела желудка при атрофическом гастрите
■Амидированный гастрин-17
Состояние слизистой оболочки антрального отдела желудка при атрофическом гастрите
По полученным результатам можно сделать утверждение о наличии инфекции в прошлом или активной инфекции H. pylori, что является необходимым условием для большинства случаев гастрита. Кроме того, результаты GastroPanel® могут подтвердить существование атрофического гастрита и локализацию воспалительного повреждения слизистой оболочки (тела, антрального отдела) .19-20
IgG-антитела к H. pylori
H. pylori — это спиралевидная, грамотрицательная бактерия, которая колонизирует желудок человека. Этот микроорганизм оседает в слизистой оболочке на желудочном эпителии и в железах, но, кажется, не проникает в клетки эпителия. Инфекция H. pylori является самой распространенной причиной хронического гастрита, поскольку слизистая оболочка вокруг областей, где колонизируется бактерия, всегда воспаляется.
Это состояние известно как хронический поверхностный гастрит или неатрофический гастрит, который длится всю жизнь, если его не лечить. Без успешного уничтожения бактерий этот хронический воспалительный процесс может привести к атрофического гастриту.21
Большинство людей, которые заражаются H. pylori, вырабатывают антитела IgG к возбудителю.22 Возрастная частота антител одинакова у мужчин и женщин.23 Многие пациенты с высоким титром антител не имеют симптомов, даже если они инфицированы H. pylori. Поэтому уровень антител не обязательно коррелирует с тяжестью клинических симптомов.
Если титр антител является единственным определенным биомаркером в GastroPanel®, который повышен, это означает поверхностный, но не атрофический гастрит, ассоциированный с H. pylori, в то время как повышенный уровень антител, связанный с аномалиями других трех биомаркеров, подтверждает диагноз атрофического гастрита, ассоциированного с H. pylori.
Проведение количественного определения антител человека класса IgG с помощью ИФА для выявления активной колонизации слизистой желудка имеет преимущество перед другими общепринятыми методами анализа (например, дыхательный тест с мочевиной 13С, тест кала на антиген): положительных больных H. pylori можно достоверно выявить также при наличии атрофического гастрита, MALT-лимфомы, язвы желудка или двенадцатиперстной кишки, а также у людей, принимающих ингибиторы протонной помпы или антибиотики. 24-26
Язвенная болезнь желудка
КУБАНСКАЯ ГОСУДАРСТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ
КАФЕДРА ОБЩЕЙ И ГОСПИТАЛЬНОЙ ХИРУРГИИ
АВАКИМЯН В.А. САВЧЕНКО Ю.П.
(хирургические аспекты)
Методические рекомендации для студентов старших курсов, интернов, клинических ординаторов и начинающих хирургов
Краснодар
2004
Оглавление
.
Глава 1. Краткий анатомо-физиологический очерк………………………. 3
Глава 2. Теории патогенеза язвенной болезни……………………………. 11
Глава 3. Хирургическое лечение гастродуоденальных язв………………. 20
• История развития хирургического лечения язвенной болезни…………. 20
• Показания к хирургическому лечению язвенной болезни……………….. 28
• Выбор метода хирургического лечения язвенной болезни……….…….. 30
• Хирургическое лечение гастродуоденальных язв,
осложненных стенозом……………………………………………………… 32
• Хирургическое лечение гастродуоденальных язв,
осложненных пенетрацией…………………………………………………. 36
3.6 Хирургическое лечение гастродуоденальных язв,
осложненных перфорацией………………………………………………… 39
3.7 Хирургическое лечение гастродуоденальных язв,
осложненных кровотечение ………………………………………………… 45
• Ведение послеоперационного периода …………………………..……… 53
Рекомендуемая литература………………………………………………….. 55
ГЛАВА 1. Краткий анатомо-физиологический очерк желудка
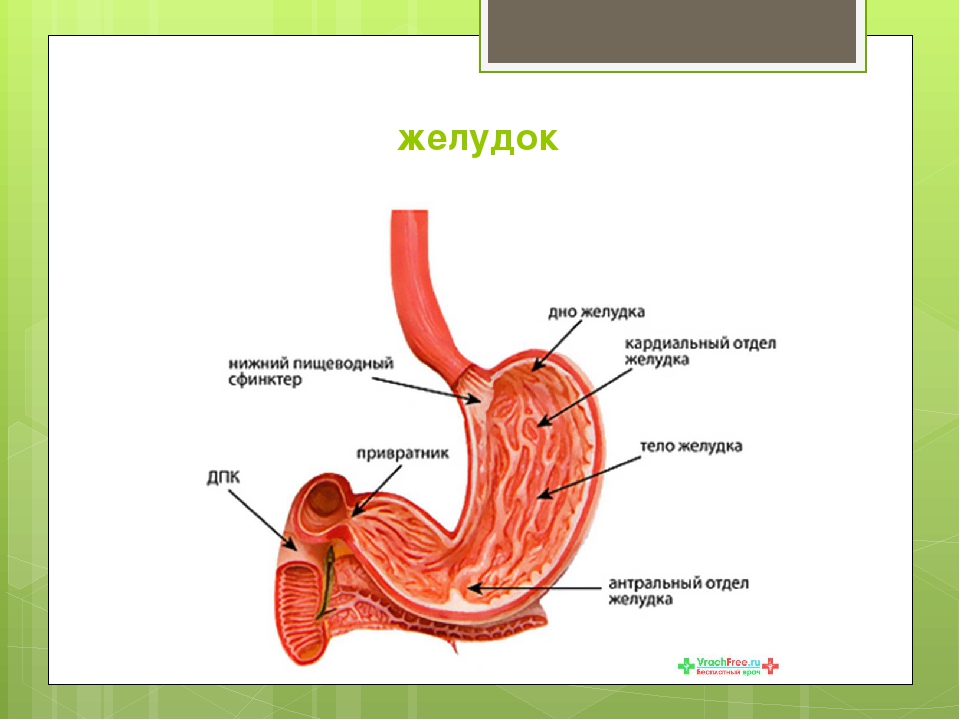
В желудке различают следующие его отделы: кардиальный, тело желудка, интермедиарный, антральный, пилорический и привратник (рис. 1). Стенка желудка состоит из трех слоев: а) наружного серозного; б) среднего мышечного и в) внутреннего слизистого с рыхлой подслизистой тканью.
Рис. 1. Анатомическое деление желудка, принятое морфологами (А) и клиницистами (Б).
1 – кардиальный отдел желудка; 2 – тело желудка; 3 — интермедиарный отдел желудка; 4 – пилорический отдел желудка;5 – привратник; 6 – антральный отдел желудка (по Л.П. Рябовой и Ц.Г. Масевич, 1975).
Серозная оболочка покрывает весь желудок, за исключением узкой полоски на большой и малой кривизне, где проходят кровеносные сосуды. Серозная оболочка переходит на желудок с соседних органов и в местах этих переходов образует связочный аппарат желудка.
Мышечный каркас желудка состоит из трех слоев гладких мышечных волокон. Что и объясняет сложный и многообразный характер сокращений желудка, и большую вариабельность его формы.
Слизистая оболочка желудка в наибольшей степени обеспечивает основную переваривающую функцию желудка, и строение ее находится в полном соответствии с этой важной задачей. Между отдельными складками слизистой оболочки, на каждом ее валике, расположены желудочные ямки. На территории свода и тела желудка расположены главные железы, у входа в желудок находятся кардиальные железы, а пилорический и антральный отделы выстланы пилорическими железами, на узком пространстве в 1-2 см, расположены интрамедиарные железы (рис. 2).
Рис. 2. Схематическое распределение желудочных желез. Желудок рассечен по большой кривизне и развернут по обе стороны (по Ю.М. Лазовскому).
1 – кардиальные железы; 2 – главные железы; 3 -интрамедиарные железы; 4 – пилорические железы.
Главные железы занимают самую большую площадь в желудке. Здесь протекают основные процессы образования соляной кислоты, и совершается секреция пепсина. Главные железы состоят из железистых особых трубок, которые оканчиваются в ямке слизистой оболочки желудка. В каждой такой трубке различают три отдела: шейку, добавочный отдел и тело железы. Желудочная ямка – это выход из железистой трубки, она выстлана слизистыми клетками. Клетки отдельных ямок, соединяясь, образуют однослойный цилиндрический эпителий желудка. Клетки мукодийного эпителия наполнены зернышками муцигена, которые выделяют желудочную слизь, характерную тем, что она не растворяется в соляной кислоте. Главная ее роль – защита слизистой оболочки желудка от переваривающего действия желудочного сока. Количество и качество слизи покровного эпителия зависит от природы раздражителя.
Шейка трубки выстлана слизистыми, малодифференцированными клетками и содержат мало секреторного материала.
Добавочный отдел составляет приблизительно 1/3 всей железистой трубки. Стенки его выстланы специальными, так называемыми, добавочными клетками, которые вырабатывают слизь. Установлено, что слизь, выделяемая клетками покровного эпителия, не растворяется, а слизь, вырабатываемая клетками шейки и добавочного отдела, растворяется в желудочной соляной кислоте.
Кроме добавочных клеток, добавочный отдел железистой трубки содержит и обкладочные клетки, которые являются источником соляной кислоты желудочного сока. Card , Marks (1960) установили, что между интенсивностью кислотообразовательной функцией желудка и числом обкладочных клеток имеется прямая тесная коррелятивная связь.
В теле железистой трубки находятся главные или пепсиногенные клетки. Гранулы этих клеток содержат предшественник пепсина – пепсиноген. В лаборатории Б.П. Бабкина (1960) установлено, что единственным источником пепсина, а так же и соляной кислоты являются главные железы. Трубки кардиальных желез выстланы большими клетками призматической формы, наполненными крупными гранулами мукодийного типа. Слизь, которая выделяется кардиальными железами, содержит бикарбонат. В кардиальных железах содержатся так же обкладочные и главные клетки, но физиологическая роль их незначительна.
Пилорическими железами выстлан весь антральный отдел. Клетки пилорических желез принадлежат к мукодийным клеткам желудка, и основная их функция заключается в снижении кислотности содержимого желудка. По мнению Б.П. Бабкина (1960), Е.Ю. Линара (1968) и других, пилорические железы выделяют гастрин.
Интермедиарные железы по своему строению напоминаю как главные, так и пилорические. Сравнительное изучение секреции пилорической и интермедиарной частей показало, что активная роль (высокая кислотность и высокая переваривающая способность желудочного сока) присуща только интермедиарной части.
Кровоснабжение желудка. Артерии желудка происходят от трех главных ветвей чревного ствола. Предназначенные для желудка ветви артерий широко анастомозируют между собой, образуя две главных дуги, расположенных вдоль большой и малой кривизнами желудка между сходящимися в этом месте листками брюшины (рис. 3). Артериальные стволы соединяются со стенкой желудка очень слабо, что крайне важно ввиду больших изменений размеров желудка. Когда желудок сокращается, артерии извиваются; когда желудок растягивается, артерии выправляются. Собственно сосудам всех слоев желудка свойственна извилистость, которая увеличивается с возрастом. Вполне вероятно, что извилистость сосудов желудка как органа, постоянно меняющего свой объем, оказывает повышенное сопротивление току крови и имеет значение регулятора кровоснабжения различных слоев стенки желудка по мере преобладания то секреторно-всасывательной, то двигательной его функции. Повышенная потребность в кровенаполнении функционирующего слоя желудка может быть удовлетворена тем раньше, чем быстрее наступит переключение усиленного тока крови в сосуды этого слоя.
Рис. 3. Артерии желудка (по Р.Д. Синельникову, 1952).
а – вид спереди, б – вид сзади.
1 – левая желудочная артерия, 2 – селезеночная артерия, 3 – общая печеночная артерия, 4 – правая желудочная артерия, 5–желудочно-двенадцатиперстнокишечная артерия, 6–правая желудочно-сальниковая артерия, 7 – левая желудочно-сальниковая артерия.
В этом отношении велика роль артериовенозных анастомозов (шунтов), как обходных путей, благодаря которым кровь может не заполнять капиллярного русла слизистого слоя желудка, не функционирующего в данный момент. Капилляры, анастомозируя между собой, образуют кольцеподобные петли, окружающие железы СОЖ. Таким образом, возникает межжелезистая сеть, простирающаяся почти на всю глубину функционального слоя СОЖ. Непосредственно под эпителием артериальные капилляры межжелезистой сети переходят в венозные капилляры. Образовавшиеся в результате слияния венозных капилляров, венулы собираются в более крупные венозные стволы, и далее через левую желудочно-сальниковую и короткие желудочные вены кровь направляется в селезеночную вену. Через правую желудочно-сальниковую вену кровь оттекает в верхнебрижеечную вену, а через венечную вену – в воротную вену. Эти вены подобно другим ветвям воротной системы, имеют выраженный мышечный слой и снабжены многочисленными клапанами.
Врачи Морозовской больницы помогли новорожденному с редким пороком развития желудочно-кишечного тракта
Мальчика, которому после рождения исполнилось 17 дней, в Морозовскую детскую больницу доставила бригада Скорой медицинской помощи. Состояние ребенка врачи-неонатологи оценили как тяжелое: он срыгивал после каждого кормления, вследствие чего отмечалась патологическая потеря веса (200 грамм от рождения).
После осмотра пациента, с учетом клинических симптомов и возраста, врачи заподозрили пилоростеноз — сужение отверстия, ведущего из желудка к двенадцатиперстной кишке за счет утолщения мышечного слоя. Однако проведенные ультразвуковые исследования диагноз не подтвердили.
Для восстановления водно электролитного баланса ребенку начали внутривенно вводить специальные вещества. Это позволило стабилизировать состояние новорожденного и предотвратить патологические потери организма.
С целью дообследования малышу было проведено рентгенографическое исследование прохождения водорастворимого рентгеноконтрастного препарата по желудочно-кишечному тракту, а также осмотр пищевода, желудка и двенадцатиперстной кишки с помощью микрокамер (эзофагогастродуоденоскопия). Специалисты диагностировали мембрану пилорического отдела желудка. Анатомически она представля¬ет собой перегородку между желудком и двенадцатиперстной кишкой.
«После предоперационной подготовки ребенку выполнили лапароскопию, которая подтвердила локальное сужение, не пропускающее нагнетаемый воздух в желудок, в месте перехода антрального отдела желудка в пилорический. На задне-боковой стенке желудка была обнаружена расположенная полукольцом мембрана. Мы иссекли мембрану, наложили швы на слизистую желудка, в тощую кишку ввели зонд для кормления и ушили желудок в поперечном направлении. Операция длилась около полутора часов», — рассказал детский хирург, обладатель звания «Московский врач» Михаил Рехвиашвили.
Как отметил врач, врожденная мембрана желудка — редкая патология. Сложность диагностики заключается в отсутствии специфических симптомов, характерных для данного заболевания. Трудность хирургического лечения в том, что мембрана состоит из подслизистого и слизистого слоя (без мышц) и сокращается во время иссечения настолько, что ее непросто определить даже при непосредственном осмотре.
В послеоперационном периоде в течение четырех суток ребенок находился в реанимации. Затем врачи удалили зонд. Рентгеноконтрастное исследование подтвердило полное восстановление работы желудка.
Мальчик был переведен в неонатологическое отделение, где находился вместе с мамой. Было возобновлено грудное вскармливание. Объем кормления постепенно увеличился до физиологической нормы. Ребенок полностью усваивал питание и начал прибавлять в весе. На десятый день после хирургического вмешательства с прибавкой в весе 670 грамм (от поступления) малыша в удовлетворительном состоянии выписали домой.
Антрум желудка — обзор
Желудочно-кишечная регуляция аппетита и потребления энергии
Аппетит и потребление энергии зависят от точной координации взаимосвязанных внутрижелудочных и тонких кишечных механизмов, запускаемых взаимодействием с потребляемыми питательными веществами. Опорожнение желудка отражает скоординированную двигательную активность проксимального отдела желудка, дистального отдела желудка (антрального отдела и привратника) и двенадцатиперстной кишки, которая контролируется в основном обратной связью нервных и гуморальных сигналов, генерируемых взаимодействием питательных веществ с тонкой кишкой.Грелин секретируется желудком и стимулирует аппетит и потребление энергии, тогда как холецистокинин (CCK), пептидный тирозинтирозин (PYY) и глюкагоноподобный полипептид-1 (GLP-1), среди прочего, секретируются тонким кишечником в ответ. к приему пищи и подавить прием пищи. Моторные и гуморальные механизмы желудка и тонкого кишечника, лежащие в основе нормального опорожнения желудка у людей, сложны и сильно варьируются: проглоченная пища должна храниться, смешиваться с пищеварительными ферментами, измельчаться на мелкие частицы и доставляться в жидкой форме в двенадцатиперстную кишку со скоростью, равной обеспечивает эффективное переваривание и всасывание.
Внутрижелудочные механизмы, снижающие потребление энергии, включают замедленную скорость опорожнения желудка, т. Е. Вывод питательных веществ из желудка с общей скоростью 1–4 ккал / мин независимо от объема у молодых людей (Meyer et al., 1981; Brener et al. al., 1983; Horowitz et al., 1994; Gentilcore et al., 2006), повышенное растяжение антрального отдела (Sturm et al., 2004; Gentilcore et al., 2006) и ингибирование концентрации грелина в плазме (Sturm et al. , 2003; Bowen et al., 2006; Pilichiewicz et al., 2007a).Потребление энергии обратно пропорционально площади антрального отдела и непосредственно концентрации грелина в плазме (Jones et al., 1997; Sturm et al., 2004; Bowen et al., 2006).
Механизмы тонкого кишечника очень чувствительны к потребляемым питательным веществам, и небольшие количества питательных веществ, доставляемые непосредственно в тонкий кишечник, обладают способностью снижать аппетит и потребление энергии, что связано с подавлением перистальтики антрального отдела и усилением перистальтики пилорического отдела (Brennan et al., 2008), что приводит к замедлению опорожнения желудка и стимуляции секреции гормонов кишечника (т.е., CCK, GLP-1, PYY и желудочный ингибирующий пептид или GIP) (Jones et al., 1997; Pilichiewicz et al., 2007a, b) и подавление грелина (Pilichiewicz et al., 2007a, b ). Было показано, что аппетит и потребление энергии обратно пропорциональны CCK в плазме (Bowen et al., 2006) и GLP-1 (Lejeune et al., 2006), а также количеству изолированных волн пилорического давления (Brennan et al., 2008 г.).
Клинические последствия рутинной биопсии антрального отдела желудка и тела
Биопсия слизистой оболочки желудка при диагностической эндоскопии дает информацию, которую невозможно получить другими способами.Наиболее частым показанием к биопсии желудка является необходимость знать, инфицирован ли пациент Helicobacter pylori и есть ли в желудке гастрит. Микроскопическое исследование образцов биопсии желудка, помимо статуса H. pylori, дает информацию о степени, степени и топографии связанных с гастритом и атрофией поражений желудка. Эта информация предоставляет дополнительные возможности для оценки риска и вероятности различных желудочных расстройств.К ним относятся: а) Преобладание или ограничение гастрита, связанного с H. pylori, в антральном отделе сильно коррелирует с повышенным риском язвенной болезни и, в частности, язвы двенадцатиперстной кишки (фенотип гастрита с язвой двенадцатиперстной кишки). б) Наличие атрофического гастрита (потеря нормальных желез) в области тела желудка указывает на низкий риск язвы, а также на снижение способности пациента выделять кислоту. c) Возникновение далеко зашедшего атрофического гастрита и кишечной метаплазии с множеством очагов в желудке (продвинутый мультифокальный атрофический гастрит), в частности, в области малой кривизны и угловой вырезки, являются признаками, указывающими на повышенный риск новообразований желудка (фенотип гастрита при раке желудка). ).г) Наличие нормальной и здоровой слизистой оболочки желудка указывает, с другой стороны, на чрезвычайно низкий риск как язвенной болезни, так и рака желудка. Помимо диагностики гастритных поражений, связанных с H. pylori, обычная биопсия желудка может выявить результаты, которые указывают на особые формы гастрита, такие как эозинофильный, лимфоцитарный, реактивный или гранулематозный гастрит (например, гастрит Крона) или гастрит Helicobacter heilmannii. Эти типы гастрита могут быть случайно обнаружены у небольшого процента пациентов, которые проходят диагностическую гастроскопию по поводу жалоб со стороны брюшной полости.
Американский журнал рентгенологии Vol. 181, No. 4 (AJR)
| Введение | Выбирать К началу страницыАБРАКТЫВведение << Материалы и методыРезультатыОбсуждениеСсылкиЦИТУРА СТАТЬИ |
|---|
КТ имеет определенные существенные преимущества перед люминальными исследованиями из-за его способности выявлять интра- и экстрамуральные аспекты стенки кишечника.То есть утолщение стенки на КТ является важным, хотя и неспецифическим, индикатором заболевания пищеварительного тракта. Распространенной ошибкой при КТ-диагностике аномального утолщения стенки является недостаточное растяжение просвета, особенно желудка. Некоторые источники предлагают 5 мм в качестве порогового значения для аномального утолщения стенки желудка, предполагая надлежащее растяжение. Однако мы обычно наблюдаем заметное утолщение стенки дистального отдела антрального отдела желудка на мультидетекторной компьютерной томографии (MDCT), которое часто превышает 5 мм, даже в условиях адекватного растяжения.Чтобы не рекомендовать ненужную эндоскопию пациентам, у которых нет никаких признаков заболевания желудка, мы попытались установить диапазон нормальных результатов антрального отдела желудка при МДКТ. Мы также предлагаем объяснение этого утолщения на основе предыдущих наблюдений за анатомией и физиологией желудка.
| Материалы и методы | Выбирать К началу страницыАБРАКТЫВведениеМатериалы и методы << РезультатыОбсуждениеСсылки ЦИТИРУЮЩИЕ СТАТЬИ |
|---|
Были ретроспективно проанализированы результаты МДКТ-сканирования с контрастированием 153 последовательных взрослых пациентов без известных или подозреваемых заболеваний желудка.Критерии исключения включали клинический анамнез или результаты MDCT злокачественных новообразований верхних отделов брюшной полости, хирургического вмешательства или воспалительного процесса. Пациенты, которые не получали пероральный и внутривенный контрастный материал, также были исключены. Средний возраст исследуемой группы составлял 53,1 года (от 19 до 86 лет). Из 153 пациентов 101 мужчина и 52 женщины.
Все исследования были выполнены на сканере MDCT (LightSpeed, General Electric Medical Systems, Милуоки, Висконсин) после введения перорального и внутривенного контрастного вещества.Наш стандартный абдоминальный протокол включает 5-миллиметровую коллимацию, скорость стола 11,25 мм / сек и интервал реконструкции 5 мм. Наша стандартная схема внутривенного контрастирования состоит из 150 мл неионного контрастного вещества, вводимого со скоростью 3 мл / сек и 60-секундной задержкой сканирования. Наша стандартная схема перорального контрастирования состоит из 1000 мл водорастворимого контрастного вещества, потребляемого в течение 45–60 минут. Ни вода, ни шипучие кристаллы обычно не используются, но используются время от времени.
Измерения в электронном виде антрального отдела желудка во время фазы воротной вены с увеличением в реальном размере (т.е. в натуральную величину) выполнялись в аксиальной плоскости на диагностической рабочей станции с помощью электронных штангенциркулей. Два рецензента выполнили все измерения, и разногласия были разрешены на основе единодушного мнения. Передние и задние антральные измерения проводились в средней части относительного утолщения стенки — вдали от привратника и исключая складки морщин. Также были приняты меры, чтобы избежать участков большей или меньшей кривой, которые могли бы привести к псевдозатуханию из-за наклонного измерения.Было получено аналогичное репрезентативное измерение передней стенки проксимального отдела тела желудка. Независимое тело желудка было выбрано для сравнения по дну и кардии, чтобы свести к минимуму частоту псевдозаготовок из-за плохого вздутия живота. Значения SD были получены для всех измерений стенки желудка.
Также были оценены морфологические характеристики и характеристики ослабления антральной стенки. Оценивались морфологические особенности: гладкий или неправильный контур, концентрическое или эксцентрическое утолщение, а также предполагаемая продольная протяженность утолщения.Помимо субъективной оценки, эксцентрическое утолщение определялось как толщина одной антральной стенки (передней или задней) менее 50% от другой. Если подслизистая линейная слабая аттенюация (настенная исчерченность) была очевидна при МДКТ, регистрировались значения ослабления в области низкого ослабления. Растяжение антрального отдела было субъективно оценено по 4-балльной шкале, при этом оценки от 1 до 4 примерно указывали на 0–25%, 26–50%, 51–75% и 76–100% воспринимаемого растяжения соответственно.
Обзор медицинских карт показал, что 10 (7%) из 153 пациентов прошли эндоскопию верхних отделов тканей в течение 8 месяцев после обследования MDCT (средний интервал 3.3 месяца). Эндоскопия не проводилась при подозрении на антральное заболевание ни у одного из этих пациентов. Показаниями к выполнению верхней эндоскопии были заболевание пищевода у пяти пациентов (дисфагия у двух, гастроэзофагеальная рефлюксная болезнь у двух и скрининг на варикозное расширение вен пищевода у одного), чрескожная эндоскопическая гастростомия у двух пациентов, анемия у двух пациентов и стойкая тошнота у одного пациента. Результаты эндоскопии у этих пациентов коррелировали с данными MDCT.
Три трупа без бальзамирования были вскрыты для дополнения результатов МДКТ in vivo.Перед вскрытием трупа было получено разрешение медицинского вуза. Все три пациента умерли от сердечно-легочных заболеваний, и ни у одного из них не было заболеваний желудка в анамнезе. У каждого трупа аккуратно иссекали весь желудок, не повреждая пилорическую область. Затем желудки были продольно разрезаны для оценки стенок тела желудка и антрального отдела желудка. Крупные образцы тканей, состоящие из полной толщины стенок, помещали в раствор формальдегида. Эти образцы позже были подготовлены для гистологической оценки со стандартным окрашиванием H и E.
Статистический анализ наших результатов проводился с использованием теста Стьюдента t . Значение p менее 0,05 считалось значимым. Были рассчитаны 95-процентные доверительные интервалы для средней толщины антрального отдела для каждой степени растяжения.
| Результаты | Выбирать К началу страницыАБРАКТЫВведениеМатериалы и методыРезультаты << ОбсуждениеСсылкиЦИТАЮЩИЕ СТАТЬИ |
|---|
Антральный отдел желудка, привратник и луковица двенадцатиперстной кишки были легко идентифицированы при МДКТ у каждого пациента.Гладкое утолщение стенки дистального отдела антрального отдела желудка относительно тела желудка наблюдалось у 152 (99%) из 153 пациентов. У оставшегося пациента присутствовало умеренное концентрическое утолщение антрального отдела желудка, но оно было меньше, чем передняя часть тела желудка. Утолщение антрального отдела распространялось на привратник у всех 153 пациентов и выглядело окружным у 147 пациентов (96%) (рис. 1, 2, 3) и эксцентрическим у шести пациентов (4%) (рис. 4A, 4B). Средняя толщина передней стенки антрального отдела составила 5,0 ± 1,9 мм. 5.2 ± 1,7 мм для задней стенки и 5,1 ± 1,6 мм в целом (диапазон 1,8–12,0 мм) (рис. 5). Разница в средней толщине передней и задней антральных стенок не была значимой. Средняя толщина передней стенки тела желудка, составляющая 2,0 ± 0,4 мм, была значительно меньше, чем толщина антрального отдела желудка ( p «0,0001).
| Увеличенная версия (203K) | Рис. 1. — Осевое мультидетекторное изображение КТ (МДКТ) с контрастным усилением у 36-летнего мужчины без желудочного заболевания показывает от легкой до умеренной равномерное концентрическое утолщение стенки с расширенным антральным отделом желудка ( наконечников стрелок, ).На этом изображении хорошо виден привратник и луковица двенадцатиперстной кишки. Такой вид антрального отдела желудка был наиболее частым при МДКТ. |
| Посмотреть увеличенную версию (183K) | Рис. сегментное утолщение окружной стенки ( стрелок, ) дистального отдела антрального отдела желудка. Обратите внимание на тонкостенное тело желудка ( стрелки ). |
| Увеличенная версия (183K) | Рис. 3. — Осевое мультидетекторное КТ-изображение с контрастным усилением у 65-летнего мужчины без желудочного заболевания показывает умеренную антральную стенку утолщение ( наконечников стрелок ) относительно тела желудка. Обратите внимание на линейное уменьшение подслизистого жира в области утолщения антрального отдела. |
| Посмотреть увеличенную версию (186K) | Рис.4А. — Преходящее асимметричное утолщение антральной стенки у 34-летнего мужчины без заболевания желудка. Осевое мультидетекторное КТ с контрастным усилением (MDCT) во время динамической фазы показывает асимметричное утолщение антральной стенки (, стрелка, ). Тонкое подслизистое слабое ослабление присутствует локально на привратнике или рядом с ним. Обратите внимание на тонкую стенку более проксимального отдела тела желудка ( стрелка ). |
| Посмотреть увеличенную версию (206K) | Рис.4Б. — Преходящее асимметричное утолщение антральной стенки у 34-летнего мужчины без заболевания желудка. Аксиальное МДКТ-изображение с контрастным усилением во время отсроченной фазы показывает разрешение асимметричного утолщения антрального отдела ( коротких стрелок ), оставляя только умеренное равномерное утолщение относительно проксимального отдела тела желудка ( длинная стрелка ). |
| Посмотреть увеличенную версию (18K) | Рис. 5. — Гистограмма показывает распределение измерений передних ( белых полос, ) и задних ( черных полос ) ) толщины антральной стенки на мультидетекторной компьютерной томографии у 153 последовательных пациентов без заболевания желудка. |
По крайней мере, одно из двух антральных измерений (переднее или заднее) превысило 5 мм у 85 пациентов (56%) и 10 мм у семи пациентов (5%). У четырех пациентов оба антральных измерения были менее 3 мм, но каждое из этих измерений было толще тела желудка. Передние и задние измерения были в пределах 1 и 3 мм друг от друга у 100 пациентов (65%) и 147 пациентов (96%) соответственно. Ни в одном случае оба антральных размера не были меньше 2 мм, но одна стенка была меньше 2 мм (1.8 или 1,9 мм) у трех пациентов. Не было очевидной корреляции между степенью утолщения антрального отдела и возрастом или полом пациента (среднее утолщение у мужчин по сравнению с женщинами, 5,1 против 4,9 мм; p = 0,4). Размер тела желудка превысил 3 мм только у трех пациентов (2%). Хотя это и не было измерено, стенка луковицы двенадцатиперстной кишки была заметно тоньше, чем прилегающий антральный отдел желудка почти у каждого пациента, и никогда не казалась толще (рис. 1 и 4A, 4B).
Предполагаемая средняя продольная протяженность утолщения антральной стенки составила 4.6 ± 1,1 см. Продольное поражение варьировалось от утолщения относительно длинного сегмента, который постепенно сужается (рис. 6A, 6B, 6C), до утолщения короткого сегмента с более резким окончанием (рис. 2). Расширение просвета антрального отдела желудка на MDCT считалось 1-й степенью (наименее растянутым) у 65 пациентов, 2-й степенью — 22 пациентами, 3-й степенью — 37 пациентов и 4-й степенью — 29 пациентами. Средняя толщина стенки антрального отдела при растяжении 1, 2, 3 и 4 степени составила 6,9, 5,1, 4,9 и 4,0 мм соответственно (рис.7). Разница в утолщении антрального отдела между каждой группой была статистически значимой ( p <0,001), за исключением сравнения растяжения 2 и 3 степени ( p = 0,58).
| Увеличенная версия (184K) | Рис. 6A. — На изображениях показано влияние степени растяжения просвета на появление концентрических длинных сегментов антрального утолщения у 62-летней женщины без заболевания желудка. Осевое мультидетекторное КТ с контрастным усилением (MDCT) во время динамической фазы показывает концентрическое утолщение антрального отдела ( стрелок, ) с умеренным растяжением просвета.Обратите внимание на заметное яркое усиление слизистой оболочки при использовании воды в качестве перорального контрастного вещества, которое может быть скрыто положительным пероральным контрастным материалом. |
| Увеличенная версия (174K) | Рис. 6B. — На изображениях показано влияние степени растяжения просвета на появление концентрических длинных сегментов антрального утолщения у 62-летней женщины без заболевания желудка. Осевое МДКТ-изображение с контрастным усилением во время отсроченной фазы показывает уменьшение растяжения просвета и дальнейшее увеличение утолщения антрального отдела ( стрелок ). |
| Посмотреть увеличенную версию (187K) | Рис. 6C. — На изображениях показано влияние степени растяжения просвета на появление концентрических длинных сегментов антрального утолщения у 62-летней женщины без заболевания желудка. Задержка аксиального изображения МДКТ с оптимальным растяжением и пациентом в положении пролежня после проглатывания шипучих кристаллов показывает уменьшенное, но стойкое утолщение антральной стенки ( стрелок ). |
| Увеличенная версия (8K) | Рис. 7. — График показывает среднюю толщину антральной стенки на мультидетекторном КТ в зависимости от степени растяжения просвета. Вздутие характеризовалось как 1 степень (наименьшая), 2, 3 или 4 (наибольшая). Столбцы указывают 95% доверительный интервал. • = степень 1, ▴ = степень 2, ▪ = степень 3, ♦ = степень 4. |
Интрамуральное низкое ослабление (настенная исчерченность) утолщенной части антрального отдела желудка было выявлено на MDCT у 36 (24%) из 153 пациентов (рис.3). В каждом случае настенной исчерченности область низкого затухания выглядела тонкой и линейной и ограничивалась подслизистой областью. Визуально незаметные случаи часто ограничивались непосредственной пилорической и препилорической областями (рис. 4A, 4B). Низкое ослабление подслизистой оболочки не наблюдалось в других частях желудка ни у одного пациента. Средняя толщина антральной стенки при наличии бороздки составила 5,6 мм по сравнению с 4,9 мм при ее отсутствии ( p = 0,045). Повторный отбор образцов с курсором вдоль области низкого ослабления подслизистой оболочки дал устойчиво отрицательное значение ослабления (единицы Хаунсфилда) у 14 (39%) из 36 пациентов.Отрицательные значения затухания указывали на отложение жира у этих пациентов, что дополнительно подтверждалось субъективной визуальной оценкой (рис. 3). Тонкая линейная геометрия области с низким затуханием не позволила разместить интересующую область для более точного определения затухания.
Верхняя эндоскопия, выполненная у 10 из 153 пациентов, не выявила признаков антрального воспаления, утолщения складок или других антральных аномалий ни у одного пациента. Средняя толщина антральной стенки на MDCT пациентов, перенесших эндоскопию, составила 4.6 мм.
В разрезе желудков трех трупов было обнаружено легкое, но заметное утолщение стенки дистального отдела антрального отдела желудка, которая доходила до привратника (рис. 8A, 8B, 8C). Точное измерение толщины стенки с помощью штангенциркуля оказалось затруднительным, но распределение утолщения антрального отдела было похоже на типичные результаты МДКТ с точки зрения продольной протяженности и периферического поражения. Гистологическое исследование образцов на полную толщину стенки из дистального отдела антрального отдела желудка и проксимального отдела тела желудка показало, что это статическое увеличение толщины антральной стенки в первую очередь является результатом основных различий в собственной мышечной мышце (рис.8A, 8B, 8C). Приблизительное соотношение толщины стенки антрального отдела к толщине стенки тела было обычно менее 2: 1 для трупных образцов, что меньше отношения 2,6: 1 для средней толщины (5,1 мм: 2,0 мм), наблюдаемой in vivo на МДКТ. Возможные причины такого несоответствия обсуждаются в следующем разделе этой статьи.
| Увеличенная версия (153K) | Рис. 8A. — Оценка желудка на основе вскрытия трупа 85-летней женщины, умершей от сердечно-легочной болезни и не страдающей желудочными заболеваниями.Фотография дистального отдела антрального отдела желудка и привратника после продольного разреза показывает легкое утолщение стенки дистального отдела антрального отдела желудка ( стрелок, ), ведущее к привратнику ( стрелок, ). Стенка тела желудка заметно тоньше (не показано). |
| Увеличенная версия (156K) | Рис. 8B. — Оценка желудка на основе вскрытия трупа 85-летней женщины, умершей от сердечно-легочной болезни и не страдающей желудочными заболеваниями.Микрофотографии с малым увеличением гистологических срезов передней стенки дистального отдела антрального отдела желудка ( B ) и проксимального отдела тела желудка ( C ) при одинаковом увеличении показывают, что относительное утолщение антрального отдела в первую очередь вызвано различиями в круговом слое гладких мышц ( звездочек, ). ). (H и E, × 20) |
| Посмотреть увеличенную версию (186K) | Рис. 8C. — Оценка желудка на основе вскрытия трупа 85-летней женщины, умершей от сердечно-легочной болезни и не страдающей желудочными заболеваниями.Микрофотографии с малым увеличением гистологических срезов передней стенки дистального отдела антрального отдела желудка ( B ) и проксимального отдела тела желудка ( C ) при одинаковом увеличении показывают, что относительное утолщение антрального отдела в первую очередь вызвано различиями в круговом слое гладких мышц ( звездочек, ). ). (H и E, × 20) |
| Обсуждение | Выбирать К началу страницыАБРАКТЫВведениеМатериалы и методыРезультатыОбсуждение << СсылкиЦитирующие статьи |
|---|
На протяжении более 50 лет исследования бария использовались для оценки утолщения складок морщин в желудке [1, 2].Однако традиционные рентгенографические методы ограничены в их способности отображать фактическую толщину стенки желудка, потому что они в первую очередь представляют собой исследования просвета. Исследования с использованием традиционной компьютерной томографии, появившиеся в конце 1970-х — начале 1980-х годов, показали, что компьютерная томография полезна для более прямой оценки стенки желудка [3–6]. Несмотря на преимущества КТ, надежное различие между аномальным и нормальным утолщением стенки на КТ оказалось трудным.
Псевдозагущение желудка из-за неполного вздутия — хорошо известное явление, особенно в области пищеводно-желудочного перехода.Однако большинство источников утверждают, что при достаточно растянутом желудке толщина стенки желудка не должна превышать 5 мм [7–10]. Наши результаты показывают, что, хотя это ограничение подходит для тела желудка, оно часто не подходит для дистального отдела антрального отдела желудка. Хотя большинство радиологов, интерпретирующих КТ брюшной полости, вероятно, полагают, что такая степень утолщения антрального отдела является нормальным явлением, в литературе имеется на удивление мало доказательств, подтверждающих это предположение. Более ранние исследования с использованием традиционной компьютерной томографии объясняли это очевидное утолщение антрального отдела артефактами, связанными с участком сканирования, поскольку изображения обычно получали с 10-миллиметровой коллимацией, а иногда — с 20-миллиметровыми интервалами [3].Грубое псевдозаготовление, связанное с артефактами движения или косым разрезом антрального отдела желудка, существенно уменьшается или устраняется с помощью КТ с одним детектором и МДКТ из-за более быстрого сканирования; более тонкие секции; и отображение непрерывных или даже перекрывающихся изображений. Несмотря на это снижение грубого псевдозернистого утолщения, мы неофициально отметили высокую частоту заметного утолщения антрального отдела на снимках МДКТ у пациентов без подозрения на заболевание желудка, что послужило мотивацией для проведения нашего исследования.По нашему опыту, дальнейшее диагностическое обследование этих пациентов, включая эндоскопию, обычно дает отрицательные результаты.
Наши результаты показывают, что относительное утолщение стенки дистального отдела антрального отдела желудка по сравнению с проксимальным отделом желудка при МДКТ является нормальным явлением. В нашей исследуемой группе пациентов без подозрения на заболевание желудка толщина антрального отдела в среднем составляла 5,1 мм, измерялась более 5 мм у большинства пациентов и составляла 10–12 мм у 5% пациентов. Для сравнения, толщина стенки независимого тела желудка в среднем составляла всего 2.0 мм и превышал 3,0 мм только у 2% пациентов. Таким образом, нормальная толщина стенки желудка является локальным измерением: порог в 5 мм кажется подходящим для сильно растянутого тела желудка, но не для дистального отдела антрального отдела желудка. Более того, использование простого линейного КТ в качестве единственного диагностического критерия желудочного заболевания недостаточно; Также необходимо учитывать морфологическую оценку однородности стенок и статического утолщения по сравнению с динамическим.
Мы также показали, что, хотя неполное растяжение имеет измеримое влияние на толщину антральной стенки, это не единственный фактор.Кроме того, позиционирование, по-видимому, влияет на утолщение антральной стенки меньше, чем остальная часть желудка, потому что средняя толщина зависимой задней стенки существенно не отличалась от независимой передней стенки (5,2 против 5,0 мм). В отличие от наблюдений, описанных для проксимального отдела желудка [10], утолщение подлежащей стенки в антральной области может сохраняться, несмотря на правильное растяжение и независимое расположение (Рис. 6A, 6B, 6C).
Утолщение антральной стенки, видимое на MDCT, возможно, лучше всего объясняется как статическими, так и динамическими компонентами.Основным статическим или анатомическим фактором утолщения антральной стенки является увеличенная мышечная оболочка. Анатомические исследования показали, что гладкие мышцы желудка, особенно круговой слой, толще и плотнее вокруг антрального отдела желудка, чем вокруг остальной части желудка [11]. Наши макроскопические и гистологические результаты вскрытия трупа подтверждают это наблюдение (рис. 8A, 8B, 8C). Однако это лежащее в основе мышечное утолщение, которое способствует продвижению антральной роли измельчения [12, 13], не является единственным фактором утолщения антральной стенки, наблюдаемого на МДКТ.
Динамические или физиологические факторы, способствующие утолщению антрального отдела, более сложны. Мы показали, что неполное вздутие — это один из факторов. Однако перистальтика желудка и возникающие в результате антральные сокращения, вероятно, не менее важны. В то время как дно желудка и проксимальный отдел желудка в основном служат пассивным резервуаром, дистальный желудок более электрически активен, генерируя интенсивные перистальтические сокращения со скоростью примерно три цикла в минуту [14]. Эти антральные сокращения можно легко наблюдать при обследовании желудка в реальном времени, например, при эндоскопии или сонографии (рис.9A, 9B, 9C). Периодические антральные сокращения также, вероятно, способствуют дополнительному утолщению (концентрическому и эксцентрическому), наблюдаемому у некоторых пациентов на MDCT, о чем свидетельствуют временные изменения, наблюдаемые в отдельных сериях (рис. 4A, 4B). Утолщение дистального отдела антрального отдела желудка, которое развивается во время сокращения при ультразвуковом исследовании, сильно напоминает утолщение коротких сегментов, наблюдаемое на MDCT у некоторых пациентов, как показано при сравнении рисунков 2 и 9A, 9B, 9C. Эти динамические события, возможно, более эффективно фиксируются на MDCT, чем на обычном компьютерном томографе, из-за более быстрого сканирования.
| Увеличенная версия (155K) | Рис. 9A. — Сонографическая картина сокращения нормального антрального отдела желудка у 34-летнего мужчины без заболевания желудка. Первоначальное поперечное сонографическое изображение наполненного водой желудка показывает хорошее расширение просвета дистального отдела антрального отдела желудка (, звездочка, ) и умеренное утолщение стенок ( стрелки, ). Обратите внимание на сходство этого изображения с рисунком 1. |
| Посмотреть увеличенную версию (153K) | Рис.9B. — Сонографическая картина сокращения нормального антрального отдела желудка у 34-летнего мужчины без заболевания желудка. Последовательные сонографические изображения показывают прогрессирующее сужение просвета и утолщение стенки дистального отдела антрального отдела желудка ( стрелок , C ) в результате активного сокращения. Обратите внимание на сходство C с рисунком 2. |
| Посмотреть увеличенную версию (163K) | Рис. 9C. — Сонографическая картина сокращения нормального антрального отдела желудка у 34-летнего мужчины без заболевания желудка.Последовательные сонографические изображения показывают прогрессирующее сужение просвета и утолщение стенки дистального отдела антрального отдела желудка ( стрелок , C ) в результате активного сокращения. Обратите внимание на сходство C с рисунком 2. |
Относительно высокая распространенность (24%) линейной подслизистой оболочки с низким затуханием или настенной бороздки в области утолщения антрального отдела поначалу нас удивила. Присутствие отрицательных значений затухания в значительном проценте этих случаев предполагает отложение подслизистого жира как причину появления полос на стенке.Хотя средняя толщина антрального отдела была немного больше у пациентов с настенной исчерченностью, разница имела лишь пограничное значение. Подобное появление подслизистого отложения жира из-за воспалительных состояний кишечника было хорошо документировано на КТ прямой кишки, толстой и тонкой кишки [15, 16]. Хотя настенная бороздка в антральном отделе желудка на MDCT может свидетельствовать о хроническом или субклиническом воспалении, необходимы дальнейшие исследования, прежде чем можно будет сделать твердые выводы о его причине или значении.Однако, основываясь на наших выводах, само по себе его присутствие не должно вызывать беспокойства по поводу клинического заболевания и, вероятно, исключает значительный инфильтративный процесс слизистой или подслизистой оболочки.
Учитывая высокую частоту нормального утолщения антральной стенки на МКТ, когда следует считать утолщение антральной стенки ненормальным? Если используется порог 10 мм, положительная прогностическая ценность, вероятно, будет низкой, потому что мы встречали это значение у 5% наших пациентов без подозрения на заболевание. Толщина антральной стенки в нашей серии никогда не превышала 12 мм.Это открытие предполагает, что 12 мм может быть более подходящим порогом. Однако жизненно важно не применять линейку просто изолированно без учета других факторов, таких как степень растяжения просвета и морфологические особенности. Эксцентрическое утолщение антрального отдела было замечено только у 4% пациентов в нашей серии. Хотя каждый случай утолщения эксцентрической стенки считался гладким, трудно исключить истинное заболевание, если это проявление сохраняется в отдельных сериях. Обширное периферическое утолщение также следует рассматривать с подозрением, если оно кажется жестким или неровным, особенно если оно не изменилось с течением времени.Помимо этих ситуаций, наши результаты показывают, что нерегулярное или эксцентрическое утолщение антрального отдела, превышающее 12 мм на КТ, следует рассматривать как ненормальное.
Дифференциальная диагностика аномального утолщения антральной стенки включает широкий спектр воспалительных, неопластических, инфильтративных и других состояний [17]. Гастрит, вызванный Helicobacter pylori , может присутствовать почти у 50% американцев старше 60 лет [2]. Согласно одному исследованию, наиболее частое проявление КТ H.pylori гастрит — это выраженное периферическое утолщение антральной стенки, в среднем 1,5–2,0 см [18]. Другие причины гайморита включают нестероидные противовоспалительные препараты, атипичные инфекции (например, цитомегаловирус, туберкулез и сифилис), перигастральные воспалительные процессы, такие как панкреатит, прием едких веществ, синдром Золлингера-Эллисона, воспалительное заболевание кишечника, васкулит и хронические гранулематозные заболевания у детей [ 19–21]. Аденокарцинома желудка (рис. 10) и лимфома представляют собой наиболее частые злокачественные причины, при этом метастатическое заболевание встречается реже [21, 22].Редко утолщение антрального отдела может быть результатом инфильтративного процесса, такого как саркоидоз, амилоидоз или эозинофильный гастрит. И наоборот, некоторые причины утолщения стенки желудка, как правило, не затрагивают антральный отдел желудка, например болезнь Менетрие и варикозное расширение вен желудка.
| Увеличить (200K) | Рис. 10. — Аномальное утолщение антральной стенки у мужчины 44 лет с аденокарциномой желудка. Осевое изображение МДКТ с контрастным усилением показывает неравномерное эксцентрическое утолщение антральной стенки ( стрелок, ) с выступом.Впоследствии была доказана аденокарцинома желудка. |
Наше исследование имеет несколько ограничений. Мы официально не оценивали сканирование MDCT у пациентов с известным заболеванием желудка, например, с симптоматическим гастритом H. pylori . Однако целью нашего исследования было установить нормальный диапазон результатов МДКТ у пациентов без подозрения на антральное заболевание, чтобы избежать ненужных дальнейших исследований. Хотя слепое сравнение с аномальными случаями было бы полезно, оно выходило за рамки нашего исследования.Однако, учитывая высокую распространенность гастрита H. pylori , субклинический гастрит как причина утолщения антрального отдела у некоторых пациентов не может быть исключен. Еще одним ограничением было отсутствие эндоскопической корреляции в большинстве случаев. Однако это ограничение было ожидаемым, потому что у пациентов в нашей серии не было подозрений на желудочное заболевание и, следовательно, они также не были протестированы на H. pylori . Мы включили нормальные результаты эндоскопии в небольшую когорту из 10 пациентов, чтобы подтвердить, что утолщение антральной стенки, наблюдаемое на MDCT в нашей популяции, не было вызвано антральным воспалением или другим болезненным состоянием.Последним ограничением нашего исследования было то, что использование положительного перорального контрастного вещества могло привести к занижению результатов измерения стенки желудка у некоторых пациентов, поскольку прилегающая жидкость с высоким коэффициентом ослабления может скрыть усиливающуюся слизистую. Эта проблема не возникает, когда вода используется в качестве перорального контрастного вещества (рис. 6A, 6B, 6C).
В заключение, гладкое и равномерное утолщение стенки дистального отдела антрального отдела желудка по сравнению с проксимальным отделом желудка является нормальным обнаружением при МДКТ. Утолщение антральной стенки обычно превышает 5 мм, но может достигать 12 мм.Связанное с этим линейное низкое ослабление подслизистой оболочки (настенная исчерченность) является относительно частым признаком. Наши результаты визуализации в сочетании с предыдущими анатомическими и физиологическими наблюдениями предполагают, что нормальное утолщение антральной стенки, вероятно, вызвано анатомическим компонентом (утолщение мышц), которое может быть дополнительно усилено динамическими факторами (антральное сокращение и неполное растяжение). При отсутствии стойкой существенной неровности антральной стенки, асимметрии или утолщения (> 12 мм) на МКТР рекомендовать дальнейшее обследование, как правило, нет необходимости у пациентов без подозрения на заболевание желудка.
Гастрэктомия | Encyclopedia.com
Определение
Цель
Демографические данные
Описание
Диагноз / подготовка
Последующий уход
Риски
Нормальные результаты
Показатели заболеваемости и смертности
Альтернативы
Антрэктомия — это резекция или хирургическое удаление части желудка, известной как антральный отдел. Антральный отдел — это нижняя треть желудка, которая находится между телом желудка и пилорическим каналом, который впадает в первую часть тонкой кишки.Он также известен как антрум пилорикум или антрум желудка. Поскольку антрэктомия — это удаление части желудка, ее иногда называют частичной или субтотальной гастрэктомией .
Антрэктомия может выполняться для лечения нескольких различных заболеваний, влияющих на пищеварительную систему:
- Язвенная болезнь (ЯБ). Антрэктомия может быть сделана для лечения осложнений из-за язв, не поддающихся лечению. Эти осложнения включают неконтролируемое или повторяющееся кровотечение и препятствия, препятствующие проникновению пищи в тонкий кишечник.Поскольку антральный отдел производит гастрин, гормон, стимулирующий выработку желудочной кислоты, его удаление снижает уровень секреции кислоты в желудке.
- Рак пищеварительного тракта и близлежащих органов. Антрэктомия может выполняться не только для удаления злокачественной язвы желудка, но и для снятия давления на нижний конец желудка, вызванного раком поджелудочной железы, желчного пузыря или печени.
- Артериовенозные мальформации (АВМ) желудка. АВМ представляют собой скопления мелких кровеносных сосудов, которые могут развиваться в различных частях пищеварительной системы.АВМ могут вызывать кровотечение в желудочно-кишечном тракте, что приводит к рвоте с кровью (рвота с кровью) или мелене (черный или дегтеобразный стул, содержащий кровь). Тип АВМ, наиболее часто встречающийся в антральном отделе, известен как синдром желудочной антральной сосудистой эктазии (ГАВЭ). Расширенные кровеносные сосуды в GAVE образуют красноватые полосы на стенке антрального отдела, которые выглядят как полосы на арбузе.
- Обструкция выхода из желудка (GOO). GOO — это не отдельное заболевание или расстройство, а состояние, при котором желудок не может опорожняться из-за закупорки привратника.Примерно в 37% случаев причина непроходимости является доброкачественной — чаще всего ЯБ, камни в желчном пузыре, безоары или рубцы, вызванные приемом соляной кислоты или другого едкого вещества. Остальные 63% случаев вызваны раком поджелудочной железы, раком желудка или другими злокачественными новообразованиями, распространившимися на пищеварительный тракт.
- Проникающие огнестрельные или ножевые ранения, вызвавшие серьезные повреждения двенадцатиперстной кишки и поджелудочной железы. Антрэктомия может быть выполнена в качестве экстренной меры, когда кровеносные сосуды, кровоснабжающие двенадцатиперстную кишку, разрушены.
Язвенная болезнь (ЯБ) довольно распространена среди населения Соединенных Штатов. По данным Центров по контролю за заболеваниями (CDC), примерно у 10% всех американцев в какой-то момент жизни разовьется язва желудка или двенадцатиперстной кишки. Около четырех миллионов взрослых ежегодно диагностируются или проходят лечение от ЯБ; один миллион будет госпитализирован на лечение; и 40 000 перенесут операцию по поводу состояния, связанного с язвой. Около 6500 американцев умирают каждый год от осложнений, связанных с ЯБД.Ежегодные убытки экономики Соединенных Штатов от язвенной болезни оцениваются более чем в 6 миллиардов долларов.
Пептические язвы могут развиться в любом возрасте, но в США они очень редки у детей и редко у подростков. Язвы двенадцатиперстной кишки чаще всего развиваются у взрослых в возрасте от 30 до 50 лет, а язвы желудка — у лиц старше 60 лет. тело желудка.Его также называют антральным отделом желудка или привратником желудка.
Безоар— Скопление посторонних веществ, обычно волос или растительных волокон или их смеси, которые иногда могут попадать в желудок или кишечник и блокировать прохождение пищи.
Демпинг-синдром — Сложная физическая реакция на пищу, слишком быстро переходящую из желудка в тонкий кишечник, характеризующаяся потоотделением, тошнотой, спазмами в животе, головокружением и другими симптомами.
Двенадцатиперстная кишка — Первая часть тонкой кишки, расположенная между привратником и тощей кишкой.
Дисфагия — Затруднение или дискомфорт при глотании.
Эндоскопия — Техника осмотра желудка или пищевода с помощью гибкого инструмента, содержащего на одном конце свет и миниатюрную видеокамеру.
Гастрин— Гормон, вырабатываемый клетками антрального отдела желудка, который стимулирует выработку желудочной кислоты.
Гастроэнтерология— Раздел медицины, специализирующийся на диагностике и лечении заболеваний желудка и кишечника.
Helicobacter pylori — Спиралевидная бактерия, которая была обнаружена в 1982 году как основная причина большинства язв желудка и двенадцатиперстной кишки.
Гематемезис— Рвота с кровью.
Melena— Стул черноватого цвета, содержащий пигменты крови или частично переваренную кровь.
Нестероидные противовоспалительные препараты (НПВП) — Термин, используемый для группы анальгетиков, которые часто назначают пациентам с артритом.Считается, что около 20% пептических язв вызваны частым применением НПВП.
Перфорация— Открытие или отверстие в тканях желудка, вызванное болезненным процессом.
Привратник — Отверстие в нижнем конце желудка, окруженное связкой мышц. Содержимое желудка перекачивается в двенадцатиперстную кишку через привратник.
Резекция — Удаление органа или структуры. Антрэктомия — это резекция антрального отдела.
Ваготомия — Перерезание или рассечение различных частей блуждающего нерва, кровоснабжающего желудок. Для уменьшения секреции кислоты проводится ваготомия.
Арбузный желудок — Тип артериовенозной мальформации (АВМ), развивающейся в антральном отделе. Расширенные кровеносные сосуды в АВМ напоминают полоски арбуза. Арбузный желудок также известен как сосудистая эктазия антрального отдела желудка или синдром GAVE.
Язвы двенадцатиперстной кишки чаще встречаются у мужчин, а язвы желудка — у женщин.К другим факторам риска ЯБ относятся тяжелое курение и семейная история язвы двенадцатиперстной кишки или желудка.
GAVE, или арбузный желудок, является очень редкой причиной желудочно-кишечного кровотечения, которое было впервые обнаружено в 1952 году. Оно было связано с такими заболеваниями, как склеродермия, цирроз печени, семейная средиземноморская лихорадка и болезни сердца. GAVE поражает женщин чуть более чем в два раза чаще, чем мужчин. Почти всегда встречается у пожилых людей; средний возраст постановки диагноза составляет 73 года у женщин и 68 лет у мужчин.
Рак желудка — 14-й по распространенности тип злокачественной опухоли в США; однако это происходит гораздо чаще в Японии и других частях Азии, чем в Западной Европе и Северной Америке. Около 24 000 человек в Соединенных Штатах ежегодно диагностируют рак желудка. Факторы риска его развития включают инфицирование слизистой оболочки желудка Helicobacter pylori; Американцы азиатского, латиноамериканского или афроамериканского происхождения; возраст 60 лет и старше; тяжелое курение; история злокачественной анемии; и диета с большим содержанием сухой соленой пищи.У мужчин больше шансов заболеть раком желудка, чем у женщин. Некоторые врачи считают, что воздействие определенных токсичных химикатов на рабочем месте также является фактором риска рака желудка.
В настоящее время почти все антрэктомии выполняются в виде открытых процедур, что означает, что они выполняются через большой разрез в брюшной полости пациента под общим наркозом. После анестезии пациента помещают мочевой катетер для контроля диуреза и вводят назогастральный зонд.После очистки живота пациента антисептиком хирург делает большой разрез от грудной клетки пациента до пупка. После отделения вышележащих слоев ткани хирург обнажает желудок. Один зажим помещается на нижнем конце, а другой зажим несколько выше, отделяя нижнюю треть живота. Режущий степлер можно использовать для удаления нижней трети (антрального отдела) и прикрепления верхней части желудка к тонкой кишке. После присоединения желудка и кишечника область промывают физиологическим раствором и разрез закрывают.
Большинство антрэктомий выполняется вместе с ваготомией . Это процедура, при которой хирург перерезает различные ветви блуждающего нерва, по которому от мозга к желудку передаются сообщения о выделении большего количества желудочной кислоты. Хирург может выбрать выполнение выборочной ваготомии, чтобы отключить ветви нерва, которые регулируют секрецию желудка, без перерезания ветвей, контролирующих опорожнение желудка.
Некоторые хирурги выполняли антрэктомию с помощью лапароскопа, что является менее инвазивным типом хирургии.Однако по состоянию на 2003 год этот метод все еще считается экспериментальным.
Диагноз
Диагностика ЯБ и других заболеваний желудка начинается с сбора анамнеза пациента, включая семейный анамнез. Во многих случаях лечащий врач пациента назначает анализы, чтобы сузить диагноз. Если пациент старше или недавно сильно похудел, врач рассмотрит возможность рака желудка. Если в анамнезе есть язвы двенадцатиперстной кишки или желудка в семье пациента, врач может задать вопросы о типе дискомфорта, который испытывает пациент.Боль, связанная с язвой двенадцатиперстной кишки, часто возникает ночью, уменьшается во время еды, но снова появляется через два-три часа после еды. С другой стороны, боль при язве желудка может усиливаться от еды и сопровождаться тошнотой и рвотой. Рвота, повторяющаяся вскоре после еды, указывает на непроходимость желудка.
Наиболее распространенными диагностическими тестами при заболеваниях желудка являются:
- Эндоскопия. Эндоскоп — это тонкая гибкая трубка с источником света и видеокамерой на одном конце, которую можно пропустить через рот и горло, чтобы посмотреть на внутреннюю часть верхних отделов пищеварительного тракта.Видеокамера, прикрепленная к эндоскопу, проецирует изображения на экран компьютера, что позволяет врачу видеть язвы, разрастания тканей и другие возможные проблемы. Эндоскоп можно использовать для сбора клеток ткани для цитологического анализа или небольшого образца ткани для биопсии. Биопсия ткани может использоваться для проверки наличия Helicobacter pylori, спиральной бактерии, которая была обнаружена в 1982 году как основная причина большинства язв желудка, а также для проверки на рак. Эндоскопия — один из самых эффективных тестов для диагностики АВМ.
- Рентгенография верхних отделов желудочно-кишечного тракта с двойным контрастированием с барием. Этот тест иногда называют серией верхних отделов желудочно-кишечного тракта. Пациенту назначают внутрь жидкую форму бария. Барий покрывает ткани, выстилающие пищевод, желудок и тонкий кишечник, что позволяет их более четко видеть на рентгеновском снимке. Радиолог также может наблюдать за движением бария по пищеварительной системе, чтобы определить местонахождение засоров.
- Дыхательный тест с уреазой. Этот тест можно использовать для мониторинга эффективности лечения язвы, а также для диагностики присутствия H.pylori . Пациенту вводят мочевину, меченную углеродом 13-C или 14-C. H. pylori производит уреазу, которая расщепляет мочевину в исследуемой дозе до аммиака и диоксида углерода, содержащего меченый углерод. Затем в дыхании пациента можно обнаружить углекислый газ, содержащий меченый углерод.
Preparation
Подготовка к антрэктомии требует проведения анализов для оценки общего состояния здоровья пациента и его пригодности к операции. Эти тесты включают ЭКГ, рентген, анализы крови и анализ мочи.Пациенту предлагается прекратить прием аспирин и другие разжижающие кровь препараты примерно за неделю до операции. После полуночи вечера перед операцией нельзя принимать твердую пищу или жидкость.
В большинстве больниц пациенту перед операцией вводят успокаивающее средство либо внутривенно, либо путем инъекции. Общая анестезия проводится в операционной .
Последующий уход в больнице после антрэктомии аналогичен послеоперационному уходу при других операциях на брюшной полости, с точки зрения ухода за разрезами , обезболивающих и антибиотиков для минимизации риска инфекции.Восстановление в домашних условиях обычно занимает несколько недель. Примерно через шесть-восемь недель после операции пациенту проводят эндоскопическое обследование.
Самым важным аспектом реабилитации после антрэктомии является пристальное внимание к диете и привычкам питания. Примерно у 30% пациентов, перенесших антрэктомию или полную гастрэктомию, развивается так называемый демпинг-синдром. Синдром демпинга возникает из-за того, что пища слишком быстро выходит из желудка после еды и «сбрасывается» в тонкий кишечник. Есть два типа демпинг-синдрома: ранний и поздний.Ранний сброс происходит через 10–20 минут после еды и характеризуется ощущением тошноты, головокружения, потливости, учащенного сердцебиения, учащенного сердцебиения и спазмов в животе. Поздний сброс происходит через один-три часа после приема пищи с высоким содержанием углеводов и сопровождается чувством слабости, голода и спутанности сознания. Большинство пациентов могут справиться с демпинг-синдромом, если есть шесть небольших приемов пищи в день, а не три больших; выбирая продукты с высоким содержанием белка и низким содержанием углеводов; тщательно пережевывая пищу; и пить жидкости между приемами пищи, а не во время еды.
Помимо синдрома раннего или позднего сброса, другие риски, связанные с антрэктомией, включают:
- Диарея. Это осложнение чаще возникает у пациентов, перенесших ваготомию, а также антрэктомию.
- Похудание. Около 30-60% пациентов, перенесших комбинированную антрэктомию / ваготомию, теряют вес после операции. Самая частая причина похудания — сокращение приема пищи из-за меньшего размера желудка. Однако в некоторых случаях пациент теряет вес, потому что питательные вещества, содержащиеся в пище, не усваиваются организмом.
- Нарушение всасывания / недоедание. Железодефицитная анемия, дефицит фолиевой кислоты и потеря кальция иногда возникают после антрэктомии, поскольку желудочная кислота необходима для всасывания железа из пищи.
- Дисфагия. Дисфагия или дискомфорт при глотании может возникнуть после антрэктомии, когда пищеварительный сок из двенадцатиперстной кишки течет вверх в пищевод и раздражает его слизистую оболочку.
- Рецидив язвы желудка.
- Безоаровая формация. Безоары — это скопления инородных материалов (обычно растительных волокон или волос) в желудке, которые могут блокировать прохождение пищи в тонкий кишечник.Они могут развиться после антрэктомии, если пациент ест продукты с высоким содержанием растительной клетчатки или плохо их пережевывает.
Нормальные результаты антрэктомии зависят от причины операции. Антрэктомия, выполняемая для уменьшения секреции кислоты в ЯБ или для удаления предраковых тканей с целью предотвращения рака желудка, успешна более чем на 95%. Еще выше вероятность успеха при лечении арбузного желудка. Антрэктомия, выполняемая для лечения рака желудка или проникающей травмы живота, менее успешна, но этот результат связан с тяжестью заболевания или травмы пациента, а не с самой хирургической процедурой.
Смертность от антрэктомии, связанной с лечением язвы, составляет около 1-2%; для антрэктомий, связанных с раком желудка, 1-3%.
Частота осложнений, связанных с антрэктомией для лечения язвы:
- Рецидив язвы: 0,5–1%.
- Демпинг-синдромы: 25-30%.
- Диарея: 10%.
С 2003 года антрэктомия больше не является первой линией лечения язвенной болезни или GAVE. Обычно его назначают пациентам с рецидивирующим кровотечением или другими состояниями, такими как злокачественные новообразования, перфорация или непроходимость.
Хотя хирургическое вмешательство, включая антрэктомию, является наиболее распространенным методом лечения рака желудка, почти всегда необходимо сочетать его с химиотерапией, лучевой терапией или биологической терапией (иммунотерапией). Причина использования комбинации методов лечения заключается в том, что рак желудка редко обнаруживается на ранней стадии. Его первые симптомы часто легкие, и их легко принять за симптомы изжоги или желудочного вируса. В результате к моменту постановки диагноза рак часто распространился за пределы желудка.
Лекарство
Лечение пептических язв, вызванных H. pylori , в последние годы изменило свое внимание с снижения уровня кислотности в желудке на уничтожение бактерий. Поскольку ни один антибиотик не эффективен в лечении инфекций H. pylori , так называемая тройная терапия обычно состоит из комбинации одного или двух антибиотиков для уничтожения бактерии плюс лекарства для снижения выработки кислоты и третьего лекарства (обычно субсалицилата висмута). для защиты слизистой оболочки желудка.
Конкретные типы лекарств, которые используются как часть тройной терапии или для облегчения дискомфорта, включают:
- блокаторы h3. Они используются вместе с антибиотиками в тройной терапии для снижения секреции кислоты в желудке. Блокаторы h3 включают циметидин, ранитидин, фамотидин и низатидин. Некоторые из них продаются без рецепта.
- Ингибиторы протонной помпы. Эти лекарства включают такие препараты, как омепразол и лансопразол. Их дают, чтобы подавить выработку желудочного сока.
- Простагландины. Их назначают для лечения язв, вызванных группой обезболивающих, известных как НПВП. Простагландины защищают слизистую оболочку желудка, а также снижают секрецию кислоты. Самым известным лекарством из этой категории является мизопростол.
КТО ВЫПОЛНЯЕТ ПРОЦЕДУРУ И ГДЕ ЭТО ВЫПОЛНЯЕТСЯ?
Антрэктомия выполняется в стационаре. Обычно его проводит специалист по желудочно-кишечной хирургии или хирургической онкологии.
- Сукральфат.Сукральфат — это соединение сахарозы и алюминия, которое покрывает язвы защитным покрытием, которое позволяет заживать эродированным тканям.
- Антациды. Эти соединения доступны в виде таблеток или жидкостей, отпускаемых без рецепта.
- Субсалицилат висмута. Этот препарат, продаваемый без рецепта под торговым названием Пепто-Бисмол, обладает некоторой антибактериальной эффективностью против H. pylori , а также защищает слизистую оболочку желудка.
Эндоскопия
Эндоскопия может использоваться как для лечения, так и для диагностики.По состоянию на 2003 год используется около 10 различных методов лечения кровоточащих язв и АВМ с помощью эндоскопа; наиболее распространены инъекции адреналина или склерозирующего раствора; нанесение термозонда на область кровотечения; или использование лазера Nd: YAG для коагуляции открытых кровеносных сосудов. Желудок арбуза теперь чаще обрабатывают коагуляцией аргоноплазмы, чем антрэктомией. Однако рецидивирующие кровотечения возникают в 15-20% язв, леченных эндоскопическими методами.
Дополнительные и альтернативные (CAM) подходы
Дополнительные и альтернативные подходы, которые использовались для лечения язв желудка, связанных с PUD, включают акупунктуру, аюрведическую медицину и травяные препараты. Аюрведическая медицина, которая является традиционной медицинской системой Индии, классифицирует людей в соответствии с метаболическим типом телосложения. Считается, что люди, принадлежащие к типу питта, особенно склонны к язвам, и их лечат с помощью диеты, в которой упор делается на «охлаждающие» продукты, включая большое количество овощей.В японской медицине часто прописывают средства от язвы, приготовленные из солодки или буплевра. Западные травники рекомендуют препараты, содержащие фенхель, пажитник, вяз скользкий или корень алтея.
ВОПРОСЫ, КОТОРЫЕ ЗАДАТЬ ВРАЧУ
- Каковы альтернативы антрэктомии при моем состоянии? Что бы вы порекомендовали и почему?
- Сколько антрэктомий вы сделали?
- Насколько вероятно, что у меня разовьется демпинг-синдром, если у меня будет процедура?
- Что вы думаете о лапароскопической антрэктомии? Могу ли я участвовать в клиническом исследовании этой процедуры?
в дополнение к солодке для облегчения боли при язве желудка.
Ресурсы
КНИГИ
«Артериовенозные мальформации». В издании The Merck Manual of Diagnosis and Therapy, , под редакцией Марка Х. Бирса, доктора медицины, и Роберта Беркова, доктора медицины. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк, 1999.
Пеллетье, Кеннет Р., доктор медицины. Лучшая альтернативная медицина, Часть II, «CAM-терапия при определенных состояниях: язвы». Нью-Йорк: Simon & Schuster, 2002.
«Язвенная болезнь». В The Merck Manual of Diagnosis and Therapy, под редакцией Марка Х.Бирс, доктор медицины, и Роберт Берков, доктор медицины. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк, 1999.
Томсон, А. Б. Р. и Э. А. Шаффер. Первые принципы гастроэнтерологии, 3-е изд. Оквилл, Онтарио: Канадская ассоциация гастроэнтерологов, 2002.
ПЕРИОДИЧЕСКИЕ ДАННЫЕ
Appleyard, M. N. и C. P. Swain. «Эндоскопические трудности в диагностике кровотечений из верхних отделов желудочно-кишечного тракта». Всемирный журнал гастроэнтерологии 7 (2001): 308–12.
Бастид, С., С. Силке, К. Моллой и др. «Желудочная антральная сосудистая эктазия — причина рефрактерной анемии при системном склерозе». Ирландский медицинский журнал 94 (ноябрь-декабрь 2001 г.): 310.
Кастелланос, Андрес, доктор медицины, Барри Д. Манн, доктор медицины, и Джеймс де Кестекер, доктор медицинских наук. «Обструкция выхода из желудка». eMedicine, , 12 февраля 2002 г. [цитировано 27 апреля 2003 г.]. www.emedicine.com/med/topic2713.htm.
Де Кестекер, Джеймс, DO. «Кровотечение из верхних отделов желудочно-кишечного тракта: хирургическая перспектива.» eMedicine, 17 октября 2002 г. [цитировано 27 апреля 2003 г.]. www.emedicine.com/med/topic3566.htm.
Фаулер, Деннис, Мэриленд. «Лапароскопическая хирургия передней кишки: менее часто выполняемые процедуры». Информационный бюллетень Центра хирургии минимального доступа, Пресвитерианская больница Нью-Йорка 2 (зима 2002 г.): 7–10.
Комар, Александр Р., доктор медицины, и Прем Патель, доктор медицины. «Травма живота, проникающая». eMedicine, , 25 апреля 2002 г. [цитировано 28 апреля 2003 г.]. www.emedicine.com/med/topic2805.htm.
Пробст А., Р. Шойбель и М. Винбек. «Лечение арбузного желудка (синдром GAVE) с помощью эндоскопической аргоноплазменной коагуляции (APC): долгосрочный результат». Zeitschrift fur Gastroenterologie 39 (июнь 2001 г.): 447–52.
Штотцер, П. О., Р. Виллен и А. Ф. Киландер. «Арбузный желудок: не только антральная болезнь». Эндоскопия желудочно-кишечного тракта 55 (июнь 2002 г.): 897–900.
Ценг, Ю. Л., М. Х. Ву, М. Ю. Линь и В. В. Лай. «Ранняя хирургическая коррекция изолированной стриктуры желудка после травмы, вызванной кислотной коррозией.» Пищеварительная хирургия 19 (2002): 276–80.
Юсофф И., Ф. Бреннан, Д. Ормонд и Б. Лоуренс. «Коагуляция аргонной плазмы для лечения желудка арбуза». Эндоскопия 34 (май 2002 г.): 407–10.
Зарзаур Б. Л., Кудск К. А., Картер К. и др. «Стрессовые язвы, требующие радикального хирургического вмешательства после тяжелой травмы». Американский хирург 67 (сентябрь 2001 г.): 875–79.
ОРГАНИЗАЦИИ
Американская гастроэнтерологическая ассоциация (AGA).4930 Del Ray Avenue, Bethesda, MD 20814. (301) 654-2055. www.gastro.org.
Американское общество эндоскопии желудочно-кишечного тракта (ASGE). 1520 Kensington Road, Suite 202, Oak Brook, IL 60523 (630) 573-0600. www.asge.org.
Канадская ассоциация гастроэнтерологов (CAG). 2902 South Sheridan Way, Oakville, ON L6J 7L6 (888) 780-0007 или (905) 829-2504. www.cag-acg.org.
Центры по контролю и профилактике заболеваний (CDC). 1600 Clifton Road, Atlanta, GA 30333. (888) MY-ULCER или (404) 639-3534.www.cdc.gov.
Национальный институт рака (NCI). Справочная служба NCI, Suite 3036A, 6116 Executive Boulevard, MSC8332, Bethesda, MD 20892-8322. (800) 4-CANCER или (800) 332-8615 (TTY). www.nci.nih.gov.
Национальный информационный центр по заболеваниям пищеварительной системы (NDDIC). 2 Information Way, Bethesda, MD 20892-3570. www.niddk.nih.gov/health/digest/pubs.
ДРУГОЕ
Национальный институт рака (NCI). Запрос данных врача (PDQ). «Рак желудка: лечение», 2 января 2003 г. [цитировано 28 апреля 2003 г.].www.nci.nih.gov/cancerinfo/pdq/treatment/gastric/healthprofessional.
Национальный информационный центр по заболеваниям пищеварительной системы (NDDIC). «Что мне нужно знать о пептических язвах», , август 2002 г. [цитировано 28 апреля 2003 г.]. Публикация NIH № 02-5042. www.niddk.nih.gov/health/digest/pubs/pepticulcers/pepticulcers.htm.
Ребекка Фрей, Ph.D.
Анксиолитики см. Антиксиолитические препараты
Массовидное поражение Дьелафоя, связанное с распространенным раком желудка в антральном отделе желудка: клинический случай и обзор литературы | Диагностическая патология
DL был впервые описан Gallard в 1896 году и впоследствии более точно описан Жоржем Дьелафуа как «exulceratio simplex» в 1898 году [9].В наше время DL интерпретируется как врожденная аномалия, характеризующаяся аномально расширенными подслизистыми артериями без образования аневризмы или внутренней аномалии стенокардии. В отличие от нормального артериального роста, артерии DL остаются стабильно большого диаметра даже в дистальных отделах. Эти отличительные гистопатологические паттерны DL были описаны Leone et al. как «смесь артериальных и венозных аномалий» [1]. Текущий случай показал увеличенные и пролиферативные скопления сосудов с артериальной морфологией в подслизистой основе под областью опухоли, что согласуется с гистопатологической картиной DL.Большая часть DL (60%) возникает в проксимальном отделе желудка, на 6 см дистальнее пищеводно-сердечного перехода на малой кривизне, и снабжается левой желудочной артерией, отходящей от чревного ствола [7]. Двенадцать процентов DL расположены в дистальном отделе антрального отдела и питаются правой желудочной артерией или аномальным сосудистым анастомозом между левой и правой желудочными артериями по малой кривизне [8, 10]. В нашем случае поражение располагалось на передней стенке дистального отдела антрального отдела желудка и на кольце привратника рядом с малой кривизной.Это нетипичное расположение может создать диагностическую проблему для эндоскопистов. Осведомленность о возможных побочных эффектах во время биопсии и резекции слизистой оболочки, которые могут быть вызваны редким явлением DL, можно легко упустить.
Эндоскопия верхних отделов желудочно-кишечного тракта является основным методом диагностики DL и эффективна почти у 70% пациентов. DL обычно представляет собой мелкие пигментированные неглубокие протрузии с легкой эрозией и без изъязвлений при эндоскопии. Часто отмечается активное выделение или сочиться из дефекта слизистой оболочки диаметром менее 5 мм.Размер ДЛ составляет примерно 10-15 мм в ширину и 5-10 мм в высоту. Ангиография может помочь в локализации поражения, особенно в случае острого кровотечения [8]. Массовидное поражение и поражение сосочков DL в желудке и тонкой кишке было зарегистрировано только в двух случаях, и вместо этого они были клинически и радиологически диагностированы как подслизистые опухоли [11, 12]. В нашем случае при эндоскопии опухоль представляла собой бляшечное образование с неглубокими изъязвлениями и изменениями слизистой оболочки, аналогичными типичной карциноме желудка, однако консистенция опухоли была мягкой и рыхлой.Дифференциальный диагноз при эндоскопии включал запущенную карциному желудка и лимфому желудка. Эта гибридная эндоскопическая находка предполагает диагноз массоподобной ДЛ.
Связь между DL и раком желудка полностью не выяснена. Taketsuka et al. предположили, что повторяющиеся эрозии и язвы на слизистой оболочке могут быть вызваны нарушением кровообращения в сосудах DL, а активная регенерация и дисплазия могут дополнительно способствовать процессу канцерогенеза. Эта гипотеза согласуется с феноменом того, что DL располагалась под раковым поражением во всех описанных случаях [4].Тем не менее, прогноз пациентов с раком желудка, сочетающимся с ДЛ, в основном зависит от патологической стадии рака желудка.
Дифференциальный диагноз этого случая включал эктазию сосудов антрального отдела желудка (GAVE) и портальную гипертензивную гастропатию. GAVE составляет до 4% всех кровотечений из верхних отделов желудочно-кишечного тракта, не связанных с варикозными расширениями, и часто ассоциируется с атрофическим гастритом и пернициозной анемией, которые являются известными факторами риска злокачественных новообразований желудка [13]. Однако сообщается, что какая-либо связь между GAVE и раком желудка встречается редко [14].Диагностированные пациенты — это преимущественно пожилые женщины со средним возрастом 73 года, и они обычно связаны с основными хроническими заболеваниями, особенно циррозом (30%) и аутоиммунными заболеваниями (62%) [15]. Характерной эндоскопической находкой является «арбузный желудок» — чередование гиперемированных полосок с нормальной слизистой оболочкой, спицеподобной радиацией от привратника к антральному отделу. Характерные гистологические картины GAVE включают расширенные капилляры и фиброзно-мышечную гиперплазию собственной пластинки, внутрисосудистые фибриновые тромбы и увеличение средней площади поперечного сечения просвета в сосудах слизистой оболочки, чего не наблюдалось в нашем случае.Другой дифференциальный диагноз — портальная гипертензивная гастропатия, обычно более выраженная на глазном дне или теле и связанная с циррозом печени.
Этот случай подчеркивает возможность сосуществования массово-подобной ДЛ и прогрессирующей аденокарциномы желудка в дистальном отделе антрального отдела. Кроме того, наш случай предупреждает эндоскопистов о риске сильного кровотечения из-за этого необычного проявления, учитывая недавние предпочтения в использовании эндоскопических методов перед хирургической резекцией для лечения ДЛ.
Значение утолщения стенки желудка, обнаруженное при КТ брюшной полости для прогнозирования злокачественного новообразования желудка
Предпосылки . Ранняя диагностика рака желудка — один из важнейших параметров, влияющих на выживаемость заболевания. В этом исследовании мы стремились подчеркнуть важность толщины стенки антрального отдела при компьютерной томографии. Метод . В исследование были включены 111 пациентов в возрасте от 18 до 95 лет, у которых было утолщение антральной стенки при компьютерной томографии, а также было выполнено эндоскопическое обследование в той же клинике.По результатам патологии пациенты были разделены на две группы: доброкачественные и злокачественные. Толщина стенки антрального отдела в компьютерной томографии, уровни гемоглобина и альбумина и возраст сравнивались между этими двумя группами. Параметры со значительными различиями были дополнительно проанализированы многомерным анализом с использованием анализа логистической регрессии. Результатов . Из 111 пациентов, включенных в исследование, 57 были мужчинами и 54 женщинами. Средний возраст составлял 65 лет. 51 пациент был классифицирован как доброкачественный и 60 — как злокачественный.Средний возраст злокачественных пациентов составил 70 лет, а доброкачественных — 59 лет (). Толщина стенки антрального отдела у злокачественных больных составила 13,68 ± 3,27 мм, а у доброкачественных — 9,22 ± 2,17 мм (). Аналогичным образом, уровень гемоглобина значительно отличался у злокачественных и доброкачественных пациентов (10,78 ± 1,57 г / дл и 12,64 ± 1,43 г / дл соответственно;). Уровни альбумина составляли 3,36 ± 0,57 мг / дл у злокачественных пациентов и 3,97 ± 0,57 мг / дл у доброкачественных пациентов (). Заключение . Оценка толщины стенки антрального отдела, возраста, показателей гемоглобина и альбумина вместе может способствовать различению доброкачественных и злокачественных патологий, затрагивающих эту область, у пациентов с подозрением на утолщение стенки желудка при КТ брюшной полости.
1. Введение
Рак желудка является четвертым по распространенности раком в мире и третьим по смертности от рака [1, 2]. Около 75% случаев рака желудка в мире наблюдается в странах Дальнего Востока, таких как Япония, Китай и Южная Корея [3]. У мужчин он встречается вдвое чаще, чем у женщин, и обычно встречается в 6 -х и 7 -х десятилетиях [4, 5]. Смертность от рака желудка за последние годы заметно снизилась [6]. Важную роль в этом снижении играет широкое использование как эндоскопических методов, так и методов радиологической визуализации.В странах с высокой заболеваемостью раком желудка, таких как Япония и Корея, частота ранней диагностики рака желудка достигает 50% [7, 8]. В западном обществе, в том числе в Турции, рак желудка диагностируется на более поздних стадиях. Диагностика на ранних стадиях — один из важнейших факторов, влияющих на лечение и выживаемость заболевания [9].
Компьютерная томография (КТ) широко применяется у пациентов, поступающих в больницу с различными жалобами. Оценка КТ опытным радиологом может помочь в ранней диагностике злокачественных новообразований желудка.Важным вопросом для ранней диагностики является способность КТ дифференцировать структуру желудочной стенки и толщину желудочной стенки патологического происхождения [10]. Увеличенная толщина стенки при КТ не всегда может быть признаком злокачественного новообразования. Толщина стенки желудка также может увеличиваться из-за доброкачественных причин, таких как гастрит, язвы, полипы, туберкулез, болезнь Крона и болезнь Менетрие. Ранняя эндоскопия и биопсия необходимы, чтобы сделать вывод о том, что толщина стенки вызвана злокачественным новообразованием [11].
Эндоскопия, запрошенная из-за толщины стенки в КТ, имеет ряд серьезных недостатков, таких как высокая стоимость, инвазивный характер, риски осложнений и отложенные сроки эндоскопического обследования. Таким образом, выбор времени для эндоскопического обследования может иметь решающее значение у пациентов с толстой стенкой на КТ. В настоящее время нет единого протокола или алгоритма для оценки этих пациентов [11, 12]. Целью настоящего исследования было определить связь утолщения стенки желудка, обнаруженного при КТ брюшной полости, запрошенного по разным причинам, с эндоскопическими данными, а также сравнить нормальную и патологическую толщину стенки.
2. Метод
Это ретроспективное исследование случай-контроль было одобрено этическим комитетом медицинского факультета Университета Токат Газиосманпаша. В отчетах КТ брюшной полости пациентов, которым с 1 января 2012 г. по 1 августа 2018 г. проводилось КТ-сканирование по любой причине, проводился поиск по фразе «утолщение стенки желудка» в электронной базе данных больницы. Пациенты, у которых компьютерная томография не соответствовала стандартному протоколу внутривенного и перорального введения контрастного вещества, пациенты без достаточного вздутия желудка, пациенты с остаточной пищей в желудке, пациенты с застойной сердечной недостаточностью, гипоальбуминемией и нефритическим синдромом, пациенты с хирургическим вмешательством на желудке , были исключены пациенты с анемией в анамнезе, пациенты с толщиной стенки желудка, которая явно свидетельствовала о раке желудка, и пациенты, которые не проходили гастроскопическое обследование в нашей больнице.Пациенты, которым в соответствии с протоколами обследований была проведена контрастная оральная контрастная КТ брюшной полости, пациенты, у которых оптимальная толщина стенки желудка могла быть измерена на их КТ-сканированиях, у которых проводились эндоскопические обследования и забор крови с интервалом в один месяц до или после КТ обследования в нашей больнице. больницы, и которые были оценены с помощью биопсии. КТ-срезы брюшной полости пациентов, включенных в исследование, были повторно обследованы опытным радиологом, не зная о результатах эндоскопической и патологической оценки.Увеличение толщины стенки желудка более 5 миллиметров (мм) считалось патологическим. Демографическая информация, значения гемоглобина (Hb) и альбумина были получены из электронных файлов. Пациенты были разделены на две группы: доброкачественные и злокачественные в соответствии с результатами эндоскопической и патологической оценки. Первая группа состояла из доброкачественных причин, таких как гастрит, хронический атрофический гастрит, кишечная метаплазия, инфекция Helicobacter pylori ( H. pylori ) и язва, а вторая группа включала злокачественные причины, такие как карцинома, лимфома, карциноид и стромальные опухоли.Толщина стенки желудка, Hb, возраст и значения альбумина в двух группах сравнивались с использованием описательной статистики.
Микробиологическое исследование на наличие H. pylori было выполнено у пациентов с доброкачественными гистопатологическими данными. Различия между H. pylori отрицательными и H. pylori положительными группами были исследованы с помощью описательной статистики. H. pylori не проводились микробиологические исследования для пациентов со злокачественными гистопатологическими результатами.
Для получения информации об общих характеристиках исследуемых групп был проведен описательный анализ. Данные для непрерывных переменных были выражены как среднее значение ± стандартное отклонение, в то время как данные для категориальных переменных были представлены как n (%). При сравнении средних количественных переменных между группами использовались независимые образцы t -тест и односторонний дисперсионный анализ. Для оценки взаимосвязи между качественными переменными использовались кросс-таблицы и тесты хи-квадрат.значения менее 0,05 считались статистически значимыми. Логистический регрессионный анализ выполнялся как многомерный анализ параметров, для которых наблюдались значительные различия при одномерном анализе. Для выявления значимых параметров в многомерном анализе был проведен анализ кривой рабочих характеристик приемника (ROC). Параметры с пороговыми значениями, чувствительностью и специфичностью> 0,600 на основе расчетов площади под кривой (AUC) считались значимыми.В расчетах использовалось статистическое программное обеспечение SPSS (версия 19, SPSS Inc., IBM Co., Somers, NY).
3. Результаты
Сообщалось, что у 536 пациентов была толщина стенки желудка. Четыреста двадцать пять пациентов, которые не соответствовали критериям исследования, были исключены из исследования. В исследование были включены 111 пациентов (57 мужчин и 54 женщины), которым была проведена КТ брюшной полости и эндоскопическая оценка. Гистопатологическая оценка выявила злокачественные новообразования у 60 пациентов (52 аденокарциномы, 5 лимфом, 2 стромальные опухоли желудочно-кишечного тракта и 1 нейроэндокринная опухоль) и доброкачественные причины у 51 пациента (48 антральный гастрит и 3 язвы желудка).
Увеличение толщины стенки желудка, возраст, Hb и уровни альбумина значительно различались между группами 1 и 2 в однофакторном анализе (). На основании многомерного логистического регрессионного анализа предполагаемое увеличение толщины стенки желудка, возраст и значения Hb были независимыми переменными при диагностике рака желудка (), в то время как альбумин не был значимым (). Характеристики исследуемых групп для этих переменных приведены в таблице 1.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
OR = отношение шансов. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
На основании анализа кривых ROC независимых переменных значения AUC были выше 0,600 для толщины стенки антрального отдела, гемоглобина и возраста (рис. 1). Предлагаемые пороговые значения и рабочие характеристики для этих переменных показаны в таблице 2.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
AUC: площадь под кривой ; AWT: толщина стенки антрального отдела; Hb: гемоглобин; PPV: положительные прогностические значения; NPV: отрицательные прогностические значения. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
4. Обсуждение
В то время как пятилетняя выживаемость при раке желудка составляла 15% в 1970-х годах, в настоящее время этот показатель составляет около 30% [7]. Самая главная причина плохого прогноза — поздняя диагностика. Важность компьютерной томографии брюшной полости, выполненной в оптимальных условиях для диагностики раннего рака желудка, была подчеркнута в заключительных декларациях двух важных международных встреч, проведенных в 2014 г. [13, 14]. Точность диагностики рака желудка при предоперационном КТ составляет от 69 до 85%.Однако диагностика рака желудка на ранней стадии затруднена. Следовательно, точность диагностики намного ниже (26–53%) [15, 16].
Пятилетняя выживаемость при раке желудка на ранней стадии колеблется от 85 до 100%. Однако этот показатель значительно ниже для запущенного рака желудка (7–27%) [17]. Увеличение толщины стенки желудка на компьютерной томографии считается патологией при ранней диагностике рака желудка. Необходимость ранней диагностики рака желудка с помощью компьютерной томографии была предметом многих исследований, посвященных изучению непатологической толщины стенки желудка.Существует множество исследований, в которых сообщается, что толщина нормальной стенки желудка при КТ в оптимальных условиях составляет менее 5 мм [18–21]. Однако есть также сообщения о том, что нормальная стенка желудка может достигать 12 мм [22].
Самым сложным местом для оценки толщины стенки желудка с помощью компьютерной томографии является антропилорическая область (дистальная часть желудка). Увеличение толщины антральной стенки в основном объясняется физиологическими причинами (такими как чрезмерные перистальтические движения в антральном отделе и толщина структуры гладкомышечной стенки), оптимальной когерентностью качества КТ-сканирования (растяжение антрального отдела) или доброкачественными причинами, такими как вторичный гастрит после ЧАС.pylori инфекция. Эта ситуация, которая считается доброкачественной и не подлежит дальнейшему исследованию, представляет собой главное препятствие для ранней диагностики опухолей, происходящих из этой области. Эндоскопическая оценка всех пациентов с утолщением стенки в антропилорической области при КТ приводит к увеличению затрат, потере труда, осложнениям и неоправданно перегруженному графику приема в отделениях эндоскопии, что, в свою очередь, приводит к увеличению времени приема и задержкам в диагностике и лечении. настоящие пациенты, нуждающиеся в неотложной помощи [20, 23].Следовательно, хорошая оценка толщины стенки, интерпретируемая на компьютерной томографии, важна с точки зрения ранней диагностики и предотвращения ненужных обследований.
Cho et al. оценили толщину антральной стенки у 120 пациентов и обнаружили, что средняя толщина стенки 12,5 мм, обусловленная доброкачественными причинами, тогда как в случаях, вторичных по отношению к злокачественным новообразованиям, она составила 19 мм [24]. В другом исследовании Tongdee et al., Толщина стенки антрального отдела по злокачественным причинам составила 16,64 ± 7,28 мм, а толщина стенки по доброкачественным причинам — 5.68 ± 2,13 мм [23, 25]. Среди наиболее частых причин доброкачественной утолщенности стенок — хронический гастрит и язвенная болезнь, из которых H. pylori является основным этиологическим фактором. В развивающихся странах более 90% населения инфицировано H. pylori , что составляет 50% в развитых странах. H. pylori чаще всего располагается в антральном отделе и обычно протекает бессимптомно [26, 27]. В исследованиях, изучающих влияние H. pylori на толщину стенки антрального отдела желудка, влияние H.pylori не было связано с толщиной стенки [21, 25]. В настоящем исследовании была обнаружена значительная разница между толщиной стенки антрального отдела в доброкачественной и злокачественной группах (OR = 1,60; 95% CI: 1,22–2,09;) (Таблица 1). При ROC-анализе для порогового значения толщины стенки антрального отдела> 11 мм AUC составляла 0,862, чувствительность составляла 75%, специфичность составляла 86%, PPV составляла 0,866, NPV составляла 0,745 и (таблица 2, рисунок 1). Это может быть хорошим намеком для клинициста, оценивающего компьютерную томографию брюшной полости.Толщина стенки может позволить раннюю диагностику и лечение пациентов. H. pylori положительный результат был у 70,5% пациентов, которые были признаны доброкачественными на основании гистопатологического исследования. Кроме того, не было никакой связи между средней толщиной стенки антрального отдела и положительностью H. pylori ().
Рак желудка у мужчин встречается в 1,8–2 раза чаще, чем у женщин. Уровень заболеваемости увеличивается с возрастом и в основном наблюдается в 6 и 7 десятилетиях.Хотя на ранних стадиях рак желудка обычно протекает бессимптомно, на поздних стадиях он может вызывать тошноту, рвоту, потерю веса и анемию [28–31]. Симптоматический период заболевания обычно связан с запущенной стадией, когда недоедание и хроническая анемия часто обнаруживаются и подтверждаются снижением уровня гемоглобина и альбумина. Средние предоперационные значения гемоглобина у этих пациентов колеблются от 11,1 г / дл до 12 г / дл [32–35]. Точно так же есть много исследований, в которых сообщается, что предоперационные значения альбумина находятся в диапазоне от 3 до 3.0 и 3,9 г / дл у пациентов с опухолями желудка [36–38]. Согласно литературным данным, при одномерном статистическом анализе наблюдалась значительная разница в возрасте, Hb и значениях альбумина между группами злокачественных и доброкачественных пациентов. Однако уровень альбумина не был значимым при многомерном логистическом регрессионном анализе. Включение пациентов с подозрением на толщину стенки, но исключение пациентов с подтвержденным раком желудка на основании результатов КТ могло привести к выводу, что низкий уровень альбумина из-за недоедания у наших пациентов не был независимой переменной (Таблица 1).Кроме того, в доброкачественную группу вошли три случая язвы. Средняя толщина стенки в этих случаях составляла 13,5 ± 1,29 мм, значение Hb составляло 9,23 ± 1,38 г / дл, а значение альбумина составляло 2,97 ± 0,49 мг / дл, что было выше, чем в других доброкачественных случаях, и аналогично таковым при злокачественных новообразованиях. группа. Хотя мы классифицировали язву желудка как доброкачественную, она относится к числу заболеваний, которые следует диагностировать и лечить на ранней стадии с точки зрения связанных с этим рисков.
Диагноз рака желудка ставится на основании патологического исследования.Таким образом, при подозрении на патологию эндоскопическая биопсия является золотым стандартом. Диагноз рака желудка нельзя поставить только с помощью компьютерной томографии, возраста, уровня гемоглобина и альбумина. Клиницисты должны быть избирательными при оценке состояния пациента. Верхнее эндоскопическое обследование не рекомендуется каждому пациенту с жалобами на эпигастральную область, поскольку это может привести к увеличению расходов на здоровье, потере труда, осложнениям, ненужному скоплению людей на приемах в отделении эндоскопии и задержкам в получении медицинской помощи пациентами, которым требуется срочная помощь.Однако толщина стенки желудка, возраст, значения альбумина и гемоглобина могут позволить клиницистам сделать прогноз и предварительный диагноз при оценке состояния пациента. Мы считаем, что уделение приоритетного внимания обследованию этих конкретных пациентов может быть эффективным в сокращении задержек в диагностике и лечении. В настоящем исследовании мы наблюдали, что толщина стенки желудка на компьютерной томографии, значения Hb, возраста и альбумина показали значительные различия между доброкачественными и злокачественными группами исследования. Эти параметры могут быть полезны для оценки пациента клиницистом, поскольку эти параметры могут способствовать диагностике и лечению пациента.Могут быть полезны более крупные проспективные когортные исследования, в которых для оценки пациентов следует принимать во внимание толщину стенки желудка, гемоглобин, возраст и альбумин в дополнение к клиническим симптомам, таким как потеря аппетита, потеря веса, тошнота и рвота. Схема клинического алгоритма для раннего выявления потенциально злокачественных больных.
Наше исследование имеет недостатки, присущие всем ретроспективным исследованиям, и, следовательно, имеет некоторые ограничения. Прежде всего, в исследование были включены только пациенты с подозрением на толщину стенки желудка, но были исключены пациенты с нормальной толщиной стенки желудка и те, у кого было сильное подозрение на опухоль желудка при оценке КТ.Еще одним ограничением был широкий возрастной диапазон. Наконец, на исход могло повлиять ограниченное количество пациентов.
5. Заключение
Толщина антральной стенки, определенная при КТ брюшной полости, уровни Hb и альбумина, а также возраст значительно различались между группами доброкачественной и злокачественной патологии желудка. Уровень гемоглобина и возраст могут значительно повлиять на исход пациентов, поскольку при верхних эндоскопических исследованиях приоритет отдавался пациентам с толщиной стенки желудка, обнаруженной на компьютерной томографии. Однако для подтверждения наших выводов необходимы дальнейшие исследования.
Доступность данных
Данные, использованные для подтверждения выводов этого исследования, можно получить у соответствующего автора по запросу.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов в отношении публикации этой статьи.
Ультразвуковое исследование желудка у детей: можно ли использовать пороговые значения антрального отдела для диагностики пустого желудка? | BJA: Британский журнал анестезии
Аннотация
Предпосылки
Сонография желудка становится ценным клиническим инструментом для оценки риска аспирации.Недавнее исследование показало, что одна отсеченная площадь поперечного сечения (ППС) в положении лежа на спине может диагностировать пустой желудок у роженицы. Это исследование устанавливает чувствительность и специфичность одного измерения отсечки CSA как в положении лежа на спине, так и в положении правого бокового пролежня (RLD) при диагностике пустого антрального отдела у педиатрических пациентов.
Методы
После индукции анестезии антральная сонография была выполнена в положении лежа на спине и в положении RLD у 100 педиатрических пациентов натощак перед эндоскопической оценкой верхних отделов позвоночника.После верхней эндоскопии любое остаточное содержимое желудка отсасывалось под прямой визуализацией, и немедленно выполнялась антральная сонография. Значения ППС антрального отдела желудка сравнивали с использованием знакового рангового критерия Вилкоксона. Кривые характеристики оператора приемника (ROC) были построены для оценки различающей способности положения антральной сонографии в диагностике пустого антрального отдела.
Результаты
Были обнаружены значительные различия между значениями CSA до и после отсасывания в положении RLD.Отсечка CSA пустого антрального отдела в положении лежа на спине и RLD составляла 2,19 см 2 (чувствительность 75%, специфичность 36%) и 3,07 см 2 (чувствительность 76%, специфичность 67%), соответственно.
Выводы
Положение RLD дает наиболее чувствительное и конкретное значение отсечки CSA, где CSA антрального отдела ≤ 3,07 см 1 год.С возрастом чувствительность и специфичность этого теста увеличивается в положении RLD.
Площадь поперечного сечения антрального отдела (CSA) может быть измерена сонографически.
Он коррелирует с объемом желудка и может использоваться для оценки риска аспирации.
Авторы изучили ППС антрального отдела у голодающих детей и измерили объем желудочного содержимого, отсасываемого эндоскопически.
ППС антрального отдела ≤3,07 см 2 в правом боковом положении был наиболее чувствительным и специфичным для натощак.
Литература, посвященная взрослым, предполагает, что пустой антральный отдел желудка легко идентифицируется с помощью ультразвука, поскольку он показывает гиперэхогенную серозную оболочку и толстую гипоэхогенную собственную мышцу и описывается как плоская структура с передней и задней стенками в непосредственной близости друг от друга или в виде круглой формы. или яйцевидный «конус», напоминающий «мишень в яблочко».Недавнее исследование показало, что единичное пороговое значение антральной CSA в положении лежа на спине может диагностировать пустой желудок у акушерских групп во время установленных родов. 11 Они сообщили, что пороговое значение CSA для антральной области в положении лежа на спине составляло 3,80 см 2 , что давало чувствительность 81% и специфичность 76% при диагностике пустого желудка (степень 0). . 11 На сегодняшний день нет педиатрических исследований, изучающих, будет ли одно измерение ППС антрального отсечения полезным для быстрой диагностики пустого желудка в широком диапазоне педиатрических возрастных групп.Целью этого исследования было установить чувствительность и специфичность одного измерения отсечки CSA для диагностики пустого антрального отдела как в положении лежа на спине, так и в положении RLD, чтобы повысить полезность этого прикроватного инструмента для оказания помощи педиатрическим пациентам.
Методы
Дизайн исследования
Это проспективное наблюдательное когортное исследование получило одобрение (E-25160) от Совета по этике совместных медицинских исследований (Университет Калгари, Калгари, штат Алабама, Канада).Эту когорту пациентов ранее изучали Спенсер и его коллеги; 14 однако, в настоящем исследовании мы выполнили отдельный вторичный анализ исторической когорты, в котором особое внимание уделялось пустому отсасываемому антральному отделу. Официальные опекуны и / или пациенты, способные понимать результаты исследования, предоставили письменное информированное согласие. Критерии включения включали детей и подростков в возрасте от 11 месяцев до 17 лет, поступивших на плановую эндоскопию верхних отделов желудочно-кишечного тракта (ЖКТ) под общей анестезией, которые следовали рекомендациям по голоданию:> 8 часов для твердых веществ и> 3 часов для прозрачных жидкостей.Критерии исключения включали кровотечение из верхних отделов желудочно-кишечного тракта в течение 1 месяца после процедуры, предшествующие операции на нижнем пищеводе или желудке, несоблюдение установленных правил голодания и длительное время> 5 мин между завершением ультразвуковой оценки и отсасыванием желудочного содержимого. Пациенты с повышенным ИМТ, гастроэзофагеальным рефлюксом или другими факторами риска аспирации не исключались из исследования.
Ультразвуковое исследование антрального отдела желудка
Анестезиологическое обеспечение индукции и проходимости дыхательных путей оставалось на усмотрение лечащего анестезиолога и оформлялось документально.Демографические данные включали вес, рост, возраст и пол. После индукции анестезии и обеспечения проходимости дыхательных путей перед эндоскопией пациентов сканировали как в положении лежа на спине, так и в положении RLD. После ультразвукового исследования пациента поместили в положение лежа на левом боку для эндоскопии верхних отделов желудочно-кишечного тракта. Детские гастроэнтерологи были слепы к результатам предыдущего ультразвукового исследования желудка. Перед эндоскопией эндоскоп был протестирован в соответствии со стандартной клинической практикой, и подача воды была отключена, чтобы избежать закапывания воды, как описано ранее. 14 Градуированная ловушка для образцов с шагом 1 мл (MED-RX 30-4010, Оквилл, Онтарио, Канада) была присоединена к эндоскопу для сбора и количественного определения аспирированного содержимого. Эндоскоп вводили трансорально и продвигали в желудок, где в него наполняли воздухом, чтобы обеспечить максимальную визуализацию и облегчить аспирацию всего видимого жидкого содержимого желудка. Эндоскоп продвигали в дистальный отдел желудка и ретрофлексировали, чтобы подтвердить отсутствие остаточной жидкости в теле или дне желудка.Градуированную ловушку для образцов отсоединили и записали объем откачиваемой жидкости. После эндоскопического исследования верхних отделов желудка детский гастроэнтеролог полностью отсосал весь желудок, и эндоскоп медленно удалили из желудка. Затем была выполнена антральная сонография в положении лежа на спине и в положении RLD. Антральный отдел желудка был идентифицирован между левой долей печени и поджелудочной железой на уровне аорты и верхней брыжеечной артерии или нижней полой вены, как описано ранее. 14 Три неподвижных изображения были записаны для каждого пациента в положении лежа на спине и в положении RLD как до, так и после эндоскопического исследования и аспирации. ППС антрального отдела желудка измеряли методом свободного отслеживания с использованием внутреннего штангенциркуля ультразвукового аппарата для отслеживания внешнего края антрального отдела, соответствующего серозной оболочке, как описано ранее. 14 Сонография антрального отдела желудка была проведена детским анестезиологом, прошедшим подготовку в области ультразвукового исследования желудка, с использованием системы Philips CX50 (Philips Healthcare, Андовер, Массачусетс, США) первоначально с криволинейным датчиком (низкая частота 2–5 МГц) или, альтернативно, с линейным датчиком. (высокая частота 7–12 МГц), если антральный отдел отделялся от поверхности кожи <3 см.Все ультразвуковые исследования желудка были выполнены одним детским анестезиологом (AOS), который прошел однодневный курс сонографии желудка (семинар ISURA Gastric US, Торонто, Канада), 3 дня (> 25 сканирований) контролируемых сканирований и регулярно выполняет ультразвуковое исследование желудка. основы для целей обучения и клинического ведения за 6 месяцев до начала исследования. Кроме того, детский анестезиолог был опытным пользователем ультразвука для регионарной анестезии и процедур сосудистого доступа.
Статистический анализ
Сто педиатрических пациентов рассматривались для включения в исследование, как описано Спенсером и его коллегами. 14 Демографические переменные были проверены на нормальность с помощью теста Шапиро – Уилка и представлены соответственно с использованием либо среднего [стандартное отклонение (sd)], либо медианы [межквартильный диапазон (IQR)]. Корреляцию между весом, ИМТ, возрастом и CSA оценивали с помощью Спирмена Rho (ρ). Измеренные значения CSA антрального отдела до и после отсасывания были стратифицированы по положению при ультразвуковой сонографии (лежа на спине и RLD) и сравнивались с использованием ранжированных тестов Вилкоксона.CSA представлены как медиана (IQR) и процентиль 95 th [95% доверительный интервал (CI)]. Кривые непараметрических характеристик оператора приемника (ROC) были построены для оценки различающей способности положения антрального отдела сонографии в диагностике пустого антрального отдела (постэндоскопическая аспирация). Чувствительность, специфичность, положительные прогностические значения (PPV) и отрицательные прогностические значения (NPV) с 95% доверительными интервалами представлены в значениях отсечки антральной CSA в положении лежа на спине и RLD, которые максимизируют сумму чувствительности и специфичности (индекс Юдена).Все статистические тесты были выполнены с использованием программного обеспечения SPSS 19.0 (IBM, Армонк, Нью-Йорк, США).
Результаты
Сто пациентов были включены в анализ RLD. Один пациент был исключен из анализа на спине, поскольку площадь антрального отдела после аспирации не могла быть измерена из-за наличия артефакта воздуха. При ультразвуковом исследовании было обнаружено, что после эндоскопической аспирации антрамы пустые. Демографические данные пациентов представлены в таблице 1. Типичный пример сонографического изображения антрального отдела до и после эндоскопической аспирации в положении RLD показан на рисунке 1.
Таблица 1Характеристики пациента ( n = 100). BSA, площадь поверхности тела; IQR, межквартильный размах; sd — стандартное отклонение; ГЭРБ, гастроэзофагеальная рефлюксная болезнь. * Двенадцать пациентов поступили с двумя показаниями; один пациент поступил с тремя показаниями
| Пол ( n ; мужчина: женщина) | 44:56 |
| Возраст [лет; медиана (IQR)] | 12,2 (8,2) |
| ИМТ [кг · м -2 ; медиана (IQR)] | 16.9 (5,6) |
| BSA [m 2 ; среднее (стандартное отклонение)] | 1,28 (0,41) |
| Показания к эндоскопии * ( n ) | |
| Целиакия | 51 |
| Эозинофильный эзофагит | 12 |
| Болезнь Крона | 6 |
| Язвенный колит | 1 |
| ГЭРБ | 8 |
| Другое | 36 |
| Пол ( n ; мужчина: женщина) | 44:56 |
| Возраст [год; медиана (IQR)] | 12.2 (8,2) |
| ИМТ [кг · м −2 ; медиана (IQR)] | 16,9 (5,6) |
| BSA [m 2 ; среднее (стандартное отклонение)] | 1,28 (0,41) |
| Показания к эндоскопии * ( n ) | |
| Целиакия | 51 |
| Эозинофильный эзофагит | 12 |
| Болезнь Крона | 6 |
| Язвенный колит | 1 |
| ГЭРБ | 8 |
| Другое | 36 |
Характеристики пациента ( n = 100).BSA, площадь поверхности тела; IQR, межквартильный размах; sd — стандартное отклонение; ГЭРБ, гастроэзофагеальная рефлюксная болезнь. * Двенадцать пациентов поступили с двумя показаниями; один пациент поступил с тремя показаниями
| Пол ( n ; мужчина: женщина) | 44:56 |
| Возраст [лет; медиана (IQR)] | 12,2 (8,2) |
| ИМТ [кг · м -2 ; медиана (IQR)] | 16,9 (5,6) |
| BSA [m 2 ; среднее (стандартное отклонение)] | 1.28 (0,41) |
| Показания к эндоскопии * ( n ) | |
| Целиакия | 51 |
| Эозинофильный эзофагит | 12 |
| Болезнь Крона | 6 |
| 1 | |
| ГЭРБ | 8 |
| Другое | 36 |
| Пол ( n ; мужской: женский) | 44:56 |
| Возраст [год ; медиана (IQR)] | 12.2 (8,2) |
| ИМТ [кг · м −2 ; медиана (IQR)] | 16,9 (5,6) |
| BSA [m 2 ; среднее (стандартное отклонение)] | 1,28 (0,41) |
| Показания к эндоскопии * ( n ) | |
| Целиакия | 51 |
| Эозинофильный эзофагит | 12 |
| Болезнь Крона | 6 |
| Язвенный колит | 1 |
| ГЭРБ | 8 |
| Другое | 36 |
Рис.1
Сонографический вид антрального отдела желудка у 12-летнего пациента (39.6 кг; 153 см) до и после эндоскопического отсасывания в правом боковом положении лежа (RLD). Предварительно отсасываемое содержимое желудка составляет 36 мл (0,91 мл, кг -1 ), а антральный отдел после отсасывания представляет собой действительно пустой антральный отдел. Внешний край антрального отдела желудка, соответствующий серозной оболочке, отмечен штриховой линией, показывающей метод свободного отслеживания для измерения площади поперечного сечения. Левая часть изображения на обеих панелях находится в цефале. L, печень; SMA, верхняя брыжеечная артерия; АО, аорта.
Рис. 1
Сонографический вид антрального отдела желудка у 12-летнего пациента (39,6 кг; 153 см) до и после эндоскопического отсасывания в положении правого бокового пролежня (RLD). Предварительно отсасываемое содержимое желудка составляет 36 мл (0,91 мл, кг -1 ), а антральный отдел после отсасывания представляет собой действительно пустой антральный отдел. Внешний край антрального отдела желудка, соответствующий серозной оболочке, отмечен штриховой линией, показывающей метод свободного отслеживания для измерения площади поперечного сечения.Левая часть изображения на обеих панелях находится в цефале. L, печень; SMA, верхняя брыжеечная артерия; АО, аорта.
Корреляция от низкой до средней между возрастом и ППС после аспирации ρ = 0,60 и ρ = 0,34 и ИМТ и ППС после аспирации ρ = 0,58 и ρ = 0,32 была обнаружена в положении лежа на спине и в положении RLD, соответственно. ППН антрального отдела после аспирации [2,55 (1,06) см 2 ] были значительно уменьшены по сравнению с участками после отсасывания [3,53 (2,36) см 2 ] при измерении в положении RLD ( P <0.001; Таблица 2). Не было обнаружено значительной разницы в измеренных ППС до [1,96 (0,93) см 2 ] и после отсасывания в положении лежа на спине [1,85 (0,84) см 2 ] ( P = 0,059; Таблица 2).
Таблица 2Измеренные площади антрального сечения до и после аспирации (см 2 ). CSA, площадь поперечного сечения; IQR, межквартильный размах; ДИ — доверительный интервал; RLD, пролежень правый боковой
| . | Предварительное всасывание CSA [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | CSA после всасывания [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | P -значение . |
|---|---|---|---|
| на спине | 1,96 (0,93) | 1,85 (0,84) | 0,059 |
| ( n = 99) | 3,37 (1,81–2,10) | 3,18 (1,72–1,99) | |
| RLD | 3,53 (2,36) | 2,55 (1,06) | <0.001 |
| ( n = 100) | 7,31 (3,55–4,28) | 4,46 (2,44–2,85) |
| . | Предварительное всасывание CSA [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | CSA после всасывания [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | P -значение . |
|---|---|---|---|
| на спине | 1.96 (0,93) | 1,85 (0,84) | 0,059 |
| ( n = 99) | 3,37 (1,81–2,10) | 3,18 (1,72–1,99) | |
| RLD | 3,53 (2,36 ) | 2,55 (1,06) | <0,001 |
| ( n = 100) | 7,31 (3,55–4,28) | 4,46 (2,44–2,85) |
Измерения до и после -сасываемые антральные сечения (см 2 ).CSA, площадь поперечного сечения; IQR, межквартильный размах; ДИ — доверительный интервал; RLD, пролежень правый боковой
| . | Предварительное всасывание CSA [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | CSA после всасывания [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | P -значение . |
|---|---|---|---|
| на спине | 1.96 (0,93) | 1,85 (0,84) | 0,059 |
| ( n = 99) | 3,37 (1,81–2,10) | 3,18 (1,72–1,99) | |
| RLD | 3,53 (2,36 ) | 2,55 (1,06) | <0,001 |
| ( n = 100) | 7,31 (3,55–4,28) | 4,46 (2,44–2,85) |
| . | Предварительное всасывание CSA [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | CSA после всасывания [см 2 ; медиана (IQR)]; 95% процентиль (95% ДИ) . | P -значение . |
|---|---|---|---|
| на спине | 1,96 (0,93) | 1,85 (0,84) | 0,059 |
| ( n = 99) | 3,37 (1,81–2,10) | 3,18 (1,72–1,99) | |
| RLD | 3,53 (2,36) | 2,55 (1,06) | <0.001 |
| ( n = 100) | 7,31 (3,55–4,28) | 4,46 (2,44–2,85) |
Дискриминационная сила ультразвукового обзора в диагностике пустого антрального отдела (постэндоскопическая аспирация) представлен кривыми ROC (рис. 2). Площадь под кривыми для положений на спине и RLD для осмотра составляла 0,54 (95% ДИ = 0,46–0,62, P = 0,396) и 0,73 (95% ДИ = 0,65–0,80, P <0,001), соответственно. Пороговые значения антрального отдела, которые максимизировали сумму чувствительности и специфичности, составляли 2.19 см 2 (лежа на спине) и 3,07 см 2 (RLD). Просмотр антрального отдела в положении RLD показал превосходные значения PPV [70% (95% ДИ: 61–78)] и NPV [74% (95% ДИ: 65–83)] (Таблица 3). Большие пороговые значения антральной CSA в положении RLD ≤3,38 см 2 или ≤3,99 см 2 повышают чувствительность теста до 80% и 90% с соответствующим снижением специфичности до 58% и 40% соответственно .
Таблица 3Площадь антрального поперечного сечения (см 2 ) пороговые значения для диагностики пустого желудка в положении лежа на спине и в положении RLD.Представленные пороговые значения представляют собой максимальное значение суммы чувствительности и специфичности (индекс Юдена) для каждой соответствующей кривой характеристики оператора приемника (ROC). CSA, площадь поперечного сечения; RLD, правый боковой пролежень; PPV, положительная прогностическая ценность; NPV, отрицательная прогностическая ценность
| УЗИ . | Отрезок антральной CSA (см 2 ) . | Чувствительность (%; 95% ДИ) . | Специфичность (%; 95% ДИ) . | PPV (%; 95% ДИ) . | NPV (%; 95% ДИ) . |
|---|---|---|---|---|---|
| на спине | ≤2,19 | 75 (66–83) | 36 (27–45) | 54 (45–62) | 59 (47–71) |
| RLD | ≤3,07 | 76 (67–84) | 67 (58–76) | 70 (61–78) | 74 (65–83) |
| УЗИ . | Отрезок антральной CSA (см 2 ) . | Чувствительность (%; 95% ДИ) . | Специфичность (%; 95% ДИ) . | PPV (%; 95% ДИ) . | NPV (%; 95% ДИ) . |
|---|---|---|---|---|---|
| на спине | ≤2,19 | 75 (66–83) | 36 (27–45) | 54 (45–62) | 59 (47–71) |
| RLD | ≤3.07 | 76 (67–84) | 67 (58–76) | 70 (61–78) | 74 (65–83) |
Площадь антрального сечения (см 2 ) пороговые значения для диагностики пустого желудка в положении лежа на спине и в положении RLD. Представленные пороговые значения представляют собой максимальное значение суммы чувствительности и специфичности (индекс Юдена) для каждой соответствующей кривой характеристики оператора приемника (ROC). CSA, площадь поперечного сечения; RLD, правый боковой пролежень; PPV, положительная прогностическая ценность; NPV, отрицательная прогностическая ценность
| УЗИ . | Отрезок антральной CSA (см 2 ) . | Чувствительность (%; 95% ДИ) . | Специфичность (%; 95% ДИ) . | PPV (%; 95% ДИ) . | NPV (%; 95% ДИ) . |
|---|---|---|---|---|---|
| на спине | ≤2,19 | 75 (66–83) | 36 (27–45) | 54 (45–62) | 59 (47–71) |
| RLD | ≤3.07 | 76 (67–84) | 67 (58–76) | 70 (61–78) | 74 (65–83) |
| УЗИ . | Отрезок антральной CSA (см 2 ) . | Чувствительность (%; 95% ДИ) . | Специфичность (%; 95% ДИ) . | PPV (%; 95% ДИ) . | NPV (%; 95% ДИ) . |
|---|---|---|---|---|---|
| на спине | ≤2.19 | 75 (66–83) | 36 (27–45) | 54 (45–62) | 59 (47–71) |
| RLD | ≤ 3,07 | 76 (67–84) | 67 (58–76) | 70 (61–78) | 74 (65–83) |
Рис. 2
Кривые непараметрических рабочих характеристик приемника (ROC) для различительной способности ультразвукового изображения после эндоскопической аспирации при диагностике пустого антрального отдела.AUC — площадь под кривой ROC с 95% доверительным интервалом; RLD, правый боковой пролежень.
Рис. 2
Кривые непараметрических рабочих характеристик приемника (ROC) для различительной способности ультразвукового изображения после эндоскопической аспирации при диагностике пустого антрального отдела. AUC — площадь под кривой ROC с 95% доверительным интервалом; RLD, правый боковой пролежень.
Обсуждение
Мы обнаружили, что с увеличением возраста с 11 месяцев до 17 лет, CSA пустого антрального отдела также увеличивается.По мере увеличения ИМТ, CSA пустого антрального отдела также увеличивался, что аналогично результатам у взрослых пациентов с ожирением, у которых антральный отдел больше, чем у их коллег, не страдающих ожирением. 12 Это первое исследование, в котором применялось использование золотого стандарта эндоскопически отсасываемого антрального отдела желудка для определения порогового значения действительно пустого антрального отдела. Пустая CSA антрального отдела ≤2,19 см 2 в положении лежа на спине давала более низкую чувствительность, специфичность, PPV и NPV по сравнению с пустым CSA антрального отдела в положении RLD.Мы установили, что одно измерение отсечки CSA 3,07 см 2 в положении RLD имеет чувствительность 76% и специфичность 67%, что обеспечивает приемлемую производительность в способности различать пустой антральный отдел. Если пороговые значения CSA были увеличены до ≤3,38 см 2 и ≤3,99 см 2 в положении RLD, чувствительность (способность правильно идентифицировать пациентов с действительно пустым желудком) этого теста возрастает до 80% и 90 %, соответственно. Соответствующее снижение специфичности до 58% и 40% соответственно предполагает, что к использованию таких значений следует подходить с осторожностью.Снижение специфичности увеличивает количество ложноположительных результатов этого теста, что может подвергнуть пациента, у которого может быть желудочное содержимое, риску аспирации. Аналогичным образом, повышение специфичности за счет чувствительности увеличивает количество ложноотрицательных результатов, предполагая, что желудок не действительно пустой, хотя на самом деле у пациента действительно пустой желудок, что может подвергнуть его ненужному инвазивному вмешательству в дыхательные пути. Следовательно, идеальное значение отсечения CSA максимизирует как чувствительность, так и специфичность, как представлено с использованием ≤3.07 см 2 в положении RLD. Это убедительно свидетельствует о том, что положение RLD является оптимальным положением сканирования для измерения порогового значения, чтобы различать пустой желудок у пациентов старше 1 года в периоперационном периоде. Мы предполагаем, что измерение CSA только в положении RLD упростило бы использование текущего алгоритма 6 , требуя от клинициста вспомнить одно пороговое значение для положения RLD, представленное в этом исследовании, тем самым улучшив полезность УЗИ желудка в загруженная детская периоперационная среда.Тем не менее, если врач не может выполнить оценку RLD или измеренное значение CSA RLD> 3,07 см 2 , мы рекомендуем использовать полную качественную и количественную оценку, как было опубликовано ранее. 6
Хотя это исследование показывает, что RLD является оптимальным положением для сканирования для максимизации диагностических прогностических значений, клинически невозможно обследовать ребенка в положении RLD (например, септическая аппендэктомия, болезненный перелом локтя), что ограничивает использование УЗИ желудка в этой обстановке.В этих ситуациях, когда ребенка нельзя поместить в положение RLD, врач может продолжить выполнение ультразвукового исследования желудка в положении лежа на спине для качественной оценки антрального отдела желудка; однако результаты этого исследования показывают, что количественные измерения CSA только в положении лежа на спине менее точны и имеют ограниченный диагностический потенциал. Потенциальные ограничения этого исследования включают возможность обобщения на другие популяции педиатрических пациентов, такие как пациенты с сопутствующими заболеваниями, такими как диабет, поскольку наше исследование было сосредоточено на выборных пациентах натощак, которым проводилась эндоскопия верхних отделов желудочно-кишечного тракта для исследования различных жалоб верхних отделов желудочно-кишечного тракта.Кроме того, это исследование плановых пациентов натощак не измеряло pH содержимого желудка, что важно в случаях, когда у пациента высокий риск аспирации. Хотя размер выборки ( n = 100) позволял использовать надежный статистический анализ, будущие исследования, воспроизводящие эти результаты, укрепят доказательства и уровень комфорта анестезиологов, полагающихся на эти пороговые значения для оценки риска аспирации. Ограничением этого исследования является широкий возрастной диапазон участников.Ожидалось, что пациенты в возрасте до 24 месяцев недостаточно представлены, учитывая, что эти молодые пациенты реже обследуются с помощью эндоскопии. В целом диагностическая статистика в этом исследовании менее чувствительна и специфична, чем у взрослых беременных пациенток; 11 однако анализ подгрупп наших самых старых пациентов подросткового возраста (возраст ≥15 лет; n = 32) выявил улучшение нашей чувствительности (88%) и специфичности (72%), что отражает результаты у взрослых пациентов. .
Для того, чтобы УЗИ желудка функционировало в качестве клинического инструмента для оказания медицинской помощи в педиатрических периоперационных условиях, будущие направления должны быть сосредоточены на валидации измерений антрального CSA у педиатрических пациентов до индукции общей анестезии в плановых и неотложных случаях. . Эти будущие исследования позволят уточнить систему качественной оценки и количественные измерения, чтобы установить безопасный клинический алгоритм определения риска аспирации.
В заключение, мы показали, что: (1) CSA пустого антрального отдела увеличивается с увеличением возраста и BMI; (2) положение RLD — оптимальное положение для диагностики пустого антрального отдела; и (3) пороговое значение CSA в антральном отделе ≤3.07 см 2 в положении RLD демонстрирует приемлемые характеристики способности различать пустой антральный отдел у педиатрических пациентов старше 1 года в течение периоперационного периода.
Авторские работы
Дизайн исследования, набор пациентов и сбор данных: A.O.S., A.M.W.
Анализ данных: A.O.S., A.M.W., J.J.M.
Статистический анализ: A.M.W.
Написание первого варианта рукописи: J.J.M.
Редакция рукописи: А.О.С., A.M.W., J.J.M.
Декларация интересов
Не объявлено.
Финансирование
Для завершения этого проекта был использован грант на незарегистрированное исследование от Департамента детской анестезии (Детская больница Альберты, Калгари, штат Алабама, Канада).
Список литературы
1Borland
LM
,Sereika
S
,Woelfel
S
и др.Легочная аспирация у педиатрических пациентов во время общей анестезии: частота и исход
.J Clin Anesth
1998
;10
:95
—102
2Flick
RP
,Схемы
G
,Warner
M
Аспирация при педиатрической анестезии: чаще ли заболеваемость по сравнению со взрослыми?
Curr Opin Anaesthesiol
2002
;15
:323
—7
3Perlas
A
,Chan
VW
,Lupu
CM
,Mitsgeakakis
N
,Ультразвуковая оценка содержимого и объема желудка
.Анестезиология
2009
;111
:82
—9
4Bouvet
L
,Mazoit
JX
,Chassard
D
,Allaouchiche
9000B
Д
Клиническая оценка ультразвукового исследования антральной области для оценки содержимого и объема желудка до операции
.Анестезиология
2011
;114
:1086
—92
5Perlas
A
,Davis
L
,Khan
M
,Mitsakakis
N
,S 9000N
,Сонография желудка у хирургического пациента натощак. Проспективное описательное исследование
. Anesth Analg
2011
;113
:93
—7
6Van de Putte
P
,Perlas
A
Ультразвуковая оценка содержимого и объема желудка
.Br J Anaesth
2014
;113
:12
—22
7Alakkad
H
,Kruisselbrink
R
,Chin
KJ
и др.Ультразвук в месте оказания медицинской помощи определяет содержимое желудка и изменяет анестезиологическое лечение плановых хирургических пациентов, которые не соблюдают инструкции по голоданию: проспективная серия клинических случаев
.Can J Anaesth
2015
;62
:1188
—95
8Арзола
C
,Cubillos
J
,Perlas
A
,Дауни
K
ho,
ho
Межэкспертная достоверность качественной ультразвуковой оценки содержимого желудка в третьем триместре беременности
.Br J Anaesth
2014
;113
:1018
—23
9Арзола
C
,Perlas
A
,Siddiqui
NT
,Carvalho
JCA
Прикроватное ультразвуковое исследование желудка у доношенных беременных перед плановым кесаревым сечением. Проспективное когортное исследование
.Анест Аналг
2015
;121
:752
—8
10Bataille
A
,Rousset
J
,Marret
E
,Капот
F
Ультрасонографическая оценка содержимого желудка во время родов при эпидуральной анальгезии: проспективное когортное исследование
.Br J Anaesth
2014
;112
:703
—7
11Джей
L
,Zieleskiewicz
L
,Desgranges
FP
и др.Определение порогового значения антральной области, измеренной в положении лежа на спине, для быстрой диагностики пустого желудка у рожениц: проспективное когортное исследование
.евро J Анестезиол
2017
;34
:150
—7
12Van de Putte
P
,Perlas
A
Сонография желудка у хирургического пациента с тяжелым ожирением: технико-экономическое обоснование
.Анест Аналг
2014
;119
:1105
—10
13Schmitz
A
,Thomas
S
,Melanie
F
и др.Ультрасонография антральной области желудка и объема желудочного содержимого у детей
.Педиатр Анаест
2012
;22
:144
—9
14Spencer
AO
,Walker
AM
,Yeung
AK
и др.Ультразвуковая оценка объема желудка у педиатрического пациента натощак, подвергающегося эндоскопии верхних отделов желудочно-кишечного тракта: разработка прогностической модели с использованием объемов отсасываемых эндоскопом
.Педиатр Анаест
2015
;25
:301
—8
15Gagey
AC
,de Queiroz Siqueira
M
,Desgranges
FP
и др.Ультразвуковая оценка содержимого желудка для определения стратегии анестезии у младенцев с гипертрофическим стенозом привратника: проспективное когортное исследование
.Br J Anaesth
2016
;116
:649
—54
16Perlas
A
,Mitsakakis
N
,Liu
L
и др.Валидация математической модели ультразвуковой оценки объема желудка при гастроскопическом исследовании
.Анест Аналг
2013
;116
:357
—63
17Schmitz
A
,Kellenberger
CJ
,Neuhaus
D
и др.Время голодания и объем желудочного содержимого у детей, подвергающихся глубокой седации пропофолом — оценка с использованием магнитно-резонансной томографии
.Педиатр Анаест
2011
;21
:685
–90
Заметки автора
© Автор, 2017.
